ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящая заявка относится, частично, к типу устройств разделения, использующих взаимно вращающиеся поверхности, по меньшей мере одна из которых содержит мембрану для фильтрации компонента от жидкости, проходящей между поверхностями; к контурам и системам потока жидкости, включающим в себя такой сепаратор; и к применению таких систем для отделения биологических клеток, таких как эритроциты, плазма или лейкоциты, от цельной крови, среды для хранения, среды взвеси, супернатанта и т.п.
УРОВЕНЬ ТЕХНИКИ
Традиционное взятие крови продолжает существенно опираться на ручное взятие цельной крови у здоровых доноров на мероприятиях по сдаче крови, при визитах доноров в центры крови или больницы и т.п. При типичном ручном взятии, цельная кровь берется путем ее простого протекания под воздействием силы тяжести и венозного давления из вены донора в контейнер для сбора. Объем забранной цельной крови обычно составляет “единицу”, которая составляет около 450 мл.
Конкретнее, при таком взятии обычно применяется предварительно собранная конструкция трубок и контейнеров или пакетов, включая первичный контейнер из эластичного пластика или пакет для приема единицы цельной крови от донора и один или более вспомогательных контейнеров или пакетов. Кровь сначала собирается в первичный контейнер, который также содержит противосвертывающее средство (обычно содержащее цитрат натрия, фосфат и декстрозу - часто называемое CPD). Консервант (часто называемый “раствор добавки” или AS, и обычно содержащий среду из физиологического раствора, аденина и глюкозы, которая называется SAG) может быть включен в качестве элемента большей по размеру конструкции пакетов и трубок, которые используются при обработке после сбора крови.
После сбора единицы цельной крови общепринятой практикой в банках крови является транспортировка единицы цельной крови, с помощью подсоединенных трубок и контейнеров, в лабораторию обработки компонентов крови, обычно называемую “вспомогательная лаборатория”, для дальнейшей обработки. Дальнейшая обработка обычно включает в себя ручную загрузку первичного контейнера и связанных с ним трубок и вспомогательных контейнеров в центрифугу для разделения цельной крови на компоненты, такие как концентрированные эритроциты и обогащенная тромбоцитами плазма или обедненная тромбоцитами плазма. Данные компоненты затем вручную отжимаются из первичного контейнера в другие предварительно подсоединенные вспомогательные контейнеры, и могут опять центрифугироваться для выделения тромбоцитов из плазмы. После этого компоненты крови могут подвергаться лейкоредукции посредством фильтрации для дальнейшей обработки или хранения. Коротко говоря, данный процесс требует больших временных затрат, является трудоемким и подвержен возможным ошибкам, связанным с человеческим фактором.
Другой типовой задачей, выполняемой банками крови и центром переливания крови, является “промывание клеток”. Оно может выполняться с целью удаления и/или замещения жидкой среды (или ее части), в которой суспендированы клетки, с целью концентрирования или дальнейшего концентрирования клеток в жидкой среде, и/или с целью очистки взвеси клеток путем удаления нежелательного клеточного или другого материала.
В предшествующих системах промывания клеток чаще всего применялось центрифугирование взвеси клеток, слив супернатанта, ресуспендирование концентрированных клеток в новых средах, а также возможное повторение данных этапов до тех пор, пока клетки во взвеси не будут представлены в достаточно высокой или желательной по другим признакам концентрации. Центробежные сепараторы, используемые в обработке крови и компонентов крови, обычно использовались в таких способах промывания клеток.
Данные процессы также требуют достаточно больших временных затрат, поскольку требуют повторяющихся ручных манипуляций с кровью или компонентами крови и сборки или разборки различных устройств обработки жидкостей. Это, естественно, повышает не только стоимость, но и потенциал для связанной с человеческим фактором ошибки или погрешности. Соответственно, несмотря на десятилетия развития устройств и процессов разделения крови, продолжает существовать потребность в лучших и/или более эффективных устройствах, системах и способах разделения, применимых к базовым методикам взятия и обработки крови.
Хотя во многих предшествующих устройствах и процедурах разделения крови применялись принципы разделения центрифугированием, существует другой класс устройств, основанных на применении мембран, которые использовались для плазмафереза, то есть отделения плазмы от цельной крови. Конкретнее, устройства этого типа используют вращающиеся друг относительно друга поверхности, одна из которых содержит пористую мембрану. Обычно устройство имеет внешний неподвижный корпус и внутренний вращающийся ротор, покрытый пористой мембраной.
Одним из таких хорошо известных устройств для плазмафереза является сепаратор Autopheresis-C®, поставляемый Fenwal, Inc. из Lake Zurich, штат Иллинойс. Подробное описание сепаратора с вращающейся мембраной можно найти в патенте США No. 5194145, выданном Schoendorfer, который включен в настоящее описание посредством ссылки. В данном патенте описывается покрытый мембраной вращатель, имеющий внутреннюю систему сбора, размещенную в неподвижной оболочке. Кровь подается в кольцевое пространство или зазор между вращателем и оболочкой. Кровь перемещается вдоль продольной оси оболочки в направлении выходной области, при этом плазма проходит через мембрану за пределы оболочки в пакет для сбора. Оставшиеся компоненты крови, в основном, эритроциты, тромбоциты и лейкоциты, переходят в выходную область между вращателем и оболочкой, и затем обычно возвращаются донору.
Было обнаружено, что сепараторы с вращающейся мембраной обеспечивают отличную скорость фильтрации плазмы, в основном благодаря уникальным схемам потока (“вихри Тейлора”), возбуждаемым в зазоре между вращающейся мембраной и оболочкой. Вихри Тейлора помогают удерживать клетки крови от осаждения на мембрану и ее загрязнения или закупоривания.
Несмотря на то, что сепараторы с вращающейся мембраной широко использовались для сбора плазмы, они обычно не использовались для сбора других компонентов крови, в частности, эритроцитов. Сепараторы с вращающейся мембраной также обычно не использовались для промывания клеток. Один из примеров сепаратора с вращающейся мембраной, примененного для промывания клеток, таких как эритроциты, описан в патенте США No. 5053121, который также включен в настоящее описании посредством ссылки во всей своей полноте. Однако в системе, описанной в этом патенте, используется два отдельных вращателя, соединенных последовательно или параллельно, для промывания “выделенной” крови пациента. Другие описания применения сепараторов с вращающейся мембраной для разделения крови или компонентов крови, также можно найти в патентах США No. 5376263; 4776964; 4753729; 5135667 и 4755300.
Объект изобретения, изложенный в настоящей заявке, предоставляет дополнительные достижения в области мембранных сепараторов, потенциального снижения стоимости и различных других достижений и преимуществ по сравнению с предшествующим ручным сбором и обработкой крови.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящий объект изобретения имеет ряд аспектов, которые могут быть применены в различных комбинациях, и изложение одного или более конкретных вариантов осуществления приведено в целях изложения и описания, а не ограничения. В изложении сущности выделено только несколько аспектов данного объекта изобретения, и дополнительные аспекты изложены на чертежах и в приведенном ниже более подробном описании.
В соответствии с одним из аспектов изложения, представлен способ для заполнения мембранного сепаратора. Мембранный сепаратор содержит корпус с верхом и низом, при этом по меньшей мере один канал является смежным с верхом и низом корпуса, при этом мембрана размещена внутри корпуса с целью вращения вокруг, по существу, вертикально ориентированной оси. Способ для заполнения включает в себя введение текучей среды для заполнения через канал, смежный с низом корпуса, и затем протекание дополнительной текучей среды для заполнения через канал, смежный с низом корпуса, с образованием поверхности раздела текучей среды для заполнения - воздух, которая продвигается вверх через корпус для вытеснения воздуха внутри корпуса и выталкивания воздуха через канал, смежный с верхом корпуса, при этом происходит одновременное смачивание мембраны. Дополнительная текучая среда для заполнения продолжает протекать через канал, смежный с низом корпуса, до тех пор, пока поверхность раздела текучая среда для заполнения - воздух не пройдет в вертикальном направлении через всю мембрану. Текучая среда для заполнения может содержать небиологическую текучую среду с низкой вязкостью или цельную кровь.
В соответствии с другим аспектом изложения, представлен контур обработки текучей среды, содержащий сепаратор, включающий в себя вращающиеся друг относительно друга поверхности внутри корпуса, при этом по меньшей мере одна из этих поверхностей содержит пористую мембрану, и поверхности разнесены с образованием продолжающегося, по существу, в осевом направлении зазора между ними. Корпус содержит по меньшей мере один впуск текучей среды и по меньшей мере один выпуск текучей среды, взаимодействующие непосредственно или косвенно с зазором, при этом выпуск расположен в нижней области корпуса, и впуск расположен в области корпуса, разнесенной вверх от выпуска в осевом направлении. Корпус, предпочтительно, имеет верхний конец и нижний конец в рабочем положении, при этом впуск близок к верхнему концу, и выпуск близок к нижнему концу. Контур обработки также содержит источник текучей среды для заполнения и трубопровод, соединяющий источник текучей среды для заполнения по меньшей мере с одним выпуском корпуса.
Дополнительно, контур обработки может, предпочтительно, содержать ротор, размещенный внутри корпуса, при этом внешние поверхности ротора разнесены с внутренней поверхностью корпуса с образованием кольцевого зазора между ними. Мембранный сепаратор и корпус, предпочтительно, могут вращаться друг относительно друга вокруг, по существу, вертикальной оси, и по меньшей мере один выпуск сообщается непосредственно с зазором между мембраной и корпусом. Впуск жидкости, предпочтительно, сообщается с зазором для доставки текучей среды, содержащей кровь или компоненты крови, в зазор, и по меньшей мере одна поверхность из внешней поверхности и внутренней поверхности имеет пористую мембрану, при этом выпуск текучей среды сообщается непосредственно с зазором или со стороной мембраны, обращенной от зазора, или и с тем, и с другим.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Указанные и другие характеристики объекта настоящего изобретения описаны в приведенном ниже подробном описании и показаны на прилагаемых фигурах, среди которых:
Фиг. 1 представляет собой вид в перспективе сепаратора с вращающейся мембраной, в парциальном сечении и с удалением частей для демонстрации деталей.
Фиг. 2 представляет собой продольный вид в поперечном сечении сепаратора с вращающейся мембраной с фиг. 1.
Фиг. 3 представляет собой контурное изображение выходных значений гематокрита и напряжения сдвига на стенке выходного клапана как функции относительной длины фильтрации и радиуса вращателя на основании теоретической проектной модели.
Фиг. 4 представляет собой контурное изображение выходных значений гематокрита и концентрации гемоглобина в плазме для выходного клапана как функции относительной длины фильтрации и радиуса вращателя на основании теоретической проектной модели, в которой тангенциальная скорость мембраны является постоянной.
Фиг. 5 представляет собой контурное изображение выходных значений гематокрита и числа Тейлора как функции относительной длины фильтрации и радиуса вращателя на основании теоретической проектной модели.
Фиг. 6 представляет собой трехмерный график концентрации гемоглобина в плазме как функции относительной длины фильтрации и радиуса вращателя на основании теоретической проектной модели.
Фиг. 7 представляет собой вид в перспективе устройства или сепаратора с вращающейся мембраной по настоящей заявке.
Фиг. 8 представляет собой схематический поперечный разрез сепаратора с вращающейся мембраной по настоящей заявке, при этом вращатель содержит радиально направленный выступ для задания отдельных областей жидкости.
Фиг. 9 представляет собой схематическое изображение автоматизированной системы разделения цельной крови для обработки ранее собранной цельной крови, содержащей одноразовый модуль контура циркуляции жидкости и долговременный контроллер или управляющий модуль, на который установлен модуль контура циркуляции жидкости.
Фиг. 10 представляет собой схему циркуляции, демонстрирующую один из вариантов осуществления потока жидкости через контур циркуляции жидкости, в соответствии с описанным в настоящем описании, для переработки единицы цельной крови в концентрированный продукт эритроцитов и продукт плазмы.
Фиг. 11 аналогична фигуре 9, но демонстрирует несколько более подробное изображение компонентов одноразового контура, или модуля циркуляции жидкости, и долговременного модуля контроллера.
Фиг. 12 представляет собой схематическое изображение альтернативного варианта осуществления системы в соответствии с настоящим изложением, в котором система применяется для разделения ранее собранной цельной крови.
Фиг. 12A представляет собой схематическое изображение еще одного альтернативного варианта осуществления, аналогичного фиг. 12.
Фиг. 13 представляет собой вид в перспективе системы разделения крови с двумя насосами, такой как показана на фиг. 9, 11, 12 и 12A.
Фиг. 14 представляет собой схематическое изображение еще одной альтернативы, аналогичной фиг. 12, за исключением того, что она включает в себя три насоса, иллюстрирующей систему в фазе заполнения.
Фиг. 15 представляет собой схематическое изображение системы с фиг. 14, иллюстрирующее систему в фазе разделения.
Фиг. 15A представляет собой схематическое изображение еще одной альтернативной системы с тремя насосами, аналогичной фиг. 14 и 15.
Фиг. 16 представляет собой схематическое изображение автоматизированной системы сбора цельной крови в соответствии с настоящим изложением, демонстрирующее конфигурацию системы для автоматизированного кабинетного сбора и обработки цельной крови донора в режиме заполнения.
Фиг. 17 представляет собой схематическое изображение системы с фиг. 16, демонстрирующее конфигурацию системы для сбора и разделения цельной крови на эритроциты и плазму.
Фиг. 18 представляет собой схематическое изображение системы с фиг. 16, демонстрирующее конфигурацию системы для прополаскивания системы противосвертывающим средством после завершения взятия крови у донора.
Фиг. 19 представляет собой схематическое изображение системы с фиг. 16, демонстрирующее конфигурацию системы в конце процедуры сбора крови.
Фиг. 20 представляет собой схематическое изображение системы с фиг. 16, демонстрирующее конфигурацию системы в необязательной конфигурации для фильтрации собранных эритроцитов через лейкоцитный фильтр.
Фиг. 21 представляет собой схематическое изображение альтернативного варианта осуществления автоматизированной системы сбора цельной крови относительно систем, показанных на фиг. 16-20, в которой компонент контура циркуляции жидкости одноразового использования содержит встроенный фильтр лейкоредукции как часть линии извлечения устройства доступа к донору.
Фиг. 22 представляет собой схематическое изображение альтернативного варианта осуществления контура циркуляции жидкости одноразового использования с фиг. 21, в котором фильтр лейкоредукции размещен в линии извлечения по ходу потока относительно входной точки, в которой противосвертывающее средство вводится в цельную кровь.
На фиг. 23 показан одноразовый набор, подходящий для промывания клеток в соответствии со способом, изложенным в настоящем описании.
На фиг. 24 показан другой вариант осуществления одноразового набора, подходящего для промывания клеток в соответствии с альтернативным способом, изложенным в настоящем описании.
На фиг. 25 показан вариант осуществления панели управления устройства, подходящего для промывания клеток в соответствии со способом, изложенным в настоящем описании.
Фиг. 26-28 представляют собой блок-схемы этапов способа промывания клеток, изложенного в настоящем описании.
Фиг. 29 представляет собой блок-схему, иллюстрирующую способ управления данными в соответствии с настоящим изложением.
Фиг. 30 представляет собой схематическое изображение системы управления данными в соответствии с настоящим изложением в комбинации с контейнером для сбора и набором для обработки.
Фиг. 31 представляет собой блок-схему, иллюстрирующую различные этапы, которые включает в себя способ для управления данными в соответствии с настоящим изложением.
ПОДРОБНОЕ ОПИСАНИЕ
Более подробное описание сепаратора с вращающейся мембраной в соответствии с настоящим изложением и его применения в различных автоматизированных системах приведено ниже. Следует понимать, что приведенное ниже описание конкретных устройств и способов предлагается в качестве примера, и не является исчерпывающим описанием всех возможных вариаций или применений. Таким образом, не предполагается, что объем изложения является ограничивающим, и должен пониматься как включающий вариации или варианты осуществления, которые будут понятны специалистам.
Обратимся к фиг. 1 и 2, на которых показана система разделения или фракционирования крови с вращающейся мембраной, обозначенная в общем как 10. Такая система 10 обычно применяется для извлечения плазмы из цельной крови, полученной у отдельного донора-человека. В целях облегчения понимания, показано только устройство выделения плазмы и связанный с ним блок привода, хотя следует понимать, что такой сепаратор образует часть одноразовой системы, содержащей пакеты для сбора, пакеты с добавками, такими как физиологический раствор или ACD, возвратные пакеты, трубки, и т.д., и что также имеются ассоциированные системы управления и система контрольно-измерительных средств для функционирования устройства.
Система 10 содержит по существу цилиндрический корпус 12, установленный концентрически вокруг продольной вертикальной центральной оси. Внутренний элемент 14 установлен концентрически с центральной осью. Корпус и внутренний элемент имеют возможность вращения друг относительно друга. В предпочтительном варианте осуществления, в соответствии с проиллюстрированным, корпус является неподвижным, и внутренний элемент является вращающимся, при этом он вращается концентрически в пределах цилиндрического корпуса 12. Границы маршрута тока крови в общем случае определены зазором 16 между внутренней поверхностью корпуса 12 и внешней поверхностью ротационного вращателя 14. Пространство между корпусом и вращателем иногда называется зазором сдвига. Типовой зазор сдвига может составлять приблизительно 0,025-0,050 дюйма (0,067-0,127 см) и может иметь равномерный размер вдоль оси, например, когда ось вращателя и корпуса совпадают. Зазор сдвига также может изменяться, например, по окружности, когда оси корпуса и вращателя смещены друг относительно друга.
Зазор сдвига также может изменяться вдоль направления оси, например, предпочтительно, ширина зазора может увеличиваться в направлении потока с целью ограничения гемолиза. Такая ширина зазора может изменяться в диапазоне от 0,025 до около 0,075 дюйма (0,06 - 0,19 см). Например, оси корпуса и ротора могут совпадать, и диаметр ротора может уменьшаться в направлении оси (направлении потока), тогда как диаметр внутренней поверхности корпуса остается постоянным, или диаметр корпуса увеличивается, и диаметр ротора остается постоянным, или диаметр обеих поверхностей изменяется. Например, ширина зазора может составлять около 0,035 дюйма (0,088 см) в конце зазора со стороны начала потока, или у конца зазора около входного клапана, и около 0,059 дюйма (0,15 см) в конце зазора со стороны конца потока. Ширина зазора может изменяться путем изменения внешнего диаметра ротора и/или внутреннего диаметра передней поверхности корпуса. Ширина зазора может изменяться линейно или пошагово, или некоторым другим желаемым образом. В любом случае, размер ширины зазора предпочтительно выбирается таким образом, чтобы при желаемой относительной скорости вращения поток Тейлора-Куэтта, такой как вихри Тейлора, создавался в зазоре, и при этом ограничивался гемолиз.
Цельная кровь подается из впускной трубки 20 через впускное отверстие 22, которое направляет кровь во входную область тока крови по маршруту, касательному к окружности вокруг верхнего конца вращателя 14. В нижнем конце цилиндрического корпуса 12 внутренняя стенка корпуса имеет выпускное отверстие 34.
Цилиндрический корпус 12 заканчивается крышкой 40 верхнего конца, имеющей концевую втулку 42, стенки которой являются немагнитными, и нижний конец 44 корпуса заканчивается выпускным отверстием 46 плазмы, концентрическим с центральной осью.
Вращатель 14 установлен с возможностью вращения между крышкой 40 верхнего конца и нижним концом 44 корпуса. Вращатель 14 содержит формованный центральный сердечник или ротор 50, внешняя поверхность которого отформована для задания ряда разнесенных в пространстве кольцевых каналов или выступов 52, разделенных кольцевыми перемычками 54. Поверхностные каналы, задаваемые кольцевыми каналами 52, соединены друг с другом посредством продольных каналов 56. На каждом конце сердечника 50 эти каналы 56 связаны с центральным отверстием или трубой 58.
В проиллюстрированном варианте осуществления поверхность ротационного вращателя 14, по меньшей мере, частично, и предпочтительно, по существу или полностью, покрыта цилиндрической пористой мембраной 62. Мембрана 62 обычно имеет номинальный размер поры 0,6 мкм, но альтернативно могут использоваться другие размеры пор. Мембраны, подходящие для способов промывания, описанных в настоящем описании, могут представлять собой волокнистые сетчатые мембраны, литые мембраны, трековые мембраны или мембраны других типов, которые будут известны квалифицированным специалистам в данной области техники. Например, в одном из вариантов осуществления, мембрана может содержать полиэфирную сетку (подложку) с частицами нейлона, отвержденными на ней, посредством чего создается извилистый путь, через который пройдут только компоненты определенного размера. В другом варианте осуществления мембрана может быть сделана из тонкого (толщиной приблизительно 15 мкм) листа, например, поликарбоната. В данном варианте осуществления, поры (отверстия) могут быть больше, чем описанные выше. Например, поры могут составлять приблизительно 3-5 мкм. Размер пор может быть таким, чтобы допускать прохождение небольших сформированных компонентов (например, тромбоцитов, микрочастиц, и т.д.), и чтобы при этом собирались нужные клетки (например, лейкоциты).
Ротационный вращатель устанавливается в крышку верхнего конца для вращения вокруг стержня 64, который запрессован в крышку 40 конца с одной стороны и размещен внутри цилиндрической несущей поверхности 65 в концевом цилиндре 66, образующем часть ротационного вращателя 14. Внутренний вращатель или внешний корпус может вращаться посредством любого устройства или системы привода вращения. В соответствии с проиллюстрированным, концевой цилиндр 66 частично охвачен кольцом 68 из магнитного материала, используемым в косвенном управлении вращателем 14. Приводной двигатель 70, внешний по отношению к корпусу 12, подсоединен с целью поворота элемента 72 кольцевого магнитного привода, который содержит, по меньшей мере, пару внутренних постоянных магнитов 74. При вращении элемента 72 кольцевого магнитного привода магнитное притяжение между кольцом 68, расположенным внутри корпуса 12, и магнитами 74, расположенными вне корпуса, присоединяет вращатель 14 к внешнему приводу, вызывающему вращение вращателя 14.
На нижнем конце ротационного вращателя 14 центральное выпускное отверстие 58 связано с центральным каналом 76 в концевом подшипнике 78, который является концентрическим с центральной осью. Место установки концевого подшипника определяется внутренним фланцем 80, который формирует нижний край центрального отверстия 82. Центральное отверстие 82 соединено с выпускным отверстием 46 плазмы. Если поверхность внутренней стороны корпуса полностью или частично покрыта мембраной, пакет сбора жидкости или труба может размещаться под мембраной для сбора плазмы и направлять ее через выпускной клапан корпуса (не показано).
I. Конструкция мембранного сепаратора
В соответствии с одним из аспектов заявки, представлен сепаратор с вращающейся мембраной, который обеспечивает улучшенные скорости потока плазмы с приемлемо низким уровнем гемолиза в сохраняемой крови. Известны различные факторы, влияющие на скорость потока фильтрации через сепараторы с вращающейся мембраной, включающие в себя скорость вращения, размер зазора между вращающейся мембраной и оболочкой, эффективную площадь мембраны, концентрацию эритроцитов (или гематокрит) и вязкость крови. Предшествующие практики проектирования устройств с вращающейся мембраной были в значительной степени эмпирическими, и им до некоторой степени способствовали неясные феноменологические описания влияния различных параметров проектирования на производительность и гемолиз. Это оказалось неэффективным относительно времени разработки и затрат технических ресурсов.
Напротив, параметры сепаратора с вращающейся мембраной по настоящей заявке были определены на основании количественных дифференциальных моделей, которые принимают во внимание локальную скорость плазмы при прохождении через мембрану и локальную концентрацию гемоглобина. Данные дифференциальные модели интегрировались по длине устройства с целью получения суммарной скорости потока плазмы и концентрации гемоглобина в плазме на выходе устройства.
Способ включает операционные входные данные на основании геометрических параметров и условий функционирования существующего сепаратора Plasmacell-C, включая гематокрит донора, скорость входного потока крови, скорость вращения и эффективную площадь мембраны. Также учитывались геометрические входные данные для радиуса ротора, ширины кольцевого зазора и длины, по которой выполняется интегрирование. См. таблицу 1 ниже.
Для получения спрогнозированных значений для гипотетических сепараторов, радиус ротора и длина фильтрации изменялись от около 1,0 до около 2,0 раз по сравнению с текущими значениями Plasmacell-C с шагом 0,05, в результате чего была получена сетка пространства параметров проектирования размером 21×21 для каждой представляющей интерес выходной переменной. Для всех устройств срез корпуса и зазор в выпускном клапане сохранялись постоянными, и зазор во входном клапане и скорость вращения изменялись соответственно. Также разрабатывались модели, которые связывали вязкость и плотность крови с гематокритом, температурой и концентрацией противосвертывающего средства.
Входные данные для расчета моделей
В одной из реализаций способа, выходные данные для скорости потока плазмы и концентрации гемоглобина были получены для различных значений радиуса ротора, скорости вращения и длины интегрирования. Результаты моделирования показаны в наложенных контурных изображениях выходного гематокрита и выходного напряжения сдвига на стенке (фиг. 3), выходного гематокрита и выходной концентрации гемоглобина в плазме (фиг. 4), и выходного гематокрита и числа Тейлора (фиг. 5), во всех случаях - как функция относительной длины фильтрации и радиуса вращателя. При использовании в настоящем документе, “длина фильтрации” понимается как осевая длина центрального сердечника ротора 50 от начала до конца каналов или выступов 52. В общем смысле, она представляет собой длину мембраны, доступную для фильтрации. “Радиус вращателя” или “диаметр вращателя” понимается как радиус или диаметр ротора с прикрепленной мембраной. На фиг. 6 показаны результаты как функция длины фильтрации и радиуса вращателя на трехмерном графике, демонстрирующем увеличение гемоглобина с увеличением размеров устройств. Данные результаты затем оценивались с целью обеспечения наилучшего баланса высокой скорости потока плазмы с приемлемо низкими уровнями гемолиза.
Модели показали, что эффективная площадь мембраны имеет наиболее сильное положительное влияние на производительность. Кроме того, хотя увеличение площади мембраны путем увеличения диаметра ротора более положительно влияет на скорости потоков, чем увеличение площади мембраны путем увеличения длины ротора, оно также увеличивает возможность гемолиза вследствие повышенной скорости мембраны, и, вследствие этого, повышения сдвигающих сил в зазоре.
Соответственно, моделирование позволило спрогнозировать длины и диаметры ротора, которые приведут к повышению площади мембран, применение которых также позволит иметь приемлемо низкие уровни гемолиза. Сепараторы-прототипы (на основании результатов моделирования) были сделаны и протестированы с целью проверки результатов, спрогнозированных посредством моделирования. Ниже в таблице 2 приведено сравнение имеющегося устройства для плазмафереза Plasmacell-C с двумя потенциальными альтернативами, основанными на моделях.
Со ссылкой на таблицу 2 и фиг. 7, сепаратор с вращающейся мембраной 10 содержит ротационный вращатель 14, который имеет диаметр вращателя D, длину фильтрации FL и суммарную длину LOA. В типичном устройстве плазмафереза, таком как сепаратор Plasmacell-C, ротор имеет диаметр D, составляющий приблизительно 2,8 см, длину фильтрации FL, составляющую приблизительно 7,6 см, и суммарную длину LOA, составляющую приблизительно 12,7 см.
В соответствии с настоящей заявкой, было обнаружено, что диаметр мембраны может быть увеличен вплоть до около 2,0 раз относительно диаметра мембраны, имеющегося в типичном устройстве плазмафереза, тогда как длина может быть увеличена вплоть до около 2,5 раз относительно длины вращающейся мембраны в типичном устройстве плазмафереза. Увеличение размера ротора в пределах данных периметров достаточно увеличивает площадь мембраны фильтра для обеспечения высокого скорости потока плазмы, при этом обеспечивая приемлемо низкий уровень гемолиза. В конкретном примере сепаратор с вращающейся мембраной по настоящей заявке может, предпочтительно, иметь диаметр D, составляющий 4,19 см, длину фильтрации FL, составляющую 14,02 см, и суммарную длину LOA, составляющую 19,56 см.
Прототипы сепараторов с вращающейся мембраной тестировались с бычьей и человеческой кровью для проверки результатов, спрогнозированных по моделям. Скорости потоков крови, составляющие 100 мл/мин, были получены при скоростях вращателя, изменяющихся в диапазоне 1000-3500 об/мин. Выходные уровни гематокрита, составляющие 80% и выше, были получены до достижения высоких уровней загрязнения мембраны. Время сбора 880 мл плазмы изменялось в диапазоне приблизительно между 18 и 20 минутами.
Как отмечалось выше, время нахождения эритроцитов в зазоре сдвига напрямую связано с величиной гемолиза. В устройствах разделения с вращающейся мембраной существуют области потока вдоль осевой длины ротора, где поток жидкости является относительно стоячим, что приводит к образованию очагов гемолиза. Качество собранных эритроцитов ухудшается в той степени, в которой эритроциты из области с высоким гемолизом перемешиваются с потоком в области с низким гемолизом.
Соответственно, согласно другому аспекту заявки, представлен способ для создания отдельных областей потока жидкости в зазоре сепаратора с вращающейся мембраной без использования затворов. Отдельные области потока снижают или минимизируют влияние смешивания жидкостей между двумя областями потока. Отдельные области потока получают посредством наличия приподнятого ребра или выступа в зазоре для снижения или минимизации зазора между вращателем и внешним цилиндром. Предпочтительно, выступ или ребро представлено на поверхности ротора за пределами места, в котором к нему прикреплена вращающаяся мембрана.
Выступ, предпочтительно, расположен таким образом, чтобы задать границу области потока высокой перфузии. Радиальный размер выступа обратно пропорционален степени смешивания, допускаемой между двумя областями, которые он задает, при этом больший радиальный размер выступ допускает меньшее смешивание. Осевой размер или протяженность выступа также обратно пропорциональна допускаемой степени смешивания, при этом больший осевой размер допускает меньшее смешивание. Осевой размер выступа, предпочтительно, имеет размер, по меньшей мере, равный размеру зазора по длине в целях минимизации образования смежных потоков Тейлора, вызывающих нежелательное смешивание.
Обратимся к фиг. 8, на которой показано схематическое представление в поперечном сечении устройства 10 разделения с вращающейся мембраной. Устройство содержит неподвижный внешний цилиндр 12 и вращающийся внутренний цилиндр 14, на котором находится фильтрующий элемент. В соответствии с настоящей заявкой, внутренний цилиндр представлен с радиальным выступом 90. Этот выступ служит для разделения зазора 16 между вращателем и внешним корпусом на две области потока. Первая область 92 жидкости имеет стоячую, непроточную область потока, обычно в части вращателя, которая выходит за пределы мембраны фильтра. Вторая область 94 потока, которая обычно контактирует с мембраной фильтра, имеет область потока с высокой перфузией.
Поскольку первая область 92 потока является непроточной, кровь, находящаяся в ней, подвержена повышенным напряжениям сдвига в течение более продолжительных периодов времени, чем кровь во второй области 94 потока. Таким образом, кровь в первой области 92 потока часто может стать гемолизированной и имеет высокие концентрации свободного гемоглобина (Hb). Выступ 90 препятствует потоку жидкости между двумя областями потока, таким образом, минимизируя степень смешивания Hb-загрязненной крови в первой области 92 с кровью с низкой Hb во второй области 94.
Хотя показано, что выступ 90 составляет единой целое с ротором, он также может быть сформирован на внутренней стороне внешнего цилиндра для достижения того же самого эффекта. Как было отмечено выше, осевой размер выступа должен иметь длину, составляющую по меньшей мере одну величину зазора. Типичное устройство разделения с вращающейся мембраной для выполнения плазмафереза обычно имеет зазор между вращателем и герметизирующей стенкой, составляющий от 0,058 см до 0,0673 см, и выступ в соответствии с настоящей заявкой мог бы иметь осевой размер в пределах того же общего диапазона. Однако большие осевые размеры для выступа приведут к сниженному смешиванию и, в одном из примеров, было обнаружено, что ротор, имеющий радиально вытянутый выступ с осевым размером 0,234 см, является эффективным.
II. Системы и способы для обработки ранее собранной цельной крови
Устройство разделения с вращающейся мембраной в соответствии с описанным выше может быть выгодно использовано в различных системах и способах обработки крови, для которых предшествующие устройства обычно не подходили, особенно, в системах и процессе для получения эритроцитов. В одном из типов системы и способа, вращатель может быть использован для обработки во “вспомогательной лаборатории” ранее собранной цельной крови, как показано на фиг. 9-15A.
Обратимся к фиг. 9, на которой схематически проиллюстрированы одноразовый контур циркуляции жидкости, или модуль A, и многоразовый долговременный контроллер, или модуль B, сконфигурированный для взаимодействия с потоком через контур жидкости A и управления им. Одноразовый контур жидкости A, как проиллюстрировано на фиг. 9, содержит множество компонентов, соединенных между собой гибкими пластиковыми трубками, определяющими маршрут потока между компонентами. Контур, предпочтительно, заранее полностью собран и предварительно стерилизован, за исключением блока с контейнером цельной крови и контейнером клеточного консерванта. Конкретнее, проиллюстрированный одноразовый контур на фиг. 9 содержит контейнер 101 цельной крови и контейнер 102 с раствором клеточного консерванта, сепаратор 108 компонентов крови, контейнер 112 для сбора плазмы, необязательный фильтр 113 редукции лейкоцитов, и контейнер 115 для сбора эритроцитов. Хотя это и не проиллюстрировано на фиг. 9, многоразовый модуль B может иметь крепления и связанные с ними весы для поддержания любого или всех контейнеров 101, 102, 112 и 115. В различных других вариантах осуществления, обсуждаемых в настоящем описании, такие крепления/весы могут не быть проиллюстрированы, но понимается, что они являются частью описываемых систем.
Контейнер 101 для сбора цельной крови может представлять собой любой подходящий контейнер, но обычно он представляет собой гибкий пластиковый мешок или пакет, в который ранее было собрано приблизительно 450 мл цельной крови. Контейнер 101 может являться частью отдельной системы в процессе сбора, и затем может присоединяться к остальной части жидкостного контура A, или может фактически являться частью контура A во время сбора. Во время сбора, в соответствии с обычной процедурой, цельная кровь смешивается с противосвертывающим средством, размещенным в первичном контейнере, с целью предотвращения преждевременной коагуляции. Соответственно, “цельная кровь” при использовании в настоящем описании включает кровь, смешанную с противосвертывающим средством.
Гибкие пластиковые трубки 105 соединены с контейнером для сбора цельной крови, например, посредством стерильного соединительного устройства или другого подходящего механизма прикрепления, и задают маршрут потока цельной крови между контейнером 101 с цельной кровью и соединением с трубками 103 раствора клеточного консерванта, которые выступают из контейнера 102 с раствором клеточного консерванта в соединение маршрута потока. Соединение маршрута потока между маршрутом потока цельной крови и маршрутом потока всех консервантов располагается во входном фиксаторе 116. Из соединения маршрут потока проходит через трубки 107 к впускному отверстию сепаратора 108.
Как показано на фиг. 9 настоящего описания, корпус сепаратора имеет выпускной клапан, который соединен с зазором между корпусом и ротором и с трубками 110 потока концентрированных эритроцитов для извлечения концентрированных эритроцитов из зазора сепаратора. Кроме того, корпус содержит выпускной клапан из ротора, который соединен со стороной мембраны, направленной в другую сторону от зазора (например, внутренняя часть ротора) и соединен с трубками 111 маршрута потока плазмы.
В целях снижения числа лейкоцитов, которые могут присутствовать в эритроцитах, одноразовый контур циркуляции жидкости A, необязательно, содержит фильтр 113 редукции лейкоцитов, который может представлять собой любую хорошо известную конструкцию для удаления лейкоцитов из концентрированных эритроцитов без чрезмерного гемолиза эритроцитов или снижения числа эритроцитов в собранном продукте. Концентрированные эритроциты из фильтра 113 редукции эритроцитов проходят через удлинение 114 по маршруту потока концентрированных эритроцитов в контейнер 15 для хранения, который может быть сделан из любого подходящего пластикового материала, совместимого с хранением эритроцитов.
Многоразовый или долговременный модуль B контроллера, который схематически показан на фиг. 9, предпочтительно, содержит датчик 104 гематокрита для определения гематокрита и цельной крови, вытекающей из контейнера 101 цельной крови. Детектор гематокрита может иметь любую подходящую схему или конструкцию, предпочтительно, в соответствии с описанным в патенте США No. 6419822, который настоящим включен в данное описание посредством ссылки.
Долговременный контроллер многоразового использования, или модуль B управления, содержит входной фиксатор 116, которым можно управлять с целью контроля жидкости из контейнера 101 цельной крови или контейнера 102 клеточного консерванта, или, необязательно, одновременно и пропорционально из обоих контейнеров 101 и 102. Для контролирования потока крови в сепаратор, модуль многоразового использования содержит впускной насос 106, который также может иметь любую подходящую конструкцию и может, например, представлять собой насос перистальтического типа, который функционирует посредством постепенного сжатия или сдавливания трубок 107, образующих маршрут впускного потока в сепаратор, насос с гибкой диафрагмой или другой подходящий насос. Датчик 117 давления взаимодействует с маршрутом впускного потока между насосом 106 и сепаратором 108 с целью определения впускного давления насоса. Датчик может выдавать данные в систему управления для обеспечения функции тревоги в случае превышения давления, недостаточного давления, или и того, и другого.
В целях контроля скорости потока концентрированных эритроцитов от сепаратора 108, многоразовый модуль также содержит выпускной насос 109, который связан с маршрутом 110 выпускного потока и функционирует аналогичным описанному в отношении впускного насоса 106 образом. Он также может иметь любую подходящую конструкцию, такую как перистальтический насос, структуру с гибкой диафрагмой или другую подходящую структуру насоса. Маршрут 111 потока плазмы, выходящей из сепаратора, предпочтительно, не контролируется насосом, и объемная скорость потока через трубки маршрута потока плазмы представляет собой разность между впускной объемной скоростью потока из насоса 106 и выпускной объемной скоростью потока из насоса 109. Модуль B многоразового использования может, однако, также содержать фиксатор 118 для управления потоком плазмы через трубки 111 маршрута потока плазмы.
Одноразовый модуль A также может содержать контейнер 112 для сбора плазмы, имеющий жидкостное соединение с маршрутом потока плазмы, для приема плазмы, отделенной сепаратором 108. Поскольку плазма проходит через пористую мембрану в сепараторе 108, плазма, которая собирается в контейнере 112, является в значительной степени безклеточной плазмой, и может подходить для введения пациентам, замораживания с целью хранения или последующей обработки.
На фиг. 10 показан общий вид маршрута(-ов) потока жидкости через систему, проиллюстрированную на фиг. 9. В частности, на ней показан поток цельной крови из контейнера 101 с одной единицей цельной крови через детектор 104 гематокрита цельной крови к соединению в маршруте потока, расположенном в бинарном фиксаторе 116. Раствор для консервирования клеток, такой как раствор для консервирования эритроцитов, вытекает из контейнера 102 эритроцитов также к соединению в бинарном фиксаторе 116. В зависимости от этапов обработки, бинарный фиксатор допускает поток цельной крови или клеточного консерванта в остальную часть системы. Необязательно, фиксатор 116 может представлять собой пропорциональный фиксатор, допускающий выбранный одновременный пропорциональный поток цельной крови и консерванта эритроцитов.
Из бинарного фиксатора 116 цельная кровь или жидкость клеточного консерванта протекает через впускной насос 106 и в устройство 108 разделения. Как объяснялось ранее, устройство разделения использует вращающиеся друг относительно друга корпус и ротор, на одном из которых находится мембрана, через которую может проходить плазма.
В одном из вариантов осуществления, мембрана находится на поверхности ротора, и плазма проходит через мембрану и через внутренний лабиринт протоков в пределах ротора, выходя в итоге в контейнер 112 для сбора плазмы. В случае, когда мембрана установлена на роторе, устройство обычно называется сепаратором с вращающейся мембраной, как показано на фиг. 10. Однако следует понимать, что мембрана потенциально может быть установлена на внутренней поверхности корпуса в направлении зазора между внутренней поверхностью стенки корпуса и внешней поверхностью мембраны, или мембрана может находиться и на внешней поверхности ротора, и на внутренней поверхности корпуса, с тем чтобы плазма проходила через мембраны одновременно, что потенциально увеличивается скорость разделения или производительность сепаратора 108. Из сепаратора 108 концентрированные эритроциты протекают через выпускной клапан корпуса, соединенный с зазором между ротором и корпусом, и через маршрут 110 потока эритроцитов и выпускной насос 109, который контролирует скорость объемного потока концентрированных эритроцитов.
Хотя гематокрит концентрированных эритроцитов, удаленных из сепаратора 108, может меняться, ожидается, что гематокрит концентрированных эритроцитов будет составлять приблизительно 80-85%. Выпускной насос 109 закачивает концентрированные эритроциты в контейнер 115 для сбора эритроцитов и, необязательно, через фильтр редукции лейкоцитов, расположенный на маршруте потока эритроцитов между насосом 109 и контейнером 115 для сбора. Воздействие насоса, выталкивающего концентрированные эритроциты через фильтр редукции лейкоцитов, помогает поддерживать время обработки в пределах целесообразного диапазона по сравнению, например, со временем, которое потребовалось бы для потока концентрированных эритроцитов через фильтр редукции лейкоцитов в ручной установке под воздействием гравитации.
Плазма, отделенная сепаратором 108, как показано на фиг. 10, протекает через устройство разделения, например, из выпускного клапана, связанного с лабиринтом протоков внутри ротора, через единичный контрольный фиксатор 118 и в контейнер 112 для сбора плазмы. Как отмечалось ранее, поскольку плазма проходит через мембрану, она является в значительной степени безклеточной и подходящей для последующего введения пациентам, замораживания и/или для обработки, например, путем фракционирования, с целью получения компонентов плазмы, предназначенных для использования в терапевтических продуктах.
Система также может содержать фильтр, такой как фильтр редукции лейкоцитов, в линии 111 потока плазмы, если есть необходимость.
Фиг. 11 иллюстрирует одну из версий потенциальной системы, использующей и одноразовый модуль A жидкостного контура, и многоразовый или долговременный модуль B контроллера. Хотя они показаны собранными друг с другом, модуль A жидкостного контура и долговременный модуль B имеют отдельное и независимое назначение и могут также использоваться с другими системами. Как можно видеть на фиг. 11, одноразовый модуль A удобно установлен напротив многоразового модуля B, который имеет связанные с ним навесы или опоры, некоторые из которых могут быть связаны с весами, для поддержания различных контейнеров одноразовой системы. Одноразовый модуль предпочтительно является, как указывалось ранее, предварительно собранным и предварительно простерилизованным. Контейнер с раствором клеточного консерванта может быть предварительно присоединен как часть одноразовой системы или может быть добавлен позднее, например, с помощью стерильного соединительного устройства или другого подходящего приспособления. Контейнер цельной крови, который содержит единицу ранее собранной цельной крови, также может быть предварительно присоединен к предварительно собранному жидкостному контуру или может быть присоединен посредством стерильного соединительного устройства или другого подходящего приспособления для соединения.
Поверхность многоразового модуля B содержит, в данном варианте осуществления, отдельный фиксатор 116a раствора для управления потоком раствора для консервации клеток из контейнера 102 раствора, который свисает с поднятой поддерживающий штанги раствора. Контейнер 101 цельной крови подвешен к весам. Весы могут иметь обычную конструкцию и могут выдавать сигнал измерения веса, который может быть использован системой управления модуля B для измерения количества цельной крови, которое остается в контейнере, и/или количества цельной крови, которое было обработано системой. Одноразовая система содержит маршрут 105 потока эритроцитов, который проходит из контейнера цельной крови через детектор 104 гематокрита и через отдельный фиксатор 116b цельной крови для управления потоком цельной крови из контейнера в систему. Маршрут 103 потока раствора клеточного консерванта и маршрут 105 потока цельной крови объединяются в соединении, таком как v-участок или y-участок, выше по ходу потока от впускного насоса 106. Объединенный маршрут потока проходит через впускной насос на впускной клапан устройства 108 разделения. Как видно на фиг. 11, многоразовый модуль B содержит блок привода, такой как магнитный блок привода, для выполнения вращения ротора в пределах корпуса сепаратора без необходимости физического прохождения элементов или компонентов привода через корпус. В данной схеме расположения ротор содержит магнитно подсоединенный элемент привода, который вращается посредством магнитного блока привода, соединенного с многоразовым модулем. Система подробнее описана в патенте США No. 5194145, выданном Schoendrofer, который включен в настоящее описание посредством ссылки.
Выпускной клапан концентрированных эритроцитов из сепаратора 108 присоединен к маршруту 110 потока эритроцитов, который проходит через выпускной насос 109 к впускному клапану необязательного фильтра 113 редукции лейкоцитов. Среда фильтра, расположенная между впускным клапаном и выпускным клапаном фильтра редукции лейкоцитов, по существу, удаляет лейкоциты из эритроцитов. Трубки 114 маршрута потока эритроцитов передают эритроциты с выпускного клапана фильтра в контейнер 115 для сбора эритроцитов.
Плазма пропускается из выпускного клапана плазмы сепаратора через фиксатор 118 контроля потока плазмы в контейнер 112 для сбора плазмы. Аналогично контейнеру цельной крови, контейнер 115 концентрированных эритроцитов и контейнер 112 плазмы подвешиваются к весам, которые могут находиться в электронном взаимодействии с системой управления долговременного или многоразового модуля B с целью предоставления информации относительно количества концентрированных эритроцитов и/или плазмы, собранных из цельной крови, или относительно скорости сбора.
Хотя данная система была проиллюстрирована с определенными основными компонентами и свойствами в соответствии с описанным выше, не предполагается, что данное описание исключает добавление, при необходимости, других компонентов, таких как датчики, насосы, фильтры и т.п. Например, необязательно, может быть желательным проведение фильтрации плазмы до ее входа в контейнер для сбора плазмы, или может быть желательным исключение фильтра лейкроредукции для эритроцитов. Хотя плазма, удаленная из сепаратора 108, является в значительной степени безклеточной плазмой, может быть необходимой фильтрация плазмы с целью последующего введения или обработки. Не предполагается, что настоящее описание исключает возможное добавление дополнительных компонентов или удаление одного или более компонентов, описанных выше.
Обратимся теперь к обработке цельной крови в проиллюстрированной системе; процесс разделения начинается с заливки системы. “Заливка” относится к способу, посредством которого мембрана подготавливается (то есть, смачивается) до начала использования. Смачивание жидкостью помогает вытеснить воздух, присутствующий в матрице мембраны, до проведения индуцированного давлением потока через мембрану. Обычно небиологическая жидкость низкой вязкости, такая как раствор клеточного консерванта (раствор эритроцитов, такой как раствор Adsol), используется для смачивания с целью осуществления наиболее эффективного вытеснения воздуха. Во время заливки жидкость удаляется из пакета 102 раствора клеточного консерванта посредством впускного насоса 106 до тех пор, пока линия 103 раствора, линия 105 цельной крови, впускная линия 107 и устройство 108 с вращающейся мембраной не будут полностью заполнены раствором. Для обеспечения надлежащей заливки, впускной насос 106 может перемещаться по часовой стрелке и против часовой стрелки во время заливки. Цель заливки раствором состоит в предотвращении формирования поверхности раздела воздух-кровь посредством создания поверхности раздела раствор-кровь, а также в смачивании мембраны в устройстве разделения. Каждая из предпринимаемых мер позволяет снизить гемолиз эритроцитов.
После того, как система была успешна залита, маршрут 103 потока клеточного раствора будет закрыт посредством впускного фиксатора 116. Проиллюстрированный впускной фиксатор представляет собой бинарный фиксатор, который может закрывать маршрут 103 потока раствора клеточной консервации или маршрут 107 потока цельной крови. Цельная кровь будет затем прокачана через маршрут 105 потока цельной крови и маршрут 107 впускного потока в сепаратор 108 посредством впускного насоса 106. Скорость потока впускного насоса 106 может изменяться от около 10 мл/мин до 150 мл/мин в зависимости от желаемого выхода продукта для конкретной процедуры. После того, как цельная кровь выходит из контейнера 101, она проходит через детектор 104 гематокрита цельной крови, который генерирует оценку гематокрита цельной крови путем измерений отражения IR LED. Подробности относительно детектора гематокрита объяснены в патенте США No. 6419822 (Название: Systems and methods for sensing red blood cell hematocrit), включенном посредством ссылки. Значение гематокрита цельной крови требуется для исходного алгоритма управления проиллюстрированной системы, но может быть важным в других системах.
После того, как цельная кровь заполнила сепаратор 108, система начинает перемещать плазму из сепаратора, который разделяет цельную кровь, входящую в устройство с вращающейся мембраной, на концентрат эритроцитов и практически безклеточную плазму. Упакованные эритроциты с гематокритом, составляющим приблизительно 80-85%, будут выкачаны из сепаратора 108 через маршрут 110 потока эритроцитов в лейкофильтр 113 эритроцитов посредством выпускного насоса 109. Выпускной насос пропускает упакованные эритроциты через лейкофильтр 113 эритроцитов, и концентрат эритроцитов, который выходит из лейкофильтра 113 эритроцитов через линию 114 эритроцитов в пакет 115 продукта эритроцитов, будет успешно обеднен лейкоцитами и также обеднен тромбоцитами. Также возможно выполнить автоматизированное разделение цельной крови без использования лейкофильтра 113 эритроцитов. В этом случае лейкофильтр 114 эритроцитов будет удален из системы, и продукт 115 эритроцитов не будет обеднен лейкоцитами или тромбоцитами.
В течение процедуры плазма проходит через маршрут 111 потока плазмы в пакет 112 плазмы со скоростью потока, равной разности между скоростью потока впускного насоса 106 и скоростью потока выпускного насоса 109, что в настоящее время выполняется в других приложениях разделения с вращающейся мембраной, таких как применяются в инструменте Autopheresis-C®, поставляемом компанией Fenwal, Inc. Давление на мембране, сгенерированное вследствие различия в скоростях потока, отслеживается датчиком 117 давления. Измерения давления используются для контроля скорости потока плазмы с применением алгоритма, описанного в заявке на патент США No. 13/095633, поданной 27 апреля 2011 (Название: SYSTEMS AND METHODS OF CONTROLLING FOULING DURING A FILTRATION PROCEDURE), настоящим включенной посредством ссылки.
Система на фигурах 9-11 будет продолжать разделять упакованные эритроциты и плазму до тех пор, пока пакет 101 цельной крови не станет пустым, что будет определено по прохождению воздуха через детектор 104 гематокрита цельной крови. В этот момент линия 105 цельной крови будет закрыта, и линия раствора клеточного консерванта будет открыта посредством впускного фиксатора 116 для запуска промывания раствором или спуска. Во время промывания раствором, раствор консерванта будет удален из пакета 102 раствора и будет закачан в сепаратор 108 посредством впускного насоса 106. Маршрут 111 потока плазмы закрывается посредством фиксатора 118 плазмы во время промывания раствором. Промывание раствором используется для спуска любой крови, остающейся в системе, в контейнер 115 продукта эритроцитов. Промывание раствором также повысит объем контейнера 115 продукта эритроцитов до уровня, необходимого для надлежащего хранения эритроцитов. После окончания промывания раствором разделение единицы цельной крови завершается.
Обратимся к фиг. 12, на которой показана еще одна альтернативная система с двумя насосами. Данный вариант осуществления отличается от показанного на фиг. 9 в основном тем, что жидкость из раствора консерванта для клеток крови добавляется после того, как эритроциты были отделены от цельной крови. Конкретнее, контейнер/пакет 101, содержащий ранее собранную цельную кровь (предпочтительно уже объединенную с противосвертывающим средством), соединяется с одноразовой системой A через сегмент трубок 107, который ведет к сепаратору 108 крови. Насос 106 взаимодействует с трубками 107 с целью закачивания цельной крови в сепаратор 108. Контейнер 102, содержащий раствор добавки для консервации эритроцитов, соединяется с контейнером 115 для сбора отделенных эритроцитов через трубки 114, через которые отделенные эритроциты также направляются в контейнер 115 через фильтр 114 лейкоцитов.
Стерильное соединение контейнеров 101, 102 с одноразовой системой может быть достигнуто посредством ряда различных способов. Контейнер 102 для раствора добавки может быть представлен как часть одноразовой системы A, и может быть объединен с остальной одноразовой частью (после стерилизации посредством, например, обработки гамма- или электронным пучком) во время итоговой упаковки после того, как оставшаяся часть одноразовых элементов была стерилизована (посредством, например, обработки паром). Альтернативно, контейнер 102 может быть сформирован как единое целое с одноразовыми элементами. В еще одной альтернативе, и контейнер 102, и контейнер 101 цельной крови могут быть отдельными от остальных одноразовых элементов и могут подсоединяться в момент использования через, например, стерильные стержневые соединения 170, показанные схематически на фиг. 10. Такие стержневые соединения, предпочтительно, имеют фильтр 0,2 мкм для поддержания стерильности.
В другом аспекте данного варианта осуществления, трубки 103, соединяющие контейнер 102 с раствором добавки с фильтром 62 лейкоцитов, также могут быть совместно сцеплены посредством насоса 109. В частности, насос 109 может представлять собой насос с двойным напором, который производит поток раствора добавки и поток эритроцитов, выходящих из сепаратора 108, с целью контроля скорости каждого на основании внутреннего диаметра трубок 103 и 110.
В варианте осуществления с фиг. 12 также используется дополнительный датчик 117b давления для отслеживания встречного давления из фильтра 113 лейкоцитов. Если встречное давление станет чрезмерным, как в случае закупорки фильтра, датчик будет осуществлять управление скоростью потока с целью обеспечения того, чтобы одноразовые элементы не разрывались вследствие избыточного давления.
III. Заливка мембраны
В соответствии с другим аспектом изложения, представлен способ для заливки мембранного фильтра, посредством которого повышается вероятность того, что будет достигнуто смачивание максимальной величины площади поверхности мембранного фильтра, в результате чего максимизируется площадь мембраны, доступная для фильтрации/разделения. В частности, когда система фильтра с вращающейся мембраной заливается в соответствии с описанным выше, при этом вращающаяся мембрана ориентирована таким образом, что ось вращения является, по существу, вертикальной, раствор для заливки входит в верхний впускной канал вращающегося сепаратора, и гравитация направляет жидкость к выпускному клапану на дне сепаратора. В таких обстоятельствах поверхностное натяжение жидкости заливки будет формировать поверхность раздела воздух-жидкость, которая может передвигаться неравномерно по поверхности мембраны, создавая нарушения. В результате этого определенные области мембраны фильтра не будут увлажняться во время заливки, что повышает потенциал захвата воздуха матрицей мембраны. Таким образом, неувлажненная область мембраны становится недоступной для разделения, что негативно сказывается на эффективности разделения мембраной, до тех пор, пока не будет создано достаточное давление для вытеснения воздуха.
Соответственно, представлен способ для заливки мембранного сепаратора, который позволяет равномернее смочить поверхность мембраны посредством обеспечения более равномерной поверхности раздела воздух-жидкость во время заливки. С этой целью жидкость заливки вводится в сепаратор таким образом, что она работает против силы тяжести при продвижении поверхности раздела жидкость-воздух в верхнем направлении через поверхность мембраны. Это помогает обеспечить более равномерное смачивание мембраны, поскольку воздух, вытесненный во время заливки, может перемещаться в одном направлении, не будучи захваченным, при продвижении поверхности раздела воздух-жидкость через мембрану.
Таким образом, в соответствии с данным альтернативным способом для заливки, жидкость заливки вводится в сепаратор через канал на дне сепаратора. Раствор для заливки продвигается вверх в корпусе сепаратора против силы тяжести для смачивания поверхности мембраны, при этом воздух выталкивается из сепаратора через канал на верху сепаратора. Хотя такая заливка “снизу вверх” описывается в контексте сепаратора с вращающейся мембраной, оно также применима к мембранному сепаратору любого типа, которому требуется заливка жидкостью до начала использования.
В соответствии с фиг. 9 и 12, сепаратор 108 ориентирован вертикально, при этом мембранный сепаратор и корпус могут вращаться друг относительно друга вокруг, в общем смысле, вертикальной оси, при этом канал для приема цельной крови расположен на верху сепаратора и каналы, через которые выходят отделенные эритроциты и плазма, расположены внизу сепаратора. Таким образом, в соответствии с одним из путей выполнения данного альтернативного способа заливки, и в соответствии с фиг. 1 и 2, раствор для заливки может быть введен через выходное отверстие 34 или выпускное отверстие 46 плазмы сепаратора с вращающейся мембраной 10, при этом воздух выталкивается через впускное отверстие 22. В соответствии с другим путем выполнения данного альтернативного способа заливки, сепаратор 10 может быть инвертирован или перевернут для заливки с тем, чтобы выходное отверстие 34 и выпускное отверстие 46 плазмы находились на верху сепаратора 10, и впускное отверстие 22 находилось внизу сепаратора 10. Раствор для заливки может затем быть введен через впускной клапан 22, при этом поверхность раздела жидкость-воздух продвигается вверх, и воздух выталкивается через выходное отверстие 34 или выпускное отверстие 46 плазмы, или через оба отверстия. После заливки, сепаратору 10 может быть возвращена его исходная ориентация, в которой впускное отверстие 22 находится наверху, и выходное отверстие 34 и выпускное отверстие 46 плазмы находятся внизу.
Еще одна альтернатива, в которой может быть использована заливка “снизу вверх” сепаратора 108 крови, описанная выше, показана на фиг. 12A. В отличие от фиг. 12, впускная линия 107 для цельной крови соединяется с более низким каналом сепаратора 108 (к которому была присоединена выпускная линия 110 в варианте осуществления с фиг. 12), тогда как выпускная линия 110 соединена с каналом на верху сепаратора 108 (к которому была присоединена впускная линия 107 в варианте осуществления с фиг. 12). Для заливки системы с фиг. 12A, фиксатор 116B открывается и насос 106 активируется для создания потока цельной крови (предпочтительно, с добавленным противосвертывающим средством) через впускную линию 107 таким образом, чтобы он входил в сепаратор 108 через канал в более низком конце корпуса. При заполнении цельной кровью корпуса сепаратора воздух выталкивается через верхний канал, с тем чтобы удалить, по существу, весь воздух из устройства и осуществить смачивание мембраны фильтра.
После завершения заливки, система продолжает функционировать, как показано на фиг. 12A, для разделения цельной крови на плазму, принимаемую в контейнере 112, и эритроциты, принимаемые в контейнере 115. В конце процедуры разделения сепаратор может промываться раствором добавки из контейнера 102.
Обратимся к фиг. 14 и 15, на которых показана еще одна альтернативная система разделения крови в соответствии с настоящим изложением. Система с фиг. 14 и 15 аналогична системам с фиг. 9, 11 и 12, за исключением того, что модуль B содержит третий насос 119 для избирательного закачивания раствора добавки в сепаратор 108 в течение фазы заливки (как показано на фиг. 14), или к отделенным эритроцитам во время фазы разделения (как показано на фиг. 15). Система с фиг. 14 и 15 также содержит дополнительный фиксатор 120 для избирательного разрешения или предотвращения потока жидкости (отделенных эритроцитов и раствора добавки) через лейкофильтр 113 и в контейнер 115 эритроцитов. До начала заливки фиксатор 20 может недолго оставаться открытым, и насос 109 может выкачивать остаточный воздух из контейнера 115 и фильтра 113, минимизируя объем воздуха, остающийся в контейнере 115 в конце данной процедуры. Как и на фиг. 12A, в системе с фиг. 14 и 15 используется заливка “снизу вверх” сепаратора 108, за исключением использования раствора добавки в качестве жидкости для заливки вместо цельной крови. В течение заливки системы, как показано на фиг. 14, воздух из одноразовой системы A выталкивается в контейнер 101 цельной крови.
В течение фазы разделения система функционирует, как показано на фиг. 15.
При завершении фазы разделения раствор добавки закачивается в сепаратор 108 (как показано в фазе заливки, проиллюстрированной на фиг. 14) для промывания сепаратора.
Обратимся к фиг. 15A, на которой показана еще одна альтернативная система. Система с фиг. 15A аналогична системе с фиг. 14 и 15 в том, что многоразовый компонент B содержит три насоса 106, 109 и 119. Однако система с фиг. 15A аналогична системе с фиг. 12A в том, что впускная линия 107 для цельной крови соединена с каналом внизу сепаратора 108, тогда как выпускная линия для отделенных эритроцитов соединена с каналом на верху сепаратора. Таким образом, в системе с фиг. 15A цельная кровь используется для заливки системы аналогично системе с фиг. 12A.
IV. Системы и способы управления данными
Система, описанная в настоящем описании, также может включать в себя решения по управлению данными. Весы и добавление устройств печатания этикеток к системе позволило бы пользователям получать этикетки с весом продукта напрямую из системы разделения по завершении процедуры. Это устраняет ручное взвешивание и запись данных, используемые в текущих способах обработки. Модуль B может содержать подходящий пользовательский интерфейс, такой как сенсорный экран, кнопочную панель или клавиатуру, а также сканер, чтобы предоставить пользователям возможность ввода информации, такой как пользовательский номер идентификации донора, идентификатор банка крови, номера набора жидкостного контура, номера партии, и т.д., которая также может улучшить эффективность управления данными в центрах производства крови.
Конкретнее, и в соответствии с еще одним аспектом настоящего изложения, представлен способ для автоматизации передачи данных, ассоциированных с контейнером для сбора цельной крови, а также другой относящейся к делу информации, в устройство обработки данных, используемое для последующего разделения цельной крови и конечного хранения контейнера или контейнеров для такого отделенного компонента или компонентов крови. Данный способ схематически проиллюстрирован на блок-схеме с фиг. 29, где представлен исходный контейнер (этап 122), который обычно содержит единицу ранее собранной цельной крови, хотя исходный контейнер может содержать ранее обработанный продукт крови. Исходный контейнер обычно имеет ассоциированные с ним данные, относящиеся к идентификации донора и времени, места сбора и т.д., при этом такие данные предпочтительно находятся в машиночитаемом формате, таком как штрихкод или метка RFID. Эти данные затем извлекаются и передаются (этап 124), и затем ассоциируются с устройством обработки данных и контейнерами конечного хранения (этап 126).
Обратимся к фиг. 30, на котором показана одна из возможных систем для применения в качестве системы управления данными в соответствии с настоящим изложением. Представлен контейнер 128 для сбора крови и отдельное устройство 130 обработки данных, имеющее три контейнера 132, 134 и 136 для конечного хранения. Во время взятия цельной крови, информация идентификации донора кодируется и ассоциируется с контейнером для собранной цельной крови. Это может быть выполнено путем ручного помещения этикетки со штрихкодом для идентификатора донора на этикетку контейнера, иглу контейнера или трубки. Также это можно сделать посредством применения записывающего устройства RFID в месте сбора, передающего идентификатор донора с весов сбора или портативного устройства на метку RFID, прикрепленную к контейнеру для сбора. Использование RFID позволяет управлять большим объемом информации, включая такие данные, как тип контейнера, дата истечения срока годности, время сбора, объем сбора, идентификатор медсестры, место сбора и т.п.
Автоматизированная передача данных между контейнером 128 для сбора и комплектом 130 обработки/контейнерами 132, 134, 136 для хранения может происходить в контексте стерильного соединения контейнера 128 для сбора с комплектом 130 обработки. Например, может быть использована электромеханическая система, которая выполняет стерильное соединение контейнера для сбора цельной крови с комплектом обработки. Такая система изложена в предварительных заявках на патент США No. 61/578690 и 61/585467, поданных 21 декабря 2011 и 11 января 2012, соответственно, которые включены в настоящее описание посредством ссылки. Устройство стерильного соединения может являться отдельно стоящим, как показано в указанных выше предварительных заявках, или может быть интегрировано с многоразовым модулем B, описанным выше. Альтернативно, система управления данными может быть просто связана с многоразовым модулем B, без устройства стерильного соединения, ассоциированного с ними. В любом случае устройство стерильного соединения или многоразовый модуль содержит программируемый контроллер, сконфигурированный для автоматического выполнения, или запроса выполнения пользователем, различных этапов способа управления данными, в соответствии с подробнее описанным ниже.
Система управления данными 138 включает в себя блок обработки, экран 140 для предоставления информации пользователю (такой как запросы и подтверждения), сенсорную панель 142 для предоставления пользователю возможности ввода информации и сканер/считыватель 144 для извлечения и передачи информации между контейнером 128 для сбора и комплектом 130 обработки. Система 138 также обеспечивает печать этикеток со штрихкодом или передачу данных на одну или более меток RFID, ассоциированных с комплектом обработки. Обратимся теперь к фиг. 31, на которой показана блок-схема, иллюстрирующая в общих чертах способ управления данными. Способ включает в себя загрузку пакета для сбора и комплекта обработки на многоразовый модуль и/или в устройство стерильного соединения (этап 140). Извлекаются данные, ассоциированные с комплектом обработки и данные, ассоциированные с контейнером для сбора (этапы 142 и 144). Как можно понять, порядок, в котором выполняются данные этапы, не является критичным. Как отмечалось выше, эти данные могут принимать форму штрихкода, метки RFID или другую форму, при этом комплект обработки и ассоциированные с ним контейнеры для сбора имеют соответствующие данные из контейнера для сбора, ассоциированного с ними. Это может принимать форму печати этикеток со штрихкодами или записи данных на метку RFID (этапы 146 и 148). Контейнер для сбора и комплект обработки соединены друг с другом, предпочтительно в процедуре стерильного соединения (этап 150), при этом такое соединение происходит в период времени в течение последовательности выполнения описанных выше этапов.
Затем кровь в контейнере для сбора обрабатывается (этап 152). Затем информация комплекта обработки/контейнера для хранения извлекается и проверяется с использованием данных контейнера для сбора (этапы 154 и 156). После такой проверки контейнеры для хранения могут быть отсоединены от контейнера для сбора (этап 158).
Система по настоящему изложению помогает пользователю в выполнении этапов, описанных выше, тем, что она выдает запросы и подтверждения для различных этапов. Например, если идентифицирующая информация имеет форму штрихкода, то система запрашивает у пользователя сканирование идентификатора штрихкода комплекта обработки и идентификатора донора контейнера для сбора. Система будет затем печатать копии этикеток штрихкодов на принтере, который является частью системы или присоединен к ней, при этом тип и количество этикеток определяется типом загруженного комплекта обработки. Система затем запрашивает у пользователя нанесение этикеток со штрихкодом на контейнеры конечного хранения. После того, как система разделяет кровь на ее компоненты, система запрашивает у пользователя сканирование идентификаторов штрихкода контейнера с конечными компонентами, с тем чтобы система могла проверить правильность информации штрихкода до отсоединения контейнеров для хранения от контейнера для сбора и комплекта обработки.
Если идентифицирующая информация ассоциирована с меткой RFID, то система автоматически сканирует метку RFID на контейнере для сбора и затем автоматически считывает информацию на RFID, включенной в комплект обработки. Затем система автоматически копирует информацию контейнера для сбора на метку или метки RFID, ассоциированные с контейнерами для хранения комплекта обработки. После того, как система разделит кровь на ее компоненты, в соответствии с типом комплекта обработки, определенным инструментом, система будет считывать метку RFID на контейнерах конечных компонентов для обеспечения возможности проверки идентифицирующей информации до отсоединения контейнеров для хранения крови от комплекта обработки и контейнера для сбора.
Предполагается, что система может использовать и штрихкод, и RFID в качестве избыточных систем, и может включать некоторые или все этапы, описанные выше, в зависимости от конкретного случая. Хотя сканер штрихкодов/считыватель RFID описан как ассоциированный с многоразовым модулем B, он может представлять собой выделенную станцию, физически отдельную от самой машины обработки, но соединенную через программное обеспечение управления данными.
Хотя данный способ управления данными был описан в связи со сбором цельной крови в контейнер, отдельный от комплекта обработки и контейнеров для хранения, он с таким же успехом может использоваться в связи с системой или комплектом, в котором контейнер для сбора составляет одно целое с комплектом обработки и его контейнерами для хранения. Кроме того, способ может быть использован в связи с обработкой цельной крови, полученной напрямую у донора, как описано ниже, при этом данные идентификации донора предоставляются донором, а не контейнером для сбора, или в процедуре промывания клеток, при этом данные идентификации ассоциированы с исходным контейнером.
V. Системы и способы для обработки цельной крови донора
В соответствии с еще одним аспектом настоящего изложения, сепаратор с вращающейся мембраной, описанный выше, может быть выгодно использован в одном этапе или в “кабинетном” сборе и разделении цельной крови на компоненты крови. Как описано ниже, представлена автоматизированная система сбора цельной крови, которая разделяет цельную кровь на одну единицу эритроцитов и плазму одновременно при взятии цельной крови у донора. Предполагается, что система является системой сбора “за один проход”, без реинфузии компонентов крови обратно донору. Система, предпочтительно, содержит одноразовый контур потока жидкости и долговременный многоразовый контроллер, который взаимодействует с контуром и управляет потоком жидкости через него. Контур потока, предпочтительно, представляет собой одноразовый предварительно простерилизованный контур потока жидкости, который, предпочтительно, содержит контейнеры для сбора эритроцитов и плазмы, противосвертывающее средство и растворы добавки эритроцитов, сепаратор и фистулу для обеспечения прохождения цельной крови от донора в жидкостный контур. Долговременный контроллер, предпочтительно, содержит управляемое микропроцессором электромеханическое устройство с механизмами клапанов, насосов и датчиков, сконфигурированными для управления потоком через контур, а также содержит системы безопасности и сигнальные функции, подходящие для процедуры взятия цельной крови.
Способ взятия крови с применением системы включает в себя выполнение прокола вены донора и извлечение цельной крови из донора в одноразовый контур, в котором она обрабатывается аппаратурой и компонентами жидкостного контура, в результате чего цельная кровь разделяется на желаемые компоненты эритроцитов и плазмы. Донор остается подключенным к системе в течение процедуры, и все жидкости остаются в линии тока одноразового набора до завершения процедуры. В “однопроходной” системе цельная кровь, предпочтительно, проходит через жидкостный контур только один раз, и ни один из компонентов крови не возвращается донору.
Эритроциты, получаемые в результате сбора, не обязательно должны подвергаться процессу лейкоредукции. Однако лейкоредукция посредством фильтрации может быть осуществлена с помощью фильтра лейкоредукции, предпочтительно, встроенного в одноразовый контур, или посредством использования отдельного контура обработки, который стерильно соединен с контейнером для сбора эритроцитов.
Аппаратура, предпочтительно, содержит интерфейс оператора, такой как сенсорный экран, кнопочная панель, мышь, клавиатура и т.д., для ввода информации и/или отображения информации. Индикатор сообщения позволяет оператору контролировать процедуру, собирать информацию о ее статусе и устранять любые сбойные ситуации при их появлении.
Обратимся к чертежам; на фиг. 16-19 можно видеть схематическое представление системы автоматизированного сбора цельной крови под общим обозначением 210, в соответствии с настоящим изложением, на различных стадиях или фазах функционирования. Система, предпочтительно, содержит многоразовый компонент 212 аппаратного обеспечения, который, предпочтительно, содержит насосы, фиксаторы и датчики давления для управления потоком жидкости, а также одноразовый предварительно собранный стерильный компонент 214 жидкостного контура, который может быть установлен на компонент аппаратного обеспечения и содержит различные контейнеры/мешки, устройство доступа к донору или фистулу, и камеру разделения крови, при этом все элементы соединены друг с другом через стерильный маршрут жидкости, такой как гибкие пластиковые трубки. Контейнеры/мешки обычно являются сгибаемыми и сделаны из подходящего пластикового материала, хорошо известного в технике. Материал контейнеров может различаться в зависимости от применения, и может содержать непластифицированные материалы, такие как не содержащие DEHP полимеры, в частности, но не только, для хранения эритроцитов.
Конкретнее, проиллюстрированный компонент или модуль 214 жидкостного контура содержит устройство 216 доступа к донору, которое содержит первый отрезок трубок 218 в качестве линии извлечения, через которую цельная кровь извлекается из донора и вводится в жидкостный контур 214. Устройство 216 доступа к донору, предпочтительно, содержит иглу, в частности, малокалиберную иглу (18-21 калибра) с целью повышения комфорта донора, с наличием предохранителя иглы, при необходимости, для предотвращения случайных проколов иглой. Трубки 218 взаимодействуют с устройством разделения крови под общим обозначением 220 и, как описано выше, используются для введения цельной крови в сепаратор.
Второй отрезок трубок 222 обеспечивает обмен жидкостями между сепаратором 220 и первым контейнером/мешком 224 для приема отделенных концентрированных эритроцитов, тогда как третий отрезок трубок 226 обеспечивает обмен жидкостями между сепаратором 220 и вторым контейнером/мешком 228 для приема плазмы.
Жидкостный контур 214 также содержит источник противосвертывающего средства (например, CPD), которое находится в третьем контейнере 230, который взаимодействует с первым отрезком трубок 218 посредством четвертого отрезка трубок 232, соединенного с трубками 218, например, посредством Y-соединителя. Жидкостный контур 214 также может содержать источник раствора консерванта для эритроцитов, которые должны быть доставлены в контейнер/мешок 224. Раствор консерванта может находиться в отдельном мешке, связанном с контейнером 224. Альтернативно, контейнер 224 может быть предварительно заполнен объемом раствора консерванта, соответствующим количеству эритроцитов, которые будут приняты им в течение процедуры сбора.
Жидкостный контур 214 также содержит встроенную систему 234 взятия проб для асептического взятия проб крови до и в течение процедуры сдачи крови. Система 234 взятия проб содержит мешок, который взаимодействует с первым отрезком трубок 218 устройства доступа к донору через пятый отрезок трубок 236, расположенный выше по ходу потока относительно соединения между трубками 218 и трубками 232, через которые вводится противосвертывающее средство. Трубки 236, предпочтительно, взаимодействуют с трубками 218 через Y-соединитель или аналогичное устройство.
Долговременный компонент 212 аппаратного обеспечения, предпочтительно, содержит первый насос 238, который взаимодействует с трубками 218 для закачивания цельной крови в устройство 220 разделения и второй насос 240, который взаимодействует с трубками 222 для транспортировки, по существу, концентрированных эритроцитов из камеры 220 разделения в первый контейнер 224 для сбора. Насосы 238, 240 являются, предпочтительно, перистальтическими, или роликовыми, насосами, которые включают в себя ротор с одним или более роликами для сжатия трубок с целью обеспечения движения жидкости через них, хотя также могут быть использованы другие подходящие конструкции насосов, такие как насосы с гибкой диафрагмой. Компонент аппаратного обеспечения также, предпочтительно, содержит третий насос 242, который взаимодействует с трубками 232 для транспортировки противосвертывающего средства к трубкам 218 линии извлечения, через которые цельная кровь транспортируется в сепаратор 220. Третий насос 242 обеспечивает дозирование потока противосвертывающего средства, и также способствует смачиванию и промыванию системы, как будет описано ниже. Однако третий насос 242 является необязательным, и противосвертывающее средство может дозироваться в линии извлечения 218 цельной крови посредством гравитационного потока, при этом трубки 232 имеют размер, обеспечивающий необходимую скорость потока в течение процедуры сбора.
Компонент 212 аппаратного обеспечения также, предпочтительно, содержит фиксаторы 244, 246, 248 и 250 для избирательной закупорки и открытия сегментов трубок 218, 232, 222 и 226, соответственно. Термин “фиксаторы” используется в настоящем документе в широком смысле, и включает в себя любой механизм, который взаимодействует с маршрутами потока, например, сегментами трубок жидкостного контура, с целью избирательного разрешения или предотвращения потока жидкости через них. Компонент 212 аппаратного обеспечения также, предпочтительно, содержит датчики 252, 254 давления в трубках 218 линии извлечения вблизи или смежно с иглой (датчик 252 давления) и вблизи или смежно с впускным клапаном сепаратора 220 (датчик 254 давления) для контроля впускного давления, например, для обнаружения коллапса вены. Также, предпочтительно, представлены весы (не показаны) по меньшей мере для первого контейнера 224 с целью предоставления обратной связи относительно объема собранных эритроцитов.
В соответствии с другим аспектом изложения, многоразовый компонент аппаратного обеспечения, предпочтительно, содержит программируемый контроллер 256 для приведения в действие насосов и фиксаторов и контроля датчиков давления и весов, с тем, чтобы процедура сбора цельной крови могла быть, по существу, автоматизирована. Контроллер 256 содержит программируемый микропроцессор и, предпочтительно, включает в себя интерфейс оператора, такой как сенсорный экран и индикатор сообщения для обеспечения оператору возможности входа и просмотра данных и управления процедурой, сбора информации по ее статусу и устранение любых сбойных ситуаций при их появлении.
Для выполнения автоматизированной процедуры сборы и разделения с помощью автоматизированной системы 210 сбора крови, изложенной выше, одноразовый жидкостный контур 214 загружается в рабочее положение на многоразовом компоненте 212 аппаратного обеспечения, как показано на фиг. 16 в прилагаемых чертежах. В фазе или стадии, показанной на фигуре 16, система заливается жидкостью для существенного удаления воздуха и смачивания мембраны фильтра. На начальной стадии первый фиксатор 244 закрыт, с тем, чтобы предотвратить обмен жидкостями между устройством 216 доступа к донору и камерой 220 разделения крови, и противосвертывающее средство прокачивается насосами 240 и 242 через трубки 218, сепаратор 212 и трубки 222 с целью заливки системы. Затем выполняется прокол вены донора с помощью иглы устройства доступа к донору с целью принятия цельной крови в трубки 218. В этот момент могут быть взяты пробы цельной крови посредством пакета 234 сбора проб.
Обратимся к фиг. 17; после заливки первый фиксатор 244 открывается для пропускания цельной крови через трубки 218 в сепаратор 220 крови, с помощью насоса 238, для начала фазы сбора/разделения процедуры сбора. Противосвертывающее средство продолжает дозироваться в линии извлечения сегмента 218 трубки через сегмент 232 трубки посредством третьего насоса 242. Эритроциты выходят из сепаратора 220 через трубки 222. Четвертый фиксатор 250 открывается для того, чтобы позволить плазме выйти из сепаратора 220 и пройти через трубку 226 во второй контейнер 228 для сбора. Первый насос 238 выдает поток цельной крови в сепаратор 220, при этом впускное давление контролируется датчиком 254, тогда как эритроциты закачиваются из камеры 220 для разделения посредством второго насоса 240. Перепад расхода между первым насосом 238 и вторым насосом 240 обеспечивает выход отделенной плазмы из сепаратора 220 во второй контейнер 228 для сбора.
Обратимся к фиг. 18; когда объем эритроцитов в первом контейнере 224 для сбора достигает предварительно определенного объема (измеренного через вес первого контейнера 224 для сбора, определенный посредством весов), весы выдают контроллеру 256 сигнал, который запрашивает у контроллера завершение процедуры сбора посредством закрытия первого фиксатора 244, вследствие чего происходит закупорка линии 218 извлечения. Устройство 216 доступа к донору может быть извлечено из донора в этот момент. Если система должна промываться, то четвертый фиксатор 250 закрывается с целью закупорки для плазмы линии 226 потока ко второму контейнеру 228 для сбора. Первый насос 238 деактивируется, тогда как третий насос 242 продолжает доставлять противосвертывающее средство в сепаратор 220, при этом противосвертывающее средство выпускается в первый контейнер 224 для сбора через сегмент 222 трубки.
Обратимся к фиг. 19; после завершения цикла промывания, второй фиксатор 246 и третий фиксатор 248 закрываются, и второй насос 240 и третий насос 242 деактивируются.
В этом момент первый контейнер 224 для сбора, содержащий, по существу, концентрированные эритроциты, может быть отсоединен от одноразового жидкостного контура 214 для хранения или для способствования лейкофильтрации. Это может быть выполнено путем простого подвешивания контейнера 224 для сбора и допущения гравитационной фильтрации эритроцитов через фильтр лейкоредукции в контейнер для конечного хранения. Однако, в соответствии с другим аспектом изложения, и как показано на фиг. 20, может быть представлен третий контейнер 258 для сбора, который находится в жидкостном взаимодействии со вторым контейнером 224 для сбора через сегмент 260 трубки, при этом сегмент 260 трубки находится в жидкостном взаимодействии с сегментом 220 трубки через Y-соединитель, расположенный на сегменте 222 трубки между выпуском сепаратора 220 и вторым насосом 240. Затем может быть открыт третий фиксатор 248 для разрешения выходного потока концентрированных эритроцитов из контейнера 224 для сбора, при этом второй насос 240 активируется и выполняет закачку в обратном направлении для обеспечения потока концентрированных эритроцитов через фильтр редукции лейкоцитов 262 и в контейнер для сбора 258. Давление, созданное насосом 240, значительно ускоряет процесс фильтрации по сравнению с вызываемой гравитацией лейкофильтрацией эритроцитов.
В качестве еще одной альтернативы, лейкоредукция может быть выполнена в отношении цельной крови в течение фазы извлечения в процессе эксплуатации. Обратимся к фиг. 21 и 22; линия извлечения трубки 218 может содержать фильтр 264 редукции лейкоцитов, который находится в одной линии с трубкой 218. Фильтр 264 расположен против направления потока от первого насоса 238, с тем, чтобы насос прилагал достаточную силу извлечения к крови для ее извлечения через фильтр 264 во время сбора. Лейкофильтр 264 может быть расположен в сегменте 218 трубки, против направления потока относительно места, где противосвертывающее средство вводится в систему (как показано на фиг. 21) или по направлению потока относительно места, где противосвертывающее средство вводится в линию 218 извлечения (как показано на фиг. 22). Размещение по направлению потока от места подсоединения противосвертывающего средства позволяет использовать противосвертывающее средство для смывания любой остающейся цельной крови из фильтра 264 после завершения извлечения из донора. Кроме того, размещение фильтра лейкоредукции в трубках 218 линии извлечения устраняет необходимость отдельного этапа фильтрации лейкоредукцией внизу по направлению потока, таким образом, дополнительно оптимизируя процесс сбора крови.
Ожидается, что автоматизированные однопроходные система и способ сбора цельной крови, описанные в настоящем описании, улучшат эффективность центра сбора крови и снизят расходы по эксплуатации путем выполнения разделения цельной крови на компоненты эритроцитов и плазмы без необходимости последующих ручных операций. Кроме того, использование малокалиберных игл в устройствах доступа к донору, используемых в системе, должно повысить комфорт донора, тогда как использование вытяжного насоса позволяет системе достичь времени взятия, аналогичного обычному сбору цельной крови. Кроме того, за счет управления сбором цельной крови посредством микропроцессора предоставляется больше возможностей для управления данными, которых обычно не имеется в текущих способах ручного сбора цельной крови, включая использование интегрированных считывателей штрихкодов и/или технологии RFID, в соответствии с описанным выше.
В соответствии с другим аспектом изложения, ниже описаны способы, системы и устройства, пригодные для промывания биологических клеток, таких как клетки крови или другие компоненты крови или биологические компоненты.
VI. Системы и способы для промывания клеток
Промывание биологических клеток может иметь несколько целей. Например, промывание клеток может использоваться для замены жидкой среды, в которой биологические клетки суспендированы. В этом случае вторая жидкая среда добавляется для замены и/или разбавления исходной жидкой среды. Части исходной жидкой среды и замещающей жидкой среды отделяются от клеток. Дополнительные замещающие жидкие среды могут добавляться до тех пор, пока концентрация исходной жидкой среды не станет ниже определенной процентной величины. В дальнейшем клетки могут быть суспендированы, например, в замещающей среде.
Промывание клеток также может быть использовано для концентрирования или дополнительного концентрирования клеток в жидкой среде. Клетки, суспендированные в жидкой среде, промываются, в результате чего часть жидкой среды отделяется и удаляется из клеток.
Кроме того, промывание клеток может быть использовано для удаления нежелательных твердых частиц, таких как крупные твердые частицы, или нежелательного клеточного материала из взвеси клеток конкретного размера, или для “очистки” желаемой взвеси клеток или другой жидкости.
Способ, системы и устройство, описанные ниже, могут быть применены для промывания клеток по любой из описанных выше причин. В частности, но без ограничения, способы, системы и устройство, описанные ниже, могут быть применены для промывания клеток крови, таких как эритроциты, или белые клетки крови (лейкоциты), или тромбоциты.
В одном конкретном варианте осуществления взвесь, содержащая белые клетки крови в жидкой культуральной среде, может промываться с целью замены культуральной среды на другую среду, такую как физиологический раствор, до начала использования или дополнительной обработки. Взвесь клеток, содержащая белые клетки крови в жидкой культуральной среде, может доставляться и вводиться в сепаратор, такой как сепаратор с вращающейся мембраной. Сепаратор с вращающейся мембраной имеет мембранный фильтр с размером пор, меньшим, чем размер белых клеток крови. В одном из вариантов осуществления, жидкая среда для промывания, содержащая замещающую жидкую среду, такую как физиологический раствор, также добавляется в сепаратор для разбавления жидкой культуральной среды. Сепаратор функционирует таким образом, что жидкости проходят через поры мембраны и извлекаются как отходы. В данном варианте осуществления, при извлечении жидкости добавляется среда для промывания, в результате чего полученная взвесь клеток содержит белые клетки крови, суспендированные в замещающей жидкой среде (например, физиологическом растворе).
В другом варианте осуществления, взвесь клеток может подвергаться концентрированию (посредством удаления супернатанта) и сбора взвеси концентрированных клеток в контейнер набора обработки. Замещающая жидкость может быть введена в сепаратор, объединена с концентрированными клетками в контейнере, и затем клетки могут быть ресуспендированы в замещающей жидкости. При необходимости ресуспендированные клетки/замещающая жидкость могут быть введены в сепаратор для дальнейшего концентрирования клеток, удаления супернатанта и ресуспендирования концентрированных клеток в дополнительной замещающей жидкости. Данный цикл может быть повторен при необходимости.
Аналогичные процессы могут быть применены для промывания эритроцитов, суспендированных в жидкой среде хранения. Взвесь клеток, содержащая эритроциты, суспендированные в жидкой среде хранения, может промываться с целью замещения жидкой среды хранения на другую среду, такую как физиологический раствор, до начала использования или дополнительной обработки. Взвесь клеток доставляется и вводится в сепаратор, такой как сепаратор с вращающейся мембраной. Сепаратор с вращающейся мембраной имеет мембранный фильтр с размером пор, меньшим, чем размер эритроцитов. В одном из вариантов осуществления, среда для промывания, то есть, замещающая жидкая среда, такая как физиологический раствор, также может добавляться в сепаратор для разбавления жидкой среды хранения. Сепаратор функционирует таким образом, что жидкость проходит через поры мембраны и извлекается как отход. При извлечении жидкости добавляется среда для промывания, в результате чего полученная взвесь клеток содержит эритроциты, суспендированные в замещающей жидкой среде (то есть, физиологическом растворе). Жидкость для промывания и/или замещающая жидкость также может являться средой для хранения, которая содержит питательные вещества и другие компоненты, которые позволяют осуществлять долговременное хранение клеток. Альтернативно, в другом варианте осуществления, эритроциты могут сначала быть сконцентрированы и удалены в контейнер, как в общих чертах описано выше. Замещающая жидкость может затем быть объединена с эритроцитами в контейнере. Замещающая жидкость может быть введена в контейнер напрямую, или может быть введена в сепаратор и через сепаратор, и затем в контейнер.
Системы, способы и устройство для промывания клеток, описанные в настоящем документе, используют одноразовый набор, который включает в себя сепаратор, такой как сепаратор с вращающейся мембраной. Одноразовый набор с сепаратором с вращающейся мембраной устанавливается на компонент аппаратного обеспечения системы, то есть, устройство разделения. Устройство разделения содержит фиксаторы, насосы, двигатели, датчики обнаружения воздуха, измерительные датчики давления, Hb-детекторы, весы, и управляющую логическую схему/микропроцессор, включенную в микропроцессор. Управляющая логическая схема/микропроцессор принимает входные данные и сигналы от оператора и/или различных датчиков, и управляет функционированием фиксаторов, насосов и двигателей.
Взвесь клеток, которая будет промываться, то есть клетки, суспендированные в среде, могут быть представлены в стерильном одноразовом исходном контейнере, который соединен, стерильным образом, с одноразовым набором. Среда для промывания, такая как физиологический раствор, или другая подходящая среда, также соединяется стерильным образом или предварительно прикрепляется к одноразовому набору. Управляющая логическая схема устройства управляет фиксаторами и насосами для передачи взвеси клеток через трубки одноразового набора на сепаратор (с вращающейся мембраной). Устройство разделения, через свою систему управления, также направляет раствор для промывания через трубки одноразового набора на сепаратор с вращающейся мембраной. Взвесь клеток и раствор для промывания могут быть смешаны внутри сепаратора с вращающейся мембраной, могут быть смешаны до введения в сепаратор с вращающейся мембраной, или могут быть объединены в контейнере после того, как взвесь клеток была сконцентрирована. Внутри сепаратора с вращающейся мембраной среда суспендирования отделяется от клеток, суспендированных в ней. Среда суспендирования и оставшаяся среда для промывания (если среда суспендирования и среда для промывания были объединены) выходит через канал для отходов, тогда как клетки проходят через отдельный выходной канал.
Если необходимо дальнейшее промывание и разбавление, то промытые клетки могут быть повторно пропущены через сепаратор с дополнительным объемом раствора для промывания. В одном из вариантов осуществления, клетки, которые должны промываться повторно, могут передаваться в один или более рабочих контейнеров, как будет описано ниже. Управляющая логическая схема устройства управляет фиксаторами и насосами для передачи взвеси клеток из рабочего контейнера через трубки на впускной клапан сепаратора с вращающейся мембраной или на впускной клапан второго сепаратора с вращающейся мембраной. Добавляется дополнительная среда для промывания, и процесс повторяется до тех пор, пока не будет достигнут приемлемый объем или концентрация клеток. Конечная взвесь клеток, содержащая клетки, предпочтительно, собирается в контейнере конечного продукта.
В соответствии с настоящим изложением, на фиг. 23-25 показаны примеры систем, подходящих для промывания биологических клеток, таких как эритроциты и белые клетки крови, но не ограничиваясь указанным. Как отмечалось выше, предполагается, что изложенные конкретные варианты осуществления являются примерами и не являются ограничивающими. Таким образом, в одном из вариантов осуществления, система, описанная в настоящем описании, содержит одноразовый набор 300 (фиг. 23 или 24) и компонент аппаратного обеспечения или устройство 400 (фиг. 25). Следует понимать, что одноразовые наборы 300 обработки, показанные на обеих фиг. 23 и 24, идентичны во многих отношениях, и общие цифровые обозначения используются на обеих фиг. 23 и 24 для идентификации идентичных или аналогичных элементов одноразовых наборов обработки. В той степени, в которой одноразовые наборы обработки различаются в структуре или в их использовании, такие различия обсуждаются ниже. Одноразовый набор 300 устанавливается на устройство 400 (фиг. 25), которое подробнее описывается ниже
Как показано на фиг. 23-24, сепаратор 301 является частью типового одноразового набора 300. Дополнительно, как будет подробнее описано ниже, одноразовый набор 300 содержит трубки, Y-соединители, рабочий(-е) пакет(-ы), мешок(-ки) с пробами, пакет(-ы) конечного продукта, пакет(-ы) с отходами и стерильный(-е) фильтр(-ы).
Взвесь клеток, которая будет промываться, обычно представлена в исходном контейнере 302, показанном на фиг. 23 и 24 отсоединенным от одноразового набора. Как отмечалось выше, исходный контейнер 302 может быть прикреплен (стерильным образом) во время использования. Исходный контейнер 302 имеет один или более каналов 303, 305 приема, один из которых может быть приспособлен для приема гвоздевого соединителя 304 (фиг. 23) одноразового набора 300. Конкретнее, исходный контейнер 302 соединен с одноразовым набором 300 через гвоздевой соединитель 304, который может соединяться с каналом 303 доступа. Более предпочтительно, однако, чтобы исходные контейнеры (и жидкости в них) не имели гвоздевого соединителя (как показано на фиг. 24), и чтобы доступ к ним осуществлялся стерильным образом посредством использования стерильных стыковочных устройств, таких как BioWelder, поставляемое компанией Sartorius AG, или SCD IIB Tubing Welder, поставляемое компанией Terumo Medical Corporation. Также может быть представлен второй канал 305 доступа для извлечения жидкости из исходного пакета 302.
Как также показано на фиг. 23-24, сегмент 306 трубки может, необязательно, содержать подблок взятия проб в ответвительном соединителе 308. Одна из ветвей ответвительного соединителя 308 может содержать маршрут потока 310, приводящий к мешку или месту 312 с пробами. Мешок или место 312 с пробами позволяет осуществлять сбор проб из входящей исходной жидкости. Поток к мешку или месту 312 с пробами обычно контролируется фиксатором 314. Другая ветвь ответвительного соединителя 308 соединена с трубками 316. Трубки 316 соединены с еще одним расположенным по ходу потока ответвительным соединителем 318. Ответвительный соединитель 318 взаимодействует с трубками 316 и трубками 320, что обеспечивает маршрут потока жидкости из рабочего пакета 322, что подробнее описано ниже. Сегмент трубки 324 выходит из одного из каналов ответвительного соединителя 318 и соединяется с каналом еще одного расположенного по ходу потока ответвительного соединителя 326. Отдельный маршрут потока, задаваемый трубками 328, также соединен с каналом ответвительного соединителя 326. Трубки 328 могут содержать встроенный стерильный барьерный фильтр 330 для фильтрации любых частиц из жидкости до того, как она попадет в маршрут потока, приводящий ко второму ответвительному соединителю 326 и, в итоге, к сепаратору 301.
В соответствии с системой, изложенной в настоящем описании, раствор для промывания может быть прикреплен (или предварительно прикреплен) к набору 300. Как показано на фиг. 23 и 24, трубки 332 (определяющие маршрут потока), предпочтительно, содержат гвоздевой соединитель 334 на своем конце. Гвоздевой соединитель 334 представлен для установления взаимодействия потоков с контейнером жидкости для промывания, таким как одноразовый пакет, содержащий физиологический раствор или другой раствор (не показан). Среда или жидкость для промывания вытекает из источника жидкости для промывания через второй гвоздевой соединитель 334, через сегмент трубки 332, где она фильтруется посредством стерильного барьерного фильтра 330, описанного выше, и затем проходит через трубки 328 к выходу ответвительного соединителя 326, описанного выше.
Сегмент трубки 336 задает маршрут потока, соединенный с одного конца с каналом ответвительного соединителя 326 и с впускным каналом сепаратора 301. Предпочтительно, в соответствии с настоящим изложением, сепаратор 301 представляет собой сепаратор с вращающейся мембраной описанного выше типа.
Как показано на фиг. 23, 24 и 25, сепаратор 301 с вращающейся мембраной имеет, по меньшей мере, два выпускных канала. Выпускной клапан 646 сепаратора 301 принимает отходы от промывания (то есть, разбавленную среду взвеси), и соединен с трубками 338, который задают маршрут потока к контейнеру 340 для отходов. Контейнер для отходов содержит еще один соединительный канал 341 для получения проб или извлечения отходов из контейнера продукта.
Сепаратор 301, предпочтительно, содержит второй выпускной клапан 648, который соединен с сегментом трубки 342. Другой конец сегмента трубки 342 соединен с ответвительным соединителем 344, который разветвляется и задает маршрут потока к одному или более рабочим контейнерам 322 и маршрут потока к контейнеру 350 конечного продукта. Контейнер 350 конечного продукта также может содержать мешок 352 с пробами (см. фиг. 23) и канал доступа или люэровский соединитель 354. Мешок 352 с пробами, показанный предварительно прикрепленным к держателю 352 трубок на фиг. 23, позволяет выполнять сбор проб конечного продукта. Контроль потока к мешку 352 с пробами, предпочтительно, осуществляется фиксатором 356. Маршрут потока через канал 354 доступа контролируется фиксатором 358.
Обратимся теперь к способу промывания с использованием набора 300 с фиг. 23 и 24; одноразовый набор 300 сначала устанавливается на панель 401 устройства разделения (то есть, аппаратного обеспечения) 400, показанную на фиг. 25. Устройство 400 содержит перистальтические насосы, фиксаторы и датчики, которые контролируют поток через одноразовый набор. Конкретнее, управление насосами, фиксаторами и т.п. обеспечивается программно-управляемым микропроцессором/контроллером устройства 400. Сегменты трубки 362, 366 и 368 (показанные на фиг. 23) избирательно стыкуются с перистальтическими насосами 402, 404 или 406 (показанными на фиг. 25). (Сегмент 368 насоса линии отходов может быть перемещен к линии 343 выпускного клапана сепаратора, при необходимости). После того, как одноразовый набор 300 устанавливается на панели 401 управления устройства 400, взвесь клеток в пакете 302 продукта прикрепляется, как было описано ранее, посредством гвоздевого соединителя 304 или посредством стерильного соединения. Среда для промывания, представленная в контейнере (не показана), прикрепляется аналогично. В соответствии с функционированием устройства 400, фиксатор 360 открывается и позволяет взвеси клеток протечь из контейнера 302 продукта.
Поток взвеси клеток продвигается посредством воздействия перистальтического насоса через трубки 324, определяемые сегментом насоса 362, в сепаратор 301 с вращающейся мембраной. Аналогично, среда для промывания продвигается посредством воздействия перистальтических насосов через длину трубки 328, определяемую сегментом насоса 366, с клапанами 362 и 364 в открытом положении. Среда для промывания протекает через трубки 332, стерильный барьерный фильтр 330, трубки 328, Y-соединитель 326 и в сепаратор 301 с вращающейся мембраной. Среда для промывания и взвесь клеток могут быть последовательно введены в сепаратор 301 с вращающейся мембраной, допуская возникновение смешивания взвеси и раствора для промывания в пределах камеры (зазора) сепаратора 301 или в рабочем контейнере 322, как описано ниже. Альтернативно, среда для промывания и взвесь клеток могут быть объединены до введения в сепаратор 301, (например), через второй ответвительный соединитель 326.
В еще одной альтернативе, взвесь клеток может быть сначала введена из исходного контейнера 302 в сепаратор 301, как в общих чертах описано выше. Взвесь клеток концентрируется внутри сепаратора 301, что позволяет супернатанту пройти через мембрану, через выпускной канал 382, в контейнер 340 для отходов. Концентрированные клетки выходят из сепаратора 301 через канал 384 и направляются в рабочий контейнер 322.
После того, как отделение концентрированных клеток от супернатанта взвеси клеток завершается, замещающая жидкость вводится из контейнера с замещающей жидкостью (не показан) в сепаратор 301 (для смывания всех оставшихся клеток) и аналогично направляется через канал 384 в рабочий контейнер 322. Концентрированные клетки ресуспендируются в замещающей жидкости внутри рабочего контейнера 322, как показано на фиг. 23. Если желательно или требуется дополнительное промывание, то система может быть предварительно запрограммирована или направлена другим способом на (повторное) введение ресуспендированных клеток/замещающей жидкости в сепаратор 301, в котором отделение концентрированных клеток от супернатанта повторяется. Конечный клеточный продукт собирается в контейнере 350 конечного продукта, где он может быть ресуспендирован с дополнительной замещающей жидкостью.
Независимо от последовательности введения взвеси клеток/раствора для промывания или используемого одноразового набора, вращательное воздействие устройства приводит к отделению клеток от оставшейся части жидкости, в которой они были суспендированы, и/или от раствора для промывания. Предпочтительно, супернатант и раствор для промывания проходят через мембрану, тогда как искомые клетки концентрируются внутри камеры сепаратора. Отходы, возникающие при разделении и включающие среду для промывания и среду супернатанта, выходят из канала 382 и протекают через трубки 338 в контейнер 340 для отходов. Поток отходов управляется перистальтическим насосом через часть трубок 338, определяемую сегментом насоса 368, к пакету 340 с продуктами отходов.
Как описано выше, взвесь концентрированных и разделенных клеток выходит из второго выпускного клапана 384 сепаратора 301 с вращающейся мембраной. Если дальнейшее промывание не требуется, то система управления закрывает фиксатор 370 и открывает фиксатор 372. Закрытие фиксатора 370 предотвращает протекание взвеси промытых клеток через трубки 346 и направляет ее через трубки 348 в пакет 350 конечного продукта. Контейнер 350 конечного продукта имеет вход для приема взвеси отделенных и промытых клеток. Контейнер 354 конечного продукта соединен с датчиком 374 веса. Устройство разделения измеряет вес 374 контейнера с целью определения того, находится ли объем собранных клеток в контейнере 350 конечного продукта в приемлемом диапазоне и, следовательно, закончен ли цикл промывания.
Если желательно или требуется дополнительное промывание взвеси разделенных клеток, то система управления устройства разделения закрывает фиксатор 372 и фиксатор 376, и открывает фиксатор 370. Закрытие фиксатора 372 предотвращает протекание взвеси клеток через трубки 348 и направляет ее через трубки 346 в рабочий пакет 322. Рабочий пакет 322 имеет впускной клапан для приема взвеси разделенных клеток. Рабочий пакет 322 соединен с датчиком 378 веса. Система управления устройства разделения определяет вес, воспринимаемый датчиком веса, с целью определения того, достаточно ли взвеси разделенных клеток присутствует в рабочем пакете 322 для проведения еще одного цикла промывания. Если определено, что присутствует достаточно взвеси, и желательно дополнительное промывание, то система управления устройства разделения открывает фиксатор 376 с целью открытия и направления взвеси разбавленных и разделенных клеток через выход рабочего пакета 322, через трубки 320 в ответвительный соединитель 318, и через датчик 380 обнаружения воздуха. Датчик 380 обнаружения воздуха обнаруживает воздух во взвеси клеток, которая проходит через трубки 324. Устройство управления и эксплуатации измеряет показания датчика 380 обнаружения воздуха и определяет, какие процессы должны быть выполнены далее.
Взвесь разделенных клеток, которая содержит клетки, суспендированные в разбавленной среде суспендирования, затем повторно проходит через процесс промывания, как описано выше. Процесс промывания может быть повторен столько раз, сколько необходимо, и, предпочтительно, до тех пор, пока взвесь разбавленных и разделенных клеток не будет иметь приемлемую остаточную концентрацию среды суспендирования. Конечная взвесь разбавленных и разделенных клеток собирается в пакете 350 конечного продукта.
Альтернативно, в отличие от повторения обработки жидкости через один рабочий контейнер, можно следовать процедуре обработки “пакетного типа” путем использования двух или более рабочих контейнеров 322 (в комбинации с контейнером 350 конечного продукта).
Одноразовый набор 300 обработки с фиг. 24, в частности, хорошо подходит для такой обработки “пакетного типа”. В соответствии с процедурой промывания клеток с использованием одноразового набора 300 с фиг. 24, клетки, первоначально выделенные из исходной среды суспендирования, удаляются из сепаратора 301 и вводятся в один из рабочих контейнеров 322a. Замещающая жидкость вводится в контейнер 322a, и клетки ресуспендируются. Ресуспендированные клетки в контейнере 322a могут затем быть введены в сепаратор 301, в котором они отделяются от супернатанта. Концентрированные клетки выходят через выпускной клапан 648 в сепаратор 301 и вводятся в новый (второй) рабочий контейнер 322b. Дополнительная замещающая жидкость может быть введена в рабочий контейнер 322b, и процесс может быть повторен, при необходимости, с еще одним новым (третьим) рабочим контейнером (не показан). Конечный клеточный продукт затем собирается в контейнере 350 конечного продукта, как описано выше.
В соответствии с описанным выше способом промывания клеток “пакетного типа”, сегменты трубки 370a, 370b и 320a, 320b могут быть соединены с фиксаторами (не показаны) для управления потоком во множество рабочих контейнеров 322a и 322b и потоком из них. Таким образом, например, фиксатор на линии 370a будет открыт, тогда как фиксатор на линии 370b будет закрыт, с тем чтобы клетки, выходящие из сепаратора 301, направлялись в (первый) рабочий контейнер 322a.
С целью дополнительного промывания, клетки, ресуспендированные в свежей замещающей жидкости из контейнера 322a, вводятся в сепаратор 301, где клетки отделяются от супернатанта, как было описано ранее. Система управления устройства 400 закрывает фиксатор (не показан на фиг. 24) на сегменте трубки 370a и открывает фиксатор (не показан на фиг. 24) на сегменте трубки 370b, с тем чтобы обеспечить возможность потока клеток в новый (второй) рабочий контейнер 322b. После итогового промывания фиксаторы (не показаны) на сегментах 370a, 370b, и т.д. закрываются, и фиксатор 372 (как показано, например, на фиг. 23) открывается, обеспечивая возможность сбора конечного продукта в контейнере 350.
На фиг. 24 показана передняя панель 401 устройства 400 разделения; то есть, аппаратное обеспечение, которое включает в себя перистальтические насосы 402, 404 и 406. Как описано выше, сегменты насоса 362, 364 и 368 из одноразового набора избирательно соединяются с перистальтическими насосами 402, 404 и 406. Перистальтические насосы сочленяются с жидкостным набором с фиг. 23 в сегментах насоса 362, 364 и 368, и продвигают взвесь клеток внутри одноразового набора, как будет понятно специалистам в данной области техники. Устройство 400 управления и эксплуатации также содержит фиксаторы 410, 412, 414. Фиксаторы 410, 412, 414 и 416 используются для управления потоком взвеси клеток через различные сегменты одноразового набора, как описано выше.
Устройство 400 также содержит несколько датчиков для измерения различных условий. Выходные данные датчиков используются устройством 400 при выполнении цикла промывания. Один или более измерительных датчиков 426 давления могут быть представлены на устройстве 400 и могут быть соединены с одноразовым набором 300 в определенных точках для отслеживания давления во время процедуры. Измерительный датчик 426 давления может быть встроен в место контроля давления внутри линии (например, в сегмент трубки 336) для отслеживания давления внутри сепаратора 301. Датчик детектора 438 воздуха также может быть соединен с одноразовым набором 300, при необходимости. Детектор 438 воздуха является необязательным и может быть представлен для обнаружения положения поверхностей раздела жидкость/воздух.
Устройство 400 содержит весы 440, 442, 444 и 446, на которых могут быть рассчитаны и взвешены конечный пакет, рабочий пакет, пакет взвеси клеток и любой дополнительный пакет, соответственно. Веса пакетов отслеживаются датчиками веса и записываются в течение процедуры промывания. По измерениям датчиков веса устройство определяет, является ли каждый из пакетов пустым, частично заполненным или полным, и управляет компонентами устройства управления и эксплуатации 200, такими как перистальтические насосы и фиксаторы 410, 412, 414, 416, 418, 420, 422 и 424.
Устройство 400 содержит по меньшей мере один блок привода, или “вращатель” 448, который осуществляет непрямое управление сепаратором с вращающейся мембраной 301. Вращатель 448 может состоять из приводного двигателя, соединенного с устройством 400 и управляемого им, и подсоединенного для поворачивания кольцевого элемента магнитного привода, содержащего, по меньшей мере, пару постоянных магнитов. При вращении кольцевого элемента привода магнитное притяжение между соответствующими магнитами внутри корпуса сепаратора с вращающейся мембраной вызывает вращение вращателя внутри корпуса сепаратора с вращающейся мембраной.
На фиг. 26-28 в форме диаграмм излагается способ промывания клеток в соответствии с изложенным в настоящем описании. Этапы, описанные ниже, выполняются посредством программно-управляемого микропроцессорного блока устройства 400, при этом определенные этапы выполняются оператором, как было отмечено выше. Обратимся сначала к фиг. 26; устройство включается на этапе 500. Устройство проводит проверки автоматической калибровки 502, включающие в себя проверку перистальтических насосов, фиксаторов и датчиков. Затем устройство 400 запрашивает у пользователя ввод выбранных процедурных параметров (этап 504), таких как выполняемая процедура промывания, объем промываемой взвеси клеток, число промываний, которое должно быть выполнено, и т.д. Оператор может затем выбирать и вводить процедурные параметры для процедуры промывания (этап 506).
Устройство (через контроллер) подтверждает ввод параметров 506, и затем запрашивает у оператора загрузку (этап 510) одноразового набора. Оператор затем загружает одноразовый набор (этап 512) в панель устройства 400. После установки одноразового набора, устройство подтверждает установку, как показано (этап 514).
После того, как одноразовый набор установлен, устройство автоматически проверяет правильность установки одноразового набора (этап 516). После того, как устройство определяет, что одноразовый набор был установлен правильно, контроллер запрашивает у оператора подсоединение взвеси клеток и среды для промывания (этап 518). Затем оператор подсоединяет среду для промывания (такую как физиологический раствор, но не ограничиваясь им) (этап 520) к одноразовому набору через гвоздевой соединитель, как было описано ранее. Затем оператор подсоединяет взвесь клеток внутри пакета с продуктом (этап 522) к одноразовому набору через гвоздевой соединитель.
Как показано на фиг. 27, после того, как взвесь клеток и среда для промывания были подсоединены к одноразовому набору, оператор подтверждает, что растворы были подсоединены (этап 524). Устройство запрашивает у оператора взятие образца взвеси клеток (этап 526). Затем оператор или устройство открывает фиксатор 528 мешка для сбора проб с целью введения жидкости в мешок для сбора проб (этап 546). После того, как мешок для сбора проб был заполнен, он запечатывается и удаляется (542) из одноразового набора. Оператор подтверждает (этап 544), что образец был взят. После удаления мешка для сбора проб одноразовый набор заливается (этап 546) для процесса промывания.
Затем контроллер устройства разделения начинает процесс промывания. Взвесь клеток, предназначенная для промывания, передается из своего контейнера (например, 302 с фиг. 23) через одноразовый набор на сепаратор 301 с вращающейся мембраной. Аналогично, среда для промывания передается из своего источника через одноразовый набор на сепаратор 301 с вращающейся мембраной. В предпочтительном варианте осуществления, исходные клетки взвеси клеток концентрируются и/или собираются в рабочем пакете (для дальнейшей обработки) или собираются в пакете конечного продукта, который впоследствии удаляется из одноразового набора. Если необходимо (дополнительное) промывание или разбавление взвеси клеток, то взвесь клеток в рабочем пакете может промываться (второй раз) той же самой или другой средой для промывания в соответствии с процессом, кратко описанным выше. До завершения каждого цикла промывания, измеряется и записывается объем или вес взвеси клеток (этап 550). Когда концентрация клеток в среде для промывания достигает приемлемого уровня, заполняется пакет конечного продукта.
Как показано на фиг. 28, как только собран желаемый объем конечного продукта, устройство управления и эксплуатации запрашивает у оператора взятия пробы и запечатывания пакета конечного продукта (этап 552). Мешок для сбора проб прикрепляется к пакету конечного продукта. Оператор затем запечатывает и удаляет из одноразового набора взвесь промытых клеток в пакет с конечным продуктом (этап 552). Затем пакет с конечным продуктом взбалтывается (этап 556). Оператор открывает мешок для сбора образцов путем удаления фиксатора (этап 558). Допускается заполнение мешка для сбора образцов (этап 560). После того, как пакет с образцами заполнен, фиксатор закрывается и мешок для сбора образцов запечатывается и удаляется (этап 562). Затем оператор запечатывает линии одноразового набора (этап 564) и подтверждает, что пакет продукта был запечатан и удален, мешок для взятия проб был заполнен и удален, и что линии одноразового набора были запечатаны (этап 566). Затем устройство управления и эксплуатации запрашивает у оператора удаление одноразового набора, как показано на этапе 568. Затем оператор удаляет и выбрасывает одноразовый набор, как показано на этапе 570.
Таким образом, изложен улучшенный сепаратор с вращающейся мембраной, а также способы и системы для применения такой вращающейся мембраны. Описание, представленное выше, приведено в целях иллюстрации, и не предполагается, что оно ограничивает объем изложения каким-либо конкретным способом, системой или установкой или устройством, описанными в настоящем описании.
| название | год | авторы | номер документа |
|---|---|---|---|
| УСТРОЙСТВА МЕМБРАННОГО РАЗДЕЛЕНИЯ, СИСТЕМЫ И СПОСОБЫ, ПРИМЕНЯЮЩИЕ УКАЗАННЫЕ УСТРОЙСТВА, И СИСТЕМЫ И СПОСОБЫ УПРАВЛЕНИЯ ДАННЫМИ | 2012 |
|
RU2595704C2 |
| УСТРОЙСТВА МЕМБРАННОГО РАЗДЕЛЕНИЯ, СИСТЕМЫ И СПОСОБЫ, ПРИМЕНЯЮЩИЕ УКАЗАННЫЕ УСТРОЙСТВА, И СИСТЕМЫ И СПОСОБЫ УПРАВЛЕНИЯ ДАННЫМИ | 2012 |
|
RU2591658C2 |
| УСТРОЙСТВА МЕМБРАННОГО РАЗДЕЛЕНИЯ, СИСТЕМЫ И СПОСОБЫ, ПРИМЕНЯЮЩИЕ УКАЗАННЫЕ УСТРОЙСТВА, И СИСТЕМЫ И СПОСОБЫ УПРАВЛЕНИЯ ДАННЫМИ | 2012 |
|
RU2601449C2 |
| УСТРОЙСТВА МЕМБРАННОГО РАЗДЕЛЕНИЯ, СИСТЕМЫ И СПОСОБЫ, ПРИМЕНЯЮЩИЕ УКАЗАННЫЕ УСТРОЙСТВА, И СИСТЕМЫ И СПОСОБЫ УПРАВЛЕНИЯ ДАННЫМИ | 2012 |
|
RU2598455C2 |
| УСТРОЙСТВА МЕМБРАННОГО РАЗДЕЛЕНИЯ, СИСТЕМЫ И СПОСОБЫ, ПРИМЕНЯЮЩИЕ УКАЗАННЫЕ УСТРОЙСТВА, И СИСТЕМЫ И СПОСОБЫ УПРАВЛЕНИЯ ДАННЫМИ | 2012 |
|
RU2597140C2 |
| СИСТЕМЫ И СПОСОБЫ ДЛЯ ОПТИМИЗАЦИИ ОБЪЕМОВ ЗАБОРА ПЛАЗМЫ | 2019 |
|
RU2776451C2 |
| Y-ОБРАЗНЫЙ СОЕДИНИТЕЛЬ ДЛЯ СИСТЕМЫ ДЛЯ ОБРАБОТКИ КРОВИ И ОДНОРАЗОВЫЙ НАБОР, СОДЕРЖАЩИЙ ЕГО | 2017 |
|
RU2742015C2 |
| СИСТЕМЫ И СПОСОБЫ ДЛЯ ОПТИМИЗАЦИИ ОБЪЕМОВ ЗАБОРА ПЛАЗМЫ | 2019 |
|
RU2752596C1 |
| Мобильное устройство для гравитационной сепарации крови и способ его применения | 2019 |
|
RU2710356C1 |
| УСТРОЙСТВО ДЛЯ ВКЛЮЧЕНИЯ БИОЛОГИЧЕСКИ АКТИВНЫХ КОМПОНЕНТОВ В ЭРИТРОЦИТЫ СПОСОБОМ ПРОТОЧНОГО ДИАЛИЗА | 2021 |
|
RU2772209C1 |
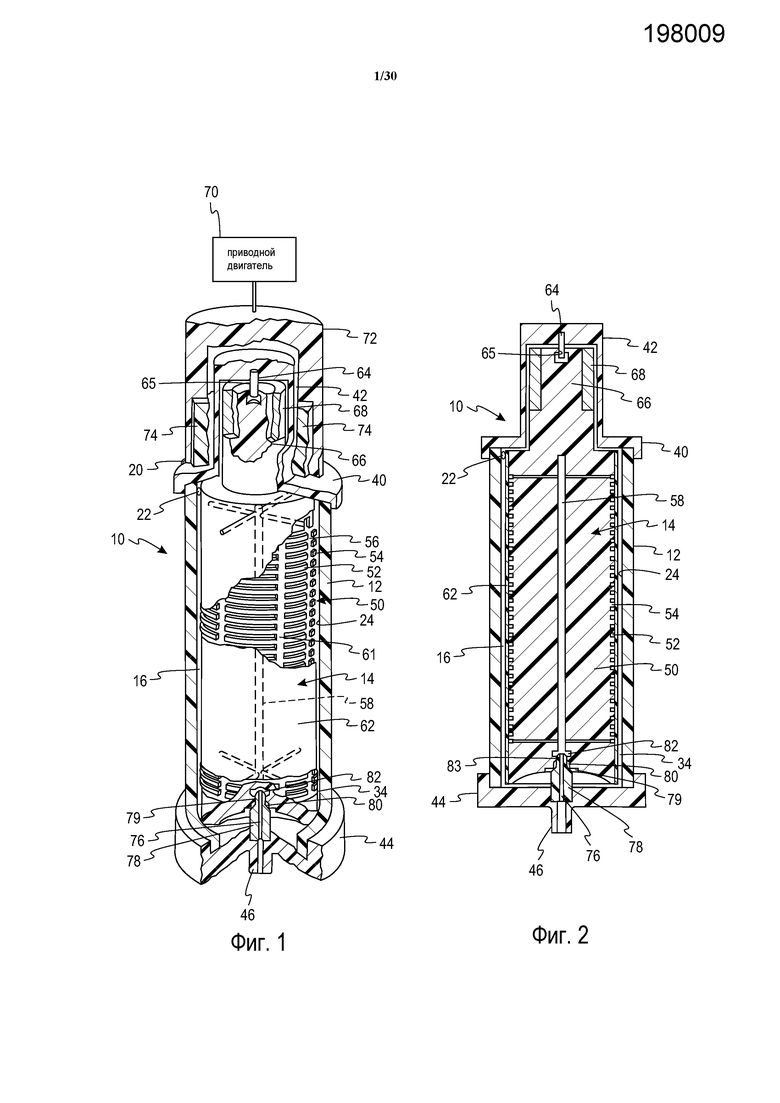
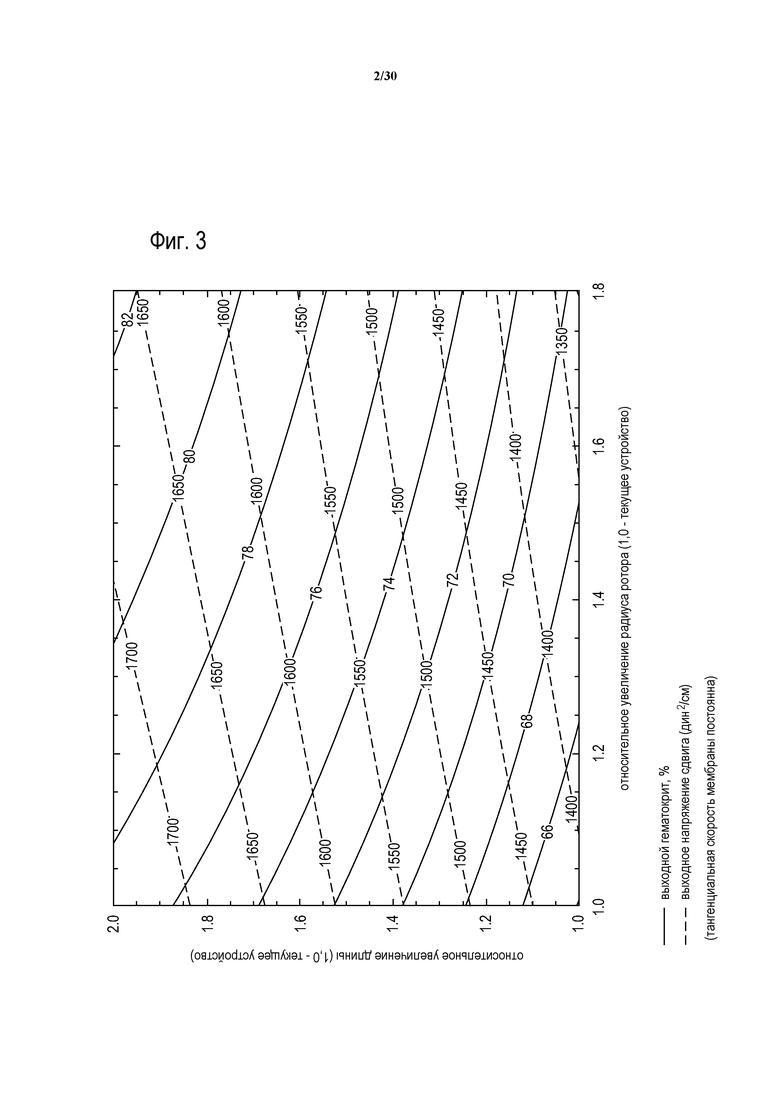

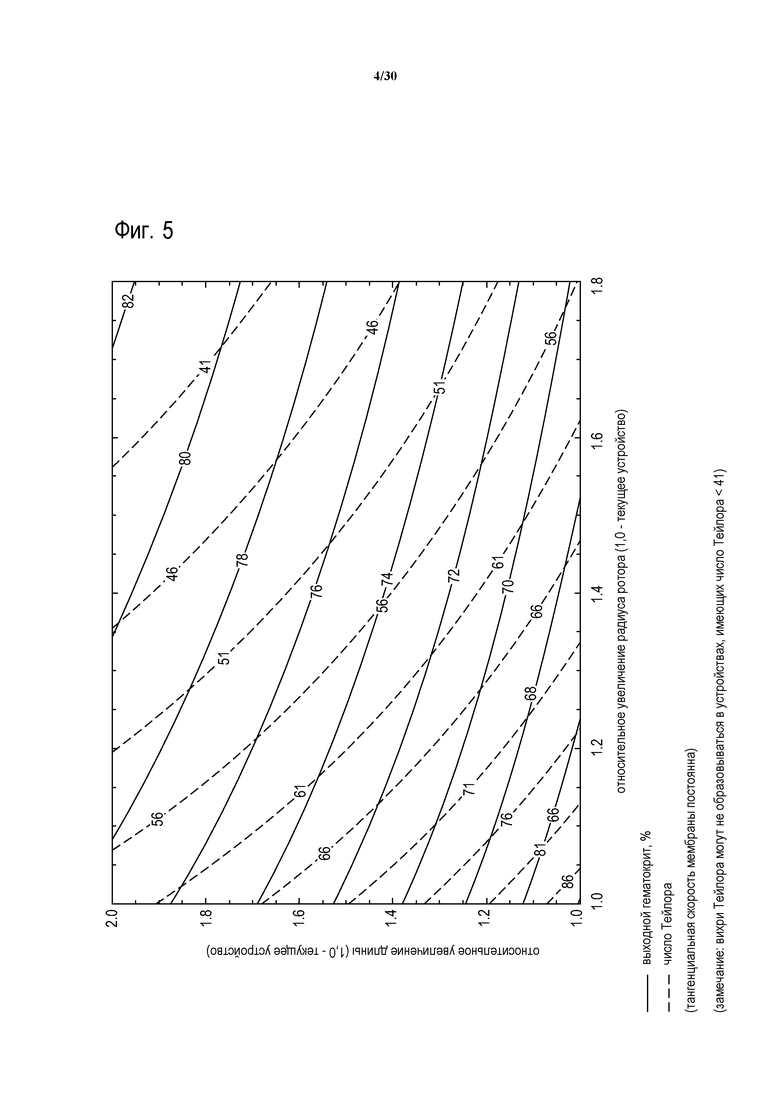
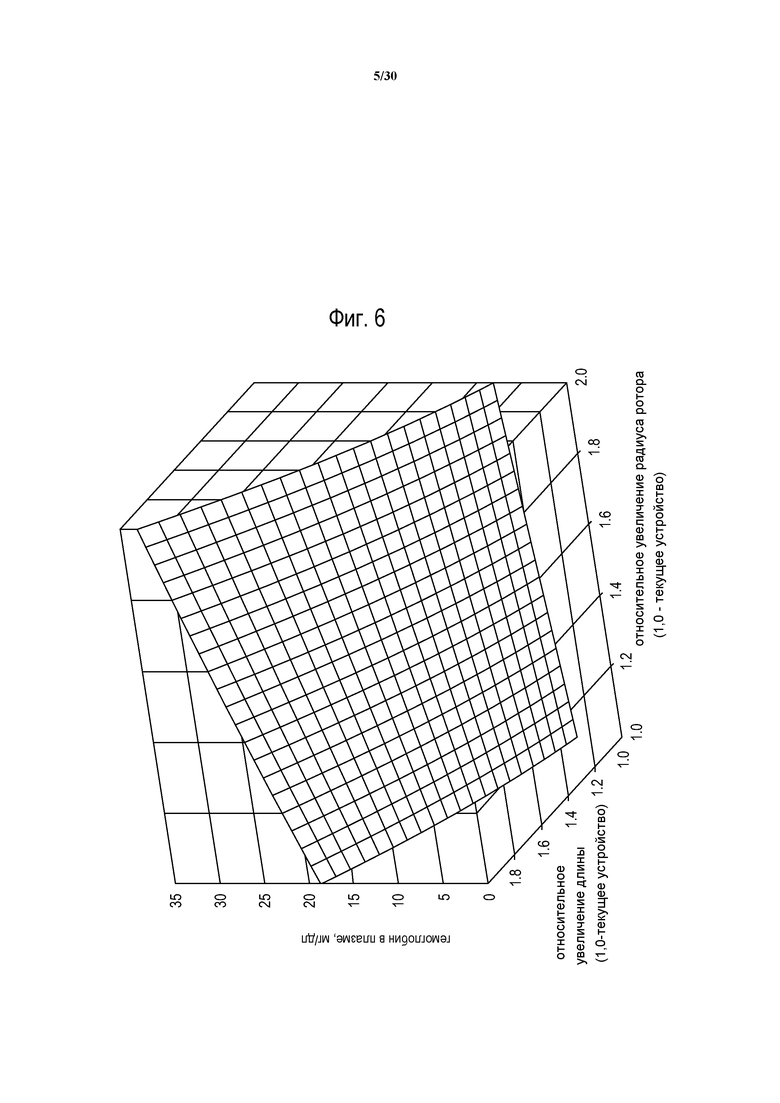
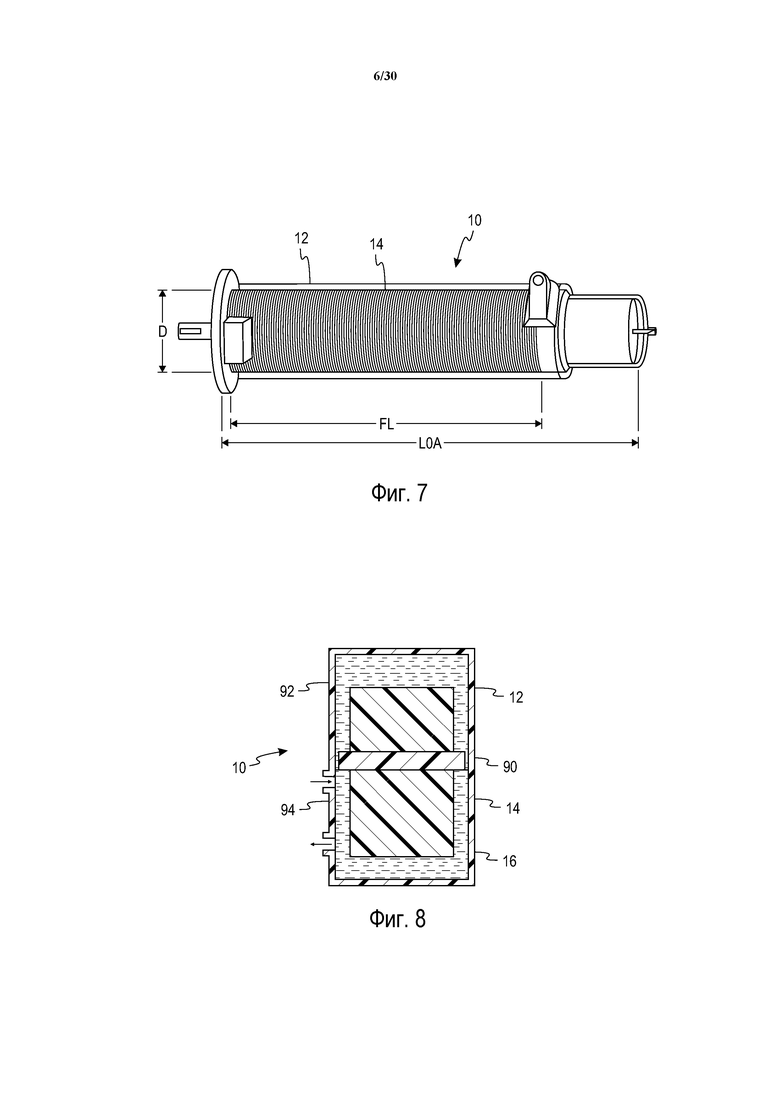

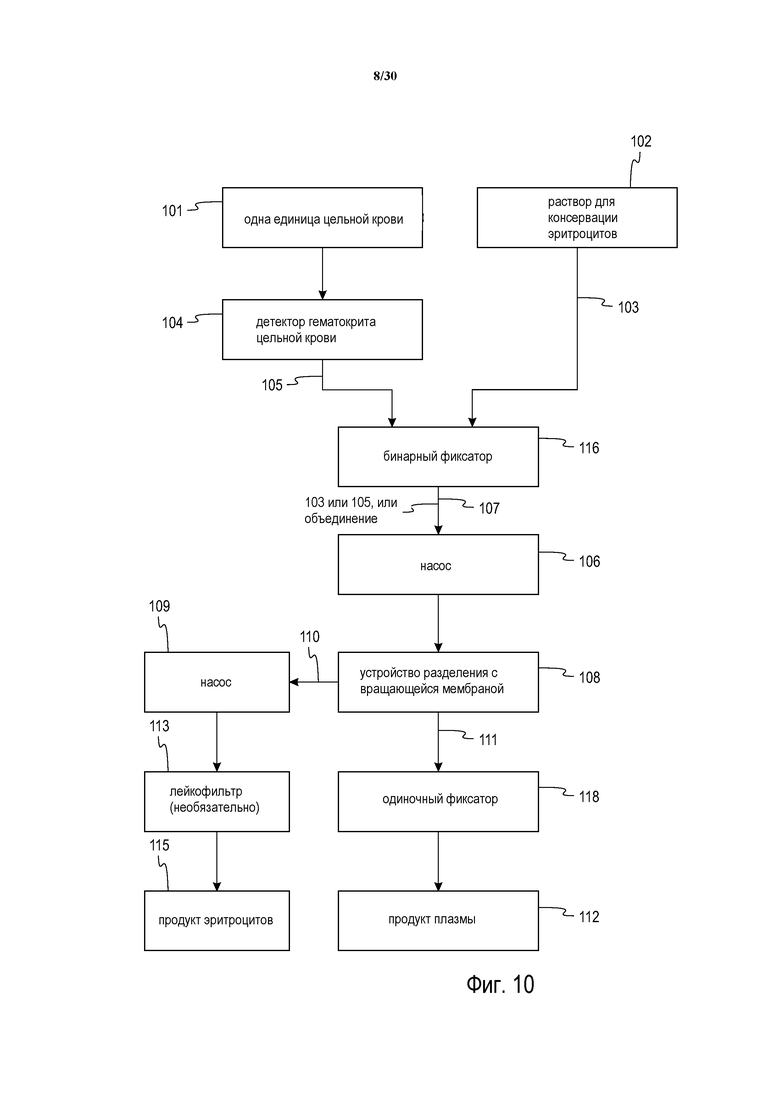
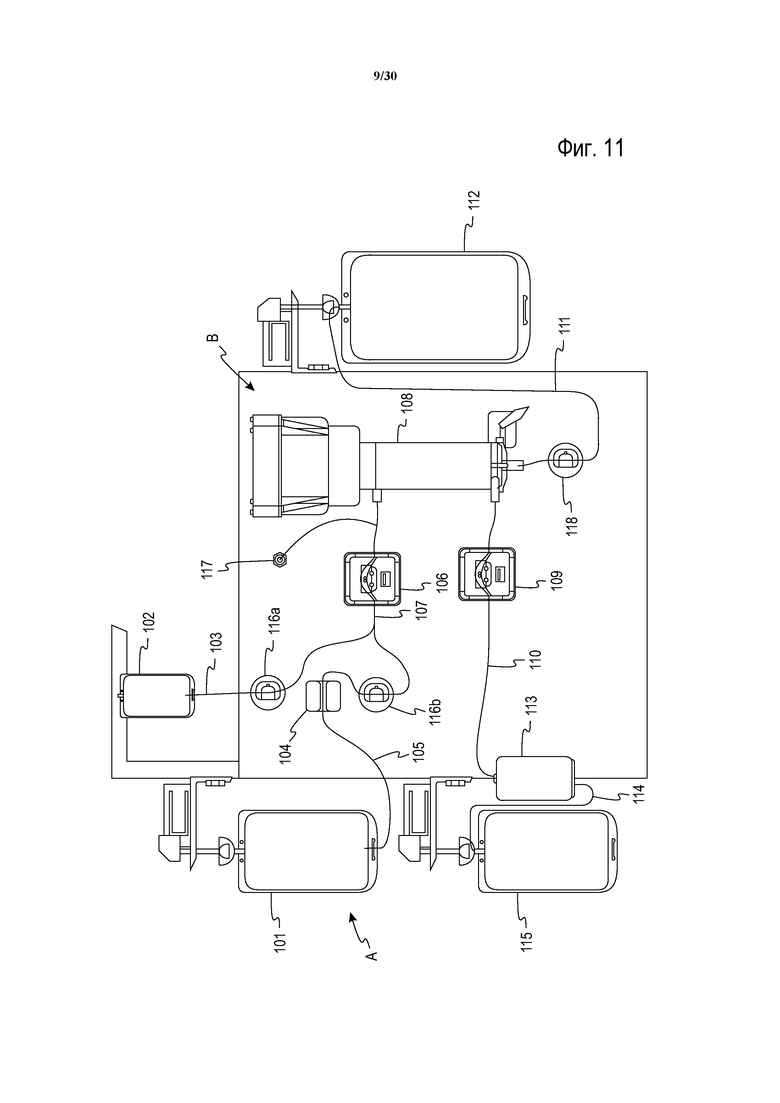
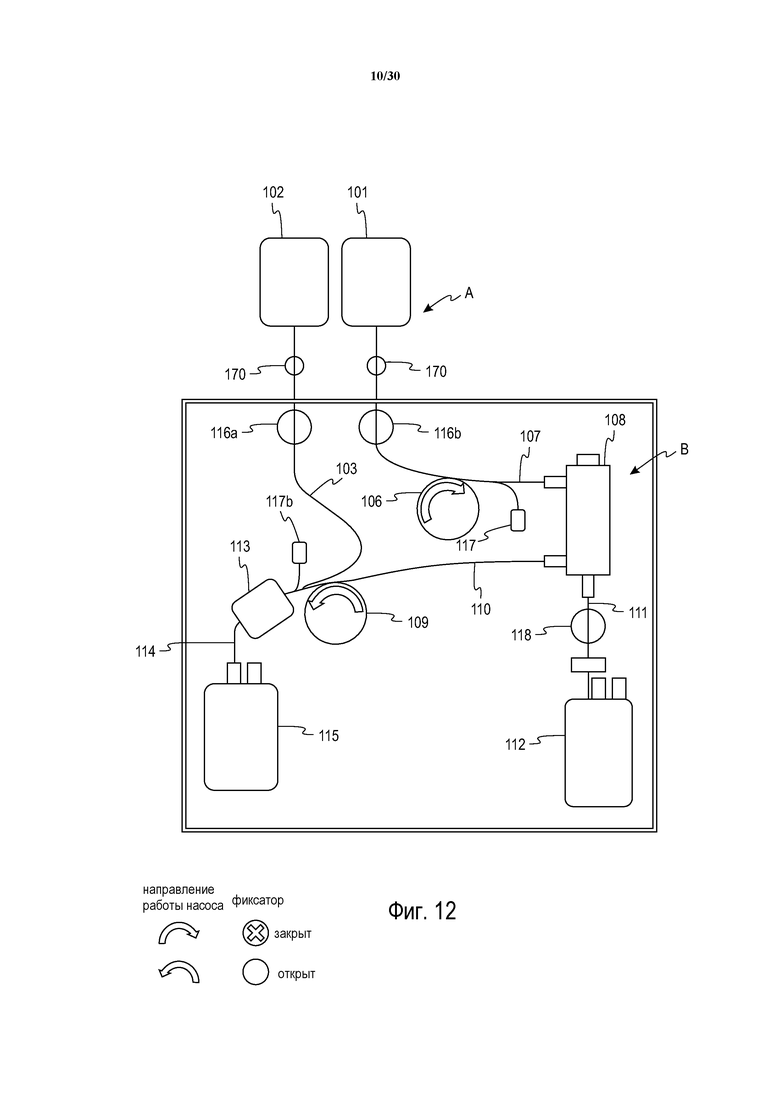
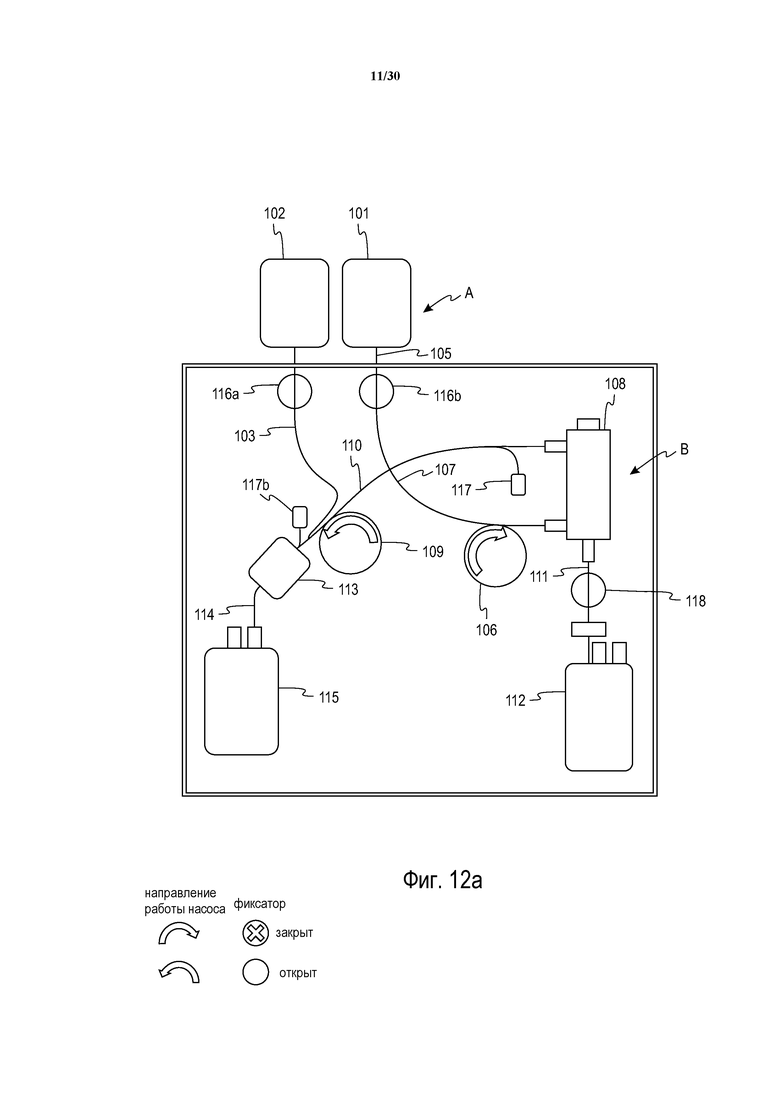
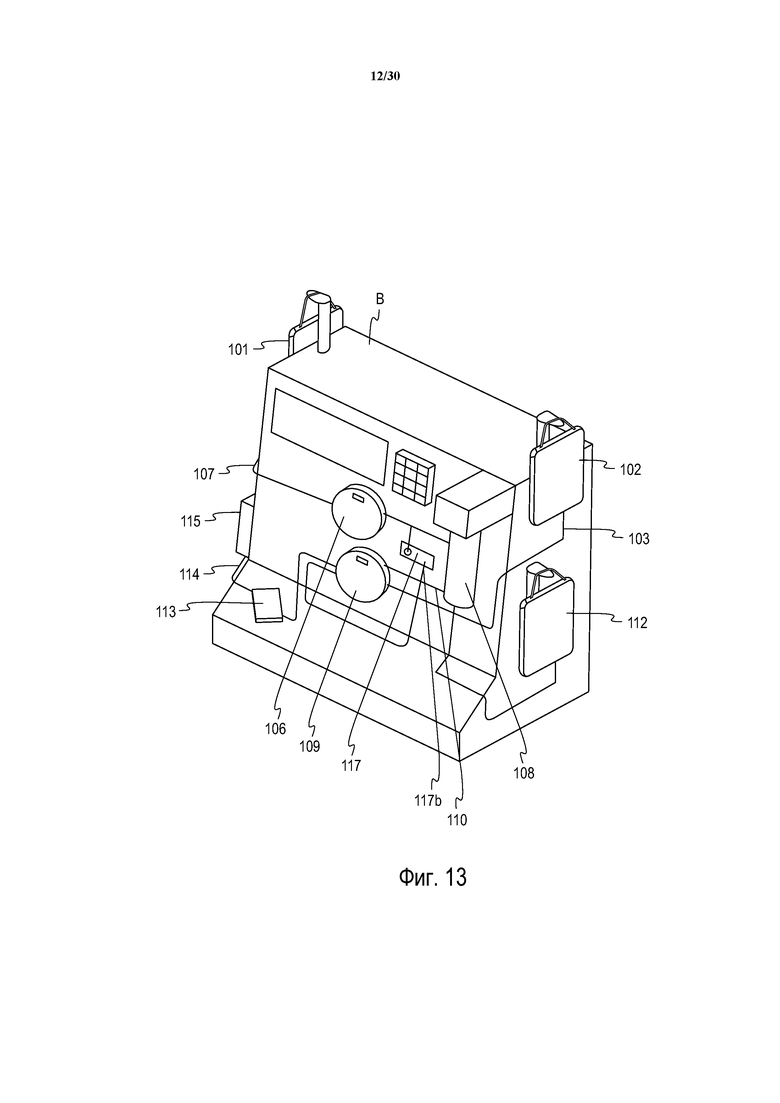
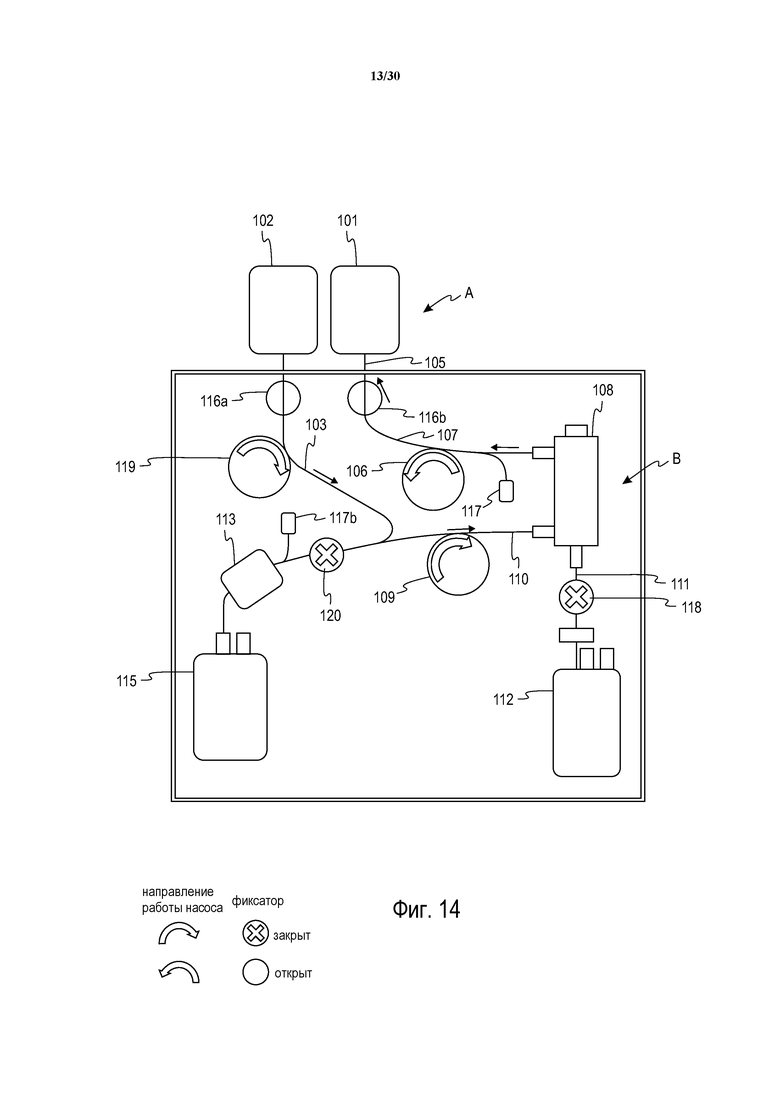
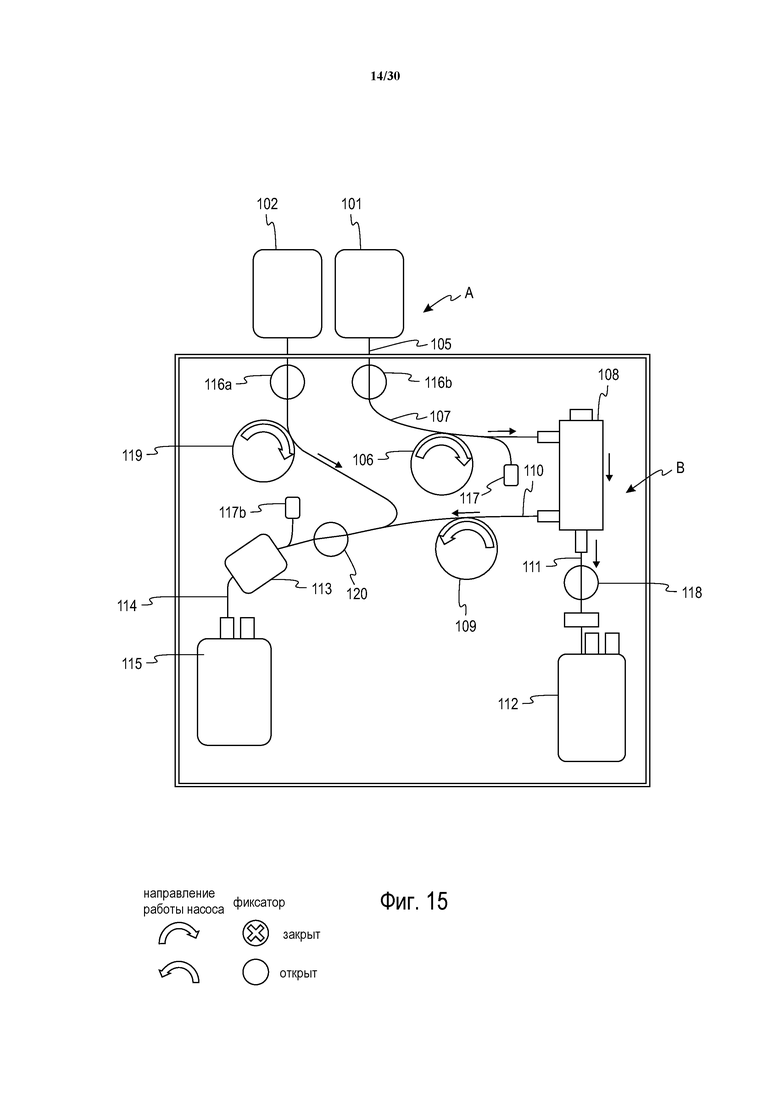
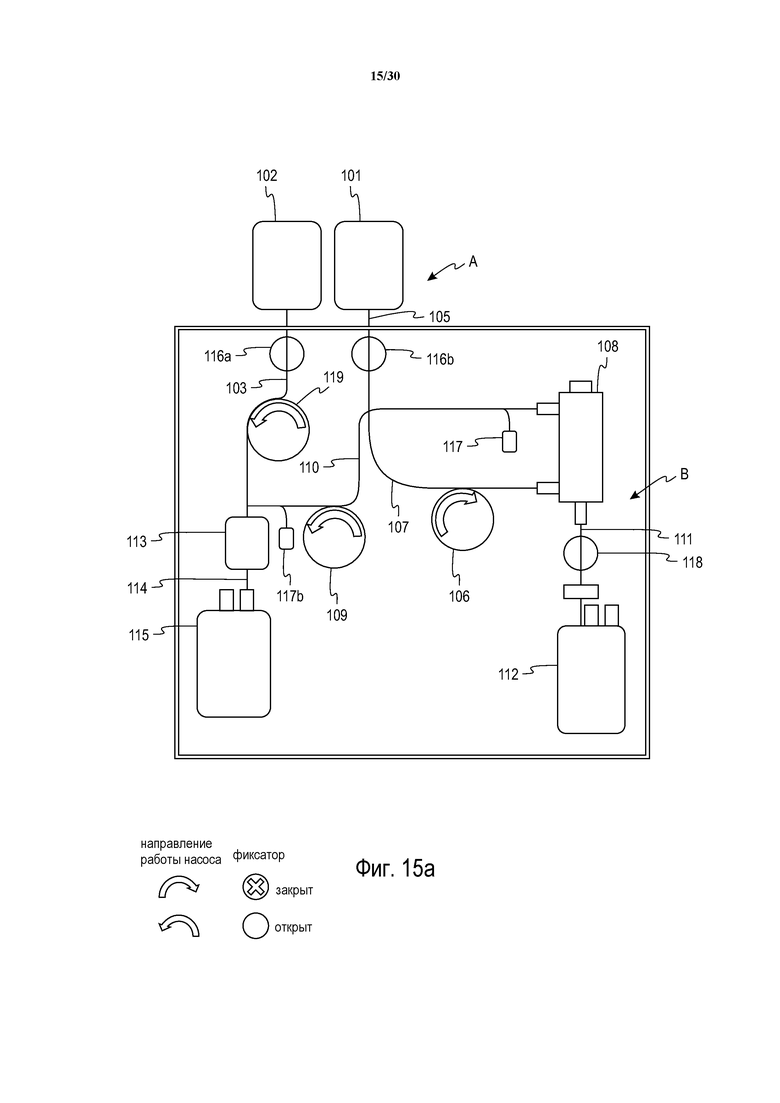
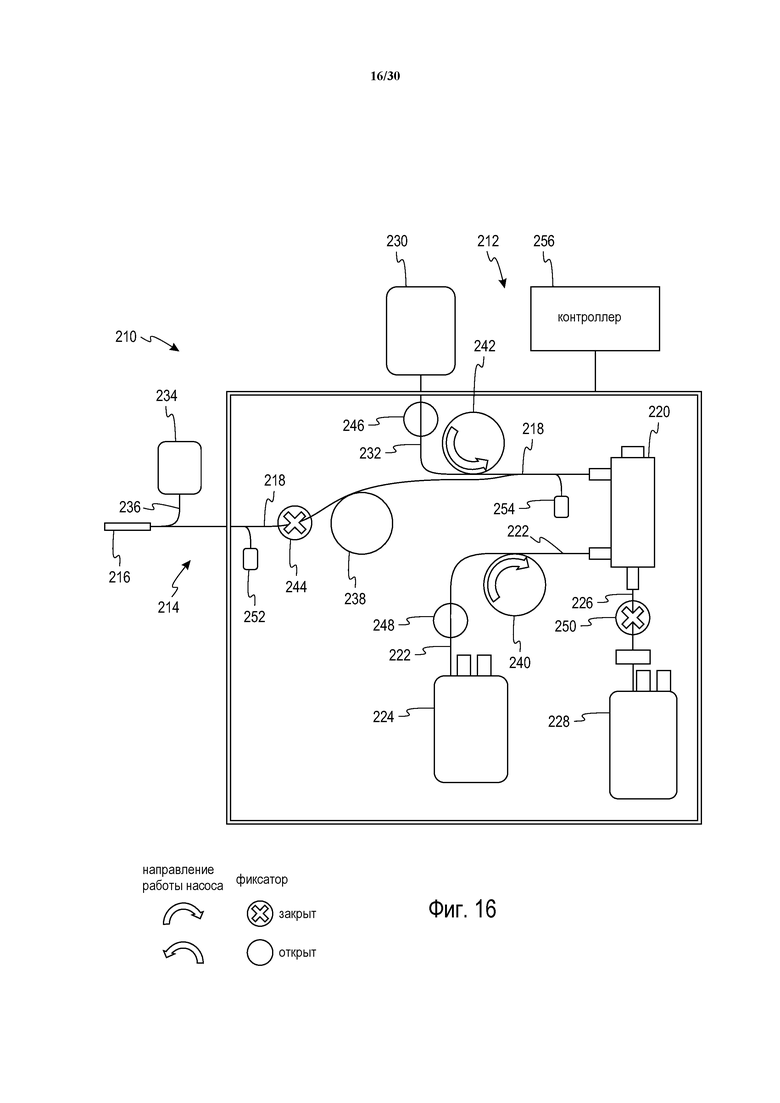

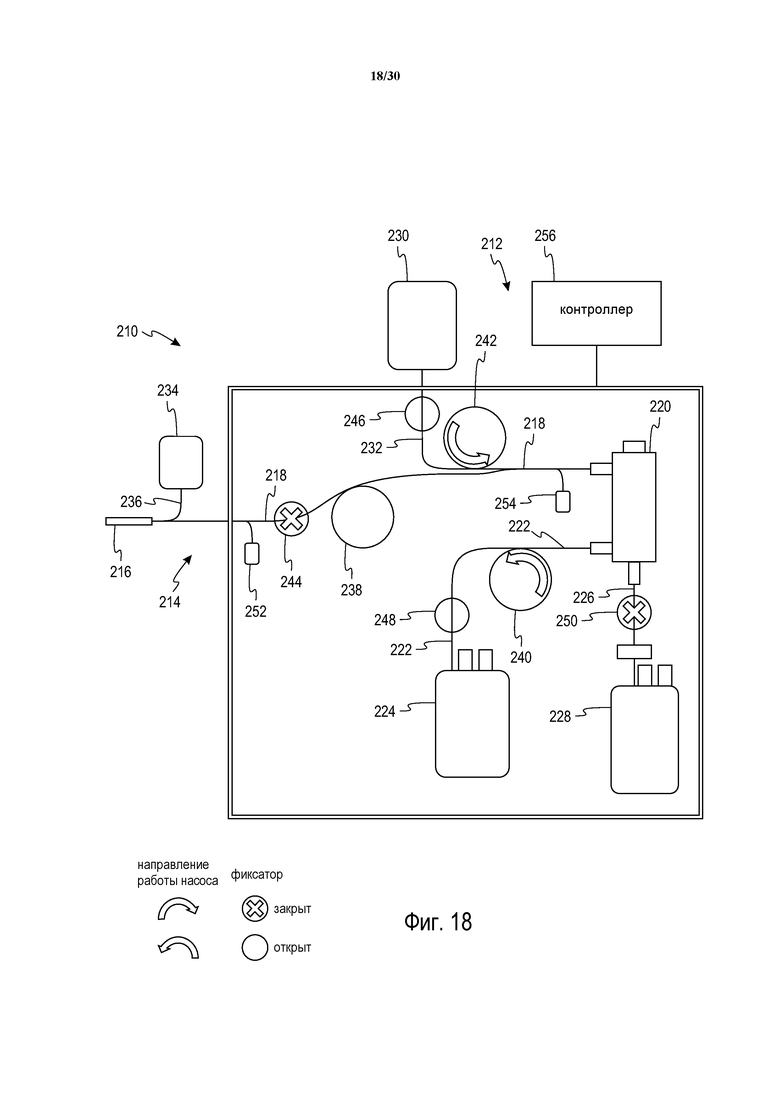
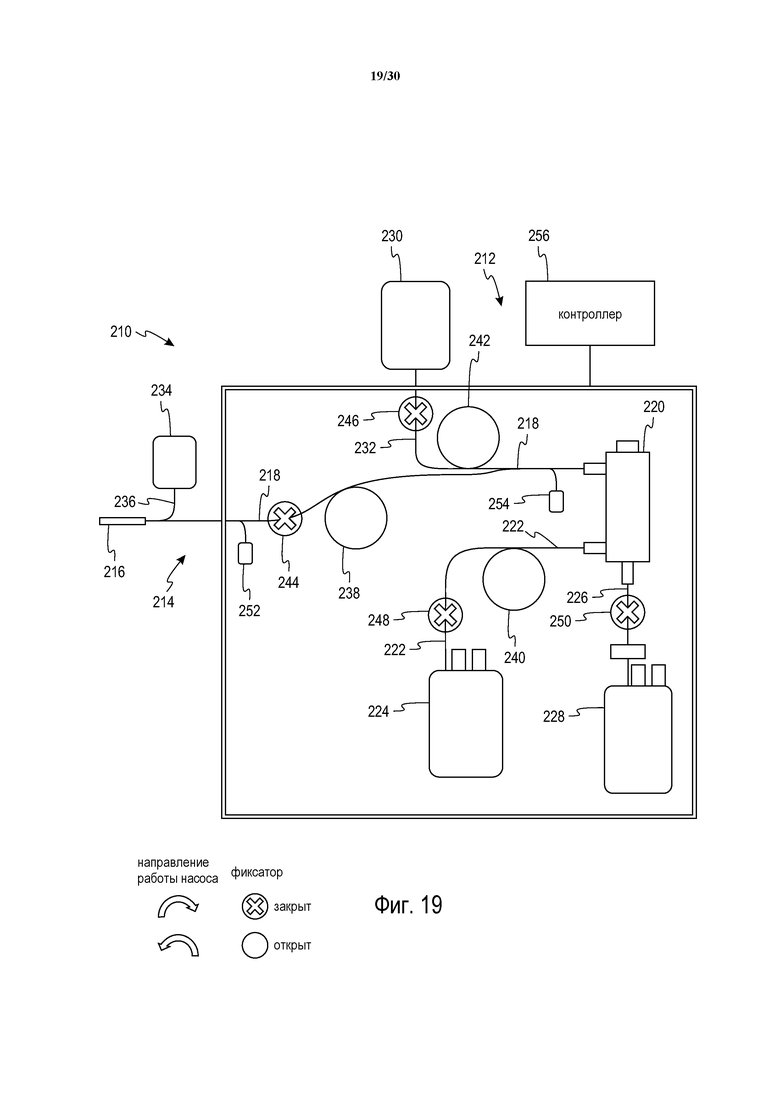
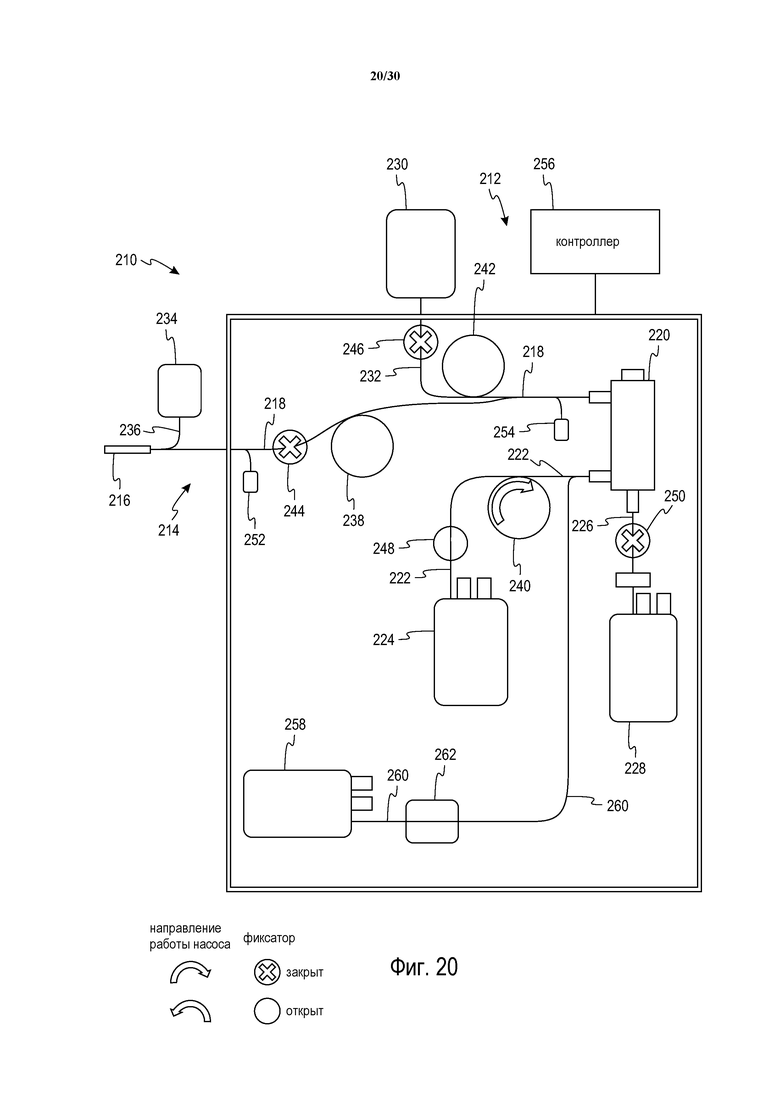
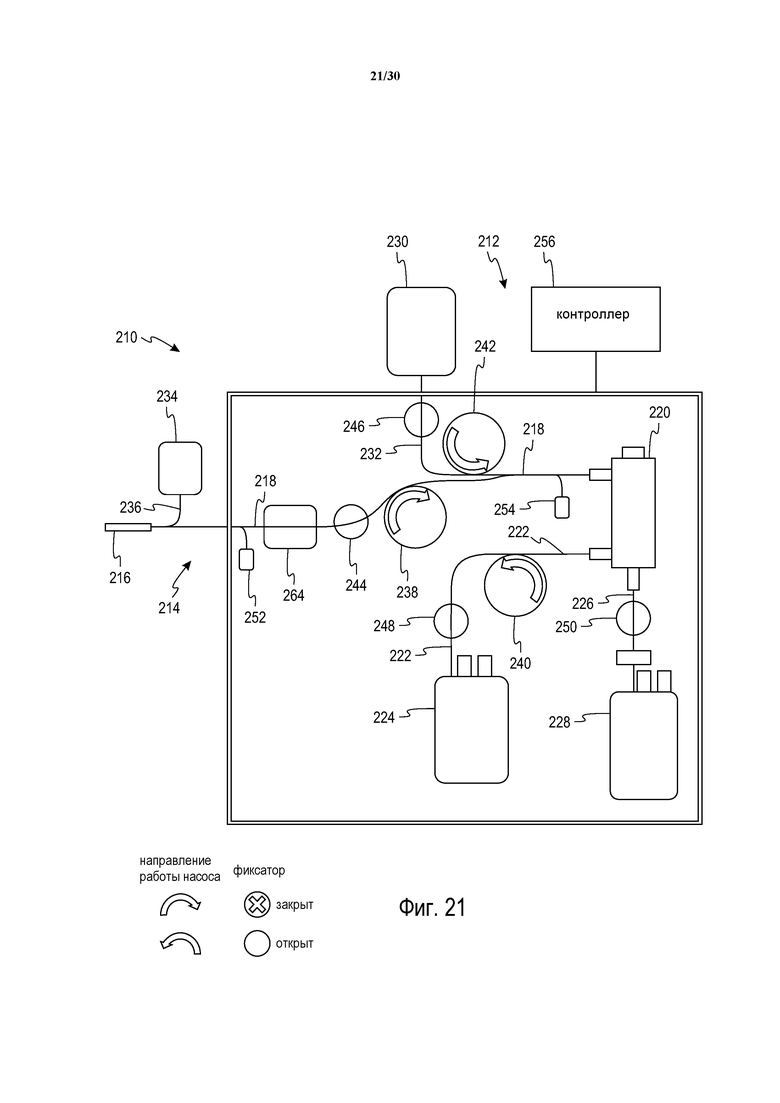
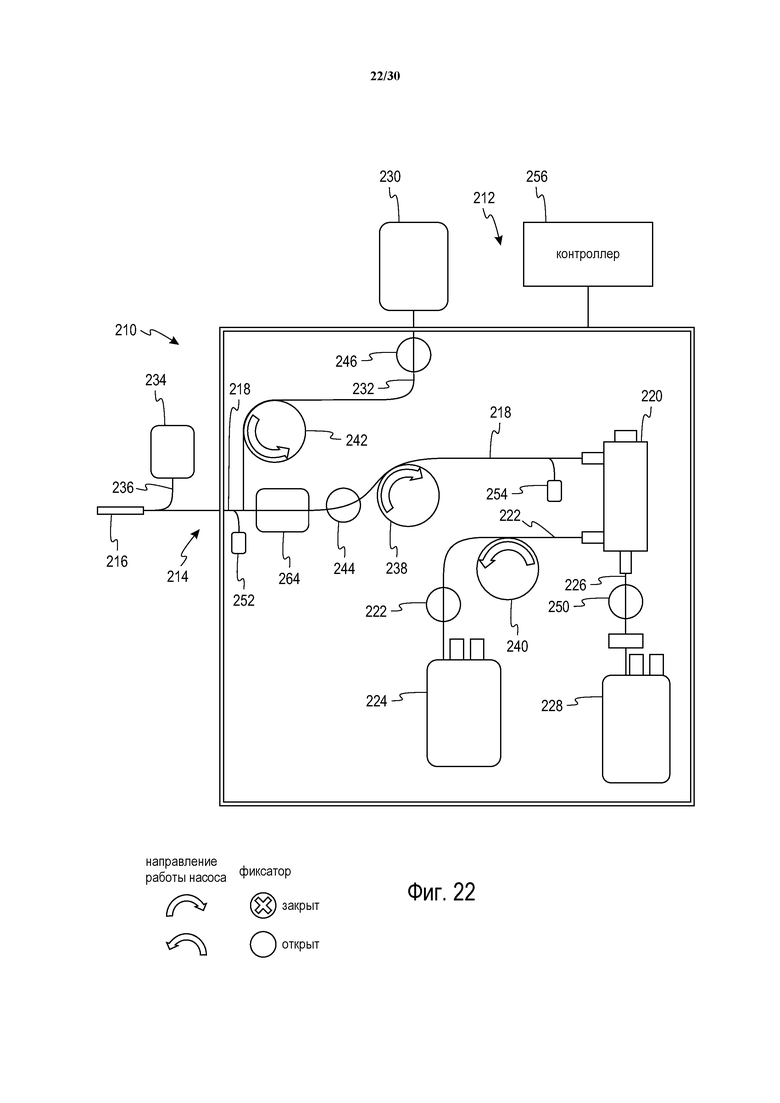

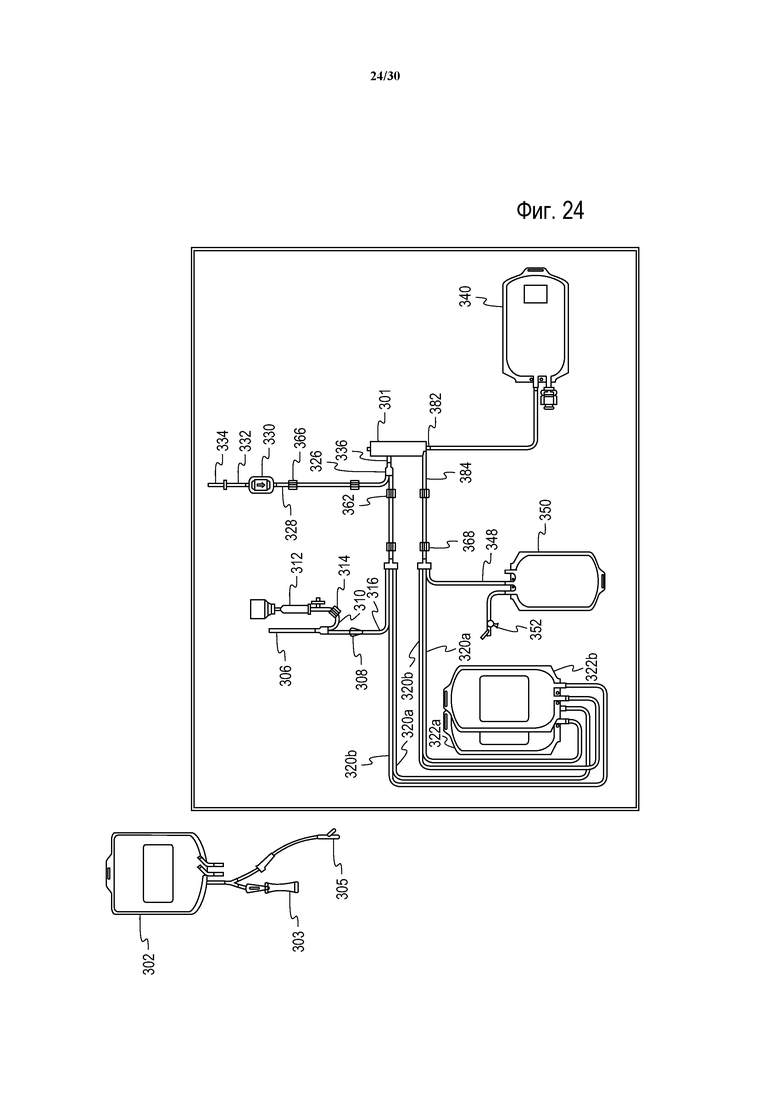
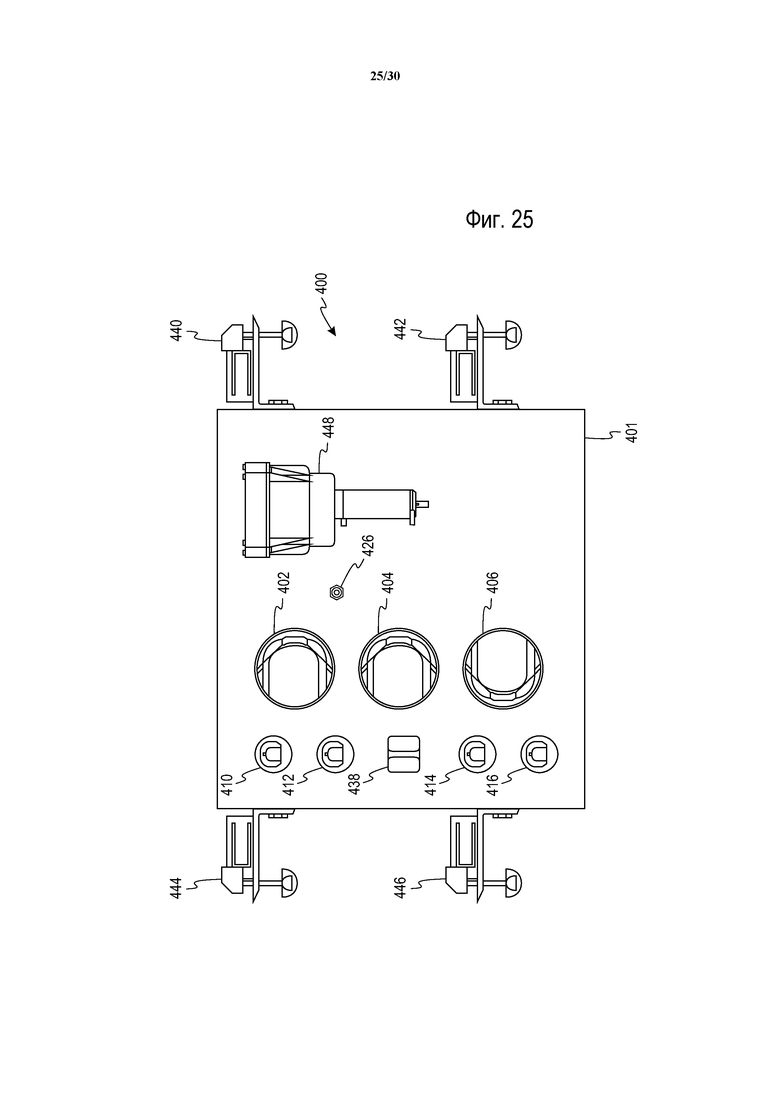
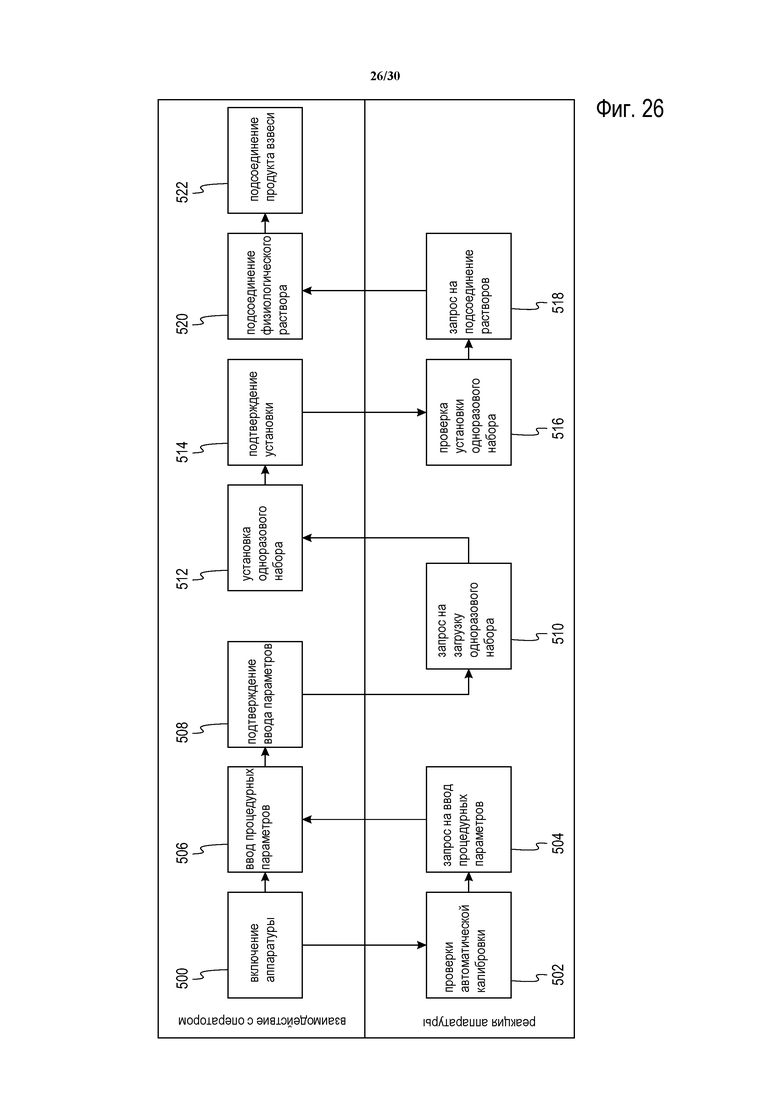
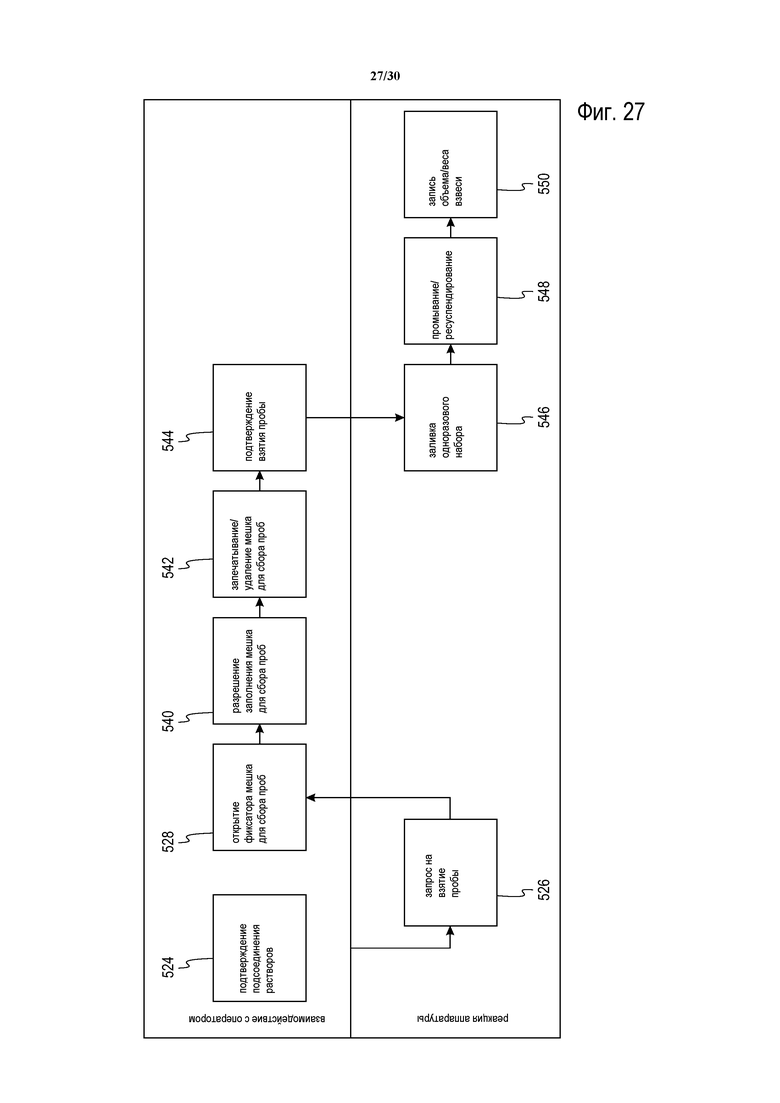
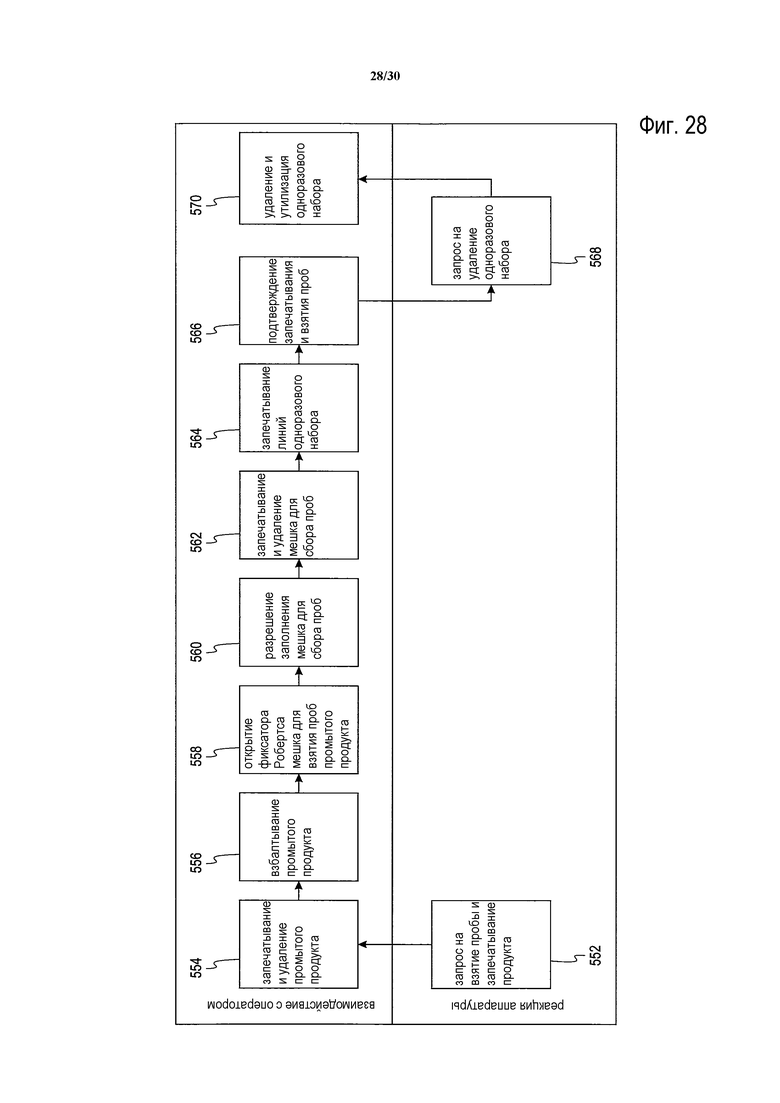
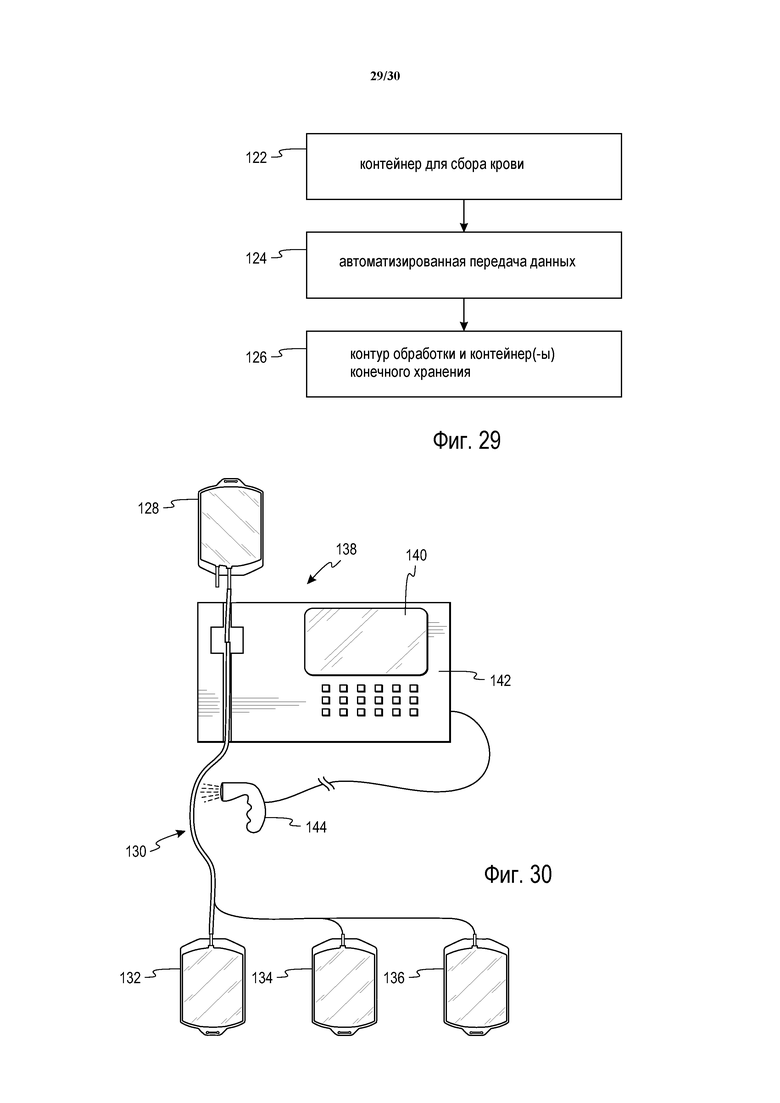
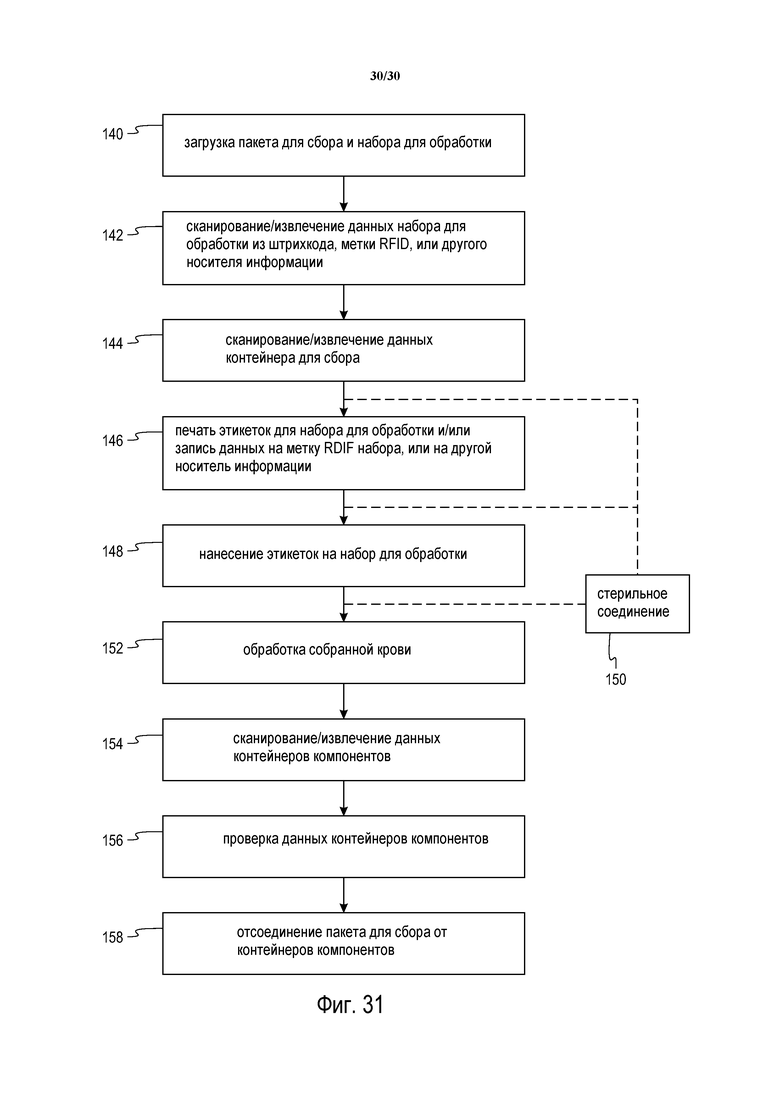
Изобретение относится к устройствам мембранного разделения. Способы заполнения мембранного сепаратора с вращающейся мембраной, в котором сепаратор содержит корпус с верхом и низом, мембрана сконфигурирована для вращения вокруг вертикально ориентированной оси, при этом между корпусом и мембраной образован зазор, при этом мембрана содержит поверхность, через которую происходит разделение, ориентированную вертикально, при этом способ содержит введение раствора для заполнения через канал внизу корпуса; протекание дополнительного раствора для заполнения через канал внизу корпуса, с тем чтобы сформировалась поверхность раздела раствор для заполнения - воздух в зазоре между корпусом и мембраной, которая продвигается вверх через корпус и вверх через поверхность мембраны для вытеснения воздуха внутри корпуса и выталкивания воздуха через канал наверху корпуса c одновременным смачиванием мембраны; и продолжение протекания дополнительного раствора для заполнения через канал внизу корпуса в зазор. Также заявлен контур обработки текучей среды. Технический результат – уменьшение риска введения пузырьков воздуха пациенту. 3 н. 9 з.п. ф-лы, 31 ил.
1. Способ для заполнения сепаратора с вращающейся мембраной, в котором сепаратор содержит корпус с верхом и низом, при этом по меньшей мере один канал является смежным с верхом и низом корпуса, при этом мембрана сконфигурирована для вращения вокруг, по существу, вертикально ориентированной оси, при этом между корпусом и мембраной образован зазор, при этом мембрана содержит поверхность, через которую происходит разделение, при этом способ содержит:
введение раствора для заполнения через канал внизу корпуса;
протекание дополнительного раствора для заполнения через канал внизу корпуса, с тем чтобы сформировалась поверхность раздела раствор для заполнения - воздух в зазоре между корпусом и мембраной, которая продвигается вверх через корпус и вверх через поверхность мембраны для вытеснения воздуха внутри корпуса и выталкивания воздуха через канал наверху корпуса, при этом происходит одновременное смачивание мембраны; и
продолжение протекания дополнительного раствора для заполнения через канал внизу корпуса в зазор до тех пор, пока поверхность раздела раствор для заполнения - воздух не пройдет в вертикальном направлении через всю мембрану.
2. Способ по п. 1, в котором раствор для заполнения содержит небиологическую текучую среду с низкой вязкостью.
3. Способ по п. 1, в котором раствор для заполнения содержит цельную кровь.
4. Способ по п. 1, дополнительно содержащий ручное инвертирование сепаратора с вращающейся мембраной для расположения внизу сепаратора канала, через который вводится раствор для заполнения в зазор.
5. Способ для заполнения мембранного сепаратора, в котором сепаратор содержит корпус с верхом и низом, при этом по меньшей мере один канал является смежным с верхом и низом корпуса, и мембрану, поддерживаемую им, зазор, образованный между корпусом и мембраной, при этом мембрана содержит поверхность, через которую происходит разделение, при этом способ содержит:
введение текучей среды для заполнения через канал внизу корпуса в зазор;
протекание дополнительной текучей среды для заполнения через канал внизу корпуса в зазор, с тем чтобы сформировалась поверхность раздела текучая среда для заполнения - воздух в зазоре между корпусом и мембраной, которая продвигается вверх через корпус для вытеснения воздуха внутри корпуса и вертикально через поверхность мембраны и выталкивания воздуха через канал наверху корпуса и для смачивания мембраны; и
продолжение протекания дополнительной текучей среды для заполнения через канал внизу корпуса до тех пор, пока поверхность раздела текучая среда для заполнения - воздух не пройдет в вертикальном направлении через всю мембрану.
6. Способ по п. 5, в котором раствор для заполнения содержит небиологическую текучую среду с низкой вязкостью.
7. Способ по п. 5, в котором раствор для заполнения содержит цельную кровь.
8. Способ по п. 5, дополнительно содержащий ручное инвертирование сепаратора с вращающейся мембраной для расположения внизу сепаратора канала, через который вводится раствор для заполнения в зазор.
9. Устройство обработки текучей среды, содержащий сепаратор, включающий в себя вращающиеся относительно друг друга поверхности внутри корпуса, при этом по меньшей мере одна из этих поверхностей содержит пористую мембрану, содержащую поверхность, через которую происходит разделение, и поверхности разнесены с образованием продолжающегося, по существу, в осевом направлении зазора между ними, и корпус содержит по меньшей мере один впуск для текучей среды и по меньшей мере один выпуск для текучей среды, взаимодействующие непосредственно или косвенно с зазором, при этом выпуск расположен в нижней области корпуса и впуск расположен в области корпуса, разнесенной вверх от выпуска в осевом направлении; источник текучей среды для заполнения; и трубопровод, соединяющий источник текучей среды для заполнения по меньшей мере с одним выпуском корпуса.
10. Устройство обработки текучей среды по п. 9, в котором мембранный сепаратор и корпус предпочтительно могут вращаться относительно друг друга вокруг, по существу, вертикальной оси и по меньшей мере один выпуск сообщается непосредственно с зазором.
11. Устройство обработки текучей среды по п. 9, содержащий ротор, содержащий внешнюю поверхность, размещенный внутри корпуса, при этом внешняя поверхность ротора разнесена с внутренней поверхностью корпуса образованием зазора, при этом впуск для текучей среды сообщается с зазором для доставки текучей среды, содержащей кровь или компоненты крови, в зазор, и по меньшей мере одна поверхность из внешней поверхности и внутренней поверхности имеет пористую мембрану, при этом выпуск для текучей среды сообщается непосредственно с зазором или со стороной мембраны, обращенной от зазора, или и с тем, и с другим.
12. Устройство обработки текучей среды по п. 11, в котором корпус имеет верхний конец и нижний конец в рабочем положении, при этом впуск близок к верхнему концу и выпуск близок к нижнему концу.
| US 6251295 A1, 26.06.2001 | |||
| Способ и приспособление для нагревания хлебопекарных камер | 1923 |
|
SU2003A1 |
| Эккер | 1947 |
|
SU85099A1 |
Авторы
Даты
2017-04-05—Публикация
2012-03-09—Подача