Изобретение относится к биотехнологии, а именно к оптическим биосенсорам, предназначенным для определения белковых молекул в малых концентрациях.
Известна композиция модифицированных полупроводников, которая содержит, по крайней мере, один полупроводниковый материал, имеющий пористую текстуру, и, по крайней мере, один элемент распознавания, модифицирующий указанный полупроводниковый материал, и обеспечивающая, по крайней мере, одну первую люминесцентную реакцию в диапазоне приблизительно 200-800 нм при освещении композиции электромагнитным излучением, по крайней мере, одной длиной волны в диапазоне приблизительно 100-1000 нм. Композиция формирует систему сенсора (патент RU 2255326 С2, Ятроквест Корпорэйшн, СА 27.06.2005).
Недостатком этой композиции является 1) использование пористых полупроводниковых материалов, требующих сложной подготовки к проведению анализа, 2) биосенсор при формировании химической связи пористая подложка-агент распознавания становится одноразовым.
Также известен биологический сенсор, состоящий из подложки, на поверхность которой нанесена металлическая пленка, на внешней поверхности которой расположен промежуточный связующий слой с адсорбированным на его поверхность биоспецифическим слоем, отличающийся тем, что промежуточный связующий слой выполнен из тонкой пленки из графена толщиной 0,3-2000 нм, или тонкой пленки из однослойных или многослойных углеродных нанотрубок толщиной 0,4-2000 нм, или тонкой пленки из оксида графена толщиной 0,7-2000 нм, а биоспецифический слой расположен на поверхности промежуточного связующего слоя конформно и однородно и выполнен с возможностью осуществления избирательного химического взаимодействия с анализируемыми биологическими молекулами (патент RU 2527699 С1, Федеральное государственное автономное образовательное учреждение высшего профессионального образования "Московский физико-технический институт (государственный университет), 10.09.2014).
К недостаткам данного биосенсора, выбранного в качестве ближайшего аналога, относятся 1) использование в качестве подложки пленки из углеродных нанотрубок, или оксида графена, или металлических пленок благородных металлов, 2) использование промежуточного слоя гидрогеля, состоящего из полисахаридов, 3) химические взаимодействия компонентов биологического сенсора. Перечисленные недостатки приводят к потере чувствительности биосенсора и возможности его повторного использования.
Техническим результатом изобретения является разработка флуоресцентного оптического ДНК-биосенсора, обладающего возможностью многократного его использования без потери чувствительности, в частности, при определении белковых молекул в малых концентрациях.
Технический результат достигается тем, что флуоресцентный оптический ДНК-биосенсор состоит из подложки и адсорбированной на подложке тонкой пленки комплекса ДНК-белок, при этом подложка выполнена из монокристаллического кремния с ориентацией поверхности (100), размером 18×18 мм и толщиной 380±20 мкм, шероховатость рабочей поверхности ≤0,06, а содержание белка в тонкой пленке составляет от 10-15 до 10-9 моль/л.
Изобретение позволяет детектировать белковые молекулы в системе ДНК-белок, сформированной на подложке из монокристаллического кремния, при малых концентрациях белковых молекул.
Краткое описание таблиц
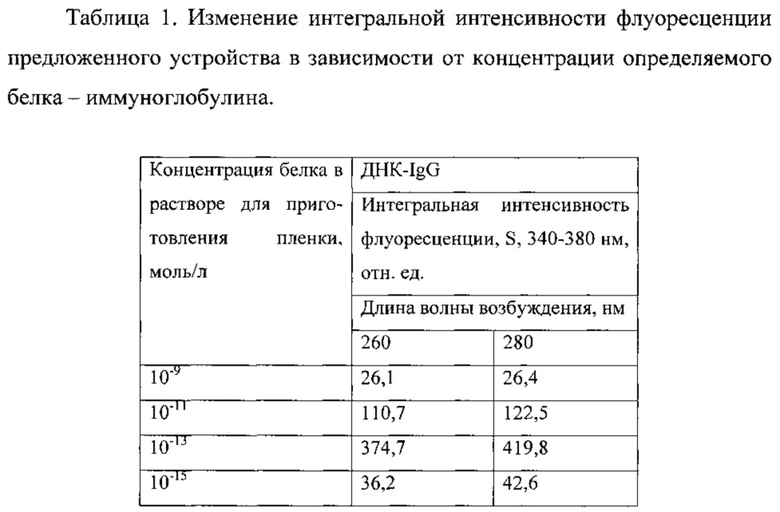
Таблица 1. Изменение интегральной интенсивности флуоресценции предложенного устройства в зависимости от концентрации определяемого белка - иммуноглобулина.
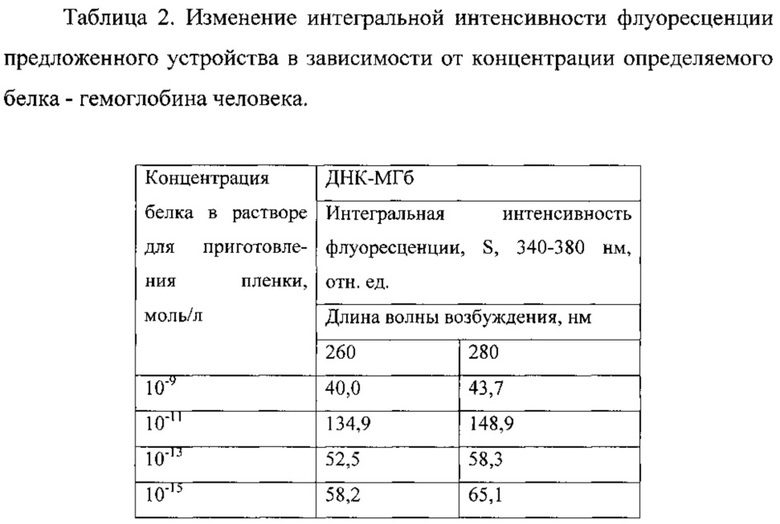
Таблица 2. Изменение интегральной интенсивности флуоресценции предложенного устройства в зависимости от концентрации определяемого белка - гемоглобина человека.
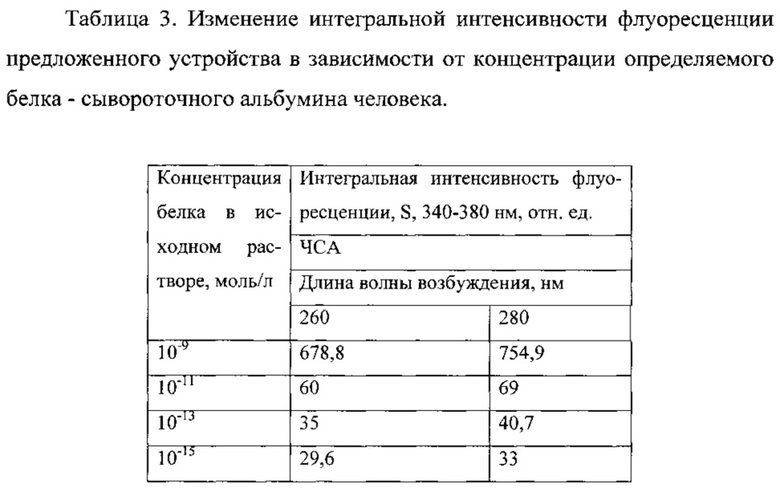
Таблица 3. Изменение интегральной интенсивности флуоресценции предложенного устройства в зависимости от концентрации определяемого белка - сывороточного альбумина человека.
Возможность осуществления заявляемого изобретения показана следующими примерами.
Пример 1. Флуоресценция подложки из монокристалла кремния до и после нанесения слоя молекул ДНК
Использовали образцы кремния с ориентацией поверхности (100), толщиной 380±20 мкм, шероховатость рабочей поверхности ≤0,06. Наблюдаемая люминесценция образцов монокристаллического кремния без добавления ДНК или белка является люминесценцией оксидной пленки на поверхности монокристаллического образца, связанной с излучением одиночных и агрегатных центров окраски (F-центров) в оксидной матрице. Так, при возбуждении светом длиной волны 260 нм (полоса поглощения ДНК) максимум полосы флуоресценции подложки наблюдали при 364 нм. Плечи в областях 355-360 и 370-375 нм свидетельствуют о различном размере кластеров в SiO2 - оксидной пленке.
При нанесении на подложку однокомпонентной пленки ДНК (1,7 мг/мл) изменение положения максимума полосы флуоресценции незначительно, при этом интенсивность флуоресценции возрастает почти в 4 раза.
В использованных нами образцах монокристаллического кремния была обнаружена собственная флуоресценция с максимумами при 688 и 722 нм. Существует модель, объясняющая возникновение фотолюминесценции свойствами границы Si-SiOx, насыщенной дефектами. На образцах пористого кремния показано, что положение полос фотолюминесценции может заметно (1,75-2 эВ) меняться при старении образцов.
Пример 2. Определение иммуноглобулина с помощью предложенного сенсора
Использовали материалы: ДНК из тимуса теленка, IgG кролика. Навеску ДНК обрабатывали ультразвуком на сонификаторе Branson 1510 (42 кГц) 40 минут в 0,1 моль/л растворе NaCl. Раствор ДНК (1,7 мг/мл) смешивали с раствором белка различных концентраций в 0,1 моль/л NaCl в соотношении 9:1 так, чтобы концентрация белка в растворе для нанесения на положку составляла от 10-9 до 10-15 моль/л.
Пленку получали методом спинкоатинга на подложке монокристаллического кремния (18×18 мм) на установке на основе центрифуги «Элекон» ЦЛМН-Р 10-02 (Россия) при скорости вращения подложки 2000 об/мин. Объем наносимого раствора - 20 мкл.
Результаты определения иммуноглобулина с помощью предложенного сенсора представлены в таблице 1.
Пример 3. Определение гемоглобина человека с помощью предложенного сенсора
Использовали материалы: ДНК из тимуса теленка, гемоглобин человека. Навеску ДНК обрабатывали ультразвуком на сонификаторе Branson 1510 (42 кГц) 40 минут в 0,1 моль/л растворе NaCl. Раствор ДНК (1,7 мг/мл) смешивали с раствором белка различных концентраций в 0,1 моль/л NaCl в соотношении 9:1 так, чтобы концентрация белка в растворе для нанесения на положку составляла от 10-9 до 10-15 моль/л.
Пленку получали методом спинкоатинга на подложках монокристаллического кремния (18×18 мм) на установке на основе центрифуги «Элекон» ЦЛМН-Р 10-02 (Россия) при скорости вращения подложки 2000 об/мин. Объем наносимого раствора - 20 мкл.
Результаты определения гемоглобина человека с помощью предложенного сенсора представлены в таблице 2.
Пример 4. Определение сывороточного альбумина человека с помощью предложенного сенсора.
Использовали материалы: ДНК из тимуса теленка, сывороточный альбумин человека (САЧ). Навеску ДНК обрабатывали ультразвуком на сонификаторе Branson 1510 (42 кГц) 40 минут в 0,1 моль/л растворе NaCl. Раствор ДНК (1,7 мг/мл) смешивали с раствором белка различных концентраций в 0,1 моль/л NaCl в соотношении 9:1 так, чтобы концентрация белка в растворе для нанесения на положку составляла от 10-9 до 10-15 моль/л.
Пленку получали методом спинкоатинга на подложках монокристаллического кремния (18×18 мм) на установке на основе центрифуги «Элекон» ЦЛМН-Р 10-02 (Россия) при скорости вращения подложки 2000 об/мин. Объем наносимого раствора - 20 мкл.
Результаты определения сывороточного альбумина человека с помощью предложенного сенсора представлены в таблице 3.
Возбуждение в полосу поглощения белка (λех=280 нм) не изменяет существенно формы спектра и кремниевой подложки, и однокомпонентной пленки ДНК на ней, приводя лишь к снижению интенсивности флуоресценции в обоих случаях по сравнению с интенсивностью, наблюдаемой при возбуждении светом с длиной волны 260 нм.
Таким образом, созданный биосенсор позволяет определять наличие белковых молекул в низких концентрациях, при этом при снижении концентрации белка в тонкой пленке наблюдали существенное усиление флуоресценции от 2,5 до 23 раз.
Изобретение относится к биотехнологии, а именно к оптическим биосенсорам, предназначенным для определения белковых молекул в малых концентрациях. Заявленный флуоресцентный оптический ДНК-биосенсор состоит из подложки, адсорбированной на подложке тонкой пленки комплекса ДНК-белок, причем подложка выполнена из монокристаллического кремния с ориентацией поверхности (100), размером 18×18 мм и толщиной 380±20 мкм, шероховатость рабочей поверхности ≤0,06, а содержание белка в тонкой пленке составляет от 10-15 до 10-9 моль/л. Технический результат - разработка флуоресцентного оптического ДНК-биосенсора, обладающего возможностью многократного его использования без потери чувствительности, в частности, при определении белковых молекул в малых концентрациях. 3 табл.
Флуоресцентный оптический ДНК-биосенсор, состоящий из подложки, адсорбированной на подложке тонкой пленки комплекса ДНК-белок, отличающийся тем, что подложка выполнена из монокристаллического кремния с ориентацией поверхности (100), размером 18×18 мм и толщиной 380±20 мкм, шероховатость рабочей поверхности ≤0,06, а содержание белка в тонкой пленке составляет от 10-15 до 10-9 моль/л.
| БИОЛОГИЧЕСКИЙ СЕНСОР И СПОСОБ СОЗДАНИЯ БИОЛОГИЧЕСКОГО СЕНСОРА | 2013 |
|
RU2527699C1 |
| RU 2015102212 A, 26.07.2013 | |||
| US 2009116020 A1, 07.05.2009 | |||
| WO 2015188215 A1, 17.12.2015 | |||
| СПОСОБ ПОЛУЧЕНИЯ ПОДЛОЖЕК С МНОНОСЛОЙНЫМ ПОКРЫТИЕМ НА ОСНОВЕ ПОЛИЭЛЕКТРОЛИТНЫХ МИКРОКАПСУЛ, СОДЕРЖАЩИХ БИОЛОГИЧЕСКИ АКТИВНЫЕ МАТЕРИАЛЫ | 2011 |
|
RU2567320C2 |
Авторы
Даты
2017-04-18—Публикация
2016-03-04—Подача