Изобретение относится к области биотехнологии, а именно к устройствам для исследования биомолекулярных взаимодействий и детектирования биомолекул с использованием поверхностного плазмонного резонанса и способам их создания. Поверхностный плазмонный резонанс - это явление возбуждения поверхностных плазмонов посредством света. Оно возникает на поверхности металлов при условии нарушенного полного внутреннего отражения. Термин «поверхностный плазмонный резонанс» в используемом в настоящем описании смысле относится к оптическому явлению, которое позволяет проводить анализ взаимодействий в режиме реального времени посредством регистрации свойств и изменений свойств исследуемого вещества на матрице.
Метод биодетектирования с использованием поверхностного плазмонного резонанса обладает рядом преимуществ по сравнению с существующими на данный момент методами, например данный метод обладает возможностью безметкового биодетектирования, то есть без использования радиоактивных или флуоресцентных меток, а также позволяет обеспечить высокие значения чувствительности биодетекторов, основанных на данном методе, и высокую скорость проводимых анализов. Предлагаемое изобретение относится к созданию устройств с детектирующими поверхностями, на которых протекают химические реакции, изучаемые данным методом.
Из уровня техники известен ряд технических решений, относящихся к созданию устройств с детектирующими поверхностями для биодетектирования с использованием поверхностного плазмонного резонанса.
Например, к известным устройствам, используемым в качестве биологических чипов, предназначенных для производства биосенсоров, относятся детектирующие поверхности, предназначенные для анализа избирательных биологических взаимодействий по патенту США US 5242828 [1] и состоящие из трех слоев: субстрата, металлической пленки и монослоя органических молекул, к которым можно прикреплять молекулы связывающего партнера анализируемого вещества и на их основе создавать биологические чипы для биодетекторов на основе поверхностного плазмонного резонанса. Используемые в данном случае биомолекулы имеют особую структуру. К недостаткам данного устройства можно отнести низкое число активных центров, к которым могут присоединяться биомолекулы, вследствие плоской структуры биослоя. Также недостатком является сложность создания устройства, поскольку молекулы описываемого биослоя не являются широкодоступными на рынке, а процессы их создания включают много этапов и требуют наличия различных химических реагентов. Также к недостаткам можно отнести сложность производства биосенсоров на основе предлагаемых устройств, поскольку для присоединения молекул связывающего партнера анализируемого вещества эти молекулы должны обладать определенными функциональными группами и, соответственно, в каждом конкретном случае требуется разработка и осуществление методов активации, что также ограничивает класс используемых анализируемых веществ.
Кроме того, известен биологический сенсор по патенту Великобритании GB 2459604 [2], состоящий из следующих слоев: подложки, металлической пленки, пленки на основе аморфного углерода и слоя биомолекул, позволяющий реализовать фотолитографические процессы организации молекул связывающего партнера анализируемого вещества на его поверхности, а также метод биодетектирования с использованием данного устройства, а также метод его создания. К недостаткам данного устройства можно отнести то, что чувствительность детектирования понижена ввиду влияния углеродных пленок на электромагнитные свойства возбуждаемых плазмонов вследствие поглощения излучения углеродными материалами. Также у пленок из аморфного углерода преимущественным механизмом связывания с биомолекулами является образование C-C связей из-за отсутствия кристаллической решетки, которая могла бы позволить другие механизмы, что в свою очередь накладывает ограничения на диапазон возможных для образования биослоя молекул и требует разработки методов активации поверхности для каждого конкретного случая.
Также из уровня техники известен биологический сенсор по заявке EP 2216642 A1 [3], содержащий металлический слой, в который включены частички алмаза. К недостаткам данного устройства относится сложность его создания, поскольку используются довольно сложные композитные структуры, а также очень низкая площадь поверхности, определяемая площадью открытых для внешней среды алмазных частиц и доступная для осаждения биомолекул, что понижает чувствительность биодетектирования.
Кроме того, известна многослойная структура, описанная в статье "Graphene-based high-performance surface plasmon resonance biosensors"[4] и включающая в себя тонкую металлическую пленку, на поверхность которой нанесена тонкая пленка на основе графена. Данная структура позволяет изучить реакцию между биологическими молекулами и графеном, однако она не обладает свойством избирательности по отношению к детектируемым молекулам, что делает ее непригодной для использования для изучения химических реакций данным методом. В данной работе пленка из графена выполняет функцию внешней поверхности, с которой непосредственно взаимодействуют все типы анализируемых биологических молекул, находящихся в растворе.
Наиболее близким к предлагаемому изобретению, выбранном в качестве прототипа предлагаемого биологического сенсора является устройство по патенту США US 5763191 [5] - универсальная связующая пленка, предназначенная для анализа избирательных биологических взаимодействий, состоящая из металлической пленки или пленки на основе оксида метала и слоя биологического реагента, прикрепляемого к поверхности металла или оксида металла за счет тиоловой, дисульфидной или фосфиновой группы с помощью связующей молекулы. Данный биологический слой способен химически взаимодействовать с другими биологическими молекулами, и на его основе можно создавать биологические сенсоры для биодетекторов на основе поверхностного плазмонного резонанса. Также к данному патенту относятся метод анализа веществ с использованием описанного устройства, а также процесс его производства. Недостатками прототипа являются сложность создания слоя биологических молекул, требующего предварительного получения соединений, содержащих необходимые функциональные группы и способных прикрепляться к поверхности золота. Кроме того, недостатком является сложность присоединения молекул связывающего партнера анализируемого вещества к данному слою, требующих разработки специальных методов активации, нацеленных на реакцию через определенные функциональные группы, подразумевающих, что данный способ активации будет работать только с определенным классом анализируемых молекул, что ограничивает возможные применения данного устройства. Кроме того, поверхность металлической пленки предложенного устройства подвержена воздействию внешней среды, что накладывает ограничение на условия работы и используемые для биодетектирования химические реактивы. Все эти недостатки не позволяют обеспечить высокую чувствительность детектирования в совокупности со специфичностью биодетектирования.
Технической задачей, решаемой в настоящем изобретении, является создание высокочувствительного и универсального биологического сенсора с высокой биоспецифичностью для биодетекторования, основанного на поверхностном плазмонном резонансе.
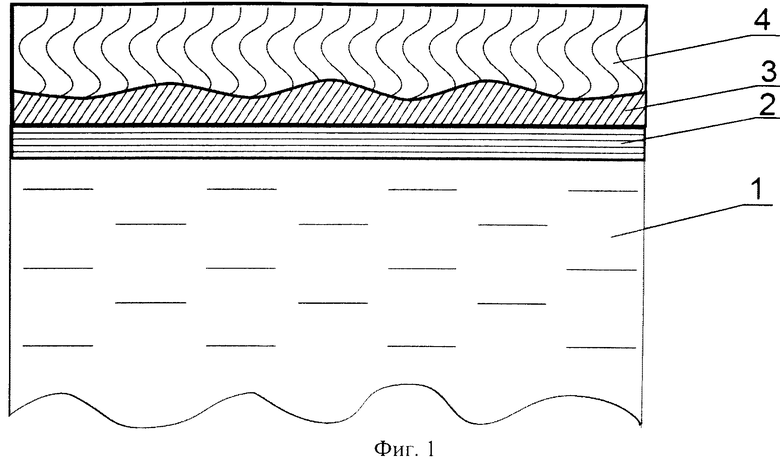
Решение поставленной технической задачи достигается путем создания биологического сенсора (фиг.1-4) для использования его в биодетектировании, основанном на поверхностном плазмонном резонансе, представляющего собой многослойную структуру, включающую подложку (1), на поверхность которой нанесена тонкая металлическая пленка (2), на внешней поверхности которой расположен промежуточный связующий слой (3), выполненный из тонкой пленки из графена толщиной 0,3-2000 нм, или тонкой пленки из однослойных или многослойных углеродных нанотрубок толщиной 0,4-2000 нм, или тонкой пленки из оксида графена толщиной 0,7-2000 нм. На поверхности промежуточного связующего слоя (3) конформно и однородно расположен биоспецифический слой (4), который выполнен с возможностью осуществления избирательного химического взаимодействия только с определенными биологическими молекулами анализируемого вещества.
Металлическая пленка (2) может быть изготовлена из таких металлов, как золото, серебро, медь и алюминий, причем ее толщина может быть равной 10-150 нм. Биоспецифический слой (4) может содержать молекулы связывающего партнера анализируемого вещества (5). Также биоспецифический слой может содержать молекулы связывающего партнера анализируемого вещества (5) и молекулы, обладающие высоким сродством к связывающим партнерам молекул анализируемого вещества (6) и образующие с ними химическую связь. Кроме того, биоспецифический слой (4) может содержать гидрогель (7), с иммобилизованными в нем молекулами связывающего партнера анализируемого вещества (5). Также биоспецифический слой может содержать гидрогель (7) с иммобилизованными в нем молекулами связывающего партнера молекул анализируемого вещества (5) и молекулами, обладающими высоким сродством к молекулам связывающего партнера анализируемого вещества (6) и образующими с ними химическую связь. В качестве гидрогеля (7) биоспецифический слой (4) может содержать полисахариды. В качестве полисахаридов могут быть использованы агароза, альгиновая кислота, декстран, каррагинан, крахмал, целлюлоза или их производные. В качестве производных декстрана биоспецифический слой может содержать, например, карбоксиметилированный декстран. Также в качестве молекул, обладающих высоким сродством к молекулам связывающего партнера анализируемого вещества (6), биоспецифический слой (4) может содержать молекулы авидина, стрептавидина и дегликозилированного авидина, молекулы связывающего партнера при этом являются биотинилированными. В качестве пары анализируемого вещества и связывающего партнера к нему могут использовать пары рецептор-лиганд, антиген-антитело, фермент-субстрат. Связывающим партнером анализируемого вещества может являться антитело или фрагмент антитела к анализируемому веществу, а также рецептор анализируемого вещества. Кроме того, связывающим партнером анализируемого вещества может являться связывающий партнер протеинов, липидов, ДНК, РНК, вирусов, клеток, бактерий или токсинов, а также химических модификаций приведенных веществ.
Использование в предлагаемом устройстве тонких пленок из графена, оксида графена, однослойных или многослойных углеродных нанотрубок, выполняющих функцию промежуточного связующего слоя биосенсора, позволяет обеспечить адсорбции на них в качестве биоспецифического слоя большого класса биологических молекул, что делает возможным использование описанного устройства для различных применений, а также защитить поверхность металлического слоя от вредного воздействия внешней среды при работе биосенсора, что позволит использовать в процессе биодетектирования реагенты, которые могли бы повредить поверхность металла, а также использовать такие плазмонные материалы, как серебро.
Сущность способа создания биологического сенсора заключается в том, что способ состоит из следующих стадий:
а) стадии нанесения металлической пленки (2) на подложку (1);
б) стадии нанесения на внешнюю поверхность металлической пленки (2) промежуточного связующего слоя (3), выполненного в виде тонкой пленки из графена толщиной 0,3-2000 нм, или тонкой пленки из однослойных или многослойных углеродных нанотрубок толщиной 0,4-2000 нм, или тонкой пленки из оксида графена толщиной 0,7-2000 нм;
в) стадии нанесения биоспецифического слоя (4), который конформно и однородно адсорбируют на поверхность промежуточного связующего (3) слоя за счет возникновения сил химического взаимодействия между молекулами промежуточного связующего слоя (3) и молекулами биоспецифического слоя (4), обусловленного стэкинг-взаимодействием или взаимодействием молекул биоспецифического слоя с функциональными группами графена, однослойных или многослойных углеродных нанотрубок или оксида графена, при этом при адсорбции обеспечивают создание большого количества центров активации на поверхности промежуточного связующего слоя со степенью заполнения поверхности молекулами биоспецифического слоя 15-100% от площади поверхности промежуточного связующего слоя.
В качестве металлической пленки (2) может быть нанесена пленка из золота, серебра, меди или алюминия толщиной 10-150 нм.
В качестве биоспецифического слоя (4) может быть нанесен слой молекул связывающего партнера анализируемого вещества (5).
Также в качестве биоспецифического слоя (4) может быть нанесен слой молекул связывающего партнера анализируемого вещества (5) и молекул, обладающих высоким сродством к молекулам связывающего партнера анализируемого вещества (6) и образующих с ними химическую связь.
Кроме того, в качестве биоспецифического слоя (4) может быть нанесен слой гидрогеля (7) с иммобилизованными в нем молекулами связывающего партнера молекул анализируемого вещества (5).
Также в качестве биоспецифического слоя (4) можно наносить слой гидрогеля (7) с иммобилизованными в нем молекулами связывающего партнера анализируемого вещества (5) и молекулами, обладающими высоким сродством к молекулам связывающего партнера анализируемого вещества (6) и образующими с ними химическую связь.
В качестве гидрогеля (7) целесообразно использовать полисахариды. В качестве полисахаридов предпочтительно наносить агарозу, альгиновую кислоту, декстран, каррагинан, крахмал, целлюлозу или их производные. В качестве производных декстрана биоспецифический слой может содержать карбоксиметилированный декстран. В качестве молекул, обладающих высоким сродством к молекулам связывающего партнера анализируемого вещества, могут быть нанесены молекулы авидина, стрептавидина и дегликозилированного авидина, молекулы связывающего партнера при этом являются биотинилированными. Взаимодействие молекул биоспецифического слоя (4) с функциональными группами графена, однослойных или многослойных углеродных нанотрубок или оксида графена может осуществляться за счет взаимодействия с такими функциональными группами, как эпоксидными, гидроксильными, карбонильными или карбоксильными группами. В качестве связывающего партнера анализируемого вещества могут использовать антитело или фрагмент антитела к анализируемому веществу, а также рецептор анализируемого вещества. Кроме того, в качестве связывающего партнера анализируемого вещества могут использовать связывающий партнер протеинов, липидов, ДНК, РНК, вирусов, клеток, бактерий или токсинов, а также химических модификаций приведенных веществ.
Заявленное изобретение поясняется следующими чертежами:
на фиг.1 изображен общий вид биологического сенсора (вид сбоку);
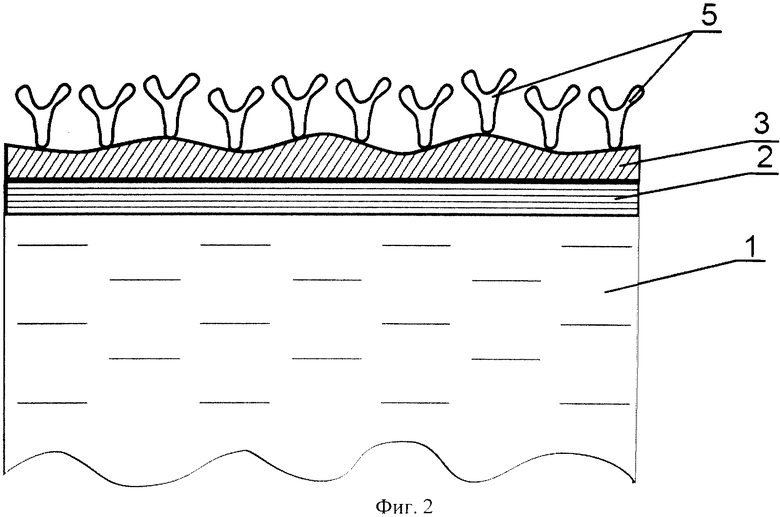
на фиг.2 изображен биологический сенсор, в котором биоспецифический слой (4) содержит молекулы связывающего партнера анализируемого вещества (5);
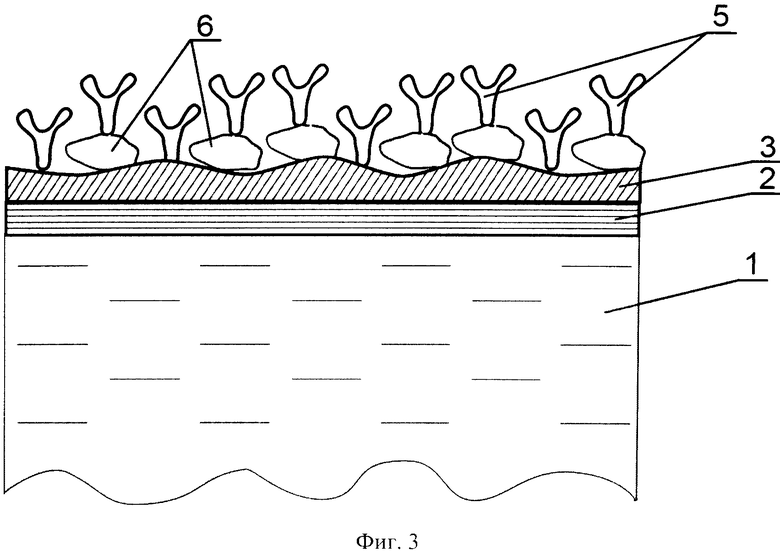
на фиг.3 изображен биологический сенсор, в котором биоспецифический слой (4) содержит молекулы связывающего партнера (5) и биологические молекулы, способные образовывать связь с молекулами связывающего партнера (6);
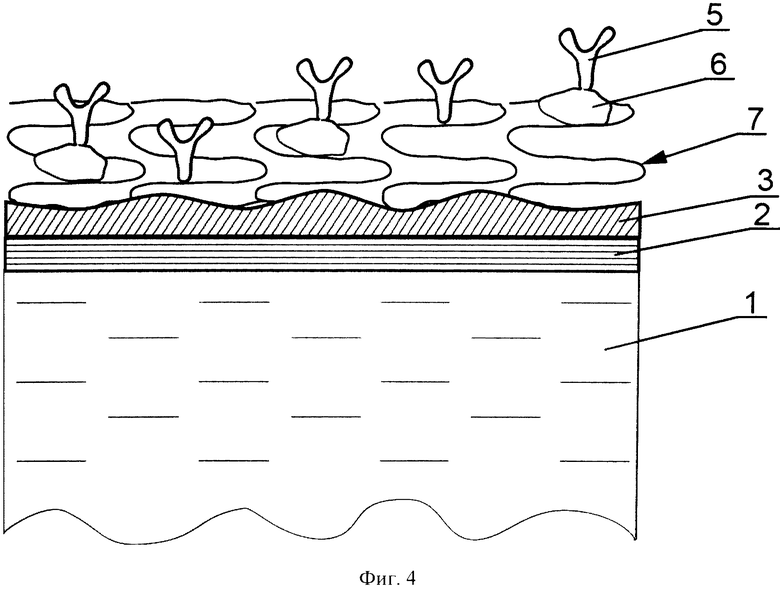
на фиг.4 изображен биологический сенсор, в котором биоспецифический слой (4) содержит гидрогель (7) с прикрепленными к нему молекулами связывающего партнера (5) и молекулами, способными образовывать связь с молекулами связывающего партнера (6);
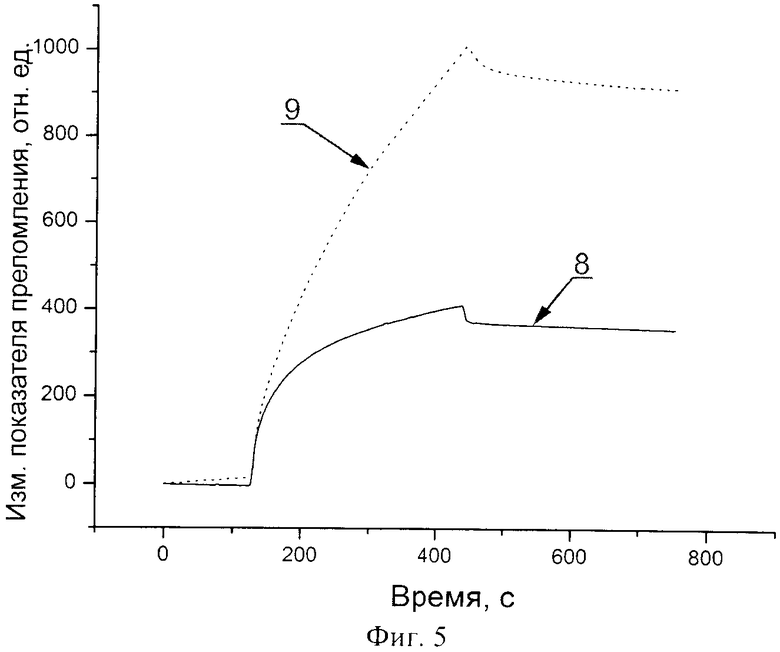
на фиг.5 изображена кинетическая кривая адсорбции молекул биотинилированных олигонуклеотидов на поверхность тонкой пленки оксида графена и на поверхность биосенсора, состоящего из слоев: подложки, металлической пленки, карбоксиметилированного декстрана, на который адсорбированны молекулы стрептавидина;
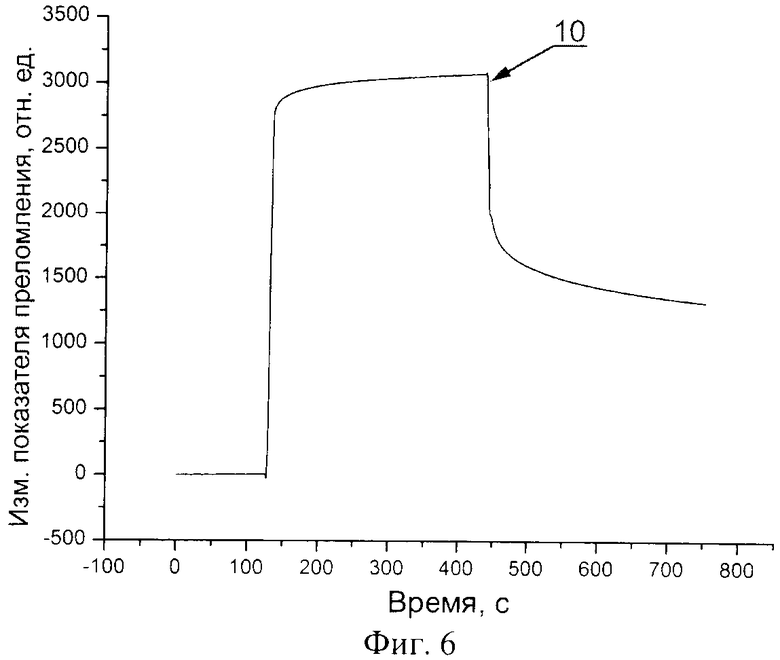
на фиг.6 приведена кинетическая кривая адсорбции молекул, способных образовывать химическую связь с молекулами связывающего партнера, на биологический сенсор на основе тонкой пленки оксида графена;
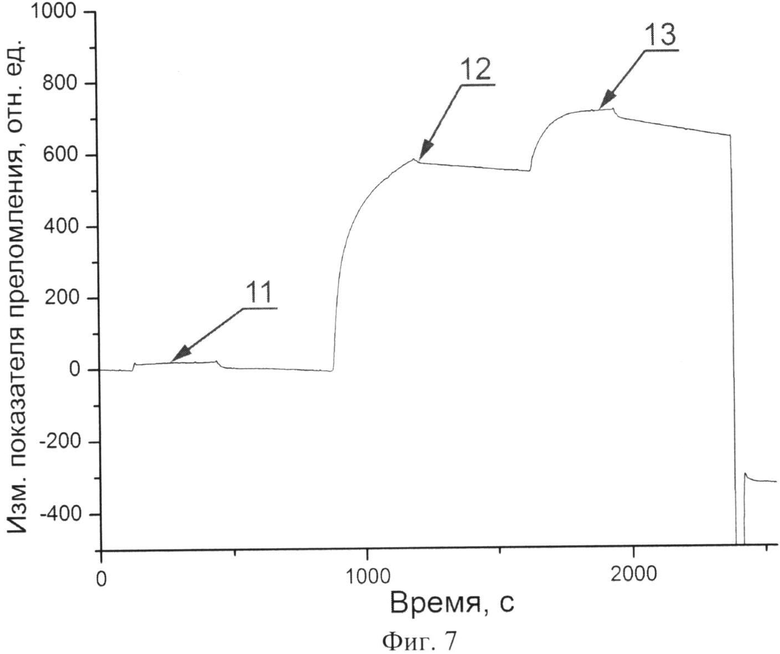
на фиг.7 приведена кинетическая кривая адсорбции олигонуклеотидов на поверхность биоспецифического слоя, включающего в себя молекулы стрептавидина;
на фиг.8 приведено изображение тонкой пленки оксида графена, нанесенной на поверхность металлической пленки и полученной с помощью растровой электронной микроскопии;
на фиг.9 приведена сравнительная таблица экспериментальных данных параметров биологических сенсоров, содержащих в качестве промежуточного связующего слоя тонкую пленку из гидрогеля и тонкую пленку из оксида графена.
Биологический сенсор (фиг.1) состоит из подложки (1), металлической пленки (2), на поверхность которой нанесен промежуточный связующий слой (3), выполненный из тонкой пленки из графена, или тонкой пленки оксида графена, или тонкой пленки из углеродных нанотрубок. На поверхность слоя (3) конформно и однородно адсорбирован биоспецифический слой (4). В качестве биоспецифического слоя может выступать слой молекул связывающего партнера анализируемого вещества (5) (фиг.2) или слой из комплекса биологических молекул (6), способных химически взаимодействовать с молекулами связывающего партнера (5) и образовавших с ними комплекс (фиг.3). Также в качестве биоспецифического слоя может выступать слой гидрогеля (7) (фиг.4), на который осаждены молекулы связывающего партнера (5) и/или комплекс из молекул связывающего партнера и биологических молекул (6), которые могут образовывать химическую связь с молекулами связывающего партнера. На фиг.5 изображена кинетическая кривая адсорбции биотинилированных олигонуклеотидов на поверхность промежуточного связующего слоя биосенсора, включающего тонкую пленку из оксида графена (кривая 8) и на поверхность биологического сенсора, включающего следующие слои: подложку, металлическую пленку и биоспецифический слой, содержащий гидрогель (карбоксиметилированный декстран) и молекулы стрептавидина - (кривая 9). По горизонтальной оси отложено время, на вертикальной - изменение показателя преломления вблизи поверхности адсорбции, пропорциональное массе молекул осажденных на поверхность. Таким образом, можно сделать вывод, что пленка на основе оксида графена обладает лучшими адсорбционными характеристиками по сравнению со слоями, содержащими гидрогель. На фиг.6 приведен график осаждения молекул стрептавидина на биологический сенсор с тонкой пленкой оксида графена.
На фиг.7 приведен график осаждения олигонуклеотидов на биологический сенсор, включающий подложку, состоящую из пластины борсиликатного стекла толщиной 0,4 мм и нанесенной на его поверхности пленки титана толщиной 2 нм. На подложку нанесена золотая пленка толщиной 40 нм, на золотую пленку нанесен промежуточный связующий слой из оксида графена толщиной 20 нм и биоспецифический слой из молекул стрептавидина, с которым образуют устойчивый комплекс молекулы, имеющие биотиновый остаток. Стрептавидин адсорбировали в течение 10 мин из раствора с концентрацией 50 мкг/мл на поверхность промежуточного связующего слоя при помощи проточной ячейки. Три пика на графике отражают осаждение олигонуклеотидов: 11, 13 - без биотинового остатка, 12 - с биотиновым остатком. Олигонуклеотиды, используемые в случае 11, 13, и в случае 12 являются комплементарными и могут образовывать связь между собой. Малость пика в случае 11 говорит о высокой биоспецифичности полученного биологического сенсора, показывающей то, что биологический сенсор взаимодействует только с определенными типами молекул. На фиг.8 приведено изображение слоя оксида графена на поверхности металлической пленки, полученное с помощью растрового электронного микроскопа. В таблице (фиг.9) приведены сравнительные данные, основанные на результатах проведенного эксперимента, биологических сенсоров, содержащих в качестве промежуточного связующего слоя тонкую пленку из гидрогеля толщиной 150 нм и тонкую пленку из оксида графена толщиной 20 нм. В случае биологического сенсора, содержащего пленку из гидрогеля, сигнал, полученный при детектировании биотинилированных ДНК и пропорциональный изменению показателя преломления вблизи поверхности биологического сенсора, составил 409 относительных единиц, а в случае биологического сенсора, содержащего пленку из оксида графена, сигнал составил 570 относительных единиц. Таким образом, отклик, а следовательно, и чувствительность при биодетектировании с использованием биологического сенсора, содержащего в качестве промежуточного связующего слоя тонкую пленку из оксида графена, выше на 40%.
Устройство работает следующим образом. К биоспецифическому слою (4) биологического сенсора подводится раствор с анализируемым веществом при помощи проточной ячейки или кюветы. При этом между анализируемым веществом и молекулами биоспецифического слоя (4) в виде молекул связывающего партнера анализируемого вещества (5), прикрепленным к поверхности промежуточной связующей пленки (3) непосредственно либо с участием биологических молекул (6), способных образовывать химическую связь с молекулами связывающего партнера, и/или гидрогелем (7), осажденным на поверхность биологического сенсора, осуществляется химическая реакция. Далее с помощью метода биодетектирования, основанного на поверхностном плазмонном резонансе, происходит получение необходимых параметров данной реакции. Суть метода состоит в том, что прикрепляемые к поверхности биологического сенсора молекулы меняют эффективный показатель преломления среды вблизи этой поверхности, изменяя таким образом резонансные условия возбуждения поверхностных плазмонов на металлическом слое (2) биологического сенсора, которые могут детектироваться различными способами. Наиболее распространенным в коммерческих устройствах способом является возбуждение поверхностных плазмонов, предложенное Кречманом [6] и состоящее в том, что падающий под определенным углом на металлическую пленку (2) со стороны подложки (1), имеющей больший показатель преломления, чем среды с биологическими молекулами, лазерный луч возбуждает поверхностные плазмоны на границе металлической пленки (2) и среды с анализируемыми биологическими молекулами. При этом оптимальные значения толщины металлической пленки (2) находятся в диапазоне 10-150 нм, верхняя граница объясняется тем фактом, что при более высоких значениях толщины пленки провал в отражении луча в схеме Кречмана будет малым, что сильно скажется на чувствительности метода. При значениях толщины пленки (2) менее 10 нм изменится форма резонансной кривой, соответствующей поверхностному плазмону, из-за изменения вида самой волноводной моды поверхностного плазмона. Далее на основе получения значений величин резонансного угла возбуждения плазмонов, резонансной длины волны, сдвига фаз в отраженном от металлической пленке луче или изменении интенсивности отраженного луча получают информацию об изменении показателя преломления среды, находящейся вблизи металлической пленки. При этом не имеет смысла наносить промежуточный связующий слой (3) на поверхность металлической пленки (2) с толщиной более 2000 нм ввиду того, что глубина проникновения электромагнитного поля поверхностного плазмона в среду около 500 нм, соответственно, молекулы, находящиеся на расстоянии более 2000 нм от поверхности металлической пленки (2), оказывают слабое влияние на условия возбуждения поверхностного плазмона, а следовательно, не могут быть детектированы. В свою очередь промежуточный связующий слой (3) толщиной более 2000 нм затруднит доступ детектируемого вещества в область, где оно может быть детектировано. Минимальная толщина промежуточного связующего слоя (3), содержащего графен, соответствует мономолекулярному слою, толщина которого принимается равной 0,3 нм [7]. Для промежуточного связующего слоя (3), содержащего оксид графена, минимальная возможная толщина, соответствующая мономолекулярному слою, равна 0,7 нм [8]. Для промежуточного связующего слоя (3), содержащего углеродные нанотрубки, минимальная возможна толщина равна диаметру углеродных нанотрубок, который может быть равен 0,4 нм [9]. При работе биологического сенсора в качестве анализируемого вещества могут использовать молекулы протеинов, липидов, ДНК, РНК, вирусы, клетки, бактерии или токсины, а также химические модификации приведенных веществ.
Способ создания биологического сенсора реализуется следующим образом.
На подложку (1) наносят металлическую пленку (2), например, при помощи электронно-лучевого осаждения. Так, например, для нанесения золотой пленки толщиной 40 нм в качестве подложки используют пластину боросиликатного стекла толщиной 0,4 мм с нанесенной на его поверхность пленкой титана толщиной 2 нм. Далее при помощи электронно-лучевого осаждения, проводимого в вакуумной камере с давлением 10-7 мм рт.ст. при ускоряющем напряжении электронов 4 кВ и температуре в камере 150 градусов Цельсия, проводят осаждение золота на подложку. Толщина и оптические свойства получаемой золотой пленки контролируется при помощи эллипсометрических измерений.
Далее на поверхность металлической пленки (2) наносят промежуточный связующий слой (3) в виде тонкой пленки на основе графена, оксида графена или однослойных или многослойных углеродных нанотрубок (изображение пленки на основе оксида графена, полученное с помощью растрового электронного микроскопа, приведено на фиг.8). Тонкую пленку из графена, оксида графена или однослойных или многослойных углеродных нанотрубок наносят с использованием раствора соответствующего вещества и его последующей фильтрацией с помощью целлюлозной мембраны. После процесса фильтрации мембрана помещается на поверхность металлической пленки и растворяется в ацетоне, оставляя тонкую пленку из графена, оксида графена или углеродных нанотрубок. Так, например, для нанесения промежуточного связующего слоя, содержащего тонкую пленку из оксида графена толщиной 20 нм, используют 1 мл раствора оксида графена в воде концентрацией 5 мкг/мл.
Следующим этапом создания биологического сенсора является стадия нанесения на промежуточный связующий слой (3) биоспецифического слоя (4), при которой осуществляют непосредственную адсорбцию из раствора молекул, составляющих биоспецифический слой, таких как молекул связывающего партнера анализируемого вещества (5), молекул, способных взаимодействовать с молекулами связывающего партнера (6) или гидрогеля (7). Раствор с биомолекулами приводят в контакт с промежуточным связующим слоем (3) с помощью, например, проточной ячейки или кюветы. На фиг.6 приведена кинетическая кривая (10) адсорбции молекул стрептавидина, являющихся связывающим партнером к молекулам, имеющим биотиновые остатки, с использованием проточной ячейки. При этом время адсорбции выбирают таким образом, чтобы наносимые биологические молекулы заняли большое количество центров активации на поверхности графена, оксида графена или углеродных нанотрубок, исключив таким образом в дальнейшем неспецифическое связывание молекул из анализируемого раствора с поверхностью биологического сенсора. При этом не требуется использование специальных веществ для создания таких пленок, кроме непосредственно наносимых молекул. Так, например, для адсорбции биоспецифического слоя, содержащего молекулы стрептавидина, на поверхность пленки из оксида графена данные молекулы адсорбируют из раствора концентрацией 10 мкг/мл при помощи проточной ячейки в течение 10 мин. В дальнейшем качество полученной поверхности можно проверить использованием тестового образца, про который известно, что молекулы из его состава не должны взаимодействовать с полученным биологическим слоем. Кинетическая кривая (12) осаждения биотинилированных ДНК на полученный биосенсор, содержащий молекулы стрептавидина, приведена на фиг.7. Малость пика (11), отражающего взаимодействие небиотинилированных молекул со слоем стрептавидина, показывает достаточный уровень малости неспецифических взаимодействий.
Предлагаемые устройство и способ его создания обеспечивают в сравнении с известным уровнем техники получение следующих технических результатов: высокую чувствительность биосенсора в сочетании с высокой биоспецифичностью; расширение спектра применения устройства; защиту металлической пленки от воздействий внешней среды, что позволит использовать в процессе биодетектирования реагенты, которые могли бы повредить поверхность металла, а также использовать такие плазмонные материалы, как серебро, легко повреждающие при воздействии внешней среды; возможность детектирования крупных биологических объектов.
Таким образом, новая взаимосвязь известных и совокупности отличительных признаков предлагаемого биосенсора и способа его создания позволяют обеспечить создание высокочувствительного и универсального биологического сенсора для биодетектирования, основанного на поверхностном плазмонном резонансе.
Предлагаемое устройство и способ его создания могут быть использованы для контроля и регистрации концентрации химических и биохимических веществ и определения параметров биомолекулярных реакций в различных промышленных процессах, происходящих с использованием биологического материала.
Предлагаемое изобретение может быть использовано также в фармацевтической промышленности для исследования фармакологических свойств и определения химического состава разрабатываемых лекарственных средств.
Кроме того, разрабатываемое устройство и способ его создания могут быть применены в процессах контроля качества продукции пищевой промышленности.
Источники информации
1. Патент US 5242828.
2. Патент GB 2459604.
3. Описание по заявке EP 2216642 A1.
4. Wijaya Е., Maaloulib N., Boukherroubb R., Szuneritsb S., Vilcota J-P., "Graphene-based high-performance surface plasmon resonance biosensors", Proceedings of SPIE, Vol.8424, 84240R, 2012.
5. Патент US 5763191.
6. Schasfoort R.B.M., Tudos A.J., Handbook of Surface Plasmon Resonance, RCS Publishing, Cambridge, 2008.
7. Blake P., Hill E.W., Castro Neto A.H., Novoselov K.S., Jiang D., Yang R., Booth T.J., and Geim A.K., "Making graphene visible", Appl. Phys. Lett., Vol.91, 063124, 2007.
8. Pandey D., Reifenberger R., Piner R., "Scanning probe microscopy study of exfoliated oxidized graphene sheets", Surface Science, V. 602, p.1607-1613, 2008.
9. Guan L., Suenaga K., and Iijima S., "Smallest Carbon Nanotube Assigned with Atomic Resolution Accuracy", Nano Letters, Vol.8, p.459-462, 2008.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ИЗГОТОВЛЕНИЯ БИОЛОГИЧЕСКОГО СЕНСОРА НА ОСНОВЕ ОКСИДА ГРАФЕНА И БИОЛОГИЧЕСКИЙ СЕНСОР НА ГИБКОЙ ПОДЛОЖКЕ | 2018 |
|
RU2697701C1 |
| Оптический сенсор на основе плазмон-индуцированной прозрачности и Фано-резонансов | 2021 |
|
RU2770648C1 |
| Способ изготовления матричного биосенсора на основе восстановленного оксида графена и матричный биосенсор на полимерной подложке | 2019 |
|
RU2745663C1 |
| Флуоресцентный оптический ДНК-биосенсор | 2016 |
|
RU2616879C1 |
| ЧУВСТВИТЕЛЬНЫЙ ЭЛЕМЕНТ БИОЛОГИЧЕСКОГО СЕНСОРА | 2016 |
|
RU2661884C2 |
| Способ получения тонких слоёв оксида графена с формированием подслоя из углеродных нанотрубок | 2018 |
|
RU2693733C1 |
| ГАЗОВЫЙ СВЧ-СЕНСОР | 2018 |
|
RU2679458C1 |
| ГАЗОАНАЛИТИЧЕСКИЙ МУЛЬТИСЕНСОРНЫЙ ЧИП НА ОСНОВЕ ГРАФЕНА И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2021 |
|
RU2775201C1 |
| ХИМИЧЕСКИ МОДИФИЦИРОВАННЫЙ ПЛАНАРНЫЙ ОПТИЧЕСКИЙ СЕНСОР, СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ И СПОСОБ АНАЛИЗА ПОЛИАРОМАТИЧЕСКИХ ГЕТЕРОЦИКЛИЧЕСКИХ СЕРОСОДЕРЖАЩИХ СОЕДИНЕНИЙ С ЕГО ПОМОЩЬЮ | 2015 |
|
RU2572801C1 |
| КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ ГКР-АКТИВНОСТЬЮ ДЛЯ ОПРЕДЕЛЕНИЯ ПОЛИАРОМАТИЧЕСКИХ ГЕТЕРОЦИКЛИЧЕСКИХ СЕРОСОДЕРЖАЩИХ СОЕДИНЕНИЙ В УГЛЕВОДОРОДНЫХ ПРОДУКТАХ, СПОСОБ ПОЛУЧЕНИЯ КОМПОЗИЦИИ, ПЛАНАРНЫЙ ТВЕРДОФАЗНЫЙ ОПТИЧЕСКИЙ СЕНСОР НА ЕЕ ОСНОВЕ И СПОСОБ ЕГО ПОЛУЧЕНИЯ, ПРИМЕНЕНИЕ СЕНСОРА ДЛЯ АНАЛИЗА ПОЛИАРОМАТИЧЕСКИХ ГЕТЕРОЦИКЛИЧЕСКИХ СЕРОСОДЕРЖАЩИХ СОЕДИНЕНИЙ | 2016 |
|
RU2627980C1 |


Группа изобретений относится к области биотехнологии, а именно к исследованию биомолекулярных взаимодействий и детектированию биомолекул с использованием поверхностного плазмонного резонанса. Описаны биологический сенсор, а также способ создания биологического сенсора с использованием тонких пленок на основе графена, оксида графена или однослойных или многослойных углеродных нанотрубок. Биологический сенсор состоит из подложки, металлической пленки, на поверхность которой нанесен промежуточный связующий слой, выполненный из тонкой пленки из графена, или тонкой пленки оксида графена, или тонкой пленки из углеродных нанотрубок. На поверхность промежуточного связующего слоя конформно и однородно адсорбирован биоспецифический слой. В качестве биоспецифического слоя может выступать слой молекул связывающего партнера анализируемого вещества или слой из комплекса биологических молекул, способных химически взаимодействовать с молекулами связывающего партнера и образовавших с ними комплекс. Также в качестве биоспецифического слоя может выступать слой гидрогеля, на который осаждены молекулы связывающего партнера и/или комплекс из молекул связывающего партнера и биологических молекул, которые могут образовывать химическую связь с молекулами связывающего партнера. Описанный способ получения биологического сенсора включает в себя стадии нанесения металлической пленки, промежуточного связующего слоя и биоспецифического слоя. Достигается высокая чувствительность биосенсора в сочетании с высокой биоспецифичностью; расширение спектра применения устройства; защита металлической пленки от воздействий внешней среды; возможность детектирования крупных биологических объектов. 2 н. и 25 з.п. ф-лы, 9 ил.
1. Биологический сенсор, состоящий из подложки, на поверхность которой нанесена металлическая пленка, на внешней поверхности которой расположен промежуточный связующий слой с адсорбированным на его поверхность биоспецифическим слоем, отличающийся тем, что промежуточный связующий слой выполнен из тонкой пленки из графена толщиной 0,3-2000 нм, или тонкой пленки из однослойных или многослойных углеродных нанотрубок толщиной 0,4-2000 нм, или тонкой пленки из оксида графена толщиной 0,7-2000 нм, а биоспецифический слой расположен на поверхности промежуточного связующего слоя конформно и однородно и выполнен с возможностью осуществления избирательного химического взаимодействия с анализируемыми биологическими молекулами.
2. Биологический сенсор по п.1, отличающийся тем, что в качестве металлической пленки используют пленку из золота, серебра, меди или алюминия толщиной 10-150 нм.
3. Биологический сенсор по п.1, отличающийся тем, что биоспецифический слой содержит молекулы связывающего партнера анализируемого вещества.
4. Биологический сенсор по п.1, отличающийся тем, что биоспецифический слой содержит молекулы связывающего партнера анализируемого вещества и молекулы, обладающие высоким сродством к связывающим партнерам молекул анализируемого вещества и образующие с ними химическую связь.
5. Биологический сенсор по п.1, отличающийся тем, что биоспецифический слой содержит гидрогель с иммобилизованными в нем молекулами связывающего партнера анализируемого вещества.
6. Биологический сенсор по п.1, отличающийся тем, что биоспецифический слой содержит гидрогель с иммобилизованными в нем молекулами связывающего партнера молекул анализируемого вещества и молекулами, обладающими высоким сродством к молекулам связывающего партнера анализируемого вещества и образующими с ними химическую связь.
7. Биологический сенсор по п.5 или 6, отличающийся тем, что в качестве гидрогеля биоспецифический слой содержит полисахариды.
8. Биологический сенсор по п.7, отличающийся тем, что в качестве полисахаридов биоспецифический слой содержит агарозу, альгиновую кислоту, декстран, каррагинан, крахмал, целлюлозу или их производные.
9. Биологический сенсор по п.8, отличающийся тем, что в качестве производных декстрана биоспецифический слой содержит карбоксиметилированный декстран.
10. Биологический сенсор по п.4 или 6, отличающийся тем, что в качестве молекул, обладающих высоким сродством к молекулам связывающего партнера анализируемого вещества, биоспецифический слой содержит молекулы авидина, стрептавидина и дегликозилированного авидина, молекулы связывающего партнера при этом являются биотинилированными.
11. Биологический сенсор по любому из пп.3-6, отличающийся тем, что связывающим партнером анализируемого вещества является антитело или фрагмент антитела к анализируемому веществу.
12. Биологический сенсор по любому из пп.3-6, отличающийся тем, что связывающим партнером анализируемого вещества является рецептор анализируемого вещества.
13. Биологический сенсор по любому из пп.3-6, отличающийся тем, что связывающим партнером анализируемого вещества является связывающий партнер протеинов, липидов, ДНК, РНК, вирусов, клеток, бактерий или токсинов, а также к химических модификаций приведенных веществ.
14. Способ создания биологического сенсора, охарактеризованного в п.1, состоящий из стадий:
а) стадии нанесения металлической пленки на подложку;
б) стадии нанесения промежуточного связующего слоя на внешнюю поверхность металлической пленки;
в) стадии нанесения биоспецифического слоя на поверхность промежуточного связующего слоя,
отличающийся тем, что в качестве промежуточного связующего слоя на внешнюю поверхность металлической пленки наносят тонкую пленку из графена толщиной 0,3-2000 нм, или тонкую пленку из однослойных или многослойных углеродных нанотрубок толщиной 0,4-2000 нм, или тонкую пленку из оксида графена толщиной 0,7-2000 нм, а биоспецифический слой конформно и однородно адсорбируют на поверхность промежуточного связующего слоя за счет возникновения сил химического взаимодействия между молекулами промежуточного связующего слоя и молекулами биоспецифического слоя, обусловленного стэкинг-взаимодействием или взаимодействием молекул биоспецифического слоя с функциональными группами графена, однослойных или многослойных углеродных нанотрубок или оксида графена, при этом при адсорбции обеспечивают создание большого количества центров активации на поверхности промежуточного связующего слоя со степенью заполнения поверхности молекулами биоспецифического слоя 15-100% от площади поверхности промежуточного связующего слоя.
15. Способ по п.14, отличающийся тем, что в качестве металлической пленки наносят пленку из золота, серебра, меди или алюминия толщиной 10-150 нанометров.
16. Способ по п.14, отличающийся тем, что в качестве биоспецифического слоя наносят слой молекул связывающего партнера анализируемого вещества.
17. Способ по п.14, отличающийся тем, что в качестве биоспецифического слоя наносят слой молекул связывающего партнера анализируемого вещества и молекул, обладающих высоким сродством к молекулам связывающего партнера анализируемого вещества и образующих с ними химическую связь.
18. Способ по п.14, отличающийся тем, что в качестве биоспецифического слоя наносят слой гидрогеля с иммобилизованными в нем молекулами связывающего партнера молекул анализируемого вещества
19. Способ по п.14, отличающийся тем, что в качестве биоспецифического слоя наносят слой гидрогеля с иммобилизованными в нем молекулами связывающего партнера анализируемого вещества и молекулами, обладающими высоким сродством к молекулам связывающего партнера анализируемого вещества и образующими с ними химическую связь.
20. Способ по п.18 или 19, отличающийся тем, что в качестве гидрогеля наносят полисахариды.
21. Способ по п.20, отличающийся тем, что в качестве полисахаридов наносят агарозу, альгиновую кислоту, декстран, каррагинан, крахмал, целлюлозу или их производные.
22. Способ по п.21, отличающийся тем, что в качестве производных декстрана биоспецифический слой содержит карбоксиметилированный декстран.
23. Способ по п.file:///7yi917 или 19, отличающийся тем, что в качестве молекул, обладающих высоким сродством к молекулам связывающего партнера анализируемого вещества, наносят молекулы авидина, стрептавидина и дегликозилированного авидина, молекулы связывающего партнера при этом являются биотинилированными.
24. Способ по п.14, отличающийся тем, что взаимодействие молекул биоспецифического слоя с функциональными группами графена, однослойных или многослойных углеродных нанотрубок или оксида графена осуществляется за счет взаимодействия с такими функциональными группами, как эпоксидные, гидроксильные, карбонильные или карбоксильные группы.
25. Способ по любому из пп.16-19, отличающийся тем, что в качестве связывающего партнера анализируемого вещества используют антитело или фрагмент антитела к анализируемому веществу.
26. Способ по любому из пп.16-19, отличающийся тем, что в качестве связывающего партнера анализируемого вещества используют рецептор анализируемого вещества.
27. Способ по любому из пп.16-19, отличающийся тем, что в качестве связывающего партнера анализируемого вещества используют связывающего партнера протеинов, липидов, ДНК, РНК, вирусов, клеток, бактерий или токсинов, а также химических модификаций приведенных веществ.
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
| Колосоуборка | 1923 |
|
SU2009A1 |
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| СЕНСОРНАЯ СТРУКТУРА НА ОСНОВЕ КВАЗИОДНОМЕРНЫХ ПРОВОДНИКОВ | 2008 |
|
RU2379671C1 |
Авторы
Даты
2014-09-10—Публикация
2013-02-20—Подача