Изобретение относится к органической химии и касается новой кристаллической модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона (леналидомид - международное непатентованное название), названной нами β-модификацией, способа ее получения и фармацевтической композиции на ее основе, которая может быть использована в фармацевтической промышленности и медицине в качестве представителя нового класса иммуномодуляторов, обладающего как иммуномодулирующими, так и антиангиогенными свойствами для лечения множественной миеломы.
Известны производные талидомида и их фармацевтически приемлемые соли в качестве представителя нового класса иммуномодуляторов, обладающих как иммуномодулирующими, так и антиангиогенными свойствами, способы их получения и содержащие их фармацевтические композиции для лечения множественной миеломы. (RU 2177944 С2 от 10.01.2002 г; RU 2209207 С2 от 27.07.2003 г; WO 2006/028964 А1 от 16.03.2006 г.; WO 2010/139266 А1 от 9.12.2010 г.; WO 2015/057043 А1 от 23.04.2015 г.; US 7462363 В2 от 23.12.2008 г.; CN 101253163 А от 27.08.2008 г. и др.).
Однако в данных патентах синтезируемые вещества не охарактеризованы на предмет их принадлежности к той или иной полиморфной модификации.
Известны кристаллические и аморфные модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона в виде гидратов, сольватов с органическими растворителями и солей с различными кислотами, а также полиморфные формы этих солей, их сольваты и гидраты, и их смеси. (WO 2009/111948 А1 от 17.09.2009 г.; WO 2009/114601 А2 от 17.09.2009 г.; WO 2011/050590 А1 от 5.05.2011 г.; WO 2011/050962 А1 от 5.05.2011 г.; WO 2011/034504 А1 от 24.03.2011 г.; US 2012/0190711 А1 от 26.07.2012 г.; WO 2015/113314 А1 от 6.08.2015 г.; CN 101817813А от 1.09.2010 г.; CN 102639522 А от 15.08.2012 г.; WO 2005/023192 А2 от 17.03.2005 г.; WO 2012/127493 А1 от 27.09.2012 г.; WO 2014/160686 А1 от 2.10.2014 г.; WO 2011/018101 А1 от 17.02.2011 г.; WO 2010/056384 А1 от 20.05.2010 г.; WO 2013/012485 А2 от 24.01.2013 г.; US 2013/0131112 А1 от 23.05.2013 г. и др.).
Однако все эти формы отличаются от заявляемой новой, не известной ранее, кристаллической β-модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона химическим составом - наличием в химической формуле гидратных, сольватных молекул, или наличием анионов кислот.
Известны кристаллические и аморфные модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона: Форма «I» дейтерированная, а также Форма «А», Форма «В» и Форма «I» из чистых рацематов (или их смесей) (WO 2011/069608 А1 от 16.06.2011 г.; WO 2014/066243 А1 от 1.05.2014 г. и др.).
Однако при синтезе этих модификаций использовали чистые рацематы или их искусственные смеси, или дейтерированный леналидомид.
Наиболее близкими к заявляемой новой, не известной ранее, кристаллической β-модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона являются кристаллические полиморфные модификации леналидомида: Форма «А», Форма «F», Форма «G», Форма «I», кристаллическая Форма «I», безводная Форма «I», Форма «Н1», Форма «новая», Форма «аморфная», (WO 2005/023192 А2 от 17.03.2005 г.; WO 2010/054833 А1 от 20.05.2010 г.; WO 2012/127493 А1 от 27.09.2012 г.; WO 2009/114601 А2 от 17.09.2009 г.; DE 102008057335 A3 от 20.05.2010 г.; WO 2010/061209 А1 от 3.06.2010 г.; WO 2011/111053 А1 от 15.09.2011 г.; WO 2011/033468 А1 от 24.03.2011 г.; CN 102453021А от 16.05.2012 г. и др.).
Известные кристаллические модификации леналидомида характеризуются физико-химическими методами анализа такими, как: ядерным магнитным резонансом (ЯМР) - совокупностью химических сдвигов (м.д.), высокоэффективной жидкостной хроматографией (ВЭЖХ) - временами удерживания (мин) и чистотой исследуемого вещества (%), методом рентгенофазового анализа (РФА) - наборами углов (2θ, град), межплоскостных расстояний (d, 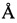 ) и их интенсивностью (I, имп./мин; Iотн.,=Ii/Imax×100, %) или непосредственно рентгенограммами (получение дифрактограмм авторы вышеприведенных патентов проводили на Cu Kα-излучении), термоаналитическими исследованиями - кривыми дифференциальной сканирующей калориметрии (ДСК) - температурами тепловых эффектов и другими.
) и их интенсивностью (I, имп./мин; Iотн.,=Ii/Imax×100, %) или непосредственно рентгенограммами (получение дифрактограмм авторы вышеприведенных патентов проводили на Cu Kα-излучении), термоаналитическими исследованиями - кривыми дифференциальной сканирующей калориметрии (ДСК) - температурами тепловых эффектов и другими.
Сходство заявляемой новой, не известной ранее, кристаллической β-модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона, с известными кристаллическими модификациями леналидомида заключается в идентичности их химических составов.
Отличие заявляемой новой, не известной ранее, кристаллической β-модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона, от известных кристаллических модификаций леналидомида заключается в различии их дифрактограмм рентгенофазового анализа (РФА): определенного набора углов 2θ (град) - межплоскостных расстояний (d, 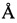 ), и их интенсивностью (Iотн.,=Ii/Imax×100, %), а также в различии их кривых дифференциальной сканирующей калориметрии (ДСК): наличием экзотермического и эндотермического эффекта при определенных температурах.
), и их интенсивностью (Iотн.,=Ii/Imax×100, %), а также в различии их кривых дифференциальной сканирующей калориметрии (ДСК): наличием экзотермического и эндотермического эффекта при определенных температурах.
Известные кристаллические модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона представляют собой порошки от практически белого до бледно-желтого цвета, без запаха, легко растворимые в метаноле, ацетонитриле, очень мало растворимые в воде.
Рассмотренные выше модификации леналидомида получают из различных исходных компонентов или одну из другой в растворах, варьируя тип растворителей, условия приготовления растворов, а также условий выделения из органических растворителей или их смесей различными методами, такими, как кристаллизацией из растворов с последующим фильтрованием, промыванием, сушкой на воздухе, вакуумной сушкой, распылительной сушкой, сублимационной сушкой или другими (US 6281230 В1 от 28.08.2001 г.; WO 2005/023192 А2 от 17.03.2005 г.; US 6555554 В2 от 29.04.2003 г.; CN 102070606 А от 25.05.2011 г.; US 2012/0046315 А1 от 23.02.2012 г.; WO 2009/097120 А1 от 6.08.2009 г.; WO 2009/114601 А2 от 17.09.2009 г.; DE 102008057335 A3 от 20.05.2010 г.; WO 2011/111053 А1 от 15.09.2011 г.; WO 2011/033468 А1 от 24.03.2011 г.; WO 2011/061611 А1 от 26.05.2011 г.; WO 2011/027326 А1 от 10.03.2011 г.; US 8946265 В2 от 3.02.2015 г. и др.).
Наиболее близким по технической сущности является способ получения аморфной модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона, заключающийся в том, что леналидомид растворяют при 20-100°С в растворителе или в смеси растворителей, охлаждают до - 55°С для замораживания и полученный замороженный материал подвергают сублимационной сушке (лиофилизируют) при остаточном давлении менее 7,5×10-2 мм рт.ст. (0,1 мбар) и определенной температурой (между температурой на продукте и температурой равной Тх - 10°С). После процесса лиофилизации, продукт нагревают до комнатной температуры. К сожалению скорости замораживания раствора леналидомида и конкретных температур сублимационной сушки (на конденсаторе и на продукте), авторы патента не указали (US 2012/0046315 А1 от 23.02.2012 г.).
Отличие способа получения заявляемой новой, не известной ранее, кристаллической β-модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-дйона от способов получения известных кристаллических и аморфных форм леналидомида состоит в том, что раствор леналидомида в смешанном водно-органическом растворителе в соотношении 10:1-10:3 при 25-80°С замораживают при скорости охлаждения не ниже 60 град/мин и подвергают сублимационной сушке.
Отличие заявляемой фармацевтической композиции на основе 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона в качестве представителя нового класса иммуномодуляторов, обладающего как иммуномодулирующими, так и антиангиогенными свойствами для лечения множественной миеломы от известной композиции (Регистр Лекарственных Средств России - Инструкция применения препарата Ревлимид®; /Revlimid®;) состоит в том, что в качестве действующего вещества используют терапевтически эффективное количество новой, не известной ранее, кристаллической β-модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона (леналидомида).
Целью изобретения является получение новой, не известной ранее, кристаллической β-модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона (леналидомида), разработка способа ее получения и применение ее в фармацевтической композиции в качестве представителя нового класса иммуномодуляторов, обладающего как иммуномодулирующими, так и антиангиогенными свойствами для лечения множественной миеломы.
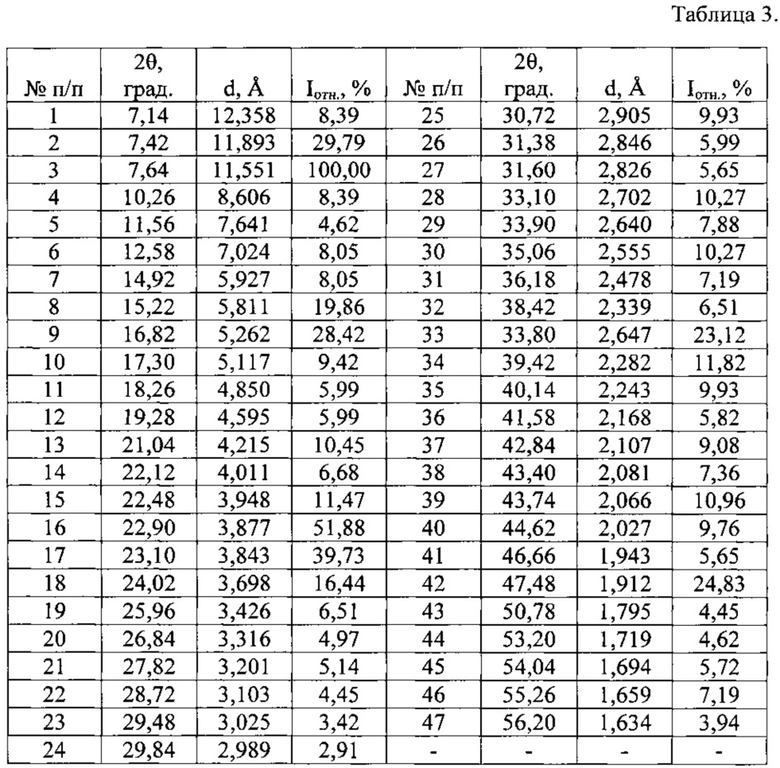
Поставленная цель достигнута настоящим изобретением, а именно получением новой, не известной ранее, кристаллической β-модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона, характеризующейся следующим набором межплоскостных расстояний (d, 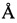 ) и соответствующих им интенсивностей (Iотн.,=Ii/Imax×100, %): 12,358-8,39%; 11,893-29,79%; 11,551-100,00%; 8,606-8,39%; 7,641-4,62%; 7,024-8,05%; 5,927-8,05%; 5,811-19,86%; 5,262-28,42%; 5,117-9,42%; 4,850-5,99%; 4,595-5,99%; 4,215-10,45%; 4,011-6,68%; 3,948-11,47%; 3,877-51,88%; 3,843-39,73%; 3,698-16,44%; 3,426-6,51%; 3,316-4,97%; 3,201-5,14%; 3,103-4,45%; 3,025-3,42%; 2,989-2,91%; 2,905-9,93%; 2,846-5,99%; 2,826-5,65%; 2,702-10,27%; 2,640-7,88%; 2,555-10,27%; 2,478-7,19%; 2,339-6,51%; 2,647-23,12%; 2,282-11,82%; 2,243-9,93%; 2,168-5,82%; 2,107-9,08%; 2,081-7,36%; 2,066-10,96%; 2,027-9,76%; 1,943-5,65%; 1,912-24,83%; 1,795-4,45%; 1,719-4,62%; 1,694-5,72%; 1,659-7,19%; 1,634-3,94%, и кривой ДСК с двумя тепловыми эффектами: экзотермическим эффектом при температуре (174,9±0,5)°С и эндотермическим эффектом при температуре (267,7±0,5)°С.
) и соответствующих им интенсивностей (Iотн.,=Ii/Imax×100, %): 12,358-8,39%; 11,893-29,79%; 11,551-100,00%; 8,606-8,39%; 7,641-4,62%; 7,024-8,05%; 5,927-8,05%; 5,811-19,86%; 5,262-28,42%; 5,117-9,42%; 4,850-5,99%; 4,595-5,99%; 4,215-10,45%; 4,011-6,68%; 3,948-11,47%; 3,877-51,88%; 3,843-39,73%; 3,698-16,44%; 3,426-6,51%; 3,316-4,97%; 3,201-5,14%; 3,103-4,45%; 3,025-3,42%; 2,989-2,91%; 2,905-9,93%; 2,846-5,99%; 2,826-5,65%; 2,702-10,27%; 2,640-7,88%; 2,555-10,27%; 2,478-7,19%; 2,339-6,51%; 2,647-23,12%; 2,282-11,82%; 2,243-9,93%; 2,168-5,82%; 2,107-9,08%; 2,081-7,36%; 2,066-10,96%; 2,027-9,76%; 1,943-5,65%; 1,912-24,83%; 1,795-4,45%; 1,719-4,62%; 1,694-5,72%; 1,659-7,19%; 1,634-3,94%, и кривой ДСК с двумя тепловыми эффектами: экзотермическим эффектом при температуре (174,9±0,5)°С и эндотермическим эффектом при температуре (267,7±0,5)°С.
Поставленная цель достигнута также разработкой способа получения новой, не известной ранее, кристаллической β-модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона, который состоит в том, что раствор леналидомида в смешанном водно-органическом растворителе в соотношении 10:1-10:3 при 25-80°С замораживают при скорости охлаждения не ниже 60 град/мин и подвергают сублимационной сушке.
Кроме того, поставленная цель достигнута применением новой, не известной ранее, кристаллической β-модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона для приготовления фармацевтической композиции в качестве представителя нового класса иммуномодуляторов, обладающего как иммуномодулирующими, так и антиангиогенными свойствами для лечения множественной миеломы. Указанная композиция содержит β-модификацию леналидомида в терапевтически эффективном количестве и, по крайней мере, один фармацевтически приемлемый носитель, разбавитель, вспомогательное вещество или наполнитель.
Из патентной и научно-технической литературы не известна кристаллическая β-модификация 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона, способ ее получения и применение ее в фармацевтической композиции в качестве представителя нового класса иммуномодуляторов, обладающего как иммуномодулирующими, так и антиангиогенными свойствами для лечения множественной миеломы.
Нами обнаружена новая, не известная ранее, кристаллическая β-модификация 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона, характеризующаяся определенным набором дифракционных максимумов (d, 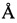 ) и их интенсивностью (Iотн., %), и наличием экзотермического и эндотермического эффектов при определенных температурах на кривой дифференциальной сканирующей калориметрии, предложены способ ее получения и применение ее для приготовления фармацевтической композиции в качестве представителя нового класса иммуномодуляторов, обладающего как иммуномодулирующими, так и антиангиогенными свойствами для лечения множественной миеломы.
) и их интенсивностью (Iотн., %), и наличием экзотермического и эндотермического эффектов при определенных температурах на кривой дифференциальной сканирующей калориметрии, предложены способ ее получения и применение ее для приготовления фармацевтической композиции в качестве представителя нового класса иммуномодуляторов, обладающего как иммуномодулирующими, так и антиангиогенными свойствами для лечения множественной миеломы.
Заявляемая новая, не известная ранее, кристаллическая β-модификация 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона представляет собой легкий, пушистый порошок от практически белого до бледно-желтого цвета, без запаха, легко растворимый в метаноле, ацетонитриле, очень мало растворимый в воде.
Для пояснения сущности заявляемого технического решения к описанию приложены следующие таблицы и рисунки:
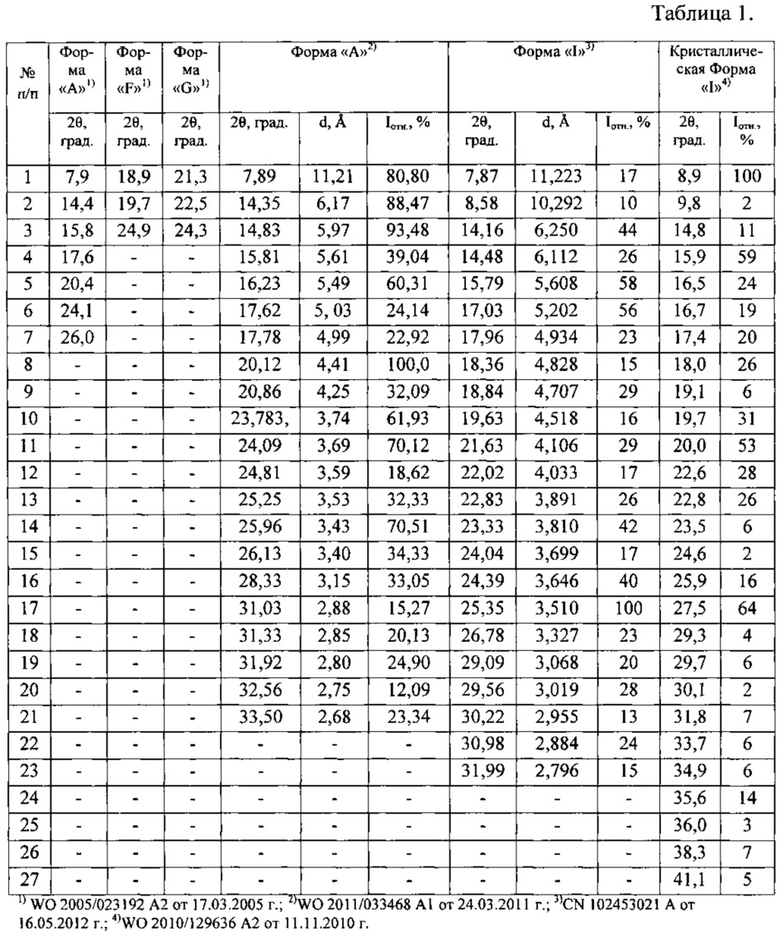
Таблица 1. Углы 2θ, град, межплоскостные расстояния (d, 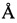 ) и их интенсивности (Iотн., %) известных модификаций леналидомида по литературным данным.
) и их интенсивности (Iотн., %) известных модификаций леналидомида по литературным данным.
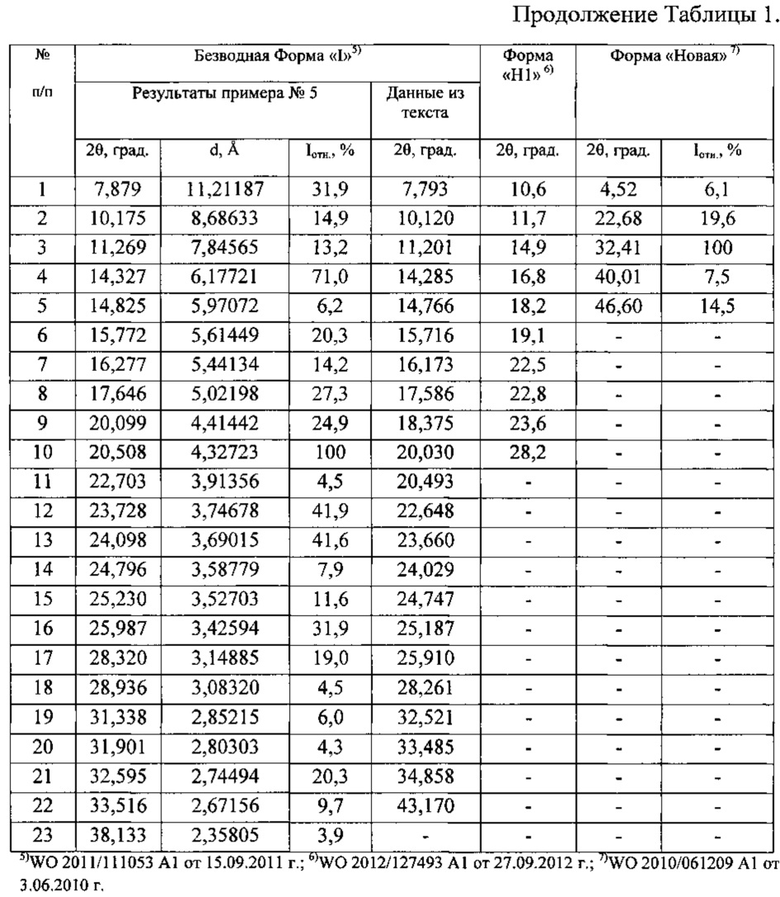
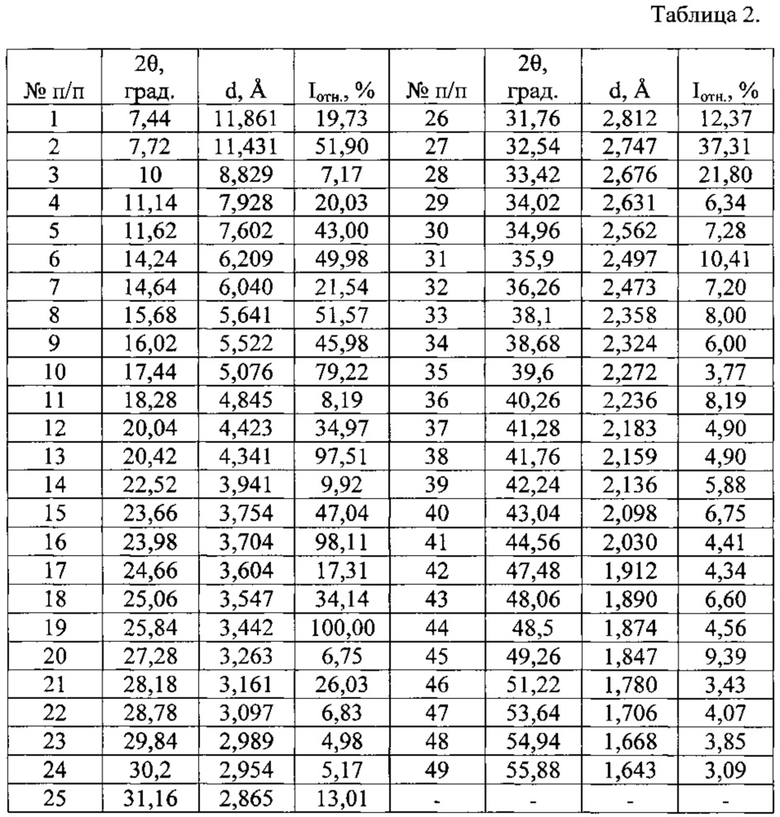
Таблица 2. Углы 2θ, град, межплоскостные расстояния (d, 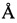 ) и их интенсивности (Iотн., %) известной кристаллической модификации леналидомида (Форма «А»), которую использовали в качестве исходного вещества.
) и их интенсивности (Iотн., %) известной кристаллической модификации леналидомида (Форма «А»), которую использовали в качестве исходного вещества.
Таблица 3. Углы 2θ, град, межплоскостные расстояния (d, 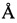 ) и их интенсивности (Iотн., %) новой, не известной ранее, кристаллической β-модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона.
) и их интенсивности (Iотн., %) новой, не известной ранее, кристаллической β-модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона.
Таблица 4. Температуры максимумов эндотермических пиков известных модификаций леналидомида по литературным данным.
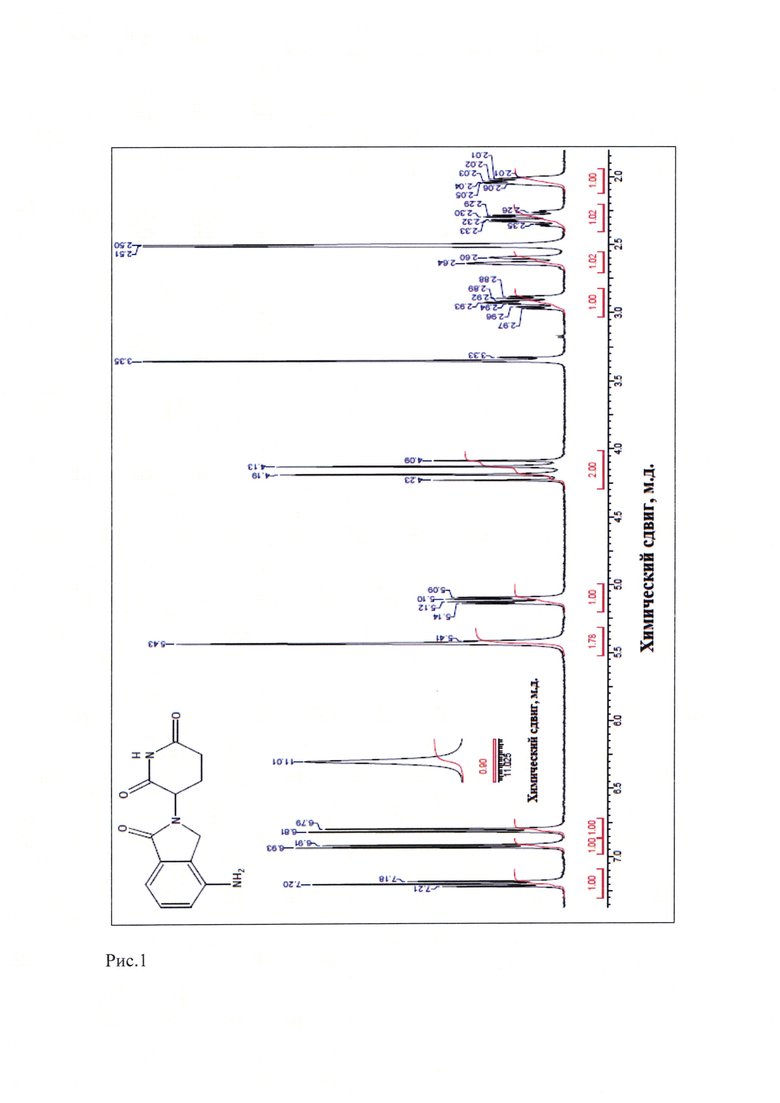
Рис. 1. ЯМР 1Н-спектр известной кристаллической модификации леналидомида (Форма «А»), которую использовали в качестве исходного вещества.
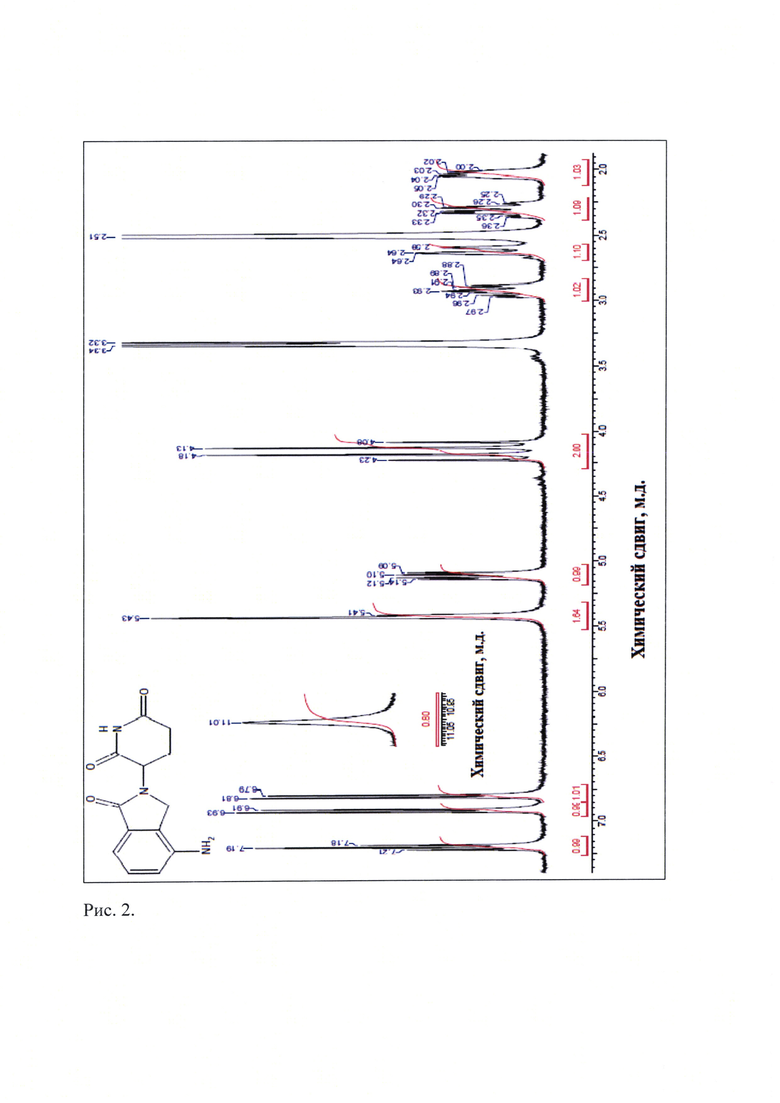
Рис. 2. ЯМР 1Н-спектр новой, не известной ранее, кристаллической β-модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона.
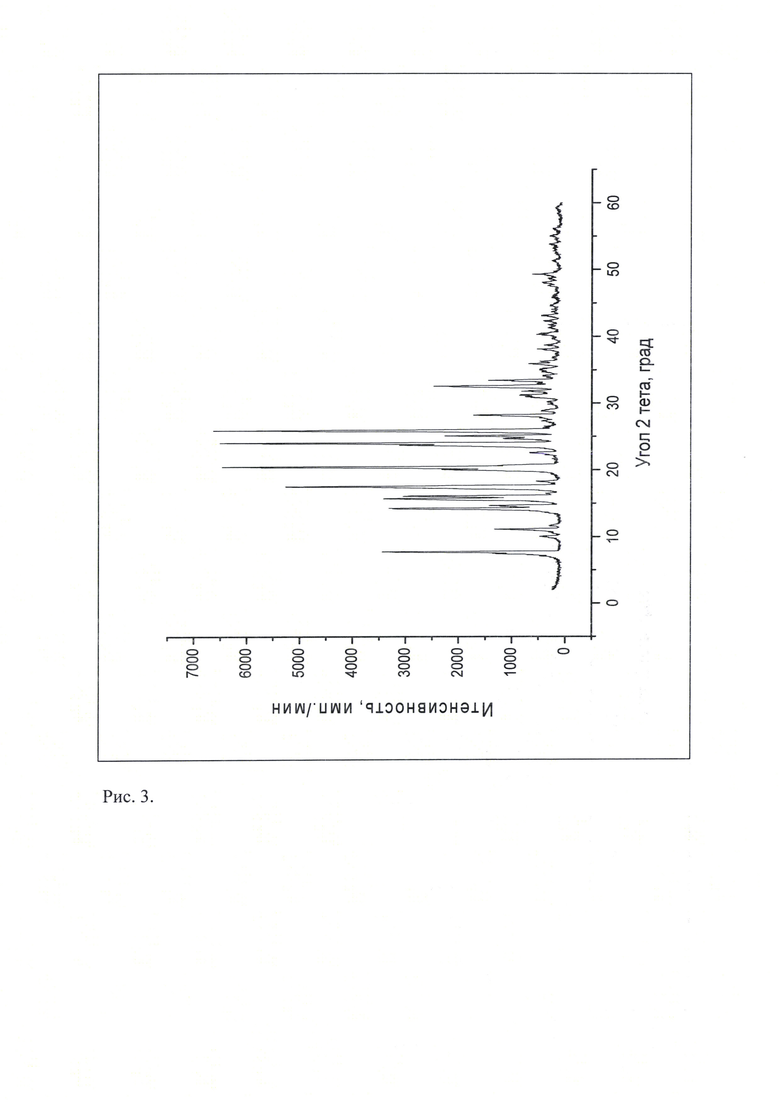
Рис. 3. Дифрактограмма известной кристаллической модификации леналидомида (Форма «А»), которую использовали в качестве исходного вещества.
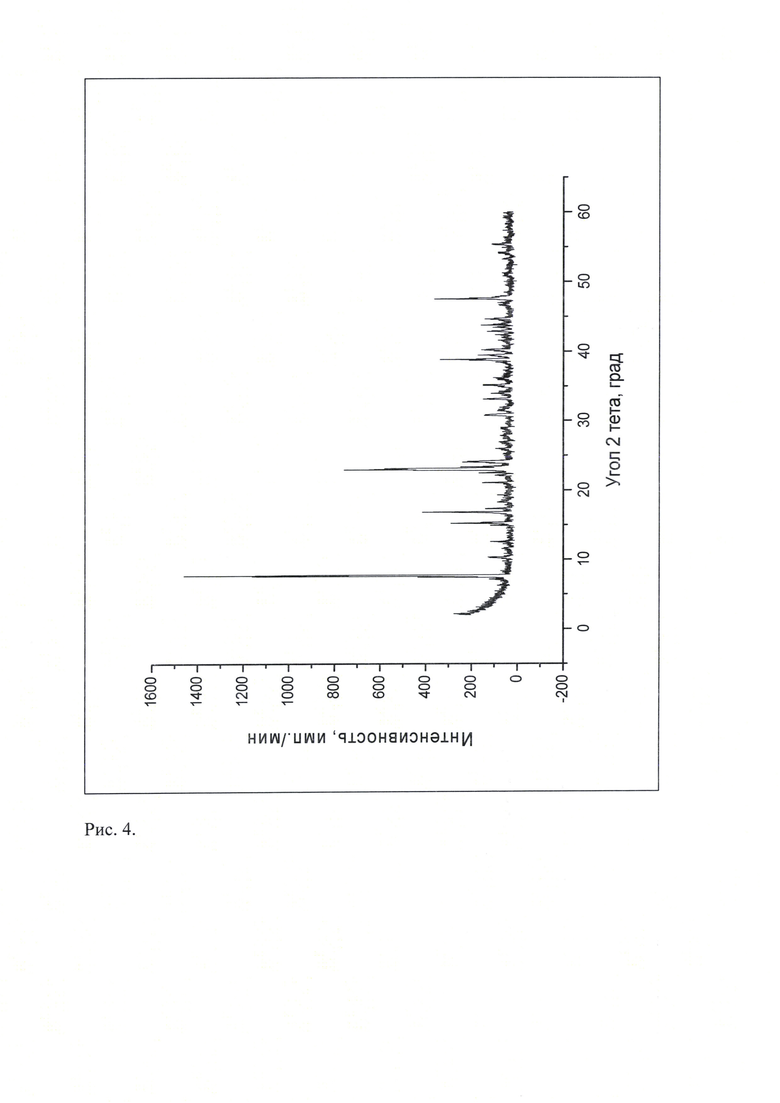
Рис. 4. Типичная дифрактограмма новой, не известной ранее, кристаллической β-модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона.
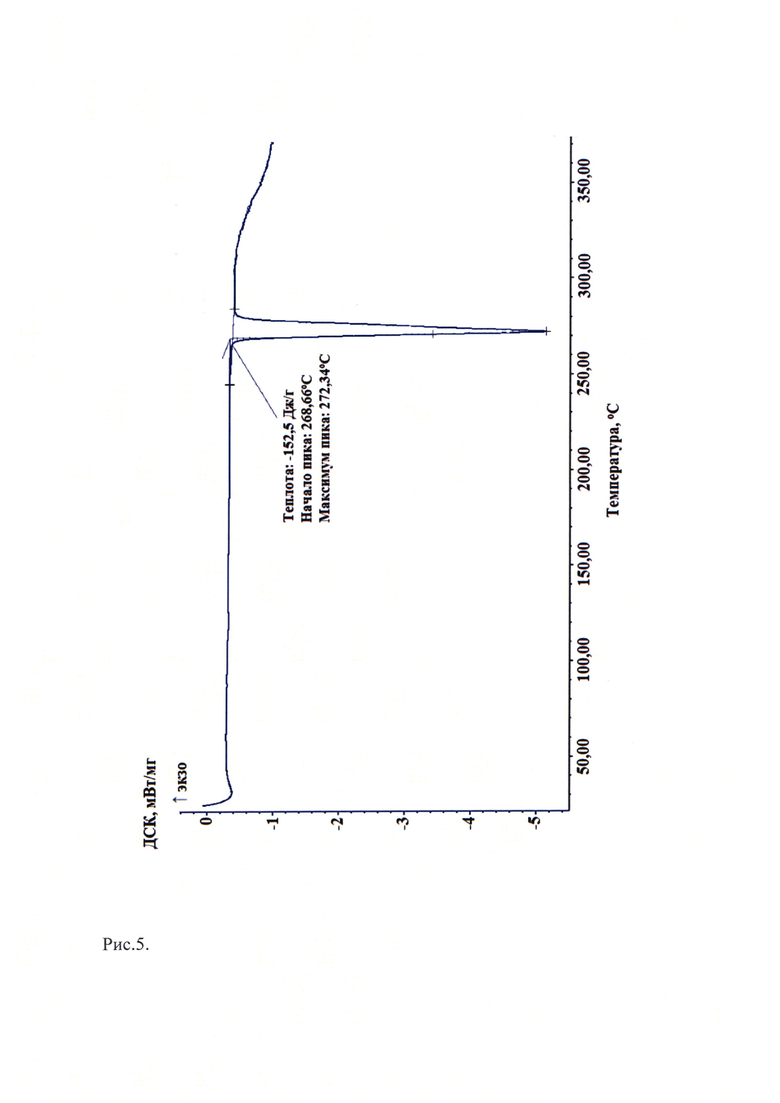
Рис. 5. Кривая дифференциальной сканирующей калориметрии известной кристаллической модификации леналидомида (Форма «А»), которую использовали в качестве исходного вещества.
Рис. 6. Типичная кривая дифференциальной сканирующей калориметрии новой, не известной ранее, кристаллической β-модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона.
Для идентификации полученного вещества был проведен комплекс физико-химических методов анализа.
Первоначально, методами ядерного магнитного резонанса (ЯМР 1Н), и высокоэффективной жидкостной хроматографии (ВЭЖХ) была установлена идентичность химических формул известной кристаллической модификации леналидомида (Форма «А»), которую использовали в качестве исходного вещества, и новой, не известной ранее, кристаллической β-модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона.
Определение химических сдвигов исходного леналидомида и полученного из него вещества было проведено в его насыщенном растворе в дейтерированном диметилсульфоксиде (ДМСО-D6) на ЯМР-спектрометре высокого разрешения VXR-400 фирмы "VARIAN" (США). Полученные данные приведены на рис. 1 и 2, соответственно. Сравнение результатов, представленных на рис.1 [известная кристаллическая модификация леналидомида (Форма «А»)], с данными, приведенными на рис. 2 [новая, не известная ранее, кристаллическая β-модификация 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона] показывает, что ЯМР-1Н-спектры исходного и полученного из него вещества практически идентичны, т.е. полученное вещество является 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона.
Хроматографическую подвижность известной кристаллической модификации леналидомида (Форма «А»), которую использовали в качестве исходного вещества и, полученной из нее, новой, не известной ранее, кристаллической β-модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона определяли методом ВЭЖХ на хроматографе Shimadzu LC-20A с детектором SPD-M20A и с колонкой длиной 50 мм, сорбентом Grace Apollo C18 "Agilent" (США) с детектированием при длине волны 210,4 нм. В качестве подвижной фазы использовали метиловый спирт и фосфатный буферный раствор с pH=3, температура колонки была равна 42°С, а скорость потока - 1 мл/мин. Объем испытуемой пробы составил 5 мкл с концентрацией 0,5 мг/мл. Оказалось, что хроматограммы известной кристаллической модификации леналидомида (Форма «А»), которую использовали в качестве исходного вещества, и новой, не известной ранее, кристаллической β-модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона содержат по одному пику основного компонента с характерными временами удерживания 10,072 мин и 10,163 мин, соответственно. Эти величины времен удерживания, в пределах ошибки определения, практически одинаковы. Чистота исследованных образцов, определенных методом ВЭЖХ составили 99,81% (исходное вещество) и 99,37% (новая, не известная ранее, кристаллическая β-модификация леналидомида).
Проведенные методом ВЭЖХ эксперименты, свидетельствуют о том, что при получении новой, не известной ранее, кристаллической β-модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона из исходного вещества - известной кристаллической модификации леналидомида (Форма «А»), разложения исходного вещества не происходит.
Таким образом экспериментальные результаты ядерного магнитного резонанса (ЯМР-1Н) и высокоэффективной жидкостной хроматографии (ВЭЖХ) однозначно свидетельствуют о том, что полученное вещество является 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил-пиперидин-2,6-диона.
Для подтверждения того, что полученное вещество является новой, не известной ранее, кристаллической β-модификацией 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона, были проведены рентгенофазовый анализ (РФА) и термоаналитические исследования.
Рентгенофазовый анализ (РФА) известной кристаллической модификации леналидомида, которую использовали в качестве исходного вещества и полученного из нее порошка проводили на дифрактометре Rigaku D/MAX-2500 (Rigaku, Япония) на CuKα излучении  . Полученные данные РФА для леналидомида, который использовали в качестве исходного вещества, приведены в табл. 2 и на рис. 3. Сравнение результатов РФА, представленных в табл. 2 и в табл. 1 (литературные данные), на рис. 3, и на рисунках, приведенных в литературных источниках (WO 2005/023192 А2 от 17.03.2005 г.; WO 2011/033468 А1 от 24.03.2011 г.), однозначно свидетельствует о том, что в качестве исходного вещества была использована известная кристаллическая модификация леналидомида - Форма «А». Результаты рентгенофазового анализа порошка, полученного из известной кристаллической модификации леналидомида, представлены в табл. 3 и на рис. 4. Сравнение полученных данных, представленных в табл. 3, табл. 2 и табл. 1, а также на рис. 3, рис. 4, и на рисунках, приведенных в литературных источниках (WO 2005/023192 А2 от 17.03.2005 г.; WO 2011/033468 А1 от 24.03.2011 г.; CN 102453021 А от 16.05.2012 г.; WO 2010/129636 А2 от 11.11.2010 г.; WO 2011/111053 А1 от 15.09.2011 г.; WO 2012/127493 А1 от 27.09.2012 г.; WO 2010/061209 А1 от 3.06.2010 г. и др.), свидетельствует о том, что полученный порошок леналидомида является новой, не известной ранее, кристаллической β-модификацией 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона.
. Полученные данные РФА для леналидомида, который использовали в качестве исходного вещества, приведены в табл. 2 и на рис. 3. Сравнение результатов РФА, представленных в табл. 2 и в табл. 1 (литературные данные), на рис. 3, и на рисунках, приведенных в литературных источниках (WO 2005/023192 А2 от 17.03.2005 г.; WO 2011/033468 А1 от 24.03.2011 г.), однозначно свидетельствует о том, что в качестве исходного вещества была использована известная кристаллическая модификация леналидомида - Форма «А». Результаты рентгенофазового анализа порошка, полученного из известной кристаллической модификации леналидомида, представлены в табл. 3 и на рис. 4. Сравнение полученных данных, представленных в табл. 3, табл. 2 и табл. 1, а также на рис. 3, рис. 4, и на рисунках, приведенных в литературных источниках (WO 2005/023192 А2 от 17.03.2005 г.; WO 2011/033468 А1 от 24.03.2011 г.; CN 102453021 А от 16.05.2012 г.; WO 2010/129636 А2 от 11.11.2010 г.; WO 2011/111053 А1 от 15.09.2011 г.; WO 2012/127493 А1 от 27.09.2012 г.; WO 2010/061209 А1 от 3.06.2010 г. и др.), свидетельствует о том, что полученный порошок леналидомида является новой, не известной ранее, кристаллической β-модификацией 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона.
Таким образом, экспериментальные результаты рентгенофазового анализа однозначно свидетельствуют о том, что полученное вещество является новой, не известной ранее, кристаллической β-модификацией 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона. Она характеризуется, отличной от других кристаллических модификаций леналидомида, совокупностью межплоскостных расстояний (d, 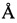 ) и соответствующих им интенсивностей (Iотн., %): 12,358-8,39%; 11,893-29,79%; 11,551-100,00%; 8,606-8,39%; 7,641-4,62%; 7,024-8,05%; 5,927-8,05%; 5,811-19,86%; 5,262-28,42%; 5,117-9,42%; 4,850-5,99%; 4,595-5,99%; 4,215-10,45%; 4,011-6,68%; 3,948-11,47%; 3,877-51,88%; 3,843-39,73%; 3,698-16,44%; 3,426-6,51%; 3,316-4,97%; 3,201-5,14%; 3,103-4,45%; 3,025-3,42%; 2,989-2,91%; 2,905-9,93%; 2,846-5,99%; 2,826-5,65%; 2,702-10,27%; 2,640-7,88%; 2,555-10,27%; 2,478-7,19%; 2,339-6,51%; 2,647-23,12%; 2,282-11,82%; 2,243-9,93%; 2,168-5,82%; 2,107-9,08%; 2,081-7,36%; 2,066-10,96%; 2,027-9,76%; 1,943-5,65%; 1,912-24,83%; 1,795-4,45%; 1,719-4,62%; 1,694-5,72%; 1,659-7,19%; 1,634-3,94%.
) и соответствующих им интенсивностей (Iотн., %): 12,358-8,39%; 11,893-29,79%; 11,551-100,00%; 8,606-8,39%; 7,641-4,62%; 7,024-8,05%; 5,927-8,05%; 5,811-19,86%; 5,262-28,42%; 5,117-9,42%; 4,850-5,99%; 4,595-5,99%; 4,215-10,45%; 4,011-6,68%; 3,948-11,47%; 3,877-51,88%; 3,843-39,73%; 3,698-16,44%; 3,426-6,51%; 3,316-4,97%; 3,201-5,14%; 3,103-4,45%; 3,025-3,42%; 2,989-2,91%; 2,905-9,93%; 2,846-5,99%; 2,826-5,65%; 2,702-10,27%; 2,640-7,88%; 2,555-10,27%; 2,478-7,19%; 2,339-6,51%; 2,647-23,12%; 2,282-11,82%; 2,243-9,93%; 2,168-5,82%; 2,107-9,08%; 2,081-7,36%; 2,066-10,96%; 2,027-9,76%; 1,943-5,65%; 1,912-24,83%; 1,795-4,45%; 1,719-4,62%; 1,694-5,72%; 1,659-7,19%; 1,634-3,94%.
Термоаналитические исследования известной кристаллической модификации леналидомида, которую использовали в качестве исходного вещества и полученной из нее новой, не известной ранее, кристаллической β-модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона проводили на термоанализаторе DSC 204 F1 Poenix (NETZSCH) в токе аргона при повышении температуры 10 град/мин. В качестве держателей образцов использовали алюминиевые кюветы. Навеска пробы составляла (1,3-4,5) мг. Полученные данные приведены на рис. 5 и рис. 6, соответственно. Видно, что на кривой дифференциальной сканирующей калориметрии известной кристаллической модификации леналидомида, которую использовали в качестве исходного вещества (рис. 5) присутствует один эндотермический эффект с максимумом при (272,3±0,5)°С. Сравнение полученных результатов (рис. 5) с литературными данными, представленными в табл. 4 показывают, что в качестве исходного вещества была использована известная кристаллическая модификация леналидомида - Форма «А». Эти исследования подтверждают результаты РФА известной кристаллической модификации леналидомида, которые показали, что в качестве исходного вещества использовали Форму «А». На рис. 6 представлена кривая дифференциальной сканирующей калориметрии новой, не известной ранее, кристаллической β-модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона. Видно, что на кривой ДСК присутствуют два тепловых эффекта: экзотермический эффект при температуре (174,9±0,5)°С и эндотермический эффект при температуре (267,7±0,5)°С. Сравнение результатов, приведенных на рис. 6 с данными, представленными на рис. 5 и в литературных источниках (табл. 4) показывает, что новая, не известная ранее, кристаллическая β-модификация 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона характеризуется, отличной от других кристаллических модификаций леналидомида, кривой ДСК с двумя тепловыми эффектами: экзотермическим эффектом при температуре (174,9±0,5)°С и эндотермическим эффектом при температуре (267,7±0,5)°С. Отметим, что известные кристаллические или аморфная модификации леналидомида характеризуются только одним эндотермическим эффектом на кривой ДСК (см. рис. 5 и табл. 4), кроме аморфной формы и Формы «новой». Они характеризуются дополнительно температурой расстекловывания (смещение базовой линии) и низкотемпературным эндотермическим пиком, соответственно. Ни одна из известных кристаллических или аморфная формы не имеют на кривой ДСК экзотермических эффектов.
Приведенные экспериментальные данные рентгенофазового анализа и термоаналитических исследований однозначно свидетельствуют о том, что полученная новая, не известная ранее, кристаллическая β-модификация 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона характеризуется, отличными от других кристаллических модификаций леналидомида, совокупностью межплоскостных расстояний и соответствующих им интенсивностей и тепловыми эффектами: экзотермическим и эндотермическим при определенных температурах на кривой дифференциальной сканирующей калориметрии.
Способ получения новой, не известной ранее, кристаллической β-модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона, заключается в том, что раствор леналидомида в смешанном водно-органическом растворителе в соотношении 10:1-10:3 при 25-80°С замораживают при скорости охлаждения не ниже 60 град/мин и подвергают сублимационной сушке.
В качестве смешанного водно-органического растворителя возможно использование, например смеси воды с растворителем, выбранным из группы: ацетонитрил, диметилформамид, низшие спирты, такие как метанол или этиловый спирт, гептан, гексан, изопропилацетат, толуол, 1-бутанол и др..
Отличие способа получения заявляемой новой, не известной ранее, кристаллической β-модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона от способа получения известных кристаллических форм леналидомида состоит в том, что раствор леналидомида в смешанном водно-органическом растворителе в соотношении 10:1-10:3 при 25-80°С замораживают при скорости охлаждения не ниже 60 град/мин и подвергают сублимационной сушке.
Предложенный способ получения, заключающийся в том, что раствор леналидомида в смешанном водно-органическом растворителе в соотношении 10:1-10:3 при 25-80°С замораживают при скорости охлаждения не ниже 60 град/мин и подвергают сублимационной сушке, позволяет получить новую, не известную ранее, кристаллическую β-модификацию 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона.
Уменьшение температуры раствора леналидомида в органическом растворителе ниже 25°С (комнатной температуры) не целесообразно поскольку требует дополнительных затрат энергии на охлаждение системы.
Увеличение температуры раствора леналидомида в смешанном водно-органическом растворителе выше 80°С также не целесообразно из-за того, что это приводит к неконтролируемому испарению органического компонента и, как следствие, образованию в системе одной из известных модификаций леналидомина. Получить новую, не известную ранее, кристаллическую β-модификацию 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона в чистом виде не удается.
Увеличение соотношения вода : органический растворитель в водно-органической смеси более 10:1 не целесообразно поскольку не позволяет получать достаточно концентрированные растворы, что не приводит к увеличению выхода целевого продукта - новой, не известной ранее, кристаллической β-модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона и лишь удорожает производство.
Уменьшение соотношения вода : органический растворитель в водно-органической смеси менее 10:3 приводит к тому, что при замораживании полученного раствора леналидомида система стеклуется - аморфизуется (образуется твердый раствор). Это приводит к тому, что при дальнейшей сублимационной сушке замороженный аморфизованный раствор плавится, из него кристаллизуются уже известные модификации. Получить новую, не известную ранее, кристаллическую β-модификацию 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона в чистом виде не удается.
Уменьшение скорости замораживания ниже 60 град/мин приводит к тому, что скорость криокристаллизации раствора леналидомида уменьшается и приближается к равновесному процессу. Это приводит к получению уже известных модификаций. Получить новую, не известную ранее, кристаллическую β-модификацию 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона в чистом виде не удается. Отметим, что известный способ замораживания смеси, содержащий леналидомид (US 2012/0046315 А1 от 23.02.2012 г.) предполагает замораживание при -55°С до твердого состояния. В этих условиях, как правило, реализуется скорость замораживания не выше (20-30) град/мин.
Сублимационная сушка замороженного раствора леналидомида необходима для получения новой, не известной ранее, кристаллической β-модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона. Предпочтительным режимом сублимационной сушки является процесс, который проводят при температурах: на конденсаторе -43°С…-75°С; на продукте -196…+50°С, и остаточном давлении в камере (9-3)×10-2 Торр в течение 22-26 ч.
Уменьшение времени сублимационной сушки меньше 22 ч приводит к получению невысохшего продукта: «порошок леналидомида - его замороженный раствор». Система при комнатной температуре плавится, порошок частично растворяется, перекристаллизовывается, образуя известные модификации. Новую, не известной ранее, кристаллическую β-модификацию 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона в чистом виде получить не удается.
Увеличение времени сублимационной сушки нецелесообразно, так как не приводит к увеличению выхода целевого продукта - новой, не известной ранее, кристаллической β-модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона и лишь удорожает производство.
Возможность осуществления предлагаемого изобретения иллюстрируется следующими примерами, но не ограничивается ими.
Пример 1. 200 мл 0,18 мас. % раствора леналидомида в водно-органическом растворителе - «вода - этанол» при соотношении 10:1, приготовленного при 80°С из известной кристаллической модификации леналидомида (Форма «А»), воды очищенной по ФС 42-2619-97 и спирта этилового ректификованного по ГОСТ 5962-2013, замораживают со скоростью 60 град/мин вливанием сразу всего объема раствора в предварительно наполненный жидким азотом (Ткип=-196°С), но не охлажденный предварительно, поддон из нержавеющей стали. Замороженный продукт на поддоне переносят в сублимационную камеру и подвергают сублимационной сушке при температурах: на конденсаторе -43°С…-48°С; на продукте -196°С…+30°С и остаточном давлении в камере (9-5)⋅10-2 Торр в течение 22 ч. Выход продукта сублимационной сушки - легкого пушистого порошка практически белого цвета составил 0,35 г (97,2 мас. %). По данным РФА полученное вещество характеризуется типичной дифрактограммой, представленной на рис. 4 и набором межплоскостных расстояний и их интенсивностями, совпадающих с соответствующими значениями для новой, не известной ранее, кристаллической β-модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона, представленными в табл. 3. По данным термоаналитических исследований полученное вещество характеризуется типичной кривой дифференциальной сканирующей калориметрии, представленной на рис. 6 и совпадающей, в пределах ошибки определения, с соответствующими значениями для новой, не известной ранее, кристаллической β-модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона. Кривая ДСК характеризуется двумя тепловыми эффектами: экзотермическим эффектом при температуре (174,6±0,5)°С и эндотермическим эффектом при температуре (267,9±0,5)°С. По данным ВЭЖХ чистота полученной новой, не известной ранее, кристаллической β-модификации леналидомида составляет 99,11%.
Пример 2. 300 мл 0,50 мас. % раствора леналидомида в водно-органическом растворителе - «вода - метанол» при соотношении 10:2, приготовленного при 60°С из известной кристаллической модификации леналидомида (Форма «А»), воды очищенной по ФС 42-2619-97 и метилового спирта марки «ХЧ» ГОСТ 2222-95, замораживают со скоростью (2-3)×102 град/мин вливанием раствора небольшими порциями в предварительно охлажденный и наполненный жидким азотом (Ткип=-196°С) поддон из нержавеющей стали. Замороженный продукт на поддоне переносят в сублимационную камеру и подвергают сублимационной сушке при температурах: на конденсаторе -52°С…-56°С; на продукте -196°С…+40°С, и остаточном давлении в камере (9-5)⋅10-2 Торр в течение 26 ч. Выход продукта сублимационной сушки - легкого, пушистого порошка бледно-желтого цвета составил 1,41 г (94,0 мас. %). По данным РФА полученное вещество характеризуется типичной дифрактограммой, представленной на рис. 4 и набором межплоскостных расстояний и их интенсивностями, совпадающих с соответствующими значениями для новой, не известной ранее, кристаллической β-модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона, представленными в табл. 3. По данным термоаналитических исследований полученное вещество характеризуется типичной кривой дифференциальной сканирующей калориметрии, представленной на рис. 6 и совпадающей с соответствующими значениями, в пределах ошибки определения, для новой, не известной ранее, кристаллической β-модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона. Кривая ДСК характеризуется двумя тепловыми эффектами: экзотермическим эффектом при температуре (175,3±0,5)°С и эндотермическим эффектом при температуре (267,5±0,5)°С. По данным ВЭЖХ чистота полученной новой, не известной ранее, кристаллической β-модификации леналидомида составляет 99,37%.
Пример 3. 150 мл 0,46 мас. % раствора леналидомида в водно-органическом растворителе - «вода - ацетонитрил» при соотношении 10:3, приготовленного при 25°С из известной кристаллической модификации леналидомида (Форма «А»), воды очищенной по ФС 42-2619-97 и ацетонитрила марки «ХЧ» ТУ 6-094326-76, замораживают со скоростью примерно 103 град/мин распылением раствора пневматической форсункой при избыточном давлении 0,4 кг/см в реактор, наполненный жидким азотом (Ткип=-196°С). Замороженный раствор, в виде микрогранул, переносят в поддон из нержавеющей стали и подвергают сублимационной сушке при температурах: на конденсаторе -70°С…-75°С; на продукте -196°С…+50°С, и остаточном давлении в камере (6-3)⋅10-2 Торр в течение 24 ч. Выход продукта сублимационной сушки - легкого, пушистого порошка бледно-желтого цвета составил 0,63 г (91,3 мас. %). По данным РФА полученное вещество характеризуется типичной дифрактограммой, представленной на рис. 4 и набором межплоскостных расстояний и их интенсивностями, совпадающих с соответствующими значениями для новой, не известной ранее, кристаллической β-модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона, представленными в табл. 3. По данным термоаналитических исследований полученное вещество характеризуется типичной кривой дифференциальной сканирующей калориметрии, представленной на рис. 6 и совпадающей с соответствующими значениями, в пределах ошибки определения, для новой, не известной ранее, кристаллической β-модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона. Кривая ДСК характеризуется двумя тепловыми эффектами: экзотермическим эффектом при температуре (174,9±0,5)°С и эндотермическим эффектом при температуре (267,7±0,5)°С. По данным ВЭЖХ чистота полученной новой, не известной ранее, кристаллической β-модификации леналидомида составляет 99,42%.
Пример 4. Фармацевтическая композиция.
Для приготовления 10,00 г композиции, включающей в качестве действующего вещества кристаллическую β-модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона и вспомогательные вещества в соотношении (мас. %):
0,38 г порошка новой, не известной ранее, кристаллической β-модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона смешивают в течение 10 минут в керамической ступке с вспомогательными веществами: 7,22 г целлюлозой микрокристаллической, 2,00 г микрокристаллической целлюлозой (по фармакопее США и Европейской фармакопее), 0,30 г кроскармеллозы натрия (по фармакопее США и Европейской фармакопее), 0,10 г магния стеарата (по ТУ 6-09-16-1533-90). Полученную смесь подвергали физико-химическим и биологическим методам анализа. По данным РФА в полученной смеси присутствует вещество, которое характеризуется набором межплоскостных расстояний и их интенсивностями, совпадающих с соответствующими значениями для новой, не известной ранее, кристаллической β-модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона, представленными в табл. 3.
Аналогичным способом и идентичным по составу была приготовлена композиция на основе известной кристаллической модификации леналидомида (Форма «А»), которую использовали в качестве исходного вещества. По данным РФА в полученной смеси присутствует вещество, которое характеризуется набором межплоскостных расстояний и их интенсивностями, совпадающих с соответствующими значениями для известной кристаллической модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона (Форма «А»), представленными в табл. 2.
Биологические эксперименты проводили на кроликах-самцах массой 2,0-2,5 кг. Для получения надежных результатов в параллельных сериях опытов использовали не менее 5ти кроликов. Определение времени появления леналидомид в крови проводили методом in vivo при пероральном введении композиции с последующим забором плазмы из ушной раковины. Во всех случаях количество вводимого в животное действующего вещества составляло 100,00 мг смеси (3,75 мг леналидомида). Оказалось, что для композиции, содержащей новую, не известную ранее, кристаллическую β-модификацию 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона в крови кроликов равно 16±3 мин, а для известной композиции, содержащей в качестве действующего вещества известную кристаллическую модификацию леналидомида (Форма «А») - 25±3 мин.
Таким образом, нами обнаружена новая, не известная ранее, кристаллическая β-модификация 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона, предложены способ ее получения и применение ее для приготовления фармацевтической композиции в качестве представителя нового класса иммуномодуляторов, обладающего как иммуномодулирующими, так и антиангиогенными свойствами для лечения множественной миеломы.
Полученная новая, не известная ранее, кристаллическая β-модификация 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона характеризуется, отличным от известных кристаллических модификаций леналидомида, набором межплоскостных расстояний (d,  ) и соответствующих им интенсивностей (Iотн., %): 12,358-8,39%; 11,893-29,79%; 11,551-100,00%; 8,606-8,39%; 7,641-4,62%; 7,024-8,05%; 5,927-8,05%; 5,811-19,86%; 5,262-28,42%; 5,117-9,42%; 4,850-5,99%; 4,595-5,99%; 4,215-10,45%; 4,011-6,68%; 3,948-11,47%; 3,877-51,88%; 3,843-39,73%; 3,698-16,44%; 3,426-6,51%; 3,316-4,97%; 3,201-5,14%; 3,103-4,45%; 3,025-3,42%; 2,989-2,91%; 2,905-9,93%; 2,846-5,99%; 2,826-5,65%; 2,702-10,27%; 2,640-7,88%; 2,555-10,27%; 2,478-7,19%; 2,339-6,51%; 2,647-23,12%; 2,282-11,82%; 2,243-9,93%; 2,168-5,82%; 2,107-9,08%; 2,081-7,36%; 2,066-10,96%; 2,027-9,76%; 1,943-5,65%; 1,912-24,83%; 1,795-4,45%; 1,719-4,62%; 1,694-5,72%; 1,659-7,19%; 1,634-3,94%, и кривой ДСК с двумя тепловыми эффектами: экзотермическим эффектом при температуре (174,9±0,5)°С и эндотермическим эффектом при температуре (267,7±0,5)°С.
) и соответствующих им интенсивностей (Iотн., %): 12,358-8,39%; 11,893-29,79%; 11,551-100,00%; 8,606-8,39%; 7,641-4,62%; 7,024-8,05%; 5,927-8,05%; 5,811-19,86%; 5,262-28,42%; 5,117-9,42%; 4,850-5,99%; 4,595-5,99%; 4,215-10,45%; 4,011-6,68%; 3,948-11,47%; 3,877-51,88%; 3,843-39,73%; 3,698-16,44%; 3,426-6,51%; 3,316-4,97%; 3,201-5,14%; 3,103-4,45%; 3,025-3,42%; 2,989-2,91%; 2,905-9,93%; 2,846-5,99%; 2,826-5,65%; 2,702-10,27%; 2,640-7,88%; 2,555-10,27%; 2,478-7,19%; 2,339-6,51%; 2,647-23,12%; 2,282-11,82%; 2,243-9,93%; 2,168-5,82%; 2,107-9,08%; 2,081-7,36%; 2,066-10,96%; 2,027-9,76%; 1,943-5,65%; 1,912-24,83%; 1,795-4,45%; 1,719-4,62%; 1,694-5,72%; 1,659-7,19%; 1,634-3,94%, и кривой ДСК с двумя тепловыми эффектами: экзотермическим эффектом при температуре (174,9±0,5)°С и эндотермическим эффектом при температуре (267,7±0,5)°С.
Кроме того, новая, не известная ранее, кристаллическая β-модификация 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона отличается повышенной биологической активностью в составе фармацевтической композиции по сравнению с действием известной кристаллической модификации леналидомида (Форма «А»), которую использовали в качестве исходного вещества.
Из вышеизложенного можно сделать вывод о том, что заявляемая новая, не известная ранее, кристаллическая β-модификация 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона, способ ее получения и применение ее для приготовления фармацевтической композиции в качестве представителя нового класса иммуномодуляторов, обладающего как иммуномодулирующими, так и антиангиогенными свойствами для лечения множественной миеломы являются новыми и удовлетворяют критериям «изобретательский уровень» и «промышленная применимость».


Изобретение касается новой кристаллической модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона (леналидомид - международное непатентованное название), названной β-модификацией, характеризующейся следующим набором межплоскостных расстояний (d, Å) и соответствующих им интенсивностей (Iотн., %): 12,358 - 8,39%; 11,893 - 29,79%; 11,551 - 100,00%; 8,606 - 8,39%; 7,641 - 4,62%; 7,024 - 8,05%; 5,927 - 8,05%; 5,811 - 19,86%; 5,262 - 28,42%; 5,117 - 9,42%; 4,850 - 5,99%; 4,595 - 5,99%; 4,215 - 10,45%; 4,011 - 6,68%; 3,948 - 11,47%; 3,877 - 51,88%; 3,843 - 39,73%; 3,698 - 16,44%; 3,426 - 6,51%; 3,316 - 4,97%; 3,201 - 5,14%; 3,103 - 4,45%; 3,025 - 3,42%; 2,989 - 2,91%; 2,905 - 9,93%; 2,846 - 5,99%; 2,826 - 5,65%; 2,702 - 10,27%; 2,640 - 7,88%; 2,555 - 10,27%; 2,478 - 7,19%; 2,339 - 6,51%; 2,647 - 23,12%; 2,282 - 11,82%; 2,243 - 9,93%; 2,168 - 5,82%; 2,107 - 9,08%; 2,081 - 7,36%; 2,066 - 10,96%; 2,027 - 9,76%; 1,943 - 5,65%; 1,912 - 24,83%; 1,795 - 4,45%; 1,719 - 4,62%; 1,694 - 5,72%; 1,659 - 7,19%; 1,634 - 3,94% и кривой ДСК с двумя тепловыми эффектами: экзотермическим эффектом при температуре (174,9±0,5)°C и эндотермическим эффектом при температуре (267,7±0,5)°C. А также способа ее получения и применения в фармацевтической промышленности и медицине в качестве представителя нового класса иммуномодуляторов, обладающего как иммуномодулирующими, так и антиангиогенными свойствами для лечения множественной миеломы. 3 н. и 1 з.п. ф-лы, 4 табл., 6 ил., 4 пр.
1. Кристаллическая β-модификация 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона, характеризующаяся следующим набором межплоскостных расстояний (d, Å) и соответствующих им интенсивностей (Iотн., %): 12,358 - 8,39%; 11,893 - 29,79%; 11,551 - 100,00%; 8,606 - 8,39%; 7,641 - 4,62%; 7,024 - 8,05%; 5,927 - 8,05%; 5,811 - 19,86%; 5,262 - 28,42%; 5,117 - 9,42%; 4,850 - 5,99%; 4,595 - 5,99%; 4,215 - 10,45%; 4,011 - 6,68%; 3,948 - 11,47%; 3,877 - 51,88%; 3,843 - 39,73%; 3,698 - 16,44%; 3,426 - 6,51%; 3,316 - 4,97%; 3,201 - 5,14%; 3,103 - 4,45%; 3,025 - 3,42%; 2,989 - 2,91%; 2,905 - 9,93%; 2,846 - 5,99%; 2,826 - 5,65%; 2,702 - 10,27%; 2,640 - 7,88%; 2,555 - 10,27%; 2,478 - 7,19%; 2,339 - 6,51%; 2,647 - 23,12%; 2,282 - 11,82%; 2,243 - 9,93%; 2,168 - 5,82%; 2,107 - 9,08%; 2,081 - 7,36%; 2,066 - 10,96%; 2,027 - 9,76%; 1,943 - 5,65%; 1,912 - 24,83%; 1,795 - 4,45%; 1,719 - 4,62%; 1,694 - 5,72%; 1,659 - 7,19%; 1,634 - 3,94%, и кривой ДСК с двумя тепловыми эффектами: экзотермическим эффектом при температуре (174,9±0,5)°C и эндотермическим эффектом при температуре (267,7±0,5)°C.
2. Способ получения кристаллической β-модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона по п. 1, характеризующийся тем, что раствор 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона в смешанном водно-органическом растворителе в соотношении 10:1-10:3 при 25-80°C замораживают при скорости охлаждения не ниже 60 град/мин и подвергают сублимационной сушке.
3. Способ по п. 2, характеризующийся тем, что сублимационную сушку замороженного раствора леналидомида проводят при температурах: на конденсаторе (-43…-75)°C; на продукте (-196…+50)°C, и остаточном давлении в камере (9-3)×10-2 Торр в течение 22-26 ч.
4. Применение кристаллической β-модификации 3-(4-амино-1-оксо-1,3-дигидро-2Н-изоиндол-2-ил)-пиперидин-2,6-диона по п. 1 в качестве активного агента, обладающего иммуномодулирующими, антиангиогенными свойствами, для приготовления фармацевтической композиции для лечения множественной миеломы.
| WO 2005023192 A2, 17.03.2005 | |||
| WO 2011033468 A1, 24.03.2011 | |||
| EA 201100750 A1, 30.12.2011. |
Авторы
Даты
2017-04-19—Публикация
2016-04-07—Подача