По настоящей заявке испрашивается приоритет патентной заявки № 61/616039, поданной 27 марта 2012, которая включена в настоящее изобретение с помощью ссылки во всей своей полноте.
УРОВЕНЬ ТЕХНИКИ
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к способам и материалам для доставки офтальмических агентов в глаз субъекта.
ОПИСАНИЕ РОДСТВЕННОГО УРОВНЯ ТЕХНИКИ
Глаукома характеризуется внутриглазным давлением, являющимся результатом, по меньшей мере, частично ослабленного оттока внутриглазной жидкости через трабекулярную сеть. Многие современные терапии для лечения глаукомы включают местное введение лекарственных средств в глаз глазными каплями. Однако местное введение имеет много недостатков, поскольку многие из лекарственных средств плохо проникают через роговую оболочку глаза и/или могут также иметь нежелательные побочные эффекты, такие как наружное раздражение и покраснение. Более того, имеется несколько задокументированных исследований, которые показывают, что пациенты испытывают большие трудности с введением местных лекарственных средств (например, глазных капель) и, следовательно, пациенты плохо соблюдают режим и указания врача при применении местных лекарственных средств для лечения глаукомы.
Имеются данные, свидетельствующие, что и пациенты и медицинские работники предпочтут традиционному местному введению глазную инъекцию, которую будут вводить 3-4 раза в год.
СУЩНОСТЬ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
Настоящее изобретение указывает на неудовлетворенную потребность в лечении офтальмическими агентами, обеспечивая устройство для доставки офтальмических лекарственных средств для прямого введения офтальмических агентов в глаз субъекта.
Один аспект настоящего изобретения относится к эластомерному материалу для перекрывания венозного потока крови в эписклеральной вене глаза субъекта, включающему, состоящему из или состоящему по существу из:
(a) центрального отверстия с внутренним диаметром в нем; и
(b) наружным диаметром 1 мм,
при этом, когда эластомерный материал помещают на глаз, часть внутреннего диаметра растягивается для установки по экватору глаза, причем после сжатия поток венозной крови в эписклеральной вене глаза перекрывается.
В одном варианте осуществления эластомерный материал имеет форму, выбранную из круглой, овальной, эллиптической, прямоугольной и квадратной формы.
В другом варианте осуществления эластомерный материал имеет наружный диаметр от приблизительно 2 мм до приблизительно 40 мм.
В других вариантах осуществления внутренний диаметр эластичного материала составляет от приблизительно 2 мм до приблизительно 20 мм.
В другом варианте осуществления эластомерный материал включает силастиковый материал.
Другой аспект настоящего изобретения относится к способу увеличения оттока внутриглазной жидкости в глазу субъекта, страдающего от глаукомы, включающему, состоящему из или состоящему по существу из:
(a) помещение эластомерного материала по настоящему изобретению по экватору глаза, посредством этого перекрывая поток венозной крови в эписклеральной вене;
(b) введение через эписклеральную вену терапевтически эффективного количества офтальмического агента; и
(c) удаление эластомерного материала с глаза.
В другом аспекте настоящее изобретение относится к способу доставки офтальмического агента в систему водного оттока, включающему, состоящему из или состоящему по существу из:
(a) помещение эластомерного материала по настоящему изобретению по экватору глаза, посредством этого перекрывая поток венозной крови в эписклеральной вене;
(b) введение через эписклеральную вену терапевтически эффективного количества офтальмического агента; и
(c) удаление эластомерного материала с глаза.
Другой аспект настоящего изобретения относится к способу доставки офтальмического агента в переднюю камеру глаза, включающему, состоящему из или состоящему по существу из:
(a) помещение эластомерного материала по настоящему изобретению по экватору глаза, посредством этого перекрывая поток венозной крови в эписклеральной вене;
(b) введение через эписклеральную вену терапевтически эффективного количества офтальмического агента; и
(c) удаление эластомерного материала с глаза.
Другой аспект настоящего изобретения относится к способу вызывания состояния, подобного глаукоме, у субъекта, включающему, состоящему из или состоящему по существу из:
(a) помещение эластомерного материала по настоящему изобретению по экватору глаза, посредством этого перекрывая поток венозной крови в эписклеральной вене;
(b) введение через эписклеральную вену эффективного количества офтальмического агента и вязкоэластичного агента;
(c) удаление эластомерного материала с глаза.
В одном варианте осуществления офтальмический агент включает агенты, усиливающие отток внутриглазной жидкости, стероиды, агонисты альфа-рецепторов, антагонисты бета-рецепторов, ингибиторы карбоангидразы, адренергические агенты, физиологически активные пептиды и/или белки, противоопухолевые агенты, антибиотики, анальгетики, противовоспалительные агенты, миорелаксанты, противоэпилептические агенты, противоязвенные агенты, противоаллергические средства, кардиотонические агенты, антиаритмические агенты, сосудорасширяющие средства, гипотензивные средства, противодиабетические средства, антигиперлипидемические средства, антикоагулянты, гемолитические средства, противотуберкулезные средства, гормоны, антагонисты наркотические анальгетики, остеокластические супрессивные средства, остеогенные стимуляторы, супрессоры ангиогенеза, антибактериальные средства, нестероидные противовоспалительные препараты (НПВП), глюкокортикоиды или другие противовоспалительные кортикостероиды, алкалоидные анальгетики, такие как опиоидные анальгетики, противовирусные средства, такие как нуклеозидные противовирусные средства или ненуклеозидные противовирусные средства, агенты против доброкачественной гипертрофии предстательной железы (ДГПЖ), противогрибковые соединения, антипролиферативные соединения, соединения против глаукомы, иммуномодулирующие соединения, агенты, препятствующие клеточному транспорту/подвижности, цитокиновые пегилированные агенты, альфа-блокаторы, антиандрогены, антихолинергические агенты, пуринергические агенты, дофаминергические агенты, местные анестетики, ваниллоиды, ингибиторы оксида азота (I), антиапоптотические агенты, ингибиторы активации макрофагов, антиметаболиты, нейропротекторы, блокаторы кальциевых каналов, антагонисты гамма-аминомасляной кислоты (ГАМК), альфа агонисты, антипсихотические агенты, ингибиторы тирозинкиназы, нуклеозидные соединения и нуклеотидные соединения и их аналоги, производные, фармацевтически приемлемые соли, сложные эфиры, пролекарства, комбинированные лекарственные средства, и их защищенные формы, и их комбинации.
В определенных вариантах осуществления агенты, усиливающие отток внутриглазной жидкости, включают этакриновую кислоту или любые ее аналоги или производные.
В других вариантах осуществления офтальмический агент вводят с вязкоэластичным агентом. В определенных вариантах осуществления вязкоэластичный агент выбран из группы, состоящей из Healon® (Abbott Laboratories Inc., Abbott Park, Illinois, USA), Healon®OVD, Healon5®OVD, HealonGV®, ProVisc® (Alcon Laboratories, Inc., Fort Worth, Texas, USA) и их комбинаций. В других вариантах осуществления отношение офтальмического агента к вязкоэластичному агенту составляет 3:1.
Другой аспект относится ко всему, что описано и проиллюстрировано в настоящем изобретении.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Приведенные выше аспекты и другие признаки настоящего изобретения объясняют в следующем описании, взятом вместе с сопровождающими его чертежами, в которых:
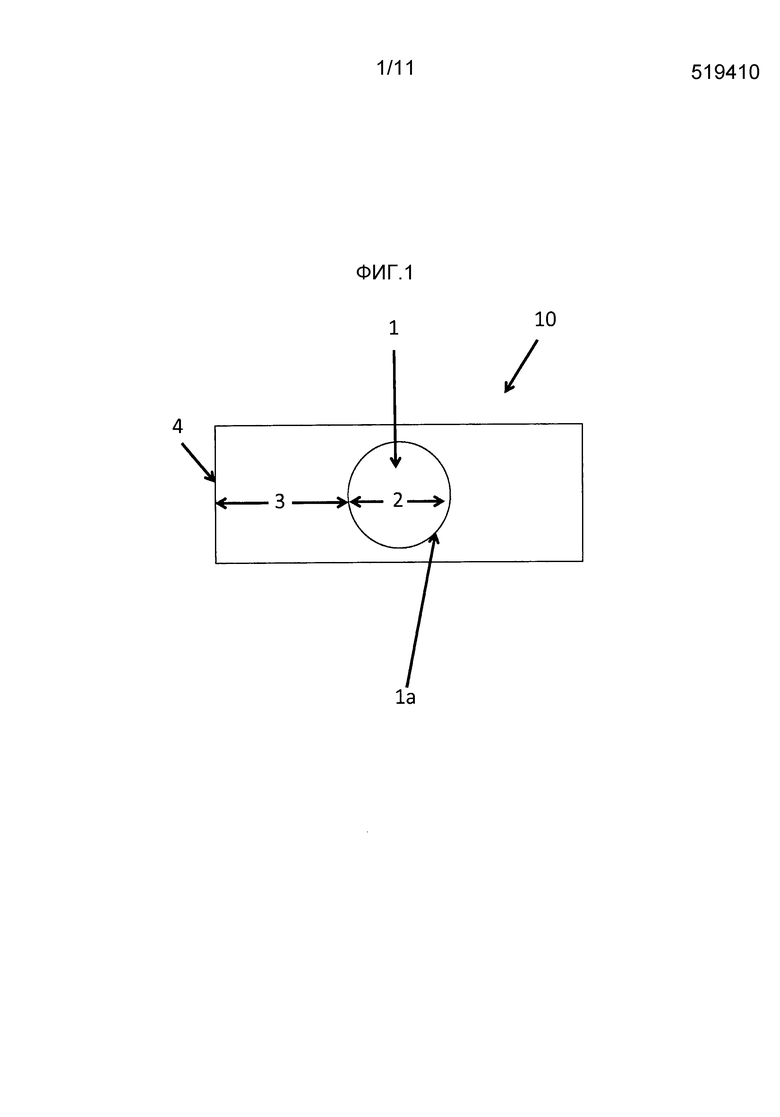
Фиг. 1 представляет собой вид сверху и сечение одного варианта осуществления эластомерного материала настоящего изобретения.
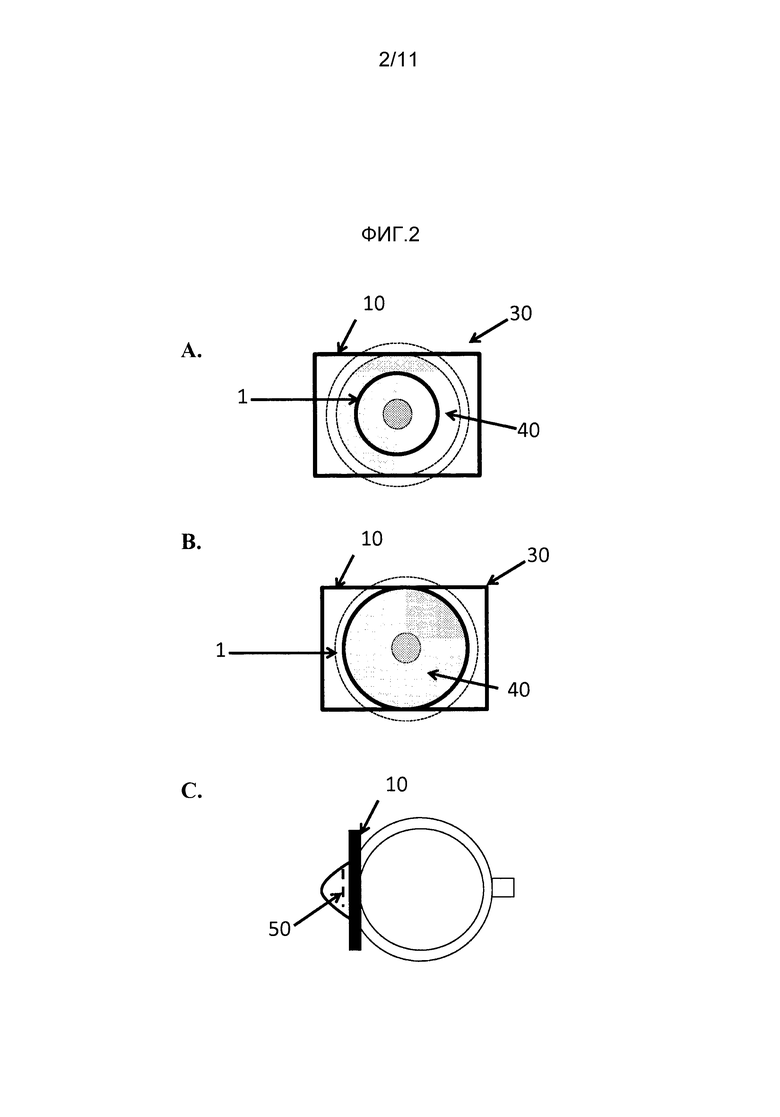
Фиг. 2a показывает первичное размещение эластомерного материала на глазе согласно одному варианту осуществления настоящего изобретения. Фиг. 2b показывает растяжение эластомерного материала на глазе согласно одному варианту осуществления настоящего изобретения. Фиг. 2c представляет собой вид сбоку, показывающий эластомерный материал в нанесенном на глаз субъекта состоянии согласно одному варианту осуществления настоящего изобретения.
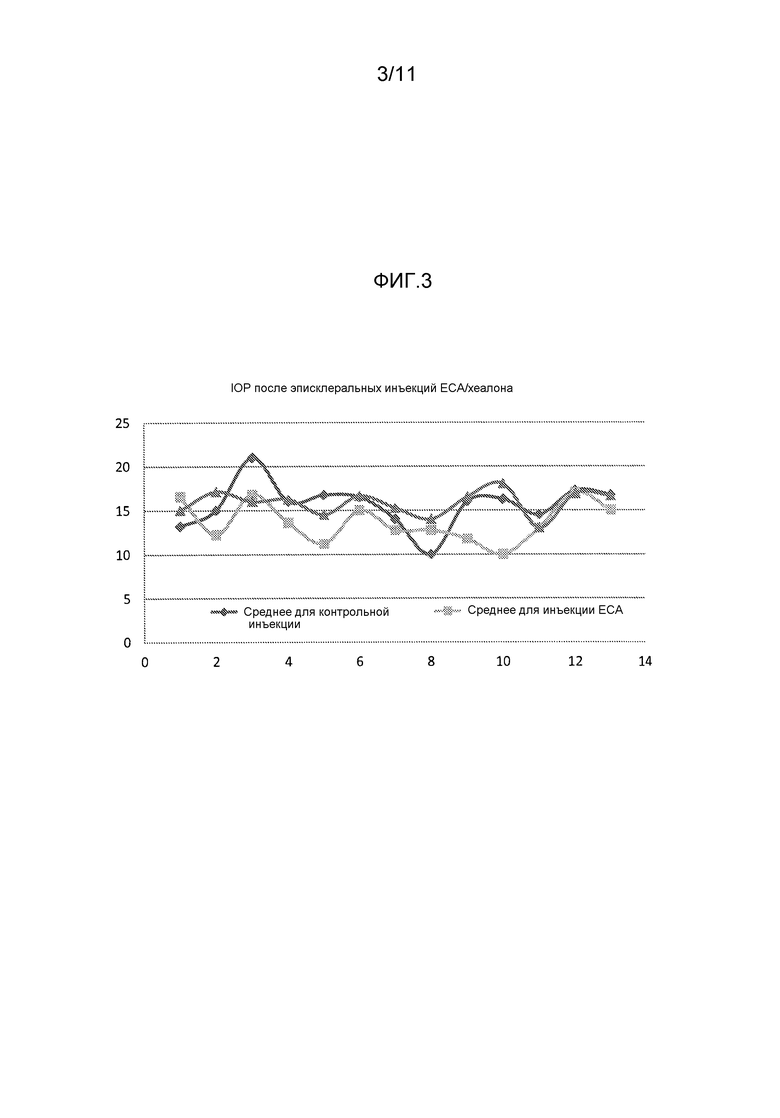
Фиг. 3 представляет собой график и соответствующие данные, показывающие эффекты EGA инъекции в эписклеральную вену, применяя вариант осуществления настоящего изобретения.
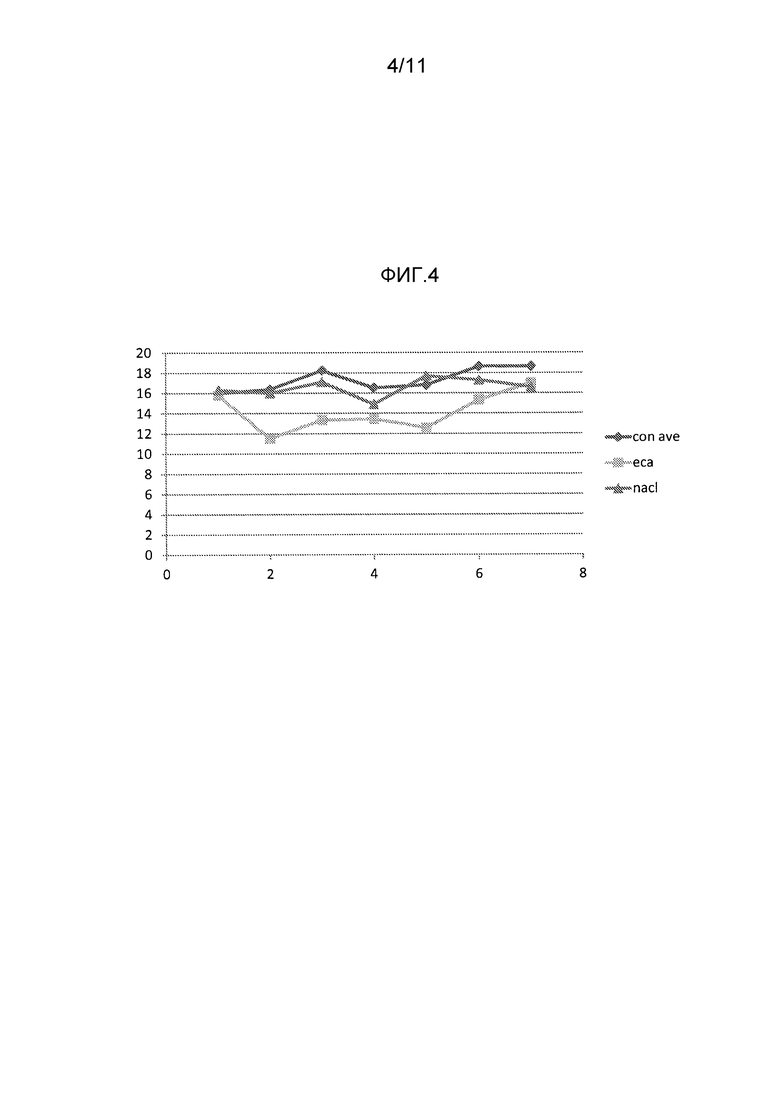
Фиг. 4 представляет собой график и соответствующие данные, показывающие эффекты EGA инъекции в эписклеральную вену, применяя вариант осуществления настоящего изобретения.
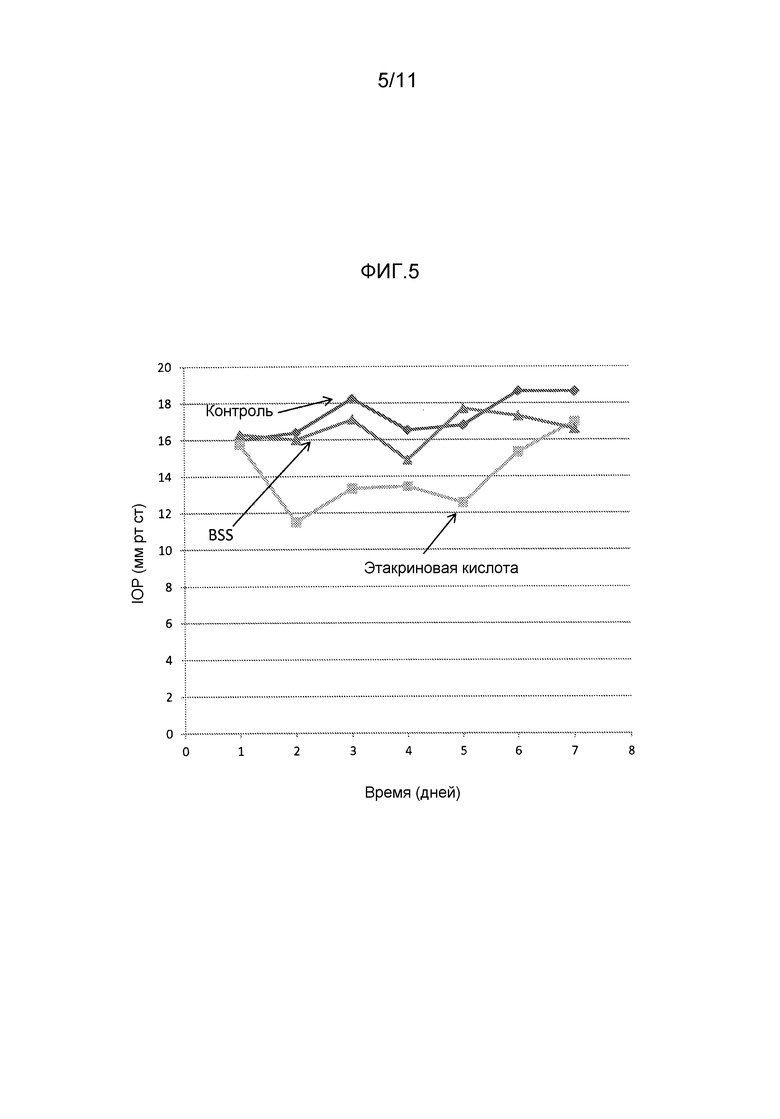
Фиг. 5 представляет собой график, показывающий, что добавление этакриновой кислоты снижает внутриглазное давление (IOP) больше, чем контроль.
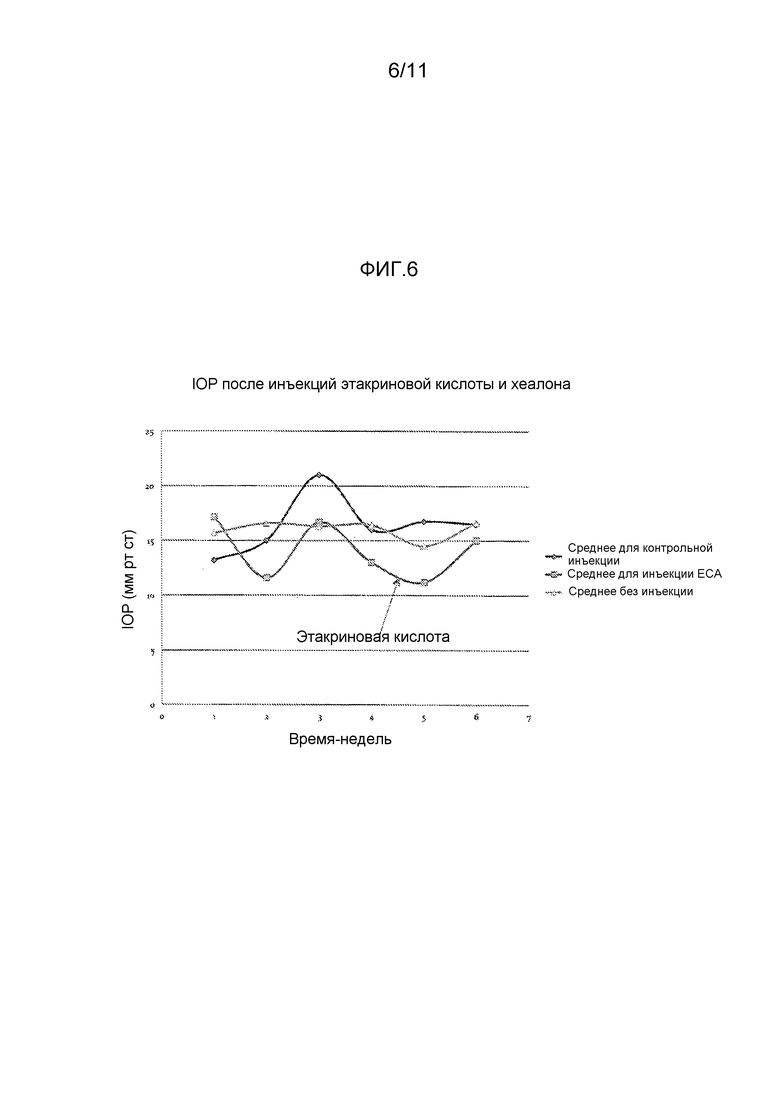
Фиг. 6 представляет собой график, показывающий, что мыши, которым вводили смесь ECA+хеалон, имели меньшие средние значения IOP, чем мыши, которым вводили BSS (контроль [con]) или которым ничего не вводили.
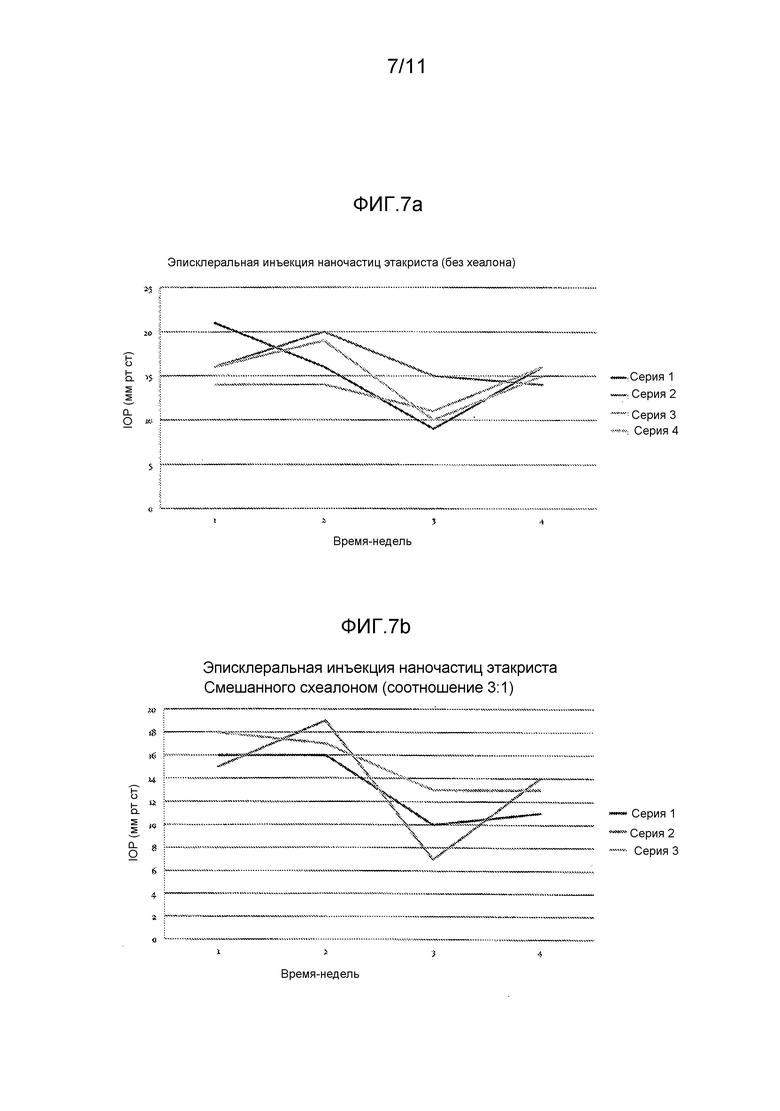
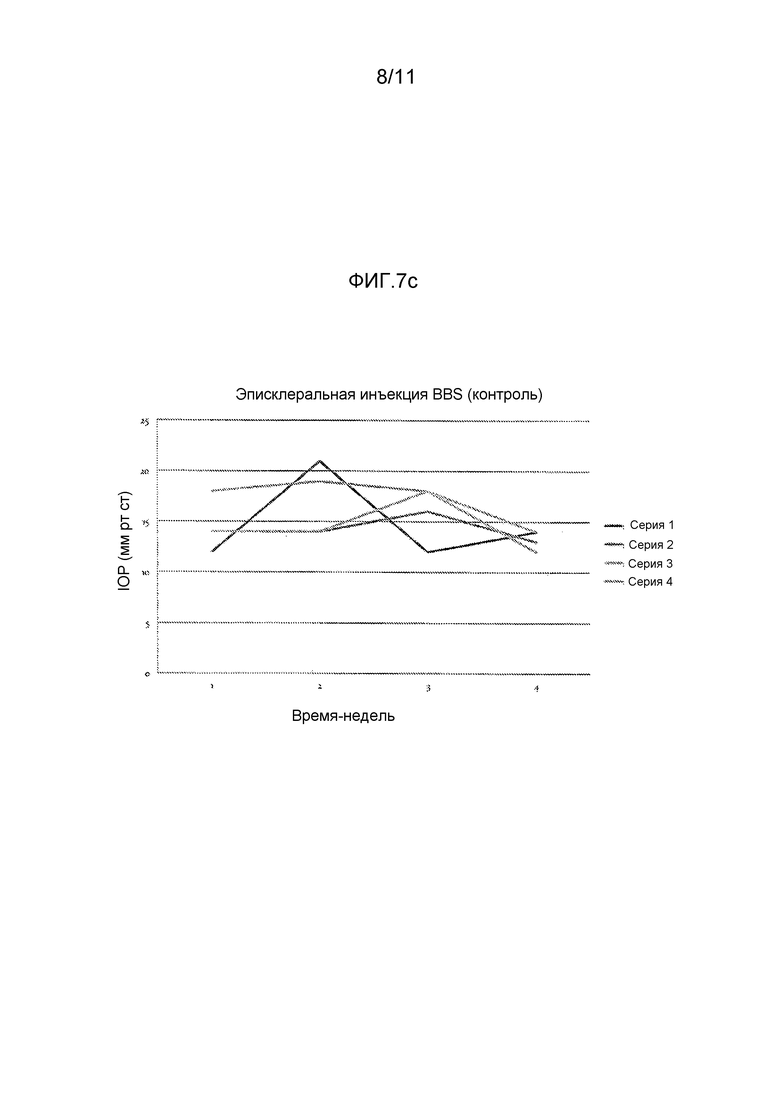
Фиг. 7 представляет собой графики, показывающие данные IOP для мышей после эписклеральной инъекции наночастиц этакриста. (a) эписклеральная инъекция мышам наночастиц этакриста (без хеалона); (b) наночастиц этакриста + хеалон (соотношение 3:1) и (c) BSS (контроль).
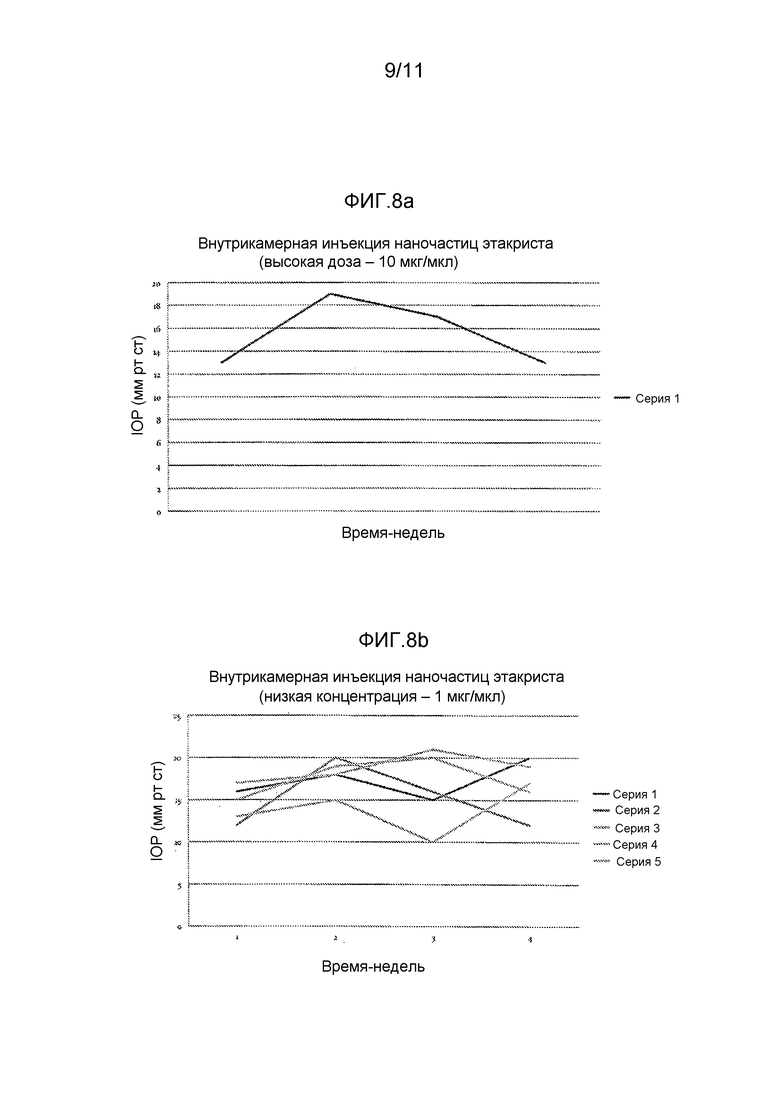
Фиг. 8 представляет собой графики, показывающие данные IOP для мышей, после внутрикамерной инъекции наночастиц этакриста, содержащих (a) большую концентрацию наночастиц (10 мкг/мкл) или (b) низкую концентрацию наночастиц (1 нг/мкл).
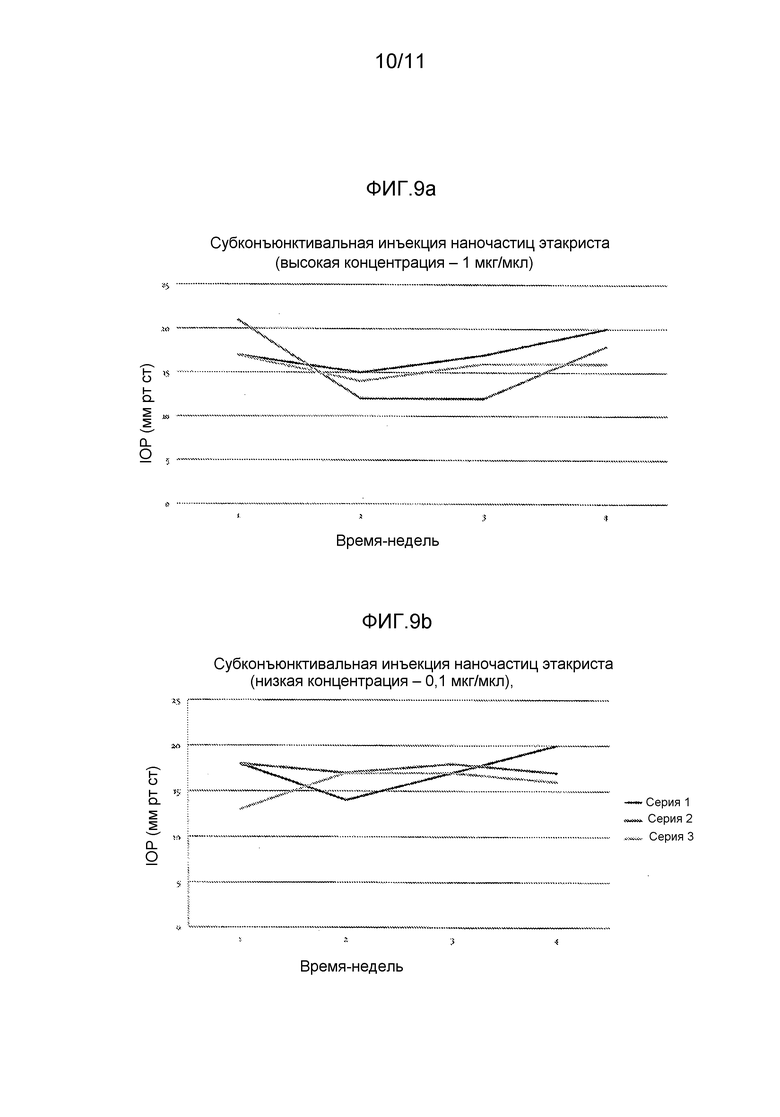
Фиг. 9 представляет собой графики, показывающие данные IOP у мышей после субконъюнктивальной инъекции наночастиц этакриста, содержащих (a) большую концентрацию (1 мкг/мкл) или (b) низкую концентрацию (0,1 мкг/мкл) наночастиц.
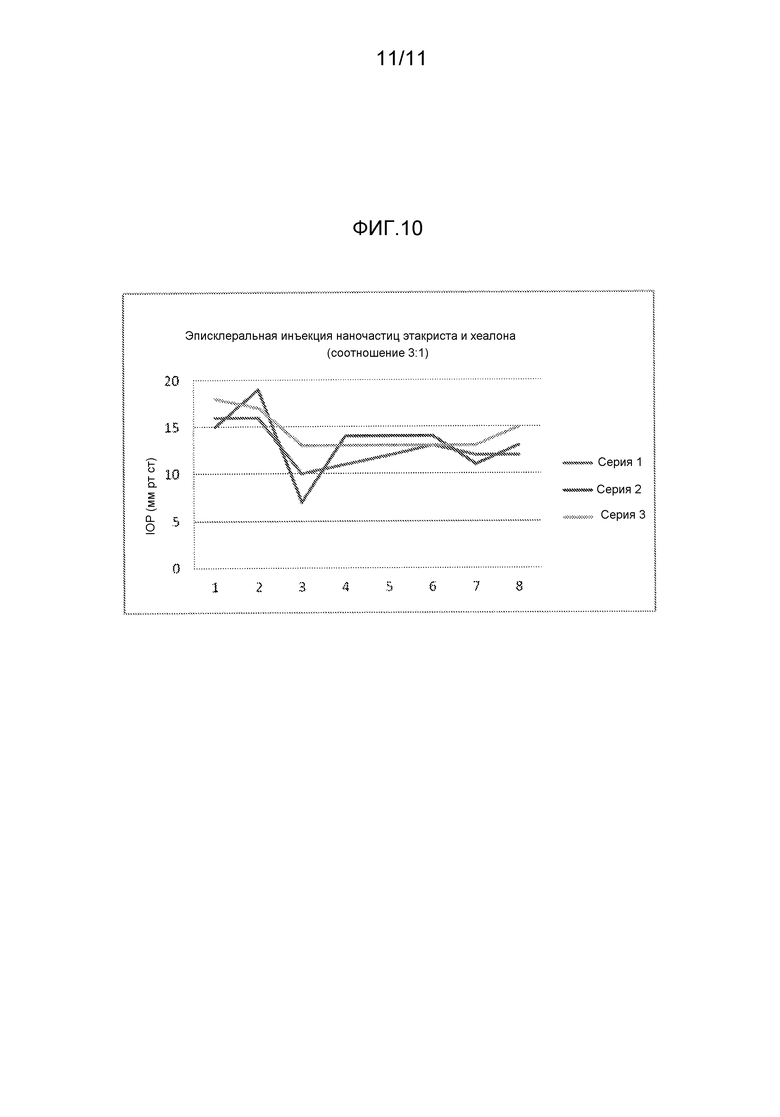
Фиг. 10 представляет собой график, показывающий эффект инъекции в эписклеральную вену наночастиц этакриста, смешанного с хеалоном в соотношении 3:1, на мышей.
ПОДРОБНОЕ ОПИСАНИЕ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
С целью поспособствовать пониманию принципов настоящего изобретения, ссылки будут делать на предпочтительные варианты осуществления, и специальный язык будут применять для их описания. Тем не менее, ясно, что не предполагается ограничение посредством этого объема настоящего изобретения, причем такие изменения и дополнительные модификации настоящего изобретения, как показанные в настоящем изобретении, предполагаются как обычно встречающиеся специалисту в данной области техники, к которому относится настоящее изобретение.
ОПРЕДЕЛЕНИЯ
Если не определено иначе, все технические термины, применяемые в настоящем изобретении, имеют значения, обычно известные специалисту в данной области техники, к которому относится настоящее изобретение. Определенные термины обсуждают в настоящем изобретении, давая дополнительное указание практикующему специалисту по описанию устройств, способов и подобных вариантов осуществления настоящего изобретения, и как осуществить и применять их. Ясно, что об одной вещи можно сказать более чем одним способом. Следовательно, альтернативный язык и синонимы можно применять для любого одного или более из терминов, обсуждаемых в настоящем изобретении. Не имеет значения, пояснен или обсуждается ли в настоящем изобретении термин или нет. Обеспечивают некоторые синонимы или взаимозаменяемые способы, материалы и подобные. Перечисление одного или нескольких синонимов или эквивалентов не исключает применения других синонимов или эквивалентов, если это не обозначено четко.
Артикли "a" и "an" применяют в настоящем изобретении для ссылки на один или более чем один (т.е. по меньшей мере один) из грамматических объектов артикля. В качестве примера, "элемент" обозначает по меньшей мере один элемент и может включать более одного элемента.
Как применяют в настоящем изобретении, предполагается, что термин "пациент" или "субъект" включает человека и животных, отличных от человека. Примеры субъектов, являющихся людьми, включают пациентов, являющихся людьми, имеющих глазное заболевание, например, глаукому. Термин "животные, отличные от человека" включает всех позвоночных, например, немлекопитающих (таких как птицы, амфибии, рептилии) и млекопитающих, таких как приматы, отличные от человека, домашние и/или сельскохозяйственные животные (такие как овцы, собаки, кошки, коровы, свиньи и т.д.) и грызуны (такие как мыши, крысы, хомяки, морские свинки и т.д.).
Как применяют в настоящем изобретении, термин "терапевтически эффективное" или "эффективное количество" относится к дозе соединения (например, офтальмического агента, агента, улучшающего отток внутриглазной жидкости, и т.д.), эффективной для вызывания требуемого эффекта. Данный термин, как применяют в настоящем изобретении, может также относиться к количеству, эффективному для вызывания требуемого in vivo эффекта у животного, млекопитающего или человека, такого как снижение внутриглазного давления, ослабление воспаления и подобных. Активное соединение может быть эффективным при широком диапазоне доз, и его обычно вводят в фармацевтически эффективном количестве. Однако ясно, что реально вводимое количество соединения будет обычно определять лечащий врач, согласно соответствующим обстоятельствам, включая заболевание, которое лечат, выбранный путь введения, реально вводимое соединение, возраст, вес и реакцию отдельного пациента, тяжесть симптомов у пациента, и подобные.
Термин "введение", как применяют в настоящем изобретении, относится к обеспечению, контакту и/или доставке соединения, такого как офтальмический агент или агент, улучшающий отток внутриглазной жидкости, и подобных, любым подходящим путем, получая требуемый эффект. Данные соединения можно вводить субъекту множеством способов, включая, но не ограничиваясь, пероральный, сублингвальный, парентеральный (например, внутривенную, подкожную, внутрикожную, внутримышечную, внутрисуставную, внутриартериальную, внутрисиновиальную, интрастернальную, интратекальную, внутриочаговую или внутричерепную инъекцию), трансдермальный, местный, буккальный, ректальный, вагинальный, назальный, офтальмологический, путем ингаляции и имплантаты. В некоторых вариантах осуществления, соединения вводят парентерально. В определенных вариантах осуществления, соединения вводят внутривенно.
"Фармацевтически приемлемый" обозначает одобренный или заслуживающий одобрения регулирующим органом федерального правительства или правительства государства или перечисленный в фармакопее США или других общепризнанных фармакопеях для применения на животных и более конкретно на людях. Он может представлять собой материал, который не является биологически или иначе нежелательным, т.е., материал можно вводить индивиду без вызывания любых нежелательных биологических эффектов или без взаимодействия пагубным способом с любым из компонентов композиции, в которой он содержится.
Термин "фармацевтически приемлемая соль" соединения обозначает соль, которая является фармацевтически приемлемой и которая обладает требуемой фармакологической активностью исходного соединения. Данные соли включают, например, соли присоединения кислоты и соли присоединения основания.
Термин "агонист" относится к соединению, которое можно смешивать с рецептором, обеспечивая или увеличивая молекулярную и клеточную активность. Агонист может представлять собой лиганд, который непосредственно связывается с рецептором. Альтернативно, агонист можно смешивать с рецептором опосредованно, например, (a) образуя комплекс с другой молекулой или белком, которые непосредственно связываются с рецептором, или (b) иначе получая в результате модификацию другого соединения, так чтобы соединение непосредственно связывалось с рецептором.
Термин "антагонист" относится к соединению, которое можно смешивать с рецептором, снижая или ингибируя молекулярную и клеточную активность. Антагонист может представлять собой лиганд, который непосредственно связывается с рецептором. Альтернативно, антагонист можно смешивать с рецептором опосредованно, например, (a) образуя комплекс с другой молекулой или белком, которые непосредственно связываются с рецептором, или (b) иначе получая в результате модификацию другого соединения так, чтобы другое соединение непосредственно связывалось с рецептором.
Как применяют в настоящем изобретении, термины, включая, но не ограничиваясь, "пептид" или "белок" или любой другой термин, применяемый для ссылки на цепь или цепи двух или более аминокислот. Термин дополнительно включает пептиды, которые подверглись посттрансляционным модификациям, например, гликозилированию, ацетилированию, фосфорилированию, амидированию, дериватизации известными защитными/блокирующими группами, протеолитическому расщеплению или модификации не встречающимися в природе аминокислотами.
Настоящее изобретение объясняется далее со ссылкой на предпочтительные варианты осуществления.
Эластомерный материал настоящего изобретения обеспечивают для удерживания потока венозной крови в эписклеральной вене глаза субъекта, и он в основном характеризуется тем, что он имеет центральное отверстие с внутренним диаметром в нем, наружным диаметром по меньшей мере 1 мм, где когда эластомерный материал помещают на глаз, часть внутреннего диаметра растягивается для установки по экватору глаза, при этом после сжатия поток венозной крови в эписклеральной вене глаза перекрывается.
Форма и размер эластомерного материала
Фиг. 1 представляет собой вид сверху и разрез одного варианта осуществления эластомерного материала настоящего изобретения. Эластомерный материал настоящего изобретения, показанный как 10 на фигуре, содержит, состоит из или состоит по существу из листа эластомерного материала, который имеет центральное отверстие 1 с внутренним диаметром 2 и наружным диаметром 3.
Плоская форма (т.е., контур наружной окружности эластомерного материала) материала, в частности, не ограничена и может включать многие различные формы, включая, но не ограничиваясь, круглую, овальную, эллиптическую, прямоугольную, квадратную и подобные. В определенных вариантах осуществления форма материала является квадратной. В других вариантах осуществления форма является по существу круглой. Как применяют в настоящем изобретении, термин "по существу круглая" не ограничивается истинной окружностью, но включает эллипс и вытянутый эллипс. В определенных вариантах осуществления, форма материала представляет собой истинную окружность.
Размер эластомерного материала настоящего изобретения также конкретно не ограничен при условии, что его можно помещать на глаз, и лицо, осуществляющее уход, может легко манипулировать с ним (т.е., легко помещать на глаз, растягивать и т.д.). В определенных вариантах осуществления, материал имеет форму, в общем показанную на фигуре I. В данных вариантах осуществления наружный диаметр 3 составляет от приблизительно 1 мм до приблизительно 20 мм, 2 мм до приблизительно 20 мм, 3 мм до приблизительно 20 мм, 4 мм до приблизительно 20 мм, 5 мм до приблизительно 20 мм, 6 мм до приблизительно 20 мм, 7 мм до приблизительно 20 мм, 8 мм до приблизительно 20 мм, 9 мм до приблизительно 20 мм, 10 мм до приблизительно 20 мм, 11 мм до приблизительно 20 мм, 12 мм до приблизительно 20 мм, 13 мм до приблизительно 20 мм, 14 мм до приблизительно 20 мм, 15 мм до приблизительно 20 мм, 16 мм до приблизительно 20 мм, 17 мм до приблизительно 20 мм, 18 мм до приблизительно 20 мм, 19 мм до приблизительно 20 мм, приблизительно 1 мм до приблизительно 30 мм, 1 мм до приблизительно 40 мм, 5 мм до приблизительно 30 мм, 5 мм до приблизительно 40 мм, 8 мм до приблизительно 30 мм, 8 мм до приблизительно 40 мм, 10 мм до приблизительно 30 мм, 10 мм до приблизительно 40 мм, 15 мм до приблизительно 30 мм, 15 мм до приблизительно 40 мм, 20 мм до приблизительно 30 мм, 20 мм до приблизительно 40 мм, 22 мм до приблизительно 30 мм, 22 мм до приблизительно 40 мм, 25 мм до приблизительно 30 мм, 25 мм до приблизительно 40 мм, 30 мм до приблизительно 40 мм, и 35 мм до приблизительно 40 мм, для облегчения лицу, осуществляющему уход, удерживания материал для того, чтобы растянуть центральное отверстие 1. В других вариантах осуществления внутренний диаметр 2 имеет достаточный размер, чтобы при растягивании он был способен устанавливаться по экватору глаза, и при возвращении в его релаксированное состояние, сжиматься так, чтобы перекрывать поток венозной крови в эписклеральной вене. В некоторых вариантах осуществления внутренний диаметр 2 составляет от приблизительно 1 мм до приблизительно 10 мм, 2 мм до приблизительно 10 мм, 3 мм до приблизительно 10 мм, 4 мм до приблизительно 10 мм, 5 мм до приблизительно 10 мм, 6 мм до приблизительно 10 мм, 7 мм до приблизительно 10 мм, 8 мм до приблизительно 10 мм, 9 мм до приблизительно 10 мм, 1 мм до приблизительно 20 мм, 2 мм до приблизительно 20 мм, 3 мм до приблизительно 20 мм, 4 мм до приблизительно 20 мм, 5 мм до приблизительно 20 мм, 6 мм до приблизительно 20 мм, 7 мм до приблизительно 20 мм, 8 мм до приблизительно 20 мм, 9 мм до приблизительно 20 мм, 10 мм до приблизительно 20 мм, 11 мм до приблизительно 20 мм, 12 мм до приблизительно 20 мм, 13 мм до приблизительно 20 мм, 14 мм до приблизительно 20 мм, 15 мм до приблизительно 20 мм, 16 мм до приблизительно 20 мм, 17 мм до приблизительно 20 мм, 18 мм до приблизительно 20 мм, 19 мм до приблизительно 20 мм.
В настоящем изобретении часть внутренней грани 1a относится к части эластичного материала, которая проходит вдоль внутренней окружности центрального отверстия. Часть внутренней грани 1a имеет толщину обычно не более чем приблизительно 0,3 мм. В определенных вариантах осуществления часть внутренней грани имеет толщину в диапазоне 0,05-0,3 мм, 0,1-0,3 мм или 0,13-0,23 мм. Аналогично, устанавливают, чтобы часть внешней грани 4 была не более чем приблизительно 0,3 мм. В некоторых вариантах осуществления часть внешней грани 4 находится в диапазоне 0,05-0,3 мм, 0,15-0,3 мм и 0,17-0,3 мм. И часть внутренней грани и часть внешней грани можно получать так, чтобы они имели по существу однородную толщину. В некоторых вариантах осуществления часть внутренней грани можно получать так, чтобы она имела уменьшающуюся толщину от внутренней грани к части внешней грани так, чтобы часть внутренней грани была толще, чем часть внешней грани. Толщина части наружного диаметра 3a обычно устанавливают такой, чтоб она была не более чем приблизительно 0,4 мм. В определенных вариантах осуществления часть наружного диаметра 3a имеет толщину в диапазоне приблизительно 0,08-0,4 мм, 0,2-0,4 мм и 0,33-0,38 мм. В некоторых вариантах осуществления часть наружного диаметра имеет толщину, большую чем 0,03 мм или большую чем и максимальная толщина части внешней грани и части внутренней грани.
СОСТАВ ЭЛАСТИЧНОГО МАТЕРИАЛА
Эластичный материал настоящего изобретения включает эластичноподобный материал, который обеспечивает растяжение центрального отверстия на приблизительно 1%-0%, 5%-40% и 10%-40%, где эластичноподобный материал имеет склонность возвращать свою первоначальную форму. На практике и как показано на фигуре 2a, материал 10 помещают на глаз 30 так, чтобы центральное отверстие располагалось над экватором 40 глаза. Затем, материал 20 растягивают так, чтобы центральное отверстие 1 было большим, чем экватор глаза (фиг. 2b). Затем, материал 20 релаксирует, где в своем релаксированном состоянии, центральное отверстие сжимается по экватору 40 глаза так, что ток венозной крови в эписклеральной вене 50 перекрывается (фиг. 2c). Данное пережатие вызывает то, что вена начинает надуваться, обеспечивая легкий доступ и визуализацию эписклеральной вены лицу, осуществляющему уход. Подходящие эластичноподобные материалы представляют собой материалы, которые являются предпочтительно биологически инертными и могут включать, но не ограничиваются, эластомерные (эластичный полимер) материалы, такие как полиуретан, полиэтилен, силоксановые эластики (например, Silastic™ силоксановые материалы), термопластичный эластомер, такой как стиролэтилен/бутиленстирол (SEBS), стиролэтилен/пропиленстирол (SEPS) этиленпропиленовый сополимер/полипропилен (EPDM-PP), полиэфирные блочные амиды (PEBAX), полиуретановые или впоследствии вулканизуемый эластомеры, такие как силиконовый каучук, латекс, полибутадиен, фторированный эластомер, полихлоропрен, полиизопрена, материалы и подобные. В определенных вариантах осуществления эластомерный материал включает Silastic™ силикон.
СПОСОБЫ ПРИМЕНЕНИЯ
Эластомерный материал, описанный в настоящем изобретении, обеспечивает доставку через глаз офтальмических агентов в канал Шлемма и отток через трабекулярную сеть глаза субъекта, сильно усиливая эффект данных агентов на глаз. Например, доставка некоторых агентов против глаукомы непосредственно в канал Шлемма и трабекулярную сеть будет обеспечивать замедленный эффект агента, длящийся в течение от нескольких недель до многих месяцев, и может заменять местное введение (например, глазные капли) применяемых в настоящее время лекарственных средств против глаукомы. Способы, описанные в настоящем изобретении, можно применять для получения дэпо лекарственных средств и, что важно, обеспечить легкую доставку данных агентов в медицинском кабинете, при этом их можно осуществлять многократно.
Один аспект настоящего изобретения относится к способу доставки офтальмического агента в систему водного оттока глаза субъекта, включающему помещение эластомерного материала, как описано в настоящем изобретении, по экватору глаза, посредством этого перекрывая поток венозной крови в эписклеральной вене, введение через эписклеральную вену терапевтически эффективного количества офтальмического агента и удаление эластомерного материала с глаза.
Другой аспект настоящего изобретения относится к способу доставки офтальмического агента в переднюю камеру глаза, включающему помещение эластомерного материала, как описано в настоящем изобретении, по экватору глаза, посредством этого перекрывая поток венозной крови в эписклеральной вене, введение через эписклеральную вену терапевтически эффективного количества офтальмического агента так, чтобы офтальмический агент доставлялся в переднюю камеру глаза, и удаление эластомерного материала с глаза.
Еще другой аспект настоящего изобретения относится к способам усиления оттока внутриглазной жидкости в глазу субъекта, страдающего от глаукомы, включающим помещение эластомерного материала, как описано в настоящем изобретении, по экватору глаза, посредством этого перекрывая поток венозной крови в эписклеральной вене, введение через эписклеральную вену терапевтически эффективного количества офтальмического агента и удаление эластомерного материала с глаза.
Предполагается, что термин "офтальмический агент", как его применяют в настоящем изобретении, включает все агенты, которые дают местный или системный физиологический или фармакологический эффект при введении млекопитающим, включая, без ограничения, любые конкретные лекарственные средства, указанные в последующем описании, и их аналоги, производные, фармацевтически приемлемые соли, сложные эфиры, пролекарства, комбинированные лекарственные средства и защищенные формы. В определенных вариантах осуществления лекарственное средство представляет собой небольшую молекулу, имеющую молекулярный вес не более чем 1000 а.е.м. Например, лекарственное средство может представлять собой небольшую молекулу, имеющую молекулярный вес не более чем или равный до приблизительно 750 а.е.м, 500 а.е.м, 450 а.е.м, 400 а.е.м, 350 а.е.м или меньше чем или равную до приблизительно 300 а.е.м.
Многие различные офтальмические агенты можно вводить в устройство, описанное в настоящем изобретении. Например, подходящие агенты включают агенты, улучшающие отток внутриглазной жидкости, стероиды, агонисты альфа-рецепторов, антагонисты бета-рецепторов, ингибиторы карбоангидразы, адренергические агенты, физиологически активные пептиды и/или белки, противоопухолевые агенты, антибиотики, анальгетики, противовоспалительные агенты, миорелаксанты, противоэпилептические агенты, противоязвенные агенты, противоаллергические средства, кардиотонические агенты, антиаритмические агенты, сосудорасширяющие средства, гипотензивные средства, противодиабетические средства, антигиперлипидемические средства, антикоагулянты, гемолитические средства, противотуберкулезные средства, гормоны, антагонисты наркотических анальгетиков, остеокластические супрессивные средства, остеогенные стимуляторы, супрессоры ангиогенеза, антибактериальные средства, нестероидные противовоспалительные препараты (НПВП), глюкокортикоиды или другие противовоспалительные кортикостероиды, алкалоидные анальгетики, такие как опиоидные анальгетики, противовирусные средства, такие как нуклеозидные противовирусные средства или ненуклеозидные противовирусные средства, агенты против доброкачественной гипертрофии предстательной железы (ДГПЖ), противогрибковые соединения, антипролиферативные соединения, соединения против глаукомы, иммуномодулирующие соединения, агенты, препятствующие клеточному транспорту/подвижности, цитокиновые пегилированные агенты, альфа-блокаторы, антиандрогены, антихолинергические агенты, пуринергические агенты, дофаминергические агенты, местные анестетики, ваниллоиды, ингибиторы оксида азота (I), антиапоптотические агенты, ингибиторы активации макрофагов, антиметаболиты, нейропротекторы, блокаторы кальциевых каналов, антагонисты гамма-аминомасляной кислоты (ГАМК), альфа агонисты, антипсихотические агенты, ингибиторы тирозинкиназы, нуклеозидные соединения, и нуклеотидные соединения и их аналоги, производные, фармацевтически приемлемые соли, сложные эфиры, пролекарства, комбинированные лекарственные средства и их защищенные формы, и агенты для генной доставки, такие как, но не ограничиваясь, лентивирусы и подобные.
Подходящие НПВП включают диклофенак, этолдолак, фенопрофен, флоктафенин, флурбипрофен, ибупрофен, индопрофен, кетопрофен, кеторолак, лорноксикам, моразон, напроксен, перизоксаль, пирпрофен, пранопрофен, супрофен, суксибузон, тропезин, ксимопрофен, залтопрофен, зилеутон и зомепирак, и их аналоги, производные, фармацевтически приемлемые соли, сложные эфиры, пролекарства, комбинированные лекарственные средства и защищенные формы.
Подходящие ингибиторы карбоангидразы включают бринзоламид, ацеталозамида, метазоламид, дихлорфенамид, этоксзоломид и дорзоламид, и их аналоги, производные, фармацевтически приемлемые соли, сложные эфиры, пролекарства, комбинированные лекарственные средства и защищенные формы.
Подходящие адренергические агенты включают бримонидин, апраклонидин, буназозин, левобетаксолол, левобунвлол, картеолол, изопреналин, фенотерол, метипранолол и кленбутерол, и их аналоги, производные, фармацевтически приемлемые соли, сложные эфиры, пролекарства, комбинированные лекарственные средства и защищенные формы.
Подходящие агонисты альфа-рецепторов включают бримонидин и его аналоги, производные, фармацевтически приемлемые соли, сложные эфиры, пролекарства, комбинированные лекарственные средства и защищенные формы.
Подходящие антагонисты бета-рецепторов включают бетаксолол и тимолол, и их аналоги, производные, фармацевтически приемлемые соли, сложные эфиры, пролекарства, комбинированные лекарственные средства и защищенные формы.
Подходящие противовирусные агенты включают невирипин и его аналоги, производные, фармацевтически приемлемые соли, сложные эфиры, пролекарства, комбинированные лекарственные средства и защищенные формы.
Подходящие алкалоидные анальгетики включают дезоморфин, дезоцин, дигидроморфина, эптазоцин, этилморфин, глафенин, гидроморфон, изоладол, кетобенидон, п-лактофенид, леворфанол, моптазинол, метазоцин, метопон, морфин, нальбуфин, налмефен, налорфин, налоксон, норлеворфанол, норморфин, оксиморфин, пентазоцин, фенперидин, фенилрамидол, трамадол и виминол, и их аналоги, производные, фармацевтически приемлемые соли, сложные эфиры, пролекарства, комбинированные лекарственные средства и защищенные формы.
Подходящие глюкокортикоиды включают 21-ацетоксипрегненолон, алклометазон, альгестон, ацетат анакортава, амцинонид, беклометазон, бетаметазон, будесонид, хлорпреднизон, клобетазол, клобетазон, клокортолона, клопреднол, кортикостерон, кортизон, кортивазол, дефлазакорт, дезонид, дезоксиметазон, дифлоразон, дифлукортолон, дифупреднат, эноксолон, флуазакорт, флуклоронид, флуметазон, флунизолид, ацетонид флуоцинолона, флуоцинонид, флуклоронид, флуметазон, флунизолид, флуокортин-бутил, флуокортолон, фторметолон, ацетат флуперолона, флупреднизолон, флурандренолид, пропионат флутиказона, гидрокортамат, гидрокортизон, мепреднизон, метилпреднизолон, параметазон, преднизолон, 21-диэтиламиноацетат преднизолона, ацетат флупредниден, формокортал, этабонат лотепреднола, медризон, фуроат мометазона, предникарбат, преднизолон, 25-диэтиламиноацетат преднизолона, фосфатпреднизолон натрия, преднизон, предниваль, преднилиден, триамцинолон, ацетонид триамцинолона, бенетонид триамцинолона и гексацетонид триамцинолона, и их аналоги, производные, фармацевтически приемлемые соли, сложные эфиры, пролекарства, комбинированные лекарственные средства и защищенные формы.
Другие подходящие стероиды включают галцинонид, пропионат галбетазола, галометазон, ацетат галопредона, изофлупредон, этабонат лотепреднола, мазипредон, римексолон и тиксокортол, и их аналоги, производные, фармацевтически приемлемые соли, сложные эфиры, пролекарства, комбинированные лекарственные средства и защищенные формы.
Подходящие BPH лекарственные средства включают финастерид и озатерон, и их аналоги, производные, фармацевтически приемлемые соли, сложные эфиры, пролекарства, комбинированные лекарственные средства и защищенные формы.
Подходящие антибактериальные соединения включают капреомицины, включая капреомицин IА, капреомицин IB, капреомицин IIA и капреомицин IIb; карбомицины, включая карбомицин; карумонам; цефаклор, цефадроксил, цефамандол, цефатризин, цефазедон, цефазолин, цевбуперазон, цевкапен-пивоксил, цевклидин, цефдинир, цевдиторен, цефим, цевтамет, цевменоксим, цевметзол, цевминокс, цеводизим, цефонизид, цефоперазон, цефоранид, цефотаксим, цефотетан, цефотиам, цефокситин, цефпимизол, цефпирамид, цефпиром, цефпрозил, цефроксанид, цефсулодин, цефтазидим, цефтерам, цефтезол, цефтибутен, цефтиофур, цефтизоксим, цефтриаксон, цефуроксим, цефузонам, цефалексин, цефалогицин, цефалоридин, цефалоспорин C, цефалотин, цефапирин, цефамицины, такие как цефамицин C, цефрадин, хлортетрациклин; кларитромицин, клиндамицин, клометоциллин, кломоциклин, клоксациллин, циклациллин, данофлоксацин, демеклоциклин, дестомицин А, диклоксациллин, диклоксациллин, диритромицин, доксициклин, эпициллин, эритромицин, этанбутол, фенбенициллин, фломоксеф, флорфеникол, флоксациллин, флумекин, фортимицин А, фортимицин B, форфомицин, форалтадон, фусидовую кислоту, гентамицин, гликониазид, гуамециклин, гетациллин, идарубицин, имипенем, изепамицин, джозамицин, канамицин, леумицины, такие как леумицин A1, линкомицин, ломефлоксацин, лоракарбеф, лимециклин, меропенам, метампициллин, метациклин, метициллин, мезлоциллин, микронаомицин, мидекамицины, такие как мидекамицин A1, микамицин, миноциклин, митомицины, такие как митомицин C, моксалактам, мупироцин, нафциллин, нетилицин, норкардианы, такие как норкардиан A, олеандомицин, окситетрациклин, панипенам, пазуфлоксацин, пенамециллин, пенициллины, такие как пенициллин G, пенициллин N и пенициллин O, пеницилловую кислоту, пентилпенициллин, пепломицин, фенетициллин, пипациклин, пиперацилин, пирлимицин, пивампициллин, пивцевалексин, порфлромицин, пропиаллин, хинациллин, рибосамицин, рифабутин, рифамид, рифампицин, рифамицин SV, рифапентин, рифаксимин, ритипенем, рекитамицин, ролитетрациклин, розарамицин, рокситромицин, санциклин, сизомицин, спартлоксацин, спектиномицин, стрептозоцин, сулбенициллин, сультамициллин, талампициллин, тейкопланин, темоциллин, тетрациклин, тострептон, тиамулин, тикарциллин, тигемонам, тилмикозин, тобрамицин, тропоспектромицин, тровафлоксацин, тилозин и ванкомицин, и их аналоги, производные, фармацевтически приемлемые соли, сложные эфиры, пролекарства, комбинированные лекарственные средства и защищенные формы.
Антипролиферативные/антимитотические лекарственные средства и пролекарства включают природные продукты, такие как алкалоиды барвинка (например, винбластин, винкристин и винорелбин), паклитаксел, эпидиподофиллотоксины (например, этопозид, тенипозид), антибиотики (например, актиномицин, даунорубицин, доксорубицин и идарубицин), антрациклины, митоксантрон, блеомицины, пликамицин (митрамицин) и митомицин, ферменты (например, L-аспарагиназу); антитромбоцитные пролекарства; антипролиферативные/антимитотические алкилирующие пролекарства, такие как азотистые иприты (меклоретамин, циклофосфамид и аналоги, мельфалан, хлорамбуцил), этиленимины и метилмеламины (гексаметилмеламин и тиотепа), алкилсульфонаты-бусульфан, нитрозомочевины (кармустин (BCNU) и аналоги, стрептозоцин), триазены, дакарбазин (DTIC); антипролиферативные/антимитотические антиметаболиты, такие как аналоги фолиевой кислоты (метотрексат), пиримидиновые аналоги (фторурацил, флоксуридин и цитарабин), пуриновые аналоги и родственные ингибиторы (меркаптопурин, тиогуанин, пентостатин и 2-хлордезоксиаденозин (кладрибином); координационные комплексы платины (цисплатину, карбоплатину), прокарбазин, гидроксимочевину, митотан, аминоглутетемид; гормоны (например, эстроген, прогестин); антикоагулянты (например, гепарин, соли синтетического гепарина и другие ингибиторы тромбина); фибринолитические пролекарства, такие как активатор тканевого плазминогена, стрептокиназа и урокиназа, аспирин, дипиридамол, тиклопидин, клопидогрель, абциксимаб; противомиграционные агенты; антисекреторные агенты (бревелдин); противовоспалительные агенты, такие как кортикостероиды (кортизол, кортизон, флудрокортизон, флуцинолон, преднизон, преднизолон, метилпреднизолон, триамцинолон, бетаметазон и дексаметазон), НПВС (салициловая кислота и производные, аспирин, ацетаминофен, индол и инденуксусную кислоту (индометацин, сулиндак и этодалак), гетероарилуксусные кислоты (толметин, диклофенак и кеторолак), арилпропионовые кислоты (например, ибупрофен и производные), антраниловые кислоты (мефенамовая кислота и меклофенамовая кислота), енольные кислоты (пироксикам, теноксикам, фенилбутазон и оксифентатразон), набуметон, соединения золота (ауранофин, ауротиоглюкоза, тиомалат золота натрия); иммуносупрессивные агенты (например, циклоспорин, такролимус (FK-506), сиролимус (рапамицин), азатиоприн и микофенолятмофетил); ангиогенные агенты, такие как фактор роста эндотелия сосудов (VEGF), фактор роста фибробластов (FGF); блокаторы рецепторов ангиотензина; доноры оксида азота; антисмысловые олигонуклеотиды и их комбинаций; ингибиторы клеточного цикла, ингибиторов mTOR, ингибиторы киназы трансдукции сигнала фактора роста, ингибиторы неоваскуляризации, ингибиторы ангиогенеза и ингибиторы апоптоза, и их аналоги, производные, фармацевтически приемлемые соли, сложные эфиры, пролекарства, комбинированные лекарственные средства и защищенные формы.
В определенных вариантах осуществления, офтальмический агент содержит агент, улучшающий отток внутриглазной жидкости. Как применяют в настоящем изобретении, термин "агент, улучшающий отток внутриглазной жидкости" относится к таким агентам, которые способны увеличивать отток внутриглазной жидкости в глазу, посредством этого снижая внутриглазное давление в глазу.
В определенных вариантах осуществления агент, улучшающий отток внутриглазной жидкости, включает этакриновую кислоту (которая представляет собой [2,3-дихлор-4-(2-метилен-1-оксобутил)фенокси]уксусную кислоту) или любой ее аналог, соль или производное. Этакриновая кислота и ее соли, производные и аналоги вместе с предпочтительными способами введения данных соединений подробно описаны в патентах США № 3255241, 4757089, 5306731, 5458883, 5863948, 6126957 и 6534082, содержание которых включено в настоящее изобретение с помощью ссылке во всей полноте.
В определенных вариантах осуществления агент, улучшающий отток внутриглазной жидкости, включает производные и аналоги этакриновой кислоты, которые могут содержать или не содержать сульфгидрильную реакционно-способную группу. Примеры агентов включают, но не ограничиваются: 2-[2,3-дихлор-4-[(Z)-2-метилбут-2-еноил]фенокси]уксусную кислоту, 2-[2,3-дихлор-4-(3-метилбут-2-еноил)фенокси|уксусную кислоту, 2-[2,3-дихлор-4-(2-метилиденбутаноил)фенокси]-2-(2,3-дигидроксипропокси)уксусную кислоту, [(2S,3R,4R)-1,3,4,5-тетрагидроксипентан-2-ил]-2-[2,3-дихлор-4-(2-метилиденбутаноил)фенокси]ацетат, 2-[2,3-дихлор-4-(2,3-диметилбутаноил)фенокси]уксусную кислоту и т.д.
В определенных вариантах осуществления агент, улучшающий отток внутриглазной жидкости, включает производные и аналоги этакриновой кислоты, которые могут содержать или не содержать сульфгидрильную реакционно-способную группу. В определенных вариантах осуществления агент, улучшающий отток внутриглазной жидкости, включает тиольные продукты присоединения этакриновой кислоты. Примеры включают, но не ограничиваются, этакриновая кислота-1-цистеин (т.е., S-[2-[4-(карбоксиметокси)-2,3-дихлорбензоил]бутил]-l-цистеин), этакриновая кислота-цистеамин (т.е. 2-(4-(2-((2-аминоэтилтио)метил)бутаноил)-2,3-дихлорфенокси)уксусную кислоту), этакриновая кислота-глутатион (т.е., 2-амино-5-(3-(2-(4-(карбоксиметокси)-2,3-дихлорбензоил)бутилтио)-1-(карбоксиметиламино)-1-оксопропан-2-иламино)-5-оксопентановую кислоту), этакриновая кислота-тиосалициловую кислоту (2-(2-(4-(карбоксиметокси)-2,3-дихлорбензоил)бутилтио)бензойную кислоту), этакриновая кислота- N-ацетилцистеин (2-ацетамидо-3-(2-(4-(карбоксиметокси)-2,3-дихлорбензоил)бутилтио)пропионовую кислоту), этакриновая кислота- N-ацетилцистеамин (т.е., 2-(4-(2-((2-ацетамидоэтилтио)метил)бутаноил)-2,3-дихлорфенокси)уксусную кислоту) или любую их соль.
В других вариантах осуществления агент, улучшающий отток внутриглазной жидкости, представляет собой этакриновую кислоту-1-цистеин (т.е. S-[2-[4-(карбоксиметокси)-2,3-дихлорбензоил]бутил]-l-цистеин) или любую его соль.
В других вариантах осуществления агент, улучшающий отток внутриглазной жидкости, представляет собой 2-[2,3-дихлор-4-[2-(метилсульфанилметил)бутаноил]фенокси]уксусную кислоту.
В другом варианте осуществления, агент, улучшающий отток внутриглазной жидкости, включает феноксиуксусную кислоту, 2,3-дихлорфеноксиуксусную кислоту, 2,4-дихлорфеноксиуксусную кислоту или любой их аналог или производное. В одном варианте осуществления агент, улучшающий отток внутриглазной жидкости, включает феноксиуксусную кислоту, 2,3-дихлорфеноксиуксусную кислоту или производное 2,4-дихлорфеноксиуксусной кислоты, который не является реакционно-способным относительно SH. В определенных вариантах осуществления нереакционно-способное относительно SH производное 2,4-дихлорфеноксиуксусной кислоты включает индакринон (т.е. 6,7-дихлор-2-метил-1-оксо-2-фенил-5-инданилоксиуксусную кислоту), тикринафен (т.е., 2-(2,3-дихлор-4-(тиофен-2-карбонил)фенокси)уксусную кислоту) или любую ее соль.
Еще другой аспект настоящего изобретения относится к способу вызывания заболевания, подобного глаукоме, у субъекта, включающему помещение эластомерного материала, как описано в настоящем изобретении, по экватору глаза, посредством этого перекрывая поток венозной крови в эписклеральной вене, введение через эписклеральную вену эффективного количества офтальмического агента и вязкоэластичного агента и удаление эластомерного материала с глаза.
Как применяют в настоящем изобретении, термин "заболевание, подобное глаукоме" относится к любому заболеванию, которое демонстрирует симптомы и/или состояния, которые связаны с глаукомой, такие как повышенное внутриглазное давление и/или повреждение зрительного нерва. Также включенными в данное определение являются состояния, такие как повышенное внутриглазное давление на фоне гипотонии, такие как после антиглаукомной операции или ситуации, связанные с увеитом.
В других вариантах осуществления офтальмический агент вводят с вязкоэластичным агентом. Как применяют в настоящем изобретении, термин "вязкоэластичный агент" относится к любому агенту, способному расширять переднюю камеру глаза, обеспечивая доставку дополнительных соединений и/или хирургических инструментов. Подходящие вязкоэластичные агенты включают, но не ограничиваются, Healon®OVD, Healon5®OVD, HealonGV®, Provic® и подобные. В определенных вариантах осуществления отношение офтальмического агента к вязкоэластичному агенту составляет 3:1.
В некоторых вариантах осуществления вязкоэластичный агент вводят перед офтальмическим агентом. В других вариантах осуществления вязкоэластичный агент вводят одновременно с офтальмическим агентом. В еще других вариантах осуществления вязкоэластичный агент вводят после офтальмического агента.
Кроме того, настоящее изобретение относится к фармацевтическим композициям, содержащим офтальмический агент, описанный в настоящем изобретении, необязательно вязкоэластичный агент и фармацевтически приемлемый носитель. Как применяют в настоящем изобретении, термин "фармацевтическая композиция" относится к комбинации по меньшей мере одного офтальмического агента, как описано в настоящем изобретении, с носителем, инертным или активным, делая композицию особенно подходящей для диагностического или терапевтического применения in vivo, in vitro или ex vivo. В определенных вариантах осуществления фармацевтическая композиция содержит офтальмический агент и вязкоэластичный агент. "Фармацевтически приемлемый носитель" относится к любому из стандартных фармацевтических носителей, такому как физиологический раствор с фосфатным буфером, вода, эмульсии (например, такие как эмульсии масла в воде или воды в масле), различные типы смачивающих агентов, разбавители и вспомогательные вещества. Композиции может также содержать стабилизаторы и консерванты. Что касается примеров носителей, стабилизаторов и вспомогательных веществ, смотри, например, Martin, Remingtonʹs Pharmaceutical Sciences, 15th Ed., Mack Publ. Co., Easton, Pa. (1975)).
Фармацевтическую композицию обычно получают в виде раствора в переносимом (приемлемом) разбавителе, таком как соляной раствор, фосфатно-солевой буферный раствор или другой физиологически переносимый разбавитель и подобном, получая водную фармацевтическую композицию.
Путь введения может являться внутривенным (I.V.), внутримышечным (I.M.), подкожным (S.C.), внутрикожным (I.D.), внутрибрюшинным (I.P.), внутриопухолевым и подобным, которые приводят в результате к вызыванию требуемой реакции. Дополнительные способы введения могут включать местное введение (глазные капли), подконъюнктивальную, внутрикамерную, интравитреальную инъекцию или инъекцию вокруг глаз или введение баллонным катетером или офтальмологическими вкладками, хирургически помещаемыми в конъюнктивальный мешок. В предпочтительных вариантах осуществления путь введения представляет собой инъекцию в эписклеральную вену.
Терапевтическая доза композиций может изменяться в зависимости, например, от способа введения соединения, здоровья и состояния пациента и решения лечащего врача. Доля или концентрация офтальмического агента, описанного в настоящем изобретении, в фармацевтической композиции может изменяться в зависимости от ряда факторов, включая дозу, химические свойства (например, гидрофобность) и путь введения. Например, офтальмические агенты, описанные в настоящем изобретении, можно обеспечивать в водном физиологическом соляном растворе, содержащем от приблизительно 0,1 до приблизительно 10% w/v агента. Некоторые из стандартных диапазонов доз составляют от приблизительно 1 г/кг до приблизительно 1 г/кг веса тела в день. Доза, вероятно, будет зависеть от таких переменных, как тип и степень развития заболевания или состояния, общее состояние здоровья конкретного пациента, относительная биологическая эффективность выбранного соединения, состав вспомогательных веществ и путь его введения. Эффективные дозы можно экстраполировать из кривых зависимости эффекта от дозы, полученных в системах испытания in vitro или на модельных животных. В одном варианте осуществления дозу вводят по меньшей мере один раз. Последующие дозы можно вводить, как указано.
ПРИМЕРЫ
Способы и материал настоящего изобретения дополнительно проиллюстрированы следующими примерами, которые не следует считать ограничивающими объем настоящего изобретения, и они приводятся в качестве иллюстрации.
ПРИМЕР 1. Эффект прямого введения этакриновой кислоты (ECA) с и без хеалона через эписклеральную вену.
Исходное внутриглазное давление измеряли для обоих глаз мыши, применяя TonoLab устройство. Кусочек перчатки из латекса помещали на экватор глаза мыши. Первоначально стеклянную микроканюлю применяли для введения или (a) раствора только этакриновой кислоты, или (b) соляного раствора в эписклеральную вену через лимб правого глаза каждой мыши. Раствор или соляной раствор вводили до наблюдения 360-градусного побледнения вокруг лимба. Затем, кусочек латекса удаляли с глаза. Затем, измеряли внутриглазное давление каждый день и затем каждую неделю в обоих глазах для каждой мыши. Инъекция только этакриновой кислоты давала свой максимальный эффект на 2 день; однако некоторый эффект сохранялся до 7 дня. Результаты приведенного выше протокола приведены в таблице I и также показаны на фигуре 4, где этакриновая кислота указана как EGA (квадраты), соляной контрольный раствор представляет собой BSS (треугольники) и необработанная группа представляет собой контроль (ромбы).
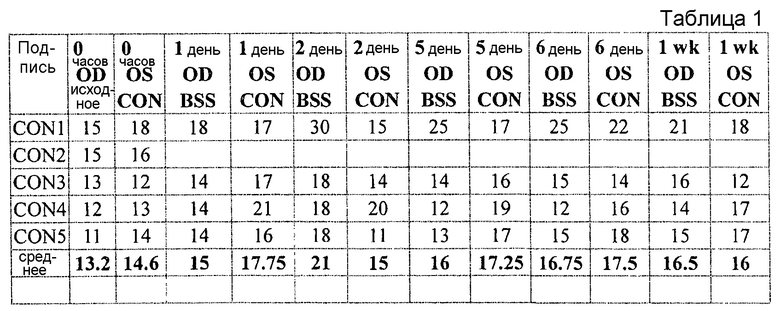
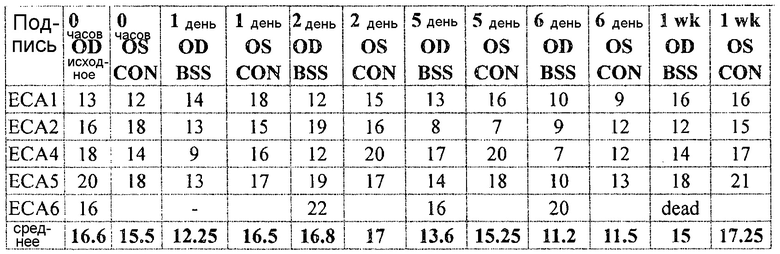
Затем, этакриновую кислоту смешивали с хеалоном в соотношении 3:1. Снова, стеклянную микроканюлю применяли для инъекции или раствора этакриновой кислоты/хеалона или BSS раствора в качестве контроля. Раствор этакриновой кислоты/хеалона давал свой максимальный эффект в течение 2 недель, но длился 3 недели. Результаты приведены в таблице 2, и также показаны на фиг. 3, где этакриновая кислота/хеалон обозначен квадратами, BSS ромбами, и контроль без инъекции треугольниками.
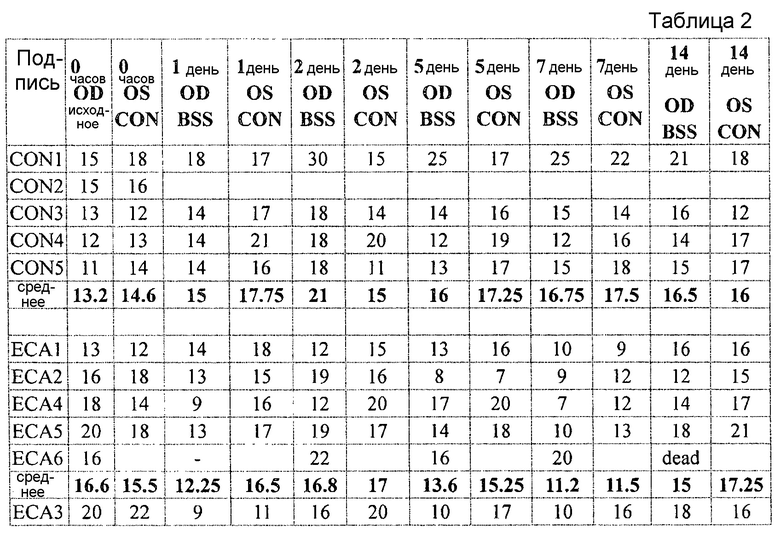
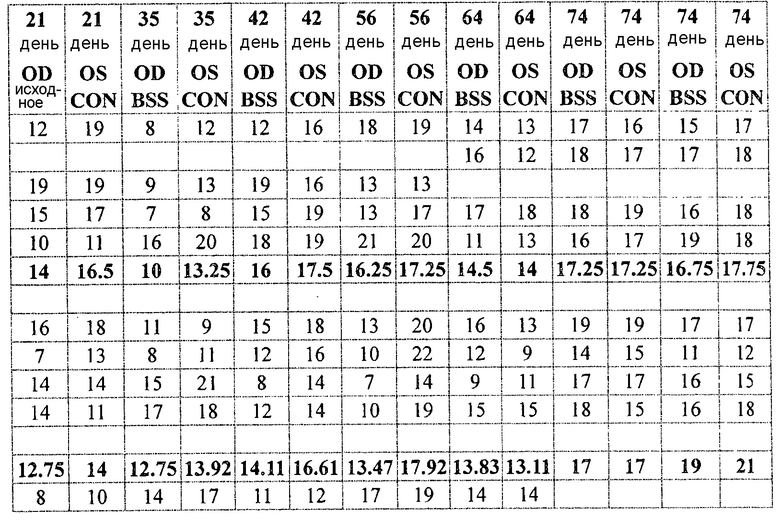
ПРИМЕР 2. Влияние замедленной доставки этакриста (этакриновая кислота + L-цистеин) в наночастицах с замедленным высвобождением на внутриглазное давление (IOP)
Пример 2.1: для исследования, может ли замедленное высвобождение из наночастиц этакриновой кислоты (EGA) (без хеалона), вводимых в эписклеральную вену, снижать внутриглазное давление в течение длительного периода времени для пациентов, страдающих от глаукомы, в правый глаз 8 C57B16 мышей вводили или наночастицы этакриста (без хеалона) (4 мыши), или сбалансированный соляной раствор (BSS) (4 мыши) в эписклеральную вену у лимба. Исходное IOP измеряли устройством TonoLab™ для грызунов перед инъекциями и затем еженедельно. Осмотр глаза с помощью щелевой лампы проводили для оценки конъюнктивального покраснения, воспаления в передней камере и мутности роговицы.
Как показано на фиг. 7a, все 4 мыши (обозначенные "серии 1, 2, 3 и 4ʹʹ) показали значительное снижение IOP в течение 3 недель, с последующим возвращением до исходной величины на 4 неделе.
Пример 2.2: для исследования, продлевает ли вязкоэластичный хеалон или аналогичное соединение, снижающие IOP эффекты наночастиц этакриста, в правый глаз 6 C57BI6 мышей вводили наночастицы этакриста плюс хеалон в соотношении 3:1 (3 мыши) или BSS (3 мыши).
Исходное IOP измеряли TonoLab™ устройством для грызунов перед инъекциями, и затем еженедельно после этого. Осмотр глаза с помощью щелевой лампы проводили для оценки конъюнктивального покраснения, воспаления в передней камере и мутности роговицы.
График на фиг. 10 показывает, что мыши с инъекцией в эписклеральную вену наночастиц этакриста, смешанного с хеалоном в соотношении 3:1, показывали значительное снижение IOP в течение 3 недель, которое продлевалось до 8 недель.
Пример 2.3: исследовали другие способы доставки наночастиц этакриста. Субконъюнктивальная доставка показана на фиг. 9a и 9b (высокая и низкая концентрации наночастиц этакриста), и внутрикамерная доставка показана на фиг. 8a и 8b (высокая и низкая концентрации наночастиц этакриста). Исходное IOP измеряли TonoLab™ устройством для грызунов перед инъекциями и затем еженедельно после этого. Осмотр глаза с помощью щелевой лампы проводили для оценки конъюнктивального покраснения, воспаления в передней камере и мутности роговицы.
Графики на фиг. 7-9 показывают следующие результаты: фиг. 7a показывает эписклеральную инъекцию мышам наночастиц этакриста (без хеалона), фиг. 7b показывает эписклеральную инъекцию наночастиц этакриста + хеалона (соотношение 3:1), и фиг. 7c показывает эписклеральную инъекцию BSS (контроль); фиг. 8a показывает внутрикамерную инъекцию наночастиц этакриста, содержащих большую концентрацию наночастиц (10 мкг/мкл), и фиг. 8b показывает внутрикамерную инъекцию низкой концентрации (1 мкг/мкл) наночастиц; и фиг. 9a-b показывают субконъюнктивальную инъекцию наночастиц этакриста, содержащих большую концентрацию (1 мкг/мкл) (фиг. 9a) или низкую концентрацию (0,1 мкг/мкл) наночастиц (фиг. 9b). На всех данных фигурах каждая отдельная "серия" представляет собой отдельную мышь.
Приведенные выше результаты предполагают, что эписклеральные инъекции наночастиц этакриста, по-видимому, являются лучшими внутрикамерных инъекций и субконъюнктивальных инъекций для снижения IOP. Кроме того, эписклеральные инъекции наночастицы этакриста, смешанного с хеалоном (в соотношении 3:1), по-видимому, являются лучшими, чем только наночастицы для снижения IOP.
Любые патенты или публикации, приведенные в настоящем изобретении, являются указывающими на уровень специалиста в данной области техники, к которому относится настоящее изобретение. Данные патенты и публикации включены в настоящее изобретение с помощью ссылки в той же степени, как если бы указывалось, что каждая отдельная публикация специально и отдельно включена с помощью ссылки.
Специалисту в данной области техники ясно, что настоящее изобретение хорошо приспособлено для достижения его целей и достижения приведенных результатов и преимуществ, а также тех, что присущи настоящему изобретению. Настоящие примеры вместе со способами, описанными в настоящем изобретении, являются в настоящее время репрезентацией предпочтительных вариантов осуществления, являются примерными, и не предполагается, что они ограничивают объем настоящего изобретения. Изменения в настоящем изобретении и другие применения будут приходить в голову специалиста в данной области техники, которые включены в сущность настоящего изобретения, как определенные объемом формулы изобретения.
Группа изобретений относится к медицине, а именно к офтальмологии, и представляет собой эластомерный материал для доставки офтальмического агента в глаз субъекта и способы применения данного материала. Эластомерный материал обеспечивает перекрытие потока венозной крови в эписклеральной вене глаза субъекта. Через эту вену может быть произведено введение офтальмического агента. Офтальмический агент, введенный таким образом, после снятия эластомерного материала попадает в Шлемов канал и трабекулярную сеть. Описанные манипуляции позволяют обеспечить пролонгированное действие препарата на структуры глаза, создать депо препарата. 5 н. и 9 з.п. ф-лы, 10 ил., 2 табл., 2 пр.
1. Эластомерный материал для перекрытия потока венозной крови в эписклеральной вене глаза субъекта, содержащий:
(a) центральное отверстие с внутренним диаметром в нем; и
(b) наружным диаметром по меньшей мере 1 мм,
причем при помещении эластомерного материала на глаз, часть внутреннего диаметра выполнена с возможностью растяжения для установки по экватору глаза и после сжатия с возможностью перекрытия потока венозной крови в эписклеральной вене глаза.
2. Эластомерный материал по п. 1, имеющий форму, выбранную из круглой, прямоугольной, квадратной.
3. Эластомерный материал по п. 1, в котором наружный диаметр составляет от приблизительно 2 мм до приблизительно 40 мм.
4. Эластомерный материал по п. 1, в котором внутренний диаметр эластичного материала составляет от приблизительно 2 мм до приблизительно 20 мм.
5. Эластомерный материал по п. 1, содержащий силастиковый материал.
6. Способ усиления оттока внутриглазной жидкости в глазу субъекта, страдающего от глаукомы, включающий этапы:
(a) размещают эластомерный материал по п. 1 по экватору глаза, посредством этого перекрывая поток венозной крови в эписклеральной вене;
(b) вводят через эписклеральную вену терапевтически эффективное количество офтальмического агента; и
(c) удаляют эластомерный материал с глаза.
7. Способ доставки офтальмического агента в систему водного оттока, предусматривающий следующие этапы:
(a) размещают эластомерный материал по п. 1 по экватору глаза, посредством этого перекрывая поток венозной крови в эписклеральной вене;
(b) вводят через эписклеральную вену терапевтически эффективное количество офтальмического агента; и
(c) удаляют эластомерный материал из глаза.
8. Способ доставки офтальмического агента в переднюю камеру глаза, предусматривающий следующие этапы:
(a) размещают эластомерный материал по п. 1 по экватору глаза, посредством этого перекрывая поток венозной крови в эписклеральной вене;
(b) вводят через эписклеральную вену терапевтически эффективное количество офтальмического агента; и
(c) удаляют эластомерный материал из глаза.
9. Способ вызывания подобного глаукоме состояния у субъекта, предусматривающий следующие этапы:
(a) помещают эластомерный материал по п. 1 по экватору глаза, посредством этого перекрывая поток венозной крови в эписклеральной вене;
(b) вводят через эписклеральную вену эффективное количество офтальмического агента и вязкоэластичного агента;
(c) удаляют эластомерный материал с глаза.
10. Способ по любому из пп. 6-9, в котором офтальмический агент выбран из группы, состоящей из улучшающих отток агентов, стероидов, агонистов альфа-рецепторов, антагонистов бета-рецепторов, ингибиторов карбоангидразы, адренергических агентов, физиологически активных пептидов и/или белков, противоопухолевых агентов, антибиотиков, анальгетиков, противовоспалительных агентов, миорелаксантов, противоэпилептических агентов, противоязвенных агентов, противоаллергических средств, кардиотонических агентов, антиаритмических агентов, сосудорасширяющих средств, гипотензивных средств, противодиабетических средств, антигиперлипидемических средств, антикоагулянтов, гемолитических средств, противотуберкулезных средств, гормонов, антагонистов наркотических анальгетиков, остеокластических супрессивных средств, остеогенных стимуляторов, супрессоров ангиогенеза, антибактериальных средств, нестероидных противовоспалительных препаратов (НПВП), глюкокортикоидов или других противовоспалительных кортикостероидов, алкалоидных анальгетиков, таких как опиоидные анальгетики, противовирусных средств, таких как нуклеозидные противовирусные средства или ненуклеозидные противовирусные средства, агентов против доброкачественной гипертрофии предстательной железы (ДГПЖ), противогрибковых соединений, антипролиферативных соединений, соединений против глаукомы, иммуномодулирующих соединений, агентов, препятствующих клеточному транспорту/подвижности, цитокиновых пегилированных агентов, альфа-блокаторов, антиандрогенов, антихолинергических агентов, пуринергических агентов, дофаминергических агентов, местных анестетиков, ваниллоидов, ингибиторов оксида азота (I), антиапоптотических агентов, ингибиторов активации макрофагов, антиметаболитов, нейропротекторов, блокаторов кальциевых каналов, антагонистов гамма-аминомасляной кислоты (ГАМК), альфа-агонистов, антипсихотических агентов, ингибиторов тирозинкиназы, нуклеозидных соединений и нуклеотидных соединений и их аналогов, производных, фармацевтически приемлемых солей, сложных эфиров, пролекарств, комбинированных лекарственных средств и их защищенных форм, и их комбинаций.
11. Способ по п. 10, в котором улучшающий отток агент содержит этакриновую кислоту или ее любые аналоги или производные.
12. Способ по любому из пп. 6-9, в котором офтальмический агент вводят с вязкоэластичным агентом.
13. Способ по п. 12, где вязкоэластичный агент выбран из группы, состоящей из Healon®OVD, Healon 5®QVD, Healon GV®, Provic® и их комбинаций.
14. Способ по п. 12, где отношение офтальмического агента к вязкоэластичному агенту составляет 3:1.
| US 7273475 B2, 25.09.2007 | |||
| US 20080177383 A1, 24.07.2008 | |||
| CONE F.E et al., Lack of neuroprotection against experimental glaucoma in c-Jun N-terminal kinase 3-knockout mice, Exp Eye Res, 2011, 92(4), p | |||
| АВТОМАТ ДЛЯ ПУСКА В ХОД ПОРШНЕВОЙ МАШИНЫ | 1920 |
|
SU299A1 |
Авторы
Даты
2017-05-02—Публикация
2013-03-15—Подача