Область техники, к которой относится изобретение
Настоящее изобретение относится к кристаллическому веществу луликоназолу и фармацевтическому препарату, содержащему указанное кристаллическое вещество.
Уровень техники
Луликоназол представляет собой противогрибковое средство, которое имеет приведенную ниже структуру и которое оказывает превосходное действие на грибы. В настоящее время луликоназол широко используется в качестве фармацевтического препарата и лекарственного средства против дерматофитии стоп и дерматофитии туловища, и его предполагается применять для действия против грибкового поражения ногтей. Что касается фармацевтического препарата (лекарственного средства) луликоназола, то известной проблемой, которая требует своего решения, является то, что луликоназол преобразуется в стереоизомеры, такие как SE-изомер и Z-изомер, и что кристаллизация луликоназола начинается сразу же после его нанесения (см., например, патентные документы 1-6). В частности, что касается изомеризации, то авторы настоящего изобретения подтвердили, что как на SE-изомер, так и на Z-изомер влияние оказывают компоненты препарата, температура и свет. Оценку стабильности луликоназола проводят в условиях хранения в течение 3 недель при 60°C, которые моделируют указанные выше обстоятельства. Таким образом, при получении луликоназола необходимо максимально сократить стадию нагревания. С другой стороны, луликоназол обладает низкой растворимостью в воде. Когда луликоназол растворяют в компоненте фармацевтического препарата, необходимо провести стадию нагревания. Требуется разработать какие-либо способы улучшения растворимости луликоназола и сократить время нагрева на стадии нагревания. Преимущество сокращения или уменьшения стадии нагревания заключается в том, что образование или формирование любого изомера, образованного или сформировавшегося на указанной стадии, не только подавляется, но и обеспечивается долговременная стабильность за счет снижения изначального количества изомера. Другими словами, подтверждено, что сокращение или уменьшение стадии растворения приводит к значительному улучшению качества.
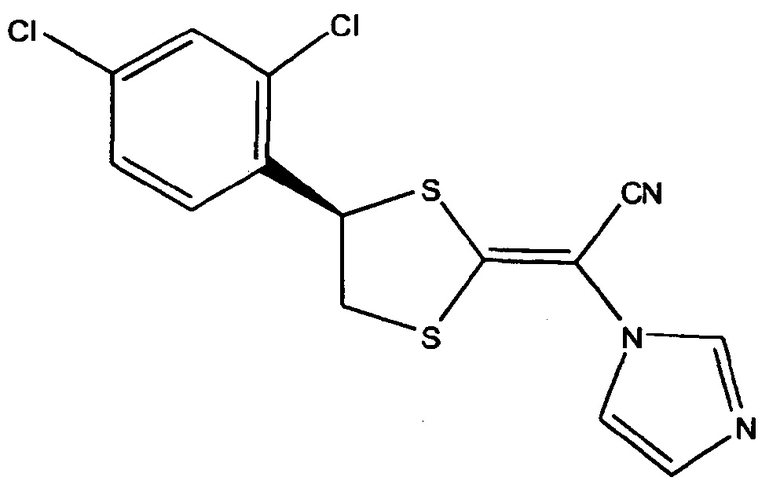
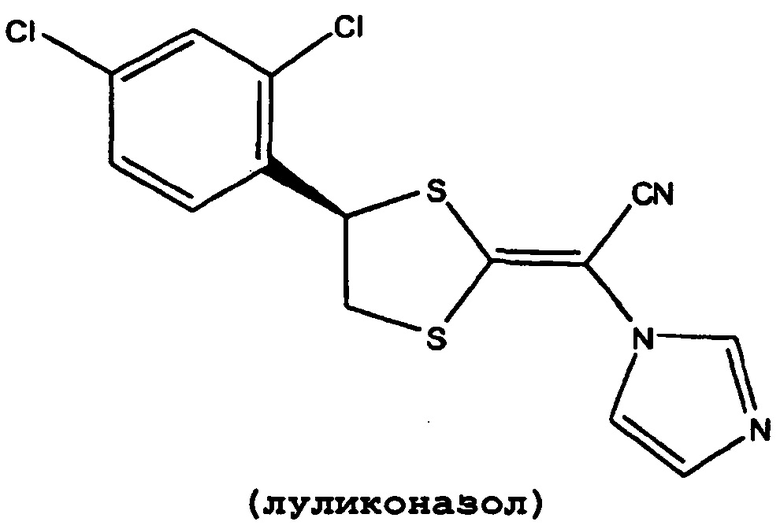
(луликоназол)
Известен способ, в котором луликоназол в качестве активного ингредиента получают, осуществляя перекристаллизацию из этилацетата и н-гексана (см., например, патентный документ 7). Тем не менее, совсем ничего не известно о перекристаллизации из спирта или о любой стадии, на которой к активному ингредиенту добавляют спирт. Таким образом, подтверждается, что в настоящее время ничего не известно о кристаллическом веществе, содержащем спирт с короткой цепью, и композиции активного фармацевтического ингредиента.
Технические документы предшествующего уровня техники
Патентные документы:
Патентный документ 1: WO 2007/102241;
Патентный документ 2: WO 2007/102242;
Патентный документ 3: WO 2007/102243;
Патентный документ 4: WO 2009/031642;
Патентный документ 5: WO 2009/031643;
Патентный документ 6: WO 2009/031644;
Патентный документ 7: JP9-100279A.
Сущность изобретения
Техническая проблема
Настоящее изобретение осуществлено с учетом вышеуказанных обстоятельств и его объектом является разработка способов улучшения растворимости луликоназола с целью улучшения стабильности фармацевтического препарата.
Решение проблемы
Принимая во внимание вышеуказанные обстоятельства, авторы настоящего изобретения провели многочисленные кропотливые исследования и приложили множество усилий, с целью отыскать средства для улучшения растворимости луликоназола, так чтобы стабильность фармацевтического препарата улучшилась. В результате было обнаружено, что подобным свойством обладает кристаллическое вещество, содержащее спирт с короткой цепью, и композиция активного фармацевтического ингредиента, и таким образом было осуществлено настоящее изобретение. Итак, сущность или отличительные признаки настоящего изобретения заключаются в следующем.
1. Кристаллическое вещество, включающее луликоназол, представленный следующей формулой, и спирт с короткой цепью, имеющий от 1 до 4 атомов углерода:
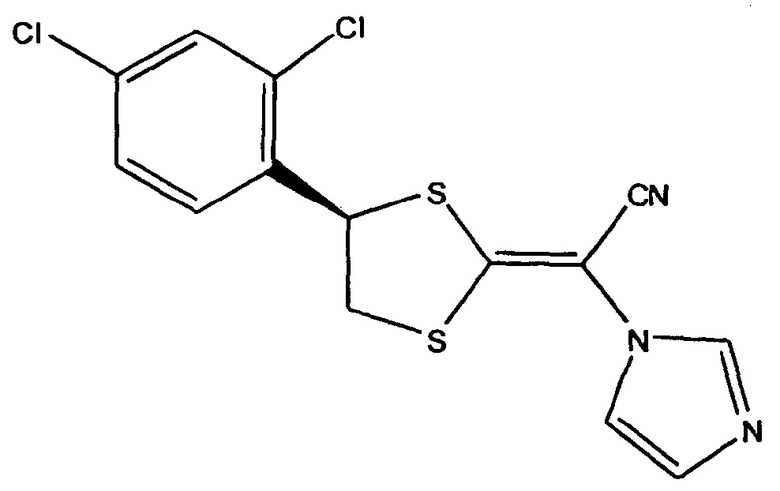
(луликоназол)
2. Кристаллическое вещество, как определено в п. 1, в котором содержание спирта с короткой цепью составляет от 100 до 10000 частей на миллион (ч/млн) по отношению к общему количеству кристаллического вещества.
3. Кристаллическое вещество, как определено в п. 1 или 2, в котором спиртом с короткой цепью является этанол.
4. Кристаллическое вещество, как определено в любом из пп. 1-3, в котором кристаллическое вещество получают перекристаллизацией вместе со спиртом с короткой цепью, который может содержать воду, с последующей сушкой и добавлением, если это необходимо, спирта с короткой цепью.
5. Композиция активного фармацевтического ингредиента, содержащая кристаллическое вещество, как определено в любом из пп. 1-4.
<6> Фармацевтический препарат, полученный путем смешивания композиции активного фармацевтического ингредиента, как определено в п. 5.
7. Способ получения фармацевтического препарата, включающий стадию растворения в растворителе кристаллического вещества, как определено в любом из пп. 1-4, или композиции активного фармацевтического ингредиента, как определено в п. 5.
8. Фармацевтический препарат, полученный по способу, как определено в п. 7.
Полезность настоящего изобретения
В соответствии с настоящим изобретением, могут быть разработаны способы улучшения растворимости луликоназола.
Краткое описание чертежей
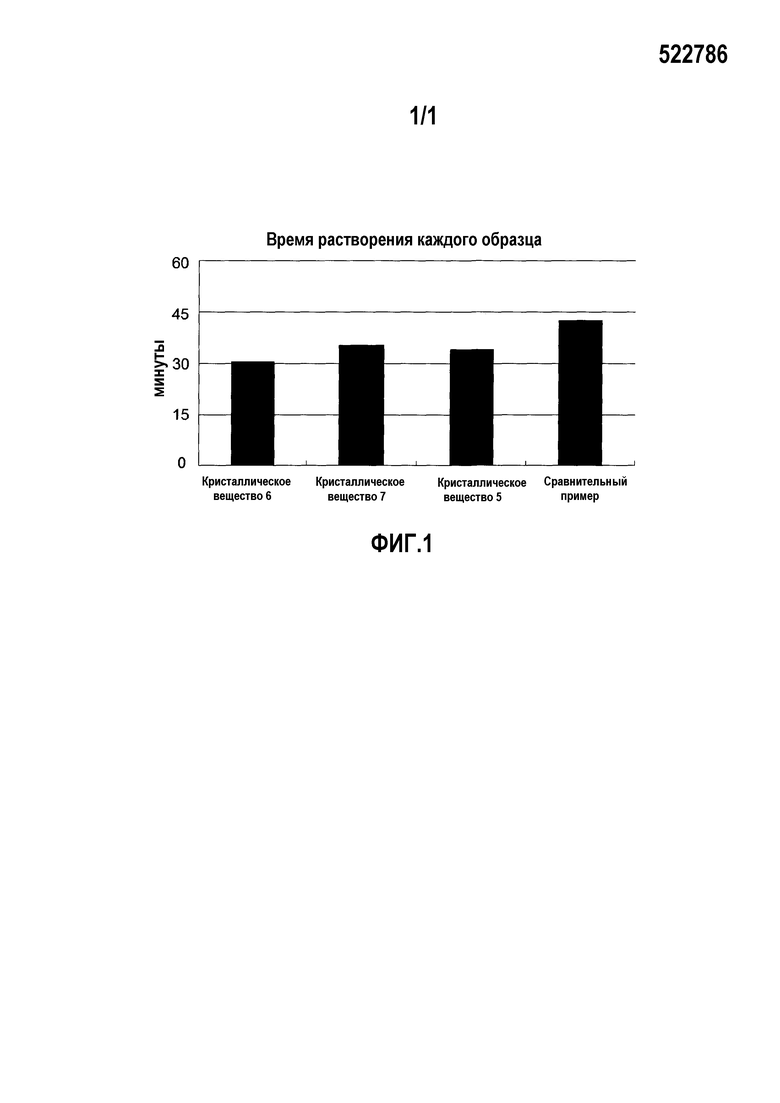
На фиг. 1 показаны результаты испытаний растворимости для кристаллического вещества по примерам и кристаллического вещества из сравнительного примера.
Описание вариантов осуществления изобретения
1. Кристаллическое вещество по настоящему изобретению
Кристаллическое вещество по настоящему изобретению отличается тем, что кристаллическое вещество содержит луликоназол и спирт с короткой цепью. Другими словами, кристаллическое вещество по настоящему изобретению можно также назвать композитом кристаллического вещества (комплексом), содержащим луликоназол и спирт с короткой цепью, или матрицей кристаллического вещества, содержащей луликоназол и спирт с короткой цепью. В данном описании указанные термины используются как синонимы, и каждый вариант, представленный указанными терминами, включен в объем настоящего изобретения.
В качестве предпочтительного примера вышеописанного спирта с короткой цепью можно привести, спирт, имеющий неразветвленную цепь или боковую цепь и содержащий от 1 до 4 атомов углерода, такой как метанол, этанол, изопропиловый спирт и бутанол [например, метанол, этанол, 1-пропанол (пропиловый спирт), 2-пропанол (изопропиловый спирт), 1-бутанол (н-бутиловый спирт), 2-бутанол (втор-бутиловый спирт), 2-метил-1-пропанол (изобутиловый спирт) и 2-метил-2-пропанол (трет-бутиловый спирт)]. В частности, предпочтительно, используют этанол. Кристаллическое вещество может содержать два или несколько спиртов, которые выбраны из вышеуказанных спиртов. По следующей причине содержание спирта с короткой цепью, как указано выше, предпочтительно, составляет от 100 до 10000 ч/млн и, более предпочтительно, составляет от 500 до 5000 ч/млн от общей массы кристаллического вещества. Так, если содержание спирта слишком мало, то эффект улучшения растворимости в некоторых случаях не проявляется. Если содержание спирта слишком велико, то в некоторых случаях устойчивость кристаллического вещества в целом ухудшается. Содержание луликоназола, предпочтительно, составляет не менее чем 95% масс. и, более предпочтительно, составляет не менее чем 99% масс. по отношению к общей массе кристаллического вещества.
Описанное выше кристаллическое вещество можно получить, например, перекристаллизацией луликоназола совместно со спиртом, имеющим короткую цепь, который может содержать воду, отделением кристаллического вещества путем фильтрации, сушкой кристаллического вещества в токе газа, при этом сохраняют требуемое содержание спирта с короткой цепью, измеряя количество спирта с короткой цепью и добавляя спирт с короткой цепью, если количество спирта с короткой цепью выходит за пределы предпочтительного диапазона. С другой стороны, если количество спирта с короткой цепью слишком велико, то регулирование можно осуществить дальнейшей сушкой в токе газа.
Перекристаллизацию можно осуществлять, используя спирт, либо содержащий воду, либо воду можно использовать в качестве плохого растворителя. Способ с плохим растворителем представляет собой способ, при котором воду, количество которой достаточно, чтобы вызвать осаждение, добавляют к спиртовому раствору, содержащему луликоназол. В предпочтительном варианте осуществления настоящего изобретения перекристаллизацию осуществляют, используя спирт, содержащий 10% воды, что является предпочтительным способом с точки зрения чистоты конечного продукта.
Перекристаллизацию можно осуществить любым обычным способом перекристаллизации.
Можно использовать вышеуказанный спирт вместе с водой. В качестве альтернативы, вышеуказанный спирт может заранее содержать воду. В обоих случаях количество используемой воды, предпочтительно, составляет, например, от 9 до 80%, от 30 до 80%, от 50 до 75% или приблизительно максимум 70% от общего количества спирта, который может содержать воду.
2. Композиция активного фармацевтического ингредиента по настоящему изобретению
Композиция активного фармацевтического ингредиента по настоящему изобретению может содержать вещества, примеси и изомеры в допустимых пределах в качестве активного фармацевтического ингредиента, отличного от луликоназола и спирта с короткой цепью. Тем не менее, наиболее предпочтительна для применения такая форма, при которой композиция состоит практически из луликоназола и спирта с короткой цепью.
Кристаллическое вещество по настоящему изобретению и композиция активного фармацевтического ингредиента, полученные как описано выше, обладают превосходной растворимостью в растворителе. Таким образом, кристаллическое вещество по настоящему изобретению и композиция активного фармацевтического ингредиента способны подавлять, например, образование любого изомера при получении фармацевтического препарата при проведении стадий, включающих стадию растворения. Таким образом, кристаллическое вещество по настоящему изобретению и композиция активного фармацевтического ингредиента могут быть использованы в качестве исходного вещества для получения указанного выше фармацевтического препарата.
3. Фармацевтический препарат по настоящему изобретению
Фармацевтический препарат по настоящему изобретению отличается тем, что он содержит вышеуказанное кристаллическое вещество по настоящему изобретению или композицию активного фармацевтического ингредиента. Вышеуказанное кристаллическое вещество или композиция активного фармацевтического ингредиента обладает превосходной растворимостью в таком растворителе, как этанол и т.п. Таким образом, желательно применять фармацевтический препарат, который получают по способу, который включает стадию растворения. В частности, возможно представить в качестве предпочтительного примера, например, фармацевтический препарат в виде раствора, фармацевтический препарат в виде эмульсии, фармацевтический препарат в виде мази типа жидкокапельной дисперсии. В частности, для приготовления фармацевтического препарата, в котором содержание луликоназола превышает 5% масс., требуется значительное время для осуществления стадии растворения. Таким образом, фармацевтический препарат по настоящему изобретению является предпочтительным с точки зрения сокращения или уменьшения времени растворения. Предпочтительное содержание луликоназола составляет от 0,1 до 30% масс. от общего количества фармацевтического препарата. Более предпочтительно, содержание луликоназола составляет от 0,5 до 15% масс. Таким образом, в том случае, когда фармацевтический препарат изготавливают в виде средства для перорального введения, такого как таблетка или т.п., скорость растворения превосходная, что является предпочтительным. Вышеуказанный фармацевтический препарат для перорального введения также принадлежит к фармацевтической композиции по настоящему изобретению.
Время, необходимое для проведения стадии растворения, зависит, например, от технологических условий (условий обработки), а также от содержания луликоназола в фармацевтическом препарате. Тем не менее, время, необходимое для проведения стадии растворения, которое требуется, если кристаллическое вещество по настоящему изобретению или композицию активного фармацевтического ингредиента используют на стадии растворения для приготовления, например, фармацевтического препарата, в котором содержание луликоназола составляет от 0,1 до 30% масс. от общего количества фармацевтического препарата, может быть не больше чем 80%, предпочтительно, не больше чем 75% и, более предпочтительно, не больше чем 70%, по сравнению со временем, которое необходимого для проведения стадии растворения при использовании любого обычного доступного луликоназола.
Фармацевтический препарат по настоящему изобретению можно получить, осуществляя способ или проводя обработку в соответствии с любым обычным способом, включающим, например, добавление к фармацевтическому препарату растворителя, красителя, антиоксиданта, хелатирующего агента, эмульгатора/диспергатора, солюбилизирующего агента, разрыхлителя, эксципиента, связующего вещества, агента для формирования покрытий и агента для коррекции вкуса/запаха, которые отличны от кристаллического вещества по настоящему изобретению или композиции активного фармацевтического ингредиента.
Фармацевтический препарат луликоназола по настоящему изобретению, полученный, как описано выше, отличается тем, что подавляется количество изомеров, по сравнению с исходными значениями, полученными сразу же после приготовления луликоназола. Количества изомеров (SE-изомера, Z-изомера), которые образуются, по сравнению с начальными значениями, полученными сразу же после получения луликоназола, могут быть такими же, как и в том случае, когда кристаллическое вещество, имеющее такую форму кристаллизации, что плоскость (11-1) является специфической поверхностью роста, получают обычными способами, например, по способу перекристаллизации из смеси н-гексан-этилацетат. Так, например, в случае SE-изомера, количество изомера может быть не больше чем 80%, предпочтительно, не больше чем 70% и, более предпочтительно, не больше чем 60%. В случае Z-изомера, количество изомера составляет не больше чем 70%, предпочтительно, не больше чем 60% и, более предпочтительно, не больше чем 50%. Что касается суммарного количества указанных SE-изомера и Z-изомера, то указанное суммарное количество может быть не больше чем 80%, предпочтительно, не больше чем 70% и, более предпочтительно, не больше чем 60%.
Высока вероятность того, что вышеуказанные изомеры, могут быть, в частности, получены на стадии растворения в растворителе. Таким образом, кристаллическое вещество по настоящему изобретению или композиция активного фармацевтического ингредиента являются наиболее предпочтительными в качестве активного ингредиента фармацевтического препарата лекарственного средства, который получают, осуществляя при этом описанную выше стадию.
Фармацевтический препарат или фармацевтическую композицию по настоящему изобретению, преимущественно, применяют для терапии или для лечения заболевания, вызванного любым грибком, или для предотвращения ухудшения заболевания, используя свойства луликоназола. Фармацевтический препарат по настоящему изобретению, преимущественно, используется также для лечения заболевания, вызванного любыми простейшими, такими как влагалищная трихомонада, или для предотвращения ухудшения заболевания. Примером заболевания, вызванного любыми грибками, может быть дерматофития стоп, такая как эпидермофития стопы, дерматофития туловища, такая как кандидоз и отрубевидный лишай, и трихофития твердой части рогового вещества, такая как грибковое поражение ногтей. Наиболее предпочтительно использовать фармацевтический препарат или фармацевтическую композицию по настоящему изобретению для лечения заболевания твердой части рогового вещества, такого как грибковое поражение ногтей, поскольку они оказывают замечательный эффект. Эффект фармацевтической композиции по настоящему изобретению наиболее ярко проявляется на ногтях. Тем не менее, указанное действие оказывается также на любой обычный дерматомикоз. Таким образом, фармацевтическая композиция, которая направлена на дерматомикоз и которая составляет сущность настоящего изобретения, также входит в технический объем настоящего изобретения. Примером вышеуказанного дерматомикоза может быть дерматофития стоп и распространение трихофитии в веществе рогового типа, при этом распространение трихофитии в веществе рогового типа, например, на пятке, включено в дерматофитию стоп. Что касается вышеуказанного дерматомикоза, то предпочтительно применять фармацевтический препарат против трихофитии, распространяющейся в веществе рогового типа, на которую обычные средства или лекарственные средства почти не оказывают воздействия, потому что эффект от настоящего изобретения весьма заметен.
Способ применения может быть соответствующим образом выбран с учетом, например, массы тела, возраста, пола, симптомов заболевания или состояния пациента. Однако в обычных случаях взрослому человеку луликоназол, предпочтительно, назначают в количестве от 0,01 до 1 г в день. Можно сослаться на количество использованного луликоназола, которое обычно применяют против заболевания, вызываемого любыми грибами.
Например, в случае любого препарата для наружного применения, можно привести пример применения соответствующего количества препарата для лечения заболевания один или несколько раз в день. Желательно, чтобы вышеописанное лечение осуществлялось ежедневно. В частности, в случае грибкового поражения ногтей, луликоназол в качестве активного ингредиента может быть нанесен в ноготь в таком количестве, которое не может быть доставлено с помощью любого обычного фармацевтического препарата. Таким образом, грибковое поражения ногтей можно лечить только с помощью наружного применения, не используя противогрибковое средство в течение длительного периода времени. Кроме того, в случае грибкового поражения ногтей повторное заражение и повторное инфицирование вызывает большие проблемы. Тем не менее, можно избежать указанного повторного заражения и повторного инфицирования за счет назначения фармацевтической композиции по настоящему изобретению в течение 1-2 недель после исчезновения симптомов. В подобной схеме назначения лекарственного средства фармацевтическая композиция по настоящему изобретению оказывает превентивное действие.
ПРИМЕРЫ
Настоящее изобретение более подробно поясняется с помощью примеров. Тем не менее, настоящее изобретение не ограничивается приведенными ниже примерами.
Пример 1
Луликоназол, который получают перекристаллизацией из смеси этилацетата и н-гексана, используют для проведения перекристаллизации из этанола, содержащего 10% воды. Кристаллическое вещество собирают фильтрованием, а затем сушат в эксикаторе с пентаоксидом фосфора. Содержание этанола в образце определяют с помощью газовой хроматографии. В результате обнаружено, что содержание этанола составляет 3500 ч/млн, т.е. образец содержит этанол. Таким образом, подтверждено, что указанный образец представляет собой кристаллическое вещество (кристаллическое вещество 1) по настоящему изобретению. Содержание этанола в луликоназоле (исходное вещество 1), который является исходным сырьем для кристаллического вещества по настоящему изобретению и который получают перекристаллизацией из этилацетата и н-гексана, не превышает предел обнаружения.
Рентгеноструктурный анализ монокристалла проводят для кристаллического вещества 1 по настоящему изобретению (название прибора: RU-H2R, производитель: Rigaku Corporation, условия: источник рентгеновского излучения: линия CuKα, температура измерения: 26°С, напряжение трубки: 50 кВ, ток трубки: 180 мА, 2θmax: 150,0°, метод структурного анализа: прямой метод (SHELX 86)). Кристаллическая система, пространственная группа, постоянная решетки и коэффициент R, которые получают из измеренных значений, представлены ниже.
Кристаллическая система: моноклинная
Пространственная группа: P21
Постоянная решетки:
a=9,0171 (9) Å
b=8,167 (1) Å
c=10,878 (1) Å
β=95,917 (9)°
коэффициент R:
R=0,046
Rw=0,047
Пример 2
Тест на элюирование (условия перемешивания: 50 об./мин) проводят для исходного вещества 1 (кристаллическое вещество из сравнительного примера) и кристаллического вещества 1 из примера 1, чтобы исследовать динамику элюирования. После подтверждения растворения всех кристаллических веществ, Z-изомер и SE-изомер, которые представляют собой изомеры, полученные в растворе, анализируют и количественно определяют с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ).
При проведении теста на элюирование в качестве растворителя используют 500 мл безводного этанола, в котором при комнатной температуре и при перемешивании растворяют 1 г образца, и одновременно измеряют время, которое требуется для растворения. Результаты представлены в таблице 1. Таким образом, видно, что время, которое требуется для растворения, мало для кристаллического вещества 1 и, таким образом, образование Z-изомера и SE-изомера на стадии растворения подавляется.
Условия проведения ВЭЖХ следующие. Колонка: CHIRALCEL OD-RH 4,6×150 мм, температура колонки: 35°С, подвижная фаза: раствор смеси метанола/2%-ного водного раствора гексафторфосфата калия (85:15, об./об.), скорость потока: 0,6 мл/мин, детектирование: 295 нм).
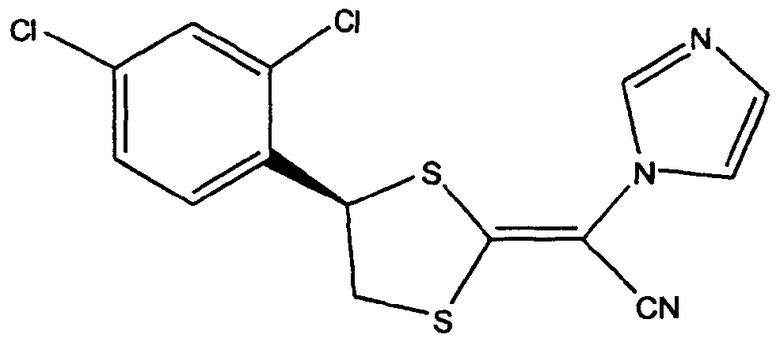
(Z-изомер)
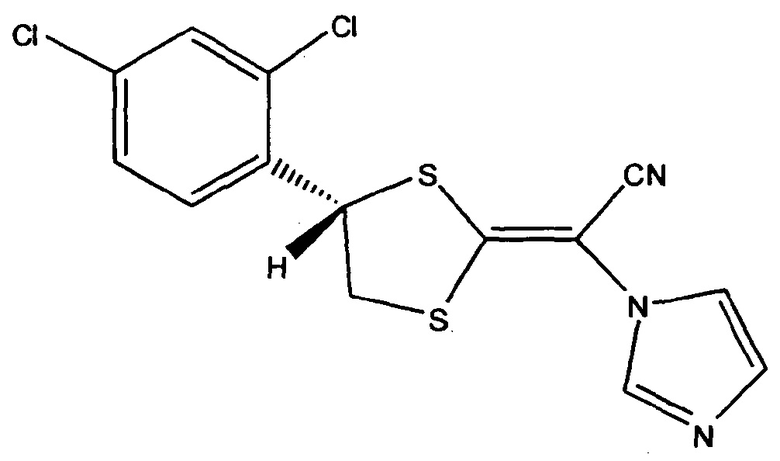
(SE-изомер)
Пример 3
Измеряют содержание спирта в образцах кристаллического вещества (кристаллические вещества 2, 3), полученных путем изменения условий проведения перекристаллизации в примере 1, и результат их растворения в этаноле наблюдают невооруженным глазом. Результаты представлены в таблице 2. Кристаллические вещества 2 и 3 представляют собой кристаллические вещества по настоящему изобретению, и их способность к растворению также удовлетворительна. Таким образом, понятно, что растворимость значительно улучшается, когда этанол содержится в количестве не менее чем 1000 ч/млн
Пример 4
Фармацевтический препарат (жидкий препарат) изготавливают с использованием кристаллического вещества 1 по настоящему изобретению. Так, компоненты состава нагревают, перемешивают и растворяют. После подтверждения растворения проводят быстрое охлаждение при перемешивании и получают фармацевтический препарат по настоящему изобретению. Время, необходимое для растворения, составляет не более 5 мин. Для данного образца определяют количество Z-изомера и SE-изомера. Содержание Z-изомера не превышает предел обнаружения, а содержание SE-изомера составляет 0,03%. Было подтверждено, что приготовление препарата проведено успешно без ухудшения стабильности.
Пример 5
Определяют содержание спирта в кристаллическом веществе 4, полученном путем изменения условий перекристаллизации в примере 1, и результат растворения в этаноле сравнивают также с результатами для кристаллического вещества по сравнительному примеру в примере 1 и для кристаллического вещества 3 с тем, чтобы сопоставить их растворимость.
Кристаллическое вещество 4 получают следующим образом. Так, 150 мл этанола добавляют к 5 г луликоназола, а затем кипятят с обратным холодильником и растворяют. Медленно при перемешивании охлаждают до достижения температуры 70°С, и выдерживают при этой температуре в течение 20 мин. Затем к полученной смеси добавляют 20 мл воды, перемешивают и охлаждают. Выпавшие кристаллы отделяют фильтрованием, после чего их сушат в течение 48 часов в токе газа при температуре 30°C и получают кристаллическое вещество 4 по настоящему изобретению. Содержание этанола в данном образце составляет 262 ч/млн. Что касается способности к растворению, то в сравнении со сравнительным примером <<кристаллическое вещество 4<кристаллическое вещество 3. Следует понимать, что эффект настоящего изобретения обеспечивается в случае кристаллического вещества 4. В соответствии с этим авторы настоящего изобретения полагают, что значение нижнего допустимого предела для спирта составляет 100 ч/млн.
Пример 6
Определяют содержание спирта в кристаллическом веществе 5, полученном путем изменения условий перекристаллизации в примере 1, и результат растворения в этаноле сравнивают также с результатами для кристаллического вещества по сравнительному примеру в примере 1 и для кристаллического вещества 2 с тем, чтобы сопоставить их растворимость.
Кристаллическое вещество 5 получают следующим образом. Так, 150 мл этанола добавляют к 5 г луликоназола, а затем кипятят с обратным холодильником и растворяют. Медленно при перемешивании охлаждают до достижения температуры 80°С, и выдерживают при этой температуре в течение 5 мин. Затем к полученной смеси медленно добавляют 15 мл воды, перемешивают и охлаждают. Выпавшие кристаллы отделяют фильтрованием, после чего их сушат в течение 24 часов в токе газа при температуре 30°C и получают кристаллическое вещество 5 по настоящему изобретению. Содержание этанола в данном образце составляет 7029 ч/млн. Что касается способности к растворению, то в сравнении со сравнительным примером <<кристаллическое вещество 2 = кристаллическое вещество 5.
Пример 7
Определяют содержание спирта в кристаллическом веществе 6, полученном путем изменения условий перекристаллизации в примере 1, и результат растворения в этаноле сравнивают также с результатами для кристаллического вещества по сравнительному примеру в примере 1, для кристаллического вещества 4 и для кристаллического вещества 3 с тем, чтобы сопоставить их растворимость.
Кристаллическое вещество 6 получают следующим образом. Так, 200 мл этанола добавляют к 5 г луликоназола, а затем кипятят с обратным холодильником и растворяют. Медленно при перемешивании охлаждают до достижения температуры 70°С и выдерживают при этой температуре в течение 10 мин. Затем к полученной смеси медленно добавляют 10 мл воды, перемешивают и охлаждают. Добавляют еще 10 мл воды и выпавшие кристаллы отделяют фильтрованием, после чего их сушат в течение 48 часов в токе газа при температуре 30°C и получают кристаллическое вещество 6 по настоящему изобретению. Содержание этанола в кристаллическом веществе 6 составляет 403 ч/млн. Что касается способности к растворению, то в сравнении со сравнительным примером <<кристаллическое вещество 4 = кристаллическое вещество 6 <кристаллическое вещество 3.
Пример 8
Определяют содержание спирта в кристаллическом веществе 7, полученном путем изменения условий перекристаллизации в примере 1, и результат растворения в этаноле сравнивают также с результатами для кристаллического вещества по сравнительному примеру в примере 1 и для кристаллического вещества 5 с тем, чтобы сопоставить их растворимость.
Кристаллическое вещество 7 получают следующим образом. Так, 200 мл 90%-ного водного раствора этанола добавляют к 5 г луликоназола, а затем кипятят с обратным холодильником и растворяют. Медленно при перемешивании охлаждают до достижения температуры 80°С, и выдерживают при этой температуре в течение 5 мин. Затем к полученной смеси медленно добавляют 15 мл воды, перемешивают и охлаждают. Выпавшие кристаллы отделяют фильтрованием, после чего их сушат в течение 24 час в токе газа при температуре 30°C и получают кристаллическое вещество 7 по настоящему изобретению. Содержание этанола в кристаллическом веществе составляет 4116 ч/млн. Что касается способности к растворению, то в сравнении со сравнительным примером <<кристаллическое вещество 5 = кристаллическое вещество 7.
Из результатов по примерам 1, 3 и 5-7 видно, что образец с большим содержанием спирта, который входит в состав кристаллического вещества по настоящему изобретению, получают путем добавления плохого растворителя при высокой температуры и путем проведения перекристаллизации в соответствии со способом, предусматривающим использование плохого растворителя (пример 6). Кроме того, также видно, что наблюдается тенденция к увеличению содержания спирта, когда влияние от добавления плохого растворителя смягчается (пример 8). Следует также понимать, что содержание алкоголя приблизительно равно нижнему предельному значению, когда перекристаллизацию осуществляется в смеси спирт/вода с большим содержанием воды или когда перекристаллизацию осуществляют, добавляя плохой растворитель при низкой температуре (примеры 5, 7).
Пример 9
Растворимость исследуют на основе способа примера 2 для кристаллических веществ 5-7 и кристаллического вещества из сравнительного примера (условия перемешивания: 200 об./мин). Время, необходимое для растворения, показано на фиг. 1. Таким образом, видно, что любое из кристаллических веществ по настоящему изобретению обладает лучшей растворимостью, чем кристаллическое вещество из сравнительного примера.
Пример 10
Определяют содержание спирта (содержание спирта, используемого при перекристаллизации) в композиции, полученной путем изменения условий перекристаллизации в примере 1, и результат растворения в этаноле сравнивают невооруженным глазом. Результаты приведены в таблице 4.
Кристаллическое вещество 8 перекристаллизовывают по приведенной ниже методике. Так, 150 мл этанола добавляют к 10 г луликоназола, а затем нагревают до достижения температуры 60°С и растворяют при перемешивании. Добавляют 50 мл воды, заранее нагретой до 70°C с последующим перемешиванием и смешиванием веществ. Кристаллы осаждаются при перемешивании в процессе охлаждения в охлажденной до 5°C воде, после чего выдерживают в течение 30 мин. Затем кристаллы отделяют фильтрованием, сушат в течение 48 часов в токе газа при температуре 40°С и получают кристаллическое вещество 8 по настоящему изобретению. Кристаллическое вещество 9 получают по той же методике, что и приведенная выше методика, за исключением того, что 50 мл метанола добавляют к 10 г луликоназола и к полученному раствору добавляют 150 мл воды. Кристаллическое вещество 10 получают по той же методике, что и приведенная выше методика, за исключением того, что 100 мл метанола добавляют к 10 г луликоназола и к полученному раствору добавляют 100 мл воды. Кристаллическое вещество 11 получают по той же методике, что и приведенная выше методика, за исключением того, что 200 мл 2-пропанола добавляют к 10 г луликоназола, а воду не добавляют. Все кристаллические вещества являются кристаллическими веществами по настоящему изобретению, при этом их способность к растворению также удовлетворительна. Таким образом, понятно, что растворимость значительно улучшается, когда спирт, имеющий от 1 до 4 атомов углерода, содержится в количестве не менее чем 500 ч/млн, более предпочтительно, не менее чем 1000 ч/млн
Пример 11
Действие активного ингредиента, содержащего спирт, исследуют с использованием кристаллического вещества 10. В качестве сравнительного примера (сравнительного кристаллического вещества) используют кристаллическое вещество, которое получают перекристаллизацией из смеси этилацетата и н-гексана и которое не содержит спирт. Прямое действие луликоназола исследуют на примере влагалищной трихомонады (клинически изолированного штамма). Готовят образцы следующим образом: 5,08 мг сравнительного кристаллического вещества добавляют в "среду трихомонады F" (Fuji Pharma), 5,08 мг кристаллического вещества 10 добавляют в указанную среду и 5 мкл воды добавляют в указанную среду (контроль). 200 мл культурального раствора, содержащего 3,93×105 клеток/мл влагалищной трихомонады, добавляют к каждому из образцов, после чего культивируют в течение 4 дней при температуре 37°С. После этого клетки трихомонады подсчитывают с помощью гемоцитометра. Результаты приведены в таблице 5. Существенное различие указанных трех образцов подтверждают при критическом значении не более чем 1%. Из полученных результатов понятно, что кристаллическое вещество по данному изобретению обладает превосходным антипротозойным действием.
Пример 12
В соответствии с составом, приведенным в таблице 6, готовят таблетку и измеряют ее твердость. В качестве измерительного устройства для определения твердости используют PTB311 (Pharma Test GmbH). Условия таблетирования следующие: давление таблетирования 1 тонна/см2 с использованием пестика и ступки диаметром 9 мм. Сравнительный пример готовят по той же самой описанной выше методике с использованием сравнительного кристаллического вещества. В таблице 7 приведены средние значения для 6 таблеток каждого образца. Из приведенных результатов следует, что кристаллическое вещество по настоящему изобретению обладает высокой твердостью и великолепной физической стабильностью. Таким образом, можно приготовить таблетку, имеющую высокую твердость, с использованием активного ингредиента, содержащего спирт, поскольку содержащий спирт активный ингредиент обладает сильным сродством к активным ингредиентам.
Применимость в промышленности
Настоящее изобретение может быть использовано при получении фармацевтических препаратов.
Изобретение относится к комплексу кристаллического луликоназола и спирта с короткой цепью, имеющего от 1 до 4 атомов углерода, где содержание спирта с короткой цепью составляет от 262 до 7029 м.д. по отношению к общему количеству комплекса
Комплекс применяют для лечения грибка. 5 н. и 2 з.п. ф-лы, 1 ил., 7 табл., 12 пр.
1. Комплекс кристаллического вещества, состоящий из луликоназола, представленного следующей формулой, и спирта с короткой цепью, имеющего от 1 до 4 атомов углерода, где содержание спирта с короткой цепью составляет от 262 до 7029 м.д. по отношению к общему количеству комплекса кристаллического вещества
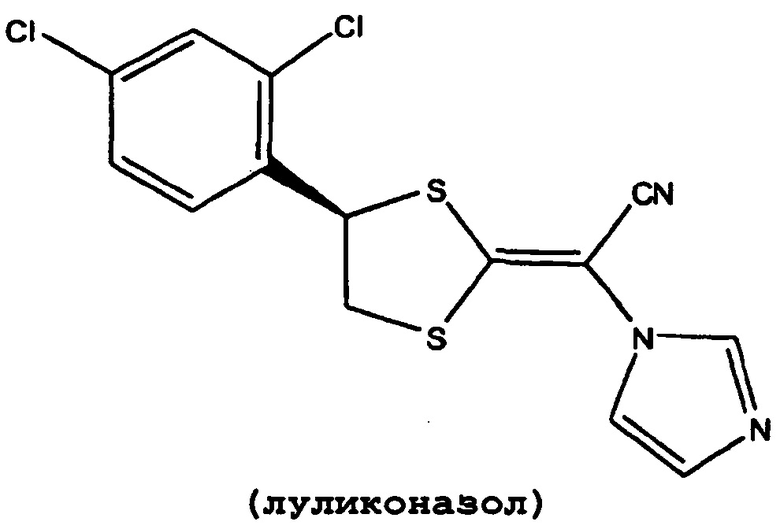
2. Комплекс кристаллического вещества по п. 1, где спиртом с короткой цепью является этанол.
3. Комплекс кристаллического вещества по п. 1 или 2, где комплекс кристаллического вещества получают перекристаллизацией со спиртом с короткой цепью, который может содержать воду, с последующей сушкой и добавлением, в случае необходимости, спирта с короткой цепью.
4. Композиция для получения фармацевтического препарата для терапии или лечения заболевания, вызванного грибком, или для предотвращения ухудшения заболевания, содержащая комплекс кристаллического вещества по любому из пп. 1-3 и по меньшей мере одно, выбранное из группы, состоящей из вещества, примеси и изомера в допустимых пределах в качестве активного фармацевтического ингредиента.
5. Фармацевтический препарат для терапии или лечения заболевания, вызванного грибком, или для предотвращения ухудшения заболевания, полученный путем смешивания композиции по п. 4 и содержащий от 0,1 до 30 мас.% луликоназола от общего количества фармацевтического препарата и по меньшей мере одно, выбранное из группы, состоящей из растворителя, красителя, антиоксиданта, хелатирующего агента, эмульгатора/диспергатора, солюбилизирующего агента, разрыхлителя, эксципиента, связующего вещества, агента для формирования покрытий и агента для коррекции вкуса/запаха.
6. Способ получения фармацевтического препарата, включающий стадию растворения в фармацевтически приемлемом растворителе комплекса кристаллического вещества по любому из пп. 1-3 или композиции по п. 4.
7. Фармацевтический препарат для терапии или лечения заболевания, вызванного грибком, или для предотвращения ухудшения заболевания, полученный по способу п. 6 и содержащий от 0,1 до 30 мас.% луликоназола от общего количества фармацевтического препарата.
| WO 2007102241,A1, 13.09.2007 | |||
| WO 1997002821,A2,30.01.1997 | |||
| RU 2008139904,A,20.04.2010. |
Авторы
Даты
2017-06-19—Публикация
2013-09-06—Подача