Изобретение относится к медицине, а именно к комбинированному составу, содержащему в качестве действующих веществ (RS)-2-(2-оксо-4-фенилпирролидин-1-ил)ацетамид и (3aS)-2-[(3S)-1-азабицикло-[2.2.2]окт-3-ил]2,3,3а,4,5,6-гексагидро-1-оксо-1Н-бенз[de]изохинолин, обладающему радиопротекторной и противорадиационной, антиэметической (антиэметогенной), антидиспепсической, антитоксической, антигипокинезической, противоадинамической, антиастеической, антидепрессивной мнемотропной и ноотропной активностью.
В условиях роста онкологических заболеваний и техногенных катастроф, сопровождающихся в том числе массовым химическим и радиационным поражениями, актуализируется разработка лекарственных средств, сочетающих в себе такие компоненты медикаментозной защиты, как профилактика или протекция, коррекция и лечение последствий химического и радиационного поражения. При этом полимодальность влияния таких препаратов должна препятствовать проявлению или значимо снижать проявления симптомокомплекса острой химической интоксикации (ОХИ) и острой лучевой болезни (ОЛБ), но не снижать эффективность химио- и радиотерапии (XT и РТ), направленных на блокаду деления атипичных клеток.
XT и РТ проявляются, как правило, симптомокомплексом, который характерен для ОХИ и ОЛБ при техногенных поражениях. Нередко из-за чрезмерной выраженности негативных симптомов, подкрепленных клиническими анализами исследования биологических материалов, приходится не только снижать дозы воздействия XT и РТ, но и прекращать лечение.
Известно, что острый период проявления химической интоксикации и лучевой болезни сопровождается однотипным симптомокомплексом: тошнотой и рвотой, анорексией, диарей, головной болью, быстрой утомляемостью, повышением и понижением температуры тела, слабостью, апатией, снижением показателей физической и психической работоспособности. Уровень и характер выраженности симптоматики при ОХИ и ОЛБ указывают на ту или иную степень заболевания, подразделяющихся на легкую, среднюю, тяжелую и крайне тяжелую. От степени поражения зависят как тактика лечения, так и прогноз последствий, но если при химическом поражении можно вычленить основные механизмы развития патологического состояния и применить средства, способные связывать и ускорять процесс выведения из организма того или иного токсического вещества, то при первичном радиационном облучении (ПРО) и лучевой болезни многообразие механизмов развития патологии чрезвычайно обширно, включая в себя все структуры и функции на клеточном и межклеточном уровнях.
При всем многообразии симптоматических лекарственных средств, антидотов и радиопротекторов пока не достигнуто существенного прорыва в данных областях практической и экстремальной медицины. Недостатком известных антиэметических (антиэметогенных) средств является кратковременность их действия, а также то, что их применение носит профилактический характер - прием препаратов осуществляется до сеанса XT и РТ. Недостатками известных радиопротекторов так же являются кратковременность их действия и низкая эффективность даже у средств с пролонгированным эффектом. При курсовом применении они чаще всего либо не оказывают должного эффекта, либо даже ухудшают состояние, проявляя побочные действия.
Среди антиэметических средств в последнее время получил широкое распространение при XT и РТ палоносетрон (синонимы: палоносетрон гидрохлорид, алокси, оницит) или (3aS)-2-[(3S)-1-азабицикло[2,2,2]окт-3-ил]-2,3,3а,4,5,6-гексагидро-1-оксо-2Н-бенз[de]изохинолин, (CAS No 119904-90-4, 135729-62-2 и 135729-62-3). Молекулы действующего вещества палоносетрон (алокси, оницит) в фармацевтически приемлемой субстанции стабилизированы молекулами гидрохлорида (могут так же применяться иные приемлемые комплексоны), что обеспечивает достаточное стабильное состояние действующего вещества в фармацевтически приемлемой субстанции. Антиэметический эффект палоносетрона связывают с ингибированием 5-НТ3 серотониновых рецепторов.
К достоинствам палоносетрона (палоносетрон гидрохлорид) можно отнести его относительно невысокие эффективные дозы, но перечень недостатков (не рекомендуется прием препарата в течение семи дней с момента проведения сеансов XT и РТ, на его фоне могут развиваться такие явления, как головная боль, головокружение, чувство беспокойства, запор, диарея, нарушения сердечного ритма и др.) препарата указывает на то, что должного прорыва в этой области пока не достигнуто.
Фундаментальное открытие, сформулированное автором (В.И. Ахапкина) в концепцию модуляторно (соразмерное влияние) - дивергентного (расхождение влияния) сопряжения с принципом триггерной трансмиссии, концептуализация модуляции и дивергентная концепция с появлением таких перспективных инновационных классов лекарственных средств как модуляторы с соразмерным влиянием, которое проявляется различными выраженностью и направлением действия в зависимости от того или иного состояния организма и дивергенты с расхождением влияния в зависимости от дозы [1-6] не имеют подтверждения их применения в радиобиологии и радиомедицине, и в химиотерапии.
Родоначальником класса истинных модуляторов (соразмерное влияние) является (RS)-2-(2-оксо-4-фенилпирролидин-1-ил)ацетамид или инновационный Фенотропил [1], содержащий биологически активные изомерные вещества, обладающие конформационной и реверсивной способностями. При всей уникальности открытой у рацемического соединения универсальной ведущей активности, наличия необычайно широкого спектра фармакологических эффектов, его отношения именно с серотонинэргической системой весьма не однозначны [6].
При известности механизмов действия палоносетрона и инновационного Фенотропила, их совместное применение не известно. Предугадать последствия их совместного действия невозможно, так как оно может проявляться конкуренцией и депримирующим влиянием и результат их совместного действия на организм непредсказуем. К тому же влияние Фенотропила при ОХИ (за исключением алкогольной интоксикации, влияния на алкогольную и никотиновую зависимость) и ОЛБ не исследовалось.
Ведущее место в первичной диагностике ОЛБ и ОХИ, а так же в определении степени их тяжести занимает эметический (эметогенный) синдром с проявлением тошноты и рвоты, включая такие признаки как частота рвотной реакции, количество рвотных актов, латентный период первого рвотного акта и продолжительность рвотного периода. Как было указано выше, блокадой эметогенного синдрома удается достичь некоторого временного положительного результата при проявлении симптомов ОЛБ и ОХИ, но эффективность таких препаратов, как правило, длится не более суток, а повторные приемы после терапевтического сеанса либо не обеспечивают необходимого эффекта, либо вовсе не дают положительного результата.
Задачей настоящего изобретения является разработка эффективного лекарственного средства, способного влиять на весь симптомокомплекс ОЛБ и ОХИ. Учитывая, что при ОХИ можно применить конкретные антидоты, в настоящих исследованиях были применены материалы и методы для выявления влияния предлагаемого комбинированного состава при различных дозах поражения животных ионизирующим излучением (ИИ). Как правило, результаты исследований при радиационном поражении имеют положительный эффект и при химическом поражении, а также при проведении радио- и химиотерапии. Пример применения палоносетрона как противорвотного средства при XT и РТ является тому подтверждением.
Технический результат изобретения заключается в достоверном снижении и устранении проявлений симптомов ОЛБ при первичном радиационном облучении (ПРО) животных, пораженных различными дозами ИИ, включая в том числе абсолютно эметогенные и к тому же не локального, а общего поражающего воздействия на организм.
Поставленная задача решается, а технический результат достигается за счет того, что в качестве такого лекарственного средства предлагается комбинированный состав, содержащий (RS)-2-(2-оксо-4-фенилпирролидин-1-ил)ацетамид и (3aS)-2-[(3S)-1-азабицикло-[2.2.2]окт-3-ил]2,3,3а,4,5,6-гексагидро-1-оксо-1Н-бенз[de]изохинолин (далее - комплексный состав или КС), обладающий, как впервые установлено радиопротекторной и противорадиационной активностью с проявлением антиэметической, антидиспепсической, антитоксической, антигипокинезической, противоадинамической, антиастеической, антидепрессивной, мнемотропной и ноотропной активностью.
Изобретение поясняется чертежами, где:
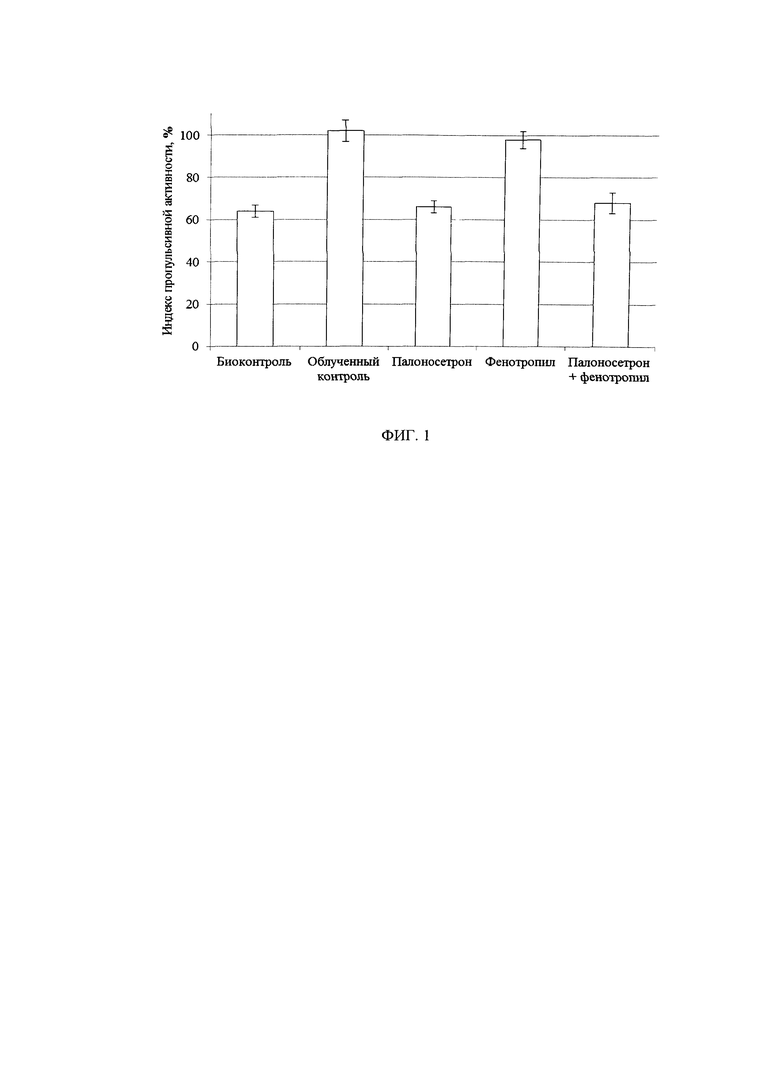
на фиг. 1 показано влияние исследуемых препаратов на индекс пропульсивной активности (ИПА) кишки крыс, облученных в дозе 180 Гр (n=12 в каждой группе),
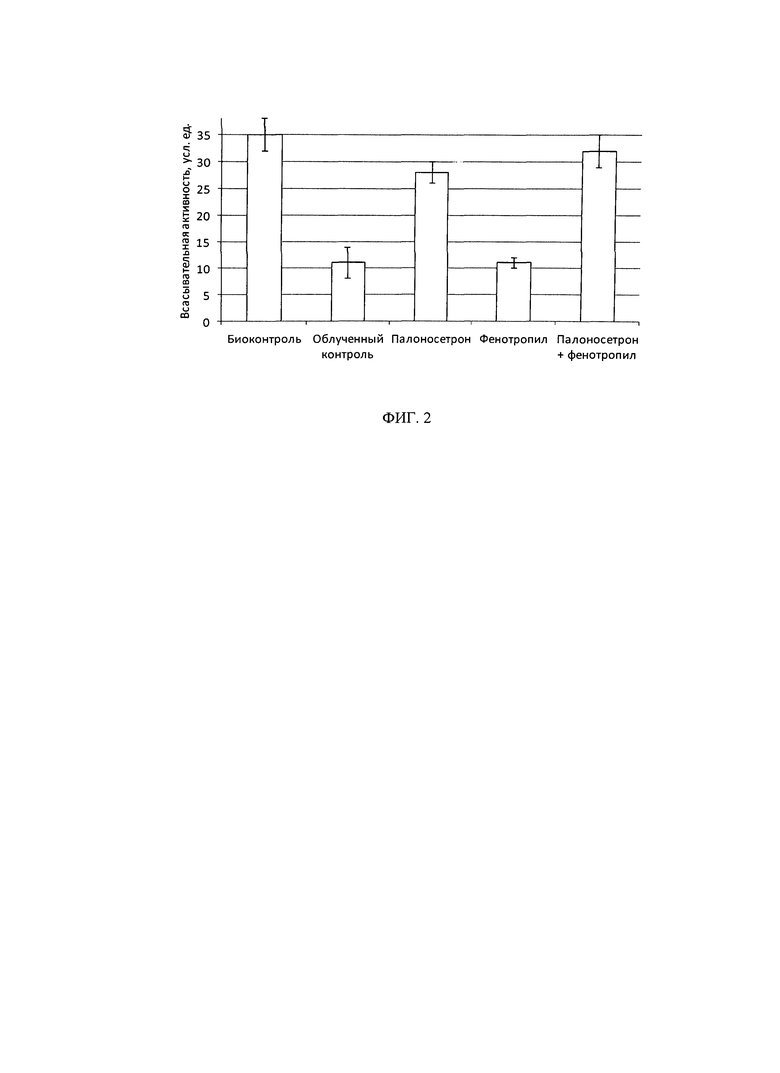
на фиг. 2 показано влияние исследуемых препаратов на всасывательную активности кишки крыс, облученных в дозе 180 Гр (n=12 в каждой группе).
Далее приводятся примеры осуществления изобретения со ссылками на прилагаемые фигуры.
Примеры осуществления изобретения
Материалы и методы
Эксперименты проведены на собаках обоего пола массой 12-18 кг, белых беспородных крысах-самцах массой 180-200 г и на белых беспородных мышах самцах с массой тела 18-20 г. В соответствии с действующими методическими рекомендациями, животных подвергали кратковременному общему равномерному гамма-облучению в дозе 5 Гр для мышей и в абсолютно эметогенных дозах, составляющих 20 и 30 Гр для собак и 180 Гр для крыс [11, 12].
Исследуемые препараты (Фенотропил, палоносетрон и комбинированный состав, содержащий Фенотропил и палоносетрон) в приготовленных (ex tempore) растворах на физиологическом растворе и воде для инъекций вводились в одних случаях за 30 и 60 мин, а в других за 15±5 мин однократно до экспериментального воздействия. В скрининговых исследованиях тестировалось влияние друг на друга входящих в состав КС веществ методом внутривенного титрования путем введения тестируемых доз в хвостовую вену мышам, а также влияние КС на двигательную активность и ориентировочно исследовательское поведение, и профилактическое влияние КС на выживаемость животных, поэтому схема введения препаратов при ПРО соответствовала их фармакокинетическим параметрам. Контрольным группам животных вводились в эквивалентном объеме физиологический раствор и вода для инъекций.
Дозы препаратов рассчитывали с применением коэффициентов межвидового переноса [13] и на основании предварительных (скрининговых) экспериментов. При абсолютно эметогенных дозах ПРО собакам палоносетрон вводили в дозе 0,01 мг/кг, а крысам - 0,03 мг/кг. Фенотропил собакам вводили в дозе из расчета 3,0 мг/кг, крысам - 100 мг/кг. Комбинированный состав содержал в себе указанные выше дозы Фенотропила и палоносетрона для собак и крыс и вводился животным по той же схеме и тем же способом, указанным выше.
О признаках, указывающих на наличие у животных ОЛБ, судили по состоянию контрольной группы животных, находящихся в тех же экспериментальных условиях, что и животные, получавшие исследуемые препараты. Фармакологические эффекты исследуемых препаратов оценивали по их влиянию на отдельные характерологические для ОЛБ симптомы и показатели поведенческих реакций животных в сравнении с животными контрольной группы. При проведении исследований использовали известные общепринятые методы и методические рекомендации [7-15]. Во всех исследованиях за животными наблюдали не менее 6-ти часов после облучения, а при исследовании влияния препаратов на выживаемость наблюдение вели в течение 30-ти суток. При этом изучали:
- влияние веществ друг на друга в КС при тестировании методом внутривенного титрования входящих в состав компонентов в терапевтически приемлемых для них дозах для человека, но в пересчете для животных соответственно в мг/кг;
- влияние препаратов на гипокинезию без воздействия ИИ. Животные подвергались 24 часовой гипокинезии в специальных клетках-пеналах после введения исследуемых веществ и через 24 часа исследовались двигательные реакции и ориентировочно-исследовательское поведение по методике «открытое поле»;
- влияние препаратов на выживаемость мышей и среднюю продолжительность жизни (СПЖ) после воздействия ПРО в дозе 5 Гр. Наблюдение вели в течение 30-ти суток.
- влияние препаратов на эметический синдром (тошнота и рвота) и диарею, а также их влияние на поведенческие реакции. Учитывали количество животных, у которых возникала эметическая реакция (по ее синдромальным показателям) и диарея (по ее синдромальным показателям);
- количественную оценку изменений двигательной активности у животных проводили на основе визуальной регистрации позы животного при отсутствии внешних раздражителей (спонтанная двигательная активность), а также по реакции животных на экспериментатора (вызванная двигательная активность) [11, 9];
- антидиспепсическую активность изучали так же по косвенным показателям, отражающим состояние всасывательной и пропульсивной функции желудочно-кишечного тракта, и по абсолютным показателям - количеству животных с диареей. Всасывательную функцию кишечника оценивали по поступлению уранина в плазму после его перорального введения (5 мг/кг в виде 0,25% раствора натриевой соли флюоресцина) [7]. Содержание уранина в плазме измеряли спустя 30 мин с помощью спектрофлюориметра MPF-3 HITACHI (Япония) при длине волны возбуждения 520 нм и экстинкции 470 нм. Пропульсивную активность кишечника оценивали по скорости продвижения в его просвете 50% стабилизированной суспензии сульфата бария [10]. Рассчитывали индекс пропульсивной активности (ИПА) как отношение длины участка кишечника, заполненного сульфатом бария через 30 мин после его введения, к общей длине кишечника в процентах;
- на наличие антидепрессивной активности указывало отсутствие у животных отказа выполнять заданные экспериментальными условиями действия;
- антигиподинамическое, ноотропное и мнемотропное действие препаратов определяли по изменению двигательной активности животных, по сохранности ориентировочно исследовательского поведения и сохранности норкового врожденного рефлекса крыс в тесте «открытое поле» [8]. Через 5 мин после облучения регистрировали изменения двигательной (по количеству пересеченных квадратов), исследовательской (по количеству норковых реакций) и ориентировочной (по количеству вертикальных стоек) активности крыс при нахождении животных в течение 180 с на открытом пространстве квадратной арены (методика открытого поля) размерами 100×100 см2, разделенной на равные квадраты со стороной 20 см и имеющими в вершинах отверстия диаметром 2 см;
- поведенческую активность изучали по способности животных выполнить заученные тесты: спасение из воды (тест «Избегание плаванием» по Barraco et al., 1978) и передвижение по перекладине (тест «Beam-walking» по Goldstein et al., 1990). Сохранность выполнения заученных тестов указывает на наличие у исследуемых продуктов ноотропной активности, а так же указывает на устранение депрессии (когда животные не отказываются от самоспасения);
- поведенческую активность в тесте «избегание плаванием», который заключается в обучении животного спасаться из воды, используя веревку (выбираясь по ней). Для выполнения теста использовали бассейн диаметром 70 см, в центре которого была подвешена веревка диаметром 1 см. Веревка была закреплена на высоте 1,2 м над поверхностью воды. Регистрировали латентный период выполнения задачи - время от помещения крысы в воду до момента, когда животное полностью забиралось на веревку [14]. Данный тест так же указывает на сохранность обучения и на устранение депрессии (животные не отказываются самоспасаться);
- поведение животных в тесте «Beam-walking», который заключается в обучении животного пересекать перекладину шириной 2,5 см и длиной 122 см, расположенную на высоте 100 см над поверхностью земли. В процессе выполнения теста фиксировали время выполнения теста и степень двигательных нарушений (в баллах от 0 - крыса не в состоянии держаться на перекладине до 6 - крыса пересекла перекладину без соскальзывания лап) [15].
Для выполнения указанных выше тестов, требующих обучения, животных предварительно тренировали, закрепляя навыки обучения в течение 3 суток. Непосредственно перед облучением фиксировали контрольное время выполнения тестов. Следующее тестирование проводили через 5 мин после воздействия ИИ. Для каждого животного вычисляли разницу (Δt) во времени выполнения тестов до и после облучения.
Статистическую обработку данных осуществляли общепринятыми методами. Значимость различий частоты возникновения симптомов оценивали с помощью точного метода Фишера, количественных и временных параметров проявлений ПРО - с помощью анализа Краскела-Уоллиса и метода Манна-Уитни с поправкой Холма. Различия между группами считали статистически значимыми при р≤0,05.
Результаты и их анализ
Пример 1. Предварительные (скрининговые) исследования на мышах показали, что:
- введение в хвостовую вену мышам методом титрования доз КС от 25.025 мг/кг до 500.5 мг/кг (при исходном содержании в КС 500 мг (RS)-2-(2-оксо-4-фенилпирролидин-1-ил)ацетамид и 0.5 мг (3aS)-2-[(3S)-1-азабицикло-[2.2.2]окт-3-ил]2,3,3а,4,5,6-гексагидро-1-оксо-1Н-бенз[de]изохинолин), приготовленного на физиологическом растворе препарата не приводило к развитию токсического действия ни в период введения КС, ни при визуальном наблюдении за мышами в течение 24 и 72 часов после введения препарата;
- внутрибрюшинное введение крысам КС (приготовленного на физиологическом растворе) в дозах 100.25, 200.25 и 300.25 мг/кг за 60 минут до 24-часовой иммобилизации в специальных клетках-пеналах повышало по сравнению с группой опытного контроля показатели двигательной активности и ориентировочно исследовательского поведения по методике открытого поля (исследования проводились через 24 часа иммобилизации) при том, что группы животных без препарата (получали физиологический раствор) имели существенно более низкие показатели по сравнению с группой контроля без экспериментального воздействия. Наибольшую эффективность демонстрировал КС в дозе 100.25 мг/кг. Исследования показали что КС обладает антигипокинезической активностью;
- внутрибрюшинное однократное введение мышам препаратов, приготовленных на физиологическом растворе - палоносетрона (0.25 мг/кг за 30 мин до опыта), Фенотропила (100 мг/кг) и КС (100.25 мг/кг) за 60 минут до ПРО в дозе 5 Гр показало (табл. 1), что палоносетрон по сравнению с контрольной группой животных не влиял на показатели выживаемости животных по сравнению с группой контроля. При этом Фенотропил и КС оказывали выраженное влияние на показатели выживаемости и средней продолжительности жизни мышей. При том, что в контрольной группе выжили 6 мышей из 12 (СПЖ составила 18 суток), в группе с Фенотропилом выжило 11 мышей из 12 (СПЖ составила 29 суток), а в группе животных с применением КС выжили 12 из 12 мышей (СПЖ составила 30-ть суток).
Таким образом, представленные в данном примере результаты скрининговых исследований показывают, что входящие в КС вещества не оказывают негативного и депримирующего влияния друг на друга. (RS)-2-(2-оксо-4-фенилпирролидин-1-ил)ацетамид и КС обладают выраженной радиопротекторной активностью при экспозиции ПРО в дозе 5 Гр, оказывая выраженное влияние на выживаемость животных и увеличивая при этом их среднюю продолжительность жизни. КС также, как установлено, обладает антигипокинезической активностью с сохранностью при этом двигательной активности и ориентировочно исследовательского поведения у животных.
Пример 2. Облучение собак в дозе 20 и 30 Гр приводило к развитию ярко выраженных симптомов ОЛБ (таблица 2) по эметическому синдрому, проявлявшемуся в контрольной группе животных уже через 28 и 17 мин (латентный период реакции) после соответствующей дозы облучения и характеризующегося неукротимой рвотой, длящейся соответственно 72.1 и 152.4 мин. Состояние животных контрольной группы соответствовало крайней степени тяжести проявления ОЛБ. При этом частота рвотной реакции составляла 90 и 100% соответственно дозам облучения 20 и 30 Гр, количество рвотных актов соответственно - 7.8 и 13.3, выраженных в абс. ед.
Применение Фенотропила не приводило к достоверному изменению состояния животных по показателям частоты рвотной реакции, латентного периода первого рвотного акта и продолжительности рвотного периода, но достоверно при этом снижало количество рвотных актов соответственно на 17 и 12% по сравнению с контрольной группой собак.
Палоносетрон, как и следовало ожидать, проявлял выраженную эффективность при всех исследуемых показателях эметического синдрома, характерных в данном случае для ОЛБ. Частота рвотной реакции сокращалась в 3 и 2 раза соответственно при дозах ИИ 20 и 30 Гр, количество рвотных актов сокращалось соответственно в 3.4 и 4.8 раза, латентный период первого рвотного акта увеличивался в 3.8 и 6.3 раза соответственно, а продолжительность рвотного периода сокращалась в 3.3 и 10.4 раза соответственно по сравнению с контрольной группой животных.
Применение комбинированного состава, содержащего Фенотропил и палоносетрон, продемонстрировало его высокую антиэметическую активность при радиационном поражении организма в сравнении с контрольной группой животных с ОЛБ на фоне поражающего воздействия ИИ, составляющего 20 и 30 Гр, а именно: частота рвотной реакции снизилась соответственно в 3 и 2 раза; количество рвотных актов снизилось в 4 и 5.5 раза соответственно; латентный период первого рвотного акта увеличился соответственно в 4.2 и 5.7 раза, продолжительность рвотного периода снизилась соответственно в 4 и 8 раз. При этом КС по антиэметической активности не только не уступал, но и по некоторым показателям превосходил палоносетрон.
При сравнении эффектов КС с эффектами палоносетрона между собой наблюдается идентичность их влияния на показатель частоты рвотной реакции, но по остальным показателям очевидны их достоверные различия. КС снижал количество рвотных актов на 18 и 15% соответственно по сравнению с эффектами палоносетрона по этому показателю, демонстрируя и несколько большую (на 5%) тенденцию активности по показателю латентного периода первого рвотного акта при дозе ИИ 20 Гр, но его эффективность была на 12.7% ниже чем у палоносетрона по этому показателю в дозе ИИ 30 Гр. По показателю продолжительности рвотного периода эффективность КС была на 21% выше и на 23% ниже таковой палоносетрона соответственно при ИИ 20 и 30 Гр. Полученные результаты показывают, что у данных препаратов при их однократном применении проявляется достаточно высокая антиэметическая активность при ПРО в дозах ИИ 20 и 30 Гр, но и имеются при этом статистически достоверные различия между собой.
Таким образом, КС показал достоверно высокую эффективность при однократном применении по показателю влияния на эметический синдром в условиях неизбежного радиационного поражения и развития ОЛБ о чем свидетельствует группа контрольных животных. То есть КС обладает достаточно высокой антиэметической активностью при радиационном поражении организма, а входящие в его состав вещества не оказывают депримирующего влияния друг на друга в комбинированном составе, не конкурируя, вероятно, друг с другом за места связывания с нейротрансмиттерами серотонинэргической системы. Отличия по некоторым показателям выраженности его эффектов от палоносетрона указывают на то, что механизм реализации эффективности данного комбинированного состава имеет отличия от механизма их реализации у палоносетрона даже при однократном применении.
Однако при таких сложнейших патологиях оценивать эффективность препаратов в ряду как радиопротекторов, так и противорадиационных средств только по одному даже ярко выраженному синдромальному показателю недостаточно. Их лечебный эффект должен быть подтвержден по другим не менее важным симптомам, затрагивающим не только не менее, но и более глубинные как функциональные, так и патогенетические системы.
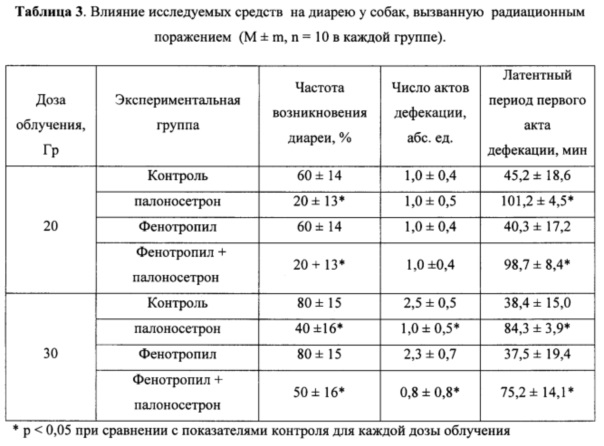
Пример 3. Другим симптомом проявления ОЛБ при ПРО, который существенно ухудшает состояние и снижает трудоспособность, является диарея. Результаты проведенных экспериментов по данному показателю представлены в таблице 3.
Полученные данные свидетельствуют о том, что после облучения в дозе 20 Гр у 60% собак наблюдали одно-, двукратную диарею, проявлявшуюся в виде актов дефекации жидкими массами со слизью, иногда с примесью крови, и сопровождавшуюся ложными позывами с капельными слизистыми выделениями. После воздействия ИИ в дозе 30 Гр диарею наблюдали у 80% собак, при этом повышалось количество актов дефекации, составив 2,5±0,5.
Введение палонострона при радиационном поражении в 20 Гр приводило к снижению частоты развития диареи в 3.0 раза, не влияло на число актов дефекации и увеличивало в 2.2 раза латентный период первого акта дефекации. На фоне радиационного поражения при ИИ 30 Гр, соответствующие эффекты палоносетрона по сравнению с контрольной группой составили: в 2 раза снизился показатель частоты возникновения диареи, в 2.5 раза снизилось число актов дефекации и 2.2 раза увеличился латентный период первого акта дефекации. Различия между группами палоносетрона по сравнению с группой контроля касались только числа актов дефекации.
Введение Фенотропила в варианте монотерапии не оказывало при однократном примении влияния на развитие диареи, вызванной радиационным поражением.
Введение КС оказывало на фоне радиационного поражения животных в дозе 20 Гр следующее влияние: в 3.0 раза снижалась частота возникновения диареи, не изменялся показатель числа актов дефекации и в 2.2 раза увеличивался латентный период первого акта дефекации. На фоне радиационного поражения животных в дозе 30 Гр показатель числа возникновения диареи снизился в 1.6 раза, в 3.1 раза снизилось число актов дефекации и в 2.0 раза увеличился латентный период первого акта дефекации.
Эффекты КС сопоставимы по данным показателям компонентов диареи с палоносетроном, но при сравнении этих групп между собой КС на 20% превосходит эффект палоносетрона по показателю числа актов дефекации у животных в группах с ПРО в дозе ИИ 30 Гр.
Таким образом, по влиянию на показатели диареи КС при однократном применении является высокоэффективным средством, оказывающим защитное действие на проявление диареи при радиационном поражении организма животных, превосходя при более тяжелых поражениях ИИ палоносетрон на 20% по показателю снижения числа актов дефекации.
В данной серии исследований так же не выявлено негативного влияния друг на друга веществ, входящих в КС.
Пример 4. Результаты изучения влияния ИИ в дозах 20 и 30 Гр на спонтанную двигательную активность животных в контрольной группе и в группах животных, которым вводились исследуемые препараты, представлены в таблице 4.
Приведенные данные свидетельствуют, что облучение животных в дозах 20-30 Гр вызывало развитие выраженной гипо- и адинамии, свойственной состоянию ОЛБ. Следует отметить, что если при облучении в дозе 20 Гр адинамию в контрольных группах наблюдали в 60% случаев, то облучение в дозе 30 Гр приводило к развитию адинамии у всех животных. В группах контроля, у всех без исключения животных наблюдались выраженные нарушения. Большинство собак контрольной группы весь период наблюдения лежали на боку с поднятой головой или положив голову на лапы. Интереса к экспериментатору не проявляли.
Введение палоносетрона позволило несколько облегчить симптоматику астеногиподинамии, вызванной радиационным поражением, но эти эффекты не были значимыми по общему числу животных без явно выраженных нарушений, составляя в среднем по группам животных с палоносетроном не более 15%. У Фенотропила этот показатель в его группах составил в среднем 45%, а в группах с КС - 40%. При этом Фенотропил и КС полностью устраняли адинамию и существенно на 45% сокращался показатель гиподинамии у животных на фоне Фенотропила, а у животных на фоне КС этот показатель сокращался в среднем на 40%.
Животные в группах с Фенотропилом и КС находились в достаточно активном состоянии, не проявляли депрессивного поведения. Они сидели или ходили, а при приближении экспериментатора подходили к нему и лишь через 4-6 часов после облучения большинство животных ложилось.
Результаты данной серии исследований показывают, что применение палоносетрона в качестве монопрепарата противопоказано лицам, находящимся под угрозой радиационного поражения и получившим радиационное поражение в случаях требующих сохранности физической и психической активности. Комбинированный состав способен в таких случаях обеспечить сохранность физической и психической активности уже с однократного применения, что является чрезвычайно важным в профессиях, связанных с экстремальными видами деятельности, а так же в случаях аварий и катастроф несущих угрозу массового радиационного поражения.
С учетом выявленной у КС антиэметической активности и способность снижать проявления диареи ставит его в ряд радиопротекторных и противорадиационных средств, способных обеспечивать защиту организма от повреждающего воздействия ИИ и одновременно оказывающих терапевтическое влияние на последствия при радиационном поражении различной степени тяжести. КС уже при однократном применении проявляет и антидепрессивную активность, что позволяет принимать правильное решение в условиях когда невозможно избежать радиационного поражения.
Пример 5. В данной серии исследований проводилось сравнительное изучение влияния разработанного КС на диспептический синдром у крыс при радиационном поражении ИИ в дозе 180 Гр. Результаты исследования представлены в таблице 5.
Приведенные данные согласуются с результатами опытов, полученными на собаках (пример 2.). В контрольной группе животных диарея развивалась у всех крыс, облученных в дозе 180 Гр, и характеризовалась многократной дефекацией жидкими массами с примесью слизи уже в ходе воздействия ИИ и на протяжении 30-40 мин после облучения. Введение Фенотропила увеличивало в 2.2 раза латентный период проявления диареи.
При изолированном введении палоносетрона частота диареи была ниже на 30% по сравнению с группой контроля, латентный период увеличился в 13.0 раз, количество актов дефекации снизилось в 6.4 раза, а продолжительность снизилась в 28.3 раза.
Эффекты КС проявлялись снижением частоты диареи на 20%, увеличением латентного периода в 16 раз, снижением количества актов дефекации в 3.2 раза со снижением продолжительности в 28.3 раза. По показателю латентного периода КС превосходил по эффективности палоносетрон на 23%.
Таким образом, есть все основания говорить о том, что и при тяжелых формах радиационного поражения КС проявляет достоверно выраженную фармакологическую активность.
О степени влияния препаратов на механизмы диареи при лучевом поражении были проведены эксперименты по исследованию пропульсивной и всасывательной активность желудочно-кишечного тракта. Как видно из полученных данных на фигуре 1, облучение крыс в дозе 180 Гр приводило к увеличению ИПА в 1,6 раза, что свидетельствует об усилении перистальтики кишки. Однократное введение Фенотропила практически не оказывало влияния на данный показатель. Иные результаты были получены при монотерапии палоносетроном и введении заявленного комбинированного состава. В обоих случаях наблюдали сохранение перистальтики кишечника облученных крыс в сравнении с группой контроля. При этом эффективность КС была достоверно несколько выше, чем на фоне палоносетрона.
На фигуре 2 приведена диаграмма, характеризующая влияние облучения и профилактического введения препаратов на всасывательную активность кишки крыс. Воздействие ИИ в дозе 180 Гр значительно (в 3,2 раза) снижало всасывание жидкости из просвета кишечника. Введение Фенотропила не оказывало выраженного влияния на всасывающую активность кишечника облученных крыс. В то же время применение палоносетрона и введение КС способствовало нормализации всасывания жидкости из просвета ЖКТ. При этом эффективность комбинированного состава была достоверно несколько выше эффективности палоносетрона.
Пример 6. Результаты изучения влияния препаратов при ОЛБ на ориентировочно-исследовательское поведение и двигательную активность крыс по методике «открытого поля», получивших дозу радиационного поражения 180 Гр, представлены в таблице 6.
Через 60 мин после облучения в контрольной группе облученных животных снизились все показатели ориентировочно-исследовательского поведения и двигательной активности в сравнении с группой интактных животных соответственно: в 2.1 раза - показатель количества пересеченных квадратов, в 1.8 раза - количество норковых реакций и в 1.7 раза - количество вертикальных стоек.
Введение палоносетрона животным не изменило их состояния по сравнению с группой опытного контроля (облученные животные), что указывает на отсутствие эффективности у палоносетрона и на функциональном, и на патогенетическом уровнях в отношении высших интегративных функций головного мозга, управляющих поведением, то есть наличие у палоносетрона антиэметического эффекта не способствует сохранности наиважнейших структур, обеспечивающих фактически выживаемость или стремление к выживаемости у высших животных.
Фенотропил и КС оказывают выраженную мнемотропную (влияние на патогенез врожденного - генетически предопределенного исследовательского поведения, которым является норковый рефлекс) и ноотропную активность (сохранность функционального исследовательского поведения, проявляющегося стремлением не только к воспроизводству приобретенных навыков, но и к обучению с преодолением стресс-негативной реакции в незнакомой обстановке). Эффект КС превышал на 14% эффект фенотропила по показателю количества пересеченных квадратов и превышая данный показатель в группе контроля с облучением почти на 99%. Количество норковых реакций по сравнению с группой контроля с облучением было выше на 36%, а количество вертикальных стоек - выше на 54%. Учитывая тяжесть радиационного поражения, данные показатели являются уникальными, прямо указывая на противорадиационную активность КС с проявлением мнемотропного и ноотропного эффектов и сохранностью ориентировочно-двигательной активности без проявления неврозоподобных состояний, ни в сторону возбуждения, ни в сторону страха, апатии или депрессии. И если недостатком Фенотропила с выраженной эффективностью по данному тесту можно отнести отсутствие у него антиэметической активности при радиационном поражении организма, то КС сочетает все изученные выше эффекты.
Пример 7. Результаты исследований по оценки влияния препаратов на способность облученных крыс выполнять заученные тесты (тест «избегание плаванием» и тест «Beam-walking») приведены в таблице 6.
В группе контрольных животных без облучения в тесте «избегание плаванием» латентный период выполнения задачи (время спасения из воды по веревке) составил 4.7 с, а в тесте «Beam-walking» время выполнения теста (пересечение перекладины) составило 1.2 с. В тесте «Beam-walking» интактные животные пересекали перекладину без единого соскальзывания.
Облучение в дозе 180 Гр существенным образом изменяло поведение экспериментальных животных. В первом тесте латентный период увеличился в 4.7 раза по сравнению с группой контроля без облучения, а во втором тесте время его выполнения (время пересечения перекладины) увеличилось в 48.7 раза и при этом четыре крысы из 12-ти были неспособны двигаться по перекладине.
Введение палоносотрона не оказывало сколько-нибудь положительного влияния на исследованные показатели и в том, и в другом тесте. Показатели на фоне применения палоносетрона не имели отличий от группы контроля с облучением.
Однократное введение Фенотропила позволило предотвратить развитие нарушений работоспособности у облученных крыс. Величина времени выполнения тестов животными, которым вводили Фенотропил, было в 2.2 и 9.4 раза ниже, чем у животных контрольной группы с облучением. КС сокращал время выполнения тестов в 1.8 и 8.7 раза соответственно. На фоне Фенотропила и КС выраженно снижалось проявление нарушений, вызванных ИИ, что способствовало выполнению тестов всеми животными, несмотря на наличие некоторых нарушений в координации движений, проявлявшихся в виде соскальзывания задних лап с перекладины и некоторого удлинения времени выполнения теста по сравнению с группой контроля без облучения. Тест избегание плаванием также указывает на присутствие антидепрессивной активности у КС с сохранностью приобретенного навыка.
Таким образом, полученные результаты исследований указывают на способность разработанного комбинированного состава, содержащего (RS)-2-(2-оксо-4-фенилпирролидин-1-ил)ацетамид и (3aS)-2-[(3S)-1-азабицикло-[2.2.2]окт-3-ил]-2,3,3а,4,5,6-гексагидро-1-оксо-1Н-бенз[de]изохинолин, оказывать радиопротекторную и противорадиационную активность с проявлением при этом антиэметического, антидиспепсического, антитоксического, антигипокинезического, противоадинамического, антиастенического, антидепрессивного, мнемотропного и ноотропного эффектов в острый период проявления лучевой болезни. При этом КС эффективно влияет на все негативные проявления, присутствующие в симпомокомплексе ОЛБ, а также повышает выживаемость и увеличивает продолжительность жизни животных.
Проведенные сравнительные экспериментальные исследования позволяют сделать вывод на примере палоносетрона, Фенотропила и КС, что для профилактики и лечения ОЛБ различной степени тяжести наилучшим образом подходят в острый период комбинированные средства, сочетающие в себе профилактические и лечебные свойства с различной направленностью их механизмов действия при условии, что входящие в состав вещества не будут друг с другом конкурировать за места связывания в нейротрансмиттерных системах и не будут оказывать друг на друга депримирующего влияния или усугублять побочные действия друг друга.
Включение в комплексный состав модулятора с соразмерным влиянием обеспечивает не только профилактический (протекторный), но и лечебный эффект по всем исследованным показателя и причем уже с однократного применения.
Учитывая, что в данных исследованиях были применены не только абсолютно эметогенные дозы ИИ, но и являющиеся летальными для животных и человека, выявленные эффекты имеют чрезвычайно важное значение. Разработанный комплексный состав, содержащий (RS)-2-(2-оксо-4-фенилпирролидин-1-ил)ацетамид и (3aS)-2-[(3S)-1-азабицикло-[2.2.2]окт-3-ил]-2,3,3а,4,5,6-гексагидро-1-оксо-1Н-бенз[de]изохинолин, может найти широкое применение для купирования негативного влияния на организм РТ и XT в онкологии, а также в экстремальных областях медицины с целью оказания профилактической и лечебной помощи при угрозе поражения и при поражении техногенными факторами, имеющими для организма человека не только неблагоприятные, но и зачастую необратимые последствия.







Литература
1. Ахапкина В.И. // Патент RU на изобретение №2480214 (приоритетом изобретения 22.09.2011 согласно указанному Патенту, зарегистрировано в Государственном реестре изобретений Российской Федерации 27 апреля 2013 г., авторы изобретения: Ахапкина В.И., Ахапкин Р.В.).
2. Ахапкина В.И., Ахапкин Р.В. Модуляторы с соразмерным влиянием и дивергенты - два новых базовых класса лекарственных средств // РМЖ - Неврология и психиатрия, №29, 2012, с. 1445-1448.
3. Ахапкина В.И., Ахапкин Р.В. Антитоксическая и антикревинговая активность Фенотропила при алкогольной и никотиновой зависимости // Наркология, №6, 2013, с. 61-65.
4. Ахапкина В.И. Реювенационная, репаративная и антикревинговая активность модуляторного препарата Фенотропил // Ж. Фарматека, №6(259), 2013, с. 130-135.
5. Ахапкина В.И. Отличительные особенности оригинально-инновационного состава Фенотропил или (RS)-2-(2-око-4-фенилпирролидин-1-ил)ацетамид, обладающего модуляторной активностью с соразмерным влиянием // Поликлиника, №4(3), 2013, с. 43-58.
6. Ахапкина В.И., Ахапкин Р.В. Выявление и оценка нейролептической активности фенотропила // Журнал неврологии и психиатрии им. С.С. Корсакова, 2013 - №7 - С. 42-46.
7. Брумберг И.Е., Пятовская Н.Н. Количественная оценка интенсивности всасывания уранина как показатель лучевого поражения желудочно-кишечного тракта животных // Радиобиология. 1980. Т. 20, вып. 2. С. 289-292.
8. Буреш Я., Бурешова О., Хьюстон Д.П. Методики и основные эксперименты по изучению мозга и поведению. - М.: Высшая школа, 1991. - 399 с.
9. Легеза В.И. и др. Количественная оценка изменений двигательной активности у собак после лучевого воздействия // Радиобиология. 1979. Т. 19, вып. 6. С. 927-930.
10. Легеза В.И. и др. О роли серотонина и гистамина в нейрогуморальных механизмах постлучевой диареи у крыс // Радиобиология. 1990. Т. 30, вып. 5. С. 607-612.
11. Методические рекомендации по изучению противорвотной активности лекарственных средств / В кн. Руководство по проведению доклинических исследований лекарственных средств. Часть первая. - М.: Гриф и К, 2012. - С. 719-724
12. Методические указания по экспериментальному и клиническому изучению средств терапии радиационных поражений и медико-биологические требования к этим средствам: Утв. МЗ СССР. - М., 1978. - 48 с.
13. Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ / Под общ. ред. Р.У. Хабриева. - М.: ОАО «Изд-во «Медицина», 2005. - 832 с.
14. Barroco, R.A., Klauenberg, В.J., Irwin, L.N. Swim escape: A multicomponent, one - trial learning task // Behav. Biol. 1978. Vol. 22. P. 114-121.
15. Goldstein, L.B., Davis, J.N. Beam-walking in rats: studies towards developing an animal model of functional recovery after brain injury // J. Neurosci. Methods. 1990. Vol. 31, №2. P. 101-107.
| название | год | авторы | номер документа |
|---|---|---|---|
| ВЕЩЕСТВО, ОБЛАДАЮЩЕЕ НЕЙРОТРОПНОЙ - НЕЙРОМОДУЛЯТОРНОЙ АКТИВНОСТЬЮ | 2006 |
|
RU2329804C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ КУПИРОВАНИЯ ПЕРВИЧНОЙ РЕАКЦИИ НА ОБЛУЧЕНИЕ И РАННЕЙ ПРЕХОДЯЩЕЙ НЕДЕЕСПОСОБНОСТИ | 2012 |
|
RU2509557C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ОНДАНСЕТРОН И МЕТАЦИН | 2001 |
|
RU2185825C1 |
| ВЕЩЕСТВО, ОБЛАДАЮЩЕЕ АНТИДЕПРЕССИВНОЙ АКТИВНОСТЬЮ | 2003 |
|
RU2232578C1 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2007 |
|
RU2363463C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ОНДАНСЕТРОН И БЕНЗАМИД | 2003 |
|
RU2228752C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ОНДАНСЕТРОН, МЕТАЦИН И БЕНЗАМИД | 2003 |
|
RU2234315C1 |
| ПРОТИВОРВОТНОЕ СРЕДСТВО БЕНЗАМИД | 2002 |
|
RU2205009C1 |
| КОМПОЗИЦИЯ ИНГРЕДИЕНТОВ ДЛЯ ПОЛУЧЕНИЯ ЛЕЧЕБНОГО ЭЛИКСИРА "ДОКТОР ПЕТРОВ" | 2002 |
|
RU2233168C2 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИДЕПРЕССАНТНЫМ, АНКСИОЛИТИЧЕСКИМ, НЕЙРОПРОТЕКТОРНЫМ И ИММУНОСТИМУЛИРУЮЩИМ ДЕЙСТВИЕМ | 2010 |
|
RU2429834C1 |
Изобретение относится к комбинированному составу, обладающему радиопротекторной и противорадиационной активностью. Указанный состав содержит (RS)-2-(2-оксо-4-фенилпирролидин-1-ил)ацетамид и (3aS)-2-[(3S)-1-азабицикло-[2.2.2]окт-3-ил]-2,3,3а,4,5,6-гексагидро-1-оксо-1Н-бенз[de]изохинолин. Изобретение обеспечивает выраженное снижение проявлений симптомов первичного радиационного облучения при поражении различными дозами ионизирующего излучения. 1 з.п. ф-лы, 2 ил., 7 табл., 7 пр.
1. Комбинированный состав, содержащий (RS)-2-(2-оксо-4-фенилпирролидин-1-ил)ацетамид и (3aS)-2-[(3S)-1-азабицикло-[2.2.2]окт-3-ил]-2,3,3а,4,5,6-гексагидро-1-оксо-1Н-бенз[de]изохинолин, обладающий радиопротекторной и противорадиационной активностью.
2. Комбинированный состав по п. 1, обладающий антиэметической, антидиспепсической, антитоксической, антигипокинезической, противоадинамической, антиастенической, антидепрессивной, мнемотропной и ноотропной активностью.
| Инструкция по медицинскоми применению препарата "ФЕНОТРОПИЛ", регистрационое удостоверение Р N002781/01 от 08.04.2009, ОАО "Щелковский витаминный завод", весь документ | |||
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| Колосоуборка | 1923 |
|
SU2009A1 |
| Инструкция по медицинскоми применению препарата "ОНИЦИТ", регистрационое удостоверение ЛП 000716 от 29.09.2011, "Хелсинн Байрекс Фармасьютикалс Лтд.", весь документ. | |||
Авторы
Даты
2017-06-21—Публикация
2014-10-14—Подача