Определение подлинности и качества лекарственного растительного сырья весьма актуально и важно, так как позволит избежать ошибки при приеме лекарственных средств и предотвратить нанесение непоправимого ущерба здоровью.
Изобретение относится к способу определения качества и подлинности лекарственного сырья зверобоя продырявленного (Hypericum perforatum L.).
По условиям фармакопейной статьи подлинность лекарственного сырья зверобоя устанавливается по внешним и микроскопическим признакам, а качество собранного материала - по сумме флавоноидов в пересчете на рутин, которая должна составлять не менее 1,5% [ФС.2.5.0015. Зверобоя трава. Hyperici herba. - 10 с.].
Известен ИК-спектроскопический экспресс-способ определения качества лекарственного растительного сырья (патент RU 2493555, МПК G01N 21/35 (2006.01)). Способ включает отбор лекарственных растений, измельчение до 0,2÷0,5 мм, исследование образцов лекарственного растительного сырья. Полученный образец помещают в приставку НПВО и регистрируют спектр на Фурье-ИК спектрометре, идентифицируют значения характеристических частот спектра, соответствующих химическому составу образца, и определяют подлинность лекарственного растительного сырья по табличным спектральным данным для эталонных образцов. По наличию функциональных групп в образце, не свойственных его химическому составу и появившихся в результате антропогенного загрязнения, определяют безопасность и качество лекарственного растительного сырья.
Данный способ не учитывает тот факт, что химический состав большинства растительных объектов близок, особенно внутри одного рода, что не исключает большую погрешность и низкую достоверность полученных результатов.
Известен способ оценки подлинности лекарственного растительного сырья (ЛРС), в том числе и травы зверобоя (патент RU 2452944, МПК G01N 30/02 (2006.01)), заключающийся в том, что образец ЛРС выдерживают 40 минут при 100°С, компоненты равновесной паровой фазы (РПФ) анализируют на стандартной колонке. Затем определяют интерполяционные характеристики сорбатов, а синхронизацию момента ввода проб РПФ и н-алканов осуществляют по сигналу детектора на часть потока из линии сброса делителя узла ввода пробы. Этот способ является информативным и может быть использован для определения подлинности лекарственного растительного сырья, однако компоненты равновесной паровой фазы не являются активными компонентами зверобоя продырявленного и не могут быть использованы для определения его качества.
Известен способ определения дубильных веществ в растительном сырье (патент RU 2439568, МПК G01N 33/52 (2006.01)), заключающийся в том, что их экстрагируют из сырья водой при кипячении, охлаждают, фильтруют, измеряют оптическую плотность аликвотной пробы при 277 нм и рассчитывают содержание суммы всех дубильных веществ по определенной формуле, далее к аликвотной пробе фильтрата добавляют 1% раствор коллагена в 1% уксусной кислоте, взбалтывают, фильтруют, измеряют оптическую плотность фильтрата при 277 нм и рассчитывают содержание осаждаемых дубильных веществ по определенной формуле. Способ позволяет повысить точность определения содержания дубильных веществ в растительном сырье и селективно определить осаждаемые и не осаждаемые дубильные вещества в растительном сырье. Полученная характеристика может служить параметром качества лекарственного растительного сырья.
К недостаткам способа относится получение значения суммарной характеристики, которая не учитывает вклад в качество сырья зверобоя такого активного компонента, как гиперфорин.
Известен способ определения подлинности растений методом ЯМР (M.S.M. Preto, M.I.B. Tavares a, P.J.O. Sebastião, R.B.V. Azeredo Determination of herb authenticity by low-field NMR. / J. Food Chem, 2013. - №136. - PP. 1272-1276), который может быть использован для дифференциации растительных образцов относительно их региональной принадлежности в короткие временные промежутки, избегая разрушения образца. Однако данный способ сложный в техническом исполнении и дорогостоящий.
Известен способ DNA mini-barcoding, основанный на данных ЯМР метода (J. Costa, В. Campos, J.S. Amaral, M.E. Nunes, M. Beatriz P.P. Oliveira, I. Mafra HRM analysis targeting ITS1 and matK loci as potential DNA mini-barcodes for the authentication of Hypericum perforatum and Hypericum androsaemum in herbal infusions. / J. Food Control, 2016. - №61. - PP. 105-114)/ Описанный вариант установления аутентичности (подлинности), по мнению авторов, может использоваться для дифференциации таких видов зверобоя, как Hypericum androsaemum и Hypericum perforatum. К недостаткам данного способа можно отнести сложность. Кроме того, способ не предполагает установления качества лекарственного сырья.
Известен способ установления соотношения суммы флавоноидов к сумме фенольных соединений для различных образцов растительного происхождения (М.P. Srivastava, R. Tiwari, N. Sharma, Assessment of phenol and flavonoid content in the plant materials. J. on New Biological Reports. 2013, Vol. 2 (2), p. 163-166), включающий анализ экстракта растительного образца для установления суммы флавоноидов колориметрическим методом с использованием хлорида алюминия и суммы фенольных соединений по методу Фолина-Чокальтеу. После этого устанавливают отношение суммы флавоноидов к сумме фенольных соединений. Полученное соотношение может быть использовано для установления качества растительного сырья. Однако отношение суммарных показателей не является строго определенным параметром для каждого растительного объекта, что снижает точность дифференциации образцов.
Наиболее близким аналогом является способ установления корреляционной зависимости между содержанием суммы флавоноидов и содержанием гиперицина в зверобое продырявленном (Hypericum perforatum L.) (А. Ghavamaldin, R. Aptin, P. Khalil, G. Mansour, T. Mariamalsadat, Study of variation of biochemical components in Hypericum perforatom L. grown in North of Iran. / J. Med. Plants Res., Vol. 6 (3). - PP. 366-372). Данный способ включает определение суммы флавоноидов по методике с использованием хлорида алюминия и гиперицина по спектрофотометрической методике, описанной в статье Европейской Фармакопеи (European Pharmacopoeia, 07/2008: 1438). Корреляционные зависимости между суммой флавоноидов и гиперицином устанавливаются с применением программы статистического обсчета. Однако данным способом нельзя установить подлинность и качество лекарственного сырья.
Техническим результатом предлагаемого изобретения является повышение достоверности в установлении подлинности и качества лекарственного сырья.
Для достижения технического результата готовят водно-спиртовой экстракт травы зверобоя (Hypericum perforatum L.), который анализируют методом высокоэффективной жидкостной хроматографии, определяют концентрации рутина и гиперфорина (ммоль/л), затем пересчитывают их содержания в зверобое (ммоль/кг), находят отношение рутина к гиперфорину, и равенство его 0,8-1,2 свидетельствует о подлинности и качестве зверобоя (Hypericum perforatum L.).
Готовят водно-спиртовой экстракт травы зверобоя продырявленного по способу, прописанному либо в Фармакопейной статье (ФС.2.5.0015. Зверобоя трава. Hyperici herba. - 10 с.), либо по способу динамической экстракции при повышенных температуре и давлении (патент RU №2568912, МПК А61К 36/38 (2006.01)).
Рутин является наиболее стабильным во времени компонентом зверобоя, что подтверждается данными многих исследователей (S. Н. Kopleman, L.L. Augsburger, A. NguyenPho, W.S. Zito Selected Physical and Chemical Properties of Commercial Hypericum perforatum Extracts Relevant for Formulated Product Quality and Performance, AAPS PharmSci 2001, 3 (4) article 26 (http://www.pharmsci.org/); A.R. Bilia, M.C. Bergonzi, G. Mazzi, F.F. Vincieri Analysis and Stability of the Constituents of Artichoke and St. John’s Wort Tinctures by HPLC-DAD and HPLC-MS, Drug Development and Industrial Pharmacy, 2002, 28 (5), p. 609-619).
Экспериментальные исследования, проведенные нами, показали, что отношение содержаний рутина и гиперфорина в образцах, независимо от их территориального происхождения, имеет значение 1.0±0.2 (таблица 1).
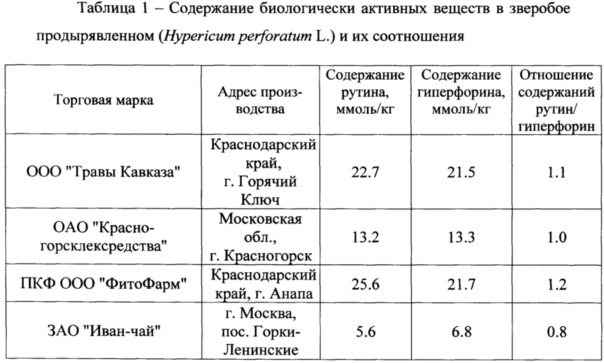

Для установления постоянства установленного соотношения содержаний рутина и гиперфорина нами были проведены исследования лекарственных сборов, представляющих смеси различных лекарственных растений, включая траву зверобоя (таблица 2). Как видно из таблицы 2, отношение содержаний этих компонентов выходит за границы установленного для зверобоя значения (1.0±0.2).
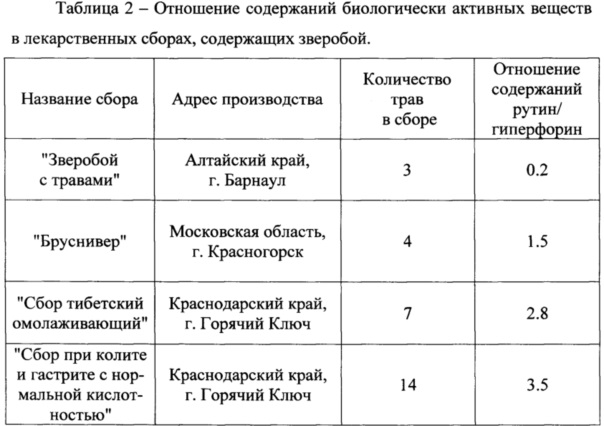
На основании полученных результатов можно сделать вывод о том, что в анализируемых сборах, кроме зверобоя продырявленного, присутствуют другие лекарственные растения.
Длительное или ненадлежащее хранение образцов зверобоя приводит к разрушению гиперфорина, обладающего биологической активностью, в результате чего значение соотношения рутин/гиперфорин нарушается (Verotta L., Appendino G., Jakupovic J., Bombardelli E., Hyperforin Analogues from St. John’s Wort (Hypericumperforatum) / J. Nat. Prod. 2000. №63. P. 412-415). Данный факт позволяет использовать изменение значения соотношения рутин/гиперфорин как параметр, определяющий качество лекарственного сырья зверобоя, что подтверждено на примере соотношений биологически активных веществ в образце травы с истекшим сроком годности (таблица 3).

Отличительными признаками заявляемого способа от наиболее близкого аналога, взятого за прототип, являются:
- определение содержания в зверобое рутина и гиперфорина, а не определение суммы флавоноидов;
- нахождение значения соотношения содержаний компонентов, по которому определяют качество и подлинность лекарственного сырья;
- использование метода высокоэффективной жидкостной хроматографии позволяет регистрировать сигнал единичного параметра, как рутина, так и гиперфорина, более корректно, чем спектрофотометрический метод, который регистрирует аналитический сигнал суммы флавоноидов, так как при этой длине волны имеют поглощение и другие органические компоненты.
Пример конкретного выполнения
Готовят водно-спиртовой экстракт зверобоя продырявленного производства «Травы Кавказа» по способу, прописанному в Фармакопейной статье (ФС.2.5.0015. Зверобоя трава. Hyperici herba. - 10 с.). Аналитическую пробу сырья измельчают до размера частиц, проходящих сквозь сито с отверстиями диаметром 1 мм. Около 1 г (точная навеска) измельченного сырья помещают в колбу со шлифом вместимостью 150 мл, прибавляют 30 мл 50% спирта. Колбу присоединяют к обратному холодильнику и нагревают на кипящей водяной бане в течение 30 мин, периодически встряхивая для смывания частиц сырья со стенок. Горячее извлечение фильтруют через вату в мерную колбу вместимостью 100 мл так, чтобы частицы сырья не попадали на фильтр. Вату помещают в колбу для экстрагирования и прибавляют 30 мл 50% спирта. Экстракцию повторяют еще дважды в описанных выше условиях, фильтруя извлечение в ту же мерную колбу. После охлаждения объем извлечения доводят 50% спиртом до метки и перемешивают. Полученный экстракт анализируют методом высокоэффективной жидкостной хроматографии. Хроматографирование осуществляется в двух системах с применением спектрофотометрического детектора: "Система 1" - для определения рутина, "Система 2" - для гиперфорина.
В "Системе 1" компоненты подвижной фазы - ацетонитрил (А) и вода, содержащая 0.1% муравьиной кислоты (В). Устанавливают градиентный режим элюирования от 95% В до 10% В. Скорость потока - 0.4 мл/мин, термостатирование колонки при 40°С. Детектирование рутина проводится при 254±2 нм. Для "Системы 2" (определение гиперфорина) в качестве компонентов подвижной фазы также используют ацетонитрил (А) и воду, содержащую 0.1% муравьиной кислоты (В). Устанавливают градиентный режим элюирования от 20% В до 0% В. Скорость потока - 0.6 мл/мин; температура термостатирования колонки - 40°С. Детектирование гиперфорина проводится при 272±2 нм.
Затем определяют концентрации биологически активных компонентов (ммоль/л), а именно рутина и гиперфорина, с использованием градуировочных кривых индивидуальных компонентов. После этого рассчитывают их содержания в исходном сырье зверобоя (ммоль/кг сухого сырья (Фармакопея СССР, 11-ое изд. Вып. 1)) по формуле:
Xв-вa=C⋅V/mСС,
где
Xв-ва - содержание вещества в образце, ммоль/кг;
С - концентрация вещества в экстракте, ммоль/л;
V - объем экстракта, л;
mCC - масса сухого сырья, кг.
После расчета получают содержания рутина и гиперфорина. Устанавливают отношение содержаний рутина и гиперфорина в сырье зверобоя продырявленного, которое равно 1,0±0,2. Анализируемое сырье аутентично и качественно.
Предлагаемый способ позволяет в течение 75-145 минут получить данные о соотношении биологически активных веществ в зверобое продырявленном, а именно рутина и гиперфорина, и, по их соотношению, установить подлинность и качество используемого сырья.
В прототипе устанавливают корреляцию между суммарным содержанием флавоноидов и содержанием гиперицина в зверобое продырявленном, но никаких результатов исследований по возможности установления его подлинности и качества не приводится.
Таким образом, предлагаемый способ является новым, практически применимым, а совокупность существенных признаков позволяет достичь технического результата, т.е. он обладает существенными отличиями.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЭКСТРАКЦИИ БИОЛОГИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ ИЗ ЗВЕРОБОЯ ПРОДЫРЯВЛЕННОГО (Hypericum perforatum L.) | 2014 |
|
RU2568912C1 |
| КОМПОЗИЦИЯ НА ОСНОВЕ ЗВЕРОБОЯ, ВКЛЮЧАЮЩАЯ СОЕДИНЕНИЯ ДИАНТРОНОВОГО РЯДА, И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2010 |
|
RU2436586C1 |
| СРЕДСТВО ДЛЯ МОЛОДНЯКА СЕЛЬСКОХОЗЯЙСТВЕННЫХ ЖИВОТНЫХ, ОБЛАДАЮЩЕЕ ИММУНОСТИМУЛИРУЮЩИМ ДЕЙСТВИЕМ, И СПОСОБ ЕГО ПРИМЕНЕНИЯ | 2003 |
|
RU2250110C1 |
| СПОСОБ ОДНОВРЕМЕННОГО ПОЛУЧЕНИЯ ГИПЕРИЦИНА И ПСЕВДОГИПЕРИЦИНА | 2015 |
|
RU2623084C2 |
| КОНЦЕНТРИРОВАННЫЙ ОТВАР ЦЕЛЕБНЫХ ТРАВ | 2006 |
|
RU2314089C1 |
| Косметическая композиция против воспалений на коже для использования в составе косметических средств | 2017 |
|
RU2646494C1 |
| Способ выделения гиперфорина и адгиперфорина из травы зверобоя продырявленного | 2019 |
|
RU2720457C1 |
| СПОСОБ ПОЛУЧЕНИЯ МНОГОКОМПОНЕНТНОЙ НАСТОЙКИ | 2021 |
|
RU2789301C2 |
| Распыляемое средство с антибактериальным эффектом | 2021 |
|
RU2748910C1 |
| СБОР ЛЕКАРСТВЕННЫХ РАСТЕНИЙ "ФИТОМОРОЗКО", ОБЛАДАЮЩИЙ ФРИГОПРОТЕКТОРНЫМ ДЕЙСТВИЕМ | 2006 |
|
RU2336896C2 |
Изобретение относится к способу определения качества и подлинности лекарственного сырья зверобоя продырявленного (Hypericum perforatum L.). Способ заключается в том, что приготавливают водно-спиртовой экстракт травы зверобоя (Hypericum perforatum L.), который анализируют методом высокоэффективной жидкостной хроматографии. Затем определяют концентрации рутина и гиперфорина (ммоль/л), на основании которых рассчитывают их содержания в зверобое (ммоль/кг), находят отношение рутина к гиперфорину, и равенство его 0,8-1,2 свидетельствует о подлинности и качестве зверобоя (Hypericum perforatum L.). Техническим результатом предлагаемого изобретения является повышение достоверности в установлении подлинности и качества лекарственного сырья. 3 табл.
Способ установления подлинности и качества зверобоя продырявленного (Hypericum perforatum L.), включающий приготовление водно-спиртового экстракта травы зверобоя, который анализируют методом высокоэффективной жидкостной хроматографии, определяют концентрации рутина и гиперфорина (ммоль/л), рассчитывают их содержания в зверобое (ммоль/кг), находят отношение содержаний рутина к гиперфорину, и равенство его 0,8-1,2 свидетельствует о подлинности и качестве зверобоя (Hypericum perforatum L.).
| А | |||
| Ghavamaldin, R | |||
| Aptin, P | |||
| Khalil, G | |||
| Mansour, T | |||
| Mariamalsadat, Study of variation of biochemical components in Hypericum perforatom L | |||
| grown in North of Iran | |||
| / J | |||
| Med | |||
| Plants Res., Vol | |||
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| - pp | |||
| Саморазгружающаяся железнодорожная платформа | 1921 |
|
SU366A1 |
| Л.Н | |||
| Зимина et al, ИССЛЕДОВАНИЕ ФЛАВОНОИДНОГО СОСТАВА ТРАВЫ ЗВЕРОБОЯ ПЯТНИСТОГО МЕТОДОМ ВЫСОКОЭФФЕКТИВНОЙ ЖИДКОСТНОЙ ХРОМАТОГРАФИИ, МЕДИЦИНСКИЙ АЛЬМАНАХ, N 2 (21), стр | |||
| Ротационный колун | 1919 |
|
SU227A1 |
| О.Е | |||
| Правдивцева et al., ИССЛЕДОВАНИЯ ПО ОБОСНОВАНИЮ НОВЫХ ПОДХОДОВ К СТАНДАРТИЗАЦИИ СЫРЬЯ И ПРЕПАРАТОВ ЗВЕРОБОЯ ПРОДЫРЯВЛЕННОГО, ХИМИЯ РАСТИТЕЛЬНОГО СЫРЬЯ | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| С | |||
| Горный компас | 0 |
|
SU81A1 |
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| US 2006003029 A1, 05.01.2006. | |||
Авторы
Даты
2017-03-23—Публикация
2015-12-25—Подача