Изобретение относится к химико-фармацевтической промышленности и касается средств группы нейролептиков.
В настоящее время психическое здоровье принадлежит к числу наиболее серьезных проблем, стоящих перед всеми странами, поскольку в тот или иной период жизни такие проблемы возникают, по крайней мере, у каждого четвертого человека. На их долю выпадает 19,5% всех лет жизни, утраченных в результате инвалидности. По данным ВОЗ только в Европейском регионе свыше 4 млн. человек страдают шизофренией; примерно 4 млн. - биполярными аффективными расстройствами и немного больше - паническими расстройствами.
Лечение психических больных, в частности больных шизофренией, сопряжено с рядом трудностей, среди которых надо отметить отсутствие выраженного терапевтического влияния классических нейролептиков на негативную симптоматику, довольно высокую частоту случаев резистентности при их применении и наличие выраженных побочных эффектов. Многие проблемы в последние годы удалось разрешить за счет внедрения в практику психиатрии так называемых атипичных нейролептиков
Одним из значимых событий в истории антипсихотических средств стало появление атипичного нейролептика клозапина. Описание первого опыта использования клозапина было представлено в 1966 г. австрийским психиатром H. Gross и соавт. Клозапин был исторически первым представителем класса так называемых «атипичных антипсихотиков», то есть антипсихотиков, отличающихся от традиционных малой вероятностью экстрапирамидных побочных явлений, лучшей переносимостью и меньшим влиянием на секрецию пролактина. Механизм действия клозапина несколько отличается от механизма действия многих нейролептиков. Эти отличия определяют значительные особенности профиля его психотропных эффектов. Антипсихотическое действие клозапина обычно объясняется его способностью блокировать дофаминовые D2- и серотониновые 5-НТ2-рецепторы головного мозга.
В настоящее время клозапин применяют при следующих заболеваниях: Шизофрения (в т.ч. при резистентности к терапии другими нейролептиками или их непереносимости), маниакальные состояния, маниакально-депрессивный психоз, психомоторное возбуждение при психопатиях, эмоциональные и поведенческие расстройства (в т.ч. у детей), тяжелые расстройства сна (http://www.vidal.ru/drugs/molecule/259).
В клинической практике используется выпускаемый препарат Ленопекс (Leponex®), таблетки немедленного высвобождения в дозах по 25 мг и 100 мг. Владельцем регистрационного удостоверения на Ленопекс (Leponex) является компания «Novartis Pharmaceuticals UK Ltd». Активной фармацевтической субстанцией является Клозапин. Каждая таблетка с риской содержит 25 мг или 100 мг Клозапина. Другие ингредиенты магния стеарат, кремния диоксид коллоидный, крахмал кукурузный, тальк, лактозы моногидрат, повидон К30.
Найден патент RU 2441651, который раскрывает таблетки клозапина и способ их получения. Способ заключается в том, что предварительно полученную сухую смесь лактозы, крахмала картофельного и клозапина увлажняют 10% водным раствором Коллидона 25, проводят влажную грануляцию, сушку при температуре 45-50°C. Полученные гранулы подвергают сухой грануляции до получения гранул со средним диаметром 1,0-1,5 мм, опудривают аэросилом и стеариновой кислотой и/или ее солью. Полученную смесь таблетируют, при этом получают таблетки со следующим соотношением компонентов, мас. %:
Как правило, рекомендуется начинать прием клозапина с дозы 12,5 мг один или два раза в день с постепенным повышением дозы с 25 мг до 50 мг в сутки, а при хорошей переносимости препарата достигается запланированная доза от 300 мг до 450 мг в сутки (прием раздельными дозами) к концу второй недели. Максимальная суточная доза - 900 мг. Средний терминальный период полураспада клозапина составляет 12 часов, поэтому для поддержания установившегося состояния необходим многократный прием препарата. Таким образом, желательно получить состав с замедленным высвобождением.
Известна международная заявка WO 2006059194 (А2) - 2006-06-08, раскрывающая состав с замедленным высвобождением, содержащий клозапин, поливинилпирролидон, полиэтиленгликоль, этилцеллюлозу, тальк, ацетон, спирт и воду. Методом влажного гранулирования получают гранулы с активным веществом, сушат, покрывают оболочкой и загружают в капсулы. В технологии используют токсические растворители.
В качестве ближайшего аналога может быть указан патент RU 2414903 (С1) - 2011-03-27, раскрывающий фармацевтический состав пролонгированного действия для перорального введения, включающий в качестве действующего вещества клозапин и в качестве вспомогательных веществ гидроксипропилметилцеллюлозу, микрокристаллическую целлюлозу, соль стеариновой кислоты, при следующих соотношении ингредиентов, мас. %:
Способ получения формы заключается в том, что в смеситель загружают просеянные гидроксипропилметилцеллюлозу, клозапин, комплекс микрокристаллической целлюлозы (МКЦ) и двуокиси кремния перемешивают в течение 7÷10 минут при скорости вращения главной мешалки 80÷100 об/мин, добавляют просеянный стеарат магния и продолжают смешивание в течение 2÷3 минут, перемешивают таблеточную и передают на стадию таблетирования. Таблетка может быть покрыта оболочкой.
Задача изобретения: разработка способа получения и фармацевтического состава клозапина - таблеток замедленного высвобождения при наличии устойчивых технологических свойств и стабильности, а также воспроизводимой кинетики высвобождения активного вещества.
Задача решается новым составом таблетированной формы с замедленным высвобождением активного начала, содержащим следующие компоненты в масс. %:
Целевой профиль замедленного высвобождения составляет по меньшей мере 21±2 часа.
В качестве фармацевтически приемлемой соли стеариновой кислоты может быть использован магния стеарат, кальция стеарат, их смесь.
Предпочтительно массовое соотношение Метоцел К4М и Метоцел К100 LV составляет 30:70.
Активный фармацевтический ингредиент, а именно клозапин (8-Хлор-11-(4-метил-1-пиперазинил)-5Н-дибензо-[b,e][1,4]диазепин), способен к сцеплению и проявляет плохую подвижность, что подтверждается коэффициентом сжимаемости. Низкая подвижность материала может давать таблетки с повышенной вариабельностью веса и содержания вследствие неравномерного распределения активного вещества в смеси, неравномерную насыпную плотность до уплотнения и, как результат, неравномерное заполнение полости матрицы таблеточного пресса. В связи с этим выбранные производственная формула и процесс должны обеспечивать хорошую текучесть и сжимаемость в готовой смеси.
Было обнаружено, что влажная грануляция проявляет тенденцию к потенциальному воздействию на стабильность вследствие влияния влаги и вероятности термического разложения лекарственного вещества во время сушки. Для сухой грануляции методом вальцевания порошкообразные частицы лекарственного вещества и наполнители соединяются под высоким давлением для образования ленты, а перед прессованием (таблетирование) разбиваются для образования гранул размалыванием. Также обнаружено, что риск неудовлетворительной однородности состава таблетки и отклонение массы таблетки с клозапином может быть снижен при осуществлении контроля фракционного состава и свойств сыпучести. Еще одним объектом изобретения является способ получения таблеток клозапина замедленного высвобождения методом вальцевания, предпочтительно при использовании субстанции клозапина микронизированной с распределением частиц по размеру d90<50 микрон. В частности, гранулометрический состав частиц с d90<50 микрон: d90-62,62 мкм, d50-25,86 мкм, d10-8,23 мкм.
Способ характеризуется тем, что Клозапин, комбинацию Метоцел К4М и Метоцел К100 LV, микрокристаллическую целлюлозу и коповидон просеивают вместе, перемешивают до однородности, добавляют магния стеарат, коллоидный диоксид кремния, перемешивают, смесь уплотняют вальцеванием, добавляют коллоидный диоксид и перемешивают вместе с предварительно уплотненными гранулами с последующим добавлением фармацевтически приемлемой соли стеариновой кислоты, перемешиванием и прессованием таблеток.
Таблетки прессуют в капсулообразной форме.
Предпочтительно перемешивание ведут при скорости мешалки 20 об/мин. Любую из стадий перемешивания осуществляют до однородного состояния, предпочтительно в течение 3-6 минут. На стадии вальцевания может использоваться сетка размером 1,6 мм для предварительной грануляции и 0,63 мм - для тонкой грануляции, и процесс осуществляют предпочтительно при гидравлическом давлении 90 бар.
Предложенный способ обеспечивает особенно хорошую текучесть и сжимаемость в готовой смеси при использовании определенных вспомогательных компонентов согласно предложенному составу.
Возможность осуществления изобретения продемонстрирована ниже представленными примерами.
Пример 1
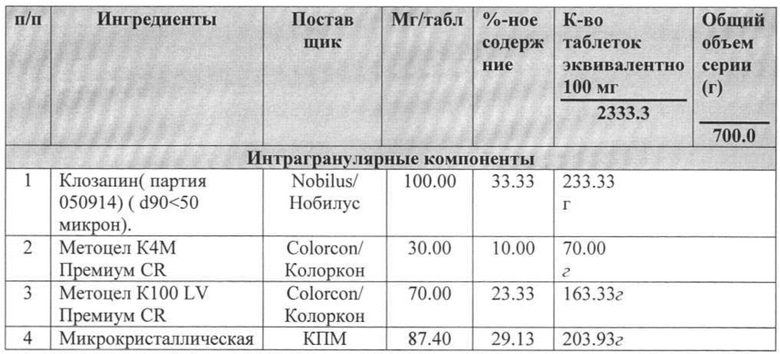
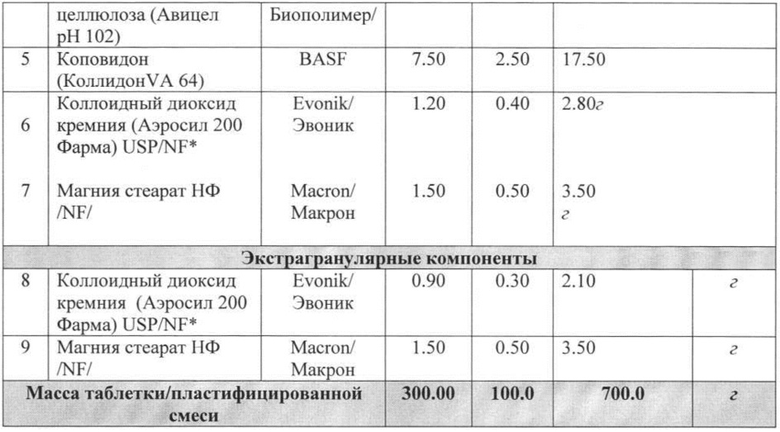
Пример 2
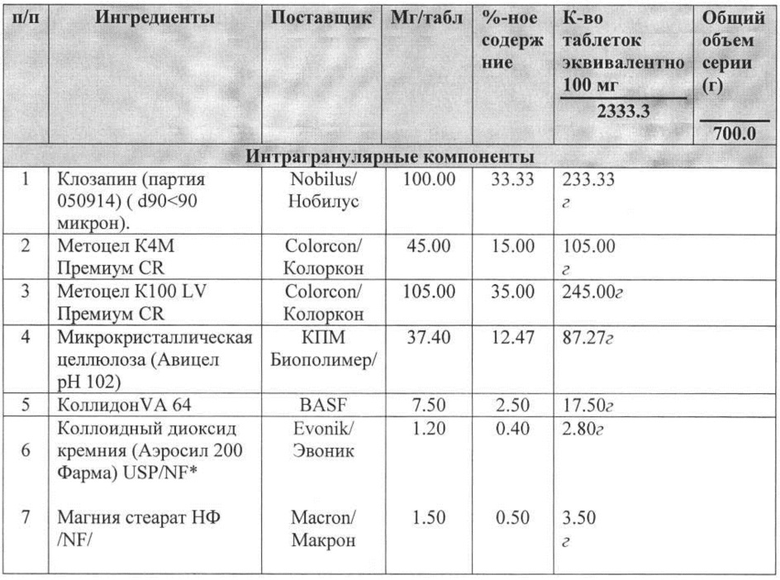
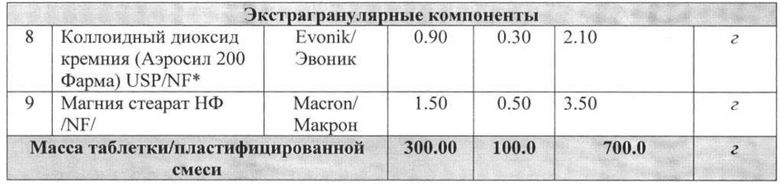
Пример 3
Способ получения
1. Просеивание интрагранулярных компонентов
Через сито ASTM#30 просеивали вместе субстанцию Клозапина, комбинацию Метоцел К4М и Метоцел К100 LV, Авицел рН 102 и Коллидон VA64.
Через сито ASTM#20 просеивали Коллоидный диоксид кремния. Через сито ASTM#60 просеивали Магния стеарат.
2. Смешивание (предварительное компактирование):
Просеянные вспомогательные вещества перемешивали в смесителе. Длительность перемешивания составила 6 минут при 20 об/мин.
Просеянный Магния стеарат добавляли к предыдущей фазе и вновь перемешивали. Длительность перемешивания составила 3 минуты при 20 об/мин.
3. Уплотнение (компактирование) вальцеванием
Вышеуказанную смесь поместили в роликовый пресс (Alexanderwerk WP120), оснащенный вальцами 25 мм. Пресс был запущен в работу согласно нижеприведенным параметрам, использовалась сетка размером 1,6 мм для предварительной грануляции и 0,63 мм - для тонкой грануляции.

4. Просеивание экстрагранулярных вспомогательных субстанций:
Через сито ASTM#20 просеивали Аэросил
Через сито ASTM#60 просеивали Магния стеарат
5. Смешивание (предварительное смазывание)
В смеситель емкостью 1 л помещали просеянный Аэросил вместе с предварительно уплотненными гранулами. Длительность перемешивания составила 4 мин при 20 об/мин.
Просеянный магния стеарат поместили в вышеупомянутый смеситель.
Смеситель запустили в работу на 2 минуты при 20 об/мин.
6. Прессование
Пластифицированную смесь помещают в таблеточный пресс с пуансонами типа D (используются 2 станции), прессуют согласно следующим параметрам:
Прессование составов, как в случае примера 1, так и в случае примера 2 было равномерным, с минимизированным отклонением от установленных параметров (менее 0,31% в отличие от прототипа с 0,96%).
Среднее значение прочности 20,63 Kp.
Пример 4
Изучение кинетики и стабильности таблеток
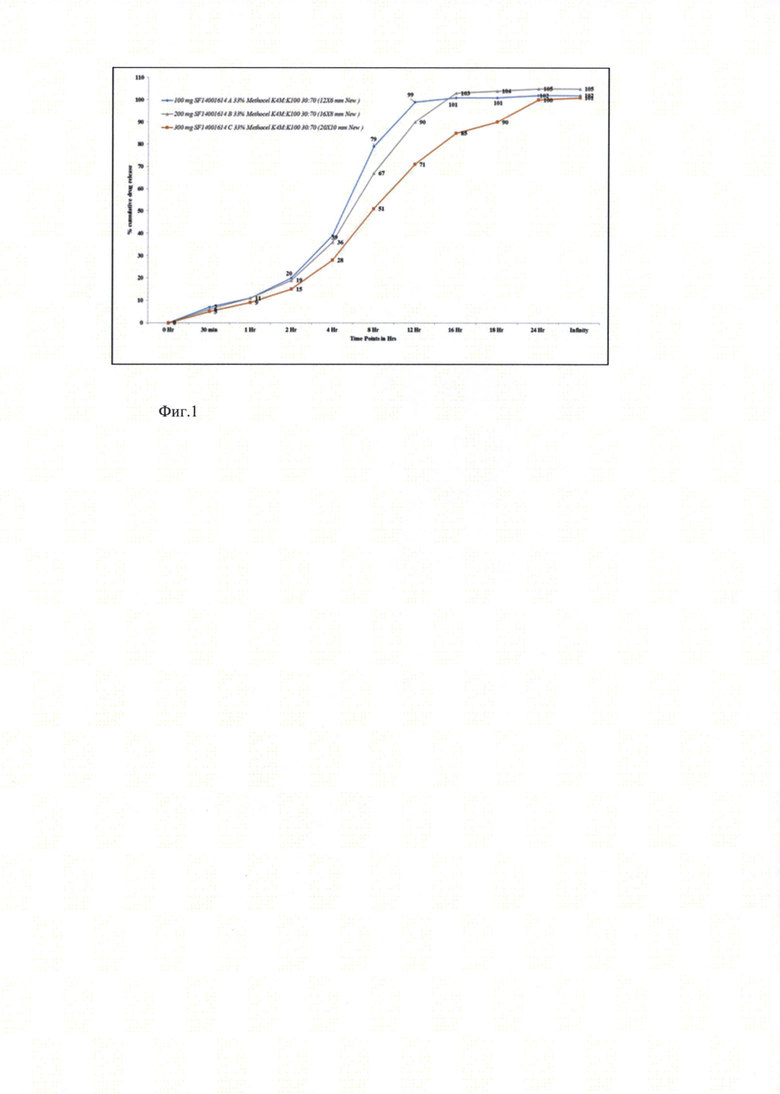
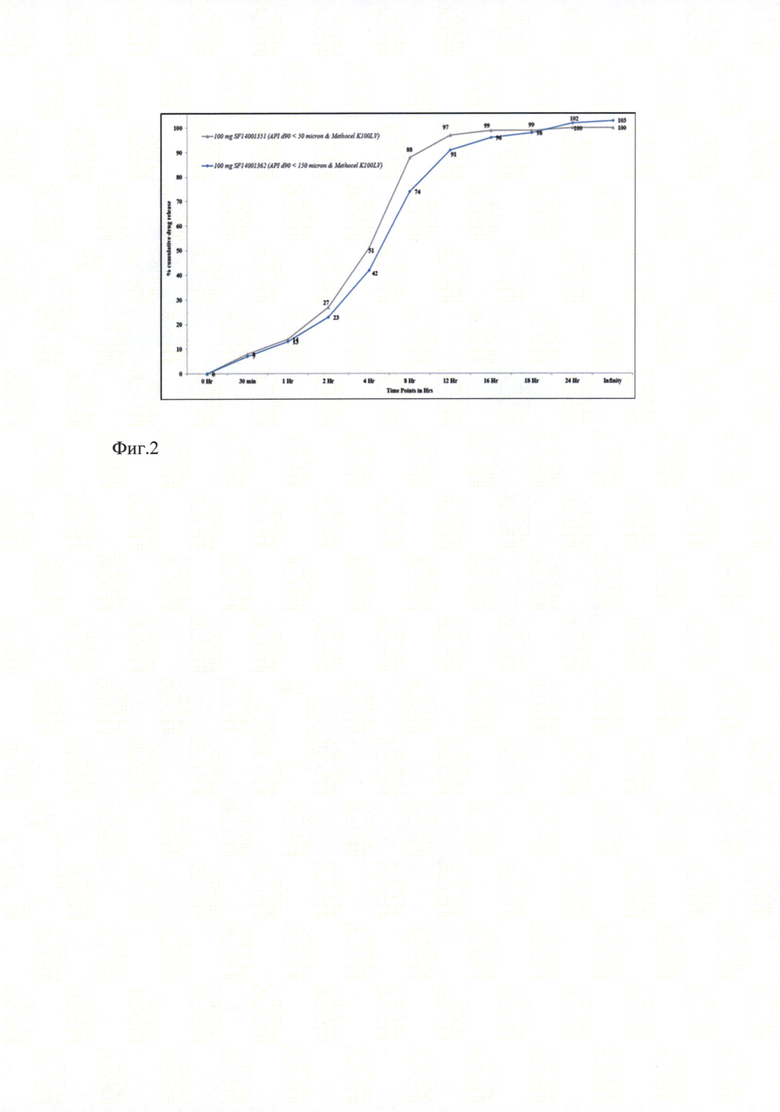
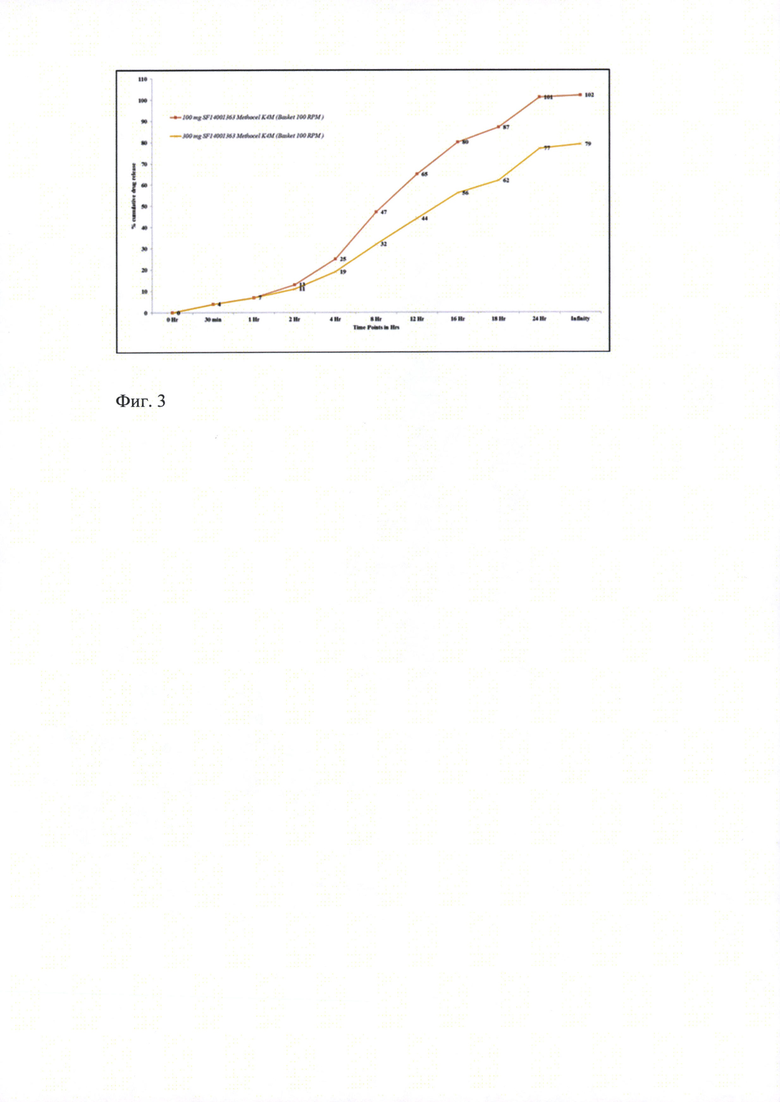
Ранее полученные результаты показали, что использование гидроксипропилметилцеллюлозы одной марки, с одной вязкостью, например как в прототипе или, например одного из метоцел К4М или К100 LV демонстрирует или слишком быстрый, или слишком медленный профиль растворения и всасывания действующего вещества (см. фиг. 1-3). Было обнаружено, что комбинация обоих полимеров К4М и К100 LV дает более высокие результаты стабильности и воспроизводимой кинетики высвобождения активного вещества, особенно в сочетании с коповидоном. Цель серии экспериментов - произвести серию таблеток клозапина замедленного высвобождения (ЗВ) методом вальцевания при использовании полимерной комбинации Метоцел К4М и К100 LV в соотношении 30:70 Серии различались по концентрации активного вещества и полимера в каждой таблетке. Таблетки были упакованы в блистеры из алюминиевой фольги ('Alu-Alu') и помещены в климатическую камеру на 6 месяцев в условия ускоренных и долгосрочных («в реальном времени») испытаний. Содержание примесей определялось методом ВЭЖХ с использованием стандартов.
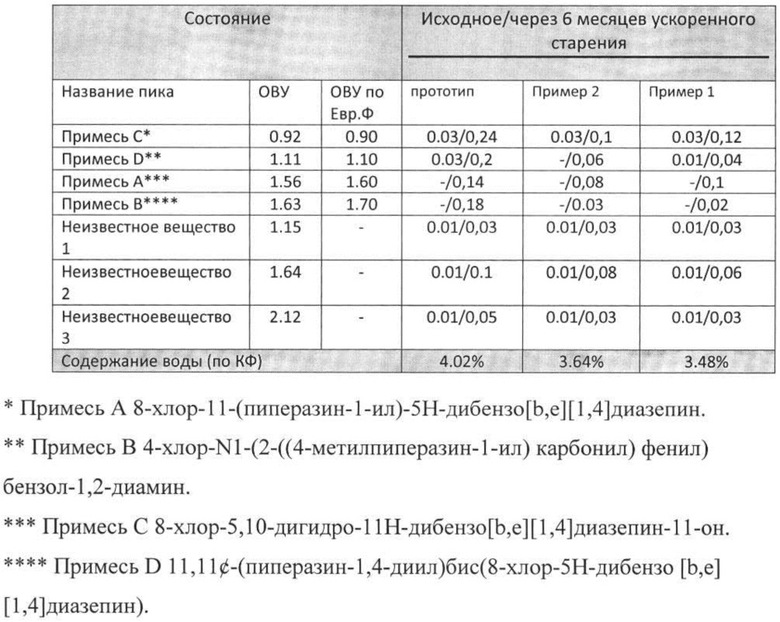
Таким образом предложенный состав имеет преимущества в отношении стабильности.
При исследовании на собаках препарат показал необходимое замедленное действие, максимальная концентрация Клозапина в плазме крови достигается постепенно и не ранее, чем через 4 часа и поддерживается более 23 часов. Относительная биодоступность составила более 50% от состава немедленного высвобождения с эквивалентной дневной дозой на фоне двукратного приема в сутки.
Препарат может широко использоваться в клинической практике как антипсихотический препарат, в частности, при шизофрении, галлюцинаторно-бредовых (бред, видения, приобретающие характер реальности) состояниях, маниакальном синдроме (неадекватно повышенном настроении, ускоренном темпе мышления, психомоторном возбуждении), ухудшении настроения и других психопатических заболеваниях.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ БИОТИН, И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2017 |
|
RU2639488C1 |
| Таблетки биотина с замедленным высвобождением и способ их получения | 2016 |
|
RU2638803C2 |
| Фармацевтическая композиция с модифицированным высвобождением на основе полиморфов клозапина | 2024 |
|
RU2836778C1 |
| ТАБЛЕТКИ КЛОЗАПИНА С ПРОЛОНГИРОВАННЫМ ВЫСВОБОЖДЕНИЕМ | 2016 |
|
RU2613192C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ С ПРОЛОНГИРОВАННЫМ ВЫСВОБОЖДЕНИЕМ С АНТИПСИХОТИЧЕСКОЙ АКТИВНОСТЬЮ И СПОСОБЫ ЕЁ ПОЛУЧЕНИЯ | 2012 |
|
RU2584653C2 |
| ФАРМАЦЕВТИЧЕСКИЙ СОСТАВ ПРОЛОНГИРОВАННОГО ДЕЙСТВИЯ НА ОСНОВЕ КЛОЗАПИНА ПЕРОРАЛЬНОГО ВВЕДЕНИЯ | 2009 |
|
RU2414903C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ПРОЛОНГИРОВАННОГО ДЕЙСТВИЯ, ОБЛАДАЮЩАЯ АНТИДЕПРЕССАНТНЫМ ДЕЙСТВИЕМ | 2008 |
|
RU2377991C1 |
| КОМПОЗИЦИИ С НЕМЕДЛЕННЫМ ВЫСВОБОЖДЕНИЕМ ЛЕКАРСТВЕННОГО СРЕДСТВА | 2010 |
|
RU2541807C2 |
| КОМПОЗИЦИИ С ПРОЛОНГИРОВАННЫМ ВЫСВОБОЖДЕНИЕМ, ВКЛЮЧАЮЩИЕ ЛАМОТРИГИН | 2003 |
|
RU2325163C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ДОРАВИРИН, ТЕНОФОВИРА ДИЗОПРОКСИЛА ФУМАРАТ И ЛАМИВУДИН | 2016 |
|
RU2736941C2 |
Группа изобретений относится к области химико-фармацевтической промышленности, а именно к фармацевтическому составу в виде таблетированной формы с замедленным высвобождением, содержащему 30-40 масс.% клозапина в качестве активного компонента и вспомогательные вещества: 20-35 масс.% Метоцел К100 LV, 10-15 масс.% Метоцел К4М, 12-30 масс.% микрокристаллической целлюлозы, 2-3 масс.% коповидона, 0,5-1 масс.% коллоидного диоксида кремния и 0,5-1 масс.% фармацевтически приемлемой соли стеариновой кислоты, а также к способу получения указанного фармацевтического состава. Группа изобретений обеспечивает получение таблеток клозапина, обладающих стабильностью и воспроизводимой кинетикой замедленного высвобождения активного вещества. 2 н. и 6 з.п. ф-лы, 4 пр., 4 табл., 3 ил.
1. Фармацевтический состав в виде таблетированной формы с замедленным высвобождением, содержащий клозапин в качестве активного компонента и вспомогательные вещества, отличающийся тем, что в качестве вспомогательных веществ содержит смесь Метоцел К100 LV и Метоцел К4М, микрокристаллическую целлюлозу, коповидон, коллоидный диоксид кремния и фармацевтически приемлемую соль стеариновой кислоты при следующем содержании, масс.%:
2. Состав по п. 1, отличающийся тем, что содержит клозапин микронизированный с распределением частиц по размеру d90<50 микрон.
3. Состав по п. 1 или 2, где массовое соотношение Метоцел К4М и Метоцел К100 LV составляет 30:70.
4. Способ получения фармацевтического состава в виде таблетированной формы с замедленным высвобождением по п. 1, характеризующийся тем, что клозапин, комбинацию Метоцел К4М и Метоцел К100 LV, микрокристаллическую целлюлозу и коповидон просеивают вместе, перемешивают до однородности, добавляют магния стеарат, коллоидный диоксид кремния, перемешивают, смесь уплотняют вальцеванием, добавляют коллоидный диоксид и перемешивают вместе с предварительно уплотненными гранулами с последующим добавлением магния стеарата, перемешиванием и прессованием таблеток.
5. Способ по п. 4, характеризующийся тем, что перемешивание ведут при скорости мешалки 20 об/мин.
6. Способ по п. 5, характеризующийся тем, что любую из стадий перемешивания осуществляют в течение 3-6 минут.
7. Способ по п. 4, характеризующийся тем, что на стадии вальцевания использовалась сетка размером 1,6 мм для предварительной грануляции и 0,63 мм - для тонкой грануляции, и процесс осуществляют при гидравлическом давлении 90 бар.
8. Способ по п. 4, характеризующийся тем, что таблетки прессуют в капсулообразной форме.
| ФАРМАЦЕВТИЧЕСКИЙ СОСТАВ ПРОЛОНГИРОВАННОГО ДЕЙСТВИЯ НА ОСНОВЕ КЛОЗАПИНА ПЕРОРАЛЬНОГО ВВЕДЕНИЯ | 2009 |
|
RU2414903C1 |
| US 2014271857 A1, 18.09.2014 | |||
| WO 2004012741 A1, 12.02.2004 | |||
| US 20140030249 A1, 30.01.2014 | |||
| Praveen S | |||
| Hiremath et al | |||
| Controlled Release Hydrophilic Matrix Tablet Formulations of Isoniazid: Design and In Vitro Studies / AAPS PharmSciTech, 2008, Vol.9, N.4, pp.1171-1178 | |||
| Sujit Biswas et al | |||
| Formulation design and in-vitro release profile evaluation of Theophylline hydrochloride sustained release tablet using different polymer at different concentration / Journal of Chemical and Pharmaceutical Research, 2014, Vol.6, N.8, pp.12-23. | |||
Авторы
Даты
2017-07-03—Публикация
2015-12-21—Подача