Область техники, к которой относится изобретение
Изобретение относится к области медицины, медицинской химии и химико-фармацевтической промышленности, в частности, к фармацевтическим композициям на основе нейролептика клозапина.
Предшествующий уровень техники
Психические заболевания ввиду их высокой распространенности является одной из наиболее актуальных проблем медицины. Так, только шизофренией и биполярными расстройствами в мире страдает до 1 % населения [1]. Для лечения таких заболеваний используют антипсихотические препараты или нейролептики, в частности, атипичный нейролептик клозапин. Клозапин обладает сильной антипсихотической, умеренной антиманиакальной и умеренной антидепрессивной активностью в сочетании с выраженным снотворным, седативным и противотревожным действием. Благодаря своим эффектам клозапин применяют для лечения психических заболеваний: шизофрении (в т.ч. при резистентности к терапии другими нейролептиками или их непереносимости), маниакальных состояний, маниакально-депрессивного психоза, психомоторного возбуждения при психопатиях, эмоциональных и поведенческих расстройств (в т.ч. у детей), тяжелых расстройств сна. Как и любой антипсихотический препарат, клозапин вызывает различные побочные негативные эффекты.
Для обеспечения стабильного антипсихотического эффекта и минимизации побочных эффектов оптимальным решением является создание лекарственных форм с модифицированным высвобождением клозапина, которые бы обеспечивали стабильную концентрацию активного вещества в крови в течение суток.
С этой целью предпринимаются попытки создания лекарственных форм с пролонгированным и замедленным высвобождением клозапина. В частности, в патенте RU2414903 описан фармацевтический состав пролонгированного действия на основе клозапина перорального введения, где в качестве веществ-пролонгаторов использованы гидроксипропилметилцеллюлоза и модифицированная диоксидом кремния микрокристаллическая целлюлоза [2]. В патенте RU2613192 описаны таблетки клозапина с пролонгированным высвобождением, где для пролонгации использована гидроксипропилметилцеллюлоза марок ГПМЦ K15М и ГПМЦ 2910 [3]. В патенте RU2624229 описаны таблетки клозапина с замедленным высвобождением и способ их получения, где замедленное высвобождение обеспечивается применением метилцеллюлозы марок Метоцел К4М и Метоцел К100 LV [4].
Наиболее близким аналогом настоящего изобретения является фармацевтический состав клозапина с пролонгированным высвобождением в виде таблеток, описанный в патенте RU2613192, содержащий следующие компоненты, мас.%:
при этом пленочная оболочка включает поливиниловый спирт, диоксид титана,
макрогол и приемлемые красители или смесь Опадрай II желтый.
Способ получения данного состава характеризуется тем, что клозапин, микрокристаллическую целлюлозу, лактозы моногидрат и комбинацию гидроксипропилметилцеллюлозы ГПМЦ К15М и гидроксипропилметилцеллюлозы ГПМЦ 2910 просеивают вместе, перемешивают в течение 3-6 мин при скорости мешалки 20 об/мин до однородности, добавляют фармацевтически приемлемую соль стеариновой кислоты и коллоидный диоксид кремния, перемешивают, смесь уплотняют вальцеванием с использованием сетки размером 1,6 мм для предварительной грануляции и сетки размером 0,63 мм для тонкой грануляции, процесс осуществляют при гидравлическом давлении 90 бар, добавляют коллоидный диоксид кремния и перемешивают вместе с предварительно уплотненными гранулами с последующим добавлением фармацевтически приемлемой соли стеариновой кислоты, перемешиванием, прессованием таблеток и нанесением на таблетки пленочного покрытия.
К недостаткам прототипа можно отнести особенности фармакокинетики, которые могут влиять на клиническую эффективность препарата. С одной стороны, описанные в прототипе и других указанных выше патентах фармацевтические составы с замедленным или пролонгированным высвобождением клозапина позволяют поддерживать эффективные концентрации активного вещества в плазме крови в течение более длительного времени (более 23 часов), чем фармацевтические составы с немедленным высвобождением. Однако, вследствие замедленного растворения, всасывания и соответственно замедленного достижения максимальной концентрации активного вещества в плазме крови (не ранее, чем через 10 ч), также с задержкой развивается фармакологический эффект, что негативно влияет на клиническую эффективность препарата.
Недостатки имеет и технология получения фармацевтических составов, описанная в прототипе. Дело в том, что субстанция клозапина обладает низкой способностью к прессованию - согласно собственным данным прессуемость образцов субстанции клозапина не превышает 10 Н. Поэтому метод прямого прессования даже при введении наполнителей не обеспечивает достаточную прочность таблеток клозапина на излом (раздавливание), которая составляет не более 40-45 Н (при норме не менее 60 Н), и истираемость - 96,0-96,2 % (при норме не менее 99 %), что негативно отражается на качестве таблеток при дальнейшем нанесении плёночной оболочки. Описанный в прототипе метод вальцевания основан на принципе компактирования сухой смеси, состоящей из активного вещества и вспомогательных компонентов. Но поскольку прессуемость смеси клозапина с наполнителями низкая, то для формирования твёрдых вальцовых компактов (брикетов) требуется достаточно высокое давление уплотнения. Уплотнение компактов (брикетов) для получения в дальнейшем прочных таблеток зачастую приводит к агломерации частиц, сначала в результате спекания и частичного плавления, а затем образования твёрдых молекулярных мостиков между частицами в результате химической реакции. Поэтому высвобождение действующего вещества из таких частиц происходит неоднородно, нелинейно (скачкообразно) и не воспроизводимо от серии к серии. Кроме того, массы, полученные вальцеванием малопластичны, так как содержат большое количество мелкой фракции и характеризуются низкой массовой долей воды из-за отсутствия увлажнения. Поэтому, для придания получаемым таблеткам удовлетворительных технологических показателей необходимо повышать давление прессования. В результате снижается пористость таблеток, удлиняется время набухания полимера и, как результат, падает степень высвобождения активного вещества (пример 4, фиг. 1). Из-за неоднородности высвобождения относительное стандартное отклонение во временных точках профиля растворения превышает норму: в точке 1 час составляет от 21 до 25 % при норме не более 20 %, в точке 4 часа - от 16,5 до 35 % при норме не более 10 %. К тому же, поскольку активная субстанция имеет жёлто-зелёное окрашивание, то при компактировании получаются неоднородные по оттенку гранулы, что отражается на качестве таблеток-ядер по показателю «описание» (пример 3, табл. 1).
Сущность изобретения
Задача настоящего изобретения - разработать фармацевтический состав, который сочетал бы совершенно противоположные свойства: с одной стороны, обеспечивал более быстрое высвобождение активного вещества и, соответственно, более быстрое (в частности, в сравнении с прототипом) достижение максимальной концентрации клозапина в плазме крови, а, с другой стороны, - сохранял пролонгированный характер высвобождения с длительным поддержанием эффективных концентраций клозапина в плазме крови.
Задача решается посредством получения фармацевтической композиции для лечения психического заболевания с модифицированным высвобождением клозапина в виде таблетки, покрытой пленочной оболочкой, содержащей в качестве действующего вещества кристаллический полиморф моногидрата клозапина (описанный как в настоящем документе, так и в патенте RU2715717) и определенный набор вспомогательных веществ, которые в совокупности обеспечивают оптимальный профиль высвобождения и фармакокинетики клозапина.
В одном аспекте настоящего изобретения фармацевтическая композиция для лечения психического заболевания с модифицированным высвобождением клозапина в виде таблетки, покрытой пленочной оболочкой, содержит следующие компоненты, мас.% в расчете на таблетку-ядро:
Клозапин в виде кристаллического полиморфа моногидрата клозапина,
характеризующегося отражением рентгеновского излучения, фиксированным на рентгеновской порошковой дифрактограмме при использовании CuKα1-излучения (длина волны 1,54056 Å) при 10,48, 10,84, 13,44, 13,94, 17,86, 18,36, 20,96, 23,14, 24,00 и 33,00 градусах 2 тета ± 0,2 градуса 2 тета (форма 1)
или
характеризующегося отражением рентгеновского излучения, фиксированным на рентгеновской порошковой дифрактограмме при использовании CuKα1-излучения (длина волны 1,54056Å) при 10,48, 10,84, 12,04, 13,92, 17,84, 20,94, 23,16, 23,96, 32,86 и 33,04 градусах 2 тета ± 0,2 градуса 2 тета (форма 2)
причем пленочная оболочка содержит поливиниловый спирт, титана диоксид, полиэтиленгликоль, тальк, алюминиевый лак хинолиновый желтый и железа оксид красный.
В частных вариантах воплощения изобретения психическое заболевание представляет собой шизофрению, маниакальное состояние, маниакально-депрессивный психоз, психомоторное возбуждение при психопатиях, эмоциональное и поведенческое расстройство, расстройство сна.
В частных вариантах воплощения изобретения композиция включает:
Клозапин в виде кристаллического полиморфа моногидрата клозапина, характеризующегося отражением рентгеновского излучения, фиксированным на рентгеновской порошковой дифрактограмме при использовании CuKα1-излучения (длина волны 1,54056Å) при 10,48, 10,84, 13,44, 13,94, 17,86, 18,36, 20,96, 23,14, 24,00 и 33,00 градусах 2 тета ± 0,2 градуса 2 тета (форма 1)
причем пленочная оболочка содержит поливиниловый спирт, титана диоксид, полиэтиленгликоль, тальк, алюминиевый лак хинолиновый желтый и железа оксид красный.
Помимо этого, поставленная задача решается посредством разработки способа получения вышеуказанной композиции, основанного на методе влажной грануляции, который позволяет получить композиции с более быстрым и одновременно равномерным и пролонгированным высвобождением действующего вещества из таблеток.
Поэтому предметом настоящего изобретения также является способ получения фармацевтической композиции по изобретению.
В одном аспекте настоящего изобретения способ получения фармацевтической композиции для лечения психического заболевания с модифицированным высвобождением клозапина в виде таблетки, покрытой пленочной оболочкой, включает следующие этапы:
- кристаллический полиморф моногидрата клозапина, микрокристаллическую целлюлозу, лактозы моногидрат, и кремния диоксид коллоидный просеивают;
- получают связующий и смачивающий компонент, представляющий собой 3-7 % водный раствор гидроксипропилметилцеллюлозы марки 2910 (тип 606), повидона марки К-17 или смесь указанных растворов;
- кристаллический полиморф моногидрата клозапина, микрокристаллическую целлюлозу и лактозы моногидрат перемешивают до однородности, добавляют связующий и смачивающий компонент и снова перемешивают;
- полученную влажную смесь сушат и проводят грануляцию;
- сгранулированную массу перемешивают с гидроксипропилметилцеллюлозой марки К15М CR, затем добавляют кремния диоксид коллоидный и магния стеарат;
- полученную смесь таблетируют прессованием и затем таблетки покрывают пленочной оболочкой.
В частных вариантах воплощения изобретения сушку влажной смеси проводят в установке псевдоожиженного слоя при температуре 50-60°С до массовой доли воды 1,0-2,0 %.
В частных вариантах воплощения изобретения грануляцию проводят через проволочную сетку с размером отверстий 1,0-1,5 мм.
В частных вариантах воплощения изобретения сгранулированную массу загружают в смеситель и перемешивают с гидроксипропилметилцеллюлозой К 15М CR в течение 3-7 минут.
В частных вариантах воплощения изобретения сгранулированную массу загружают в смеситель и перемешивают с гидроксипропилметилцеллюлозой К 15М CR в течение 5 мин, затем добавляют кремния диоксид коллоидный и магния стеарат и перемешивают в течение 3-5 мин.
В частных вариантах воплощения изобретения водный раствор связующего и смачивающего компонента представляет собой 5 % раствор.
В результате осуществления изобретения достигаются следующие технические результаты:
- разработана новая фармацевтическая композиция для лечения психического заболевания с модифицированным высвобождением клозапина в виде таблетки, покрытой пленочной оболочкой, на основе кристаллического полиморфа клозапина, причем указанная композиция сочетает быстрое высвобождение клозапина и быстрое достижение его максимальной концентрации в плазме крови с пролонгированным характером высвобождения и длительным поддержанием эффективной концентрации в плазме крови;
- фармацевтическая композиция по изобретению характеризуется свойствами, которые очень важны в клинической практике для обеспечения быстро достигаемого и стабильного в течение суток клинического эффекта у больных психическими заболеваниями при однократном приеме препарата;
- разработан новый и эффективный способ получения фармацевтической композиции для лечения психического заболевания с модифицированным высвобождением клозапина в виде таблетки, покрытой пленочной оболочкой на основе влажной грануляции, причем указанный способ позволяет получить композиции с более быстрым и одновременно равномерным и пролонгированным высвобождением активного вещества из таблеток;
- способ по изобретению обеспечивает улучшенные (в частности, по сравнению с прототипом) характеристики таблеточной массы по описанию, фракционному составу, насыпной плотности, сыпучести и прессуемости, важные с точки зрения технологичности процесса и обеспечения равномерного пролонгированного высвобождения активного вещества.
Подробное раскрытие изобретения
Краткое описание чертежей
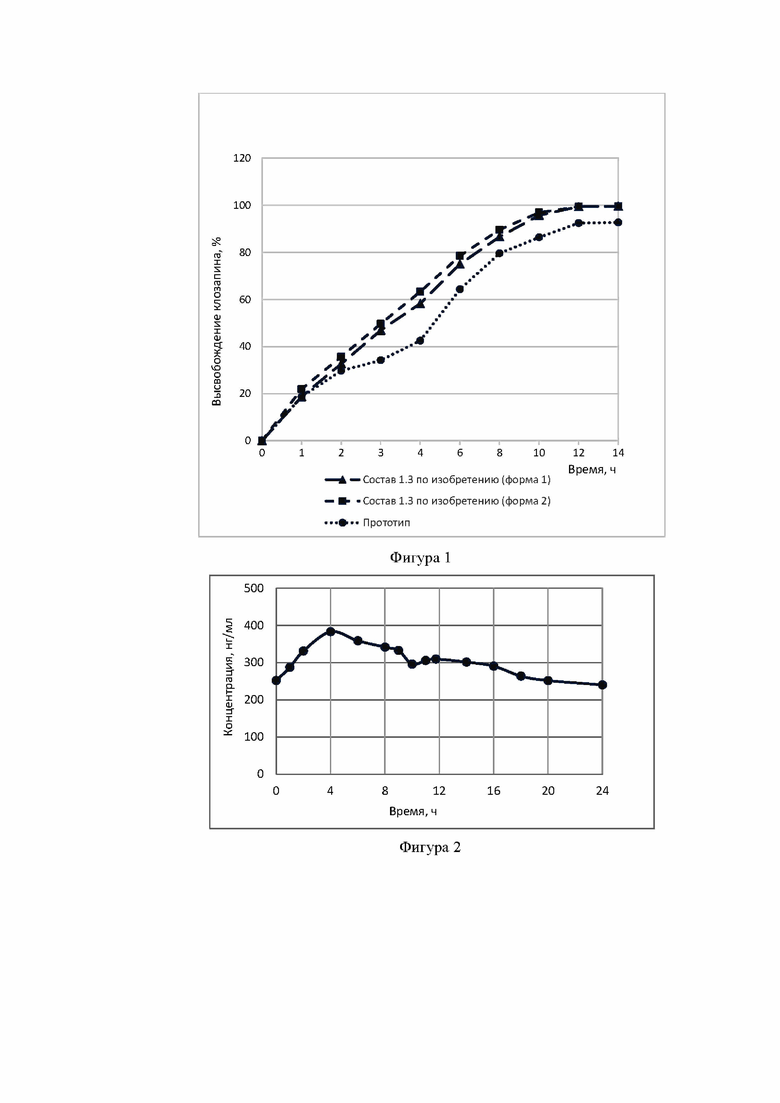
Фигура 1. Кинетика высвобождения клозапина из фармацевтических композиций. На данной фигуре изображена кинетика высвобождения клозапина из фармацевтических композиций по изобретению - состава 1.3 (форма 1) и состава 1.3 (форма 2) в сравнении с прототипом.
Фигура 2. Фармакокинетический профиль клозапина в плазме крови человека. На данной фигуре изображена динамика концентрации клозапина в плазме крови человека (пациентов с диагнозом шизофрения) на 14-й день ежедневного однократного приема фармацевтической композиции по изобретению - состава 1.3 (форма 1).
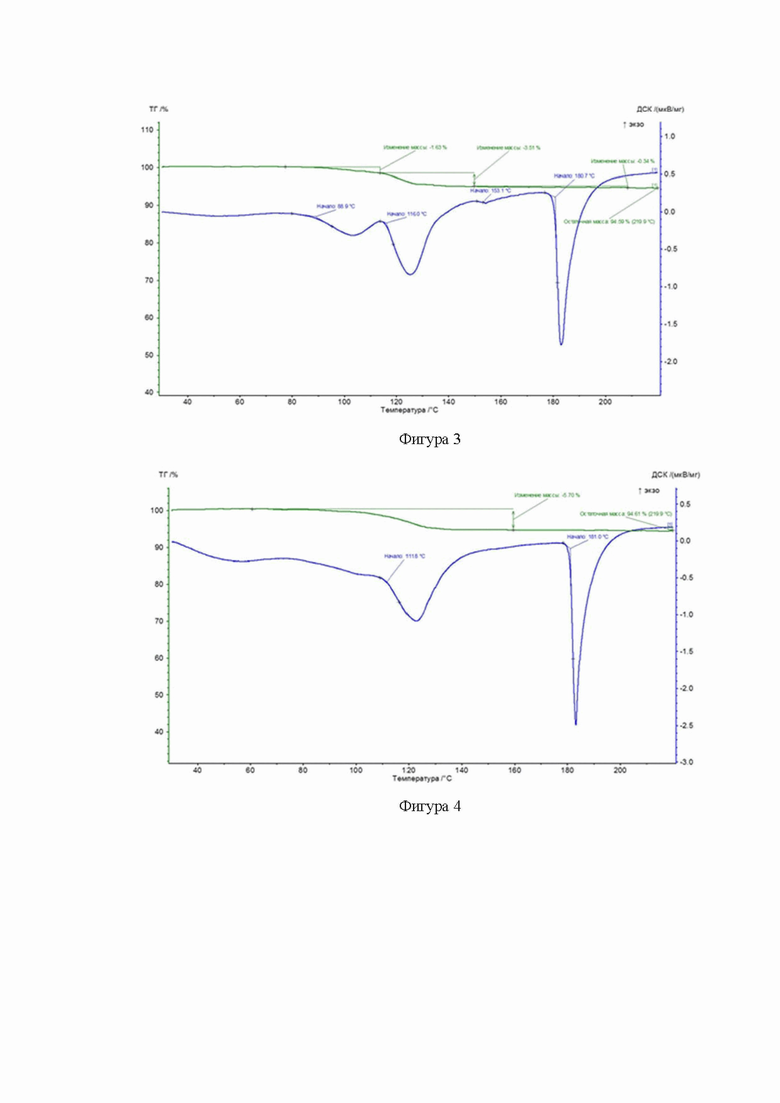
Фигура 3. TGA-диаграмма кристаллического полиморфа моногидрата клозапина формы 1. На данной фигуре представлена диаграмма термогравиметрического анализа кристаллического полиморфа моногидрата клозапина формы 1 при его нагревании в сухой среде.
Фигура 4. TGA-диаграмма кристаллического полиморфа моногидрата клозапина формы 2. На данной фигуре представлена диаграмма термогравиметрического анализа кристаллического полиморфа моногидрата клозапина формы 2 при его нагревании в сухой среде.
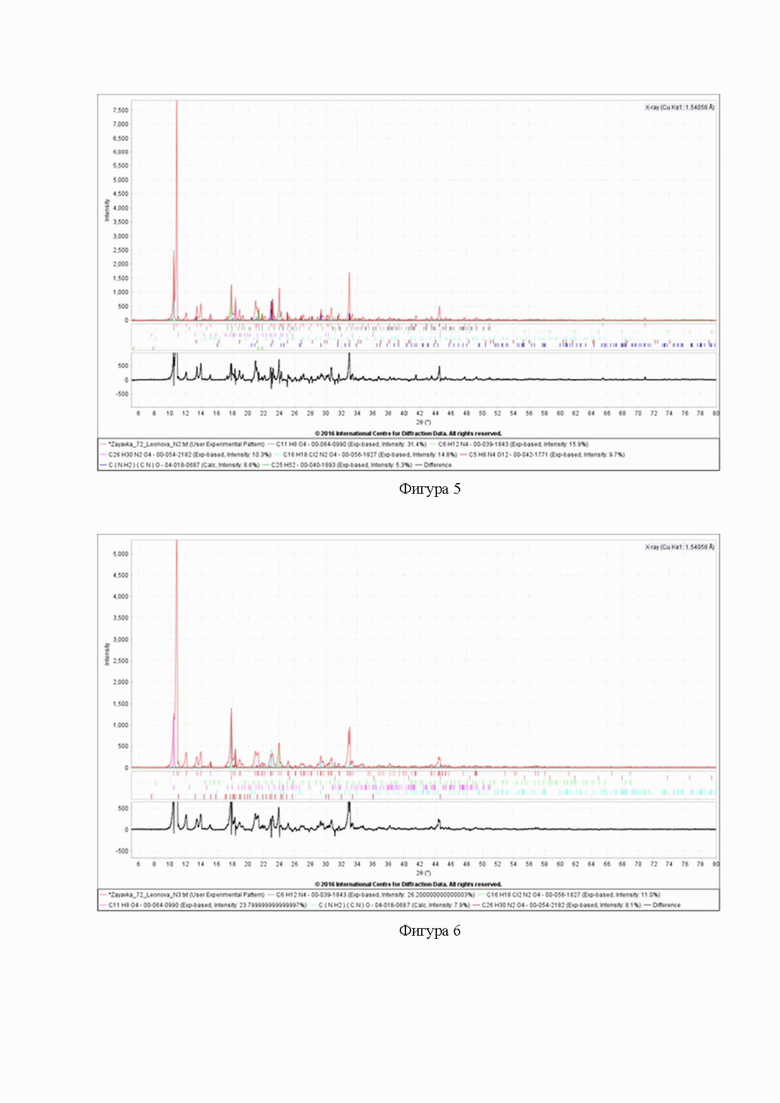
Фигура 5. Дифрактограмма кристаллического полиморфа моногидрата клозапина формы 1. На данной фигуре представлена рентгеновская порошковая дифрактограмма кристаллического полиморфа моногидрата клозапина формы 1 при использовании CuKα1-излучения.
Фигура 6. Дифрактограмма кристаллического полиморфа моногидрата клозапина формы 2. На данной фигуре представлена рентгеновская порошковая дифрактограмма кристаллического полиморфа моногидрата клозапина формы 2 при использовании CuKα1-излучения.
Определения (термины)
Для лучшего понимания настоящего изобретения ниже приведены некоторые термины, использованные в настоящем описании изобретения. Следующие определения применяются в данном документе, если иное не указано явно.
Если термины специально не определены где-либо в данном документе, то все технические и научные термины, используемые в данном документе, имеют значение, общепринятые для специалиста в той области техники, к которой относится это изобретение.
В настоящем описании и в последующей формуле изобретения, если контекстом не предусмотрено иное, слова «иметь», «включать» и «содержать» или их вариации, например, такие как «имеет», «имеющий», «включает», «включающий», «содержит» или «содержащий», следует понимать, как включение указанного целого или группы целых, но не исключение любого другого целого или группы целых. Указанные термины не предназначены для того, чтобы их истолковывали как «состоит только из».
Также здесь перечисление числовых диапазонов по конечным точкам включает все числа, входящие в этот диапазон.
Действующее вещество по изобретению представляет собой кристаллический полиморф (форма 1 или форма 2) моногидрата клозапина. Обе формы, а также способы их получения, подробно описаны и раскрыты в документе RU2715717, который включен в настоящий документ в качестве ссылки. Так, в частности, кристаллический полиморф моногидрата клозапина формы 1 может характеризоваться TGA-диаграммой, представленной на фиг. 3. При нагревании моногидрата в сухой среде, значительная потеря массы начинается уже при слегка повышенной температуре и заканчивается при температуре приблизительно 110°С. В данном примере диаграмма показывает потерю массы 0,57 мг воды, соответствующую 5,2 мас.% воды, которая означает, что данный образец потерял приблизительно 1 моль воды на моль клозапина при нагревании.
Кристаллический полиморф моногидрата клозапина формы 2 может характеризоваться TGA-диаграммой, представленной на фиг. 4. При нагревании моногидрата в сухой среде, значительная потеря массы начинается уже при слегка повышенной температуре и заканчивается при температуре приблизительно 110°С. В данном примере диаграмма показывает потерю массы 0,57 мг воды, соответствующую 5,2 мас.% воды, которая означает, что данный образец потерял приблизительно
1 моль воды на моль клозапина при нагревании.
Кристаллический полиморф моногидрата клозапина формы 1 может также характеризоваться картиной дифракции рентгеновских лучей, по существу, такой картиной, как представленная на фиг. 5. Картина была получена при использовании CuKα1-излучения в трансмиссионном режиме, где интенсивности отражений, изображенные на фигуре, а также интенсивности отражений, установленные выше, не являются необходимым предварительным условием, а могут изменяться.
Кристаллический полиморф моногидрата клозапина формы 2 может также характеризоваться картиной дифракции рентгеновских лучей, по существу, такой картиной, как представленная на фиг. 6. Картина была получена при использовании CuKα1-излучения в трансмиссионном режиме, где интенсивности отражений, изображенные на фигуре, а также интенсивности отражений, установленные выше, не являются необходимым предварительным условием, а могут изменяться.
Осуществление изобретения
Известно, что кристаллические полиморфы веществ могут различаться по физико-химическим свойствам, в том числе по растворимости в различных средах [6]. Известно также, что кристаллические гидраты органических веществ могут обладать лучшей растворимостью в воде, хотя при этом авторы отмечают проблему стабильности кристаллогидратов и сложность прогнозирования их растворимости [7, 8]. Поэтому использование в фармацевтической композиции кристаллических полиморфов гидратов активных соединений потенциально может приводить к более быстрому и полному высвобождению активного соединения, в частности, из таблеток. Следовательно, лучшая растворимость кристаллических полиморфов гидратов (в том числе кристаллических полиморфов моногидрата клозапина) сама по себе не является неожиданной. При этом, зная об улучшенной растворимости для таких кристаллических полиморфов, очевидно ожидать потерю пролонгированного характера высвобождения и получение состава с немедленным высвобождением, в том числе и клозапина. Однако, благодаря разработке композиции на основе определенных кристаллических полиморфов моногидрата клозапина по изобретению совместно с определенными вспомогательными веществами, а также благодаря способу получения композицию по изобретению, удалось добиться неожиданного результата: новая фармацевтическая композиция с модифицированным высвобождением сочетает быстрое высвобождение клозапина и быстрое достижение его максимальной концентрации в плазме крови с пролонгированным характером высвобождения и длительным поддержанием эффективной концентрации в плазме крови. Хотя в случае улучшенной растворимости действующего вещества следовало ожидать потери пролонгированности высвобождения и менее длительного поддержания эффективной концентрации в плазме крови. Неожиданно установленные свойства новой фармацевтической композиции по изобретению очень важны в клинической практике для обеспечения быстро достигаемого и стабильного в течение суток клинического эффекта у больных психическими заболеваниями при однократном приеме препарата.
Для получения таблеточных масс на основе композиции заявленного состава с кристаллическими полиморфами моногидратов клозапина потребовалось разработать технологию получения такой композиции. Помимо этого, способ получения фармацевтической композиции по изобретению также влияет на обеспечение свойств этой композиции, указанных выше. На основании проведённых исследований по разработке технологии приготовления таблеточных масс клозапина с модифицированным высвобождением за основу был использован метод влажной грануляции смеси, состоящей из полиморфов клозапина и наполнителей - целлюлозы микрокристаллической и лактозы моногидрата. В качестве связующих компонентов для влажной грануляции использовалась гидроксипропилметилцеллюлоза низкой вязкости - марки 2910 (тип 606), повидон марки К-17 или их смеси. Полученные указанным способом фармацевтические композиции обеспечивают более быстрое и одновременно равномерное и пролонгированное высвобождение активного вещества из таблеток, в соответствии с заданными параметрами в установленные временные интервалы. Улучшенный профиль растворения неожиданно также приводит к аналогичным положительным изменениям фармакокинетического профиля: при введении композиции по заявленному изобретению максимальная концентрация в плазме крови человека достигается уже через 4-6 ч; период полувыведения составляет 24-26 ч, что обеспечивает поддержание эффективной концентрации клозапина в плазме крови в течение более 24 ч. Такая фармакокинетика обеспечивает стабильный уровень препарата в плазме крови и стабильный клинический эффект препарата при его ежедневном однократном применении.
Для наилучшего понимания изобретения приводятся следующие примеры. Эти примеры приведены только в иллюстративных целях и не должны толковаться как ограничивающие сферу применения изобретения в любой форме.
Пример 1 Варианты составов фармацевтических композиций по изобретению
Состав 1 (варианты состава 1.1 - 1.4):
- кристаллического полиморфа (форма 1) моногидрата клозапина, характеризующегося отражением рентгеновского излучения, фиксированным на рентгеновской порошковой дифрактограмме при использовании CuKα1-излучения (длина волны 1,54056Å) при 10,48, 10,84, 13,44, 13,94, 17,86, 18,36, 20,96, 23,14, 24,00 и 33,00 градусах 2 тета ± 0,2 градуса 2 тета,
или
- кристаллического полиморфа (форма 2) моногидрата клозапина характеризующегося отражением рентгеновского излучения, фиксированным на рентгеновской порошковой дифрактограмме при использовании CuKα1-излучения (длина волны 1,54056Å) при 10,48, 10,84, 12,04, 13,92, 17,84, 20,94, 23,16, 23,96, 32,86 и 33,04 градусах 2 тета ± 0,2 градуса 2 тета
Состав 2 (варианты состава 2.1 - 2.5):
- кристаллического полиморфа (форма 1) моногидрата клозапина, характеризующегося отражением рентгеновского излучения, фиксированным на рентгеновской порошковой дифрактограмме при использовании CuKα1-излучения (длина волны 1,54056Å) при 10,48, 10,84, 13,44, 13,94, 17,86, 18,36, 20,96, 23,14, 24,00 и 33,00 градусах 2 тета ± 0,2 градуса 2 тета,
или
- кристаллического полиморфа (форма 2) моногидрата клозапина характеризующегося отражением рентгеновского излучения, фиксированным на рентгеновской порошковой дифрактограмме при использовании CuKα1-излучения (длина волны 1,54056Å) при 10,48, 10,84, 12,04, 13,92, 17,84, 20,94, 23,16, 23,96, 32,86 и 33,04 градусах 2 тета ± 0,2 градуса 2 тета
Состав 3 (варианты состава 3.1 - 3.5):
- кристаллического полиморфа (форма 1) моногидрата клозапина, характеризующегося отражением рентгеновского излучения, фиксированным на рентгеновской порошковой дифрактограмме при использовании CuKα1-излучения (длина волны 1,54056Å) при 10,48, 10,84, 13,44, 13,94, 17,86, 18,36, 20,96, 23,14, 24,00 и 33,00 градусах 2 тета ± 0,2 градуса 2 тета,
или
- кристаллического полиморфа (форма 2) моногидрата клозапина характеризующегося отражением рентгеновского излучения, фиксированным на рентгеновской порошковой дифрактограмме при использовании CuKα1-излучения (длина волны 1,54056Å) при 10,48, 10,84, 12,04, 13,92, 17,84, 20,94, 23,16, 23,96, 32,86 и 33,04 градусах 2 тета ± 0,2 градуса 2 тета
Состав 4 (варианты состава 4.1 - 4.5):
- кристаллического полиморфа (форма 1) моногидрата клозапина, характеризующегося отражением рентгеновского излучения, фиксированным на рентгеновской порошковой дифрактограмме при использовании CuKα1-излучения (длина волны 1,54056Å) при 10,48, 10,84, 13,44, 13,94, 17,86, 18,36, 20,96, 23,14, 24,00 и 33,00 градусах 2 тета ± 0,2 градуса 2 тета,
или
- кристаллического полиморфа (форма 2) моногидрата клозапина характеризующегося отражением рентгеновского излучения, фиксированным на рентгеновской порошковой дифрактограмме при использовании CuKα1-излучения (длина волны 1,54056Å) при 10,48, 10,84, 12,04, 13,92, 17,84, 20,94, 23,16, 23,96, 32,86 и 33,04 градусах 2 тета ± 0,2 градуса 2 тета
Пример 2 Технология получения фармацевтической композиции
Ниже описан способ получения фармацевтической композиции (таблетки, покрытые оболочкой, состав 1.3 из примера 1, содержание клозапина в таблетке - 200 мг) по изобретению с использованием лабораторного оборудования.
Для удаления из сырья механических включений и крупной фракции сырьё: кристаллический полиморф моногидрата клозапина, микрокристаллическую целлюлозу, лактозы моногидрат, кремния диоксид коллоидный и магния стеарат просеивают отдельно на ситах через капроновые сетки.
В качестве увлажнителя (связующий и смачивающий компонент) используют 5 % раствор гидроксипропилметилцеллюлозы марки 2910 (тип 606). Для приготовления увлажнителя из 0,063 кг гидроксипропилметилцеллюлозы 2910 (тип 606) и 1,19 кг воды очищенной готовят 5 % раствор путём растворения при перемешивании и дальнейшей фильтрации через капроновое сито.
Для получения таблеточной массы методом влажной грануляции в горизонтальный смеситель загружают целлюлозу микрокристаллическую, лактозы моногидрат, клозапин и перемешивают в течение 10-15 мин. В один приём вносят увлажнитель - 5 % раствор гидроксипропилметилцеллюлозы 2910 (тип 606) и перемешивают в течение (5-7) мин. Влажную массу сушат в установке псевдоожиженного слоя при температуре 50-60°С до массовой доли воды 1,0-2,0 %, затем просеивают через металлическую сетку с размером отверстий 1,0-1,5 мм.
Сгранулированную массу вновь загружают в смеситель, добавляют отвешенное количество (0,60 кг) гидроксипропилметилцеллюлозы К 15М CR и перемешивают в течение 5 мин. Затем, в полученную массу загружают кремния диоксид коллоидный
(0,06 кг) и магния стеарат (0,03 кг), перемешивают в течение 3-5 мин.
Из полученной таблеточной массы отбирают пробу для определения массовой доли воды (1,5-2,5 %). При положительном результате анализа таблеточную массу выгружают из смесителя, просеивая его через металлическую сетку с ячейками размером 1,0-1,5 мм.
Выход таблеточной массы составляет от 96 до 100 % от массы субстанции и вспомогательных веществ, загруженных на стадию получения таблеточной массы.
Таблетирование проводят на роторном таблеточном прессе РТМ-12 пуансонами двояковогнутой формы (радиус кривизны 1,1·D), диаметром 12 мм ± 0,05 мм. Получают таблетки-ядра клозапина со средней массой 470 мг ± 5 % (от 447 мг до 494 мг), прочностью на излом ~ 90 Н; прочностью на истирание - не менее 98,0 %.
Для приготовления суспензии для плёночной оболочки в колбу, снабженную мешалкой, загружают 1,22 кг воды очищенной комнатной температуры. Затем постепенно, при постоянном перемешивании, загружают плёнкообразующую систему опадрай II желтый (содержащую в своем составе поливиниловый спирт, титана диоксид, полиэтиленгликоль, тальк, алюминиевый лак хинолиновый желтый и железа оксид красный) - 0,22 кг и продолжают перемешивание в течение 40-45 минут. Приготовленную суспензию фильтруют через капроновую сетку.
Нанесение плёночной оболочки проводят на лабораторном дражировочном котле фирмы «Erweka». В сухой и чистый котёл загружают таблетки-ядра клозапина 200 мг и обкатывают их в течение 2-3 минут. После обкатки таблетки-ядра обеспыливают, удаляя таблетки с нарушенной поверхностью. Обкатанные таблетки должны иметь ровные края, не иметь на поверхности пыльцы. Одновременно с обкаткой ведут прогрев таблеток до температуры в слое 42-45°С. Перед подачей плёнкообразующей суспензии вне котла настраивают факел распыления, регулируя подачу сжатого воздуха, размер частиц распыляемой суспензии и угол конуса распыления.
Процесс распыления суспензии ведут в следующем технологическом режиме:
- давление сжатого воздуха на распылении - 1,3-1,5 атм;
- температура в слое таблеток во время процесса - 32-38°С;
- скорость насоса при подаче суспензии - 2-5 об/мин.
Нанесение суспензии ведут до достижения средней массы таблеток 485 мг ± 5 % (от 461 мг до 509 мг). Масса оболочки на основе плёнкообразущей системы составляет ~ 3 % от массы таблетки, покрытой оболочкой. Расход суспензии при нанесении оболочки в лабораторном котле составляет ~ 0,30-0,35 кг на 1 кг таблеток-ядер. Время покрытия таблеток-ядер (на лабораторном котле) составляет 3-3,5 часа. Полученная оболочка должна иметь ровную, гладкую поверхность. По окончании нанесения плёнки на таблетки, останавливают подачу суспензии, а таблетки продолжают вращать, отключив подачу тёплого воздуха с целью предотвращения слипания таблеток. Проводят отбраковку таблеток по внешнему виду.
Пример 3 Сравнение характеристик таблеточных масс, полученных методами влажной грануляции и методом вальцевания
Сравнили физические и технологические характеристики таблеточных масс, полученных методом влажной грануляции (по заявленному изобретению) и методом вальцевания (согласно прототипу). Для удобства сравнения обоими методами были получены таблеточные массы, содержащие клозапин и вспомогательные вещества в соответствие с примером 1, состав 1.3 (полиморф - форма 1), который идентичен прототипу по составу вспомогательных веществ и отличается от прототипа только использованием в качестве действующего вещества определенного кристаллического полиморфа (формы 1) клозапина. Изученные характеристики таблеточных масс приведены в таблице 1.
Таблица 1. Характеристики таблеточных масс, полученных способом по изобретению и способом сравнения.
(по изобретению)
(согласно прототипу)
> 200 мкм, %;
≤ 200 мкм, %
45
78
Как показывают представленные результаты, метод влажной грануляции, использованный в настоящем изобретении, обеспечивает, в сравнении с методом вальцевания, лучшие характеристики таблеточной массы по описанию, фракционному составу, насыпной плотности, сыпучести и прессуемости, важные с точки зрения технологичности процесса и обеспечения равномерного пролонгированного высвобождения клозапина.
Пример 4 Профиль высвобождения клозапина из фармацевтических композиций на основе кристаллических полиморфов моногидрата клозапина
Сравнивали кинетику высвобождения клозапина из заявленных фармацевтических композиций (состав 1.3 из примера 1), содержащих в качестве действующего вещества кристаллические полиморфы (формы 1 или 2) моногидрата клозапина, и композицию по прототипу, содержащую в качестве действующего вещества клозапин безводный, который стандартно используется различными фармпроизводителями для производства лекарственных средств на основе клозапина. Все три композиции содержали одинаковое количество клозапина - 200 мг на 1 таблетку, и одни и те же вспомогательные вещества, как прописано в примере 1 для состава 1.3. В качестве среды использовали солянокислый буферный раствор с pH 1,2. Результаты анализа приведены на фиг. 1.
Как показывают представленные результаты, фармацевтические композиции, содержащие кристаллический полиморф (формы 1 или 2) моногидрата клозапина и вспомогательные вещества по заявленному изобретению, полученные с использованием технологии влажной грануляции, обеспечивают равномерное и полное высвобождение клозапина, сохраняя при этом пролонгированный характер высвобождения. Также необходимо отметить, что фармацевтические композиции по заявленному изобретению обеспечивают более быстрое высвобождение действующего вещества из таблеток в сравнении с прототипом: через 1 час - около 20 %; через 4 часа - от 55 до 65 %; через 8 часов - более 80 % с достижением максимума (практически 100 %) через 12-14 часов.
Пример 5 Фармакокинетика фармацевтических композиций на основе кристаллических полиморфов моногидрата клозапина
Улучшенный профиль растворения заявленных фармацевтических композиций обеспечивает достижение лучших параметров фармакокинетики. В доклиническом исследовании на животных (мини-свиньи) и клиническом исследовании продемонстрирована высокая биодоступность заявленных фармацевтических композиций с модифицированным высвобождением клозапина при однократном приеме в сутки - не менее 100 % относительно композиций немедленного высвобождения, принимаемых в эквивалентной дозе однократно или двукратно в сутки, что значительно превышает относительную биодоступность (более 50 %) составов с пролонгированным и замедленным высвобождением клозапина, ранее описанных в RU2613192 и RU2624229. Детальная оценка фармакокинетических параметров была проведена в ходе клинического исследования на 18 пациентах с диагнозом шизофрения. На фигуре 2 показан усредненный фармакокинетический профиль клозапина в плазме крови пациентов на 14-й день ежедневного приема в режиме 1 раз в сутки фармацевтической композиции, содержащей 200 мг клозапина и вспомогательные вещества, соответствующие составу 1.3 (включающий форму 1) из примера 1. Как показывают представленные данные, фармацевтическая композиция по предлагаемому изобретению обеспечивает более быстрое достижение максимальной концентрации клозапина в плазме крови - через 4 часа, а не через 8-10 часов, как описано в RU2613192. При этом сохраняется выраженный пролонгированный эффект - период полувыведения составил 26,5 часов, что обеспечивает поддержание эффективных концентраций клозапина в плазме крови более 24 часов. Важно также отметить стабильность концентрации, отсутствие выраженных колебаний концентрации клозапина в течение суток, что обеспечивает стабильный клинический эффект препарата при его ежедневном однократном применении.
Приведенные в примерах 4 и 5 данные о динамике растворения и фармакокинетике убедительно демонстрируют, что заявленные фармацевтические составы с модифицированным высвобождением клозапина на основе кристаллических полиморфов моногидрата клозапина обладают неожиданным сочетанием свойств - быстрым достижением и длительным поддержанием эффективных концентраций клозапина в организме пациентов с психическим заболеванием при однократном ежедневном приеме.
Несмотря на то, что изобретение описано со ссылкой на раскрываемые варианты воплощения, для специалистов в данной области должно быть очевидно, что конкретные подробно описанные эксперименты приведены лишь в целях иллюстрирования настоящего изобретения, и их не следует рассматривать как каким-либо образом ограничивающие объем изобретения. Должно быть понятно, что возможно осуществление различных модификаций без отступления от сути настоящего изобретения.
Список литературы, которая включена в настоящее описание изобретения в качестве ссылок:
1. Demyttenaere K., Bruffaerts R. и соавт. Prevalence, severity, and unmet need for treatment of mental disorders in the World Health Organization World Mental Health Surveys. JAMA. 2004 Jun 2;291(21):2581-90. doi: 10.1001/jama.291.21.2581.
2. Патент RU2414903.
3. Патент RU2613192.
4. Патент RU2624229.
5. Патент RU2715717.
6. Brog, J.-P., Chanez, C.-L., Crochet, A., & Fromm, K. M. (2013). Polymorphism, what it is and how to identify it: a systematic review. RSC Adv., 2013, 3, 16905-16931. doi:10.1039/c3ra41559g.
7. Banaru A. M., Slovokhotov Yu. L. Crystal hydrates of organic compounds. Journal of Structural Chemistry. Vol. 56, No. 5, pp. 967-982, 2015.
8. Franklin S. J., Younis U. S., Myrdal P. B. Estimating the Aqueous Solubility of Pharmaceutical Hydrates. J Pharm Sci. 2016 Jun; 105(6): 1914-1919. doi: 10.1016/j.xphs.2016.03.040.
| название | год | авторы | номер документа |
|---|---|---|---|
| КРИСТАЛЛИЧЕСКИЕ ПОЛИМОРФЫ МОНОГИДРАТЫ 8-ХЛОР-11-(4-МЕТИЛ-1-ПИПЕРАЗИНИЛ)-5Н-ДИБЕНЗО[b,e][1,4]ДИАЗЕПИНА (КЛОЗАПИНА) | 2018 |
|
RU2715717C1 |
| ТАБЛЕТКИ КЛОЗАПИНА С ПРОЛОНГИРОВАННЫМ ВЫСВОБОЖДЕНИЕМ | 2016 |
|
RU2613192C1 |
| АНТИБАКТЕРИАЛЬНАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2013 |
|
RU2561037C2 |
| ТВЕРДЫЕ ПРЕПАРАТЫ, СОДЕРЖАЩИЕ ТОФОГЛИФЛОЗИН, И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2014 |
|
RU2700164C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2011 |
|
RU2589842C2 |
| КРИСТАЛЛИЧЕСКИЕ ФОРМЫ N-[4-(ХЛОРДИФТОРМЕТОКСИ)ФЕНИЛ]-6-[(3R)-3-ГИДРОКСИПИРРОЛИДИН-1-ИЛ]-5-(1H-ПИРАЗОЛ-5-ИЛ)ПИРИДИН-3-КАРБОКСАМИДА | 2020 |
|
RU2836337C2 |
| КРИСТАЛЛИЧЕСКИЕ СОЛЬВАТЫ ГИДРОХЛОРИДА 6-(ПИПЕРИДИН-4-ИЛОКСИ)-2Н-ИЗОХИНОЛИН-1-OHA | 2012 |
|
RU2619129C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ С ПРОЛОНГИРОВАННЫМ ВЫСВОБОЖДЕНИЕМ ДЛЯ ЛЕЧЕНИЯ ЦЕРЕБРОВАСКУЛЯРНЫХ РАССТРОЙСТВ | 2014 |
|
RU2611339C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ВКЛЮЧАЮЩАЯ МЕМАНТИН И ЦИТИКОЛИН, А ТАКЖЕ ЛЕКАРСТВЕННАЯ ФОРМА НА ОСНОВЕ УКАЗАННОЙ ФАРМАЦЕВТИЧЕСКОЙ КОМПОЗИЦИИ, ВКЛЮЧАЮЩЕЙ МЕМАНТИН И ЦИТИКОЛИН, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ ЛЕКАРСТВЕННОЙ ФОРМЫ НА ОСНОВЕ ФАРМАЦЕВТИЧЕСКОЙ КОМПОЗИЦИИ, ВКЛЮЧАЮЩЕЙ МЕМАНТИН И ЦИТИКОЛИН | 2020 |
|
RU2810575C1 |
| КОМПОЗИЦИИ С ПРОЛОНГИРОВАННЫМ ВЫСВОБОЖДЕНИЕМ, ВКЛЮЧАЮЩИЕ ЛАМОТРИГИН | 2003 |
|
RU2325163C2 |
Группа изобретений относится к области медицинской химии и химико-фармацевтической промышленности, в частности к фармацевтической композиции на основе нейролептика клозапина и способу ее получения. Композиция для лечения психического заболевания с модифицированным высвобождением клозапина, отличающимся сочетанием быстрого и пролонгированного высвобождения в виде таблетки, покрытой пленочной оболочкой, содержит в таблетке-ядре в качестве действующего вещества клозапин в виде кристаллического полиморфа моногидрата клозапина определенной формы и вспомогательные вещества: целлюлозу микрокристаллическую (МКЦ); лактозы моногидрат; гидроксипропилметилцеллюлозу марки К15М CR (ГПМЦ К15М CR); связующий и смачивающий компонент, выбранный из гидроксипропилметилцеллюлозы марки 2910 тип 606 (ГПМЦ 2910 тип 606) и/или повидона марки К-17; кремния диоксид коллоидный и магния стеарат в определенном количестве. Способ получения указанной выше композиции включает следующие этапы: просеивают отдельно указанный выше полиморф клозапина, МКЦ, лактозы моногидрат и кремния диоксид коллоидный; получают связующий и смачивающий компонент, представляющий собой водный раствор ГПМЦ 2910 тип 606, повидона марки К-17 или смесь указанных растворов; указанные выше полиморф клозапина, МКЦ и лактозы моногидрат перемешивают до однородности, добавляют связующий и смачивающий компонент и снова перемешивают; полученную влажную смесь сушат и проводят грануляцию; сгранулированную массу перемешивают с ГПМЦ К15М CR, затем добавляют кремния диоксид коллоидный и магния стеарат; полученную смесь таблетируют прессованием и затем покрывают таблетки пленочной оболочкой. Использование группы изобретений обеспечивает быстрое высвобождение клозапина при приеме таблетки и быстрое достижение его максимальной концентрации в плазме крови с пролонгированным характером высвобождения и длительным поддержанием эффективной концентрации в плазме крови. 2 н. и 7 з.п. ф-лы, 6 ил., 1 табл., 5 пр.
1. Фармацевтическая композиция для лечения психического заболевания с модифицированным высвобождением клозапина, отличающимся сочетанием быстрого и пролонгированного высвобождения, в виде таблетки, покрытой пленочной оболочкой, содержащая следующие компоненты, мас.% в расчете на таблетку-ядро:
причем пленочная оболочка содержит поливиниловый спирт, титана диоксид, полиэтиленгликоль, тальк, алюминиевый лак хинолиновый желтый и железа оксид красный.
2. Фармацевтическая композиция по п. 1, в которой психическое заболевание представляет собой шизофрению, маниакальное состояние, маниакально-депрессивный психоз, психомоторное возбуждение при психопатиях, эмоциональное и поведенческое расстройство, расстройство сна.
3. Фармацевтическая композиция по п. 1, в которой, мас.%:
причем пленочная оболочка содержит поливиниловый спирт, титана диоксид, полиэтиленгликоль, тальк, алюминиевый лак хинолиновый желтый и железа оксид красный.
4. Способ получения фармацевтической композиции для лечения психического заболевания с модифицированным высвобождением клозапина, отличающимся сочетанием быстрого и пролонгированного высвобождения, в виде таблетки, покрытой пленочной оболочкой, по п. 1, включающий следующие этапы:
кристаллический полиморф моногидрата клозапина, микрокристаллическую целлюлозу, лактозы моногидрат и кремния диоксид коллоидный просеивают отдельно;
получают связующий и смачивающий компонент, представляющий собой водный раствор гидроксипропилметилцеллюлозы марки 2910 тип 606, повидона марки К-17 или смесь указанных растворов;
кристаллический полиморф моногидрата клозапина, микрокристаллическую целлюлозу и лактозы моногидрат перемешивают до однородности, добавляют связующий и смачивающий компонент и снова перемешивают;
полученную влажную смесь сушат и проводят грануляцию;
сгранулированную массу перемешивают с гидроксипропилметилцеллюлозой марки К15М CR, затем добавляют кремния диоксид коллоидный и магния стеарат;
полученную смесь таблетируют прессованием и затем таблетки покрывают пленочной оболочкой.
5. Способ по п. 4, в котором сушку влажной смеси проводят в установке псевдоожиженного слоя при температуре 50-60 °С до массовой доли воды 1,0-2,0 %.
6. Способ по п. 4, в котором грануляцию проводят через проволочную сетку с размером отверстий 1,0-1,5 мм.
7. Способ по п. 4, в котором сгранулированную массу загружают в смеситель и перемешивают с гидроксипропилметилцеллюлозой К15М CR в течение 5 мин, затем добавляют кремния диоксид коллоидный и магния стеарат и перемешивают в течение 3-5 мин.
8. Способ по п. 4, в котором водный раствор связующего и смачивающего компонента представляет собой 3-7 % раствор.
9. Способ по п. 8, в котором водный раствор связующего и смачивающего компонента представляет собой 5 % раствор.
| ТАБЛЕТКИ КЛОЗАПИНА С ПРОЛОНГИРОВАННЫМ ВЫСВОБОЖДЕНИЕМ | 2016 |
|
RU2613192C1 |
| КРИСТАЛЛИЧЕСКИЕ ПОЛИМОРФЫ МОНОГИДРАТЫ 8-ХЛОР-11-(4-МЕТИЛ-1-ПИПЕРАЗИНИЛ)-5Н-ДИБЕНЗО[b,e][1,4]ДИАЗЕПИНА (КЛОЗАПИНА) | 2018 |
|
RU2715717C1 |
| Приспособление для прессования стружки | 1930 |
|
SU29180A1 |
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| ТАБЛЕТКИ И ГРАНУЛИРОВАННЫЕ ПОРОШКИ, СОДЕРЖАЩИЕ 6-ФТОР-3-ГИДРОКСИ-2-ПИРАЗИНКАРБОКСАМИД | 2010 |
|
RU2527766C2 |
| CN 108619103 A, 09.10.2018 | |||
| Способ приготовления лака | 1924 |
|
SU2011A1 |
Авторы
Даты
2025-03-21—Публикация
2024-04-04—Подача