Предлагаемое изобретение относится к области органической химии, конкретно, к способу получения 10,14-бис(о,м,n-галогенфенил)-7,8,12,16,17-пентаокса-10,14-диазаспиро[5.11]гептадеканов (1):
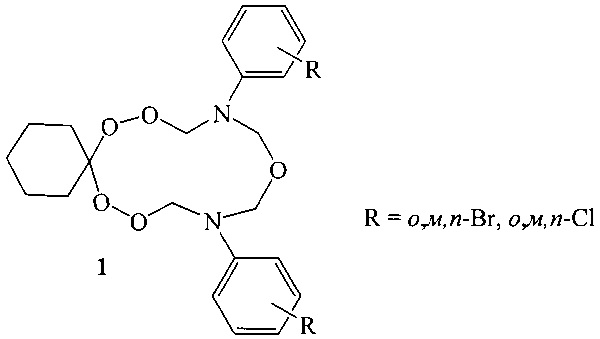
N-Содержащие тетраоксаны применяются в медицине в качестве препаратов, обладающих противомалярийной (Opsenica I., Opsenica D., Lanteri C.A., Anova L., Milhous W.K., Smith K.S., Solaja B.A. // J. Med. Chem. - 2008. - Vol. 51. - P. 2261-2266), противоопухолевой и антигельминтной активностью (Vennerstrom J.L., Arbe-Barnes S., Brun R., Chavman S.A., Chiv F.C.K. // Nature. - 2004. - Vol. 430. - P. 900-904).
Известен способ (Hye-Sook Kim, Yasuharu Shibata, Yusuke Wataya, Kaoru Tsuchiya, Araki Masuyama, Masatomo Nojima // J. Med. Chem. - 1999. - Vol. 42. - P. 2604-2609) получения 1,2,4,5,7-пентаоксаканов формулы (2) с выходом 12% ацидолизом смеси 1-фенилциклопентена с перекисью водорода и бензальдегидом по схеме:
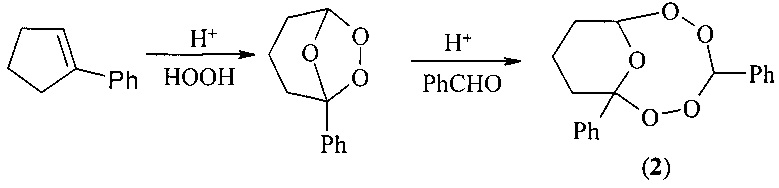
Известный способ не позволяет получать 10,14-бис(о,м,n-галогенфенил)-7,8,12,16,17-пентаокса-10,14-диазаспиро[5.11]гептадеканы общей формулы (1).
Известен способ (Kevin J. McCullough, Yoshihiro Ushigoe, Shogo Tanaka, Shin-ichi Kawamura, Araki Masuyama, Masatomo Nojiama // J. Chem. Soc., Perkin Trans. - 1998 - Vol. 1. - P. 3059-3064) получения производного 1,2,4,6,8-пентаоксакана формулы (3) с выходами 23-34% взаимодействием α-алкоксигидропероксидов с алифатическими альдегидами в условиях кислотного катализа с последующим добавлением формальдегида по схеме:
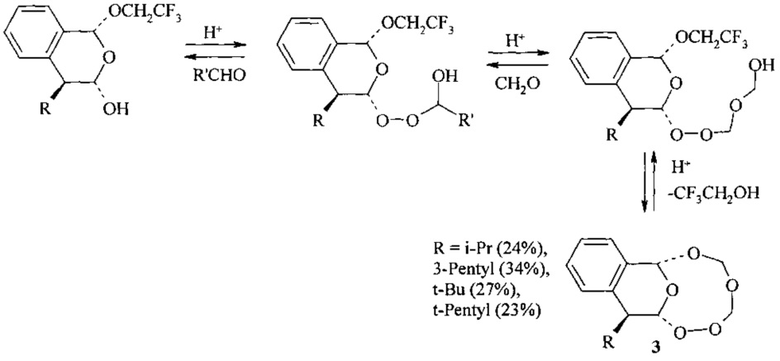
Известным способом не могут быть получены 10,14-бис(о,м,n-галогенфенил)-7,8,12,16,17-пентаокса-10,14-диазаспиро[5.11]гептадеканы общей формулы (1).
Известен способ (Hye-Sook Kim, Kaoru Tsuchiya, Yasuharu Shibata, Yusuke Wataya, Yoshihiro Ushigoe, Araki Masuyama, Masatomo Nojima, Kevin J. McCullough // J. Chem. Soc., Perkin Trans. - 1999 - Vol. 1. - P. 1867-1870) получения 1,2,4,5,7-пентаоксакана формулы (3) с выходом 15% озонолизом производного индена с образованием бис-гидропероксида, который превращают в бис-силилидизохроман, последний подвергают взаимодействию с бензальдегидом по схеме:
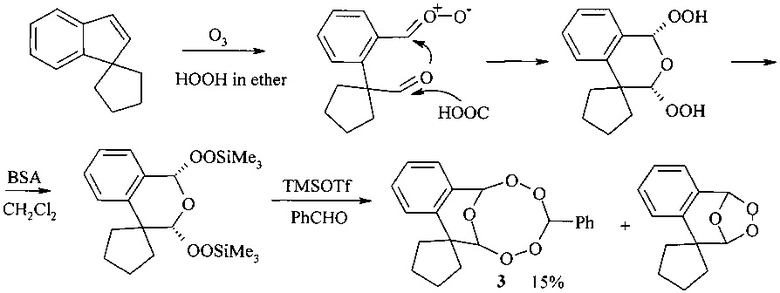
Таким образом, в литературе отсутствуют сведения о селективном получении 10,14-бис(о,м,n-галогенфенил)-7,8,12,16,17-пентаокса-10,14-диазаспиро[5.11]гептадеканов формулы (1).
Предлагается новый способ селективного получения 10,14-бис(о,м,n-галогенфенил)-7,8,12,16,17-пентаокса-10,14-диазаспиро[5.11]гептадеканов общей формулы (1).
Сущность способа заключается во взаимодействии 1,1-бис-[N-(пероксиметил)-N-(о,м,n-галоген(хлор-, бром-)фенил)]циклогексана с формальдегидом в присутствии катализатора Sm(NO3)3⋅6H2O, взятыми в мольном соотношении 1,1-бис-[N-(пероксиметил)-N-(о,м,n-галогенфенил)]циклогексан : формальдегид : Sm(NO3)3⋅6H2O = 10:20:(0.3-0.7), предпочтительно 10:20:0.5, при комнатной температуре (20°C) и атмосферном давлении в тетрагидрофуране (ТГФ) в качестве растворителя в течение 4-6 ч. Выход 10,14-бис(о,м,n-галогенфенил)-7,8,12,16,17-пентаокса-10,14-диазаспиро[5.11]гептадеканов (1) составляет 80-91%. Реакция протекает по схеме:
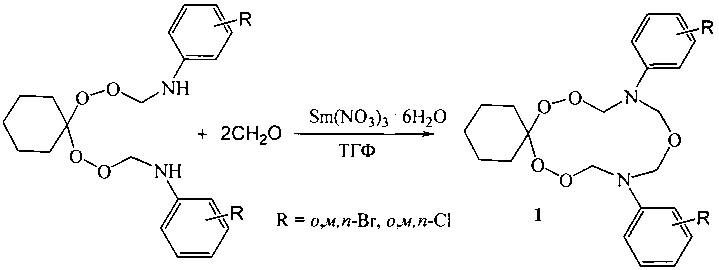
10,14-Бис(о,м,n-галогенфенил)-7,8,12,16,17-пентаокса-10,14-диазаспиро[5.11]гептадеканы (1) образуются только лишь с участием формальдегида и 1,1-бис-[N-(пероксиметил)-N-(о,м,n-галогенфенил)]циклогексана. В присутствии других альдегидов (например, уксусный альдегид, бензальдегид) целевые продукты (1) не образуются. Без катализатора реакция не идет.
Проведение указанной реакции в присутствии катализатора Sm(NO3)3⋅6H2O больше 7 мол. % не приводит к существенному увеличению выхода целевого продукта (1). Использование катализатора Sm(NO3)3⋅6H2O менее 3 мол. % снижает выход (1), что связано, возможно, со снижением каталитически активных центров в реакционной массе. Реакции проводили при температуре 20°C. При температуре выше 20°C (например, 60°C) снижается селективность реакции и увеличиваются энергозатраты, а при температуре ниже 20°C (например, -10°C) снижается скорость реакции. Опыты проводили в ТГФ, т.к. в нем хорошо растворяются исходные реагенты.
Существенные отличия предлагаемого способа
В известном способе реакция идет с участием в качестве исходных соединений озонида, перекиси водорода, силильных производных, бензальдегида. Известный способ не позволяет получать пентаоксаспироалканы общей формулы (1).
В предлагаемом способе в качестве исходных реагентов применяются 1,1-бис-[N-(пероксиметил)-N-(о,м,n-галогенфенил)]циклогексаны и формальдегид, a Sm(NO3)3⋅6H2O применяется в каталитических количествах. В отличие от известных способов предлагаемый способ позволяет синтезировать индивидуальные 10,14-бис(о,м,n-галогенфенил)-7,8,12,16,17-пентаокса-10,14-диазаспиро[5.11]гептадеканы (1).
Способ поясняется следующими примерами.
ПРИМЕР 1. Способ получения 1,1-бис-[N-(пероксиметил)-N-(o-хлорфенил)]циклогексана
В сосуд Шленка, установленный на магнитной мешалке, при температуре ~20°C помещают 5 мл H2O, 1.46 мл (20 ммоль) водного раствора (37%) формальдегида и 1.48 г (10 ммоль) 1,1-дигидропероксициклогексана, перемешивают в течение 30 мин, добавляют 1.27 (10 ммоль) о-хлоранилина. Реакционную смесь перемешивают при температуре ~20°C в течение 2 ч, экстрагируют хлороформом, выделяют 1,1-бис-[N-(пероксиметил)-N-(о-хлорфенил)]циклогексан с выходом 85%.
Другие примеры, подтверждающие способ, приведены в табл. 1.

ПРИМЕР 2. В сосуд Шленка, установленный на магнитной мешалке, при температуре ~20°C помещают 5 мл тетрагидрофурана, 1.46 мл (20 ммоль) водного раствора (37%) формальдегида и 4.27 г (10 ммоль) 1,1-бис-[N-(пероксиметил)-N-(о-хлорфенил)]циклогексана, затем добавляют 0.062 г (0.5 ммоль) Sm(NO3)2⋅6H2O. Реакционную смесь перемешивают при температуре ~20°C в течение 5 ч, выделяют 10,14-бис(о-хлорфенил)-7,8,12,16,17-пентаокса-10,14-диазаспиро[5.11]гептадекан с выходом 86%.
Другие примеры, подтверждающие способ, приведены в табл. 2.
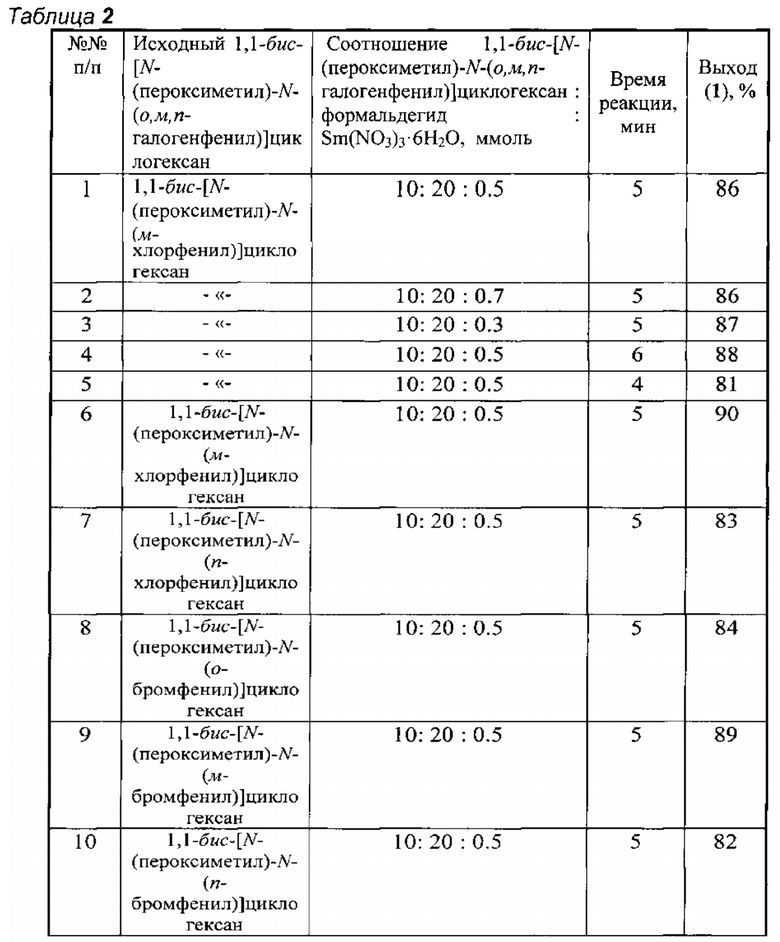
Все опыты проводили в ТГФ при комнатной температуре (~20°C).
Спектральные характеристики 1,1-бис-[N-(пероксиметил)-N-(о-хлорфенил)]циклогексана:
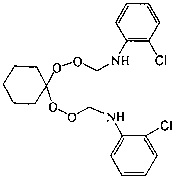
Спектральные характеристики 1,1-бис-[N-(пероксиметил)-N-(м-хлорфенил)]циклогексана:
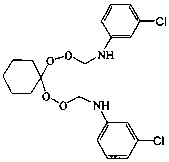
Спектральные характеристики 1,1-бис-[N-(пероксиметил)-N-(n-хлорфенил)]циклогексана:
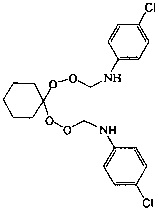
Спектральные характеристики 1,1-бис-[N-(пероксиметил)-N-(о-бромфенил)]циклогексана:
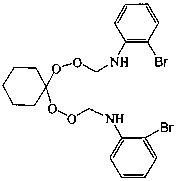
Спектральные характеристики 1,1-бис-[N-(пероксиметил)-N-(м-бромфенил)]циклогексана:
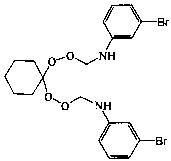
Спектральные характеристики 1,1-бис-[N-(пероксиметил)-N-(n-бромфенил)]циклогексана:
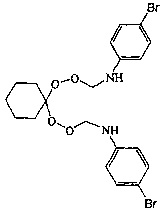
Спектральные характеристики 10,14-бис(о-хлорфенил)-7,8,12,16,17-пентаокса-10,14-диазаспиро[5.11]гептадекана:
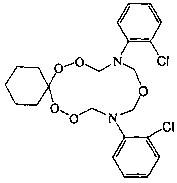
Спектральные характеристики 10,14-бис(м-хлорфенил)-7,8,12,16,17-пентаокса-10,14-диазаспиро[5.11]гептадекана:
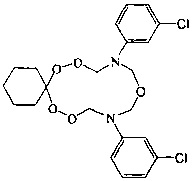
Спектральные характеристики 10,14-бис(n-хлорфенил)-7,8,12,16,17-пентаокса-10,14-диазаспиро[5.11]гептадекана:
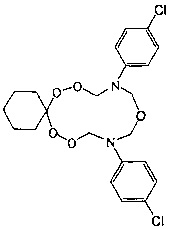
Спектральные характеристики 10,14-бис(о-бромфенил)-7,8,12,16,17-пентаокса-10,14-диазаспиро[5.11]гептадекана:
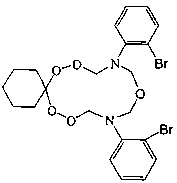
Спектральные характеристики 10,14-бис(м-бромфенил)-7,8,12,16,17-пентаокса-10,14-диазаспиро[5.11]гептадекана:
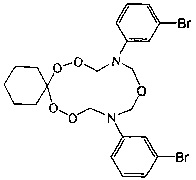
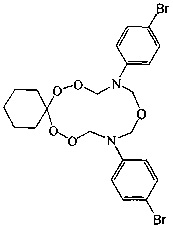
Спектральные характеристики 10,14-бис(n-бромфенил)-7,8,12,16,17-пентаокса-10,14-диазаспиро[5.11]гептадекана:
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 10,14-БИС(3-ХЛОРФЕНИЛ)-12-ГАЛОГЕНФЕНИЛ-7,8,16,17-ТЕТРАОКСА-10,12,14-ТРИАЗАСПИРО[5,11]ГЕПТАДЕКАНОВ | 2016 |
|
RU2632665C1 |
| СПОСОБ ПОЛУЧЕНИЯ 10-АРИЛ-7,8,12,13-ТЕТРАОКСА-10-АЗАСПИРО[5.7]ТРИДЕКАНОВ | 2014 |
|
RU2584950C1 |
| СПОСОБ ПОЛУЧЕНИЯ 3-(о, м, n-ГАЛОГЕНФЕНИЛ)-3, 4-ДИГИДРО-2Н-БЕНЗО[f][1, 5, 3]ДИТИАЗЕПИНОВ | 2016 |
|
RU2632661C2 |
| СПОСОБ ПОЛУЧЕНИЯ 6-[4-ГИДРОКСИ(ТИО,КАРБОКСИ)ФЕНИЛ]-1,11-ДИОКСА-4,8-ДИТИА-6-АЗАЦИКЛОТРИДЕКАНОВ | 2016 |
|
RU2640211C2 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛ 2-(1,11-ДИОКСА-4,8-ДИТИА-6-АЗАЦИКЛОТРИДЕКАН-6-ИЛ)АЛКАНОАТОВ | 2016 |
|
RU2632670C2 |
| АЗАКРАУНСОДЕРЖАЩИЕ N-АРИЛ-1,8-НАФТАЛИМИДЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2017 |
|
RU2656106C1 |
| Лиганд для получения комплекса переходного металла, способ его получения и способ получения комплекса переходного металла с использованием лиганда | 2015 |
|
RU2616628C2 |
| (3bR*,7aR*,10bR*,14aR*-cis-14c,14d)-2,9 БИС(ГАЛОГЕНФЕНИЛ)ОКТАДЕКАГИДРО-1Н,8Н-2,3а,7b,9,10a,14b-ГЕКСААЗАДИБЕНЗО[fg,op]ТЕТРАЦЕНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2021 |
|
RU2787455C1 |
| ЦИНКОВЫЕ КОМПЛЕКСЫ 5-[2-ГИДРОКСИ(ТОЗИЛАМИНО)БЕНЗИЛИДЕНАМИНО]-2-(2-ТОЗИЛАМИНОФЕНИЛ)-1АЛКИЛБЕНЗИМИДАЗОЛОВ, ОБЛАДАЮЩИЕ ФОТОЛЮМИНЕСЦЕНТНОЙ АКТИВНОСТЬЮ | 2013 |
|
RU2532904C1 |
| Комплексы цинка и кадмия N-[2-(алкилиминометил)фенил]-4-метилбензолсульфамидов, обладающие люминесцентной активностью | 2017 |
|
RU2650529C1 |
Изобретение относится к способу получения 10,14-бис(о,м,n-галогенфенил)-7,8,12,16,17-пентаокса-10,14-диазаспиро[5.11]гептадеканов общей формулы (1):
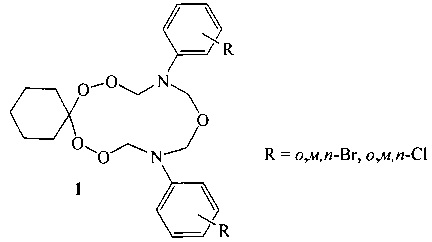 , которые могут найти применение в качестве препаратов, обладающих противомалярийной, противоопухолевой и антигельминтной активностью. Технический результат: разработан новый способ получения 10,14-бис(о,м,n-галогенфенил)-7,8,12,16,17-пентаокса-10,14-диазаспиро[5.11]гептадеканов, который позволяет получать индивидуальные продукты. 2 табл., 1 пр.
, которые могут найти применение в качестве препаратов, обладающих противомалярийной, противоопухолевой и антигельминтной активностью. Технический результат: разработан новый способ получения 10,14-бис(о,м,n-галогенфенил)-7,8,12,16,17-пентаокса-10,14-диазаспиро[5.11]гептадеканов, который позволяет получать индивидуальные продукты. 2 табл., 1 пр.
Способ получения 10,14-бис(о,м,n-галогенфенил)-7,8,12,16,17-пентаокса-10,14-диазаспиро[5.11]гептадеканов общей формулы (1):
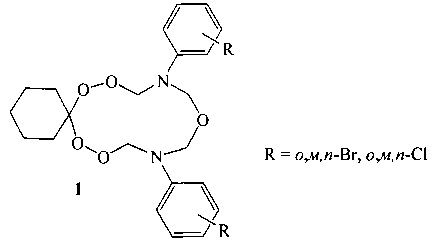
отличающийся тем, что 1,1-бис-[N-(пероксиметил)-N-(о,м,n-галоген(хлор-, бром-)фенил)]циклогексаны подвергают взаимодействию с формальдегидом в присутствии катализатора Sm(NO3)3⋅6H2O, при мольном соотношении 1,1-бис-[N-(пероксиметил)-N-(о,м,n-галоген]циклогексан : формальдегид : Sm(NO3)3 ⋅ 6H2O = 10:20:(0.3-0.7), при комнатной температуре (20°C) и атмосферном давлении в тетрагидрофуране в качестве растворителя в течение 4-6 ч.
| RU 2015122317 A, 10.06.2015. |
Авторы
Даты
2017-10-09—Публикация
2016-06-17—Подача