ТЕХНИЧЕСКАЯ ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к соли камфорсульфоновой кислоты (камсилату) (1r,1R,4R)-4-метокси-5ʺ-метил-6ʺ-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ-амина и к фармацевтическим композициям, содержащим эту соль. Кроме того, настоящее изобретение относится к терапевтическим способам, при которых эту соль используют для лечения и/или предупреждения связанных с Aβ патологий, таких как синдром Дауна, β-амилоидная ангиопатия, такая как, без ограничения, церебральная амилоидная ангиопатия или наследственное церебральное кровоизлияние, расстройства, ассоциированные с когнитивным нарушением, такие как, без ограничения, MCI (ʺумеренное когнитивное нарушениеʺ), болезнь Альцгеймера, потеря памяти, симптомы дефицита внимания, ассоциированные с болезнью Альцгеймера, нейродегенерация, ассоциированная с такими заболеваниями, как болезнь Альцгеймера, или деменция, включая деменцию смешанного сосудистого и дегенеративного происхождения, пресенильную деменцию, сенильную деменцию и деменцию, ассоциированную с болезнью Паркинсона, прогрессивный надъядерный паралич или кортикальная базальная дегенерация.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
На начальной стадии невропатологическим явлением, отличающим болезнь Альцгеймера (AD), является отложение состоящего из 40-42 остатков амилоидного β-пептида (Aβ) в паренхиме головного мозга и церебральных сосудах. Большой массив генетических, биохимических данных и данных in vivo подтверждает центральную роль Aβ в патологическом каскаде, который в конце приводит к AD. У пациентов обычно имеются ранние симптомы (чаще всего потеря памяти) в их шестой или седьмой декаде жизни. Заболевание прогрессирует с нарастанием деменции и повышением отложения Aβ. Параллельно в нейронах аккумулируется гиперфосфорилированная форма ассоциированного с микротрубочками белка тау, что приводит к плеторе опасных воздействий на нейрональную функцию. Превалирующая рабочая гипотеза касательно преходящей взаимосвязи между Aβ и тау патологиями констатирует, что в моделях этого заболевания у людей и животных отложение Aβ предшествует агрегации тау-белка. В этих обстоятельствах стоит отметить, что точная молекулярная структура Aβ, опосредующая эту патологическую функцию, в настоящее время является предметом интенсивных исследований. Вероятней всего, существует континуум токсических молекулярных структур в диапазоне от Aβ-олигомеров низшего порядка до надмолекулярных агрегатов, таких как Aβ-фибриллы.
Aβ-пептид представляет собой интегральный фрагмент типа I белка АРР (белок-предшественник амилоида Aβ), белка, который повсеместно экспрессируется в тканях человека. Поскольку растворимый Aβ может присутствовать как в плазме крови, так и в спинномозговой жидкости (CSF) и в среде из культивированных клеток, АРР должен претерпевать протеолиз. Существует три основных типа расщепления АРР, которые имеют отношение к патологии AD, так называемые α-, β- и γ-расщепления. α-Расщепление, которое происходит приблизительно в середине Аβ-домена в АРР, осуществляется металлопротеазами ADAM10 или ADAM17 (последняя также известна как ТАСЕ (TNFα-конвертирующий фермент). β-Расщепление, происходящее по N-концу Aβ, производится трансмембранным аспартилпротеазным ферментом, расщепляющим белок-предшественник амилоида по бета-сайту (Beta site АРР Cleaving Enzyme 1 (ВАСЕ1)). γ-Расщепление, создающее С-концы Aβ и последующее высвобождение пептида, осуществляется мультисубъединичной аспартилпротеазой, именуемой γ-секретазой. Расщепление, осуществляемое ADAM10/17, с последующим расщеплением γ-секретазой приводит к высвобождению растворимого пептида р3, усеченного по N-концу фрагмента Aβ, который не образует амилоидные отложения у людей. Этот протеолитический путь обычно называется неамилоидогенным путем метаболизма. Последующие расщепления, осуществляемые ВАСЕ1 и γ-секретазой, образуют интактный Аβ-пептид, поэтому эта схема процессинга называется амилоидогенным путем метаболизма. Зная это, можно предвидеть два возможных пути снижения продуцирования Aβ: стимулирование неамилоидогенного процессинга или ингибирование или модулирование амилоидогенного процессинга. Данная заявка фокусируется на последней стратегии, а именно на ингибировании или модулировании амилоидогенного процессинга.
Амилоидогенные бляшки и сосудистая амилоидная ангиопатия также служат отличительными характеристиками головного мозга пациентов с трисомией 21 (синдром Дауна), наследственным церебральным кровоизлиянием с амилоидозом голландского типа (HCHWA-D) и другими нейродегенеративными расстройствами. Нейрофибриллярные клубки также возникают при других нейродегенеративных расстройствах, включая расстройства, вызывающие деменцию (Varghese, J., et al, Journal of Medicinal Chemistry, 2003, 46, 4625-4630). β-Амилоидные отложения представляют собой преимущественно агрегат Аβ-пептида, который, в свою очередь, является продуктом протеолиза белка-предшественника амилоида (АРР). Более конкретно, Аβ-пептид образуется в результате расщепления АРР по С-концу одной или более γ-секретазами и по N-концу ферментом β-секретазой (ВАСЕ), также известным как аспартилпротеаза, или Asp2, или фермент, расщепляющий АРР по бета-сайту (ВАСЕ), как часть β-амилоидогенного пути.
Активность ВАСЕ напрямую связана с образованием Aβ-пептида из АРР (Sinha, et al, Nature, 1999, 402, 537-540), и исследования все больше показывают, что ингибирование ВАСЕ ингибирует продуцирование Аβ-пептида (Roberds, S. L, et al, Human Molecular Genetics, 2001, 10, 1317-1324). BACE является мембраносвязанным белком типа 1, который синтезируется как частично активный профермент и обильно экспрессируется в ткани головного мозга. Считается, что он проявляет основную β-секретазную активность и является скорость-ограничивающей стадией в продуцировании амилоид-β-пептида (Aβ).
Следовательно, лекарственные средства, которые снижают или блокируют активность ВАСЕ, должны снижать уровни Aβ и уровни фрагментов Aβ в головном мозге или везде, где происходит отложение Aβ или его фрагментов, и поэтому должны замедлять образование амилоидных бляшек и прогрессирование AD или других болезней, в которые вовлечено отложение Aβ или его фрагментов. Таким образом, ВАСЕ является важным кандидатом для разработки лекарственных средств для лечения и/или профилактики связанных с Aβ патологий, таких как синдром Дауна, β-амилоидная ангиопатия, такая как, без ограничения, церебральная амилоидная ангиопатия, или наследственное церебральное кровоизлияние, расстройства, ассоциированные с когнитивным нарушением, таким как, без ограничения, MCI (ʺумеренное когнитивное нарушениеʺ), болезнь Альцгеймера, потеря памяти, симптомы дефицита внимания, ассоциированные с болезнью Альцгеймера, нейродегенерация, ассоциированная с такими заболеваниями, как болезнь Альцгеймера, или деменция, включая деменцию смешанного сосудистого и нейродегенеративного происхождения, пресенильную деменцию, сенильную деменцию и деменцию, ассоциированную с болезнью Паркинсона, прогрессивный надъядерный паралич или кортикальная базальная дегенерация.
Поэтому будет полезным ингибировать отложение Aβ и его фрагментов путем ингибирования ВАСЕ ингибиторами, такими как соединения, предложенные в данной заявке.
Терапевтический потенциал ингибирования отложения Аβ побудил многие исследовательские группы изолировать и определять характеристики секретаз и идентифицировать их потенциальные ингибиторы.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Фиг. 1 представляет собой рентгеновскую порошковую дифрактограмму камсилатной соли (1r,1'R,4R)-4-метокси-5ʺ-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ-амина.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к камсилатной соли соединения (1r,1'R,4R)-4-метокси-5ʺ-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ-амин. Камсилатная соль (1r,1'R,4R)-4-метокси-5ʺ-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ-амина альтернативно может быть описана как соль камфорсульфоновой кислоты (1r,1'R,4R)-4-метокси-5ʺ-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ-амина.
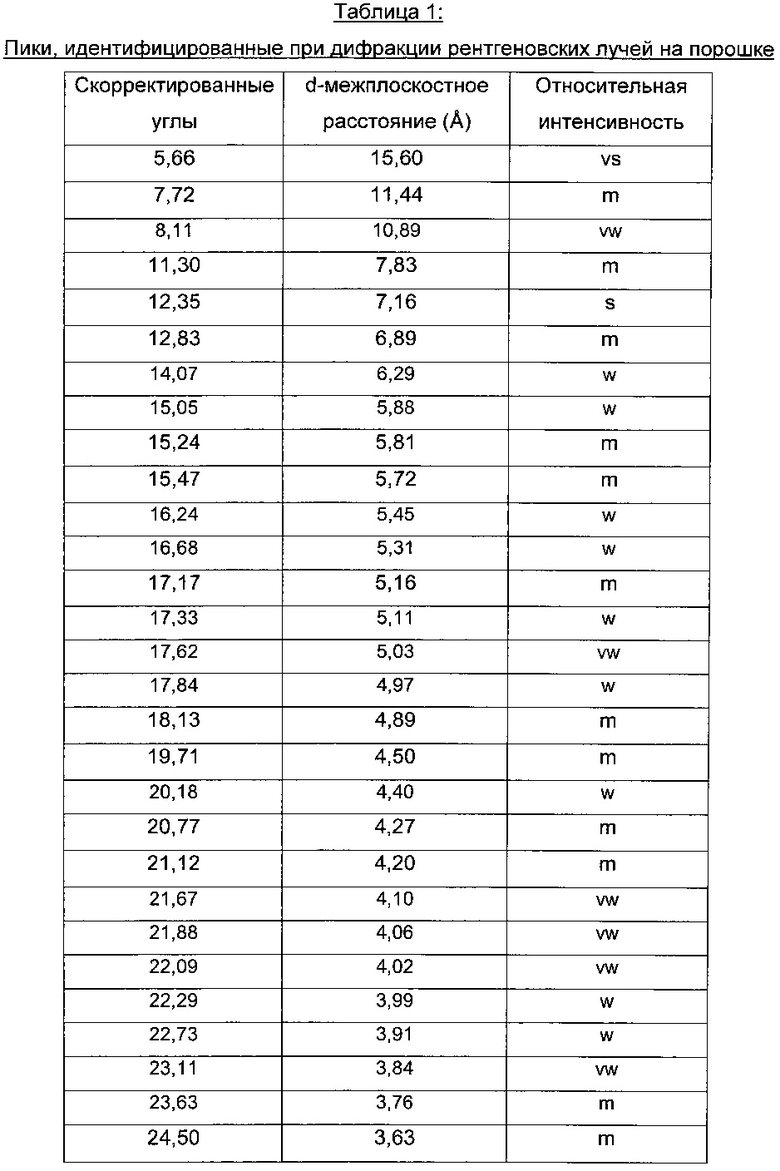
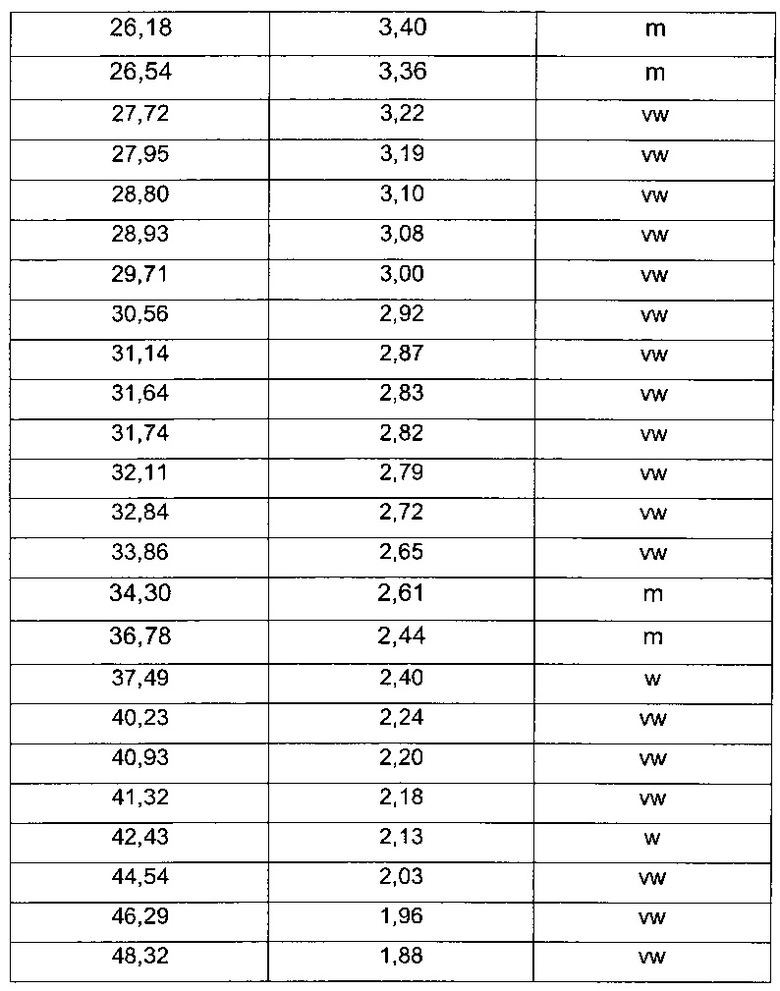
Одним воплощением настоящего изобретения является камсилатная соль соединения (1r,1'R,4R)-4-метокси-5ʺ-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ-амин, характеризующаяся тем, что она дает картину дифракции рентгеновских лучей на порошке (ДРЛП), демонстрирующую пики со значениями d-межплоскостного расстояния, которые представлены в Таблице 1.
Другим воплощением настоящего изобретения является камсилатная соль соединения (1r,1'R,4R)-4-метокси-5ʺ-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ-амин, характеризующаяся тем, что она дает картину дифракции рентгеновских лучей на порошке (ДРЛП), демонстрирующую пики со значениями d-межплоскостного расстояния, которые представлены в Таблице 2.

Использованный в данном документе термин “камсилатная соль соединения (1r,1'R,4R)-4-метокси-5ʺ-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ-амин” также охватывает все его сольваты и сокристаллы.
Альтернативные соли соединения (1r,1'R,4R)-4-метокси-5ʺ-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ-амин включают сукцинатную, гидрохлоридную, фосфатную, сульфатную, фумаратную и 1,5-нафталиндисульфонатную соль.
В конкретном аспекте изобретения предложена фармацевтическая композиция, содержащая в качестве активного ингредиента терапевтически эффективное количество камсилатной соли соединения (1r,1'R,4R)-4-метокси-5ʺ-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ-амин совместно с фармацевтически приемлемыми эксципиентами, носителями или разбавителями.
В другом аспекте изобретения предложена камсилатная соль соединения (1r,1'R,4R)-4-метокси-5ʺ-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'H-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ-амин для использования в качестве лекарственного средства.
В другом аспекте изобретения предложено применение камсилатной соли соединения (1r,1'R,4R)-4-метокси-5ʺ-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ-амин в качестве лекарственного средства для лечения или предупреждения связанной с Aβ патологии.
В другом аспекте изобретения предложено применение камсилатной соли соединения (1r,1'R,4R)-4-метокси-5ʺ-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ-амин в качестве лекарственного средства для лечения или предупреждения связанной с Aβ патологии, где указанной связанной с Aβ патологией является синдром Дауна, Р-амилоидная ангиопатия, церебральная амилоидная ангиопатия, наследственное церебральное кровоизлияние, расстройство, ассоциированное с когнитивным нарушением, MCI (“умеренное когнитивное нарушение”), болезнь Альцгеймера, потеря памяти, симптомы дефицита внимания, ассоциированные с болезнью Альцгеймера, нейродегенерация, ассоциированная с болезнью Альцгеймера, деменция смешанного сосудистого происхождения, деменция дегенеративного происхождения, пресенильная деменция, сенильная деменция, деменция, ассоциированная с болезнью Паркинсона, прогрессивный надъядерный паралич или кортикальная базальная дегенерация.
В другом аспекте изобретения предложено применение камсилатной соли соединения (1r,1'R,4R)-4-метокси-5ʺ-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ-амин в качестве лекарственного средства для лечения или предупреждения болезни Альцгеймера.
В другом аспекте изобретения предложено применение камсилатной соли соединения (1r,1'R,4R)-4-метокси-5ʺ-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ-амин в изготовлении лекарственного средства для лечения или предупреждения связанной с Aβ патологии.
В другом аспекте изобретения предложено применение камсилатной соли соединения (1r,1'R,4R)-4-метокси-5ʺ-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ-амин в изготовлении лекарственного средства для лечения или предупреждения связанной с Aβ патологии, где указанной связанной с Aβ патологией является синдром Дауна, β-амилоидная ангиопатия, церебральная амилоидная ангиопатия, наследственное церебральное кровоизлияние, расстройство, ассоциированное с когнитивным нарушением, MCI (ʺумеренное когнитивное нарушениеʺ), болезнь Альцгеймера, потеря памяти, симптомы дефицита внимания, ассоциированные с болезнью Альцгеймера, нейродегенерация, ассоциированная с болезнью Альцгеймера, деменция смешанного сосудистого происхождения, деменция дегенеративного происхождения, пресенильная деменция, сенильная деменция, деменция, ассоциированная с болезнью Паркинсона, прогрессивный надъядерный паралич или кортикальная базальная дегенерация.
В другом аспекте изобретения предложено применение камсилатной соли соединения (1r,1'R,4R)-4-метокси-5ʺ-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ-амин в изготовлении лекарственного средства для лечения или предупреждения болезни Альцгеймера.
В другом аспекте изобретения предложен способ ингибирования активности ВАСЕ, включающий приведение указанного ВАСЕ в контакт с камсилатной солью соединения (1r,1R,4R)-4-метокси-5ʺ-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ-амин.
В другом аспекте изобретения предложен способ лечения или предупреждения связанной с Aβ патологии у пациента, нуждающегося в таком лечении или предупреждении, включающий введение указанному пациенту терапевтически эффективного количества камсилатной соли соединения (1r,1'R,4R)-4-метокси-5ʺ-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ-амин.
В другом аспекте изобретения предложен способ лечения или предупреждения связанной с Aβ патологии у пациента, нуждающегося в таком лечении или предупреждении, включающий введение указанному пациенту терапевтически эффективного количества камсилатной соли соединения (1r,1'R,4R)-4-метокси-5ʺ-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ-амин, где указанной связанной с Аβ патологией является синдром Дауна, β-амилоидная ангиопатия, церебральная амилоидная ангиопатия, наследственное церебральное кровоизлияние, расстройство, ассоциированное с когнитивным нарушением, MCI (ʺумеренное когнитивным нарушениеʺ), болезнь Альцгеймера, потеря памяти, симптомы дефицита внимания, ассоциированные с болезнью Альцгеймера, нейродегенерация, ассоциированная с болезнью Альцгеймера, деменция смешанного сосудистого происхождения, деменция дегенеративного происхождения, пресенильная деменция, сенильная деменция, деменция, ассоциированная с болезнью Паркинсона, прогрессивный надъядерный паралич или кортикальная базальная дегенерация.
В другом аспекте изобретения предложен способ лечения или предупреждения болезни Альцгеймера у пациента, нуждающегося в таком лечении или предупреждении, включающий введение указанному пациенту терапевтически эффективного количества камсилатной соли соединения (1r,1R,4R)-4-метокси-5ʺ-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ-амин.
В некоторых воплощениях настоящего изобретения предложен способ ингибирования активности ВАСЕ, включающий приведение ВАСЕ в контакт с камсилатной солью соединения (1r,1'R,4R)-4-метокси-5ʺ-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ-амин. Считается, что ВАСЕ показывает основную β-секретазную активность и рассматривается как скоростьограничивающая стадия в продуцировании амилоидного белка (Aβ). Таким образом, ингибирование ВАСЕ ингибиторами, такими как соединения, предложенные в данной заявке, может быть полезным для ингибирования отложения Aβ его фрагментов. Поскольку отложение Aβ и его фрагментов связано с такими заболеваниями, как болезнь Альцгеймера, ВАСЕ является важным кандидатом для разработки лекарственных средств для лечения и/или профилактики связанных с Aβ патологий, таких как синдром Дауна и β-амилоидная ангиопатия, такая как, без ограничения, церебральная амилоидная ангиопатия, наследственное церебральное кровоизлияние, расстройства, ассоциированные с когнитивным нарушением, таким как, без ограничения, MCI (ʺумеренное когнитивное нарушениеʺ), болезнь Альцгеймера, потеря памяти, симптомы дефицита внимания, ассоциированные с болезнью Альцгеймера, нейродегенерация, ассоциированная с такими заболеваниями, как болезнь Альцгеймера, или деменция, включая деменцию смешанного сосудистого и дегенеративного происхождения, пресенильную деменцию, сенильную деменцию и деменцию, ассоциированную с болезнью Паркинсона, прогрессивный надъядерный паралич или кортикальная базальная дегенерация.
В некоторых воплощениях настоящего изобретения предложен способ профилактики связанных с Aβ патологий, таких как синдром Дауна и β-амилоидная ангиопатия, такая как, без ограничения, церебральная амилоидная ангиопатия, наследственное церебральное кровоизлияние, расстройства, ассоциированные с когнитивным нарушением, таким как, без ограничения, MCI (ʺумеренное когнитивное нарушениеʺ), болезнь Альцгеймера, потеря памяти, симптомы дефицита внимания, ассоциированные с болезнью Альцгеймера, нейродегенерация, ассоциированная с такими заболеваниями, как болезнь Альцгеймера, или деменция, включая деменцию смешанного сосудистого и дегенеративного происхождения, пресенильную деменцию, сенильную деменцию и деменцию, ассоциированную с болезнью Паркинсона, прогрессивный надъядерный паралич или кортикальная базальная дегенерация, включающий введение млекопитающему (включая человека) терапевтически эффективного количества камсилатной соли соединения (1r,1'R,4R)-4-метокси-5ʺ-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ-амин.
В некоторых воплощениях настоящего изобретения предложен способ лечения или предупреждения связанных с Aβ патологий, таких как синдром Дауна и β-амилоидная ангиопатия, такая как, без ограничения, церебральная амилоидная ангиопатия, наследственное церебральное кровоизлияние, расстройства, ассоциированные с когнитивным нарушением, таким как, без ограничения, MCI (ʺумеренное когнитивным нарушениеʺ), болезнь Альцгеймера, потеря памяти, симптомы дефицита внимания, ассоциированные с болезнью Альцгеймера, нейродегенерация, ассоциированная с такими заболеваниями, как болезнь Альцгеймера, или деменция, включая деменцию смешанного сосудистого и дегенеративного происхождения, пресенильную деменцию, сенильную деменцию и деменцию, ассоциированную с болезнью Паркинсона, прогрессивный надъядерный паралич или кортикальная базальная дегенерация, путем введения млекопитающему (включая человека) камсилатной соли соединения (1r,1'R,4R)-4-метокси-5ʺ-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ-амин и агента, улучшающего когнитивную способность, и/или агента, улучшающего память. В некоторых воплощениях настоящего изобретения предложен способ лечения или предупреждения связанных с Аβ патологий, таких как синдром Дауна и β-амилоидная ангиопатия, такая как, без ограничения, церебральная амилоидная ангиопатия, наследственное церебральное кровоизлияние, расстройства, ассоциированные с когнитивным нарушением, таким как, без ограничения, MCI (ʺумеренное когнитивное нарушениеʺ), болезнь Альцгеймера, потеря памяти, симптомы дефицита внимания, ассоциированные с болезнью Альцгеймера, нейродегенерация, ассоциированная с такими заболеваниями, как болезнь Альцгеймера, или деменция, включая деменцию смешанного сосудистого и дегенеративного происхождения, пресенильную деменцию, сенильную деменцию и деменцию, ассоциированную с болезнью Паркинсона, прогрессивный надъядерный паралич или кортикальная базальная дегенерация, путем введения млекопитающему (включая человека) камсилатной соли соединения (1r,1'R,4R)-4-метокси-5ʺ-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ-амин и ингибитора холинэстеразы или противовоспалительного агента.
В некоторых воплощениях настоящего изобретения предложен способ лечения или предупреждения связанных с Aβ патологий, таких как синдром Дауна и β-амилоидная ангиопатия, такая как, без ограничения, церебральная амилоидная ангиопатия, наследственное церебральное кровоизлияние, расстройства, ассоциированные с когнитивным нарушением, таким как, без ограничения, MCI (ʺумеренное когнитивное нарушениеʺ), болезнь Альцгеймера, потеря памяти, симптомы дефицита внимания, ассоциированные с болезнью Альцгеймера, нейродегенерация, ассоциированная с такими заболеваниями, как болезнь Альцгеймера, или деменция, включая деменцию смешанного сосудистого и дегенеративного происхождения, пресенильную деменцию, сенильную деменцию и деменцию, ассоциированную с болезнью Паркинсона, прогрессивный надъядерный паралич или кортикальная базальная дегенерация, или любого другого заболевания, расстройства или состояния, описанного в данном документе, путем введения млекопитающему (включая человека) соединения по настоящему изобретению и атипичного антипсихотического агента. Атипичные антипсихотические агенты включают, без ограничения, оланзапин (продаваемый как Zyprexa), арипипразол (продаваемый как Ability), рисперидон (продаваемый как Risperdal), кветиапин (продаваемый как Seroquel), клозапин (продаваемый как Clozaril), зипразидон (продаваемый как Geodon) и оланзапин/флуоксетин (продаваемый как Symbyax).
В некоторых воплощениях у млекопитающего или человека, которого лечат камсилатной солью соединения (1r,1'R,4R)-4-метокси-5ʺ-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ-амин, диагностировано конкретное заболевание или расстройство, такое, как описано в данном документе. В этих случаях млекопитающее или человек, которого лечат, нуждается в таком лечении. Диагностику, однако, не обязательно осуществляют заранее.
Определения, изложенные в этой заявке, предназначены для разъяснения терминов, использованных в тексте данной заявки. Термин ʺв данном документеʺ означает всю заявку.
В данном документе ʺфармацевтически приемлемыйʺ относится к тем соединениям, веществам, композициям и/или лекарственным формам, которые в рамках обоснованного медицинского суждения являются подходящими для использования в контакте с тканями людей и животных без чрезмерной токсичности, раздражения, аллергической реакции или другой проблемы или осложнения, соизмеримыми с разумным соотношением польза/риск.
Лечение деменции, определенное в данном документе, можно применять в качестве монотерапии, или оно может включать в себя, в дополнение к соединению по изобретению, традиционную химиотерапию. Такая химиотерапия может включать одну или более из следующих категорий агентов: ингибиторы ацетил-холинэстеразы, противовоспалительные агенты, агенты, улучшающие когнитивную способность, и/или агенты, улучшающие память, или атипичные антипсихотические агенты.
Такое совместное лечение может быть осуществлено путем вспомогательного, параллельного, одновременного, последовательного или раздельного введения доз индивидуальных компонентов лечения. В таких комбинированных продуктах используются соединения по данному изобретению.
Дополнительная традиционная химиотерапия может включать агенты одной или более следующих категорий: (1) антидепрессанты, (2) атипичные антипсихотические агенты, (3) антипсихотические агенты, (4) анксиолитики, (5) противосудорожные средства, (6) применяемые в настоящее время терапии болезни Альцгеймера, (7) терапии болезни Паркинсона, (8) терапии мигрени, (9) терапии инсульта, (10) терапии недержания мочи, (11) терапии невропатической боли, (12) терапии ноцицептивной боли, (13) терапии бессонницы и (14) стабилизаторы настроения. Известные виды лечения для вышеуказанных терапий могут быть использованы в комбинации с описанным в данном документе изобретением.
В таких комбинированных продуктах используют камсилатную соль соединения (1r,1'R,4R)-4-метокси-5ʺ-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ-амин в диапазоне дозировок, указанном в данном документе, и другое фармацевтически активное соединение или соединения в пределах одобренных диапазонов дозировок и/или определенных специалистом в данной области.
Соединения по настоящему изобретению можно вводить перорально, парентерально, трансбуккально, вагинально, ректально, ингаляцией, инсуффляцией, сублингвально, внутримышечно, подкожно, местно, интраназально, интраперитонеально, интраторакально, внутривенно, эпидурально, интратекально, интрацеребровентрикулярно и инъекцией в суставы.
Дозировка будет зависеть от пути введения, тяжести заболевания, возраста и массы тела пациента и других факторов, на которые обычно обращает внимание лечащий врач при определении индивидуального режима и уровня дозировки, наиболее подходящих для конкретного пациента.
Эффективным количеством соединения по настоящему изобретению для применения в лечении деменции является количество, достаточное для облегчения симптомов у теплокровного животного, в частности человека, симптомов деменции, для снижения прогрессирования деменции или для снижения у пациентов с симптомами деменции риска ухудшения состояния.
В дополнение к соединениям по настоящему изобретению фармацевтическая композиция по данному изобретению может также содержать один или более фармакологических агентов, ценных для лечения одного или более болезненных состояний, упомянутых в данном документе, или ее можно вводить совместно (одновременно или последовательно) с одним или более такими агентами.
Количество камсилатной соли соединения (1r,1'R,4R)-4-метокси-5ʺ-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ-амин, которое нужно вводить, будет варьировать для пациента, которого лечат, и будет варьировать от примерно 10 нг/кг массы тела до 100 мг/кг массы тела в сутки и предпочтительно будет составлять от 10 нг/кг до 10 мг/кг в сутки. Например, дозировки без труда могут быть определены специалистами в данной области из этого описания изобретения и из знаний в данной области. Таким образом, специалист без труда сможет определить количество соединения и возможных добавок, разбавителей и/или носителей в композициях и количество, которое нужно вводить в способах по изобретению.
СПОСОБЫ ПОЛУЧЕНИЯ
Камсилатная соль (1r,1'R,4R)-4-метокси-5ʺ-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ-амина
Камсилатная соль соединения (1r,1'R,4R)-4-метокси-5ʺ-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ-амин может быть получена, начиная с растворения (1r,1'R,4R)-4-метокси-5ʺ-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2-инден-1'2'-имидазол]-4ʺ-амина в подходящем растворителе, например 2-пропаноле, ацетонитриле или ацетоне или их смесях с водой с последующим смешиванием полученного раствора с самой (1S)-(+)-10-камфорсульфоновой кислотой или с (1S)-(+)-10-камфорсульфоновой кислотой, растворенной в подходящем растворителе, например 2-пропаноле или воде, при температуре от комнатной температуры до 80°C. Кристаллизация может быть осуществлена путем выпаривания растворителя и/или охлаждения раствора или непосредственно в результате реакции кристаллизации соли. Для запуска кристаллизации могут быть использованы затравочные кристаллы. Затравки могут быть получены из самой партии путем взятия образца раствора небольшого объема и последующего быстрого охлаждения его, чтобы вызвать кристаллизацию. Кристаллы затем добавляют в партию в качестве затравок.
ДРЛП анализ
Анализ дифракции рентгеновских лучей на порошке (ДРЛП) выполняли на образцах, приготовленных стандартными методамами, например как описано в Giacovazzo, С.et al (1995), Fundamentals of Crystallography, Oxford University Press; Jenkins, R. and Snyder, R.L. (1996), Introduction to X-Ray Powder Diffractometry, John Wiley & Sons, New York; Bunn, C.W. (1948), Chemical Crystallography, Clarendon Press, London; или Klug, H.P. & Alexander, L.E. (1974), X-ray Diffraction Procedures, John Wiley and Sons, New York. Рентгеновские дифракционные анализы выполняли с использованием дифрактометра PANanlytical X'Pert PRO MPD в течение 96 минут от 1 до 60° 2θ. Значения расстояний при ДРЛП могут варьировать в пределах ±2 в позиции последнего знака после десятичной запятой.
Относительные интенсивности получали из дифрактограмм, измеренных с переменными щелями. Измеренные относительные интенсивности по отношению к наибольшему пику приведены как очень сильные (vs) выше 50%, как сильные (s) от 25 до 50%, как средние (m) от 10 до 25%, как слабые (w) от 5 до 10% и как очень слабые (vw) ниже 5% относительно высоты пика. Для специалиста в данной области будет очевидно, что ДРЛП интенсивности могут варьировать между разными образцами и разными подготовками образцов по множеству различных причин, включая предпочтительную ориентацию. Для специалиста в данной области будет очевидно также, что меньшие сдвиги в измеренном угле и, следовательно, d-межплоскостном расстоянии могут возникать по разным причинам, включая колебание уровня поверхности образца в дифрактометре.
ПРИМЕРЫ
Пример 1
6'-Бромспиро[циклогексан-1,2'-инден]-1',4(3'Н)-дион

трет-Бутоксид калия (223 г, 1,99 моль) загружали в реактор вместимостью 100 л, содержащий перемешиваемую смесь 6-бром-1-инданона (8,38 кг, 39,7 моль) в THF (16,75 л) при 20-30°C. Затем в эту смесь загружали метилакрилат (2,33 л, 25,8 моль) в течение 15 минут, поддерживая температуру 20-30°C. Добавляли раствор трет-бутоксида калия (89,1 г, 0,79 моль) в THF (400 мл), затем добавляли метилакрилат (2,33 л, 25,8 моль) в течение 20 минут при 20-30°C. Затем добавляли третью порцию трет-бутоксида калия (90 г, 0,80 моль) в THF (400 мл), после чего добавляли третью порцию метилакрилата (2,33 л, 25,8 моль) в течение 20 минут при 20-30°C. трет-Бутоксид калия (4,86 кг, 43,3 моль), растворенный в THF (21,9 л), загружали в реактор в течение 1 часа при 20-30°C. Реакционную смесь нагревали до приблизительно 65°C, и 23 л растворителя отгоняли. Температуру реакции снижали до 60°C, и в смесь добавляли 50%-ный водный раствор гидроксида калия (2,42 л, 31,7 моль) в воде (51,1 л) в течение 30 минут при 55-60°C, после чего смесь перемешивали в течение 6 часов при 60°C, охлаждали до 20°C в течение 2 часов. После перемешивания в течение 12 часов при 20°C твердое вещество отфильтровывали, промывали дважды смесью воды (8,4 л) и THF (4,2 л) и затем сушили при 50°C в вакууме с получением 6'-бромспиро[циклогексан-1,2'-инден]-1',4(3'Н)-диона (7,78 кг; 26,6 моль). 1Н ЯМР (500 МГц, DMSO-d6) δ м.д. (миллионные доли) 1.78-1.84 (m, 2Н), 1.95 (td, 2Н), 2.32-2.38 (m, 2Н), 2.51-2.59 (m, 2Н), 3.27 (s, 2Н), 7.60 (d, 1Н), 7.81 (m, 1Н), 7.89 (m, 1Н).
Пример 2
(1r,4r)-6'-Бром-4-метоксиспиро[циклогексан-1,2'-инден]-1'(3'Н)-он
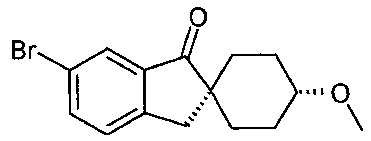
Комплекс бора с трет-бутиламином (845 г, 9,7 моль), растворенный в DCM (3,8 л), загружали в суспензию 6'-бромспиро[циклогексан-1,2'-инден]-1',4(3'Н)-диона (7,7 кг, 26,3 моль) в DCM (42,4 л) при приблизительно 0-5°C в течение приблизительно 25 минут. Реакционную смесь перемешивали при 0-5°C в течение 1 часа, после чего анализ подтвердил, что конверсия составила >98%. Загружали раствор, приготовленный из хлорида натрия (2,77 кг), воды (13,3 л) и 37%-ной соляной кислоты (2,61 л, 32 моль). Смесь нагревали до приблизительно 15°C, и после расслоения фазы разделяли. Органическую фазу возвращали в реактор вместе с метилметансульфонатом (2,68 л, 31,6 моль) и хлоридом тетрабутиламмония (131 г, 0,47 моль), и смесь энергично перемешивали при 20°C. Затем в энергично перемешиваемую реакционную смесь загружали 50%-ный гидроксид натрия (12,5 л, 236 моль) в течение приблизительно 1 часа, и реакционную смесь энергично перемешивали в течение ночи при 20°C. Добавляли воду (19 л), и водную фазу после отделения отбрасывали. Органический слой нагревали до приблизительно 40°C, и 33 л растворителя отгоняли. Загружали этанол (21 л), и возобновляли перегонку с увеличением температуры (22 л отгоняли при повышении температуры до 79°C). Загружали этанол (13,9 л) при приблизительно 75°C. Загружали воду (14,6 л) в течение 30 минут, поддерживая температуру 72-75°C. Приблизительно 400 мл раствора выводили в полиэтиленовую бутылку вместимостью 500 мл, и образец спонтанно кристаллизовался. Эту порцию охлаждали до 50°C, и образец закристаллизовавшейся суспензии добавляли назад в раствор. Смесь охлаждали до 40°C. Смесь охлаждали до 20°C в течение 4 часов, после чего ее перемешивали в течение ночи. Твердое вещество отфильтровывали, промывали смесью этанола (6,6 л) и воды (5 л) и сушили при 50°C в вакууме с получением (1r,4r)-6'-бром-4-метоксиспиро[циклогексан-1,2'-инден]-1'(3'Н)-она (5,83 кг, 18,9 моль) 1Н ЯМР (500 МГц, DMSO-d6) δ м.д. 1.22-1.32 (m, 2Н), 1.41-1.48 (m, 2Н), 1.56 (td, 2Н), 1.99-2.07 (m, 2Н), 3.01 (s, 2Н), 3.16-3.23 (m, 1Н), 3.27 (s, 3Н), 7.56 (d, 1Н), 7.77 (d, 1Н), 7.86 (dd, 1Н).
Пример 3
Гидрохлорид (1r,4r)-6'-бром-4-метоксиспиро[циклогексан-1,2'-инден]-1'(3'Н)-имина
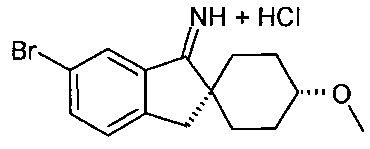
(1r,4r)-6'-Бром-4-метоксиспиро[циклогексан-1,2'-инден]-1'(3'Н)-он (5,82 кг; 17,7 моль) загружали в реактор вместимостью 100 л при температуре окружающей среды, затем добавляли этоксид титана(IV) (7,4 л; 35,4 моль) и раствор трет-бутилсульфинамида (2,94 кг; 23,0 моль) в 2-метилтетрагидрофуране (13,7 л). Смесь перемешивали и нагревали до 82°C.После 30 минут при 82°C температуру дальше увеличивали (вплоть до 97°C), и 8 л растворителя отгоняли. Реакционную смесь охлаждали до 87°C и добавляли 2-метилтетрагидрофуран (8,2 л) при реакционной температуре 82°C. Реакционную смесь перемешивали при 82°C в течение ночи. Реакционную температуру повышали (до 97°C), и 8,5 л растворителя отгоняли. Реакционную смесь охлаждали до 87°C и добавляли 2-метилтетрагидрофуран (8,2 л), что дало реакционную температуру 82°C.Через 3,5 часа реакционную температуру опять увеличивали (до 97°C), и 8 л растворителя отгоняли. Реакционную смесь охлаждали до 87°C и добавляли 2-метилтетрагидрофуран (8,2 л), что дало реакционную температуру 82°C. Через 2 часа реакционную температуру опять увеличивали (до 97°C), и 8,2 л растворителя отгоняли. Реакционную смесь охлаждали до 87°C и добавляли 2-метилтетрагидрофуран (8,2 л), что дало реакционную температуру 82°C. Реакционную смесь перемешивали в течение ночи при 82°C. Реакционную температуру опять увеличивали (до 97°C), и 8 л растворителя отгоняли. Реакционную смесь охлаждали до 25°C. Загружали дихлорметан (16,4 л). В отдельный реактор добавляли воду (30 л) и при энергичном перемешивании добавляли сульфат натрия (7,54 кг), и полученный раствор охлаждали до 10°C. В этот водный раствор добавляли серную кислоту (2,3 л, 42,4 моль), и температуру доводили до 20°C. Отбирали 6 л кислотного водного раствора и сохраняли его на будущее. Органическую реакционную смесь загружали в кислотный водный раствор в течение 5 минут, хорошо перемешивая. Сосуд с органической реакционной смесью промывали дихлорметаном (16,4 л), и дихлорметановый промывочный раствор также добавляли в кислотную воду. Смесь перемешивали в течение 15 минут и затем оставляли отстаиваться в течение 20 минут. Нижнюю водную фазу удаляли и добавляли сохраненные 6 л кислотной промывочной жидкости, затем добавляли воду (5,5 л). Смесь перемешивали в течение 15 минут и затем оставляли расслаиваться в течение 20 минут. Нижний органический слой отбирали в бутыли, а верхний водный слой отбрасывали. Органический слой загружали назад в сосуд, затем добавляли сульфат натрия (2,74 кг), и смесь перемешивали в течение 30 минут. Сульфат натрия отфильтровывали и промывали дихлорметаном (5,5 л), и объединенные органические фазы загружали в чистый сосуд. Эту партию нагревали для дистилляции (собирали 31 л, максимальная температура 57°C). Партию охлаждали до 40°C и добавляли дихлорметан (16,4 л). Партию нагревали для дистилляции (собирали 17 л, максимальная температура 54°C). Партию охлаждали до 20°C и добавляли дихлорметан (5,5 л) и этанол (2,7 л). В реакционную загружали смесь 2М раствора хлористого водорода в диэтиловом эфире (10,6 л; 21,2 моль) в течение 45 минут, поддерживая температуру 16-23°C.Полученную суспензию перемешивали при 20°C в течение 1 часа, после чего твердое вещество отфильтровывали и промывали 3 раза смесью 1:1 дихлорметана и диэтилового эфира (3×5,5 л). Твердое вещество сушили при 50°C в вакууме с получением гидрохлорида (1r,4r)-6'-бром-4-метоксиспиро[циклогексан-1,2'-инден]-1'(3'Н)-имина (6,0 кг; 14,3 моль; выход 82% (масс.) по результатам 1Н ЯМР) 1Н ЯМР (500 МГц, DMSO-d6) δ м.д. 130 (m, 2Н), 1.70 (d, 2Н), 1.98 (m, 2Н), 2.10 (m, 2Н), 3.17 (s, 2Н), 3.23 (m, 1Н), 3.29 (s, 3Н), 7.61 (d, 1Н), 8.04 (dd, 1Н), 8.75 (d, 1Н), 12.90 (br s, 2Н). Пример 4
(1r,4r)-6'-Бром-4-метокси-5ʺ-метил-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ(3ʺН)-тион
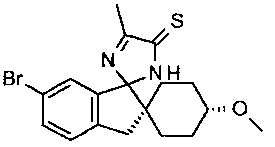
Триметилортоформиат (4,95 л; 45,2 моль) и диизопропилэтиламин (3,5 л; 20,0 моль) загружали в реактор, содержащий гидрохлорид (1r,4r)-6'-бром-4-метоксиспиро[циклогексан-1,2'-инден]-1'(3'Н)-имина (6,25 кг; 14,9 моль) в изопропаноле (50,5 л). Реакционную смесь перемешивали и нагревали до 75°C в течение 1 часа с получением прозрачного раствора. Устанавливали температуру 70°C, и 2М раствор 2-оксопропантиоамида в изопропаноле (19,5 кг; 40,6 моль) загружали в течение 1 часа, после чего реакционную смесь перемешивали в течение ночи при 69°C. В эту партию вносили затравку (1r,4r)-6'-бром-4-метокси-5ʺ-метил-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ(3ʺН)-тиона (3 г; 7,6 ммоль), температуру понижали до 60°C, и смесь перемешивали в течение 1 часа. Смесь концентрировали дистилляцией (температура дистилляции приблизительно 60°C; 31 л отгоняли). Добавляли воду (31 л) в течение 1 часа, и температуру понижали с 60°C до 25°C в течение 90 минут, после чего смесь перемешивали в течение 3 часов. Твердое вещество отфильтровывали, промывали дважды изопропанолом (2×5,2 л) и сушили в вакууме при 40°C с получением (1r,4r)-6'-бром-4-метокси-5ʺ-метил-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ(3ʺН)-тиона (4,87 кг; 10,8 моль; выход 87% (масс.) по результатам 1Н ЯМР).
Пример 5
Соль (1r,1'R,4R)-6'-бром-4-метокси-5ʺ-метил-3'Н-диспиро-[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ-амина с D(+)-10-камфорсульфоновой кислотой
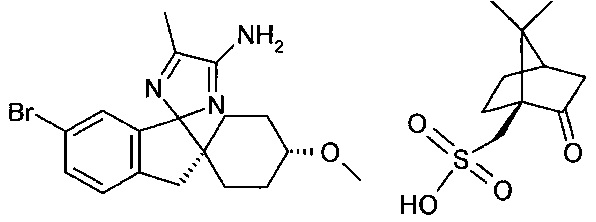
7М раствор аммиака в метаноле (32 л; 224 моль) загружали в реактор, содержащий (1r,4r)-6'-бром-4-метокси-5ʺ-метил-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ(3ʺН)-тион (5,10 кг; 11,4 моль) и дигидрат ацетата цинка (3,02 кг; 13,8 моль). Реактор герметично закрывали, и смесь нагревали до 80°C и перемешивали в течение 24 часов, после чего ее охлаждали до 30°C. Загружали 1-бутанол (51 л), и реакционную смесь концентрировали в вакууме, отгоняя приблизительно 50 л. Добавляли 1-бутанол (25 л), и смесь концентрировали в вакууме, отгоняя 27 л. Смесь охлаждали до 30°C и загружали 1М раствор гидроксида натрия (30 л; 30 моль). Двухфазную смесь перемешивали в течение 15 минут. Нижнюю водную фазу отделяли. Загружали воду (20 л), и смесь перемешивали в течение 30 минут. Нижнюю водную фазу отделяли. Органическую фазу нагревали до 70°C, после чего загружали (1S)-(+)-10-камфорсульфоновую кислоту (2,4 кг; 10,3 моль). Смесь перемешивали в течение 1 часа при 70°C и затем охлаждали до 20°C в течение 3 часов. Твердое вещество отфильтровывали, промывали этанолом (20 л) и сушили в вакууме при 50°C с получением соли (1r,4r)-6'-бром-4-метокси-5ʺ-метил-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ-амина с (+)-10-камфорсульфоновой кислотой (3,12 кг; 5,13 моль; выход 102% (масс.) по результатам 1Н ЯМР).
Пример 6
(1r,1'R,4R)-4-метокси-5ʺ-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ-амин
Na2PdCl4 (1,4 г; 4,76 ммоль) и 3-(ди-трет-бутилфосфоний)-пропан-сульфонат (2,6 г; 9,69 ммоль), растворенный в воде (0,1 л), загружали в сосуд, содержащий соль (1r,4r)-6'-бром-4-метокси-5ʺ-метил-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ-амина с (+)-10-камфорсульфоновой кислотой (1 кг; 1,58 моль), карбонат калия (0,763 кг; 5,52 моль) в смеси 1-бутанола (7,7 л) и воды (2,6 л). Смесь осторожно продували азотом, после чего загружали 5-(проп-1-инил)пиридин-3-ил-бороновую кислоту (0,29 кг; 1,62 моль), и смесь снова осторожно продували азотом. Реакционную смесь нагревали до 75°C и перемешивали в течение 2 часов, после чего анализ показал полную конверсию. Температуру доводили до 45°C. Перемешивание останавливали, и нижнюю водную фазу отделяли. Органический слой промывали 3 раза водой (3×4 л). Реакционную температуру доводили до 22°C и загружали поглотитель Phosphonics SPM32 (0,195 кг), и эту смесь перемешивали в течение ночи. Поглотитель отфильтровывали и промывали 1-бутанолом (1 л). Реакционную смесь концентрировали дистилляцией при пониженном давлении до 3 л. Загружали бутилацетат (7,7 л), и смесь снова концентрировали до 3 л дистилляцией при пониженном давлении. Загружали бутилацетат (4,8 л), и смесь нагревали до 60°C.Смесь перемешивали в течение 1 часа, после чего ее концентрировали до приблизительно 4 л дистилляцией при пониженном давлении. Устанавливали температуру 60°C и добавляли гептаны (3,8 л) в течение 20 минут. Смесь охлаждали до 20°C в течение 3 часов и затем перемешивали в течение ночи. Твердое вещество отфильтровывали и промывали дважды смесью 1:1 бутилацетат:гептан (2×2 л). Продукт сушили в вакууме при 50°C с получением (1r,R,4R)-4-метокси-5ʺ-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ-амина (0,562 кг; 1,36 моль; выход 100% (масс.) по результатам 1Н ЯМР). 1Н ЯМР (500 МГц, DMSO-d6) δ м.д. 0.97 (d, 1Н), 1.12-1.30 (m, 2Н), 1.37-1.51 (m, 3Н), 1.83 (d, 2H), 2.G9 (s, 3Н), 2.17 (s, 2Н), 2.89-3.12 (m, 3Н), 3.20 (s, 3Н), 6.54 (s, 2Н), 6.83 (s, 1Н), 7.40 (d, 1Н), 7.54 (d, 1Н), 7.90 (s, 1Н). 8.51 (d, 1Н), 8.67(d, 1Н)
Пример 7
Получение камсилатной соли (1r,1'R,4R)-4-метокси-5ʺ-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ-амина
1,105 кг (1r,1'R,4R)-4-метокси-5ʺ-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ-амина растворяли в 8,10 л 2-пропанола и 475 мл воды при 60°C. Затем загружали 1,0 моль-эквивалент (622 г) (1S)-(+)-10-камфорсульфоновой кислоты при 60°C.Суспензию перемешивали до тех пор, пока вся (1S)-(+)-10-камфорсульфоновая кислота не растворилась. Добавляли вторую порцию 2-пропанола (6,0 л) при 60°C, и затем содержимое дистиллировали, собирая 4,3 л дистиллята. Затем загружали 9,1 л гептана при 65°C. После выдержки в течение одного часа реакционная смесь становилась мутной. Затем осуществляли дополнительную дистилляцию при примерно 75°C, и собирали 8,2 л дистиллята. Реакционную смесь затем охлаждали до 20°C в течение 2 ч и выдерживали при этой температуре в течение ночи. Затем партию фильтровали и промывали смесью 1,8 л 2-пропанола и 2,7 л гептана. В конце вещество сушили при пониженном давлении и при 50°C. Выход составил 1,44 кг (83,6% (масс.)). 1Н ЯМР (400 МГц, DMSO-d6) δ м.д. 12.12 (1Н, s), 9,70 (2Н, d, J40.2), 8.81 (1Н, d, J2.1), 8.55 (1Н, d, J1.7), 8.05 (1Н, dd, J2.1, 1.7), 7.77 (1Н, dd, J7.8, 1.2), 7.50 (2Н, m), 3.22 (3Н, s), 3.19 (1Н, d, J16.1), 3.10 (1H, d, J16.1), 3.02 (1H, m), 2.90 (1H, d, J14.7), 2.60 (1H, m), 2.41 (1H, d, J14.7), 2.40 (3H, s), 2.22 (1H, m), 2.10 (3H, s), 1.91 (3H, m), 1.81 (1H, m), 1.77 (1H, d, J18.1), 1.50 (2H, m), 1.25 (6H, m), 0.98 (3H, s), 0.69 (3H, s).
БИОЛОГИЧЕСКИЕ АНАЛИЗЫ
Уровень активности камсилатной соли (1r,1'R,4R)-4-метокси-5ʺ-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ-амина может быть протестирован с использованием следующих методов:
Анализ методом TR-FRET
Фермент β-секретазу, используемую в анализе методом TR-FRET (резонансный перенос энергии флуоресценции с временным разрешением), получали следующим образом.
кДНК для растворимой части В-секретазы человека (АА1-АА460) клонировали с использованием экспрессионного вектора млекопитающих ASP2-Fc10-1-IRES-GFP-neoK. Осуществляли слияние гена с Fc доменом IgGI (метка аффинности) и стабильно клонировали в клетки НЕК 293. Очищенный sBACE-Fc хранили при -80°C в 50 мМ глицине с рН 2,5, доводили до рН 7,4 1М Tris, и он имел чистоту 40%.
Фермент (усеченная форма) разводили до 6 мкг/мл (исходный раствор 1,3 мг/мл) и субстрат TruPoint ВАСЕ1 до 200 нМ (исходный 120 мкМ) в реакционном буфере (ацетат натрия, chaps (3-((3-холамидопропил)диметиламмонио)-1-пропансульфоновая кислота), triton х-100, EDTA, рН 4,5). Фермент и соединение в диметилсульфоксиде (конечная концентрация DMSO 5%) смешивали и преинкубировали в течение 10 минут при комнатной температуре. Затем добавляли субстрат, и реакционную смесь инкубировали в течение 15 минут при комнатной температуре. Реакцию останавливали добавлением 0,35 об. стоп-раствора (ацетат натрия, рН 9). Флуоресценцию продукта измеряли на планшет-ридере Victor II при длине волны возбуждения 340-485 нм и длине волны эмиссии 590-615 нм. Конечная концентрация фермента составляла 2,7 мкг/мл; конечная концентрация субстрата составляла 100 нМ (Km примерно 250 нМ). Контрольный диметилсульфоксид, вместо тестируемого соединения, определял уровень активности 100%, и активность 0% определяли по лункам без фермента (заменен реакционным буфером) или по дозе насыщения известного ингибитора, 2-амино-6-[3-(3-метоксифенил)фенил]-3,6-диметил-5Н-пиримидин-4-она. Контрольный ингибитор также использовали в анализах зависимости доза-эффект, и он имел IC50 примерно 150 нМ.
В этом анализе камсилатная соль (1r,1'R,4R)-4-метокси-5ʺ-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2'-инден-1',2'-имидазол]-4ʺ-амина имела среднюю IC50 0,2 нМ.
Анализ высвобождения sAPPβ
Клетки SH-SY5Y культивируют в среде, содержащей DMEM/F-12 с Glutamax, 10% FCS и 1% не являющихся незаменимыми аминокислот, и криоконсервируют и хранят при -140°C в концентрации 7,5-9,5×106 клеток на флакон. Клетки оттаивают и засевают в концентрации примерно 10000 клеток на лунку в среде, содержащей DMEM/F-12 с Glutamax, 10% FCS и 1% не являющихся незаменимыми аминокислот, в 384-луночный планшет, обработанный культурой ткани, 100 мкл клеточной суспензии на лунку. Планшеты с клетками затем инкубируют в течение 7-24 ч при 37°C, 5% CO2. Клеточную среду удаляют, затем добавляют 30 мкл соединения, разведенного в среде, содержащей DMEM/F-12 с Glutamax, 10% FCS, 1% не являющихся незаменимыми аминокислот и 1% PeSt, до конечной концентрации 1% DMSO. Соединения инкубируют с клетками в течение 17 ч (в течение ночи) при 37°C, 5% CO2. Планшеты Meso Scale Discovery (MSD) используют для детектирования высвобождения sAPPB. Планшеты MSD с sAPPB блокируют в 1% BSA в Tris промывочном буфере (40 мкл на лунку) в течение 1 ч на шейкере при комнатной температуре и промывают 1 раз Tris промывочным буфером (40 мкл на лунку). 20 мкл среды переносят в предварительно блокированные и промытые микропланшеты MSD с sAPPG, и планшеты с клетками затем используют в анализе АТР (аденозинтрифосфат) для измерения цитотоксичности. Планшеты MSD инкубируют при встряхивании при комнатной температуре в течение 2 ч, и среду отбрасывают. Добавляют 10 мкл детекторного антитела (1 нМ) на лунку, затем инкубируют при встряхивании при комнатной температуре в течение 2 ч и затем отбрасывают. Добавляют 40 мкл на лунку буфера для считывания, и планшеты считывают в визуализаторе SECTOR Imager.
Анализ АТР
Как указано в анализе высвобождения sAPPB, после переноса 20 мкл среды из планшетов с клетками на детекцию sAPPB планшеты используют для анализа цитотоксичности, используя набор для определения клеточной пролиферации/цитотоксичности ViaLightTM Plus компании Cambrex Bioscience, который позволяет измерять общий клеточный уровень АТР. Анализ выполняют согласно протоколу производителя. Коротко, добавляют 10 мкл на лунку реагента для лизиса клеток. Планшеты инкубируют при комнатной температуре в течение 10 мин. Через две минуты после добавления 25 мкл разведенного ViaLightTM Plus АТР реагента измеряют люминесценцию. Тох (токсикологическим) порогом является сигнал ниже 75% от контроля.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЗАМЕЩЕННЫЕ N-АРИЛБЕНЗАМИДЫ И РОДСТВЕННЫЕ СОЕДИНЕНИЯ ДЛЯ ЛЕЧЕНИЯ АМИЛОИДНЫХ ЗАБОЛЕВАНИЙ И СИНУКЛЕИНОПАТИИ | 2005 |
|
RU2381213C2 |
| СОЛИ СУЛЬФАТЫ N-(3-(4-(3-(ДИИЗОБУТИЛАМИНО)ПРОПИЛ)ПИПЕРАЗИН-1ИЛ)ПРОПИЛ)-1Н-БЕНЗО[D]ИМИДАЗОЛ-2-АМИНА, ИХ ПОЛУЧЕНИЕ И ИХ ПРИМЕНЕНИЕ | 2013 |
|
RU2655454C2 |
| 1,4 ТИАЗЕПИНЫ/СУЛЬФОНЫ В КАЧЕСТВЕ ИНГИБИТОРОВ ВАСЕ1 И(ИЛИ) ВАСЕ2 | 2012 |
|
RU2600931C2 |
| БИЦИКЛИЧЕСКИЕ ГЕТЕРОАРИЛЬНЫЕ ПРОИЗВОДНЫЕ | 2019 |
|
RU2815806C2 |
| ПРОИЗВОДНОЕ ЦИННАМИДА ТИПА МОРФОЛИНА | 2006 |
|
RU2381225C1 |
| НОВЫЕ ДИСПИРО-ИНДОЛИНОНЫ, ИНГИБИТОРЫ MDM2/p53 ВЗАИМОДЕЙСТВИЯ, СПОСОБ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2015 |
|
RU2629750C2 |
| ПРОЛЕКАРСТВЕННЫЕ ПРОИЗВОДНЫЕ 1,3-ДИАМИНО-2-ГИДРОКСИПРОПАНА | 2003 |
|
RU2357962C2 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ПРЕДОТВРАШЕНИЯ ИЛИ ЛЕЧЕНИЯ ТАУПАТИИ | 2018 |
|
RU2739199C1 |
| PROTAC, ЦЕЛЕНАПРАВЛЕННО ВОЗДЕЙСТВУЮЩИЕ НА ТАУ-БЕЛОК, И СВЯЗАННЫЕ С НИМИ СПОСОБЫ ПРИМЕНЕНИЯ | 2017 |
|
RU2805523C2 |
| ПРОИЗВОДНЫЕ АЦИЛАМИНОТИАЗОЛА, ИХ ПОЛУЧЕНИЕ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ПРОДУКЦИИ БЕТА-АМИЛОИДНОГО ПЕПТИДА | 2004 |
|
RU2360907C2 |
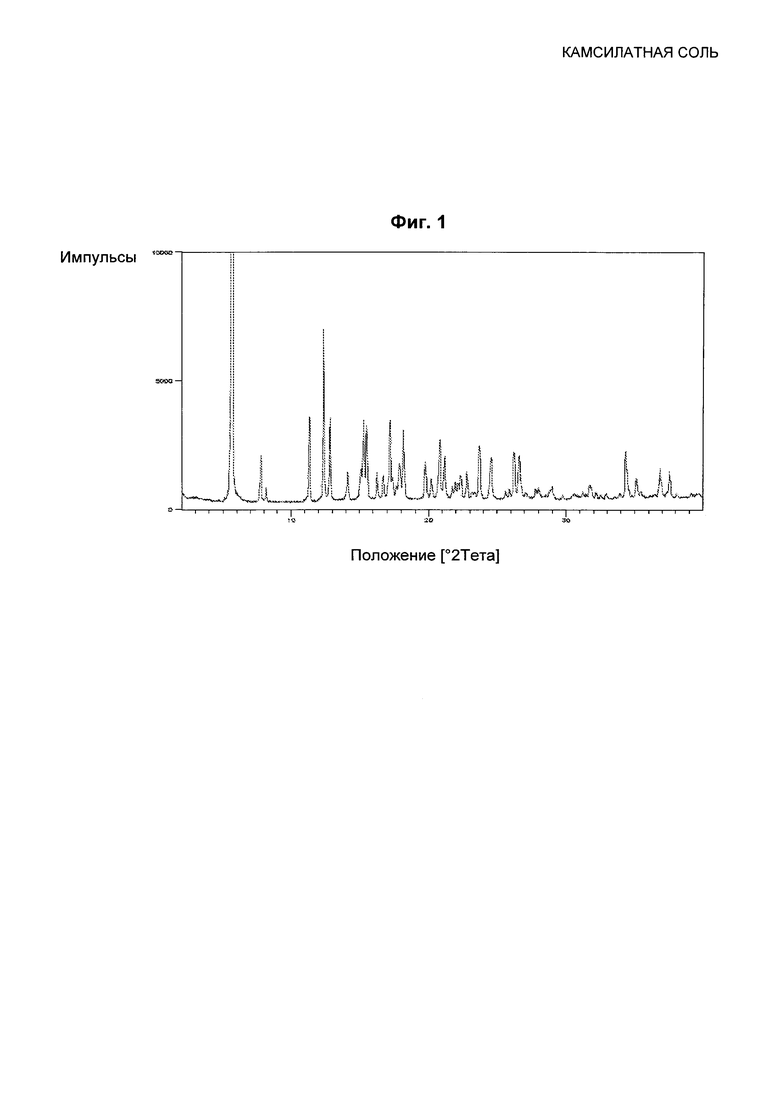
Изобретение относится к области органической химии, а именно к камсилатной соли (1r,1'R,4R)-4-метокси-5ʺ-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2'-инден-1'2'-имидазол]-4ʺ-амина. Также изобретение относится к фармацевтической композиции, содержащей эту соль, и способу лечения, основанному на использовании указанной камсилатной соли. Технический результат: получена новая соль, полезная при лечении связанных с Aβ патологий, таких как болезнь Альцгеймера, синдром Дауна, β-амилоидная ангиопатия и др. 6 н. и 4 з.п. ф-лы, 1 ил., 2 табл., 7 пр.
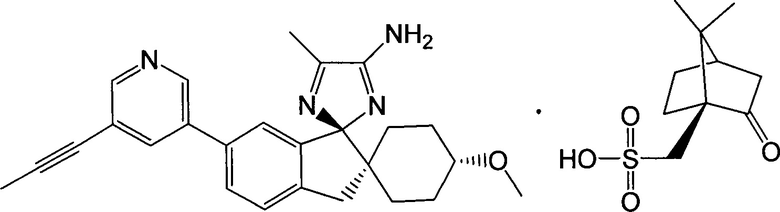
1. Камсилатная соль (1r,1'R,4R)-4-метокси-5''-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2'-инден-1',2''-имидазол]-4''-амина:
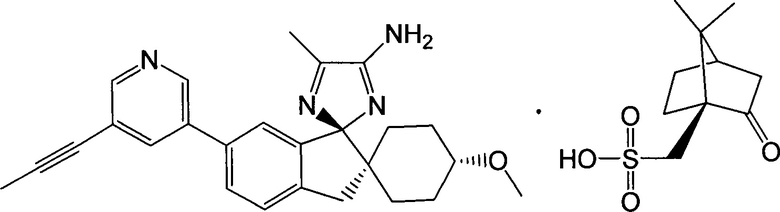 .
.
2. Камсилатная соль (1r,1'R,4R)-4-метокси-5''-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2'-инден-1',2''-имидазол]-4''-амина:
 ,
,
характеризующаяся тем, что указанная камсилатная соль имеет картину дифракции рентгеновских лучей на порошке (ДРЛП), демонстрирующую, по существу, следующие очень сильные (vs), сильные (s) и средние (m) пики с d-значениями:
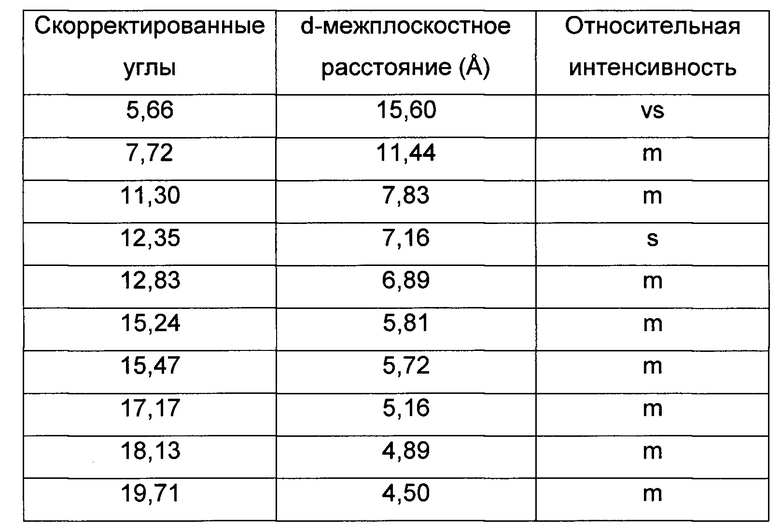
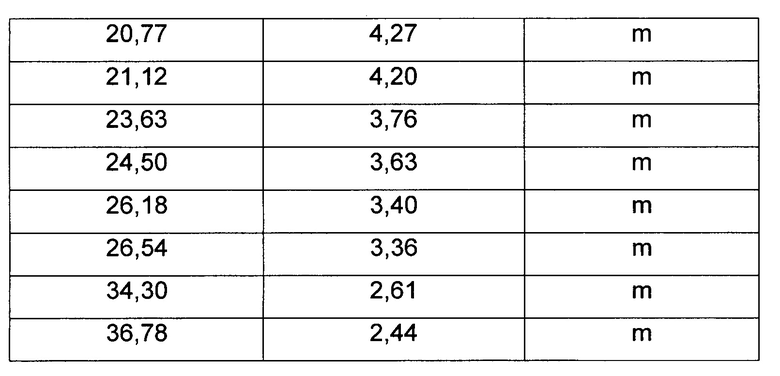
3. Камсилатная соль (1r,1'R,4R)-4-метокси-5''-метил-6'-[5-(проп-1-ин-1-ил)пиридин-3-ил]-3'Н-диспиро[циклогексан-1,2'-инден-1',2''-имидазол]-4''-амина:
 ,
,
характеризующаяся тем, что указанная камсилатная соль имеет картину дифракции рентгеновских лучей на порошке, по существу такую, как показанная на Фиг.1.
4. Фармацевтическая композиция для лечения или предупреждения связанной с Аβ (амилоидный β-пептид) патологии, содержащая в качестве активного ингредиента терапевтически эффективное количество соли по пп.1, 2 или 3 совместно с по меньшей мере одним фармацевтически приемлемым эксципиентом, носителем или разбавителем.
5. Соль по пп.1, 2 или 3 для использования в качестве лекарственного средства для лечения или предупреждения связанной с Аβ патологии.
6. Соль по п.5 для использования в качестве лекарственного средства для лечения или предупреждения связанной с Аβ патологии, где указанной связанной с Аβ патологией является синдром Дауна, β-амилоидная ангиопатия, церебральная амилоидная ангиопатия, наследственное церебральное кровоизлияние, расстройство, ассоциированное с когнитивным нарушением, MCI ("умеренное когнитивное нарушение"), болезнь Альцгеймера, потеря памяти, симптомы дефицита внимания, ассоциированные с болезнью Альцгеймера, нейродегенерация, ассоциированная с болезнью Альцгеймера, деменция смешанного сосудистого происхождения, деменция дегенеративного происхождения, пресенильная деменция, сенильная деменция, деменция, ассоциированная с болезнью Паркинсона, прогрессивный надъядерный паралич или кортикальная базальная дегенерация.
7. Соль по п.6 для использования в качестве лекарственного средства для лечения или предупреждения болезни Альцгеймера.
8. Способ лечения или предупреждения связанной с Аβ патологии у пациента, нуждающегося в таком лечении или предупреждении, включающий введение указанному пациенту терапевтически эффективного количества соли по пп.1, 2 или 3.
9. Способ по п.8, где указанной связанной с Аβ патологией является синдром Дауна, β-амилоидная ангиопатия, церебральная амилоидная ангиопатия, наследственное церебральное кровоизлияние, расстройство, ассоциированное с когнитивным нарушением, MCI ("умеренное когнитивное нарушение"), болезнь Альцгеймера, потеря памяти, симптомы дефицита внимания, ассоциированные с болезнью Альцгеймера, нейродегенерация, ассоциированная с болезнью Альцгеймера, деменция смешанного сосудистого происхождения, деменция дегенеративного происхождения, пресенильная деменция, сенильная деменция, деменция, ассоциированная с болезнью Паркинсона, прогрессивный надъядерный паралич или кортикальная базальная дегенерация.
10. Способ лечения или предупреждения болезни Альцгеймера у пациента, нуждающегося в таком лечении или предупреждении, включающий введение указанному пациенту терапевтически эффективного количества соли по пп.1, 2 или 3.
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| RU 2008121756 A, 27.12.2009. | |||
Авторы
Даты
2017-12-12—Публикация
2013-06-20—Подача