Область техники, к которой относится изобретение
Настоящее изобретение относится к производному циннамида типа морфолина и к фармацевтическому средству, содержащему данное соединение в качестве активного ингредиента. Более конкретно настоящее изобретение относится к непептидному двуядерному производному циннамида и ингибитору продукции амилоида-β (далее называемого как Aβ), который содержит данное соединение в качестве активного ингредиента и особенно эффективен при лечении нейродегенеративного заболевания, вызываемого Aβ, такого как болезнь Альцгеймера или синдром Дауна.
Предпосылки создания изобретения
Болезнь Альцгеймера является заболеванием, характеризующимся дегенерацией и потерей нейронов, а также образованием старческих бляшек и нейрофибриллярной дегенерацией. В настоящее время болезнь Альцгеймера лечат только методами симптоматической терапии с использованием средства для улучшения симптомов, типичным представителем которого является ингибитор ацетилхолинэстеразы, а фундаментальное лекарственное средство, ингибирующее прогрессирование заболевания, все еще не создано. Необходимо разработать способ контроля причины возникновения патологии, чтобы создать фундаментальное лекарственное средство для лечения болезни Альцгеймера.
Считается, что Aβ-белки в качестве метаболитов амилоидных белков-предшественников (далее называемых как APP) сильно вовлечены в процессы дегенерации и потери нейронов и возникновения симптомов деменции (см. непатентные документы 1 и 2). Aβ-белок содержит в качестве основных ингредиентов Aβ40, состоящий из 40 аминокислот, и Aβ42, в котором число аминокислот на две больше на С-конце. Известно, что Aβ40 и Aβ42 обладают высокой агрегационной способностью (см. непатентный документ 3) и являются основными составляющими старческих бляшек (см. непатентные документы 3, 4 и 5). Известно также, что Aβ40 и Aβ42 отличаются увеличенной мутацией в генах APP и пресенилина, которая наблюдается при болезни Альцгеймера семейного типа (см. непатентные документы 6, 7 и 8). Поэтому ожидается, что соединение, понижающее продукцию Aβ40 и Aβ42, будет ингибитором прогрессирования или профилактическим средством для болезни Альцгеймера.
Aβ продуцируется в результате расщепления APP β-секретазой и затем γ-секретазой. По этой причине были предприняты попытки создания ингибиторов β-секретазы и γ-секретазы, чтобы ингибировать продукцию Aβ. Многие из указанных ингибиторов секретаз уже известны, например пептиды и миметики пептидов, такие как L-685458 (см. непатентный документ 9) и LY-411575 (см. непатентные документы 10, 11 и 12).
[Непатентный документ 1] Klein WL, and seven others, Alzheimer,s disease-affected brain: Presence of oligomeric A(ligands (ADDLs) suggests a molecular basis for reversible memory loss, Proceding National Academy of Science USA 2003, Sep 2; 100(18), p.10417-10422;
[Непатентный документ 2] Nitsch RM, and sixteen others, Antibodies against β-amyloid slow cognitive decline in Alzheimer,s disease, Neuron, 2003, May 22; 38, p.547-554;
[Непатентный документ 3] Jarrett JT, and two others, The carboxy terminus of the (amyloid protein is critical for the seeding of amyloid formation: Implications for the pathogenesis of Alzheimer,s disease, Biochemistry, 1993, 32(18), p.4693-4697;
[Непатентный документ 4] Glenner GG, и one other, Alzheimer,s disease: initial report of the purification and characterization of a novel cerebrovascular amyloid protein, Biochemical and biophysical research communications, 1984, May 16, 120(3), p.885-890;
[Непатентный документ 5] Masters CL, and five others, Amyloid plaque core protein in Alzheimer disease and Down syndrome, Proceding National Academy of Science USA, 1985, Jun, 82(12), p.4245-4249;
[Непатентный документ 6] Gouras GK, and eleven others, Intraneuronal Aβ42 accumulation in human brain, American Journal of Pathology, 2000, Jan, 156(1), p.15-20;
[Непатентный документ 7] Scheuner D, and twenty others, Secreted amyloid β-protein similar to that in the senile plaques of Alzheimer,s disease is increased in vivo by the presenilin 1 and 2 and APP mutations linked to familial Alzheimer,s disease, Nature Medicine, 1996, Aug, 2(8), p.864-870;
[Непатентный документ 8] Forman MS, and four others, Differential effects of the swedish mutant amyloid precursor protein on β-amyloid accumulation and secretion in neurons and nonneuronal cells, The Journal of Biological Chemistry, 1997, Dec 19, 272(51), p.32247-32253;
[Непатентный документ 9] Shearman MS, and nine others, L-685,458, an Aspartyl Protease Transition State Mimic, Is a Potent Inhibitor of Amyloid β-Protein Precursor γ-Secretase Activity, Biochemistry, 2000, Aug 1, 39(30), p.8698-8704;
[Непатентный документ 10] Shearman MS, and six others, Catalytic Site-Directed γ-Secretase Complex Inhibitors Do Not Discriminate Pharmacologically between Notch S3 and β-APP Cleavages, Biochemistry, 2003, Jun 24, 42(24), p.7580-7586;
[Непатентный документ 11] Lanz TA, and three others, Studies of A(pharmacodynamics in the brain, cerebrospinal fluid, and plasma in young (plaque-free) Tg2576 mice using the γ-secretase inhibitor N2-[(2S)-2-(3,5-difluorophenyl)-2-hydroxyethanoyl]-N1-[(7S)-5-methyl-6-oxo-6,7-dihydro-5H-dibenzo[b,d]azepin-7-yl]-L-alaninamide (LY-411575), The journal of pharmacology and experimental therapeutics, 2004, Apr, 309(1), p.49-55;
[Непатентный документ 12] Wong GT, and twelve others, Chronic treatment with the γ-secretase inhibitor LY-411,575 inhibits β-amyloid peptide production and alters lymphopoiesis and intestinal cell differentiation, The journal of biological chemistry, 2004, Mar 26, 279(13), p.12876-12882.
Раскрытие сущности изобретения
Задачи, решаемые изобретением
Как описано выше, соединение, которое ингибирует продукцию Aβ40 и Aβ42 из APP, предполагается в качестве терапевтического или профилактического средства для заболевания, вызываемого Aβ, типичным представителем которого является болезнь Альцгеймера. Однако непептидное соединение, обладающее высокой эффективностью в отношении ингибирования продукции Aβ40 и Aβ42, все еще не известно. Следовательно, существует потребность в новом соединении с низкой молекулярной массой, которое будет ингибировать продукцию Aβ40 и Aβ42.
Средства решения указанных задач
В результате обширных исследований авторы настоящего изобретения обнаружили непептидное производное циннамида типа морфолина, которое ингибирует прежде всего продукцию Aβ40 и Aβ42 из APP, и, таким образом, разработали профилактическое или терапевтическое средство для заболевания, вызываемого Aβ, типичным представителем которого является болезнь Альцгеймера. Данная находка привела к созданию настоящего изобретения.
В частности, в соответствии с настоящим изобретением предлагаются:
1) Соединение, представленное формулой (I):
[Формула 1]

или его фармакологически приемлемая соль, где
(a) R1, R2, R3 и R4 являются одинаковыми или различными, и каждый представляет собой атом водорода или C1-6алкильную группу;
X1 представляет собой C1-6алкиленовую группу, где C1-6алкиленовая группа может быть замещена 1-3 гидроксильными группами или С1-6алкильными группами, где C1-6алкильные группы могут быть замещены 1-3 гидроксильными группами; или C3-13циклоалкильной группой, образованной двумя С1-6алкильными группами, вместе присоединенными к одному и тому же атому углерода C1-6алкиленовой группы;
Xa представляет собой метоксигруппу или атом фтора;
Xb представляет собой атом кислорода или метиленовую группу, при условии, что Xb представляет собой только атом кислорода, когда Xa представляет собой метоксигруппу; и
Ar1 представляет собой арильную группу, пиридинильную группу, арилоксигруппу или пиридинилоксигруппу, которая может быть замещена 1-3 заместителями, выбранными из группы A1 заместителей;
(b) Ar1-X1- представляет собой C3-8циклоалкильную группу, конденсированную с бензольным кольцом, где одна метиленовая группа в C3-8циклоалкильной группе может быть замещена атомом кислорода, C3-8циклоалкильная группа может быть замещена 1-3 гидроксильными группами и/или C1-6алкильными группами, и бензольное кольцо может быть замещено 1-3 заместителями, выбранными из группы A1 заместителей, и R1, R2, R3, R4, Xa и Xb являются такими, как определено в (a);
(c) один из R1 и R2 и один из R3 и R4 являются одинаковыми или различными и каждый представляет собой атом водорода или C1-6алкильную группу; другой из R1 и R2 и другой из R3 и R4, вместе с атомами углерода, к которым они соответственно присоединены, образуют C3-8циклоалкильную группу, где C3-8циклоалкильная группа может быть замещена 1-3 заместителями, выбранными из группы A1 заместителей, и X1, Xa, Xb и Ar1 являются такими, как определено в (a) или (b);
(d) Ar1-X1- и R4, вместе с атомом азота, к которому группа Ar1-X1- присоединена, и атомом углерода, к которому R4 присоединен, образуют 4-8-членную азотсодержащую гетероциклическую группу, которая может быть замещена арильной группой или пиридинильной группой, где одна метиленовая группа в 4-8-членной азотсодержащей гетероциклической группе может быть замещена метиленовой группой, замещенной 1 или 2 заместителями, выбранными из группы A1 заместителей, виниленовой группой, которая может быть замещена 1 или 2 заместителями, выбранными из группы A1 заместителей, атомом кислорода или иминогруппой, которая может быть замещена заместителем, выбранным из группы A1 заместителей, и арильная или пиридинильная группа может быть замещена 1-3 заместителями, выбранными из группы A1 заместителей, Xb представляет собой атом кислорода, и R1, R2, R3 и Xa являются такими, как определено в (a) и (b);
(e) R1 и R2, вместе с атомом углерода, к которому они присоединены, образуют C3-8циклоалкильную группу, и R3, R4, X1, Xa, Xb и Ar1 являются такими, как определено в (a) и (b); или
(f) R3 и R4, вместе с атомом углерода, к которому они присоединены, образуют C3-8циклоалкильную группу, и R1, R2, X1, Xa, Xb и Ar1 являются такими, как определено в (a) и (b)
(группа А1 заместителей: (1) атом галогена, (2) гидроксильная группа, (3) цианогруппа, (4) C3-8циклоалкильная группа, (5) C3-8циклоалкоксигруппа, (6) C1-6алкильная группа, где C1-6алкильная группа может быть замещена 1-5 атомами галогена или одной-тремя C1-6алкоксигруппами, (7) аминогруппа, которая может быть замещена одной или двумя C1-6алкильными группами, где C1-6алкильные группы могут быть замещены 1-5 атомами галогена, (8) C1-6алкоксигруппа, где C1-6алкоксигруппа может быть замещена 1-5 атомами галогена, и (9) карбамоильная группа, которая может быть замещена одной или двумя C1-6алкильными группами, где C1-6алкильные группы могут быть замещены 1-3 атомами галогена);
2) Соединение или его фармакологически приемлемая соль по пункту 1) выше, где соединение представлено формулой (I-a):
[Формула 2]
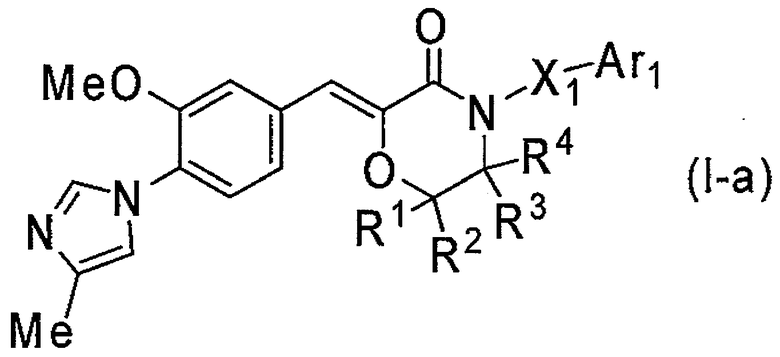
где R1, R2, R3, R4, X1 и Ar1 являются такими, как определено выше в пункте 1);
3) Соединение или его фармакологически приемлемая соль по пункту 1) выше, где соединение представлено формулой (II):
[Формула 3]

где R1, R2, R3, R4, Xa и Xb являются такими, как определено выше в пункте 1), R5 и R6 являются одинаковыми или различными и каждый представляет собой атом водорода или C1-6алкильную группу, где C1-6алкильная группа может быть замещена 1-3 гидроксильными группами, и Ar1-a представляет собой фенильную группу или пиридинильную группу, которая может быть замещена 1-3 заместителями, выбранными из группы A1 заместителей, определенной выше в пункте 1);
4) Соединение или его фармакологически приемлемая соль по пункту 3) выше, где соединение представлено формулой (II-a):
[Формула 4]

где R1, R2, R3 и R4 являются такими, как определено выше в пункте 1), и R5, R6 и Ar1-a являются такими, как определено выше в пункте 3);
5) Соединение или его фармакологически приемлемая соль по пункту 3) выше, где соединение представлено формулой (II-b):
[Формула 5]

где R1, R2, R3 и R4 являются такими, как определено выше в пункте 1), и R5, R6 и Ar1-a являются такими, как определено выше в пункте 3);
6) Соединение или его фармакологически приемлемая соль по пункту 3) выше, где соединение представлено формулой (II-c):
[Формула 6]

где R1, R2, R3 и R4 являются такими, как определено выше в пункте 1), R7 представляет собой атом водорода или C1-6алкильную группу и Ar1-a является таким, как определено выше в пункте 3);
7) Соединение или его фармакологически приемлемая соль по пункту 3) выше, где соединение представлено формулой (II-d):
[Формула 7]
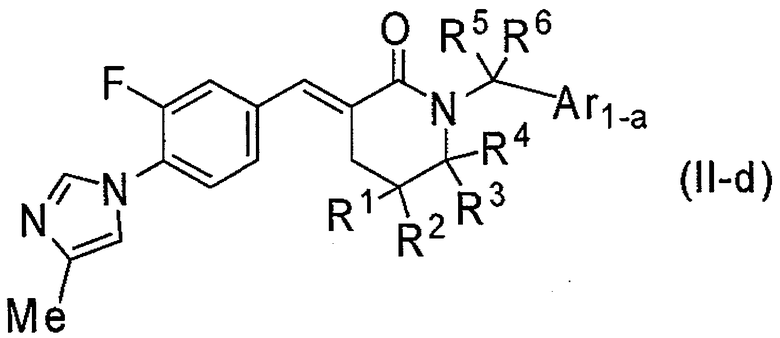
где R1, R2, R3 и R4 являются такими, как определено выше в пункте 1), и R5, R6 и Ar1-a являются такими, как определено выше в пункте 3);
8) Соединение или его фармакологически приемлемая соль по пункту 3) выше, где соединение представлено формулой (II-e):
[Формула 8]
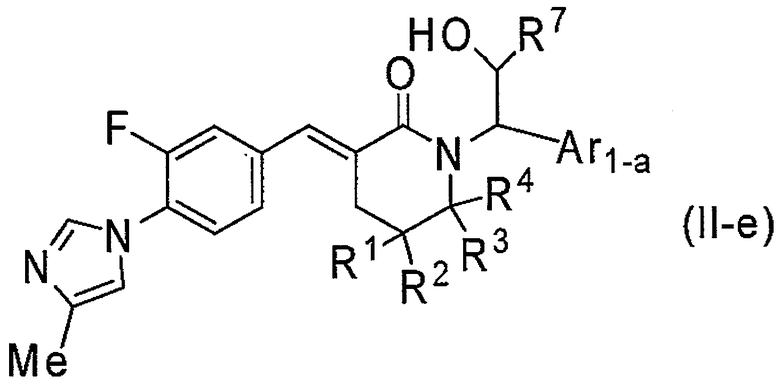
где R1, R2, R3 и R4 являются такими, как определено выше в пункте 1), Ar1-a является таким, как определено выше в пункте 3), и R7 является таким, как определено выше в пункте 6);
9) Соединение или его фармакологически приемлемая соль по пункту 1) выше, где соединение представлено формулой (I-b):
[Формула 9]

где R1, R2, R3 и R4 являются такими, как определено выше в пункте 1), R13 и R14 являются одинаковыми или различными и каждый представляет собой атом водорода или заместитель, выбранный из группы A1 заместителей, определенной выше в пункте 1), и Y представляет собой метиленовую группу или атом кислорода;
10) Соединение или его фармакологически приемлемая соль по пункту 9) выше, где R13 и R14 являются одинаковыми или различными и каждый представляет собой атом водорода, атом галогена или C1-6алкоксигруппу;
11) Соединение или его фармакологически приемлемая соль по пункту 1) выше, где соединение представлено формулой (I-c):
[Формула 10]

где R1 и R2 являются такими, как определено выше в пункте 1), Ar1-c представляет собой фенильную группу или пиридинильную группу, которая может быть замещена 1-3 заместителями, которые являются одинаковыми или различными и выбраны из группы A1 заместителей, Z1 представляет собой метиленовую группу или виниленовую группу, которая может быть замещена 1 или 2 заместителями, выбранными из группы A1 заместителей, определенной выше в пункте 1), атомом кислорода или иминогруппой, которая может быть замещена заместителем, выбранным из группы A1 заместителей,
и n и m являются одинаковыми или различными и каждый представляет собой целое число от 0 до 2;
12) Соединение или его фармакологически приемлемая соль по пункту 11) выше, где Z1 представляет собой метиленовую группу, где метиленовая группа может быть замещена 1 или 2 заместителями, которые являются одинаковыми или различными и выбраны из группы, состоящей из C1-6алкильной группы и гидроксильной группы, и n и m, каждый, равен 1;
13) Соединение или его фармакологически приемлемая соль по пункту 11) выше, где Z1 представляет собой атом кислорода, и n и m равно целому числу 1;
14) Соединение или его фармакологически приемлемая соль по пункту 1) выше, где Ar1 представляет собой арильную группу или пиридинильную группу, или арильную группу или пиридинильную группу, замещенную 1-3 атомами галогена;
15) Соединение или его фармакологически приемлемая соль по пункту 1) выше, где Ar1 представляет собой фенильную группу или пиридинильную группу, или фенильную группу или пиридинильную группу, замещенную 1-3 атомами галогена;
16) Соединение или его фармакологически приемлемая соль по пункту 1) выше, где соединение выбрано из следующей группы, включающей:
1) (Z)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-(3,4,5-трифторбензил)морфолин-3-он,
2) (Z)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-(2,3,4-трифторбензил)морфолин-3-он,
3) (Z)-(S)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метил-4-(3,4,5-трифторбензил)морфолин-3-он,
4) (Z)-(R)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метил-4-(3,4,5-трифторбензил)морфолин-3-он,
5) (Z)-(S)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метил-4-(2,3,4-трифторбензил)морфолин-3-он,
6) (Z)-(R)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метил-4-(2,3,4-трифторбензил)морфолин-3-он,
7) (Z)-4-[(S)-1-(4-фторфенил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
8) (Z)-(R)-4-[(S)-1-(4-фторфенил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
9) (Z)-(S)-4-[(S)-1-(4-фторфенил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
10) (Z)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-[(S)-1-(3,4,5-трифторфенил)этил]морфолин-3-он,
11) (Z)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-[(R)-1-(3,4,5-трифторфенил)этил]морфолин-3-он,
12) (Z)-4-[(S)-хроман-4-ил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
13) (Z)-(S)-4-[(S)-хроман-4-ил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
14) (Z)-(R)-4-[(S)-хроман-4-ил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
15) (Z)-(6S,9aR)-6-(4-фторфенил)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)бензилиден]гексагидропиридо[2,1-c][1,4]оксазин-4-он,
16) (Z)-(6R,9aS)-6-(4-фторфенил)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)бензилиден]гексагидропиридо[2,1-c][1,4]оксазин-4-он,
17) (Z)-(S)-4-[(S)-1-(6-хлорпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
18) (Z)-(S)-4-[(R)-1-(6-хлорпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
19) (Z)-(S)-4-[(S)-1-(5-хлорпиридин-2-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
20) (Z)-(S)-4-[(R)-1-(5-хлорпиридин-2-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
21) (Z)-(S)-4-[(S)-1-(2,6-дифторпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
22) (Z)-(S)-4-[(R)-1-(2,6-дифторпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
23) (Z)-(S)-4-[(S)-1-(2,3-дифторпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
24) (Z)-(S)-4-[(R)-1-(2,3-дифторпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
25) (Z)-(S)-4-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
26) (Z)-4-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
27) (Z)-4-[(R)-1-(4-фторфенил)-2-гидроксиэтил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
28) (Z)-(6R)-4-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
29) (Z)-4-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]морфолин-3-он,
30) (Z)-4-[(1R,2R)-1-(3,4-дифторфенил)-2-гидроксипропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]морфолин-3-он,
31) (Z)-(S)-4-[(1R,2R)-1-(4-фторфенил)-2-гидроксипропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
32) (Z)-4-[(1R,2R)-1-(4-фторфенил)-2-гидроксипропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
33) (Z)-(S)-4-[(1R,2R)-1-(3,4-дифторфенил)-2-гидроксипропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
34) (Z)-4-[(1R,2R)-1-(3,4-дифторфенил)-2-гидроксипропил]-2-[1-[3-метокси-4-(метилимидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
35) (Z)-(S)-4-[(S)-2-гидрокси-1-метил-1-(3,4,5-трифторфенил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
36) (Z)-(6S)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метил-4-[(S)-1-(3,4,5-трифторфенил)этил]морфолин-3-он,
37) (Z)-(6S)-4-[1-(4-фторфенил)-1-метилэтил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
38) (Z)-(6S)-4-[1-(4-фторфенил)циклопропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
39) (Z)-(6S,9aR)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)бензилиден]-6-(3,4,5-трифторфенил)гексагидропиридо[2,1-c][1,4]оксазин-4-он,
40) (Z)-(6S,9aR)-6-(3,4-дифторфенил)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)бензилиден]гексагидропиридо[2,1-c][1,4]оксазин-4-он,
41) (Z)-(6S,9aR)-6-(2,6-дифторпиридин-3-ил)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)бензилиден]гексагидропиридо[2,1-c][1,4]оксазин-4-он,
42) (Z)-(S)-4-[(S)-1-(5-фторпиридин-2-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
43) (Z)-(S)-4-[(S)-1-(2-хлорпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
44) (Z)-(S)-4-[(S)-1-(2-хлор-3-фторпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
45) (Z)-(S)-4-[(S)-1-(2,6-дифторпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
46) (Z)-4-[(S)-1-(2-хлорпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
47) (Z)-4-[(S)-1-(2,6-дифторпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
48) (Z)-4-[(S)-1-(6-фторпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
49) (Z)-4-[(S)-1-(6-хлорпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
50) (Z)-4-[(S)-1-(2,3-дифторпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
51) (Z)-4-[(S)-1-(5-хлорпиридин-2-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
52) (Z)-(R)-4-[(S)-1-(2,6-дифторпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
53) (Z)-(S)-4-(4-фторбензил)-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
54) (Z)-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-[(S)-1-(4-трифторфенил)этил]-6,6-диметилморфолин-3-он,
55) (Z)-4-[(S)-хроман-4-ил]-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
56) (Z)-(S)-4-[(S)-хроман-4-ил]-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
57) (Z)-(S)-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-6-метилморфолин-3-он,
58) (Z)-(S)-4-[(1R,2R)-1-(3,4-дифторфенил)-2-гидроксипропил]-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
59) (Z)-(S)-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-[(1R,2R)-1-(4-фторфенил)-2-гидроксипропил]-6-метилморфолин-3-он,
60) (Z)-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-6,6-диметилморфолин-3-он,
61) (Z)-4-[(1R,2R)-1-(3,4-дифторфенил)-2-гидроксипропил]-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
62) 1-[1-(2,4-дифторфенил)этил]-3-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]-(E)-метилиден}пиперидин-2-он,
63) (E)-(S)-3-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}-1-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-5-метилпиперидин-2-он,
64) (E)-3-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}-1-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]пиперидин-2-он,
65) (E)-3-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}-1-[(2R,3R)-3-гидрокси-1,1-диметилиндан-2-ил]пиперидин-2-он,
66) (E)-3-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}-1-[(S)-2-гидрокси-1-метил-1-(3,4,5-трифторфенил)этил]пиперидин-2-он,
67) (E)-3-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}-1-[1-(4-фторфенил)-1-метилэтил]пиперидин-2-он,
68) (E)-(R)-3-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}-1-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-5-метилпиперидин-2-он,
69) (E)-(S)-1-[(1R,2R)-1-(3,4-дифторфенил)-2-гидроксипропил]-3-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}-5-метилпиперидин-2-он,
70) (Z)-(6S,8aR)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)бензилиден]-6-(3,4,5-трифторфенил)тетрагидропирроло[2,1-c][1,4]оксазин-4-он,
71) (6S,9aR)-6-(4-хлорфенил)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]-(Z)-метилиден}гексагидропиридо[2,1-c][1,4]оксазин-4-он,
72) (6R,9aR)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]-(Z)-метилиден}-6-(3,4,5-трифторфенил)-тетрагидро[1,4]оксазино[3,4-c][1,4]оксазин-4-он,
73) (6R,9aR)-6-(3,4-дифторфенил)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]-(Z)-метилиден}тетрагидро[1,4]оксазино[3,4-c][1,4]оксазин-4-он,
74) (6R,9aR)-6-(4-фторфенил)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]-(Z)-метилиден}тетрагидро[1,4]оксазино[3,4-c][1,4]оксазин-4-он и
75) (6R,9aR)-6-(4-хлорфенил)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]-(Z)-метилиден}тетрагидро[1,4]оксазино[3,4-c]оксазин-4-он;
17) Фармацевтическое средство, содержащее соединение или его фармакологически приемлемую соль по любому из пунктов 1)-16) выше в качестве активного ингредиента;
18) Фармацевтическое средство по пункту 17) выше для предупреждения или лечения заболевания, вызываемого амилоидом-β, и
19) Фармацевтическое средство по пункту 18) выше, где заболеванием, вызываемым амилоидом-β, является болезнь Альцгеймера, старческая деменция, синдром Дауна или амилоидоз.
Соединение общей формулы (I) или его фармакологически приемлемая соль по настоящему изобретению и профилактическое или терапевтическое средство для заболевания, вызываемого Aβ, по настоящему изобретению являются новыми и не описаны в каких-либо публикациях.
Далее объяснено применение значений, терминов и тому подобное, используемых в данном описании, и настоящее изобретение описано более подробно.
В данном описании структурная формула соединения может для удобства представлять какой-либо изомер. Однако настоящее изобретение включает все изомеры и изомерные смеси, такие как геометрические изомеры, которые могут образовываться в связи со структурой соединения, оптические изомеры, образование которых основано на наличии асимметричного атома углерода, стереоизомеры и таутомеры. Настоящее изобретение не ограничивается описанием выбранной из соображений удобства химической формулы и может охватывать любой из изомеров или их смеси. Соответственно, соединение по настоящему изобретению может иметь в молекуле асимметричный углеродный атом и существовать в виде оптически активного соединения или рацемата, и настоящее изобретение включает, но без ограничений, как оптически активное соединение, так и рацемат. Хотя могут существовать кристаллические полиморфы соединения, данное соединение не ограничивается ими и может существовать в форме монокристалла или смеси монокристаллов. Соединение может быть негидратированным или гидратом.
“Заболевание, вызываемое Aβ” относится к широкому кругу заболеваний, таких как болезнь Альцгеймера (см., например, Klein WL, and seven others, Alzheimer's disease-affected brain: Presence of oligomeric A(ligands (ADDLs) suggests a molecular basis for reversible memory loss, Proceding National Academy of Science USA, 2003, Sep 2, 100(18), p.10417-10422; Nitsch RM, and sixteen others, Antibodies against β-amyloid slow cognitive decline in Alzheimer's disease, Neuron, 2003, May 22, 38(4), p.547-554; Jarrett JT, and two others, The carboxy terminus of the (amyloid protein is critical for the seeding of amyloid formation: Implications for the pathogenesis of Alzheimer's disease, Biochemistry, 1993, May 11, 32(18), p.4693-4697; Glenner GG, and one other, Alzheimer's disease а: initial report of the purification and characterization of a novel cerebrovascular amyloid protein, Biochemical and biophysical research communications, 1984, May 16, 120(3), p.885-890; Masters CL, and six others, Amyloid plaque core protein in Alzheimer disease and Down syndrome, Proceding National Academy of Science USA, 1985, June, 82(12), p.4245-4249; Gouras GK, and eleven others, Intraneuronal Aβ42 accumulation in human brain, American journal of pathology, 2000, Jan, 156(1), p.15-20; Scheuner D, and twenty others, Secreted amyloid β-protein similar to that in the senile plaques of Alzheimer's disease is increased in vivo by the presenilin 1 and 2 and APP mutations linked to familial Alzheimer's disease, Nature Medicine, 1996, Aug, 2(8), p.864-870; and Forman MS, and four others, Differential effects of the swedish mutant amyloid precursor protein on β-amyloid accumulation and secretion in neurons and nonneuronal cells, The journal of biological chemistry, 1997, Dec 19, 272(51), p.32247-32253), старческая деменция (см., например, Blass JP, Brain metabolism and brain disease: Is metabolic deficiency the proximate cause of Alzheimer dementia? Journal of Neuroscience Research, 2001, Dec 1, 66(5), p.851-856), лобно-височная деменция (см., например, Evin G, and eleven others, Alternative transcripts of presenilin-1 associated with frontotemporal dementia, Neuroreport, 2002, Apr 16, 13(5), p.719-723), болезнь Пика (см., например, Yasuhara O, and three others, Accumulation of amyloid precursor protein in brain lesions of patients with Pick disease, Neuroscience Letters, 1994, Apr 25, 171(1-2), p.63-66), синдром Дауна (см., например, Teller JK, and ten others, Presence of soluble amyloid β-peptide precedes amyloid plaque formation in Down's syndrome, Nature Medicine, 1996, Jan, 2(1), p.93-95; and Tokuda T, and six others, Plasma levels of amyloid (proteins Aβ1-40 and Aβ1-42(43) are elevated in Down's syndrome, Annals of Neurology, 1997, Feb, 41(2), p.271-273), церебральная ангиопатия (см., например, Hayashi Y, and nine others, Evidence for presenilin-1 involvement in amyloid angiopathy in the Alzheimer's disease-affected brain, Brain Research, 1998, Apr 13, 789(2), p.307-314; Barelli H, and fifteen others, Characterization of new polyclonal antibodies specific for 40 and 42 amino acid-long amyloid (peptides: their use to examine the cell biology of presenilins and the immunohistochemistry of sporadic Alzheimer's disease and cerebral amyloid angiopathy cases, Molecular Medicine, 1997, Oct, 3(10), p.695-707; Calhoun ME, and ten others, Neuronal overexpression of mutant amyloid precursor protein results in prominent deposition of cerebrovascular amyloid, Proceding National Academy of Science USA, 1999, Nov 23, 96(24), p.14088-14093; and Dermaut B, and ten others, Cerebral amyloid angiopathy is a pathogenic lesion in Alzheimer's Disease due to a novel presenilin-1 mutation, Brain, 2001, Dec, 124(12), p.2383-2392), наследственная церебральная геморрагия с амилоидозом (голландского типа) (см., например, Cras P, and nine others, Presenile Alzheimer dementia characterized by amyloid angiopathy and large amyloid core type senile plaques in the APP 692Ala -->Gly mutation, Acta Neuropathologica (Berl), 1998, Sep, 96(3), p.253-260; Herzig MC, and fourteen others, A(is targeted to the vasculature in a mouse model of hereditary cerebral hemorrhage with amyloidosis, Nature Neuroscience, 2004, Sep, 7(9), p.954-960; van Duinen SG, and five others, Hereditary cerebral hemorrhage with amyloidosis in patients of Dutch origin is related to Alzheimer disease, Proceding National Academy of Science USA, 1987, Aug, 84(16), p.5991-5994; and Levy E, and eight others, Mutation of the Alzheimer's disease amyloid gene in hereditary cerebral hemorrhage, Dutch type, Science, 1990, Jun 1, 248(4959), p.1124-1126), когнитивное нарушение (см., например, Laws SM, and seven others, Association between the presenilin-1 mutation Glu318Gly and complaints of memory impairment, Neurobiology of Aging, 2002, Jan-Feb, 23(1), p.55-58), нарушение памяти и неспособность к обучению (см., например, Vaucher E, and five others, Object recognition memory and cholinergic parameters in mice expressing human presenilin 1 transgenes, Experimental Neurology, 2002 Jun, 175(2), p.398-406; Morgan D, and fourteen others, A(peptide vaccination prevents memory loss in an animal model of Alzheimer's disease, Nature, 2000 Dec 21-28, 408(6815), p.982-985; and Moran PM, and three others, Age-related learning deficits in transgenic mice expressing the 751-amino acid isoform of human β-amyloid precursor protein, Proceding National Academy of Science USA, 1995, June 6, 92(12), p.5341-5345), амилоидоз, церебральная ишемия (см., например, Laws SM, and seven others, Association between the presenilin-1 mutation Glu318Gly and complaints of memory impairment, Neurobiology of Aging, 2002, Jan-Feb, 23(1), p.55-58; Koistinaho M, and ten others, β-amyloid precursor protein transgenic mice that harbor diffuse A(deposits but do not form plaques show increased ischemic vulnerability: Role of inflammation, Proceding National Academy of Science USA, 2002, Feb 5, 99(3), p.1610-1615; and Zhang F, and four others, Increased susceptibility to ischemic brain damage in transgenic mice overexpressing the amyloid precursor protein, The journal of neuroscience, 1997, Oct 15, 17(20), p.7655-7661), сосудистая деменция (см., например, Sadowski M, and six others, Links between the pathology of Alzheimer's disease and vascular dementia, Neurochemical Research, 2004, Jun, 29(6), p.1257-1266), офтальмоплегия (см., например, O'Riordan S, and seven others, Presenilin-1 mutation (E280G), spastic paraparesis, and cranial MRI white-matter abnormalities, Neurology, 2002, Oct 8, 59(7), p.1108-1110), рассеянный склероз (см., например, Gehrmann J, and four others, Amyloid precursor protein (APP) expression in multiple sclerosis lesions, Glia, 1995, Oct, 15(2), p.141-51; and Reynolds WF, and six others, Myeloperoxidase polymorphism is associated with gender specific risk for Alzheimer's disease, Experimental Neurology, 1999, Jan, 155(1), p.31-41), травма головы, краниальная травма (см., например, Smith DH, and four others, Protein accumulation in traumatic brain injury, NeuroMolecular Medicine, 2003, 4(1-2), p.59-72), апраксия (см., например, Matsubara-Tsutsui M, and seven others, Molecular evidence of presenilin 1 mutation in familial early onset dementia, American journal of Medical Genetics, 2002, Apr 8, 114(3), p.292-298), первичное заболевание, семейная амилоидная нейропатия, болезнь повтора триплетов (см., например, Kirkitadze MD, and two others, Paradigm shifts in Alzheimer's disease and other neurodegenerative disorders: the emerging role of oligomeric assemblies, Journal of Neuroscience Research, 2002, Sep 1, 69(5), p.567-577; Evert BO, and eight others, Inflammatory genes are upreglulated in expanded ataxin-3-expressing cell lines and spinocerebellar ataxia type 3 brains, The Journal of Neuroscience, 2001, Aug 1, 21(15), p.5389-5396; and Mann DM, and one other, Deposition of amyloid(A4) protein within the brains of persons with dementing disorders other than Alzheimer's disease and Down's syndrome, Neuroscience Letters, 1990, Feb 5, 109(1-2), p.68-75), болезнь Паркинсона (см., например, Primavera J, and four others, Brain accumulation of amyloid-(in Non-Alzheimer Neurodegeneration, Journal of Alzheimer's Disease, 1999, Oct, 1(3), p.183-193), деменция с тельцами Леви (см., например, Giasson BI, and two others, Interactions of amyloidogenic proteins. NeuroMolecular Medicine, 2003, 4(1-2), p.49-58; Masliah E, and six others, β-amyloid peptides enhance α-synuclein accumulation and neuronal deficits in a trancgenic mouse model linking Alzheimer's disease and Parkinson's disease, Proceding National Academy of Science USA, 2001, Oct 9, 98(21), p.12245-12250; Barrachina M, and six others, Amyloid-(deposition in the cerebral cortex in Dementia with Lewy bodies is accompanied by a relative increase in AβPP mRNA isoforms containing the Kunitz protease inhibitor, Neurochemistry International, 2005, Feb, 46(3), p.253-260; and Primavera J, and four others, Brain accumulation of amyloid-(in Non-Alzheimer Neurodegeneration, Journal of Alzheimer's Disease, 1999, Oct, 1(3), p.183-193), комплекс паркинсонизм-деменция (см., например, Schmidt ML, and six others, Amyloid plaques in Guam amyotrophic lateral sclerosis/ parkinsonism-dementia complex contain species of A(similar to those found in the amyloid plaques of Alzheimer's disease and pathological aging, Acta Neuropathologica (Berl), 1998, Feb, 95(2), p.117-122; and Ito H, and three others, Demonstration of (amyloid protein-containing neurofibrillary tangles in parkinsonism-dementia complex on Guam, Neuropathology and applied neurobiology, 1991, Oct, 17(5), p.365-373), лобно-височная деменция и паркинсонизм, связанный с хромосомой 17 (см., например, Rosso SM, and three others, Coexistent tau and amyloid pathology in hereditary frontotemporal dementia with tau mutations, Annals of the New York academy of sciences, 2000, 920, p.115-119), деменция с аргирофильными зернами (см., например, Tolnay M, and four others, Low amyloid (Aβ) plaque load and relative predominance of diffuse plaques distinguish argyrophilic grain disease from Alzheimer's disease, Neuropathology and applied neurobiology, 1999, Aug, 25(4), p.295-305), болезнь Ниманна-Пика (см., например, Jin LW, and three others, Intracellular accumulation of amyloidogenic fragments of amyloid-(precursor protein in neurons with Niemann-Pick type C defects is associated with endosomal abnormalities, American Journal of Pathology, 2004, Mar, 164(3), p.975-985), боковой амиотрофический склероз (см., например, Sasaki S, and one other, Immunoreactivity of β-amyloid precursor protein in amyotrophic lateral sclerosis, Acta Neuropathologica(Berl), 1999, May, 97(5), p.463-468; Tamaoka A, and four others, Increased amyloid (protein in the skin of patients with amyotrophic lateral sclerosis, Journal of neurology, 2000, Aug, 247(8), p.633-635; Hamilton RL, and one other, Alzheimer disease pathology in amyotrophic lateral sclerosis, Acta Neuropathologica, 2004, Jun, 107(6), p.515-522; and Turner BJ, and six others, Brain β-amyloid accumulation in transgenic mice expressing mutant superoxide dismutase 1, Neurochemical Research, 2004, Dec, 29(12), p.2281-2286), гидроцефалия (см., например, Weller RO, Pathology of cerebrospinal fluid and interstitial fluid of the CNS: Significance for Alzheimer disease, prior disorders and multiple sclerosis, Journal of Neuropathology and Experimental Neurology, 1998, Oct, 57(10), p.885-894; Silverberg GD, and four others, Alzheimer's disease, normal-pressure hydrocephalus, and senescent changes in CSF circulatory physiology: a hypothesis, Lancet neurology, 2003, Aug, 2(8), p.506-511; Weller RO, and three others, Cerebral amyloid angiopathy: Accumulation of A(in interstitial fluid drainage pathways in Alzheimer's disease, Annals of the New York academy of sciences, 2000, Apr, 903, p.110-117; Yow HY, and one other, A role for cerebrovascular disease in determining the pattern of β-amyloid deposition in Alzheimer's disease, Neurology and applied neurobiology, 2002, 28, p.149; and Weller RO, and four others, Cerebrovasculardisease is a major factor in the failure of elimination of A(from the aging human brain, Annals of the New York academy of sciences, 2002, Nov, 977, p.162-168), парапарез (см., например, O'Riordan S, and seven others, Presenilin-1 mutation (E280G), spastic paraparesis, and cranial MRI white-matter abnormalities, Neurology, 2002, Oct 8, 59(7), p.1108-1110; Matsubara-Tsutsui M, and seven others, Molecular evidence of presenilin 1 mutation in familial early onset dementia, American journal of Medical Genetics, 2002, Apr 8, 114(3), p.292-298; Smith MJ, and eleven others, Variable phenotype of Alzheimer's disease with spastic paraparesis, Annals of Neurology, 2001, 49(1), p.125-129; and Crook R, and seventeen others, A variant of Alzheimer's disease with spastic pararesis and unusual plaques due to deletion of exon 9 of presenilin 1, Nature Medicine, 1998, Apr; 4(4), p.452-455), прогрессивный супрануклеарный паралич (см., например, Barrachina M, and six others, Amyloid-(deposition in the cerebral cortex in Dementia with Lewy bodies is accompanied by a relative increase in AβPP mRNA isoforms containing the Kunitz protease inhibitor, Neurochemistry International, 2005, Feb, 46(3), p.253-260; and Primavera J, and four others, Brain accumulation of amyloid-(in Non-Alzheimer Neurodegeneration, Jornal of Alzheimer's Disease, 1999, Oct, 1(3), p.183-193), внутримозговое кровоизлияние (см., например, Atwood CS, and three others, Cerebrovascular requirement for sealant, anti-coagulant and remodeling molecules that allow for the maintenance of vascular integrity and blood supply, Brain Research Reviews, 2003, Sep, 43(1), p.164-78; and Lowenson JD, and two others, Protein aging: Extracellular amyloid formation and intracellular repair, Trends in cardiovascular medicine, 1994, 4(1), p.3-8), конвульсия (см., например, Singleton AB, and thirteen others, Pathology of early-onset Alzheimer's disease cases bearing the Thr113-114ins presenilin-1 mutation, Brain, 2000, Dec, 123(Pt12), p.2467-2474), легкое когнитивное нарушение (см., например, Gattaz WF, and four others, Platelet phospholipase A2 activity in Alzheimer's disease and mild cognitive impairment, Journal of Neural Transmission, 2004, May, 111(5), p.591-601; and Assini A, and fourteen others, Plasma levels of amyloid β-protein 42 are increased in women with mild cognitive impariment, Neurology, 2004, Sep 14, 63(5), p.828-831) и артериосклероз (см., например, De Meyer GR, and eight others, Platelet phagocytosis and processing of β-amyloid precursor protein as a mechanism of macrophage activation in atherosclerosis, Circulation Reserach, 2002, Jun 14, 90(11), p.1197-1204).
"C1-6алкиленовая группа" относится к алкиленовой группе, содержащей 1-6 углеродных атомов. Предпочтительные примеры группы включают метиленовую группу, этиленовую группу, пропиленовую группу, бутиленовую группу и пентиленовую группу.
“C1-6алкильная группа" относится к алкильной группе, содержащей 1-6 углеродных атомов. Предпочтительные примеры группы включают неразветвленные или разветвленные алкильные группы, такие как метильная группа, этильная группа, н-пропильная группа, изопропильная группа, н-бутильная группа, изобутильная группа, трет-бутильная группа, н-пентильная группа, изопентильная группа, неопентильная группа, н-гексильная группа, 1-метилпропильная группа, 1,2-диметилпропильная группа, 1-этилпропильная группа, 1-метил-2-этилпропильная группа, 1-этил-2-метилпропильная группа, 1,1,2-триметилпропильная группа, 1-метилбутильная группа, 2-метилбутильная группа, 1,1-диметилбутильная группа, 2,2-диметилбутильная группа, 2-этилбутильная группа, 1,3-диметилбутильная группа, 2-метилпентильная группа и 3-метилпентильная группа.
“C3-13циклоалкильная группа” относится к циклической алкильной группе, содержащей 3-13 углеродных атомов. Предпочтительные примеры группы включают циклопропильную группу, циклобутильную группу, циклопентильную группу, циклогексильную группу, циклогептильную группу, циклооктильную группу, циклононанильную группу, циклодеканильную группу, циклоундеканильную группу, циклододеканильную группу и циклотридеканильную группу.
“Арильная группа” относится к "6-14-членной циклической ароматической углеводородной группе" или "5-14-членной ароматической гетероциклической группе". "6-14-Членная циклическая ароматическая углеводородная группа", используемая в данном описании, относится к моноциклической, бициклической или трициклической ароматической углеводородной группе, содержащей 6-14 углеродных атомов. Предпочтительные примеры группы включают 6-14-членные моноциклические, бициклические или трициклические ароматические углеводородные группы, такие как фенильная группа, инденильная группа, нафтильная группа, азуленильная группа, гепталенильная группа, бифенильная группа, флуоренильная группа, феналенильная группа, фенантренильная группа и антраценильная группа. "5-14-Членная ароматическая гетероциклическая группа" относится к моноциклической, бициклической или трициклической ароматической гетероциклической группе, содержащей 5-14 углеродных атомов. Предпочтительные примеры группы включают (1) азотсодержащие ароматические гетероциклические группы, такие как пирролильная группа, пиридильная группа, пиридазинильная группа, пиримидинильная группа, пиразинильная группа, пиразолинильная группа, имидазолильная группа, индолильная группа, изоиндолильная группа, индолизинильная группа, пуринильная группа, индазолильная группа, хинолильная группа, изохинолильная группа, хинолизинильная группа, фталазинильная группа, нафтиридинильная группа, хиноксалинильная группа, хиназолинильная группа, циннолинильная группа, птеридинильная группа, имидазотриазинильная группа, пиразинопиридазинильная группа, акридинильная группа, фенантридинильная группа, карбазолильная группа, перимидинильная группа, фенантролинильная группа и фенацильная группа, (2) содержащие серу ароматические гетероциклические группы, такие как тиенильная группа и бензотиенильная группа, (3) кислородсодержащие ароматические гетероциклические группы, такие как фурильная группа, пиранильная группа, циклопентапиранильная группа, бензофуранильная группа и изобензофуранильная группа, и (4) ароматические гетероциклические группы, содержащие два или более гетероатомов, выбранных из группы, состоящей из атома азота, атома серы и атома кислорода, такие как тиазолильная группа, изотиазолильная группа, бензотиазолинильная группа, бензотиадиазолильная группа, фенотиазинильная группа, изоксазолильная группа, фуразанильная группа, феноксазинильная группа, пиразолоксазолильная группа, имидазотиазолильная группа, тиенофурильная группа, фуропирролильная группа и пиридооксазинильная группа.
“Арилоксигруппа" относится к группе, в которой атом водорода в ароматическом углеводородном кольце "6-14-членной циклической ароматической углеводородной группы" или атом водорода в ароматическом гетероцикле "5-14-членной ароматической гетероциклической группы" замещен атомом кислорода.
“C3-8циклоалкильная группа, конденсированная с бензольным кольцом" может быть, например, группой формулы:
[Формула 11]

Бензольное кольцо может быть замещено 1-3 заместителями, выбранными из группы A1 заместителей, одна метиленовая группа в C3-8циклоалкильной группе может быть замещена атомом кислорода и C3-8циклоалкильная группа может быть замещена 1-3 гидроксильными группами и/или C1-6алкильными группами.
"4-8-Членная азотсодержащая гетероциклическая группа, образованная группой Ar1-X1- и R4 вместе с атомом азота, к которому Ar1-X1- присоединена, и атомом углерода, к которому R4 присоединен" может быть, например, группой формулы:
[Формула 12]
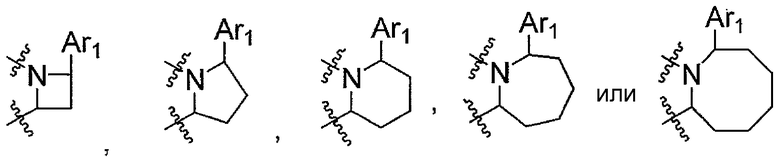
4-8-Членная азотсодержащая гетероциклическая группа может быть замещена арильной группой или пиридинильной группой, где арильная группа или пиридинильная группа может быть замещена 1-3 заместителями, выбранными из группы A1 заместителей. Кроме того, одна метиленовая группа в 4-8-членной азотсодержащей гетероциклической группе может быть замещена метиленовой группой, замещенной 1 или 2 заместителями, выбранными из группы A1 заместителей, виниленовой группой, которая может быть замещена 1 или 2 заместителями, выбранными из группы A1 заместителей, атомом кислорода или иминогруппой, которая может быть замещена заместителем, выбранным из группы A1 заместителей.
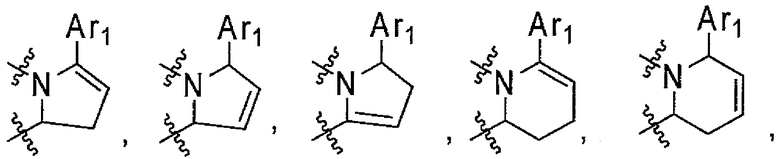
4-8-Членная азотсодержащая гетероциклическая группа, содержащая одну метиленовую группу, которая может быть замещена метиленовой группой, замещенной 1 или 2 заместителями, выбранными из группы A1 заместителей, виниленовой группой, которая может быть замещена 1 или 2 заместителями, выбранными из группы A1 заместителей, атомом кислорода или иминогруппой, которая может быть замещена заместителем, выбранным из группы A1 заместителей, может быть, например, группой, конкретно представленной формулой:
[Формула 13]

“C1-6ацильная группа", используемая в данном описании, относится к ацильной группе, содержащей 1-6 углеродных атомов. Предпочтительные примеры группы включают формильную группу, ацетильную группу, пропионильную группу, бутирильную группу, изобутирильную группу, пентаноильную группу и гексаноильную группу.
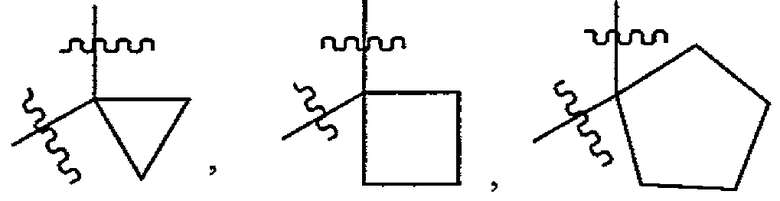
“C3-8циклоалкильная группа, образованная R1 и R2 вместе с атомом углерода, к которому они присоединены", или “C3-8циклоалкильная группа, образованная R3 и R4 вместе с атомом углерода, к которому они присоединены", может быть, например, группой, конкретно представленной формулой:
[Формула 14]

“C1-6алкиленовая группа, где C1-6алкиленовая группа может быть замещена 1-3 гидроксильными группами или С1-6алкильными группами, где C1-6алкильные группы могут быть замещены 1-3 гидроксильными группами, или C3-13циклоалкильной группой, образованной двумя С1-6алкильными группами, вместе присоединенными к одному и тому же атому углерода C1-6алкиленовой группы", может быть, например, группой, конкретно представленной формулой:
[Формула 15]


Группа А1 заместителей относится к следующим группам.
Группа А1 заместителей: (1) атом галогена, (2) гидроксильная группа, (3) цианогруппа, (4) C3-8циклоалкильная группа, (5) C3-8циклоалкоксигруппа, (6) C1-6алкильную группу, где C1-6алкильная группа может быть замещена 1-5 атомами галогена или одной-тремя C1-6алкоксигруппами, (7) аминогруппа, которая может быть замещена одной или двумя C1-6алкильными группами, где C1-6алкильные группы могут быть замещены 1-5 атомами галогена, (8) C1-6алкоксигруппа, где C1-6алкоксигруппа может быть замещена 1-5 атомами галогена, и (9) карбамоильная группа, которая может быть замещена одной или двумя C1-6алкильными группами, где C1-6алкильные группы могут быть замещены 1-3 атомами галогена.
"Атом галогена" при использовании в данном описании относится к атому фтора, атому хлора, атому брома, атому йода или подобному и предпочтительно является атомом фтора, атомом хлора или атомом брома.
“C3-8циклоалкильная группа” относится к циклической алкильной группе, содержащей 3-8 углеродных атомов. Предпочтительные примеры группы включают циклопропильную группу, циклобутильную группу, циклопентильную группу, циклогексильную группу, циклогептильную группу и циклооктильную группу.
“C3-8циклоалкоксигруппа" относится к циклической алкильной группе, содержащей 3-8 углеродных атомов, в которой один атом водорода замещен атомом кислорода. Предпочтительные примеры группы включают циклопропоксигруппу, циклобутоксигруппу, циклопентоксигруппу, циклогексоксигруппу, циклогептилоксигруппу и циклооктилоксигруппу.
“C1-6алкильная группа” является такой, как определено выше, и конкретные примеры группы описаны выше.
“C1-6алкоксигруппа" относится к алкильной группе, содержащей 1-6 углеродных атомов, в которой атом водорода замещен атомом кислорода. Предпочтительные примеры группы включают метоксигруппу, этоксигруппу, н-пропоксигруппу, изопропоксигруппу, н-бутоксигруппу, изобутоксигруппу, втор-бутоксигруппу, трет-бутоксигруппу, н-пентоксигруппу, изопентоксигруппу, втор-пентоксигруппу, трет-пентоксигруппу, н-гексоксигруппу, изогексоксигруппу, 1,2-диметилпропоксигруппу, 2-этилпропоксигруппу, 1-метил-2-этилпропоксигруппу, 1-этил-2-метилпропоксигруппу, 1,1,2-триметилпропоксигруппу, 1,1,2-триметилпропоксигруппу, 1,1-диметилбутоксигруппу, 2,2-диметилбутоксигруппу, 2-этилбутоксигруппу, 1,3-диметилбутоксигруппу, 2-метилпентоксигруппу, 3-метилпентоксигруппу и гексилоксигруппу.
"Аминогруппа, которая может быть замещена одной или двумя C1-6алкильными группами”, относится к аминогруппе, в которой один или два атома водорода замещены одной или двумя алкильными группами, содержащими 1-6 углеродных атомов. Предпочтительные примеры группы включают метиламиногруппу, диметиламиногруппу, этиламиногруппу, диэтиламиногруппу, н-пропиламиногруппу и ди-н-пропиламиногруппу.
“Карбамоильная группа, которая может быть замещена одной или двумя C1-6алкильными группами”, относится к карбамоильной группе, в которой один или два атома водорода замещены одной или двумя алкильными группами, содержащими 1-6 углеродных атомов. Предпочтительные примеры группы включают метилкарбамоильную группу, диметилкарбамоильную группу, этилкарбамоильную группу, диэтилкарбамоильную группу, н-пропилкарбамоильную группу и ди-н-пропилкарбамоильную группу.
В данном описании не существует особых ограничений на "фармакологически приемлемую соль", только чтобы она была фармакологически приемлемой солью, образованной соединением общей формулы (I), то есть была профилактическим или терапевтическим средством для заболевания, вызываемого Aβ. Предпочтительные конкретные примеры соли включают гидрогалогениды (такие как гидрофториды, гидрохлориды, гидробромиды и гидройодиды), соли неорганических кислот (такие как сульфаты, нитраты, перхлораты, фосфаты, карбонаты и бикарбонаты), органические карбоксилаты (такие как ацетаты, оксалаты, малеаты, тартраты, фумараты и цитраты), органические сульфонаты (такие как метансульфонаты, трифторметансульфонаты, этансульфонаты, бензолсульфонаты, толуолсульфонаты и камфорсульфонаты), соли аминокислот (такие как аспартаты и глутаматы), соли четвертичного амина, соли щелочных металлов (такие как натриевые соли и калиевые соли) и соли щелочноземельных металлов (такие как магниевые соли и кальциевые соли).
Далее описано соединение формулы (I) по настоящему изобретению.
В соединении формулы (I) или его фармакологически приемлемой соли предпочтительно:
(a) R1, R2, R3 и R4 являются одинаковыми или различными и каждый представляет собой атом водорода или C1-6алкильную группу;
X1 представляет собой C1-6алкиленовую группу, где C1-6алкиленовая группа может быть замещена 1-3 гидроксильными группами или С1-6алкильными группами, где C1-6алкильные группы могут быть замещены 1-3 гидроксильными группами; или C3-13циклоалкильной группой, образованной двумя С1-6алкильными группами, вместе присоединенными к одному и тому же атому углерода C1-6алкиленовой группы;
Xa представляет собой метоксигруппу или атом фтора;
Xb представляет собой атом кислорода или метиленовую группу, при условии, что Xb представляет собой только атом кислорода, когда Xa представляет собой метоксигруппу; и
Ar1 представляет собой арильную группу, пиридинильную группу, арилоксигруппу или пиридинилоксигруппу, которая может быть замещена 1-3 заместителями, выбранными из группы A1 заместителей;
(b) Ar1-X1- представляет собой C3-8циклоалкильную группу, конденсированную с бензольным кольцом, где одна метиленовая группа в C3-8циклоалкильной группе может быть замещена атомом кислорода, C3-8циклоалкильная группа может быть замещена 1-3 гидроксильными группами и/или C1-6алкильными группами и бензольное кольцо может быть замещено 1-3 заместителями, выбранными из группы A1 заместителей, и R1, R2, R3, R4, Xa и Xb являются такими, как определено в (a);
(c) один из R1 и R2 и один из R3 и R4 являются одинаковыми или различными и каждый представляет собой атом водорода или C1-6алкильную группу, другой из R1 и R2 и другой из R3 и R4, вместе с атомами углерода, к которым они соответственно присоединены, образуют C3-8циклоалкильную группу, где C3-8циклоалкильная группа может быть замещена 1-3 заместителями, выбранными из группы A1 заместителей, и X1, Xa, Xb и Ar1 являются такими, как определено в (a) или (b);
(d) Ar1-X1- и R4, вместе с атомом азота, к которому Ar1-X1- присоединена, и атомом углерода, к которому R4 присоединен, образуют 4-8-членную азотсодержащую гетероциклическую группу, которая может быть замещена арильной группой или пиридинильной группой, где одна метиленовая группа в 4-8-членной азотсодержащей гетероциклической группе может быть замещена метиленовой группой, замещенной 1 или 2 заместителями, выбранными из группы A1 заместителей, виниленовой группой, которая может быть замещена 1-3 заместителями, выбранными из группы A1 заместителей, атомом кислорода или иминогруппой, которая может быть замещена заместителем, выбранным из группы A1 заместителей, и арильная или пиридинильная группа может быть замещена 1-3 заместителями, выбранными из группы A1 заместителей, Xb представляет собой атом кислорода, и R1, R2, R3 и Xa являются такими, как определено в (a) и (b);
(e) R1 и R2, вместе с атомом углерода, к которому они присоединены, образуют C3-8циклоалкильную группу, и R3, R4, X1, Xa, Xb и Ar1 являются такими, как определено в (a) и (b); или
(f) R3 и R4, вместе с атомом углерода, к которому они присоединены, образуют C3-8циклоалкильную группу, и R1, R2, X1, Xa, Xb и Ar1 являются такими, как определено в (a) и (b);
и особенно предпочтительно:
(a) R1, R2, R3 и R4 являются одинаковыми или различными и каждый представляет собой атом водорода или C1-6алкильную группу;
X1 представляет собой C1-6алкиленовую группу, где C1-6алкиленовая группа может быть замещена 1-3 гидроксильными группами или С1-6алкильными группами, где C1-6алкильные группы могут быть замещены 1-3 гидроксильными группами;
Xa представляет собой метоксигруппу или атом фтора;
Xb представляет собой атом кислорода или метиленовую группу, при условии, что Xb представляет собой только атом кислорода, когда Xa представляет собой метоксигруппу; и
Ar1 представляет собой арильную группу, пиридинильную группу, арилоксигруппу или пиридинилоксигруппу, которая может быть замещена 1-3 заместителями, выбранными из группы A1 заместителей;
(b) Ar1-X1- представляет собой C3-8циклоалкильную группу, конденсированную с бензольным кольцом, где одна метиленовая группа в C3-8циклоалкильной группе может быть замещена атомом кислорода, C3-8циклоалкильная группа может быть замещена 1-3 гидроксильными группами и/или C1-6алкильными группами и бензольное кольцо может быть замещено 1-3 заместителями, выбранными из группы A1 заместителей, и R1, R2, R3, R4, Xa и Xb являются такими, как определено в (a); или
(d) Ar1-X1- и R4, вместе с атомом азота, к которому группа Ar1-X1- присоединена, и атомом углерода, к которому R4 присоединен, образуют 4-8-членную азотсодержащую гетероциклическую группу, которая может быть замещена арильной группой или пиридинильной группой, где одна метиленовая группа в 4-8-членной азотсодержащей гетероциклической группе может быть замещена метиленовой группой, замещенной 1 или 2 заместителями, выбранными из группы A1 заместителей, виниленовой группой, которая может быть замещена 1-3 заместителями, выбранными из группы A1 заместителей, атомом кислорода или иминогруппой, которая может быть замещена заместителем, выбранным из группы A1 заместителей, и арильная или пиридинильная группа может быть замещена 1-3 заместителями, выбранными из группы A1 заместителей, Xb представляет собой атом кислорода, и R1, R2, R3 и Xa являются такими, как определено в (a) и (b).
В соединении формулы (I) или его фармакологически приемлемой соли
Ar1 предпочтительно представляет собой арильную группу или пиридинильную группу, или арильную группу или пиридинильную группу, замещенную 1-3 атомами галогена.
В соединении формулы (I) или его фармакологически приемлемой соли
Ar1 более предпочтительно представляет собой фенильную группу или пиридинильную группу, или фенильную группу или пиридинильную группу, замещенную 1-3 атомами галогена.
В соединении формулы (I) или его фармакологически приемлемой соли
Xa предпочтительно представляет собой метоксигруппу или атом фтора.
В соединении формулы (I) или его фармакологически приемлемой соли
Xb предпочтительно представляет собой атом кислорода или метиленовую группу, при условии, что Xb представляет собой только атом кислорода, когда Xa представляет собой метоксигруппу.
В соединении формулы (I) или его фармакологически приемлемой соли
предпочтительно 1) R1, R2, R3 и R4 являются одинаковыми или различными и каждый представляет собой атом водорода или C1-6алкильную группу, 2) один из R1 и R2 и один из R3 и R4 являются одинаковыми или различными и каждый представляет собой атом водорода или C1-6алкильную группу, а другой из R1 и R2 и другой из R3 и R4, вместе с атомами углерода, к которым они соответственно присоединены, образуют C3-8циклоалкильную группу, где C3-8циклоалкильная группа может быть замещена 1-3 заместителями, выбранными из группы A1 заместителей, 3) R1 и R2, вместе с атомом углерода, к которому они присоединены, образуют C3-8циклоалкильную группу, и R3 и R4 являются одинаковыми или различными и каждый представляет собой атом водорода или C1-6алкильную группу или 4) R3 и R4, вместе с атомом углерода, к которому они присоединены, образуют C3-8циклоалкильную группу и R1 и R2 являются одинаковыми или различными и каждый представляет собой атом водорода или C1-6алкильную группу.
В соединении формулы (I) или его фармакологически приемлемой соли
X1 предпочтительно представляет собой C1-6алкиленовую группу, где C1-6алкиленовая группа может быть замещена 1-3 гидроксильными группами или С1-6алкильными группами, где C1-6алкильные группы могут быть замещены 1-3 гидроксильными группами, X1 более предпочтительно представляет собой -CR5R6-, где R5 и R6 являются одинаковыми или различными и каждый представляет собой атом водорода или C1-6алкильную группу, где C1-6алкильная группа может быть замещена 1-3 гидроксильными группами, и X1 наиболее предпочтительно представляет собой -CH-C(OH)R7-, где R7 представляет собой C1-6алкильную группу.
В соединении формулы (I) или его фармакологически приемлемой соли
Ar1 предпочтительно представляет собой арильную группу, пиридинильную группу, арилоксигруппу или пиридинилоксигруппу, которая может быть замещена 1-3 заместителями, выбранными из группы A1 заместителей, и Ar1 более предпочтительно представляет собой арильную группу или пиридинильную группу, которая может быть замещена 1-3 заместителями, выбранными из группы A1 заместителей.
В соединении формулы (II) или его фармакологически приемлемой соли:
Ar1-a предпочтительно представляет собой фенильную группу или пиридинильную группу, которая может быть замещена 1-3 заместителями, выбранными из группы A1 заместителей; и
Ar1-a более предпочтительно представляет собой фенильную группу или пиридинильную группу, которая может быть незамещенной или может быть замещена 1-3 атомами галогена.
В соединении формулы (II) или его фармакологически приемлемой соли
предпочтительно R5 и R6 являются одинаковыми или различными и каждый представляет собой атом водорода или C1-6алкильную группу, где C1-6алкильная группа может быть замещена 1-3 гидроксильными группами.
В соединении формулы (II) или его фармакологически приемлемой соли
Xa предпочтительно представляет собой метоксигруппу или атом фтора.
В соединении формулы (II) или его фармакологически приемлемой соли
Xb предпочтительно представляет собой атом кислорода или метиленовую группу, при условии, что Xb представляет собой только атом кислорода, когда Xa представляет собой метоксигруппу.
В соединении формулы (II) или его фармакологически приемлемой соли
предпочтительно 1) R1, R2, R3 и R4 являются одинаковыми или различными и каждый представляет собой атом водорода или C1-6алкильную группу, 2) один из R1 и R2 и один из R3 и R4 являются одинаковыми или различными и каждый представляет собой атом водорода или C1-6алкильную группу, а другой из R1 и R2 и другой из R3 и R4, вместе с атомами углерода, к которым они соответственно присоединены, образуют C3-8циклоалкильную группу, где C3-8циклоалкильная группа может быть замещена 1-3 заместителями, выбранными из группы A1 заместителей, 3) R1 и R2, вместе с атомом углерода, к которому они присоединены, образуют C3-8циклоалкильную группу, и R3 и R4 являются одинаковыми или различными и каждый представляет собой атом водорода или C1-6алкильную группу или 4) R3 и R4, вместе с атомом углерода, к которому они присоединены, образуют C3-8циклоалкильную группу, и R1 и R2 являются одинаковыми или различными и каждый представляет собой атом водорода или C1-6алкильную группу.
В соединении формулы (I-a) или его фармакологически приемлемой соли
X1 предпочтительно представляет собой C1-6алкиленовую группу, где C1-6алкиленовая группа может быть замещена 1-3 гидроксильными группами или С1-6алкильными группами, где C1-6алкильные группы могут быть замещены 1-3 гидроксильными группами, X1 более предпочтительно представляет собой -CR5R6-, где R5 и R6 являются одинаковыми или различными и каждый представляет собой атом водорода или C1-6алкильную группу, где C1-6алкильная группа может быть замещена 1-3 гидроксильными группами, и X1 наиболее предпочтительно представляет собой -CH-C(OH)R7-, где R7 представляет собой C1-6алкильную группу.
В соединении формулы (I-a) или его фармакологически приемлемой соли
Ar1 предпочтительно представляет собой арильную группу, пиридинильную группу, арилоксигруппу или пиридинилоксигруппу, которая может быть замещена 1-3 заместителями, выбранными из группы A1 заместителей, и Ar1 более предпочтительно представляет собой арильную группу или пиридинильную группу, которая может быть замещена 1-3 заместителями, выбранными из группы A1 заместителей.
В соединении формулы (I-a) или его фармакологически приемлемой соли
предпочтительно 1) R1, R2, R3 и R4 являются одинаковыми или различными и каждый представляет собой атом водорода или C1-6алкильную группу, 2) один из R1 и R2 и один из R3 и R4 являются одинаковыми или различными и каждый представляет собой атом водорода или C1-6алкильную группу, а другой из R1 и R2 и другой из R3 и R4, вместе с атомами углерода, к которым они соответственно присоединены, образуют C3-8циклоалкильную группу, где C3-8циклоалкильная группа может быть замещена 1-3 заместителями, выбранными из группы A1 заместителей, 3) R1 и R2, вместе с атомом углерода, к которому они присоединены, образуют C3-8циклоалкильную группу, и R3 и R4 являются одинаковыми или различными и каждый представляет собой атом водорода или C1-6алкильную группу или 4) R3 и R4, вместе с атомом углерода, к которому они присоединены, образуют C3-8циклоалкильную группу, и R1 и R2 являются одинаковыми или различными и каждый представляет собой атом водорода или C1-6алкильную группу.
В соединении формулы (I-b) или его фармакологически приемлемой соли
предпочтительно R13 и R14 являются одинаковыми или различными и представляют собой атом водорода или заместитель, выбранный из группы A1 заместителей, и более предпочтительно R13 и R14 являются одинаковыми или различными и каждый представляет собой атом водорода, атом галогена или C1-6алкоксигруппу.
В соединении формулы (I-b) или его фармакологически приемлемой соли
Y предпочтительно представляет собой метиленовую группу или атом кислорода.
В соединении формулы (I-b) или его фармакологически приемлемой соли
предпочтительно 1) R1, R2, R3 и R4 являются одинаковыми или различными и каждый представляет собой атом водорода или C1-6алкильную группу, 2) один из R1 и R2 и один из R3 и R4 являются одинаковыми или различными и каждый представляет собой атом водорода или C1-6алкильную группу, а другой из R1 и R2 и другой из R3 и R4, вместе с атомами углерода, к которым они соответственно присоединены, образуют C3-8циклоалкильную группу, где C3-8циклоалкильная группа может быть замещена 1-3 заместителями, выбранными из группы A1 заместителей, 3) R1 и R2, вместе с атомом углерода, к которому они присоединены, образуют C3-8циклоалкильную группу, и R3 и R4 являются одинаковыми или различными и каждый представляет собой атом водорода или C1-6алкильную группу или 4) R3 и R4, вместе с атомом углерода, к которому они присоединены, образуют C3-8циклоалкильную группу, и R1 и R2 являются одинаковыми или различными и каждый представляет собой атом водорода или C1-6алкильную группу.
В соединении формулы (I-c) или его фармакологически приемлемой соли:
Ar1-c предпочтительно представляет собой фенильную группу или пиридинильную группу, которая может быть замещена 1-3 заместителями, выбранными из группы A1 заместителей; и
Ar1-c более предпочтительно представляет собой фенильную группу или пиридинильную группу, которая может быть незамещенной или может быть замещена 1-3 атомами галогена.
В соединении формулы (I-c) или его фармакологически приемлемой соли:
Z1 предпочтительно представляет собой метиленовую группу или виниленовую группу, которая может быть замещена 1 или 2 заместителями, выбранными из группы A1 заместителей, атомом кислорода или иминогруппой, которая может быть замещена заместителем, выбранным из группы A1 заместителей;
Z1 более предпочтительно представляет собой метиленовую группу, которая может быть замещена 1 или 2 заместителями, выбранными из группы A1 заместителей, или атомом кислорода; и
Z1 наиболее предпочтительно представляет собой метиленовую группу, где метиленовая группа может быть замещена 1 или 2 заместителями, которые являются одинаковыми или различными и выбраны из группы, состоящей из C1-6алкильной группы и гидроксильной группы, или атомом кислорода.
В соединении формулы (I-c) или его фармакологически приемлемой соли предпочтительно n и m являются одинаковыми или различными и каждый представляет собой целое число от 0 до 2, и более предпочтительно n и m, каждый равен 1.
В соединении формулы (I-c) или его фармакологически приемлемой соли предпочтительно 1) R1 и R2 являются одинаковыми или различными и каждый представляет собой атом водорода или C1-6алкильную группу или 2) R1 и R2, вместе с атомом углерода, к которому они присоединены, образуют C3-8циклоалкильную группу.
В соединении формулы (II-a), (II-b) или (II-d) или его фармакологически приемлемой соли предпочтительно 1) R1, R2, R3 и R4 являются одинаковыми или различными и каждый представляет собой атом водорода или C1-6алкильную группу, 2) один из R1 и R2 и один из R3 и R4 являются одинаковыми или различными и каждый представляет собой атом водорода или C1-6алкильную группу, а другой из R1 и R2 и другой из R3 и R4, вместе с атомами углерода, к которым они соответственно присоединены, образуют C3-8циклоалкильную группу, где C3-8циклоалкильная группа может быть замещена 1-3 заместителями, выбранными из группы A1 заместителей, 3) R1 и R2, вместе с атомом углерода, к которому они присоединены, образуют C3-8циклоалкильную группу, и R3 и R4 являются одинаковыми или различными и каждый представляет собой атом водорода или C1-6алкильную группу или 4) R3 и R4, вместе с атомом углерода, к которому они присоединены, образуют C3-8циклоалкильную группу, и R1 и R2 являются одинаковыми или различными и каждый представляет собой атом водорода или C1-6алкильную группу.
В соединении формулы (II-a), (II-b) или (II-d) или его фармакологически приемлемой соли предпочтительно R5 и R6 являются одинаковыми или различными и каждый представляет собой атом водорода или C1-6алкильную группу, где C1-6алкильная группа может быть замещена 1-3 гидроксильными группами.
В соединении формулы (II-a), (II-b) или (II-d) или его фармакологически приемлемой соли:
Ar1-a предпочтительно представляет собой фенильную группу или пиридинильную группу, которая может быть замещена 1-3 заместителями, выбранными из группы A1 заместителей; и
Ar1-a более предпочтительно представляет собой фенильную группу или пиридинильную группу, которая может быть незамещенной или может быть замещена 1-3 атомами галогена.
В соединении формулы (II-c) или (II-e) или его фармакологически приемлемой соли
предпочтительно 1) R1, R2, R3 и R4 являются одинаковыми или различными и каждый представляет собой атом водорода или C1-6алкильную группу, 2) один из R1 и R2 и один из R3 и R4 являются одинаковыми или различными и каждый представляет собой атом водорода или C1-6алкильную группу, а другой из R1 и R2 и другой из R3 и R4, вместе с атомами углерода, к которым они соответственно присоединены, образуют C3-8циклоалкильную группу, где C3-8циклоалкильная группа может быть замещена 1-3 заместителями, выбранными из группы A1 заместителей, 3) R1 и R2, вместе с атомом углерода, к которому они присоединены, образуют C3-8циклоалкильную группу, и R3 и R4 являются одинаковыми или различными и каждый представляет собой атом водорода или C1-6алкильную группу или 4) R3 и R4, вместе с атомом углерода, к которому они присоединены, образуют C3-8циклоалкильную группу, и R1 и R2 являются одинаковыми или различными и каждый представляет собой атом водорода или C1-6алкильную группу.
В соединении формулы (II-c) или (II-e) или его фармакологически приемлемой соли
R7 предпочтительно представляет собой атом водорода или C1-6алкильную группу.
В соединении формулы (II-c) или (II-e) или его фармакологически приемлемой соли:
Ar1-a предпочтительно представляет собой фенильную группу или пиридинильную группу, которая может быть замещена 1-3 заместителями, выбранными из группы A1 заместителей; и
Ar1-a более предпочтительно представляет собой фенильную группу или пиридинильную группу, которая может быть незамещенной или может быть замещена 1-3 атомами галогена.
В частности, например, соединение, выбранное из следующей группы, или его фармакологически приемлемая соль является особенно подходящим и полезно в качестве терапевтического или профилактического средства для заболевания, вызываемого амилоидом-β, такого как болезнь Альцгеймера, старческая деменция, синдром Дауна или амилоидоз, включающей:
1) (Z)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-(3,4,5-трифторбензил)морфолин-3-он,
2) (Z)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-(2,3,4-трифторбензил)морфолин-3-он,
3) (Z)-(S)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метил-4-(3,4,5-трифторбензил)морфолин-3-он,
4) (Z)-(R)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метил-4-(3,4,5-трифторбензил)морфолин-3-он,
5) (Z)-(S)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метил-4-(2,3,4-трифторбензил)морфолин-3-он,
6) (Z)-(R)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метил-4-(2,3,4-трифторбензил)морфолин-3-он,
7) (Z)-4-[(S)-1-(4-фторфенил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
8) (Z)-(R)-4-[(S)-1-(4-фторфенил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
9) (Z)-(S)-4-[(S)-1-(4-фторфенил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
10) (Z)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-[(S)-1-(3,4,5-трифторфенил)этил]морфолин-3-он,
11) (Z)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-[(R)-1-(3,4,5-трифторфенил)этил]морфолин-3-он,
12) (Z)-4-[(S)-хроман-4-ил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
13) (Z)-(S)-4-[(S)-хроман-4-ил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
14) (Z)-(R)-4-[(S)-хроман-4-ил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
15) (Z)-(6S,9aR)-6-(4-фторфенил)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)бензилиден]гексагидропиридо[2,1-c][1,4]оксазин-4-он,
16) (Z)-(6R,9aS)-6-(4-фторфенил)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)бензилиден]гексагидропиридо[2,1-c][1,4]оксазин-4-он,
17) (Z)-(S)-4-[(S)-1-(6-хлорпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
18) (Z)-(S)-4-[(R)-1-(6-хлорпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
19) (Z)-(S)-4-[(S)-1-(5-хлорпиридин-2-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
20) (Z)-(S)-4-[(R)-1-(5-хлорпиридин-2-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
21) (Z)-(S)-4-[(S)-1-(2,6-дифторпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
22) (Z)-(S)-4-[(R)-1-(2,6-дифторпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
23) (Z)-(S)-4-[(S)-1-(2,3-дифторпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
24) (Z)-(S)-4-[(R)-1-(2,3-дифторпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
25) (Z)-(S)-4-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
26) (Z)-4-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
27) (Z)-4-[(R)-1-(4-фторфенил)-2-гидроксиэтил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
28) (Z)-(6R)-4-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
29) (Z)-4-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]морфолин-3-он,
30) (Z)-4-[(1R,2R)-1-(3,4-дифторфенил)-2-гидроксипропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]морфолин-3-он,
31) (Z)-(S)-4-[(1R,2R)-1-(4-фторфенил)-2-гидроксипропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
32) (Z)-4-[(1R,2R)-1-(4-фторфенил)-2-гидроксипропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
33) (Z)-(S)-4-[(1R,2R)-1-(3,4-дифторфенил)-2-гидроксипропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
34) (Z)-4-[(1R,2R)-1-(3,4-дифторфенил)-2-гидроксипропил]-2-[1-[3-метокси-4-(метилимидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
35) (Z)-(S)-4-[(S)-2-гидрокси-1-метил-1-(3,4,5-трифторфенил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
36) (Z)-(6S)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метил-4-[(S)-1-(3,4,5-трифторфенил)этил]морфолин-3-он,
37) (Z)-(6S)-4-[1-(4-фторфенил)-1-метилэтил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
38) (Z)-(6S)-4-[1-(4-фторфенил)циклопропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
39) (Z)-(6S,9aR)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)бензилиден]-6-(3,4,5-трифторфенил)гексагидропиридо[2,1-c][1,4]оксазин-4-он,
40) (Z)-(6S,9aR)-6-(3,4-дифторфенил)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)бензилиден]гексагидропиридо[2,1-c][1,4]оксазин-4-он,
41) (Z)-(6S,9aR)-6-(2,6-дифторпиридин-3-ил)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)бензилиден]гексагидропиридо[2,1-c][1,4]оксазин-4-он,
42) (Z)-(S)-4-[(S)-1-(5-фторпиридин-2-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
43) (Z)-(S)-4-[(S)-1-(2-хлорпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
44) (Z)-(S)-4-[(S)-1-(2-хлор-3-фторпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
45) (Z)-(S)-4-[(S)-1-(2,6-дифторпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
46) (Z)-4-[(S)-1-(2-хлорпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
47) (Z)-4-[(S)-1-(2,6-дифторпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
48) (Z)-4-[(S)-1-(6-фторпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
49) (Z)-4-[(S)-1-(6-хлорпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
50) (Z)-4-[(S)-1-(2,3-дифторпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
51) (Z)-4-[(S)-1-(5-хлорпиридин-2-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
52) (Z)-(R)-4-[(S)-1-(2,6-дифторпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
53) (Z)-(S)-4-(4-фторбензил)-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
54) (Z)-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-[(S)-1-(4-трифторфенил)этил]-6,6-диметилморфолин-3-он,
55) (Z)-4-[(S)-хроман-4-ил]-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
56) (Z)-(S)-4-[(S)-хроман-4-ил]-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
57) (Z)-(S)-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-6-метилморфолин-3-он,
58) (Z)-(S)-4-[(1R,2R)-1-(3,4-дифторфенил)-2-гидроксипропил]-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
59) (Z)-(S)-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-[(1R,2R)-1-(4-фторфенил)-2-гидроксипропил]-6-метилморфолин-3-он,
60) (Z)-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-6,6-диметилморфолин-3-он,
61) (Z)-4-[(1R,2R)-1-(3,4-дифторфенил)-2-гидроксипропил]-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
62) 1-[1-(2,4-дифторфенил)этил]-3-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]-(E)-метилиден}пиперидин-2-он,
63) (E)-(S)-3-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}-1-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-5-метилпиперидин-2-он,
64) (E)-3-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}-1-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]пиперидин-2-он,
65) (E)-3-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}-1-[(2R,3R)-3-гидрокси-1,1-диметилиндан-2-ил]пиперидин-2-он,
66) (E)-3-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}-1-[(S)-2-гидрокси-1-метил-1-(3,4,5-трифторфенил)этил]пиперидин-2-он,
67) (E)-3-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}-1-[1-(4-фторфенил)-1-метилэтил]пиперидин-2-он,
68) (E)-(R)-3-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}-1-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-5-метилпиперидин-2-он,
69) (E)-(S)-1-[(1R,2R)-1-(3,4-дифторфенил)-2-гидроксипропил]-3-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}-5-метилпиперидин-2-он,
70) (Z)-(6S,8aR)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)бензилиден]-6-(3,4,5-трифторфенил)тетрагидропирроло[2,1-c][1,4]оксазин-4-он,
71) (6S,9aR)-6-(4-хлорфенил)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]-(Z)-метилиден}гексагидропиридо[2,1-c][1,4]оксазин-4-он,
72) (6R,9aR)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]-(Z)-метилиден}-6-(3,4,5-трифторфенил)тетрагидро[1,4]оксазино[3,4-c][1,4]оксазин-4-он,
73) (6R,9aR)-6-(3,4-дифторфенил)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]-(Z)-метилиден}тетрагидро[1,4]оксазино[3,4-c][1,4]оксазин-4-он,
74) (6R,9aR)-6-(4-фторфенил)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]-(Z)-метилиден}тетрагидро[1,4]оксазино[3,4-c][1,4]оксазин-4-он и
75) (6R,9aR)-6-(4-хлорфенил)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]-(Z)-метилиден}тетрагидро[1,4]оксазино[3,4-c]оксазин-4-он.
Предпочтительными вариантами осуществления соединения общей формулы (I) являются такие, как описано выше. Фармацевтически активный ингредиент по настоящему изобретению не ограничивается соединениями, конкретно описанными в данном описании, и может быть произвольно выбран любой вариант осуществления в пределах определения соединения общей формулы (I).
Ниже описаны способы получения соединения общей формулы (I) по настоящему изобретению.
Соединение, представленное общей формулой (I):
[Формула 16]

где R1, R2, R3, R4, X1, Xa, Xb и Ar1 являются такими, как определено выше, синтезируют способом, как, например, следующий общий способ получения 1 или общий способ получения 2. Очевидно, что для подходящего получения соединения по настоящему изобретению способ включает соответствующую стадию реакции введения защиты и стадию реакции снятия защиты с использованием защитной группы, известной специалисту в данной области, которую выбирают соответственно для каждой стадии (см., например, T. Greene et al., "Protective Groups in Organic Synthesis", John Wiley & Sons, Inc., New York, 1981). Очевидно также, что для подходящего получения соединения по настоящему изобретению все изомеры и изомерные смеси, такие как геометрические изомеры, которые могут образовываться из структуры данного соединения, оптические изомеры, образование которых основано на наличии асимметричного атома углерода, стереоизомеры и таутомеры, могут быть получены в виде отдельного соединения по подходящей для каждой стадии методике, известной специалисту в данной области, такой как фракционированная кристаллизация или колоночная хроматография.
Общий способ получения 1
Ниже описан общий способ получения 1, конкретно используемый для получения соединения общей формулы (I) по настоящему изобретению.
[Формула 17]

На данной схеме R1, R2, R3, R4, X1 (который может иметь защитную группу, когда X1 содержит гидроксильную группу), Xa, Xb и Ar1 являются такими, как определено выше.
Приведенный выше общий способ получения 1 является примером способа получения соединения общей формулы (I), включающего преобразование альдегида (1) и 0,3-3,0 эквивалентов амида (2a) из расчета на альдегид (1) в альдольный аддукт (3) альдольной конденсацией на стадии 1-1 и последующую дегидратацию аддукта.
Преобразование альдольного аддукта (3) в соединение (I)
Соединение общей формулы (I) может быть получено преобразованием альдольного аддукта (3) реакцией дегидратации на стадии 1-2. Соответственно, реакцию дегидратации на стадии 1-2 варьируют в соответствии с исходным соединением и особо не ограничивают, только чтобы условия были подобны условиям данной реакции. Для данной реакции может быть использован известный способ, описанный во многих публикациях (см., например, Jikken Kagaku Koza (Courses in Experimental Chemistry), vol.19, Yuki Gosei (Organic Synthesis) [1], edited by The Chemical Society of Japan, Maruzen Co., Ltd., June 1992, p.194-226). Предпочтительные примеры способа включают i) способ, включающий обработку альдольного аддукта (3) кислотой (см., например, Jikken Kagaku Koza (Courses in Experimental Chemistry), vol.19, Yuki Gosei (Organic Synthesis) [1], edited by The Chemical Society of Japan, Maruzen Co., Ltd., June 1992, p.194-196) и ii) способ, включающий преобразование спиртовой группы альдольного аддукта (3) в уходящую группу, такую как сульфонатная группа или атом галогена, и последующую обработку аддукта основанием (см., например, Jikken Kagaku Koza (Courses in Experimental Chemistry), vol.19, Yuki Gosei (Organic Synthesis) [1], edited by The Chemical Society of Japan, Maruzen Co., Ltd., June 1992, p.198-205).
В способе i) условия использования кислоты, растворителя и температуры варьируют в соответствии с исходным соединением и особо не ограничивают. Используют 0,1-10 эквивалентов кислоты, такой как хлористо-водородная кислота, серная кислота, фосфорная кислота, гидросульфид калия, щавелевая кислота, п-толуолсульфоновая кислота, комплекс трифторид бора-эфир, тионилхлорид или оксид алюминия, из расчета на альдольный аддукт (3). Способ может быть осуществлен без растворителя или с растворителем или смесью растворителей, который(ая) не тормозит реакцию и дает возможность исходному соединению растворяться в нем(ней) до определенной степени. Предпочтительные примеры используемого растворителя включают воду, ацетон, диметилсульфоксид и гексаметилфосфорамид. Кроме того, комбинация 0,1-10 эквивалентов кислоты из расчета на альдольный аддукт (3) с органическим основанием, таким как пиридин, может повысить скорость реакции и выход реакции. Температура реакции должна быть такой, которая может обеспечить завершение реакции, не способствуя образованию нежелательного побочного продукта, и предпочтительно находится в диапазоне, например, от комнатной температуры до 200°C. В предпочтительных условиях реакция предпочтительно завершается, например, за 0,5-24 часа, и ход реакции можно контролировать известными методами хроматографии. Нежелательный побочный продукт может быть удален методом, известным специалисту в данной области, таким как традиционный метод хроматографии, экстракция и/или кристаллизация.
Предпочтительные примеры уходящей группы в способе ii) включают ацетильную группу, метансульфонатную группу, п-толуолсульфонатную группу, атом хлора, атом брома и атом йода. Способ, включающий преобразование в такую уходящую группу, варьируют в соответствии с исходным соединением и особо не ограничивают. В качестве такого преобразования может быть использован способ, известный специалисту в данной области. Предпочтительно 1,0-10 эквивалентов ацетилирующего агента, такого как ацетилхлорид и уксусный ангидрид, или сульфонирующего агента, такого как метансульфонилхлорид и п-толуолсульфонилхлорид, или 1,0-10 эквивалентов галогенирующего агента, такого как тионилхлорид, из расчета на альдольный аддукт (3), например, могут быть использованы предпочтительно, например, в галогенированном растворителе, таком как метиленхлорид и хлороформ, неполярном растворителе, таком как толуол и бензол, простом эфирном растворителе, таком как тетрагидрофуран или диметиловый эфир этиленгликоля; или смешанном растворителе из указанных растворителей. Температура реакции должна быть такой, которая может обеспечить завершение реакции, не способствуя образованию нежелательного побочного продукта, и предпочтительно находится в диапазоне, например, от -78 до 100°C. В предпочтительных условиях реакция предпочтительно завершается, например, за 1-24 часа, и ход реакции можно контролировать известными методами хроматографии. Нежелательный побочный продукт может быть удален методом, известным специалисту в данной области, таким как традиционный метод хроматографии, экстракция и/или кристаллизация. В реакции образования уходящей группы как второй стадии в качестве основания предпочтительно используют, например, 0,1-10 эквивалентов органического основания, такого как диазабициклоундецен, пиридин, 4-диметиламинопиридин и триэтиламин, соли четвертичного аммония, такой как тетрабутиламмонийгидроксид, соли щелочного металла со спиртом, такой как метоксид натрия или трет-бутоксид калия, гидроксида щелочного металла, такого как гидроксид натрия, карбоната щелочного металла, такого как карбонат лития или карбонат калия, или металлоорганического реагента, такого как диизопропиламид лития, из расчета на альдольный аддукт (3) предпочтительно, например, в галогенированном растворителе, таком как метиленхлорид, неполярном растворителе, таком как толуол, полярном растворителе, таком как ацетонитрил, диметилформамид или диметилсульфоксид, простом эфирном растворителе, таком как тетрагидрофуран или диметиловый эфир этиленгликоля, или смешанном растворителе из указанных растворителей.
В качестве растворителя может быть использовано также органическое основание, такое как пиридин. Температура реакции должна быть такой, которая может обеспечить завершение реакции, не способствуя образованию нежелательного побочного продукта, и предпочтительно находится в диапазоне, например, от -78 до 100°C. В предпочтительных условиях реакция предпочтительно завершается, например, за 1-24 часа, и ход реакции можно контролировать известными методами хроматографии. Нежелательный побочный продукт может быть удален методом, известным специалисту в данной области, таким как традиционный метод хроматографии, экстракция и/или кристаллизация.
Получение альдольного аддукта (3)
Альдольный аддукт (3) может быть получен, например, из альдегида (1) и амида (2a) в соответствии со стадией 1-1. В частности, реакцию альдольной конденсации на стадии 1-1 варьируют в соответствии с исходным соединением и особо не ограничивают, только чтобы условия были подобны условиям данной реакции. Для данной реакции может быть использован способ, известный специалисту в данной области (см., например, Jikken Kagaku Koza (Courses in Experimental Chemistry), vol.20, Yuki Gosei (Organic Synthesis) [11], edited by The Chemical Society of Japan, Maruzen Co., Ltd., July 1992, p.94-100). Предпочтительные примеры способа включают i) способ, включающий преобразование амида (2a) в енолят щелочного металла предпочтительно, например, 1,0-5,0 эквивалентами основания, такого как предпочтительно диизопропиламид лития, гидрид натрия или метоксид натрия, с последующим взаимодействием енолята с альдегидом (1) (см., например, Jikken Kagaku Koza (Courses in Experimental Chemistry), vol.20, Yuki Gosei (Organic Synthesis) [11], edited by The Chemical Society of Japan, Maruzen Co., Ltd., July 1992, p.97-98) и ii) способ, включающий преобразование амида (2a) в енолят щелочного металла предпочтительно, например, 1,0-5,0 эквивалентами основания, такого как предпочтительно диизопропиламид лития, гидрид натрия, или метоксид натрия, взаимодействие енолята с галогенидом кремния, предпочтительно, таким как триметилхлорсилан или трет-бутилдиметилхлорсилан, с получением непосредственно простого силиленолового эфира и последующим взаимодействием эфира с альдегидом (1) в присутствии кислоты Льюиса, предпочтительно, такой как тетрахлорид титана или трифторид бора (см., например, Jikken Kagaku Koza (Courses in Experimental Chemistry), vol.20, Yuki Gosei (Organic Synthesis) [11], edited by The Chemical Society of Japan, Maruzen Co., Ltd., July 1992, p.96-97).
Используемые растворитель и температуру реакции варьируют в соответствии с исходным соединением и особо не ограничивают. В качестве растворителя, который не тормозит реакцию и дает возможность исходному соединению растворяться в нем до определенной степени, предпочтительно может быть использован, например, простой эфирный растворитель, такой как тетрагидрофуран, 1,4-диоксан или диэтиловый эфир, галогенированный растворитель, такой как метиленхлорид, 1,2-дихлорэтан или хлороформ, неполярный растворитель, такой как толуол или ксилол, или смешанный растворитель из указанных растворителей. Температура реакции должна быть такой, которая может обеспечить завершение реакции, не способствуя образованию нежелательного побочного продукта, и предпочтительно находится в диапазоне, например, от -78°C до комнатной температуры. В предпочтительных условиях реакция предпочтительно завершается, например, за 0.5-24 часа, и ход реакции можно контролировать известными методами хроматографии. Нежелательный побочный продукт может быть удален методом, известным специалисту в данной области, таким как традиционный метод хроматографии, экстракция и/или кристаллизация.
Получение альдегида (1)
[Формула 18]


На данной схеме Xa является таким, как определено выше; L1 представляет собой атом фтора, атом хлора, атом брома, атом йода, сульфонатную группу, такую как трифлатная группа, группа триалкилолово, группа бороновой кислоты или боронатная группа, и L2 представляет собой C1-С3алкоксикарбонильную группу, такую как метилсложноэфирная группа, альдегидная группа или цианогруппа.
Получение альдегида (1)
Альдегид (1) может быть получен из соединения (1a) в качестве исходного в соответствии со стадией 2-5. В частности, стадию 2-5 варьируют в соответствии с исходным соединением и особо не ограничивают, только чтобы условия были подобны условиям данной реакции. Для данной реакции может быть использован способ, известный специалисту в данной области. Например, когда L2 представляет собой алкоксикарбонильную группу, может быть использована реакция восстановления, описанная во многих известных публикациях (см., например, Jikken Kagaku Koza (Courses in Experimental Chemistry), vol.26, Yuki Gosei (Organic Synthesis) [VIII], edited by The Chemical Society of Japan, Maruzen Co., Ltd., April 1992, p.159-266). Предпочтительно, требуемый альдегид может быть получен, например, методом восстановления с использованием гидрида металла, такого как диизобутилалюминийгидрид. Более предпочтительно, требуемый альдегид может быть эффективно получен, например, методом восстановления с использованием литийалюминийгидрида или алюмогидридного комплекса в присутствии амина (см., например, T. Abe et al., "Tetrahedron", 2001, vol.57, p.2701-2710).
Например, когда L2 представляет собой цианогруппу, может быть использована реакция восстановления, описанная во многих известных публикациях (см., например, Jikken Kagaku Koza (Courses in Experimental Chemistry), vol.26, Yuki Gosei (Organic Synthesis) [VIII], edited by The Chemical Society of Japan, Maruzen Co., Ltd., April 1992, p.159-266). Предпочтительно, требуемый альдегид может быть получен, например, методом восстановления с использованием гидрида металла, такого как бис(2-метоксиэтокси)алюминийгидрид натрия или диизобутилалюминийгидрид (см., например, Jikken Kagaku Koza (Courses in Experimental Chemistry), vol.26, Yuki Gosei (Organic Synthesis) [VIII], edited by The Chemical Society of Japan, Maruzen Co., Ltd., April 1992, p.231).
Альтернативно, требуемый альдегид может быть синтезирован осуществлением стадий восстановления соединения (1a) до спирта по методике, известной специалисту в данной области (см., например, Jikken Kagaku Koza (Courses in Experimental Chemistry), vol.26, Yuki Gosei (Organic Synthesis) [VIII], edited by The Chemical Society of Japan, Maruzen Co., Ltd., April 1992, p.159-266), и последующим окислением спирта до альдегида (см., например, Jikken Kagaku Koza (Courses in Experimental Chemistry), vol.23, Yuki Gosei (Organic Synthesis) [V], edited by The Chemical Society of Japan, Maruzen Co., Ltd., October 1991, p.1-550).
Основание, используемое в реакции восстановления, варьируют в соответствии с исходным соединением и особо не ограничивают. В качестве основания может быть использован вторичный амин. Предпочтительно, требуемый альдегид может быть эффективно получен при использовании 0,1-1,0 эквивалента неразветвленного или циклического вторичного алкиламина, например такого, как диэтиламин или пирролидин, из расчета на соединение (1a). Используемые растворитель и температуру реакции варьируют в соответствии с исходным соединением и особо не ограничивают. В качестве растворителя, который не тормозит реакцию и дает возможность исходному соединению растворяться в нем до определенной степени, предпочтительно может быть использован, например, простой эфирный растворитель, такой как тетрагидрофуран, 1,4-диоксан или диэтиловый эфир, неполярный растворитель, такой как толуол или ксилол, или смешанный растворителе из указанных растворителей. Температура реакции должна быть такой, которая может обеспечить завершение реакции, не способствуя образованию нежелательного побочного продукта, и предпочтительно находится в диапазоне, например, от -78°C до комнатной температуры. В предпочтительных условиях реакция предпочтительно завершается, например, за 0,5-24 часа, и ход реакции можно контролировать известными методами хроматографии. Нежелательный побочный продукт может быть удален методом, известным специалисту в данной области, таким как традиционный метод хроматографии, экстракция и/или кристаллизация.
Количество окислителя, используемого на стадии окисления, варьируют в соответствии с исходным соединением и особо не ограничивают. Количество составляет предпочтительно 0,1-10 эквивалентов из расчета на соединение (1a). Растворитель и температуру реакции варьируют в соответствии с исходным соединением и особо не ограничивают. В качестве растворителя, который не тормозит реакцию и дает возможность исходному соединению растворяться в нем до определенной степени, предпочтительно может быть использован, например, простой эфирный растворитель, такой как тетрагидрофуран, 1,4-диоксан или диэтиловый эфир, галогенированный растворитель, такой как метиленхлорид, 1,2-дихлорэтан или хлороформ, неполярный растворитель, такой как толуол или ксилол, или смешанный растворитель из указанных растворителей. Температура реакции должна быть такой, которая может обеспечить завершение реакции, не способствуя образованию нежелательного побочного продукта, и предпочтительно находится в диапазоне, например, от -78°C до 100°C. В предпочтительных условиях реакция предпочтительно завершается, например, за 0,5-24 часа, и ход реакции можно контролировать известными методами хроматографии. Нежелательный побочный продукт может быть удален методом, известным специалисту в данной области, таким как традиционный метод хроматографии, экстракция и/или кристаллизация.
Получение соединения (1a)
Соединение (1a) может быть получено, например, из соединения (4a) в качестве исходного в соответствии со стадией 2-1 или из соединения (4d) в качестве исходного в соответствии со стадией 2-4.
Стадия 2-1
Стадию 2-1 варьируют в соответствии с исходным соединением и особо не ограничивают, только чтобы условия были подобны условиям данной реакции. Для данной реакции может быть использован способ, известный специалисту в данной области. Например, способ на стадии 2-1 может быть представлять собой реакцию замещения из соединения (4a) в качестве исходного с использованием 0,3-10 эквивалентов метилимидазола из расчета на соединение (4a). Используемые растворитель и температуру реакции на данной стадии варьируют в соответствии с исходным соединением и особо не ограничивают. В качестве растворителя, который не тормозит реакцию и дает возможность исходному соединению растворяться в нем до определенной степени, предпочтительно может быть использован, например, простой эфирный растворитель, такой как тетрагидрофуран, 1,4-диоксан или диэтиловый эфир, галогенированный растворитель, такой как метиленхлорид, 1,2-дихлорэтан или хлороформ, полярный растворитель, такой как дихлорбензол, диметилформамид или N-метилпирролидон, неполярный растворитель, такой как толуол, ксилол или мезитилен, растворитель в виде органического основания, такой как диазабициклоундецен, пиридин или триэтиламин, или смешанный растворитель из указанных растворителей. Температура реакции должна быть такой, которая может обеспечить завершение реакции, не способствуя образованию нежелательного побочного продукта, и предпочтительно находится в диапазоне, например, от 0°C до 200°C. На данной стадии можно использовать, например, 0,1-10 эквивалентов органического основания, такого как диазабициклоундецен, пиридин или триэтиламин, соли щелочного металла со спиртом, такой как метоксид натрия или трет-бутоксид калия, гидроксида щелочного металла, такого как гидроксид натрия, или карбоната щелочного металла, такого как карбонат цезия или карбонат калия, из расчета на соединение (4a). В предпочтительных условиях реакция предпочтительно завершается, например, за 0,5-24 часа, и ход реакции можно контролировать известными методами хроматографии. Нежелательный побочный продукт может быть удален методом, известным специалисту в данной области, таким как традиционный метод хроматографии, экстракция и/или кристаллизация.
Получение соединения (4a)
Соединение (4a) является коммерчески доступным или может быть получено способом, известным специалисту в данной области. Если соединение (4a) не является коммерчески доступным, оно может быть получено, например, метилированием соответствующего фенольного соединения способом, известным специалисту в данной области, когда Xa представляет собой метоксигруппу.
Стадия 2-4
Стадию 2-4 варьируют в соответствии с исходным соединением и особо не ограничивают, только чтобы условия были подобны условиям данной реакции. Для данной реакции может быть использован способ, известный специалисту в данной области. Требуемое соединение (1a) может быть получено, например, нагреванием соединения (4d) и 1,0-20 эквивалентов аммиака или аммониевой соли из расчета на соединение (4d). Используемые растворитель и температуру реакции варьируют в соответствии с исходным соединением и особо не ограничивают. В качестве растворителя, который не тормозит реакцию и дает возможность исходному соединению растворяться в нем до определенной степени, предпочтительно можно использовать, например, простой эфирный растворитель, такой как тетрагидрофуран, 1,4-диоксан или диэтиловый эфир, галогенированный растворитель, такой как метиленхлорид, 1,2-дихлорэтан или хлороформ, спиртовой растворитель, такой как этанол или изопропанол, полярный растворитель, такой как диметилформамид или N-метилпирролидон, неполярный растворитель, такой как толуол или ксилол, органическую кислоту, такую как уксусная кислота, пропионовая кислота или трифторуксусная кислота, или смешанный растворитель из указанных растворителей. Предпочтительно, соединение (1a) может быть эффективно получено, например, используя 1,0-10 эквивалентов ацетата аммония из расчета на соединение (4d) в растворителе в виде уксусной кислоты. Температура реакции должна быть такой, которая может обеспечить завершение реакции, не способствуя образованию нежелательного побочного продукта, и предпочтительно находится в диапазоне, например, от комнатной температуры до 200°C. В предпочтительных условиях реакция предпочтительно завершается, например, за 1-24 часа, и ход реакции можно контролировать известными методами хроматографии. Нежелательный побочный продукт может быть удален методом, известным специалисту в данной области, таким как традиционный метод хроматографии, экстракция и/или кристаллизация.
Получение соединения (4d)
Соединение (4d) может быть получено, например, из соединения (4c) в качестве исходного в соответствии со стадией 2-3. В частности, стадию 2-3 варьируют в соответствии с исходным соединением и особо не ограничивают, только чтобы условия были подобны условиям данной реакции. Для данной реакции может быть использован способ, известный специалисту в данной области. Соединение (4d) может быть получено, например, перемешиванием соединения (4c) и 2-галогенированного ацетона (например, 0,5-5,0 эквивалентов 2-хлорацетона, 2-бромацетона или 2-иодацетона из расчета на соединение (4c)) в присутствии основания. Предпочтительно используют 0,5-5,0 эквивалентов основания из расчета на соединение (4c). Примеры используемого основания включают гидриды щелочных металлов, такие как гидрид натрия и гидрид лития, соли щелочных металлов, такие как карбонат калия, карбонат натрия и карбонат цезия, и алкоксиды металлов, такие как метоксид натрия и трет-бутилкалий. Используемые растворитель и температуру реакции варьируют в соответствии с исходным соединением и особо не ограничивают. В качестве растворителя, который не тормозит реакцию и дает возможность исходному соединению растворяться в нем до определенной степени, предпочтительно может быть использован, например, простой эфирный растворитель, такой как тетрагидрофуран, 1,4-диоксан или диэтиловый эфир, галогенированный растворитель, такой как метиленхлорид, 1,2-дихлорэтан или хлороформ, полярный растворитель, такой как диметилформамид или N-метилпирролидон, неполярный растворитель, такой как толуол или ксилол, или смешанный растворитель из указанных растворителей. Температура реакции должна быть такой, которая может обеспечить завершение реакции, не способствуя образованию нежелательного побочного продукта, и предпочтительно находится в диапазоне, например, от комнатной температуры до 200°C. В предпочтительных условиях реакция предпочтительно завершается, например, за 1-24 часа, и ход реакции можно контролировать известными методами хроматографии. Нежелательный побочный продукт может быть удален методом, известным специалисту в данной области, таким как традиционный метод хроматографии, экстракция и/или кристаллизация.
Получение соединения (4c)
Требуемое соединение (4c) может быть получено, например, способом, включающим нагревание соединения (4b) при кипении с обратным холодильником в муравьиной кислоте, или способом, включающим использование муравьиной кислоты и конденсирующего агента дегидратации, предпочтительно, такого как ангидрид кислоты или дициклогексилкарбодиимид. Соединение (4c) может быть эффективно получено, используя предпочтительно, например, 1-20 эквивалентов муравьиной кислоты и предпочтительно, например, 1-3 эквивалента конденсирующего агента дегидратации. Используемый растворитель варьируют в соответствии с исходным соединением и особо не ограничивают. В качестве растворителя, который не тормозит реакцию и дает возможность исходному соединению растворяться в нем до определенной степени, предпочтительно может быть использован, например, простой эфирный растворитель, такой как тетрагидрофуран, 1,4-диоксан или диэтиловый эфир, галогенированный растворитель, такой как метиленхлорид, 1,2-дихлорэтан или хлороформ, полярный растворитель, такой как диметилформамид или N-метилпирролидон, неполярный растворитель, такой как толуол или ксилол, или смешанный растворитель из указанных растворителей. Температура реакции должна быть такой, которая может обеспечить завершение реакции, не способствуя образованию нежелательного побочного продукта, и предпочтительно находится в диапазоне, например, от комнатной температуры до 100°C. В предпочтительных условиях реакция предпочтительно завершается, например, за 1-24 часа, и ход реакции можно контролировать известными методами хроматографии. Нежелательный побочный продукт может быть удален методом, известным специалисту в данной области, таким как традиционный метод хроматографии, экстракция и/или кристаллизация.
Получение соединения (4b)
Соединение (4b) является коммерчески доступным или может быть получено способом, известным специалисту в данной области. Если соединение (4b) не является коммерчески доступным, оно может быть получено, например метилированием соответствующего нитрофенольного соединения способом, известным специалисту в данной области, и последующим восстановлением нитрогруппы, когда Xa представляет собой метоксигруппу.
Получение амида (2a)
[Формула 19]
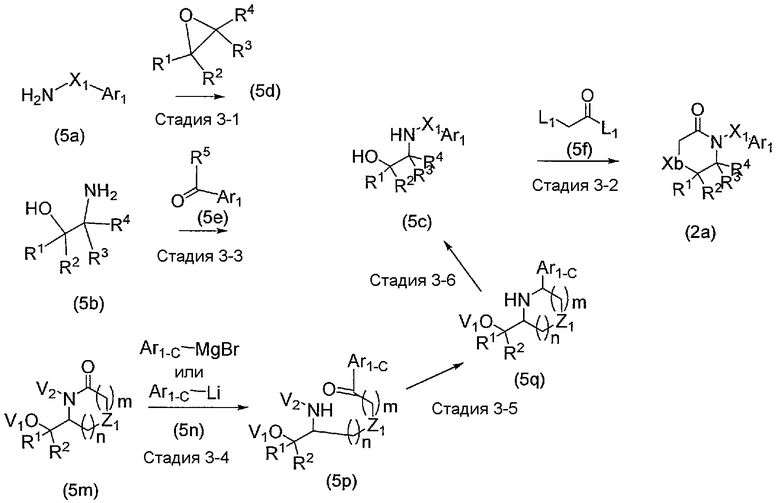
На данной схеме L1, R1, R2, R3, R4, R5 (который может иметь защитную группу, когда R5 содержит гидроксильную группу), X1 (который может иметь защитную группу, когда X1 содержит гидроксильную группу), Ar1, Ar1 - C, Z1, m и n являются такими, как определено выше; Xb представляет собой атом кислорода; V1 представляет собой защитную группу для атома кислорода, такую как метильная группа, этильная группа, бензильная группа, аллильная группа, трифенилметильная группа, трет-бутильная группа или трет-бутилдиметилсилильная группа, и V2 представляет собой защитную группу для атома азота, такую как трет-бутилоксикарбонильная группа или бензилоксикарбонильная группа.
На представленной выше схеме показан пример способа получения амида (2a). В частности, на схеме реакций показаны (i) способ, включающий преобразование амина (5a) в качестве исходного соединения, который является коммерчески доступным или получен способом, известным специалисту в данной области, в соединение (5c) в соответствии со стадией 3-1 и последующее образование оксоморфолинового кольца на стадии 3-2; (ii) способ, включающий преобразование соединения (5b) в качестве исходного, которое является коммерчески доступным или получено способом, известным специалисту в данной области, в соединение (5c) в соответствии со стадией 3-3 и затем образование оксоморфолинового кольца на стадии 3-2, когда заместитель X1 содержит по меньшей мере один атом водорода, или (iii) способ, включающий преобразование соединения (5m) в качестве исходного, которое является коммерчески доступным или получено способом, известным специалисту в данной области, в соединение (5p) взаимодействием с металлоорганическим реагентом (5n) в соответствии со стадией 3-4, преобразование соединения (5p) в соединение (5q) снятием защиты с атома азота и осуществление внутримолекулярной реакции восстановительного аминирования на стадии 3-5, преобразование соединения (5q) в соединение (5c) снятием защиты с атома кислорода на стадии 3-6 и последующее образование оксоморфолинового кольца на стадии 3-2.
Преобразование соединения (5c) в амид (2a)
Стадию 3-2 варьируют в соответствии с исходным соединением и особо не ограничивают, только чтобы условия были подобны условиям данной реакции. Реакция может быть выполнена способом, известным специалисту в данной области. Предпочтительно, реакцию целесообразно проводить при интенсивном перемешивании, например, соединения (5c) и 1,0-10 эквивалентов соединения (5f) из расчета на соединение (5c) в двухфазном растворителе для реакции, составленном из органического растворителя и оснóвного раствора. Используемые растворитель и температуру реакции варьируют в соответствии с исходным соединением и особо не ограничивают. Растворитель предпочтительно является растворителем, который не тормозит реакцию и дает возможность исходному соединению растворяться в нем до определенной степени. Предпочтительные примеры растворителя, который может быть использован, включают растворители в виде простых эфиров, такие как диэтиловый эфир, галогенированные растворители, такие как метиленхлорид, 1,2-дихлорэтан, и хлороформ, и неполярные растворители, такие как толуол и ксилол. Предпочтительные примеры оснóвного раствора, который может быть использован, включают растворы солей щелочных металлов, таких как гидроксид натрия, гидроксид калия, карбонат натрия, карбонат калия, карбонат цезия и бикарбонат натрия. Температура реакции должна быть такой, которая может обеспечить завершение реакции, не способствуя образованию нежелательного побочного продукта, и предпочтительно находится в диапазоне, например, от -78°C до комнатной температуры. В предпочтительных условиях реакция предпочтительно завершается, например, за 0,5-24 часа, и ход реакции можно контролировать известными методами хроматографии. Нежелательный побочный продукт может быть удален методом, известным специалисту в данной области, таким как традиционный метод хроматографии, экстракция и/или кристаллизация.
Предпочтительно, реакцию также целесообразно проводить при смешивании соединения (5c), например, с 1,0-10 эквивалентами соединения (5f) из расчета на соединение (5c) в оснóвных условиях. Используемые растворитель и температуру реакции варьируют в соответствии с исходным соединением и особо не ограничивают. Растворитель предпочтительно является растворителем, который не тормозит реакцию и дает возможность исходному соединению растворяться в нем до определенной степени. Предпочтительные примеры растворителя, который может быть использован, включают растворители в виде простых эфиров, такие как диэтиловый эфир и тетрагидрофуран, галогенированные растворители, такие как метиленхлорид, 1,2-дихлорэтан и хлороформ, и неполярные растворители, такие как толуол и ксилол. Используемое основание варьируют в соответствии с исходным соединением и особо не ограничивают. Количество основания предпочтительно составляет 1,0-10 эквивалентов из расчета на соединение (5c). Примеры основания, которое может быть использовано, включают соли щелочных металлов, такие как гидроксид натрия, гидроксид калия, карбонат натрия, карбонат калия, карбонат цезия и бикарбонат натрия, и органические основания, такие как диазабициклоундецен, пиридин, 4-диметиламинопиридин и триэтиламин. Температура реакции должна быть такой, которая может обеспечить завершение реакции, не способствуя образованию нежелательного побочного продукта, и предпочтительно находится в диапазоне, например, от -78°C до комнатной температуры. В предпочтительных условиях реакция предпочтительно завершается, например, за 0,5-24 часа, и ход реакции можно контролировать известными методами хроматографии. Нежелательный побочный продукт может быть удален методом, известным специалисту в данной области, таким как традиционный метод хроматографии, экстракция и/или кристаллизация.
Получение соединения (5f)
Соединение (5f) является коммерчески доступным или может быть получено способом, известным специалисту в данной области. Соединение (5f) предпочтительно является, например, хлорацетилхлоридом или бромацетилбромидом.
Получение соединения (5c)
Соединение (5c) является коммерчески доступным или может быть получено способом, известным специалисту в данной области. Предпочтительно, соединение (5c) может быть получено, например, (i) преобразованием амина (5a) в качестве исходного соединения, который является коммерчески доступным или получен способом, известным специалисту в данной области, в соединение (5c) в соответствии со стадией 3-1; (ii) преобразование соединения (5b) в качестве исходного, которое является коммерчески доступным или получено способом, известным специалисту в данной области, в соединение (5c) в соответствии со стадией 3-3 или (iii) преобразование соединения (5m) в качестве исходного, которое является коммерчески доступным или получено способом, известным специалисту в данной области, в соединение (5p) взаимодействием с металлоорганическим реагентом (5n) в соответствии со стадией 3-4, преобразование соединения (5p) в соединение (5q) снятием защиты с атома азота и осуществление внутримолекулярной реакции восстановительного аминирования на стадии 3-5 и преобразование соединения (5q) в соединение (5c) снятием защиты с атома кислорода на стадии 3-6.
Преобразование соединения (5a) в соединение (5c)
Стадию 3-1 варьируют в соответствии с исходным соединением и особо не ограничивают, только чтобы условия были подобны условиям данной реакции. Для данной реакции может быть использован способ, известный специалисту в данной области. Предпочтительные примеры способа включают реакцию раскрытия кольца с использованием соединения (5a) и 1,0-10 эквивалентов оксиранового соединения (5d) из расчета на соединение (5a). Используемые растворитель и температуру реакции варьируют в соответствии с исходным соединением и особо не ограничивают. Растворитель предпочтительно является растворителем, который не тормозит реакцию и дает возможность исходному соединению растворяться в нем до определенной степени, или содержащим его смешанным растворителем. Примеры растворителя, который может быть использован, включают растворители в виде простых эфиров, такие как диэтиловый эфир, галогенированные растворители, такие как метиленхлорид, 1,2-дихлорэтан и хлороформ, и неполярные растворители, такие как толуол и ксилол. Предпочтительный результат может быть получен без растворителя. Температура реакции должна быть такой, которая может обеспечить завершение реакции, не способствуя образованию нежелательного побочного продукта, и предпочтительно находится в диапазоне, например, от комнатной температуры до 300°C. В предпочтительных условиях реакция предпочтительно завершается, например, за 0,5-24 часа, и ход реакции можно контролировать известными методами хроматографии. Нежелательный побочный продукт может быть удален методом, известным специалисту в данной области, таким как традиционный метод хроматографии, экстракция и/или кристаллизация. Реакция предпочтительно может быть также продолжена добавлением кислоты Льюиса, такой как трифторид бора, тетраизопропоксид титана или перхлорат лития (см., например, Synthesis, 2004, vol.10, p.1563-1565).
Получение соединения (5a)
Соединение (5a) является коммерчески доступным или может быть получено способом, известным специалисту в данной области. Если соединение (5a) не является коммерчески доступным, оно может быть получено способом, описанным в литературе и известным специалисту в данной области (см., например, Shin Jikken Kagaku Koza (New Courses in Experimental Chemistry), vol.14, Yuki Kagobutsu No Gosei To Hannou (Synthesis and Reaction of Organic Compounds) [III], edited by The Chemical Society of Japan, Maruzen Co., Ltd., February 1978, p.1332-1399). Предпочтительные примеры способа включают i) способ, включающий преобразование соответствующего карбонильного производного в соединение (5a) реакцией восстановительного аминирования; ii) способ, включающий восстановление соответствующего карбонильного производного до спиртового производного, получение аминного эквивалента (предпочтительно, например, азидной группы или имидной группы) из спиртового производного реакцией замещения, известной специалисту в данной области, и последующее преобразование аминного эквивалента в соединение (5a) реакцией преобразования, известной специалисту в данной области; iii) способ, включающий преобразование соответствующего карбонильного производного в оксимпроизводное и последующее восстановление оксимпроизводного до соединения (5a) реакцией восстановления, известной специалисту в данной области; iv) способ, включающий преобразование соответствующего олефинового соединения в спиртовое производное реакцией окисления, получение аминного эквивалента (предпочтительно, например, азидной группы или имидной группы) из спиртового производного реакцией замещения, известной специалисту в данной области, и последующее преобразование аминного эквивалента в соединение (5a) реакцией преобразования, известной специалисту в данной области, и v) способ, включающий преобразование соответствующего олефинового соединения в аминоспиртовое производное реакцией присоединения и преобразование аминоспиртового производного в соединение (5a) реакцией преобразования, известной специалисту в данной области. Соединение (5a) может быть коммерчески доступным в виде оптически активного соединения или получено способом, известным специалисту в данной области, в виде оптически активного соединения (см., например, Chem. Rev., 1994, vol.94, p.2483-2547; Tetrahedron Letters, 1996, vol.37, p.3219-3222; and Organic Letters, 2000, vol.2, p.2821-2824). Соединения по настоящему изобретению может быть получено в виде оптически активного соединения их указанного соединения в качестве исходного.
Получение оксиранового соединения (5d)
Оксирановое соединение (5d) является коммерчески доступным или может быть получено способом, известным специалисту в данной области. Если оксирановое соединение (5d) не является коммерчески доступным, оно может быть получено способом, описанным в литературе и известным специалисту в данной области (см., например, Shin Jikken Kagaku Koza (New Courses in Experimental Chemistry), vol.14, Yuki Kagobutsu No Gosei To Hannou (Synthesis and Reaction of Organic Compounds) [1], edited by The Chemical Society of Japan, Maruzen Co., Ltd., November 1977, p.567-611). Соединение (5d) может быть коммерчески доступным в виде оптически активного соединения или получено способом, известным специалисту в данной области, в виде оптически активного соединения (см., например, K.B. Sharpless et al., "Comprehensive Organic Synthesis", B.M. Trost, Pergamon, 1991, vol.7, ch.3-2). Соединение по настоящему изобретению может быть получено в виде оптически активного соединения их указанного соединения в качестве исходного.
Преобразование соединения (5b) в соединение (5c)
Стадию 3-3 варьируют в соответствии с исходным соединением и особо не ограничивают, только чтобы условия были подобны условиям данной реакции. Для данной реакции может быть использован способ, известный специалисту в данной области. Предпочтительно, способ может представлять собой реакцию восстановительного аминирования между соединением (5b) и карбонильным соединением (5e) (см., например, Shin Jikken Kagaku Koza (New Courses in Experimental Chemistry), vol.14, Yuki Kagobutsu No Gosei To Hannou (Synthesis and Reaction of Organic Compounds) [III], edited by The Chemical Society of Japan, Maruzen Co., Ltd., February 1978, p.1380-1384). Например, способ предпочтительно является способом, включающим нагревание при кипении с обратным холодильником карбонильного соединения (5e) и 0,5-5,0 эквивалентов соединения (5b) в присутствии кислотного катализатора, такого как обычная неорганическая кислота, такая как хлористо-водородная кислота или серная кислота, что более предпочтительно, органическая кислота, такая как метансульфоновая кислота, п-толуолсульфоновая кислота или камфорсульфоновая кислота, или соль органической кислоты, такая как п-толуолсульфонат пиридиния (предпочтительно, например, 0,01-0,5 эквивалента), чтобы вызвать реакцию дегидратации, и восстановление полученного иминного производного до требуемого аминного производного предпочтительно, например, 1,0-10 эквивалентами гидрида металла, такого как литийалюминийгидрид или борогидрид натрия, из расчета на иминное производное. Можно также обработать карбонильное соединение (5e) и 0,5-5,0 эквивалентов соединения (5b) в инертном растворителе, таком как тетрагидрофуран, в присутствии катализатора в виде кислоты Льюиса, предпочтительно, такой как тетраизопропоксид титана (предпочтительно 0,01-0,5 эквивалента), и затем восстановить полученное соединение 1,0-10 эквивалентами гидрида металла, такого как борогидрид натрия. Также предпочтительно использовать способ, включающий восстановление карбонильного производного (5e) и предпочтительно, например, 0,5-5,0 эквивалентов соединения (5b) предпочтительно, например, 1,0-10 эквивалентами гидрида металла, такого как триацетоксиборогидрид натрия или цианборогидрид натрия, в инертном растворителе, таком, предпочтительно, как дихлорметан, 1,2-дихлорэтан, тетрагидрофуран, метанол или этанол, с получением требуемого аминного производного. Предпочтительно, для подходящего продолжения реакции добавить, например, 1,0-10 эквивалентов кислого вещества, такого как уксусная кислота или хлористо-водородная кислота. Температуру реакции варьируют в соответствии с исходным соединением и особо не ограничивают. Однако температура реакции должна быть такой, которая может обеспечить завершение реакции, не способствуя образованию нежелательного побочного продукта, и предпочтительно находится в диапазоне, например, от комнатной температуры до 100°C. В предпочтительных условиях реакция предпочтительно завершается, например, за 0,5-24 часа, и ход реакции можно контролировать известными методами хроматографии. Нежелательный побочный продукт может быть удален методом, известным специалисту в данной области, таким как традиционный метод хроматографии, экстракция и/или кристаллизация.
Получение соединения (5b)
Соединение (5b) является коммерчески доступным или может быть получено способом, известным специалисту в данной области. Если соединение (5b) не является коммерчески доступным, оно может быть получено способом, описанным в литературе и известным специалисту в данной области (см., например, Shin Jikken Kagaku Koza (New Courses in Experimental Chemistry), vol.14, Yuki Kagobutsu No Gosei To Hannou (Synthesis and Reaction of Organic Compounds) [III], edited by The Chemical Society of Japan, Maruzen Co., Ltd., February 1978, p.1332-1399). Соединение (5b) может быть коммерчески доступным в виде оптически активного соединения или получено способом, известным специалисту в данной области, в виде оптически активного соединения (см., например, Tetrahedron Letters, 1996, vol.37, p.3219-3222). Соединение по настоящему изобретению может быть получено в виде оптически активного соединения их указанного соединения в качестве исходного.
Получение карбонильного соединения (5e)
Карбонильное соединение (5e) является коммерчески доступным или может быть получено способом, известным специалисту в данной области. Если карбонильное соединение (5e) не является коммерчески доступным, оно может быть получено способом, описанным в литературе и известным специалисту в данной области (см., например, Shin Jikken Kagaku Koza (New Courses in Experimental Chemistry), vol.14, Yuki Kagobutsu No Gosei To Hannou (Synthesis and Reaction of Organic Compounds) [11], edited by The Chemical Society of Japan, Maruzen Co., Ltd., December 1977, p.633-875).
Преобразование соединения (5q) в соединение (5c)
Стадию 3-6 варьируют в соответствии с исходным соединением и особо не ограничивают, только чтобы условия были подобны условиям данной реакции. Может быть использован способ снятия защиты, известный специалисту в данной области (см., например, T. Greene et al., "Protective Groups in Organic Synthesis", John Wiley & Sons, Inc., New York, 1981). Альтернативно, стадия 3-6 предпочтительно может быть выполнена, например, получая соединение (5q) в виде сложноэфирного производного, где R1 и R2 образуют карбонильную группу, и затем, восстанавливая сложноэфирное производное реакцией восстановления, известной специалисту в данной области, когда каждый из R1 и R2 представляет собой атом водорода.
Получение соединения (5q)
Соединение (5q) является коммерчески доступным или может быть получено способом, известным специалисту в данной области. Если соединение (5q) не является коммерчески доступным, оно предпочтительно может быть получено, например, из соединения (5p) в качестве исходного в соответствии со стадией 3-5. В частности, соединение (5q) предпочтительно может быть получено проведением двух стадий удаления защитной группы для атома азота соединения (5p) способом, включающим снятие защиты, известным специалисту в данной области (см., например, T. Greene et al., "Protective Groups in Organic Synthesis", John Wiley & Sons, Inc., New York, 1981), и последующее подвергание соединения внутримолекулярной реакции восстановительного аминирования (см., например, Shin Jikken Kagaku Koza (New Courses in Experimental Chemistry), vol.14, Yuki Kagobutsu No Gosei To Hannou (Synthesis and Reaction of Organic Compounds) [III], edited by The Chemical Society of Japan, Maruzen Co., Ltd., February 1978, p.1380-1384). Альтернативно, указанные стадии могут, предпочтительно, быть выполнены, например, с использованием в качестве исходного соединения (5p), где R1 и R2 образуют карбонильную группу.
Получение соединения (5p)
Соединение (5p) является коммерчески доступным или может быть получено способом, известным специалисту в данной области. Если соединение (5p) не является коммерчески доступным, оно предпочтительно может быть получено, например, из соединения (5m) в качестве исходного в соответствии со стадией 3-4. Например, соединение (5p) может быть подходящим образом получено взаимодействием соединения (5m) с 0,5-5,0 эквивалентами металлоорганического реагента (5n), коммерчески доступного или полученного способом, известным специалисту в данной области, нуклеофильной реакцией, известной специалисту в данной области. Используемый растворитель варьируют в соответствии с исходным соединением и особо не ограничивают. Растворитель предпочтительно является растворителем, который не тормозит реакцию и дает возможность исходному соединению растворяться в нем до определенной степени, или смешанным растворителем из таких растворителей. Примеры растворителя, который может быть использован, включают растворители в виде простых эфиров, такие как диэтиловый эфир и тетрагидрофуран, галогенированные растворители, такие как метиленхлорид, 1,2-дихлорэтан и хлороформ, и неполярные растворители, такие как толуол и ксилол. Температуру реакции варьируют в соответствии с исходным соединением и особо не ограничивают. Однако температура реакции должна быть такой, которая может обеспечить завершение реакции, не способствуя образованию нежелательного побочного продукта, и предпочтительно находится в диапазоне, например, от -78°C до 50°C. В предпочтительных условиях реакция предпочтительно завершается, например, за 0,5-24 часа, и ход реакции можно контролировать известными методами хроматографии. Нежелательный побочный продукт может быть удален методом, известным специалисту в данной области, таким как традиционный метод хроматографии, экстракция и/или кристаллизация. Альтернативно, предпочтительно использовать в качестве исходного, например, соединение (5m), где R1 и R2 образуют карбонильную группу.
Получение соединения (5m)
Соединение (5m) является коммерчески доступным или может быть получено способом, известным специалисту в данной области. Если соединение (5m) не является коммерчески доступным, оно предпочтительно может быть получено, например, подвергая соответствующее исходное соединение реакции введения защиты, известной специалисту в данной области (см., например, T. Greene et al., "Protective Groups in Organic Synthesis", John Wiley & Sons, Inc., New York, 1981; or T. Sakamoto et al., "J. Org. Chem.", 1996, vol.61, p.8496). Альтернативно, предпочтительно использовать в качестве исходного, например, соединение, где R1 и R2 образуют карбонильную группу.
Общий способ получения 2
Ниже описан общий способ получения 2, обычно используемый для получения соединения общей формулы (I) по настоящему изобретению.
[Формула 20]

На данной схеме Ar1, R1, R2, R3, R4, L1, X1, Xa и Xb являются такими, как определено выше, L3 представляет собой трифенилфосфониевую группу, фосфитную группу или силильную группу, и V представляет собой защитную группу для карбоксильной группы, такую как метильная группа, этильная группа, бензильная группа, аллильная группа, трифенилметильная группа, трет-бутильная группа или трет-бутилдиметилсилильная группа.
Представленный выше общий способ получения 2 является примером способа получения соединения общей формулы (I), включающего конденсацию альдегида (1) с амидом (2b) на стадии 4-1, или примером способа получения соединения общей формулы (I), включающего конденсацию альдегида (1) со сложным эфиром (6a) на стадии 4-1 и последующее взаимодействие полученного соединения (6b) с амином (5a) на стадии 4-2.
Стадия 4-1
Реакцию конденсации стадии 4-1 варьируют в соответствии с исходным соединением и особо не ограничивают, только чтобы условия были подобны условиям данной реакции. Для данной реакции может быть использован известный способ, описанный во многих публикациях. Предпочтительные примеры способа включают реакцию Виттига, реакцию Хорнера-Эммонса и реакцию Петерсона (см., например, Jikken Kagaku Koza (Courses in Experimental Chemistry), vol.19, Yuki Gosei (Organic Synthesis) [1], edited by The Chemical Society of Japan, Maruzen Co., Ltd., June 1992, p.57-85).
Реакцию Виттига осуществляют с использованием соединения (2b) или (6a), где L3 представляет собой соль, галогенид трифенилфосфония, предпочтительно, например, 0,8-1,5 эквивалента альдегида (1) и предпочтительно, например 1,0-5,0 эквивалентов основания. Данная реакция может представлять собой i) способ, включающий первоначальную обработку соединения (2b) или (6a) и основания с образованием илида фосфора и последующее добавление альдегида (1) к полученному илиду, или (ii) способ, включающий добавление основания в присутствии соединения (2b) или (6a) и альдегида (1). Данную реакцию предпочтительно проводят в присутствии растворителя, с точки зрения упрощения ведения процесса и эффективности перемешивания. Используемый растворитель варьируют в соответствии с исходным соединением и используемым основанием и особо не ограничивают, лишь бы растворитель не тормозил реакцию и давал возможность исходному соединению растворяться в нем до определенной степени. Предпочтительные примеры растворителя включают полярные растворители, такие как нитрометан, ацетонитрил, 1-метил-2-пирролидон, N,N-диметилформамид и диметилсульфоксид, растворители в виде простых эфиров, такие как тетрагидрофуран, 1,4-диоксан и 1,2-диметоксиэтан, неполярные растворители, такие как бензол, толуол и ксилол, спиртовые растворители, такие как этанол и метанол, галогенированные растворители, такие как хлороформ и дихлорметан, воду и смешанные растворители из указанных растворителей. Используемое основание варьируют в соответствии с исходным соединением и растворителем. Предпочтительные примеры основания включают гидроксиды щелочных металлов, такие как гидроксид натрия, гидроксид калия и гидроксид лития, карбонаты щелочных металлов, такие как карбонат натрия, карбонат калия и бикарбонат натрия, щелочно-металлические соли спиртов, такие как метоксид натрия и трет-бутоксид калия, органические основания, такие как триэтиламин, пиридин и диазабициклононен, металлоорганические соединения, такие как бутиллитий и диизобутиламид лития, и гидриды щелочных металлов, такие как гидрид натрия. Температура реакции должна быть такой, которая может обеспечить завершение реакции, не способствуя образованию нежелательного побочного продукта, и предпочтительно находится в диапазоне, например, от -78 до 150°C. В предпочтительных условиях реакция завершается за 1-24 часа, и ход реакции можно контролировать известными методами хроматографии. Нежелательный побочный продукт может быть удален методом, известным специалисту в данной области, таким как традиционный метод хроматографии, экстракция и/или кристаллизация.
Реакцию Хорнера-Эммонса осуществляют с использованием, например, соединения (2b) или (6a), где L3 представляет собой фосфит, предпочтительно 0,8-1,5 эквивалента альдегида (1) и предпочтительно, например, 1,0-5,0 эквивалентов основания. Данная реакция может представлять собой i) способ, включающий первоначальную обработку соединения (2b) или (6a) и основания с образованием карбаниона и последующее добавление альдегида (1) к полученному карбаниону, или (ii) способ, включающий добавление основания в присутствии соединения (2b) или (6a) и альдегида (1). Данную реакцию предпочтительно проводят в присутствии растворителя, с точки зрения упрощения ведения процесса и эффективности перемешивания. Используемый растворитель варьируют в соответствии с исходным соединением и используемым основанием и особо не ограничивают, лишь бы растворитель не тормозил реакцию и давал возможность исходному соединению растворяться в нем до определенной степени. Предпочтительные примеры растворителя включают полярные растворители, такие как 1-метил-2-пирролидон, N,N-диметилформамид и диметилсульфоксид, растворители в виде простых эфиров, такие как тетрагидрофуран, 1,4-диоксан и 1,2-диметоксиэтан, неполярные растворители, такие как бензол, толуол и ксилол, спиртовые растворители, такие как этанол и метанол, воду и смешанные растворители из указанных растворителей. Используемое основание варьируют в соответствии с исходным соединением и растворителем. Предпочтительные примеры основания включают гидроксиды щелочных металлов, такие как гидроксид натрия, гидроксид калия, и гидроксид лития, карбонаты щелочных металлов, такие как карбонат натрия, карбонат калия и бикарбонат натрия, щелочно-металлические соли спиртов, такие как метоксид натрия и трет-бутоксид калия, органические основания, такие как триэтиламин, пиридин и диазабициклононен, металлоорганические соединения, такие как бутиллитий и диизобутиламид лития, гидриды щелочных металлов, такие как гидрид натрия, и щелочно-металлические соли аммония, такие как амид натрия. Температура реакции должна быть такой, которая может обеспечить завершение реакции, не способствуя образованию нежелательного побочного продукта, и предпочтительно находится в диапазоне, например, от -78 до 150°C. В предпочтительных условиях реакция предпочтительно завершается, например, за 1-24 часа, и ход реакции можно контролировать известными методами хроматографии. Нежелательный побочный продукт может быть удален методом, известным специалисту в данной области, таким как традиционный метод хроматографии, экстракция и/или кристаллизация.
Реакцию Петерсона осуществляют с использованием соединения (2b) или (6a), где L3 представляет собой силильную группу, предпочтительно, например, 0,8-1,5 эквивалента альдегида (1) и предпочтительно, например, 1,0-5,0 эквивалентов основания. Данная реакция может представлять собой i) способ, включающий первоначальную обработку соединения (2b) или (6a) и основания с образованием карбаниона и последующее добавление альдегида (1) к полученному карбаниону, или (ii) способ, включающий добавление основания в присутствии соединения (2b) или (6a) и альдегида (1). Данную реакцию предпочтительно проводят в присутствии растворителя, с точки зрения упрощения ведения процесса и эффективности перемешивания. Используемый растворитель варьируют в соответствии с исходным соединением и используемым основанием и особо не ограничивают, лишь бы растворитель не тормозил реакцию и давал возможность исходному соединению растворяться в нем до определенной степени. Предпочтительные примеры растворителя включают полярные растворители, такие как 1-метил-2-пирролидон, N,N-диметилформамид и диметилсульфоксид, растворители в виде простых эфиров, такие как тетрагидрофуран, 1,4-диоксан и 1,2-диметоксиэтан, неполярные растворители, такие как бензол, толуол и ксилол, спиртовые растворители, такие как этанол и метанол, воду и смешанные растворители из указанных растворителей. Используемое основание варьируют в соответствии с исходным соединением и растворителем. Предпочтительные примеры основания включают гидроксиды щелочных металлов, такие как гидроксид натрия, гидроксид калия и гидроксид лития, карбонаты щелочных металлов, такие как карбонат натрия, карбонат калия и бикарбонат натрия, щелочно-металлические соли спиртов, такие как метоксид натрия и трет-бутоксид калия, органические основания, такие как триэтиламин, пиридин и диазабициклононен, металлоорганические соединения, такие как бутиллитий и диизобутиламид лития, гидриды щелочных металлов, такие как гидрид натрия, и щелочно-металлические соли аммония, такие как амид натрия. Температура реакции должна быть такой, которая может обеспечить завершение реакции, не способствуя образованию нежелательного побочного продукта, и предпочтительно находится в диапазоне, например, от -78 до 150°C. В предпочтительных условиях реакция предпочтительно завершается, например, за 1-24 часа, и ход реакции можно контролировать известными методами хроматографии. Нежелательный побочный продукт может быть удален методом, известным специалисту в данной области, таким как традиционный метод хроматографии, экстракция и/или кристаллизация.
Стадия 4-2
Стадия 4-2 является примером способа, включающего взаимодействие соединения (6b) с амином (5a) и последующее преобразование продукта реакции в соединение общей формулы (I). Примеры данной стадии включают i) удаление защитной группы соединения (6b) способом, известным специалисту в данной области (см., например, T. Greene et al., "Protective Groups in Organic Synthesis" (John Wiley & Sons.Inc., New York, 1981), осуществление дегидратационной конденсации соединения с амином (5a) способом, известным специалисту в данной области (см., например, Shin Jikken Kagaku Koza (New Courses in Experimental Chemistry), vol.14, Yuki Kagobutsu No Gosei To Hannou (Synthesis and Reaction of Organic Compounds) [III], edited by The Chemical Society of Japan, Maruzen Co., Ltd., February 1978, p.1136-1162; and "Yukikagaku Jikken No Tebiki (Introduction to Organic Chemistry Experiments) [4]", Kagaku-Dojin Publishing Company, Inc., September 1990, p.27-52), и преобразование конденсата в соединение общей формулы (I) обработкой в оснóвных условиях, и ii) связывание соединения (6b) с амином (5a) способом, известным специалисту в данной области, удаление защитной группы и преобразование полученного соединения в соединение общей формулы (I) непосредственно внутримолекулярной реакцией амидирования. На данной стадии соединение (6b) и амин (5a) могут быть преобразованы в соединение общей формулы (I) в одну стадию реакции подбором подходящих условий.
Получение амида (2b)
[Формула 21]

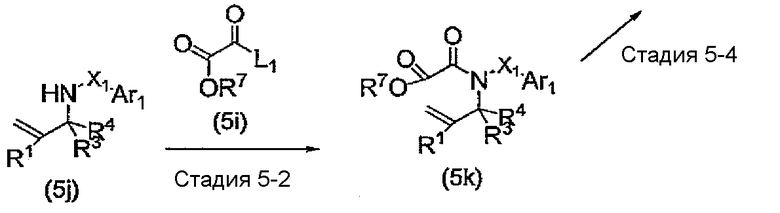
На данной схеме Ar1, L1, L3, R1, R2, R3, R4, X1 и Xb являются такими, как определено выше, и R7 представляет собой низшую алкильную группу.
На представленной выше схеме показан пример способа получения амида (2b). В частности, амид (2b) может быть получен способом, известным специалисту в данной области, хотя способ варьируют в соответствии с исходным соединением. Предпочтительные примеры способа включают способ, включающий получение амида (2b) из амида (2a) в качестве исходного соединения в соответствии со стадией 5-1, способ, включающий преобразование соединения (5c) в качестве исходного в соединение (2c) на стадии 5-2 и последующее преобразование соединения (2c) в амид (2b) на стадии 5-3, и способ, включающий преобразование соединения (5j) в качестве исходного в соединение (5k) на стадии 5-2 и последующее преобразование соединения (5k) в амид (2b) на стадии 5-4.
Преобразование амида (2a) в амид (2b)
Стадию 5-1 варьируют в соответствии с исходным соединением и особо не ограничивают, только чтобы условия были подобны условиям данной реакции. Для данной реакции может быть использован способ, известный специалисту в данной области. Предпочтительно, например, стадия 5-1 представляет собой i) реакцию Виттига, где L3 представляет собой трифенилфосфониевую группу, и данная реакция заключается в способе, включающем галогенирование амида (2a) способом, известным специалисту в данной области (см., например, Jikken Kagaku Koza (Courses in Experimental Chemistry), vol.19, Yuki Gosei (Organic Synthesis) [1], edited by The Chemical Society of Japan, Maruzen Co., Ltd., June 1992, p.430-438), и последующее взаимодействие полученного соединения с трифенилфосфином (см., например, Organic Reaction, 1965, vol.14, p.270). Альтернативно, стадия 5-1 представляет собой ii) реакцию Хорнера-Эммонса, где L3 представляет собой фосфит, и данная реакция заключается в способе, включающем галогенирование амида (2a) способом, известным специалисту в данной области (см., например, Jikken Kagaku Koza (Courses in Experimental Chemistry), vol.19, Yuki Gosei (Organic Synthesis) [1], edited by The Chemical Society of Japan, Maruzen Co., Ltd., June 1992, p.430-438), и последующее взаимодействие полученного соединения с алкилфосфинитом в соответствии с реакцией Арбузова (см., например, Chemical Review, 1981, vol.81, p.415) или с фосфонитом металла в соответствии с реакцией Бекера (см., например, Journal of the American Chemical Society, 1945, vol.67, p.1180), с получением амида (2b). Альтернативно, на стадии 5-1 можно использовать способ получения амида (2b) из амида (2a) и хлорфосфата в присутствии основания (см., например, The Journal of Organic Chemistry, 1989, vol.54, p.4750). Альтернативно, стадия 5-1 представляет собой iii) реакцию Петерсона, где L3 представляет собой силильную группу, и данная реакция заключается в способе получения амида (2b) из амида (2a) и триалкилсилилхлорида в присутствии основания (см., например, Journal of Organometallic Chemistry, 1983, vol.248, p.51).
Преобразование амида (2c) в амид (2b)
Стадию 5-3 варьируют в соответствии с исходным соединением и особо не ограничивают, только чтобы условия были подобны условиям данной реакции. Для данной реакции может быть использован способ, известный специалисту в данной области. Предпочтительно, например, стадия 5-3 может представлять собой способ, включающий восстановление карбонильного фрагмента сложного эфира до спирта (см., например, Jikken Kagaku Koza (Courses in Experimental Chemistry), vol.26, Yuki Gosei (Organic Synthesis) [VIII], edited by The Chemical Society of Japan, Maruzen Co., Ltd., April 1992, p.159-266), преобразование спирта в галогенсодержащее соединение (см., например, Shin Jikken Kagaku Koza (New Courses in Experimental Chemistry), vol.14, Yuki Kagobutsu No Gosei To Hannou (Synthesis and Reaction of Organic Compounds) [1], edited by The Chemical Society of Japan, Maruzen Co., Ltd., November 1977, p.331-450), и преобразование галогенсодержащего соединения в реактив Виттига (2b) (см., например, Organic Reaction, 1965, vol.14, p.270) или в реактив Хорнера-Эммонса (2b) в соответствии с реакцией Арбузова (см., например, Chemical Review, 1981, vol.81, p.415). Альтернативно, спирт может быть преобразован в реактив Виттига (2b) взаимодействием с гидробромидом триаллилфосфора (см., например, Synth. Commun., 1996, vol.26, p.3091-3095; and Tetrahedron Lett., 2001, vol.42, p.1309-1331).
Получение амида (2c)
Амид (2c) может быть получен способом, известным специалисту в данной области, хотя способ варьируют в соответствии с исходным соединением. Предпочтительно, амид (2c) может быть получен из соединения (5c) в качестве исходного, например, через стадию 5-2. Предпочтительно, на данной стадии реакцию целесообразно проводить при интенсивном перемешивании соединения (5c) и, например, 1,0-10 эквивалентов соединения (5g) из расчета на соединение (5c) в двухфазном растворителе для реакции, состоящем из органического растворителя и оснóвного раствора. Используемые растворитель и температуру реакции варьируют в соответствии с исходным соединением и особо не ограничивают. Растворитель предпочтительно является растворителем, который не тормозит реакцию и дает возможность исходному соединению растворяться в нем до определенной степени, или смешанным растворителем из таких растворителей. Предпочтительные примеры органического растворителя, который может быть использован, включают растворители в виде простых эфиров, такие как диэтиловый эфир, галогенированные растворители, такие как метиленхлорид, 1,2-дихлорэтан и хлороформ, и неполярные растворители, такие как толуол и ксилол. Предпочтительно, используют 1,0 или более эквивалентов оснóвного раствора. Предпочтительные примеры оснóвного раствора, который может быть использован, включают растворы солей щелочных металлов, таких как гидроксид натрия, гидроксид калия, карбонат натрия, карбонат калия, карбонат цезия и бикарбонат натрия. Температура реакции должна быть такой, которая может обеспечить завершение реакции, не способствуя образованию нежелательного побочного продукта, и предпочтительно находится в диапазоне, например, от -78°C до комнатной температуры. В предпочтительных условиях реакция предпочтительно завершается, например, за 0,5-24 часа, и ход реакции можно контролировать известными методами хроматографии. Нежелательный побочный продукт может быть удален методом, известным специалисту в данной области, таким как традиционный метод хроматографии, экстракция и/или кристаллизация.
Можно также использовать на стадии 5-2 способ, включающий взаимодействие соединения (5c) с предпочтительно, например, 1,0-5,0 эквивалентами соединения (5g) в присутствии основания, такого как, предпочтительно, органический амин, например триэтиламин, изопропилэтиламин или пиридин (предпочтительно, например, 1,0-5,0 эквивалентов). Используемые растворитель и температуру реакции варьируют в соответствии с исходным соединением и особо не ограничивают. Растворитель предпочтительно является растворителем, который не тормозит реакцию и дает возможность исходному соединению растворяться в нем до определенной степени. Предпочтительные примеры органического растворителя, который может быть использован, включают растворители в виде простых эфиров, такие как диэтиловый эфир, галогенированные растворители, такие как метиленхлорид, 1,2-дихлорэтан и хлороформ, и неполярные растворители, такие как толуол и ксилол. Температура реакции должна быть такой, которая может обеспечить завершение реакции, не способствуя образованию нежелательного побочного продукта, и предпочтительно находится в диапазоне, например, от -78°C до 100°C. В предпочтительных условиях реакция предпочтительно завершается, например, за 0,5-24 часа, и ход реакции можно контролировать известными методами хроматографии. Нежелательный побочный продукт может быть удален методом, известным специалисту в данной области, таким как традиционный метод хроматографии, экстракция и/или кристаллизация.
На стадии 5-2, реакцию можно также подходящим образом провести, нагревая соединение (5c) и 1,0-20 эквивалентов соединения (5h), где R7 представляет собой низший алкил, из расчета на соединение (5c). Используемые растворитель и температуру реакции варьируют в соответствии с исходным соединением и особо не ограничивают. Растворитель предпочтительно является растворителем, который не тормозит реакцию и дает возможность исходному соединению растворяться в нем до определенной степени, или смешанным растворителем из таких растворителей. Предпочтительные примеры органического растворителя, который может быть использован, включают растворители в виде простых эфиров, такие как диэтиловый эфир, галогенированные растворители, такие как метиленхлорид, 1,2-дихлорэтан и 1,2-дихлорбензол, неполярные растворители, такие как толуол и ксилол, полярные растворители, такие как диметилформамид и N-метилпирролидон, и спиртовые растворители, такие как метанол, этанол, 2-пропанол и трет-бутанол. Реакцию можно также подходящим образом провести без растворителя. Температура реакции должна быть такой, которая может обеспечить завершение реакции, не способствуя образованию нежелательного побочного продукта, и предпочтительно находится в диапазоне, например, от 50°C до 200°C. В предпочтительных условиях реакция предпочтительно завершается, например, за 0,5-24 часа, и ход реакции можно контролировать известными методами хроматографии. Нежелательный побочный продукт может быть удален методом, известным специалисту в данной области, таким как традиционный метод хроматографии, экстракция и/или кристаллизация.
На стадии 5-2 реакцию можно также подходящим образом провести, используя соединение (5c) и 1,0-5,0 эквивалентов соединения (5i) в описанных выше условиях реакции или их сочетании. Реакцию можно также подходящим образом провести добавлением межфазного катализатора, которым является соль четвертичного аммония, такая как тетрабутиламмонийхлорид или бензилтриэтиламмонийхлорид, или кислотное соединение, такое как п-толуолсульфоновая кислота или камфорсульфоновая кислота.
Получение соединений (5g), (5h) и (5i)
Соединения (5g), (5h) и (5i) являются коммерчески доступными или могут быть получены способом, известным специалисту в данной области. Если соединения не являются коммерчески доступными, они могут быть получены этерификацией или галогенированием соответствующего производного щавелевой кислота способом, известным специалисту в данной области.
Преобразование соединения (5k) в оксоморфолин (2b)
Стадию 5-4 варьируют в соответствии с исходным соединением и особо не ограничивают, только чтобы условия были подобны условиям данной реакции. Для данной реакции может быть использован способ, известный специалисту в данной области. Предпочтительно, например, стадия 5-4 может представлять собой способ, включающий преобразование олефинового фрагмента соединения (5k) в полуацетальное производное реакцией окислительного отщепления и реакцию внутримолекулярной циклизации (см., например, Shin Jikken Kagaku Koza (New Courses in Experimental Chemistry), vol.14, Yuki Kagobutsu No Gosei To Hannou (Synthesis and Reaction of Organic Compounds) [1], edited by The Chemical Society of Japan, Maruzen Co., Ltd., November 1977, p.331-450), и преобразование полуацетального производного в реактив Виттига (2b) (см., например, Organic Reaction, 1965, vol.14, p.270) или в реактив Хорнера-Эммонса (2b) в соответствии с реакцией Арбузова (см., например, Chemical Review, 1981, vol.81, p.415). Полуацетальное производное также может быть преобразовано в реактив Виттига (2b) взаимодействием с гидробромидом триаллилфосфора (см., например, Synth. Commun., 1996, vol.26, p.3091-3095; and Tetrahedron Lett., 2001, vol.42, p.1309-1331). Реакцию окислительного отщепления олефинового фрагмента варьируют в соответствии с исходным соединением и особо не ограничивают, только чтобы условия были подобны условиям данной реакции. Предпочтительном, например, озоновое окисление (см., например, Shin Jikken Kagaku Koza (New Courses in Experimental Chemistry), vol.15, Sanka To Kangen (Oxidation and Reduction) [I-2], edited by The Chemical Society of Japan, Maruzen Co., Ltd., September 1976, p.563-603). Реакцию окислительного отщепления и реакцию внутримолекулярной циклизации можно в подходящих условиях проводить непрерывно, и поэтому они являются подходящими для получения соединения (2b).
Получение соединения (5k)
Соединение (5k) может быть получено из соединения (5j) и предпочтительно, например, 1,0-5,0 эквивалентов соединения (5i) из расчета на соединение (5j) в соответствии со стадией 5-2.
Получение соединения (5j)
Соединение (5j) является коммерчески доступным или может быть получено способом, известным специалисту в данной области. Если соединение (5j) не является коммерчески доступным, его предпочтительно получают, например, внутримолекулярной реакцией гидроаминирования амина или сульфониламида, содержащего алленильную группу, используя металлический катализатор, когда R4 и X1 связаны друг с другом, с образованием азотсодержащего гетероцикла (см., например, Journal of The American Chemical Society, 2003, vol.125, p.11956; and Tetrahedron Lett., 1998, vol.39, p.5421-5424). Данную реакцию варьируют в соответствии с исходным соединением и особо не ограничивают, только чтобы условия были подобны условиям данной реакции. Металлический катализатор предпочтительно состоит, например, из 0,001-0,1 эквивалента палладиевого комплекса, такого как ацетат палладия(II), дихлорбис(трифенилфосфин)палладий(II), тетракис(трифенилфосфин)палладий(0) или димер аллилпалладийхлорид. Реакцию можно также подходящим образом провести добавлением предпочтительно, например, 0,001-0,1 эквивалента фосфорного лиганда, предпочтительно такого как 2,2'-бис(дифенилфосфино)-1,1'-бинафтил или 1,1'-бис(дифенилфосфино)ферроцен. Реакцию также можно подходящим образом провести добавлением предпочтительно, например, 0,001-10 эквивалентов уксусной кислоты или хлористо-водородной кислоты. Используемые растворитель и температуру реакции варьируют в соответствии с исходным соединением и особо не ограничивают. Растворитель предпочтительно является растворителем, который не тормозит реакцию и дает возможность исходному соединению растворяться в нем до определенной степени, или смешанным растворитель из таких растворителей. Предпочтительные примеры органического растворителя, который может быть использован, включают растворители в виде простых эфиров, такие как диэтиловый эфир и тетрагидрофуран, галогенированные растворители, такие как метиленхлорид и 1,2-дихлорэтан, неполярные растворители, такие как толуол и ксилол, полярные растворители, такие как диметилформамид и N-метилпирролидон, и спиртовые растворители, такие как метанол, этанол, 2-пропанол и трет-бутанол. Температура реакции должна быть такой, которая может обеспечить завершение реакции, не способствуя образованию нежелательного побочного продукта, и предпочтительно находится в диапазоне, например, от 50°C до 200°C. В предпочтительных условиях реакция предпочтительно завершается, например, за 0,5-24 часа, и ход реакции можно контролировать известными методами хроматографии. Нежелательный побочный продукт может быть удален методом, известным специалисту в данной области, таким как традиционный метод хроматографии, экстракция и/или кристаллизация.
Получение соединения (6a)
[Формула 22]
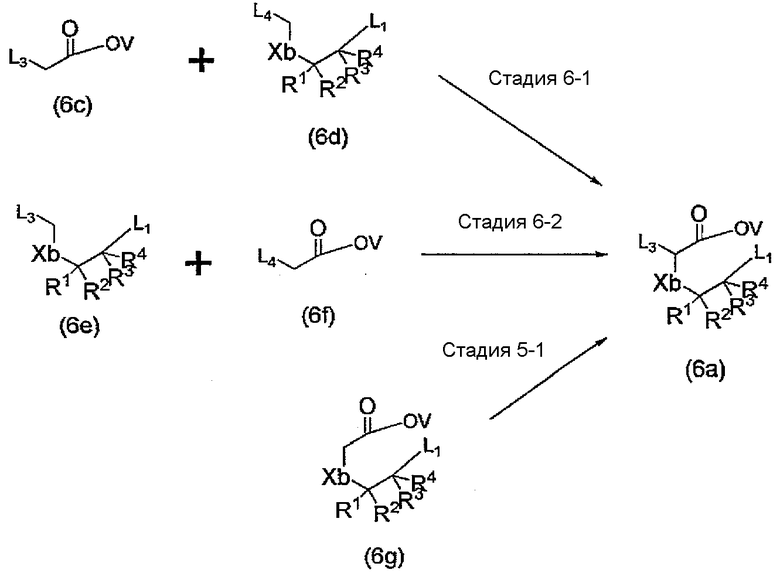
На данной схеме R1, R2, R3, R4, V, L1, L3 и Xb являются такими, как определено выше, и L4 является таким, как определено для L1.
На представленной выше схеме показан пример получения соединения (6a). В частности, соединение (6a) является коммерчески доступным или может быть получено по методике, представленной на приведенной выше схеме реакций и известной специалисту в данной области (см., например, C. Patois et al., "Synth. Commun.", 1991, vol.22, p.2391; и J.A. Jackson et al., "J. Org. Chem.", 1989, vol.20, p.5556). Стадия 6-1 является стадией получения требуемого соединения (6a) обработкой фосфоната (6c), например, 1,0-2,0 эквивалентами соединения (6d) из расчета на фосфонат (6c) в оснóвных условиях. Альтернативно, стадия 6-2 является стадией получения требуемого соединения (6a) обработкой соединения (6e), например, 1,0-2,0 эквивалентами сложного эфира (6f) в оснóвных условиях. Требуемое соединение (6a) может быть также получено, например, из соединения (6g) в соответствии с описанной выше стадией 5-1.
Используемое основание на данной стадии варьируют в соответствии с исходным соединением и не ограничивают. Предпочтительно, используют, например, 1,0-1,5 эквивалента основания, такого как гидрид натрия, н-бутиллитий, диизопропиламид лития, бис(триметилсилил)амид лития или бис(триметилсилил)амид натрия. Растворитель, используемый на данной стадии, варьируют в соответствии с исходным соединением, и особо не ограничивают, только чтобы растворитель не тормозил реакцию и давал возможность исходному соединению растворяться в нем до определенной степени. Предпочтительные примеры растворителя включают гексан, толуол, диэтиловый эфир, тетрагидрофуран, N,N-диметилформамид, гексаметилфосфорный триамид и смешанный растворитель, такой как описано выше. Температура реакции должна быть такой, которая может обеспечить завершение реакции, не способствуя образованию нежелательного побочного продукта, и предпочтительно находится в диапазоне, например, от -78°C до 150°C. В предпочтительных условиях реакция завершается за 1-24 часа, и ход реакции можно контролировать известными методами хроматографии. Нежелательный побочный продукт может быть удален методом, известным специалисту в данной области, таким как метод традиционной хроматографии и/или кристаллизация.
Фосфонат (6c), соединение (6d), соединение (6e), сложный эфир (6f) и соединение (6g), используемые на данной стадии, являются коммерчески доступными или могут быть получены способом, известным специалисту в данной области.
Соединение общей формулы (I) или его фармакологически приемлемая соль по настоящему изобретению обладает эффектом ингибирования продукции Aβ40 или Aβ42 и, таким образом, эффективно(а) в качестве профилактического или терапевтического средства для заболевания, вызываемого амилоидом-β, и особенно эффективно(а) в качестве профилактического или терапевтического средства для нейродегенеративного заболевания, вызываемого Aβ, такого как болезнь Альцгеймера или синдром Дауна.
Соединения, охватываемые настоящим изобретением, проявляют полезные превосходные фармацевтические свойства, например активность in vitro, активность in vivo, растворимость, стабильность, фармакокинетику и низкую токсичности.
Профилактическое или терапевтическое средство для заболевания, вызываемого Aβ, в соответствии с настоящим изобретением может быть получено традиционным способом. Предпочтительные примеры дозированной формы включают таблетки, порошки, микрогранулы, гранулы, таблетки с покрытием, капсулы, сиропы, пастилки, дозированные формы для ингаляции, суппозитории, растворы для инъекций, мази, глазные растворы, глазные мази, капли в нос, ушные капли, припарки и лосьоны. Терапевтическое или профилактическое средство может быть получено с использованием обычно используемых ингредиентов, таких как эксципиент, связующее вещество, лубрикант, красящее вещество и корригент, и ингредиентов, используемых по потребности, таких как стабилизатор, эмульгатор, вещество, облегчающее абсорбцию, поверхностно-активное вещество, регулятор pH, консервант и антиоксидант, и может быть получено смешиванием ингредиентов, обычно используемых в качестве материалов для изготовления фармацевтических препаратов. Примеры таких ингредиентов включают животные и растительные масла, такие как соевое масло, говяжий жир и синтетические глицериды; углеводороды, такие как жидкий парафин, сквалан и твердый парафин; сложно эфирные масла, такие как октилдодецилмиристат и изопропилмиристат; высшие спирты, такие как цетостеариловый спирт и бегениловый спирт; силиконовую смолу; силиконовое масло; поверхностно-активные вещества, такие как сложный эфир полиоксиэтилена и жирной кислоты, сложный эфир сорбитана и жирной кислоты, сложный эфир глицерина и жирной кислоты, сложный эфир полиоксиэтиленсорбитана и жирной кислоты, полиоксиэтилен-гидрогенизированное касторовое масло и блок-сополимер полиоксиэтилена и полиоксипропилена; водорастворимые полимеры, такие как гидроксиэтилцеллюлоза, полиакриловая кислота, карбоксивиниловый полимер, полиэтиленгликоль, поливинилпирролидон и метилцеллюлоза; низшие спирты, такие как этанол и изопропанол; многоатомные спирты, такие как глицерин, пропиленгликоль, дипропиленгликоль и сорбит; сахара, такие как глюкоза и сахароза; неорганические порошки, такие как кремниевый ангидрид, алюмосиликат магния и силикат алюминия, и очищенную воду. Примеры эксципиента включают лактозу, кукурузный крахмал, сахарозу, глюкозу, маннит, сорбит, кристаллическую целлюлозу и диоксид кремния. Примеры используемого связующего вещества включают поливиниловый спирт, простой поливиниловый эфир, метилцеллюлозу, этилцеллюлозу, аравийскую камедь, трагакант, желатин, шеллак, гидроксипропилметилцеллюлозу, гидроксипропилцеллюлозу, поливинилпирролидон, блок-сополимер полипропиленгликоля и полиоксиэтилена и меглумин. Примеры используемого дезинтегранта включают крахмал, агар, желатиновый порошок, кристаллическую целлюлозу, карбонат кальция, бикарбонат натрия, цитрат кальция, декстрин, пектин и кальцийкарбоксиметилцеллюлозу. Примеры используемого лубриканта включают стеарат магния, тальк, полиэтиленгликоль, диоксид кремния и гидрогенизированное растительное масло. Примеры используемого красящего вещества включают красящие вещества, приемлемые для фармацевтических препаратов. Примеры корригента включают порошок какао, ментол, эмпазм (empasm), мятное масло, борнеол и порошок корицы.
Например, препарат для орального введения получают смешением служащего в качестве активного ингредиента соединения или его соли или гидрата соединения или соли, эксципиента и, когда требуется, например, связующего вещества, дезинтегранта, лубриканта, красящего вещества и корригента и последующим превращением смеси, например, в порошок, мелкие гранулы, гранулы, таблетки, таблетки с покрытием или капсулы традиционным способом. Очевидно, что таблетки или гранулы при необходимости могут быть снабжены подходящим покрытием, например, сахарным покрытием. Сироп или препарат для инъекций получают смешением, например, регулятора рН, солюбилизатора и изотонизирующего средства и, когда требуется, способствующего растворению вспомогательного средства, стабилизатора и тому подобного традиционным способом. Наружный препарат может быть изготовлен традиционным способом без особых ограничений. В качестве материала для основы может быть использован любой из многочисленных материалов, обычно используемых для фармацевтического препарата, квазилекарственного средства (quasi drug), косметического средства или тому подобного. Примеры материала для основы включают такие материалы, как животные и растительные масла, минеральные масла, эфирные масла, воски, высшие спирты, жирные кислоты, силиконовые масла, поверхностно-активные вещества, фосфолипиды, спирты, многоатомные спирты, водорастворимые полимеры, глинистые минералы и дистиллированную воду. При необходимости могут быть добавлены регулятор рН, антиоксидант, хелатообразователь, консервант и фунгицид, красящее вещество, вкусовое вещество или тому подобное. Кроме того, при необходимости может быть подмешан ингредиент, обладающий эффектом индуцирования дифференциации, такой как усилитель кровотока, бактерицид, противовоспалительное средство, активатор клеток, витамин, аминокислота, увлажнитель или кератолитическое средство. Дозу терапевтического или профилактического средства по настоящему изобретению варьируют, например, в соответствии со степенью проявления симптомов, возрастом, полом, массой тела, способом введения, типом соли и конкретным видом болезни. Соединение формулы (I) или его фармакологически приемлемую соль по настоящему изобретению вводят орально взрослому обычно примерно от 30 мкг до 10 г, предпочтительно от 100 мкг до 5 г и более предпочтительно от 100 мкг до 100 мг в сутки или вводят взрослому путем инъекции примерно от 30 мкг до 1 г, предпочтительно от 100 мкг до 500 мг и более предпочтительно от 100 мкг до 30 мг в сутки одной дозой или разделенными дозами, соответственно.
Наилучший вариант осуществления изобретения
Далее настоящее изобретение описано более подробно со ссылками на примеры и примеры испытаний. Но примеры и примеры испытаний даны только для целей иллюстрации. Профилактическое или терапевтическое средство по настоящему изобретению для заболевания, вызываемого Aβ, ни в коем случае не ограничивается следующими ниже конкретными примерами. Специалист в данной области сможет в полной мере реализовать настоящее изобретение, внося различные модификации не только в следующие примеры и примеры испытаний, но и в данное описание, а также модификации в пределах объема формулы изобретения, приложенной к данному описанию.
В следующих далее примерах использованы следующие сокращения:
ДМФА: диметилформамид
ТГФ: тетрагидрофуран
LAH: литийалюминийгидрид
WSC: гидрохлорид 1-этил-3-(3-диметиламинопропил)карбодиимида
HOBT: 1-гидроксибензотриазол
DIEA: диизопропилэтиламин
TEA: триэтиламин
TBAF: тетрабутиламмонийфторид
DBU: 1,8-диазабицикло[5.4.0]ундец-7-ен
трет: третичный
LDA: диизопропиламин лития
Пример 1
Синтез (Z)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-(3,4,5-трифторбензил)морфолин-3-она
[Формула 23]

Синтез 3-метокси-4-(4-метил-1H-имидазол-1-ил)бензальдегида
Синтез метил 3-метокси-4-нитробензоата
Метилйодид (463 г) добавляли по каплям к смеси 3-гидрокси-4-нитробензойной кислоты (199 г) с карбонатом калия (450 г) в ДМФА (1 л) при комнатной температуре. Реакционный раствор перемешивали при комнатной температуре в течение ночи и затем к реакционному раствору добавляли метилйодид (230 г). Реакционный раствор дополнительно перемешивали при комнатной температуре в течение 6 часов. Реакционный раствор вливали в ледяную воду и выпавшее в осадок твердое вещество отделяли фильтрованием. Полученное твердое вещество сушили при 50°C в течение ночи, с получением 178 г указанного в заголовке соединения. Характеристические значения соответствовали известным значениям (CAS #5081-37-8).
Синтез метил 4-амино-3-метоксибензоата
10% Палладий на углероде (содержащий 50% воды, 15 г) добавляли к раствору метил 3-метокси-4-нитробензоата (150 г) в метаноле (600 мл) и ТГФ (300 мл) и реакционный раствор перемешивали при давлении водорода 0,9 МПа при 50°C-64°C в течение 6,5 часов. Реакционный раствор оставляли охлаждаться до комнатной температуры и затем фильтровали через целит. Полученный фильтрат концентрировали при пониженном давлении, с получением 134 г указанного в заголовке соединения. Характеристические значения соответствовали известным значениям (CAS #41608-64-4).
Синтез метил 4-формиламино-3-метоксибензоата
Уксусный ангидрид (268 мл) добавляли по каплям к муравьиной кислоте (401 мл) при комнатной температуре и реакционный раствор перемешивали при комнатной температуре в течение 40 минут. Раствор метил 4-амино-3-метоксибензоата (134 г) в ТГФ (600 мл) добавляли по каплям к реакционному раствору при комнатной температуре и реакционный раствор перемешивали в течение одного часа. Добавляли к реакционному раствору 3,8 л ледяной воды и выпавшее в осадок твердое вещество отфильтровывали и вновь промывали водой (2 л). Полученное твердое вещество сушили при 50°C в течение ночи, с получением 111 г указанного в заголовке соединения. Характеристические значения соответствовали известным значениям (CAS #700834-18-0).
Синтез метил 4-[формил-(2-оксопропил)амино]-3-метоксибензоата
Хлорацетон (84,5 мл) добавляли по каплям к смеси метил 4-формиламино-3-метоксибензоата (111 г), карбоната цезия (346 г) и йодида калия (8,78 г) в ДМФА (497 мл) при комнатной температуре и реакционный раствор перемешивали в течение трех часов. Карбонат цезия (173 г) и хлорацетон (42,0 мл) добавляли к реакционному раствору, который затем перемешивали при комнатной температуре в течение двух часов. Ледяную воду и этилацетат добавляли к реакционному раствору и органический слой отделяли. Этилацетат добавляли к водному слою и органический слой отделяли. Органические слои объединяли и промывали водой и насыщенным раствором соли в указанном порядке. Полученные органические слои сушили над безводным сульфатом магния и затем концентрировали при пониженном давлении. Остаток разбавляли толуолом и раствор концентрировали при пониженном давлении. трет-Бутилметиловый эфир и гептан добавляли к полученному остатку, выпавшее в осадок твердое вещество отделяли фильтрованием и промывали раствором 50% трет-бутилметилового эфира в гептане. Полученное твердое вещество сушили на воздухе в течение ночи, с получением 118 г указанного в заголовке соединения.
1H-ЯМР (CDCl3) δ (м.д.): 2,19 (с, 3H), 3,91 (с, 3H), 3,94 (с, 3H), 4,49 (с, 2H), 7,31 (д, J=8,0 Гц, 1H), 7,63 (д, J=2,0 Гц, 1H), 7,69 (дд, J=8,0, 2,0 Гц, 1H), 8,33 (с, 1H).
Синтез метил 3-метокси-4-(4-метил-1H-имидазол-1-ил)бензоата
Раствор метил 4-[формил-(2-оксопропил)амино]-3-метоксибензоата (118 г) и ацетата аммония (172 г) в уксусной кислоте (255 мл) нагревали и перемешивали при 140°C в течение одного часа. По окончании реакции реакционный раствор нейтрализовали водным аммиаком при охлаждении льдом. Этилацетат добавляли к реакционному раствору и органический слой отделяли. Полученный органический слой сушили над безводным сульфатом магния, затем фильтровали на рыхлом слое силикагеля и фильтрат концентрировали при пониженном давлении. трет-Бутилметиловый эфир и гептан добавляли к остатку, выпавшее в осадок твердое вещество отделяли фильтрованием и промывали раствором 50% трет-бутилметилового эфира в гептане. Полученное твердое вещество сушили на воздухе в течение ночи, с получением 68,4 г указанного в заголовке соединения. Далее, кристаллизационный маточный раствор концентрировали при пониженном давлении и остаток очищали хроматографией на колонке с силикагелем (элюирующий растворитель: система гептан-этилацетат), с получением 22,3 г указанного в заголовке соединения.
1H-ЯМР (CDCl3) δ (м.д.): 2,30 (с, 3H), 3,94 (с, 3H), 3,96 (с, 3H), 6,98 (ушир.с, 1H), 7,32 (д, J=8,4 Гц, 1H), 7,71-7,73 (м, 2H), 7,79 (ушир.с, 1H).
Синтез 3-метокси-4-(4-метил-1H-имидазол-1-ил)бензальдегида
Раствор пирролидина (18 мл) в ТГФ (45 мл) добавляли по каплям к раствору бис(2-метоксиэтокси)алюмогидрида натрия (65% раствор в толуоле, 56 мл) в ТГФ (60 мл) при -5°C или ниже в течение 15 минут. Реакционный раствор перемешивали при комнатной температуре в течение одного часа. Затем суспензию трет-бутоксида (2,10 г) в ТГФ (15 мл) добавляли по каплям к реакционному раствору при комнатной температуре и реакционный раствор перемешивали в течение 15 минут. Полученный реакционный раствор добавляли по каплям к раствору метил 3-метокси-4-(4-метил-1H-имидазол-1-ил)бензоата (20 г) в ТГФ (50 мл) при охлаждении льдом в течение 30 минут. Реакционный раствор перемешивали при комнатной температуре в течение двух часов и затем добавляли к нему по каплям 5н. раствор гидроксида натрия (150 мл). Этилацетат добавляли к реакционному раствору и органический слой отделяли. Органический слой промывали насыщенным раствором аммонийхлорида и насыщенным раствором соли в указанном порядке. Органический слой сушили над безводным сульфатом магния, фильтровали на рыхлом слое силикагеля и затем фильтрат концентрировали при пониженном давлении. Остаток разбавляли этилацетатом и выпавшее в осадок твердое вещество отделяли фильтрованием. Полученное твердое вещество сушили на воздухе в течение ночи, с получением 7,10 г указанного в заголовке соединения. Далее, кристаллизационный маточный раствор концентрировали при пониженном давлении и остаток очищали хроматографией на колонке с силикагелем (элюирующий растворитель: система гептан-этилацетат-2-пропанол), с получением 2,65 г указанного в заголовке соединения.
1H-ЯМР (CDCl3) δ (м.д.): 2,31 (с, 3H), 3,97 (с, 3H), 7,02 (ушир.с, 1H), 7,44 (д, J=8,0 Гц, 1H), 7,55 (дд, J=1,6, 8,0 Гц, 1H), 7,58 (д, J=1,6 Гц, 1H), 7,84 (ушир.с, 1H), 10,00 (с, 1H).
Синтез 2-[(3,4,5-трифторбензил)амино]этанола
Триацетоксиборогидрид натрия (14,1 г) добавляли к раствору 3,4,5-трифторбензальдегида (5,0 мл), этаноламина (3,52 г) и уксусной кислоты (10,1 мл) в ТГФ (100 мл) при охлаждении льдом и реакционный раствор перемешивали при комнатной температуре в течение четырех часов и 30 минут. Ледяную воду добавляли к реакционному раствору. Реакционный раствор доводили до pH 7-8 5н. раствором гидроксида натрия и насыщенным раствором бикарбоната натрия и затем экстрагировали хлороформом. Органический слой сушили над безводным сульфатом магния, затем фильтровали и маточный раствор концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с использованием силикагеля (хлороформ:метанол=1:100-1:5), с получением 6,91 г указанного в заголовке соединения.
1H-ЯМР (CDCl3) δ (м.д.): 2,80 (т, J=4,8 Гц, 2H), 3,69 (т, J=4,8 Гц, 2H), 3,78 (с, 2H), 6,96-7,00 (м, 2H).
Синтез 4-(3,4,5-трифторбензил)морфолин-2,3-диона
Смесь 2-[(3,4,5-трифторбензил)амино]этанола (6,91 г) и диэтилоксалата (20 мл) перемешивали при 170°C в течение одного часа. Реакционный раствор концентрировали при пониженном давлении и затем добавляли к остатку диэтиловый эфир. Выпавшие в осадок кристаллы отделяли фильтрованием и затем сушили на воздухе, с получением 7,38 г указанного в заголовке соединения.
1H-ЯМР (CDCl3) δ (м.д.): 3,61 (т, J=4,8 Гц, 2H), 4,49 (т, J=4,8 Гц, 2H), 4,63 (с, 2H), 6,95-6,99 (м, 2H).
Синтез 2-гидрокси-4-(3,4,5-трифторбензил)морфолин-3-она
1М раствор три-втор-бутилборогидрида лития в ТГФ (31,4 мл) добавляли по каплям к раствору 4-(3,4,5-трифторбензил)морфолин-2,3-диона (7,38 г) в ТГФ при -15°C и реакционный раствор перемешивали в течение двух часов. 5н. Раствор гидроксида натрия (2,85 мл) и 30% водный пероксид водорода (968 мкл) добавляли по каплям к реакционному раствору при 20°C или ниже, который затем перемешивали при 10°C в течение одного часа. Бисульфит натрия (888 мг) добавляли к реакционному раствору, который затем перемешивали в течение 30 минут. Насыщенный раствор соли и хлороформ добавляли к реакционному раствору и органический слой отделяли. Органический слой сушили над безводным сульфатом магния и затем концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с использованием силикагеля (гептан:этилацетат=1:1-0:100), с получением 3,94 г указанного в заголовке соединения.
1H-ЯМР (CDCl3) δ (м.д.): 3,11-3,16 (м, 1H), 3,47-3,54 (м, 1H), 3,80-3,86 (м, 1H), 4,28-4,35 (м, 1H), 4,40 (д, J=14,8 Гц, 1H), 4,67 (д, J=14,8 Гц, 1H), 5,37 (с, 1H), 6,90-6,94 (м, 2H).
Синтез (Z)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-(3,4,5-трифторбензил)морфолин-3-она
Тионилхлорид (16,1 мл) добавляли к раствору 2-гидрокси-4-(3,4,5-трифторбензил)морфолин-3-она (3,94 г) в метиленхлориде и реакционный раствор перемешивали при 50°C в течение одного часа. Реакционный раствор концентрировали при пониженном давлении и остаток разбавляли метиленхлоридом. Затем трифенилфосфин (5,2 г) добавляли при охлаждении льдом и реакционный раствор перемешивали при комнатной температуре в течение 4,5 часов. Реакционный раствор концентрировали при пониженном давлении. Этанол (64,6 мл), TEA (4,2 мл) и 3-метокси-4-(4-метил-1H-имидазол-1-ил)бензальдегид (2,72 г) добавляли к остатку и реакционный раствор нагревали при кипении с обратным холодильником в течение двух часов. Реакционный раствор концентрировали при пониженном давлении и остаток разбавляли 2н. водной хлористо-водородной кислотой и этилацетатом. Затем отделяли водный слой. Органический слой промывали 2н. водной хлористо-водородной кислотой. Затем все водные слои объединяли и подщелачивали концентрированным раствором гидроксида натрия. Органический слой отделяли экстракцией из щелочного раствора хлороформом, затем сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с использованием NH силикагеля (гептан:этилацетат=1:1-0:100), с получением 1,92 г указанного в заголовке соединения.
1H-ЯМР (CDCl3) δ (м.д.): 2,34 (с, 3H), 3,56 (т, J=4,8 Гц, 2H), 3,87 (с, 3H), 4,28 (т, J=4,8 Гц, 2H), 4,66 (с, 2H), 6,93 (с, 1H), 6,95-6,99 (м, 3H), 7,23 (д, J=8,0 Гц, 1H), 7,40 (дд, J=8,0, 1,2 Гц, 1H), 7,42 (д, J=1,2 Гц, 1H), 7,85 (с, 1H).
ESI-МС; m/z 444[M++H].
Пример 2
Синтез (Z)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-(2,3,4-трифторбензил)морфолин-3-она
[Формула 24]

Синтез 2-[(2,3,4-трифторбензил)амино]этанола
891 мг указанного в заголовке соединения получали из 2,3,4-трифторбензальдегида (1,0 г), этаноламина (573 мг), уксусной кислоты (1,79 мл) и триацетоксиборогидрида натрия (2,65 г) по аналогичной методике примера 1.
1H-ЯМР (CDCl3) δ (м.д.): 2,80 (т, J=5,2 Гц, 2H), 3,69 (т, J=5,2 Гц, 2H), 3,88 (с, 2H), 6,94-6,96 (м, 1H), 7,07-7,09 (м, 1H).
Синтез 4-(2,3,4-трифторбензил)морфолин-2,3-диона
903 мг указанного в заголовке соединения получали из 2-[(2,3,4-трифторбензил)амино]этанола (891 мг) и диэтилоксалата (8,0 мл) по аналогичной методике примера 1.
1H-ЯМР (CDCl3) δ (м.д.): 3,70 (т, J=5,2 Гц, 2H), 4,50 (т, J=5,2 Гц, 2H), 4,73 (с, 2H), 6,97-7,04 (м, 1H), 7,18-7,25 (м, 1H).
Синтез 2-гидрокси-4-(2,3,4-трифторбензил)морфолин-3-она
126 мг указанного в заголовке соединения получали из 4-(2,3,4-трифторбензил)морфолин-2,3-диона (350 мг) и 1М раствора три-втор-бутилборогидрида лития в ТГФ (1,49 мл) по аналогичной методике примера 1.
1H-ЯМР (CDCl3) δ (м.д.): 3,20-3,25 (м, 1H), 3,53-3,59 (м, 1H), 3,81-3,86 (м, 1H), 4,26-4,33 (м, 1H), 4,60 (д, J=15,2 Гц, 1H), 4,67 (д, J=15,2 Гц, 1H), 5,31 (с, 1H), 6,96-7,01 (м, 1H), 7,13-7,15 (м, 1H).
Синтез (Z)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-(2,3,4-трифторбензил)морфолин-3-она
95,8 мг указанного в заголовке соединения получали из 2-гидрокси-4-(2,3,4-трифторбензил)морфолин-3-она (126 мг), тионилхлорида (516 мкл), трифенилфосфина (166 мг) и 3-метокси-4-(4-метил-1H-имидазол-1-ил)бензальдегида (93,9 мг) по аналогичной методике примера 1.
1H-ЯМР (CDCl3) δ (м.д.): 2,35 (с, 3H), 3,64 (т, J=4,8 Гц, 2H), 3,86 (с, 3H), 4,28 (т, J=4,8 Гц, 2H), 4,75 (с, 2H), 6,89 (с, 1H), 6,95 (с, 1H), 6,97-7,02 (м, 1H), 7,17-7,24 (м, 2H), 7,38 (дд, J=8,4, 1,2 Гц, 1H), 7,41 (д, J=1,2 Гц, 1H), 7,88 (с, 1H).
ESI-МС; m/z 444[M++H].
Пример 3
Синтез (Z)-(S)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метил-4-(3,4,5-трифторбензил)морфолин-3-она
[Формула 25]

Синтез (S)-1-(3,4,5-трифторбензиламино)пропан-2-ола
410 мг указанного в заголовке соединения получали из 3,4,5-трифторбензальдегида (370 мг), (S)-1-амино-2-пропанола (260 мг), уксусной кислоты (0,662 мл) и триацетоксиборогидрида натрия (981 мг) по аналогичной методике примера 1.
1H-ЯМР (CDCl3) δ (м.д.): 1,17 (д, J=6,4 Гц, 3H), 2,45 (дд, J=12,0, 9,2 Гц, 1H), 2,72 (дд, J=12,0, 2,8 Гц, 1H), 3,75 (д, J=13,2 Гц, 1H), 3,80 (д, J=13,2 Гц, 1H), 3,82-3,85 (м, 1H), 6,96-7,00 (м, 2H).
Синтез (S)-6-метил-4-(3,4,5-трифторбензил)морфолин-2,3-диона
439 мг указанного в заголовке соединения получали из (S)-1-(3,4,5-трифторбензиламино)пропан-2-ола (410 мг) и диэтилоксалата (2,0 мл) по аналогичной методике примера 1.
1H-ЯМР (CDCl3) δ (м.д.): 1,44 (д, J=6,4 Гц, 3H), 3,35 (дд, J=13,6, 3,2 Гц, 1H), 3,55 (дд, J=13,6, 9,6 Гц, 1H), 4,55 (д, J=15,2 Гц, 1H), 4,67 (д, J=15,2 Гц, 1H), 4,73-4,78 (м, 1H), 6,94-6,98 (м, 2H).
Синтез (S)-2-гидрокси-6-метил-4-(3,4,5-трифторбензил)морфолин-3-она
308 мг указанного в заголовке соединения получали из (S)-6-метил-4-(3,4,5-трифторбензил)морфолин-2,3-диона (400 мг) и 1М раствора три-втор-бутилборогидрида лития в ТГФ (1,70 мл) по аналогичной методике примера 1.
1H-ЯМР (CDCl3) δ (м.д.): 1,26 (д, J=6,0 Гц, 3H), 3,06 (дд, J=12,0, 3,2 Гц, 1H), 3,22 (дд, J=12,0, 12,0 Гц, 1H), 4,36 (д, J=14,8 Гц, 1H), 4,46-4,52 (м, 1H), 4,66 (д, J=14,8 Гц, 1H), 5,37 (с, 1H), 6,90-6,94 (м, 2H).
Синтез (Z)-(S)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метил-4-(3,4,5-трифторбензил)морфолин-3-она
339 мг указанного в заголовке соединения получали из (S)-2-гидрокси-6-метил-4-(3,4,5-трифторбензил)морфолин-3-она (308 мг), тионилхлорида (817 мкл), трифенилфосфина (353 мг) и 3-метокси-4-(4-метил-1H-имидазол-1-ил)бензальдегида (218 мг) по аналогичной методике примера 1.
1H-ЯМР (CDCl3) δ (м.д.): 1,46 (д, J=6,4 Гц, 3H), 2,34 (с, 3H), 3,28 (дд, J=12,8, 2,8 Гц, 1H), 3,50 (дд, J=12,8, 9,6 Гц, 1H), 3,87 (с, 3H), 4,36-4,40 (м, 1H), 4,58 (д, J=14,8 Гц, 1H), 4,69 (д, J=14,8 Гц, 1H), 6,90 (с, 1H), 6,94-6,98 (м, 3H), 7,23 (д, J=8,4 Гц, 1H), 7,37 (дд, J=8,4, 2,0 Гц, 1H), 7,54 (д, J=2,0 Гц, 1H), 7,85 (с, 1H).
ESI-МС; m/z 458[M++H].
Пример 4
Синтез (Z)-(R)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метил-4-(3,4,5-трифторбензил)морфолин-3-она
[Формула 26]

Синтез (R)-1-(3,4,5-трифторбензиламино)пропан-2-ола
1,1 г указанного в заголовке соединения получали из 3,4,5-трифторбензальдегида (1,0 г), (R)-1-амино-2-пропанола (704 мг), уксусной кислоты (1,79 мл) и триацетоксиборогидрида натрия (2,65 г) по аналогичной методике примера 1. Значения ЯМР данного соединения соответствовали значениям S-изомера.
Синтез (R)-6-метил-4-(3,4,5-трифторбензил)морфолин-2,3-диона
1,15 г указанного в заголовке соединения получали из (R)-1-(3,4,5-трифторбензиламино)пропан-2-ола (1,1 г) и диэтилоксалата (4,0 мл) по аналогичной методике примера 1. Значения ЯМР данного соединения соответствовали значениям S-изомера.
Синтез (R)-2-гидрокси-6-метил-4-(3,4,5-трифторбензил)морфолин-3-она
323 мг указанного в заголовке соединения получали из (R)-6-метил-4-(3,4,5-трифторбензил)морфолин-2,3-диона (400 мг) и 1М раствора три-втор-бутилборогидрида лития в ТГФ (1,70 мл) по аналогичной методике примера 1. Значения ЯМР данного соединения соответствовали значениям S-изомера.
Синтез (Z)-(R)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метил-4-(3,4,5-трифторбензил)морфолин-3-она
346 мг указанного в заголовке соединения получали из (R)-2-гидрокси-6-метил-4-(3,4,5-трифторбензил)морфолин-3-она (323 мг), тионилхлорида (853 мкл), трифенилфосфина (368 мг) и 3-метокси-4-(4-метил-1H-имидазол-1-ил)бензальдегида (228 мг) по аналогичной методике примера 1. Значения ЯМР данного соединения соответствовали значениям S-изомера.
Пример 5
Синтез (Z)-(S)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метил-4-(2,3,4-трифторбензил)морфолин-3-она
[Формула 27]

Синтез (S)-1-(2,3,4-трифторбензиламино)пропан-2-ола
968 мг указанного в заголовке соединения получали из 2,3,4-трифторбензальдегида (1,0 г), (S)-1-амино-2-пропанола (704 мг), уксусной кислоты (1,79 мл) и триацетоксиборогидрида натрия (2,65 г) по аналогичной методике примера 1.
1H-ЯМР (CDCl3) δ (м.д.): 1,16 (д, J=6,0 Гц, 3H), 2,47 (дд, J=11,6, 9,2 Гц, 1H), 2,72 (дд, J=11,6, 2,8 Гц, 1H), 3,83-3,88 (м, 1H), 3,89 (с, 2H), 6,92-6,99 (м, 1H), 7,06-7,10 (м, 1H).
Синтез (S)-6-метил-4-(2,3,4-трифторбензил)морфолин-2,3-диона
917 мг указанного в заголовке соединения получали из (S)-1-(2,3,4-трифторбензиламино)пропан-2-ола (968 мг) и диэтилоксалата (8,0 мл) по аналогичной методике примера 1.
1H-ЯМР (CDCl3) δ (м.д.): 1,45 (д, J=6,4 Гц, 3H), 3,48 (дд, J=13,6, 3,2 Гц, 1H), 3,62 (дд, J=13,6, 10,0 Гц, 1H), 4,66 (д, J=15,2 Гц, 1H), 4,74-4,80 (м, 1H), 4,75 (д, J=15,2 Гц, 1H), 7,00-7,03 (м, 1H), 7,21-7,27 (м, 1H).
Синтез (S)-2-гидрокси-6-метил-4-(2,3,4-трифторбензил)морфолин-3-она
196 мг указанного в заголовке соединения получали из (S)-6-метил-4-(2,3,4-трифторбензил)морфолин-2,3-диона (350 мг) и 1М раствора три-втор-бутилборогидрида лития в ТГФ (1,49 мл) по аналогичной методике примера 1.
1H-ЯМР (CDCl3) δ (м.д.): 1,25 (д, J=7,2 Гц, 3H), 3,13 (дд, J=12,0, 3,2 Гц, 1H), 3,26 (дд, J=12,0, 12,0 Гц, 1H), 4,47-4,51 (м, 1H), 4,58 (д, J=15,6 Гц, 1H), 4,64 (д, J=15,6 Гц, 1H), 5,33 (с, 1H), 6,95-7,00 (м, 1H), 7,12-7,15 (м, 1H).
Синтез (Z)-(S)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метил-4-(2,3,4-трифторбензил)морфолин-3-она
197 мг указанного в заголовке соединения получали из (S)-2-гидрокси-6-метил-4-(2,3,4-трифторбензил)морфолин-3-она (196 мг), тионилхлорида (500 мкл), трифенилфосфина (243 мг) и 3-метокси-4-(4-метил-1H-имидазол-1-ил)бензальдегида (139 мг) по аналогичной методике примера 1.
1H-ЯМР (CDCl3) δ (м.д.): 1,46 (д, J=6,4 Гц, 3H), 2,31 (с, 3H), 3,39 (дд, J=12,8, 2,8 Гц, 1H), 3,55 (дд, J=12,8, 9,6 Гц, 1H), 3,85 (с, 3H), 4,37-4,40 (м, 1H), 4,68 (д, J=15,2 Гц, 1H), 4,77 (д, J=15,2 Гц, 1H), 6,86 (с, 1H), 6,93 (с, 1H), 6,94-7,03 (м, 1H), 7,16-7,24 (м, 1H), 7,21 (д, J=8,4 Гц, 1H), 7,33 (дд, J=8,4, 2,0 Гц, 1H), 7,52 (д, J=2,0 Гц, 1H), 7,75 (с, 1H).
ESI-МС; m/z 458[M++H].
Пример 6
Синтез (Z)-(R)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метил-4-(2,3,4-трифторбензил)морфолин-3-она
[Формула 28]
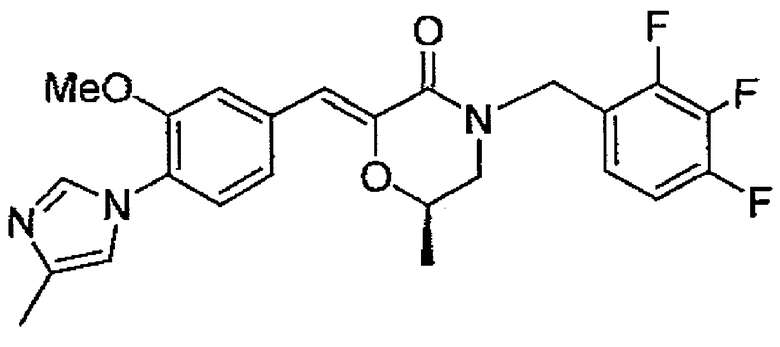
Синтез (R)-1-(2,3,4-трифторбензиламино)пропан-2-ола
1,09 г указанного в заголовке соединения получали из 2,3,4-трифторбензальдегида (1,0 г), (R)-1-амино-2-пропанола (704 мг), уксусной кислоты (1,79 мл) и триацетоксиборогидрида натрия (2,65 г) по аналогичной методике примера 1. Значения ЯМР данного соединения соответствовали значениям S-изомера.
Синтез (R)-6-метил-4-(2,3,4-трифторбензил)морфолин-2,3-диона
874 мг указанного в заголовке соединения получали из (R)-1-(2,3,4-трифторбензиламино)пропан-2-ола (1,09 г) и диэтилоксалата (8,0 мл) по аналогичной методике примера 1. Значения ЯМР данного соединения соответствовали значениям S-изомера.
Синтез (R)-2-гидрокси-6-метил-4-(2,3,4-трифторбензил)морфолин-3-она
213 мг указанного в заголовке соединения получали из (R)-6-метил-4-(2,3,4-трифторбензил)морфолин-2,3-диона (350 мг) и 1М раствора три-втор-бутилборогидрида лития в ТГФ (1,49 мл) по аналогичной методике примера 1. Значения ЯМР данного соединения соответствовали значениям S-изомера.
Синтез (Z)-(R)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метил-4-(2,3,4-трифторбензил)морфолин-3-она
187 мг указанного в заголовке соединения получали из (R)-2-гидрокси-6-метил-4-(2,3,4-трифторбензил)морфолин-3-она (213 мг), тионилхлорида (500 мкл), трифенилфосфина (264 мг) и 3-метокси-4-(4-метил-1H-имидазол-1-ил)бензальдегида (151 мг) по аналогичной методике примера 1. Значения ЯМР данного соединения соответствовали значениям S-изомера.
Пример 7
Синтез (Z)-4-[(S)-1-(4-фторфенил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-она
[Формула 29]

Синтез 1-[(S)-1-(4-фторфенил)этиламино]-2-метилпропан-2-ола
Изобутиленоксид (1,0 г) и (S)-1-(4-фторфенил)этиламин (2,25 мл) добавляли к раствору перхлората лития (14,8 г) в эфире (27,8 мл) при комнатной температуре и реакционный раствор перемешивали при комнатной температуре в течение 1,5 часов. Изобутиленоксид (0,5 мл) добавляли к реакционному раствору, который затем перемешивали в течение ночи. Ледяную воду и хлороформ добавляли к реакционному раствору и органический слой отделяли. Затем органический слой сушили над безводным сульфатом магния и затем концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с использованием силикагеля (хлороформ:2-пропанол=100:1-1:1), с получением 2,13 г указанного в заголовке соединения.
1H-ЯМР (CDCl3) δ (м.д.): 1,13 (с, 3H), 1,16 (с, 3H), 1,35 (д, J=6,8 Гц, 3H), 2,32 (д, J=11,6 Гц, 1H), 2,44 (д, J=11,6 Гц, 1H), 3,75 (кв, J=6,8 Гц, 1H), 6,99-7,10 (м, 2H), 7,23-7,30 (м, 2H).
Синтез 4-[(S)-1-(4-фторфенил)этил]-6,6-диметилморфолин-2,3-диона
1,44 г указанного в заголовке соединения получали из 1-[(S)-1-(4-фторфенил)этиламино]-2-метилпропан-2-ола (2,13 г) и диэтилоксалата (7,0 мл) по аналогичной методике примера 1.
1H-ЯМР (CDCl3) δ (м.д.): 1,19 (с, 3H), 1,44 (с, 3H), 1,56 (д, J=6,8 Гц, 3H), 3,00 (д, J=13,6 Гц, 1H), 3,31 (д, J=13,6 Гц, 1H), 6,02 (кв, J=6,8 Гц, 1H), 7,06-7,10 (м, 2H), 7,30-7,36 (м, 2H).
Синтез 4-[(S)-1-(4-фторфенил)этил]-2-гидрокси-6,6-диметилморфолин-3-она
1,22 г указанного в заголовке соединения получали из 4-[(S)-1-(4-фторфенил)этил]-6,6-диметилморфолин-2,3-диона (1,20 г) и 1М раствора три-втор-бутилборогидрида лития в ТГФ (4,97 мл) по аналогичной методике примера 1.
1H-ЯМР (CDCl3) δ (м.д.): 0,97 (с, 1,5H), 1,08 (с, 1,5H), 1,24 (с, 1,5H), 1,31 (с, 1,5H), 1,52 (д, J=6,8 Гц, 1,5H), 1,53 (д, J=6,8 Гц, 1,5H), 2,05 (с, 3H), 2,79 (д, J=12,8 Гц, 0,5H), 2,87 (д, J=12,8 Гц, 0,5H), 3,08 (д, J=12,8 Гц, 0,5H), 3,13 (д, J=12,8 Гц, 0,5H), 3,77 (ушир.с, 1H), 5,26 (д, J=4,0 Гц, 0,5H), 5,29 (д, J=4,0 Гц, 0,5H), 5,93 (кв, J=6,8 Гц, 0,5H), 5,99 (кв, J=6,8 Гц, 0,5H), 7,03-7,07 (м, 2H), 7,26-7,35 (м, 2H).
Синтез (Z)-4-[(S)-1-(4-фторфенил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-она
500 мг указанного в заголовке соединения получали из 4-[(S)-1-(4-фторфенил)этил]-2-гидрокси-6,6-диметилморфолин-3-она (1,21 г), тионилхлорида (3,3 мл), трифенилфосфина (1,42 г) и 3-метокси-4-(4-метил-1H-имидазол-1-ил)бензальдегида (880 мг) по аналогичной методике примера 1.
1H-ЯМР (CDCl3) δ (м.д.): 1,35 (д, J=6,8 Гц, 3H), 1,57 (д, J=7,2 Гц, 3H), 2,30 (с, 3H), 2,89 (дд, J=12,8, 9,2 Гц, 1H), 3,18 (дд, J=12,8, 2,8 Гц, 1H), 3,85 (с, 3H), 4,31-4,36 (м, 1H), 6,11 (кв, J=7,2 Гц, 1H), 6,88 (с, 1H), 6,93 (с, 1H), 7,03-7,08 (м, 2H), 7,20 (д, J=8,0 Гц, 1H), 7,29-7,35 (м, 3H), 7,52 (д, J=2,0 Гц, 1H), 7,75 (с, 1H).
ESI-МС; m/z 450[M++H].
Примеры 8 и 9
Синтез (Z)-(R)-4-[(S)-1-(4-фторфенил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она и (Z)-(S)-4-[(S)-1-(4-фторфенил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она
[Формула 30]

Синтез 1-[(S)-1-(4-фторфенил)этиламино]пропан-2-она
Смесь (S)-1-(4-фторфенил)этиламина (5,0 г), хлорацетона (4,78 мл), карбоната цезия (13,9 г) и ДМФА (50 мл) перемешивали при комнатной температуре в течение ночи. Реакционный раствор разбавляли водой и этилацетатом и затем органический слой отделяли. Органический слой сушили над безводным сульфатом магния и затем концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с использованием силикагеля (гексан:этилацетат=5:1-0:100), с получением 5,1 г указанного в заголовке соединения.
1H-ЯМР (CDCl3) δ (м.д.): 1,37 (д, J=6,8 Гц, 3H), 2,07 (с, 3H), 3,37 (с, 2H), 3,74 (кв, J=6,8 Гц, 1H), 6,97-7,03 (м, 2H), 7,24-7,29 (м, 2H).
ESI-МС; m/z 196[M++H].
Синтез 1-[(S)-1-(4-фторфенил)этиламино]пропан-2-ола
Борогидрид натрия (2,39 г) добавляли к раствору 1-[(S)-1-(4-фторфенил)этиламино]пропан-2-она (2,5 г) в этаноле (25 мл) при охлаждении льдом и затем реакционный раствор перемешивали при комнатной температуре в течение одного часа. Реакционный раствор разбавляли ледяной водой и этилацетатом и затем органический слой отделяли. Органический слой сушили над безводным сульфатом магния и затем концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с использованием силикагеля (хлороформ:2-пропанол=100:1-0:100), с получением 1,18 г указанного в заголовке соединения в виде смеси диастереомеров.
1H-ЯМР (CDCl3) δ (м.д.): 1,09 (д, J=6,4 Гц, 0,9H), 1,10 (д, J=6,0 Гц, 2,1H), 1,35 (д, J=7,2 Гц, 0,9H), 1,36 (д, J=6,4 Гц, 2,1H), 2,22 (дд, J=12,0, 9,6 Гц, 0,3H), 2,33 (дд, J=12,0, 9,2 Гц, 0,7H), 2,52 (дд, J=12,4, 3,6 Гц, 0,7H), 2,59 (дд, J=11,6, 2,8 Гц, 0,3H), 3,61-3,66 (м, 0,3H), 3,74-3,80 (м, 0,7H), 6,99-7,03 (м, 2H), 7,24-7,29 (м, 2H).
Синтез 4-[(S)-1-(4-фторфенил)этил]-6-метилморфолин-2,3-диона
1,20 г указанного в заголовке соединения получали в виде смеси диастереомеров из 1-[(S)-1-(4-фторфенил)этиламино]пропан-2-ола (1,18 г) и диэтилоксалата (4,06 мл) по аналогичной методике примера 1.
1H-ЯМР (CDCl3) δ (м.д.): 1,31 (д, J=6,8 Гц, 1,8H), 1,37 (д, J=6,8 Гц, 1,2H), 1,55 (д, J=6,8 Гц, 1,2H), 1,56 (д, J=6,8 Гц, 1,8H), 2,96 (дд, J=12,0, 9,6 Гц, 0,6H), 3,04 (дд, J=12,0, 3,6 Гц, 0,4H), 3,26 (дд, J=12,0, 3,6 Гц, 0,6H), 3,38 (дд, J=12,0, 9,6 Гц, 0,4H), 4,42-4,52 (м, 0,4H), 4,64-4,74 (м, 0,6H), 5,93-6,02 (м, 1H), 7,09-7,12 (м, 2H), 7,29-7,39 (м, 2H).
Синтез 4-[(S)-1-(4-фторфенил)этил]-2-гидрокси-6-метилморфолин-3-она
382 мг указанного в заголовке соединения получали в виде смеси диастереомеров из 4-[(S)-1-(4-фторфенил)этил]-6-метилморфолин-2,3-диона (500 мг) и 1М раствора три-втор-бутилборогидрида лития в ТГФ (2,19 мл) по аналогичной методике примера 1.
1H-ЯМР (CDCl3) δ (м.д.): 1,19 (д, J=6,8 Гц, 1,5H), 1,20 (д, J=6,8 Гц, 1,5H), 1,53 (д, J=6,8 Гц, 3H), 2,61 (дд, J=12,4, 10,8 Гц, 0,5H), 2,74 (дд, J=12,0, 2,8 Гц, 0,5H), 2,94 (дд, J=12,4, 2,8 Гц, 0,5H), 3,12 (дд, J=12,0, 11,2 Гц, 0,5H), 4,11-4,26 (м, 0,5H), 4,37-4,42 (м, 0,5H), 5,35 (с, 0,5H), 5,37 (с, 0,5H), 5,95 (кв, J=6,8 Гц, 0,5H), 5,99 (кв, J=6,8 Гц, 0,5H), 7,02-7,07 (м, 2H), 7,25-7,32 (м, 2H).
Синтез (Z)-(R)-4-[(S)-1-(4-фторфенил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она и (Z)-(S)-4-[(S)-1-(4-фторфенил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она
628 мг указанного в заголовке соединения получали в виде смеси диастереомеров из 4-[(S)-1-(4-фторфенил)этил]-2-гидрокси-6-метилморфолин-3-она (382 мг), тионилхлорида (330 мкл), трифенилфосфина (504 мг) и 3-метокси-4-(4-метил-1H-имидазол-1-ил)бензальдегида (294 мг) по аналогичной методике примера 1. Часть смеси диастереомеров разделяли с помощью CHIRALCELTM OJ-H производства ф. Daicel Chemical Industries, Ltd. (2 см×25 см; подвижная фаза: гексан:этанол=80:20), с получением указанного в заголовке оптически активного соединения со временем удерживания 25 минут (>95% de) и указанного в заголовке оптически активного соединения со временем удерживания 29 минут (>95% de).
Характеристические значения указанного в заголовке оптически активного соединения со временем удерживания 25 минут (пример 8) являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,38 (д, J=6,4 Гц, 3H), 1,55 (д, J=7,2 Гц, 3H), 2,30 (с, 3H), 2,97 (дд, J=12,8, 2,4 Гц, 1H), 3,33 (дд, J=12,8, 9,6 Гц, 1H), 3,85 (с, 3H), 4,09-4,12 (м, 1H), 6,13 (кв, J=7,2 Гц, 1H), 6,89 (с, 1H), 6,94 (с, 1H), 7,03-7,09 (м, 2H), 7,21 (д, J=8,4 Гц, 1H), 7,32-7,36 (м, 3H), 7,53 (д, J=2,8 Гц, 1H), 7,74 (с, 1H).
ESI-МС; m/z 436[M++H].
Характеристические значения указанного в заголовке оптически активного соединения со временем удерживания 29 минут (пример 9) являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,35 (д, J=6,8 Гц, 3H), 1,57 (д, J=7,2 Гц, 3H), 2,30 (с, 3H), 2,89 (дд, J=12,8, 9,2 Гц, 1H), 3,18 (дд, J=12,8, 2,8 Гц, 1H), 3,85 (с, 3H), 4,31-4,36 (м, 1H), 6,11 (кв, J=7,2 Гц, 1H), 6,88 (с, 1H), 6,93 (с, 1H), 7,03-7,08 (м, 2H), 7,20 (д, J=8,0 Гц, 1H), 7,29-7,35 (м, 3H), 7,52 (д, J=2,0 Гц, 1H), 7,75 (с, 1H).
ESI-МС; m/z 436[M++H].
Примеры 10 и 11
Синтез (Z)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-[(S)-1-(3,4,5-трифторфенил)этил]морфолин-3-она и (Z)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-[(R)-1-(3,4,5-трифторфенил)этил]морфолин-3-она
[Формула 31]
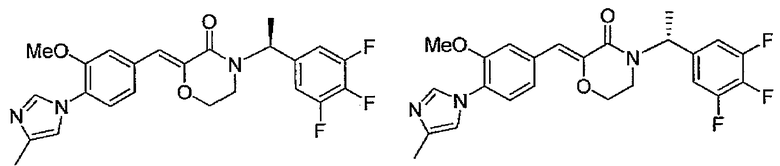
Синтез 2-[1-(3,4,5-трифторфенил)этиламино]этанола
Смесь 3,4,5-трифторацетофенона (2,0 г), этаноламина (2,0 г) и толуола (20 мл) нагревали при кипении с обратным холодильником в аппарате Дина-Старка в течение 2,5 часов. Реакционный раствор концентрировали при пониженном давлении, затем остаток разбавляли этанолом (30 мл) и добавляли при охлаждении льдом борогидрид натрия (1,0 г). Смесь перемешивали при комнатной температуре в течение трех часов и затем разбавляли 2н. раствором гидроксида натрия и хлороформом. Затем органический слой отделяли. Органический слой сушили над безводным сульфатом магния и затем концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с использованием силикагеля (хлороформ:метанол=50:1-5:1), с получением 860 мг указанного в заголовке соединения.
1H-ЯМР (CDCl3) δ (м.д.): 1,36 (д, J=6,8 Гц, 3H), 2,56-2,68 (м, 1H), 2,68-2,73 (м, 1H), 3,62-3,80 (м, 3H), 6,92-7,00 (м, 2H).
Синтез 4-[1-(3,4,5-трифторфенил)этил]морфолин-2,3-диона
340 мг указанного в заголовке соединения получали из 2-[1-(3,4,5-трифторфенил)этиламино]этанола (860 мг) и диэтилоксалата (5,0 мл) по аналогичной методике примера 1.
1H-ЯМР (CDCl3) δ (м.д.): 1,55 (д, J=6,4 Гц, 3H), 3,15-3,21 (м, 1H), 3,52-3,59 (м, 1H), 4,31-4,37 (м, 1H), 4,41-4,46 (м, 1H), 5,90 (кв, J=6,4 Гц, 1H), 6,97-7,01 (м, 2H).
Синтез 2-гидрокси-4-[1-(3,4,5-трифторфенил)этил]морфолин-3-она
273 мг указанного в заголовке соединения получали в виде смеси диастереомеров из 4-[1-(3,4,5-трифторфенил)этил]морфолин-2,3-диона (340 мг) и 1М раствора три-втор-бутилборогидрида лития в ТГФ (1,45 мл) по аналогичной методике примера 1.
1H-ЯМР (CDCl3) δ (м.д.): 1,52 (д, J=7,2 Гц, 3H), 2,78-2,83 (м, 0,5H), 2,95-3,03 (м, 0,5H), 3,10-3,15 (м, 0,5H), 3,43-3,50 (м, 0,5H), 3,78-3,84 (м, 0,5H), 4,12-4,18 (м, 0,5H), 4,22-4,28 (м, 0,5H), 4,24 (ушир.с, 1H), 5,34 (с, 0,5H), 5,36 (с, 0,5H), 5,88-5,98 (м, 1H), 6,92-6,99 (м, 1H).
Синтез (Z)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-[(S)-1-(3,4,5-трифторфенил)этил]морфолин-3-она и (Z)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-[(R)-1-(3,4,5-трифторфенил)этил]морфолин-3-она
145 мг указанного в заголовке соединения получали в виде рацемата из 2-гидрокси-4-[1-(3,4,5-трифторфенил)этил]морфолин-3-она (273 мг), тионилхлорида (1,12 мл), трифенилфосфина (360 мг) и 3-метокси-4-(4-метил-1H-имидазол-1-ил)бензальдегида (204 мг) по аналогичной методике примера 1.
1H-ЯМР (CDCl3) δ (м.д.): 1,55 (д, J=6,8 Гц, 3H), 2,29 (с, 3H), 3,08-3,13 (м, 1H), 3,48-3,55 (м, 1H), 3,85 (с, 3H), 4,08-4,14 (м, 1H), 4,23-4,27 (м, 1H), 6,06 (кв, J=6,8 Гц, 1H), 6,90 (с, 1H), 6,92 (с, 1H), 6,96-7,02 (м, 2H), 7,20 (д, J=8,0 Гц, 1H), 7,37 (дд, J=8,0, 1,6 Гц, 1H), 7,38 (д, J=1,6 Гц, 1H), 7,71 (с, 1H).
ESI-МС; m/z 458[M++H].
Часть рацемата разделяли с помощью CHIRALPAKTM IA производства ф. Daicel Chemical Industries, Ltd. (2 см×25 см; подвижная фаза: гексан:этанол=80:20), с получением указанного в заголовке оптически активного соединения со временем удерживания 21 минут (>99% ee: пример 11) и указанного в заголовке оптически активного соединения со временем удерживания 24 минут (95% ee: пример 10). Значения ЯМР данных оптически активных соединений соответствовали значениям ЯМР рацемата.
Пример 12
Синтез (Z)-4-[(S)-хроман-4-ил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-она
[Формула 32]
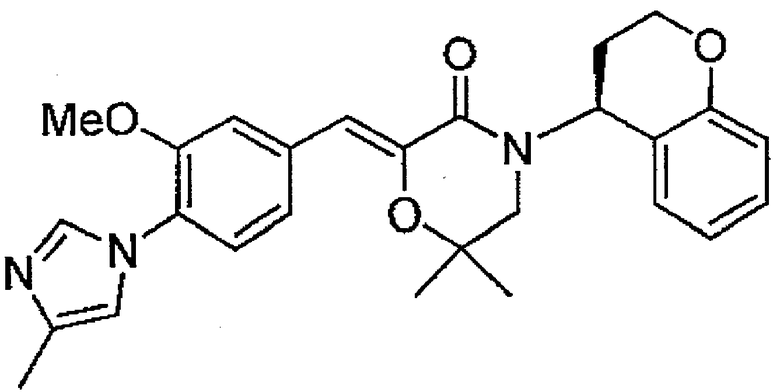
Синтез 1-[[(S)-хроман-4-ил]амино]-2-метилпропан-2-ола
5,62 г указанного в заголовке соединения получали из перхлората лития (29,6 г), эфира (55,6 мл), (S)-4-аминохромана (4,13 г), полученного способом, описанным в литературе (см., например, T. Mukaiyama et al., "A European Journal of Chemistry", 2003, vol.9, p.4485-4509), и изобутиленоксида (3,46 мл) по аналогичной методике примера 7.
1H-ЯМР (CDCl3) δ (м.д.): 1,20 (с, 6H), 1,93-1,98 (м, 1H), 2,04-2,09 (м, 1H), 2,69 (с, 2H), 3,80-3,85 (м, 1H), 4,19-4,32 (м, 2H), 6,83 (д, J=8,4 Гц, 1H), 6,91 (т, J=8,4 Гц, 1H), 7,17 (т, J=8,4 Гц, 1H), 7,33 (д, J=8,4 Гц, 1H).
Синтез 4-[(S)-хроман-4-ил]-6,6-диметилморфолин-2,3-диона
1,53 г указанного в заголовке соединения получали из 1-[[(S)-хроман-4-ил]амино]-2-метилпропан-2-ола (5,62 г) и диэтилоксалата (20 мл) по аналогичной методике примера 7.
1H-ЯМР (CDCl3) δ (м.д.): 1,45 (с, 3H), 1,48 (с, 3H), 2,10-2,17 (м, 1H), 2,23-2,27 (м, 1H), 3,23 (с, 2H), 4,18-4,30 (м, 2H), 5,96 (дд, J=8,4, 7,2 Гц, 1H), 6,90 (д, J=8,4 Гц, 1H), 6,95 (т, J=8,4 Гц, 1H), 7,05 (д, J=8,4 Гц, 1H), 7,23 (т, J=8,4 Гц, 1H).
Синтез 4-[(S)-хроман-4-ил]-2-гидрокси-6,6-диметилморфолин-3-она
1,11 г указанного в заголовке соединения получали из 4-[(S)-хроман-4-ил]-6,6-диметилморфолин-2,3-диона (1,50 г) и 1М раствора три-втор-бутилборогидрида лития в ТГФ (6,0 мл) по аналогичной методике примера 7.
1H-ЯМР (CDCl3) δ (м.д.): 1,26 (с, 3H), 1,31 (с, 1,5H), 1,32 (с, 1,5H), 2,10-2,25 (м, 2H), 2,99 (д, J=13,2 Гц, 0,5H), 3,05 (д, J=13,2 Гц, 1H), 3,12 (д, J=13,2 Гц, 0,5H), 4,17-4,25 (м, 1H), 4,26-4,35 (м, 1H), 5,36 (с, 0,5H), 5,37 (с, 0,5H), 5,89-5,99 (м, 1H), 6,84-6,87 (м, 1H), 6,90-6,94 (м, 1H), 7,01-7,04 (м, 0,5H), 7,08-7,11 (м, 0,5H), 7,16-7,21 (м, 1H).
Синтез (Z)-4-[(S)-хроман-4-ил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-она
Трифенилфосфонийбромид (292 мг) добавляли к раствору 4-[(S)-хроман-4-ил]-2-гидрокси-6,6-диметилморфолин-3-она (196 мг) в ацетонитриле (10 мл) и реакционный раствор нагревали при кипении с обратным холодильником в течение двух часов. Реакционный раствор концентрировали при пониженном давлении. К остатку добавляли этанол (15 мл), TEA (221 мкл) и 3-метокси-4-(4-метил-1H-имидазол-1-ил)бензальдегид (138 мг) и реакционный раствор нагревали при кипении с обратным холодильником в течение 2,5 часов. Реакционный раствор концентрировали при пониженном давлении и разбавляли насыщенным раствором бикарбоната натрия и этилацетатом, затем органический слой отделяли. Органический слой сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с использованием NH силикагеля (гептан:этилацетат=1:1-0:100) и затем очищали колоночной хроматографией с использованием силикагеля (гептан:этилацетат=1:1-0:100), с получением 167 мг указанного в заголовке соединения.
1H-ЯМР (CDCl3) δ (м.д.): 1,42 (с, 3H), 1,44 (с, 3H), 2,14-2,22 (м, 2H), 2,33 (с, 3H), 3,12 (д, J=12,8 Гц, 1H), 3,19 (д, J=12,8 Гц, 1H), 3,87 (с, 3H), 4,22-4,34 (м, 2H), 6,13 (дд, J=8,8, 6,8 Гц, 1H), 6,86-6,95 (м, 4H), 7,10 (д, J=7,2 Гц, 1H), 7,19 (д, J=7,2 Гц, 1H), 7,22 (д, J=8,4 Гц, 1H), 7,37 (дд, J=8,4, 1,6 Гц, 1H), 7,57 (д, J=1,6 Гц, 1H), 7,80 (с, 1H).
ESI-МС; m/z 460[M++H].
Примеры 13 и 14
Синтез (Z)-(S)-4-[(S)-хроман-4-ил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она и (Z)-(R)-4-[(S)-хроман-4-ил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она
[Формула 33]

70,3 мг указанного в заголовке соединения получали в виде смеси диастереомеров из перхлората лития (3,56 г), эфира (6,7 мл), (S)-4-аминохроман (1,0 г) и пропиленоксида (609 мкл) в качестве исходных соединений по аналогичной методике примера 7. Смесь разделяли с помощью CHIRALPAKTM AD-H производства ф. Daicel Chemical Industries, Ltd. (2 см×25 см; подвижная фаза: этанол 100%), с получением указанного в заголовке оптически активного соединения со временем удерживания 18 минут (>99% de) и указанного в заголовке оптически активного соединения со временем удерживания 20 минут (95% de).
Характеристические значения указанного в заголовке оптически активного соединения со временем удерживания 18 минут (пример 13) являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,41 (д, J=6,0 Гц, 3H), 2,28-2,10 (м, 2H), 2,33 (с, 3H), 3,09 (дд, J=13,2, 3,2 Гц, 1H), 3,17 (дд, J=13,2, 8,8 Гц, 1H), 3,87 (с, 3H), 4,20-4,40 (м, 3H), 6,07 (дд, J=9,2, 6,8 Гц, 1H), 6,86-6,95 (м, 4H), 7,06 (д, J=7,6 Гц, 1H), 7,18 (д, J=8,4 Гц, 1H), 7,23 (д, J=8,0 Гц, 1H), 7,38 (д, J=8,4 Гц, 1H), 7,55 (с, 1H), 7,81 (с, 1H).
ESI-МС; m/z 446[M++H].
Характеристические значения указанного в заголовке оптически активного соединения со временем удерживания 20 минут (пример 14) являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,41 (д, J=6,4 Гц, 3H), 2,10-2,21 (м, 2H), 2,36 (с, 3H), 3,09 (дд, J=12,8, 2,8 Гц, 1H), 3,33 (дд, J=12,8, 10,0 Гц, 1H), 3,87 (с, 3H), 4,21-4,38 (м, 3H), 6,14 (дд, J=9,2, 7,2 Гц, 1H), 6,86-6,96 (м, 4H), 7,06 (д, J=7,6 Гц, 1H), 7,18-7,26 (м, 2H), 7,38 (д, J=8,4 Гц, 1H), 7,57 (с, 1H), 7,89 (с, 1H).
ESI-МС; m/z 446[M++H].
Пример 15
Синтез (Z)-(S)-4-(6-хлорпиридин-2-илметил)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она
[Формула 34]
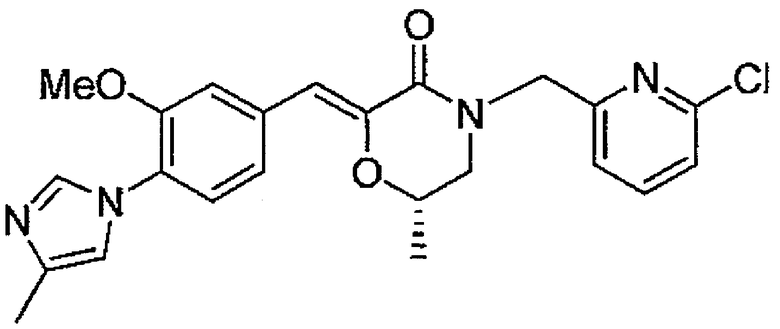
Синтез (S)-1-[(6-хлорпиридин-2-илметил)амино]пропан-2-ола
394 мг указанного в заголовке соединения получали из 2-хлор-6-формилпиридина (500 мг), (S)-1-амино-2-пропанола (318 мг), уксусной кислоты (0,808 мл) и триацетоксиборогидрида натрия (1,12 г) по аналогичной методике примера 1.
1H-ЯМР (CDCl3) δ (м.д.): 1,16 (д, J=6,0 Гц, 3H), 2,49 (дд, J=12,0, 9,2 Гц, 1H), 2,78 (дд, J=12,0, 2,8 Гц, 1H), 3,83-3,87 (м, 1H), 3,93 (с, 2H), 7,23 (д, J=8,0 Гц, 1H), 7,24 (д, J=8,0 Гц, 1H), 7,64 (т, J=8,0 Гц, 1H).
Синтез (S)-4-(6-хлорпиридин-2-илметил)-6-метилморфолин-2,3-диона
411 мг указанного в заголовке соединения получали из (S)-1-[(6-хлорпиридин-2-илметил)амино]пропан-2-ола (394 мг) и диэтилоксалата (3,0 мл) по аналогичной методике примера 1.
1H-ЯМР (CDCl3) δ (м.д.): 1,46 (д, J=6,8 Гц, 3H), 3,71 (дд, J=13,6, 3,2 Гц, 1H), 3,79 (дд, J=13,6, 9,6 Гц, 1H), 4,69 (д, J=15,2 Гц, 1H), 4,77 (д, J=15,2 Гц, 1H), 4,84-4,90 (м, 1H), 7,30 (д, J=8,0 Гц, 1H), 7,32 (д, J=8,0 Гц, 1H), 7,68 (т, J=8,0 Гц, 1H).
Синтез (S)-4-(6-хлорпиридин-2-илметил)-2-гидрокси-6-метилморфолин-3-она
273 мг указанного в заголовке соединения получали из (S)-4-(6-хлорпиридин-2-илметил)-6-метилморфолин-2,3-диона (411 мг) и 1М раствора три-втор-бутилборогидрида лития в ТГФ (1,64 мл) по аналогичной методике примера 1.
1H-ЯМР (CDCl3) δ (м.д.): 1,27 (д, J=6,0 Гц, 3H), 3,30 (дд, J=12,0, 3,2 Гц, 1H), 3,39 (дд, J=12,0, 10,8 Гц, 1H), 4,48-4,52 (м, 1H), 4,49 (д, J=15,2 Гц, 1H), 4,81 (д, J=15,2 Гц, 1H), 5,35 (с, 1H), 7,27 (д, J=7,6 Гц, 1H), 7,28 (д, J=7,6 Гц, 1H), 7,66 (т, J=7,6 Гц, 1H).
Синтез (Z)-(S)-4-(6-хлорпиридин-2-илметил)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она
27,9 мг указанного в заголовке соединения получали из (S)-4-(6-хлорпиридин-2-илметил)-2-гидрокси-6-метилморфолин-3-она (237 мг), тионилхлорида (1,01 мл), трифенилфосфина (315 мг) и 3-метокси-4-(4-метил-1H-имидазол-1-ил)бензальдегида (21,6 мг) по аналогичной методике примера 1.
1H-ЯМР (CDCl3) δ (м.д.): 1,47 (д, J=6,4 Гц, 3H), 2,34 (с, 3H), 3,57 (дд, J=12,8, 2,8 Гц, 1H), 3,68 (дд, J=12,0, 10,0 Гц, 1H), 3,86 (с, 3H), 4,43-4,46 (м, 1H), 4,76 (с, 2H), 6,85 (с, 1H), 6,95 (с, 1H), 7,22 (д, J=8,0 Гц, 1H), 7,31 (д, J=7,6 Гц, 1H), 7,33 (д, J=8,0 Гц, 1H), 7,35 (дд, J=7,6, 1,6 Гц, 1H), 7,55 (д, J=1,6 Гц, 1H), 7,66 (т, J=8,0 Гц, 1H), 7,84 (с, 1H).
Примеры 16 и 17
Синтез (Z)-(6S,9aR)-6-(4-фторфенил)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)бензилиден]гексагидропиридо[2,1-c][1,4]оксазин-4-она и (Z)-(6R,9aS)-6-(4-фторфенил)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)бензилиден]гексагидропиридо[2,1-c][1,4]оксазин-4-она
[Формула 35]

Синтез 1-(4-фторфенил)гепта-5,6-диенил-1-амина
2,65 г указанного в заголовке соединения получали из (4-фторбензил)-(4-фторбензилиден)амина (3 г) и 6-иодгекса-1,2-диена (2,97 г) согласно способу, описанному в Journal of the American Chemical Society, 2003, vol.125, p.11956. Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,25-1,37 (м, 1H), 1,39-1,50 (м, 1H), 1,63-1,75 (м, 2H), 1,95-2,04 (м, 2H), 3,88 (д, J=6,8 Гц, 1H), 4,63 (дт, J=6,8, 2,8 Гц, 2H), 5,04 (квинтет, J=6,8 Гц, 1H), 6,99 (т, J=8,8 Гц, 2H), 7,26 (дд, J=8,8, 5,6 Гц, 2H).
Синтез (2R*,6S*)-2-(4-фторфенил)-6-винилпиперидина
Уксусную кислоту (0,74 мл) добавляли к раствору димера аллилпалладийхлорида (472 мг) и 1,1'-бис(дифенилфосфино)ферроцена (1,43 г) в ТГФ (200 мл) и реакционный раствор перемешивали при комнатной температуре в течение 10 минут. Раствор 1-(4-фторфенил)гепта-5,6-диенил-1-амина (2,65 г) в ТГФ (50 мл) добавляли к реакционному раствору, который затем перемешивали при 70°C в течение 1,5 часов. Реакционный раствор оставляли охлаждаться до комнатной температуры. Затем добавляли к реакционному раствору диэтиловый эфир и 1н. водную хлористо-водородную кислоту и отделяли водный слой. Полученный водный слой промывали диэтиловым эфиром и затем 5н. раствор гидроксида натрия добавляли к водному слою, пока pH не доходило до 11 или ниже. Хлороформ добавляли к водному слою и органический слой отделяли. Полученный органический слой сушили над сульфатом магния и концентрировали при пониженном давлении, с получением 2,4 г указанного в заголовке соединения. Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,24-1,60 (м, 3H), 1,67-1,77 (м, 2H), 1,88-1,95 (м, 1H), 3,24-3,30 (м, 1H), 3,67 (дд, J=11,2, 2,8 Гц, 1H), 5,01 (ушир.д, J=10,4 Гц, 1H), 5,17 (ушир.д, J=16,8 Гц, 1H), 5,88 (ддд, J=16,8, 10,4, 6,4 Гц, 1H), 6,98 (т, J=8,8 Гц, 2H), 7,35 (дд, J=8,8, 5,6 Гц, 2H).
ESI-МС; m/z 206[M++H].
Синтез этил[(2R*,6S*)-2-(4-фторфенил)-6-винилпиперидин-1-ил]оксоацетата
Этилоксалатхлорид (0,5 мл) добавляли к раствору (2R*,6S*)-2-(4-фторфенил)-6-винилпиперидина (520 мг) и DIEA (0,66 мл) в метиленхлориде (10 мл) и реакционный раствор перемешивали при комнатной температуре в течение одного часа. Хлороформ и 1н. водную хлористо-водородную кислоту добавляли к реакционному раствору и органический слой отделяли. Полученный органический слой промывали насыщенным водным раствором бикарбоната натрия, сушили над сульфатом магния и затем концентрировали при пониженном давлении. Остаток очищали хроматографией на колонке с силикагелем (элюирующий растворитель: гептан→гептан:этилацетат=1:1), с получением 426 мг указанного в заголовке соединения. Характеристическое значение данного соединения является следующим:
ESI-МС: m/z 306[M++H].
Синтез (6R*,9aS*)-6-(4-фторфенил)-3-гидроксигексагидропиридо[2,1-c][1,4]оксазин-4-она
Раствор этил[(2R*,6S*)-2-(4-фторфенил)-6-винилпиперидин-1-ил]оксоацетата (220 мг) в метаноле (5 мл) охлаждали до -78°C и газообразный озон барботировали через реакционный раствор в течение 20 минут. Борогидрид натрия (164 мг) добавляли к реакционному раствору при перемешивании при -78°C и реакционный раствор перемешивали при данной температуре в течение 30 минут. Этилацетат и насыщенный раствор аммонийхлорида добавляли к реакционному раствору и органический слой отделяли. Полученный органический слой сушили над сульфатом магния и затем концентрировали при пониженном давлении. Остаток очищали хроматографией на колонке с силикагелем (элюирующий растворитель: гептан:этилацетат=1:1→этилацетат), с получением 26 мг указанного в заголовке соединения. Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,35-1,50 (м, 2H), 1,57-1,67 (м, 2H), 2,05-2,26 (м, 2H), 3,57 (ушир.с, 1H), 3,80 (дд, J=11,6, 3,6 Гц, 1H), 3,88-3,98 (м, 1H), 4,11 (т, J=11,6 Гц, 1H), 5,22 (т, J=4,0 Гц, 1H), 5,28 (с, 1H), 7,01 (т, J=8,8 Гц, 2H), 7,19 (дд, J=8,8, 5,6 Гц, 2H).
ESI-МС; m/z 220[M++H].
Синтез [(6R*,9aS*)-6-(4-фторфенил)-4-оксооктагидропиридо[2,1-c][1,4]оксазин-3-ил]трифенилфосфонийбромида
Раствор (6R*,9aS*)-6-(4-фторфенил)-3-гидроксигексагидропиридо[2,1-c][1,4]оксазин-4-она (26 мг) и трифенилфосфонийбромида (40 мг) в ацетонитриле (3 мл) нагревали при кипении с обратным холодильником в течение одного часа и 30 минут. Реакционный раствор оставляли охлаждаться до комнатной температуры и затем растворитель выпаривали при пониженном давлении, с получением 57 мг указанного в заголовке соединения. Характеристическое значение данного соединения является следующим:
ESI-МС: m/z 510[M+].
Синтез (Z)-(6S*,9aR*)-6-(4-фторфенил)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)бензилиден]гексагидропиридо[2,1-c][1,4]оксазин-4-она
Триэтиламин (0,03 мл) добавляли к раствору [(6R*,9aS*)-6-(4-фторфенил)-4-оксооктагидропиридо[2,1-c][1,4]оксазин-3-ил]трифенилфосфонийбромида (57 мг) и 3-метокси-4-(4-метил-1H-имидазол-1-ил)бензальдегида (21 мг) в этаноле (5 мл) и реакционный раствор перемешивали при комнатной температуре в течение двух часов. Реакционный раствор концентрировали при пониженном давлении. Затем остаток очищали хроматографией на колонке с силикагелем (носитель: Chromatorex NH; элюирующий растворитель: гептан:этилацетат=1:1→этилацетат), с получением 27 мг указанного в заголовке соединения. Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,40-1,58 (м, 2H), 1,65-1,76 (м, 2H), 2,18-2,25 (м, 2H), 2,31 (с, 3H), 3,85 (с, 3H), 4,07 (кв, J=10,8 Гц, 1H), 4,07-4,15 (м, 1H), 4,34 (дд, J=10,8, 2,4 Гц, 1H), 5,38 (т, J=4,0 Гц, 1H), 6,82 (с, 1H), 6,92 (ушир.с, 1H), 7,02 (т, J=8,4 Гц, 2H), 7,20 (д, J=8,0 Гц, 1H), 7,22 (дд, J=8,0, 3,6 Гц, 2H), 7,37 (дд, J=8,0, 1,2 Гц, 1H), 7,39 (д, J=1,2 Гц, 1H), 7,74 (д, J=1,2 Гц, 1H).
ESI-МС; m/z 448[M++H].
Синтез (Z)-(6S,9aR)-6-(4-фторфенил)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)бензилиден]гексагидропиридо[2,1-c][1,4]оксазин-4-она и (Z)-(6R,9aS)-6-(4-фторфенил)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)бензилиден]гексагидропиридо[2,1-c][1,4]оксазин-4-она
Рацемат (Z)-(6S*,9aR*)-6-(4-фторфенил)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)бензилиден]гексагидропиридо[2,1-c][1,4]оксазин-4-она, полученный выше (27 мг), разделяли с помощью CHIRALCELTM OJ-H производства ф. Daicel Chemical Industries, Ltd. (2 см×25 см; подвижная фаза: гексан:этанол=1:1), с получением указанного в заголовке оптически активного соединения со временем удерживания 24 минут (6,7 мг;>99% ee) и указанного в заголовке оптически активного соединения со временем удерживания 31 минут (4,9 мг;>99% ee).
Характеристические значения указанного в заголовке оптически активного соединения со временем удерживания 24 минут (пример 16) являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,40-1,58 (м, 2H), 1,65-1,76 (м, 2H), 2,18-2,25 (м, 2H), 2,31 (с, 3H), 3,85 (с, 3H), 4,07 (кв, J=10,8 Гц, 1H), 4,07-4,15 (м, 1H), 4,34 (дд, J=10,8, 2,4 Гц, 1H), 5,38 (т, J=4,0 Гц, 1H), 6,82 (с, 1H), 6,92 (ушир.с, 1H), 7,02 (т, J=8,4 Гц, 2H), 7,20 (д, J=8,0 Гц, 1H), 7,22 (дд, J=8,0, 3,6 Гц, 2H), 7,37 (дд, J=8,0, 1,2 Гц, 1H), 7,39 (д, J=1,2 Гц, 1H), 7,74 (д, J=1,2 Гц, 1H).
ESI-МС; m/z 448[M++H].
Характеристические значения указанного в заголовке оптически активного соединения со временем удерживания 31 минут (пример 17) являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,40-1,58 (м, 2H), 1,65-1,76 (м, 2H), 2,18-2,25 (м, 2H), 2,31 (с, 3H), 3,85 (с, 3H), 4,07 (кв, J=10,8 Гц, 1H), 4,07-4,15 (м, 1H), 4,34 (дд, J=10,8, 2,4 Гц, 1H), 5,38 (т, J=4,0 Гц, 1H), 6,82 (с, 1H), 6,92 (ушир.с, 1H), 7,02 (т, J=8,4 Гц, 2H), 7,20 (д, J=8,0 Гц, 1H), 7,22 (дд, J=8,0, 3,6 Гц, 2H), 7,37 (дд, J=8,0, 1,2 Гц, 1H), 7,39 (д, J=1,2 Гц, 1H), 7,74 (д, J=1,2 Гц, 1H).
ESI-МС; m/z 448[M++H].
Примеры 18 и 19
Синтез (Z)-(S)-4-[(S)-1-(6-хлорпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она и (Z)-(S)-4-[(R)-1-(6-хлорпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она
[Формула 36]

Синтез (S)-1-[1-(6-хлорпиридин-3-ил)этиламино]пропан-2-ола
44,9 мг указанного в заголовке соединения получали из перхлората лития (340 мг), эфира (0,64 мл), 1-(6-хлорпиридин-3-ил)этиламина (100 мг: CAS #132219-51-3) и (S)-пропиленоксида (61 мкл) по аналогичной методике примера 7.
1H-ЯМР (CDCl3) δ (м.д.): 1,11 (д, J=6,4 Гц, 1,5H), 1,12 (д, J=6,4 Гц, 1,5H), 1,39 (д, J=6,8 Гц, 1,5H), 1,40 (д, J=6,8 Гц, 1,5H), 2,21 (дд, J=12,0, 9,2 Гц, 0,5H), 2,38 (дд, J=12,0, 8,8 Гц, 0,5H), 2,49 (дд, J=12,0, 2,4 Гц, 0,5H), 2,63 (дд, J=12,0, 2,8 Гц, 0,5H), 3,68-3,87 (м, 2H), 7,31 (д, J=8,0 Гц, 0,5H), 7,32 (д, J=8,0 Гц, 0,5H), 7,67 (дд, J=8,0, 2,0 Гц, 0,5H), 7,68 (дд, J=8,0, 2,0 Гц, 0,5H), 8,30 (д, J=2,0 Гц, 0,5H), 8,31 (д, J=2,0 Гц, 0,5H).
Синтез (S)-4-[1-(6-хлорпиридин-3-ил)этил]-6-метилморфолин-2,3-диона
37,4 мг неочищенного указанного в заголовке соединения получали из (S)-1-[1-(6-хлорпиридин-3-ил)этиламино]пропан-2-ола (44,8 мг) и диэтилоксалата (1,0 мл) по аналогичной методике примера 7.
1H-ЯМР (CDCl3) δ (м.д.): 1,36 (д, J=6,0 Гц, 1,5H), 1,41 (д, J=6,0 Гц, 1,5H), 1,62 (д, J=7,2 Гц, 1,5H), 1,65 (д, J=7,2 Гц, 1,5H), 3,03-3,11 (м, 1H), 3,34 (дд, J=14,0, 3,2 Гц, 0,5H), 3,47 (дд, J=13,6, 10,4 Гц, 0,5H), 4,52-4,55 (м, 0,5H), 4,71-4,76 (м, 0,5H), 5,94-5,99 (м, 1H), 7,37 (д, J=8,4 Гц, 1H), 7,64 (дд, J=8,4, 2,4 Гц, 0,5H), 7,68 (дд, J=8,4, 2,4 Гц, 0,5H), 8,37 (д, J=2,4 Гц, 0,5H), 8,39 (д, J=2,4 Гц, 0,5H).
Синтез (S)-4-[1-(6-хлорпиридин-3-ил)этил]-2-гидрокси-6-метилморфолин-3-она
3,9 мг указанного в заголовке соединения получали из (S)-4-[1-(6-хлорпиридин-3-ил)этил]-6-метилморфолин-2,3-диона (37,4 мг) и 1М раствора три-втор-бутилборогидрида лития в ТГФ (153 мкл) по аналогичной методике примера 7.
1H-ЯМР (CDCl3) δ (м.д.): 1,22 (д, J=7,2 Гц, 1,5H), 1,23 (д, J=7,2 Гц, 1,5H), 1,57 (д, J=8,4 Гц, 3H), 2,68 (дд, J=12,0, 10,8 Гц, 0,5H), 2,75 (дд, J=12,0, 2,8 Гц, 0,5H), 3,02 (дд, J=12,0, 2,8 Гц, 0,5H), 3,18 (дд, J=12,0, 10,8 Гц, 0,5H), 4,26-4,30 (м, 0,5H), 4,43-4,47 (м, 0,5H), 5,34 (с, 0,5H), 5,36 (с, 0,5H), 5,96 (кв, J=7,2 Гц, 0,5H), 5,99 (кв, J=7,2 Гц, 0,5H), 7,33 (д, J=8,4 Гц, 0,5H), 7,34 (д, J=8,4 Гц, 0,5H), 7,59 (дд, J=8,4, 2,4 Гц, 0,5H), 7,63 (дд, J=8,4, 2,4 Гц, 0,5H), 8,34 (д, J=2,4 Гц, 0,5H), 8,35 (д, J=2,4 Гц, 0,5H).
Синтез (Z)-(S)-4-[(S)-1-(6-хлорпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она и (Z)-(S)-4-[(R)-1-(6-хлорпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она
Указанное в заголовке соединение получали в виде смеси диастереомеров из (S)-4-[1-(6-хлорпиридин-3-ил)этил]-2-гидрокси-6-метилморфолин-3-она (3,9 мг), трифенилфосфонийбромида (5,81 мг) и 3-метокси-4-(4-метил-1H-имидазол-1-ил)бензальдегида (3,43 мг) по аналогичной методике примеров 16 и 17. Смесь диастереомеров разделяли с помощью CHIRALPAKTM AD-H производства ф. Daicel Chemical Industries, Ltd. (2 см×25 см; подвижная фаза: этанол 100%), с получением указанного в заголовке оптически активного соединения со временем удерживания 19 минут (1,25 мг;>80% de) и указанного в заголовке оптически активного соединения со временем удерживания 25 минут (0,85 мг;>84% de).
Характеристические значения указанного в заголовке оптически активного соединения со временем удерживания 19 минут (пример 19) являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,39 (д, J=6,8 Гц, 3H), 1,62 (д, J=6,8 Гц, 3H), 2,36 (с, 3H), 2,96 (дд, J=13,2, 4,8 Гц, 1H), 3,26 (дд, J=13,2, 2,4 Гц, 1H), 3,86 (с, 3H), 4,31-4,40 (м, 1H), 6,13 (кв, J=6,8 Гц, 1H), 6,88 (с, 1H), 6,96 (с, 1H), 7,22 (д, J=8,4 Гц, 1H), 7,34 (д, J=8,0 Гц, 1H), 7,36 (д, J=8,0 Гц, 1H), 7,52 (с, 1H), 7,64 (дд, J=8,4, 2,8 Гц, 1H), 7,93 (с, 1H), 8,38 (д, J=2,8 Гц, 1H).
ESI-МС; m/z 453[M++H].
Характеристические значения указанного в заголовке оптически активного соединения со временем удерживания 25 минут (пример 18) являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,42 (д, J=6,0 Гц, 3H), 1,61 (д, J=7,2 Гц, 3H), 2,39 (с, 3H), 2,99 (дд, J=12,8, 2,4 Гц, 1H), 3,41 (дд, J=12,8, 10,4 Гц, 1H), 3,87 (с, 3H), 4,10-4,20 (м, 1H), 6,15 (кв, J=7,2 Гц, 1H), 6,89 (с, 1H), 6,97 (с, 1H), 7,23 (д, J=8,4 Гц, 1H), 7,35 (д, J=7,6 Гц, 1H), 7,37 (д, J=7,6 Гц, 1H), 7,55 (с, 1H), 7,67 (дд, J=8,4, 2,4 Гц, 1H), 7,99 (с, 1H), 8,39 (д, J=2,4 Гц, 1H).
ESI-МС; m/z 453[M++H].
Примеры 20 и 21
Синтез (Z)-(S)-4-[(S)-1-(5-хлорпиридин-2-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она и (Z)-(S)-4-[(R)-1-(5-хлорпиридин-2-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она
[Формула 37]

Синтез 1-(5-хлорпиридин-2-ил)этанола
Йодид меди (148 мг), 1-этоксивинилтри-н-бутилолово (2,97 мл) и бис(трифенилфосфин)палладий(II)хлорид (183 мг) добавляли к раствору 2-бром-5-хлорпиридина (1 г) в ацетонитриле (30 мл) и реакционный раствор перемешивали в атмосфере азота при 100°C в течение трех часов. Реакционный раствор снова доводили до комнатной температуры. Добавляли 10 мл 5н. хлористо-водородной кислоты и реакционный раствор нагревали при кипении с обратным холодильником в течение 30 минут. Реакционный раствор снова доводили до комнатной температуры и нейтрализовали 5н. раствором гидроксида натрия. Диэтиловый эфир добавляли к реакционному раствору и органический слой отделяли. Органический слой сушили над безводным сульфатом магния и затем растворитель выпаривали при пониженном давлении. Остаток растворяли в тетрагидрофуране (30 мл) и метаноле (10 мл). Борогидрид натрия (492 мг) добавляли и реакционный раствор перемешивали при комнатной температуре в течение одного часа. Воду и диэтиловый эфир добавляли к реакционному раствору и органический слой отделяли. Органический слой промывали насыщенным раствором соли и сушили над безводным сульфатом магния. Растворитель выпаривали при пониженном давлении и остаток очищали хроматографией на колонке с силикагелем (элюирующий растворитель: гексан-диэтиловый эфир), с получением 503 мг указанного в заголовке соединения.
1H-ЯМР (CDCl3) δ (м.д.): 1,50 (д, J=6,8 Гц, 3H), 4,90 (кв, J=6,8 Гц, 1H), 7,28 (дд, J=0,8, 0,8 Гц, 1H), 7,67 (дд, J=8,4, 2,8 Гц, 1H), 8,50 (дд, J=2,8, 0,8 Гц, 1H).
Синтез 2-(1-азидоэтил)-5-хлорпиридина
Дифенилфосфорилазид (1,0 мл) добавляли к раствору 1-(5-хлорпиридин-2-ил)этанола (503 мг) в толуоле (8 мл) в атмосфере азота. Реакционный раствор охлаждали льдом и добавляли к раствору по каплям 1,8-диазабицикло[5,4,0]ундец-7-ен (0,69 мл). Реакционный раствор перемешивали в течение трех часов. Затем раствор снова доводили до комнатной температуры и перемешивали в течение ночи. Воду и диэтиловый эфир добавляли к реакционному раствору и органический слой отделяли. Органический слой сушили над сульфатом магния и затем растворитель выпаривали при пониженном давлении. Остаток очищали хроматографией на колонке с силикагелем (элюирующий растворитель: гексан-диэтиловый эфир), с получением 337 мг указанного в заголовке соединения.
1H-ЯМР (CDCl3) δ (м.д.): 1,60 (д, J=6,8 Гц, 3H), 4,66 (кв, J=6,8 Гц, 1H), 7,32 (д, J=8,4 Гц, 1H), 7,69 (дд, J=8,4, 2,8 Гц, 1H), 8,54 (д, J=2,8 Гц, 1H).
Синтез 1-(5-хлорпиридин-2-ил)этиламина
Воду (3 мл) и трифенилфосфин (702 мг) добавляли к раствору 2-(1-азидоэтил)-5-хлорпиридина (333 мг) в тетрагидрофуране (10 мл) и реакционный раствор перемешивали при 60°C в течение двух часов. Реакционный раствор снова доводили до комнатной температуры. Дихлорметан и 5н. хлористо-водородную кислоту добавляли к реакционному раствору и отделяли водный слой. Водный слой подщелачивали (pH 14) 5н. раствором гидроксида натрия. Затем дихлорметан добавляли к реакционному раствору и органический слой отделяли. Органический слой сушили над безводным сульфатом магния и растворитель выпаривали при пониженном давлении, с получением 260 мг указанного в заголовке соединения.
1H-ЯМР (CDCl3) δ (м.д.): 1,42 (д, J=6,4 Гц, 3H), 4,18 (кв, J=6,4 Гц, 1H), 7,28 (д, J=8,4 Гц, 1H), 7,63 (дд, J=8,4, 2,4 Гц, 1H), 8,50 (д, J=2,4 Гц, 1H).
Синтез (Z)-(S)-4-[(S)-1-(5-хлорпиридин-2-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она и (Z)-(S)-4-[(R)-1-(5-хлорпиридин-2-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она
115 мг указанного в заголовке соединения получали в виде смеси диастереомеров из 1-(5-хлорпиридин-2-ил)этиламина (200 мг) в качестве исходного соединения по аналогичной методике примеров 18 и 19. Часть смеси диастереомеров разделяли с помощью CHIRALPAKTM IA производства ф. Daicel Chemical Industries, Ltd. (2 см×25 см; подвижная фаза: этанол 100%), с получением указанного в заголовке оптически активного соединения со временем удерживания 17 минут (12,3 мг;>99% de) и указанного в заголовке оптически активного соединения со временем удерживания 20 минут (21,4 мг; 94% de).
Характеристические значения указанного в заголовке оптически активного соединения со временем удерживания 17 минут (пример 20) являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,38 (д, J=6,4 Гц, 3H), 1,61 (д, J=7,2 Гц, 3H), 2,31 (с, 3H), 3,19 (дд, J=13,2, 9,6 Гц, 1H), 3,52 (дд, J=13,2, 2,4 Гц, 1H), 3,85 (с, 3H), 4,33-4,42 (м, 1H), 6,04 (кв, J=7,2 Гц, 1H), 6,83 (с, 1H), 6,93 (с, 1H), 7,20 (д, J=8,0 Гц, 1H), 7,32 (дд, J=8,0, 1,6 Гц, 1H), 7,33 (д, J=8,4 Гц, 1H), 7,51 (д, J=1,6 Гц, 1H), 7,65 (дд, J=8,4, 2,4 Гц, 1H), 7,77 (с, 1H), 8,52 (д, J=2,4 Гц, 1H).
ESI-МС; m/z 453[M++H].
Характеристические значения указанного в заголовке оптически активного соединения со временем удерживания 20 минут (пример 21) являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,45 (д, J=6,4 Гц, 3H), 1,60 (д, J=7,2 Гц, 3H), 2,55 (с, 3H), 3,48 (дд, J=12,8, 10,0 Гц, 1H), 3,60 (дд, J=12,8, 2,4 Гц, 1H), 3,89 (с, 3H), 4,20-4,27 (м, 1H), 5,97 (кв, J=7,2 Гц, 1H), 6,81 (с, 1H), 7,02 (с, 1H), 7,22 (д, J=7,6 Гц, 1H), 7,37 (д, J=8,4 Гц, 1H), 7,38 (дд, J=7,6, 1,2 Гц, 1H), 7,60 (д, J=1,2 Гц, 1H), 7,66 (дд, J=8,4, 2,4 Гц, 1H), 8,48 (с, 1H), 8,51 (д, J=2,4 Гц, 1H).
ESI-МС; m/z 453[M++H].
Примеры 22 и 23
Синтез (Z)-(S)-4-[(S)-1-(2,6-дифторпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она и (Z)-(S)-4-[(R)-1-(2,6-дифторпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она
[Формула 38]

Раствор н-бутиллития в ТГФ (2,62M, 29,1 мл) добавляли по каплям к раствору диизопропиламина (11,7 мл) в тетрагидрофуране (310 мл) при охлаждении льдом в атмосфере азота. Реакционный раствор перемешивали при охлаждении льдом в течение одного часа и затем охлаждали до -78°C. Раствор 2,6-дифторпиридина (8 г) в тетрагидрофуране (10 мл) добавляли по каплям к реакционному раствору. Реакционный раствор перемешивали при -78°C в течение трех часов. Затем добавляли в токе азота избыточное количество раздробленного сухого льда и реакционный раствор перемешивали при -78°C в течение 20 минут и при комнатной температуре в течение трех часов. Воду и диэтиловый эфир добавляли к реакционному раствору и отделяли водный слой. Водный слой доводили до pH 1 концентрированной хлористо-водородной кислотой. Этилацетат добавляли к водному слою и органический слой отделяли. Органический слой сушили над безводным сульфатом магния и растворитель выпаривали при пониженном давлении, с получением 10,4 г указанного в заголовке соединения.
1H-ЯМР (CD3OD) δ (м.д.): 7,08 (дд, J=8,4, 2,8 Гц, 1H), 8,58 (дд, J=17,2, 8,4 Гц, 1H).
Синтез 2,6-дифтор-N-метокси-N-метилникотинамида
Гидрохлорид N,O-диметилгидроксиламина (14,7 г), WSC (28,9 г) и HOBt (20,4 г) добавляли к раствору 2,6-дифторникотиновой кислоты (6 г) и диизопропилэтиламина (10 мл) в ДМФА (100 мл) и реакционный раствор перемешивали при комнатной температуре в течение двух суток. Воду и этилацетат добавляли к реакционному раствору и органический слой отделяли. Органический слой сушили над безводным сульфатом магния и растворитель выпаривали при пониженном давлении. Полученный остаток очищали хроматографией на колонке с силикагелем (носитель: Chromatorex NH; элюирующий растворитель: этилацетат), с получением 7,01 г указанного в заголовке соединения.
1H-ЯМР (CDCl3) δ (м.д.): 3,37 (с, 3H), 3,58 (ушир.с, 3H), 6,90 (дд, J=8,0, 2,8 Гц, 1H), 8,02 (дд, J=16,0, 8,0 Гц, 1H).
1-(2,6-дифторпиридин-3-ил)этанон
Раствор метилмагнийбромида в ТГФ (0,96M, 88,1 мл) добавляли к раствору 2,6-дифтор-N-метокси-N-метилникотинамида (7,01 г) в тетрагидрофуране (180 мл) при охлаждении льдом и реакционный раствор перемешивали при охлаждении льдом в течение двух часов. Насыщенный раствор аммонийхлорида и этилацетат добавляли к реакционному раствору при охлаждении льдом и органический слой отделяли. Органический слой промывали насыщенным раствором соли и сушили над безводным сульфатом магния. Растворитель выпаривали при пониженном давлении и остаток очищали хроматографией на колонке с силикагелем (элюирующий растворитель: гексан-этилацетат), с получением 4,74 г указанного в заголовке соединения.
1H-ЯМР (CDCl3) δ (м.д.): 2,05 (с, 3H), 6,93-6,97 (м, 1H), 8,46-8,52 (м, 1H).
1-(2,6-дифторпиридин-3-ил)этаноноксим
Гидроксиламинсульфат (13,1 г) и ацетат натрия (10,9 г) добавляли к раствору 1-(2,6-дифторпиридин-3-ил)этанона (4,18 г) в водном ТГФ (50%, 200 мл) и реакционный раствор перемешивали при комнатной температуре в течение ночи. Воду и этилацетат добавляли к реакционному раствору и органический слой отделяли. Органический слой сушили над безводным сульфатом магния и растворитель выпаривали при пониженном давлении. Полученный остаток очищали хроматографией на колонке с силикагелем (носитель: Chromatorex NH; элюирующий растворитель: этилацетат), с получением 2,44 г указанного в заголовке соединения.
1H-ЯМР (CDCl3) δ (м.д.): 2,05 (с, 3H), 6,93-6,97 (м, 1H), 8,46-8,52 (м, 1H).
1-(2,6-дифторпиридин-3-ил)этиламин
Цинк (9,29 г) добавляли тремя порциями к раствору 1-(2,6-дифторпиридин-3-ил)этаноноксима (2,44 г) в трифторуксусной кислоте (100 мл) и реакционный раствор перемешивали при комнатной температуре в течение двух часов. Реакционный раствор подщелачивали (pH 14) 5н. гидроксидом натрия, фильтровали через целит и целит промывали хлороформом. Органический слой отделяли и сушили над безводным сульфатом магния и растворитель выпаривали при пониженном давлении, с получением 1,61 г указанного в заголовке соединения.
1H-ЯМР (CDCl3) δ (м.д.): 1,42 (д, J=6,8 Гц, 1H), 4,39 (кв, J=6,8 Гц, 1H), 6,82 (дд, J=8,0, 2,8 Гц, 1H), 8,02 (дд, J=17,2, 8,0 Гц, 1H).
Синтез (Z)-(S)-4-[(S)-1-(2,6-дифторпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она и (Z)-(S)-4-[(R)-1-(2,6-дифторпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она
Указанное в заголовке соединение (170 мг) получали в виде смеси диастереомеров из 1-(2,6-дифторпиридин-3-ил)этиламина (330 мг) в качестве исходного соединения по аналогичной методике примеров 18 и 19. Полученную смесь диастереомеров (10 мг) разделяли с помощью CHIRALPAKTM IA производства ф. Daicel Chemical Industries, Ltd. (2 см×25 см; подвижная фаза: гексан:этанол=7:3), с получением указанного в заголовке оптически активного соединения со временем удерживания 33 минут (4,7 мг) и указанного в заголовке оптически активного соединения со временем удерживания 39 минут (3,8 мг).
Характеристическое значение указанных в заголовке соединений смеси диастереомеров является следующим.
ESI-МС: m/z 455[M++H].
Характеристические значения указанного в заголовке оптически активного соединения со временем удерживания 33 минут (пример 22) являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,44 (д, J=6,4 Гц, 3H), 1,67 (д, J=7,2 Гц, 3H), 2,31 (с, 3H), 3,23 (дд, J=12,8, 10,0 Гц, 1H), 3,42 (дд, J=12,8, 2,8 Гц, 1H), 3,84 (с, 3H), 4,37 (м, 1H), 5,74 (кв, J=7,2 Гц, 1H), 6,81 (с, 1H), 6,87 (дд, J=8,0, 2,8 Гц, 1H), 6,93 (дд, J=1,2, 1,2 Гц, 1H), 7,20 (д, J=8,0 Гц, 1H), 7,31 (дд, J=8,4, 1,6 Гц, 1H), 7,50 (д, J=1,6 Гц, 1H), 7,77 (с, 1H), 8,00 (м, 1H).
Характеристические значения указанного в заголовке оптически активного соединения со временем удерживания 39 минут (пример 23) являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,46 (д, J=6,4 Гц, 3H), 1,65 (д, J=7,2 Гц, 3H), 2,32 (с, 3H), 3,32 (дд, J=12,8, 2,8 Гц, 1H), 3,50 (дд, J=12,8, 9,6 Гц, 1H), 3,85 (с, 3H), 4,29 (м, 1H), 5,80 (кв, J=7,2 Гц, 1H), 6,82 (с, 1H), 6,87 (дд, J=8,0, 2,8 Гц, 1H), 6,93 (дд, J=1,2, 1,2 Гц, 1H), 7,20 (д, J=8,0 Гц, 1H), 7,31 (дд, J=8,0, 1,6 Гц, 1H), 7,51 (д, J=1,6 Гц, 1H), 7,79 (с, 1H), 7,99 (м, 1H).
Другой синтез в примере 22:
Синтез (Z)-(S)-4-[(S)-1-(2,6-дифторпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она
[Формула 39]

Синтез 1-(2,6-дифторпиридин-3-ил)этанола
Диизопропиламин (134 мл) добавляли по каплям к смешанному раствору, состоящему из раствора н-бутиллития в гексане (2,62 M, 368 мл) и тетрагидрофурана (800 мл), в атмосфере азота при -60°C или ниже. Реакционный раствор перемешивали в течение 30 минут и затем раствор 2,6-дифторпиридина (100 г) в тетрагидрофуране (100 мл) добавляли по каплям к реакционному раствору при -60°C или ниже. Реакционный раствор перемешивали в течение одного часа и затем ацетальдегид (97,6 мл) добавляли по каплям к реакционному раствору. Затем к реакционному раствору добавляли по каплям 2н. водную хлористо-водородную кислоту (1,000 мл). Затем к реакционному раствору добавляли этилацетат (1,000 мл) и толуол (1,000 мл) и органический слой отделяли. Органический слой концентрировали при пониженном давлении, с получением 129 г указанного в заголовке соединения.
1H-ЯМР (CDCl3) δ (м.д.): 1,51 (д, J=5,6 Гц, 3H), 2,00 (с, 1H), 5,13-5,16 (м, 1H), 6,84 (дд, J=8,0, 2,1 Гц, 1H), 8,05 (дд, J=16,0, 8,0 Гц, 1H).
Синтез (+)-ди-п-толуоил-D-тартрата (S)-1-[(S)-1-(2,6-дифторпиридин-3-ил)этиламино]пропан-2-ола
Раствор 1-(2,6-дифторпиридин-3-ил)этанола (216 г) в толуоле (300 мл) добавляли к раствору тионилбромида (337 г) в толуоле (1,500 мл) при охлаждении льдом и реакционный раствор перемешивали при комнатной температуре в течение трех часов. Ледяную воду и толуол добавляли к реакционному раствору и органический слой отделяли. Органический слой промывали водой (1,000 мл) три раза. Органический слой сушили над безводным сульфатом магния и затем фильтровали через рыхлый слой силикагеля. (S)-1-амино-2-пропанол (157 г), карбонат цезия (1,28 кг) и ДМФА (2,500 мл) добавляли к фильтрату и реакционный раствор перемешивали при комнатной температуре в течение ночи. Реакционный раствор фильтровали и затем маточный раствор концентрировали при пониженном давлении. Остаток разбавляли этанолом (1,000 мл). Затем добавляли раствор (+)-ди-п-толуоил-D-винной кислоты (152 г) в этаноле (500 мл) и реакционный раствор перемешивали при комнатной температуре в течение одного часа. Выпавшие в осадок кристаллы отделяли фильтрованием и промывали этанолом. Кристаллы сушили при 80°C в течение двух часов и суспендировали в смешанном растворителе этанол (2,000 мл)-гептан (1,000 мл). Затем реакционный раствор нагревали и перемешивали при 80°C. Через час реакционный раствор снова доводили до комнатной температуры и кристаллы отделяли фильтрованием. Кристаллы промывали этанолом и сушили при 80°C в течение ночи, с получением 155 г указанного в заголовке соединения.
1H-ЯМР (ДМСО-d6) δ (м.д.): 1,02 (д, J=6,0 Гц, 6H), 1,37 (д, J=6,8 Гц, 6H), 2,36 (с, 6H), 2,37-2,51 (м, 4H), 3,67-3,71 (м, 2H), 4,14-4,16 (м, 2H), 5,65 (с, 2H), 7,21 (дд, J=8,0, 2,0 Гц, 2H), 7,31 (д, J=8,4, Гц, 4H), 7,82 (д, J=8,4, Гц, 4H), 8,27 (дд, J=17,6, 8,0 Гц, 2H).
Синтез (S)-4-[(S)-1-(2,6-дифторпиридин-3-ил)этил]-6-метилморфолин-2,3-диона
(+)-Ди-п-толуоил-D-тартрат (S)-1-[(S)-1-(2,6-дифторпиридин-3-ил)этиламино]пропан-2-ола (199 г) растворяли в 5н. водном растворе гидроксида натрия (450 мл), воде (1,000 мл) и смеси 50% толуол-ТГФ (2,000 мл) и органический слой отделяли. Водный слой промывали смесью 50% толуол-ТГФ (800 мл) три раза. Органические слои объединяли и концентрировали при пониженном давлении. Затем диэтилоксалат (200 мл) добавляли к остатку и реакционный раствор нагревали и перемешивали при 140-150°C. Через три часа реакционный раствор разбавляли толуолом (500 мл) и затем охлаждали льдом при перемешивании. Выпавшие в осадок кристаллы отделяли фильтрованием, промывали толуолом и диэтиловым эфиром и затем сушили на воздухе, с получением 103 г указанного в заголовке соединения.
1H-ЯМР (CDCl3) δ (м.д.): 1,43 (д, J=6,8 Гц, 3H), 1,70 (д, J=6,8 Гц, 3H), 3,36 (дд, J=13,2, 8,8 Гц, 1H), 3,52 (дд, J=13,2, 2,1 Гц, 1H), 4,72-4,78 (м, 1H), 5,59 (кв, J=6,8 Гц, 1H), 6,88 (дд, J=8,0, 2,8 Гц, 1H), 8,01 (дд, J=16,8, 8,0 Гц, 1H).
Синтез (S)-4-[(S)-1-(2,6-дифторпиридин-3-ил)этил]-2-гидрокси-6-метилморфолин-3-она
1М раствор три-втор-бутилборогидрида лития в ТГФ (20 мл) добавляли по каплям к раствору (S)-4-[(S)-1-(2,6-дифторпиридин-3-ил)этил]-6-метилморфолин-2,3-диона (4,5 г) в ТГФ при -50°C или ниже и реакционный раствор перемешивали в течение двух часов. К реакционному раствору при -10°C или ниже добавляли по каплям 5н. раствор гидроксида натрия (1,66 мл) и 30% водный пероксид водорода (6,78 мл) и реакционный раствор перемешивали в течение одного часа. Бисульфит натрия (520 мг) добавляли к реакционному раствору, который затем перемешивали в течение 30 минут. Насыщенный раствор соли и смесь 50% толуол-ТГФ добавляли к реакционному раствору и органический слой отделяли. Водный слой промывали смесью 50% толуол-ТГФ. Органические слои объединяли и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с использованием силикагеля (гептан:этилацетат=1:1-0:100), с получением 4,52 г указанного в заголовке соединения.
1H-ЯМР (CDCl3) δ (м.д.): 1,25 (д, J=6,8 Гц, 2,58H), 1,30 (д, J=6,8 Гц, 0,42H), 1,60 (д, J=6,8 Гц, 2,58H), 1,62 (д, J=6,8 Гц, 0,42H), 2,90 (дд, J=12,8, 8,8 Гц, 0,86H), 3,09 (дд, J=12,8, 8,8 Гц, 0,14H), 3,11 (дд, J=12,8, 2,1 Гц, 0,86H), 3,31 (дд, J=12,8, 2,1 Гц, 0,14H), 4,39-4,49 (м, 1H), 5,14 (с, 0,14H), 5,30 (с, 0,86H), 5,50 (кв, J=6,8 Гц, 0,14H), 5,71 (кв, J=6,8 Гц, 0,86H), 6,87 (дд, J=8,0, 2,8 Гц, 1H), 7,96 (дд, J=16,8, 8,0 Гц, 1H).
Синтез (Z)-(S)-4-[(S)-1-(2,6-дифторпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она
Трифенилфосфонийбромид (6,52 г) добавляли к раствору (S)-4-[(S)-1-(2,6-дифторпиридин-3-ил)этил]-2-гидрокси-6-метилморфолин-3-она (4,3 г) в ацетонитриле и реакционный раствор нагревали при кипении с обратным холодильником в течение одного часа. Триэтиламин (5,28 мл) и 3-метокси-4-(4-метил-1H-имидазол-1-ил)бензальдегид (3,42 г) добавляли к реакционному раствору, который затем нагревали при кипении с обратным холодильником в течение 1,5 часов. Реакционный раствор концентрировали при пониженном давлении и остаток разбавляли 2н. водной хлористо-водородной кислотой и этилацетатом. Затем отделяли водный слой. Органический слой промывали 2н. водной хлористо-водородной кислотой. Затем все водные слои объединяли и подщелачивали концентрированным раствором гидроксида натрия. Органический слой отделяли экстракцией из щелочного раствора этилацетатом и затем промывали насыщенным раствором бикарбоната натрия. Органический слой сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с использованием NH силикагеля (гептан:этилацетат=1:1-0:100), с получением 4,06 г указанного в заголовке соединения. Характеристические значения соответствовали таковым в примере 22.
Примеры 24 и 25
Синтез (Z)-(S)-4-[(S)-1-(2,3-дифторпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она и (Z)-(S)-4-[(R)-1-(2,3-дифторпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она
[Формула 40]
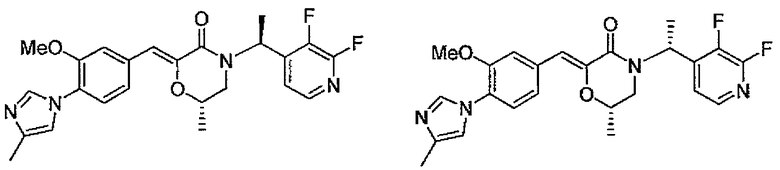
1-(2,6-дифторпиридин-3-ил)этиламин
1,13 г указанного в заголовке соединения получали из 2,3-дифторизоникотиновой кислоты (2,49 г), которая является известным соединением (см., например, Journal of Organic Chemistry, 2005, vol.70, p.3039-3045), по аналогичной методике примеров 22 и 23.
1H-ЯМР (CDCl3) δ (м.д.): 1,44 (д, J=6,8 Гц, 3H), 4,50 (кв, J=6,8 Гц, 1H), 7,33 (дд, J=4,8, 4,8 Гц, 1H), 7,94 (д, J=4,8 Гц, 1H).
Синтез (Z)-(S)-4-[(S)-1-(2,3-дифторпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она и (Z)-(S)-4-[(R)-1-(2,3-дифторпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она
Указанное в заголовке соединение (500 мг) получали в виде смеси диастереомеров из 1-(2,6-дифторпиридин-3-ил)этиламина (500 мг) в качестве исходного соединения по аналогичной методике примеров 18 и 19. Полученную смесь диастереомеров (10 мг) разделяли с помощью CHIRALPAKTM IA производства ф. Daicel Chemical Industries, Ltd. (2 см×25 см; подвижная фаза: гексан:этанол=7:3), с получением указанного в заголовке оптически активного соединения со временем удерживания 39 минут (2,6 мг) и указанного в заголовке оптически активного соединения со временем удерживания 43 минут (3,0 мг).
Характеристическое значение указанных в заголовке соединений смеси диастереомеров является следующим:
ESI-МС: m/z 455[M++H].
Характеристические значения указанного в заголовке оптически активного соединения со временем удерживания 39 минут (пример 24) являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,46 (д, J=6,8 Гц, 3H), 1,67 (д, J=7,2 Гц, 3H), 2,31 (с, 3H), 3,24 (дд, J=13,2, 9,6 Гц, 1H), 3,43 (дд, J=13,2, 2,8 Гц, 1H), 3,85 (с, 3H), 4,39 (м, 1H), 5,93 (кв, J=7,2 Гц, 1H), 6,83 (с, 1H), 6,94 (дд, J=0,8, 0,8 Гц, 1H), 7,19-7,27 (м, 2H), 7,32 (дд, J=8,4, 1,6 Гц, 1H), 7,51 (д, J=1,6 Гц, 1H), 7,79 (д, J=1,2 Гц, 1H), 7,99 (дд, J=5,2, 0,8 Гц, 1H).
Характеристические значения указанного в заголовке оптически активного соединения со временем удерживания 43 минут (пример 25) являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,49 (д, J=6,4 Гц, 3H), 1,66 (д, J=7,2 Гц, 3H), 2,32 (с, 3H), 3,29 (дд, J=12,8, 2,8 Гц, 1H), 3,54 (дд, J=12,8, 9,6 Гц, 1H), 3,85 (с, 3H), 4,34 (м, 1H), 5,97 (кв, J=7,2 Гц, 1H), 6,84 (с, 1H), 6,94 (с, 1H), 7,18-7,23 (м, 2H), 7,33 (дд, J=8,4, 1,6 Гц, 1H), 7,51 (д, J=1,6 Гц, 1H), 7,80 (д, J=1,2 Гц, 1H), 7,99 (дд, J=5,2, 0,8 Гц, 1H).
Пример 26
Синтез (Z)-(S)-4-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она
[Формула 41]

Синтез 1,2,3-трифтор-5-[(E)-пропенил]бензола
Тетракистрифенилфосфинпалладий(0) (4,66 г) и фторид цезия (21,4 г) добавляли к раствору 1-бром-3,4,5-трифторбензола (8,5 г) и транс-1-пропен-1-илбороновой кислоты (4,1 г) в диоксане (95 мл) и воде (5 мл) в атмосфере азота и реакционный раствор перемешивали при 80°C в течение пяти часов. Реакционный раствор снова доводили до комнатной температуры. Затем гексан и воду добавляли к реакционному раствору и нерастворимые вещества удаляли фильтрованием. Органический слой отделяли, затем промывали водой и нерастворимый материал вновь удаляли фильтрованием. Органический слой отделяли, затем последовательно промывали водой и насыщенным раствором соли. Органический слой сушили над безводным сульфатом магния и затем растворитель выпаривали при пониженном давлении. Полученный неочищенный продукт очищали хроматографией на колонке с силикагелем (гексан), с получением 5,83 г указанного в заголовке соединения.
1H-ЯМР (CDCl3) δ (м.д.): 1,88 (д, J=6,0 Гц, 3H), 6,18 (кв.д, J=6,0, 16,0 Гц, 1H), 6,24 (д, J=16,0 Гц, 1H), 6,85-6,96 (м, 2H).
Синтез (1S,2S)-1-(3,4,5-трифторфенил)пропан-1,2-диола
1,2,3-Трифтор-5-[(E)-пропенил]бензол (5,83 г) добавляли к охлаждаемому льдом смешанному раствору AD-Mix-((47,5 г) и метансульфонамида (3,22 г) в трет-бутаноле (170 мл) и воде (170 мл) и реакционный раствор перемешивали при 5°C в течение ночи. Затем сульфит натрия (51 г) добавляли к реакционному раствору, который затем перемешивали в течение одного часа. Реакционный раствор экстрагировали метиленхлоридом три раза. Объединенные органические слои промывали 2н. раствором гидроксида натрия и затем содержащий гидроксид натрия слой снова экстрагировали метиленхлоридом. Органические слои объединяли, сушили над безводным сульфатом магния и затем растворитель выпаривали при пониженном давлении. Полученный неочищенный продукт очищали хроматографией на колонке с силикагелем (гексан:этилацетат=9:1-1:1), с получением 5,54 г указанного в заголовке соединения.
1H-ЯМР (CDCl3) δ (м.д.): 1,12 (д, J=6,4 Гц, 3H), 2,20 (ушир.с, 1H), 2,79 (ушир.с, 1H), 3,78 (кв.д, J=6,4, 6,4 Гц, 1H), 4,34 (д, J=6,4 Гц, 1H), 6,96-7,05 (м, 2H).
Синтез (1R,2S)-1-азидо-1-(3,4,5-трифторфенил)пропан-2-ола
Таблетку гидроксида натрия (110 мг) добавляли к раствору (1S,2S)-1-(3,4,5-трифторфенил)пропан-1,2-диола (5,54 г) в диметилкарбонате (15 мл) в атмосфере азота и реакционный раствор перемешивали при 70°C в течение 45 минут. Затем наружную температуру повышали до 100°C и диметилкарбонат удаляли, продувая азотом. Затем к остатку добавляли диметилкарбонат (5 мл) и удаляли, продувая азотом. Добавляли к остатку ТГФ и нерастворимые вещества удаляли фильтрованием через целит. Затем растворитель выпаривали при пониженном давлении, с получением 6,13 г карбонатного соединения.
Воду (0,5 мл) и азид натрия (1,92 г) добавляли к раствору карбонатного соединения в ДМФА (20 мл) в атмосфере азота и реакционный раствор перемешивали при 110°C в течение ночи. Диэтиловый эфир добавляли к реакционному раствору, доведенному до комнатной температуры, и реакционный раствор последовательно промывали водой (три раза) и насыщенным раствором соли. Органический слой сушили над безводным сульфатом магния и затем растворитель выпаривали при пониженном давлении. Полученный остаток очищали хроматографией на колонке с силикагелем (гексан:этилацетат=19:1-9:1), с получением 5,16 г указанного в заголовке соединения.
1H-ЯМР (CDCl3) δ (м.д.): 1,14 (д, J=6,4 Гц, 3H), 1,79 (ушир.с, 1H), 3,97 (кв.д, J=6,4, 4,8 Гц, 1H), 4,42 (д, J=4,8 Гц, 1H), 6,96-7,05 (м, 2H).
Синтез трет-бутил[(1R,2S)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]карбамата
Трифенилфосфин (5,85 г) добавляли к раствору (1R,2S)-1-азидо-1-(3,4,5-трифторфенил)пропан-2-ола (5,16 г) в ТГФ (75 мл) в атмосфере азота и реакционный раствор перемешивали при комнатной температуре в течение 10 минут. Затем воду (5 мл) добавляли к реакционному раствору, который затем перемешивали при 60°C в течение 3,5 часов. Реакционный раствор снова доводили до комнатной температуры и ди-трет-бутилдикарбонат (5,35 г) добавляли к реакционному раствору, который затем перемешивали при комнатной температуре в течение 45 минут. Растворитель выпаривали при пониженном давлении и затем полученный остаток очищали хроматографией на колонке с силикагелем (толуол:этилацетат=9:1), с получением 5,88 г указанного в заголовке соединения.
1H-ЯМР (CDCl3) δ (м.д.): 1,07 (д, J=6,4 Гц, 3H), 1,41 (с, 9H), 4,10 (ушир.с, 1H), 4,47 (ушир.с, 1H), 5,44 (ушир.с, 1H), 6,92-7,01 (м, 2H).
Синтез (1R,2R)-2-трет-бутоксикарбониламино-1-метил-2-(3,4,5-трифторфенил)этил 4-нитробензоата
Диизопропилазодикарбоксилат (6 мл) добавляли по каплям к раствору трет-бутил[(1R,2S)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]карбамата (5,88 г), 4-нитробензойной кислоты (4,84 г) и трифенилфосфина (7,59 г) в ТГФ (100 мл) при охлаждении льдом в атмосфере азота и реакционный раствор перемешивали при комнатной температуре в течение двух часов. Растворитель выпаривали при пониженном давлении и полученный остаток очищали хроматографией на колонке с силикагелем (толуол:этилацетат=97:3). Затем полученный порошок растирали в смеси толуол-гексан, с получением 6,69 г указанного в заголовке соединения.
1H-ЯМР (CDCl3) δ (м.д.): 1,37 (с, 9H), 1,38 (д, J=6,4 Гц, 3H), 4,85 (ушир.с, 1H), 5,16 (д, J=9,2 Гц, 1H), 5,41 (кв.д, J=6,4, 6,0 Гц, 1H), 6,92-7,01 (м, 2H), 8,16 (д, J=8,8 Гц, 2H), 8,29 (д, J=8,8 Гц, 2H).
Синтез трет-бутил[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]карбамата
Порошок карбоната калия (6,43 г) добавляли к смешанному раствору (1R,2R)-2-трет-бутоксикарбониламино-1-метил-2-(3,4,5-трифторфенил)этил 4-нитробензоата (7,03 г) в смеси метанол (90 мл)-ТГФ (10 мл) и реакционный раствор перемешивали при комнатной температуре в течение одного часа. Этилацетат добавляли к реакционному раствору, который затем последовательно промывали водой и насыщенным раствором соли (два раза). Органический слой сушили над безводным сульфатом магния и растворитель выпаривали при пониженном давлении. Диэтиловый эфир добавляли к полученному остатку и нерастворимые вещества удаляли фильтрованием. Фильтрат концентрировали и полученный остаток очищали хроматографией на колонке с силикагелем (толуол:этилацетат=6:1), с получением 4,49 г указанного в заголовке соединения.
1H-ЯМР (CDCl3) δ (м.д.): 1,28 (д, J=6,4 Гц, 3H), 1,44 (с, 9H), 4,01 (ушир.с, 1H), 4,48 (ушир.с, 1H), 5,35 (ушир.с, 1H), 6,90-7,00 (м, 2H).
Синтез трет-бутил[(1R,2R)-2-трет-бутилдифенилсиланилокси-1-(3,4,5-трифторфенил)пропил]карбамата
трет-Бутилхлордифенилсилан (2,0 мл) добавляли четырьмя порциями к раствору трет-бутил[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]карбамата (610 мг) и имидазола (817 мг) в ДМФА (3 мл) в атмосфере азота и реакционный раствор перемешивали при комнатной температуре в течение трех часов. Этилацетат добавляли к реакционному раствору, который затем последовательно промывали водой, 1н. хлористо-водородной кислотой, водой, насыщенным раствором бикарбоната натрия и насыщенным раствором соли. Органический слой сушили над безводным сульфатом магния и затем растворитель выпаривали при пониженном давлении. Полученный остаток очищали хроматографией на колонке с силикагелем (гексан:диэтиловый эфир=49:1-19:1), с получением 684 мг указанного в заголовке соединения.
1H-ЯМР (CDCl3) δ (м.д.): 0,95 (с, 9H), 1,13 (д, J=6,4 Гц, 3H), 1,47 (с, 9H), 4,02 (ушир.с, 1H), 4,46 (ушир.с, 1H), 5,34 (ушир.с, 1H), 6,69-6,80 (м, 2H), 7,28-7,46 (м, 8H), 7,55 (д, J=8,4 Гц, 2H).
Синтез (1R,2R)-2-трет-бутилдифенилсиланилокси-1-(3,4,5-трифторфенил)пропиламина
Трифторуксусную кислоту (0,5 мл) добавляли к раствору трет-бутил[(1R,2R)-2-трет-бутилдифенилсиланилокси-1-(3,4,5-трифторфенил)пропил]карбамата (370 мг) в метиленхлориде (2 мл) и реакционный раствор перемешивали при комнатной температуре в течение 11 часов. Насыщенный раствор бикарбоната натрия добавляли к реакционному раствору и затем смесь экстрагировали этилацетатом. Органический слой промывали насыщенным раствором бикарбоната натрия и насыщенным раствором соли и затем растворитель выпаривали при пониженном давлении, с получением 275 мг указанного в заголовке соединения.
1H-ЯМР (CDCl3) δ (м.д.): 0,93 (д, J=6,4 Гц, 3H), 1,02 (с, 9H), 3,81 (д, J=4,8 Гц, 1H), 3,91 (д.кв, J=4,8, 6,0 Гц, 1H), 6,88-6,97 (м, 2H), 7,32-7,46 (м, 6H), 7,57 (д, J=8,0 Гц, 2H), 7,55 (д, J=8,0 Гц, 2H).
Синтез (S)-1-[(1R,2R)-2-трет-бутилдифенилсиланилокси-1-(3,4,5-трифторфенил)пропиламино]пропан-2-ола
Раствор (S)-(-)-пропиленоксида (0,1 мл) и (1R,2R)-2-трет-бутилдифенилсиланилокси-1-(3,4,5-трифторфенил)пропиламина (212 мг) в диэтиловом эфире (1 мл) добавляли к суспензии перхлората лития (750 мг) в диэтиловом эфире (1 мл) и реакционный раствор перемешивали в атмосфере азота при комнатной температуре в течение ночи. Метиленхлорид и ледяную воду добавляли к реакционному раствору. После перемешивания реакционного раствора органический слой отделяли. Водный слой снова экстрагировали метиленхлоридом. Органические слои объединяли, сушили над безводным сульфатом магния и затем растворитель концентрировали при пониженном давлении. Полученный остаток очищали хроматографией на колонке с силикагелем (этилацетат:гептан=9:1-4:1), с получением 172 мг указанного в заголовке соединения.
1H-ЯМР (CDCl3) δ (м.д.): 0,83 (д, J=6,0 Гц, 3H), 1,06 (с, 9H), 1,08 (м, 3H), 2,20-2,50 (м, 3H), 3,47 (ушир.с, 1H), 3,59 (ушир.с, 1H), 3,86 (ушир.с, 1H), 6,78-6,95 (м, 2H), 7,36-7,48 (м, 6H), 7,67 (д, J=6,8 Гц, 4H).
Синтез (S)-4-[(1R,2R)-2-трет-бутилдифенилсиланилокси-1-(3,4,5-трифторфенил)пропил]-6-метилморфолин-2,3-диона
Оксалилхлорид (45 мкл) добавляли по каплям к раствору (S)-1-[(1R,2R)-2-трет-бутилдифенилсиланилокси-1-(3,4,5-трифторфенил)пропиламино]пропан-2-ола (171 мг), TEA (0,17 мл) и 4-(N,N-диметиламино)пиридина (8 мг) в метиленхлориде (2 мл) при охлаждении льдом в атмосфере азота и реакционный раствор перемешивали при той же температуре в течение двух часов. Ледяную воду добавляли к реакционному раствору и затем смесь экстрагировали этилацетатом. Затем органический слой последовательно промывали водой, 1н. хлористо-водородной кислотой, водой, насыщенным раствором бикарбоната натрия и насыщенным раствором соли. Органический слой сушили над безводным сульфатом магния и растворитель выпаривали при пониженном давлении. Полученный остаток очищали хроматографией на колонке с силикагелем (гептан:этилацетат=9:1-3:1), с получением 96 мг указанного в заголовке соединения.
1H-ЯМР (CDCl3) δ (м.д.): 1,02 (с, 9H), 1,19 (д, J=6,0 Гц, 3H), 1,28 (д, J=6,4 Гц, 3H), 3,20 (дд, J=5,6, 13,2 Гц, 1H), 3,68 (дд, J=2,4, 13,2 Гц, 1H), 4,42 (д.кв, J=5,6, 6,0 Гц, 1H), 4,62 (ддкв, J=2,4, 5,6, 6,4 Гц, 1H), 5,51 (д, J=5,6 Гц, 1H), 6,82-6,94 (м, 2H), 7,40-7,54 (м, 6H), 7,62 (д, J=8,0 Гц, 2H), 7,67 (д, J=8,0 Гц, 2H).
Синтез (S)-4-[(1R,2R)-2-трет-бутилдифенилсиланилокси-1-(3,4,5-трифторфенил)пропил]-2-гидрокси-6-метилморфолин-3-она
Раствор три-втор-бутилборогидрида лития (1,06 моль) в ТГФ (0,25 мл) добавляли по каплям к раствору (S)-4-[(1R,2R)-2-трет-бутилдифенилсиланилокси-1-(3,4,5-трифторфенил)пропил]-6-метилморфолин-2,3-диона (95 мг) в ТГФ (3 мл) в атмосфере азота при -20°C и реакционный раствор перемешивали при той же температуре в течение 30 минут. 5н. Раствор гидроксида натрия (0,03 мл) и 30% водный пероксид водорода (0,07 мл) добавляли к реакционному раствору, который затем перемешивали при охлаждении льдом в течение одного часа. Затем порошок бисульфита натрия (20 мг) добавляли и реакционный раствор перемешивали при комнатной температуре в течение 30 минут. Насыщенный раствор соли добавляли к реакционному раствору и затем экстрагировали этилацетатом. Органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом магния и затем растворитель выпаривали при пониженном давлении. Полученный остаток очищали хроматографией на колонке с силикагелем (гептан:этилацетат=1:1), с получением 93 мг указанного в заголовке соединения.
1H-ЯМР (CDCl3) δ (м.д.): 1,01 (с, 9H), 1,11 (д, J=6,0 Гц, 3H), 1,19 (д, J=6,4 Гц, 3H), 2,88 и 2,99 (дд, J=12,0, 12,0 Гц, 1H), 3,12 и 3,48 (дд, J=2,4, 12,0 Гц, 1H), 3,16 и 3,91 (д, J=2,8 Гц, 1H), 4,35-4,55 (м, 2H), 5,11 и 5,30 (д, J=3,6 Гц, 1H), 5,40 и 5,49 (д, J=6,8 Гц, 1H), 6,79-6,94 (м, 2H), 7,38-7,54 (м, 6H), 7,65 (д, J=8,0 Гц, 2H), 7,69 (д, J=8,0 Гц, 2H).
Синтез (Z)-(S)-4-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она
Раствор (S)-4-[(1R,2R)-2-трет-бутилдифенилсиланилокси-1-(3,4,5-трифторфенил)пропил]-2-гидрокси-6-метилморфолин-3-она (92 мг) и трифенилфосфингидробромида (68 мг) в ацетонитриле (4 мл) нагревали при кипении с обратным холодильником в атмосфере азота в течение одного часа. Растворитель выпаривали при пониженном давлении и полученный остаток растворяли в этаноле (4 мл). К полученному реакционному раствору добавляли 3-метокси-4-(4-метил-1H-имидазол-1-ил)бензальдегид, полученный в примере 1 (40 мг), и TEA (0,12 мл) и реакционный раствор перемешивали в атмосфере азота при комнатной температуре в течение ночи. Растворитель выпаривали при пониженном давлении. Полученный остаток растворяли в трифторуксусной кислоте (1 мл) и реакционный раствор перемешивали при комнатной температуре в течение двух часов. Реакционный раствор вливали в насыщенный раствор бикарбоната натрия и затем экстрагировали этилацетатом. Органический слой промывали насыщенным раствором бикарбоната натрия и насыщенным раствором соли и затем растворитель выпаривали при пониженном давлении. Полученный остаток очищали колоночной хроматографией с использованием NH силикагеля (гептан:этилацетат=1:1-0:1), с получением 61,9 мг указанного в заголовке соединения.
1H-ЯМР (CDCl3) δ (м.д.): 1,33 (д, J=6,0 Гц, 3H), 1,42 (д, J=6,0 Гц, 3H), 2,34 (с, 3H), 3,20 (дд, J=9,6, 12,8 Гц, 1H), 3,61 (дд, J=2,4, 12,8 Гц, 1H), 3,85 (с, 3H), 4,42-4,52 (м, 2H), 5,35 (д, J=6,8 Гц, 1H), 6,85 (с, 1H), 6,95 (с, 1H), 7,06-7,15 (м, 2H), 7,22 (д, J=8,0 Гц, 1H), 7,33 (дд, J=1,6, 8,0 Гц, 1H), 7,53 (д, J=1,6 Гц, 1H), 7,86 (с, 1H).
ESI-МС; m/z 502[M++H].
Пример 27
Синтез (Z)-4-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-она
[Формула 42]

3,15 мг указанного в заголовке соединения получали из (1R,2R)-2-трет-бутилдифенилсиланилокси-1-(3,4,5-трифторфенил)пропиламина, полученного в примере 26 (280 мг), и изобутиленоксида (63 мкл) в качестве исходных соединений по аналогичной методике примера 26.
1H-ЯМР (CDCl3) δ (м.д.): 1,28 (с, 3H), 1,34 (д, J=6,0 Гц, 3H), 1,47 (с, 3H), 2,31 (с, 3H)3,19 (д, J=12,8 Гц, 1H), 3,61 (д, J=12,8 Гц, 1H), 3,85 (с, 3H), 4, 46 (д.кв, J=6,8, 6,0 Гц, 1H), 5,40 (д, J=6,8 Гц, 1H), 6,91 (с, 1H), 6,93 (с, 1H), 7,09-7,17 (м, 2H), 7,21 (д, J=8,4 Гц, 1H), 7,32 (дд, J=1,6, 8,4 Гц, 1H), 7,53 (д, J=1,6 Гц, 1H), 7,77 (с, 1H).
ESI-МС; m/z 516[M++H].
Пример 28
Синтез (Z)-4-[(R)-1-(4-фторфенил)-2-гидроксиэтил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-она
[Формула 43]
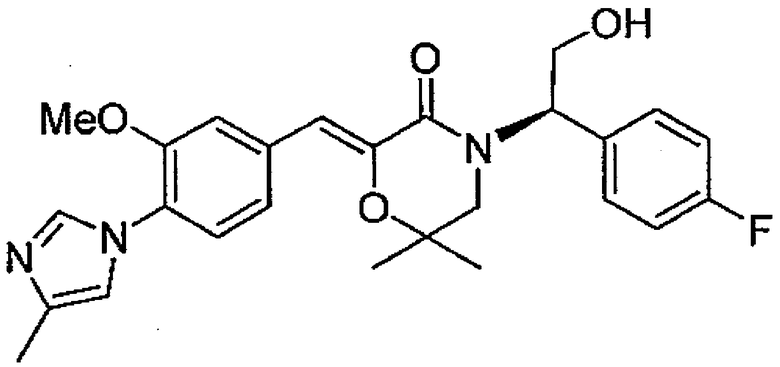
3,48 мг указанного в заголовке соединения получали из (R)-2-трет-бутилдифенилсиланилокси-1-(4-фторфенил)этиламина (300 мг) и изобутиленоксида (101 мкл) в качестве исходных соединений по аналогичной методике примера 26.
1H-ЯМР (CDCl3) δ (м.д.): 1,25 (с, 3H), 1,43 (с, 3H), 2,34 (с, 3H), 3,06 (д, J=12,8 Гц, 1H), 3,39 (д, J=12,8 Гц, 1H), 3,84 (с, 3H), 4,12-4,23 (м, 2H), 5,87 (дд, J=6,0, 2,4 Гц, 1H), 6,88 (с, 1H), 6,94 (с, 1H), 7,04-7,09 (м, 2H), 7,19 (дд, J=8,4, 4,8 Гц, 1H), 7,29-7,34 (м, 3H), 7,52 (д, J=4,8 Гц, 1H), 7,92 (с, 1H).
ESI-МС; m/z 466[M++H].
Пример 29
Синтез (Z)-(6R)-4-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она
[Формула 44]

144 мг указанного в заголовке соединения получали из (1R,2R)-2-трет-бутилдифенилсиланилокси-1-(3,4,5-трифторфенил)пропиламина, полученного в примере 26 (500 мг), и (R)-(+)-пропиленоксида (0,12 мл) в качестве исходных соединений по аналогичной методике примера 26.
1H-ЯМР (CDCl3) δ (м.д.): 1,33 (д, J=6,4 Гц, 3H), 1,42 (д, J=6,4 Гц, 3H), 2,30 (с, 3H), 3,25 (дд, J=12,8, 2,4 Гц, 1H), 3,62 (дд, J=12,8, 10,0 Гц, 1H), 3,84 (с, 3H), 4,19 (ддд, J=10,0, 6,4, 2,4 Гц, 1H), 4,50 (тд, J=6,4, 6,0 Гц, 1H), 5,41 (д, J=6,0 Гц, 1H), 6,86 (с, 1H), 6,93 (с, 1H), 7,05-7,16 (м, 2H), 7,20 (д, J=8,0 Гц, 1H), 7,32 (дд, J=8,0, 1,6 Гц, 1H), 7,51 (д, J=1,6 Гц, 1H), 7,74 (с, 1H).
Пример 30
Синтез (Z)-4-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]морфолин-3-она
[Формула 45]

Синтез этил[(1R,2R)-2-трет-бутилдифенилсиланилокси-1-(3,4,5-трифторфенил)пропиламино]ацетата
Карбонат цезия (242 мг) и этилбромацетат (103 мкл) добавляли к раствору (1R,2R)-2-трет-бутилдифенилсиланилокси-1-(3,4,5-трифторфенил)пропиламина, полученного в примере 26 (274 мг), в ДМФА (5 мл) и реакционный раствор перемешивали при комнатной температуре в течение 11 часов. Ледяную воду и этилацетат добавляли к реакционному раствору и органический слой отделяли. Органический слой последовательно промывали полунасыщенным раствором соли и насыщенным раствором соли, сушили над безводным сульфатом магния и затем растворитель выпаривали при пониженном давлении. Полученный остаток очищали хроматографией на колонке с силикагелем (гексан:диэтиловый эфир=19:1), с получением 190 мг указанного в заголовке соединения.
1H-ЯМР (CDCl3) δ (м.д.): 0,75 (д, J=6,4 Гц, 3H), 1,09 (с, 9H), 1,26 (т, J=7,2 Гц, 3H), 3,03 (д, J=16,8 Гц, 1H), 3,24 (д, J=16,8 Гц, 1H), 3,57 (д, J=6,8 Гц, 1H), 3,80-3,92 (м, 1H), 4,19 (кв, J=7,2 Гц, 2H), 6,88-6,98 (м, 2H), 7,36-7,48 (м, 6H), 7,67-7,77 (м, 4H).
Синтез 2-[(1R,2R)-2-трет-бутилдифенилсиланилокси-1-(3,4,5-трифторфенил)пропиламино]этанола
Борогидрид лития (20 мг) добавляли к раствору этил[(1R,2R)-2-трет-бутилдифенилсиланилокси-1-(3,4,5-трифторфенил)пропиламино]ацетата (158 мг) в ТГФ (3 мл) в атмосфере азота и реакционный раствор перемешивали при комнатной температуре в течение одних суток. Насыщенный раствор сульфата натрия добавляли к реакционному раствору и затем выпавшие в осадок нерастворимые вещества удаляли фильтрованием через целит. Метанол добавляли к фильтрату и затем растворитель выпаривали при пониженном давлении. Полученный остаток очищали хроматографией на колонке с силикагелем (гептан:этилацетат=4:1), с получением 103 мг указанного в заголовке соединения.
ESI-МС: m/z 488[MH+].
Синтез 4-[(1R,2R)-2-трет-бутилдифенилсиланилокси-1-(3,4,5-трифторфенил)пропил]морфолин-2,3-диона
Раствор 2-[(1R,2R)-2-трет-бутилдифенилсиланилокси-1-(3,4,5-трифторфенил)пропиламино]этанола (102 мг) в диэтилоксалате (2 мл) перемешивали при 170°C в течение одного часа и 30 минут. Диэтилоксалат выпаривали при пониженном давлении и полученный остаток очищали хроматографией на колонке с силикагелем (гептан:этилацетат=9:1-6:1), с получением 48 мг указанного в заголовке соединения.
1H-ЯМР (CDCl3) δ (м.д.): 0,99 (с, 9H), 1,18 (д, J=6,0 Гц, 3H), 3,47 (ддд, J=14,0, 5,6, 3,2 Гц, 1H), 3,83 (ддд, J=14,0, 8,0, 3,6 Гц, 1H), 4,27-4,43 (м, 3H), 5,54 (д, J=5,2 Гц, 1H), 6,80-6,90 (м, 2H), 7,36-7,54 (м, 6H), 7,62 (д, J=8,0 Гц, 2H), 7,67 (д, J=8,0 Гц, 2H).
Синтез (Z)-4-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]морфолин-3-она
18 мг указанного в заголовке соединения получали из 4-[(1R,2R)-2-трет-бутилдифенилсиланилокси-1-(3,4,5-трифторфенил)пропил]морфолин-2,3-диона (47 мг) по аналогичной методике примера 26.
1H-ЯМР (CDCl3) δ (м.д.): 1,33 (д, J=6,0 Гц, 3H), 2,40 (с, 3H), 3,41 (ддд, J=13,2, 6,4, 3,2 Гц, 1H), 3,81 (ддд, J=13,2, 7,2, 3,2 Гц, 1H), 3,87 (с, 3H), 4,17 (ддд, J=11,2, 7,2, 3,2 Гц, 1H), 4,30 (ддд, J=11,2, 6,4, 3,2 Гц, 1H), 4,51 (дт, J=6,4, 6,0 Гц, 1H), 5,42 (д, J=6,4 Гц, 1H), 6,88 (с, 1H), 6,98 (с, 1H), 7,08-7,17 (м, 2H), 7,23 (д, J=8,0 Гц, 1H), 7,40 (дд, J=8,0, 1,6 Гц, 1H), 7,43 (д, J=1,6 Гц, 1H), 8,04 (с, 1H).
Пример 31
Синтез (Z)-4-[(1R,2R)-1-(3,4-дифторфенил)-2-гидроксипропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]морфолин-3-она
[Формула 46]
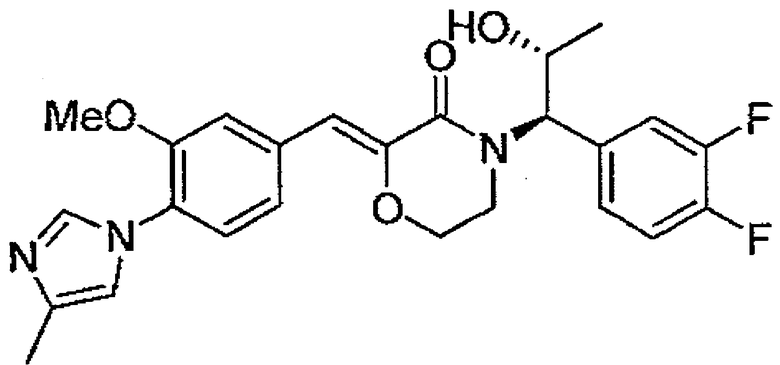
Синтез (1R,2R)-2-трет-бутилдифенилсиланилокси-1-(3,4-дифторфенил)пропиламина
5,37 г указанного в заголовке соединения получали из 1-бром-3,4-дифторбензола (19 г) по аналогичной методике примера 26. Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 0,86 (д, J=6,4 Гц, 3H), 1,03 (с, 9H), 3,82 (д, J=6,0 Гц, 1H), 3,89 (дкв, J=6,4, 6,0 Гц, 1H), 6,95-7,13 (м, 3H), 7,32-7,44 (м, 6H), 7,59 (дд, J=7,2, 2,8 Гц, 2H), 7,65 (дд, J=7,2, 2,8 Гц, 2H).
Синтез (Z)-4-[(1R,2R)-1-(3,4-дифторфенил)-2-гидроксипропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]морфолин-3-она
7,3 мг указанного в заголовке соединения получали из (1R,2R)-2-трет-бутилдифенилсиланилокси-1-(3,4-дифторфенил)пропиламина (825 мг) по аналогичной методике примера 26. Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,33 (д, J=6,4 Гц, 3H), 2,29 (с, 3H), 3,38 (м, 1H), 3,76 (м, 1H), 3,84 (с, 3H), 4,13 (м, 1H), 4,27 (м, 1H), 4,51 (д.кв, J=7,6, 6,4 Гц, 1H), 5,44 (д, J=7,6 Гц, 1H), 6,87 (с, 1H), 6,92 (с, 1H), 7,14-7,20 (м, 3H), 7,27-7,39 (м, 3H), 7,70 (с, 1H).
Пример 32
Синтез (Z)-(S)-4-[(1R,2R)-1-(4-фторфенил)-2-гидроксипропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она
[Формула 47]

Синтез (1R,2R)-2-трет-бутилдифенилсиланилокси-1-(4-фторфенил)пропиламина
113 мг указанного в заголовке соединения получали из 1-бром-4-фторбензола по аналогичной методике примера 26. Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 0,83 (д, J=6,4 Гц, 3H), 1,03 (с, 9H), 3,85 (д, J=6,0 Гц, 1H), 3,92 (дкв, J=6,4, 6,0 Гц, 1H), 6,92-6,97 (м, 2H), 7,21-7,25 (м, 2H), 7,31-7,43 (м, 6H), 7,59 (дд, J=7,2, 2,8 Гц, 2H), 7,66 (дд, J=7,2, 2,8 Гц, 2H).
Синтез (Z)-(S)-4-[(1R,2R)-1-(4-фторфенил)-2-гидроксипропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она
Указанное в заголовке соединение получали из (1R,2R)-2-трет-бутилдифенилсиланилокси-1-(4-фторфенил)пропиламина по аналогичной методике примера 26. Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,30 (д, J=6,0 Гц, 3H), 1,38 (д, J=6,4 Гц, 3H), 2,29 (с, 3H), 3,12 (дд, J=12,8, 10,0 Гц, 1H), 3,51 (дд, J=12,8, 2,8 Гц, 1H), 3,83 (с, 3H), 4,39-4,50 (м, 2H), 5,41 (д, J=7,6 Гц, 1H), 6,84 (с, 1H), 6,92 (с, 1H), 7,04-7,08 (м, 2H), 7,19 (д, J=8,0 Гц, 1H), 7,30-7,38 (м, 3H), 7,50 (с, 1H), 7,70 (с, 1H).
Пример 33
Синтез (Z)-4-[(1R,2R)-1-(4-фторфенил)-2-гидроксипропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-она
[Формула 48]
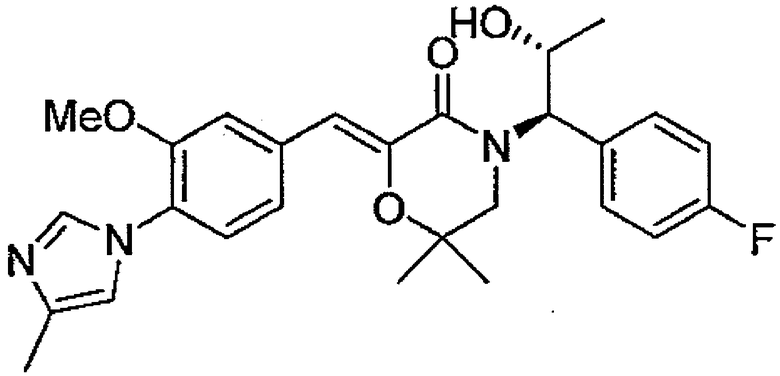
259 мг указанного в заголовке соединения получали из (1R,2R)-2-трет-бутилдифенилсиланилокси-1-(4-фторфенил)пропиламина по аналогичной методике примера 27. Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,20 (с, 3H), 1,31 (д, J=6,0 Гц, 3H), 1,43 (с, 3H), 2,29 (с, 3H), 3,15 (д, J=12,8 Гц, 1H), 3,52 (д, J=12,8 Гц, 1H), 3,83 (с, 3H), 4,45 (д.кв, J=8,8, 6,0 Гц, 1H), 5,47 (д, J=8,8 Гц, 1H), 6,89 (с, 1H), 6,91 (с, 1H), 7,03-7,08 (м, 2H), 7,18 (д, J=8,0 Гц, 1H), 7,30 (дд, J=8,0, 1,6 Гц, 1H), 7,36-7,40 (м, 2H), 7,52 (д, J=1,6 Гц, 1H), 7,70 (с, 1H).
Пример 34
Синтез (Z)-(S)-4-[(1R,2R)-1-(3,4-дифторфенил)-2-гидроксипропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она
[Формула 49]

198 мг указанного в заголовке соединения получали из (1R,2R)-2-трет-бутилдифенилсиланилокси-1-(3,4-дифторфенил)пропиламина по аналогичной методике примера 26. Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,32 (д, J=6,4 Гц, 3H), 1,40 (д, J=6,0 Гц, 3H), 2,29 (с, 3H), 3,16 (дд, J=12,8, 10,0 Гц, 1H), 3,56 (дд, J=12,8, 2,8 Гц, 1H), 3,83 (с, 3H), 4,41-4,48 (м, 2H), 5,38 (д, J=7,6 Гц, 1H), 6,84 (с, 1H), 6,92 (с, 1H), 7,11-7,20 (м, 3H), 7,26-7,32 (м, 2H), 7,50 (с, 1H), 7,70 (с, 1H).
Пример 35
Синтез (Z)-4-[(1R,2R)-1-(3,4-дифторфенил)-2-гидроксипропил]-2-[1-[3-метокси-4-(метилимидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-она
[Формула 50]

172 мг указанного в заголовке соединения получали из (1R,2R)-2-трет-бутилдифенилсиланилокси-1-(3,4-дифторфенил)пропиламина по аналогичной методике примера 27. Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,24 (с, 3H), 1,33 (д, J=6,4 Гц, 3H), 1,45 (с, 3H), 2,29 (с, 3H), 3,17 (д, J=12,8 Гц, 1H), 3,56 (д, J=12,8 Гц, 1H), 3,84 (с, 3H), 4,45 (д.кв, J=7,6, 6,4 Гц, 1H), 5,42 (д, J=7,6 Гц, 1H), 6,89 (с, 1H), 6,91 (с, 1H), 7,14-7,20 (м, 3H), 7,27-7,32 (м, 2H), 7,52 (с, 1H), 7,70 (с, 1H).
Пример 36
Синтез (Z)-(S)-4-[(S)-2-гидрокси-1-метил-1-(3,4,5-трифторфенил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она
[Формула 51]

2,2 мг указанного в заголовке соединения получали из (S)-4-[(S)-2-трет-бутилдифенилсиланилокси-1-метил-1-(3,4,5-трифторфенил)этил]морфолин-2,3-диона по аналогичной методике примера 26, используя (R)-2-трет-бутилдифенилсиланилокси-1-метил-1-(3,4,5-трифторфенил)этиламин, полученный в соответствии с публикацией (например, J. Org. Chem. 2001, 66, p.8778), в качестве исходного соединения. Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,43 (д, J=6,4 Гц, 3H), 1,70 (с, 3H), 2,32 (с, 3H), 3,14 (м, 1H), 3,20 (м, 1H), 3,72 (д, J=12,8 Гц, 1H), 3,86 (с, 3H), 4,14 (д, J=12,8 Гц, 1H), 4,33 (м, 1H), 6,79 (с, 1H), 6,95 (с, 1H), 6,95-7,01 (м, 2H), 7,22 (д, J=8,0 Гц, 1H), 7,34 (д, J=8,0 Гц, 1H), 7,50 (с, 1H), 7,85 (с, 1H).
Пример 37
Синтез (Z)-(6S)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метил-4-[(S)-1-(3,4,5-трифторфенил)этил]морфолин-3-она
[Формула 52]

Синтез (R)-1-(3,4,5-трифторфенил)этанола
К раствору (+)-DIP-хлорида (11,8 г) в ТГФ (200 мл), охлажденному до -30°C, добавляли по каплям 3,4,5-трифторацетофенон (5,0 г) [CAS 220141-73-1] в атмосфере азота. Реакционный раствор перемешивали при той же температуре в течение пяти часов и при комнатной температуре в течение одного часа, и затем ТГФ выпаривали при пониженном давлении. К раствору полученного остатка в диэтиловом эфире (150 мл) добавляли по каплям 6,5 мл диэтаноламина и реакционный раствор перемешивали при комнатной температуре в течение ночи. Нерастворимые вещества удаляли фильтрованием и затем выпаривали растворитель. К полученному остатку добавляли гексан и нерастворимые вещества снова удаляли фильтрованием. Фильтрат очищали хроматографией на колонке с силикагелем (гептан:этилацетат=19:1-4:1), с получением 3,69 г указанного в заголовке соединения.
1H-ЯМР (CDCl3) δ (м.д.): 1,46 (д, J=6,8 Гц, 3H), 4,85 (кв, J=6,8, 1H), 6,98-7,05 (м, 2H).
Синтез 5-((S)-1-азидоэтил)-1,2,3-трифторбензола
К раствору (R)-1-(3,4,5-трифторфенил)этанола (3,6 г) и дифенилфосфорного азида (6,0 мл) в толуоле (70 мл) добавляли по каплям при охлаждении льдом 1,8-диазабицикло[5,4,0]ундец-7-ен (4,1 мл). Реакционный раствор перемешивали при той же температуре в течение одного часа и при комнатной температуре в течение ночи. Воду добавляли к реакционному раствору и органический слой отделяли. Затем водный слой снова экстрагировали толуолом. Органические слои объединяли и последовательно промывали 1н. хлористо-водородной кислотой, водой, насыщенным раствором бикарбоната натрия и насыщенным раствором соли. Органические слои сушили над безводным сульфатом магния и затем растворитель выпаривали при пониженном давлении. Полученный остаток очищали хроматографией на колонке с силикагелем (гептан:этилацетат=49:1), с получением 858 мг указанного в заголовке соединения.
1H-ЯМР (CDCl3) δ (м.д.): 1,50 (д, J=6,8 Гц, 3H), 4,56 (кв, J=6,8, 1H), 6,92-7,01 (м, 2H).
Синтез (S)-1-(3,4,5-трифторфенил)этиламина
Трифенилфосфин (1,23 г) добавляли к раствору 5-((S)-1-азидоэтил)-1,2,3-трифторбензола (858 мг) в ТГФ (20 мл) в атмосфере азота и реакционный раствор перемешивали при комнатной температуре в течение пяти минут. Затем воду (2,5 мл) добавляли к реакционному раствору, который затем перемешивали при 60°C в течение 2,5 часов. Реакционный раствор снова доводили до комнатной температуры и затем экстрагировали 2н. хлористо-водородной кислотой (два раза). Содержащий хлористо-водородную кислоту экстракционный слой промывали этилацетатом и затем подщелачивали 5н. раствором гидроксида натрия и затем экстрагировали метиленхлоридом (два раза). Метиленхлоридный слой сушили над безводным сульфатом магния и растворитель выпаривали при пониженном давлении, с получением 348 мг указанного в заголовке соединения. Затем выполняли следующую операцию, чтобы выделить указанное в заголовке соединение, оставшееся в разбавленном этилацетатом реакционном растворе. Диэтиловый эфир добавляли к разбавленному раствору и затем смесь экстрагировали водой. Водный экстракционный слой промывали диэтиловым эфиром и затем подщелачивали 5н. раствором гидроксида натрия и затем экстрагировали метиленхлоридом (два раза). Метиленхлоридный слой сушили над безводным сульфатом магния и растворитель выпаривали при пониженном давлении, с получением 413 мг указанного в заголовке соединения.
1H-ЯМР (CDCl3) δ (м.д.): 1,33 (д, J=6,4 Гц, 3H), 4,08 (кв, J=6,4, 1H), 6,95-7,04 (м, 2H).
Синтез (Z)-(6S)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метил-4-[(S)-1-(3,4,5-трифторфенил)этил]морфолин-3-она
882 мг указанного в заголовке соединения получали из (S)-1-(3,4,5-трифторфенил)этиламина (1,15 г) и (S)-(-)-пропиленоксида (0,46 мл) в качестве исходных соединений по аналогичной методике примеров 18 и 19.
1H-ЯМР (CDCl3) δ (м.д.): 1,40 (д, J=6,4 Гц, 3H), 1,54 (д, J=7,2 Гц, 3H), 2,29 (с, 3H), 2,96 (дд, J=12,8, 5,6 Гц, 1H), 3,20 (дд, J=12,8, 3,2 Гц, 1H), 3,85 (с, 3H), 4,30-4,40 (м, 1H), 6,04 (кв, J=7,2 Гц, 1H), 6,88 (с, 1H), 6,92 (д, J=1,2 Гц, 1H), 6,92-7,00 (м, 2H), 7,20 (д, J=8,0 Гц, 1H), 7,33 (дд, J=8,0, 1,6 Гц, 1H), 7,50 (д, J=1,6 Гц, 1H), 7,86 (д, J=1,2 Гц, 1H).
Пример 38
Синтез (Z)-(6S)-4-[1-(4-фторфенил)-1-метилэтил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она
[Формула 53]
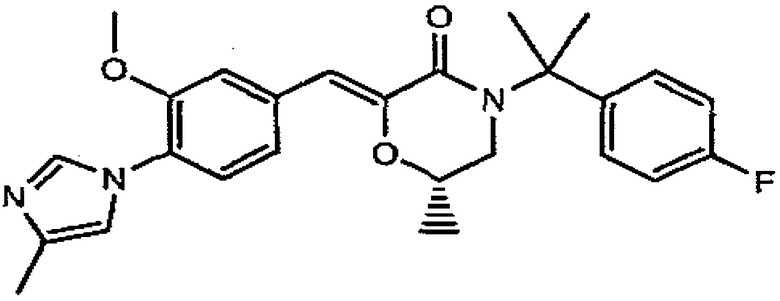
97,8 мг указанного в заголовке соединения получали из 1-(4-фторфенил)-1-метилэтиламина (500 мг) [CAS #17797-10-3] и (S)-(-)-пропиленоксида (0,23 мл) в качестве исходных соединений по аналогичной методике примера 26.
1H-ЯМР (CDCl3) δ (м.д.): 1,50 (д, J=6,0 Гц, 3H), 1,76 (с, 3H), 1,77 (с, 3H), 2,28 (с, 3H), 3,49 (дд, J=13,2, 9,6 Гц, 1H), 3,56 (дд, J=13,2, 2,8 Гц, 1H), 3,82 (с, 3H), 4,38 (дтд, J=9,6, 6,0, 2,8 Гц, 1H), 6,66 (с, 1H), 6,91 (с, 1H), 7,00 (дд, J=8,8, 8,8 Гц, 2H), 7,16 (д, J=8,0 Гц, 1H), 7,24-7,33 (м, 3H), 7,45 (д, J=1,2 Гц, 1H), 7,68 (д, J=1,6 Гц, 1H).
Пример 39
Синтез (Z)-(6S)-4-[1-(4-фторфенил)циклопропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она
[Формула 54]

213 мг указанного в заголовке соединения получали из 1-(4-фторфенил)циклопропиламина (726 мг) [CAS #474709-83-6] и (S)-(-)-пропиленоксида (0,4 мл) в качестве исходных соединений по аналогичной методике примера 26.
1H-ЯМР (CDCl3) δ (м.д.): 1,30-1,42 (м, 4H), 1,44 (д, J=6,0 Гц, 3H), 2,29 (с, 3H), 3,47 (дд, J=12,8, 3,2 Гц, 1H), 3,53 (дд, J=12,8, 9,6 Гц, 1H), 3,84 (с, 3H), 4,33 (дтд, J=9,6, 6,0, 3,2 Гц, 1H), 6,82 (с, 1H), 6,92 (д, J=1,2 Гц, 1H), 6,99 (дд, J=8,8, 8,8 Гц, 2H), 7,18 (д, J=8,0 Гц, 1H), 7,30 (дд, J=8,0, 2,0 Гц, 1H), 7,35 (дд, J=8,8, 5,2 Гц, 2H), 7,49 (д, J=2,0 Гц, 1H), 7,68 (д, J=1,2 Гц, 1H).
Пример 40
Синтез (Z)-(6S,9aR)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)бензилиден]-6-(3,4,5-трифторфенил)гексагидропиридо[2,1-c][1,4]оксазин-4-она
[Формула 55]

Синтез метил (R)-2-трет-бутоксикарбониламино-6-оксо-6-(3,4,5-трифторфенил)гексаноата
К раствору 2-метилового эфира 1-трет-бутилового эфира (R)-6-оксопиперидин-1,2-дикарбоновой кислоты (CAS No. 183890-36-0, 7,5 г) в ТГФ (200 мл) добавляли по каплям при -40°C 3,4,5-трифторфенилмагнийбромид (0,35М раствор в диэтиловом эфире, 100 мл) и реакционный раствор перемешивали при комнатной температуре в течение 6 часов. Насыщенный раствор аммонийхлорида и этилацетат добавляли к реакционному раствору и органический слой отделяли. Полученный органический слой сушили над сульфатом магния и затем концентрировали при пониженном давлении. Остаток очищали хроматографией на колонке с силикагелем (элюирующий растворитель: гептан→гептан:этилацетат=1:1), с получением 4,0 г указанного в заголовке соединения. Характеристическое значение данного соединения является следующим:
ESI-МС: m/z 412[M++Na].
Синтез метил (2R,6S)-6-(3,4,5-трифторфенил)пиперидина-2-карбоксилата
Раствор 4н. хлористо-водородной кислоты в этилацетате (20 мл) добавляли к раствору метил (R)-2-трет-бутоксикарбониламино-6-оксо-6-(3,4,5-трифторфенил)гексаноата (4,0 г) в этилацетате (20 мл) и реакционный раствор перемешивали при комнатной температуре в течение 14 часов. Реакционный раствор концентрировали при пониженном давлении. Затем добавляли к остатку этилацетат и насыщенный водный раствор бикарбоната натрия и органический слой отделяли. Полученный органический слой сушили над сульфатом магния и затем концентрировали при пониженном давлении. К раствору полученного остатка в этилацетате (50 мл) добавляли 10% палладий на углероде (100 мг) и реакционный раствор перемешивали в токе водорода при комнатной температуре в течение 6 часов. Реакционный раствор фильтровали через целит и фильтрат концентрировали при пониженном давлении, с получением 2,7 г указанного в заголовке соединения. Характеристическое значение данного соединения является следующим:
ESI-МС: m/z 274[M++H].
Синтез [(2R,6S)-6-(3,4,5-трифторфенил)пиперидин-2-ил]метанола
LAH (75 мг) добавляли тремя порциями к раствору метил (2R,6S)-6-(3,4,5-трифторфенил)пиперидина-2-карбоксилата (270 мг) в ТГФ (5 мл) при -20°C в течение 15 минут. Реакционный раствор перемешивали при -20°C в течение одного часа и последовательно добавляли к нему воду (0,1 мл), 5н. раствор гидроксида натрия (0,1 мл) и воду (0,3 мл). Смесь нагревали до комнатной температуры и фильтровали через целит. Фильтрат концентрировали при пониженном давлении, с получением 242 мг указанного в заголовке соединения. Характеристическое значение данного соединения является следующим:
ESI-МС: m/z 246[M++H].
Синтез (4R,6S)-6-(3,4,5-трифторфенил)гексагидропиридо[2,1-c][1,4]оксазин-3,4-диона
Смесь [(2R,6S)-6-(3,4,5-трифторфенил)пиперидин-2-ил]метанола (242 мг) с диэтилоксалатом (1,3 мл) нагревали и перемешивали при 120°C в течение одного часа. Реакционный раствор оставляли охлаждаться до комнатной температуры и выпавшее в осадок твердое вещество отделяли фильтрованием. Полученное твердое вещество промывали эфиром и сушили на воздухе, с получением 228 мг указанного в заголовке соединения. Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,36-1,48 (м, 1H), 1,58-1,67 (м, 1H), 1,70-1,87 (м, 2H), 2,10-2,24 (м, 2H), 4,09-4,18 (м, 1H), 4,37 (т, J=11,6 Гц, 1H), 4,43 (дд, J=11,6, 3,6 Гц, 1H), 5,19 (т, J=4,0 Гц, 1H), 6,82-6,90 (м, 2H).
Синтез (4R,6S)-3-гидрокси-6-(3,4,5-трифторфенил)гидроксигексагидропиридо[2,1-c][1,4]оксазин-4-она
1М раствор три-втор-бутилборогидрида лития в ТГФ (0,79 мл) добавляли по каплям к раствору (4R,6S)-6-(3,4,5-трифторфенил)гексагидропиридо[2,1-c][1,4]оксазин-3,4-диона (228 мг) в ТГФ (10 мл) при -15°C и реакционный раствор перемешивали при -15°C в течение трех часов. Последовательно добавляли к реакционному раствору при -15°C 5н. раствор гидроксида натрия (0,25 мл) и 20% водный пероксид водорода (0,05 мл). Реакционный раствор оставляли охлаждаться до комнатной температуры и перемешивали в течение одного часа. Раствор этилацетата и сульфита натрия добавляли к реакционному раствору и органический слой отделяли. Полученный органический слой промывали насыщенным раствором соли, сушили над сульфатом магния и затем концентрировали при пониженном давлении. Остаток очищали хроматографией на колонке с силикагелем (элюирующий растворитель: гептан:этилацетат=1:1→этилацетат), с получением 240 мг указанного в заголовке соединения. Характеристическое значения данного соединения является следующим:
ESI-МС: m/z 302[M++H].
Синтез (Z)-(6S,9aR)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)бензилиден]}-6-(3,4,5-трифторфенил)гексагидропиридо[2,1-c][1,4]оксазин-4-она
Раствор (4R,6S)-3-гидрокси-6-(3,4,5-трифторфенил)гидроксигексагидропиридо[2,1-c][1,4]оксазин-4-она (240 мг) и трифенилфосфонийбромида (328 мг) в ацетонитриле (10 мл) нагревали при кипении с обратным холодильником в течение одного часа и затем оставляли охлаждаться до комнатной температуры. Добавляли к реакционному раствору 3-метокси-4-(4-метил-1H-имидазол-1-ил)бензальдегид (172 мг) и триэтиламин (0,33 мл) и реакционный раствор перемешивали при комнатной температуре в течение 13 часов. Этилацетат и насыщенный водный раствор бикарбоната натрия добавляли к реакционному раствору и органический слой отделяли. Полученный органический слой промывали насыщенным раствором соли, сушили над сульфатом магния и затем концентрировали при пониженном давлении. Остаток очищали хроматографией на колонке с силикагелем (носитель: Chromatorex NH; элюирующий растворитель: гептан:этилацетат=1:1→этилацетат→этилацетат:метанол=9:1), с получением 1300 мг указанного в заголовке соединения. Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,38-1,58 (м, 2H), 1,66-1,84 (м, 2H), 2,06-2,14 (м, 1H), 2,17-2,28 (м, 1H), 2,30 (с, 3H), 3,86 (с, 3H), 4,04 (т, J=10,0 Гц, 1H), 4,06-4,14 (м, 1H), 4,36 (ушир.д, J=8,4 Гц, 1H), 5,26 (т, J=4,0 Гц, 1H), 6,83 (с, 1H), 6,86-6,93 (м, 2H), 6,94 (ушир.с, 1H), 7,21 (д, J=8,0 Гц, 1H), 7,38 (дд, J=8,0, 1,6 Гц, 1H), 7,39 (д, J=1,6 Гц, 1H), 7,73 (ушир.с, 1H).
Пример 41
Синтез (Z)-(6S,9aR)-6-(3,4-дифторфенил)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)бензилиден]гексагидропиридо[2,1-c][1,4]оксазин-4-она
[Формула 56]
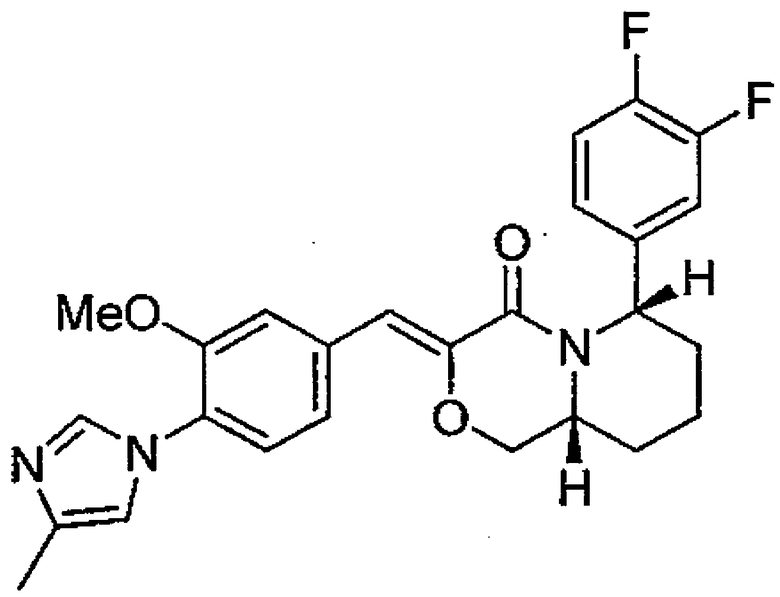
Синтез метил (R)-2-трет-бутоксикарбониламино-6-(3,4-дифторфенил)-6-оксогексаноата
К раствору 2-метилового эфира 1-трет-бутилового эфира (R)-6-оксопиперидин-1,2-дикарбоновой кислоты (CAS No. 183890-36-0, 5,8 г) в ТГФ (200 мл) добавляли по каплям при -40°C 3,4-дифторфенилмагнийбромид (0,5М раствор в ТГФ, 50 мл) и реакционный раствор перемешивали при -40°C в течение семи часов. Насыщенный раствор аммонийхлорида и этилацетат добавляли к реакционному раствору и смесь нагревали до комнатной температуры. Затем органический слой отделяли, полученный органический слой сушили над сульфатом магния и затем концентрировали при пониженном давлении. Остаток очищали хроматографией на колонке с силикагелем (элюирующий растворитель: гептан→гептан:этилацетат=1:1), с получением 3,8 г указанного в заголовке соединения. Характеристическое значение данного соединения является следующим:
ESI-МС: m/z 394[M++Na].
Синтез метил (2R,6S)-6-(3,4-дифторфенил)пиперидина-2-карбоксилата
Раствор 4н. хлористо-водородной кислоты в этилацетате (20 мл) добавляли к раствору метил (R)-2-трет-бутоксикарбониламино-6-(3,4-дифторфенил)-6-оксогексаноата (3,8 г) в этилацетате (20 мл) и реакционный раствор перемешивали при комнатной температуре в течение 5,5 часов. Реакционный раствор концентрировали при пониженном давлении. Затем этилацетат и насыщенный водный раствор бикарбоната натрия добавляли к остатку и органический слой отделяли. Полученный органический слой сушили над сульфатом магния и затем концентрировали при пониженном давлении. К раствору полученного остатка в метаноле (20 мл) добавляли 10% палладий на углероде (50 мг) и реакционный раствор перемешивали в токе водорода при комнатной температуре в течение двух часов. Реакционный раствор фильтровали через целит и фильтрат концентрировали при пониженном давлении, с получением 2,1 г указанного в заголовке соединения. Характеристическое значение данного соединения является следующим:
ESI-МС: m/z 256[M++H].
Синтез [(2R,6S)-6-(3,4-дифторфенил)пиперидин-2-ил]метанола
LAH (90 мг) добавляли тремя порциями к раствору метил (2R,6S)-6-(3,4-дифторфенил)пиперидина-2-карбоксилата (300 мг) в ТГФ (5 мл) при -15°C в течение 15 минут. Реакционный раствор перемешивали при -15°C в течение одного часа и последовательно добавляли к нему воду (0,1 мл), 5н. раствор гидроксида натрия (0,1 мл) и воду (0,3 мл). Смесь нагревали до комнатной температуры и фильтровали через целит. Фильтрат концентрировали при пониженном давлении, с получением 267 мг указанного в заголовке соединения. Характеристическое значение данного соединения является следующим:
ESI-МС: m/z 228[M++H].
Синтез (4R,6S)-6-(3,4-дифторфенил)гексагидропиридо[2,1-c][1,4]оксазине-3,4-диона
Смесь [(2R,6S)-6-(3,4-дифторфенил)пиперидин-2-ил]метанола (267 мг) с диэтилоксалатом (1,6 мл) нагревали и перемешивали при 120°C в течение одного часа. Реакционный раствор оставляли охлаждаться до комнатной температуры и выпавшее в осадок твердое вещество отделяли фильтрованием. Полученное твердое вещество промывали эфиром и сушили на воздухе, с получением 192 мг указанного в заголовке соединения. Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,38-1,48 (м, 1H), 1,55-1,66 (м, 1H), 1,68-1,83 (м, 2H), 2,12-2,25 (м, 2H), 3,99-4,18 (м, 1H), 4,35 (т, J=11,6 Гц, 1H), 4,42 (дд, J=11,6, 3,2 Гц, 1H), 5,27 (т, J=4,0 Гц, 1H), 6,94-6,99 (м, 1H), 7,01-7,07 (м, 1H), 7,10-7,17 (м, 1H).
Синтез (4R,6S)-6-(3,4-дифторфенил)-3-гидроксигексагидропиридо[2,1-c][1,4]оксазин-4-она
1М раствор три-втор-бутилборогидрида лития в ТГФ (0,71 мл) добавляли по каплям к раствору (4R,6S)-6-(3,4-дифторфенил)гексагидропиридо[2,1-c][1,4]оксазин-3,4-диона (192 мг) в ТГФ (10 мл) при -15°C и реакционный раствор перемешивали при -15°C в течение трех часов. Последовательно добавляли к реакционному раствору при -15°C 5н. раствор гидроксида натрия (0,25 мл) и 20% водный пероксид водорода (0,05 мл). Реакционный раствор оставляли охлаждаться до комнатной температуры и перемешивали в течение одного часа. Раствор этилацетата и сульфита натрия добавляли к реакционному раствору и органический слой отделяли. Полученный органический слой промывали насыщенным раствором соли, сушили над сульфатом магния и затем концентрировали при пониженном давлении. Остаток очищали хроматографией на колонке с силикагелем (элюирующий растворитель: гептан:этилацетат=1:1→этилацетат), с получением 151 мг указанного в заголовке соединения. Характеристическое значение данного соединения является следующим:
ESI-МС: m/z 284[M++H].
Синтез (Z)-(6S,9aR)-6-(3,4-дифторфенил)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)бензилиден]гексагидропиридо[2,1-c][1,4]оксазин-4-она
Раствор (4R,6S)-6-(3,4-дифторфенил)-3-гидроксигексагидропиридо[2,1-c][1,4]оксазин-4-она (151 мг) и трифенилфосфонийбромида (220 мг) в ацетонитриле (7 мл) нагревали при кипении с обратным холодильником в течение одного часа и затем оставляли охлаждаться до комнатной температуры. К реакционному раствору добавляли 3-метокси-4-(4-метил-1H-имидазол-1-ил)бензальдегид (115 мг) и триэтиламин (0,22 мл) и реакционный раствор перемешивали при комнатной температуре в течение 12 часов. Этилацетат и насыщенный водный раствор бикарбоната натрия добавляли к реакционному раствору и органический слой отделяли. Полученный органический слой промывали насыщенным раствором соли, сушили над сульфатом магния и затем концентрировали при пониженном давлении. Остаток очищали хроматографией на колонке с силикагелем (носитель: Chromatorex NH; элюирующий растворитель: гептан:этилацетат=1:1→этилацетат), с получением 150 мг указанного в заголовке соединения. Характеристические значения соединения являются следующими:
ESI-МС; m/z 466[M++H].
1H-ЯМР (CDCl3) δ (м.д.): 1,38-1,58 (м, 2H), 1,66-1,80 (м, 2H), 2,10-2,28 (м, 2H), 2,30 (с, 3H), 3,85 (с, 3H), 4,03 (т, J=10,4 Гц, 1H), 4,05-4,16 (м, 1H), 4,35 (дд, J=10,4, 2,0 Гц, 1H), 5,33 (т, J=4,0 Гц, 1H), 6,82 (с, 1H), 6,92 (ушир.с, 1H), 6,98-7,02 (м, 1H), 7,04-7,16 (м, 2H), 7,20 (д, J=8,0 Гц, 1H), 7,35 (д, J=2,0 Гц, 1H), 7,36 (дд, J=8,0, 2,0 Гц, 1H), 7,71 (д, J=1,2 Гц, 1H).
Пример 42
Синтез (Z)-(6S,9aR)-6-(2,6-дифторпиридин-3-ил)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)бензилиден]гексагидропиридо[2,1-c][1,4]оксазин-4-она
[Формула 57]

Синтез метил (R)-2-трет-бутоксикарбониламино-6-(2,6-дифторпиридин-3-ил)-6-оксогексаноата
LDA (1,5М раствор в ТГФ, 3,2 мл) добавляли к раствору 2,6-дифторпиридина (492 мг) в ТГФ (25 мл) при -78°C и реакционный раствор перемешивали при -78°C в течение 2,5 часов. Раствор 2-метилового эфира 1-трет-бутилового эфира (R)-6-оксопиперидин-1,2-дикарбоновой кислоты (CAS No. 183890-36-0, 1,0 г) в ТГФ (5 мл) добавляли к реакционному раствору при -78°C. Реакционный раствор перемешивали при -78°C в течение одного часа и при 0°C в течение 2,5 часов. Насыщенный раствор аммонийхлорида и этилацетат добавляли к реакционному раствору и смесь нагревали до комнатной температуры. Затем органический слой отделяли, полученный органический слой сушили над сульфатом магния и затем концентрировали при пониженном давлении. Остаток очищали хроматографией на колонке с силикагелем (элюирующий растворитель: гептан:этилацетат=1:1→этилацетат), с получением 148 мг указанного в заголовке соединения. Характеристическое значение данного соединения является следующим:
ESI-МС: m/z 395[M++Na].
Синтез (Z)-(6S,9aR)-6-(2,6-дифторпиридин-3-ил)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)бензилиден]гексагидропиридо[2,1-c][1,4]оксазин-4-она
18 мг указанного в заголовке соединения получали из метил (R)-2-трет-бутоксикарбониламино-6-(2,6-дифторпиридин-3-ил)-6-оксогексаноата (148 мг) по аналогичной методике примера 41. Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,44-1,63 (м, 2H), 1,68-1,81 (м, 1H), 1,85-1,94 (м, 1H), 2,09-2,27 (м, 2H), 2,29 (с, 3H), 3,84 (с, 3H), 4,05 (т, J=10,0 Гц, 1H), 4,07-4,15 (м, 1H), 4,39 (ушир.д, J=8,4 Гц, 1H), 5,25 (т, J=5,2 Гц, 1H), 6,76 (с, 1H), 6,79 (дд, J=8,0, 3,2 Гц, 1H), 6,92 (ушир.с, 1H), 7,19 (д, J=7,6 Гц, 1H), 7,35 (дд, J=7,6, 1,6 Гц, 1H), 7,36 (д, J=1,6 Гц, 1H), 7,70 (ушир.с, 1H), 7,73 (дд, J=17,2, 8,0 Гц, 1H).
Примеры 43 и 44
Синтез (Z)-4-[(R)-1-(2,6-дифторпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]морфолин-3-она и (Z)-4-[(S)-1-(2,6-дифторпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]морфолин-3-она
[Формула 58]

Рацемат указанных в заголовке соединений получали из 2,6-дифторпиридина, аминоэтанола и 3-метокси-4-(4-метил-1H-имидазол-1-ил)бензальдегида в качестве исходных соединений по аналогичной методике другого процесса синтеза примера 22. Полученный рацемат разделяли с помощью CHIRALPAKTM IA производства ф. Daicel Chemical Industries, Ltd. (2 см×25 см; подвижная фаза: гексан:этанол=6:4), с получением указанного в заголовке оптически активного соединения со временем удерживания 18 минут (38,7 мг) и указанного в заголовке оптически активного соединения со временем удерживания 22 минут (37,9 мг).
Характеристические значения указанного в заголовке оптически активного соединения со временем удерживания 18 минут (пример 43) являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,68 (д, J=6,8 Гц, 3H), 2,29 (с, 3H), 3,41-3,47 (м, 1H), 3,63-3,68 (м, 1H), 3,85 (с, 3H), 4,22-4,28 (м, 2H), 5,77 (кв, J=6,8 Гц, 1H), 6,83 (с, 1H), 6,87 (дд, J=8,4, 2,8 Гц, 1H), 6,92 (с, 1H), 7,20 (д, J=8,4 Гц, 1H), 7,35 (д, J=8,4 Гц, 1H), 7,38 (с, 1H), 7,71 (с, 1H), 8,00 (дд, J=16,8, 8,4 Гц, 1H).
Характеристические значения указанного в заголовке оптически активного соединения со временем удерживания 22 минут (пример 44) являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,68 (д, J=6,8 Гц, 3H), 2,29 (с, 3H), 3,41-3,47 (м, 1H), 3,63-3,68 (м, 1H), 3,85 (с, 3H), 4,22-4,28 (м, 2H), 5,77 (кв, J=6,8 Гц, 1H), 6,83 (с, 1H), 6,87 (дд, J=8,4, 2,8 Гц, 1H), 6,92 (с, 1H), 7,20 (д, J=8,4 Гц, 1H), 7,35 (д, J=8,4 Гц, 1H), 7,38 (с, 1H), 7,71 (с, 1H), 8,00 (дд, J=16,8, 8,4 Гц, 1H).
Примеры 45 и 46
Синтез (Z)-(S)-4-[(S)-1-(2-фторпиридин-5-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она и (Z)-(S)-4-[(R)-1-(2-фторпиридин-5-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она
[Формула 59]

Синтез 1-(6-фторпиридин-3-ил)этиламина
1-(6-Фторпиридин-3-ил)этанон (7,8 г) синтезировали из 6-фторникотиновой кислоты (10 г) по аналогичной методике примера 22. Указанное в заголовке соединение (457 мг) получали из 1-(6-фторпиридин-3-ил)этанона (1,09 г). Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,40 (д, J=6,4 Гц, 3H), 4,21 (кв, J=6,4 Гц, 1H), 6,90 (дд, J=3,2, 8,4 Гц, 1H), 7,84 (м, 1H), 8,17 (д, J=0,8 Гц, 1H).
Синтез (Z)-(S)-4-[(S)-1-(6-фторпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она и (Z)-(S)-4-[(R)-1-(6-фторпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она
Диастереомерную смесь указанных в заголовке соединений (48 мг) получали в виде неочищенного продукта из 1-(6-фторпиридин-3-ил)этиламина (457 мг) по аналогичной методике примера 22. Полученную смесь диастереомеров (45 мг) разделяли с помощью CHIRALPAKTM IA производства ф. Daicel Chemical Industries, Ltd. (2 см×25 см; подвижная фаза: гексан:этанол=8:2), с получением указанного в заголовке оптически активного соединения со временем удерживания 57 минут (20 мг) и указанного в заголовке оптически активного соединения со временем удерживания 63 минут (6,8 мг).
Характеристическое значение диастереомерной смеси указанных в заголовке соединений является следующим:
ESI-МС: m/z 437[M++H].
Характеристические значения указанного в заголовке оптически активного соединения со временем удерживания 57 минут являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,39 (д, J=6,4 Гц, 3H), 1,62 (д, J=7,6 Гц, 3H), 2,30 (д, J=0,8 Гц, 3H), 2,95 (дд, J=9,6, 12,8 Гц, 1H), 3,26 (дд, J=2,8, 13,2 Гц, 1H), 3,85 (с, 3H), 4,37 (м, 1H), 6,15 (кв, J=7,2 Гц, 1H), 6,89 (с, 1H), 6,93 (с, 1H), 6,96 (дд, J=2,8, 8,4 Гц, 1H), 7,21 (д, J=8,0 Гц, 1H), 7,34 (м, 1H), 7,51 (д, J=1,6 Гц, 1H), 7,72 (д, J=1,2 Гц, 1H), 7,77 (м, 1H), 8,21 (дд, J=1,2, 1,2 Гц, 1H).
Характеристические значения указанного в заголовке оптически активного соединения со временем удерживания 63 минут являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,42 (д, J=6,4 Гц, 3H), 1,61 (д, J=7,2 Гц, 3H), 2,30 (с, 3H), 2,99 (дд, J=2,8, 12,4 Гц, 1H), 3,40 (дд, J=10,0, 12,4 Гц, 1H), 3,86 (с, 3H), 4,13 (м, 1H), 6,17 (кв, J=6,8 Гц, 1H), 6,89 (с, 1H), 6,94 (с, 1H), 6,96 (дд, J=2,8, 8,8 Гц, 1H), 7,21 (д, J=8,4 Гц, 1H), 7,34 (дд, J=1,6, 8,4 Гц, 1H), 7,53 (д, J=1,6 Гц, 1H), 7,73 (д, J=1,2 Гц, 1H), 7,81 (м, 1H), 8,22 (д, J=1,6 Гц, 1H).
Примеры 47 и 48
Синтез (Z)-(S)-4-[(S)-1-(2-фторпиридин-4-ил)этил]-2-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}-6-метилморфолин-3-она и (Z)-(S)-4-[(R)-1-(2-фторпиридин-4-ил)этил]-2-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}-6-метилморфолин-3-она
[Формула 60]

Указанное в заголовке соединение получали в виде смеси диастереомеров по аналогичной методике примера 22 из 1-(2-фторпиридин-4-ил)этиламина, полученного по аналогичной методике примера 22. Соединение разделяли с помощью CHIRALCEL OD-H производства ф. Daicel Chemical Industries, Ltd. (2 см×25 см; подвижная фаза: система этанол-гексан), с получением указанного в заголовке соединения со временем удерживания 23 минут (пример 47) и указанного в заголовке соединения со временем удерживания 26 минут (пример 48). Характеристические значения указанного в заголовке соединения примера 47 являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,42 (д, J=6,0 Гц, 3H), 1,60 (д, J=7,2 Гц, 3H), 2,30 (с, 3H), 3,03 (дд, J=12,4, 9,2 Гц, 1H), 3,24 (дд, J=13,2, 2,8 Гц, 1H), 3,86 (с, 3H), 4,34-4,42 (м, 1H), 6,11 (т, J=7,2 Гц, 1H), 6,89 (ушир.с, 1H), 6,90 (с, 1H), 6,94 (ушир.с, 1H), 7,14 (ушир.д, J=5,2 Гц, 1H), 7,22 (д, J=8,0 Гц, 1H), 7,35 (дд, J=8,0, 1,6 Гц, 1H), 7,52 (д, J=1,6 Гц, 1H), 7,73 (д, J=1,2 Гц, 1H), 8,23 (д, J=5,2 Гц, 1H).
Примеры 49 и 50
Синтез (Z)-(S)-4-[(S)-1-(5-фторпиридин-2-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она и (Z)-(S)-4-[(R)-1-(5-фторпиридин-2-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она
[Формула 61]

Синтез 1-(5-фторпиридин-2-ил)этанона
Йодид меди (811 мг), 1-этоксивинилтри-н-бутилолово (19,2 мл) и бис(трифенилфосфин)палладий(II)хлорид (1 г) добавляли к раствору 2-бром-5-фторпиридина (5 г) в ацетонитриле (250 мл) и реакционный раствор нагревали и перемешивали в атмосфере азота при 100°C в течение двух часов. Реакционный раствор снова доводили до комнатной температуры и растворитель выпаривали при пониженном давлении. Остаток разбавляли этилацетатом и промывали насыщенным раствором соли. Органический слой сушили над сульфатом магния и растворитель выпаривали при пониженном давлении. Остаток разбавляли ацетоном (120 мл) и к реакционному раствору добавляли (1S)-(+)-10-камфорсульфоновую кислоту (9,9 г). После подтверждения тонкослойной хроматографией образования целевого продукта растворитель выпаривали при пониженном давлении. Остаток разбавляли эфиром и нейтрализовали карбонатом натрия. Добавляли к реакционному раствору воду и отделяли органический раствор. Органический слой сушили над сульфатом магния и остаток очищали хроматографией на колонке с силикагелем (носитель: Chromatorex; элюирующий растворитель: гексан-этилацетат), с получением 3,55 г указанного в заголовке соединения. Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 2,71 (с, 3H), 7,51 (м, 1H), 8,11 (ддд, J=0,4, 4,8, 8,8 Гц, 1H), 8,51 (д, J=2,8 Гц, 1H).
Синтез 1-(5-фторпиридин-2-ил)этиламина
Указанное в заголовке соединение (483 мг) получали из 1-(5-фторпиридин-2-ил)этанона (525 мг) по аналогичной методике примера 22. Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,42 (д, J=6,4 Гц, 3H), 4,18 (кв, J=6,4 Гц, 1H), 7,30-7,37 (м, 2H), 8,41 (д, J=2,4 Гц, 1H).
Синтез (Z)-(S)-4-[(S)-1-(5-фторпиридин-2-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она и (Z)-(S)-4-[(R)-1-(5-фторпиридин-2-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она
Диастереомерную смесь указанных в заголовке соединений (248 мг) получали в виде неочищенного продукта из 1-(5-фторпиридин-2-ил)этиламина (483 мг) по аналогичной методике примера 22. Полученную смесь диастереомеров (30 мг) разделяли с помощью CHIRALPAKTM OD-H производства ф. Daicel Chemical Industries, Ltd. (2 см×25 см; подвижная фаза: гексан:этанол=8:2) и CHIRALPAKTM AD-H производства ф. Daicel Chemical Industries, Ltd. (2 см×25 см; подвижная фаза: этанол), с получением указанного в заголовке оптически активного соединения со временем удерживания 23 минут (1,7 мг) и указанного в заголовке оптически активного соединения со временем удерживания 27 минут (3,9 мг).
Характеристическое значение диастереомерной смеси указанных в заголовке соединений является следующим:
ESI-МС: m/z 437[M++H].
Характеристические значения указанного в заголовке оптически активного соединения со временем удерживания 23 минут являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,37 (д, J=6,4 Гц, 3H), 1,61 (д, J=7,2 Гц, 3H), 2,29 (с, 3H), 3,17 (дд, J=1,2, 13,2 Гц, 1H), 3,52 (дд, J=2,8, 13,2 Гц, 1H), 3,84 (с, 3H), 4,37 (м, 1H), 6,06 (кв, J=6,4 Гц, 1H), 6,84 (с, 1H), 6,92 (с, 1H), 7,20 (д, J=8,4 Гц, 1H), 7,32 (м, 1H), 7,37-7,40 (м, 2H), 7,51 (д, J=1,2 Гц, 1H), 7,71 (д, J=1,2 Гц, 1H), 8,42 (дд, J=1,2, 1,2 Гц, 1H).
Характеристические значения указанного в заголовке оптически активного соединения со временем удерживания 27 минут являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,43 (д, J=6,8 Гц, 3H), 1,60 (д, J=7,2 Гц, 3H), 2,29 (с, 3H), 3,43-3,56 (м, 2H), 3,85 (с, 3H), 4,17 (м, 1H), 6,02 (кв, J=6,8 Гц, 1H), 6,83 (с, 1H), 6,93 (с, 1H), 7,20 (д, J=8,0 Гц, 1H), 7,32 (д, 1H), 7,36-7,43 (м, 2H), 7,53 (д, J=1,6 Гц, 1H), 7,71 (д, J=1,2 Гц, 1H), 8,41 (д, J=1,6 Гц, 1H).
Пример 51
Синтез (Z)-(S)-4-[(S)-1-(2-хлорпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она
[Формула 62]

Синтез 1-(2-хлорпиридин-4-ил)этанона
Указанное в заголовке соединение (7,18 г) получали из 2-хлоризоникотиновой кислоты (8,5 г) по аналогичной методике примера 22. Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 2,63 (с, 3H), 7,66 (м, 1H), 7,77 (м, 1H), 8,59 (м, 1H).
Синтез (R)-1-(2-хлорпиридин-4-ил)этанола
Раствор 1-(2-хлорпиридин-4-ил)этанона (7,18 г) в тетрагидрофуране (10 мл) добавляли по каплям к раствору (+)-DIP-хлорида (19,2 г) в тетрагидрофуране (340 мл) при -20°C и реакционный раствор перемешивали при той же температуре в течение ночи. Реакционный раствор снова доводили до комнатной температуры и растворитель выпаривали при пониженном давлении. Остаток разбавляли эфиром, добавляли диэтаноламин (12,1 г) и реакционный раствор перемешивали при комнатной температуре в течение четырех часов. Нерастворимые вещества отделяли фильтрованием через целит и маточный раствор концентрировали при пониженном давлении. Остаток очищали хроматографией на колонке с силикагелем (носитель: Chromatorex, элюирующий растворитель: гептан-этилацетат), с получением указанного в заголовке соединения (3,84 г). Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,50 (д, J=6,8 Гц, 3H), 4,90 (м, 1H), 7,21 (м, 1H), 7,36 (м, 1H), 8,34 (дд, J=0,4, 5,2 Гц, 1H).
Синтез 4-((S)-1-азидоэтил)-2-хлорпиридина
Дифенилфосфорилазид (6,57 мл) добавляли к раствору (R)-1-(2-хлорпиридин-4-ил)этанола в толуоле (50 мл) в атмосфере азота и реакционный раствор охлаждали до 0°C. DBU (4,52 мл) добавляли к реакционному раствору, который затем нагревали до комнатной температуры и перемешивали в течение ночи. Воду и эфир добавляли к реакционному раствору и органический слой отделяли. Органический слой сушили над сульфатом магния и остаток очищали хроматографией на силикагеле (носитель: Chromatorex; элюирующий растворитель: гексан-этилацетат), с получением указанного в заголовке соединения (4,44 г). Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,55 (д, J=6,8 Гц, 3H), 4,62 (д, J=6,8 Гц, 1H), 7,18 (м, 1H), 7,30 (м, 1H), 8,39 (дд, J=0,4, 5,2 Гц, 1H).
Синтез (S)-1-(2-хлорпиридин-4-ил)этиламина
Трифенилфосфин (9,56 г) добавляли к раствору 4-((S)-1-азидоэтил)-2-хлорпиридина (4,44 г) в смеси тетрагидрофуран-вода (4:1, 50 мл), реакционный раствор нагревали и перемешивали при 60°C в течение двух часов. Реакционный раствор снова доводили до комнатной температуры и растворитель выпаривали при пониженном давлении. Хлороформ и 5н. хлористо-водородную кислоту добавляли к остатку и отделяли водный слой. Водный слой подщелачивали 5н. гидроксидом натрия. Хлороформ добавляли к реакционному раствору и органический слой отделяли. Органический слой сушили над сульфатом магния и растворитель выпаривали при пониженном давлении, с получением указанного в заголовке соединения (2,24 г). Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,38 (д, J=6,8 Гц, 3H), 4,12 (д, J=6,8 Гц, 1H), 7,36 (м, 1H), 7,30 (м, 1H), 8,31 (д, J=5,2 Гц, 1H).
Синтез (Z)-(S)4-[(S)-1-(2-хлорпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она
Указанное в заголовке соединение, содержащее геометрический изомер (518 мг), получали из (S)-1-(2-хлорпиридин-4-ил)этиламина (1,25 г) по аналогичной методике примеров 18 и 19. Полученную смесь (54 мг) разделяли с помощью CHIRALPAKTM IA производства ф. Daicel Chemical Industries, Ltd. (2 см×25 см; подвижная фаза: гексан:этанол=7:3), с получением указанного в заголовке соединения со временем удерживания 38 минут (6,5 мг). Характеристические значения соединения являются следующими.
Характеристические значения указанного в заголовке оптически активного соединения со временем удерживания 38 минут являются следующими:
ESI-МС; m/z 453[M++H].
1H-ЯМР (CDCl3) δ (м.д.): 1,42 (д, J=6,8 Гц, 3H), 1,59 (д, J=7,2 Гц, 3H), 2,30 (д, J=0,8 Гц, 3H), 3,02 (дд, J=9,6, 12,8 Гц, 1H), 3,23 (дд, J=2,4, 13,2 Гц, 1H), 3,85 (с, 3H), 4,36 (м, 1H), 6,07 (кв, J=7,2 Гц, 1H), 6,90 (с, 1H), 6,94 (дд, J=1,2, 1,2 Гц, 1H), 7,17 (м, 1H), 7,22 (д, J=8,0 Гц, 1H), 7,28 (м, 1H), 7,36 (м, 1H), 7,52 (д, J=1,2 Гц, 1H), 7,73 (д, J=1,2 Гц, 1H), 8,39 (дд, J=0,8, 5,2 Гц, 1H).
Пример 52
Синтез (Z)-(S)-4-[(S)-1-(2-хлор-3-фторпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она
[Формула 63]

Синтез 2-хлор-3-фторизоникотиновой кислоты
Указанное в заголовке соединение (6,34 г) получали из 2-хлор-3-фторпиридина (5 г) по аналогичной методике примера 22. Характеристические значения соединения являются следующими:
1H-ЯМР (ДМСО-d6) δ (м.д.): 7,78 (дд, J=4,8, 4,8 Гц, 1H), 8,27 (д, J=4,8 Гц, 1H).
Синтез (S)-1-(2-хлор-3-фторпиридин-4-ил)этиламина
Указанное в заголовке соединение (3,13 г) получали из 2-хлор-3-фторизоникотиновой кислоты (6,34 г) по аналогичной методике примера 51. Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,42 (д, J=6,8 Гц, 3H), 4,45 (кв, J=6,8 Гц, 1H), 7,40 (ддд, J=0,4, 4,8, 4,8 Гц, 1H), 8,18 (д, J=4,8 Гц, 1H).
Синтез (Z)-(S)-4-[(S)-1-(2-хлор-3-фторпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она
Указанное в заголовке соединение, содержащее геометрический изомер (623 мг), получали из (S)-1-(2-хлор-3-фторпиридин-4-ил)этиламина (1,2 г) по аналогичной методике примеров 18 и 19. Полученную смесь (14 мг) разделяли с помощью CHIRALPAKTM IA производства ф. Daicel Chemical Industries, Ltd. (2 см×25 см; подвижная фаза: гексан:этанол=1:1), с получением указанного в заголовке соединения со временем удерживания 24 минут (9,5 мг). Характеристические значения соединения являются следующими:
ESI-МС; m/z 471[M++H].
1H-ЯМР (CDCl3) δ (м.д.): 1,46 (д, J=6,4 Гц, 3H), 1,67 (д, J=7,2 Гц, 3H), 2,29 (с, 3H), 3,23 (дд, J=9,6, 12,4 Гц, 1H), 3,41 (дд, J=2,4, 12,8 Гц, 1H), 3,85 (с, 3H), 4,38 (м, 1H), 5,87 (кв, J=7,2 Гц, 1H), 6,83 (с, 1H), 6,93 (с, 1H), 7,20 (д, J=8,4 Гц, 1H), 7,30-7,33 (м, 2H), 7,50 (д, J=1,2 Гц, 1H), 7,72 (с, 1H), 8,23 (д, J=5,2 Гц, 1H).
Пример 53
Синтез (Z)-(S)-4-[(S)-1-(2,6-дифторпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она
[Формула 64]

Указанное в заголовке соединение получали по аналогичной методике примеров 18 и 19 из (S)-1-(2,6-дифторпиридин-4-ил)этиламина, полученного по аналогичной методике примера 51.
ESI-МС; m/z 455[M++H].
1H-ЯМР (CDCl3) δ (м.д.): 1,44 (д, J=6,4 Гц, 3H), 1,61 (д, J=7,2 Гц, 3H), 2,30 (с, 3H), 3,09 (дд, J=9,2, 12,8 Гц, 1H), 3,27 (дд, J=2,4, 12,8 Гц, 1H), 3,86 (с, 3H), 4,34-4,44 (м, 1H), 6,09 (кв, J=7,2 Гц, 1H), 6,78 (с, 2H), 6,90 (с, 1H), 6,94 (с, 1H), 7,22 (д, J=8,0 Гц, 1H), 7,35 (д, J=8,0 Гц, 1H), 7,52 (с, 1H), 7,72 (с, 1H).
Пример 54
Синтез (Z)-4-[(S)-1-(2-хлорпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-она
[Формула 65]

Синтез 4-[(S)-1-(2-хлорпиридин-4-ил)этил]-6,6-диметилморфолин-2,3-диона
Перхлорат лития (10,2 г) добавляли к раствору (S)-1-(2-хлорпиридин-4-ил)этиламина, полученного в примере 51 (1 г), в эфире (18,5 мл) и реакционный раствор перемешивали в течение пяти минут. Изобутиленоксид (1,7 мл) добавляли к реакционному раствору, который затем перемешивали в течение ночи. Добавляли к реакционному раствору при 0°C 5н. раствор гидроксида натрия и затем смесь экстрагировали хлороформом. Органический слой сушили над сульфатом магния и растворитель выпаривали при пониженном давлении. Дихлорметан (20 мл) и пиридин (20 мл) добавляли к остатку и реакционный раствор охлаждали до 0°C. Оксалилхлорид (669 мкл) добавляли к реакционному раствору, который затем перемешивали при 0°C в течение одного часа и при комнатной температуре в течение одного часа. Оксалилхлорид (0,4 мл) добавляли к реакционному раствору, который дополнительно перемешивали в течение одного часа. Растворитель выпаривали при пониженном давлении. Воду и этилацетат добавляли к остатку и органический слой отделяли. Органический слой сушили над сульфатом магния и остаток очищали хроматографией на колонке с силикагелем (Chromatorex; элюирующий растворитель: гептан-этилацетат), с получением указанного в заголовке соединения (1,07 г). Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,31 (с, 3H), 1,49 (с, 3H), 1,59 (д, J=7,2 Гц, 3H), 3,05 (д, J=13,6, 1H), 3,35 (д, J=14,0 Гц, 1H), 5,97 (кв, J=7,2 Гц, 1H), 7,21 (ддд, J=0,8, 1,2, 5,2 Гц, 1H), 7,30 (дд, J=0,8, 0,8 Гц, 1H), 8,42 (д, J=5,2 Гц, 1H).
Синтез (Z)-4-[(S)-1-(2-хлорпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-она
Указанное в заголовке соединение, содержащее геометрический изомер (1,33 г), получали из 4-[(S)-1-(2-хлорпиридин-4-ил)этил]-6,6-диметилморфолин-2,3-диона (1,07 г) по аналогичной методике примеров 18 и 19. Полученную смесь (56 мг) разделяли с помощью CHIRALPAKTM IA производства ф. Daicel Chemical Industries, Ltd. (2 см×25 см; подвижная фаза: гексан:этанол=7:3), с получением указанного в заголовке соединения со временем удерживания 36 минут (13 мг). Характеристические значения соединения являются следующими:
ESI-МС; m/z 467[M++H].
1H-ЯМР (CDCl3) δ (м.д.): 1,31 (с, 3H), 1,46 (с, 3H), 1,57 (д, J=7,2 Гц, 3H), 2,30 (с, 3H), 2,95 (д, J=12,8 Гц, 1H), 3,29 (д, J=12,8 Гц, 1H), 3,86 (с, 3H), 6,13 (кв, J=7,2 Гц, 1H), 6,93 (дд, J=1,2, 1,2 Гц, 1H), 6,94 (с, 1H), 7,20-7,23 (м, 2H), 7,31 (дд, J=0,8, 0,8 Гц, 1H), 7,35 (дд, J=1,6, 8,0 Гц, 1H), 7,53 (д, J=1,6 Гц, 1H), 7,72 (д, J=1,2 Гц, 1H), 8,40 (д, J=4,8 Гц, 1H).
Пример 55
Синтез (Z)-4-[(S)-1-(2,6-дифторпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-она
[Формула 66]

Синтез (S)-1-(2,6-дифторпиридин-3-ил)этиламина
Указанное в заголовке соединение (9,36 г) получали из 2,6-дифторпиридина (15 г) по аналогичной методике примера 52. Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,40 (д, J=6,8 Гц, 3H), 4,37 (кв, J=6,8 Гц, 1H), 6,81 (дд, J=2,8, 8,0 Гц, 1H), 8,02 (дд, J=8,0, 8,0 Гц, 1H).
Синтез (Z)-4-[(S)-1-(2,6-дифторпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-она
Указанное в заголовке соединение, содержащее геометрический изомер (422 мг), получали из (S)-1-(2,6-дифторпиридин-3-ил)этиламина (500 мг) по аналогичной методике примеров 18 и 19. Полученную смесь (10 мг) разделяли с помощью CHIRALPAKTM IA производства ф. Daicel Chemical Industries, Ltd. (2 см×25 см; подвижная фаза: гексан:этанол=7:3), с получением указанного в заголовке соединения со временем удерживания 28 минут (6,8 мг). Характеристические значения соединения являются следующими:
ESI-МС; m/z 469[M++H].
1H-ЯМР (CDCl3) δ (м.д.): 1,35 (с, 3H), 1,46 (с, 3H), 1,65 (д, J=7,2 Гц, 3H), 2,30 (д, J=0,8 Гц, 3H), 3,20 (д, J=12,8 Гц, 1H), 3,43 (д, J=12,4 Гц, 1H), 3,84 (с, 3H), 5,86 (кв, J=7,2 Гц, 1H), 6,86 (с, 1H), 6,88 (дд, J=2,8, 8,4 Гц, 1H), 6,92 (м, 1H), 7,19 (д, J=8,4 Гц, 1H), 7,31 (дд, J=2,0, 8,4 Гц, 1H), 7,51 (д, J=1,6 Гц, 1H), 7,71 (д, J=1,6 Гц, 1H), 8,01 (дд, J=8,0, 9,2 Гц, 1H).
Пример 56
Синтез (Z)-4-[(S)-1-(6-фторпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-она
[Формула 67]

Синтез (S)-1-(6-фторпиридин-3-ил)этиламина
Указанное в заголовке соединение (3,95 г) получали из 6-фторникотиновой кислоты (10 г) по аналогичной методике примера 52. Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,40 (д, J=6,4 Гц, 3H), 4,21 (кв, J=6,4 Гц, 1H), 6,90 (дд, J=3,2, 8,4 Гц, 1H), 7,84 (м, 1H), 8,17 (д, J=0,8 Гц, 1H).
Синтез (Z)-4-[(S)-1-(6-фторпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-она
Указанное в заголовке соединение, содержащее геометрический изомер (1,02 г), получали из (S)-1-(6-фторпиридин-3-ил)этиламина (500 мг) по аналогичной методике примеров 18 и 19. Полученную смесь (1,01 г) перекристаллизовывали из смеси этилацетат/эфир, с получением указанного в заголовке оптически активного соединения (120 мг). Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,23 (с, 3H), 1,45 (с, 3H), 1,61 (д, J=7,2 Гц, 1H), 2,30 (с, 3H), 2,92 (д, J=12,8 Гц, 1H), 3,32 (д, J=12,4 Гц, 1H), 3,85 (с, 3H), 6,21 (кв, J=7,2 Гц, 1H), 6,92-6,97 (м, 3H), 7,21 (д, J=8,0 Гц, 1H), 7,33 (дд, J=0,8, 8,0 Гц, 1H), 7,52 (д, J=1,2 Гц, 1H), 7,71 (д, J=0,8 Гц, 1H), 7,81 (м, 1H), 8,22 (с, 1H).
Пример 57
Синтез (Z)-4-[(S)-1-(6-хлорпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-она
[Формула 68]
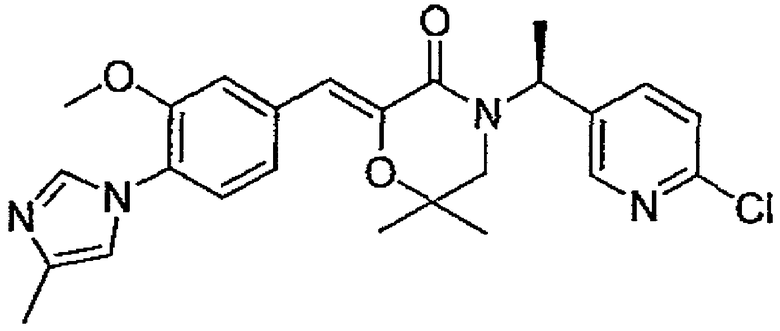
Синтез (S)-1-(6-хлорпиридин-3-ил)этиламина
Указанное в заголовке соединение (7,04 г) получали из 6-хлорникотиновой кислоты (13 г) по аналогичной методике примера 52. Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,39 (д, J=6,4 Гц, 3H), 4,19 (кв, J=6,4 Гц, 1H), 7,29 (д, J=8,0 Гц, 1H), 7,70 (дд, J=2,4, 8,0 Гц, 1H), 8,36 (д, J=2,4 Гц, 1H).
Синтез (Z)-4-[(S)-1-(6-хлорпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-она
Указанное в заголовке соединение, содержащее геометрический изомер, получали из (S)-1-(6-хлорпиридин-3-ил)этиламина (600 мг) по аналогичной методике примеров 18 и 19, и перемешивали в растворе смеси трифторуксусная кислота/хлороформ/4н. хлористо-водородная кислота (5/5/2) в этилацетате в течение четырех часов, для изомеризации Е-изомера в Z-изомер. Реакционный раствор нейтрализовали 5н. раствором NaOH и затем экстрагировали этилацетатом. Органический слой сушили над сульфатом магния и растворитель выпаривали при пониженном давлении. Остаток очищали хроматографией на колонке с силикагелем (Chromatorex NH; гептан/этилацетат→этилацетат/метанол), с получением указанного в заголовке соединения (251 мг).
1H-ЯМР (CDCl3) δ (м.д.): 1,24 (с, 3H), 1,45 (с, 3H), 1,60 (д, J=7,2 Гц, 1H), 2,30 (с, 3H), 2,92 (д, J=12,4 Гц, 1H), 3,30 (д, J=12,4 Гц, 1H), 3,85 (с, 3H), 6,19 (кв, J=7,2 Гц, 1H), 6,92 с, 1H), 6,93 (д, J=3,2 Гц, 1H), 7,20 (д, J=8,4 Гц, 1H), 7,32-7,36 (м, 2H), 7,52 (с, 1H), 7,68 (дд, J=2,4, 8,4 Гц, 1H), 7,71 (д, J=0,8 Гц, 1H), 8,40 (д, J=2,4 Гц, 1H).
Пример 58
Синтез (Z)-4-[(S)-1-(2,3-дифторпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-она
[Формула 69]
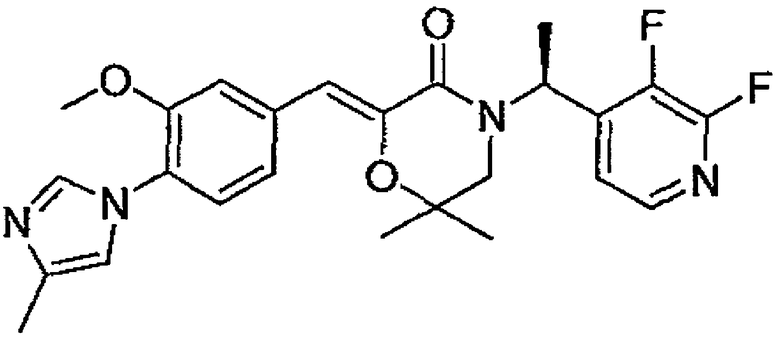
Синтез (S)-1-(2,3-дифторпиридин-4-ил)этиламина
Указанное в заголовке соединение (7,09 г) получали из 2,3-дифторизоникотиновой кислоты (16,6 г), которая является известным соединением (см., например, The Journal of Organic Chemistry, 2005, vol.70, p.3039-3045), по аналогичной методике примера 52. Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,42 (д, J=6,4 Гц, 3H), 4,49 (кв, J=6,4 Гц, 1H), 7,32 (дд, J=4,8, 4,8 Гц, 1H), 7,93 (д, J=4,8 Гц, 1H).
Синтез (Z)-4-[(S)-1-(2,3-дифторпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-она
Указанное в заголовке соединение, содержащее геометрический изомер, получали из (S)-1-(2,3-дифторпиридин-4-ил)этиламина (1 г) по аналогичной методике примеров 18 и 19 и изомеризовали по аналогичной методике примера 57, с получением указанного в заголовке соединения (830 мг). Характеристические значения соединения являются следующими:
ESI-МС; m/z 469[M++H].
1H-ЯМР (CDCl3) δ (м.д.): 1,37 (с, 3H), 1,47 (с, 3H), 1,65 (д, J=7,2 Гц, 1H), 2,30 (с, 3H), 3,18 (д, J=12,4 Гц, 1H), 3,42 (д, J=12,4 Гц, 1H), 3,85 (с, 3H), 6,04 (кв, J=7,2 Гц, 1H), 6,88 (с, 1H), 6,93 (с, 1H), 7,20 (д, J=8,4 Гц, 1H), 7,23-7,33 (м, 2H), 7,51 (с, 1H), 7,71 (с, 1H), 8,00 (д, J=3,2 Гц, 1H).
Пример 59
Синтез (Z)-4-[(S)-1-(5-фторпиридин-2-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-она
[Формула 70]

Синтез (S)-1-(5-фторпиридин-2-ил)этиламина
Указанное в заголовке соединение (1,23 г) получали из 1-(5-фторпиридин-2-ил)этанона, описанного в примере 49 (3,05 г), по аналогичной методике примера 52. Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,42 (д, J=6,4 Гц, 3H), 4,17 (кв, J=6,4 Гц, 1H), 7,30-7,39 (м, 1H), 8,40 (д, J=2,4 Гц, 1H).
Синтез (Z)-4-[(S)-1-(5-фторпиридин-2-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-она
Указанное в заголовке соединение, содержащее геометрический изомер, получали из (S)-1-(5-фторпиридин-2-ил)этиламина (700 мг) по аналогичной методике примеров 18 и 19 и изомеризовали по аналогичной методике примера 57, с получением указанного в заголовке соединения (640 мг). Характеристические значения соединения являются следующими:
ESI-МС; m/z 451[M++H].
1H-ЯМР (CDCl3) δ (м.д.): 1,16 (с, 3H), 1,46 (с, 3H), 1,59 (д, J=6,8 Гц, 1H), 2,29 (с, 3H), 3,34 (д, J=12,8 Гц, 1H), 3,47 (д, J=12,8 Гц, 1H), 3,84 (с, 3H), 6,10 (кв, J=7,2 Гц, 1H), 6,86 (с, 1H), 6,92 (дд, J=1,2, 1,2 Гц, 1H), 7,19 (д, J=8,4 Гц, 1H), 7,31 (дд, J=2,0, 8,4 Гц, 1H), 7,36-7,46 (м, 2H), 7,53 (д, J=2,8 Гц, 1H), 7,70 (м, 1H), 8,41 (д, J=2,8 Гц, 1H).
Пример 60
Синтез (Z)-4-[(S)-1-(5-хлорпиридин-2-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-она
[Формула 71]
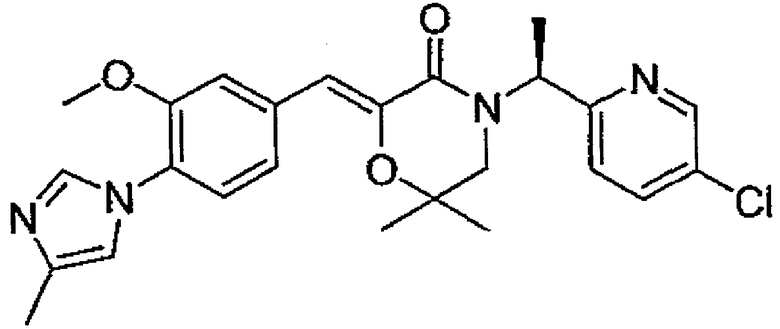
Синтез (S)-1-(5-хлорпиридин-2-ил)этиламина
Указанное в заголовке соединение (2,72 г) получали из 1-(5-хлорпиридин-2-ил)этанона, описанного в примере 20 (4,29 г), по аналогичной методике примера 52. Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,42 (д, J=6,4 Гц, 3H), 4,17 (кв, J=6,4 Гц, 1H), 7,30-7,39 (м, 1H), 8,40 (д, J=2,4 Гц, 1H).
Синтез (Z)-4-[(S)-1-(5-хлорпиридин-2-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-она
Указанное в заголовке соединение, содержащее геометрический изомер, получали из (S)-1-(5-хлорпиридин-2-ил)этиламина (1 г) по аналогичной методике примеров 18 и 19 и изомеризовали по аналогичной методике примера 57, с получением указанного в заголовке соединения (310 мг). Характеристические значения соединения являются следующими:
ESI-МС; m/z 467[M++H].
1H-ЯМР (CDCl3) δ (м.д.): 1,19 (с, 3H), 1,46 (с, 3H), 1,59 (д, J=6,8 Гц, 1H), 2,29 (с, 3H), 3,35 (д, J=12,8 Гц, 1H), 3,48 (д, J=12,8 Гц, 1H), 3,84 (с, 3H), 6,08 (кв, J=6,8 Гц, 1H), 6,86 (с, 1H), 6,92 (с, 1H), 7,19 (д, J=8,0 Гц, 1H), 7,31 (д, J=8,4 Гц, 1H), 7,38 (д, J=8,0 Гц, 1H), 7,53 (с, 1H), 7,66 (дд, J=1,6, 8,4, 1H), 7,70 (с, 1H), 8,51 (д, J=2,0 Гц, 1H).
Соединения в таблицах 1-1 и 1-2 получали по аналогичной методике.
Таблица 1-1
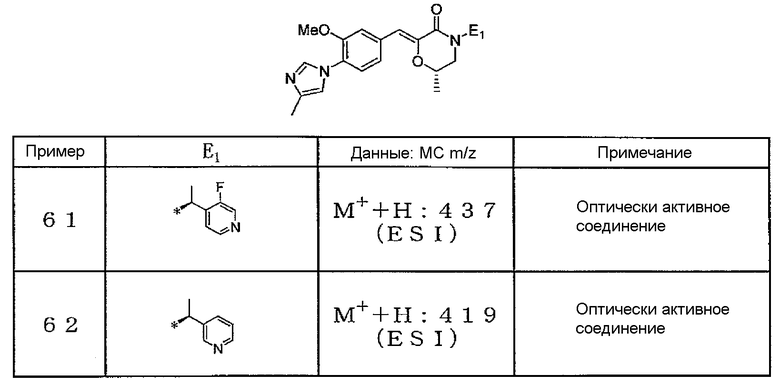
Таблица 1-2

Пример 65
Синтез (Z)-(S)-4-(4-фторбензил)-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она
[Формула 72]
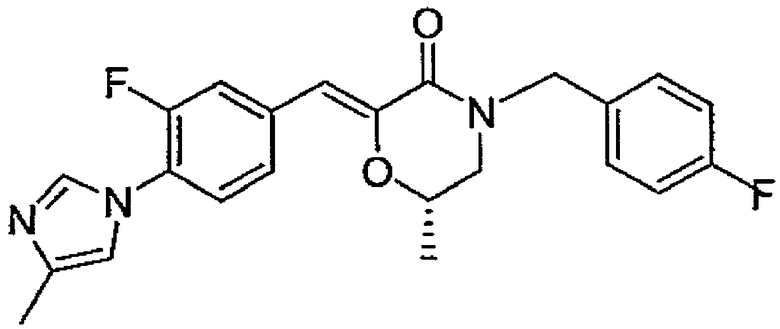
9,06 мг указанного в заголовке соединения получали из (S)-4-(4-фторбензил)-2-гидрокси-6-метилморфолин-3-она, тионилхлорида, трифенилфосфина и 3-фтор-4-(4-метил-1H-имидазол-1-ил)бензальдегида по аналогичной методике примера 5.
1H-ЯМР (CDCl3) δ (м.д.): 1,44 (д, J=6,8 Гц, 3H), 2,38 (с, 3H), 3,26 (дд, J=12,8, 3,2 Гц, 1H), 3,43 (дд, J=12,8, 9,6 Гц, 1H), 4,32-4,40 (м, 1H), 4,62 (д, J=14,4 Гц, 1H), 4,73 (д, J=14,4 Гц, 1H), 6,87 (с, 1H), 7,01-7,09 (м, 3H), 7,27-7,35 (м, 3H), 7,50 (д, J=8,4 Гц, 1H), 7,77 (д, J=12,8 Гц, 1H), 7,96 (с, 1H).
Пример 66
Синтез (Z)-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-[(S)-1-(4-трифторфенил)этил]-6,6-диметилморфолин-3-она
[Формула 73]
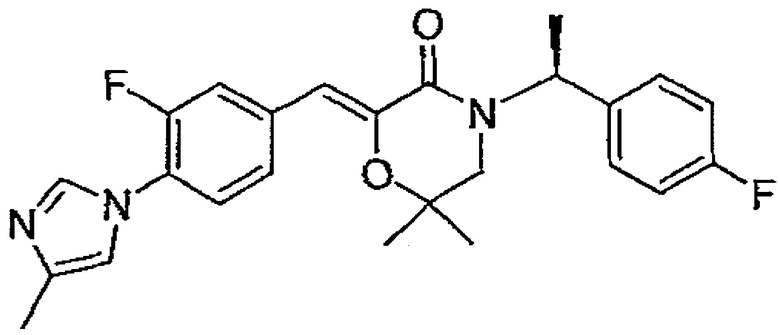
31,55 мг указанного в заголовке соединения получали из 4-[(S)-1-(4-фторфенил)этил]-2-гидрокси-6,6-диметилморфолин-3-она, тионилхлорида, трифенилфосфина и 3-фтор-4-(4-метил-1H-имидазол-1-ил)бензальдегида по аналогичной методике примера 7.
1H-ЯМР (CDCl3) δ (м.д.): 1,20 (с, 3H), 1,43 (с, 3H), 1,55 (д, J=6,8 Гц, 3H), 2,34 (с, 3H), 2,90 (д, J=12,8 Гц, 1H), 3,24 (д, J=12,8 Гц, 1H), 6,16 (кв, J=6,8 Гц, 1H), 6,87 (с, 1H), 7,00 (с, 1H), 7,04-7,08 (м, 2H), 7,28-7,36 (м, 3H), 7,47 (дд, J=8,4, 1,6 Гц, 1H), 7,74 (дд, J=12,8, 1,6 Гц, 1H), 7,85 (с, 1H).
Пример 67
Синтез (Z)-4-(4-фторбензил)-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметил морфолин-3-она
[Формула 74]

44,7 мг указанного в заголовке соединения получали из 4-(4-фторбензил)-2-гидрокси-6,6-диметилморфолин-3-она, тионилхлорида, трифенилфосфина и 3-фтор-4-(4-метил-1H-имидазол-1-ил)бензальдегида по аналогичной методике примера 7.
1H-ЯМР (CDCl3) δ (м.д.): 1,39 (с, 6H), 2,57 (с, 3H), 3,35 (с, 2H), 4,67 (с, 2H), 6,89 (с, 1H), 7,03-7,08 (м, 2H), 7,13 (с, 1H), 7,29-7,33 (м, 2H), 7,41 (дд, J=8,0, 8,0 Гц, 1H), 7,57 (д, J=8,0 Гц, 1H), 7,82 (д, J=12,8 Гц, 1H), 8,70 (с, 1H).
Пример 68
Синтез (Z)-4-[(S)-хроман-4-ил]-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-она
[Формула 75]
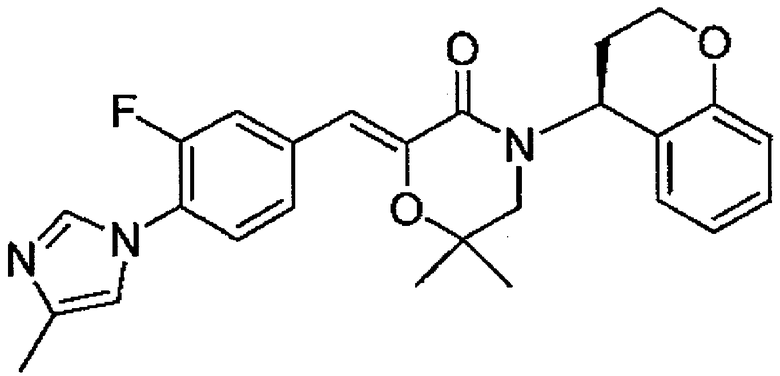
25,4 мг указанного в заголовке соединения получали из 4-[(S)-хроман-4-ил]-2-гидрокси-6,6-диметилморфолин-3-она, трифенилфосфонийбромида и 3-фтор-4-(4-метил-1H-имидазол-1-ил)бензальдегида по аналогичной методике примера 12.
1H-ЯМР (CDCl3) δ (м.д.): 1,43 (с, 3H), 1,45 (с, 3H), 2,14-2,21 (м, 2H), 2,34 (с, 3H), 3,12 (д, J=13,2 Гц, 1H), 3,19 (д, J=13,2 Гц, 1H), 4,23-4,33 (м, 2H), 6,11 (т, J=7,2 Гц, 1H), 6,86-6,95 (м, 3H), 7,01 (с, 1H), 7,09 (д, J=8,0 Гц, 1H), 7,20 (т, J=8,0 Гц, 1H), 7,32 (т, J=8,0 Гц, 1H), 7,49 (д, J=8,0 Гц, 1H), 7,76 (дд, J=12,8, 1,2 Гц, 1H), 7,82 (с, 1H).
Примеры 69 и 70
Синтез (Z)-(S)-4-[(S)-хроман-4-ил]-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она и (Z)-(R)-4-[(S)-хроман-4-ил]-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она
[Формула 76]
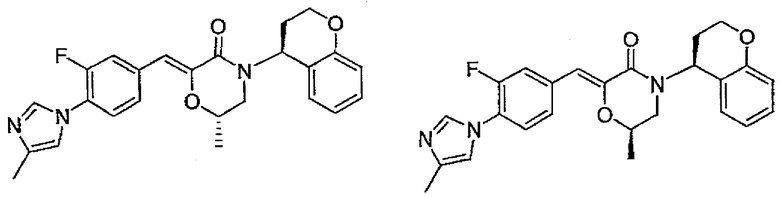
66,4 мг указанного в заголовке соединения получали в виде смеси диастереомеров из 4-[(S)-хроман-4-ил]-2-гидрокси-6-метилморфолин-3-она, трифенилфосфонийбромида и 3-фтор-4-(4-метил-1H-имидазол-1-ил)бензальдегида в качестве исходных соединений по аналогичной методике примеров 12, 13 и 14. Смесь разделяли с помощью CHIRALPAKTM AD-H производства ф. Daicel Chemical Industries, Ltd. (2 см×25 см; подвижная фаза: этанол 100%), с получением указанного в заголовке оптически активного соединения со временем удерживания 20 минут (>99% de) и указанного в заголовке оптически активного соединения со временем удерживания 24 минут (>99% de).
Характеристические значения указанного в заголовке оптически активного соединения со временем удерживания 20 минут (пример 69) являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,43 (д, J=6,0 Гц, 3H), 2,14-2,24 (м, 2H), 2,35 (с, 3H), 3,12-3,15 (м, 2H), 4,24-4,38 (м, 3H), 6,05 (дд, J=8,8, 6,4 Гц, 1H), 6,86-6,89 (м, 2H), 6,93 (т, J=7,2 Гц, 1H), 7,01-7,07 (м, 2H), 7,20 (т, J=8,0 Гц, 1H), 7,33 (т, J=8,0 Гц, 1H), 7,51 (д, J=8,0 Гц, 1H), 7,78 (д, J=12,8 Гц, 1H), 7,87 (с, 1H).
Характеристические значения указанного в заголовке оптически активного соединения со временем удерживания 24 минут (пример 70) являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,42 (д, J=6,0 Гц, 3H), 2,14-2,20 (м, 2H), 2,36 (с, 3H), 3,10 (дд, J=12,8, 2,4 Гц, 1H), 3,32 (дд, J=12,8, 10,0 Гц, 1H), 4,24-4,37 (м, 3H), 6,13 (т, J=8,4 Гц, 1H), 6,86-6,94 (м, 3H), 7,02-7,07 (м, 2H), 7,20 (т, J=8,4 Гц, 1H), 7,33 (т, J=8,4 Гц, 1H), 7,51 (д, J=8,4 Гц, 1H), 7,78 (дд, J=12,8, 1,2 Гц, 1H), 7,89 (с, 1H).
Пример 71
Синтез (Z)-(S)-4-(6-хлорпиридин-2-илметил)-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она
[Формула 77]
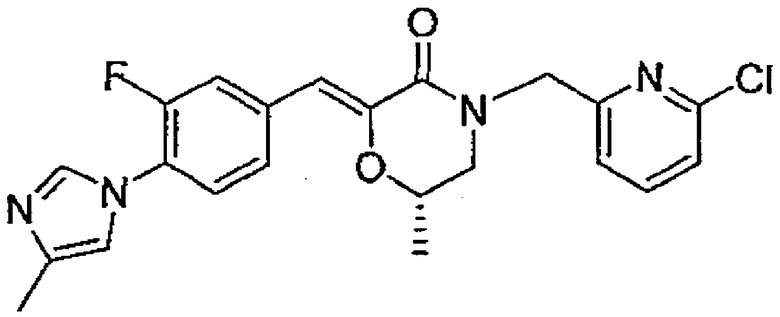
24,3 мг указанного в заголовке соединения получали из (S)-4-(6-хлорпиридин-2-илметил)-2-гидрокси-6-метилморфолин-3-она, тионилхлорида, трифенилфосфина и 3-фтор-4-(4-метил-1H-имидазол-1-ил)бензальдегида по аналогичной методике примера 15.
1H-ЯМР (CDCl3) δ (м.д.): 1,48 (д, J=6,0 Гц, 3H), 2,33 (с, 3H), 3,59 (дд, J=12,8, 2,8 Гц, 1H), 3,68 (дд, J=12,8, 9,6 Гц, 1H), 4,43-4,47 (м, 1H), 4,73 (д, J=14,8 Гц, 1H), 4,78 (д, J=14,8 Гц, 1H), 6,82 (с, 1H), 7,00 (с, 1H), 7,26-7,33 (м, 3H), 7,47 (дд, J=8,4, 1,6 Гц, 1H), 7,66 (дд, J=8,0, 8,0 Гц, 1H), 7,75 (дд, J=12,8, 1,6 Гц, 1H), 7,80 (с, 1H).
Пример 72
Синтез (Z)-(S)-4-[(S)-1-(6-хлорпиридин-3-ил)этил]-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она
[Формула 78]

Указанное в заголовке соединение (11,6 мг) получали из 3-фтор-4-(4-метил-1H-имидазол-1-ил)бензальдегида в качестве исходного соединения по аналогичной методике примеров 18 и 19.
1H-ЯМР (CDCl3) δ (м.д.): 1,40 (д, J=6,4 Гц, 3H), 1,62 (д, J=7,2 Гц, 3H), 2,31 (с, 3H), 2,95 (дд, J=12,8, 9,2 Гц, 1H), 3,28 (дд, J=12,8, 2,8 Гц, 1H), 4,35-4,41 (м, 1H), 6,12 (кв, J=7,2 Гц, 1H), 6,85 (с, 1H), 6,99 (с, 1H), 7,31 (т, J=8,4 Гц, 1H), 7,34 (д, J=8,4 Гц, 1H), 7,46 (дд, J=8,4, 2,0 Гц, 1H), 7,63 (дд, J=8,4, 2,4 Гц, 1H), 7,72 (дд, J=13,2, 2,0 Гц, 1H), 7,74 (с, 1H), 8,38 (д, J=2,4 Гц, 1H).
Пример 73
Синтез (Z)-(S)-4-[(S)-1-(2,6-дифторпиридин-3-ил)этил]-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она
[Формула 79]

Указанное в заголовке соединение (11,2 мг) получали из 3-фтор-4-(4-метил-1H-имидазол-1-ил)бензальдегида в качестве исходного соединения по аналогичной методике другого процесса синтеза примера 22.
1H-ЯМР (CDCl3) δ (м.д.): 1,45 (д, J=6,4 Гц, 3H), 1,67 (д, J=6,8 Гц, 3H), 2,30 (с, 3H), 3,22 (дд, J=12,8, 5,2 Гц, 1H), 3,44 (дд, J=12,8, 3,2 Гц, 1H), 4,34-4,42 (м, 1H), 5,73 (кв, J=6,8 Гц, 1H), 6,76 (с, 1H), 6,87 (дд, J=8,0, 3,2 Гц, 1H), 6,97 (с, 1H), 7,29 (д, J=8,0 Гц, 1H), 7,42 (д, J=8,0 Гц, 1H), 7,70 (д, J=11,2 Гц, 1H), 7,75 (с, 1H), 7,99 (дд, J=16,0, 8,0 Гц, 1H).
Пример 74
Синтез (Z)-(S)-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-6-метилморфолин-3-она
[Формула 80]

Синтез 3-фтор-4-(4-метил-1H-имидазол-1-ил)бензальдегида
К раствору 3,4-дифторбензальдегида (40,0 г) в ДМФА (533 мл) добавляли при комнатной температуре 4-метилимидазол (46,4 г) и карбонат калия (78,0 г) и реакционный раствор перемешивали при 90°C в течение 6 часов. Реакционный раствор оставляли охлаждаться до комнатной температуры. Этилацетат добавляли к реакционному раствору, который затем последовательно промывали водой и насыщенным раствором соли. Полученный органический слой сушили над сульфатом магния и затем концентрировали при пониженном давлении. Остаток очищали хроматографией на колонке с силикагелем (элюирующий растворитель: система гептан-этилацетат) и осаждали трет-бутилметиловым эфиром, с получением 10,1 г указанного в заголовке соединения. Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 2,33 (д, J=0,8 Гц, 3H), 7,07 (ушир.с, 1H), 7,57 (дд, J=7,2, 7,2 Гц, 1H), 7,76-7,82 (м, 2H), 7,87 (ушир.с, 1H), 10,01 (д, J=1,6 Гц, 1H).
Синтез (Z)-(S)-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-6-метилморфолин-3-она
Раствор (S)-4-[(1R,2R)-2-трет-бутилдифенилсиланилокси-1-(3,4,5-трифторфенил)пропил]-2-гидрокси-6-метилморфолин-3-она (2,16 г) и трифенилфосфингидробромида (1,61 г) в ацетонитриле (70 мл) нагревали при кипении с обратным холодильником в атмосфере азота в течение одного часа. Растворитель выпаривали при пониженном давлении и полученный остаток растворяли в этаноле (80 мл). К полученному реакционному раствору добавляли 3-фтор-4-(4-метил-1H-имидазол-1-ил)бензальдегид (869 мг) и TEA (2,68 мл) и реакционный раствор перемешивали в атмосфере азота при комнатной температуре в течение 10 часов. Растворитель выпаривали при пониженном давлении. Полученный остаток растворяли в смешанном растворителе из трифторуксусной кислоты (30 мл) и метиленхлорида (30 мл) и реакционный раствор перемешивали при комнатной температуре в течение 13 часов. Реакционный раствор вливали в насыщенный раствор бикарбоната натрия и затем экстрагировали этилацетатом. Органический слой промывали насыщенным раствором бикарбоната натрия и насыщенным раствором соли и затем растворитель выпаривали при пониженном давлении. Полученный остаток очищали колоночной хроматографией с использованием NH силикагеля (гептан:этилацетат=1:1-0:1) и осаждали смесью гептан-этилацетат с получением 1,32 г указанного в заголовке соединения.
1H-ЯМР (CDCl3) δ (м.д.): 1,33 (д, J=6,4 Гц, 3H), 1,42 (д, J=6,0 Гц, 3H), 2,30 (с, 3H), 3,19 (дд, J=12,4, 9,2 Гц, 1H), 3,63 (дд, J=12,4, 2,0 Гц, 1H), 4,44-4,49 (м, 2H), 5,36 (д, J=6,8 Гц, 1H), 6,80 (с, 1H), 6,97 (с, 1H), 7,09 (дд, J=8,4, 6,4 Гц, 2H), 7,29 (т, J=8,4 Гц, 1H), 7,44 (дд, J=8,4, 2,0 Гц, 1H), 7,71 (дд, J=12,8, 1,2 Гц, 1H), 7,74 (с, 1H).
Пример 75
Синтез (Z)-(S)-4-[(1R,2R)-1-(3,4-дифторфенил)-2-гидроксипропил]-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-она
[Формула 81]

1,15 г указанного в заголовке соединения получали по аналогичной методике примера 26, из (S)-4-[(1R,2R)-2-трет-бутилдифенилсиланилокси-1-(3,4-дифторфенил)пропил]-2-гидрокси-6-метилморфолин-3-она, полученного из 1-бром-4,5-дифторбензола в качестве исходного соединения, и 3-фтор-4-(4-метил-1H-имидазол-1-ил)бензальдегида.
1H-ЯМР (CDCl3) δ (м.д.): 1,31 (д, J=6,4 Гц, 3H), 1,41 (д, J=6,8 Гц, 3H), 2,20 (д, J=6,4 Гц, 1H), 2,30 (с, 3H), 3,15 (дд, J=12,8, 9,6 Гц, 1H), 3,57 (дд, J=12,8, 2,4 Гц, 1H), 4,42-4,48 (м, 2H), 5,38 (д, J=7,6 Гц, 1H), 6,80 (с, 1H), 6,97 (с, 1H), 7,12-7,18 (м, 2H), 7,26-7,31 (м, 2H), 7,44 (дд, J=8,4, 2,0 Гц, 1H), 7,71 (дд, J=12,8, 1,6 Гц, 1H), 7,73 (с, 1H).
Пример 76
Синтез (Z)-(S)-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-[(1R,2R)-1-(4-фторфенил)-2-гидроксипропил]-6-метилморфолин-3-она
[Формула 82]
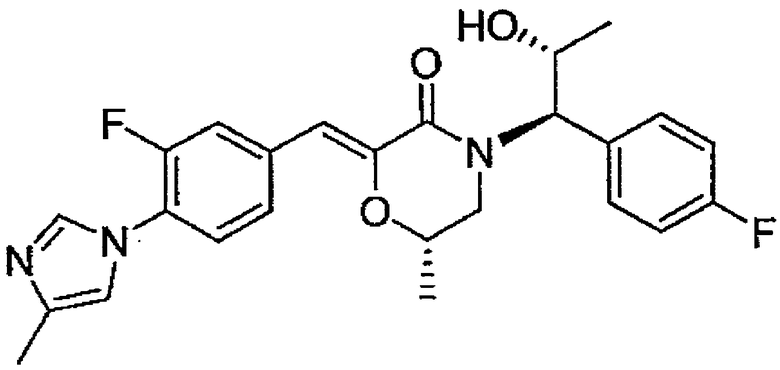
11,0 мг указанного в заголовке соединения получали по аналогичной методике примера 26, из (S)-4-[(1R,2R)-2-трет-бутилдифенилсиланилокси-1-(4-фторфенил)пропил]-2-гидрокси-6-метилморфолин-3-она, полученного из 1-бром-4-фторбензола в качестве исходного соединения, и 3-фтор-4-(4-метил-1H-имидазол-1-ил)бензальдегида.
1H-ЯМР (CDCl3) δ (м.д.): 1,31 (д, J=6,0 Гц, 3H), 1,38 (д, J=6,0 Гц, 3H), 2,30 (с, 3H), 3,12 (дд, J=12,8, 9,6 Гц, 1H), 3,57 (дд, J=12,8, 2,4 Гц, 1H), 4,46-4,50 (м, 2H), 5,46 (д, J=8,0 Гц, 1H), 6,79 (с, 1H), 6,97 (с, 1H), 7,05-7,09 (м, 2H), 7,27-7,31 (м, 1H), 7,36-7,39 (м, 2H), 7,43 (дд, J=8,4, 1,6 Гц, 1H), 7,70 (дд, J=13,2, 1,6 Гц, 1H), 7,76 (с, 1H).
Пример 77
Синтез (Z)-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-6,6-диметилморфолин-3-она
[Формула 83]

11,6 мг указанного в заголовке соединения получали по аналогичной методике примера 27, из полученного 4-[(1R,2R)-2-трет-бутилдифенилсиланилокси-1-(3,4,5-трифторфенил)пропил]-2-гидрокси-6,6-диметилморфолин-3-она и 3-фтор-4-(4-метил-1H-имидазол-1-ил)бензальдегида.
1H-ЯМР (CDCl3) δ (м.д.): 1,28 (с, 3H), 1,34 (д, J=6,0 Гц, 3H), 1,47 (с, 3H), 2,30 (с, 3H), 2,35 (д, J=4,8 Гц, 1H), 3,19 (д, J=12,8 Гц, 1H), 3,60 (д, J=12,8 Гц, 1H), 4,41-4,50 (м, 1H), 5,40 (д, J=7,2 Гц, 1H), 6,84 (с, 1H), 6,97 (с, 1H), 7,12 (дд, J=8,4, 6,4 Гц, 2H), 7,28 (т, J=8,4 Гц, 1H), 7,43 (дд, J=8,4, 2,0 Гц, 1H), 7,71 (дд, J=12,8, 1,2 Гц, 1H), 7,73 (с, 1H).
Пример 78
Синтез (Z)-4-[(1R,2R)-1-(3,4-дифторфенил)-2-гидроксипропил]-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-она
[Формула 84]

13,9 мг указанного в заголовке соединения получали по аналогичной методике примера 27, из полученного 4-[(1R,2R)-2-трет-бутилдифенилсиланилокси-1-(3,4-дифторфенил)пропил]-2-гидрокси-6,6-диметилморфолин-3-она и 3-фтор-4-(4-метил-1H-имидазол-1-ил)бензальдегида.
1H-ЯМР (CDCl3) δ (м.д.): 1,25 (с, 3H), 1,32 (д, J=6,0 Гц, 3H), 1,46 (с, 3H), 2,15 (д, J=6,4 Гц, 1H), 2,30 (с, 3H), 3,17 (д, J=12,8 Гц, 1H), 3,55 (д, J=12,8 Гц, 1H), 4,43-4,48 (м, 1H), 5,42 (д, J=7,6 Гц, 1H), 6,85 (с, 1H), 6,97 (с, 1H), 7,14-7,18 (м, 2H), 7,27-7,30 (м, 2H), 7,43 (дд, J=8,4, 1,6 Гц, 1H), 7,71 (дд, J=13,2, 1,6 Гц, 1H), 7,73 (с, 1H).
Пример 79
Синтез (Z)-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-[(1R,2R)-1-(4-фторфенил)-2-гидроксипропил]-6,6-диметилморфолин-3-она
[Формула 85]

35,1 мг указанного в заголовке соединения получали по аналогичной методике примера 27, из полученного 4-[(1R,2R)-2-трет-бутилдифенилсиланилокси-1-(4-фторфенил)пропил]-2-гидрокси-6,6-диметилморфолин-3-она и 3-фтор-4-(4-метил-1H-имидазол-1-ил)бензальдегида.
1H-ЯМР (CDCl3) δ (м.д.): 1,18 (с, 3H), 1,31 (д, J=6,0 Гц, 3H), 1,44 (с, 3H), 2,31 (с, 3H), 3,16 (д, J=12,8 Гц, 1H), 3,56 (д, J=12,8 Гц, 1H), 4,45-4,49 (м, 1H), 5,51 (д, J=8,4 Гц, 1H), 6,84 (с, 1H), 6,97 (с, 1H), 7,03-7,09 (м, 2H), 7,25-7,30 (м, 1H), 7,35-7,44 (м, 3H), 7,70 (д, J=12,8 Гц, 1H), 7,76 (с, 1H).
Пример 80
Синтез (Z)-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-[(R)-1-(4-фторфенил)-2-гидроксиэтил]-6,6-диметилморфолин-3-она
[Формула 86]
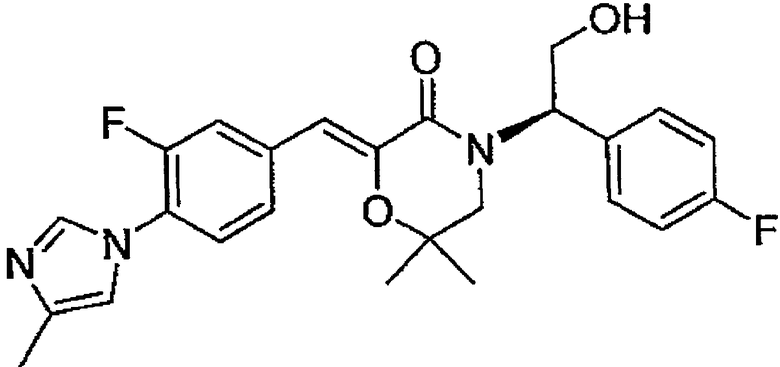
18,6 мг указанного в заголовке соединения получали по аналогичной методике примера 28, из полученного 4-[(R)-2-трет-бутилдифенилсиланилокси-1-(4-фторфенил)этил]-2-гидрокси-6,6-диметилморфолин-3-она и 3-фтор-4-(4-метил-1H-имидазол-1-ил)бензальдегида.
1H-ЯМР (CDCl3) δ (м.д.): 1,26 (с, 3H), 1,44 (с, 3H), 2,32 (с, 3H), 3,06 (д, J=12,8 Гц, 1H), 3,40 (д, J=12,8 Гц, 1H), 4,09-4,26 (м, 2H), 5,87 (дд, J=8,0, 5,6 Гц, 1H), 6,85 (с, 1H), 6,98 (с, 1H), 7,04-7,10 (м, 2H), 7,22-7,26 (м, 1H), 7,33-7,39 (м, 3H), 7,69 (д, J=12,8 Гц, 1H), 7,75 (с, 1H).
Соединения в таблице 2 получали по аналогичной методике.
Таблица 2

Примеры 82 и 83
Синтез 1-[1-(2,4-дифторфенил)этил]-3-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]-(E)-метилиден}пиперидин-2-она
[Формула 87]

Синтез 3-фтор-4-(4-метил-1H-имидазол-1-ил)бензальдегида
3,4-Дифторбензальдегид (30,0 г) растворяли в ДМФА (400 мл) и добавляли к раствору при комнатной температуре 4-метил-1H-имидазол (34,8 г) и карбонат калия (58,5 г). Реакционный раствор перемешивали при 90°C в течение 6 часов. Реакционный раствор оставляли охлаждаться до комнатной температуры. Затем добавляли к реакционному раствору этилацетат и воду и органический слой отделяли. Полученный органический слой промывали насыщенным раствором соли, сушили над сульфатом магния и затем концентрировали при пониженном давлении. Остаток очищали хроматографией на колонке с силикагелем (элюирующий растворитель: система гептан-этилацетат), осаждали трет-бутилметиловым эфиром и отделяли фильтрованием, с получением 6,28 г указанного в заголовке соединения. Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 2,32 (д, J=0,8 Гц, 3H), 7,07 (ушир.с, 1H), 7,57 (дд, J=7,2, 7,2 Гц, 1H), 7,76-7,82 (м, 2H), 7,87 (ушир.с, 1H), 10,01 (д, J=1,6 Гц, 1H).
Синтез трет-бутил (E)-5-хлор-2-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}валерата
3-Фтор-4-(4-метил-1H-имидазол-1-ил)бензальдегид (2,29 г) и трет-бутил 5-хлор-2-(диэтоксифосфорил)валерат (3,68 г) растворяли в смешанном растворителе из ТГФ (30 мл) и этанола (10 мл). Моногидрат гидроксида лития (1,41 г) добавляли к реакционному раствору при комнатной температуре и реакционный раствор перемешивали при комнатной температуре в течение 18 часов. Насыщенный водный раствор бикарбоната натрия добавляли к реакционному раствору и затем смесь экстрагировали этилацетатом. Полученный экстракт сушили над сульфатом магния и затем концентрировали при пониженном давлении. Остаток очищали хроматографией на колонке с силикагелем (элюирующий растворитель: система гептан-этилацетат), осаждали трет-бутилметиловым эфиром и гептаном и отделяли фильтрованием, с получением 1,96 г указанного в заголовке соединения. Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,56 (с, 9H), 1,98-2,07 (м, 2H), 2,31 (д, J=0,8 Гц, 3H), 2,64-2,70 (м, 2H), 3,59 (т, J=6,4 Гц, 2H), 7,01 (ушир.д, J=1,2 Гц, 1H), 7,22-7,31 (м, 2H), 7,39 (дд, J=8,0 Гц, 8,0 Гц, 1H), 7,55 (с, 1H), 7,77-7,80 (м, 1H).
Синтез трифторацетата (E)-5-хлор-2-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}валериановой кислоты
Хлороформ (5 мл) и TFA (10 мл) добавляли к трет-бутил (E)-5-хлор-2-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}валерату (1,96 г) и реакционный раствор перемешивали при комнатной температуре в течение одного часа. Реакционный раствор концентрировали при пониженном давлении. Остаток осаждали метиленхлоридом, этилацетатом и гептаном и отделяли фильтрованием, с получением 2,19 г указанного в заголовке соединения. Характеристическое значение данного соединения является следующим:
ESI-МС: m/z 323[M++H].
Синтез (E)-1-[1-(2,4-дифторфенил)этил]-3-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}пиперидин-2-она
DIEA (0,12 мл), WSC (88 мг) и HOBT (62 мг) добавляли к раствору трифторацетата (E)-5-хлор-2-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}валериановой кислоты (100 мг) и 1-(2,4-дифторфенил)этиламина (54 мг) в ДМФА (5 мл) при комнатной температуре и реакционный раствор перемешивали при комнатной температуре в течение одного часа. Этилацетат добавляли к реакционному раствору, который затем последовательно промывали насыщенным водным раствором бикарбоната натрия, водой, насыщенным раствором аммонийхлорида и насыщенным раствором соли. Полученный органический слой сушили над сульфатом магния и затем концентрировали при пониженном давлении. Остаток очищали хроматографией на колонке с силикагелем (носитель: Chromatorex NH; элюирующий растворитель: система гептан-этилацетат), с получением 98 мг [1-(2,4-дифторфенил)этил]амида (E)-5-хлор-2-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}валериановой кислоты. [1-(2,4-Дифторфенил)этил]амид (E)-5-хлор-2-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}валериановой кислоты (98 мг) растворяли в ДМФА (3 мл). Добавляли к реакционному раствору при комнатной температуре 60% гидрид натрия (10 мг) и реакционный раствор перемешивали при комнатной температуре в течение 30 минут. Насыщенный водный раствор бикарбоната натрия добавляли к реакционному раствору и затем смесь экстрагировали этилацетатом. Полученный экстракционный слой сушили над сульфатом магния и затем концентрировали при пониженном давлении. Остаток очищали хроматографией на колонке с силикагелем (носитель: Chromatorex NH; элюирующий растворитель: система гептан-этилацетат), с получением 69 мг указанного в заголовке соединения в виде рацемата. Соединение (20 мг) разделяли с помощью CHIRALCEL OJ-H производства ф. Daicel Chemical Industries, Ltd. (2 см×25 см; подвижная фаза: этанол-гексан system), с получением указанного в заголовке оптически активного соединения со временем удерживания 18 минут (пример 82) (7 мг) и указанного в заголовке оптически активного соединения со временем удерживания 24 минут (пример 83) (4 мг). Характеристические значения указанного в заголовке соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,59 (д, J=6,8 Гц, 3H), 1,77-1,87 (м, 2H), 2,31 (д, J=0,8 Гц, 3H), 2,69-2,82 (м, 1H), 2,98-3,06 (м, 1H), 3,26-3,33 (м, 1H), 3,69-3,76 (м, 1H), 6,13 (кв, J=6,8 Гц, 1H), 6,81 (ддд, J=10,4, 8,8, 2,8 Гц, 1H), 6,85-6,91 (м, 1H), 6,98 (ушир.с, 1H), 7,19-7,28 (м, 2H), 7,31-7,38 (м, 2H), 7,74 (ушир.с, 1H), 7,80 (ушир.с, 1H).
Пример 84
Синтез (E)-(S)-3-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}-1-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-5-метилпиперидин-2-она
[Формула 88]

Синтез ((R)-3-бром-2-метилпропокси)трет-бутилдифенилсилана
трет-Бутилдифенилхлорсилан (83 мл) и имидазол (30 г) добавляли к раствору (R)-3-бром-2-метил-1-пропанола (45 г) в ТГФ (150 мл) при охлаждении льдом и реакционную смесь перемешивали при комнатной температуре в течение ночи. Добавляли к реакционной смеси воду и затем смесь экстрагировали этилацетатом. Органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом магния и затем концентрировали при пониженном давлении. Остаток очищали хроматографией на колонке с силикагелем (носитель: Chromatorex NH; элюирующий растворитель: система гептан-этилацетат), с получением 117 г указанного в заголовке соединения. Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,00 (дд, J=0,8 Гц, 6,8 Гц, 3H), 1,06 (с, 9H), 2,00-2,09 (м, 2H), 3,50-3,65 (м, 4H), 7,36-7,46 (м, 6H), 7,65-7,68 (м, 4H).
Синтез трет-бутил (S)-5-(трет-бутилдифенилсиланилокси)-2-(диэтоксифосфорил)-4-метилвалерата
Раствор трет-бутил диэтилфосфоноацетата (64 г) в ТГФ (100 мл) добавляли по каплям к суспензии гидрида натрия (содержащего 40% минерального масла, 13,2 г) в ТГФ (400 мл) при охлаждении льдом и реакционную смесь перемешивали при комнатной температуре в течение 75 минут. Раствор ((R)-3-бром-2-метилпропокси)трет-бутилдифенилсилана (99,4 г) в ТГФ (100 мл) добавляли по каплям к реакционной смеси, которую затем нагревали при кипении с обратным холодильником в течение 23 часов. Ледяную воду добавляли к реакционной смеси и затем смесь экстрагировали этилацетатом. Органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом магния и затем концентрировали при пониженном давлении. Остаток очищали хроматографией на колонке с силикагелем (элюирующий растворитель: система гептан-этилацетат), с получением 74,6 г указанного в заголовке соединения. Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 0,91-0,95 (м, 3H), 1,05 (с, 9H), 1,29-1,35 (м, 6H), 1,45 (с, 9H), 1,68-1,79 (м, 1H), 1,83-2,04 (м, 1H), 2,16-2,26 (м, 1H), 2,95-3,14 (м, 1H), 3,46-3,51 (м, 2H), 4,09-4,17 (м, 4H), 7,35-7,42 (м, 6H), 7,63-7,67 (м, 4H).
трет-Бутил (E)-(S)-5-(трет-бутилдифенилсиланилокси)-2-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-метилвалерат
Раствор трет-бутил (4S)-5-(трет-бутилдифенилсиланилокси)-2-(диэтоксифосфорил)-4-метилвалерата в ТГФ (50 мл) добавляли к раствору трет-бутоксикалия (3,3 г) в ТГФ (50 мл) в атмосфере азота при -70°C и реакционную смесь перемешивали в течение 40 минут. Раствор 3-фтор-4-(4-метил-1H-имидазол-1-ил)бензальдегида (6 г) в ТГФ (50 мл) добавляли к реакционной смеси при -70°C и реакционную смесь перемешивали в течение 100 минут и при комнатной температуре в течение ночи. Воду добавляли к реакционной смеси и затем смесь экстрагировали этилацетатом. Органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом магния и затем концентрировали при пониженном давлении. Остаток очищали хроматографией на колонке с силикагелем (элюирующий растворитель: система гептан-этилацетат), с получением 9,34 г указанного в заголовке соединения. Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,55 (с, 9H), 1,99-2,08 (м, 2H), 2,30 (с, 3H), 2,63-2,71 (м, 2H), 3,59 (т, J=6,4 Гц, 2H), 3,87 (с, 3H), 6,93 (м, 1H), 7,00 (д, J=1,2 Гц, 1H), 7,09 (дд, J=8,4, 1,2 Гц, 1H), 7,27 (д, J=8,4 Гц, 1H), 7,58 (с, 1H), 7,72 (м, 1H).
Синтез трет-бутил (E)-(S)-5-хлор-2-[3-фтор-4-(4-метилимидазол-1-ил)фенил]метилиден]-4-метилвалерата
TBAF (1М раствор в ТГФ, 22,8 мл) добавляли к раствору трет-бутил (E)-(S)-5-(трет-бутилдифенилсиланилокси)-2-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-метилвалерата (9,34 г) в ТГФ (100 мл) при охлаждении льдом и реакционную смесь перемешивали при комнатной температуре в течение четырех часов. Ледяную воду добавляли к реакционной смеси и затем смесь экстрагировали этилацетатом. Органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом магния и затем концентрировали при пониженном давлении. Остаток очищали хроматографией на колонке с силикагелем (элюирующий растворитель: система гептан-этилацетат), целевые фракции собирали и концентрировали, с получением бесцветного масла (4,2 г). Трифенилфосфин (3,15 г) растворяли в растворе бесцветного масла в метиленхлориде (50 мл). N-хлорсукцинимид (1,47 г) добавляли к реакционному раствору при охлаждении льдом и реакционную смесь перемешивали при 0°C в течение одного часа. Ледяную воду добавляли к реакционной смеси и затем смесь экстрагировали хлороформом. Органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом магния и затем концентрировали при пониженном давлении. Остаток очищали хроматографией на колонке с силикагелем (носитель: Chromatorex NH; элюирующий растворитель: система гептан-этилацетат), с получением 2,84 г указанного в заголовке соединения. Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 0,96 (д, J=6,8 Гц, 3H), 1,55 (с, 9H), 2,12-2,22 (м, 1H), 2,49 (дд, J=14 Гц, 8 Гц, 1H), 2,74 (дд, J=14 Гц, 6,4 Гц, 1H), 3,37-3,46 (м, 2H), 7,00-7,02 (м, 1H), 7,22-7,29 (м, 1H), 7,38 (т, J=8 Гц, 1H), 7,56 (с, 1H), 7,77 (т, J=1,6 Гц, 1H).
Синтез гидрохлорида (E)-(S)-5-хлор-2-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}-4-метилвалериановой кислоты
Раствор трет-бутил (E)-(S)-5-хлор-2-[3-фтор-4-(4-метилимидазол-1-ил)фенил]метилиден]-4-метилвалерата (2,84 г) в трифторуксусной кислоте (20 мл) перемешивали при комнатной температуре в течение одного часа. Реакционную смесь концентрировали при пониженном давлении, добавляли к остатку этилацетат (10 мл) и раствор 4н. хлористо-водородной кислоты в этилацетате (10 мл) и реакционный раствор концентрировали при пониженном давлении. Данную операцию повторяли два раза. Добавляли к остатку диэтиловый эфир и реакционную смесь растирали шпателем. Отвержденное и осажденное нерастворимое вещество отделяли фильтрованием, с получением 2,05 г указанного в заголовке соединения. Характеристическое значение данного соединения является следующим:
ESI-МС: m/z 337[M++H].
Синтез (E)-(S)-3-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}-1-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-5-метилпиперидин-2-она
DIEA (0,47 мл), WSC (257 мг) и HOBT (181 мг) добавляли к суспензии гидрохлорида (E)-(S)-5-хлор-2-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}-4-метилвалериановой кислоты (250 мг) и гидрохлорида (1R,2R)-1-амино-1-(3,4,5-трифторфенил)пропан-2-ола (243 мг) в ДМФА (5 мл) при комнатной температуре и реакционный раствор перемешивали при комнатной температуре в течение одного часа. Этилацетат добавляли к реакционному раствору, который затем последовательно промывали насыщенным водным раствором бикарбоната натрия, водой, насыщенным раствором аммонийхлорида и насыщенным раствором соли. Полученный органический слой сушили над сульфатом магния и затем концентрировали при пониженном давлении. Остаток растворяли в ДМФА (8 мл). Добавляли 60% гидрид натрия (32 мг) при 0°C и реакционный раствор перемешивали при 0°C в течение одного часа. Этилацетат добавляли к реакционному раствору, который затем последовательно промывали насыщенным водным раствором бикарбоната натрия, водой, насыщенным раствором аммонийхлорида и насыщенным раствором соли. Полученный органический слой сушили над сульфатом магния и затем концентрировали при пониженном давлении. Остаток очищали хроматографией на колонке с силикагелем (носитель: Chromatorex NH; элюирующий растворитель: система гептан-этилацетат→система этилацетат-метанол), с получением 176 мг указанного в заголовке соединения. Характеристические значения соединения являются следующими:
ESI-МС; m/z 488[M++H].
1H-ЯМР (CDCl3) δ (м.д.): 1,03 (д, J=6,8 Гц, 3H), 1,32 (д, J=6,4 Гц, 3H), 1,86-2,00 (м, 1H), 2,31 (с, 3H), 2,39 (ддд, J=15,6, 11,6, 2,8 Гц, 1H), 2,65 (ушир.с, 1H), 2,93 (ушир.д, J=15,6, 3,6 Гц, 1H), 3,20-3,29 (м, 2H), 4,44-4,53 (м, 1H), 5,32 (д, J=7,2 Гц, 1H), 6,99-7,02 (м, 1H), 7,05-7,11 (м, 2H), 7,22-7,30 (м, 2H), 7,39 (дд, J=8,0, 8,0 Гц, 1H), 7,75-7,78 (м, 1H), 7,81 (ушир.с, 1H).
Пример 85
Синтез (E)-3-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}-1-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]пиперидин-2-она
[Формула 89]
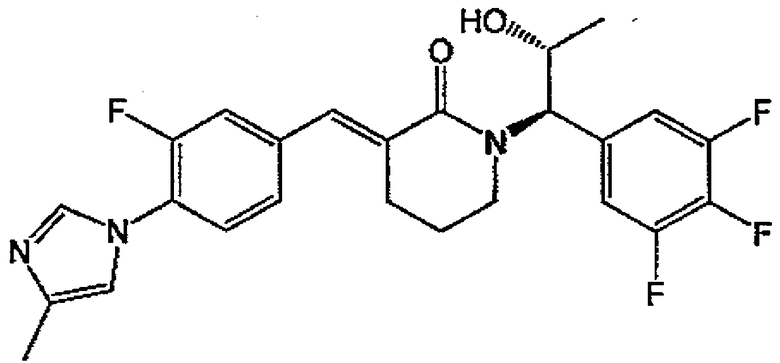
Раствор 4н. хлористого водорода в диоксане (10 мл) добавляли к раствору трет-бутил[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]карбамата (2,85 г) в диоксане (10 мл) при комнатной температуре и реакционный раствор перемешивали при комнатной температуре в течение пяти часов. Гексан (80 мл) добавляли к реакционному раствору при комнатной температуре и реакционный раствор перемешивали при комнатной температуре в течение 20 минут. Полученное твердое вещество отделяли фильтрованием, с получением гидрохлорида (1R,2R)-1-амино-1-(3,4,5-трифторфенил)пропан-2-ола (2,16 г). DIEA (1,59 мл), WSC (880 мг) и HOBT (620 мг) добавляли к раствору трифторацетата (E)-5-хлор-2-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}валериановой кислоты (1,00 г) и гидрохлорида (1R,2R)-1-амино-1-(3,4,5-трифторфенил)пропан-2-ола (664 мг) в ДМФА (25 мл) при комнатной температуре и реакционный раствор перемешивали при комнатной температуре в течение одного часа. Этилацетат добавляли к реакционному раствору, который затем последовательно промывали насыщенным водным раствором бикарбоната натрия, водой, насыщенным раствором аммонийхлорида и насыщенным раствором соли. Полученный органический слой сушили над сульфатом магния и затем концентрировали при пониженном давлении. Полученное твердое вещество промывали гептаном, с получением [(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]амида (E)-5-хлор-2-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}валериановой кислоты (1,10 г). [(1R,2R)-2-Гидрокси-1-(3,4,5-трифторфенил)пропил]амид (E)-5-хлор-2-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}валериановой кислоты (1,10 г) растворяли в ДМФА (25 мл). Добавляли к реакционному раствору при комнатной температуре 60% гидрид натрия (104 мг) и реакционный раствор перемешивали при комнатной температуре в течение одного часа. Этилацетат добавляли к реакционному раствору, который затем последовательно промывали насыщенным водным раствором бикарбоната натрия, водой, насыщенным раствором аммонийхлорида и насыщенным раствором соли. Полученный органический слой сушили над сульфатом магния и затем концентрировали при пониженном давлении. Остаток очищали хроматографией на колонке с силикагелем (носитель: Chromatorex NH; элюирующий растворитель: система гептан-этилацетат→система этилацетат-метанол), осаждали этилацетатом и гептаном и отделяли фильтрованием, с получением 780 мг указанного в заголовке соединения. Характеристические значения соединения являются следующими:
ESI-МС; m/z 474[M++H].
1H-ЯМР (CDCl3) δ (м.д.): 1,31 (д, J=6,0 Гц, 3H), 1,77-1,98 (м, 2H), 2,31 (д, J=0,8 Гц, 3H), 2,73 (ушир.д, J=6,4 Гц, 1H), 2,77-2,85 (м, 2H), 3,27 (ддд, J=12,4, 7,2, 4,0 Гц, 1H), 3,54 (ддд, J=12,4, 8,0, 4,0 Гц, 1H), 4,43-4,53 (м, 1H), 5,28 (д, J=7,6 Гц, 1H), 6,99-7,02 (м, 1H), 7,04-7,12 (м, 2H), 7,23-7,31 (м, 2H), 7,38 (дд, J=8,0, 8,0 Гц, 1H), 7,75-7,77 (м, 1H), 7,80-7,83 (м, 1H).
Пример 86
Синтез (E)-1-[(1R,2R)-1-(3,4-дифторфенил)-2-гидроксипропил]-3-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}пиперидин-2-она
[Формула 90]

Раствор 4н. хлористого водорода в этилацетате (10 мл) добавляли к раствору трет-бутил[(1R,2R)-1-(3,4-дифторфенил)-2-гидроксипропил]карбамата (960 мг) в метаноле (10 мл) при комнатной температуре и реакционный раствор перемешивали при комнатной температуре в течение 30 минут. Реакционный раствор концентрировали при пониженном давлении, с получением гидрохлорида (1R,2R)-1-амино-1-(3,4-дифторфенил)пропан-2-ола (747 мг). DIEA (1,59 мл), WSC (880 мг) и HOBT (620 мг) добавляли к раствору трифторацетата (E)-5-хлор-2-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}валериановой кислоты (1,00 г) и гидрохлорида (1R,2R)-1-амино-1-(3,4-дифторфенил)пропан-2-ола (612 мг) в ДМФА (20 мл) при комнатной температуре и реакционный раствор перемешивали при комнатной температуре в течение одного часа. Этилацетат добавляли к реакционному раствору, который затем последовательно промывали насыщенным водным раствором бикарбоната натрия, водой, насыщенным раствором аммонийхлорида и насыщенным раствором соли. Полученный органический слой сушили над сульфатом магния и затем концентрировали при пониженном давлении. Полученное твердое вещество промывали гептаном с получением [(1R,2R)-1-(3,4-дифторфенил)-2-гидроксипропил]амида (E)-5-хлор-2-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}валериановой кислоты (977 мг). [(1R,2R)-1-(3,4-Дифторфенил)-2-гидроксипропил]амид (E)-5-хлор-2-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}валериановой кислоты (977 мг) растворяли в ДМФА (25 мл). Добавляли к реакционному раствору при комнатной температуре 60% гидрид натрия (95 мг) и реакционный раствор перемешивали при комнатной температуре в течение 30 минут. Воду добавляли к реакционному раствору и затем смесь экстрагировали этилацетатом. Полученный экстракт сушили над сульфатом магния и затем концентрировали при пониженном давлении. Остаток очищали хроматографией на колонке с силикагелем (носитель: Chromatorex NH; элюирующий растворитель: система этилацетат-метанол), осаждали этилацетатом и гептаном и отделяли фильтрованием, с получением 740 мг указанного в заголовке соединения. Характеристические значения соединения являются следующими:
ESI-МС; m/z 456[M++H].
1H-ЯМР (CDCl3) δ (м.д.): 1,30 (д, J=6,0 Гц, 3H), 1,74-1,96 (м, 2H), 2,31 (д, J=0,4 Гц, 3H), 2,68-2,85 (м, 3H), 3,19-3,28 (м, 1H), 3,47-3,56 (м, 1H), 4,43-4,52 (м, 1H), 5,36 (д, J=8,0 Гц, 1H), 6,99 (с, 1H), 7,10-7,18 (м, 2H), 7,21-7,29 (м, 3H), 7,36 (дд, J=8,4, 7,6 Гц, 1H), 7,75 (ушир.с, 1H), 7,80 (ушир.с, 1H).
Соединения в таблицах 3-1, 3-2 и 3-3 получали по аналогичной методике.
[Таблица 3-1]

Таблица 3-2

Таблица 3-3

Пример 106
Синтез (Z)-(6S,8aR)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)бензилиден]-6-(3,4,5-трифторфенил)тетрагидропирроло[2,1-c][1,4]оксазин-4-она
[Формула 91]

Синтез этил (2R,5S)-5-(3,4,5-трифторфенил)пирролидин-2-карбоксилата
К раствору 2-этилового эфира 1-трет-бутилового эфира (R)-5-оксопирролидин-1,2-дикарбоновой кислоты (CAS No. 128811-48-3; 4,1 г) в тетрагидрофуране (100 мл) добавляли по каплям при -40°C в течение 20 минут 3,4,5-трифторфенилмагнийбромид (0,35М раствор в диэтиловом эфире; 55 мл) и реакционный раствор перемешивали при -40°C в течение пяти часов. Добавляли к раствору насыщенный водный раствор аммонийхлорида и этилацетат. Реакционный раствор нагревали до комнатной температуры и органический слой отделяли. Полученный органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом магния и затем концентрировали при пониженном давлении. Остаток очищали хроматографией на колонке с силикагелем (гептан→гептан:этилацетат=1:1), с получением 4,8 г этил (R)-2-трет-бутоксикарбониламино-5-оксо-5-(3,4,5-трифторфенил)пентаноата. Раствор 4н. хлористо-водородной кислоты в этилацетате (30 мл) добавляли к раствору полученного этил (R)-2-трет-бутоксикарбониламино-5-оксо-5-(3,4,5-трифторфенил)пентаноата в этилацетате (30 мл) и раствор перемешивали в течение 15 часов. Реакционный раствор концентрировали при пониженном давлении. Этилацетат и насыщенный водный раствор бикарбоната натрия добавляли к остатку и органический слой отделяли. Полученный органический слой сушили над безводным сульфатом магния и затем концентрировали при пониженном давлении. К раствору остатка в этилацетате (50 мл) добавляли 10% палладий на углероде (100 мг) и реакционный раствор перемешивали в токе водорода при 1 атм в течение 6 часов. Реакционный раствор фильтровали через целит и фильтрат концентрировали при пониженном давлении, с получением 2,91 г указанного в заголовке соединения. Характеристическое значение данного соединения является следующим:
ESI-МС: m/z 274[M++H].
Синтез [(2R,5S)-5-(3,4,5-трифторфенил)пирролидин-2-ил]метанола
LAH (483 мг) добавляли к раствору этил (2R,5S)-5-(3,4,5-трифторфенил)пирролидин-2-карбоксилата (2,91 г) в ТГФ (50 мл) при -15°C в течение одного часа. Реакционный раствор перемешивали при -15°C в течение 19 часов. Воду (0,5 мл), 5н. раствор гидроксида натрия (0,5 мл) и воду (1,5 мл) последовательно добавляли к реакционному раствору и смесь перемешивали при комнатной температуре в течение 30 минут. Реакционный раствор фильтровали через целит и фильтрат концентрировали при пониженном давлении, с получением 2,4 г указанного в заголовке соединения. Характеристические значения соединения являются следующими:
ESI-МС; m/z 232[M++H].
1H-ЯМР (CDCl3) δ (м.д.): 1,51-1,63 (м, 1H), 1,66-1,77 (м, 1H), 1,89-2,00 (м, 1H), 2,10-2,20 (м, 1H), 3,43 (дд, J=10,0, 5,6 Гц, 1H), 3,47-3,55 (м, 1H), 3,64 (дд, J=10,0, 3,6 Гц, 1H), 4,23 (т, J=8,0 Гц, 1H), 7,02 (т, J=8,0 Гц, 2H).
Синтез (Z)-(6S,8aR)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)бензилиден]-6-(3,4,5-трифторфенил)тетрагидропирроло[2,1-c][1,4]оксазин-4-она
521 мг указанного в заголовке соединения получали из [(2R,5S)-5-(3,4,5-трифторфенил)пирролидин-2-ил]метанола в качестве исходного соединения по аналогичной методике примера 41. Характеристические значения соединения являются следующими:
ESI-МС; m/z 470[M++H].
1H-ЯМР (CDCl3) δ (м.д.): 1,71-1,82 (м, 1H), 1,92-1,98 (м, 1H), 2,10-2,20 (м, 2H), 2,30 (с, 3H), 2,37-2,48 (м, 1H), 3,86 (с, 3H), 4,09-4,13 (м, 1H), 4,68 (д, J=8 Гц, 1H), 5,14 (д, J=9,2 Гц, 1H), 6,75 (с, 1H), 6,84 (дд, J=8,4 Гц, 6,4 Гц, 2H), 6,93-6,94 (м, 1H), 7,21 (д, J=8 Гц, 1H), 7,37-7,41 (м, 2H), 7,72 (д, J=1,2 Гц, 1H).
Пример 107
Синтез (6S,9aR)-6-(4-хлорфенил)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]-(Z)-метилиден}гексагидропиридо[2,1-c][1,4]оксазин-4-она
[Формула 92]
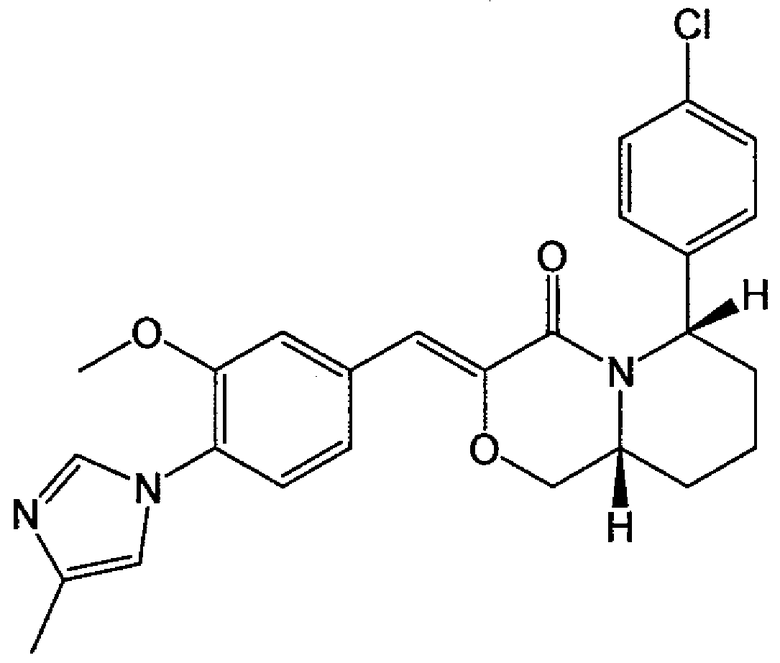
Синтез метил (2R,6S)-6-(4-хлорфенил)пиперидин-2-карбоксилата
К раствору 1-трет-бутил (R)-6-оксопиперидин-1,2-дикарбоксилата (CAS No,183890-36-0, 9,00 г) в ТГФ (120 мл) добавляли 4-хлорфенилмагнийбромид (1,0М раствор в диэтиловом эфире, 42 мл) в атмосфере азота при -78°C в течение 20 минут. Реакционный раствор перемешивали при температуре от -78 до -40°C в течение 1,5 часов и затем гасили насыщенным раствором аммонийхлорида при -40°C. Добавляли к реакционному раствору воду и затем смесь экстрагировали этилацетатом. Полученный экстракт сушили над сульфатом магния и затем концентрировали при пониженном давлении. Остаток очищали хроматографией на колонке с силикагелем (элюирующий растворитель: система гептан-этилацетат), с получением метил (R)-2-трет-бутоксикарбониламино-6-(4-хлорфенил)-6-оксогексаноата (9,53 г). Раствор 4н. хлористого водорода в этилацетате (90 мл) добавляли к раствору метил (R)-2-трет-бутоксикарбониламино-6-(4-хлорфенил)-6-оксогексаноата (9,53 г) в этилацетате (90 мл) при комнатной температуре и реакционный раствор перемешивали при комнатной температуре в течение 12 часов. Реакционный раствор концентрировали при пониженном давлении и остаток подщелачивали насыщенным раствором бикарбоната натрия. Затем хлороформ добавляли к остатку и смесь перемешивали при комнатной температуре в течение двух часов. Органический слой отделяли, сушили над сульфатом магния и затем концентрировали при пониженном давлении. К раствору остатка в метаноле (150 мл) при 0°C добавляли цианборогидрид натрия (3,29 г) и затем уксусную кислоту (4,27 мл) и реакционный раствор перемешивали при 0°C в течение одного часа и при комнатной температуре в течение одного часа. Насыщенный раствор бикарбоната натрия добавляли к реакционному раствору и затем смесь экстрагировали хлороформом. Полученный экстракт сушили над сульфатом магния и затем концентрировали при пониженном давлении. Остаток очищали хроматографией на колонке с силикагелем (элюирующий растворитель: система гептан-этилацетат) и осаждали смесью гептан-диизопропиловый эфир, с получением 2,47 г указанного в заголовке соединения. Характеристические значения соединения являются следующими:
ESI-МС; m/z 254[M++H].
1H-ЯМР (CDCl3) δ (м.д.): 1,38-1,60 (м, 3H), 1,72-1,78 (м, 1H), 1,96-2,03 (м, 1H), 2,05-2,12 (м, 1H), 2,17 (ушир.с, 1H), 3,49 (дд, J=10,8, 2,8 Гц, 1H), 3,63 (дд, J=11,2, 2,8 Гц, 1H), 3,73 (с, 3H), 7,25-7,34 (м, 4H).
Синтез [(2R,6S)-6-(4-хлорфенил)пиперидин-2-ил]метанола
Литийалюминийгидрид (508 мг) суспендировали в ТГФ (50 мл) в атмосфере азота. Метил (2R,6S)-6-(4-хлорфенил)пиперидин-2-карбоксилат (2,47 г) добавляли к суспензии при -20°C и реакционный раствор перемешивали при -20°C в течение одного часа. Воду (0,51 мл), 5н. раствор гидроксида натрия (0,51 мл) и воду (1,53 мл) последовательно добавляли к реакционному раствору при -20°C и реакционный раствор перемешивали при комнатной температуре в течение 15 минут. Этилацетат добавляли к реакционному раствору. Затем реакционный раствор фильтровали через целит и фильтрат концентрировали при пониженном давлении. Остаток очищали хроматографией на колонке с силикагелем (носитель: Chromatorex NH; элюирующий растворитель: система гептан-этилацетат), с получением 1,90 г указанного в заголовке соединения. Характеристическое значение данного соединения является следующим:
ESI-МС: m/z 226[M++H].
Синтез (6S,9aR)-6-(4-хлорфенил)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]-(Z)-метилиден}гексагидропиридо[2,1-c][1,4]оксазин-4-она
199 мг указанного в заголовке соединения получали из [(2R,6S)-6-(4-хлорфенил)пиперидин-2-ил]метанола (270 мг) по аналогичной методике примера 40. Характеристические значения соединения являются следующими:
ESI-МС; m/z 464[M++H].
1H-ЯМР (CDCl3) δ (м.д.): 1,39-1,54 (м, 2H), 1,66-1,77 (м, 2H), 2,14-2,25 (м, 2H), 2,30 (с, 3H), 3,86 (с, 3H), 4,03-4,13 (м, 2H), 4,35 (дд, J=10,4, 2,4 Гц, 1H), 5,37 (т, J=4,0 Гц, 1H), 6,83 (с, 1H), 6,93 (с, 1H), 7,20-7,23 (м, 3H), 7,30-7,33 (м, 2H), 7,36-7,40 (м, 2H), 7,73 (с, 1H).
Пример 108
Синтез (6R,9aR)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]-(Z)-метилиден}-6-(3,4,5-трифторфенил)тетрагидро[1,4]оксазино[3,4-c][1,4]оксазин-4-она
[Формула 93]

Синтез (S)-5-бензилоксиметилморфолин-3-она
Бромацетилхлорид (5,06 мл) добавляли к смешанному раствору из (R)-(+)-2-амино-3-бензилокси-1-пропанола (10 г) в толуоле (100 мл) и 2н. раствора гидроксида натрия (100 мл) при охлаждении льдом. Реакционный раствор перемешивали при 0°C в течение 30 минут и затем при 60°C в течение одного часа. Реакционный раствор снова доводили до комнатной температуры. Затем смешанный раствор толуол-ТГФ (1:1) добавляли к реакционному раствору и органический слой отделяли. Полученный органический слой сушили над безводным сульфатом магния и затем концентрировали при пониженном давлении. Остаток очищали хроматографией на колонке с силикагелем (элюирующий растворитель: система гептан-этилацетат), с получением 1,36 г указанного в заголовке соединения. Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 3,42 (т, J=9,2 Гц, 1H), 3,54 (дд, J=9,2, 5,2 Гц, 1H), 3,62 (дд, J=12,0, 6,0 Гц, 1H), 3,75 (м, 1H), 3,86 (дд, J=12,0, 4,0 Гц, 1H), 4,12 (д, J=16,8 Гц, 1H), 4,18 (д, J=16,8 Гц, 1H), 4,53 (с, 2H), 6,29 (ушир.с, 1H), 7,28-7,40 (м, 5H).
Синтез трет-бутил (S)-3-бензилоксиметил-5-оксоморфолин-4-карбоксилата
TEA (1,72 мл), 4-диметиламинопиридин (189 мг) и ди-трет-бутилдикарбонат (2,02 г) добавляли к раствору (S)-5-бензилоксиметилморфолин-3-она (1,36 г) в ацетонитриле (25 мл). Реакционный раствор перемешивали при комнатной температуре в течение двух часов. Затем насыщенный раствор соли и этилацетат добавляли к реакционному раствору и органический слой отделяли. Полученный органический слой сушили над безводным сульфатом магния и затем концентрировали при пониженном давлении. Остаток очищали хроматографией на колонке с силикагелем (элюирующий растворитель: система гептан-этилацетат), с получением 1,65 г указанного в заголовке соединения. Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,50 (с, 9H), 3,57 (дд, J=8,8, 4,8 Гц, 1H), 3,68-3,75 (м, 2H), 4,08-4,28 (м, 4H), 4,53 (д, J=12,0 Гц, 1H), 4,58 (д, J=12,0 Гц, 1H), 7,25-7,36 (м, 5H).
Синтез трет-бутил{(S)-1-бензилоксиметил-2-[2-оксо-2-(3,4,5-трифторфенил)этокси]этил}карбамата
К суспензии магния (249 мг) в диэтиловом эфире (5 мл) добавляли по каплям 1-бром-3,4,5-трифторбензол (446 мкл) при 40°C в течение 10 минут и реакционный раствор перемешивали при 40°C в течение одного часа. Полученный раствор добавляли по каплям к раствору трет-бутил (S)-3-бензилоксиметил-5-оксоморфолин-4-карбоксилата (1,1 г) в тетрагидрофуране (30 мл) при -40°C в течение 10 минут и реакционный раствор перемешивали при -40°C в течение одного часа. Насыщенный раствор аммонийхлорида добавляли к раствору небольшими порциями при -40°C и реакционный раствор снова доводили до комнатной температуры. Этилацетат добавляли к реакционному раствору и органический слой отделяли. Полученный органический слой промывали насыщенным раствором соли и затем сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали хроматографией на колонке с силикагелем (система гептан-этилацетат), с получением 952 мг указанного в заголовке соединения. Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 1,43 (с, 9H), 3,54 (дд, J=9,2, 6,0 Гц, 1H), 3,61-3,71 (м, 3H), 3,96 (м, 1H), 4,51 (с, 2H), 4,61 (с, 2H), 5,02 (м, 1H), 7,21-7,35 (м, 5H), 7,50-7,62 (м, 2H).
Синтез [(3S,5R)-5-(3,4,5-трифторфенил)морфолин-3-ил]метанола
Раствор 4н. хлористо-водородной кислоты в этилацетате (30 мл) добавляли к раствору трет-бутил{(S)-1-бензилоксиметил-2-[2-оксо-2-(3,4,5-трифторфенил)этокси]этил}карбамата (3,55 г) в этилацетате (30 мл) при комнатной температуре. Реакционный раствор перемешивали при комнатной температуре в течение одного часа и затем концентрировали при пониженном давлении. К раствору полученного остатка в метаноле (50 мл) добавляли 10% палладий на углероде (содержащий 50% воды, 167 мг) и реакционный раствор перемешивали в атмосфере водорода при комнатной температуре в течение 18 часов. Палладий на углероде удаляли из реакционного раствора фильтрованием и затем фильтрат концентрировали при пониженном давлении. Насыщенный раствор бикарбоната натрия и этилацетат добавляли к полученному остатку и органический слой отделяли. Органический слой промывали насыщенным раствором соли. Полученный органический слой сушили над безводным сульфатом магния и затем концентрировали при пониженном давлении. Остаток очищали хроматографией на колонке с силикагелем (элюирующий растворитель: система гептан-этилацетат), с получением 1,52 г указанного в заголовке соединения. Характеристические значения соединения являются следующими:
1H-ЯМР (CDCl3) δ (м.д.): 3,13-3,22 (м, 2H), 3,34 (дд, J=10,8, 10,4 Гц, 1H), 3,53 (дд, J=10,8, 6,4 Гц, 1H), 3,67 (дд, J=10,8, 4,0 Гц, 1H), 3,77 (дд, J=10,8, 3,2 Гц, 1H), 3,85 (дд, J=10,8, 3,2 Гц, 1H), 3,96 (дд, J=10,4, 3,2 Гц, 1H), 7,02-7,25 (м, 2H).
Синтез (6R,9aR)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]-(Z)-метилиден}-6-(3,4,5-трифторфенил)тетрагидро[1,4]оксазино[3,4-c][1,4]оксазин-4-она
Указанное в заголовке соединение (110 мг) получали из [(3S,5R)-5-(3,4,5-трифторфенил)морфолин-3-ил]метанола (250 мг) по аналогичной методике примера 40. Характеристические значения соединения являются следующими:
ESI-МС; m/z 486[M++H].
1H-ЯМР (CDCl3) δ (м.д.): 2,28 (с, 3H), 3,46-3,55 (м, 1H), 3,64 (дд, J=7,6, 12,4 Гц, 1H), 3,83 (с, 3H), 4,06-4,26 (м, 3H), 4,30 (м, 1H), 4,36 (дд, J=2,4, 10,4 Гц, 1H), 4,74 (дд, J=4,4, 7,2 Гц, 1H), 6,77 (с, 1H), 6,91 (ушир.с, 1H), 6,95-6,99 (м, 2H), 7,19 (д, J=8,8 Гц, 1H), 7,31-7,34 (м, 2H), 7,70 (д, J=0,8 Гц, 1H).
Пример 109
Синтез (6R,9aR)-6-(3,4-дифторфенил)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]-(Z)-метилиден}тетрагидро[1,4]оксазино[3,4-c][1,4]оксазин-4-она
[Формула 94]

185 мг указанного в заголовке соединения получали из [(3S,5R)-5-(3,4-дифторфенил)морфолин-3-ил]метанола (338 мг) по аналогичной методике примера 108. Характеристические значения соединения являются следующими:
ESI-МС; m/z 468[M++H].
1H-ЯМР (CDCl3) δ (м.д.): 2,29 (с, 3H), 3,53 (дд, J=11,2, 11,2 Гц, 1H), 3,68 (дд, J=12,0, 7,2 Гц, 1H), 3,84 (с, 3H), 4,04-4,21 (м, 3H), 4,27-4,37 (м, 2H), 4,80 (дд, J=7,2, 4,4 Гц, 1H), 6,78 (с, 1H), 6,91 (с, 1H), 7,06-7,20 (м, 4H), 7,31-7,34 (м, 2H), 7,70 (с, 1H).
Пример 110
Синтез (6R,9aR)-6-(4-фторфенил)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]-(Z)-метилиден}тетрагидро[1,4]оксазино[3,4-c][1,4]оксазин-4-она
[Формула 95]
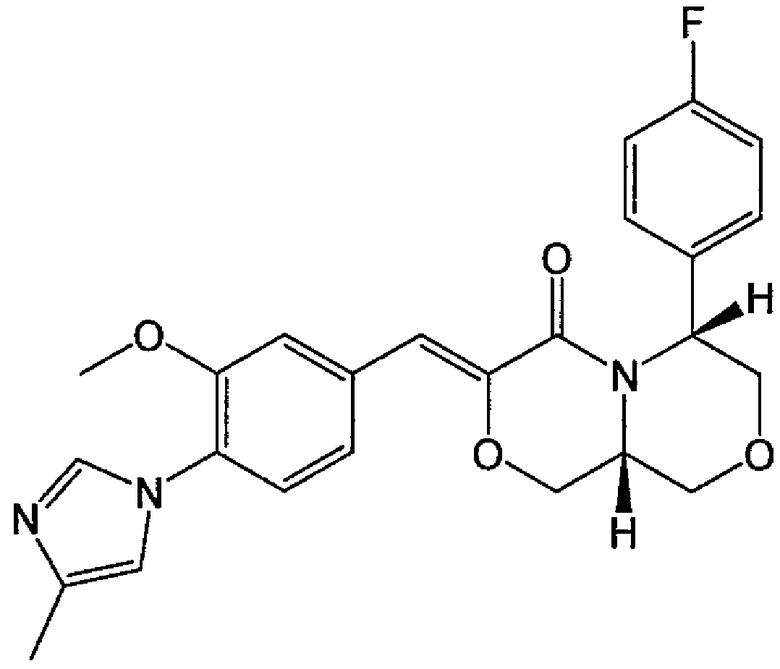
242 мг указанного в заголовке соединения получали из [(3S,5R)-5-(4-фторфенил)морфолин-3-ил]метанола (311 мг) по аналогичной методике примера 108. Характеристические значения соединения являются следующими:
ESI-МС; m/z 450[M++H].
1H-ЯМР (CDCl3) δ (м.д.): 2,29 (с, 3H), 3,55 (дд, J=11,6, 11,6 Гц, 1H), 3,72 (дд, J=12,0, 7,6 Гц, 1H), 3,83 (с, 3H), 4,02-4,21 (м, 3H), 4,30-4,36 (м, 2H), 4,85 (дд, J=7,6, 4,0 Гц, 1H), 6,79 (с, 1H), 6,91 (с, 1H), 7,03-7,07 (м, 2H), 7,19 (д, J=8,8 Гц, 1H), 7,30-7,34 (м, 4H), 7,70 (с, 1H).
Пример 111
Синтез (6R,9aR)-6-(4-хлорфенил)-3-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]-(Z)-метилиден]тетрагидро[1,4]оксадино[3,4-c]оксадин-4-она
[Формула 96]

Указанное в заголовке соединение (357 мг) получали из [(3S,5R)-5-(4-хлорфенил)морфолин-3-ил]метанола (470 мг) по аналогичной методике примера 108. Характеристические значения соединения являются следующими:
ESI-МС; m/z 466[M++H].
1H-ЯМР (CDCl3) δ (м.д.): 2,29 (с, 3H), 2,52 (т, J=11,2 Гц, 1H), 3,68 (дд, J=12,4, 8,0 Гц, 1H), 3,83 (с, 3H), 4,04 (дд, J=11,2, 4,4 Гц, 1H), 4,09-4,20 (м, 2H), 4,26-4,36 (м, 2H), 4,81 (дд, J=7,6, 4,4 Гц, 1H), 6,78 (с, 1H), 6,91 (с, 1H), 7,19 (д, J=8,4 Гц, 1H), 7,23-7,34 (м, 6H), 7,70 (с, 1H).
Авторы настоящего изобретения провели следующие испытания, чтобы показать полезность соединения общей формулы (I) по настоящему изобретению.
Пример 1 испытания
Количественное определение Aβ-пептида в культуре нейронов из головного мозга плода крысы
(1) Первичная культура нервных клеток крысы
Первичные культуры нейронов получали из коры головного мозга 18-дневных эмбрионов крыс Wistar (Charles River Japan, Yokohama, Japan). В частности, эмбрионы были асептически извлечены из беременных крыс под эфирной анестезией. Мозг извлекали из эмбриона и погружали в охлаждаемую льдом среду L-15 (например, Invitrogen Corp.Cat #11415-064, Carlsbad, CA, USA, or SIGMA L1518). Кору головного мозга собирали из извлеченного мозга под стереоскопическим микроскопом. Собранные фрагменты коры головного мозга ферментативно обрабатывали в ферментном растворе, содержащем 0,25% трипсин (Invitrogen Corp.Cat #15050-065, Carlsbad, CA, USA) и 0,01% DNase (Sigma D5025, St. Louis, MO, USA), при 37°C в течение 30 минут для диспергирования клеток. Затем ферментативную реакцию останавливали добавлением к раствору инактивированной лошадиной сыворотки. Ферментативно обработанный раствор центрифугировали при 1500 об/мин в течение пяти минут для удаления супернатанта. К полученной клеточной массе добавляли 5-10 мл среды. В качестве среды (Neurobasal/B27/2-ME) использовали нейробазальную среду (Invitrogen Corp.Cat #21103-049, Carlsbad, CA, USA), дополненную 2% B27 добавкой (Invitrogen Corp.Cat #17504-044, Carlsbad, CA, USA), 25 мкМ 2-меркаптоэтанолом (2-ME, WAKO Cat #139-06861, Osaka, Japan), 0,5 мМ L-глуамином (Invitrogen Corp.Cat #25030-081, Carlsbad, CA, USA) и антибиотиками с антимикотиками (Invitrogen Corp.Cat #15240-062, Carlsbad, CA, USA). Однако для анализа использовали указанную выше нейробазальную среду, не дополненную 2-ME (Neurobasal/B27). Клетки вновь диспергировали умеренной обработкой с помощью пипетки клеточной массы, к которой добавляли указанную среду. Клеточную дисперсию фильтровали через 40-мкм нейлоновую сетку (Cell Strainer, Cat #35-2340, Becton Dickinson Labware, Franklin Lakes, NJ, USA) для удаления оставшейся клеточной массы и в результате получали суспензию нервных клеток. Суспензию нервных клеток разводили указанной средой и затем помещали в объеме 100 мкл/лунка при начальной плотности клеток 5×105 клеток/см2 на 96-луночный полистирольный культуральный планшет, предварительно покрытый поли-L- или D-лизином (Falcon Cat #35-3075, Becton Dickinson Labware, Franklin Lakes, NJ, USA, покрытый поли-L-лизином, используя способ, описанный ниже, или BIOCOATTM cell environments Poly-D-lysine cell ware 96-well plate, Cat #35-6461, Becton Dickinson Labware, Franklin Lakes, NJ, USA). Покрытие поли-L-лизином осуществляли следующим образом. 100 мкг/мл раствора поли-L-лизина (SIGMA P2636, St. Louis, MO, USA) асептически готовили, используя 0,15 M боратный буфер (pH 8,5). По 100 мкл/лунка полученного раствора вносили в лунки 96-луночного полистирольного культурального планшета и инкубировали при комнатной температуре в течение одного или более часов, или при 4°C в течение ночи или более. Снабженный покрытием 96-луночный полистирольный культуральный планшет промывали стерильной водой четыре раза или более, затем сушили или прополаскивали, например, стерильной PBS или средой, и использовали для посева клеток. Посеянные клетки выращивали на культуральном планшете при 37°C в атмосфере 5% CO2-95% воздуха в течение одних суток. Затем всю среду заменяли свежей средой NeurobasalTM/B27/2-ME и затем клетки культивировали еще трое суток.
(2) Внесение соединения
На четвертые сутки культивирования в лунки планшета вносили лекарственное средство следующим образом. Всю среду удаляли из лунок и вносили в них по 180 мкл/лунка нейробазальной среды, не содержащей 2-ME и содержащей 2% B-27 (Neurobasal/B27). Раствор испытуемого соединения в диметилсульфоксиде (далее называемом как ДМСО) разводили средой Neurobasal/B27 таким образом, чтобы начальная концентрация была равна 10-кратной конечной концентрации. В находящуюся в лунках среду добавляли по 20 мкл/лунка полученного разбавленного раствора и тщательно смешивали его со средой. Конечная концентрация ДМСО составляла 1% или менее. В контрольную группу добавляли только ДМСО.
(3) Взятие образца
После добавления соединения клетки культивировали в течение трех суток и всю среду собирали. Полученную среду использовали в качестве образца для ELISA. Образец не разводили для измерения Aβx-42 методом ELISA и разводили до 5-кратного разведения разбавителем, поставляемым с набором ELISA, для ELISA измерения Aβx-40.
(4) Оценка выживаемости клеток
Выживаемость клеток оценивали MTT анализом по следующей методике. После сбора среды в лунки вносили по 100 мкл/лунка предварительно подогретой среды. Затем в лунки добавляли по 8 мкл/лунка раствора 8 мг/мл MTT (SIGMA M2128, St. Louis, MO, USA) в D-PBS(-) (забуференный фосфатом солевой раствор Дульбекко, SIGMA D8537, St. Louis, MO, USA). 96-луночный полистирольный культуральный планшет инкубировали в инкубаторе при 37°C в атмосфере 5% CO2-95% воздуха в течение 20 минут. Добавляли по 100 мкл/лунка буфера для MTT лизиса и кристаллы MTT формазана тщательно растворяли в буфере в инкубаторе при 37°C в атмосфере 5% CO2-95% воздуха. Затем измеряли оптическую плотность при 550 нм в каждой лунке. Буфер для MTT лизиса получали следующим образом. 100 г SDS (додецилсульфат натрия (лаурилсульфат натрия), WAKO 191-07145, Osaka, Japan) растворяли в смешанном растворе 250 мл N,N'-диметилформамида (WAKO 045-02916, Osaka, Japan) с 250 мл дистиллированной воды. Затем к раствору добавляли по 350 мкл концентрированной хлористо-водородной кислоты и концентрированной уксусной кислоты для обеспечения конечного pH около 4,7.
При измерении лунки, не содержащие посеянных клеток и содержащие только среду и раствор MTT, считали фоном (bkg). Измеренные значения соответственно применяли в следующей формуле, вычитая из них bkg значения. Таким образом, для сравнения и оценки активности в отношении выживаемости клеток вычисляли процентное отношение к контрольной группе (группа, не обработанная лекарственным веществом, CTRL) (% CTRL).
% CTRL=(A550_sample-A550_bkg)/(A550_CTRL-bkg)×100
(A550_sample: оптическая плотность при 550 нм лунки с образцом,
A550_bkg: оптическая плотность при 550 нм фоновой лунки,
A550_CTRL: оптическая плотность при 550 нм лунки контрольной группы)
(5) Определение A(методом ELISA
Для определения A(методом ELISA использовали набор Human/Rat (Amyloid (42) ELISA Kit Wako (#290-62601) и набор Human/Rat (Amyloid (40) ELISA Kit Wako (#294-62501) ф. Wako Pure Chemical Industries, Ltd., или набор Human Amyloid beta (1-42) Assay Kit (#27711) и набор Human Amyloid beta (1-40) Assay Kit (#27713) ф. Immuno-Biological Laboratories, Co., Ltd. (IBL Co., Ltd.). Анализ Aβ-ELISA проводили в соответствии с инструкциями, рекомендованными производителями (методики, описанные в прилагаемых публикациях). Тем не менее, Aβ-калибровочную кривую получали, используя бета-амилоидный пептид 1-42, крысиный и бета-амилоидный пептид 1-40, крысиный (Calbiochem, #171596 [Aβ42], #171593 [Aβ40]).
(6) Результаты
Результаты показаны в таблицах 4-1, 4-2 и 4-3 в виде процентного отношения к концентрации Aβ в среде контрольной группы (% CTRL).
Результаты в таблицах 4-1, 4-2 и 4-3, подтвердили, что соединения по настоящему изобретению обладают эффектом ингибирования продукции Aβ42.
Пример 2 испытания
Эффект на продукцию амилоида (в цереброспинальной жидкости, головном мозге и плазме крыс
Животных перемещали в лабораторию в день, предшествующий началу эксперимента (день 0). Предварительные индивидуальные номера наносили масляным карандашом на хвост животных. Измеряли их массу тела и назначали место обработки. Затем животным снова присваивали индивидуальные номера. Крысам принудительно вводили орально носитель или образец (5 мл/кг) один раз в день в течение трех дней после начала эксперимента (день 1). Через шесть часов после последнего орального введения крысам вводили внутрибрюшинно нембутал (Dainippon Pharmaceutical Co., Ltd., Osaka) (50 мг/кг). Рассекали под анестезией заднюю область шеи и вставляли в мозжечково-мозговую цистерну иглу 25G для взятия примерно 100 мкл цереброспинальной жидкости. Взятую цереброспинальную жидкость вносили в пробирку, содержащую 1 мкл p-ABSF (100 ммоль/л), и хранили во льду, чтобы не допустить разложения Aβ. Затем вскрывали брюшную полость и, пользуясь шприцем с гепарином, брали из брюшной аорты около 2,5 мл крови и хранили ее во льду. И, наконец, крыс умерщвляли, извлекали головной мозг и слегка промывали его насыщенным раствором соли, после чего измеряли влажную массу каждой половины мозга, каждую половину мозга помещали в 15 мл пробирку и замораживали жидким азотом. Взятый образец мозга хранили замороженным до момента проведения измерения. Цереброспинальную жидкость центрифугировали при 4°C при 7000 об/мин в течение пяти минут и затем собирали супернатант для определения количества Aβ. Кровь центрифугировали при 4°C при 3000 об/мин в течение пяти минут и затем собирали плазму для определения количества Aβ.
Для определения количества Aβ40 и Aβ42 цереброспинальную жидкость или плазму разводили разбавителем, поставляемым с набором для измерения количества Aβ. К мозговой ткани (правый мозг) добавляли 70% муравьиную кислоту в количестве 1 мл на 100 мг (влажная масса) ткани и подвергали ткань ультразвуковой обработке. Сразу после ультразвуковой обработки смесь подвергали 20-кратному разведению трис-буфером (0,9 моль/л) (pH 12) и нейтрализовали. Нейтрализованную жидкость непосредственно использовали для измерения количества Aβ.
Количество Aβ определяли по инструкции, приложенной к измерительному набору. В частности, на микропланшет, содержащий твердофазные антитела к Aβ40 и Aβ42, наносили по 100 мкл разбавленной цереброспинальной жидкости, разбавленного образца плазмы или исходной мозговой жидкости до нейтрализации. Добавляли на микропланшет 100 мкл каждой из различных концентраций стандартных растворов Aβ и проводили реакцию при 4°C в течение ночи. Микропланшет промывали пятикратно промывочным раствором, поставляемым с измерительным набором. Затем вносили на микропланшет HRP-меченное вторичное антитело и проводили реакцию при 4°C в течение одного часа. По окончании реакции микропланшет промывали пять раз тем же промывочным раствором, окрашивали TMB раствором и останавливали реакцию окрашивания стоп-раствором. Затем измеряли оптическую плотность при 450 нм с помощью SPECTRA MAX 190 (Molecular Devices, Sunnyvale, California, USA). Концентрацию Aβ40 и Aβ42 вычисляли по стандартной кривой.
Эффекты изобретения
Соединение общей формулы (I) или его фармакологически приемлемая соль по настоящему изобретению обладает эффектом снижения продукции Aβ42 или тому подобное. Следовательно, настоящее изобретение может, в частности, предоставить терапевтическое или профилактическое средство для нейродегенеративного заболевания, вызываемого Aβ, такого как болезнь Альцгеймера или синдром Дауна.
Промышленная применимость
Соединение общей формулы (I) по настоящему изобретению обладает эффектом снижения продукции Aβ40 и Aβ42 и, таким образом, особенно полезно в качестве профилактического или терапевтического средства для нейродегенеративного заболевания, вызываемого Aβ, такого как болезнь Альцгеймера или синдром Дауна.
| название | год | авторы | номер документа |
|---|---|---|---|
| МОДУЛЯТОРЫ МОНОАЦИЛГЛИЦЕРИНЛИПАЗЫ | 2019 |
|
RU2797323C2 |
| ЦИННАМИДНОЕ СОЕДИНЕНИЕ | 2005 |
|
RU2361872C2 |
| ЗАМЕЩЕННЫЕ ГЕТЕРОЦИКЛЫ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМАЯ СОЛЬ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ БЛОКАДЫ РЕЦЕПТОРОВ НЕЙРОКИНИНА-1 У МЛЕКОПИТАЮЩИХ, СПОСОБ ДЛЯ БЛОКАДЫ РЕЦЕПТОРОВ НЕЙРОКИНИНА-1 У МЛЕКОПИТАЮЩИХ | 1993 |
|
RU2140914C1 |
| ИНГИБИТОРНЫЕ СОЕДИНЕНИЯ | 2013 |
|
RU2673079C2 |
| АЗОТСОДЕРЖАЩИЕ КОНДЕНСИРОВАННЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ПРОДУКЦИИ БЕТА-АМИЛОИДА | 2010 |
|
RU2515976C2 |
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ МОРФОЛИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ, СПОСОБ СНИЖЕНИЯ КОЛИЧЕСТВА ТАХИКИНИНОВ ПРИ ЛЕЧЕНИИ ИЛИ ПРОФИЛАКТИКЕ ФИЗИОЛОГИЧЕСКИХ СОСТОЯНИЙ, АССОЦИИРУЕМЫХ С ИЗБЫТКОМ ТАХИКИНИНОВ | 1994 |
|
RU2131426C1 |
| ПРОИЗВОДНЫЕ МАННОЗЫ ДЛЯ ЛЕЧЕНИЯ БАКТЕРИАЛЬНЫХ ИНФЕКЦИЙ | 2014 |
|
RU2678327C2 |
| ПИРИДИЛДИМЕТИЛСУЛЬФОНОВОЕ ПРОИЗВОДНОЕ | 2006 |
|
RU2404968C2 |
| ПРОИЗВОДНЫЕ МАННОЗЫ ДЛЯ ЛЕЧЕНИЯ БАКТЕРИАЛЬНЫХ ИНФЕКЦИЙ | 2013 |
|
RU2667060C2 |
| АРИЛ-ЗАМЕЩЕННЫЕ КАРБОКСАМИДНЫЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ БЛОКАТОРОВ КАЛЬЦИЕВЫХ ИЛИ НАТРИЕВЫХ КАНАЛОВ | 2010 |
|
RU2575168C2 |
Настоящее изобретение относится к производному циннамида типа морфолина общей формулы I или его фармакологически приемлемой соли, где (a) R1, R2, R3 и R4 являются одинаковыми или различными и каждый представляет собой атом водорода или C1-6алкильную группу; X1 представляет собой C1-6алкиленовую группу, где С1-6алкиленовая группа может быть замещена 1-3 гидроксильными группами или С1-6алкильными группами, или С3-8циклоалкильной группой, образованной двумя С1-6алкильными группами, вместе присоединенными к одному и тому же атому углерода С1-6алкиленовой группы; Ха представляет собой метоксигруппу или атом фтора; Xb представляет собой атом кислорода или метиленовую группу, при условии, что Xb представляет собой только атом кислорода, когда Ха представляет собой метоксигруппу; и Ar1 представляет собой арильную группу, пиридинильную группу, которая может быть замещена 1-3 заместителями, выбранными из группы Al заместителей; (b) Ar1-X1-представляет собой С5-7циклоалкильную группу, конденсированную с бензольным кольцом, где одна метиленовая группа в С5-7циклоалкильной группе может быть заменена атомом кислорода, С5-7циклоалкильная группа может быть замещена 1-3 гидроксильными группами и/или C1-6алкильными группами, и R1, R2, R3, R4, Ха и Xb являются такими, как определено в (a); (d) Ar1-X1- и R4, вместе с атомом азота, к которому группа Ar1-X1- присоединена, и атомом углерода, к которому R4 присоединен, образуют 5-7-членную азотсодержащую гетероциклическую группу, которая замещена арильной группой или пиридинильной группой, где одна метиленовая группа в 5-7-членной азотсодержащей гетероциклической группе может быть заменена атомом кислорода, и арильная или пиридинильная группа может быть замещена 1-3 заместителями, выбранными из группы Al заместителей, Xb представляет собой атом кислорода, и R1, R2, R3 и Ха являются такими, как определено в (а) и (b); группа Al заместителей: (1) атом галогена. Также настоящее изобретение относится к фармацевтической композиции, содержащей соединение формулы I, полезной при лечении болезни Альцгеймера, старческой деменции, синдрома Дауна или амилоидоза. Технический результат: получены новые производные циннамида типа морфолина, обладающие ингибирующей активностью в отношении продукции амилоида-β. 2 н. и 15 з.п. ф-лы, 9 табл.
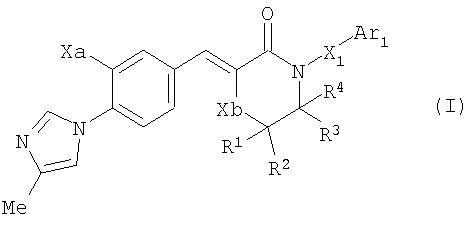
1. Соединение, представленное формулой (I):
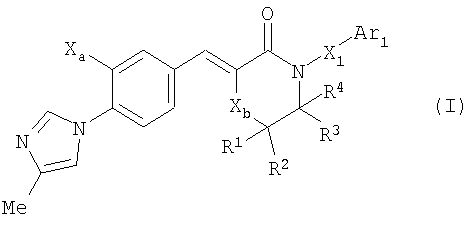
или его фармакологически приемлемая соль, где
(a) R1, R2, R3 и R4 являются одинаковыми или различными, и каждый представляет собой атом водорода или C1-6алкильную группу;
X1 представляет собой C1-6алкиленовую группу, где C1-6алкиленовая группа может быть замещена 1-3 гидроксильными группами или С1-6алкильными группами, или С3-8циклоалкильной группой, образованной двумя C1-6алкильными группами, вместе присоединенными к одному и тому же атому углерода C1-6алкиленовой группы;
Ха представляет собой метоксигруппу или атом фтора;
Xb представляет собой атом кислорода или метиленовую группу, при условии, что Xb представляет собой только атом кислорода, когда Ха представляет собой метоксигруппу; и
Ar1 представляет собой арильную группу, пиридинильную группу, которая может быть замещена 1-3 заместителями, выбранными из группы Al заместителей;
(b) Ar1-X1- представляет собой С5-7циклоалкильную группу, конденсированную с бензольным кольцом, где одна метиленовая группа в С5-7циклоалкильной группе может быть заменена атомом кислорода, С5-7циклоалкильная группа может быть замещена 1-3 гидроксильными группами и/или C1-6алкильными группами, и R1, R2, R3, R4, Ха и Xb являются такими, как определено в (а);
(d) Ar1-X1- и R4, вместе с атомом азота, к которому группа Ar1-X1-присоединена, и атомом углерода, к которому R4 присоединен, образуют 5-7-членную азотсодержащую гетероциклическую группу, которая замещена арильной группой или пиридинильной группой, где одна метиленовая группа в 5-7-членной азотсодержащей гетероциклической группе может быть заменена атомом кислорода, и арильная или пиридинильная группа может быть замещена 1-3 заместителями, выбранными из группы Al заместителей, Xb представляет собой атом кислорода, и R1, R2, R3 и Ха являются такими, как определено в (а) и (b);
группа Al заместителей: (1) атом галогена.
2. Соединение или его фармакологически приемлемая соль по п.1, где соединение представлено формулой (I-а):

где R1, R2, R3, R4, X1 и Ar1 являются такими, как определено в п.1.
3. Соединение или его фармакологически приемлемая соль по п.1, где соединение представлено формулой (II):

где R1, R2, R3, R4, Ха и Xb являются такими, как определено в п.1, R5 и R6 являются одинаковыми или различными, и каждый представляет собой атом водорода или C1-6алкильную группу, где C1-6алкильная группа может быть замещена 1-3 гидроксильными группами, и Ar1-a представляет собой фенильную группу или пиридинильную группу, которая может быть замещена 1-3 заместителями, выбранными из группы А1 заместителей, определенной в п.1.
4. Соединение или его фармакологически приемлемая соль по п.3, где соединение представлено формулой (II-а):

где R1, R2, R3 и R4 являются такими, как определено в п.1, и R5, R6 и Ar1-a являются такими, как определено в п.3.
5. Соединение или его фармакологически приемлемая соль по п.3, где соединение представлено формулой (II-b):

где R1, R2, R3 и R4 являются такими, как определено в п.1, и R5, R6 и Ar1-a являются такими, как определено в п.3.
6. Соединение или его фармакологически приемлемая соль по п.3, где соединение представлено формулой (II-с):

где R1, R2, R3 и R4 являются такими, как определено в п.1, R7 представляет собой атом водорода или C1-6алкильную группу и Ar1-a является таким, как определено в п.3.
7. Соединение или его фармакологически приемлемая соль по п.3, где соединение представлено формулой (II-d):
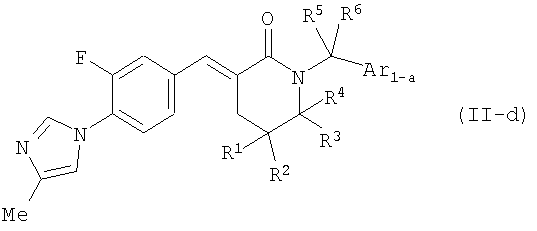
где R1, R2, R3 и R4 являются такими, как определено в п.1, и R5, R6 и Ar1-a являются такими, как определено в п.3.
8. Соединение или его фармакологически приемлемая соль по п.3, где соединение представлено формулой (II-е):

где R1, R2, R3 и R4 являются такими, как определено в п.1, Ar1-a является таким, как определено в п.3, и R7 является таким, как определено в п.6.
9. Соединение или его фармакологически приемлемая соль по п.1, где соединение представлено формулой (I-b):

где R1, R2, R3 и R4 являются такими, как определено в п.1, R13 и R14 являются одинаковыми или различными и каждый представляет собой атом водорода или заместитель, выбранный из группы Al заместителей, определенной в п.1, и Y представляет собой метиленовую группу или атом кислорода.
10. Соединение или его фармакологически приемлемая соль по п.1, где соединение представлено формулой (I-c):

где R1 и R2 являются такими, как определено в п.1, Ar1-c представляет собой фенильную группу или пиридинильную группу, которая может быть замещена 1-3 заместителями, которые являются одинаковыми или различными и выбраны из группы Al заместителей, Z1 представляет собой метиленовую группу или атом кислорода, и n и m являются одинаковыми или различными и каждый представляет собой целое число от 0 до 2, при условии, что n+m представляет собой целое число от 1 до 3.
11. Соединение или его фармакологически приемлемая соль по п.10, где Z1 представляет собой метиленовую группу.
12. Соединение или его фармакологически приемлемая соль по п.10, где Z1 представляет собой атом кислорода, и n и m представляют собой целое число 1.
13. Соединение или его фармакологически приемлемая соль по п.1, где Ar1 представляет собой фенильную группу или пиридинильную группу, или фенильную группу или пиридинильную группу, замещенную 1-3 атомами галогена.
14. Соединение или его фармакологически приемлемая соль по п.1, где соединение выбрано из следующей группы, включающей:
1) (Z)-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-4-(3,4,5-трифторбензил)морфолин-3-он,
2) (Z)-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-4-(2,3,4-трифторбензил)морфолин-3-он,
3) (Z)-(S)-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6-метил-4-(3,4,5-трифторбензил)морфолин-3-он,
4) (Z)-(R)-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6-метил-4-(3,4,5-трифторбензил)морфолин-3-он,
5) (Z)-(S)-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6-метил-4-(2,3,4-трифторбензил)морфолин-3-он,
6) (Z)-(R)-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6-метил-4-(2,3,4-трифторбензил)морфолин-3-он,
7) (Z)-4-[(S)-1-(4-фторфенил)этил]-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
8) (Z)-(R)-4-[(S)-1-(4-фторфенил)этил]-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
9) (Z)-(S)-4-[(S)-1-(4-фторфенил)этил]-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
10) (Z)-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-4-[(S)-1-(3,4,5-трифторфенил)этил]морфолин-3-он,
11) (Z)-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-4-[(R)-1-(3,4,5-трифторфенил)этил]морфолин-3-он,
12) (Z)-4-[(S)-хроман-4-ил]-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
13) (Z)-(S)-4-[(S)-хроман-4-ил]-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
14) (Z)-(R)-4-[(S)-хроман-4-ил]-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
15) (Z)-(6S,9aR)-6-(4-фторфенил)-3-{1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]}гексагидропиридо[2,1-с][1,4]оксазин-4-он,
16) (Z)-(6R,9aS)-6-(4-фторфенил)-3-{1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]}гексагидропиридо[2,1-с][1,4]оксазин-4-он,
17) (Z)-(S)-4-[(S)-1-(6-хлорпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
18) (Z)-(S)-4-[(R)-1-(6-хлорпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
19) (Z)-(S)-4-[(S)-1-(5-хлорпиридин-2-ил)этил]-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
20) (Z)-(S)-4-[(R)-1-(5-хлорпиридин-2-ил)этил]-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
21) (Z)-(S)-4-[(S)-1-(2,6-дифторпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
22) (Z)-(S)-4-[(R)-1-(2,6-дифторпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
23) (Z)-(S)-4-[(S)-1-(2,3-дифторпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
24) (Z)-(S)-4-[(R)-1-(2,3-дифторпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
25) (Z)-(S)-4-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
26) (Z)-4-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
27) (Z)-4-[(R)-1-(4-фторфенил)-2-гидроксиэтил]-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
28) (Z)-(6R)-4-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
29) (Z)-4-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]морфолин-3-он,
30) (Z)-4-[(1R,2R)-1-(3,4-дифторфенил)-2-гидроксипропил]-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]морфолин-3-он,
31) (Z)-(5)-4-[(1R,2R)-1-(4-фторфенил)-2-гидроксипропил]-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
32) (Z)-4-[(1R,2R)-1-(4-фторфенил)-2-гидроксипропил]-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
33) (Z)-(S)-4-[(1R,2R)-1-(3,4-дифторфенил)-2-гидроксипропил]-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
34) (Z)-4-[(1R,2R)-1-(3,4-дифторфенил)-2-гидроксипропил]-2-[1-[3-метокси-4-(метилимидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
35) (Z)-(5)-4-[(5)-2-гидрокси-1-метил-1-(3,4,5-трифторфенил)этил]-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
36) (Z)-(6S)-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6-метил-4-[(S)-1-(3,4,5-трифторфенил)этил]морфолин-3-он,
37) (Z)-(6S)-4-[1-(4-фторфенил)-1-метилэтил]-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
38) (Z)-(6S)-4-[1-(4-фторфенил)циклопропил]-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
39) (Z)-(6S,9aR)-3-{1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]}-6-(3,4,5-трифторфенил)гексагидропиридо[2,1-с][1,4]оксазин-4-он,
40) (Z)-(6S,9aR)-6-(3,4-дифторфенил)-3-{1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]}гексагидропиридо[2,1-с][1,4]оксазин-4-он,
41) (Z)-(6S,9aR)-6-(2,6-дифторпиридин-3-ил)-3-{1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]}гексагидропиридо[2,1-с][1,4]оксазин-4-он,
42) (Z)-(S)-4-[(S)-1-(5-фторпиридин-2-ил)этил]-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
43) (Z)-(S)-4-[(S)-1-(2-хлорпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
44) (Z)-(S)-4-[(S)-1-(2-хлор-3-фторпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
45) (Z)-(S)-4-[(S)-1-(2,6-дифторпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
46) (Z)-4-[(S)-1-(2-хлорпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
47) (Z)-4-[(S)-1-(2,6-дифторпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
48) (Z)-4-[(S)-1-(6-фторпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
49) (Z)-4-[(S)-1-(6-хлорпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
50) (Z)-4-[(S)-1-(2,3-дифторпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
51) (Z)-4-[(S)-1-(5-хлорпиридин-2-ил)этил]-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
52) (Z)-(R)-4-[(S)-1-(2,6-дифторпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
53) (Z)-(S)-4-(4-фторбензил)-2-[1-[3-фтор-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
54) (Z)-2-[1-[3-фтор-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-4-[(S)-1-(4-трифторфенил)этил]-6,6-диметилморфолин-3-он,
55) (Z)-4-[(S)-хроман-4-ил]-2-[1-[3-фтор-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
56) (Z)-(S)-4-[(S)-хроман-4-ил]-2-[1-[3-фтор-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
57) (Z)-(S)-2-[1-[3-фтор-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-4-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-6-метилморфолин-3-он,
58) (Z)-(S)-4-[(1R,2R)-1-(3,4-дифторфенил)-2-гидроксипропил]-2-[1-[3-фтор-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
59) (Z)-(S)-2-[1-[3-фтор-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-4-[(1R,2R)-1-(4-фторфенил)-2-гидроксипропил]-6-метилморфолин-3-он,
60) (Z)-2-[1-[3-фтор-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-4-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-6,6-диметилморфолин-3-он,
61) (Z)-4-[(1R,2R)-1-(3,4-дифторфенил)-2-гидроксипропил]-2-[1-[3-фтор-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
62) 1-[1-(2,4-дифторфенил)этил]-3-{1-[3-фтор-4-(4-метил-1Н-имидазол-1-ил)фенил]-(Е)-метилиден}пиперидин-2-он,
63) (E)-(S)-3-{1-[3-фтор-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден}-1-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-5-метилпиперидин-2-он,
64) (Е)-3-{1-[3-фтор-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден}-1-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]пиперидин-2-он,
65) (Е)-3-{1-[3-фтор-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден}-1-[(2R,3R)-3-гидрокси-1,1-диметилиндан-2-ил]пиперидин-2-он,
66) (Е)-3-{1-[3-фтор-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден}-1-[(S)-2-гидрокси-1-метил-1-(3,4,5-трифторфенил)этил]пиперидин-2-он,
67) (Е)-3-{1-[3-фтор-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден}-1-[1-(4-фторфенил)-1-метилэтил]пиперидин-2-он,
68) (E)-(R)-3-{1-[3-фтор-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден}-1-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-5-метилпиперидин-2-он,
69) (E)-(S)-1-[(1R,2R)-1-(3,4-дифторфенил)-2-гидроксипропил]-3-{1-[3-фтор-4-(4-метил-1Н-имидазол-1-ил)фенил]метилиден}-5-метилпиперидин-2-он,
70) (Z)-(6S,8aR)-3-{1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)бензилиден]-6-(3,4,5-трифторфенил)тетрагидропирроло[2,1-с][1,4]оксазин-4-он,
71) (6S,9aR)-6-(4-хлорфенил)-3-{1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]-(Z)-метилиден}гексагидропиридо[2,1-с][1,4]оксазин-4-он,
72) (6R,9aR)-3-{1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]-(2)-метилиден}-6-(3,4,5-трифторфенил)-тетрагидро[1,4]оксазино[3,4-с][1,4]оксазин-4-он,
73) (6R,9aR)-6-(3,4-дифторфенил)-3-{1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]-(Z)-метилиден}тетрагидро[1,4]оксазино[3,4-с][1,4]оксазин-4-он,
74) (6R,9aR)-6-(4-фторфенил)-3-{1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]-(Z)-метилиден}тетрагидро[1,4]оксазино[3,4-с][1,4]оксазин-4-он и
75) (6R,9aR)-6-(4-хлорфенил)-3-{1-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]-(Z)-метилиден}тетрагидро[1,4]оксазино[3,4-с]оксазин-4-он.
15. Фармацевтическая композиция, обладающая ингибирующей активностью в отношении продукции амилоида-β, содержащая соединение или его фармакологически приемлемую соль по любому из пп.1-14 в качестве активного ингредиента.
16. Фармацевтическая композиция по п.15 для предупреждения или лечения заболевания, вызываемого амилоидом-β.
17. Фармацевтическая композиция по п.17, где заболеванием, вызываемым амилоидом-β, является болезнь Альцгеймера, старческая деменция, синдром Дауна или амилоидоз.
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| БЕНЗОКСАЗИНОВЫЕ ИЛИ ПИРИДООКСАЗИНОВЫЕ СОЕДИНЕНИЯ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ, ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, ОБЛАДАЮЩИЕ АНТИБАКТЕРИАЛЬНОЙ АКТИВНОСТЬЮ, СПОСОБЫ ЛЕЧЕНИЯ БАКТЕРИАЛЬНЫХ ИНФЕКЦИЙ | 1996 |
|
RU2191179C2 |
Авторы
Даты
2010-02-10—Публикация
2006-10-27—Подача