Область техники
Изобретение относится к новым сепарационным материалам на основе силикагелевой матрицы, которые могут быть использованы в ионной хроматографии в качестве сорбентов для определения органических и неорганических анионов, а также в режиме гидрофильной хроматографии для определения полярных биологически активных соединений.
Уровень техники
Сорбенты для ионной хроматографии анионов характеризуются наличием в структуре четвертичных аммониевых групп, тогда как для сорбентов, используемых в гидрофильной хроматографии необходимо наличие на поверхности матрицы гидрофильных фрагментов - гидроксогрупп, аминогрупп и др. Структура функционального слоя сорбента, то есть набор конкретных функциональных групп, расположение этих групп на поверхности матрицы и относительно друг друга, а также способ закрепления такого слоя на матрице оказывают значительное влияние на селективность сорбента.
Из уровня техники известны способы модифицирования силикагелевых матриц для получения сорбентов для ионной хроматографии, обычно реализуется вариант электростатического закрепления. Например, известны полиэлектролитные анионообменные сорбенты на основе матриц, представляющих собой силикагель, модифицированных водорастворимым полимером, содержащим в цепи положительно заряженные четвертичные аммониевые группы (O.V. Krokhin, A.D. Smolenkov, N.V. Svintsova, O.N. Obrezkov, O.A. Shpigun, Modified silica as a stationary phase for ion chromatography. // J. Chromatogr. A. 1995. V. 706. P. 93-98). Для их приготовления матрицу - оксид кремния марки Silasorb C8 - смешивали с додецилбензилсульфоновой кислотой (для создания отрицательного заряда на поверхности матрицы). Затем проводили модифицирование полимером, содержащим положительно заряженные четвертичные аммониевые группы в цепи - например, раствором поли(N-этил-4-винилпиридиния бромида) или поли(диметилдиаллиламмония хлорида). Удерживание водорастворимого полимера в этом случае осуществляется за счет электростатических взаимодействий между отрицательно заряженной поверхностью матрицы и положительно заряженными четвертичными аммониевыми группами в цепи полимера. Одним из достоинств полиэлектролитных сорбентов является их высокая эффективность, обусловленная тем, что при таком подходе к синтезу отсутствует диффузия анионов вглубь частицы матрицы, что приводит к отсутствию размывания хроматографических пиков. Однако существенным недостатком полиэлектролитных сорбентов является их невысокая стабильность, которая приводит к постепенному снижению ионообменной емкости в результате изменения конформации электростатически закрепленного водорастворимого полимера, а также его постепенного смывания с поверхности матрицы.
В то же самое время, при работе в режиме гидрофильной хроматографии, где используются подвижные фазы с высоким содержанием органического растворителя, необходимую стабильность может обеспечить только ковалентное закрепление функционального слоя, так как электростатические взаимодействия значительно ослабевают в органических средах (P. Jandera, Stationary and mobile phases in hydrophilic interaction liquid chromatography: a review. // Anal. Chim. Acta. 2011. V. 692. P. 1-25).
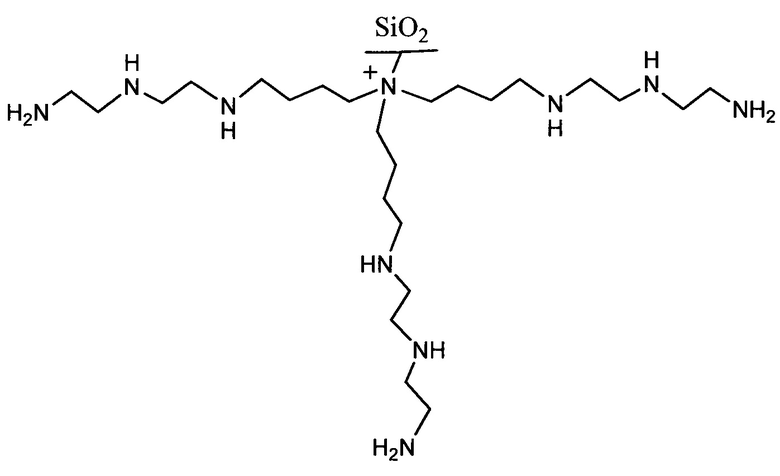
Известен принятый за прототип анионообменный сорбент для определения органических и неорганических анионов методом ионной хроматографии, в том числе анионов слабоудерживаемых органических кислот и оксигалогенидов (патент RU 2575454, МПК B01J 20/22, опубл. 20.02.2016). Сорбент содержит матрицу, выбранную из ряда: полимер на основе дивинилбензола, выступающего в качестве сшивающего агента для данного полимера, полиметакрилат, диоксид кремния, диоксид титана, диоксид циркония или оксид алюминия, аминированную первичным амином, и удаленный от поверхности матрицы с помощью спейсера водорастворимый полимер, содержащий четвертичные аммониевые функциональные группы в цепи, при этом общая формула сорбента соответствует формуле:
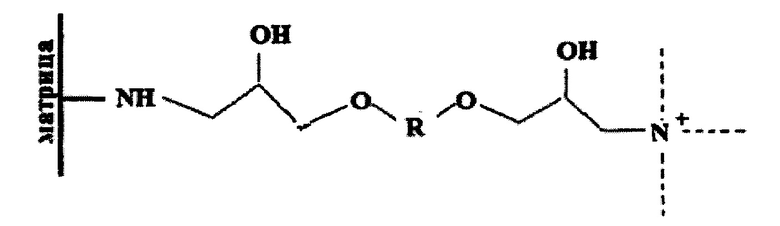
где R=(CH2)n, n=2-8,
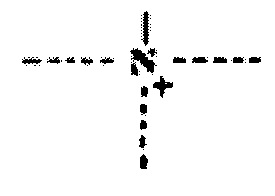 - четвертичный атом азота.
- четвертичный атом азота.
Способ получения такого анионообменного сорбента включает следующую последовательность операций:
- в качестве исходного соединения берут матрицу, выбранную из ряда полимера на основе дивинилбензола, в котором дивинилбензол является сшивающим агентом, полиметакрилата, диоксида кремния, диоксида титана, диоксид циркония или оксида алюминия;
- аминируют ее первичным амином;
- химически прививают к ней спейсер на основе соединения из класса диглицидиловых эфиров;
- модифицируют полученные соединения водорастворимым полимером, содержащим в цепи первичные, вторичные либо третичные аминогруппы до получения четвертичных аммониевых групп, химически привитых к оксирановому кольцу диглицидиловых эфиров.
Такой сорбент предназначен для ионной хроматографии анионов и характеризуется высокой селективностью и эффективностью в режиме ионной хроматографии, однако не является достаточно универсальным для селективного разделения биологически активных веществ в режиме гидрофильной хроматографии, поскольку не обеспечивает достаточного удерживания этих соединений. Это связано с наличием положительно заряженных четвертичных аммониевых групп во внешней части функционального слоя, которые вызывают отталкивание некоторых классов полярных веществ, протонируемых в кислой среде соединениями, таких как аминокислоты и водорастворимые витамины, что приводит к малым временам удерживания таких соединений и, как следствие, к низкой селективности и плохому разрешению пиков. Еще одним недостатком такого сорбента является недостаточная стабильность привитого слоя при работе в щелочных и слабощелочных средах, поскольку четвертичные аммониевые группы подвергаются элиминированию по Гофману с отщеплением аминогруппы, что ведет к постепенной утрате сорбентом его разделяющей способности. Третьим серьезным недостатком является необходимость длительного уравновешивания (около 4-х часов) хроматографической колонки с таким сорбентом, то есть длительное время выхода фонового сигнала элюента на плато со значением не более 100 ед. опт. пл.*10-3, особенно в средах с высоким содержанием органического растворителя, что связано с конформационной подвижностью привитого водорастворимого полимера.
Чтобы соответствовать всем требованиям, предъявляемым к современным сорбентам для ионной, а также для гидрофильной хроматографии, и быть пригодными для решения широкого круга все более сложных современных аналитических задач, требующих одновременного высокочувствительного определения все большего числа соединений ионной и гидрофильной природы в различных объектах, сорбенты должны обладать все более совершенными эксплуатационными и хроматографическими характеристиками, а также быть мультифункциональными, то есть селективными к нескольким классам соединений и пригодными для работы в нескольких вариантах хроматографии.
Раскрытие изобретения
Задачей предлагаемого изобретения является создание сорбента для определения соединений ионной и гидрофильной природы, обладающего улучшенными эксплуатационными и хроматографическими характеристиками.
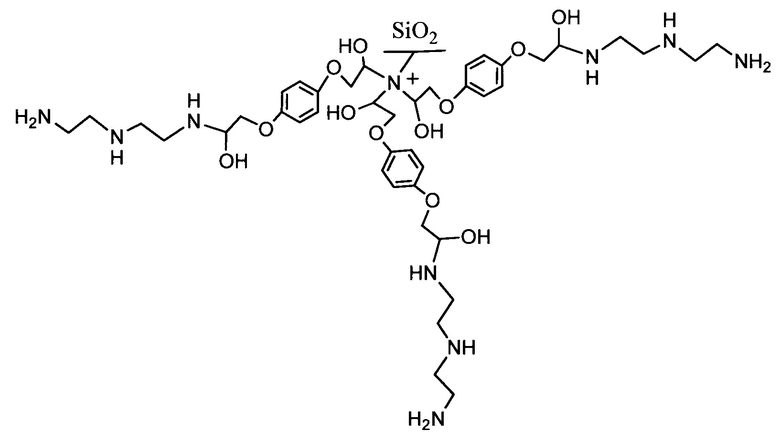
Поставленная задача решается предлагаемым сорбентом для определения органических и неорганических анионов методом ионной хроматографии и полярных биологически активных соединений - аминокислот, водорастворимых витаминов и сахаров - методом гидрофильной хроматографии, содержащим силикагелевую матрицу с химически привитой четвертичной аммониевой группой, и соединенные с ней с помощью совпадающих спейсеров R1 незаряженные атомы азота с заместителями R2, входящие в состав ди- или триамина, при этом общая формула сорбента соответствует формуле:
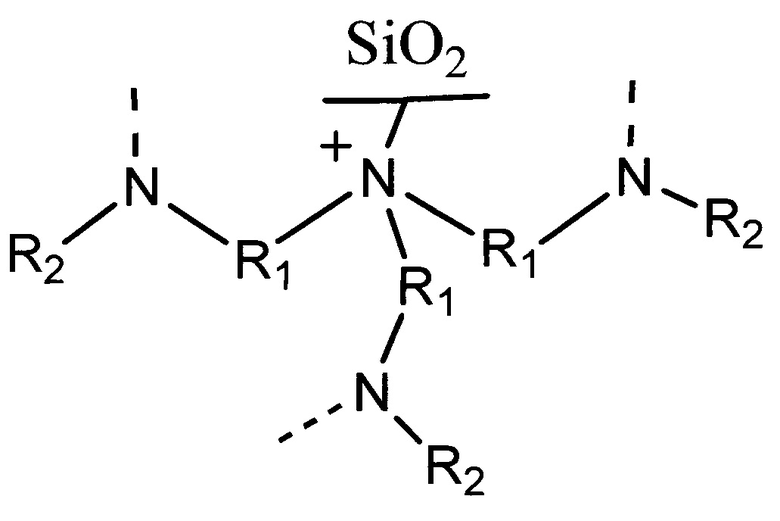
где R1 представляет собой алкильную, алканольную группу или эфирсодержащую группу;
R2 представляет собой Н, Alkyl, Alkyl-OH.
Предпочтительно в качестве силикагелевой матрицы использовать матрицу с диаметром частиц 1-10 мкм.
В настоящей заявке под спейсером подразумевается любой радикал, который может соединять между собой указанные фрагменты структуры - силикагелевую матрицу и химически привитую к ней четвертичную аммониевую группу; вторичную или третичную аммониевую группу ди- или триамина и четвертичную аммониевую группу, химически привитую к матрице.
При этом спейсеры, соединяющие четвертичную аммониевую функциональную группу, привитую к матрице, со вторичными или третичными аминогруппами, входящими в состав по крайней мере одного ди- или триамина, в предлагаемом сорбенте выбраны из ряда наиболее распространенных спейсеров: алкильный, алканольный спейсер или спейсер, содержащий эфирные группы (Zatirakha A.V., Smolenkov A.D., Shpigun О.A. Preparation and chromatographic performance of polymer-based anion exchangers for ion chromatography: a review. // Anal. Chim. Acta. 2016. V. 904. P. 33-50).
В качестве алкильных спейсеров могут быть использованы дигалогеналканы, такие как 1,2-дибромэтан, 1,3-дибромпропан, 1,4-дибромбутан, 1,5-дибромпентан.
В качестве алканольных спейсеров могут быть использованы 1,3-дибромпропанол-2, 1,5-дибромпентанол-3, 1,4-дибромбутанол-2 и другие дигалогеналканы, содержащие гидроксидные группы.
В качестве спейсеров, содержащих эфирные группы, могут быть использованы диглицидиловые эфиры, например 1,4-бутандиолдиглицидиловый эфир, резорциндиглицидиловый эфир, 1,2-этандиолдиглицидиловый эфир, этиленгликольдиглицидиловый эфир.
В качеств ди- и триаминов могут быть использованы, например, этилендиамин, диэтилентриамин, бис(гексаметилен)триамин, N,N'-бис(2-гидроксиэтил)этилендиамин.
Селективность такого сорбента по анионам в режиме ионной хроматографии обеспечивается наличием четвертичной аммониевой группы в структуре, которая находится «внутри» функционального слоя и экранирована вторичными или третичными группами ди- или триаминов, вследствие чего доступ к ней гидроксид-ионов затруднен, и вероятность элиминирования по Гофману очень мала. В то же время вторичные и третичные аминогруппы по внешней части функционального слоя обеспечивают возможность работы в режиме гидрофильной хроматографии и селективность к различным классам биологически активных соединений, при этом данные группы не подвергаются элиминированию, что обеспечивает стабильность сорбента. Кроме того, благодаря отсутствию на поверхности объемного конформационно-подвижного полимера, хроматографическая колонка с сорбентом быстро (за 30 минут) приходит в равновесие (то есть фоновый сигнал элюента выходит на плато со значением не более 100 ед. опт. пл. *10-3) перед началом анализа как в водных, так и в органических средах.
Технический результат при этом заключается в появлении возможности эксплуатации сорбентов в режимах и ионной, и гидрофильной хроматографии, улучшении хроматографических характеристик, а именно - в расширении селективности на такие классы полярных биологически активных соединений как аминокислоты, сахара и водорастворимые витамины, а также в улучшении эксплуатационных характеристик, а именно - в повышении стабильности в подвижных фазах, используемых в режимах ионной и гидрофильной хроматографии, и снижении времени уравновешивания сорбента в хроматографической колонке перед анализом с 4-х часов до 30 минут.
Краткое описание чертежей
На Фиг. 1 представлены хроматограммы разделения модельных смесей анионов, аминокислот, сахаров и водорастворимых витаминов на полученном сорбенте. Высота пиков измерялась в микросименсах.
Осуществление изобретения
Заявляемые сорбенты могут быть получены известными в литературе способами, в частности по способу, описанному выше в прототипе.
Общим для всех подходов является необходимость использования аминированной матрицы - силикагеля с привитыми первичными аминогруппами. Для синтеза можно использовать коммерчески доступный аминированный силикагель, а также обычный немодифицированный силикагель с диаметром частиц 1-10 мкм, на поверхности которого необходимо закрепить аминогруппы. Одним из возможных подходов для получения аминированного силикагеля является модифицирование силикагелевой матрицы аминопропилтриметоксисиланом, что приводит к образованию первичных аминогрупп на поверхности матрицы (Fuying Dong, Depeng Ma, Shengyu Feng. Aminopropyl-modified silica as cross-linkers of polysiloxane containing γ-chloropropyl groups for preparing heat-curable silicone rubber. // Polymer Testing. 2016. V. 52. P. 124-132).
Для модифицирования силикагелевых матриц могут быть также использованы другие силаны как минимум с одним аминоалкильным заместителем. Альтернативным вариантом получения аминированного силикагеля может являться его обработка глицидилоксипропилтриметоксисиланом или другим силилирующим реагентом, содержащим эпоксидную группу в структуре, с получением эпоксидированного силикагеля, который затем обрабатывают раствором аммиака или другим амином для раскрытия эпоксидных колец и прививки аминогрупп (Nesterenko P.N., Haddad P.R. Zwitterionic ion-exchangers in liquid chromatography. // Anal. Sci. 2000. V. 16. P. 565-574).
Для введения спейсеров далее полученные на поверхности аминогруппы алкилируют бифункциональным соединением, например диглицидиловым эфиром, дигалогеналканом или дигалогенпроизводным спиртов до образования четвертичных аммониевых групп. Затем ди- или триамины закрепляют на привитых спейсерах с помощью реакции аминирования, протекающей обычно при 50-70°С (Shchukina O.I., Zatirakha A.V., Smolenkov A.D., Nesterenko P.N., Shpigun O.A. Anion exchangers with branched functional anion exchange layers of different hydrophilicity for ion chromatography. // J. Chromatogr. A. 2015. V. 1408. P. 78-86).
Приведенные ниже примеры подтверждают, но не ограничивают заявляемые объекты изобретения.
Пример 1. Получение сорбента на основе силикагеля с диаметром частиц 5 мкм с химически привитой четвертичной аммониевой группой и соединенными с ней с помощью совпадающих спейсеров, содержащих эфирные группы, молекулами этилендиамина.
1) выбор матрицы
В качестве исходной матрицы брали аминированный силикагель Диасфер-Амин («БиоХиммак СТ», Россия) с диаметром частиц 5 мкм.
2) закрепление диамина к четвертичной аммониевой группе через спейсер
В колбу на 100 мл помещали 1 г матрицы, добавили 20 мл воды и 1 мл 1,4-бутандиолдиглицидилового эфира. Реакционную смесь перемешивали в течение 1,5 ч с помощью механической мешалки со скоростью 500 об/мин при температуре 60°С, затем отфильтровали на стеклянном фильтре и промыли 100 мл деионизованной воды. Затем суспензировали продукт на ультразвуковой ванне в 20 мл воды и добавили 2 мл этилендиамина. Реакционную смесь перемешивали в течение 1 ч с помощью механической мешалки со скоростью 500 об/мин при температуре 60°С, затем отфильтровали на стеклянном фильтре и промыли 100 мл деионизованной воды.
Полученный в результате сорбент соответствует формуле
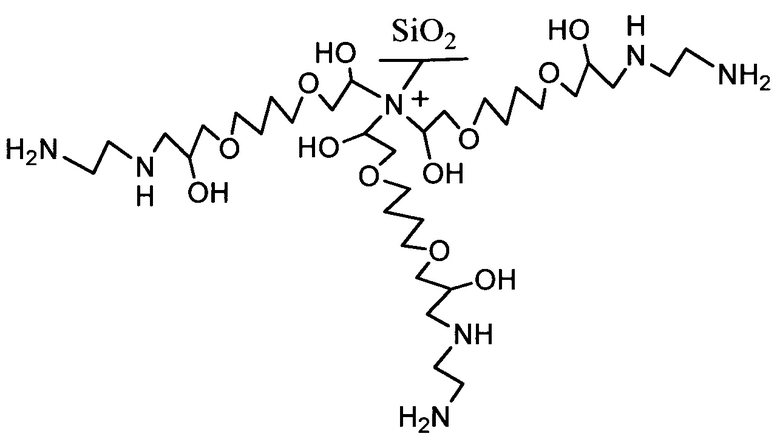
Пример 2. Получение сорбента на основе силикагеля с диаметром частиц 5 мкм с химически привитой четвертичной аммониевой группой и соединенными с ней с помощью совпадающих алканольных спейсеров молекулами этилендиамина.
Получение сорбента проводили как в примере 1, но на стадии 2 вместо (1,4-бутандиол)диглицидилового эфира брали 1,5-дибромпентанол-3 в эквивалентном количестве.
Полученный в результате сорбент соответствует формуле
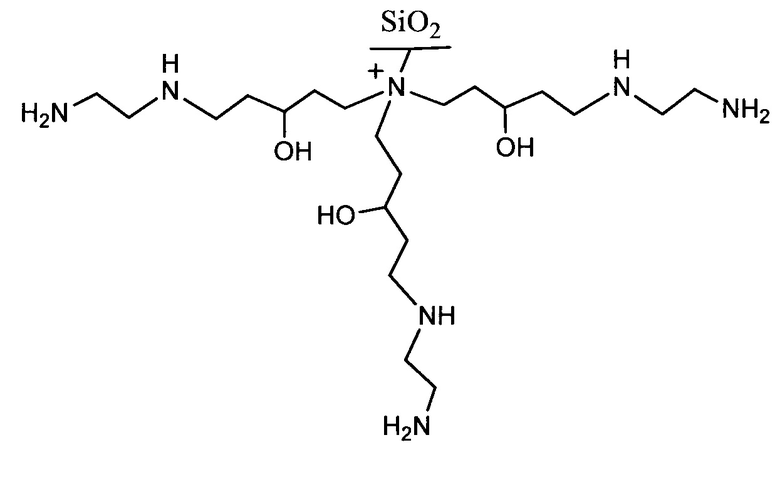
Пример 3. Получение сорбента на основе силикагеля с диаметром частиц 5 мкм с химически привитой четвертичной аммониевой группой и соединенными с ней с помощью совпадающих алканольных спейсеров молекулами диэтилентриамина.
Все как в примере 1, но на стадии 2 вместо 1,4-бутандиолдиглицидилового эфира берут 1,3-дибромпропанол-2 в эквивалентном количестве, а вместо этилендиамина берут диэтилентриамин в эквивалентном количестве.
Полученный в результате сорбент соответствует формуле
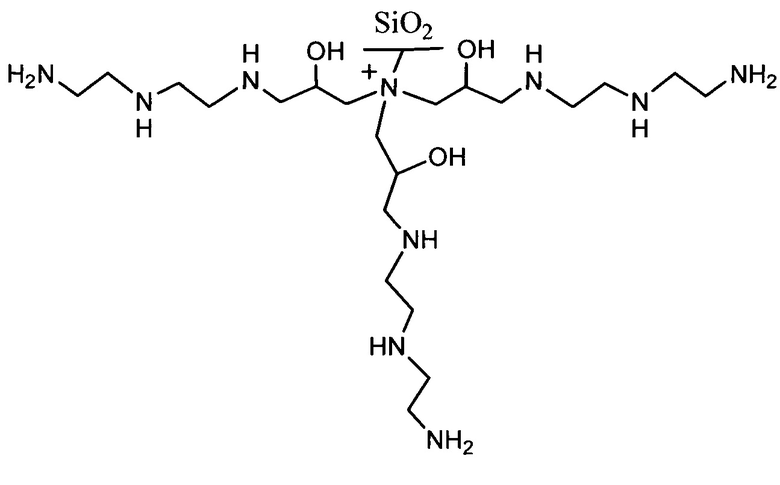
Пример 4. Получение сорбента на основе силикагеля с диаметром частиц 7 мкм с химически привитой четвертичной аммониевой группой и соединенными с ней с помощью совпадающих спейсеров, содержащих эфирные группы, молекулами бис(гексаметилен)триамина.
Получение сорбента проводили как в примере 1, только вместо аминированного силикагеля с диаметром частиц 5 мкм брали аминированный силикагель с диаметром частиц 7 мкм, а на стадии 3 вместо этилендиамина брали бис(гексаметилен)триамин в эквивалентном количестве.
Полученный в результате сорбент соответствует формуле
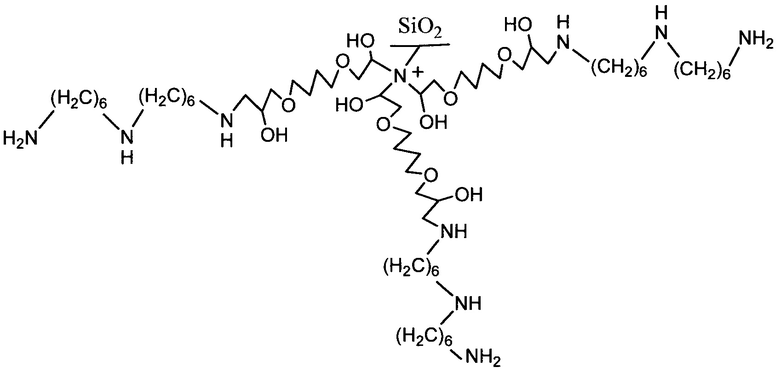
Пример 5. Получение сорбента на основе силикагеля с диаметром частиц 5 мкм с химически привитой четвертичной аммониевой группой и соединенными с ней с помощью совпадающих алкильных спейсеров молекулами диэтилентриамина.
Получение сорбента проводили как в примере 1, только на стадии 2 вместо 1,4-бутандиолдиглицидилового эфира брали 1,3-дибромпропан, а вместо этилендиамина - диэтилентриамин в эквивалентном количестве
Полученный в результате сорбент соответствует формуле
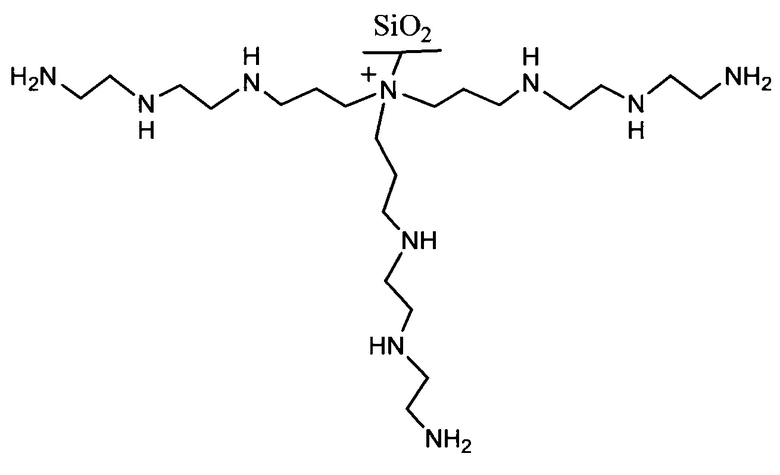
Пример 6. Получение сорбента на основе силикагеля с диаметром частиц 5 мкм с химически привитой четвертичной аммониевой группой и соединенными с ней с помощью совпадающих алкильных спейсеров молекулами диэтилентриамина.
Получение сорбента проводили как в примере 1, только на стадии 2 вместо 1,4-бутандиолдиглицидилового эфира брали 1,4-дибромбутан, а вместо этилендиамина - диэтилентриамин в эквивалентном количестве.
Полученный в результате сорбент соответствует формуле
Пример 7. Получение сорбента на основе силикагеля с диаметром частиц 5 мкм с химически привитой четвертичной аммониевой группой и соединенными с ней с помощью совпадающих спейсеров, содержащих эфирные группы, молекулами диэтилентриамина.
Получение сорбента проводили как в примере 1, только на стадии 2 вместо 1,4-бутандиолдиглицидилового эфира брали резорциндиглицидиловый эфир, а вместо этилендиамина - диэтилентриамин в эквивалентном количестве.
Полученный в результате сорбент соответствует формуле
Пример 8. Разделение органических и неорганических анионов с помощью мультифункционального сорбента в режиме ионной хроматографии.
В качестве модельной смеси была взята смесь 10 анионов, содержащая хлорид, нитрит, бромид, нитрат, иодид, роданид, ацетат, формиат, пропионат и бромат в концентрации по 50 мг/л каждого компонента. Смесь готовили путем добавления по 1 мл концентрированного раствора каждого компонента с содержанием 5000 мг/л в мерную колбу на 100 мл и последующего доведения до метки деионизованной водой. Разделение смеси проводили с помощью мультифункционального сорбента, полученного в примере 1. Сорбент упаковали в хроматографические колонки размером 100×3 мм под давлением 400 бар и проводили разделение смеси анионов в варианте ионной хроматографии со спектрофотометрическим детектированием при длине волны 254 нм. Для получения хроматограммы использовали жидкостной хроматограф Dionex Ultimate 3000 ("Thermo Fisher Scientific", США). В качестве подвижной фазы использовали гидрофталат калия с pH 4 и концентрацией 3 мМ при скорости потока 1 мл/мин. Высота пиков измерялась в микросименсах. Время уравновешивания колонки составило 30 минут. Данный сорбент позволил разделить 10 указанных анионов примерно за 16 минут с хорошим разрешением и симметрией пиков. Полученная хроматограмма, содержащая 10 пиков, приведенная на Фиг. 1(A), подтверждает селективное разделение присутствующих в модельной смеси 10 анионов в режиме ионной хроматографии. При этом стоит отметить отсутствие размывания и малую ширину пиков, что свидетельствует о высокой эффективности заявляемого сорбента (50000-80000 тт/м для разных анионов из представленного ряда) в режиме ионной хроматографии.
Пример 9. Разделение аминокислот с помощью мультифункционального сорбента в режиме гидрофильной хроматографии.
В качестве модельной смеси была взята смесь 7 аминокислот, содержащая фенилаланин, метионин, тирозин, оксипролин, аспарагин, аланин, серии в концентрации по 20 мг/л каждого компонента. Смесь готовили путем добавления по 0,5 мл концентрированного раствора каждого компонента с содержанием 2000 мг/л в мерную колбу на 50 мл и последующего доведения до метки деионизованной водой. Разделение смеси проводили с помощью мультифункционального сорбента, полученного в примере 1. Сорбент упаковали в хроматографические колонки размером 100×3 мм под давлением 400 бар и проводили разделение смеси аминокислот в варианте гидрофильной хроматографии со спектрофотометрическим детектированием при длине волны 210 нм. Для получения хроматограммы использовали жидкостной хроматограф Dionex Ultimate 3000 ("Thermo Fisher Scientific", США). В качестве подвижной фазы использовали раствор состава 80% CH3CN: 20% фосфатный буферный раствор, pH 6.5 (2 mM в п. ф.) при скорости потока 1 мл/мин. Высота пиков измерялась в микросименсах. Время уравновешивания колонки составило 30 минут. Данный сорбент позволил разделить 7 указанных аминокислот менее чем за 6 минут с хорошим разрешением и симметрией пиков. Полученная хроматограмма, содержащая 7 пиков, приведенная на Фиг. 1(Б), подтверждает селективное разделение присутствующих в модельной смеси аминокислот в режиме гидрофильной хроматографии. При этом стоит отметить отсутствие размывания и малую ширину пиков, что свидетельствует о высокой эффективности заявляемого сорбента (30000-45000 тт/м для разных аминокислот из представленного ряда) в режиме гидрофильной хроматографии.
Пример 10. Разделение водорастворимых витаминов с помощью мультифункционального сорбента в режиме гидрофильной хроматографии.
Все как в примере 7, только вместо смеси аминокислот в качестве модельной смеси брали смесь водорастворимых витаминов, содержащую никотиновую кислоту (B3), никотинамид (B3), аскорбиновую кислоту (C), B6, B12, B1, B2 в концентрации по 10 мг/л каждого компонента. Смесь готовили путем добавления по 1 мл концентрированного раствора каждого компонента с содержанием 1000 мг/л в мерную колбу на 100 мл и последующего доведения до метки деионизованной водой. В качестве подвижной фазы используют раствор состава 100 мМ CH3COONH4, pH 5,8 / ацетонитрил (градиентное элюирование); детектирование проводят при длине волны 270 нм. Время уравновешивания колонки составило 30 минут. Данный сорбент позволил разделить 7 указанных витаминов менее чем за 12 минут с хорошим разрешением и симметрией пиков. Полученная хроматограмма, содержащая 7 пиков, приведенная на Фиг. 1(B), подтверждает селективное разделение присутствующих в модельной смеси водорастворимых витаминов в режиме гидрофильной хроматографии. При этом стоит отметить отсутствие размывания и малую ширину пиков, что свидетельствует о высокой эффективности заявляемого сорбента (30000-45000 тт/м для разных водорастворимых витаминов из представленного ряда) в режиме гидрофильной хроматографии.
Пример 11. Разделение сахаров с помощью мультифункционального сорбента в режиме гидрофильной хроматографии.
Все как в примере 7, только вместо смеси аминокислот в качестве модельной смеси брали смесь сахаров, содержащую мальтозу, глюкозу, сахарозу, лактозу, рамнозу, ксилозу, фруктозу в концентрации по 50 мг/л каждого компонента. Смесь готовят путем путем добавления по 1 мл концентрированного раствора каждого компонента с содержанием 5000 мг/л в мерную колбу на 100 мл и последующего доведения до метки деионизованной водой. В качестве подвижной фазы использовали раствор состава вода:ацетонитрил (15%:85%) при скорости потока 0,44 мл/мин; используют рефрактометрическое детектирование при длине волны 270 нм. Время уравновешивания колонки составило 30 минут. Данный сорбент позволил разделить 7 указанных сахаров примерно за 20 минут с хорошим разрешением и симметрией пиков. Полученная хроматограмма, содержащая 7 пиков, приведенная на Фиг. 1(Г), подтверждает селективное разделение присутствующих в модельной смеси сахаров в режиме гидрофильной хроматографии. При этом стоит отметить отсутствие размывания и довольно малую ширину пиков, что свидетельствует о высокой эффективности заявляемого сорбента (25000-35000 тт/м для разных сахаров из представленного ряда) в режиме гидрофильной хроматографии.
Аналогичные результаты были получены при испытании всех заявляемых мультифункциональных сорбентов.
Хроматографические характеристики полученных в примерах 1-7 мультифункциональных сорбентов представлены в таблице 1.
Как видно из приведенных примеров и таблицы 1, полученные сорбенты обладают высокой эффективностью (50000-80000 тт/м в варианте ионной хроматографии), селективностью (позволяют проводить одновременное определение не менее 11 анионов в режиме ионной хроматографии, а в режиме гидрофильной хроматографии - не менее 7 аминокислот, 7 сахаров и 6 водорастворимых витаминов) и стабильностью (минимальный срок эксплуатации без изменения времен удерживания аналитов составляет 5 месяцев). Кроме того, предложенные способы получения дают возможность варьирования селективности мультифункциональных сорбентов путем варьирования структуры спейсеров и закрепленных ди- и триаминов.
Подходы к синтезу предложенных анионообменных сорбентов просты и экспрессны в исполнении (длительность синтеза 2,5 часа) и не требует использования высокотоксичных и канцерогенных реагентов.
Таким образом, предлагаемое изобретение подтверждают достижение заявленных показателей, а именно: повышенная стабильность сорбентов обеспечивает срок службы не менее 5 месяцев, эффективность повышается до 80000 тт/м и дает хорошее разрешение пиков, а повышенная селективность к различным классам соединений позволяет работать в режимах как ионной, так и гидрофильной хроматографии и подтверждает разделяющую способность сорбента в части разделения 11 неорганических и органических анионов, 7 сахаров, 7 аминокислот и 7 водорастворимых витаминов за один анализ, не являющуюся предельной. Сорбент позволяет за один хроматографический анализ получить данные о содержании соединений одного класса в составе многокомпонентной смеси.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОРБЕНТ ДЛЯ ОПРЕДЕЛЕНИЯ СОЕДИНЕНИЙ ГИДРОФИЛЬНОЙ ПРИРОДЫ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2019 |
|
RU2730316C1 |
| АНИОНООБМЕННЫЙ СОРБЕНТ ДЛЯ ОПРЕДЕЛЕНИЯ ОРГАНИЧЕСКИХ И НЕОРГАНИЧЕСКИХ АНИОНОВ МЕТОДОМ ИОННОЙ ХРОМАТОГРАФИИ | 2016 |
|
RU2627384C1 |
| АНИОНООБМЕННЫЙ СОРБЕНТ ДЛЯ ИОНОХРОМАТОГРАФИЧЕСКОГО ОПРЕДЕЛЕНИЯ ОРГАНИЧЕСКИХ И НЕОРГАНИЧЕСКИХ АНИОНОВ И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2014 |
|
RU2575454C2 |
| АНИОНООБМЕННЫЙ СОРБЕНТ ДЛЯ ИОНОХРОМАТОГРАФИЧЕСКОГО ОПРЕДЕЛЕНИЯ ОРГАНИЧЕСКИХ И НЕОРГАНИЧЕСКИХ АНИОНОВ И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2014 |
|
RU2562650C1 |
| АНИОНООБМЕННЫЙ СОРБЕНТ ДЛЯ ХРОМАТОГРАФИЧЕСКОГО ОПРЕДЕЛЕНИЯ НЕОРГАНИЧЕСКИХ ИОНОВ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2019 |
|
RU2715197C1 |
| АНИОНООБМЕННЫЙ СОРБЕНТ ДЛЯ ОДНОВРЕМЕННОГО ИОНОХРОМАТОГРАФИЧЕСКОГО ОПРЕДЕЛЕНИЯ ПОЛЯРИЗУЕМЫХ И НЕПОЛЯРИЗУЕМЫХ НЕОРГАНИЧЕСКИХ АНИОНОВ И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2012 |
|
RU2496571C1 |
| СПОСОБ ПОЛУЧЕНИЯ ХИРАЛЬНОЙ ПЛАНАРНОЙ ПЛАСТИНЫ ДЛЯ ТОНКОСЛОЙНОЙ ХРОМАТОГРАФИИ ОПТИЧЕСКИХ ИЗОМЕРОВ | 2012 |
|
RU2545315C2 |
| СПОСОБ ПОЛУЧЕНИЯ ОРГАНО-НЕОРГАНИЧЕСКОГО ВЫСОКООСНОВНОГО АНИОНООБМЕННИКА | 2010 |
|
RU2438780C2 |
| СОРБЕНТ ДЛЯ РАЗДЕЛЕНИЯ ОПТИЧЕСКИХ ИЗОМЕРОВ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2004 |
|
RU2255802C1 |
| АНИОНООБМЕННЫЙ СОРБЕНТ ДЛЯ ОДНОВРЕМЕННОГО ИОНОХРОМАТОГРАФИЧЕСКОГО ОПРЕДЕЛЕНИЯ ПОЛЯРИЗУЕМЫХ И НЕПОЛЯРИЗУЕМЫХ НЕОРГАНИЧЕСКИХ АНИОНОВ И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2010 |
|
RU2429070C1 |

Изобретение относится к сепарационным материалам, которые могут быть использованы в ионной хроматографии в качестве сорбентов для определения органических и неорганических анионов, а также в режиме гидрофильной хроматографии для определения полярных биологически активных соединений. Сорбент содержит матрицу на основе силикагеля с привитой четвертичной аммониевой группой и соединённые с ней с помощью спейсеров атомы азота с заместителями, входящие в состав диамина или триамина. Сорбент обладает улучшенными эксплуатационными и хроматографическими характеристиками. Сорбент эффективен для разделения неорганических анионов, слабоудерживаемых органических кислот, аминокислот, сахаров и витаминов. 8 з.п. ф-лы, 1 ил., 1 табл., 11 пр.
1. Сорбент для определения соединений ионной и/или гидрофильной природы, характеризующийся тем, что содержит силикагелевую матрицу с химически привитой четвертичной аммониевой группой и соединенные с ней с помощью совпадающих спейсеров R1 незаряженные атомы азота с заместителями R2, входящие в состав ди- или триамина, при этом общая формула сорбента соответствует формуле
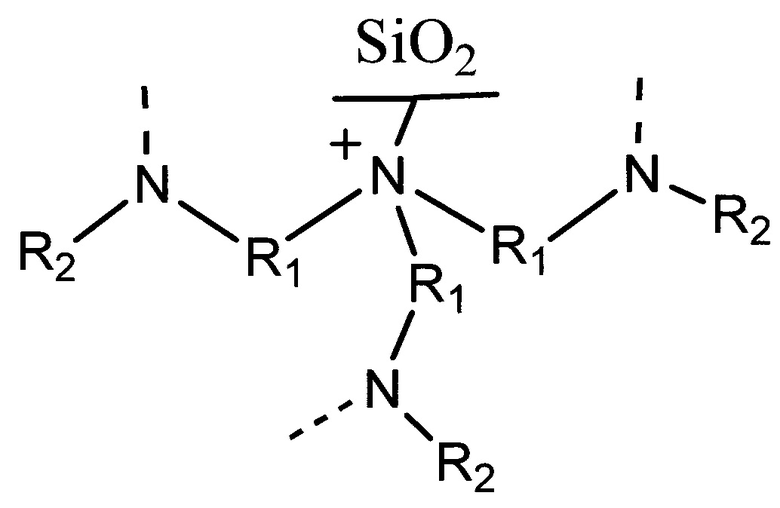
где R1 представляет собой алкильную, алканольную группу или эфирсодержащую группу; R2 представляет собой Н, Alkyl, Alkyl-OH.
2. Сорбент по п. 1, характеризующийся тем, что используют силикагелевую матрицу с диаметром частиц 1-10 мкм.
3. Сорбент по п. 1, характеризующийся тем, что в качестве ди- и триаминов используют этилендиамин, диэтилентриамин, бис(гексаметилен)триамин, N,N'-бис(2-гидроксиэтил)этилендиамин.
4. Сорбент по п. 1, характеризующийся тем, что в качестве алкильных спейсеров используют дигалогеналканы.
5. Сорбент по п. 1, характеризующийся тем, что в качестве алканольных спейсеров используют дигалогеналканы, содержащие гидроксидные группы.
6. Сорбент по п. 1, характеризующийся тем, что в качестве спейсеров, содержащих эфирные группы, используют диглицидиловые эфиры.
7. Сорбент по п. 4, характеризующийся тем, что дигалогеналканы выбирают из группы, включающей 1,2-дибромэтан, 1,3-дибромпропан, 1,4-дибромбутан, 1,5-дибромпентан.
8. Сорбент по п. 5, характеризующийся тем, что дигалогеналканы, содержащие гидроксидные группы, выбирают из группы, включающей 1,3-дибромпропанол-2, 1,5-дибромпентанол-3, 1,4-дибромбутанол-2.
9. Сорбент по п. 6, характеризующийся тем, что диглицидиловые эфиры выбирают из группы, включающей 1,4-бутандиолдиглицидиловый эфир, резорциндиглицидиловый эфир, 1,2-этандиолдиглицидиловый эфир, этиленгликольдиглицидиловый эфир.
| АНИОНООБМЕННЫЙ СОРБЕНТ ДЛЯ ИОНОХРОМАТОГРАФИЧЕСКОГО ОПРЕДЕЛЕНИЯ ОРГАНИЧЕСКИХ И НЕОРГАНИЧЕСКИХ АНИОНОВ И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2014 |
|
RU2575454C2 |
| АНИОНООБМЕННЫЙ СОРБЕНТ ДЛЯ ИОНОХРОМАТОГРАФИЧЕСКОГО ОПРЕДЕЛЕНИЯ ОРГАНИЧЕСКИХ И НЕОРГАНИЧЕСКИХ АНИОНОВ И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2014 |
|
RU2562650C1 |
| US 20150133294 A1, 14.05.2015 | |||
| Pavel Jandera, Stationary and mobil phases in interaction chromatography a review, Analytical Chimica Acta, 692, 2011, 1-25 | |||
| Bogullaw Buszewski, Hydrophilic interaction liquid chromatography (HILIC)-a powerful seperation technique, Anal Bioanal Chem., 2012, 402(1), 231-247. | |||
Авторы
Даты
2017-12-15—Публикация
2016-12-19—Подача