Область техники
Изобретение относится к области органической и аналитической химии, а именно к новым сепарационным материалам на основе силикагелевой матрицы и способам их получения, которые могут быть использованы в режиме гидрофильной хроматографии для определения полярных биологически активных соединений.
Уровень техники
Для сорбентов, используемых в гидрофильной хроматографии, необходимо наличие на поверхности матрицы гидрофильных фрагментов - амидных, аминогрупп, гидроксогрупп и др. Структура функционального слоя сорбента, то есть набор конкретных функциональных групп, их расположение на поверхности матрицы и относительно друг друга, а также способ закрепления такого слоя на матрице оказывают существенное влияние на селективность и эффективность сорбента.
Из уровня техники известны несколько путей закрепления функциональных групп на поверхности силикагелевых матриц для получения сорбентов для гидрофильной хроматографии. Адсорбционное модифицирование матрицы обладает существенным недостатком: нанесенная фаза с течением времени может смываться элюентом. При работе в режиме гидрофильной хроматографии, где используются подвижные фазы с высоким содержанием органического растворителя, необходимую стабильность может обеспечить только ковалентное закрепление функционального слоя, так как электростатические взаимодействия значительно ослабевают в органических средах (P. Jandera, Stationary and mobile phases in hydrophilic interaction liquid chromatography: a review. // Anal. Chim. Acta. 2011. V.692. P. 1-25). Именно поэтому на сегодняшний день химическое модифицирование является основным способом синтеза стабильных сорбентов [Стыскин Е.Л., Ициксон Л.Б., Брауде Е.В. Практическая высокоэффективная жидкостная хроматография. М.: Химия, 1986. С. 91]. Традиционно используемые пути ковалентного закрепления функционального слоя на силикагелевой матрице - хлорметилирование силанольных групп поверхности, а также их взаимодействие с органохлорсиланами или органоалкоксисиланами. Например, аминопропилсиликагель получают взаимодействием немодифицированной силикагелевой матрицы с аминопропилтриметоксисиланом [Лошин А.А. Новые ионообменники на основе силикагеля, поверхностно-модифицированного поливинилпиридином и полиэтиленимином, для ионохроматографического определения анионов. Дисс.канд. хим. наук. Москва. 2016].
В настоящее время в связи с усложнением решаемых аналитических задач синтез новых селективных неподвижных фаз требует более сложных процедур ковалентного модифицирования. Например, для одновременного введения в функциональный слой сорбентов различных групп сначала получают соответствующие лиганды и только после этого закрепляют их на поверхности силикагелевой матрицы [Gargano A.F. G, Leek В.Т., Lindner W., Lammerhofer М. Mixed-mode chromatography with zwitterionic phosphopeptidomimetic selectors from Ugi multicomponent reaction // J. Chromatogr. A. 2013. V. 1317. P. 12-21; Ferreira C.C., Gama M.R., Silva G.S., Pereira A.W., Collins C.H, Jardim I.C. S.F. Synthesis and evaluation of a pentafluorobenzamide stationary phase for HPLC separations in the reversed phase and hydrophilic interaction modes // J. Sep.Sci. 2018. V. 41. P. 1-22; Kotoni D.,  I., Ciogli A., Villani C, Capitani D., Gasparrini F. Design and
I., Ciogli A., Villani C, Capitani D., Gasparrini F. Design and
evaluation of hydrolytically stable bidentate urea-type stationary phases for hydrophilic interaction chromatography // J. Chromatogr. A. 2012. V.1232. P. 196-211].
Из уровня техники известен сорбент на основе силикагелевой матрицы для определения органических и неорганических анионов в режиме ионной хроматографии, а также для определения полярных биологически активных соединений в режиме гидрофильной хроматографии, соответствующий следующей формуле (1):
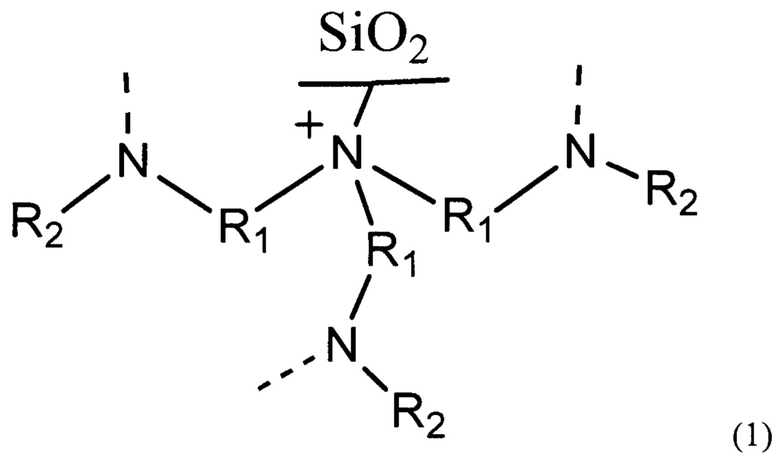
где R1 представляет собой алкильную, алканольную группу или эфирсодержащую группу; R2 представляет собой Н, Alkyl, Alkyl-OH. Однако данный сорбент уступает в селективности и эффективности по нейтральным и кислотным полярным аналитам: способен разделить не более 7 сахаров и неселективен к органическим кислотам.
Известен принятый за прототип сорбент для определения соединений ионной и гидрофильной природы, в том числе аминокислот, сахаров и водорастворимых витаминов [Garganoa A. F.G, Leekb Т., Lindnera W., Lammerhofer М. Mixed-mode chromatography with zwitterionic phosphopeptidomimetic selectors from Ugi multicomponent reaction // J. Chromatogr. A. 2013. V. 1317. P. 12-21], содержащий силикагелевую матрицу с химически привитым тиопропильным фрагментом и соединенные с ним с лиганды, содержащие амидные и фосфониевые группы и заместители R1, R2, R3, при этом общая формула сорбента соответствует формуле (2):
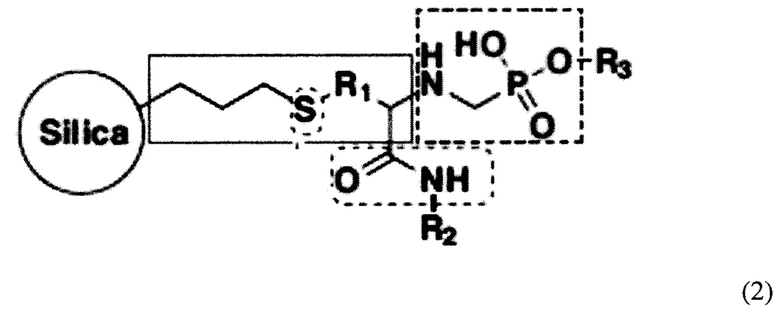
где R1 представляет собой алкильную группу;
R2 представляет собой трет-бутильный или оксазиновый фрагмент; R3 представляет собой Н или СН3.
Способ получения такого сорбента включает следующую последовательность операций:
- в качестве исходного соединения берут матрицу на основе диоксида кремния (диаметр частиц 5 мкм);
- матрицу предварительно модифицируют бис-триметилсилил ацетамидом, таким образом прививая тиопропильные группы, и высушивают в печи;
- получают лиганд путем добавления 1-аминометилфосфоновой кислоты к выбранному альдегиду в метаноле, введения гидроксида тетрабутиламмония и изоцианида и проведения реакции в микроволновом поле при 100°С в течение 2,5 ч, отфильтровывают продукты и продолжают реакцию с оставшимся осадком, содержащим непрореагировавшую кислоту, в течение следующих 2,5 часов. Фильтрат упаривают и выделяют лиганд путем жидкость-жидкостной хроматографии.
- модифицируют лиганд бромотриметилсиланом при комнатной температуре в течение суток, путем отгонки заменяют растворитель с дихлорметана на метанол, выдерживают 2 ч при 50°С и концентрируют под вакуумом.
- прививают модифицированный лиганд к матрице в течение 6-24 ч, промывают и высушивают при 60°С, затем упаковывают в колонки.
Такой сорбент предназначен для обращено-фазовой хроматографии гидрофобных соединений и разделения биологически активных веществ в режиме гидрофильной хроматографии, характеризуется приемлемой селективностью и эффективностью, однако не является достаточно универсальным для селективного разделения некоторых классов биологически активных веществ, таких как органические кислоты, поскольку не обеспечивает достаточного удерживания этих соединений. Это связано с наличием отрицательно заряженных фосфониевых групп во внешней части функционального слоя, которые придают сорбенту свойства катионообменника, вызывают электростатическое отталкивание веществ кислотного характера и не способствуют их хроматографическому разделению, что приводит к низкой селективности и плохому разрешению пиков. Еще одним недостатком такого сорбента является недостаточная гидрофильность функционального слоя вследствие наличия гидрофобных алкильных спейсеров, соединяющих матрицу с лигандом. С этой точки зрения использование спейсеров с полярными группами позволит повысить гидрофилизацию поверхности, что приведет к увеличению факторов удерживания полярных аналитов и увеличению селективности. Также способ получения такого сорбента длительный, трудоемкий и многостадийный, занимает от 3 до 4 суток, влекущий потери на каждой стадии синтеза и образование в реакционной среде побочных продуктов реакции Пассерини, которая протекает параллельно путем взаимодействия трех реагентов без участия четвертого -аминосоединения.
Чтобы соответствовать всем требованиям, предъявляемым к современным сорбентам для гидрофильной хроматографии, и быть пригодными для решения широкого круга все более сложных современных аналитических задач, требующих одновременного высокочувствительного определения все большего числа полярных соединений в различных объектах, сорбенты должны обладать все более совершенными эксплуатационными и хроматографическими характеристиками, а также быть селективными к нескольким классам соединений.
Раскрытие изобретения
Задачей предлагаемой группы изобретений является получение сорбента для определения полярных веществ, обладающего улучшенными эксплуатационными и хроматографическими характеристиками, а также разработка способа его получения.
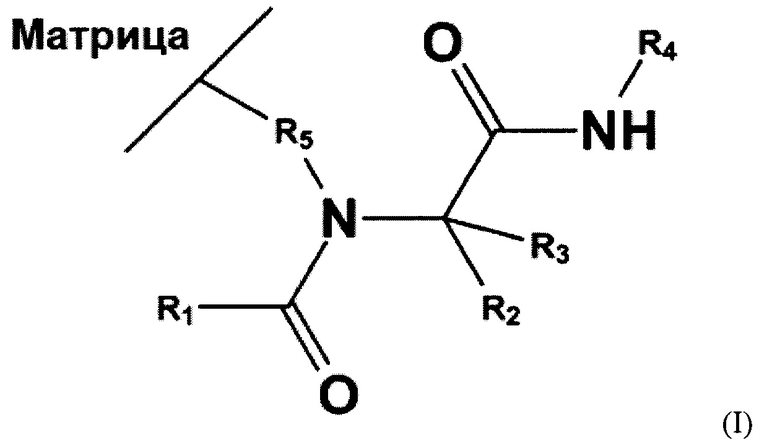
Техническим результатом предлагаемой группы изобретений является создание высокоселективного гидрофильного сорбента, обладающего высокими стабильностью, селективностью и эффективностью, способ получения которого дает возможность варьирования селективности в широких пределах, является простым, быстрым и хорошо воспроизводимым, позволяя достигнуть селективное разделение смесей полярных веществ различных классов с эффективностью порядка 40000-60000 тт/м, а также сохранять стабильность в течение длительного времени - не менее 4 месяцев. Предлагаемое изобретение позволяет существенно сократить трудоемкость процесса, время синтеза и число промежуточных стадий очистки, поскольку подразумевает однореакторный синтез путем простого последовательного добавления реагентов к аминированной матрице. При таком подходе, когда матрица выступает в качестве аминокомпонента, побочные продукты реакции Пассерини способны образовываться только в растворе и не закрепляются на частицах аминированной матрицы, поскольку реакция Пассерини протекает без участия амина, и возможные побочные продукты легко удаляются промыванием сорбента. Максимально возможный выход четырехкомпонентной реакции получения модифицированных сорбентов подтвержден увеличенными по сравнению с матрицей и достигшими постоянных значений при дальнейшем увеличении времени реакции факторами удерживания сахаров, уридина и аналитов теста Танака для гидрофильных сорбентов. Поставленная задача решается предлагаемым сорбентом для определения полярных биологически активных соединений - аминокислот, водорастворимых витаминов, сахаров и органических кислот - методом гидрофильной хроматографии, содержащим матрицу с химически привитым по атому азота лигандом, содержащим заместители R1, R2, R3, R4. Данный атом азота может быть прикреплен к матрице с помощью алкильного спейсера R5 (формула I) либо с помощью спейсера, содержащего алкильный фрагмент R5 с закрепленной вторичной, третичной аминогруппой либо четвертичной аммониевой группой, с которой соединены одинаковые или разные спейсеры R6, R7, R8, хотя бы один из которых содержит атом азота, на котором получен лиганд из формулы I (формула II). Сорбент содержит матрицу, выбранную из ряда: полимер на основе дивинилбензола, выступающего в качестве сшивающего агента для данного полимера, полиметакрилат, диоксид кремния, диоксид титана, диоксид циркония или оксид алюминия, аминированную первичным амином. При этом общая формула сорбента соответствует формуле I:
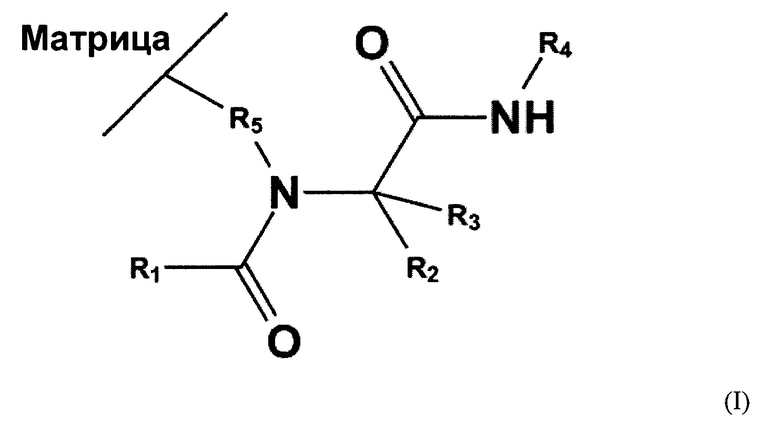
или формуле II:
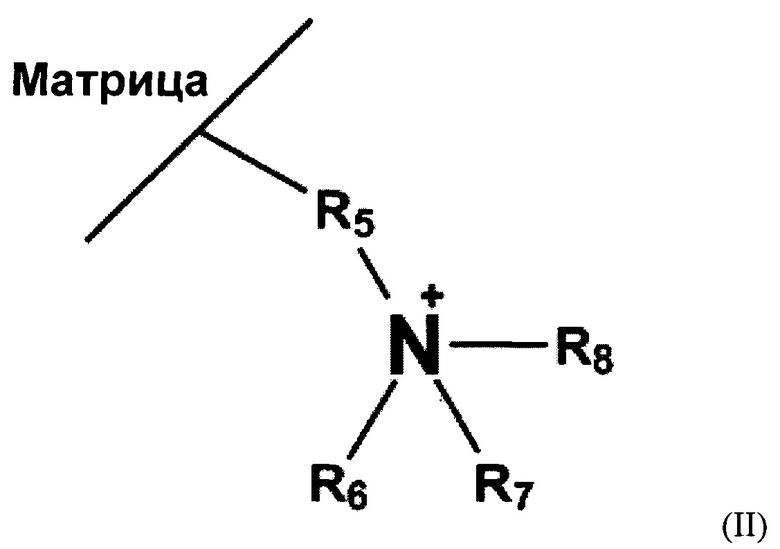
где R1-R4 представляют собой Н или алкильный фрагмент С1-С8, который может содержать заместители одинаковые или разные, в том числе гидроксильные, карбонильные, карбоксильные, эфирные и аминогруппы;
R5 представляет собой алкильный фрагмент С1-С14, который может содержать различные заместители, в том числе гидроксильные, карбонильные, карбоксильные, эфирные и аминогруппы;
R6-R8 одинаковые или разные, представляют собой Н или алкильный фрагмент С1-С14, который может содержать различные заместители одинаковые или разные, в том числе гидроксильные, карбонильные, карбоксильные, эфирные и аминогруппы; как минимум один из них связан с атомом азота, на котором закреплены заместители R1-R4 таким же способом и расположением, как в формуле 1. Возможно также отсутствие одного либо двух заместителей из R6-R8, в таком случае атом азота, с которым они соединены, не несет положительного заряда.
В качестве полимера на основе дивинилбензола, выступающего в качестве сшивающего агента, наиболее оптимальные результаты дает использование сополимера стирола и дивинилбензола или сополимера этилвинилбензола и дивинилбензола.
При этом лучшие результаты получают, когда размер частиц полимера составляет 3-10 мкм, а степень сшивки не менее 25%.
При использовании в качестве матрицы полиметакрилата наиболее оптимальные результаты получают при размере частиц матрицы, составляющем 3-10 мкм.
А при использовании в качестве матрицы оксидов, выбранных из ряда диоксид кремния, диоксид титана, оксид алюминия или диоксид циркония оптимальные результаты получают при размере частиц матрицы, составляющем 1-10 мкм.
В настоящей заявке под спейсером подразумевается любой радикал, который может соединять между собой указанные фрагменты структуры - матрицу и химически привитую к ней первичную аминогруппу, вторичную или третичную аминогруппу ди- или триамина или четвертичную аммониевую группу, химически привитую к матрице.
При этом спейсеры, соединяющие четвертичную аммониевую функциональную группу, привитую к матрице, со вторичными или третичными аминогруппами, входящими в состав по крайней мере одного ди- или триамина, в предлагаемом сорбенте выбраны из ряда наиболее распространенных спейсеров: алкильный, алканольный спейсер или спейсер, содержащий эфирные группы (Zatirakha A.V., Smolenkov A.D., Shpigun О.А. Preparation and chromatographic performance of polymer-based anion exchangers for ion chromatography: a review. //Anal. Chim. Acta. 2016. V.904. P.33-50).
В качестве алкильных спейсеров могут быть использованы дигалогеналканы, выбранные из ряда, включающего 1,2-дибромэтан, 1,3-дибромпропан, 1,4-дибромбутан, 1,5-дибромпентан.
В качестве алканольных спейсеров могут быть использованы 1,3-дибромпропанол-2, 1,5-дибромпентанол-3, 1,4-дибромбутанол-2 и другие дигалогеналканы, содержащие гидроксидные группы.
В качестве спейсеров, содержащих эфирные группы, могут быть использованы диглицидиловые эфиры, выбранные из ряда, включающего 1,4-бутандиолдиглицидиловый эфир, резорциндиглицидиловый эфир, 1,2-этандиолдиглицииловый эфир, этиленгликольдиглицидиловый эфир.
В качестве ди- и триаминов могут быть использованы амины, выбранные из ряда, включающего этилендиамин, диэтилентриамин, бис(гексаметилен)триамин, N,N***'-бис(2-гидроксиэтил)этилендиамин.
В качестве кислотного компонента-заместителя R1 могут быть использованы, например, кислотные остатки уксусной, пропионовой, молочной, гликолевой кислот.
В качестве карбонильного компонента-заместителя R2, R3 могут быть использованы радикалы, соседствующие с карбонильной группой альдегидов и кетонов, выбранных из ряда, включающего ацетальдегид, формальдегид, пропионовый альдегид, метилэтилкетон.
В качестве изоцианидного компонента-заместителя R4 могут быть использованы заместители у изонитрильной группы изоцианидов, выбранных из ряда, включающего трет-бутил изоцианид, циклогексил изоцианид, метил изоцианоацетат, этил изоцианоацетат.
Селективность такого сорбента по органическим кислотам в режиме гидрофильной хроматографии обеспечивается наличием кислотного фрагмента в структуре, которая находится на поверхности функционального слоя, а также отсутствием отрицательно заряженных фрагментов в структуре лиганда. В то же время амидные группы по внешней части функционального слоя обеспечивают возможность работы в режиме гидрофильной хроматографии и селективность к различным классам биологически активных соединений, при этом данные группы не подвергаются элиминированию, что обеспечивает стабильность сорбента. Кроме того, благодаря отсутствию на поверхности объемного конформационно-подвижного полимера, хроматографическая колонка с сорбентом быстро (за 30 минут) приходит в равновесие (то есть фоновый сигнал элюента выходит на плато со значением не более 100 ед. опт.пл.*10-3) перед началом анализа как в водных, так и в органических средах.
Еще одним аспектом изобретения является способ получения сорбента, включающий следующую последовательность операций:
- в качестве исходного соединения берут аминированную матрицу, выбранную из ряда аминированных: полимера на основе дивинилбензола, в котором дивинилбензол является сшивающим агентом, полиметакрилата, диоксида кремния, диоксида титана, диоксид циркония или оксида алюминия.
- модифицируют данные соединения путем последовательного добавления карбонильного соединения, изоцианида и органической кислоты до получения лиганда, химически привитого к атому азота.
Дополнительно к исходному соединению химически можно привить спейсер, содержащий аминогруппу. Для введения спейсеров полученные на поверхности аминогруппы алкилируют бифункциональным соединением, например, диглицидиловым эфиром, дигалогеналканом или дигалогенпроизводным спиртов до образования вторичных или третичных аминогрупп либо четвертичных аммониевых групп. Затем моно-, ди- или три-амины закрепляют на привитых спейсерах с помощью реакции аминирования, протекающей обычно при 50-70°С (Shchukina O.I., Zatirakha A.V., Smolenkov A.D., Nesterenko P.N., Shpigun O.A. Anion exchangers with branched functional anion exchange layers of different hydrophilicity for ion chromatography. // J. Chromatogr. A. 2015. V.1408. P. 78-86), и полученную аминированную матрицу модифицируют по реакции Уги, добавляя карбонильное соединение, изоцианид и кислоту в строгой последовательности и выдерживая реакционную смесь при комнатной температуре и перемешивании в течение 0,5-24 ч.
В качестве карбонильного соединения могут быть использованы альдегиды или кетоны, выбранные из ряда, включающего ацетальдегид, формальдегид, пропионовый альдегид, метилэтилкетон.
В качестве изоцианида могут быть использованы изоцианиды, выбранные из ряда, включающего трет-бутилизоцианид, циклогексил изоцианид, метил изоцианоацетат, этил изоцианоацетат.
В качестве органической кислоты могут быть использованы кислоты, выбранные из ряда, включающего ледяную уксусную кислоту, пропионовую, молочную, гликолевую кислоту.
Оптимальным, но не единственно возможным является соотношение компонентов, взятых из расчета, что на 1,0 мольный эквивалент аминированной матрицы (по количеству азота аминогрупп) берут по меньшей мере 1,0 эквивалента каждого из реагентов, а именно: карбонильного соединения, изоцианида, кислоты.
Верхняя граница содержания используемых реагентов не ограничивается, т.к. избыток какого-либо реагента не уменьшает выходов реакций, однако при большом избытке может понадобиться дополнительная очистка продуктов реакций.
После смешения компонентов реакционную смесь перемешивают при комнатной температуре с помощью механической мешалки до получения постоянного значения фактора удерживания уридина, превышающего таковое значение для аминированной матрицы не менее чем на 10% при контроле характеристик сорбента в условиях гидрофильной хроматографии согласно (Kawachi Y., Ikegami Т., Takubo Н., Ikegami Y., Miyamoto M., Tanaka N. Chromatographic characterization of hydrophilic interaction liquid chromatography stationary phases: Hydrophilicity, charge effects, structural selectivity, and separation efficiency // J. Chromatogr. A. 2011. V. 1218. P. 5903-5919). Предпочтительно перемешивание проводить со скоростью 500±200 об/мин в течение 0.5-24 часов, затем полученную смесь отфильтровывают на стеклянном пористом фильтре (размер пор 16-40) и полученную твердую фазу промывают этанолом и ацетонитрилом для удаления оставшихся реагентов и возможных побочных продуктов.
Такой способ синтеза неподвижной фазы является уникальным в своем роде, поскольку в реакции непосредственно участвует аминированная матрица, и образующийся лиганд сразу же будет закрепляться на ней. Более того, при использовании аминопропилсиликагеля в качестве аминокомпонента в этой реакции можно избежать образования побочных продуктов конкурирующей реакции непосредственно на матрице, поскольку конкурирующая реакция Пассерини протекает без участия аминированного реагента в водно-органической фазе. Получающиеся таким образом побочные продукты не закрепляются на матрице, а остаются в растворе и легко удаляются на стадии промывки сорбента, тем самым обеспечивается селективное модифицирование матрицы выбранным лигандом. Это перспективный подход для синтеза сорбентов, поскольку обеспечивается возможность простого, быстрого и хорошо воспроизводимого модифицирования, позволяющего проводить одновременное включение нескольких типов функциональных групп и их варьирование.
Краткое описание чертежей
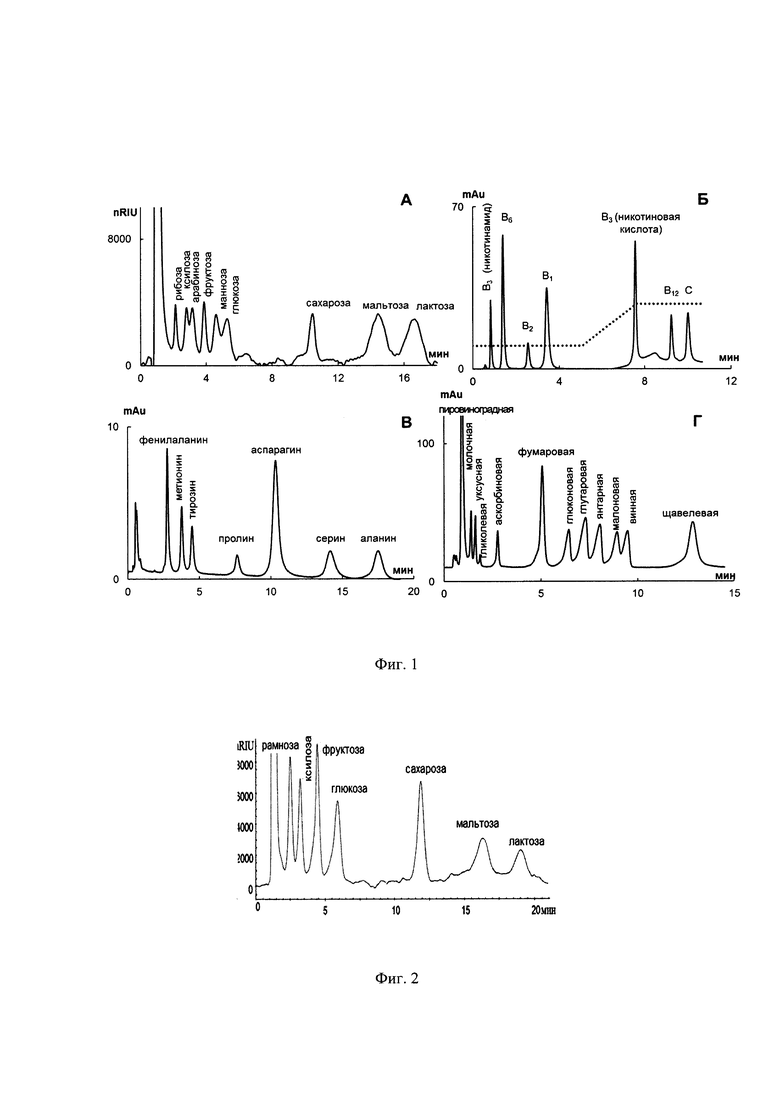
На Фиг. 1 представлены хроматограммы разделения модельных смесей аминокислот, органических кислот, сахаров и водорастворимых витаминов на полученном сорбенте. Высота пиков измерялась в миллиединицах оптической плотности.
На Фиг. 2 представлена хроматограмма разделения модельной смеси сахаров на сорбенте-прототипе. Высота пиков измерялась в наноединицах индексов рефракции.
Осуществление изобретения
Все используемые реагенты являются коммерчески доступными, все процедуры, если не оговорено особо, осуществляли при комнатной температуре или температуре окружающей среды, то есть в диапазоне от 18 до 25°С; контроль за ходом реакции осуществляли при помощи гидрофильной хроматографии, упаковывая продукт в стальную колонку и получая факторы удерживания уридина до достижения их постоянных величин в условиях, указанных в (Kawachi Y., Ikegami Т., Takubo Н., Ikegami Y., Miyamoto M., Tanaka N. Chromatographic characterization of hydrophilic interaction liquid chromatography stationary phases: Hydrophilicity, charge effects, structural selectivity, and separation efficiency // J. Chromatogr. A. 2011. V. 1218. P. 5903- 5919), и время реакции указано только для иллюстрации.
Общим для всех подходов является необходимость использования аминированной матрицы с привитыми первичными аминогруппами. Для синтеза можно использовать коммерчески доступный аминированный силикагель, а также обычный немодифицированный силикагель с диаметром частиц 1-10 мкм, на поверхности которого необходимо закрепить аминогруппы. Одним из возможных подходов для получения аминированного силикагеля является модифицирование силикагелевой матрицы аминопропилтриметоксисиланом, что приводит к образованию первичных аминогрупп на поверхности матрицы (Fuying Dong, Depeng Ma, Shengyu Feng. Aminopropyl-modified silica as cross-linkers of polysiloxane containing y-chloropropyl groups for preparing heat-curable silicone rubber. // Polymer Testing. 2016. V.52. P. 124-132)
Для модифицирования силикагелевых матриц могут быть также использованы другие силаны как минимум с одним аминоалкильным заместителем. Альтернативным вариантом получения аминированного силикагеля может являться его обработка глицидилоксипропилтриметоксисиланом или другим силилирующим реагентом, содержащим эпоксидную группу в структуре, с получением эпоксидированного силикагеля, который затем обрабатывают раствором аммиака или другим амином для раскрытия эпоксидных колец и прививки аминогрупп (Nesterenko P.N., Haddad P.R. Zwitterionic ion-exchangers in liquid chromatography. // Anal. Sci. 2000. V. 16. P. 565-574.).
Для введения спейсеров далее полученные на поверхности аминогруппы алкилируют бифункциональным соединением, например, диглицидиловым эфиром, дигалогеналканом или дигалогенпроизводным спиртов до образования вторичных или третичных аминогрупп либо четвертичных аммониевых групп. Затем моно-, ди- или три-амины закрепляют на привитых спейсерах с помощью реакции аминирования, протекающей обычно при 50-70°С (Shchukina O.I., Zatirakha A.V., Smolenkov A.D., Nesterenko P.N., Shpigun O.A. Anion exchangers with branched functional anion exchange layers of different hydrophilicity for ion chromatography. // J. Chromatogr. A. 2015. V.1408. P. 78-86), и полученную аминированную матрицу модифицируют по реакции Уги, добавляя карбонильное соединение, изоцианид и кислоту в строгой последовательности и выдерживая реакционную смесь при комнатной температуре и перемешивании в течение 0,5-24 ч.
Приведенные ниже примеры подтверждают, но не ограничивают заявляемые объекты изобретения.
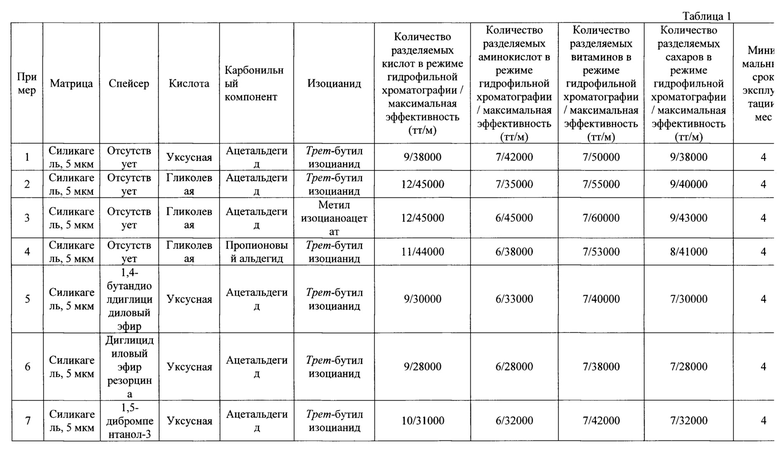
В таблице 1 приведены хроматографические характеристики полученных по примерам 1-7 гидрофильных сорбентов.
Пример 1. Получение сорбента на основе силикагеля с диаметром частиц 5 мкм с химически привитым лигандом, полученным с использованием уксусной кислоты, ацетальдегида, трет-бутил изоцианида.
1) выбор матрицы
В качестве исходной матрицы брали аминированный силикагель Диасфер-Амин («БиоХиммак СТ», Россия) с диаметром частиц 5 мкм.
2) закрепление лиганда к атому азота
1) В качестве исходной матрицы берут аминированный диоксид кремния с диаметром частиц 5 мкм.
2) химическая прививка спейсера: отсутствует.
3) модификация полученного соединения путем конструирования лиганда с амидными группами:
К 1,2 г аминопропилсиликагеля добавляли 73 мкл ацетальдегида, 125 мкл трет-бутилизоцианида и 74 мкл ледяной уксусной кислоты. Реакционную смесь перемешивали в течение 0,5 часов при комнатной температуре с помощью механической мешалки «Eurostar» («IKA-Werke», Германия) со скоростью 500 об/мин, затем отфильтровывали на стеклянном фильтре пористостью 16-40 и промывали 100 мл этанола и 80 мл ацетонитрила. Максимально возможный выход реакции модифицирования матрицы подтверждался достижением большего по сравнению с исходной матрицей не менее чем на 10% и постоянного значения фактора удерживания уридина при контроле характеристик сорбента в условиях гидрофильной хроматографии.
Время, затраченное на синтез, составило 0,5 часа.
Стабильность полученного сорбента демонстрируется сохранением времен удерживания и эффективности по полярным аналитам в течение 4 месяцев эксплуатации в интервале рН 3,5-7. Полученный в результате сорбент соответствует формуле (I-а):
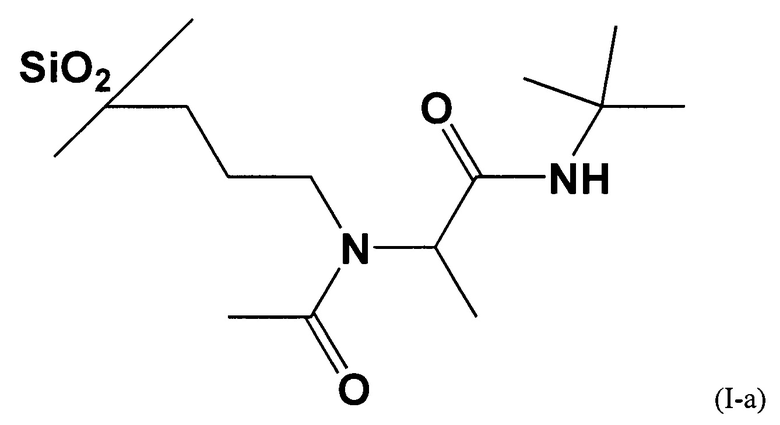
Пример 2. Получение сорбента на основе силикагеля с диаметром частиц 5 мкм с химически привитым лигандом, полученным с использованием гликолевой кислоты, ацетальдегида, трет-бутил изоцианида.
Получение сорбента проводили как в примере 1, но на стадии 3 вместо уксусной кислоты брали гликолевую кислоту в эквимолярном количестве. Время, затраченное на синтез, составило 24 часа.
Полученный в результате сорбент соответствует формуле (I-б):
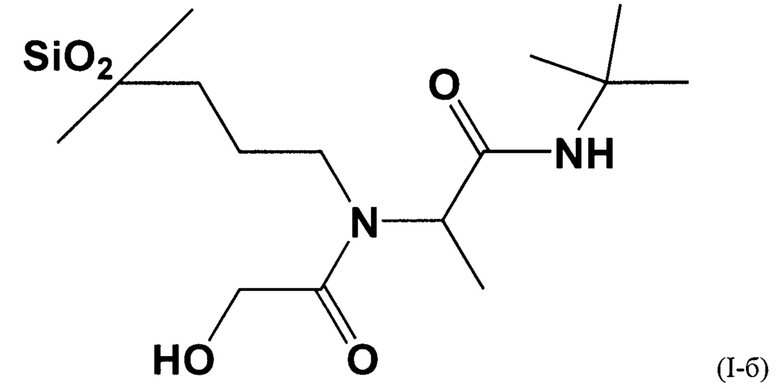
Пример 3. Получение сорбента на основе силикагеля с диаметром частиц 5 мкм с химически привитым лигандом, полученным с использованием гликолевой кислоты, ацетальдегида, метил изоцианоацетата.
Получение сорбента проводили как в примере 1, но на стадии 3 вместо трет-бутилизоцианида брали метил изоцианоацетат в эквимолярном количестве. Время, затраченное на синтез, составило 24 часа.
Полученный в результате сорбент соответствует формуле (I-в):
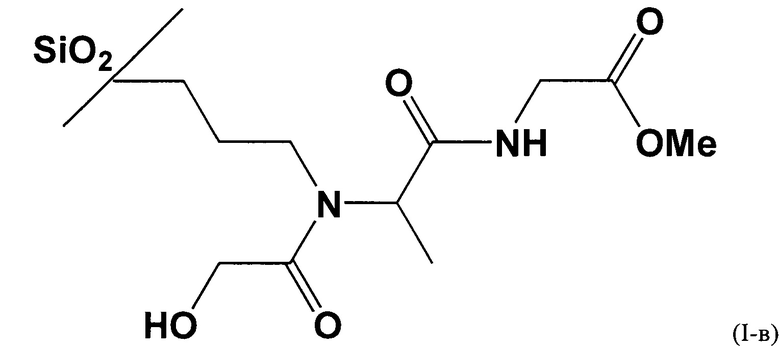
Пример 4. Получение сорбента на основе силикагеля с диаметром частиц 5 мкм с химически привитым лигандом, полученным с использованием гликолевой кислоты, пропионового альдегида, трет-бутил изоцианида.
Получение сорбента проводили как в примере 1, но на стадии 3 вместо ацетальдегида брали пропионовый альдегид в эквивалентном количестве. Время, затраченное на синтез, составило 24 часа.
Полученный в результате сорбент соответствует формуле (I-г)
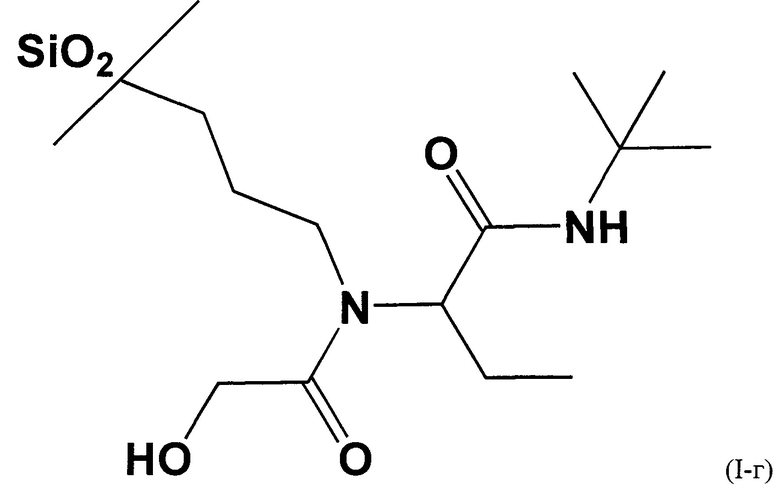
Пример 5. Получение сорбента на основе силикагеля с диаметром частиц 5 мкм с химически привитым через спейсер лигандом, полученным с использованием уксусной кислоты, ацетальдегида, трет-бутил изоцианида.
1) выбор матрицы
В качестве исходной матрицы брали аминированный силикагель Диасфер-Амин («БиоХиммак СТ», Россия) с диаметром частиц 5 мкм.
2) закрепление лиганда к атому азота
1) В качестве исходной матрицы берут аминированный диоксид кремния с диаметром частиц 5 мкм.
2) химическая прививка спейсера:
В колбу на 100 мл помещали 1 г матрицы, добавили 20 мл воды и 1 мл 1,4-бутандиолдиглицидилового эфира. Реакционную смесь перемешивали в течение 1,5 ч с помощью механической мешалки со скоростью 500 об/мин при температуре 60°С, затем отфильтровали на стеклянном фильтре и промыли 100 мл деионизованной воды. Затем суспензировали продукт на ультразвуковой ванне мощностью 100 Вт в течение 1 мин в 20 мл воды и добавили 2 мл этилендиамина. Реакционную смесь перемешивали в течение 1 ч с помощью механической мешалки со скоростью 500 об/мин при температуре 60°С, затем отфильтровали на стеклянном фильтре и промыли 100 мл деионизованной воды.
3) модификация полученного соединения путем конструирования лиганда с амидными группами:
Модифицирование сорбента проводили как на стадии 3 в примере 1.
Полученный в результате сорбент соответствует формуле (IIa).
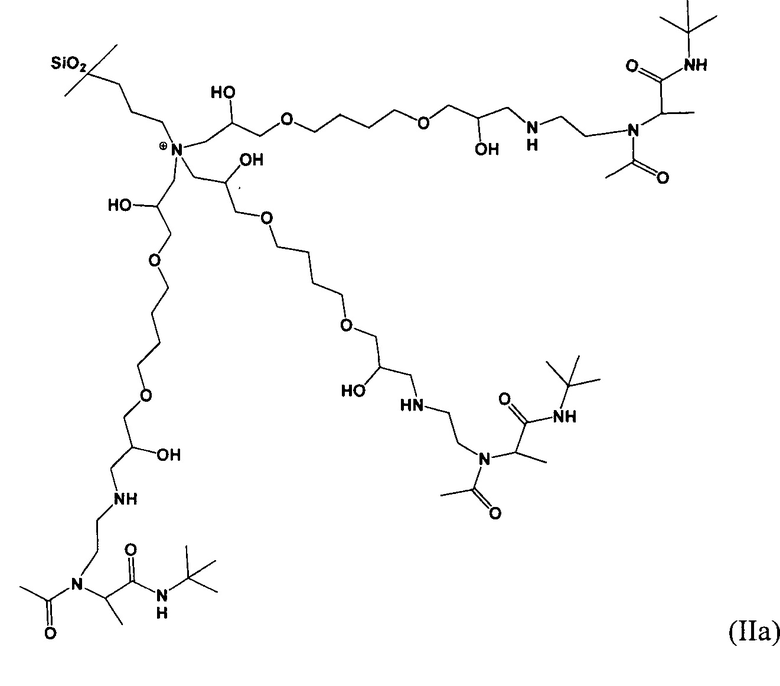
Время, затраченное на синтез, составило 4 часа.
Пример 6. Получение сорбента на основе силикагеля с диаметром частиц 5 мкм с химически привитым через спейсер лигандом, полученным с использованием уксусной кислоты, ацетальдегида, трет-бутил изоцианида.
Получение сорбента проводили как в примере 5, но на стадии 2 вместо 1,4-бутандиолдиглицидилового эфира брали диглицидиловый эфир резорцина в эквивалентном количестве.
Полученный в результате сорбент соответствует формуле (IIб)
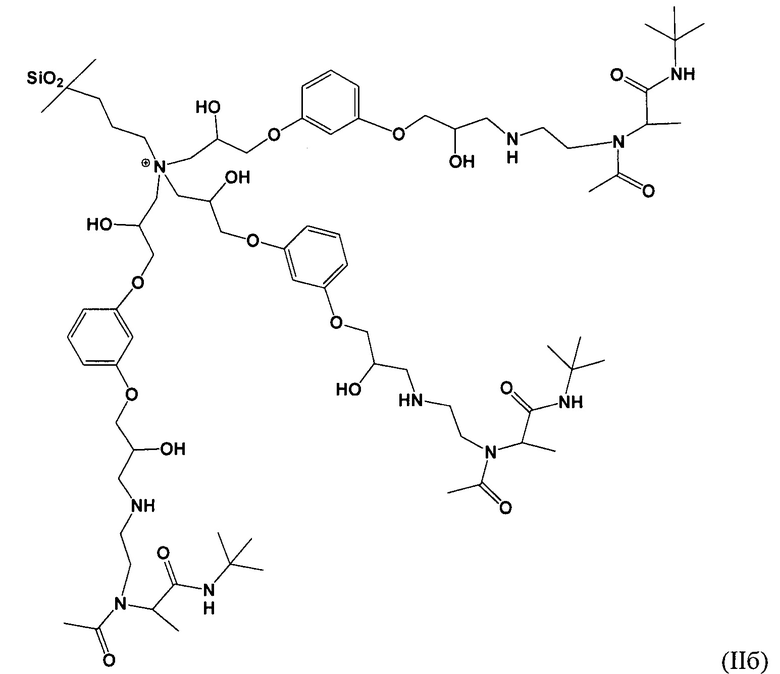
Время, затраченное на синтез, составило 4 часа.
Пример 7. Получение сорбента на основе сополимера стирола и дивинилбензола с диаметром частиц 3 мкм с химически привитым через спейсер лигандом, полученным с использованием уксусной кислоты, ацетальдегида, трет-бутил изоцианида.
1) выбор матрицы
В качестве исходной матрицы берут аминированный сополимер стирола и дивинилбензола (ПС-ДВБ) со степенью сшивки 50% и диаметром частиц 3 мкм.
2) закрепление лиганда к атому азота
Получение сорбента проводили как в примере 5, но на стадии 2 вместо 1,4-бутандиолдиглицидилового эфира брали 1,5-дибромпентанол-3 в эквивалентном количестве.
Полученный в результате сорбент соответствует формуле (IIв)
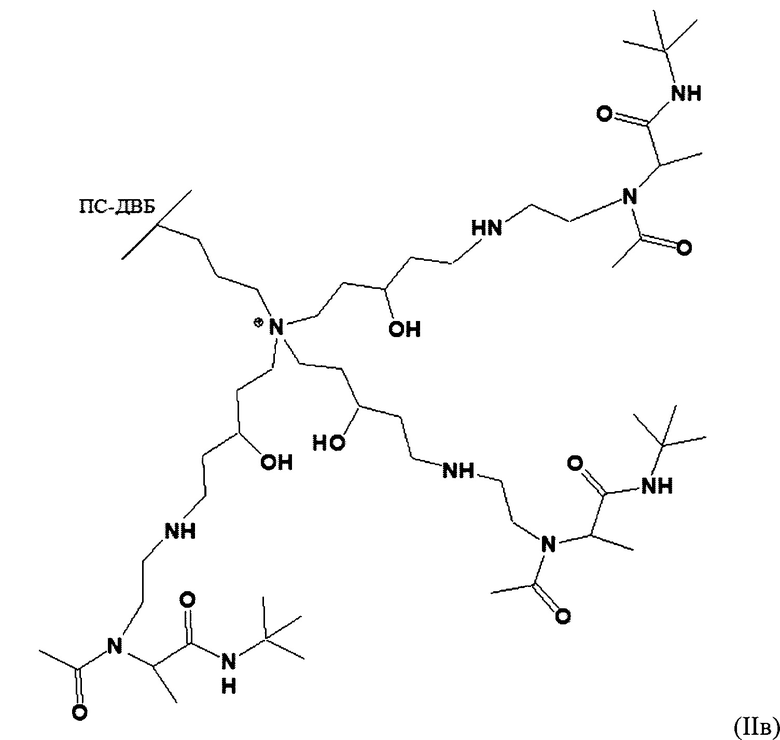
Время, затраченное на синтез, составило 4 часа.
Пример 8. Разделение органических кислот с помощью сорбента в режиме гидрофильной хроматографии.
В качестве модельной смеси была взята смесь 12 кислот, содержащая пировиноградную, молочную, уксусную, гликолевую, аскорбиновую, фумаровую, глюконовую, глутаровую, янтарную, малоновую, винную, щавелевую в концентрации по 50 мг/л каждого компонента. Смесь готовили путем добавления по 1 мл концентрированного раствора каждого компонента с содержанием 5000 мг/л в мерную колбу на 100 мл и последующего доведения до метки деионизованной водой. Разделение смеси проводили с помощью сорбента, полученного в примере 2. Сорбент упаковали в хроматографические колонки размером 100×3 мм под давлением 400 бар и проводили разделение смеси анионов в варианте ионной хроматографии со спектрофотометрическим детектированием при длине волны 220 нм. Для получения хроматограммы использовали жидкостной хроматограф Dionex Ultimate 3000 ("Thermo Fisher Scientific", США). В качестве подвижной фазы использовали фосфатный буферный раствор с рН 7,5 и концентрацией 10 мМ при скорости потока 1 мл/мин. Высота пиков измерялась в миллиединицах оптической плотности. Время уравновешивания колонки составило 30 минут. Данный сорбент позволил разделить 12 указанных кислот примерно за 12 минут с хорошим разрешением и симметрией пиков. Полученная хроматограмма, содержащая 12 пиков, приведенная на Фиг. 1(Г), подтверждает селективное разделение присутствующих в модельной смеси 12 кислот в режиме гидрофильной хроматографии. При этом стоит отметить отсутствие размывания и малую ширину пиков, что свидетельствует о высокой эффективности заявляемого сорбента (25000-45000 тт/м для разных кислот из представленного ряда).
Пример 9. Разделение аминокислот с помощью сорбента в режиме гидрофильной хроматографии.
В качестве модельной смеси была взята смесь 7 аминокислот, содержащая фенилаланин, метионин, тирозин, оксипролин, аспарагин, аланин, серии в концентрации по 20 мг/л каждого компонента. Смесь готовили путем добавления по 0,5 мл концентрированного раствора каждого компонента с содержанием 2000 мг/л в мерную колбу на 50 мл и последующего доведения до метки деионизованной водой. Разделение смеси проводили с помощью мультифункционального сорбента, полученного в примере 1. Сорбент упаковали в хроматографические колонки размером 100×3 мм под давлением 400 бар и проводили разделение смеси аминокислот в варианте гидрофильной хроматографии со спектрофотометрическим детектированием при длине волны 210 нм. Для получения хроматограммы использовали жидкостной хроматограф Dionex Ultimate 3000 ("Thermo Fisher Scientific", США). В качестве подвижной фазы использовали раствор состава 80% CH3CN: 20% фосфатный буферный раствор, рН 6.5 (10 мМ в п.ф.) при скорости потока 1 мл/мин. Высота пиков измерялась в миллиединицах оптической плотности. Время уравновешивания колонки составило 30 минут. Данный сорбент позволил разделить 7 указанных аминокислот менее чем за 20 минут с хорошим разрешением и симметрией пиков. Полученная хроматограмма, содержащая 7 пиков, приведенная на Фиг. 1(B), подтверждает селективное разделение присутствующих в модельной смеси аминокислот в режиме гидрофильной хроматографии. При этом стоит отметить отсутствие размывания и малую ширину пиков, что свидетельствует о высокой эффективности заявляемого сорбента (25000-45000 тт/м для разных аминокислот из представленного ряда) в режиме гидрофильной хроматографии.
Пример 10. Разделение водорастворимых витаминов с помощью сорбента в режиме гидрофильной хроматографии.
Все как в примере 9, только вместо смеси аминокислот в качестве модельной смеси брали смесь водорастворимых витаминов, содержащую никотиновую кислоту (В3), никотинамид (В3), аскорбиновую кислоту (С), В6, В12, B1, В2 в концентрации по 10 мг/л каждого компонента. Смесь готовили путем добавления по 1 мл концентрированного раствора каждого компонента с содержанием 1000 мг/л в мерную колбу на 100 мл и последующего доведения до метки деионизованной водой. В качестве подвижной фазы используют раствор состава 100 мМ CH3COONH4, рН 5,8 / ацетонитрил (градиентное элюирование); детектирование проводят при длине волны 270 нм. Время уравновешивания колонки составило 30 минут. Данный сорбент позволил разделить 7 указанных витаминов менее чем за 12 минут с хорошим разрешением и симметрией пиков. Полученная хроматограмма, содержащая 7 пиков, приведенная на Фиг. 1(Б), подтверждает селективное разделение присутствующих в модельной смеси водорастворимых витаминов в режиме гидрофильной хроматографии. При этом стоит отметить отсутствие размывания и малую ширину пиков, что свидетельствует о высокой эффективности заявляемого сорбента (30000-50000 тт/м для разных водорастворимых витаминов из представленного ряда) в режиме гидрофильной хроматографии.
Пример 11. Разделение сахаров с помощью сорбента в режиме гидрофильной хроматографии.
Все как в примере 9, только вместо смеси аминокислот в качестве модельной смеси брали смесь сахаров, содержащую мальтозу, глюкозу, маннозу, сахарозу, лактозу, рамнозу, ксилозу, арабинозу, фруктозу в концентрации по 50 мг/л каждого компонента. Смесь готовят путем путем добавления по 1 мл концентрированного раствора каждого компонента с содержанием 5000 мг/л в мерную колбу на 100 мл и последующего доведения до метки деионизованной водой. В качестве подвижной фазы использовали раствор состава вода: ацетонитрил (15%: 85%) при скорости потока 1,0 мл/мин; используют рефрактометрическое детектирование. Время уравновешивания колонки составило 30 минут. Данный сорбент позволил разделить 9 указанных сахаров примерно за 20 минут с хорошим разрешением и симметрией пиков. Полученная хроматограмма, содержащая 9 пиков, приведенная на Фиг. 1(A), подтверждает селективное разделение присутствующих в модельной смеси сахаров в режиме гидрофильной хроматографии. При этом стоит отметить отсутствие размывания и довольно малую ширину пиков, что свидетельствует о высокой эффективности заявляемого сорбента (25000-35000 тт/м для разных сахаров из представленного ряда) в режиме гидрофильной хроматографии.
Аналогичные результаты были получены при испытании всех заявляемых гидрофильных сорбентов.
Хроматографические характеристики полученных в примерах 1-7 сорбентов представлены в таблице 1.
Как видно из приведенных примеров и таблицы 1, полученные сорбенты обладают высокой эффективностью (30000-60000 тт/м в варианте гидрофильной хроматографии), селективностью (позволяют проводить одновременное определение не менее 9 кислот не менее 6 аминокислот, 7 сахаров и 7 водорастворимых витаминов) в режиме гидрофильной хроматографии, - и стабильностью (минимальный срок эксплуатации без изменения времен удерживания аналитов составляет 4 месяца). Кроме того, предложенные способы получения дают возможность варьирования селективности сорбентов путем варьирования структуры спейсеров и заместителей в лиганде.
Подходы к синтезу предложенных сорбентов просты в исполнении и не требует использования высокотоксичных и канцерогенных реагентов.
Обеспечиваемые преимущества в селективности продемонстрированы на Фиг. 1, 2: изобретение позволяет разделить смесь 9 сахаров по сравнению с 7 у вышеуказанного прототипа. О более высокой гидрофильности предлагаемого типа сорбентов свидетельствуют большие значения фактора удерживания уридина в условиях анализа, приведенных в (Kawachi Y., Ikegami Т., Takubo Н., Ikegami Y., Miyamoto M., Tanaka N. Chromatographic characterization of hydrophilic interaction liquid chromatography stationary phases: Hydrophilicity, charge effects, structural selectivity, and separation efficiency // J. Chromatogr. A. 2011.V. 1218. P. 5903-5919), составляющие не менее 1,5 по сравнению с 1,1 у вышеупомянутого прототипа.
Таким образом, предлагаемое изобретение подтверждают достижение заявленных показателей, а именно: повышенная стабильность сорбентов обеспечивает срок службы не менее 4 месяцев, эффективность повышается до 60000 тт/м и дает хорошее разрешение пиков, а повышенная селективность к различным классам соединений позволяет работать в режиме гидрофильной хроматографии и подтверждает разделяющую способность сорбента в части разделения 9 кислот, 7 сахаров, 6 аминокислот и 7 водорастворимых витаминов за один анализ, не являющуюся предельной. Сорбент позволяет за один акт хроматографирования получить данные о содержании соединений одного класса в составе многокомпонентной смеси.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОРБЕНТ ДЛЯ ОПРЕДЕЛЕНИЯ СОЕДИНЕНИЙ ИОННОЙ И ГИДРОФИЛЬНОЙ ПРИРОДЫ | 2016 |
|
RU2638660C1 |
| АНИОНООБМЕННЫЙ СОРБЕНТ ДЛЯ ОПРЕДЕЛЕНИЯ ОРГАНИЧЕСКИХ И НЕОРГАНИЧЕСКИХ АНИОНОВ МЕТОДОМ ИОННОЙ ХРОМАТОГРАФИИ | 2016 |
|
RU2627384C1 |
| АНИОНООБМЕННЫЙ СОРБЕНТ ДЛЯ ИОНОХРОМАТОГРАФИЧЕСКОГО ОПРЕДЕЛЕНИЯ ОРГАНИЧЕСКИХ И НЕОРГАНИЧЕСКИХ АНИОНОВ И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2014 |
|
RU2562650C1 |
| АНИОНООБМЕННЫЙ СОРБЕНТ ДЛЯ ИОНОХРОМАТОГРАФИЧЕСКОГО ОПРЕДЕЛЕНИЯ ОРГАНИЧЕСКИХ И НЕОРГАНИЧЕСКИХ АНИОНОВ И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2014 |
|
RU2575454C2 |
| АНИОНООБМЕННЫЙ СОРБЕНТ ДЛЯ ХРОМАТОГРАФИЧЕСКОГО ОПРЕДЕЛЕНИЯ НЕОРГАНИЧЕСКИХ ИОНОВ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2019 |
|
RU2715197C1 |
| СПОСОБ ПОЛУЧЕНИЯ ХИРАЛЬНОЙ ПЛАНАРНОЙ ПЛАСТИНЫ ДЛЯ ТОНКОСЛОЙНОЙ ХРОМАТОГРАФИИ ОПТИЧЕСКИХ ИЗОМЕРОВ | 2012 |
|
RU2545315C2 |
| НОВЫЕ АФФИННЫЕ ЛИГАНДЫ И ИХ ПРИМЕНЕНИЕ | 1996 |
|
RU2175261C2 |
| ГИДРОФИЛЬНЫЕ ГЕЛИ, ПОЛУЧЕННЫЕ ИЗ ПРИВИТЫХ ФОТОИНИЦИАТОРОВ | 2011 |
|
RU2575348C2 |
| Способ получения альфа-фетопротеина, иммобилизованного на ПЭТ-микрочастицах | 2018 |
|
RU2731415C2 |
| СОРБЕНТ НА ОСНОВЕ МОДИФИЦИРОВАННОГО СИЛИКАГЕЛЯ | 2017 |
|
RU2661213C1 |
Изобретение относится к сорбенту для определения соединений гидрофильной природы и способу его получения. Сорбент содержит матрицу с химически привитым по атому азота лигандом, содержащим заместители R1, R2, R3, R4, при этом атом азота прикреплен к матрице с помощью алкильного спейсера R5, либо с помощью спейсера, содержащего алкильный фрагмент R5 с закрепленной вторичной, третичной аминогруппой либо четвертичной аммониевой группой, с которой могут быть дополнительно соединены одинаковые или разные спейсеры R6, R7, R8, хотя бы один из которых содержит атом азота, на котором получен лиганд. При этом R1-R4 представляют собой Н или алкильный фрагмент С1-С8, который может содержать заместители одинаковые или разные, в том числе гидроксильные, карбонильные, карбоксильные, эфирные и аминогруппы, R5 представляет собой алкильный фрагмент С1-С14, который может содержать различные заместители, в том числе гидроксильные, карбонильные, карбоксильные, эфирные и аминогруппы, R6-R8 одинаковые или разные, представляют собой Н или алкильный фрагмент С1-С14, который может содержать заместители одинаковые или разные, в том числе гидроксильные, карбонильные, карбоксильные, эфирные и аминогруппы, причем как минимум один из них связан с атомом азота, на котором закреплены заместители R1-R4. Способ получения сорбента представляет собой модифицирование аминированной матрицы путем последовательного добавления карбонильного соединения, изоцианида и органической кислоты до получения лиганда, химически привитого к атому азота. Изобретение обеспечивает простой, быстрый и хорошо воспроизводимый способ получения гидрофильного сорбента, обладающего высокими стабильностью, селективностью и эффективностью, а также возможность варьирования селективности в широких пределах. 2 н. и 6 з.п. ф-лы, 1 табл., 11 пр., 5 ил.
1. Сорбент для определения соединений гидрофильной природы, характеризующийся тем, что содержит матрицу с химически привитым по атому азота лигандом, содержащим заместители R1, R2, R3, R4, при этом атом азота может быть прикреплен к матрице с помощью алкильного спейсера R5
формула сорбента (I):
либо с помощью спейсера, содержащего алкильный фрагмент R5 с закрепленной вторичной, третичной аминогруппой либо четвертичной аммониевой группой, с которой соединены одинаковые или разные спейсеры R6, R7, R8, хотя бы один из которых содержит атом азота, на котором получен лиганд формулы I
(формула II):
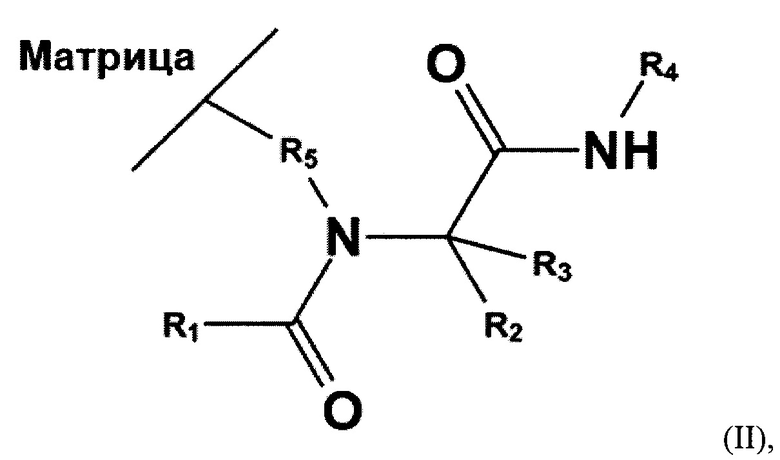
где R1-R4 представляют собой Н или алкильный фрагмент С1-С8, который может содержать заместители одинаковые или разные, в том числе гидроксильные, карбонильные, карбоксильные, эфирные и аминогруппы;
R5 представляет собой алкильный фрагмент С1-С14, который может содержать различные заместители, в том числе гидроксильные, карбонильные, карбоксильные, эфирные и аминогруппы;
R6-R8 одинаковые или разные, представляют собой Н или алкильный фрагмент С1-С14, который может содержать заместители одинаковые или разные, в том числе гидроксильные, карбонильные, карбоксильные, эфирные и аминогруппы; как минимум один из них связан с атомом азота, на котором закреплены заместители R1-R4 таким же способом и расположением, как в формуле I, при этом возможно также отсутствие одного либо двух заместителей из R6-R8.
2. Сорбент по п. 1, характеризующийся тем, что матрицу, выбирают из ряда, включающего полимер на основе дивинилбензола, выступающего в качестве сшивающего агента для данного полимера, полиметакрилат, диоксид кремния, диоксид титана, диоксид циркония или оксид алюминия, аминированную первичным амином.
3. Сорбент по п. 1, характеризующийся тем, что используют матрицу с размером частиц 1-10 мкм.
4. Способ получения сорбента по п. 1, характеризующийся тем, что аминированную матрицу модифицируют путем последовательного добавления карбонильного соединения, изоцианида и органической кислоты до получения лиганда, химически привитого к атому азота.
5. Способ по п. 4, характеризующийся тем, что на 1,0 мольный эквивалент аминированной матрицы берут по меньшей мере 1,0 эквивалента карбонильного соединения, изоцианида, органической кислоты.
6. Способ по п. 4, характеризующийся тем, что в качестве карбонильного соединения используют альдегиды или кетоны, выбранные из ряда, включающего ацетальдегид, формальдегид, пропионовый альдегид, метилэтилкетон.
7. Способ по п. 4, характеризующийся тем, что в качестве изоцианида используют изоцианиды, выбранные из ряда, включающего трет-бутилизоцианид, циклогексил изоцианид, метил изоцианоацетат, этил изоцианоацетат.
8. Способ по п. 4, характеризующийся тем, что в качестве органической кислоты используют кислоты, выбранные из ряда, включающего ледяную уксусную кислоту, пропионовую, молочную, гликолевую кислоту.
| СОРБЕНТ ДЛЯ ОПРЕДЕЛЕНИЯ СОЕДИНЕНИЙ ИОННОЙ И ГИДРОФИЛЬНОЙ ПРИРОДЫ | 2016 |
|
RU2638660C1 |
| ANDREA F G GARGANO, TOMAS LEEK, WOLFGANG LINDNER, MICHAEL LАMMERHOFER, Mixed-mode chromatography with zwitterionic phosphopeptidomimetic selectors from Ugi multicomponent reaction Journal of Chromatography A, volume 1317, p | |||
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
| CLAUDIO DE CASTRO FERREIRA, MARIANA ROBERTO GAMA, GISELE SILVESTRE DA SILVA, | |||
Авторы
Даты
2020-08-21—Публикация
2019-12-17—Подача