Изобретение относится к области медицины, а именно к перинатологии, акушерству и гинекологии, и может быть использовано для прогнозирования хронической гипоксии плода (ХГП) у женщин, забеременевших с помощью экстракорпорального оплодотворения (ЭКО).
Актуальность разработки способа определяется тем, что ХГП ведет к формированию полиорганной патологии, нарушению развития или повреждению ЦНС у ребенка в 60-80% случаев, способствует увеличению частоты соматической и инфекционной патологии, задержке нервно-психического и физического развития в более поздние возрастные периоды [Видеркер Т.В., Ремнева О.В., Фадеева Н.И. Клинические, инструментальные и биохимические маркеры гипоксии плода в прогнозировании поражений центральной нервной системы у новорожденного // Рос. вестник акушера-гинеколога. - 2008. - №6. - С. 4-8]. Известно, что перинатальная гипоксия инициирует процессы, приводящие к повышению проницаемости клеточных мембран, гибели нейронов и глиальных клеток вследствие некроза и/или апоптоза, нарушению функции гематоэнцефалического барьера, попаданию в системный кровоток мозговых антигенов, стимулирующих иммунную систему на выработку аутомозговых антител [Шниткова Е.В. Формирование здоровья, прогноз, диагностика и профилактика его нарушений в онтогенезе у детей и подростков, перенесших перинатальную гипоксию: автореф. дис. …д-ра мед. наук. - Иваново, 1999. - 59 с.]. Доказано, что наиболее чувствительна к кислородной недостаточности нервная ткань плода [Косолапова О.И., Малыгина Е.Н. Кислотно-основное состояние крови новорожденных детей с признаками гипоксии при рождении // Здоровье человека на Севере. - №2. - 2008. - С. 38-40]. При гипоксических повреждениях головного мозга патологический процесс не ограничивается первичным очагом, возникают вторичные изменения с вовлечением ранее не поврежденных нейронов, формируя прогредиентное течение энцефалопатии. Поэтому исход этого заболевания становится очевидным лишь тогда, когда возраст ребенка приближается к году жизни [Роль гипоксически-травматических повреждений головного мозга в формировании инвалидности с детства / Ю.И. Барашнев [и др.] // Российский вестник перинаталогии и педиатрии. - 2006. - №4. - С. 41-46; Изменения адаптации и их коррекция у детей грудного возраста с постгипоксическими изменениями ЦНС / Т.Д. Измайлова [и др.] // Педиатрия. - 2002. - №1. - С. 27-30]. Поэтому необходимо разработать объективные критерии прогнозирования развития ХГП, что позволит предотвратить развитие нарушений здоровья гипоксического генеза у детей, родившихся после ЭКО, и тем самым снизить у них формирование инвалидности и перинатальной смертности.
Известны различные способы прогнозирования и доклинической диагностики развития внутриутробной гипоксии плода.
Известен способ прогнозирования плацентарной недостаточности и внутриутробной гипоксии по определению содержания молекул средней массы (МСМ) в биосубстратах (сыворотка крови и моча) при нормальной и осложненной беременности у женщин и их новорожденных. Считается, что МСМ могут проникать через плацентарный барьер, оказывая непосредственное токсическое воздействие на плод и вызывая патологические нарушения, приводят к синдрому полиорганной недостаточности.
Однако данный способ прогнозирования не специфичен, не обладает достаточной степенью точности, трудоемкий в исполнении, требует дорогостоящего оборудования, нет разработанных стандартов для получения точных количественных показателей, поэтому результаты реакции выражаются в единицах оптической плотности [Патент №2148256 Российская Федерация. Способ доклинического прогнозирования плацентарной недостаточности / Смиренина И.В., Пестрикова Т.Ю. // Изобретения. Полезные модели. - 2000. - №12].
Известен способ доклинической диагностики гипоксии плода, проводимый по крови беременной с определением малонового диальдегида (МДА), антиокислительной активности (АОА) и антиокислительной защиты организма (АОЗ), как отношение АОА/МДА в эритроцитах, при снижении АОЗ до 1,90-0,82 диагностируют гипоксию плода.
Однако у предлагаемого способа доклинической диагностики гипоксии плода не известна точность, для объективного анализа необходимо учитывать концентрацию одновременно нескольких показателей (гидроперекисей липидов и активность каталазы). Методика определения МДА и АОА, на которую ссылаются авторы, не является корректной, а следовательно, достоверной для прогнозирования гипоксии плода [Патент №1752185 СССР, Способ диагностики гипоксии плода / Мусаев А.Т., Банкова В.В. // Изобретение. - 1992. - №28. - С. 242-243].
Ближайшим аналогом заявляемого способа является способ прогнозирования развития внутриутробной гипоксии плода по определению фонда свободных аминокислот в венозной крови беременных в третьем триместре беременности и перед родами. При условии установления гипераминоацидемии рассчитывают коэффициент отношения незаменимых аминокислот к заменимым. При величине коэффициента 0,5 и менее прогнозируют развитие внутриутробной гипоксии в системе «мать-плацента-плод» на фоне метаболических нарушений беременной.
Недостатком предлагаемого способа является двукратное определение нескольких биохимических показателей; трудоемкость метода; использование дорогостоящего оборудования; отсутствие точности прогноза [Патент №2334985 Российская Федерация. Способ прогнозирования развития внутриутробной гипоксии плода / Тарханова А.Э., Ковальчук Л.А., Прохоров В.Н. // Изобретения. Полезные модели. - 2008. - №27].
Техническим решением заявляемого способа является прогнозирование развития ХГП у женщин, забеременевших с помощью ЭКО, а также упрощение и повышение точности способа до 87,0%. Прогноз осуществляется до наступления беременности. Техническое решение осуществляется путем определения содержания тиреотропного гормона (ТТГ) в венозной крови у женщины перед процедурой ЭКО. При значении данного показателя более 1,92 мМЕ/л прогнозируют развитие хронической гипоксии плода.
Новизна способа заключается в том, что впервые прогнозирование развития ХГП у женщин, забеременевших с помощью ЭКО, проводят перед процедурой ЭКО по определению содержания ТТГ в венозной крови.
Функция щитовидной железы (ЩЖ) и репродуктивная функция женщины тесно взаимосвязаны [Перминова С.Т., Фадеев В.В., Корнеева И.Е. Репродуктивная функция женщин с патологией щитовидной железы // Проблемы репродукции. - 2006. - Т. 12, №1. - С. 70-77]. Эта взаимосвязь обусловлена общими центральными механизмами регуляции и наиболее отчетливо проявляется во время беременности. Известно, что беременности, индуцированные с помощью метода ЭКО, представляют собой группу риска по развитию осложнений: высокой частоты ранних репродуктивных потерь, многоплодия, раннего гестоза, тяжелого синдрома гиперстимуляции яичников, фетоплацентарной недостаточности, угрозы преждевременных родов, развития патологических состояний у плода [Назаренко Т.А., Дуринян Э.Р., Чечурова Т.Н. Эндокринное бесплодие у женщин. Диагностика и лечение. - М., 2004. - 72 с.]. Высокая стероидная нагрузка вследствие гиперстимуляции яичников, а также прием большого числа гормональных препаратов влияют на метаболизм гормонов гипофизарно-тиреоидной системы. Так, A. Muller и соавт. при исследовании функции ЩЖ у женщин в программе ЭКО в период непосредственно после завершения стимуляции суперовуляции обнаружили значительное повышение уровня сывороточного тиреотропного гормона (ТТГ) и снижение связанного Т4 (тироксина) по сравнению с их исходными уровнями [A.F. Muller [et al.] Decrease of free thyroxine levels after controlled ovarian hyperstimulation. - 2000. - Vol. 85 (2) / - P. 545-548]. Сходные результаты получены Л.Л. Бостанджян, которая выявила повышение уровня ТТГ и снижение уровня связанного Т4 в сыворотке крови пациенток ко дню переноса эмбрионов и через 14 дней после переноса эмбрионов, что свидетельствует о напряжении гипофизарно-тиреоидной системы на фоне стимуляции суперовуляции в программе ЭКО [Бостанджян Л.Л. Влияние контролируемой стимуляции суперовуляции у пациенток программы ЭКО на функциональное состояние тиреоидной системы // Проблемы репродукции. - 2004. - №5. - С. 22-4]. Многие авторы полагают, что гормоны тиреоидной системы действуют однонаправленно с фолликулостимулирующим гормоном, оказывая прямое стимулирующее действие на функции гранулезных клеток, включая их морфологическую дифференциацию, стимулируют секрецию прогестерона и эстрадиола желтым телом, влияют на способность ооцитов к оплодотворению, качество и жизнеспособность эмбрионов [Wakim A.N., Polizotto S.L., Burholt D.R. Influense of thyroxine on human granulosa cell steroidogenesis in vitro // J Assist Reprod Genet. - 1995. - Vol. 12 (4). - P. 274-27]. Ранее проводимые исследования показали, что уровень ТТГ значительно выше у женщин с низким качеством ооцитов и неудачными попытками программ ЭКО и переноса эмбриона (ПЭ) [Рорре К., Velkeniers В. Female infertility and the thyroid // Best Practice & Research Clinical Endocrinology & Metabolism. - 2004. - Vol. 18 (2) - P. 153-165]. Некоторые исследователи акцентируют внимание на то, что уровень ТТГ является одним из показателей прогноза эффективности программ вспомогательных репродуктивных технологий (ВРТ) и свидетельствует о важной роли ТТГ в физиологии ооцитов [Serum prolactin and TSH in an in vitro fertilization population: is there a link between fertilization and thyroid function? / D.W. Cramer et al. // J Assisted Reprod Genet. - 2003. - Vol. 20 (6). - P. 210-215].
Кроме того, потребность в тиреоидных гормонах (ТГ) во время беременности увеличивается на 40-50%, а гипотироксинемия любого происхождения имеет самые неблагоприятные последствия именно на ранних сроках беременности. Это обусловлено, с одной стороны, высоким уровнем обменных процессов во время беременности, с другой - трансплацентарным транспортом ТГ от матери к плоду, которые необходимы для процессов эмбриогенеза, созревания всех органов и систем и в первую очередь для формирования и созревания ЦНС будущего ребенка [Subclinical hyperthyroidism and pregnancy outcomes/ В.M. Casey et al. // Obstet. Gynecol. - 2006. - Vol. 107, №2 (Pt. 1). - P. 337-341]. Как отдельный орган щитовидная железа у плода начинает функционировать с 12-й недели внутриутробного развития, до этого срока потребность плода в ТГ полностью компенсируется гормонами матери [Guidelines of the American Thyroid Association for the diagnosis and management of thyroid disease during pregnancy and postpartum / A. Stagnaro-Green et al. // Thyroid. - 2011. - Vol. 21, №10. - P. 1081-1125]. В то же время во время беременности за счет увеличивающейся потребности и повышенной почечной экскреции снижается в циркуляции содержание йода - структурного компонента ТГ [Нестеренко О.С. Особенности развития детей от женщин с тиреоидной патологией // Российский педиатрический журнал. - 2001. - №6. - С. 29-30]. По нашему мнению, у женщин во время индуцированной беременности увеличивается риск развития дисбаланса гормонов гипофизарно-тиреоидной системы, что обуславливает нарушение физиологического течения беременности и способствует формированию ХГП.
Отличительные признаки способа: установлен новый прогностический параметр содержания ТТГ перед процедурой ЭКО, при количественном значении которого более 1,92 мМЕ/л прогнозируют развитие хронической гипоксии плода у женщин, забеременевших с помощью экстракорпорального оплодотворения.
Способ осуществляется стандартно следующим образом.
У женщин с бесплодием в анамнезе перед проведением процедуры ЭКО забирают венозную кровь в количестве 2 мл, после образования сгустка центрифугируют при 1500 об/мин в течение 10 минут и определяют уровень тиреотропного гормона (ТТГ) в 50 мКл сыворотки крови методом твердофазного хемилюминесцентного иммунометрического анализа с использованием двойных антител набором реагентов Rapid TSN (IMMULITE Rapid TSH, производитель: Siemens Healthcare Diagnostics, USA) согласно инструкции. Результат получают через 2 часа 30 мин в мМЕ/л.
Сущность заявляемого способа поясняется следующими примерами.
Пример 1.
Семья Б. наблюдалась в центре планирования семьи и репродукции с диагнозом вторичное бесплодие, обусловленное отсутствием овуляции. Эндометриоз тазовой брюшины. Продолжительность бесплодия 4 года. Брак первый, зарегистрированный. Возраст отца 35 лет, в анамнезе - остеохондроз. Заключение по спермограмме: астенозооспермия. Возраст матери 32 года. В анамнезе: медицинский аборт, перенесенные операции - лапароскопия. Содержание тиреотропного гормона перед процедурой ЭКО составило 3,18 мМЕ/л. В случае наступления беременности прогнозируется ХГП. Беременность наступила после ЭКО с первой попытки при использовании длинного протокола, протекала на фоне угрозы прерывания в I, III триместрах беременности. По данным УЗИ - раннее старение плаценты, взвесь в околоплодных водах, синдром задержки роста плода (СЗРП). Кардиотокография - 1,41. Диагноз: хроническая гипоксия плода. Произошли первые своевременные роды в 38,6 недель. Кесарево сечение в нижнем сегменте матки. Родилась живая доношенная девочка массой тела 2650 г, длиной тела 52 см, оценка по шкале Апгар 6-7 баллов. Диагноз при рождении: умеренная асфиксия на фоне хронической гипоксии плода, синдрома задержки внутриутробного развития 1 ст. асимметричного варианта. Проконсультирована неврологом, проведена нейросонография: перинатальное поражение центральной нервной системы (ПП ЦНС) гипоксического генеза, церебральная ишемия 1 степени, ВЖК 1 степени, синдром возбуждения. Таким образом, прогноз ХГП по предлагаемому способу подтвердился.
Пример 2.
Семья П. наблюдалась в ЦПС с диагнозом вторичное бесплодие. Брак второй, зарегистрированный. Продолжительность бесплодия 5 лет. Возраст отца 33 года. Заключение по спермограмме: астенозооспермия. Возраст матери 33 года. В анамнезе: хронический сальпингит, хронический эндометрит; две внематочные беременности; перенесенные операции - тубэктомия. Содержание тиреотропного гормона перед процедурой ЭКО составило 2,0 мМЕ/л. В случае наступления беременности прогнозируется ХГП. Беременность наступила после ЭКО со второй попытки при использовании длинного протокола, протекала на фоне угрозы прерывания в III триместре беременности. УЗИ - взвесь в околоплодных водах. Кардиотокография - 1,37. Диагноз: хроническая гипоксия плода. Произошли первые своевременные роды при беременности 38,5 недель. Кесарево сечение в нижнем сегменте матки. Родилась живая доношенная девочка с массой тела 2850 г, длиной тела 49 см, оценка по шкале Апгар 7-8 баллов. Конъюгационная желтуха. Таким образом, прогноз ХГП по предлагаемому способу подтвердился.
Пример 3.
Семья Е. наблюдалась в ЦПС с диагнозом вторичное бесплодие, обусловленное отсутствием овуляции. Синдром поликистозных яичников. Брак первый, зарегистрированный. Продолжительность бесплодия 3 года. Возраст отца 25 лет. Заключение по спермограмме: астенозооспермия. Возраст матери 26 лет. В анамнезе: уреаплазмоз; перенесенные операции - лапароскопия. Содержание тиреотропного гормона перед процедурой ЭКО составило 1,79 мМЕ/л. В случае наступления беременности прогноз - отсутствие ХГП. Беременность наступила после ЭКО с первой попытки при использовании короткого протокола, протекала без особенностей (по данным УЗИ и допплерометрии). Кардиотокография - 0,87. Произошли первые своевременные роды при беременности 38,5 недель. Кесарево сечение в нижнем сегменте матки. Родился доношенный мальчик с массой тела 3400 г, длиной тела 52 см, оценка по шкале Апгар 8-9 баллов. Диагноз при выписке: доношенный новорожденный. Таким образом, прогноз по предлагаемому способу подтвердился.
Пример 4.
Семья П. наблюдалась в ЦПС с диагнозом первичное бесплодие, трубный фактор. Брак второй, незарегистрированный. Продолжительность бесплодия два года. Возраст отца 27 лет. Заключение по спермограмме: астенозооспермия, олигоспермия, тератозооспермия. Проводилось лечение. Возраст матери 28 лет. В анамнезе: хронический сальпингит, эктопия шейки матки, миома матки; перенесенные операции: тубэктомия. Содержание тиреотропного гормона перед процедурой ЭКО составило 0,7 мМЕ/л. В случае наступления беременности прогноз - отсутствие ХГП. Беременность наступила после ЭКО с первой попытки при использовании длинного протокола, протекала без особенностей (по данным УЗИ и допплерометрии). Кардиотокография - 0,71. Произошли первые своевременные роды при беременности 38,0 недель. Кесарево сечение в нижнем сегменте матки. Родилась доношенная девочка с массой тела 3550 г, длиной тела 53 см, оценка по шкале Апгар 8-9 баллов. Диагноз при выписке: доношенный новорожденный. Таким образом, прогноз по предлагаемому способу подтвердился.
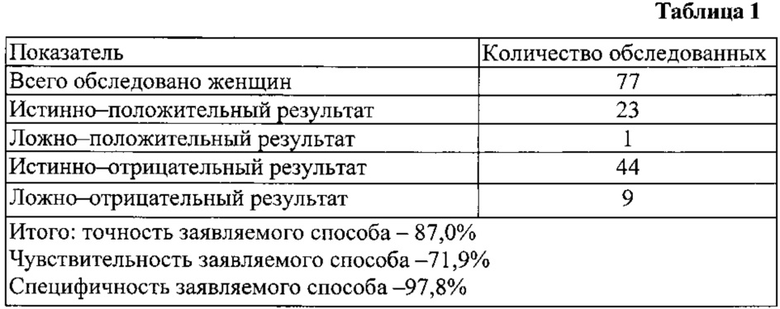
Указанным способом обследовано 77 женщин с бесплодием в анамнезе.
Результаты исследования представлены в таблице 1.
Преимущества способа
1. Исследование проводится женщине перед процедурой ЭКО, что позволяет своевременно сформировать группы риска по развитию ХГП для проведения профилактических мероприятий.
2. Предлагаемый способ имеет высокую точность - 87,0%, чувствительность - 71,9%, специфичность - 97,8%.
3. Данный способ является неинвазивным для ребенка.
4. Дешевизна способа.
5. Метод является скрининговым, т.е. позволяет обследовать большое количество женщин.
Таким образом, заявленный способ прост в исполнении и позволяет с высокой точностью прогнозировать развитие ХГП у женщин, забеременевших с помощью ЭКО, своевременно профилактировать у них нарушение функции щитовидной железы, начиная с этапа ЭКО. Своевременно принятые профилактические мероприятия будут способствовать снижению частоты ХГП у женщин, забеременевших с помощью ЭКО, и одновременно позволят снизить экономические затраты на их лечение.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ прогнозирования развития внутрижелудочковых кровоизлияний у новорожденных, родившихся после экстракорпорального оплодотворения | 2016 |
|
RU2639134C2 |
| СПОСОБ РАННЕЙ ДИАГНОСТИКИ МИНИМАЛЬНОЙ ТИРЕОИДНОЙ ДИСФУНКЦИИ У БЕРЕМЕННЫХ | 2006 |
|
RU2311646C1 |
| СПОСОБ ОТБОРА БЕРЕМЕННЫХ I-II ТРИМЕСТРОВ ДЛЯ ПРОВЕДЕНИЯ КОРРЕГИРУЮЩЕЙ ТЕРАПИИ ДИСФУНКЦИИ ЩИТОВИДНОЙ ЖЕЛЕЗЫ | 2005 |
|
RU2297794C1 |
| СПОСОБ АНТЕНАТАЛЬНОЙ ПРОФИЛАКТИКИ НАРУШЕНИЙ ЗДОРОВЬЯ НОВОРОЖДЕННЫХ | 2004 |
|
RU2277917C2 |
| Способ прогноза развития синдрома гиперстимуляции яичников при применении вспомогательных репродуктивных технологий | 2015 |
|
RU2612839C1 |
| Способ прогнозирования степени риска нарушения репродуктивного здоровья у женщин второго поколения потомков, прародители которых находились в зоне радиационного воздействия | 2016 |
|
RU2622373C1 |
| Способ прогнозирования течения невротических, связанных со стрессом расстройств | 2015 |
|
RU2613111C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА ЗАБОЛЕВАНИЙ ЩИТОВИДНОЙ ЖЕЛЕЗЫ У ЖЕНЩИН ПЕРИМЕНОПАУЗАЛЬНОГО ВОЗРАСТА | 2009 |
|
RU2421127C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ НОРМАЛИЗАЦИИ ФУНКЦИИ ЩИТОВИДНОЙ ЖЕЛЕЗЫ В ТЕЧЕНИЕ НЕОНАТАЛЬНОГО ПЕРИОДА У ДЕТЕЙ С ПРЕХОДЯЩИМ НЕОНАТАЛЬНЫМ ГИПОТИРЕОЗОМ | 2004 |
|
RU2277850C2 |
| СПОСОБ АНТЕНАТАЛЬНОГО ПРОГНОЗИРОВАНИЯ ПОСЛЕДСТВИЙ ПЕРИНАТАЛЬНЫХ ПОРАЖЕНИЙ НЕРВНОЙ СИСТЕМЫ У ДЕТЕЙ | 2011 |
|
RU2449287C1 |
Изобретение относится к медицине, а именно к перинатологии, акушерству и гинекологии, и может быть использовано для прогнозирования хронической гипоксии плода (ХГП) у женщин, забеременевших с помощью ЭКО. Для этого у женщин перед процедурой ЭКО в венозной крови определяют содержание тиреотропного гормона и при его значении более 1,92 мМЕ/л прогнозируют развитие ХГП. Способ позволяет повысить точность и специфичность прогнозирования ХГП у женщин, забеременевших с помощью метода ЭКО, при простоте его выполнения с выделением группы риска формирования ХГП для своевременного проведения профилактических мероприятий. 1 табл., 4 пр.
Способ прогнозирования хронической гипоксии плода путем биохимического исследования периферической венозной крови, отличающийся тем, что перед процедурой экстракорпорального оплодотворения определяют содержание тиреотропного гормона и при его значении более 1,92 мМЕ/л прогнозируют развитие хронической гипоксии плода у женщин, забеременевших с помощью экстракорпорального оплодотворения.
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ПАТОЛОГИИ ПОЧЕК У НОВОРОЖДЕННЫХ | 2012 |
|
RU2484762C1 |
| WO 2013014112 A1, 31.03.2013 | |||
| БАЙБАРИНА Г.В | |||
| Индуцированная беременность: особенности течения и значение генетических факторов в невынашивании | |||
| Автореферат на соиск.уч.ст | |||
| канд.мед.наук//М., 2004, 23с | |||
| GRABAR W | |||
| Interconnection between assisted reproductive technologies, pregnancy complications and risk of birth defects// Georgian Med News | |||
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
Авторы
Даты
2017-12-19—Публикация
2016-06-24—Подача