Перекрестная ссылка на родственные заявки
Настоящая заявка претендует на приоритет в соответствии с §119(e) раздела 35 Свода федеральных законов США по предварительной заявке на патент США No.61/259,748, озаглавленной как "Композиции и способы ингибирования клеточной адгезии к RGD связывающим сайтам", поданной 10 ноября 2009, полное содержание которой включено сюда посредством ссылки.
Область техники
Настоящее изобретение в целом относится к области химии и медицины и более конкретно к композициям веществ и способам, пригодных для ингибирования клеточной адгезии Arg-Gly-Asp ("RGD" трипептид) связывающими сайтами, и относится к лечению заболеваний, таких как воспаление, заживления ран, предотвращения образования рубцов, тромбоза, метастазирования рака и опухолей, пролиферативной или непролиферативной диабетической ретинопатии, разжижения стекловидного тела, индукции отслойки сетчатки задней от поверхности стекловидного тела (PVD), патогенеза витреоретинальных заболеваний, таких как плавающие помутнения, идиопатический разрыв макулы, макулярный тракционный синдром, возрастная макулярная дегенерация, влажная макулярная дегенерация, хориоидальная неоваскуляризация, витреоретинальная хирургия, окклюзия вен, неоваскуляризация роговицы, ишемия зрительного нерва, рубеоз радужки, и к предотвращению образования рубцов при хирургии глаукомы.
Уровень техники
Последовательность RGD-трипептида присутствует в составе многих белков и играет важную роль в клеточной адгезии. Примеры белков, в которых присутствует последовательность RGD-трипептида, включают коллаген, фибронектин, витронектин, фактор Виллебранда (ФВ), некоторые дизинтегрины и некоторые дискоидины.
Интегрины представляют собой гетеродимерные рецепторы на поверхности клеток и опосредуют адгезию между клетками и внеклеточным матриксом (ВКМ) путем связывания их с лигандами, имеющими доступную для связывания последовательность RGD. Нормальное интегрин-RGD связывание, как предполагается, играет важную роль в экспрессии генов, участвующих в росте клеток, миграции и выживании. Нарушения регулирования такого роста клеток, миграции и выживания может привести к ряду болезненных состояний, включая тромбоз, воспаление и рак. Таким образом, RGD-пептиды изучались как потенциальные мимитики белков клеточной адгезии, а также рассматривалась их способность связываться с интегринами для их использования терапевтических целей, таких как ингибирование апоптоза, ангиогенеза, опухолей, для использования их мультимерных форм как внутренних агентов лучевой терапии, а также визуализирующих рак агентов и как лекарственное противораковое средство.
В глазах интегрины влияют целый ряд процессов, в том числе развитие глаза, миграция клеток, заживление и некоторые патологические процессы. Интегрины также могут модулировать воспаление и тромбоз в тканях глаза. При введении интравитреально пептид RGD, как сообщается, может быть причиной отслойки сетчатки от задней поверхности стекловидного тела в моделях на животных и, таким образом, может быть полезен в лечении некоторых заболеваний сетчатки и/или в облегчении в удалении стекловидного тела в ходе витрэктомии [См. Olivera, L.B. и др., RGD Peptide-Assisted Vitrectomy to Facilitate Induction oƒ a Posterior Vitreous Detachment: a New Principe in Pharmacological Vitreolysis; Current Eye Research (8): 333-40 (25 декабря 2002)].
Сущность изобретения
Настоящее изобретение обеспечивает новые соединения, содержащие RGCys-вую кислоту (например, R-G-NH-CH(CH2-SО3H)COOH или Arg-Gly-NH-CH(CH2-SO3Н)СООН) и ее производные (в том числе фармацевтически приемлемые соли, гидраты, стереоизомеры, мультимеры, циклические формы, линейные формы, конъюгаты с лекарственными средствами, пролекарства и их производные).
Настоящее изобретение также относится к композициям и способам ингибирования клеточной адгезии к RGD-сайтам связывания или предоставления других диагностических или терапевтических агентов против RGD-сайтов связывания у субъекта (человека или животного) путем введения субъекту эффективного количества композиции, содержащей пептид RGCys-овой кислоты или его производное (в том числе фармацевтически приемлемые соли, гидраты, стереоизомеры, мультимеры, циклические формы, линейные формы, конъюгаты с лекарственными средствами, пролекарства и их производные). Конкретные примеры RGC-ового пептида по настоящему изобретению включают линейную форму Arg-Gly-NH-CH(CH2-SO3H)COOH (в частности, упомянутые здесь, как Соединение 1) и циклическую форму Arg-Gly-NH-CH(CH2-SO3H)COOH) (в частности, упомянутые здесь, как Соединение 2).
Общие формулы производных RGCys-овой кислоты по настоящему изобретению включают, но не ограничиваясь этим, соединения, соответствующие Общим формулам I-VII, представленным ниже:
Общая формула I:
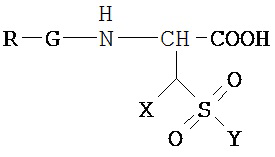
где X выбран из: Н, С1-С6 алкила, Ph или SO3H, a Y=ОН или NH2.
Общая формула II:
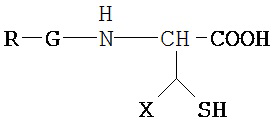
где X выбран из: Н, C1-С6 алкила, Ph или SO3H.
Общая формула III:
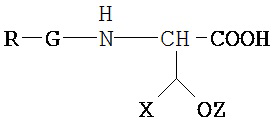
где X выбран из: Н, С1-С6 алкила, Ph или SO3H, и где Z выбран из: Н или SO3H.
Общая формула IV:
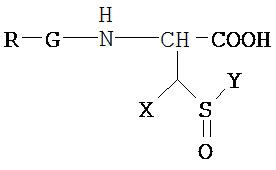
где X выбран из: Н, C1-С6 алкила, Ph или SO3H; Y выбран из: ОН или NH2.
Общая формула V:
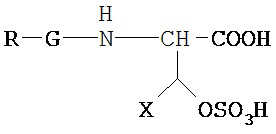
где X выбран из: Н, C1-С6 алкила, Ph или SO3H.
Общая формула VI:
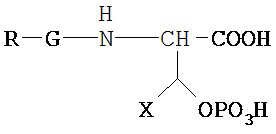
где X выбран из: Н, C1-С6 алкила, Ph или SO3H.
Общая формула VII:
X1-RGCys-овая кислота-Х
где X и X1 выбраны из циклического или линейного - Phe-Val-Ala, -Phe-Leu-Ala, -Phe-Val-Gly, -Phe-Leu-Gly, -Phe-Pro-Gly, -Phe-Pro-Ala, -Phe-Val или любой соли любой комбинации D-изомера или L-изомера Arg, Gly, Cys, Phe, Val, Ala, Leu, Pro, Thr.
Примеры циклических форм Общей формулы VII включают, но не обязательно ограничиваются этим:
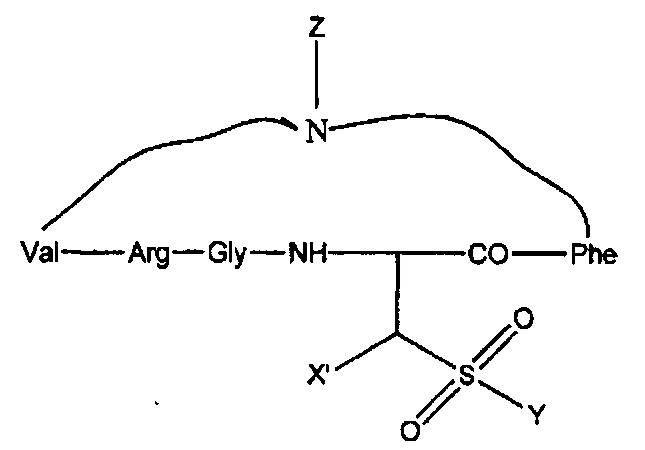
где X' выбран из: H, C1-С6 алкила, Ph или SO3H, a Z выбран из Н или Me; Y выбран из ОН, NH2.
Сульфокислоты являются более сильными кислотами, чем соответствующие карбоновые кислоты. Высокая полярность группы сульфокислоты приводит к усилению межмолекулярных связей. Например, RG-Цистеиновая кислота, которая имеет более поляризованную О-Н связь, может образовывать более сильные водородные связи, чем RG-Аспарагиновая кислота (RGD-пептид), который имеет относительно менее поляризованную О-Н связь, с амидными группами белков в интегриновом сайте связывания и/или сильнее взаимодействует с ионами металлов в составе интегринового сайта связывания.
Как описано более подробно в данном описании, был синтезирован и испытан на животных один конкретный пример Общей формулы VII, Глицинил-Аргинил-Глицинил-Цистеин-Треонил-Пролин-СООН (GRG-Цистеиновая кислота ТП; далее именуется как Соединение 1). Было обнаружено, что он является эффективным в стимулировании отслоения задней поверхности стекловидного тела от поверхности сетчатки (PVD) путем ингибирования взаимодействий интегрин - внеклеточный матрикс (ВКМ). Как описано также более подробно в данном описании, Соединение 1 было протестировано в модели заживления раны с использованием эндотелиальных клеток пупочной вены человека (HUVEC), и было показано, что оно ингибирует клеточную адгезию на 74% в течение 12 часов по сравнению с ингибированием на 40% циклическим RGD-пептидом. Эти исследования показывают и подтверждают, что Глицинил-Аргинил-Глицинил-Цистеин-Треонил-Пролин-СООН может связываться с интегрином даже сильнее, чем RGD-пептид.
Пептид RGCys-овой кислоты, который может существовать как в L-форме, так и в D-форме, является конкурентным ингибитором интегрин-ВКМ взаимодействий.
Последовательности пептида RGCys-овой кислоты могут быть представлены протеаза-устойчивыми производными, циклическими производными или производными пролекарств, либо могут быть связаны с системами доставки лекарста или моноклональных антител.
Композиции по настоящему изобретению пригодны для ингибирования ангиогенеза и могут быть использованы для лечения воспаления, заживления ран, тромбоза, раковых метастаз и опухолей. Дальнейшее полезное применение может быть найдено в офтальмологии, включая пролиферативную или непролиферативную диабетическую ретинопатию, разжижение стекловидного тела, индукцию отслоения задней поверхности стекловидного тела (PVD), патогенез витреоретинальных заболеваний, таких как идиопатический макулярный разрыв, витреомакулярная тракция, возрастная дегенерация желтого пятна, влажная дегенерация макулы, хориоидальная неоваскуляризация, витреоретинальная хирургия, окклюзия вен и профилактика образования рубцов при хирургии глаукомы. Кроме того, мультимерные и/или радиоактивно-меченные композиции по настоящему изобретению пригодны в качестве диагностических/визуализирующих агентов для обнаружения опухолей и в качестве радиотерапевтических препаратов для лечения опухолей, а также в качестве направленных переносчиков противораковых лекарств, благодаря их свойствам нацеливания на опухоль.
Биоматериалы, соединенные с RGC-пептидом, также могут обеспечить синтетическое адгезивное микроокружение для увеличения времени жизни и роста клеток и для инжениринга живых тканей при их использовании в тканевой инженерии и в регенеративной медицине. Благодаря своему свойству связывать интегриновые рецепторы адгезии, RGC-пептиды могут обеспечить адгезионный сигнал при связывании их с биоматериалом или подложкой. Материалы на основе RGC опосредуют клеточную адгезию, распространение и миграцию клеток. Кроме того, интегрин-опосредованная клеточная адгезия способствует пролиферации и выживанию клеток и играет ключевую роль в сборке и организации многоклеточных структур и тканей.
Препараты для лечения макулярной дегенерации, как Луцентис и Авастин, основаны на ингибировании VEGF, который в противном случае вызывает рост новых сосудов, ангиогенез и, следовательно, способствует отеку макулы. Было известно, что небольшой пептид RGD может индуцировать апоптоз посредством ингибирования взаимодействия с внеклеточным матриксом благодаря конкурентному связыванию, как показано Бруксом и соавт. в Патенте США №6,500,924.
RGD пептид-связывающий и распознающий мотив можно найти в белках внеклеточного матрикса и интегринах, которые связывают внутриклеточный цитоскелет клеток с ВКМ путем распознавания RGD-эпитопов адгезии. См., например, Foos, R.Y., Invest. Opthalmol. Vis. Sci. (1972) 11, 801-808. Клетки, не связанные с ВКМ, как правило, подвергаются апоптозу.
В общем, взаимодействие между фибробластами и гликопротеиновыми компонентами внеклеточного матрикса вызывает формирование рубца, опосредованное, прежде всего, взаимодействием RGD-содержащей аминокислотной последовательности с интегринами клеточной поверхности. Также известно, что RGD-последовательность участвует во взаимодействиях клетка - ВКМ при воспалительных и гомеостатических реакциях (см. Hershkoviz С.М. и соавт., Invest. Opthalmol. Vis. Sci. (1994), 35, 2585-2591), а интегрины играют важную роль в миграции клеток при заживлении ран или патологических процессах и модуляции воспаления и тромбоза. Таким образом, эффективные антагонисты интегрина, такие как RGD-пептиды, могут быть очень полезны в качестве фармакологических агентов, в частности противовоспалительных, антиметастатических или антитромботических агентов (см. Elner S.G., Elner V.M., IOVS (1996) 37: 696-701). В литературе также сообщается, что CD44 рецептор гиалуроновой кислоты опосредует взаимодействий клетка-клетка и клетка-матрикс благодаря своей аффинности для гиалуроновой кислоты, а также, возможно, благодаря своей аффинности для других лигандов, таких как остеопонтин, коллаген и матриксные металлопротеазы (ММП).
Адгезия к гиалуронану играет важную роль в миграции клеток, росте опухоли и ее прогрессировании, он участвует в активации лимфоцитов, рециркуляции и хоминге, а также в кроветворении. Измененная экспрессия или дисфункция вызывает многочисленные патогенные проявления (см., например, Jiang D., Annu. Rev. Cell. Dev. Biol. (2007) 23: 435-461; и Knudson, W. и др., Matrix Bio. (2002), 21: 15-23).
Недавно было показано, что взаимодействие CD44 и клеточных матриксных компонентов (например, НА) играет важную роль в развитии различных воспалительных заболеваниях, и нарушение взаимодействий гиалуронан-СD44 может привести к улучшению хориоидальной неоваскуляризации (см. Hiroshi Mochimaru и др., Invest. Ophthalmol. Vis. Sci. (2009) 50: 4410-4415).
Эти сведения показывают, что молекулы адгезии, такие как RGD-пептид или CD44, в межклеточных взаимодействиях и взаимодействиях клетка-ЕСМ играют важную роль в развитии многих патогенных заболеваний, и ингибирование таких взаимодействий может стать новой терапевтической целью в лечении этих заболеваний.
Для синтетических пептидов также было показано связывание их с интегринами и факторами роста. Для циклических пентапептидов, содержащих RGD-последовательность, было установлено ингибирование связывания витронектина с ανβ3 интегрином (см. Michael A. Dechantsreiter и др., J. Med. Chem. (1999) 42: 3033-3040), и обоих витронектина и фибронектина с ανβ3 и ανllbβ3 интегринами (см. Roland Haubner и соавт., J. Am. Chem. Soc, (1996) 118: 7461-7472). Было показано, что такое ингибирование может найти применение в лечении многочисленных несвязанных между собой заболеваний. В исследованиях на хомяках показано, что эти циклические пентапептиды задерживают рост и метатезирование опухоли по сравнению с контрольными животными (см. М.A. Buerkle и др., British J. Cancer (2002) 86: 788-795). Для таких пентапептидов также показано уменьшение связывания серповидных красных кровяных клеток с эндотелием сосудов и улучшение гемодинамического поведения (см. Eileen М. Finnegan и др., J. Am. Physiol. Heart Circ. Physiol. (2007) 293: H1038-H1045). Другой циклический пептид, содержащий RGD-последовательность, проявил сильное связывание с ανβ1 интегрином, известным как играющий важную роль в связывании лейкоцитов при воспалительных и иммунных реакциях (см. Pina М. Cardarelli и соавт., J. Biol. Chem. (1994) 269: 18668-18673). Синтетические сульфатированные тетрапептиды проявили сильное связывание с VEGF (см. Maynard, J.A. Hubbell, Acta Biomaterialia (2005) 1: 451-459).
Кроме того, важным и полезным приложением является то, что димерный RGD-пептид, конъюгированный с лекарственным средством, показан как пригодный для интегрин-нацеленной доставки лекарств в опухоль (см. Chen и соавт., J. Med. Chem., (2005) 48 (4): 1098-1106).
В другом не менее важном и полезном приложении мультимерные радиомеченные RGD-пептиды показаны как пригодные в качестве диагностических/визуализирующих агентов для выявления опухолей и в качестве агентов для лучевой терапии конкретных опухолевых мишеней и лечения их путем воздействия на интегрин ανβ3 (см. Zi-Bo Li и др., J. Nucl. Medicine (2007) 48: 1162-1171).
В офтальмологии образование рубцов при заживлении ран фибробластами является одной из основных проблем, в частности глаукомы. Это связано с взаимодействиями между фибробластами и гликопротеиновыми компонентами ВКМ. Распознавание ВКМ гликопротеинов происходит через интегрины на поверхности клетки, которые являются специфичными для эпитопов адгезии, таких как последовательность Arg-Gly-Asp (или RGD). RGD-последовательность, которая присутствует в составе некоторых белков плазмы крови, в том числе фибронектина (FN) и витронектина (VN), участвует во взаимодействиях клетка - ВКМ, которые возникают при воспалительных и гомеостатических реакциях. Ингибирование взаимодействия между фибробластами и гликопротеинами ВКМ уменьшает образование рубцов (см. Rami Hershkoviz др., Invest. Ophthalmol. Vis. Sci. (1994) 35: 2585-2591).
Фибриллы коллагена в задней коре стекловидного тела связаны с витреоретинальной поверхностью, в частности, на внутренней пограничной мембране поверхности сетчатки (см. Sebag J., Eye (1992), 6: 541-552). В связи с присоединением к стекловидному телу, диску зрительного нерва, вдоль основных сосудов сетчатки и с лицевой стороны, весь задний полюс играет важную роль в патогенезе витреоретинальных заболеваний, таких как идиопатический макулярный разрыв, витреомакулярный тракционный синдром, пролиферативная диабетическая ретинопатия и т.д. (Akiba J. Quiroz М.А. и соавт., Ophthalmol. (1990) 97, 1619-1655).
Ингибирование ангиогенеза, как было ранее показано, может повлиять на диабетическую ретинопатию и макулярную дегенерацию, которые являются результатом разрастания кровеносных сосудов глаза. При этих заболеваниях сосуды нарушают нормальную структуру глаза или блокируют доступ света к задней части глаза. Новые кровеносные сосуды являются первичной патологией, а прекращение роста кровеносных сосудов может предотвратить слепоту. Таким образом, ангиоингибирование может обеспечить не только лечение этих заболеваний, но и вылечить их полностью. Кроме того, было предположено, что отделение стекловидного тела от сетчатки может облегчить макулярную тракцию, что снижает риск образования макулярного разрыва. Соответственно, ингибирование на задней поверхности стекловидного тела фибронектина и ламинина, связывающих интегрины на витреоретинальной поверхности, может предотвратить образование новых сосудов сетчатки глаза при диабетической ретинопатии и окклюзии вен сетчатки (см. Akiba J. Quiroz MA, Ophthalmol. (1990) 97, 1619-1655; Kelly N.E. и др., Arch. Ophthalmol. (1991) 109, 654-659, и Kado M. и др., J. Am. Ophthalmol. (1988) 105: 20-24).
В последние годы хирургические процедуры стекловидного тела значительно улучшились с целью уменьшить витреоретинальную тракцию и уменьшить отек сетчатки. Несмотря на непрерывное совершенствование хирургической техники и приборов, по-прежнему остается трудоемким атравматическое удаление коры стекловидного тела у ряда пациентов, особенно у больных диабетической ретинопатией и педиатрических пациентов, из-за осложнений, таких как разрывы или отслойка сетчатки и повреждение нервных волокон сетчатки (см. Sebag J., Arch. Clin. Exp. Ophthalmol. (1987) 225: 89-93; и Han D.P. и др., Arch. Ophthalmol. (1998) 106: 998-1000) и т.д. Таким образом, является весьма желательным менее травматичный подход селективного отделения поверхности стекловидного тела без повреждения сетчатки. В последние годы в литературе указывались различные фармакологические агенты для отделения витреоретинальной поверхности (см. Trese М.Т., Eye (2002) 16: 365-368; Gandorfer А. и др., J. Am. Ophthalmol. (2002) 133: 156-159, и Hesse L. и др., Eye Res. (2000) 70: 31-39). Фармакологический витреолизис с использованием ферментов, таких как гиалуронидаза (см. патент США №6,863,886 Karageozian и др.) и аутологичный плазмин (Sakuma Т. и др., Nippon Ganka Gakkai Zassi (2003) 107: 709-718) ранее был изучен для облечения расщепления внеклеточного матрикса и провоцирования отделения задней поверхности стекловидного тела. Тем не менее, неспецифические разрушения прилегающих тканей ферментами затрудняют их терапевтическое применение. В последние годы новый подход с использованием неферментативных фармакологических агентов, таких как мочевина (см. Nickerson С.и др., J. Biomechanics (2008) 41: 1840-1846, и Macromol. Symp.(2005): 183-189) и пептид RGD (см. Leonardo В. и др., Curr. Eye Res. (2002) 25: 333-340), был исследован, принимая во внимание влияние на разделение витреоретинальной поверхности. Было показано, что синтетический аналог пептида RGD конкурирует за RGD-мотив в белках ВКМ, нарушая интегрин - ВКМ взаимодействия и ослабляя их in vitro (Williams J.A., Pathol. Bio. (1992) 40: 813-821; Gehlsen K.P. и др., J. Cell Biol. (1988) 106: 925-930; Pierschbacher M.D. и др., J. Biol. Chem., (1987) 262: 17294-17298, и Zhon L.L. и др., IOVS (1996) 37: 104-113) и in vivo. Таким образом, интравитреальные инъекции раствора RGD-пептидов приводят к  высвобождению RGD-эпитопов из нерастворимых белков ВКМ на поверхности сетчатки, а следовательно, облегчая неферментативную PVD в моделях на кроликах. Очевидно, что эти результаты показывают, что витреоретинальная поверхность включает в себя интегриновое соединение с RGD-мотивом ВКМ, а также адгезию коллагена коры стекловидного тела на внутренней пограничной ламеле (ВПЛ). RGD-пептиды и их производные способствуют миграции эпителиальных клеток в ране (см. P.M. Merz и др., J. Burn Care Res. (1996) 17: 199-206), а также поддерживают свою биологическую активность при введении в составе синтетических биоматериалов, таких как гидрогели (см. MP Lutolf и др., Proc. Nat. Acad. Sci. (2003) 100: 5413-5418, а также MP Lutolf и др., Nature Biotechnol. (2003) 21: 513-518), других полимерных матриц (см. Horng-Ban Lin и др., J. Biomed. Materials Res. (2004) 28: 329-342), так поверхностных пленок на твердых субстратах (D.M. Ferris и др., Biomaterials (1999) 20: 2323-2331). RGD-пептиды также способствуют повышению адгезии эпителиальных или эндотелиальных клеток сосудистых протезов (см. K. Walluscheck и др., Eur. J. Vascular and Endovascular Surgery (1996) 12: 321-330) и других искусственных органов (см. Jeschke, Brigette, Biomaterials (2002) 23: 3455-3463), покрытых этой пептидной последовательностью, и было показано, что они обеспечивают поддержание возобновления роста нервов (см. М. Rafiuddin Ahmed и др., Brain Res. (2003) 993: 208-6). Биологически активная поверхность протеза может содержать синтетические волокна смолы или полимеры.
высвобождению RGD-эпитопов из нерастворимых белков ВКМ на поверхности сетчатки, а следовательно, облегчая неферментативную PVD в моделях на кроликах. Очевидно, что эти результаты показывают, что витреоретинальная поверхность включает в себя интегриновое соединение с RGD-мотивом ВКМ, а также адгезию коллагена коры стекловидного тела на внутренней пограничной ламеле (ВПЛ). RGD-пептиды и их производные способствуют миграции эпителиальных клеток в ране (см. P.M. Merz и др., J. Burn Care Res. (1996) 17: 199-206), а также поддерживают свою биологическую активность при введении в составе синтетических биоматериалов, таких как гидрогели (см. MP Lutolf и др., Proc. Nat. Acad. Sci. (2003) 100: 5413-5418, а также MP Lutolf и др., Nature Biotechnol. (2003) 21: 513-518), других полимерных матриц (см. Horng-Ban Lin и др., J. Biomed. Materials Res. (2004) 28: 329-342), так поверхностных пленок на твердых субстратах (D.M. Ferris и др., Biomaterials (1999) 20: 2323-2331). RGD-пептиды также способствуют повышению адгезии эпителиальных или эндотелиальных клеток сосудистых протезов (см. K. Walluscheck и др., Eur. J. Vascular and Endovascular Surgery (1996) 12: 321-330) и других искусственных органов (см. Jeschke, Brigette, Biomaterials (2002) 23: 3455-3463), покрытых этой пептидной последовательностью, и было показано, что они обеспечивают поддержание возобновления роста нервов (см. М. Rafiuddin Ahmed и др., Brain Res. (2003) 993: 208-6). Биологически активная поверхность протеза может содержать синтетические волокна смолы или полимеры.
Краткое описание чертежей
На рисунке 1 показано влияние трех пептидов, а именно циклического RGD-пептида, RGC-пептида (Соединение 1) и RGE-пептида, на кинетику заживление ран;
На рисунке 2 показана ВЭЖХ хроматограмма RGC-пептида (Соединение 1);
На рисунке 3 показаны масс-хроматограммы Electrospray RGC-пептид (Соединение 1);
На рисунке 4 показаны ВЭЖХ хроматограммы циклического RGC-пептида (Соединение 2) и
На рисунке 5 показаны масс-хроматограммы Electrospray циклического RGC-пептида (Соединение 2).
Подробное описание изобретения
Настоящее изобретение относится к новым соединениям, в том числе соединениям Общих формул I по VII, указанным выше. Конкретные примеры включают линейные формы Arg-Gly-NH-CH(CH2-SO3H)COOH (например, упомянутые здесь, как Соединение 1) и циклическую форму Arg-Gly-NH-CH(CH2-SО3Н)СООН (например, упомянутые здесь как Соединение 2), а также их производные, в том числе фармацевтически приемлемые соли, гидраты, стереоизомеры, мультимеры, циклические формы, линейные формы, многомерные формы, конъюгаты с лекарственным средством, пролекарства и их производные.
Примеры
Синтез Соединений 1 и 2
Может быть проведен традиционный твердофазный синтез пептидов (SPPS, см. R.B. Merrifield, J. Am. Chem. Soc. (1963) 85 (14): 2149-2154), известней специалистам в данной области техники. SPPS является предпочтительным методом синтеза благодаря высокой производительности. В общем, первый этап твердофазного пептидного синтеза заключается в сборке пептидной цепи с протекторными производными аминокислот на полимерной подложке. На втором этапе этой технологии проводят отщепление пептида от подложки с одновременным расщеплением всех боковых протекторных групп, получая незрелый свободный пептид. Общий принцип SPPS заключается в повторяющихся циклах связывания - депротекции. Свободный N-концевой амин пептида, прикрепленного к твердофазной подложке, соединяется с отдельной N-протекторной аминокислотной единицей. Эта единица затем подвергается депротекции, открывая новый N-концевой амин, к которому далее может быть присоединена аминокислота. См. "Asymmetric Synthesis", Von G.M. Coppola и H.F. Schuster; John Wiley & Sons, Нью-Йорк 1987, где описаны стратегии синтеза, протекции и депротекции, а также "Greene's Protective Groups in Organic Synthesis", Peter G.M. Wuts и Theodora W. Greene, (2-е издание) J. Wiley & Sons, 1991, где описаны стратегии протекции и депротекции.
Из двух основных используемых форм твердофазного синтеза пептидов - Fmoc (9-флуоренилметилоксикарбонил; щелочная лабильная альфа-амино-протекторная группа) и t-Boc (трет-бутилоксикарбонил; кислотная лабильная протекторная группа) предпочтительнее в синтезе пептидов по настоящему изобретению использование Fmoc. Для каждого отдельного способа применяются различные смолы и стадии протекции боковых аминокислот и последовательные стадии расщепления/депротекции. После отщепления от подложки пептиды, как правило, очищают с помощью обратно-фазовой ВЭЖХ с использованием колонок, таких как С-18, С-8 и С-4.
Пример твердофазного синтеза пептидов
Ниже приведен план этапов синтеза пептидов на Wang смоле в качестве твердого носителя, используя щелочную лабильную 9-флуоренилметилоксикарбонил (Fmoc) протекторную группу.
Fmoc депротекция
Вводят 0,08 ммоль Fmoc-Pro-Wang смолы в колонку, оснащенную пластиковой крышкой. Промывают смолу дважды порциями DMF (диметилформамидом) по 3 мл в течение 1 минуты для каждой. Затем добавляют около 3 мл 20% пиперидина в DMF, в результате чего происходит снятие Fmoc в течение 15 минут. В течение этого времени круговыми движениями мягко перемешивают или взбалтывают колонку для обеспечения полного смешивания. После завершения реакции (около 15 мин) содержимое сливают, а смолу снова смывают DMF (4×3 мл).
Присоединение амидной связи
Желаемую Fmoc-защищенную аминокислоту, Fmoc-Thr-TBU (3 экв. по отношению к смоле нагрузка указывается поставщиком) и DIEA (6 экв.) в DCM (0,5 М по отношению к аминокислоте) затем добавляют к смоле. Смесь охлаждают до -20°С в течение 20 минут. Далее, к реакционной среде добавляют бензотриазол-1-ил-окситрипирролидинофосфониум гексафторфосфат (РуВОР), пептид, другие реагенты, используемые в твердофазном синтезе пептидов (3 экв.). После встряхивания при - 20°С в течение 8 часов реакционную смесь сливают, и смолы промывают DCM (3х).
После Fmoc депротекции с использованием 20% пипердина в DMF (15 мин) и промывкой DMF (3 раза) протектируется Fmoc следующая аминокислота (3 экв., по отношению к используемой смоле), РуВор (так же, как указано выше).
Отщепление
Для получения пептида в форме свободной кислоты эфирная связь расщепляется с использованием сильно кислотной среды, например TFA (трифторуксусная кислота). Смолу обрабатывают 2-3 мл раствора трифторуксусной кислоты и воды 95:5. Осторожно перемешивают смолу в течение 25 минут. Затем сливают колонку и тщательно собирают фильтрат в коллекторный стеклянный сосуд.
Синтез Соединения 1 (GRG-Цистеиновая кислота ТП):
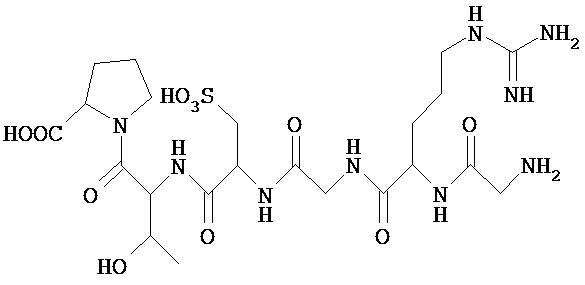
Этап 1. Загрузка смолы: о-хлоротритил смола с пролином, используемым в качестве стартового материала.
Этап 2. Сборка пептида: для сборки пептида используется Fmoc синтез. Протекторные аминокислоты активированы РуВОР, а концевые группы Fmoc удалены с помощью 20% пиперидина в DMF. Следующие протекторные аминокислоты используются в порядке, в котором они представлены ниже:
a. Fmoc-Thr-TBU (Fmoc треонин-t-бутиловый эфир)
b. Fmoc-Цистеиновая кислота-Pfp (Fmoc-Цистеиновая кислота-пентафторфениловый эфир)
c. Fmoc-Gly (Fmoc глицин)
d. Fmoc-Arg-Pbf (Nα-Fmос-Nω-(2,2,4,6,7пентаметилдигидробензофуран-5-сульфонил)-L-аргинин)
e. Fmoc-Gly (Fmoc-глицин)
Этап 3. Отщепление пептида от смолы: полученный пептид отщепляется от твердой подложки, а протекторные группы удалятся раствором 85,5% TFA, 5% раствором фенола, 2% воды, 5% тиоанизола и 2,5% этандитиола.
Этап 4. Очистка: для очистки полученного RGC-пептида используется высокоэффективная жидкостная хроматография (ВЭЖХ).
Количество Соединения 1, приготовленного, как описано выше, было проанализировано с помощью высокоэффективной жидкостной хроматографии, обеспечивая >98% область/область по чистоте [ВЭЖХ условия: Буфер А: 0,1% трифторуксусная кислота (TFA) в воде; Буфер В: 0,1% TFA в ацетонитриле; Подвижная фаза (ПФ) А: 97% буфера А и 3% буфера В, Подвижная фаза В: 79% буфера А и 21% буфера В; Подвижная фаза С: 50% буфера А и 50% буфера В, градиент см. ниже Таблицу 1; скорость потока: 1,0 мл/мин; колонка: Water Symmetry® C18, 5μ, 4,6×250 мм, температура колонки: 30°С; детектор: УФ@ 220 нм; объем введенного образца: 20,0 мкл; подготовка образца: 20 мкл образца, разведенного в 1,0 мл Подвижной фазы А [около 0,5 мг/мл)]. Соответствующее хроматограммы ВЭЖХ показаны на рис.2. Кроме того, молекулярная масса очищенного Соединения 1, полученного путем последовательного добавления соответствующих аминокислот для синтеза пептидной последовательности, была определена с помощью электроспрей масс-спектрометрии и составила 638,3 а.е.м. (теоретическая масса: 637,7 а.е.м.), подтверждая идентичность Соединению 1. Электроспрей масс-спектрограммы Соединения 1 показана на рис.3.
Синтез Соединения 2 (Цикло-RGСуs-овая кислота fN(CH3)V):
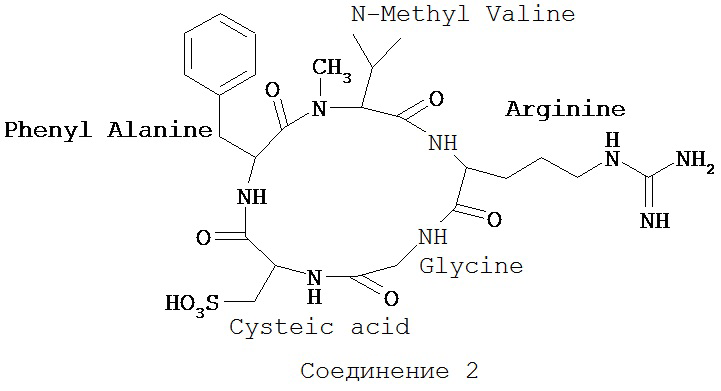
Этап 1. Загрузка смолы: о-хлоротритил смола используется в качестве исходного материала. Fmос-N-метил-L-Val присоединяется к смоле.
Этап 2. Сборка пептида: Fmoc синтез используется для сборки пептида. Протекторные аминокислоты активированы РуВОР, а концевые группы Fmoc удалены с помощью 20% пиперидина в DMF. Следующие протекторные аминокислоты используются в порядке, в котором они представлены ниже:
a. Fmoc-Phe (Fmoc-фенилаланин)
b. Fmoc-цистеиновая кислотно-Pfp (Fmoc-цистеиновая кислота - пентафторфениловый эфир)
c. Fmoc-Gly (Fmoc-глицин)
d. Fmoc-Arg-Pbf (Nα-Рmос-Nω)-(2,2,4,6,7пентаметилдигидробензофуран-5-сульфонил)-L-аргинин)
Этап 3. Отщепление пептида из смолы: пептид отщепляется от твердой поддержки с помощью уксусной кислоты /TFA/ DCM (1:3:3)
Этап 4. Циклизация и депротекция для получения желаемого циклического пептида: циклизация через in situ активацию с использованием дифенилфосфорилазида и бикарбоната натрия при сильном разбавлении. Боковые цепи депротектируются с использованием 85,5% TFA, 5% раствор фенола, 2% воды, 5% тиоанизола, 2,5% этандитиола.
Этап 5. Очистка: для очистки используется ВЭЖХ.
Количество Соединения 2, приготовленного так, как описано выше, было проанализировано с помощью высокоэффективной жидкостной хроматографии как >99% область/область по чистоте (ВЭЖХ условия: Подвижная фаза А: 0,1% трифторуксусная кислота в воде, В: 0,1% TFA в (80% ацетонитрил плюс 20% воды); градиент от 26% до 36% в течение 20 минут; скорость потока: 1,0 мл/мин; колонка Phenomenex С18 (2) 4,6×150 мм, 5μ, 100А, детектор УФ@ 220 нм; объем введенного образца: 100,0 мкл). Соответствующее хроматограммы ВЭЖХ показаны на рис.4. Кроме того, молекулярная масса очищенного Соединения 2, полученного путем последовательного добавления соответствующих аминокислот для синтеза пептидной последовательности, была определена с помощью электроспрей масс-спектрометрии и составила 625,3 а.е.м. (теоретическая масса: 625,77 а.е.м.), подтверждая идентичность Соединению 2. Электроспрей масс-спектрограмма Соединения 2 показана на рис.5.
Способы ингибирования клеточной адгезии
Настоящее изобретение также относится к способам ингибирования клеточной адгезии к RGD-сайтам связывания у субъекта, являющегося человеком или животным, путем введения субъекту эффективного количества RGCys-овой кислоты (например, линейной формы R-G-NH-CH(CH2-SO3H)COOH или циклической формы RG-NH-CH(CH2-SO3H)COOH) или их производных (в том числе фармацевтически приемлемых солей, гидратов, стереоизомеров, мультимеров, циклических форм, линейных форм, конъюгатов с лекарственными средствами, пролекарств и их производных).
Заявитель обнаружил, что синтетические пептиды RGCys-овой кислоты по настоящему изобретению вызывают апоптоз путем конкурентного ингибирования прикрепления клетки к компонентам ВКМ. Таким образом, представленные синтетические пептиды RGCys-овой кислоты и их производные могут быть использованы в качестве действующих антагонистов интегрина как лечебное средство против ангиогенеза, воспаления, раковых метастаз, тромбоза, профилактики и лечения рубцов, а также фармакологических агентов витреолизиса. Кроме того, важным аспектом настоящего изобретения является то, что предусмотрена улучшенная направленность на α, β интегрины с применением мультимерных и радиомеченных RGC-пептидов для использования в качестве радиотерапевтических средств для обнаружения опухолей (диагностические или визуализирующие агенты) и их лечения. Еще одним важным аспектом является улучшенные функции конъюгатов RGC-пептидов и мультимерных конъюгатов RGC-пептидов в качестве переносчиков лекарственных средств, например как переносчиков противораковых лекарств для эффективной нацеленности на опухоль.
Как описано в здесь, сульфокислоты в составе RGC-пептидов являются более сильными кислотами, чем соответствующие карбоновые кислоты в RGD-пептидах. Такая высокая полярность группы сульфокислоты приводит к усилению межмолекулярных связей. Например, RGCys-овая кислота, которая имеет более поляризованную О-Н связь, может образовывать более сильные водородные связи, чем RG-Аспарагиновая кислота, которая обладает относительно менее поляризованной О-Н связью, с амидными группами и/или с аминокислотами боковых цепей белка в интегриновом сайте связывания и/или имеет более сильные взаимодействия с ионами металлов в интегриновом сайте связывания. Таким образом, новые RGC-пептиды и их производные по настоящему изобретению представляют улучшенные соединения и композиции по сравнению с соответствующим RGC-пептидами в распознавании и связывании интегриновым рецептором.
Кроме того, у больных сахарным диабетом с хронической гипергликемией, связанной с повышенным ЮР, открытая угловая глаукома, в частности, как сообщается, связана с накоплением фибронектина в трабекулярной сетчатой ткани, избыток фибронектина, как полагают, препятствуют оттоку жидкости (см. Oshitari, Т. и соавт., Am. J. Ophthalmol. (2007) 143: 363-365). Вовлечение фибронектина в взаимодействия клетка-ВКМ в трабекулярной сети указывает на начальную стадию открытой угловой глаукомы (см. Mark С. Filla и др., Invest. Ophthalmol. Vis. Sci. (2002) 43: 151-161; и Cheryl R. Harm и др., Ophthalmic Res. (2001) 33: 314-324). Также сообщалось, что эндотелиальные клетки канала Шлемма взаимодействуют с внеклеточным матриксом, оказывая влияние на облегчение оттока (см. Cindy К. Bahler и др., Invest. Ophthalmol. Vis. Sci. (2004) 45: 2246-2254). В связи с ингибированием оттока жидкости при наличии избыточных компонентов внеклеточного матрикса, таких как фибронектин, применение пептидов RGCys-овой кислоты и ее производных может быть пригодным для лечения повышенного ЮР у больных сахарным диабетом.
Предпочтительный пептид RGCys-овой кислоты может быть слитым полипептидом, циклическим или линейным полипептидом, производным полипептида, в том числе производным пептида RGCys-овой кислоты или ассоциированным или связанным с системами доставки лекарственных препаратов или других лекарствами, таких как, например, противораковые препараты, мультимерный RGC-пептид, моноклональное антитело, содержащее последовательность RGCys-овой кислоты, которое иммунореактивно к сайту связывания интегрина, или его функциональный фрагмент.
Полипептиды, содержащие RGCys-овую кислоту, могут иметь последовательности, соответствующие аминокислотной последовательности природного адгезионного сайта связывания интегрина, таких как присутствующие в фибриногене, фибронектине, витронектине, факторе Виллебранда, ламинине, тромбоспондине и другим им подобным лигандам.
Настоящая пептидная последовательность состоит из трех аминокислот, имея терминальные гуанидино-, сульфоновую и карбоксильную группы и их производных, связанных и/или ассоциированных с системами доставки лекарств, в том числе пептидных фрагментов, гликопротеинов и полимерных групп, таких как ПЭГ, плуроник и других полимерных групп, а также липосом и наночастиц. Фармацевтические композиции, содержащие их, для лечения различных патологических расстройств включают инъекции, гели, суспензии, мази, твердые и жидкие лекарственные формы.
Интегриновые рецепторы, связанные с мотивом клеточной адгезии, такие как фибронектин, витронектин, ламинин, фибриноген, тромбоспондин и фактор Виллебранда, представляют собой целевой эпитоп пептида RGCys-овой кислоты и ее производных. Трипептид, RGCys-овая кислота была обнаружен как узнаваемая минимальная аминокислотная последовательность связывающих доменов клетки. Эта последовательность может также участвовать в иммунных функциях, несвязанных с интегринами. Таким образом, было обнаружено, что синтетическая последовательность RGCys-овой кислоты имитирует RGD связывающий домен клетки, а также то, что замена на α-углерод аспарагиновой кислоты дает более сильное сродство к целевому интегрину. Сульфокислоты в RGC-пептидах являются более сильными кислотами, чем соответствующие карбоновые кислоты в RGD-пептидах. Такая повышенная полярность группы сульфокислоты приводит к усилению межмолекулярных связей. Например, RG-Цистеиновая кислота, которая имеет более поляризованную О-Н связь, может образовывать более сильные водородные связи, чем RG-Аспарагиновая кислота, которая обладает относительно менее поляризованной О-Н связью, с амидными группами и/или аминокислотами боковых цепей в интегриновом сайте связывания и/или сильнее взаимодействует с ионами металлов в составе интегринового сайта связывания.
Наиболее общими формулами последовательностей RGCys-овой кислоты по настоящему изобретению являются следующие:
Формула А:
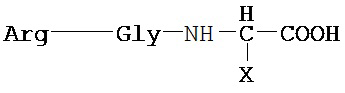
где Х=-CH(R1)-S(=O)2-Y;
-CH(R1)-SH;
-CH(R1)-OZ;
-CH(R1)S(=O)Y;
-CH(R1)-O-S(=O)2-OX1 и
-CH(R1)-O-P(=O)2-OX1;
где Y=OX1, NH2; X1=-H, C1-С6 линейный алкил, фенил;
R1=H, C1-С6 линейный алкил, фенил или SO3H;
Z=Н, SO3H.
Формула В:
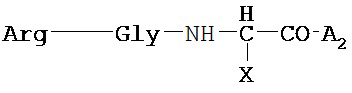
где X=-CH(R1)-S(=O)2-Y;
-CH(R1)-SH;
-CH(R1)-OZ;
-CH(R1)S(=O)Y;
-CH(R1)-O-S(=O)2-OX1 и
-CH(R1)-O-P(=O)2-OX1; где Y=OX1, NH2; X1=-H, C1-С6 линейный алкил, фенил;
R1=H, C1-С6 линейный алкил, фенил или SO3H;
Z=Н, SO3H и
А2 выбран из: -Phe-Val-Ala, -Phe-Leu-Ala, -Phe-Val-Gly, -Phe-Leu-Gly, -Phe-Pro-Gly, -Phe-Pro-Ala, -Phe-Val или их соли или N-алкилированного производного. Также может быть использована любая комбинация D-формы или L-формы Arg, Gly, Cys, Phe, Val, Ala, Leu, Pro, Thr, также как и циклические формы, представленные ниже.
Примеры циклических форм включают:
Формула С:
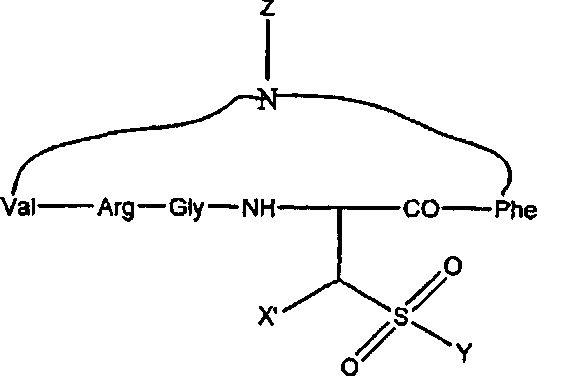
где X' выбран из: Н, C1-C6 алкила, Ph, SO3H; Y=ОН, NH2 и Z=Н, СН3.
Циклические формы также включают пента- и гептапептиды, такие как, например, конкретное соединение Общей формулы С, а именно Соединение 2 (Цикло-RGCys-овая кислота fN(СН3)V), представленная ниже:
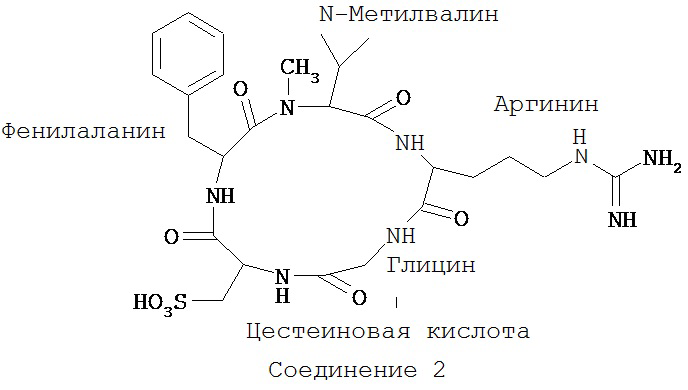
Формула А охватывает Общие формулы I-VI, описанные здесь. Формула В включает Общую формулу VII, описанную здесь. Формула D:
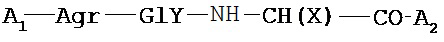
где X=-CH(R1)-S(=O)2-Y;
-CH(R1)-SH;
-CH(R1)-OZ;
CH(R1)S(=O)Y;
-CH(R1)-O-S(=O)2-OX1 и
-CH(R1)-O-P(=O)2-OX1;
где Y=OX1, NH2; X1=-H, C1-С6 линейный алкил, фенил;
R1=H, C1-С6 линейный алкил, фенил или SO3H
Z=Н, SO3H и
A1 и А2 выбраны из: -Phe-Val-Ala, -Phe-Leu-Ala, -Phe-Val-Gly, -Phe- Leu-Gly, -Phe-Pro-Gly, -Phe-Pro-Ala, -Phe-Val или их соли или N-алкилированного производного. Также может быть использована любая комбинация D-формы или L-формы Arg, Gly, Cys, Phe, Val, Ala, Leu, Pro, Thr, также как и циклические формы, представленные ниже.
Замещенные последовательности RGCys-овой кислоты включают аналоги циклической RGCys-овой кислоты.
RGCys-овая кислота и ее производные могут применяться подкожно, дерматологически, офтальмологически и системно, с использованием системы доставки лекарств или любых фармацевтически приемлемых форм дозирования инъекций, либо твердых препаратов или мазей.
Соединения по настоящему изобретению могут быть введены любым способом, который подходит для обеспечения предполагаемого терапевтического эффекта, включая, но не ограничиваясь этим: пероральный, ректальный, внутривенный, внутриартериальный, внутрикожный, подкожный, внутримышечный, интратекальный, подъязычный, щечной, интраназальный, чресслизистый, трансдермальный, местный, внутриглазной, интравитреальный, другие энтеральные, другие парентеральные и/или другой(-ие) возможный(-ые) путь(-и) введения.
Соединения по настоящему изобретению могут быть введены в любой дозе, которая обеспечивает предполагаемый терапевтический эффект, избегая неблагоприятных или токсических эффектов. Обычная доза, при которой могут быть введены соединения по настоящему изобретению, для человека находятся в диапазоне примерно от 1 нг/кг до 1,0 г/кг.
Там, где это возможно и целесообразно, соединения по настоящему изобретению необязательно могут быть подготовлены в форме липосом или наночастиц (например, нанокапсул). Формирование и использование липосом, в общем, известно специалистам в данной области. Липосомы образуются из фосфолипидов, диспергированных в водной среде так, что они самопроизвольно образуют многослойные концентрические двухслойные везикулы, иногда называемые многослойными везикулами (MLV). MLV, как правило, имеют диаметр от 25 нм до 4 мкм. При использовании ультразвука MLV формируют небольшие однослойные везикулы (SUV) примерно от 200 до 500 ангстрем в диаметре, ядра которых содержат водный раствор. В общем, при распылении в водной среде фосфолипиды могут образовывать различные структуры помимо липосом, в зависимости от молярного соотношения липидов к воде. При низком молярном соотношении липидов к воде образуют липосомы. Физические характеристики липосом зависит от рН, тоничности и наличия или отсутствия двухвалентных катионов. Липосомы могут взаимодействовать с клетками с помощью различных механизмов, в том числе 1) эндоцитоза (например, фагоцитоз липосом клетками, такими как макрофаги и нейтрофилы), адсорбции на поверхности клетки, 2) взаимодействие с компонентами клеточной поверхности, 3) слияние с плазматической клеточной мембраной путем включения липосом в липидный бислой в мембране или 4) передача липосомальных липидов клеточной или субклеточной мембране, или наоборот. Возможны вариации липосомальных препаратов в зависимости от того, каков механизм(ы) взаимодействия липосом с клетками в придаточных пазухах носа, слизистой оболочки носа, и т.д.
Нанокапсула представляет собой наночастицу, которая состоит из корпуса и пространства, в котором могут быть размещены желаемые вещества. Методы формирования нанокапсул известны в уровне техники. Можно получить полимерные нанокапсулы конкретных размеров и форм. Они могут быть изготовлены как монодисперсные частицы, которые имеют определенные физические и химические свойства и, таким образом, могут быть адаптированы для облегчения высвобождения терапевтических или диагностических веществ в ответ на конкретные бимолекулярные целевые механизмы, такие как рН, количество жидкости слизистой или других условий в придаточных носовых пазухах или в другой области уха, носа или горла, где они высвобождаются. Нанокапсулы могут быть использованы в настоящем изобретении как «умные лекарственные средства», которые имеют специфические химические рецепторы или сайты связывания, которые будут связываться со специфическими клетками-мишенями (например, раковыми клетками или клетками, связанных с воспалительными условиями).
Ниже приведены неограничивающие примеры лекарственных средств для фармацевтических препаратов, содержащие соединения по настоящему изобретению. Также включены примеры по безопасности и/или эффективности, показанные при использовании примерного RGC-пептида или производные в ингибировании клеточной адгезии. Используемые здесь термины "RGCys-овый пептид", "RGC-пептид", "RGCys-пептид" и "соединения по настоящему изобретению" должны восприниматься как синонимы композиций, содержащих последовательности RGCys-овой кислоты и их производных, в том числе, но не ограничиваясь, тех, которые определены Общими формулами I-VII и Соединениями 1 и 3-5, как описано здесь.
Пример 1. Фармацевтические композиции
Ниже приведены примеры фармацевтических препаратов I-Х, которые содержат пептиды RGC-овой кислоты по настоящему изобретению, такие как любой из тех, которые определены Общими формулами I-VII, или любое Соединение 1-5, как описано здесь.
Препарат I
Пептид RGCys-овой кислоты (RGCys-пептид) от 0,0001 мг до 10 г
Препарат II
Препарат III
Препарат IV
Препарат V
Препарат VI
Препарат VII
Консервант
Препарат VIII
Консервант
Препарат IX
Консервант
Препарат X
Консервант
Пример 2. Сравнение PVD-индуцированных эффектов RGD-пептидов и Глицил-Аргинил-Глицил-Цистеин-Треонил-Пролин-СООН (GRG-Цистеиновая кислота ТП; Соединение 1) на кроликах
В этом примере эффекты PVD-индицирования RGD-пептидами и Глицил-Аргинил-Глицил-Цистеин-Треонил-Пролин-СООН (пептид RGCys-овой кислоты; GRG Cys-овая кислота TP; Соединение 1) сравнивались на кроликах. Протокол этого исследования был следующим:
Протокол:
Модель-животное
a) 20 самцов и самок кроликов
b) весом примерно 1,5-2,5 кг
c) разделены на 2 группы
i) 10 кроликам интравитреально вводили 2,5% RGD-раствор с рН=6,5
a) в 10 правых глаз вводили 2,5% RGD-раствор
b) в 5 левых глаз использовались как BSS-контроль
c) в 5 левых глаз вводили 2,5% RGD + 0,02% ЭДТА с рН=6,5
ii) 10 кроликам интравитреально вводили 2,5% RGCys-овый раствор с рН=6,5
a) в 10 правых глаз вводили 2,5% RGCys-овый раствор с рН=6,5
b) в 10 левых глаз вводили 2,5% RGCys-овый раствор + 0,02% ЭДТА с рН=6,5
Активные реагенты
d) Натрия ЭДТА - 99,0-100,5% от Spectrum Chemical Corp.
e) RGCys-овая кислота - cGMP от поставщика (чистота >98%).
f) RGD - cGMP от поставщика (чистота >98%).
g) BSS-раствор
И RGCys-овая кислота, RGD, RGCys-овая кислота + натрия ЭДТА, RGD+натрия ЭДТА, и BSS-раствор вводили в полость стекловидного тела за 24 часа до препарирования. Кролики (10 мг/кг массы тела) подвергались анестезии с помощью внутримышечной инъекции 2,0 мл 1:1 ксилазина (100 мг/мл) и кетамина гидрохлорида (100 мг/мл). Зрачки расширялись с помощью местного введения циклопенталата гидрохлорида 1% и фенилэфрина гидрохлорида 10%.
Все животные были первоначально осмотрены с помощью биомикроскопии с использованием щелевой лампы и непрямой офтальмоскопии для того, чтобы исключить всех животных, у которых уже имеются витреоретинальные нарушения. Интравитреальные инъекций 0,10 см3 вводились на 2 мм сзади от края роговицы в верхнем носовом квадранте с использованием 30-мерной иглы и 1,0 см3 шприца. Были приняты меры по избеганию повреждения линзы или сетчатки.
Двадцать четыре часа после инъекции и непосредственно перед началом механической витрэктомии было проведено ультразвуковое В-сканирование с целью определения состояния задней поверхности стекловидного тела, а также степени разжижения стекловидного тела. Двухпортовую витрэктомию pars plana проводили с использованием инфузионного волоконно-оптического световода и ножа для стекловидного тела, соединенного с витреотомом. Через 30 секунд коровой витрэктомии нож для стекловидного тела направляется на перипапиллярную поверхность сетчатки, где с использованием низкочастотных аспирации (<30 ммГц) проводят разделение задней коровой поверхности стекловидного тела от поверхности сетчатки в 4 квадрантах. Были пересажены склеротомы и проведено послеоперационное ультразвуковое В-сканирование с целью определения наличия и степени любого присутствующего PVD в каждом секторе. Животных усыпляли с помощью внутрисердечной инъекции натрия фенобарбитала, а глаза были немедленно инокулированы.
Классификация по разжижению стекловидного тела и PVD для оценки степени PVD проведена на основе послеоперационного ультразвукового В-сканирования:
Степень 0. а) отслоение задней поверхности стекловидного тела не наблюдается.
б) разжижение стекловидного тела
Степень 1. а) стекловидное тело отслаивается в 2 или менее квадрантах.
б) разжижение стекловидного тела
Степень 2. а) стекловидное тело отслаивается в 3 или более квадрантах, но с сохранением фокального соединения вдоль медуллярных лучей
б) разжижение стекловидного тела
Степень 3. а) стекловидное тело полностью отслаивается от поверхности сетчатки
б) разжижение стекловидного тела
Все глаза прорезались острой бритвой в верхнем полюсе, прилегающем к гладкой части ресничного тела, непосредственно после инокулирования для обеспечения быстрого проникновения фиксатором. Были приняты меры по избежанию повреждения прилегающих сетчатки и хрусталика. Глаза были погружены в 2% параформальдегид плюс 2,5% глутаральдегид в течение как минимум 24 часов при температуре 4 градуса Цельсия. Один задний сегмент был удален, дегидратирован в метаноле и высушен в углекислом газе до критической точки, покрыт напылением золота и отснят с помощью сканирующего электронного микроскопа.
Результаты:
Инъекция: 2,5% RGCys-овой кислоты
Группа 1. Исходно все животные не имели PVD в обоих глазах
Группа 2. Исходно все животные не имели PVD в обоих глазах
Группа 3. Исходно все животные не имели PVD в обоих глазах
е тело отслоилось в 2 или менее Q
Группа 4. Исходно все животные не имели PVD в обоих глазах
Результаты кинетического анализа в Примере 4 настоящего исследования показывают, что RGD и RGCys-овая кислота (GRG-Цистеиновая кислота TP; Соединение 1) имеют аналогичные свойства, а инъекции 2,5% RGCys-овой кислоты интравитреально вызывает полное отделение стекловидного тела от сетчатки в течение 24 часов, и добавление к стекловидному телу RGD и RGCys-овой кислоты у кроликов полностью в разжижает его.
В целом, активность RGCys-овой кислоты эквивалентна или чуть лучше, чем RGD при стимулировании полного PVD у кроликов и разжижении стекловидного тела. Возможно, это связано с его сильной конкурирующей связывающей способностью к сайтам связывания интегрина при его взаимодействии с внеклеточным матриксом, чем RGD. Как описано в данной работе, сульфокислоты являются более сильными кислотами, чем соответствующие карбоновые кислоты.
Такая высокая полярность группы сульфокислоты приводит к усилению межмолекулярных связей. Например, RG-Цистеиновая кислота, которая имеет более поляризованные О-Н связи, может образовывать более сильные водородные связи, чем RG-Аспарагиновой кислоты, которая обладает относительно менее поляризованными О-Н связями, с амидными группами и/или аминокислотами боковых цепей в интегриновом сайте связывания и/или сильнее взаимодействует с ионами металлов в составе интегринового сайта связывания. Результаты также показывают, что при введении соединения с 0,02% натрия эдетатом, активность ни RGD, ни RGCys-овой кислоты не изменяется.
Результаты также показывают, что нет никаких побочных эффектов при интравитреальном введении соединений RGCys-овой кислоты Соединения 1 или RGD-соединения.
Пример 3. Исследование безопасности множественных инъекций RGC-пептида Соединения 1 (GRG-Цистеиновой кислоты TP) в глаз кролика
В этом примере в глаза 5 самцов и 4 самок Новозеландских кроликов весом примерно 1,5-2,5 кг вводили множественные инъекции RGC-пептида Соединения 1, и глаза были протестированы так, как описано в следующих параграфах.
Протокол исследования был следующим:
А) Исходное состояние: В начале исследования правые и левые глаза всех 9 кроликов были обследованы путем биомикроскопии с помощью щелевой лампы и офтальмоскопии для подтверждения того, что животные исходно не имеют витреоретинальных нарушений. Кроме того, проводились ультразвуковое В-сканирование, а также ERG-сканирование на левых и правых глазах всех 9 животных для получения базовых значений.
Б) Экспериментальное лечение: затем все 9 кроликов получили интравитреальные инъекции либо RGC-раствора, либо физиологического раствора (контроль). Растворы для лечения были подготовлены следующим образом:
RGC-раствор: 2,5 мг / 100 мкл раствора RGC Соединения 1, содержащего 0,02 мг динатрия ЭДТА + 0,80 мг хлорида натрия и USP стерильной воды для инъекций с рН 6,5.
Физиологический раствор (контроль): USP изотонический стерильный физиологический раствор, имеющий скорректированный рН 6,5.
Режим дозирования был следующим:
1) В правый глаз каждого из 9 кроликов вводили интравитреально 100 2,5 мг / 100 мкл RGC-раствора (общая введенная доза Соединения 1=2,5 мг).
2) В левый глаз каждого из 9 кроликов вводили интравитреально 100 мкл физиологического раствора (контроль).
3) На следующий день после начальных интравитреальных инъекций правые и левые глаза всех 9 кроликов были осмотрены путем биомикроскопии с использованием щелевой лампы и непрямой офтальмоскопии для оценки побочных эффектов инъекции.
4) На 7-й день после 1ой инъекции правые и левые глаза всех 9 кроликов вновь осматривали путем биомикроскопии с использованием щелевой лампы и непрямой офтальмоскопии для оценки побочных эффектов инъекции. Кроме того, проводилось ERG-сканирование правых и левых глаз всех животных для определения изменений по отношению к исходному состоянию.
5) У группы из 3 кроликов под номерами 901, 904 и 909, выбранных случайным образом, проводилась механическая витрэктомия на правых и левых глазах этих трех выбранных животных для определения состояния задней поверхности стекловидного тела.
6) Три случайно выбранных животных под номерами 901, 904 и 909 были подвергнуты эвтаназии с помощью внутрисердечной инъекции натрия фенобарбитала, и немедленно извлекали глаза. Все глаза подвергались прорезанию острой бритвой верхнем полюсе, прилегающем к гладкой части ресничного тела, непосредственно после извлечения для обеспечения быстрого проникновения фиксатором. Были приняты меры по избежанию повреждения прилегающих сетчатки и хрусталика. Глаза были погружены в 2% параформальдегида плюс 2,5% глютаральдегида в течение как минимум 24 часов при температуре 4 градуса Цельсия. Один задний сегмент был удален, обезвожен в метаноле и высушен в углекислом газе до критической точки, покрыт напылением из золота и отснят с помощью сканирующего электронного микроскопа. Другие образцы были подвергнуты гистопатологическому анализу.
Остальным 6 кроликам под номерами 902, 903, 905, 906, 907 и 908 ввели вторую инъекцию через 7 дней после первой инъекции.
1) В правый глаз каждого из 6 оставшихся кроликов вновь вводили интравитреально 100 2,5 мг / 100 мкл RGC-раствора (общая введенная вторая доза Соединения 1=2,5 мг).
2) В левый глаз каждого из 6 оставшихся кроликов вновь вводили интравитреально ЮОмкл физиологического раствора (контроль).
3) На следующий день после 2ой интравитреальной инъекции правые и левые глаза всех 6 оставшихся кроликов были вновь осмотрены путем биомикроскопии с использованием щелевой лампы и непрямой офтальмоскопии для оценки побочных эффектов инъекции.
4) На 7-й день после 2ой инъекции извлеченные правые и левые глаза всех 6 кроликов были осмотрены путем биомикроскопии с использованием щелевой лампы и непрямой офтальмоскопия для оценки наличие побочных эффектов от инъекций. Кроме того, было проведено ERG-сканирование левых и правых глаз всех животных для определения наличия изменений относительно исходного состояния.
5) Три кролика под номерами 902, 903 и 907, выбранных случайным образом из оставшихся 6 животных, подвергались витрэктомии на правых и левых глазах для определения состояния задней поверхности стекловидного тела.
6) Три случайно выбранных животных под номерами 902, 903, и 907 затем были умерщвлены с помощью внутрисердечной инъекции натрия фенобарбитала, и были немедленно извлечены глаза. Все глаза прорезались острой бритвой в верхнем полюсе, прилегающем к гладкой части ресничного тела, непосредственно после извлечения для обеспечения быстрого проникновения фиксатором. Были приняты меры по избежанию повреждения прилегающих сетчатки и хрусталика. Глаза погружались в раствор 2% параформальдегида плюс 2,5% глутаральдегида в течение как минимум 24 часов при температуре 4 градуса Цельсия. Один задний сегмент был удален, обезвожен в метаноле и высушен в углекислом газе до критической точки, покрыт напылением из золота и сфотографирован с помощью сканирующего электронного микроскопа. Другие образцы были подвергнуты гистопатологической экспертизе.
Оставшейся группе из 3 кроликов под номерами 905, 906, и 908 была затем введена третья инъекция, через 14 дней после первой инъекции, а именно:
1) в правый глаз каждого из 3 оставшихся кроликов был вновь введен интравитреально 100 2,5 мг / 100 мкл RGC-раствора (общая введенная доза 2,5 мг Соединения 1).
2) в левый глаз каждого из 3 оставшихся кроликов было вновь введено интравитреально 100 мкл физиологического раствора (контроль).
3) На следующий день после 3ей интравитреальной инъекции правые и левые глаза всех 6 оставшихся кроликов были осмотрены путем биомикроскопии с использованием щелевой лампы и непрямой офтальмоскопии для проверки наличия побочных эффектов от инъекции.
4) На 7-й день после 3ей инъекции правые и левые глаза всех 3 оставшихся кроликов были осмотрены путем биомикроскопия с использованием щелевой лампы и непрямой офтальмоскопии для проверки наличия побочных эффектов от инъекции. Кроме того, было проведено ERG-сканирование левых и правых глаз всех животных для проверки наличия изменения по сравнению с исходным состоянием.
5) Проводилась механическая витрэктомии на правых и левых глазах 3 оставшихся животных (под номерами 905, 906 и 908) для определения состояния задней поверхности стекловидного тела.
6) Три оставшихся животных (под номерами 905, 906 и 908) были подвергнуты эвтаназии с помощью внутрисердечной инъекции натрия фенобарбитала, и были немедленно извлечены глаза. Все глаза прорезались острой бритвой в верхнем полюсе, прилегающем к гладкой части ресничного тела, непосредственно после извлечения для обеспечения быстрого проникновения фиксатором. Были приняты меры по избежанию повреждения прилегающих сетчатки и хрусталика. Глаза погружались в раствор 2% параформальдегида плюс 2,5% глутаральдегида в течение как минимум 24 часов при температуре 4 градуса Цельсия. Один задний сегмент был удален, обезвожен в метаноле и высушен в углекислом газе до критической точки, покрыт напылением из золота и отснят с помощью сканирующего электронного микроскопа. Другие образцы были подвергнуты гистопатологической экспертизе.
3) Активные реагенты
Активные химические реагенты, используемые в этом исследовании, были следующими:
а. Динатрия ЭДТА - 99,0-100,5% от Spectrum Chemical Corp.
б. RGC-пептид (Соединение 1).
в. USP стерильный изотонический физиологический раствор.
4) Исследуемые препараты
а) RGC-раствор: 2,5 мг / 100 мкл раствора RGC, содержащий 0,02 мг динатрия ЭДТА + 0,80 мг хлорида натрия и USP стерильной воды для инъекций, доведенный до рН 6,5. Стерильный фильтр 0,22 μ в пробирке 2,0 мл.
б) Физиологический раствор (контроль): USP изотонический стерильный физиологический раствор, доведенный до рН 6,5. Профильтрованный через стерильный фильтр 0,22 μ фильтр в стерильную пробирку.
5) Анестезия для инъекций препарата.
а. Внутримышечные инъекции 2,0 мл 1:1 ксилазина (100 мг/мл) и кетамина гидрохлорид (100 мг/мл).
б. Зрачки расширялись с помощью местного применения циклопентотал гидрохлорида 1% и фенилэфрина гидрохлорида 10%.
6) Подготовка интравинтральных инъекций:
Стерильный флакон с RGC-раствором, содержащим 2,5 мг / 100 пл и изотонический стерильный физиологический раствор, доведенный до рН 6,5.
Перед введением исследователь удостоверяется в том, что в шприце на 1,0 см3 содержится 0,10 см3 (100 микролитров) раствора.
7) Процедура инъекций:
До тех пор пока интравитреальные инъекции не приведут к такому уровню расстройства зрения, при котором нарушается нормальная повседневная активность кроликов, влияние инъекции считается недействительным, согласно решению по животным руководства Ассоциации исследований в области зрения и офтальмологии.
И RGC-раствор, и стерильные физиологические растворы вводили в полость стекловидного тела после завершения начального обследования кроликов путем биомикроскопии с использованием щелевой лампы, офтальмоскопии и ERG. Кролики (10 мг/кг массы тела) были анестезированы внутримышечной инъекцией 2,0 мл 1:1 раствора ксилазина (100 мг/мл) и кетамина гидрохлорида (100 мг/мл). Зрачки были расширены местным введением циклопентотала гидрохлорида 1% и фенилэфрина гидрохлорида 10%.
Все животные были изначально осмотрены путем биомикроскопии с использованием щелевой лампы и непрямой офтальмоскопии для того, чтобы исключить тех животные, у которых уже имеются витреоретинальные нарушения. Интравитреальные инъекций 0,10 см3 вводились на 2 мм сзади от края роговицы в верхнем носовом квадранте с использованием 30-мерной иглы и 1,0 см3 шприца. Были приняты меры по избежанию повреждения линзы или сетчатки.
Через семь дней после инъекции на животных осуществляли механическую витрэктомию. Двухпортовую витрэктомию pars plana проводили с использованием инфузионного волоконно-оптического световода и ножа для стекловидного тела, соединенного с витреотомом. Через 30 секунд коровой витрэктомии нож для стекловидного тела направляется на перипапиллярную поверхность сетчатки, где с использованием низкочастотных аспирации (<30 ммГц) проводят разделение задней коровой поверхности стекловидного тела от поверхности сетчатки в 4 квадрантах. Животных усыпляли с помощью внутрисердечной инъекции натрия фенобарбитала, и немедленно извлекали глаза.
Все глаза прорезались острой бритвой в верхнем по люсе, прилегающем к гладкой части ресничного тела, непосредственно после извлечения для обеспечения быстрого проникновения фиксатором. Были приняты меры по избежанию повреждения прилегающих сетчатки и хрусталика. Глаза погружались в раствор 2% параформальдегида плюс 2,5% глутаральдегида в течение как минимум 24 часов при температуре 4 градуса Цельсия. Один задний сегмент был удален, обезвожен в метаноле и высушен в углекислом газе до критической точки, покрыт напылением из золота и отснят сканирующим электронным микроскопом.
Анализ результатов
Данные о безопасности препаратов между глазами, обработанными RGC-раствором и стерильным физиологическим раствором, анализировали с помощью следующих методов:
i) биомикроскопии с использованием щелевой лампы;
ii) офтальмоскопии;
iii) ERG;
iv) гистопатологии и
v) электронной микроскопии.
Безопасность профиля:
Первое интравитреальное введение 100 мкл 2,5% RGC-раствора группе из девяти кроликов под номерами 901, 902, 903, 904, 905, 906, 907, 908, 909 не вызвало никаких значительных проявлений токсичности на протяжении всего времени. Не было никаких существенных различий в побочных эффектах между группами, получавшими 2,5% RGC-раствор и изотонический физиологический раствор. Отсутствие токсичности было определено при клиническом обследовании, непрямой офтальмоскопии и ультразвуковом В-сканировании, а также механической витрэктомии.
Биомикроскопия с использованием щелевой лампы была проведена так, как описано в литературе, на веках, конъюнктиве и склере, роговице, эндотелиальных изменениях, передне-камерной реакции, радужной оболочки, хрусталике и капсуле, а также передней поверхности стекловидного тела для обнаружения признаков воспаления, и показала почти полное отсутствие воспалительных реакции при интравитреальных инъекциях 100 мкл 2,5% RGC-раствора и изотонического физиологического раствора. Для всех изученных значений и во всех исследуемых группах не наблюдалось никаких признаков существенной токсичности, индуцированной тестируемым образцом.
На протяжении всего исследования также проводилась клиническая оценка заднего сегмента для того, чтобы удостоверится в отсутствии существенных проявлений токсичности для сетчатки. Непрямая офтальмоскопия, а также микроскопия щелевой лампой для оценки дна были проведены в каждый момент времени исследования, уделяя особое внимание проявлению любых признаков токсичности для сетчатки. Задний сегмент оценивался на любые изменения в плотности стекловидного тела, на разжижение стекловидного тела, прикрепления стекловидного тела и возможность кровотечения. Сетчатку оценивали на предмет токсичности для ретинального пигментного эпителия, сосудов сетчатки с возможностью кровоизлияния в сетчатку глаза, экссудаты, разрывов или отслоения сетчатки. Изменения в ретинальном пигментном эпителии относительно исходного состояния не наблюдались, для всех исследуемых значений и во всех исследуемых группах не было зафиксировано никаких признаков значительных изменений задних сегментов, индуцированных тестируемым образцом. Важно отметить, что ERG-сканирование, которое было проведено на девяти животных до интравитреальных инъекций, а также ERG-сканирование, которое было проведено на всех животных на 1 день и 7 день после инъекции, не показало никаких признаков существенных изменений или токсичности, индуцированных тестируемым образцом.
Второе интравитреальное введение 100 мкл 2,5% RGC-раствора группе из шести кроликов под номерами 902, 903, 905, 906, 907, 908 не повлияло на появление токсичности за все время исследования. Не выявлено никаких существенных различий в побочных эффектах между группами, получавшими 2,5% RGC-раствор и изотонический физиологический раствор. Отсутствие токсичности определялось при клиническом обследовании, непрямой офтальмоскопии и ультразвуковом В-сканирование, а также механической витрэктомии.
Биомикроскопия с использованием щелевой лампы была проведена так, как описано в литературе, и была сфокусирована на веках, конъюнктиве и склере, роговице, эндотелиальных изменениях, передне-камерной реакции, радужной оболочки, хрусталике и капсуле, а также передней поверхности стекловидного тела для обнаружения признаков воспаления, и показала почти полное отсутствие воспалительных реакции при интравитреальных инъекциях 100 мкл 2,5% RGC-раствора и изотонического физиологического раствора. Для всех изученных значений и во всех исследуемых группах не наблюдалось никаких признаков существенной токсичности, индуцированной тестируемым образцом.
На протяжении всего исследования также проводилась клиническая оценка заднего сегмента для того, чтобы удостоверится, что нет никаких существенных проявлений токсичности для сетчатки. Непрямая офтальмоскопия, а также микроскопия щелевой лампой для оценки дна были проведены в каждый момент времени исследования, уделяя особое внимание проявлению любых признаков токсичности для сетчатки. Задний сегмент оценивался на изменения в плотности стекловидного тела, разжижение стекловидного тела, соединение стекловидного тела и возможность кровотечения. Сетчатку оценивали на предмет токсичности для ретинального пигментного эпителия, сосудов сетчатки с возможностью кровоизлияния в сетчатку глаза, экссудаты, разрывов или отслоения сетчатки. Изменения в ретинальном пигментном эпителии относительно исходного состояния за 7 дней до повторного лечения не наблюдались, для всех исследуемых значений и во всех исследуемых группах не было зафиксировано никаких признаков значительных изменений задних сегментов, индуцированных тестируемым образцом. Важно отметить, что ERG-сканирование, которое было проведено на шести животных во второй раз после интравитреальных инъекций, а также ERG-сканирование, которое было проведено на всех животных на 8 день и 14 день после инъекции, не показало никаких признаков существенных изменений или токсичности, индуцированных тестируемым образцом.
Третье интравитреальное введение 100 мкл 2,5% RGC-раствора группе из трех кроликов под номерами 905, 906, 908 не повлияло на появление токсичности за все время исследования. Не выявлено никаких существенных различий в побочных эффектах между группами, получавшими 2,5% RGC-раствор и изотонический физиологический раствор. Отсутствие токсичности определялось при клиническом обследовании, непрямой офтальмоскопии и ультразвуковом В-сканирование, а также механической витрэктомии.
Биомикроскопия с использованием щелевой лампы была проведена так, как описано в литературе, и была сфокусирована на веках, конъюнктиве и склере, роговице, эндотелиальных изменениях, передне-камерной реакции, радужной оболочки, хрусталике и капсуле, а также передней поверхности стекловидного тела для обнаружения признаков воспаления, и показала почти полное отсутствие воспалительных реакции при интравитреальных инъекциях 100 мкл 2,5% RGC-раствора и изотонического физиологического раствора. Для всех изученных значений и во всех исследуемых группах не наблюдалось никаких признаков существенной токсичности, индуцированной тестируемым образцом.
На протяжении всего исследования также проводилась клиническая оценка заднего сегмента для того, чтобы удостоверится в отсутствии существенных проявлений токсичности для сетчатки. Непрямая офтальмоскопия, а также микроскопия щелевой лампой для оценки дна проводились в каждый момент времени исследования, уделяя особое внимание проявлению любых признаков токсичности для сетчатки. Задний сегмент оценивался на любые изменения в плотности стекловидного тела, разжижение стекловидного тела, соединение стекловидного тела и возможность кровотечения. Сетчатку оценивали на предмет токсичности для ретинального пигментного эпителия, сосудов сетчатки с возможностью кровоизлияния в сетчатку глаза, экссудаты, разрывов или отслоения сетчатки. Изменения в ретинальном пигментном эпителии относительно исходного состояния за 14 дней до третьего лечения не наблюдались, для всех исследуемых значений и во всех исследуемых группах не было зафиксировано никаких признаков значительных изменений задних сегментов, индуцированных тестируемым образцом. Важно отметить, что ERG-сканирование, которое было проведено на шести животных в третий раз после интравитреальных инъекций, а также ERG-сканирование, которое было проведено на всех животных на 15 день и 21 день после инъекции, не показало никаких признаков существенных изменений или токсичности, индуцированные тестируемым образцом.
Пример 4. Противоадгезионные свойства RGC-пептидов: кинетические исследования заживления ран с помощью Соединения 1 (GRG-Цистеиновой кислоты ТП), циклического RGD и RGE
В этом примере в модели заживления ран было продемонстрировано, что RGC-пептиды обладают противовоспалительными адгезионными свойствами и, следовательно, могут предотвратить развитие многих патологических витреоретинальных заболеваний и подавлять метастазы меланомы и раковых клеток толстой кишки у человека.
Для тестирования антиадгезионных свойств RGC-пептидов in vitro был проведен ранозаживляющим анализ с использованием эндотелиальных клеток пупочной вены человека (HUVEC). HUVEC были посеяны и выращены до образования плотного монослоя на поверхности, покрытой фибронектином. Раны (царапины) были сделаны путем протаскивания кончика пипетки по монослою HUVEC. Затем клетки инкубировали в свежей питательной среде, содержащей пептид RGC (Соединение 1, 10 мМ), а области ран сфотографированы в пяти различных областях в различные моменты времени (0, 4, 8, 12, 16, 20, 24 часов) для определения кинетики закрытия раны. Уровень закрытия раны был количественно определен по отношению к первоначальной площади раны, которые вновь занимались HUVEC путем клеточной адгезии, миграции и пролиферации.
В контрольных исследованиях вместо RGC (Соединение 1) были использованы следующие пептиды: циклический RGD-пептид (1 мМ, положительный контроль) и RGE-пептид (1 мМ, отрицательный контроль).
Влияние пептидов на кинетику заживления ран представлено на рисунке 1.
Результаты приведены в процентах от первоначальной площади. Уровни погрешностей соответствуют стандартному отклонению размера раны в 2-6 независимых испытаний.
Результаты кинетики HUVEC закрытия раны показывают, что RGC-пептид ингибирует заживление ран HUVEC на 70% после 24 часов, в то время как циклический RGD (пептид на основе RGD, N-метилированный циклический RGDf-N(Me)V; Циленгитид) ингибирует заживление ран HUVEC на 45% после 24 часов. Они оба сравнивались с отрицательным контролем пептида RGE, который препятствует заживлению ран HUVEC 0% через 24 часа. Эффекты RGC (Соединение 1) количественно сопоставимы с активностью пептидов на основе RGD, общепризнанного ингибитора интегрин-связывающей активности. Кроме того, RGC-пептид проявляет сходные свойства с активностью пептида на основе RGD, не вызывая апоптоз клеток HUVEC.
Как описано в данной работе, сильной адгезией между стекловидным телом и сетчаткой можно объяснить возможное развитие многих патологических витреоретинальной заболеваний, таких как витреомакулярный тракционный синдром, пролиферативная диабетическая ретинопатия, макулярный разрыв, возрастная макулярная дегенерация и плавающие тельца. Таким образом, весьма желателен атравматической неинвазивный подход по достижению задней поверхности стекловидного тела, помимо механического отделения стекловидного тела от внутренней поверхности сетчатки (см. Tezel, Т.Н. и др., Retina (1998) 18: 7-15; и Verstraeten, T.С. и др., Arch. Ophthalmol. (1993) 111: 849-854).
Как описано в настоящем документе, считается, что компоненты ВКМ, в частности коллагеновые фибриллы кортикального слоя стекловидного тела прикрепляются к внутренней поверхности сетчатки за счет интегриновых сайтов связывания (см. Foos, R.Y., Invest. Ophthalmol. Vis. Sci. (1972) 11: 801-808) во внутренней пограничной ламелле (ВПЛ). Известно также, что основные адгезивные гликопротеины ВПЛ в глазах, такие как фибронектин и ламилин, крепко связаны с интегринами (см. Cutis, Т.М. и др., Am. J. Physiol. (1995) 269: L248-L260; Elner, S.C. и др., IOVS (1996) 37: 696-701; и Horman, S.M. и др., Am. J. Physiol. (1995) 269. L248-L260) через последовательности RGD (Arg-Gly-Asp), а некоторые интегрины связывают RGD мотив, присутствующий у белков ВКМ. Кроме того, известно, что фибронектин связывается с некоторыми другими интегринами помимо ανβ3, в то время как витронектин является ανβ3-специфичным.
Основное соединение интегринов с ВКМ включает последовательность Arg-Gly-Asp (RGD), где последовательность RGD связывается в небольшой расщелине, расположенной между α- и β-субъединицами на вершине интегрина (см. Xiong и др., Science (2002) 296: 151-155). Такая связь позволяет модулировать различные сигнальные пути клетки, в том числе клеточную адгезию, миграцию, дифференциацию, ангиогенез и заживление ран (см. Ruoslahti Е., и др., Science (1987) 238. 491-497; и J. Clin. Invest. (1991) 87: 1-5).
Поскольку внеклеточный матрикс стекловидного тела, в частности фибриллы коллагена, соединены через интегриновые сайты связывания с клеточной сетчаткой, интравитреальные инъекции RGC-пептидов (олигопептидов) могут работать как RGD мотив внеклеточного матрикса стекловидного тела и клеточной сетчатки путем конкурентного связывания с теми же интегриновыми рецепторными сайтами.
Некоторые исследователи (см. Ruoslahti, Е. и др., Science (987) 238: 491-497; Hynes, R.A., и др., Cell (1992) 68: 303-322, и Humphries, M.J., J. Cell Sci. (1990) 97: 585-592) показали, что многие интегрины (ανβ3, α5β1, α11β3 и др.) могут ингибироваться небольшими пептидами, которые обладают последовательностями RGD мотива. Также хорошо описано, что ανβ3 и α5β1 интегрины, также как и витронектин и фибронектин, проявляют чрезмерную активность в опухолях, таких как клетки меланомы человека (см. Nip, J., J. Clin. Invest., (1992) 90: 1406-1413), клетки рака молочной железы человека (см. Rong, L. и др., Invest. Ophthalmol. Vis. Sci. (2009) 50: 5988-5996), а пигментированные эпителиальные клетки сетчатки человека (Peter С. Brooks и др., J. Clin. Invest., (1995) 96: 1815-1822). Таким образом, было продемонстрировано, что существует хорошая корреляция между метастатическими потенциалами клеток меланомы человека и адгезией клеток меланомы к витронектину лимфатических узлов через ανβ3 интегриновый рецептор, a также показано, что адгезия ингибируется RGD-содержащими пептидами (Nip, J., J. Clin. Invest., (1992) 90: 1406-1413). Это показывает, что RGD-пептиды могут быть важными антиангиогенестическими агентами.
Кроме того, на линии раковых клеток толстой кишки человека было продемонстрировано, что в случае увеличения клеточной адгезии, увеличивается метастатическая активность (Lehmann, М., Cancer Res. (1994), 54. 2102-2107). Поэтому агенты, препятствующие адгезии клеток, эффективно подавляют рак толстой кишки и меланомы с метастазами.
На основании результатов исследования заживления ран, где было показано, что RGC ингибирует адгезию клеток, и экстраполяции метастатического потенциала RGC в моделях меланомы и рака толстой кишки, можно сделать вывод, что RGC-пептиды и их производные могут эффективно подавлять опухоль метастазы, например, меланомы и рака толстой кишки.
Пример 5. Использование пептидов RGC для направлености или доставки агентов к опухоли
В этом примере рассмотрен димерный RGC-пептид-Паклитаксел конъюгат (Соединение 3), показанный ниже. Эта композиция является пригодной в качестве противоопухолевого агента. Димерный RGC-пептид селективно связывается с интегриновыми рецепторами, экспрессия которых повышена в некоторых раковых клетках, и является полезным для лечения некоторых метастазирующих типов рака, таких как, например, метастазирующий рак молочной железы, путем ингибирования клеточной адгезии.
Соединение 3:
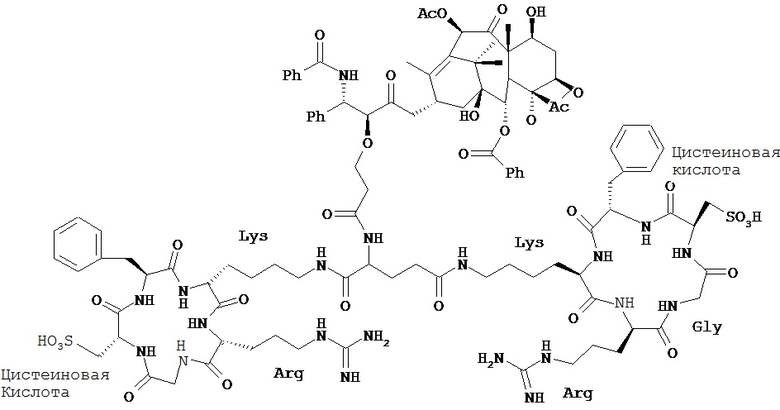 Соединение 3
Соединение 3
Синтез и механизмы действия, биораспределения и опухолевой селективности соответствующих RGD аналогов Соединения 3 описаны Chen, X. и др.;. Synthesis and Biological Evaluation of Dimeric RGD Peptede-Paclitaxel Conjugate as a Model for Integrin-Targeted Drug Delivery; J. Med. Chem., (2005) 48 (4): 1098-1106).
Хотя Соединение 3 содержит определенный противоопухолевый агент, Паклитаксел, связанный с димерным пептидом RGC, должно быть понятно, что это воплощение настоящего изобретения включает в себя все мономерные или многомерные формы RGC-пептидов, связанных с любым возможным диагностическим или терапевтическим агентом, который может быть использован для диагностики, визуализации или лечения опухоли или других интегрин-содержащих тканей или структур. Примеры противоопухолевых веществ, которые могут быть конъюгированы с мономерными или мультимерными RGC-пептидами в соответствии с настоящим изобретением могут включать противоопухолевые агенты (например, химиотерапевтические препараты, модификаторы биологической реакции, ингибиторы васкуляризации, блокаторы рецепторов гормонов, криотерапевтические агенты или другие вещества, которые разрушают или подавляют неоплазию или опухоль), такие как, алкилирующие агенты или другие вещества, которые напрямую уничтожают раковые клетки через разрушение их ДНК (например, циклофосфамид, изофосфамид), нитрозомочевина или другие вещества, которые уничтожают раковые клетки путем ингибирования изменений, необходимых для репарации ДНК в клетках (например, кармустин (BCNU) и ломустин (CCNU)), антиметаболиты и другие вещества, которые блокируют рост раковых клеток, влияя на определенные функции клетки, как правило, синтез ДНК (например, 6-меркаптопурин и 5-фторурацил (5FU), противоопухолевые антибиотики и другие соединения, которые действуют путем связывания или интеркаляции в ДНК и предупреждения синтеза РНК (например, доксорубицин, даунорубицин, эпирубицин, идарубицин, митомицин-С и блеомицин), растительные (например, Vinca) алкалоидов и другие противоопухолевые препараты, полученные из растений (например, винкристин и винбластин), стероидные гормоны, ингибиторы гормонов, антагонисты рецепторов гормонов и другие вещества, которые влияют на рост гормон-зависимых типов рака (например, тамоксифен, герцептин, ингибиторы ароматазы, такие как аминоглутетамид и форместан, триазол ингибиторы, такие как летрозол и анастразол, стероидные ингибиторы, такие как экземестан), антиангиогенестические белки, малые молекулы, агенты генной терапии и/или другие вещества, которые подавляют ангиогенез и васкуляризацию опухолей (например, мет-1, мет-2, талидомид), бевацизумаб (Авастин), скваламин, эндостатин, ангиостатин, Ангиозим, АЕ-941 (Неовастат), СС-5013 (Ревимид), Medi-522 (Витаксин), 2-метоксиэстрадиол (2МЕ2, Панзем), карбоксиамидотриазол (CAI), пролекарство комбретастатина А4 (СА4Р), SU 6668, SU 11248, BMS-275291, COL-3, EMD 121974, IMC-1C11, IM862, TNP-470, целекоксиб (Целебрекс), рофекоксиб (Vioxx), интерферон альфа, интерлейкин-12 (IL-12) или соединения, указанных в Science Vol.289, стр.1197-1201 (17 августа 2000), который включен в настоящее описание посредством ссылки, модификаторы биологических реакций (например, интерферон, бацилла Кальметта-Герена (БЦЖ), моноклональные антитела, интерлюкин 2, гранулоциты колониестимулирующий фактор (GCSF) и т.д., PGDF-рецепторы, герцептин, аспарагиназа, бусулфан, карбоплатин, цисплатин, кармустин, хлорамбуцил, цитарабин, дакарбазина, этопозид, флукарбазон, флуорорацил, гемцитабин, гидроксимочевина, ифосфамид, иринотекан, ломустин, мелфалан, меркаптопурин, метотрексат, тиогуанин, тиотепа, томудекс, топотекан, треосульфан, винбластин, винкристин, митоазитрон, оксалиплатин, прокарбазин, стрептоцин, таксол, таксотер, аналоги, представители одного и того же класса и производные этих соединений, а также других противоопухолевые агенты, не перечисленные здесь.
Пример 6. 64СU-меченные мультимерные RGC-пептиды для визуализации интегрин-экспрессирующих опухолей
В этом примере показано, что 64СU-меченные тетрамерные и октамерные RGC-пептиды по настоящему изобретению (Соединений 4 и 5, соответственно) могут использоваться в качестве радиотерапевтических агентов для визуализации и диагностики (например, радиомечения опухоли для PET-сканирования), а также для направленности или доставки терапевтических агентов в опухоли или других клетки, которые экспрессируют интегрины, такие как опухоли, экспрессирующие ανβ3 интегрины.
Соединение 4:
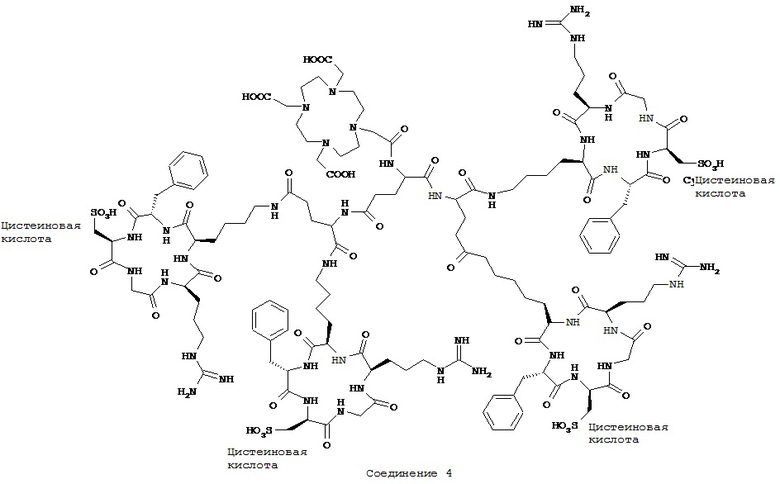
Соединение 5:
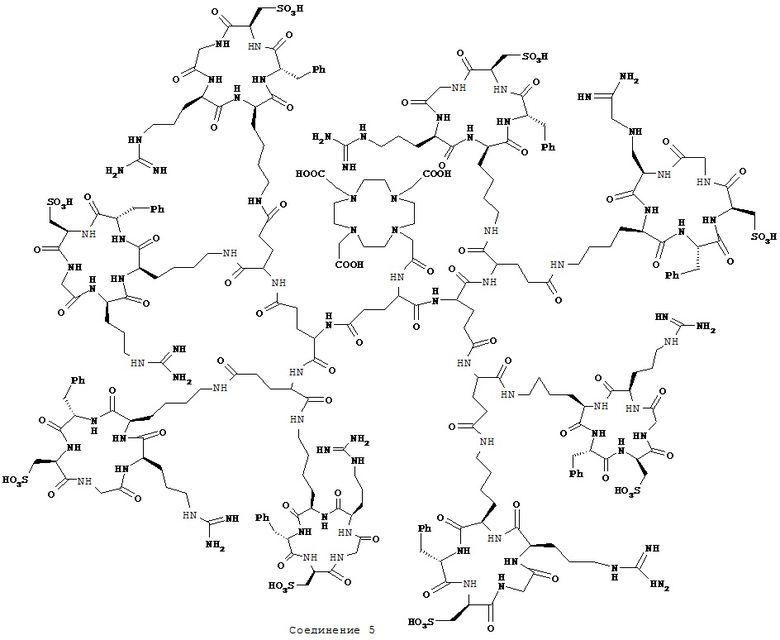
Соединение 5
Синтез и механизмы действия, биораспределения, селективности для опухоли и РЕТ-связанное использование соответствующих RGD аналогов Соединений 4 и 5 было описано Li, Z. и соавт., 64CU-Labeled Tetrameric and Octameric RGD Peptides for small animal PET of Tumor ανβ3 Integrin Expression; J. Nucl. Med. 48 (7), стр.1162-1171 (2007).
Как используется здесь, любая ссылка на лечение заболевания или расстройства не должна толковаться как включающая предупреждение или профилактику заболевания или расстройства до того, как оно появилось или было обнаружено, а также лечение заболевания или расстройства после того, как оно появилось или было обнаружено.
Следует отметить, что изобретение было описано здесь со ссылкой на некоторые конкретные примеры и варианты воплощения, но могут быть сделаны различные добавления, удаления, изменения и модификации раскрытых примеров и вариантов, не отходя от предполагаемой сущности и объема изобретения. Например, любой элемент или признаки одного из вариантов воплощения или примера могут быть включены или могут быть использованы с другим вариантом или примером, если не предусмотрено иное, в случае если это сделает воплощение или пример непригодным для использования по назначению. Кроме того, если последовательность способа или процесса была описана и перечислена в определенном порядке, порядок соответствующих этапов может быть изменен, если не указано иное или если это не нарушит реализацию назначения способа или процесса. Все приемлемые добавления, удаления, изменения и дополнения должны быть рассмотрены как аналоги описанных примеров и вариантов и должны быть включены в объем притязаний по следующей формуле. Все публикации и патентные документы, упомянутые в настоящем документе, включены в настоящий документ посредством ссылки в полном объеме для всех целей в той же степени, как если бы каждый из них был описан здесь индивидуально.
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТАГОНИСТЫ ИНТЕГРИНОВЫХ РЕЦЕПТОРОВ И ИХ ПРИМЕНЕНИЕ | 2012 |
|
RU2721907C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ ПОДАВЛЕНИЯ АНГИОГЕНЕЗА | 2010 |
|
RU2786127C2 |
| СПОСОБЫ И КОМПОЗИЦИИ, ИСПОЛЬЗУЕМЫЕ ДЛЯ ИНГИБИРОВАНИЯ αβ-ОПОСРЕДОВАННОГО АНГИОГЕНЕЗА | 1997 |
|
RU2195312C2 |
| СПОСОБЫ И КОМПОЗИЦИИ, ПРИГОДНЫЕ ДЛЯ ИНГИБИРОВАНИЯ АНГИОГЕНЕЗА | 1995 |
|
RU2162712C2 |
| RGD-СОДЕРЖАЩИЕ ПЕПТИДОМИМЕТИКИ И ИХ ПРИМЕНЕНИЕ | 2009 |
|
RU2519736C2 |
| ПЕПТИДНЫЕ СОЕДИНЕНИЯ | 2005 |
|
RU2393167C2 |
| СОЕДИНЕНИЯ НА ОСНОВЕ ПЕПТИДОВ ДЛЯ НАПРАВЛЕННОЙ ДОСТАВКИ К РЕЦЕПТОРАМ ИНТЕГРИНОВ | 2002 |
|
RU2303042C2 |
| ИНГИБИТОРЫ ИНТЕГРИНА ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЯ ГЛАЗ | 2002 |
|
RU2311177C2 |
| Способ лечения пролиферативных процессов заднего отрезка глаза | 2018 |
|
RU2684927C1 |
| СПОСОБЫ И КОМПОЗИЦИИ, ИСПОЛЬЗУЕМЫЕ ДЛЯ ИНГИБИРОВАНИЯ АНГИОГЕНЕЗА | 1997 |
|
RU2194528C2 |
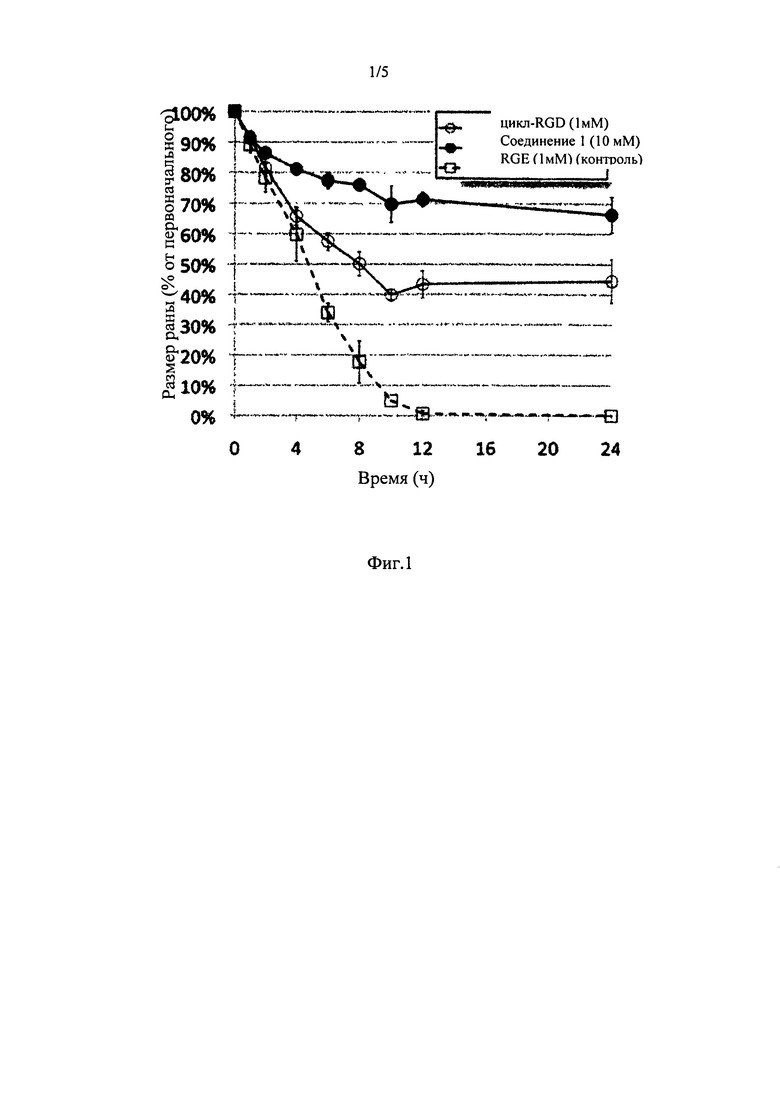
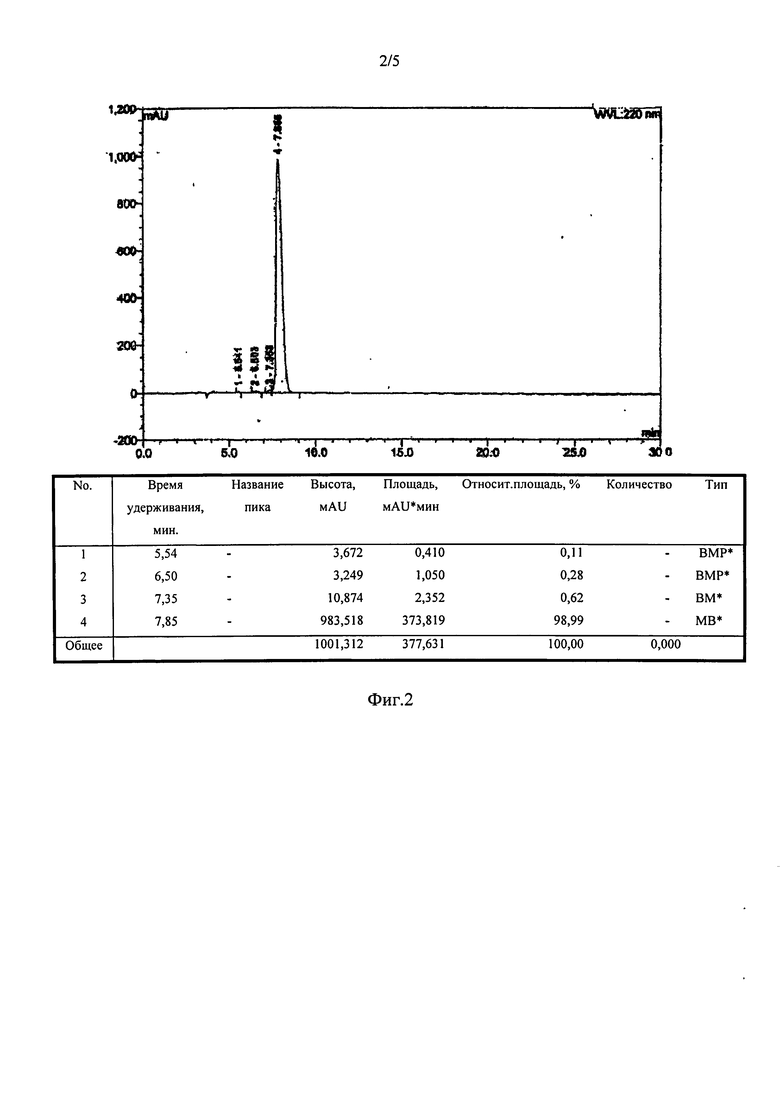
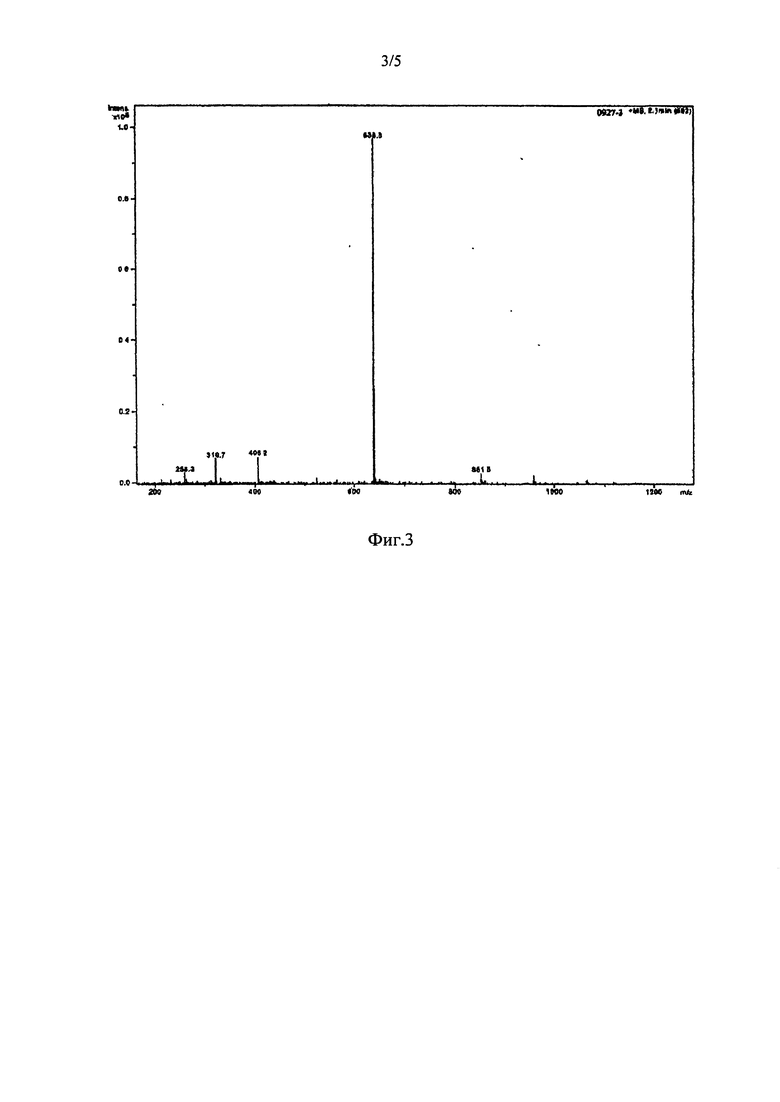
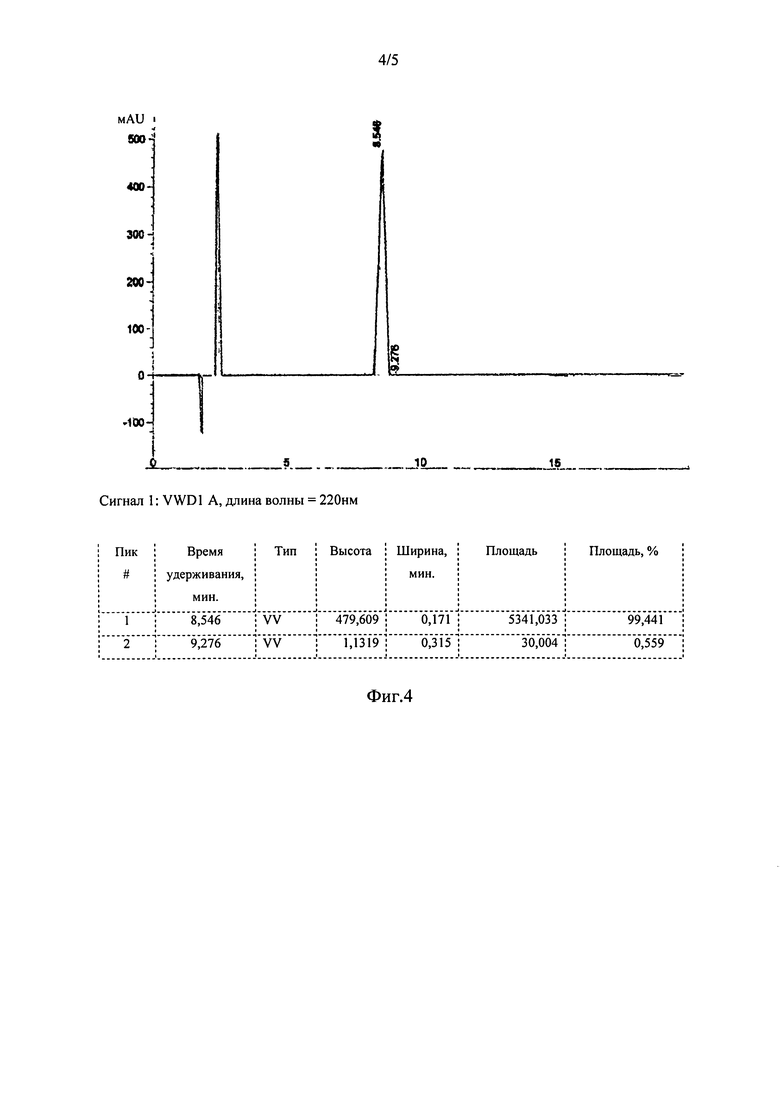
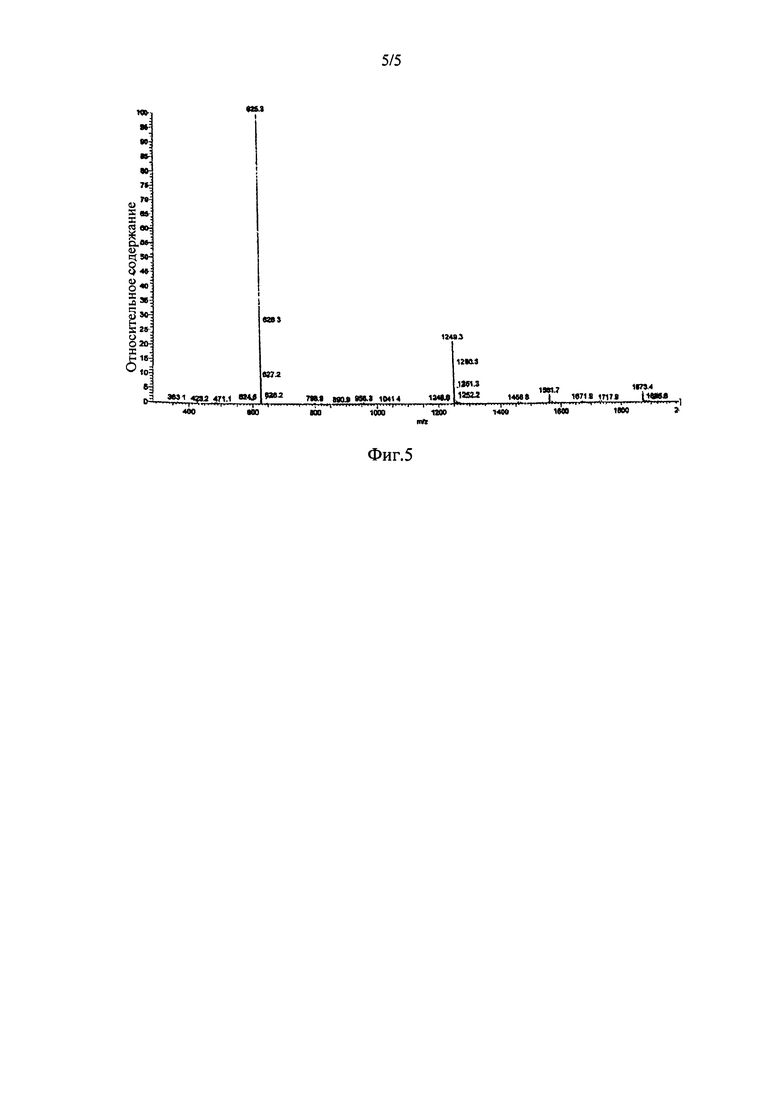
Группа изобретений относится к области фармацевтики и медицины и касается пептида, содержащего последовательность глицин-аргинин-глицин-цистеиновая кислота-треонин-пролин, который ингибирует клеточную адгезию к RGD-сайтам связывания. Также описаны композиция, и способ лечения витреоретинального заболевания, и способ стимуляции витреолизиса, разжижения стекловидного тела или витреоретинальной отслойки. Группа изобретений обеспечивает лечение заболеваний сетчатки и/или облегчение в удалении стекловидного тела в ходе витрэктомии. 5 н. и 5 з.п. ф-лы, 6 пр., 5 ил., 2 табл.
1. Пептид, ингибирующий клеточную адгезию к RGD-сайтам связывания, содержащий Глицин-Аргинин-Глицин-Цистеиновая кислота-Треонин-Пролин.
2. Пептид по п. 1, имеющий структурную формулу:
Соединение 1
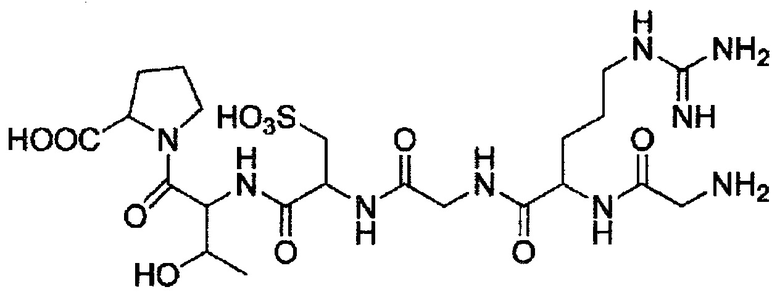
3. Фармацевтическая композиция, ингибирующая клеточную адгезию к RGD-сайтам связывания, причем композиция содержит пептид по п. 1 или 2 в сочетании с фармацевтически приемлемым носителем.
4. Фармацевтическая композиция по п. 3, предназначенная для лечения витреоретинального заболевания или заживления ран.
5. Фармацевтическая композиция по п. 4, где витреоретинальное заболевание выбрано из: плавающих помутнений, идиопатических разрывов макулы, макулярного тракционного синдрома, возрастной макулярной дегенерации, влажной макулярной дегенерации, хориоидальной неоваскуляризации, витреоретинальной операции, окклюзии вены, неоваскуляризации роговицы, ишемии зрительного нерва, рубеоза радужки и диабетической ретинопатии.
6. Способ лечения витреоретинального заболевания, включающий введение субъекту, нуждающемуся в этом, пептида по п. 1 или 2.
7. Способ лечения витреоретинального заболевания по п. 6, в котором введение указанного пептида вызывает заднюю отслойку стекловидного тела.
8. Способ лечения витреоретинального заболевания по п. 6, в котором витреоретинальное заболевание выбрано из: плавающих помутнений, идиопатических разрывов макулы, макулярного тракционного синдрома, возрастной макулярной дегенерации, влажной макулярной дегенерации, хориоидальной неоваскуляризации, витреоретинальной операции, окклюзии вены, неоваскуляризации роговицы, ишемии зрительного нерва, рубеоза радужки и диабетической ретинопатии.
9. Способ снижения витреоретинальной или витреомакулярной тракции, включающий введение субъекту, нуждающемуся в этом, пептида по п. 1 или 2.
10. Способ стимуляции витреолизиса, разжижения стекловидного тела или витреоретинальной отслойки, включающий введение субъекту, нуждающемуся в этом, пептида по п. 1 или 2.
| WO 2006017619 A2, 16.02.2006 | |||
| US 6087330, 11.07.2000 | |||
| MEN L,WANGY | |||
| Further studies in fragmentation of protonated ions of peptides containing aspartic acid, glutamic acid, cysteine sulfunic acid, and cysteine sulfonic acid | |||
| Rapid Commun Mass Spectrom, 2005, 19910, 23-30 | |||
| US 2003059422 А1, 27.03.2003 | |||
| CHANG JC et al | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Biomaterials, 2009, Oct, 30(31): 6265-75. | |||
Авторы
Даты
2018-01-25—Публикация
2010-11-10—Подача