Изобретение относится к ветеринарии, вирусологии и биотехнологии, в частности к получению вакцины для специфической профилактики инфекционного ринотрахеита крупного рогатого скота (ИРТ КРС). ИРТ - остро протекающая контагиозная болезнь КРС вирусной этиологии, наносящая значительный экономический ущерб скотоводству.
Вирус ИРТ вызывает заболевание КРС различных возрастных групп, которое проявляется пятью формами: поражением верхних дыхательных путей, вагинитами, энцефалитами, конъюктивитами и артритами. Кроме того, у телят возможна пневмония.
Болезнь широко распространена во всем мире. В США в 1954-1956 гг.она протекала как эпизоотия с большим экономическим ущербом. Частые случаи ИРТ отмечены в Канаде, Южной Африке, Новой Зеландии, Австралии, Англии, Германии, Франции, Швеции, Швейцарии, Австрии, Италии, Румынии и других странах. В нашей стране ИРТ был впервые диагностирован в 1968 г. и подтвержден вирусологически в 1969 г. в связи с ввозом различных пород КРС из некоторых вышеуказанных стран, неблагополучных по данной инфекции.
Экономический ущерб, наносимый ИРТ, слагается из снижения удоев в период болезни (до 50-60%), значительного увеличения сервис-периода и яловости коров, болевших вагинальной формой, слабого развития больного молодняка и значительным процентом гибели и выбраковки телят. При хронической серозно-гнойной пневмонии погибает до 20% молодняка.
Вакцинопрофилактика ИРТ занимает ведущее место в комплексе противоэпизоотических мер, направленных на борьбу с этим заболеванием. Для профилактики ИРТ применяют как живые, так и инактивированные вакцины, полученные из вируса, репродуцированного в различных культурах клеток (1, 2, 3).
Известна живая моновакцина против ИРТ, изготовленная из штамма "ТК-А (ВИЭВ)-2", включающая вируссодержащий материал в 0,5% растворе гидролизата лактальбумина на растворе Хенкса, защитную среду из сахарозы 4% и желатина 2% взятую в соотношении к вирусному материалу 1:9 [4]. Вакцину вводят животным двукратно подкожно по 1,0-2,0 мл.
Технологичность живых вакцин в производстве и их простота использования не вызывает сомнения, но иммунная реакция у животных при введении не всегда стабильна и в ряде случаев вызывает осложнения после вакцинации. В настоящее время для специфической профилактики ИРТ КРС используют инактивированные вакцины как сорбированные, так и эмульсионные.
Известна инактивированная вакцина против инфекционного ринотрахеита крупного рогатого скота, предусматривающая культивирование штамма "ТК-А инфекционного ринотрахеита в перевиваемой культуре почек теленка MDBK до активности 7,25-8,9 lg ТЦД50/мл. Инактивацию вируссодержащего материала проводят теотропином в концентрации 0,05-0,5% при температуре 36-38°С в течение 1-6 сут с последующим добавлением масляного адъюванта [5].
Известна инактивированная вакцина против инфекционного ринотрахеита крупного рогатого скота, включающая концентрированный антиген вируса инфекционного ринотрахеита штамм Herpesvirus I "Щапово" с титром 7,5-8,5 lg ТЦД50/мл и масляный адъювант в соотношении 90:10, а также смеси антибиотиков на мл вакцины: пенициллин 100-200 ЕД, стрептомицин 100-200 мкг и нистатин 50-100 мг [6]. Вакцину вводят животным подкожно в дозе 2,0-6,0 мл или внутрикожно в дозе 0,2-0,3 мл. Вакцина безвредна и обеспечивает создание иммунитета у 80-93% привитых животных. Недостатком этого штамма является трудоемкость концентрирования полиэтиленгликолем 6000 (ПЭГ) вируссодержащего материала для получения необходимого количества антигена в прививочной дозе.
Известна также инактивированная вакцина против инфекционного ринотрахеита крупного рогатого скота, включающая инактивированный 0,05%-м формальдегидом штамм, «Молдавский» вируса инфекционного ринотрахеита, репродуцированный в культуре перевиваемых клеток почки овцы с конечным титром инфекционности 8,0 lg ТЦД50/мл, эмульгированный с полимерным адъювантом Montanide Gel в соотношении 85:15. При внутрикожном введении в дозе 0,4 см3/голову двукратно с интервалом 21 сутки она активизирует в организме вакцинированных животных индукцию вируснейтрализующих антител в титрах до 7,6 log2 и защищает от клинического проявления заболевания инфекционным ринотрахеитом до 60 суток [7]. Недостатком известного штамма является его неаттенуированность и выраженная патогенность для восприимчивых животных.
Известна инактивированная вакцина против инфекционного ринотрахеита крупного рогатого скота, включающая штамм "ВНИИЗЖ-ДЕП" вируса инфекционного ринотрахеита крупного рогатого скота, репродуцированного в перевиваемой культуре клеток, взятой из ряда, состоящего из перевиваемых культур клеток ВНК-21, MDBK и ЗКГ, с биологической активностью 6,0 lg ТЦД50/мл, инактивированного аминоэтилэтиленимином (АЭЭИ), с масляным адъювантом в соотношении 30,0:70,0 мас. %. АЭЭИ используют в концентрации 0,1-0,2% с последующей его нейтрализацией тиосульфатом натрия [8].
Известна сорбированная инактивированная вакцина, содержащая антигенный материал из штамма "ВНИИЗЖ-ДЕП" вируса инфекционного ринотрахеита крупного рогатого скота, репродуцированного в перевиваемой культуре клеток (ВНК-21, MDBK и ЗКГ) с биологической активностью 6,0 lg ТЦД50/мл; инактивированного аминоэтилэтиленимином (АЭЭИ) в концентрации 0,1-0,2%, содержащая адъюванты гидроокись алюминия (в виде 10% геля в количестве 19,6-49,6 мас. % и дополнительно сапонин (в виде 10% водного раствора в количестве 0,4 мас. %). Вакцина обладает высокой антигенной и иммуногенной активностью и безвредностью [9].
Данный аналог является наиболее близким к предлагаемому изобретению, но АЭЭИ является токсичным веществом для персонала биофабрики. Сапонин не производят в нашей стране, а цены на закупку по импорту постоянно увеличиваются.
В связи с этим актуальной остается проблема инактивированной сорбированной вакцины против ИРТ КРС, обладающей высокой биологической, антигенной, иммуногенной активностью и безвредностью, пригодной для иммунизации животных всех половозрастных групп.
Задачей настоящего изобретения стало получение сухой инактивированной безвредной высокоиммуногенной вакцины с использованием нового адъюванта, обеспечивающей создание напряженного иммунитета у крупного рогатого скота к инфекционному ринотрахеиту.
Намеченная цель достигнута тем, что в качестве антигена используется вирус инфекционного ринотрахеита, штамм-антиген Herpesvirus bovis 1, депонированный в коллекции РУП "Институт экспериментальной ветеринарии им. С.Н. Вышелесского" с регистрационным номером «КМИЭВ-У123» с активностью 7,3-7,8 lg ТЦЦ50/мл [10].
В качестве адъюванта применяли хитозана сукцинат. Сырьем для производства хитозана является хитин. Это продукт нерастворим в воде, в разбавленных кислотах, концентрированных щелочах и растворим в безводной муравьиной и 78,4-97,2% фосфорной кислотах, концентрированных растворах солей (LiCNS, CaCl2 и др.).
При взаимодействии хитина с концентрированными щелочами при высокой температуре происходит его деацетилирование с превращением в хитозан. Хитозан - желтоватая аморфная масса, нерастворим в воде, щелочах; растворим в разбавленных неорганических кислотах. Из этих растворов он осаждается щелочью. Отмечено, что наличие водорастворимой олигомерной фракции хитозана в препаратах на его основе стимулирует заживление ран, усиливает противоопухолевое и иммуностимулирующее действие (11).
В качестве адъюванта применяли этоний отечественного производства, представляющий собой белый кристаллический порошок со специфическим запахом, слегка горьковатым вкусом, не летучий, хорошо растворим в воде, спирте, изотоническом и гипертоническом (не выше 5%) растворе натрия хлорида, трудно растворим в ацетоне, бензоле, эфире; рН 1% водного раствора 4,1-5,5. Препарат несовместим с мылами, кислотами, а также окислителями. Данное вещество является бисчетвертичным аммониевым соединением: 1,2-этилен-бис(N-диметил-карбдецилоксиметил) аммоний -C30H62N2O4Cl2.
Этоний обладает бактериостатическим/бактерицидным эффектом, применяют в качестве адъюванта (12).
Технический результат заключается в повышении антигенной и иммуногенной активности вакцины и ее безвредности, а также в расширении арсенала средств специфической профилактики ИРТ КРС.
Указанный технический результат достигнут созданием вакцины против ИРТ КРС сорбированной инактивированной, охарактеризованной следующей совокупностью признаков:
1. Вакцина против ИРТ КРС, сорбированная инактивированная.
2. Антигенный материал из возбудителя ИРТ КРС, репродуцированного в чувствительной биологической системе и подвергнутого инактивации, в эффективном количестве.
2.1. В качестве антигенного материала из возбудителя ИРТ КРС антигенный материал из штамма Herpesvirus bovis 1 «КМИЭВ-V123» вируса ИРТ КРС.
2.2. Антигенный материал из штамма Herpesvirus bovis 1 «КМИЭВ-V123» вируса ИРТ КРС, репродуцированного в перевиваемой культуре клеток и подвергнутого инактивации.
2.3. Антигенный материал из штамма Herpesvirus bovis 1 «КМИЭВ-V123» вируса ИРТ КРС, репродуцированного в перевиваемой культуре клеток ВНК-21 и инактивированного теотропином.
2.4. Антигенный материал из штамма Herpesvirus bovis 1 «КМИЭВ-V123» вируса ИРТ КРС, репродуцированного в перевиваемой культуре клеток ВНК-21 с биологической активностью, по меньшей мере, 7,3-7,8 lg ТЦД50/мл, и инактивированного теотропином.
2.5. Антигенный материал из штамма Herpesvirus bovis 1 «КМИЭВ-V123» вируса ИРТ КРС, репродуцированного в перевиваемой культуре клеток ВНК-21 с биологической активностью, по меньшей мере, 7,3-7,8 lg ТЦЦ50/мл, и инактивированного теотропином, в концентрации 0,2%.
2.6. Антигенный материал из штамма Herpesvirus bovis 1 «КМИЭВ-V123» вируса ИРТ КРС, репродуцированного в перевиваемой культуре клеток MDBK (или ПТ-80, «Таурус», ЛЭК) и инактивированного теотропином.
2.7. Антигенный материал из штамма Herpesvirus bovis 1 «КМИЭВ-V123» вируса ИРТ КРС, репродуцированного в перевиваемой культуре клеток MDBK (или ПТ-80, «Таурус», ЛЭК) с биологической активностью, по меньшей мере, 7,3-7,8 lg ТЦД50/см3, и инактивированного теотропином.
2.8. Антигенный материал из штамма Herpesvirus bovis 1 «КМИЭВ-V123» вируса ИРТ КРС, репродуцированного в перевиваемой культуре клеток MDBK (или ПТ-80, «Таурус», ЛЭК) с биологической активностью, по меньшей мере, 7,3-7,8 lg ТЦД50/мл, и инактивированного теотропином, в концентрации 0,2%.
3. Адъювант.
3.1. Из адъювантов - хитозана сукцинат.
3.2. В виде 2% раствора хитозана сукцината в изотоническом растворе натрия хлорида (рН 7,0-7,2).
3.3. Хитозана сукцинат в количестве 0, 25-0,5%.
3.4. Из адъювантов - дополнительно этоний.
3.5. В виде 10% водного раствора этония.
3.6. Этоний в количестве 0,4%.
4. Защитная среда для сублимационного высушивания.
4.1. 2% раствор хитозана сукцината в изотоническом растворе натрия хлорида (рН 7,0-7,2).
4.1. Хитозана сукцинат в количестве 0, 25-0,5%.
5. Антигенный материал из штамма Herpesvirus bovis 1 «КМИЭВ-V123» вируса ИРТ КРС, репродуцированного в перевиваемой культуре клеток, взятой из группы, состоящей из перевиваемой культуры клеток ВНК-21, MDBK (или ПТ-80, «Таурус», ЛЭК), с биологической активностью, по меньшей мере, 7,3-7,8 lg ТЦД50/мл и инактивированного теотропином, содержащий в качестве адъювантов - хитозана сукцинат и дополнительно этоний, а в качестве защитной среды для сублимационного высушивания - хитозана сукцинат в соотношении, мас. %:
Предлагаемое изобретение включает совокупность существенных признаков, обеспечивающих получение результатов во всех случаях, на которые испрашивается правовая охрана:
1. Вакцина против ИРТ КРС, сорбированная инактивированная.
2. Антигенный материал из штамма Herpesvirus bovis 1 «КМИЭВ-V123» вируса ИРТ КРС, репродуцированного в чувствительной биологической системе и подвергнутого инактивации, в эффективном количестве.
3. Адъювант.
Предлагаемое изобретение характеризуется также другими признаками, выражающими конкретные формы выполнения или особые условия его использования:
1. Антигенный материал из штамма Herpesvirus bovis 1 «КМИЭВ-V123» вируса ИРТ КРС, репродуцированного в перевиваемой культуре клеток и подвергнутого инактивации.
2. Антигенный материал из штамма Herpesvirus bovis 1 «КМИЭВ-V123» вируса ИРТ КРС, репродуцированного в перевиваемой культуре клеток ВНК-21 и инактивированного теотропином.
3. Антигенный материал из штамма Herpesvirus bovis 1 «КМИЭВ-V123» вируса ИРТ КРС, репродуцированного в перевиваемой культуре клеток ВНК-21 с биологической активностью, по меньшей мере, 7,3-7,8 lg ТЦД50/мл, и инактивированного теотропином.
4. Антигенный материал из штамма Herpesvirus bovis 1 «КМИЭВ-V123» вируса ИРТ КРС, репродуцированного в перевиваемой культуре клеток ВНК-21 с биологической активностью, по меньшей мере, 7,3-7,8 lg ТЦЦ50/мл, и инактивированного теотропином, в концентрации 0,2%.
5. Антигенный материал из штамма Herpesvirus bovis 1 «КМИЭВ-V123» вируса ИРТ КРС, репродуцированного в перевиваемой культуре клеток MDBK (или ПТ-80, «Таурус», ЛЭК) и инактивированного теотропином.
6. Антигенный материал из штамма Herpesvirus bovis 1 «КМИЭВ-V123» вируса ИРТ КРС, репродуцированного в перевиваемой культуре клеток ВНК-21, MDBK (или ПТ-80, «Таурус», ЛЭК) с биологической активностью, по меньшей мере, 7,3-7,8 lg ТЦД50/мл инактивированного теотропином.
7. Антигенный материал из штамма Herpesvirus bovis 1 «КМИЭВ-V123» вируса ИРТ КРС, репродуцированного в перевиваемой культуре клеток MDBK (или ПТ-80, «Таурус», ЛЭК) с биологической активностью, по меньшей мере, 7,3-7,8 lg ТЦД50/см3 и инактивированного теотропином, в концентрации 0,2%.
8. Из адъювантов - хитозана сукцинат.
9. В виде 2% раствора хитозана сукцината в изотоническом растворе натрия хлорида (рН 7,0-7,2).
10. Хитозана сукцинат в количестве 0, 25-0,5%.
11. Из адъювантов - дополнительно этоний.
12. В виде 10% водного раствора.
13. Этоний в количестве 0,4%.
14. Защитная среда для сублимационного высушивания.
15. Хитозана сукцинат в количестве 0, 25-0,5%.
16. Антигенный материал из штамма Herpesvirus bovis 1 «КМИЭВ-V123» вируса ИРТ КРС, репродуцированного в перевиваемой культуре клеток, взятой из группы, состоящей из перевиваемой культуры клеток ВНК-21, MDBK (или ПТ-80, «Таурус», ЛЭК), с биологической активностью, по меньшей мере, 7,3-7,8 lg ТЦД50/мл и инактивированного теотропином, содержащий в качестве адъювантов - хитозана сукцинат и дополнительно этоний, а в качестве защитной среды для сублимационного высушивания - хитозана сукцинат в соотношении, мас. %:
Признаками изобретения, характеризующими предлагаемую вакцину и совпадающими с признаками прототипа, в том числе родовое понятие, отражающее назначение, являются:
1. Вакцина против ИРТ КРС, сорбированная инактивированная.
2. Антигенный материал из возбудителя ИРТ КРС, репродуцированного в чувствительной биологической системе и подвергнутого инактивации.
3. По меньшей мере, один адъювант.
По сравнению с вакциной прототипом существенным отличительным признаком предлагаемой вакцины является то, что в качестве антигенного материала из возбудителя ИРТ КРС она содержит антигенный материал из штамма Herpesvirus bovis 1 «КМИЭВ-V123» вируса ИРТ КРС в эффективном количестве.
Предлагаемое изобретение характеризуется также другими отличительными признаками, выражающими конкретные формы выполнения или особые условия его исполнения:
1. Антигенный материал из штамма Herpesvirus bovis 1 «КМИЭВ-V123» вируса ИРТ КРС, репродуцированного в перевиваемой культуре клеток и подвергнутого инактивации.
2. Антигенный материал из штамма Herpesvirus bovis 1 «КМИЭВ-V123» вируса ИРТ КРС, репродуцированного в перевиваемой культуре клеток ВНК-21 и инактивированного теотропином.
3. Антигенный материал из штамма Herpesvirus bovis 1 «КМИЭВ-V123» вируса ИРТ КРС, репродуцированного в перевиваемой культуре клеток ВНК-21 с биологической активностью, по меньшей мере, 7,3-7,8 lg ТЦД50/мл, и инактивированного теотропином.
4. Антигенный материал из штамма Herpesvirus bovis 1 «КМИЭВ-V123» вируса ИРТ КРС, репродуцированного в перевиваемой культуре клеток ВНК-21 с биологической активностью, по меньшей мере, 7,3-7,8 lg ТЦД50/мл, и инактивированного теотропином, в концентрации 0,2%.
5. Антигенный материал из штамма Herpesvirus bovis 1 «КМИЭВ-V123» вируса ИРТ КРС, репродуцированного в перевиваемой культуре клеток MDBK (или ПТ-80, «Таурус», ЛЭК) и инактивированного теотропином.
6. Антигенный материал из штамма Herpesvirus bovis 1 «КМИЭВ-V123» вируса ИРТ КРС, репродуцированного в перевиваемой культуре клеток MDBK (или ПТ-80, «Таурус», ЛЭК) с биологической активностью, по меньшей мере, 7,3-7,8 lg ТЦД50/мл, и инактивированного теотропином.
7. Антигенный материал из штамма Herpesvirus bovis 1 «КМИЭВ-V123» вируса ИРТ КРС, репродуцированного в перевиваемой культуре клеток MDBK (или ПТ-80, «Таурус», ЛЭК) с биологической активностью, по меньшей мере, 7,3-7,8 lg ТЦД50/мл, и инактивированного теотропином, в концентрации 0,2%.
8. Из адъювантов - хитозана сукцинат.
9. В виде 2% раствора хитозана сукцината в изотоническом растворе натрия хлорида (рН 7,0-7,2).
10. Хитозана сукцинат в количестве 0,25-0,5%.
11. Из адъювантов - дополнительно этоний.
12. В виде 10% водного раствора.
13. Этоний в количестве 0,4%.
14. Защитная среда для сублимационного высушивания.
15. Хитозана сукцинат в количестве 0, 25-0,5%.
16. Антигенный материал из штамма Herpesvirus bovis 1 «КМИЭВ-V123» вируса ИРТ КРС, репродуцированного в перевиваемой культуре клеток, взятой из группы, состоящей из перевиваемой культуры клеток ВНК-21, перевиваемой культуры клеток MDBK (или ПТ-80, «Таурус», ЛЭК), с биологической активностью, по меньшей мере, 7,3-7,8 lg ТЦД50/мл и инактивированного теотропином, содержащий в качестве адъювантов хитозана сукцинат и дополнительно этоний, а в качестве защитной среды для сублимационного высушивания - хитозана сукцинат в соотношении, мас. %.
По сравнению с вакциной - прототипом предлагаемая вакцина обладает более высокой антигенной и иммуногенной активностью и безвредностью; расширяет арсенал средств профилактики ИРТ КРС.
Достижение технического результата от использования предлагаемого изобретения объясняется тем, что в состав предлагаемой вакцины введен антигенный материал из нового штамма Herpesvirus bovis 1 «КМИЭВ-V123» вируса ИРТ КРС, обладающего высокой биологической, антигенной и иммуногенной активностью в нативном виде и после инактивации и обеспечивающего получение вакцины, создающей напряженный и длительный иммунитет у привитых животных. Данный штамм безопасен в экологическом отношении и способен накапливаться с высокой активностью при выращивании роллерным методом в перевиваемых культурах клеток. Используемый при инактивации вирусного сырья теотропин, обладающий стабильностью при хранении, поддающийся стандартизации, улучшает условия труда вакцинного производства. Применение в качестве адъюванта хитозана сукцината позволяет получить сорбированную вакцину, способную к сублимационному высушиванию из-за защитных свойств хитозана сукцината. Использование дополнительно этония повышает безвредность вакцины, обеспечивает защиту от контаминации бактериями, микоплазмами и другими гемагглютинирующими вирусами.
Проведенный заявителем анализ уровня техники, включающий поиск по патентным и научно-техническим источникам информации и выявление источников, содержащих, сведения об аналогах предлагаемого изобретения, позволил установить, что заявитель не обнаружил источники, характеризующиеся признаками, тождественными (идентичными) всем существенным признакам предлагаемого изобретения.
Определение из перечня выявленных аналогов прототипа как наиболее близкого по совокупности существенных признаков аналога позволило установить совокупность существенных по отношению к усматриваемому заявителем техническому результату отличительных признаков
предлагаемой вакцины, изложенных в независимом пункте формулы изобретения.
Следовательно, заявляемое решение соответствует патентоспособности «новизна». Для проверки соответствия предлагаемого решения условию патентоспособности «изобретательский уровень» проведен дополнительный поиск известных решений для выявления признаков, включенных в отличительную часть независимого пункта формулы изобретения. Результаты поиска показали, что предлагаемое решение не вытекает для специалиста явным образом из известного уровня техники, изложенного в соответствующем разделе описания (не выявлены решения, имеющие признаки, совпадающие с отличительными признаками предлагаемого изобретения), а также не выявлено влияние предусматриваемых существенными признаками предлагаемого изобретения преобразований для достижения технического результата.
Следовательно, предлагаемая вакцина соответствует условию патентоспособности «изобретательский уровень».
Сущность предлагаемого изобретения пояснена примерами его исполнения, которые не ограничивают объем изобретения.
Предлагаемую вакцину готовили следующим образом.
Производственный штамм вируса инфекционного ринотрахеита Herpesvirus bovis 1 «КМИЭВ-V123» размножают в перевиваемых культурах клеток: почки сирийского хомячка - ВНК-21; почки теленка MDBK (почки теленка - ПТ-80, «Таурус» или легкого эмбриона коров). Заражение культур клеток проводят вируссодержащей культуральной жидкостью в дозе 1-5 ТЦД/клетка. Зараженные культуры при стационарном или роллерном культивировании инкубируют при 37,0±0,5°С в течение 24-72 ч, затем вируссодержащую жидкость собирают и используют для изготовления вакцины с активностью 7,3-7,8 lg ТЦД50/мл. В вируссодержащую культуральную жидкость для инактивации добавляют теотропин в конечной концентрации 0,2% в течение 24-36 часов при 37,0±1,0°С при периодическом перемешивании. Далее проводят контроль полноты инактивации вируса в культуре клеток, после чего антиген вируса ИРТ помещают в емкость (реактор) и смешивают со стерильным адъювантом, представляющим собой 2% раствор хитозана сукцината, растворенного в стерильном изотоническом растворе натрия хлорида, рН 7,0- 7,2; на одну часть адъюванта добавляют 3 части антигена при получении 0,5% или на одну часть адъюванта 7 частей антигена при получении 0, 25% раствора. Далее вводят адъювант этоний виде 10% раствора для получения конечной концентрации 0,4%).
Полученную смесь тщательно перемешивают, расфасовывают во флаконы объемом 20,0 по 5,0 мл и подвергают лиофильному высушиванию. Для этого проводят замораживание при - 60°С в течение 18 ч, после чего проводят вакуумное обезвоживание при температуре полки - 40°С. Скорость нагревания на этапе досушивания составляет 4-6°С/ч. Конечная температура материала 25°С.
Пример 1
Для изготовления одного литра вакцины брали:
- Антиген вируса ИРТ штамм «КМИЭВ - V123» в культуре клеток ВНК-21 с титром 7,5 lg ТЦД50/мл, инактивированный теотропином в конечной концентрации 0,2%, - 750,0 мл;
- 2% раствор хитозана сукцината, растворенного в стерильном изотоническом растворе натрия хлорида, рН 7,0-7,2 - 250 мл (для получения 0,50% раствора).
Полученную вакцину вводили телятам и коровам внутрикожно двукратно с интервалом 14-45 дней в дозе 0,2-0,3 мл.
После введения вакцины с использованием в качестве этого адъюванта осложнений у коров и телят не наблюдалось, животные активно передвигались, принимали корм и воду охотно, признаки угнетения не отмечались.
Пример 2
Для изготовления одного литра вакцины брали:
- Антиген вируса ИРТ штамм «КМИЭВ - V123» в культуре клеток ВНК-21 с титром 7,5 lg ТЦД50/мл, инактивированный теотропином в конечной концентрации 0,2%, - 875,0 мл;
- 2% раствор хитозана сукцината, растворенного в стерильном изотоническом растворе натрия хлорида, рН 7,0-7,2 - 125 мл (для получения 0,25% раствора).
Полученную вакцину вводили телятам и коровам внутрикожно двукратно с интервалом 14-45 дней в дозе 0,2-0,3 мл.
После введения вакцины с использованием в качестве этого адъюванта осложнений у коров и телят не наблюдалось, животные активно передвигались, принимали корм и воду охотно, признаки угнетения не отмечались.
Пример 3
Для изготовления одного литра вакцины брали:
- Антиген вируса ИРТ штамм «КМИЭВ - V123» в культуре клеток MDBK с титром 7,5 lg ТЦД50/мл, инактивированный теотропином в конечной концентрации 0,2%, - 750,0 мл;
- 2% раствор хитозана сукцината, растворенного в стерильном изотоническом растворе натрия хлорида, рН 7,0-7,2 - 250 мл (для получения 0,50% раствора).
Полученную вакцину вводили телятам и коровам внутрикожно двукратно с интервалом 14-45 дней в дозе 0,2-0,3 мл.
После введения вакцины с использованием в качестве этого адъюванта осложнений у коров и телят не наблюдалось, животные активно передвигались, принимали корм и воду охотно, признаки угнетения не отмечались.
Пример 4
Для изготовления одного литра вакцины брали:
- Антиген вируса ИРТ штамм «КМИЭВ - V123» в культуре клеток MDBK с титром 7,51 lg ТЦД50/мл, инактивированный теотропином в конечной концентрации 0,2%, - 875,0 мл;
- 2% раствор хитозана сукцината, растворенного в стерильном изотоническом растворе натрия хлорида, рН 7,0-7,2 - 125 мл (для получения 0,25% раствора).
Полученную вакцину вводили телятам и коровам внутрикожно двукратно с интервалом 14-45 дней в дозе 0,2-0,3 мл.
После введения вакцины с использованием в качестве этого адъюванта осложнений у коров и телят не наблюдалось, животные активно передвигались, принимали корм и воду охотно, признаки угнетения не отмечались.
Пример 5
Для изготовления одного литра вакцины брали:
- Антиген вируса ИРТ штамм «КМИЭВ - V123» в культуре клеток ВНК-21 с титром 7,5 lg ТЦД50/мл, инактивированный теотропином в конечной концентрации 0,2%, - 960,0 мл;
- 10% водный раствор этония - 40 мл (для получения конечной концентрации 0,4%).
Полученную вакцину вводили телятам и коровам внутрикожно двукратно с интервалом 14-45 дней в дозе 0,2-0,3 мл.
После введения вакцины с использованием в качестве этого адъюванта осложнений у коров и телят не наблюдалось, животные активно передвигались, принимали корм и воду охотно, признаки угнетения не отмечались.
Пример 6
Для изготовления одного литра вакцины брали:
- Антиген вируса ИРТ штамм «КМИЭВ - V123» в культуре клеток MDBK с титром 7,5 lg ТЦД50/мл, инактивированный теотропином в конечной концентрации 0,2%, - 960,0 мл;
- 10% водный раствор этония - 40 мл (для получения конечной концентрации 0,4%).
Полученную вакцину вводили телятам и коровам внутрикожно двукратно с интервалом 14-45 дней в дозе 0,2-0,3 мл.
После введения вакцины с использованием в качестве этого адъюванта осложнений у коров и телят не наблюдалось, животные активно передвигались, принимали корм и воду охотно, признаки угнетения не отмечались.
Пример 7
Производственный штамм вируса инфекционного ринотрахеита Herpesvirus bovis 1 «КМИЭВ - V123» размножают в перевиваемых культурах клеток: почки сирийского хомячка - ВНК-21; почки теленка MDBK (почки теленка - ПТ-80, «Таурус» или легкого эмбриона коров). Заражение культур клеток проводят вируссодержащей культуральной жидкостью в дозе 1-5 ТЦД/клетка. Зараженные культуры при стационарном или роллерном культивировании инкубируют при 37,0±0,5°С в течение 24-72 ч, затем вируссодержащую жидкость собирают и используют для изготовления вакцины с активностью 7,3-7,8 lg ТЦД50/мл. В вируссодержащую культуральную жидкость для инактивации добавляют теотропин в конечной концентрации 0,2% в течение 24-36 часов при 37,0±1,0°С при периодическом перемешивании. Далее проводят контроль полноты инактивации вируса в культуре клеток. Далее к полученной инактивированной вирусной суспензии добавляют адъювант этоний, хитозана сукцинат в качестве адъюванта и защитной среды при сублимационном высушивании, получая вакцину при следующем соотношении компонентов, мас. %:
Для повышения сроков хранения вакцина подвергается сублимационному высушиванию по следующей схеме: замораживание проводят при -60°С в течение 18 ч., вакуумное обезвоживание при температуре полки - 40°С, скорость нагревания на этапе досушиваниия составляет 4-6°С. Конечная температура материала 25°С.
Полученную вакцину расфасовывают и проверяют на стерильность, авирулентность, безвредность, иммуногенную активность.
Во время проведения производственных испытаний (по примеру 1-7) у коров опытных и контрольных групп не было отмечено абортов и мертворожденных плодов и было получено 100% телят. При внутрикожной инъекции на месте введения образовывалось ограниченное утолщение кожного покрова диаметром 7-9 мм, которое исчезало спустя 2-3 дня.
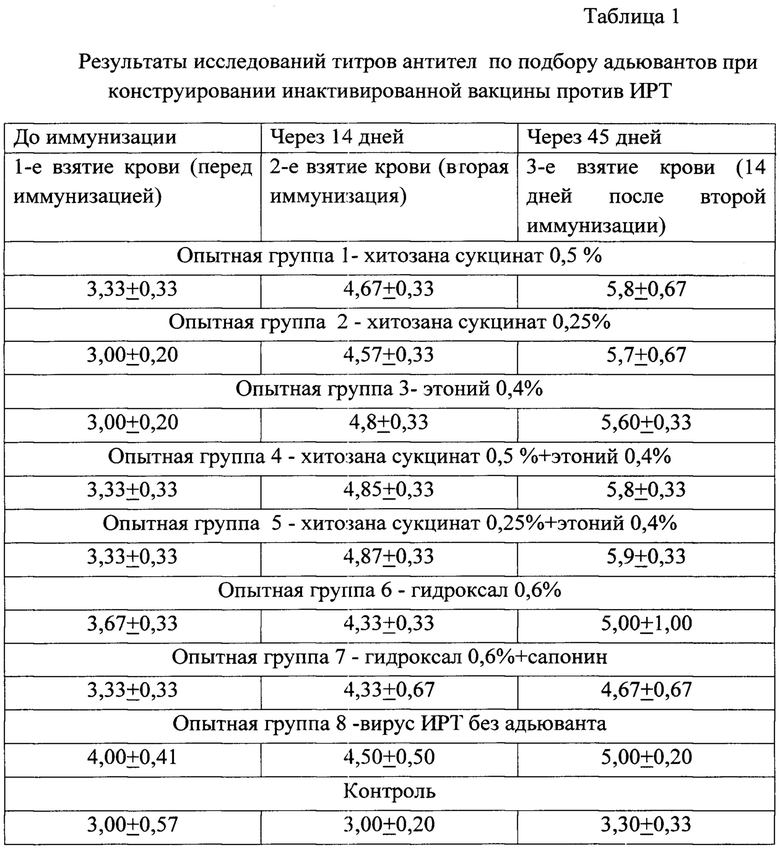
В таблице 1 приведены результаты изучения титров антител против ИРТ при использовании различных адъювантов.
Таким образом, использование хитозана сукцината в качестве адъюванта позволяет существенно повысить уровень поствакцинального иммунитета у телят.
Оценка эффективности вакцины проводилась по показателям заболеваемости и падежа у новорожденных или вакцинированных телят. Данные по эффективности вакцины при внутримышечном введении представлены в таблицах 2 и 3.
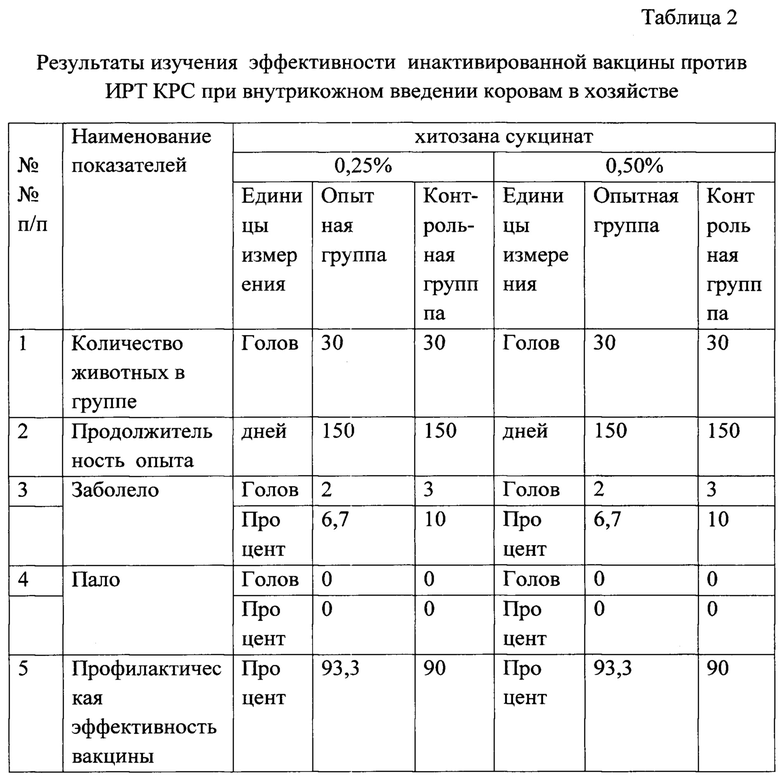

При внутрикожном введении профилактическая эффективность вакцины составила 93,3% у новорожденных телят и 92,3% у вакцинированных телят.
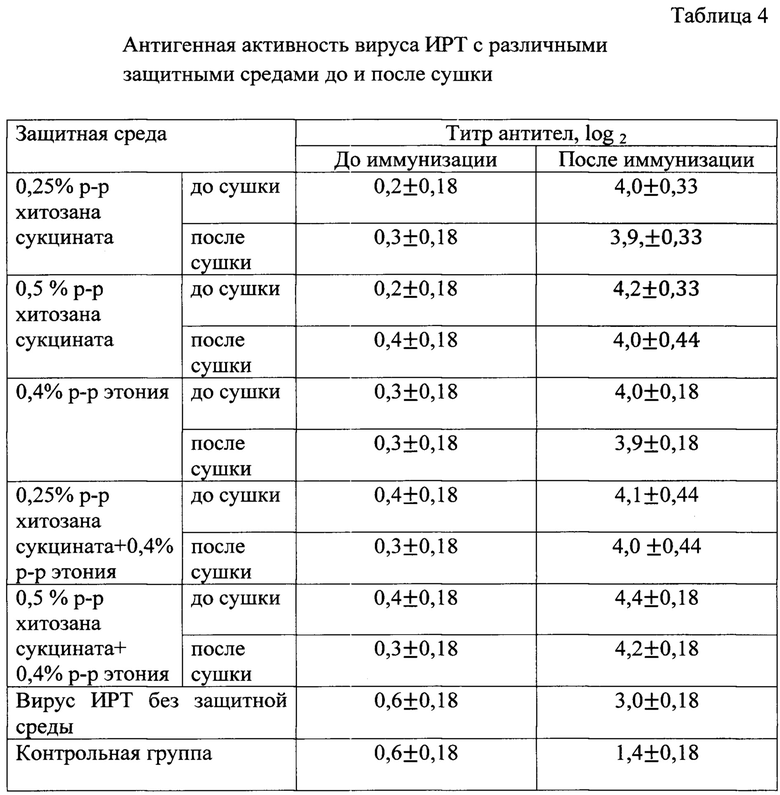
Хитозан сукцината и этоний защищают антигены вируса ринотрахеита крупного рогатого скота при лиофильном высушивании.
Таким образом, разработанная инактивированная вакцина против инфекционного ринотрахеита крупного рогатого скота для внутрикожного введения показала высокую эффективность, способствует снижению заболеваемости и обеспечивает профилактический эффект на уровне 92,3-93,3%.
Отличительной особенностью данной вакцины является использование в качестве антигена высокоиммуногенного полевого штамма вируса ИРТ «КМИЭВ-V123», а также существенное снижение объема вводимой вакцины.
Нами впервые получена сухая инактивированная безвредная высокоиммуногенная вакцина против инфекционного ринотрахеита крупного рогатого скота, обеспечивающая создание у привитых животных напряженного иммунитета.
Вакцина, полученная предложенным способом, нашла применение в животноводческих хозяйствах, как откормочного направления, так и репродуктивного, а также на станциях искусственного осеменения. Применение вакцины позволит существенно снизить заболеваемость инфекционным ринотрахеитом, что будет способствовать повышению мясной и молочной продуктивности животных.
Список использованных источников литера
1. Инфекционные болезни животных: Справочник. Под ред. Д.Ф. Осидзе. - Агропромиздат. - 1987, 19-99.
2. Юров К.П. и Шуляк А.Ф. Герпесвирусы - возбудителя массовых заболеваний крупного рогатого скота. Ветеринария, 1998, 11, 10-12.
3. Сюрин В.Н., Самуйленко А.Я., Соловьев Б.В. и Фомина Н.В. Вирусные болезни животных. - М., ВНИТИБП, 630-646., 4 г.
4. Авторское свидетельство СССР 692128, А61К 30/118, 1977 г.
5. Патент Российской Федерации 2090210, А61К 39/265, 1997 г.
6. Патент Российской Федерации 2059415, А61К 39/265, 1996 г.
7. Декларацiйний патент на корисну модель №51311 Украiна, А61К 39/245, 2010 г.
8. Патент Российской Федерации 2271220, А61К 39/265, 2004 г.
9. Патент Российской Федерации 2268747, А61К 39/265, 2006 г.
10. Патент BY 18414 от 2014.08.30 «Аттенуированный штамм вируса инфекционного ринотрахеита крупного рогатого скота Bovine herpesvirus-1 КМИЭВ - V123 - штамм- антиген».
(Положительное решение на выдачу патента по заявке на изобретение 20110162 от 11.02.2011 г. - Национальный центр интеллектуальной собственности Республики Беларусь).
11. Хитин и Хитозан. Получения, свойства и применение /Под ред. К.Г. Скрябина, Г.А. Вихоревой, В.П. Варламова. - М.: Наука, 2002 - 364 с.
12. Патент Российской Федерации 2521513, А61К 39/265, 2014 г.
| название | год | авторы | номер документа |
|---|---|---|---|
| ВАКЦИНА ПРОТИВ ИНФЕКЦИОННОГО РИНОТРАХЕИТА КРУПНОГО РОГАТОГО СКОТА ЭМУЛЬСИОННАЯ ИНАКТИВИРОВАННАЯ | 2004 |
|
RU2271220C1 |
| ШТАММ ТК-А/К ВИРУСА ИНФЕКЦИОННОГО РИНОТРАХЕИТА КРУПНОГО РОГАТОГО СКОТА ДЛЯ ИЗГОТОВЛЕНИЯ ВАКЦИННЫХ И ДИАГНОСТИЧЕСКИХ ПРЕПАРАТОВ | 2004 |
|
RU2279474C1 |
| ВАКЦИНА ПРОТИВ ИНФЕКЦИОННОГО РИНОТРАХЕИТА КРУПНОГО РОГАТОГО СКОТА СОРБИРОВАННАЯ ИНАКТИВИРОВАННАЯ | 2004 |
|
RU2268747C1 |
| Способ профилактики инфекционного ринотрахеита у телят | 2021 |
|
RU2775580C1 |
| ВАКЦИНА АССОЦИИРОВАННАЯ ПРОТИВ ПАРАГРИППА-3, ИНФЕКЦИОННОГО РИНОТРАХЕИТА И ВИРУСНОЙ ДИАРЕИ КРУПНОГО РОГАТОГО СКОТА ЭМУЛЬСИОННАЯ ИНАКТИВИРОВАННАЯ | 2012 |
|
RU2504400C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ АССОЦИИРОВАННОЙ ИНАКТИВИРОВАННОЙ КУЛЬТУРАЛЬНОЙ ВАКЦИНЫ ПРОТИВ ИНФЕКЦИОННОГО РИНОТРАХЕИТА И ПАРАГРИППА-3 КРУПНОГО РОГАТОГО СКОТА | 2005 |
|
RU2288007C2 |
| АССОЦИИРОВАННАЯ ВАКЦИНА ПРОТИВ ИНФЕКЦИОННОГО РИНОТРАХЕИТА И КОРОНАВИРУСНОЙ ИНФЕКЦИИ КРУПНОГО РОГАТОГО СКОТА ЭМУЛЬСИОННАЯ ИНАКТИВИРОВАННАЯ | 2007 |
|
RU2378017C2 |
| АССОЦИИРОВАННАЯ ВАКЦИНА ПРОТИВ ПАРАГРИППА-3, ИНФЕКЦИОННОГО РИНОТРАХЕИТА И КОРОНАВИРУСНОЙ ИНФЕКЦИИ КРУПНОГО РОГАТОГО СКОТА ЭМУЛЬСИОННАЯ ИНАКТИВИРОВАННАЯ | 2007 |
|
RU2378014C2 |
| ВАКЦИНА АССОЦИИРОВАННАЯ ПРОТИВ АДЕНОВИРУСНОЙ, ГЕРПЕСВИРУСНОЙ ИНФЕКЦИЕЙ, ПАРАГРИППА-3 И ВИРУСНОЙ ДИАРЕИ-БОЛЕЗНИ СЛИЗИСТЫХ ОБОЛОЧЕК КРУПНОГО РОГАТОГО СКОТА ИНАКТИВИРОВАННАЯ ЭМУЛЬСИОННАЯ | 2012 |
|
RU2517733C1 |
| ШТАММ "ВНИИЗЖ" ВИРУСА ИНФЕКЦИОННОГО РИНОТРАХЕИТА КРУПНОГО РОГАТОГО СКОТА ДЛЯ ИЗГОТОВЛЕНИЯ ВАКЦИННЫХ И ДИАГНОСТИЧЕСКИХ ПРЕПАРАТОВ | 2002 |
|
RU2221040C1 |
Изобретение относится к области ветеринарии, вирусологии и биотехнологии и касается вакцины против инфекционного ринотрахеита крупного рогатого скота. Представленная вакцина содержит антигенный материал из штамма Herpesvirus bovis 1«КМИЭВ - V123» вируса ИРТ КРС с биологической активностью 7,3-7,8 lg ТЦД50/мл, репродуцированного в перевиваемой культуре клеток ВНК-21, а в качестве адъюванта содержит смесь этония в виде 10% водного раствора и хитозана сукцината в виде 2% раствора в изотоническом растворе натрия хлорида с рН 7,0-7,2. Изобретение обеспечивает возможность получения вакцины, обладающей высокой антигенной и иммуногенной активностью и безвредностью. 1 з.п. ф-лы, 4 табл., 7 пр.
1. Вакцина против инфекционного ринотрахеита крупного рогатого скота сорбированная инактивированная, сухая, содержащая антигенный материал из штамма Herpesvirus bovis 1«КМИЭВ - V123» вируса ИРТ КРС, репродуцированного в чувствительной биологической системе и подвергнутого инактивации теотропином в концентрации 0,2%, и адъювант хитозана сукцинат, отличающаяся тем, что в качестве антигенного материала она содержит антигенный материал из штамма Herpesvirus bovis 1«КМИЭВ - V123» вируса ИРТ КРС с биологической активностью 7,3-7,8 lg ТЦД50/мл, репродуцированного в перевиваемой культуре клеток ВНК-21, а в качестве адъюванта содержит смесь этония в виде 10% водного раствора и хитозана сукцината в виде 2% раствора в изотоническом растворе натрия хлорида с рН 7,0-7,2, взятых в соотношении, мас. %:
2. Вакцина по п. 1, отличающаяся тем, что она дополнительно подвергается процессу сублимационного высушивания, а в качестве защитной среды для сублимационного высушивания хитозана сукцинат в соотношении, мас. %:
| ВАКЦИНА ПРОТИВ ИНФЕКЦИОННОГО РИНОТРАХЕИТА КРУПНОГО РОГАТОГО СКОТА СОРБИРОВАННАЯ ИНАКТИВИРОВАННАЯ | 2004 |
|
RU2268747C1 |
| Газоанализатор | 1928 |
|
SU18414A1 |
| US 0005601816 A1, 11.02.1997. | |||
Авторы
Даты
2018-02-08—Публикация
2016-08-05—Подача