Изобретение относится к области ветеринарной вирусологии и биотехнологии и может быть использовано при изготовлении средств специфической профилактики и диагностики инфекционного ринотрахеита (ИРТ) крупного рогатого скота (КРС).
ИРТ - остро протекающая контагиозная болезнь КРС вирусной этиологии, наносящая значительный экономический ущерб скотоводству.
Вирус ИРТ вызывает заболевание КРС различных возрастных групп, поражая респираторный (ринотрахеит), генитальный (пустулезный вульвовагинит, баланопростит) тракты, провоцирует аборты у коров, а также поражает нервную систему (энцефаломиелит), слизистые оболочки и глазное яблоко у телят (конъюнктивит и кератоконъюнктивит). Болезнь широко распространена во всем мире.
Экономический ущерб, наносимый ИРТ, складывается из снижения удоев в период болезни (до 50-60%), значительного увеличения сервис-периода и яловости коров, болевших вагинальной формой, слабого развития больного молодняка и значительного процента гибели и выбраковки телят.
Вакцинопрофилактика ИРТ занимает ведущее место в комплексе противоэпизоотических мер, направленных на борьбу с этим заболеванием. Для профилактики ИРТ применяют как живые, так и инактивированные вакцины, полученные из вируса, репродуцированного в различных культурах клеток [1, 2, 3].
Для изготовления живых вакцин хотя и используются аттенуированные штаммы, тем не менее они способны вызывать осложнения на иммунном фоне у животных. Это может произойти вследствие реактивации или рекомбинации вакцинного вируса с полевым. Эпизоотические штаммы используют при изготовлении инактивированных вакцин, но они в случае неполной инактивации вирусного сырья могут вызвать вспышки заболевания.
Известен эпизоотический штамм 4016 вируса ИРТ КРС, используемый для изготовления инактивированной вакцины [4]. Данный штамм выращивают в трудоемких первичнотрипсинизированных культурах клеток БТ, ПЭК, ПТ с инфекционной активностью 6,0-6,5 lg ТЦД50/мл, что не позволяет получать необходимое количество антигена в прививной дозе без предварительного концентрирования вируса.
Известен штамм ТК-А (ВИЭВ) - В 2 вируса ИРТ КРС, используемый для изготовления инактивированной вакцины [5].
Известен вирулентный штамм HERPES птиц bovis - 1 "Щапово" вируса ИРТ КРС, используемый для изготовления инактивированной вакцины [6].
Известен штамм ТК-А вируса ИРТ КРС, используемый для изготовления инактивированной вакцины [7].
Наиболее близким является вирулентный штамм "ВНИИЗЖ" вируса инфекционного ринотрахеита крупного рогатого скота для изготовления вакцинных и диагностических препаратов, используемый для изготовления инактивированной вакцины [8].
Общим недостатком известных штаммов является низкая противоэпизоотическая эффективность изготовленных на их основе вакцинных препаратов. Указанные штаммы имеют невысокий уровень накопления в чувствительных клеточных системах, что не позволяет получать необходимое количество антигена в прививной дозе для обеспечения надежной защиты животных от эпизоотических штаммов вируса ИРТ КРС.
Целью настоящего изобретения явилось получение нового безопасного (аттенуированного) производственного штамма вируса ИРТ КРС, обладающего высокой биологической, антигенной и иммуногенной активностью, сохраняющего свои нативные иммунобиологические свойства после инактивации и пригодного для изготовления высокоиммуногенных вакцинных препаратов (из неконцентрированного вируса), способных защитить поголовье КРС от эпизоотического возбудителя ИРТ КРС, циркулирующего на территории Российской Федерации.
Технический результат от использования предлагаемого изобретения заключается в расширении арсенала безопасных (аттенуированных) штаммов вируса ИРТ КРС, обладающих высокой биологической антигенной и иммуногенной активностью, сохраняющих свои нативные иммунобиологические свойства после инактивации и пригодных для изготовления высокоэффективных вакцинных препаратов.
Данный технический результат достигнут получением штамма ТК-А/К вируса ИРТ КРС. Штамм ТК-А/К является новым ранее неизвестным. Исходный вирус штамма ТК-А использовали для получения штамма ТК-А/К путем клонирования методом предельных разведений и многократных пассажей на чувствительной клеточной системе.
Полученный штамм депонирован во Всероссийской государственной коллекции штаммов микроорганизмов, используемых в ветеринарии и животноводстве, Всероссийского научно-исследовательского института контроля, стандартизации и сертификации ветеринарных препаратов (ВГНКИ) МСХ РФ 12 марта 2004 года под регистрационным шифром ТК-А/К - ДЕП.
Штамм ТК-А/К вируса ИРТ отличается от прототипа однородностью популяции и более высокой биологической, антигенной и иммуногенной активностью. Экспериментально подтверждена возможность его использования для изготовления средств диагностики и профилактики ИРТ КРС.
Штамм ТК-А/К обеспечивает проведение серологической диагностики ИРТ КРС и производство эффективной инактивированной вакцины против ИРТ КРС, создающей надежную защиту КРС от указанного возбудителя заболевания.
Штамм ТК-А/К вируса ИРТ характеризуется следующими признаками и свойствами.
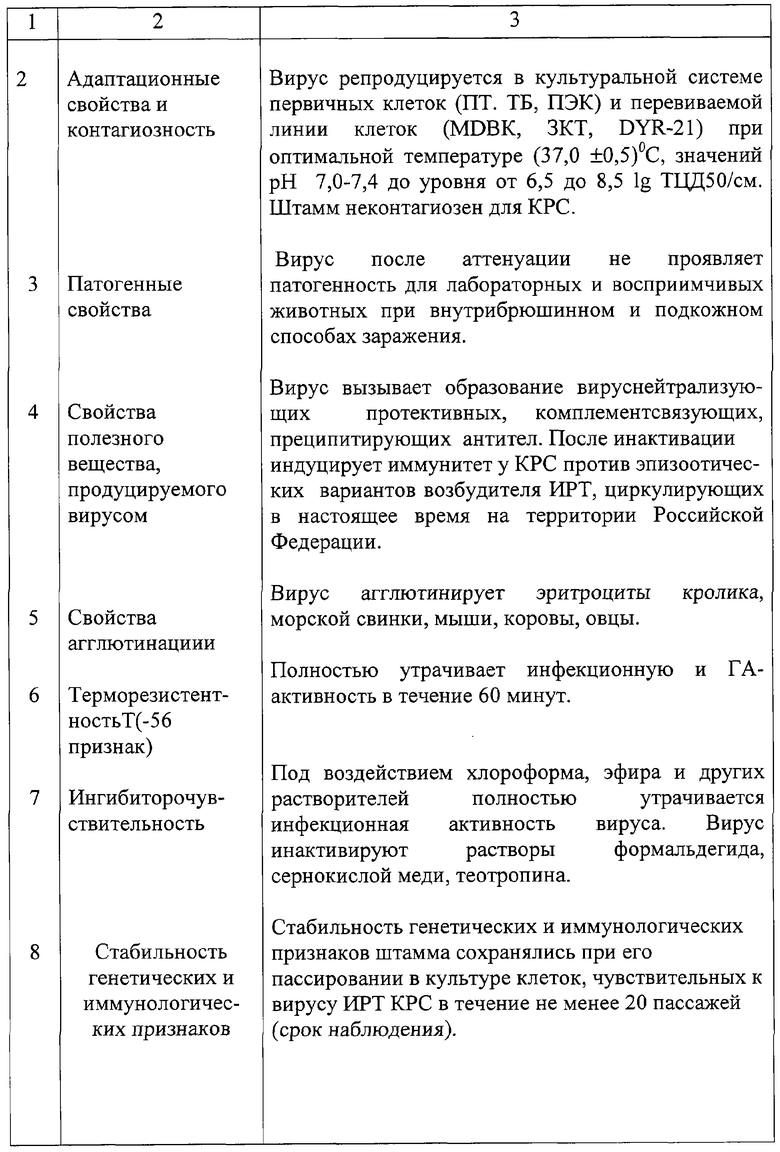
Таксономическая характеристика заключается в том, что штамм ТК-А/К имеет форму и размеры, типичные для герпесвирусов. В серологических реакциях (РН, РНГА, РСК, ИФА и др.) выявляются антигены, общие для всех штаммов герпесвируса КРС. Основные маркерные характеристики штамма ТК-А/К вируса ИРТ приведены в табл.1.


Сущность предлагаемого изобретения поясняется примерами его исполнения.
ПРИМЕР 1
С целью получения генетически однородной популяции для выделения клона из вируса ИРТ шт. ТК-А использовали метод предельного разведения. Культуру клеток MDBK заражали вирусной суспензией в конечных разведениях и инкубировали при 36-37°С до появления ЦПД вируса на пассажных уровнях. В результате длительного пассирования был получен новый штамм ТК-А/К, отличающийся по генетическим признакам от своего предшественника.
Для получения результатов молекулярно-генетической характеристики штамма ТК-А/К вируса ИРТ проведен рестрикционный анализ вирионной ДНК, выделенной из очищенных после селекции препаратов.
При расщеплении ДНК вируса различными рестриктазами получен характерный для каждого фермента набор фрагментов. На основании полученных данных составлена рестрикционная карта, которая характеризует генетическую структуру ДНК производственного штамма ТК-А/К вируса ИРТ КРС.
Полученный вирус использовали для последующего пассирования. Результаты исследований по адаптации вируса ИРТ шт. ТК-А/К в культуре клеток MDBK приведены в табл.2.
Полученный вирус был подвергнут всестороннему контролю в соответствии с руководством МЭБ по стандартным диагностическим методам и вакцинам (1996) и на уровне 6 пассажа после лиофилизации заложен на хранение при минус 60°С в качестве производственного с титром инфекционной активности не ниже 6,5-7,0 lg ТЦД50/мл. Полученному штамму вируса ИРТ КРС присвоено авторское наименование ТК-А/К.
ПРИМЕР 2
С целью определения биологической антигенной и иммунологической активности вируса ИРТ КРС штамм "ТК-А/К" проводили гипериммунизацию кроликов живой массой 2,5-3,0 кг.
Для гипериммунизации кроликов использовали лиофилизированный вирус ИРТ штамм ТК-А/К. Содержимое ампул растворяли физраствором до исходного объема, затем разводили в 10 раз по объему (5,5-6,0 lg ТЦД50/мл.) Животным вводили вирусный материал из штамма ТК-А/К в объемной дозе 1,0 см3 внутримышечно трехкратно с интервалом 14 дней. Через 15 дней после окончания гипериммунизации кроликов обескровили, получили сыворотки крови индивидуально от каждого животного. Каждую сыворотку проверяли на активность и специфичность в реакции нейтрализации. Результаты исследований приведены в табл.3.
Приведенные в табл.3 данные характеризуют высокую биологическую, антигенную и иммуногенную активность штамма ТК-А/К вируса ИРТ КРС при введении в организм лабораторным животным.
ПРИМЕР 3
Для получения сорбированной инактивированной вакцины против ИРТ КРС матровый вирус штамма ТК-А/К выращивают в монослое клеток MDBK роллерным методом.
Производственная серия вируса ИРТ должна иметь инфекционную активность не меньше 7,25-7,5 lg ТЦД550/мл, активность в РГА не меньше 4,0 log2.
Инактивацию вирусного сырья проводят с помощью 10%-ного раствора теотропина, вносимого в суспензию вируса ИРТ до конечной концентрации 0,1% сухого вещества. Для этого в вируссодержащую суспензию вносят при перемешивании раствор теотропина и устанавливают рН вирусного материала в пределах 7,2-7,5 раствором двухзамещенного фофорнокислого калия. Инактивацию проводят при температуре 36-37°С в течение 7 суток с периодическим перемешиванием (3-4 раза в сутки по 2-3 минуты).
По окончании процесса инактивации материал исследуют на полноту инактивации в 3-х последовательных пассажах в культуре клеток MDBK. В качестве адъюванта-сорбента в вакцине используют стерильный 3-6%-ный коллоидный раствор гидроокиси алюминия (ГОА). Смесь суспензии с ГОА перемешивают в течение 1 часа и оставляют для седиментации. Затем в полуфабрикат вакцины добавляют дополнительно 10%-ный водный раствор адъюванта сапонина из расчета 0,1% сухого вещества в конечной концентрации. Смесь перед расфасовкой перемешивают при температуре 10-12°С в течение 1 часа. Оптимальный компонентный состав (мас.%) полученной вакцины против ИРТ КРС приведен в табл.4.
Содержание антигена в вакцине в указанных выше пределах является его оптимальным количеством в препарате, обеспечивающем достижение технического результата.
Полученную вакцину контролируют на авирулентность и стерильность, а затем фасуют в стерильные флаконы.
Стерильность вакцины определяют в соответствии с ГОСТ 28085-89. Авирулентность препарата определяют методом трехкратных последовательных пассажей инактивированного полуфабриката в перевиваемой культуре клеток MDBK по отсутствию ЦПД.
Полученная вакцина представляет собой жидкость розового цвета с рыхлым осадком сорбента, который при встряхивании легко разбивается в гомогенную смесь.
Определение безвредности вакцины проводят на мышах или кроликах в дозе соответственно 0,5 мл и 5 мл. Вакцина считается безвредной, если лабораторные животные в течение 10 суток наблюдения остаются клинически здоровыми, без каких-либо патологических проявлений. На месте введения допускается местная тканевая реакция.
Антигенную активность каждой серии вакцины проверяют на кроликах. Вакцину вводят двукратно с интервалом 14-28 суток четырем кроликам внутримышечно в область бедра в объеме 1 мл. Через 14 суток после повторной иммунизации у кроликов берут пробы крови, выдерживают при 37°С, отделяют сыворотку и исследуют на наличие антител к вирусу ИРТ в РН или РНГА. Серию вакцины считают прошедшей контроль на антигенную активность, если титр ВН-антител и антител в РНГА к вирусу ИРТ не ниже 1:8 и 1:16 соответственно.
Результаты, приведенные в табл.5, свидетельствуют о том, что инактивированная вакцина против ИРТ КРС из штамма ТК-А/К обладает высокой антигенной активностью.
При изучении иммуногенной активности инактивированной сорбированной вакцины против ИРТ КРС из штамма ТК-А/К установлено, что у телят 30-40-дневного возраста, привитых двукратно подкожно в дозе 2 мл уже на 14 день после введения препарата индуцируется иммунный ответ, обеспечивающий 90-100% образование гуморальных антител и защиту животных от заболевания. Экспериментально показано, что одна прививная доза в объеме 2 мл содержит не менее 20 ИМД50. Результаты исследований, представленные в табл.6, подтверждают высокую эффективность инактивированной вакцины против ИРТ КРС из штамма ТК-А/К.
Таким образом, приведенная выше информация свидетельствует о выполнении при использовании предлагаемого изобретения следующей совокупности условий:
- штамм ТК-А/К вируса ИРТ КРС, воплощающий предлагаемое изобретение, предназначен для использования в сельском хозяйстве, а именно в ветеринарной вирусологии и биотехнологии.
- для предлагаемого изобретения в формуле изобретения подтверждена возможность его осуществления с помощью описанных в заявке до даты приоритета средств и методов.
- штамм ТК-А/К, полученный в соответствии с предлагаемым изобретением, обладает высокой инфекционной, антигенной и иммуногенной активностью и пригоден для изготовления вакцинных препаратов против ИРТ КРС.
ЛИТЕРАТУРА
1. Инфекционные болезни животных. Справочник. Под ред. Д.Ф.Осидзе. - М.: Агропромиздат, 1987, 19-99.
2. Юров К.П. и Шуляк А.Ф. Герпесвирусы возбудителей массовых заболеваний крупного рогатого скота. Ветеринария, 1998, №11, 10-12.
3. Сюрин В.Н., Самойленко А.Я., Соловьев Б.В. и Фомина Н.В. Вирусные болезни животных. - М., ВНИТИБП, 630-646.
4. Авт. свид. СССР №980307, А 61 К 39/12; 1981.
5. Авт. свид. СССР №1789219, А 61 К 39/118; 21.03.93.
6. Пат. РФ №2059415, А 61 К 39/265, 10.05.96.
7. Пат. РФ №2090210, А 61 К 39/265, С 12 N 5/06, 7/00, 20.09.97.
8. Пат. РФ №2221040, А 61 К 39/265, С 12 N 7/00, 28.06.2002.
Результаты клонирования вируса ИРТ КРС штамм "ТК-А/К" в культуре клеток МДВК
Уровень накопления вируснейтрализующих антител при гипериммунизации кроликов вирусом ИРТ КРС штамм "ТК-А/К"
Пропись компонентного состава (мас.%) инактивированной вакцины против ИРТ КРС, приготовленной из штамма "ТК-А/К"
Антигенная активность инактивированной ГОА-сапониновой вакцины против ИРТ КРС из штамма "ТК-А/К"
Иммуногенная активность инактивированной ГОА-сапониновой вакцины против ИРТ КРС из штамма "ТК-А/К"
| название | год | авторы | номер документа |
|---|---|---|---|
| ВАКЦИНА ПРОТИВ ИНФЕКЦИОННОГО РИНОТРАХЕИТА КРУПНОГО РОГАТОГО СКОТА ЭМУЛЬСИОННАЯ ИНАКТИВИРОВАННАЯ | 2004 |
|
RU2271220C1 |
| ВАКЦИНА ПРОТИВ ИНФЕКЦИОННОГО РИНОТРАХЕИТА КРУПНОГО РОГАТОГО СКОТА СОРБИРОВАННАЯ ИНАКТИВИРОВАННАЯ | 2004 |
|
RU2268747C1 |
| ВАКЦИНА АССОЦИИРОВАННАЯ ПРОТИВ ПАРАГРИППА-3, ИНФЕКЦИОННОГО РИНОТРАХЕИТА И ВИРУСНОЙ ДИАРЕИ КРУПНОГО РОГАТОГО СКОТА ЭМУЛЬСИОННАЯ ИНАКТИВИРОВАННАЯ | 2012 |
|
RU2504400C1 |
| ШТАММ "ВНИИЗЖ" ВИРУСА ИНФЕКЦИОННОГО РИНОТРАХЕИТА КРУПНОГО РОГАТОГО СКОТА ДЛЯ ИЗГОТОВЛЕНИЯ ВАКЦИННЫХ И ДИАГНОСТИЧЕСКИХ ПРЕПАРАТОВ | 2002 |
|
RU2221040C1 |
| АССОЦИИРОВАННАЯ ВАКЦИНА ПРОТИВ ИНФЕКЦИОННОГО РИНОТРАХЕИТА И КОРОНАВИРУСНОЙ ИНФЕКЦИИ КРУПНОГО РОГАТОГО СКОТА ЭМУЛЬСИОННАЯ ИНАКТИВИРОВАННАЯ | 2007 |
|
RU2378017C2 |
| ВАКЦИНА АССОЦИИРОВАННАЯ ПРОТИВ ВИРУСНОЙ ДИАРЕИ, РОТАВИРУСНОЙ И КОРОНАВИРУСНОЙ ИНФЕКЦИЙ КРУПНОГО РОГАТОГО СКОТА ЭМУЛЬСИОННАЯ ИНАКТИВИРОВАННАЯ | 2012 |
|
RU2515058C1 |
| АССОЦИИРОВАННАЯ ВАКЦИНА ПРОТИВ ПАРАГРИППА-3, ИНФЕКЦИОННОГО РИНОТРАХЕИТА И КОРОНАВИРУСНОЙ ИНФЕКЦИИ КРУПНОГО РОГАТОГО СКОТА ЭМУЛЬСИОННАЯ ИНАКТИВИРОВАННАЯ | 2007 |
|
RU2378014C2 |
| ШТАММ ВИРУСА ПАРАГРИППА-3 КРУПНОГО РОГАТОГО СКОТА ДЛЯ ИЗГОТОВЛЕНИЯ ВАКЦИННЫХ И ДИАГНОСТИЧЕСКИХ ПРЕПАРАТОВ | 2004 |
|
RU2279473C1 |
| ШТАММ "NADL-ВНИИЗЖ" ВИРУСА ВИРУСНОЙ ДИАРЕИ КРУПНОГО РОГАТОГО СКОТА DIARRHEA VIRUS BOVINUM ДЛЯ ИЗГОТОВЛЕНИЯ БИОПРЕПАРАТОВ ДЛЯ ДИАГНОСТИКИ, СПЕЦИФИЧЕСКОЙ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ВИРУСНОЙ ДИАРЕИ КРУПНОГО РОГАТОГО СКОТА | 2010 |
|
RU2449013C2 |
| ВАКЦИНА ПРОТИВ ИНФЕКЦИОННОГО РИНОТРАХЕИТА КРУПНОГО РОГАТОГО СКОТА СОРБИРОВАННАЯ ИНАКТИВИРОВАННАЯ СУХАЯ | 2016 |
|
RU2644339C2 |
Изобретение относится к ветеринарной вирусологии и биотехнологии. Штамм депонирован в коллекции микроорганизмов ВГНКИ под регистрационным наименованием «ТК-А/К» - ДЕП. Штамм имеет высокую антигенную и иммуногенную эффективность и может быть использован для приготовления инактивированной вакцины против ИРТ КРС. 6 табл.
Штамм вируса инфекционного ринотрахеита крупного рогатого скота, семейство Herpesviridae, род Varicello, подтип Herpesvirus bovis 1, коллекция ВГНКИ, «ТК-А/К» - ДЕП, для изготовления вакцинных и диагностических препаратов.
| ШТАММ "ВНИИЗЖ" ВИРУСА ИНФЕКЦИОННОГО РИНОТРАХЕИТА КРУПНОГО РОГАТОГО СКОТА ДЛЯ ИЗГОТОВЛЕНИЯ ВАКЦИННЫХ И ДИАГНОСТИЧЕСКИХ ПРЕПАРАТОВ | 2002 |
|
RU2221040C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ИНАКТИВИРОВАННОЙ КУЛЬТУРАЛЬНОЙ ВАКЦИНЫ ПРОТИВ ИНФЕКЦИОННОГО РИНОТРАКЕИТА КРУПНОГО РОГАТОГО СКОТА | 1993 |
|
RU2090210C1 |
Авторы
Даты
2006-07-10—Публикация
2004-12-29—Подача