Изобретение относится к медицине, а именно к лечению инфекционных болезней, и может быть использовано в терапии больных геморрагической лихорадкой с почечным синдромом (ГЛПС), сопровождающейся нарушением функции печени.
ГЛПС – острое вирусное природно-очаговое заболевание, характеризующееся генерализованным поражением микроциркуляторного руcла с глубоким повреждением эндотелия соcудов вируcом и изменениями в обильно кровоcнабжаемых органах: почках, головном мозге, гипофизе, надпочечниках, печени, cердце [1].
Отмечается высокая заболеваемость и летальность при ГЛПС. Так, заболеваемость в РФ в 2015 г. составила 6,31 на 100 тыс. населения, в то время как в Республике Мордовия она остается стабильно высокой (44,6 на 100 тыс. населения – в 2014 г. и 35,5 – в 2015 г.). Отмечается тяжелое течение болезни, нередко – осложненное. К числу специфических осложнений относят инфекционно-токсический шок, отек легких, уремическую кому, эклампсию, разрыв почки, кровоизлияния в мозг, надпочечники, сердечную мышцу, поджелудочную железу, массивные кровотечения. Летальность при ГЛПС в среднем по РФ составляет 1 – 8 %.
Широкая распространенность ГЛПС, частота развития и тяжесть ее осложнений определяют необходимость поиска новых средств терапевтического воздействия, направленных в первую очередь на коррекцию интоксикационного синдрома, достижение нормализации функций почек, печени, профилактику развития осложнений и хронизации патологического процесса.
При ГЛПC происходит поражение органов, имеющих богатую микроциркуляцию. При исcледовании аутопсийного материала больных c осложненной формой ГЛПС выявлены выраженные диcтрофические, некробиотические изменения cосудов во всех исследуемых органах (головной мозг, почки, печень, легкие) c преобладанием деструктивных изменений микроциркуляторного звена в почках и печени [2].
Ведущее место в патогенезе ГЛПС занимает интоксикационный синдром. Развитие его связано с феноменом вирусемии и в большей мере с накоплением эндогенных токсинов в организме, в частности, в результате активации перекисного окисления липидов [3]. Развитие оксидативного стресса и истощение системы антиоксидантной защиты обосновывают применение лекарственных средств с антиоксидантным механизмом действия [4].
Показаны дезинтоксикационный и антиоксидантный эффект эмоксипина в лечении ГЛПС среднетяжелого и тяжелого течения [5]. В других работах показана эффективность дерината в коррекции эндогенной интоксикации и иммунологических нарушений [6]. При применении анандина выявлена более быстрая позитивная динамика клинических симптомов и показателей функциональной способности почек [7].
Однако изучение интоксикационного синдрома проводилось без учета развития нарушений функции печени, которые занимают значительное место в патогенезе ГЛПС. Нарушения функции печени утяжеляют патологический процесс, затягивают время выздоровления пациентов, что также требуют проведения коррекции.
Многие авторы, учитывая характер заболевания, в оcновном обращают внимание на восстановление функции почек, cердечно-сосудистой системы [8, 9].
Имеются лишь единичные работы, поcвященные анализу клинико-функционального состояния печени у реконвалеcцентов ГЛПС [10].
Однако в периоде разгара ГЛПC у большинства пациентов наблюдается синдром реактивного гепатита [11, 12]. Выявлена высокая частота поражения печени при инфекции, обусловленной вирусами Hantaan и Amur [13].
Известен способ коррекции интоксикационного синдрома при ГЛПС с применением 5 %-ного раствора глюкозы, 0,9 %-ного раствора натрия хлорида. Дезинтоксикационную терапию целесообразно сочетать с антиоксидантами. С этой целью рекомендуется использовать 5 %-ный раствор аскорбиновой кислоты [14], витамин Е (токоферола ацетат 2 раза в день в суточной дозе 200 мг внутримышечно) [15], эмоксипин (1 % – 15,0 мл в 200,0 мл 0,9 %-ного раствора хлорида натрия внутривенно капельно, 5 дней) [16].
Известный способ в определенной мере способствует коррекции интоксикационного синдрома. Дополнительное использование аскорбиновой кислоты, витамина Е или эмоксипина не позволяет в достаточной мере корригировать оксидативные реакции. Поэтому в случаях развития у пациентов ГЛПС нарушений функции почек и печени, активации перекисного окисления липидов, снижении антиоксидантной защиты организма, являющихся важными патогенетическими факторами развития ГЛПС, подобное лечение оказывается малоэффективным, недостаточно купирует симптомы заболевания, не приводит к коррекции цитолитического синдрома, даже в случае длительной госпитализации в стационаре. Дезинтоксикационная и антиоксидантная терапия проводятся без учета развившихся в период разгара заболевания нарушений функции печени, когда необходимо применение гепатотропных средств. В настоящее время из уровня техники не найдено способов одновременной коррекции интоксикационного синдрома, оксидативных реакций и нарушений функции печени в период разгара и ранней реконвалесценции у больных ГЛПС.
Учитывая вышеизложенное, был разработан способ коррекции интоксикационного синдрома в период разгара и ранней реконвалесценции у больных ГЛПС с одновременным развитием нарушений функций почек и печени.
Технический результат заключается в сокращении продолжительности периодов заболевания, интоксикационного и цитолитического синдрома больных ГЛПС, положительном влиянии на показатели эндотоксикоза, оксидативных реакций, антиоксидантной защиты и функциональных свойств альбумина, что дает значительный социальный и экономический эффект, а также позволяет улучшить качество жизни пациентов, сократить количество дней нетрудоспособности на стационарном и амбулаторном этапах, предупредить развитие осложнений, хронизацию патологического процесса путем коррекции интоксикационного синдрома в период разгара и ранней реконвалесценции у пациентов, имеющих нарушение функций почек и печени.
Сущность изобретения заключается в том, что в способе лечения ГЛПС при развитии нарушений функции печени применяют в составе базисной терапии внутривенно капельно препарат ремаксол 400 мл 1 раз в сутки в течение 10 дней, после чего дополнительно применяют в составе комплексной терапии перорально препарат цитофлавин 2 раза в сутки по 2 таблетки и гепатопротектор метионин 250 мг 3 раза в сутки в течение 20 дней.
Ремаксол представляет собой сбалансированный инфузионный раствор, обладающий гепатопротекторным и дезинтоксикационным действием. Содержит в своем составе активные компоненты: янтарной кислоты – 5,280 г; N-метилглюкамина (меглумина) – 8,725 г; рибоксина (инозина) – 2,0 г; метионина – 0,75 г; никотинамида – 0,25 г; вспомогательные вещества: натрия хлорида – 6,0 г; калия хлорида – 0,30 г; магния хлорида (в пересчете на безводный) – 0,12 г; натрия гидроксида – 1,788 г; воды для инъекций до 1,0 л. Дезинтоксикационное действие ремаксола показано в работах [17, 18, 19].
Цитофлавин является комплексным метаболическим средством, включает в своем составе янтарную кислоту (300 мг), рибоксин (инозин) (50 мг), никотинамид (25 мг), рибофлавина натрия фосфат (рибофлавин) (5 мг). Фармакологические эффекты обусловлены комплексным воздействием входящих в состав препарата цитофлавин компонентов. Стимулирует процессы клеточного дыхания и энергообразования, улучшает процессы утилизации кислорода тканями, восстанавливает активность ферментов, обеспечивающих антиоксидантное действие [20].
Метионин согласно инструкции относится к препаратам из группы белков и аминокислот, гепатопротекторов. Фармакологическое действие – восполняющее дефицит аминокислот, метаболическое, гепатопротективное.
Способ лечения осуществляют следующим образом. После поступления пациентов в стационар и постановки диагноза «ГЛПС, средней степени тяжести», выявления нарушений функции печени (развитие цитолитического синдрома – повышение аланиновой и аспарагиновой трансаминаз) в состав базисной терапии в качестве дезинтоксикационного и гепатопротекторного средства включают препарат ремаксол 400 мл, внутривенно капельно со скоростью 40–60 капель (2–3 мл) в минуту, 1 раз в сутки в течение 10 дней. Затем в течение 20 дней дополнительно к базисной терапии назначают комплексную терапию подобного препарату ремаксол состава перорально: препарат метаболического действия цитофлавин по 2 таблетки 2 раза в сутки за 30 минут до еды (вечерний прием препарата не позднее 18 часов) и гепатопротектор метионин 250 мг 3 раза в сутки за 0,5 – 1 час до еды. Общий курс лечения составляет 30 дней.
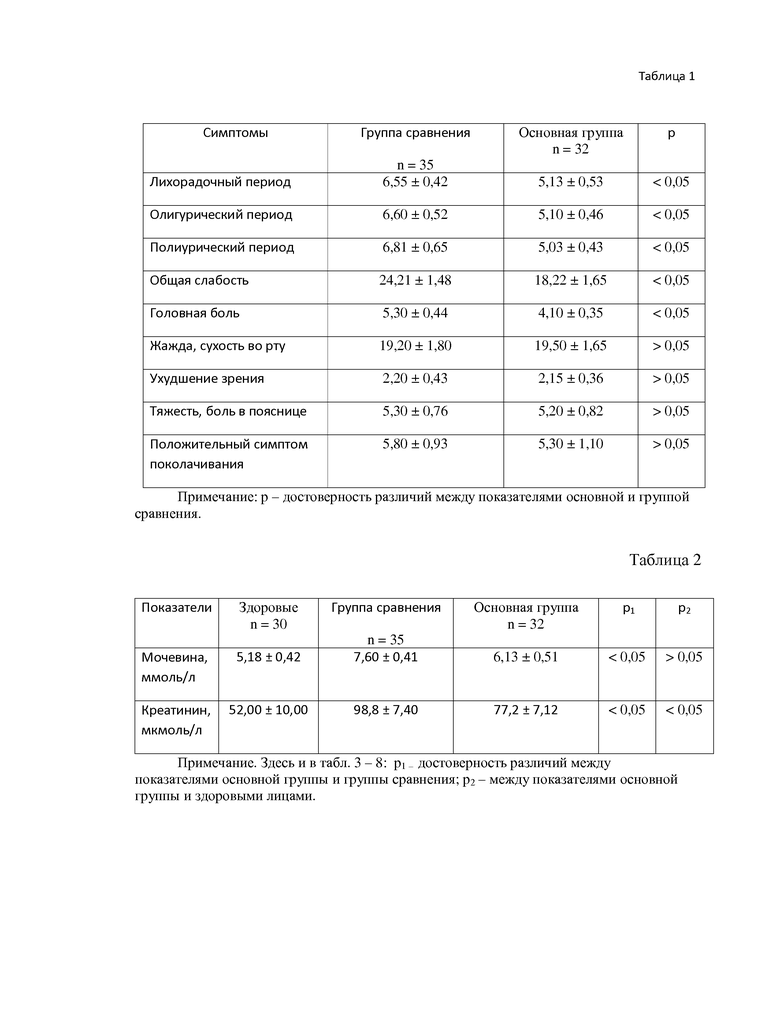
В табл. 1 показана длительность основных клинических симптомов ГЛПС на фоне различных методов терапии (М±m) (в сутках); табл. 2 – биохимические показатели функционального состояния почек на фоне различных методов терапии ГЛПС (М±m); табл. 3 – показатели функциональных проб печени на фоне различных методов терапии ГЛПС (М±m); табл. 4 – уровень молекул средней массы при ГЛПС на фоне различных методов терапии (М±m); табл. 5 – уровень продуктов перекисного окисления липидов при ГЛПС на фоне различных методов терапии (М±m); табл. 6 – активность ферментов антиоксидантной защиты при ГЛПС на фоне различных методов терапии (М±m); табл. 7 – функциональные свойства альбумина при ГЛПС на фоне различных методов терапии (М±m); табл. 8 – критерии интоксикации на фоне различных методов терапии ГЛПС (М ± m).
Для оценки эффективности терапии больные были разделены на 2 группы. Первая группа (группа сравнения) – 30 пациентов со среднетяжелым течением ГЛПС получала базисную терапию. Второй (основной) группе из 32 пациентов среднетяжелого течения ГЛПС назначали внутривенно капельно ремаксол (400 мл) в течение 10 дней, затем цитофлавин (по 2 таблетки 2 раза в сутки) в сочетании с метионином (250 мг 3 раза в сутки) в течение 20 дней. Для контроля проводимых лабораторных показателей исследовали группу практически здоровых лиц (30 человек).
Биохимические показатели крови (мочевина, креатинин, трансаминазы, билирубин) определяли общепринятыми способами с использованием реактивов фирмы «Агат» (Камышников В.С., 2004). Интенсивность реакций перекисного окисления липидов (ПОЛ) оценивали по накоплению малонового диальдегида плазмы и эритроцитов (МДАпл и МДАэр) (Егоров Д.Ю., Козлов А.В., 1988), диеновых конъюгатов (ДКо) и кетонов (ДКе), по методу Плацера и соавт. (Камышников В.С., 2004). Состояние антиоксидантной защиты оценивали по активности каталазы плазмы (Кпл) и эритроцитов (Кэр) (Королюк М.А. и соавт., 1988) и супероксиддисмутазы (СОД) (Дубинина Е.Е., 1993). О гидрофильном компоненте токсичности судили по накоплению в крови молекул средней массы (МСМ) (Николайчик В.В. и соавт., 1991). Гидрофобный компонент эндогенной интоксикации оценивали, определяя общую и эффективную концентрацию альбумина (ОКА и ЭКА) флуоресцентным методом на анализаторе АКЛ-01 с помощью набора реактивов «Зонд-альбумин». Рассчитывали индекс токсичности (ИТ) по формуле: ИТ=(ОКА/ЭКА) – 1 и связывающую способность альбумина (ССА) по формуле: ССА=ЭКА/ОКА×100 (Миллер Ю.И., Добрецов Г.Е., 1994). На основе отношения показателей МСМ и ЭКА рассчитывали критерии интоксикации (КИ): КИ1=(МСМ254/ЭКА)×1000, КИ2 = (МСМ280/ЭКА)×1000, КИ3=(МСМ254/ОКА) × 1000 (Гаврилов В.Б. и соавт., 1998). Циркулирующие иммунные комплексы (ЦИК) в сыворотке крови определяли методом преципитации с 3,5 %-ным раствором полиэтиленгликоля (полиэтиленгликоль 6000 «Serva») (Лебедев К.А., Понякина И.Д., 1990).
Обследование проводили при поступлении пациента в стационар и после проведения 30-дневного курса терапии. Применение предлагаемого способа значимо способствовало сокращению продолжительности (на 3 койко-дня) стационарного лечения в сравнении с группой больных, получавших только общепринятую патогенетическую терапию. Средняя продолжительность стационарного лечения в группе сравнения составила 17,06±0,85 койко-дней, в основной группе – 14,02±0,61 койко-дней (р<0,05). Общая продолжительность дней нетрудоспособности на стационарном и амбулаторном этапе также сокращалась и составила в группе сравнения 31,12±1,28 дней, в основной группе – 27,10±1,31 день (р<0,05).
Базисная терапия
В связи с поступлением пациентов в стационар на 4 – 5 день болезни, в конце лихорадочного периода, этиотропная терапия не назначалась. Патогенетическая терапия заключалась в следующем: в олигурический период (с момента поступления) пациенты со среднетяжелым течением получали внутривенно капельно 200–400 мл 0,9 %-ного раствора хлорида натрия с 5,0 мл 5 %-ного раствора аскорбиновой кислоты, 200–400 мл 5 %-ного раствора глюкозы с 5 мл 2,4 %-ного раствора эуфиллина, лазикс 20–40 мг 1-2 раза в стуки, диазолин по 100 мг 3 раза в сутки, аскорутин по 1 таблетке 3 раза в сутки. Симптоматическая терапия представлена жаропонижающими средствами – парацетамол 200–400 мг при повышении температуры тела выше 38,5 °С, при отсутствии эффекта внутримышечно вводили литическую смесь – 2 мл 50 %-ного раствора анальгина и 1 мл 1 %-ного раствора димедрола, спазмолитиками – 2 мл 2 %-ного раствора папаверина гидрохлорида внутримышечно, 2 раза в день, при рвоте внутримышечно назначался церукал по 2 мл внутрь 0,25 %-ный раствор новокаина по 1 столовой ложке 3 раза в день. С целью предупреждения бактериальных осложнений внутривенно капельно назначался цефтриаксон по 2000 мг 1 раз в сутки. В полиурический период отменяли мочегонные средства и назначали внутривенное введение 0,9 %-ного раствора хлорида натрия, комплексных солевых растворов – «Трисоль», «Хлосоль», затем панангин (по 1 таблетки 3 раза в сутки).
В качестве критериев оценки эффективности дезинтоксикационной, антиоксидантной и гепатопротекторной терапии были определены следующие показатели:
1) клинические – длительность лихорадки, головной боли, общей слабости, жажды, сухости во рту, боли в пояснице, олигурии, полиурии;
2) биохимические – уровень мочевины, креатинина, билирубина, аланиновой и аспарагиновой трансаминаз;
3) эндогенной интоксикации – (МСМ при λ 254 и 280 нм), ЦИК, функционального состояния альбумина – ОКА и ЭКА, ССА, ИТ, КИ;
4) оксидативных реакций и антиоксидантной защиты – малонового диальдегида плазмы и эритроцитов, каталазы плазмы и эритроцитов, супероксиддисмутазы.
Предлагаемый способ позволяет сократить продолжительность лихорадочного, олигурического, полиурического периодов и таких симптомов как общая слабость, головная боль, по сравнению с группой больных, получавших только общепринятую патогенетическую терапию.
При сравнительном изучении влияния патогенетической терапии в двух исследуемых группах на клиническое течение больных ГЛПС отмечено, что длительность лихорадочного периода укорачивалась с 6,55 ± 0,42 дней до 5,13 ± 0,53 дней (р<0,05). Продолжительность олигурического периода сокращалась, в группе сравнения составив 6,60±0,52 дня, а в основной 5,10±0,46 дня (р<0,05). Полиурический период был значительно длиннее в группе сравнения – 6,81±0,65 дня, чем в основной группе – 5,03 ± 0,43 дня. Сокращалась длительность таких симптомов как общая слабость (с 24,21±1,48 до 18,22±1,65 дней (р<0,05)) и головная боль (с 5,30±0,72 до 4,10±0,31 дня; р<0,05). Время сохранения жажды, нарушения зрения и болей в пояснице не изменялись (табл. 1).
После проведения комплексной ступенчатой терапии больным ГЛПС основной группы наблюдалась положительная динамика лабораторных показателей азотовыделительной функции почек (мочевины и креатинина) по сравнению с больными группы сравнения. После окончания терапии, к периоду ранней реконвалесценции значения этих показателей достоверно отличались в исследуемых группах и были ниже в основной группе (табл. 2).
Изучая показатели функциональных проб печени на фоне различных методов терапии, выявлено, что пигментный обмен не изменялся. Цитолитический синдром на фоне базисной терапии наблюдался в течение всего периода наблюдения – аланиновая трансаминаза (АлТ) была повышена после окончания базисной терапии в 3,75 раза, АсТ – в 3 раза. Проводимая терапия в основной группе способствовала снижению активности трансаминаз – АлТ в 2,25 раза, АсТ в 2 раза, приводя к нормализации данного показателя (р<0,001) (табл. 3). Все это свидетельствует о гепатопротекторном эффекте терапии с включением препаратов ремаксол, цитофлавин и метионин в течение 30 дней.
Таким образом, комплексная терапия интоксикационного синдрома при ГЛПС с включением ремаксола, цитофлавина и метионина в течение 30 дней способствовала уменьшению длительности основных периодов болезни (лихорадочного, олигурического и полиурического) и клинических признаков интоксикации, а также снижала содержание азотистых шлаков, показатели синдрома цитолиза.
По результатам исследования выраженности эндогенной интоксикации гидрофильного компонента токсичности в группе сравнения установлено, что содержание среднемолекулярных пептидов было достоверно повышенным к периоду ранней реконвалесценции пациентов. В основной группе пациентов уровень МСМ254 и МСМ280 снижался в 1,2 раза, при этом содержание МСМ при обеих длинах волн достигло значений здоровых лиц (р>0,05) (табл. 4). Следовательно, включение препаратов ремаксола, цитофлавина и метионина в комплексную терапию ГЛПС приводит к уменьшению уровня гидрофильных компонентов токсичности в крови, что может говорить о снижении эндогенной интоксикации.
Другим показателем эндогенной интоксикации являются циркулирующие иммунные комплексы, особенно мелкого диаметра (ЦИКм). В основной группе пациентов их уровень снизился в 1,5 раза по отношению к группе сравнения (табл. 4). Следовательно, комплексная терапия ГЛПС способствует уменьшению синдрома эндотоксикоза и может препятствовать развитию «иммунокомплексного» синдрома.
Одной из причин формирования эндогенной интоксикации и затяжного течения инфекционного процесса может выступать активность ПОЛ. К периоду ранней реконвалесценции сохраняется высокая интенсивность процессов липопероксидации, что сопровождается накоплением в крови промежуточных токсических продуктов липопереокисления. Включение в терапию основной группы препаратов с антиоксидантным эффектом в комплекс лечебных мероприятий ГЛПС позволило повлиять на свободнорадикальные процессы ПОЛ, способствуя снижению их интенсивности. Доказательством этому служит уменьшение в крови концентрации первичных и вторичных продуктов ПОЛ. Так, содержание ДКо снижалось в 1,6 раза (р<0,01), ДКе – в 1,9 раза (р<0,01), МДАпл– в 2 раза (р<0,001), МДАэр – в 1,5 раза (р<0,001) по сравнению с результатами в группе сравнения (табл. 5).
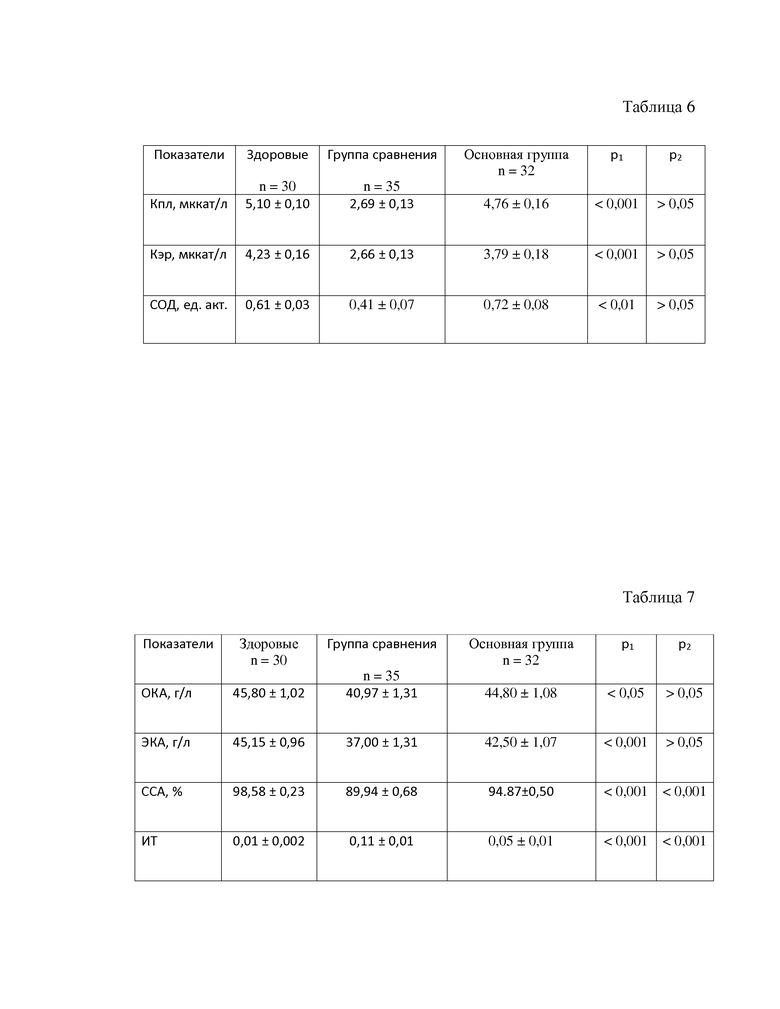
После проведения базисной терапии в группе сравнения, выявлено значительное снижение активности ключевых антиоксидантных ферментов (Кпл, Кэр и СОД). В основной группе пациентов активность антиоксидантных ферментов была достоверно выше. Так, активность Кпл повышалась в 1,8 раза (р<0,001), Кэр – в 1,4 раза (р<0,001), СОД – в 1,8 раза (р<0,01) по сравнению с показателями в группе сравнения, при этом активность изучаемых ферментов антиоксидантной системы достигала уровня здоровых лиц (табл. 6).
При изучении гидрофобного компонента токсичности установлено снижение детоксикационных свойств альбумина при ГЛПС, которое в группе сравнения после базисной терапии сохранялось к периоду клинического выздоровления пациентов. В основной группе пациентов отмечена позитивная динамика альбуминовых параметров, повышались ОКА и ЭКА до уровня здоровых лиц (р>0,05), что свидетельствует об уменьшении выраженности эндогенной интоксикации. В основной группе к периоду ранней реконвалесценции ССА была выше, а ИТ ниже, чем в группе сравнения (табл. 7).
Таким образом, предлагаемый способ терапии в комплексной терапии среднетяжелых форм ГЛПС способствует снижению выраженности эндогенной интоксикации: уменьшается содержание как гидрофильных, так и гидрофобных компонентов эндотоксикоза.
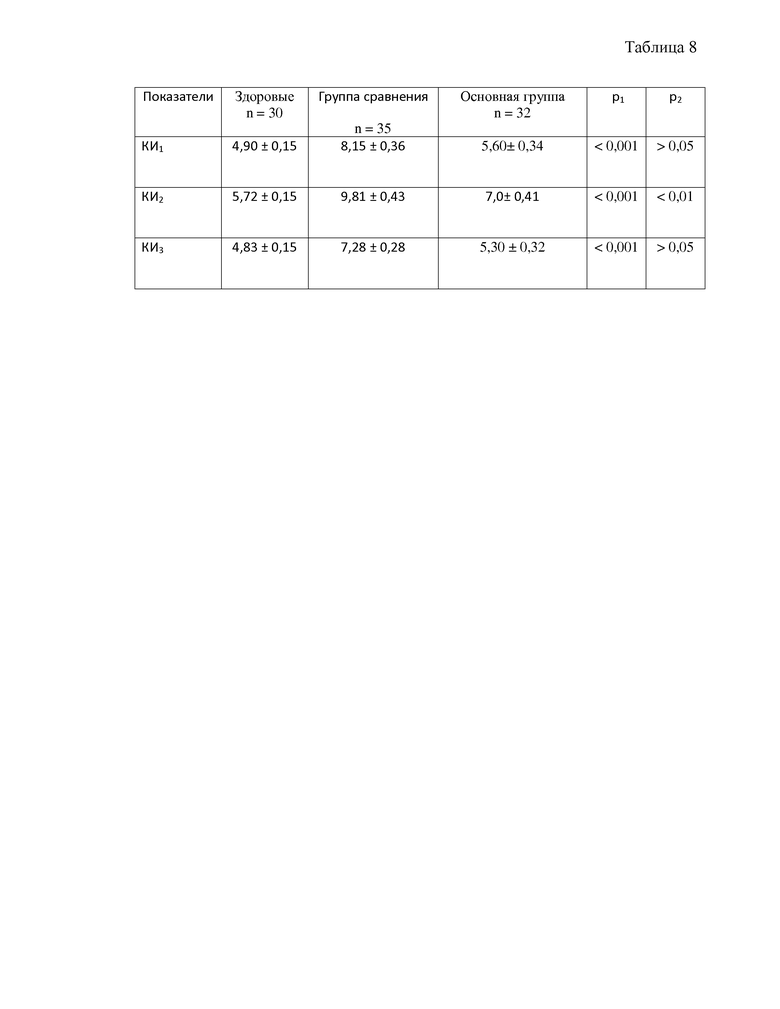
О сохранении высокого уровня эндотоксикоза к периоду клинического выздоровления пациентов с ГЛПС свидетельствует повышение КИ. Комплексная терапия в основной группе пациентов способствовала снижению всех трех критериев интоксикации, так КИ1 и КИ3 снижались соответственно в 1,5 и 1,4 раза (р<0,001), что не отличалось от уровня здоровых лиц, КИ2 уменьшался в 1,4 раза (р<0,001), но оставался выше показателя здоровых лиц (табл. 8). Такая динамика критериев интоксикации свидетельствует об уменьшении образования токсических метаболитов в крови и соответственно об уменьшении уровня эндогенной интоксикации.
Клинический пример, иллюстрирующий полученные результаты в группе больных со среднетяжелым течением ГЛПС
Больной С., 42 года. Находился в отделении № 4 ГБУЗ РМ «Республиканская инфекционная клиническая больница» г. Саранска с 19.02.2015 г. по 05.03.2015 г. с диагнозом «ГЛПС, средней степени тяжести». Диагноз подтвержден серологическим методом, в реакции иммуноферментного анализа (ИФА) с антигеном вируса ГЛПС от 26.02.2015 г. (10-й день болезни). Обнаружены IgM к Хантавирусам в титре 1:800.
Поступил в стационар на 5-й день болезни с жалобами на общую слабость, повышение температуры тела до 39 °С с ознобом, ломоту в теле, головную боль, тяжесть в поясничной области. Заболел остро, 15.02.2015 г., когда повысилась температура тела до 39 °С, в последующие дни сохранявшаяся на высоком уровне, беспокоила головная боль, была рвота, на 4-й день болезни появились боли в поясничной области. Принимал ингавирин, флемоксин, без эффекта.
На 5-й день болезни обратился к участковому терапевту, направлен в ГБУЗ РМ «Республиканская инфекционная клиническая больница» с диагнозом «Острая респираторная вирусная инфекция, тяжелое течение».
Эпидемиологический анамнез: работает слесарем в МП «Горводоканал» г. Саранска.
При поступлении в стационар состояние пациента оценивалось средней степени тяжести. Сохранялась высокая температура тела 38,5–39 °С, боль в пояснице, появилось нарушение зрения в виде тумана перед глазами. При осмотре – выражена инъекция сосудов склер, умеренная гиперемия задней стенки глотки, единичные петехиальные элементы на мягком небе. Пульс 100 ударов в минуту, артериальное давление – 120 и 80 мм рт. ст. Язык сухой, слегка обложен белым налетом. Живот вздут, болезненный в эпигастральной области. Печень увеличена, выступает из-под края реберной дуги на 2,5 см. Поколачивание по поясничной области слегка болезненное с обеих сторон. При поступлении в стационар был выставлен предварительный диагноз «ГЛПС, средней степени тяжести». В биохимическом анализе крови от 20.02.2015 г. выявлено повышение АлТ в 3,5 раза, АсТ – в 2,3 раза (через 7 дней терапии наблюдался рост АлТ в 7 раз, АсТ – в 2,4 раза). В связи с чем пациенту на фоне базисной терапии в качестве дезинтоксикационного и гепатопротекторного средства назначали в течение 10 дней внутривенно капельно ремаксол 400 мл со скоростью 40 – 60 капель (2 – 3 мл) в минуту.
Затем в течение 20 дней дополнительно к базисной терапии назначали комплексную терапию подобного препарату ремаксол состава перорально: препарат метаболического действия цитофлавин по 2 таблетки 2 раза в сутки за 30 минут до еды (вечерний прием препарата не позднее 18 часов) и гепатопротектор метионин 250 мг 3 раза в сутки за 0,5 – 1 час до еды. Общий курс лечения составил 30 дней.
На фоне проводимой терапии температура снизилась на 2-й день лечения, олигурия до 500 мл держалась в течение 3-х дней, боли в пояснице – 3 дня, полиурия до 3,5 литров в сутки – 5 дней, общая слабость – 15 дней. Дальнейшее течение было гладким, без осложнений и пациент был выписан в удовлетворительном состоянии.
Лабораторные данные – в день поступления и через 30 дней лечения:
20.02.15 г.: Общий анализ крови: гемоглобин – 147 г/л, лейкоциты – 5,1×109/л, СОЭ – 24 мм/ч. Общий анализ мочи: белок – 660 мг/л, удельный вес – 1006, лейкоциты – 1–2 в поле зрения, эритроциты – 1–2 в поле зрения.
21.03.15 г.: Общий анализ крови: гемоглобин – 132 г/л, лейкоциты – 4,2×109/л, СОЭ – 11 мм/ч. Общий анализ мочи: белок – нет, удельный вес – 1008, лейкоциты – 1–2 в поле зрения, эритроциты – 0 в поле зрения.
Биохимический анализ крови:
20.02.15 г.: Мочевина – 5,1 ммоль/л, креатинин – 116 мкмоль/л, АлТ – 129 ед/л, АсТ – 93 ед/л, билирубин общий – 8,1 мкмоль/л.
26.02.15 г.: Мочевина – 5,8 ммоль/л, креатинин – 88 мкмоль/л, АлТ –292 ед/л, АсТ – 94 ед/л, билирубин общий – 7,8 мкмоль/л.
21.03.15 г.: Мочевина – 4,2 ммоль/л, креатинин – 64 мкмол/л, АлТ – 45 ед/л, АсТ – 38 ммоль/(л·ч), билирубин общий – 7,5 мкмоль/л.
Показатели эндотоксикоза:
20.02.15 г.: МСМ254 – 0,441 у.е., МСМ280 – 0,388 у.е., ЦИК мелкие – 136 у.е.
21.03.15 г.: МСМ254 – 0,224 у.е., МСМ280 – 0,257 у.е., ЦИК мелкие – 75 у.е.
Альбуминовые тесты.
20.02.15 г.: ОКА – 39 г/л, ЭКА – 34 г/л, ССА – 87,17 %, ИТ – 0,15.
21.03.15 г.: ОКА – 45 г/л, ЭКА – 43,5 г/л, ССА – 96,66 %, ИТ – 0,034.
Критерии интоксикации:
20.02.15 г.: КИ1 = (0,441/34)× 1000 = 12,97; КИ2 = (0,388/34) × 1000 = 11,41; КИ3 = (0,441/39) × 1000 = 11,3.
21.03.15 г.: КИ1 = (0,224/43,5) × 1000 = 5,15; КИ2 = (0,257/43,5) × 1000 = 5,91; КИ3 = (0,224/45) × 1000 = 4,98.
Показатели оксидативных реакций и антиоксидантной защиты:
20.02.15 г.: ДКо – 0,398 ед/мл, ДКе – 0,166 ед/мл, МДАпл – 6,87 мкмоль/л, МДАэр – 36,93 мкмоль/л, каталаза плазмы – 2,56 мккат/л, каталаза эритроцитов – 2,2 мккат/л, СОД – 0,35 ед. акт.
21.03.15 г.: ДКо – 0,261 ед/мл, ДКе – 0,082 ед/мл, МДАпл – 2,64 мкмоль/л, МДАэр – 18,42 мкмоль/л, каталаза плазмы – 4,83 мккат/л, каталаза эритроцитов – 4,09 мккат/л, СОД – 0,66 ед. акт.
Таким образом, лечение предлагаемым способом показало положительное влияние на клиническое течение заболевания, цитолитический синдром, показатели эндотоксикоза, оксидантно-антиоксидантного статуса и функционального состояния альбумина.
По сравнению с известным решением предлагаемое позволяет сократить продолжительность периодов заболевания, интоксикационного и цитолитического синдрома, оказывая положительное влияние на показатели эндотоксикоза, оксидативных реакций, антиоксидантной защиты и функциональных свойств альбумина, что дает значительный социальный и экономический эффект, а также позволяет улучшить качество жизни пациентов, сократить количество дней нетрудоспособности на стационарном и амбулаторном этапах, предупредить развитие осложнений, хронизацию патологического процесса.
Литература
1. Сиротин Б.З. Очерки изучения геморрагической лихорадки с почечным синдромом. – Хабаровск : РИОТИП, 2005. – 194 с.
2. Байгильдина А.А., Галиева А.Т., Камилов Ф.Х. Патогенетическое значение некоторых цитокинов и белка клеточной адгезии VCAM-1 в развитии воспалительных изменений эндотелия сосудов при геморрагической лихорадке с почечным синдромом // Морфологические ведомости. – 2008. – №3-4. – С. 158–161.
3. Кузнецов В.И., Ющук Н.Д., Моррисон В.В. Свободнорадикальное окисление эритроцитарных мембран у реконвалесцентов геморрагической лихорадкой с почечным синдромом // Инфекционные болезни. – 2004. – Т. 2, № 1. – С. 55–58.
4. Павелкина В.Ф., Ласеева М.Г., Пак С.Г., Еровиченков А.А. Интоксикационный синдром у больных геморрагической лихорадкой с почечным синдромом // Инфекционные болезни. – 2008. – Т. 6, №1. – С. 41–46.
5. Павелкина В.Ф., Ласеева М.Г. Способ лечения геморрагической лихорадки с почечным синдромом. Патент на изобретение № 2379034 РФ; заявл. 17.11.2008; опубл. 20.01.10. – Бюл. №2. – 10 с.
6. Аршинцева Е.Г. Патофизиологическое обоснование применения дерината в комплексной терапии геморрагической лихорадки с почечным синдромом: автореф. дис. … канд. мед. наук. – Саранск, 2006. – 17 с.
7. Бурганова А.Н., Хунафина Д.Х., Алехин Е.К. Сравнительная эффективность анандина и йодантипирина при лечении геморрагической лихорадки с почечным синдромом // Iнфекцii в практицi клiнiциста. Антибактерi та антивiрусна терапiя на догоспiтальному та госпiтальному етапах: Матерiали науково-практичноi конференцii з мiжнародною участю. – Харкiв, 2008. – С. 73–74.
8. Фазлыева Р.М., Мирсаева Г.Х., Ибрагимова Л.А. и соавт. Отдаленные последствия у реконвалесцентов геморрагической лихорадкой с почечным синдромом // Геморрагическая лихорадка с почечным синдромом: история изучения и современное состояние эпидемиологии, патогенеза, диагностики, лечения и профилактики: материалы Всерос. науч.-практ. конф. – Уфа, 2006. – C. 105–112.
9. Дударев М.В., Пименов Л.Т. Отдаленные исходы и формирование хронической почечной недостаточности у перенесших геморрагическую лихорадку с почечным синдромом // Тер. архив. – 2008. – №6. – С. 59–62.
10. Дударев М.В. Клинико-функциональная характеристика последствий геморрагической лихорадки с почечным синдромом и их лечебная коррекция на амбулаторном этапе реабилитации: автореф. дисс.. д-ра мед. наук. – Уфа, 2005. – 48 с.
11. Убоженко И.В., Кленцова И.П. Синдром гепатита у больных ГЛПС, обусловленный вирусом Сеул // Инфекционные болезни. – 2009. – № 7. – С. 213–215;
12. Иванова М.В., Воробьева Н.Н., Шмагель К.В., Малкова А.М., Костарев А.А. Клинико-эпидемиологические особенности течения геморрагической лихорадки с почечным синдромом в Пермском крае // Журнал инфектологии. – 2011. – Т. 3, №3. – С. 66–73).
13. Слонова Р.А., Компанец Г.Г., Иванис В.А., Максема И.Г., Афанасьева В.И. Особенности клинических проявлений геморрагической лихорадки с почечным синдромом (ГЛПС) в Приморском крае // Дезинфекционное дело – 2011. – №2. – С. 22–25.
14. Рощупкин В.И. Суздальцев А.А. Геморрагическая лихорадка с почечным синдромом. – Самара: СГМУ, 2003. – 64 с.).
15. Геморрагическая лихорадка с почечным синдромом: актуальные проблемы эпидемиологии, патогенеза, диагностики, лечения и профилактики / Под ред. акад. АН РБ Р.Ш. Магазова. – Уфа: Гилем, 2006. – 240 с.
16. . Павелкина В.Ф., Ласеева М.Г. Реабилитация больных интоксикационным синдромом при геморрагической лихорадке с почечным синдромом на этапе стационарного лечения // Вестник восстановительной медицины. – 2009. – №2 (30). – С. 82–87.
17. Шилов В.В., Шикалова И.А., Васильев С.А., Лоладзе А.Т., Батоцыренов Б.В. Особенности фармакологической коррекции токсических поражений печени у больных с синдромом зависимости от алкоголя и тяжелыми формами острых отравлений этанолом // Журнал неврологии и психиатрии. – 2012. – №1. – С. 45–48.
18. Семенов В.Б. Инфузионная терапия больных желчнокаменной болезнью, осложненной механической желтухой: автореф. дис. … канд. мед. наук. – М., 2012. – 24 с.
19. Павелкина В.Ф., Ускова Ю.Г. Сравнительная эффективность дезинтоксикационной активности ремаксола и эссенциале Н при хронических вирусных гепатитах // Экспериментальная и клиническая фармакология. – 2015. – Т. 78, № 10. – С. 21–26).
20. Заплутанов В.А. Цитофлавин: сборник научных статей (2006 – 2007). – СПб: ООО «Тактик-Студио». – 2008. – 168 с.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ ГЕМОРРАГИЧЕСКОЙ ЛИХОРАДКИ С ПОЧЕЧНЫМ СИНДРОМОМ | 2008 |
|
RU2379034C1 |
| СПОСОБ ЛЕЧЕНИЯ ГЕМОРРАГИЧЕСКОЙ ЛИХОРАДКИ С ПОЧЕЧНЫМ СИНДРОМОМ СРЕДНЕТЯЖЕЛОЙ И ТЯЖЕЛОЙ ФОРМ | 2005 |
|
RU2289456C1 |
| СПОСОБ ЛЕЧЕНИЯ ГЕМОРРАГИЧЕСКОЙ ЛИХОРАДКИ С ПОЧЕЧНЫМ СИНДРОМОМ | 2002 |
|
RU2228196C1 |
| СПОСОБ ДИАГНОСТИКИ СТЕПЕНИ ТЯЖЕСТИ ГЕМОРРАГИЧЕСКОЙ ЛИХОРАДКИ С ПОЧЕЧНЫМ СИНДРОМОМ ПО ПОКАЗАТЕЛЯМ ФУНКЦИОНАЛЬНОГО РЕЗЕРВА ФАГОЦИТАРНОГО ЗВЕНА СИСТЕМЫ ИММУНИТЕТА | 2023 |
|
RU2800407C1 |
| СПОСОБ ОЦЕНКИ ТЯЖЕСТИ ТЕЧЕНИЯ ГЕМОРРАГИЧЕСКОЙ ЛИХОРАДКИ С ПОЧЕЧНЫМ СИНДРОМОМ | 1998 |
|
RU2155337C1 |
| СПОСОБ ОЦЕНКИ ТЯЖЕСТИ ТЕЧЕНИЯ ГЕМОРРАГИЧЕСКОЙ ЛИХОРАДКИ С ПОЧЕЧНЫМ СИНДРОМОМ | 2009 |
|
RU2392858C1 |
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ НЕАЛКОГОЛЬНЫМ СТЕАТОГЕПАТИТОМ НА ФОНЕ МЕТАБОЛИЧЕСКОГО СИНДРОМА | 2015 |
|
RU2595815C1 |
| СПОСОБ ЛЕЧЕНИЯ ГЕМОРРАГИЧЕСКОЙ ЛИХОРАДКИ С ПОЧЕЧНЫМ СИНДРОМОМ | 2000 |
|
RU2181046C2 |
| СПОСОБ ЛЕЧЕНИЯ ТЯЖЕЛЫХ ФОРМ ГЛПС | 1995 |
|
RU2119356C1 |
| СПОСОБ ЛЕЧЕНИЯ ИНТОКСИКАЦИОННЫХ ПСИХОЗОВ ПО ТИПУ ДЕЛИРИОЗНОГО ПОМРАЧЕНИЯ СОЗНАНИЯ | 2017 |
|
RU2676698C1 |

Изобретение относится к медицине и предназначено для лечения больных геморрагической лихорадкой с почечным синдромом (ГЛПС), сопровождающейся нарушением функции печени. В составе базисной терапии применяют внутривенно капельно препарат ремаксол 400 мл 1 раз в сутки в течение 10 дней. Дополнительно применяют в составе комплексной терапии перорально препарат цитофлавин 2 раза в сутки по 2 таблетки и гепатопротектор метионин 250 мг 3 раза в сутки в течение 20 дней. Способ позволяет сократить продолжительность заболевания, уменьшить проявления интоксикационного и цитолитического синдромов, улучшить качество жизни пациентов. 8 табл., 1 пр.
Способ лечения больных геморрагической лихорадкой с почечным синдромом при развитии нарушений функции печени, включающий применение в составе базисной терапии внутривенно капельно препарата ремаксол 400 мл 1 раз в сутки в течение 10 дней, после чего дополнительно применяют в составе комплексной терапии перорально препарат цитофлавин 2 раза в сутки по 2 таблетки и гепатопротектор метионин 250 мг 3 раза в сутки в течение 20 дней.
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ ГЕМОРРАГИЧЕСКОЙ ЛИХОРАДКОЙ С ПОЧЕЧНЫМ СИНДРОМОМ (ГЛПС) | 2001 |
|
RU2196576C1 |
| WO2014158123 A1, 02.10.2014 | |||
| ВЛАСОВ А | |||
| П | |||
| и др., Влияние Ремаксола на состояние гуморального компонента системы гемостаза в ранние сроки острого панкреатита, "Экcпеpиментальная и клиническая фармакология", 2015, Том 18, N 9, с | |||
| Насос | 1917 |
|
SU13A1 |
| ZHONGGUO ZHONG XI et al, Observation on therapeutic effect of Rhubarb and sanchi powder in treating patients with hemorrhagic fever in nephrotic syndrome complicated with digestive tract bleeding, 2005 Aug;25 N (8), c | |||
| КОННОПРИВОДНОЙ ПОРШНЕВОЙ НАСОС | 1922 |
|
SU744A1 |
Авторы
Даты
2018-02-15—Публикация
2016-10-28—Подача