Изобретение относится к медицине, а именно к экспериментальной хирургии, и может быть использовано с целью профилактики кровотечений на фоне применения варфарина в эксперименте.
Применение варфарина показано при пароксизмальной или постоянной формах мерцательной аритмии и в случаях наличия внутрисердечного тромбоза, угрозе возникновения эмболических мозговых инсультов. Длительный прием варфарина используется также после трансплантации клапанов сердца и при всех других ситуациях, когда необходима продленная (в течение месяцев и лет), либо пожизненная антитромботическая терапия (Диагностика и лечение фибрилляции предсердий. Рекомендации РКО, ВНОА и АССХ, 2012 г. - 112 С.).
Одним из основных осложнений при варфаринотерапии считаются кровотечения, которые при геморрагическом инсульте, макрогематурии и обширных кишечных кровотечениях могут привести к летальному исходу (Ansell, J. Pharmacology and Management of the Vitamin K Antagonists / J. Ansell, J. Hirsh, E. Hylek et al // Chest. - 2008. - Vol. 133. - P. 160-198.). Риск тяжелой кровопотери у пациентов, принимающих варфарин, резко увеличивается при травмах или неотложных хирургических вмешательствах, выполненных по жизненным показаниям. Это связано с тем, что после отмены антикоагулянтное действие варфарина сохраняется около 5 суток. Поэтому в настоящее время является актуальным создание эффективных способов профилактики кровотечений с использованием новых современных препаратов, позволяющих быстро, с минимальным количеством побочных эффектов снижать объем кровопотери.
Известен способ профилактики и лечения кровотечений, вызванных применением варфарина, путем применения свежезамороженной плазмы (Городецкий, В.М. Инфузионно-трансфузионная терапия / В.М. Городецкий, Г.М. Галстян, Е.М. Шулутко // Интенсивная терапия: национальное руководство: в 2 т. / под ред. Б.Р. Гельфанда, А.И. Салтанова. - М.: ГЭОТАР-Медиа, 2011. - Т. 1. - С. 187-189.). Свежезамороженную плазму переливают внутривенно из расчета 15 мл/кг массы тела с последующим, через 4-8 часов, повторным переливанием в объеме 5-10 мл/кг.
Свежезамороженная плазма содержит в своем составе близкий к физиологическому уровню весь комплекс факторов протромбинового комплекса (факторы II, V, VII, X), синтез которых в клетках печени нарушается варфарином, что приводит к низкой эффективности известного способа, а его использование сопряжено с риском инфекционных осложнений, связанных с трансфузией, а именно: острое повреждение легких (TRALI - transfusion-related acute lung injury), аллергические реакции, иммуносупрессия (Колосков, А.В. Современные представления о показаниях для трансфузии свежезамороженной плазмы / А.В. Колосков // Гематология и трансфузиология. - 2005. - №6. - С. 41-45.). Кроме того, свежезамороженную плазму рекомендуют реже и из-за того, что она менее стандартизирована по содержанию факторов свертывания и может быть причиной перегрузки объемом, особенно у кардиальных больных (Суханова, Г.А. Возможности применения препарата Протромплекс в клинической практике / Г.А. Суханова, В.В. Вдовин, П.В. Свирин // Тромбоз, гемостаз и реология. - 2011. - №1(45). - С. 24.).
Наиболее близким по достигаемому техническому результату способом профилактики и лечения кровотечений, вызванных применением варфарина, является применение концентрата протромбинового комплекса (препарат Протромплекс фирмы Baxter AG, США), состоящего их 4-х (II, VII, IX, X) витамин К-зависимых факторов свертывания (Leal-Noval SR. / _Efficacy of the prothrombin complex concentrate prothromplex in patients requiring urgent reversal of vitamin K antagonists or presenting with uncontrolled bleeding: a retrospective, single center study / Leal-Noval SR,  R, Bautista-Paloma J, Casado M, Arellano-Orden V, Leal-Romero M,
R, Bautista-Paloma J, Casado M, Arellano-Orden V, Leal-Romero M,  E, Puppo-Moreno A,
E, Puppo-Moreno A,  M. / Blood Coagul Fibrinolysis. 2013 Dec; 24(8):862-8. doi: 10.1097/MBC.0b013e3283650cf9.).
M. / Blood Coagul Fibrinolysis. 2013 Dec; 24(8):862-8. doi: 10.1097/MBC.0b013e3283650cf9.).
Концентрат протромбинового комплекса назначают внутривенно в виде раствора в дозе 25-50 МЕ/кг массы тела. Разовую дозу и частоту введения устанавливают индивидуально с учетом исходных показателей системы свертывания, локализации и выраженности кровотечения, клинического состояния пациента.
Однако известный способ обладает низкой эффективностью и может быть связан с риском возникновения побочных эффектов, а именно: артериальные и венозные тромбозы (Zemrak, W.R. Thrombotic complications following the administration of high-dose prothrombin complex concentrate for acute warfarin reversal / W.R. Zemrak, E. Kelley, N.L. Kovacic et al // Am. J. Emerg. Med. - 2016. - Vol. 8:1736.e1-3. doi: 10.1016;) и связанные с ними тромбоэмболические осложнения (Barton, С.А. Risk of thromboembolic events after protocolized warfarin reversal with 3-factor PCC and factor VIIa / C.A. Barton, N.B. Johnson, J. Case et al // Am. J. Emerg. Med. - 2015. - Vol. - 11:1562-6. doi: 10.1016), острое повреждение почек (Christian, J.W. A word of caution on renal risks of prothrombin complex concentrate use in cardiac surgery / J.W. Christian // Crit Care. 2016; 20: 63. doi: 10.1186/s13054-016-1254-0), инфаркт миокарда, синдром диссеминированного внутрисосудистого свертывания, анафилактические реакции (Инструкция по применению препарата Протромплекс 600. - рег. №: ЛСР-010486/08 от 24.12.08. - Компания Бакстер, США. - Код ATX: B02BD01).
Авторы предлагают эффективный способ профилактики кровотечений, вызванных применением варфарина в эксперименте, позволяющий клинически значимо предотвращать кровопотерю путем применения фибрин-мономера, который является белком, получаемым из стерильной плазмы человека. Фибрин-мономер не является антидотом варфарина и быть использован в качестве системного гемостатического средства, не требует дополнительного использования свежезамороженной плазмы. Фибрин-мономер обеспечивает быструю и стойкую остановку интраоперационного паренхиматозного кровотечения в эксперименте на животных, а так же «in vitro» при добавлении к человеческой плазме пацианта, получающего варфарин, и приводит к быстрому формированию стойкого сгустка фибрина.
Фибрин-мономер является первым системным гемостатиком, который может использоваться с целью профилактики варфариновых кровотечений, не являясь антидотом варфарина и не действуя непосредственно на последний.
Техническим результатом заявляемого изобретения является создание эффективного способа профилактики кровотечений, вызванных применением варфарина перед хирургическими вмешательствами.
Технический результат достигается тем, что кроликам-самцам породы шиншилла за один час до хирургического вмешательства вводят раствор, содержащий фибрин-мономер в концентрации 11 мг/мл и мочевину в концентрации 150 мг/мл, при этом доза фибрин-мономера составляет 0,25 мг/кг.
Эффективность заявляемого способа подтверждена фигурами 1 и 2 в виде таблиц.
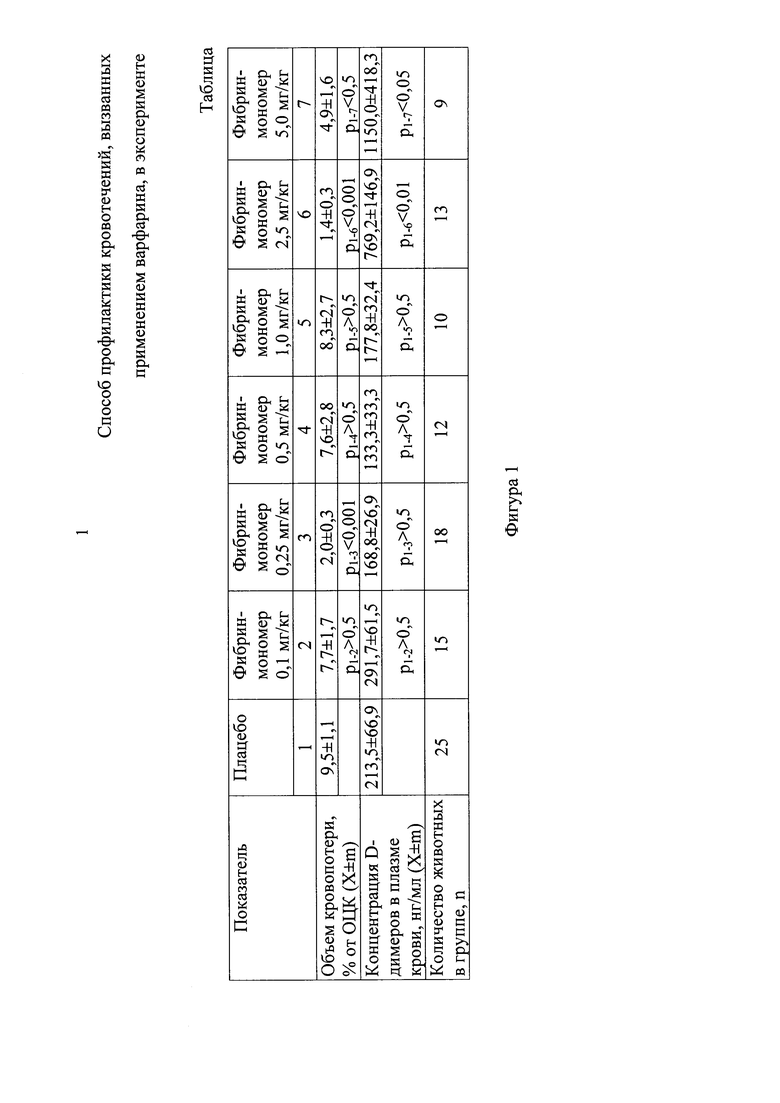
На фиг. 1 представлен подбор эффективной и безопасной дозы фибрин-мономера.
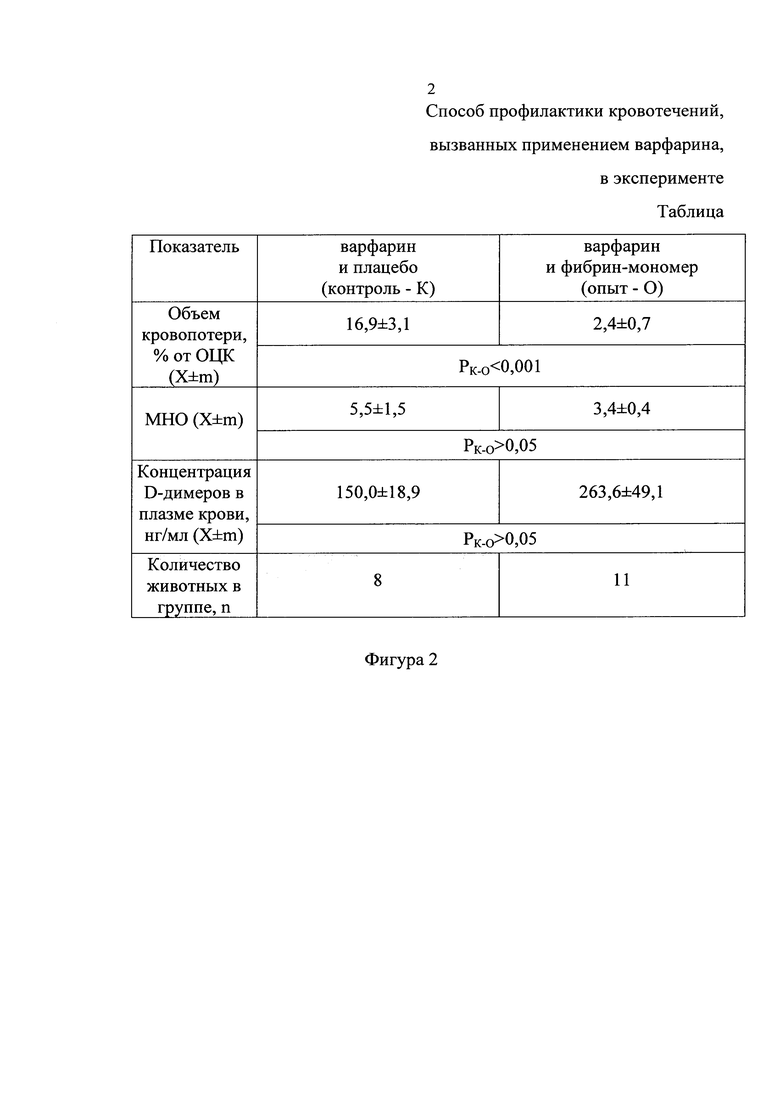
На фиг. 2 проиллюстрированы показатели кровоточивости и системы гемостаза у животных контрольной и опытной групп. У интактных животных, не принимавших варфарин (n=9), международное нормализованное отношение (MHO) составляло 1,1±0,2 при использовании для его расчета коммерческого тромбопластина с международным индексом чувствительности (МИЧ), равным 1,2.
На фигурах 1 и 2 даны следующие обозначения:
1. 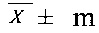 , где
, где 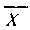 - выборочное среднее; m - стандартная ошибка выборочного среднего.
- выборочное среднее; m - стандартная ошибка выборочного среднего.
2. Объем кровопотери (в % от ОЦК) - часть потерянной крови от общего ее циркулирующего объема (ОЦК), выраженная в процентах.
3. Международное нормализованное отношение (MHO), рассчитанное как:
А) 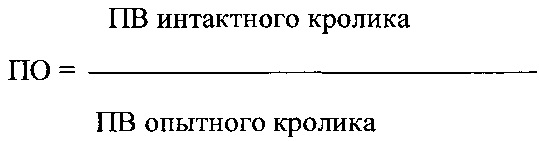
Б) MHO=ПОМИЧ,
где: ПО - протромбиновое отношение;
ПВ - протромбиновое время;
МИЧ - международный индекс чувствительности тромбопластина.
Для определения MHO используют коммерческий тромбопластин с международным индексом чувствительности (МИЧ), равным 1,2 (Баркаган, З.С. Диагностика и контролируемая терапия нарушений системы гемостаза / Баркаган З.С, Момот А.П. - Москва: Ньюдиамед - АО, 2008. - 292 с.), который в настоящее время является наиболее чувствительным тестом коагулограммы к действию варфарина.
4. Концентрация D-димеров (в нг/мл) - содержание продуктов деградации стабилизированного фибрина в плазме крови, являющихся маркерами образования фибрина и его растворения под действием плазмина.
5. p - уровень статистической значимости различий сравниваемых показателей.
6. n - количество животных в группе.
Способ осуществляют следующим образом.
Для профилактики кровотечения используют производное фибриногена из плазмы крови человека - фибрин-мономер (ООО фирма «Технология-Стандарт»), представляющий собой лиофильно высушенный растворимый порошок белого цвета с мочевиной, расфасованный в пенициллиновом флаконе, закрытом резиновой пробкой и обжатом алюминиевым колпачком, в количестве 22 мг во флаконе, который готовят следующим образом: во флакон с лиофильно высушенным фибрин-мономером с мочевиной добавляют 2 мл стерильной дистиллированной воды для инъекций, перемешивают аккуратным покачиванием без образования пены до полного растворения вещества в течение 2-3 минут. Полученный раствор содержит фибрин-мономер в концентрации 11 мг/мл и мочевину в концентрации 150 мг/мл.
В качестве контроля использовали раствор плацебо - раствор мочевины в концентрации 150 мг/мл, не содержащий активного вещества - фибрин-мономера. Во флакон с лиофильно высушенным раствором мочевины добавляют 2 мл стерильной дистиллированной воды для инъекций, перемешивают аккуратным покачиванием до полного растворения вещества в течение 2-3 минут.
Наиболее эффективная дозировка фибрин-мономера была подобрана экспериментально. В эксперименте использовали 68 кроликов-самцов породы «Шиншилла» массой 2-4 кг. Все животные были поделены на 7 групп. Доза фибрин-мономера была подобрана из диапазона дозировок от 0,1 мг/кг до 5,0 мг/кг массы тела. Данные подтверждены фигурой 1.
Схема эксперимента.
Первая группа состояла из 8 животных, которым внутривенно вводили плацебо в объеме 0,5 мл. Спустя один час после введения раствора плацебо проводили забор крови из краевой вены уха для оценки концентрации D-димеров в плазме крови. Описано, что увеличение концентрации D-димеров в плазме крови сопровождает венозный тромбоз и тромбоэмболию легочной артерии (Савельев, B.C. Российские клинические рекомендации по диагностике, лечению и профилактике венозных тромбоэмболических осложнений / B.C. Савельев, Е.И. Чазов, Е.И. Гусев и др. // Флебология. - 2010. - Т. 4. - №1. - выпуск 2. - С. 2-37). После этого животных наркотизировали и им выполняли срединную лапаротомию по белой линии живота под общим обезболиванием. В рану выводили левую долю печени и на ее диафрагмальной поверхности наносили стандартной по площади и глубине травма при помощи специального приспособления-ограничителя (металлической пластины с круглым отверстием в центре). Срезанный сегмент в вертикальной проекции имел вид круга или эллипса, его размеры и форма были постоянны (Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ / под ред. Р.Ю. Хабриева, 2 изд., перераб. и доп. - М.: ОАО - Издательство «Медицина», 2005. - 828 с.). Образовавшаяся кровоточащая рана с ровными краями и равномерной кривизной имела диаметр примерно 1,5 см, глубину примерно 0,5 см. После нанесения стандартной травмы замеряли объем кровопотери. Данный показатель определяется путем промакивания предварительно взвешенных сухих стерильных салфеток кровью из раны печени, до полной остановки кровотечения с формированием стабильного сгустка. Салфетки взвешивали на электронных весах сразу же после промакивания. Вес всех салфеток суммировали и учитывали объем потерянной крови. Объем кровопотери рассчитывали в процентах от общего ее циркулирующего объема.
Вторая группа состояла из 9 животных, которой внутривенно вводили фибрин-мономер в дозе 0,1 мг/кг.
Третья группа состояла из 11 животных, которым внутривенно вводили фибрин-мономер в дозе 0,25 мг/кг.
Четвертая группа состояла из 10 животных, которым внутривенно вводили фибрин-мономер в дозе 0,5 мг/кг.
Пятая группа состояла из 10 животных, которым внутривенно вводили фибрин-мономер в дозе 1,0 мг/кг.
Шестая группа состояла из 11 животных, которым вводили внутривенно вводили фибрин-мономер в дозе 2,5 мг/кг.
Седьмая группа состояла из 9 животных, которым внутривенно вводили фибрин-мономер в дозе 5,0 мг/кг.
Спустя один час после введения раствора фибрин-мономера у животных каждой из групп проводился забор крови из краевой вены уха для оценки концентрации D-димеров в плазме крови. После этого животных наркотизировали и им выполняли срединную лапаротомию по белой линии живота под общим обезболиванием с травмой печени и определением объема кровопотери по описанной выше схеме.
Как видно из таблицы №1 наиболее эффективными дозами фибрин-мономера для статистически значимого уменьшения кровопотери являются 0,25 мг/кг и 2,5 мг/кг (p<0,001 в обоих случаях). В то же время дозы фибрин-мономера выше 1,0 мг/кг обладают значительной тромбогенностью, которая оценивалась по нарастанию концентрации D-димеров в плазме крови, являющихся классическим маркером фибринообразования и фибринолиза. Таким образом, в качестве наиболее эффективной и безопасной для дальнейших экспериментов была выбрана доза фибрин-мономера 0,25 мг/кг.
Для исследования эффективности заявляемого способа все животные были разделены на две группы: первая группа - контрольная, состоящая из 8 животных, получала варфарин и плацебо; вторая группа - опытная, состоящая из 11 животных, получала варфарин и фибрин-мономер в дозе 0,25 мг/кг. Данные подтверждены фигурой 2.
Схема эксперимента
1. В течение 14 дней животные контрольной группы получали перорально варфарин (Варфарин Никомед (Warfarin Nycomed), Nycomed Dannmark, ApS (Дания), регистрационный номер: П N013469/01 от 25.12.07 г.) в дозе 0,4 мг/кг массы тела. Ежедневная доза варфарина подбиралась таким образом, чтобы международное нормализованное отношение (MHO) непосредственно перед экспериментом равнялась 3,0 или превышало эту величину.
В день эксперимента у животных контрольной группы из краевой вены уха забирали кровь (Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ / под ред. Р.Ю. Хабриева, 2 изд., перераб. и доп. - М.: ОАО - Издательство «Медицина», 2005. - 828 с.) для исследования исходных показателей системы гемостаза.
После забора крови сразу внутривенно вводили плацебо в объеме 0,5 мл. Спустя один час после введения раствора плацебо животных наркотизировали и им выполняли срединную лапаротомию по белой линии живота под общим обезболиванием. В рану выводили левую долю печени и на ее диафрагмальной поверхности наносили стандартную по площади и глубине травму при помощи специального приспособления-ограничителя (металлической пластины с круглым отверстием в центре). Срезанный сегмент в вертикальной проекции имел вид круга или эллипса, его размеры и форма были постоянны (Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ / под ред. Р.Ю. Хабриева, 2 изд., перераб. и доп. - М.: ОАО - Издательство «Медицина», 2005. - 828 с.). Образовавшаяся кровоточащая рана с ровными краями и равномерной кривизной имела диаметр примерно 1,5 см, глубину примерно 0,5 см.
После нанесения стандартной травмы замеряли объем кровопотери. Данный показатель определяли путем промакивания предварительно взвешенных сухих стерильных салфеток кровью из раны печени, до полной остановки кровотечения с формированием стабильного сгустка. Салфетки взвешивали на электронных весах сразу же после промакивания. Вес всех салфеток суммировали и учитывали объем потерянной крови. Объем кровопотери рассчитывали в процентах от общего ее циркулирующего объема.
2. В течение 14 дней животные опытной группы получали перорально варфарин (Варфарин Никомед (Warfarin Nycomed), Nycomed Dannmark, ApS (Дания), регистрационный номер: П N013469/01 от 25.12.07 г.) в дозе 0,4 мг/кг массы тела. Ежедневная доза варфарина подбиралась таки образом, чтобы международное нормализованное отношение (MHO) непосредственно перед экспериментом равнялась 3,0 или превышало эту величину.
В день эксперимента у животных опытной группы из краевой вены уха забирали кровь (Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ / под ред. Р.Ю. Хабриева, 2 изд., перераб. и доп. - М.: ОАО - Издательство «Медицина», 2005. - 828 с.) для исследования исходных показателей системы гемостаза.
После забора крови сразу внутривенно вводили фибрин-мономер в дозе 0,25 мг/кг. Спустя один час после введения раствора фибрин-мономера животных наркотизировали и им выполняли срединную лапаротомию по белой линии живота под общим обезболиванием. В рану выводили левую долю печени и на ее диафрагмальной поверхности наносили стандартную по площади и глубине травма при помощи специального приспособления-ограничителя (металлической пластины с круглым отверстием в центре). Срезанный сегмент в вертикальной проекции имел вид круга или эллипса, его размеры и форма были постоянны (Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ / под ред. Р.Ю. Хабриева, 2 изд., перераб. и доп. - М.: ОАО - Издательство «Медицина», 2005. - 828 с.). Образовавшаяся кровоточащая рана с ровными краями и равномерной кривизной имела диаметр примерно 1,5 см, глубину примерно 0,5 см.
После нанесения стандартной травмы замеряли объем кровопотери. Данный показатель определяли путем промакивания предварительно взвешенных сухих стерильных салфеток кровью из раны печени, до полной остановки кровотечения с формированием стабильного сгустка. Салфетки взвешивали на электронных весах сразу же после промакивания. Вес всех салфеток суммировали и учитывали объем потерянной крови. Объем кровопотери рассчитывали в процентах от общего ее циркулирующего объема. Как видно из таблицы №2, объем кровопотери (в % от объема циркулирующей крови) в опытной группе по сравнению с контрольной был ниже в 5,5 раза (p<0,001).
По представленным данным при сравнении показателей системы гемостаза в обеих группах животных был продемонстрирован эффект действия варфарина в виде увеличения MHO по сравнению с интактными животными, при стабильной концентрации D-димеров.
Таким образом, заявляемый способ обладает высокой эффективностью, так как не только снижает объем кровопотери, но и не повышает вероятность возникновения тромбозов.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОФИЛАКТИКИ КРОВОТЕЧЕНИЙ, ВЫЗВАННЫХ ПРИМЕНЕНИЕМ ДАБИГАТРАНА ЭТЕКСИЛАТА, В ЭКСПЕРИМЕНТЕ | 2013 |
|
RU2552331C1 |
| СПОСОБ ПРОФИЛАКТИКИ ИНТРАОПЕРАЦИОННЫХ КРОВОТЕЧЕНИЙ, ВЫЗВАННЫХ ВВЕДЕНИЕМ ГЕПАРИНА ДО ОПЕРАЦИИ | 2013 |
|
RU2544805C1 |
| Способ профилактики кровотечений, вызванных применением антиагрегантов, в эксперименте | 2017 |
|
RU2645630C1 |
| СПОСОБ ПРОФИЛАКТИКИ КРОВОТЕЧЕНИЙ, ВЫЗВАННЫХ ПРИМЕНЕНИЕМ СТРЕПТОКИНАЗЫ, В ЭКСПЕРИМЕНТЕ | 2014 |
|
RU2552339C1 |
| СПОСОБ ВЕДЕНИЯ ПАЦИЕНТОВ ПОСЛЕ ПРОТЕЗИРОВАНИЯ ТРИКУСПИДАЛЬНОГО КЛАПАНА | 2009 |
|
RU2465894C2 |
| Способ профилактики и лечения интра- и послеоперационного паренхиматозного кровотечения при комбинированных операциях на легких с частичной или тотальной костальной плеврэктомией у больных с исходными рисками развития венозных тромбоэмболических осложнений | 2019 |
|
RU2710232C1 |
| КОМБИНАТОРНАЯ ТЕРАПИЯ ДЛЯ ЛЕЧЕНИЯ ГЕМОРРАГИЧЕСКОГО ШОКА | 2015 |
|
RU2651778C2 |
| КОМБИНАТОРНАЯ ТЕРАПИЯ ДЛЯ ЛЕЧЕНИЯ ГЕМОРРАГИЧЕСКОГО ШОКА | 2018 |
|
RU2663464C1 |
| Способ лечения кровотечений из верхних отделов желудочно-кишечного тракта | 2016 |
|
RU2657756C2 |
| СПОСОБ ПРОМЫШЛЕННОГО ПОЛУЧЕНИЯ ФИБРИН-МОНОМЕРА ИЗ ПЛАЗМЫ КРОВИ | 2012 |
|
RU2522237C2 |
Изобретение относится к медицине, в частности к экспериментальной хирургии, и касается профилактики кровотечений, вызванных применением варфарина до хирургического вмешательства. Для этого кроликам-самцам породы шиншилла за один час до операции вводят раствор, содержащий фибрин-мономер в концентрации 11 мг/мл и мочевину в концентрации 150 мг/мл. При этом доза фибрин-мономера составляет 0,25 мг/кг. Способ обладает высокой эффективностью, так как не только снижает объем кровопотери, но и безопасен при использовании. 2 ил.
Способ профилактики кровотечений, вызванных применением варфарина, в эксперименте, заключающийся в том, что кроликам-самцам породы шиншилла за один час до хирургического вмешательства вводят раствор, содержащий фибрин-мономер в концентрации 11 мг/мл и мочевину в концентрации 150 мг/мл, при этом доза фибрин-мономера составляет 0,25 мг/кг.
| LEAL-NOVAL SR | |||
| et al | |||
| Efficacy of the prothrombin complex concentrate prothromplex in patients requiring urgent reversal of vitamin K antagonists or presenting with uncontrolled bleeding: a retrospective, single center study | |||
| Blood Coagul Fibrinolysis | |||
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
| СПОСОБ ПРОФИЛАКТИКИ ИНТРАОПЕРАЦИОННЫХ КРОВОТЕЧЕНИЙ, ВЫЗВАННЫХ ВВЕДЕНИЕМ ГЕПАРИНА ДО ОПЕРАЦИИ | 2013 |
|
RU2544805C1 |
| СПОСОБ ПРОФИЛАКТИКИ КРОВОТЕЧЕНИЙ, ВЫЗВАННЫХ ПРИМЕНЕНИЕМ СТРЕПТОКИНАЗЫ, В ЭКСПЕРИМЕНТЕ | 2014 |
|
RU2552339C1 |
| СПОСОБ ПРОФИЛАКТИКИ КРОВОТЕЧЕНИЙ, ВЫЗВАННЫХ ПРИМЕНЕНИЕМ ДАБИГАТРАНА ЭТЕКСИЛАТА, В ЭКСПЕРИМЕНТЕ | 2013 |
|
RU2552331C1 |
| US 20110066182 A1, 17.03.2011 | |||
| ТЕР-АРУТЮНЯНЦ А.А | |||
| Сравнительная оценка специфической фармакологической активности различных гемостатических средств местного и системного действия автореферат дисс | |||
| канд | |||
| мед | |||
| наук, Москва, 2009, 24 с | |||
| МОРЕВА О.В | |||
| Факторы, определяющие риск геморрагических осложнений у больных с адекватно подобранной дозой варфарина | |||
| Дисс | |||
| канд | |||
| мед | |||
| наук, М., 16.05.2016, с.124 | |||
| WADA H et al | |||
| Increased hemostatic molecular markers in patients undergoing anticoagulant therapy | |||
| Semin Thromb Hemost | |||
| ЩИТОВОЙ ДЛЯ ВОДОЕМОВ ЗАТВОР | 1922 |
|
SU2000A1 |
Авторы
Даты
2018-02-21—Публикация
2016-10-06—Подача