Изобретение относится к медицине, а именно к экспериментальной хирургии, и может быть использовано с целью профилактики кровотечения на фоне применения антикоагулянта дабигатрана этексилата.
Антикоагулянты широко используют у больных кардиологического и хирургического профиля с целью профилактики или лечения тромбозов. Однако их применение влечет за собой риск возможных осложнений в виде кровотечений (Савельев, B.C. Российские клинические рекомендации по диагностике, лечению и профилактике венозных тромбоэмболических осложнений. / И.С. Савельев, Е.И. Чазов, Е.И. Гусев, А.И. Кириенко и др. // Флебология. - 2010. - Т.4. - №1. - Вып.2. - С.2-37).
С целью профилактики тромбоэмболических осложнений у больных с фибрилляцией предсердий и при ортопедических операциях используют пероральный антикоагулянт - дабигатрана этексилат (Диагностика и лечение фибрилляции предсердий: рек. РКО, ВНОА и АССХ. М. - 2012. - 112 с.; Момот, А.П. Тромбопрофилактика эноксапарином и дабигатраном после эндопротезирования тазобедренного сустава. / А.П. Момот, И.В. Меркулов, Е.В. Григорьева и др. // Вестник травматологии и ортопедии им. Н.И. Приорова. - 2011. - №2. - С.67-70). Однако несмотря на эффективность применение его небезопасно, поскольку побочным эффектом на фоне приема дабигатрана этексилата являются кровотечения.
В настоящее время не существует способа профилактики кровотечений, вызванных применением дабигатрана этексилата. Специфический антидот к дабигатрана этексилату отсутствует, на что указывают не только публикации в этой области (Siegal, D.M. Reversal of novel oral anticoagulants in patients with major bleeding. / D.M. Siegal, A. Cuker // J. Thromb Thrombolysis. [Электронный ресурс] - 2013. - Vol.35, N 3. - P.391-398. - Режим доступа: http://http://www.ncbi.nlm.nih.gov/pubmed?term=Cuker%20A[Author]&cauthor=true&cauthor_uid=23389753), но и производитель данного лекарственного препарата (инструкция по применению препарата, регистрационный номер ЛСР-007065/09; дата регистрации 07.09.09 г.).
Из отечественных и зарубежных источников не обнаружено эффективного способа профилактики кровотечений, вызванных применением дабигатрана этексилата.
Известен способ снижения кровотечения после приема дабигатрана этексилата путем применения свежезамороженной плазмы (Abraham, N.S. Novel anticoagulants: bleeding risk and management strategies. / N.S. Abraham, D.L. Castillo // Curr Opin Gastroenterol. [Электронный ресурс] - 2013. - Vol.29, N 6. - P.676-683. - Режим доступа: http://www.ncbi.nlm.nih.gov/pubmed/24100724), которая содержит в своем составе весь комплекс участников свертывающей системы крови, физиологических антикоагулянтов и фибринолитических реакций.
Однако свежезамороженная плазма имеет низкую эффективность при кровотечениях, связанных с приемом дабигатрана этексилата (Akwaa, F. Treatment of bleeding complications when using oral anticoagulants for prevention of strokes. / F. Akwaa, A.C. Spyropoulos // Curr Treat Options Cardiovasc [Электронный ресурс] - 2013. - Vol.15, N 3. - P.288-298. - Режим доступа: http://www.ncbi.nlm.nih.gov/pubmed/23494907), и ее использование сопряжено с риском инфекционных осложнений, аллергических реакций, иммуносупрессии (Колосков, А.В. Современные представления о показаниях для трансфузии свежезамороженной плазмы. / А.В. Колосков // Гематология и трансфузиология. - 2005. - №6. - С.41-45).
Известен способ коррекции геморрагических осложнений после приема дабигатрана этексилата путем применения антиингибиторного коагулянтного комплекса (Фейба), состоящего из четырех витамин К-зависимых факторов свертывания - II, VIIa, IX, X (Khoo, T.L. The use of FEIBA® in the correction of coagulation abnormalities induced by dabigatran. / T.L. Khoo, C. Weatherburn, G. Kershaw, C.J. Reddel, J. Curnow, S. Dunkley // Int J Lab Hematol. [Электронный ресурс] - 2013. - Vol.35, N 35. - P.222-224. - Режим доступа: http://www.ncbi.nlm.nih.gov/pubmed/23020832).
Однако известный способ также является малоэффективным, так как не может клинически значимо купировать кровотечения, вызванные приемом дабигатрана этексилата (Akwaa, F. Treatment of bleeding complications when using oral anticoagulants for prevention of strokes. / F. Akwaa, A.C. Spyropoulos // Curr Treat Options Cardiovasc [Электронный ресурс] - 2013. - Vol.15, N 3. - P.288-298. - Режим доступа: http://www.ncbi.nlm.nih.gov/pubmed/23494907). Кроме того, применение антиингибиторного коагулянтного комплекса (Фейба) сопряжено с высоким риском развития тромбозов (К. Tomokiyo, Y. Nakatomi, Т. Araki, K. Teshima, Н. Nakano, Т. Nakagaki, S. Miyamoto, A. Funatsu, S. Iwanaga // Vox Sang [Электронный ресурс] - 2003. - Vol.85, N 4. - P.290-299. - Режим доступа: http://www.ncbi.nlm.nih.gov/pubmed/14633255; инструкция по применению препарата, регистрационный номер П №013644/01, дата регистрации 04.05.08).
Авторы предлагают безопасный и эффективный способ профилактики кровотечений, вызванных применением дабигатрана этексилата, в эксперименте, позволяющий клинически значимо предотвращать кровотечения.
Техническим результатом заявляемого изобретения является создание эффективного способа профилактики кровотечений, вызванных применением дабигатрана этексилата перед хирургическими вмешательствами.
Технический результат достигается путем внутривенного введения раствора фибрин-мономера в дозе 0,25 мг/кг за один час до оперативного вмешательства.
Эффективность заявляемого способа подтверждена фиг.1 и 2 в виде таблиц.
На фиг.1 представлен подбор эффективной и безопасной дозы фибрин-мономера.
На фиг.2 проиллюстрированы показатели кровоточивости и системы гемостаза у животных контрольной и опытной групп.
На фиг.1 и 2 даны следующие обозначения:
1. 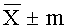
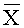
2. Объем кровопотери (в % от ОЦК) - часть потерянной крови от общего ее циркулирующего объема (ОЦК), выраженная в процентах.
3. Концентрация D-димеров (в нг/мл) - содержание продуктов деградации стабилизированного фибрина в плазме крови, являющихся маркерами образования фибрина и его растворения под действием плазмина.
4. АПТВ (в секундах) - активированное парциальное тромбопластиновое время.
5. p - уровень статистической значимости различий сравниваемых показателей.
6. n - количество животных в группе.
Способ осуществляют следующим образом.
В эксперименте используют кроликов-самцов породы «Шиншилла» массой 2-4 кг. Для профилактики кровотечения используют производное фибриногена из плазмы крови человека - фибрин-мономер (ООО фирма «Технология-Стандарт»), представляющий собой лиофильно высушенный растворимый порошок белого цвета с мочевиной, расфасованный в пенициллиновом флаконе, закрытом резиновой пробкой и обжатом алюминиевым колпачком, в количестве 22 мг во флаконе, который готовят следующим образом: во флакон с лиофильно высушенным фибрин-мономером с мочевиной добавляли 2 мл стерильной дистиллированной воды для инъекций, перемешивали аккуратным покачиванием без образования пены до полного растворения вещества в течение 2-3 минут. Полученный раствор содержал фибрин-мономер в концентрации 11 мг/мл и мочевину в концентрации 150 мг/мл.
В качестве контроля использовали раствор плацебо - раствор мочевины в концентрации 150 мг/мл, не содержащий активного вещества - фибрин-мономера. Во флакон с лиофильно высушенным раствором мочевины добавляли 2 мл стерильной дистиллированной воды для инъекций, перемешивали аккуратным покачиванием до полного растворения вещества в течение 2-3 минут.
Наиболее эффективная дозировка фибрин-мономера была подобрана экспериментально. В эксперименте использовали 68 кроликов-самцов. Все животные были поделены на 7 групп. Доза фибрин-мономера была подобрана из диапазона дозировок от 0,1 мг/кг до 5,0 мг/кг массы тела. Данные подтверждены фиг.1.
Схема эксперимента.
Первая группа состояла из 8 животных, которым внутривенно вводили плацебо в объеме 0,5 мл. Спустя один час после введения раствора плацебо проводили забор крови из краевой вены уха для оценки концентрации D-димеров в плазме крови. Описано, что увеличение концентрации D-димеров в плазме крови сопровождает венозный тромбоз и тромбоэмболию легочной артерии (Савельев B.C., Чазов Е.И., Гусев Е.И., Кириенко А.И. и др. Российские клинические рекомендации по диагностике, лечению и профилактике венозных тромбоэмболических осложнений // Флебология. - 2010. - Т.4, №1. - выпуск 2. - С.2-37). После этого животных наркотизировали и им выполняли срединную лапаротомию по белой линии живота под общим обезболиванием. В рану выводили левую долю печени и на ее диафрагмальной поверхности наносили стандартную по площади и глубине травму при помощи специального приспособления-ограничителя (металлической пластины с круглым отверстием в центре). Срезанный сегмент в вертикальной проекции имел вид круга или эллипса, его размеры и форма были постоянны (Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ. / Под ред. Р.Ю. Хабриева. - 2 изд., перераб. и доп. - М.: ОАО - Издательство «Медицина», 2005. - 828 с.). Образовавшаяся кровоточащая рана с ровными краями и равномерной кривизной имела диаметр примерно 1,5 см, глубину примерно 0,5 см. После нанесения стандартной травмы замеряли объем кровопотери. Данный показатель определяли путем промакивания предварительно взвешенных сухих стерильных салфеток кровью из раны печени до полной остановки кровотечения с формированием стабильного сгустка. Салфетки взвешивали на электронных весах сразу же после промакивания. Вес всех салфеток суммировали и учитывали объем потерянной крови. Объем кровопотери рассчитывали в процентах от общего ее циркулирующего объема.
Вторая группа состояла из 9 животных, которой внутривенно вводили фибрин-мономер в дозе 0,1 мг/кг.
Третья группа состояла из 11 животных, которым внутривенно вводили фибрин-мономер в дозе 0,25 мг/кг.
Четвертая группа состояла из 10 животных, которым внутривенно вводили фибрин-мономер в дозе 0,5 мг/кг.
Пятая группа состояла из 10 животных, которым внутривенно вводили фибрин-мономер в дозе 1,0 мг/кг.
Шестая группа состояла из 11 животных, которым внутривенно вводили фибрин-мономер в дозе 2,5 мг/кг.
Седьмая группа состояла из 9 животных, которым внутривенно вводили фибрин-мономер в дозе 5,0 мг/кг.
Спустя один час после введения раствора фибрин-мономера у животных каждой из групп проводили забор крови из краевой вены уха для оценки концентрации D-димеров в плазме крови. После этого животных наркотизировали и им выполняли срединную лапаротомию по белой линии живота под общим обезболиванием с травмой печени и определением объема кровопотери по описанной выше схеме.
Как видно на фиг.1, наиболее эффективными дозами фибрин-мономера для статистически значимого уменьшения кровопотери являются 0,25 мг/кг и 2,5 мг/кг (p<0,001 в обоих случаях). В то же время дозы фибрин-мономера выше 1,0 мг/кг обладают значительной тромбогенностью, которая оценивалась по нарастанию концентрации D-димеров в плазме крови, являющихся классическим маркером фибринообразования и фибринолиза. Таким образом, в качестве наиболее эффективной и безопасной для дальнейших экспериментов была выбрана доза фибрин-мономера 0,25 мг/кг.
Для исследования эффективности заявляемого способа все животные были разделены на две группы: первая группа - контрольная, состоящая из 10 животных, получала дабигатрана этексилат и плацебо; вторая группа - опытная, состоящая из 12 животных, получала дабигатрана этексилат и фибрин-мономер.
Схема эксперимента.
1. За двое суток до эксперимента у животных контрольной группы из краевой вены уха забирали кровь (Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ. / Под ред. Р.Ю. Хабриева. - 2 изд., перераб. и доп. - М.: ОАО - Издательство «Медицина», 2005. - 828 с.) для исследования исходных показателей системы гемостаза. Наиболее чувствительными тестами коагулограммы к действию дабигатрана этексилата являются: активированное парциальное тромбопластиновое время свертывания, тромбиновое время свертывания и эхитоксовое время свертывания (Момот А.П. Мониторинг использования дабигатрана в качестве средства профилактики тромбоэмболических осложнений после артропластики тазобедренного сустава. / А.П. Момот, Е.В. Григорьев, Л.П. Цывкина // Клиническая лабораторная диагностика: Научно-практический журнал. - 2012. - №5. - С.40-42. - ISSN 0869-2084). В день эксперимента животным контрольной группы энтерально вводили дабигатрана этексилат в дозе 15-20 мг на кг массы тела. Данная доза препарата являлась превышающей в пять раз среднетерапевтическую дозу для лечебного применения у человека (Прадакса (Pradaxa), Boehringer Ingelheim Pharma GmbH & Co. KG, Германия, регистрационный номер: ЛСР-007065/09 от 07.09.09 г.). Через два часа проводился забор крови из краевой вены уха для оценки системы гемостаза.
После забора крови сразу внутривенно вводили плацебо в объеме 0,5 мл. Спустя один час после введения раствора плацебо животных наркотизировали и им выполняли срединную лапаротомию по белой линии живота под общим обезболиванием. В рану выводили левую долю печени и на ее диафрагмальной поверхности наносили стандартную по площади и глубине травму при помощи специального приспособления-ограничителя (металлической пластины с круглым отверстием в центре). Срезанный сегмент в вертикальной проекции имел вид круга или эллипса, его размеры и форма были постоянны (Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ. / Под ред. Р.Ю. Хабриева, 2 изд., перераб. и доп. М.: ОАО «Издательство «Медицина», 2005. - 828 с.). Образовавшаяся кровоточащая рана с ровными краями и равномерной кривизной имела диаметр примерно 1,5 см, глубину примерно 0,5 см.
После нанесения стандартной травмы замеряли объем кровопотери. Данный показатель определяли путем промакивания предварительно взвешенных сухих стерильных салфеток кровью из раны печени до полной остановки кровотечения с формированием стабильного сгустка. Салфетки взвешивали на электронных весах сразу же после промакивания. Вес всех салфеток суммировали и учитывали объем потерянной крови. Объем кровопотери рассчитывали в процентах от общего ее циркулирующего объема.
2. За двое суток до эксперимента у животных опытной группы из краевой вены уха забирали кровь (Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ. / Под ред. Р.Ю. Хабриева, 2 изд., перераб. и доп. М.: ОАО «Издательство «Медицина», 2005. - 828 с.) для исследования исходных показателей системы гемостаза.
В день эксперимента животным опытной группы энтерально вводили дабигатрана этексилат в дозе 15-20 мг на кг массы тела. Данная доза препарата являлась в пять раз превышающей среднетерапевтическую дозу для лечебного применения у человека (Прадакса (Pradaxa), Boehringer Ingelheim Pharma GmbH & Co. KG, Германия, регистрационный номер: ЛСР-007065/09 от 07.09.09 г.). Через два часа проводился забор крови из краевой вены уха для оценки системы гемостаза.
После забора крови сразу внутривенно вводили фибрин-мономер в дозе 0,25 мг/кг. Спустя один час после введения раствора фибрин-мономера животных наркотизировали и им выполняли срединную лапаротомию по белой линии живота под общим обезболиванием. В рану выводили левую долю печени и на ее диафрагмальной поверхности наносили стандартную по площади и глубине травму при помощи специального приспособления-ограничителя (металлической пластины с круглым отверстием в центре). Срезанный сегмент в вертикальной проекции имел вид круга или эллипса, его размеры и форма были постоянны (Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ. / Под ред. Р.Ю. Хабриева, 2 изд., перераб. и доп. М.: ОАО «Издательство «Медицина», 2005. - 828 с.). Образовавшаяся кровоточащая рана с ровными краями и равномерной кривизной имела диаметр примерно 1,5 см, глубину примерно 0,5 см.
После нанесения стандартной травмы замеряли объем кровопотери. Данный показатель определяли путем промакивания предварительно взвешенных сухих стерильных салфеток кровью из раны печени до полной остановки кровотечения с формированием стабильного сгустка. Салфетки взвешивали на электронных весах сразу же после промакивания. Вес всех салфеток суммировали и учитывали объем потерянной крови. Объем кровопотери рассчитывали в процентах от общего ее циркулирующего объема.
Эффективность заявляемого способа проиллюстрирована фиг.2, в которой приведены сравнительные данные объем кровопотери, концентрации D-димеров и системы гемостаза, позволяющие продемонстрировать эффективность заявляемого способа. Как видно из таблицы фиг.2, объем кровопотери (в % от объема циркулирующей крови) в опытной группе по сравнению с контрольной был ниже в 2,3 раза (p<0,01).
По представленным данным при сравнении показателей системы гемостаза в обеих группах животных был продемонстрирован эффект действия дабигатрана этексилата в виде резкого удлинения активированного парциального тромбопластинового времени, тромбинового времени и эхитоксового времени свертывания, что соответствовало описанным ранее изменениям в системе гемостаза плазмы крови человека (Момот А.П. Мониторинг использования дабигатрана в качестве средства профилактики тромбоэмболических осложнений после артропластики тазобедренного сустава. / А.П. Момот, Е.В. Григорьев, Л.П. Цывкина // Клиническая лабораторная диагностика: Научно-практический журнал. - 2012. - №5. - С.40-42. - ISSN 0869-2084).
Таким образом, заявляемый способ обладает высокой эффективностью, так как не только снижает объем кровопотери, но и не повышает вероятность возникновения тромбозов.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ профилактики кровотечений, вызванных применением антиагрегантов, в эксперименте | 2017 |
|
RU2645630C1 |
| Способ профилактики кровотечений, вызванных применением варфарина в эксперименте | 2016 |
|
RU2645414C1 |
| СПОСОБ ПРОФИЛАКТИКИ ИНТРАОПЕРАЦИОННЫХ КРОВОТЕЧЕНИЙ, ВЫЗВАННЫХ ВВЕДЕНИЕМ ГЕПАРИНА ДО ОПЕРАЦИИ | 2013 |
|
RU2544805C1 |
| СПОСОБ ПРОФИЛАКТИКИ КРОВОТЕЧЕНИЙ, ВЫЗВАННЫХ ПРИМЕНЕНИЕМ СТРЕПТОКИНАЗЫ, В ЭКСПЕРИМЕНТЕ | 2014 |
|
RU2552339C1 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИКОАГУЛЯНТНОЙ (ИНГИБИТОР IIA ФАКТОРА), АНТИТРОМБОТИЧЕСКОЙ, ПРОТИВОВОСПАЛИТЕЛЬНОЙ АКТИВНОСТЯМИ И СОДЕРЖАЩЕЕ 5,7-ДИ(ТИОФЕН-2-ИЛ)-4,5-ДИГИДРО-[1,2,4]ТРИАЗОЛО[1,5-а]ПИРИМИДИН | 2022 |
|
RU2798587C1 |
| Антикоагулянтное лекарственное средство, представляющее собой синтетический дипептид Ac-Trp-Arg-Pip ⋅HCl, фармацевтическая композиция, включающая это антикоагулянтное лекарственное средство | 2019 |
|
RU2712194C1 |
| СПОСОБ ЛЕЧЕНИЯ ИЛИ ПРОФИЛАКТИКИ ТРОМБОЗА С ИСПОЛЬЗОВАНИЕМ ЭТЕКСИЛАТА ДАБИГАТРАНА ИЛИ ЕГО СОЛИ С УЛУЧШЕННОЙ ЭФФЕКТИВНОСТЬЮ ПО СРАВНЕНИЮ СО СТАНДАРТНЫМ ЛЕЧЕНИЕМ ВАРФАРИНОМ | 2009 |
|
RU2530645C2 |
| СПОСОБ ПРОФИЛАКТИКИ ХРОНИЧЕСКОЙ СУЛЕМОВОЙ КОАГУЛОПАТИИ У КРЫС В ЭКСПЕРИМЕНТЕ | 2022 |
|
RU2788609C1 |
| СПОСОБ ПРОФИЛАКТИКИ ХРОНИЧЕСКОЙ МОЛИБДЕНОВОЙ КОАГУЛОПАТИИ | 2020 |
|
RU2739690C1 |
| Способ профилактики хронической свинцовой коагулопатии у экспериментальных животных | 2019 |
|
RU2706386C1 |

(57) Изобретение относится к области ветеринарии и предназначено для профилактики кровотечений, вызванных применением дабигатрана этексилата, в эксперименте. Кроликам-самцам породы шиншилла за один час до хирургического вмешательства внутривенно вводят раствор. Раствор готовят следующим образом: в лиофильно высушенный фибрин-мономер с мочевиной добавляют стерильную дистиллированную воду для инъекций так, чтобы полученный раствор содержал фибрин-мономер в концентрации 11 мг/мл и мочевину в концентрации 150 мг/мл, и перемешивают до полного растворения вещества. Доза фибрин-мономера составляет 0,25 мг/кг. Способ высокоэффективен для профилактики кровотечений, вызванных применением дабигатрана этексилата, в эксперименте. 2 ил., 1 пр.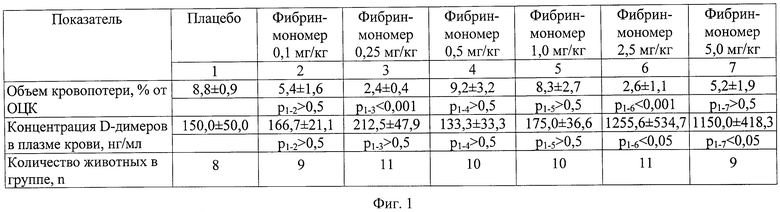
Способ профилактики кровотечений, вызванных применением дабигатрана этексилата, в эксперименте, заключающийся в том, что кроликам-самцам породы шиншилла за один час до хирургического вмешательства внутривенно вводят раствор, который готовят следующим образом: в лиофильно высушенный фибрин-мономер с мочевиной добавляют стерильную дистиллированную воду для инъекций так, чтобы полученный раствор содержал фибрин-мономер в концентрации 11 мг/мл и мочевину в концентрации 150 мг/мл, и перемешивают до полного растворения вещества, при этом доза фибрин-мономера составляет 0,25 мг/кг.
| WO 2008092656 A1, 07.08.2008 | |||
| RU 2005140621 A, 26.12.2005 | |||
| МОИСЕЕВ С.В | |||
| Новые пероральные антикоагулянты в лечении венозных тромбоэмболических осложнений// Флебология, 2012, N1, с.32-36 |
Авторы
Даты
2015-06-10—Публикация
2013-12-30—Подача