Область техники
Настоящее изобретение относится к терапевтическому средству при артрозе, включающему в качестве активного ингредиента циклическую фосфатидовую кислоту или карбоциклическую фосфатидовую кислоту.
Предшествующий уровень техники
Подтипы артроза включают, например, остеоартрит, суставной ревматизм и ревматическую лихорадку, и количество пациентов с остеоартритом и суставным ревматизмом достаточно велико. Соответственно, остеоартрит и суставной ревматизм расцениваются как основные подтипы артроза. Остеоартрит классифицируют как врожденный или вторичный остеоартрит или первичный остеоартрит, вызванный деформацией суставного хряща, обусловленной старением. Количество пациентов с первичным остеоартритом возрастает при увеличении популяции пожилых людей. Существуют значительные различия между остеоартритом и суставным ревматизмом в отношении причин заболеваний и клинических состояний, хотя указанные заболевания имеют следующие общие признаки: в конечном итоге функции суставов нарушаются в результате деструкции суставного хряща. К настоящему времени противовоспалительные обезболивающие средства, такие как аспирин и индометацин, используют в качестве средств лечения ревматических заболеваний, таких как остеоартрит. Однако такие противовоспалительные обезболивающие средства не оказывают каких-либо ингибирующих эффектов на деструкцию суставного хряща. Кроме того, ингибирующие эффекты терапевтических средств, таких как препараты золота, иммуносупрессивные средства и препараты стероидов, на деструкцию суставного хряща еще не были подтверждены в клинических условиях.
Суставной хрящ состоит из хондроцитов и хрящевой матрицы. Хрящевые матрицы имеют сложную трехмерную структуру, образованную коллагенами, которые представляют собой волокнистые белки, продуцируемые хондроцитами, и протеогликанами (белково-полисахаридными комплексами), связанными с гиалуроновыми кислотами. Нормальная функция суставов поддерживается посредством удержания большого количества воды в хрящевой матрице.
В добавление к средствам для лечения остеоартрита, описанным выше, в клинических условиях использовали внутрисуставные инъекции гиалуроновой кислоты, которые демонстрировали эффекты защиты и восстановления суставного хряща и эффект увлажнения суставов. Однако такая методика является инвазивной и, следовательно, не удовлетворительной с точки зрения QOL пациента.
Сущность изобретения
Задача, решаемая посредством изобретения
Задачей настоящего изобретения является предоставление терапевтического средства при артрозе, которое проявляет ингибирующие эффекты в отношении деструкции суставного хряща и высокий терапевтический эффект в отношении артроза.
Средства для решения задачи
Авторы настоящего изобретения считают, что деструкцию суставного хряща можно ингибировать посредством ускорения продукции гиалуроновой кислоты в суставных хондроцитах и что это может быть эффективным средством для лечения остеоартрита. Они провели направленные исследования и, как следствие, обнаружили, что циклические фосфатидовые кислоты и их производные в существенной степени ускоряют продукцию гиалуроновой кислоты в хондроцитах, полученных от пациентов с остеоартритом, и что такие эффекты наблюдают в моделях остеоартроза на животных. Это привело к осуществлению настоящего изобретения.
Следовательно, настоящее изобретение предоставляет терапевтическое средство при артрозе, которое включает в качестве активного ингредиента соединение, представленное формулой (I):
Формула 1
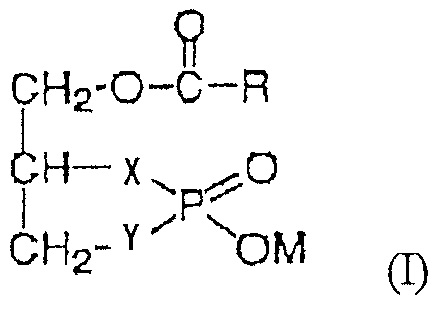
где R представляет собой линейную или разветвленную алкильную группу, имеющую от 1 до 30 атомов углерода, линейную или разветвленную алкенильную группу, имеющую от 2 до 30 атомов углерода, или линейную или разветвленную алкинильную группу, имеющую от 2 до 30 атомов углерода, которые могут содержать циклоалкановый или ароматический цикл; Х и Y каждый независимо представляет собой атом кислорода или метиленовую группу с условием, что Х и Y одновременно не являются метиленовой группой; и М представляет собой атом водорода или атом щелочного металла.
Предпочтительно в формуле (I) Х и Y представляют собой атом кислорода.
Предпочтительно в формуле (I) или Х, или Y представляет собой атом кислорода, и другой представляет собой метиленовую группу.
Предпочтительно соединение, представленное формулой (I), представляет собой карбоциклическую фосфатидовую кислоту, 1-олеоил-циклическую фосфатидовую кислоту, 1-пальмитолеил циклическую фосфатидовую кислоту или их производное.
Настоящее изобретение дополнительно предоставляет способ лечения артроза, включающий введение соединения, представленного вышеуказанной формулой (I), пациенту с артрозом.
Настоящее изобретение дополнительно предоставляет применение соединения, представленного вышеуказанной формулой (I), для получения средства для лечения артроза.
Эффекты изобретения
Настоящее изобретение может предоставлять средство для лечения артроза, которое ингибирует деструкцию суставного хряща и обладает терапевтическими эффектами в отношении артроза.
Краткое описание чертежей
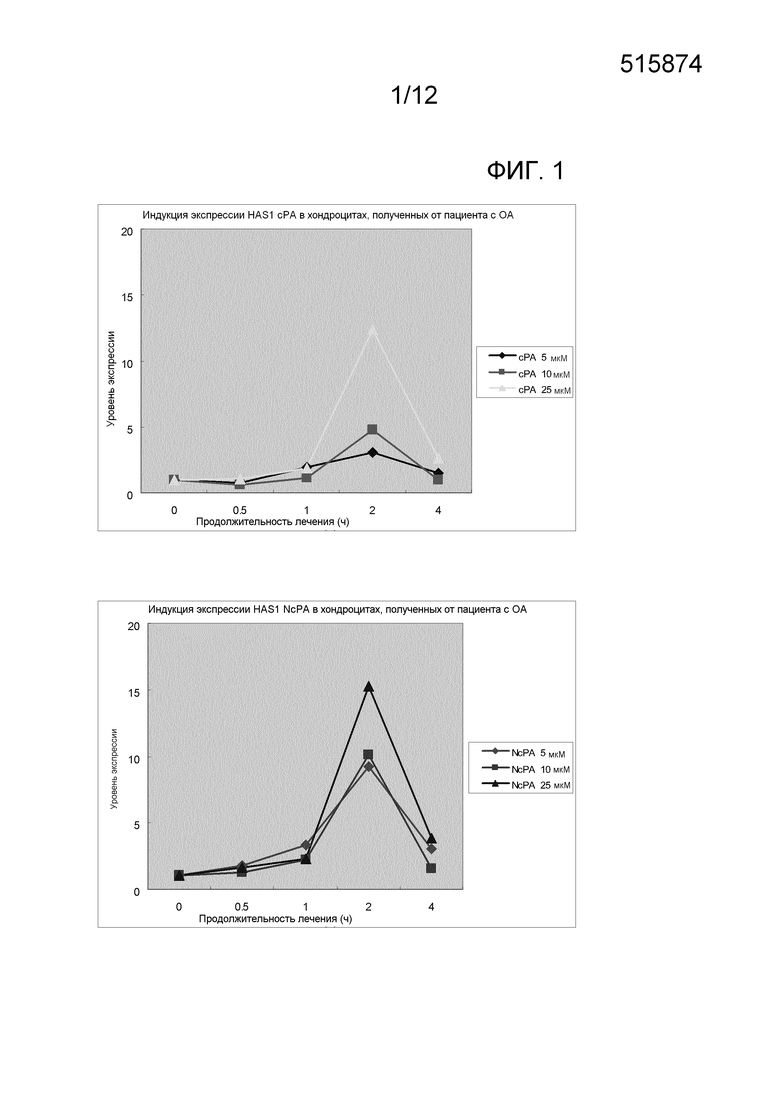
На фиг. 1 показаны результаты исследования эффектов производного циклической фосфатидовой кислоты на экспрессию гена синтазы гиалуроновой кислоты (HAS1) в хондроцитах, полученных от пациента с остеоартритом.
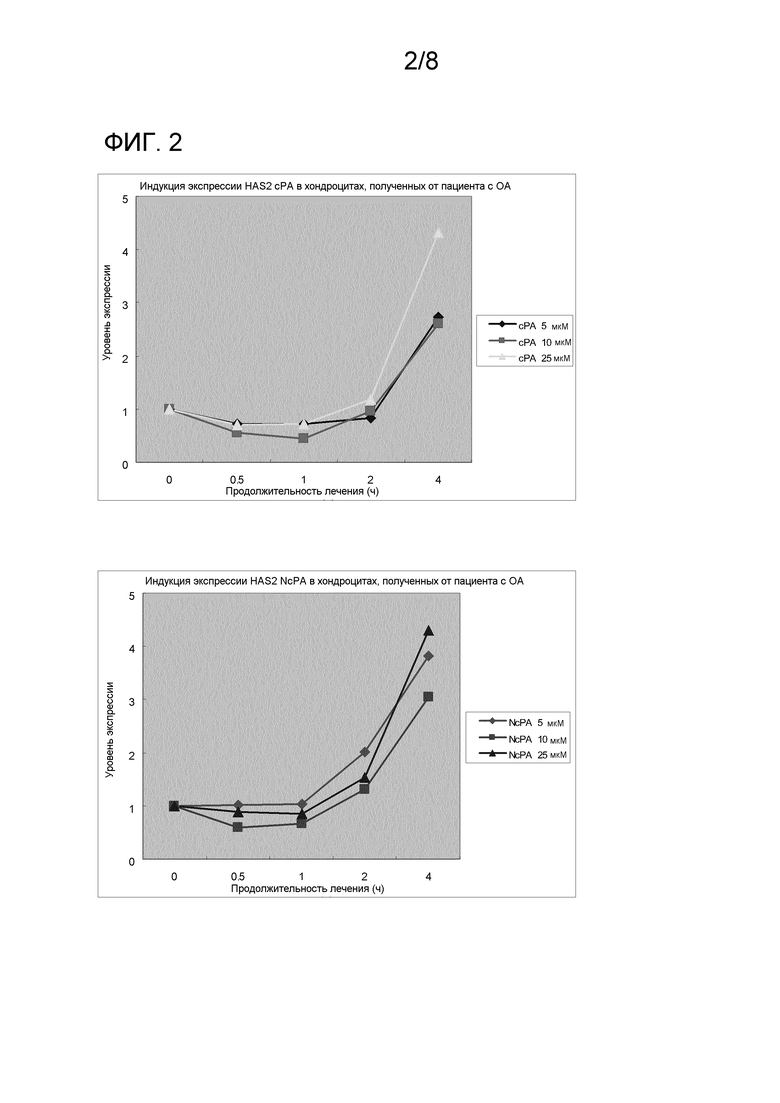
На фиг. 2 показаны результаты исследования эффектов производного циклической фосфатидовой кислоты на экспрессию гена синтазы гиалуроновой кислоты (HAS2) в хондроцитах, полученных от пациента с остеоартритом.
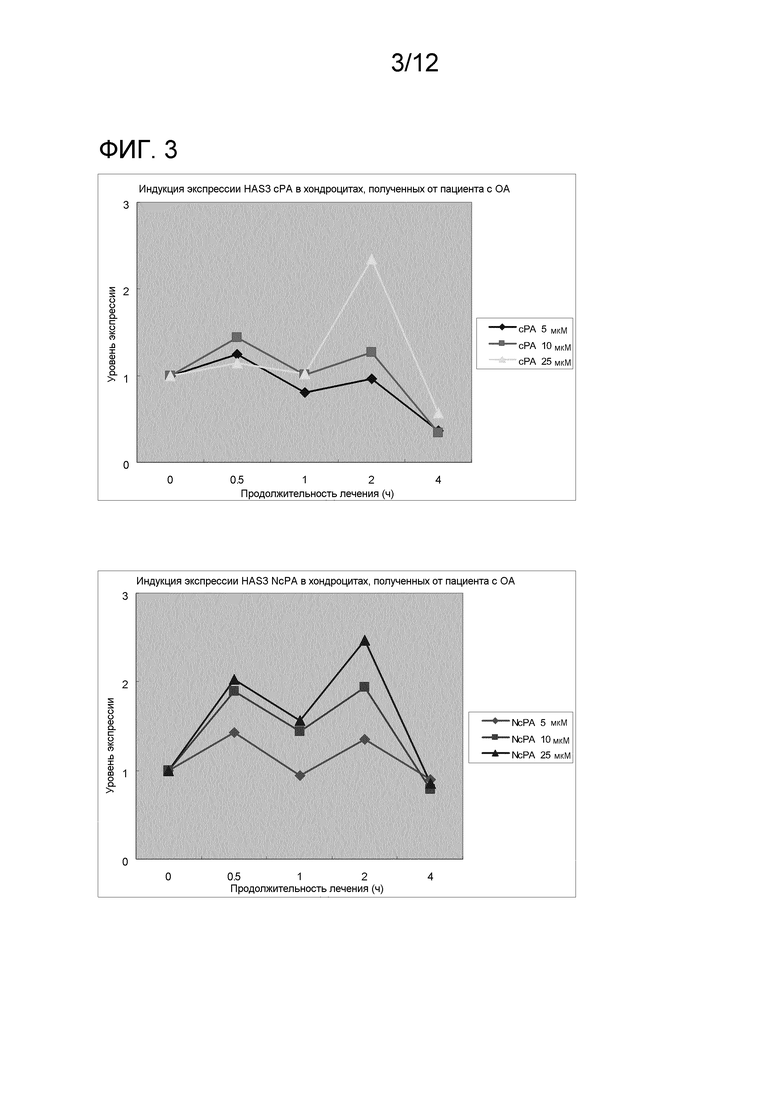
На фиг. 3 показаны результаты исследования эффектов производного циклической фосфатидовой кислоты на экспрессию гена синтазы гиалуроновой кислоты (HAS3) в хондроцитах, полученных от пациента с остеоартритом.
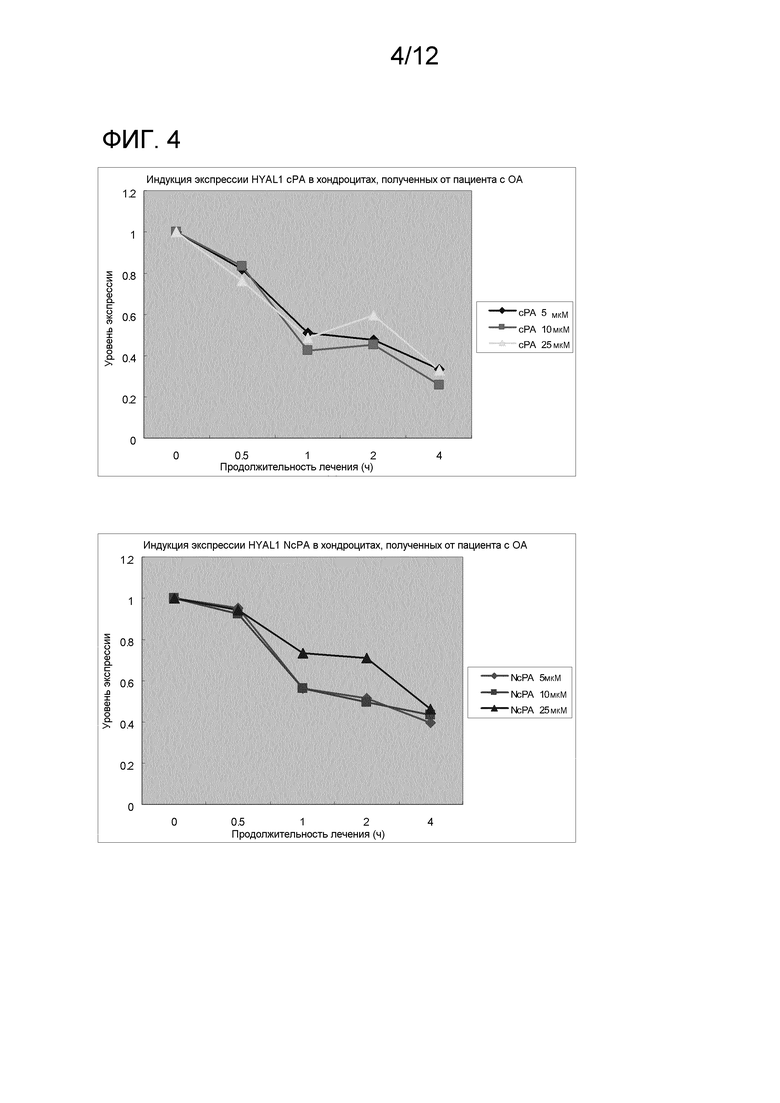
На фиг. 4 показаны результаты исследования эффектов производного циклической фосфатидовой кислоты на экспрессию гена гиалуронидазы (HYAL1) в хондроцитах, полученных от пациента с остеоартритом.
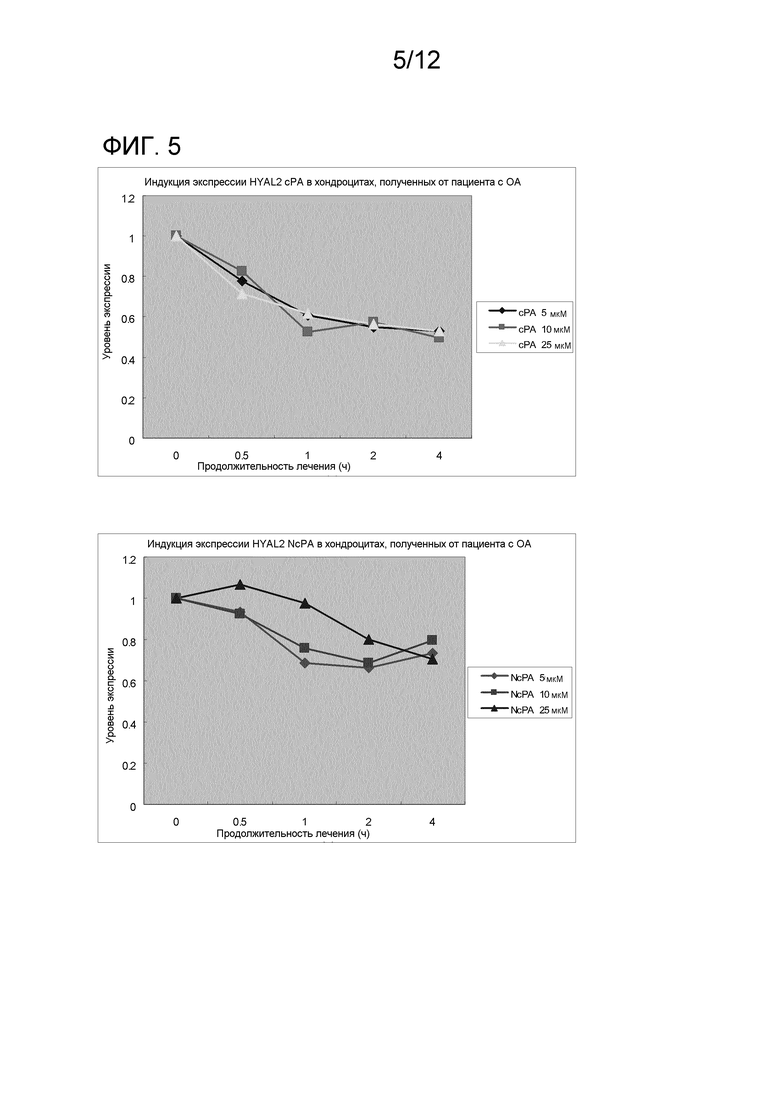
На фиг. 5 показаны результаты исследования эффектов производного циклической фосфатидовой кислоты на экспрессию гена гиалуронидазы (HYAL2) в хондроцитах, полученных от пациента с остеоартритом.
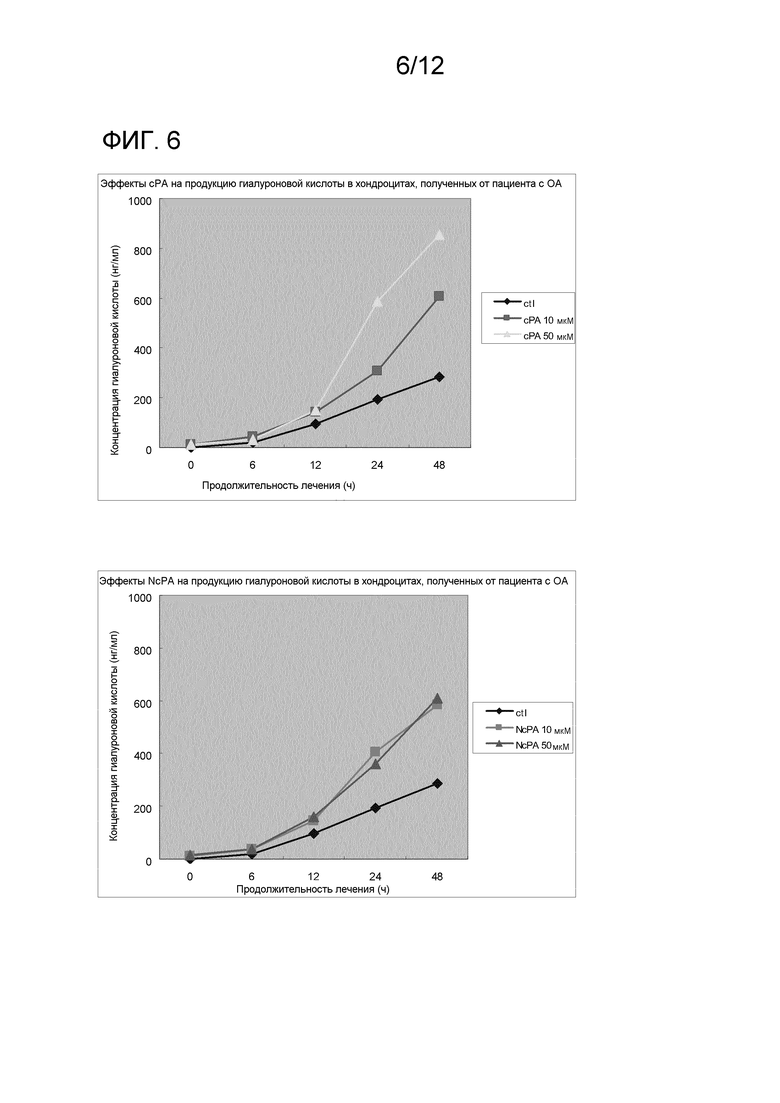
На фиг. 6 показаны результаты исследования эффектов производного циклической фосфатидовой кислоты на продукцию гиалуроновой кислоты в хондроцитах, полученных от пациента с остеоартритом.
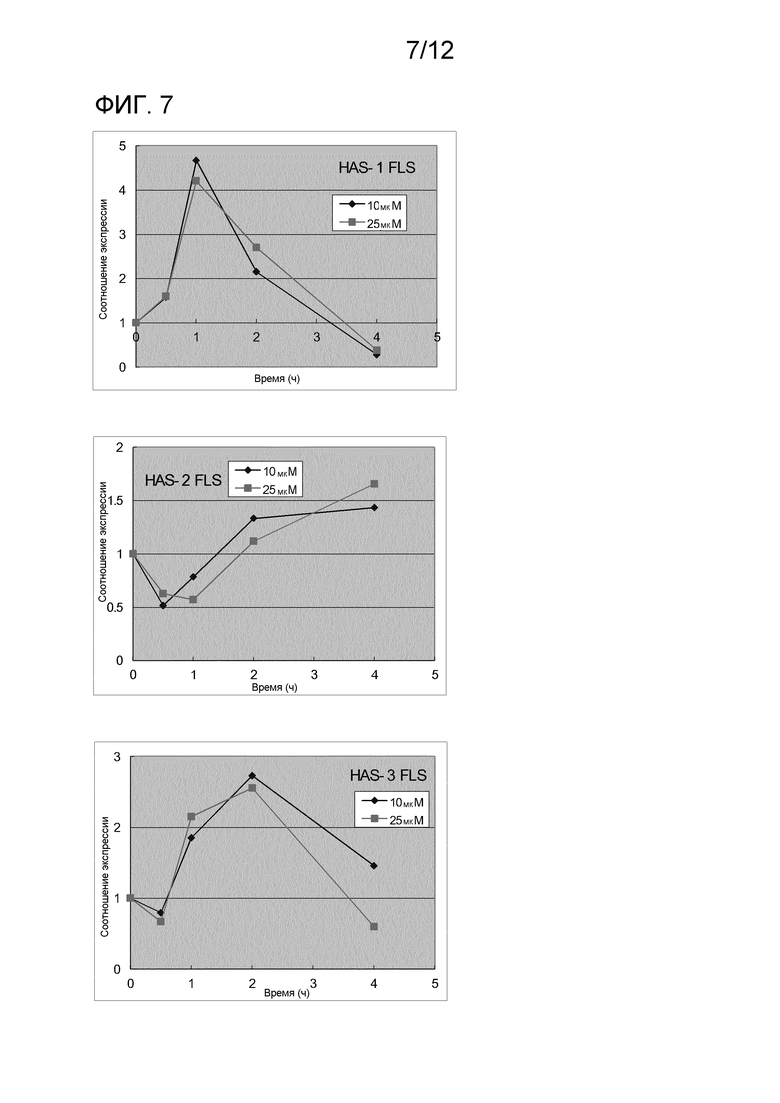
На фиг. 7 показаны результаты исследования эффектов производного циклической фосфатидовой кислоты (тестируемое соединение: ScPA) на экспрессию генов синтазы гиалуроновой кислоты (HAS1, HAS2 и HAS3) в синовиоцитах, полученных от пациента с остеоартритом.
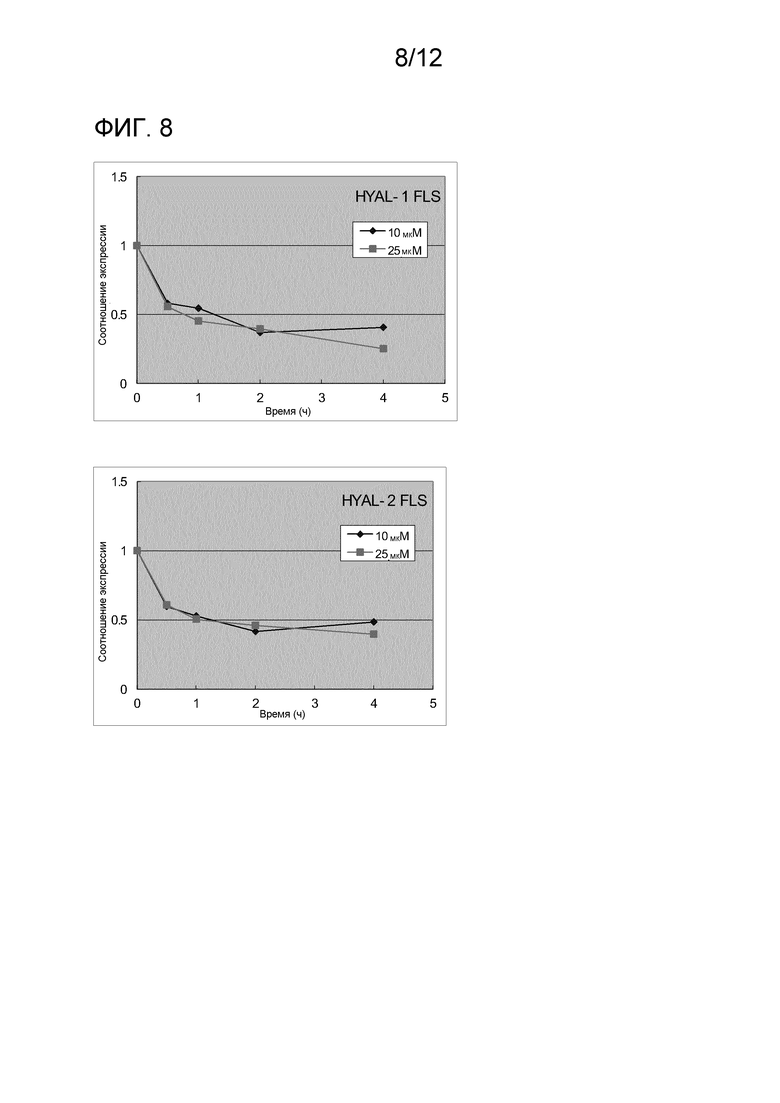
На фиг. 8 показаны результаты исследования эффектов производного циклической фосфатидовой кислоты на экспрессию генов гиалуронидазы (HYAL1 и HYAL2) в синовиоцитах, полученных от пациента с остеоартритом.
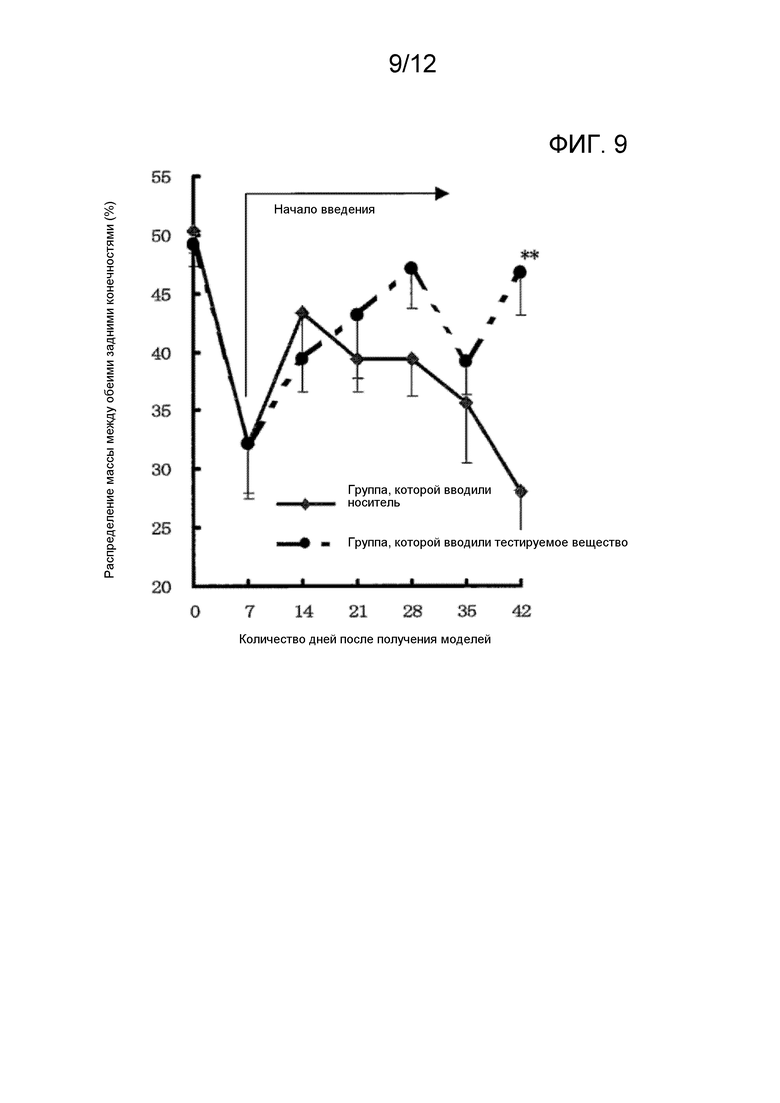
На фиг. 9 показаны изменения в оценке боли (распределение массы между задними конечностями). Среднее ± стандартная ошибка, n=6; по сравнению с группой 1 (группа, которой вводили носитель)*, **; уровень достоверности при р<0,05 и р< 0,01 (t-критерий Стьюдента и t критерий Аспина-Уэлча).
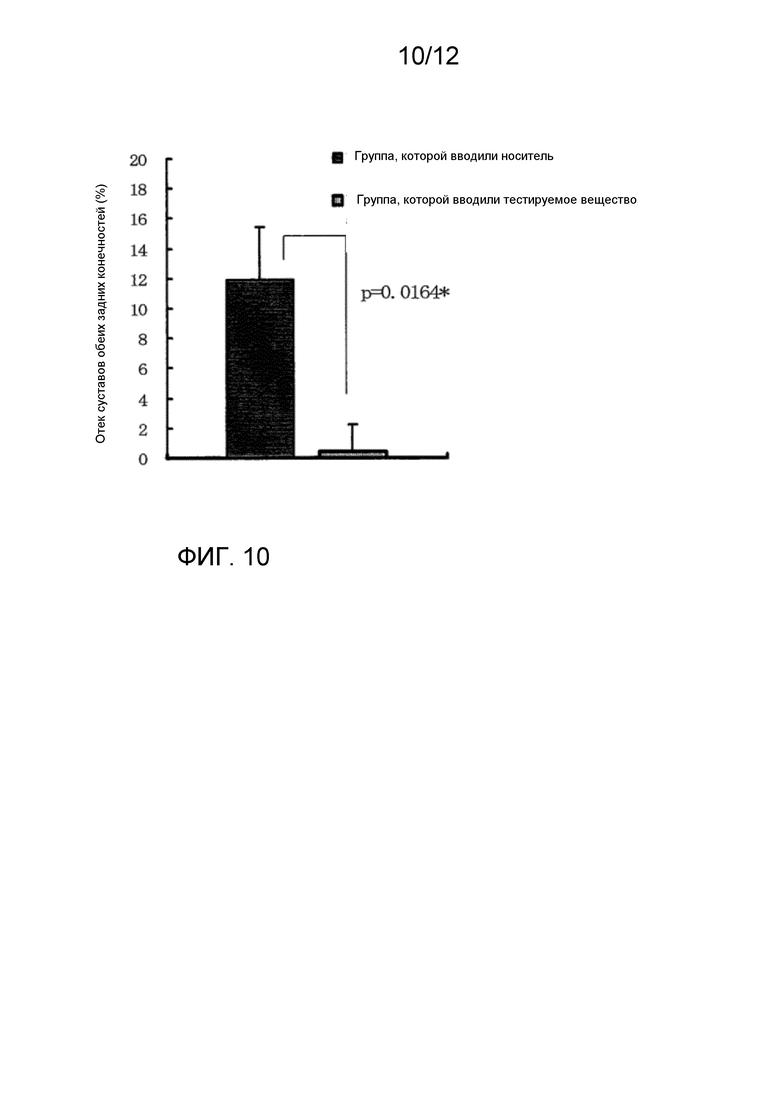
На фиг. 10 показаны результаты оценки отека (отек суставов обеих задних конечностей). Среднее ± стандартная ошибка, n=6; по сравнению с группой 1 (группе вводили носитель)*, **; уровень достоверности при р<0,05 и р< 0,01 (t-критерий Стьюдента и t критерий Аспина-Уэлча).
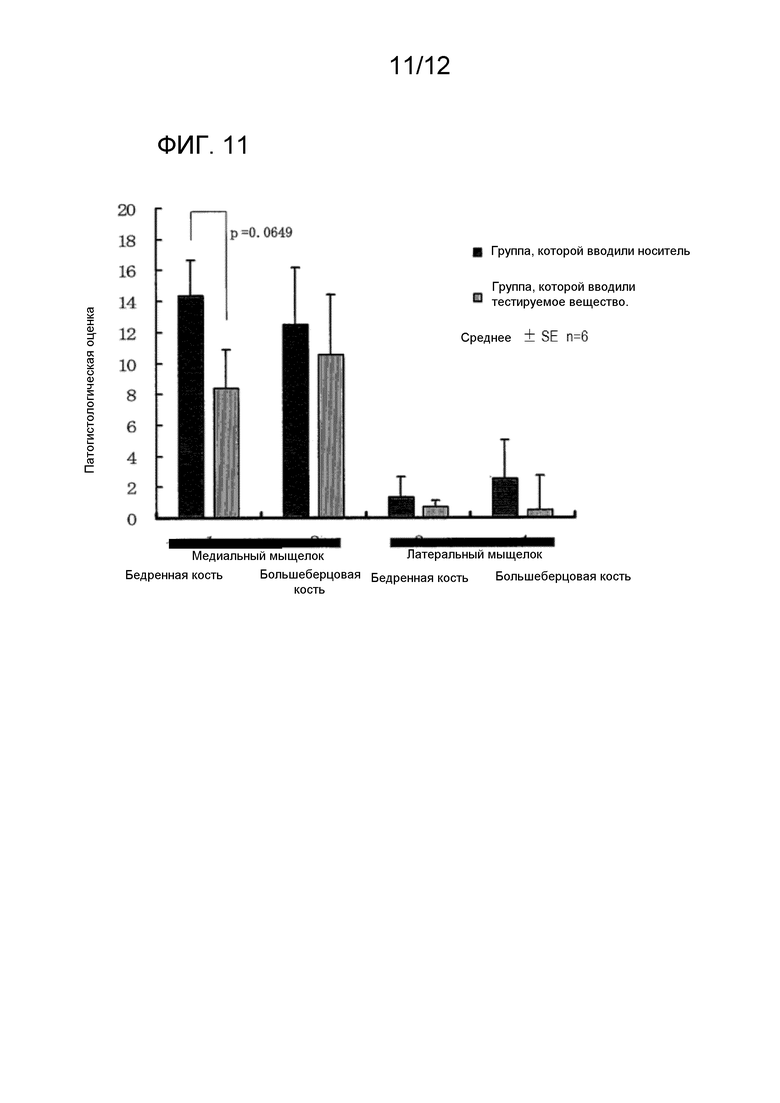
На фиг. 11 показана патогистологическая оценка мыщелка бедренной кости и большеберцовой кости.
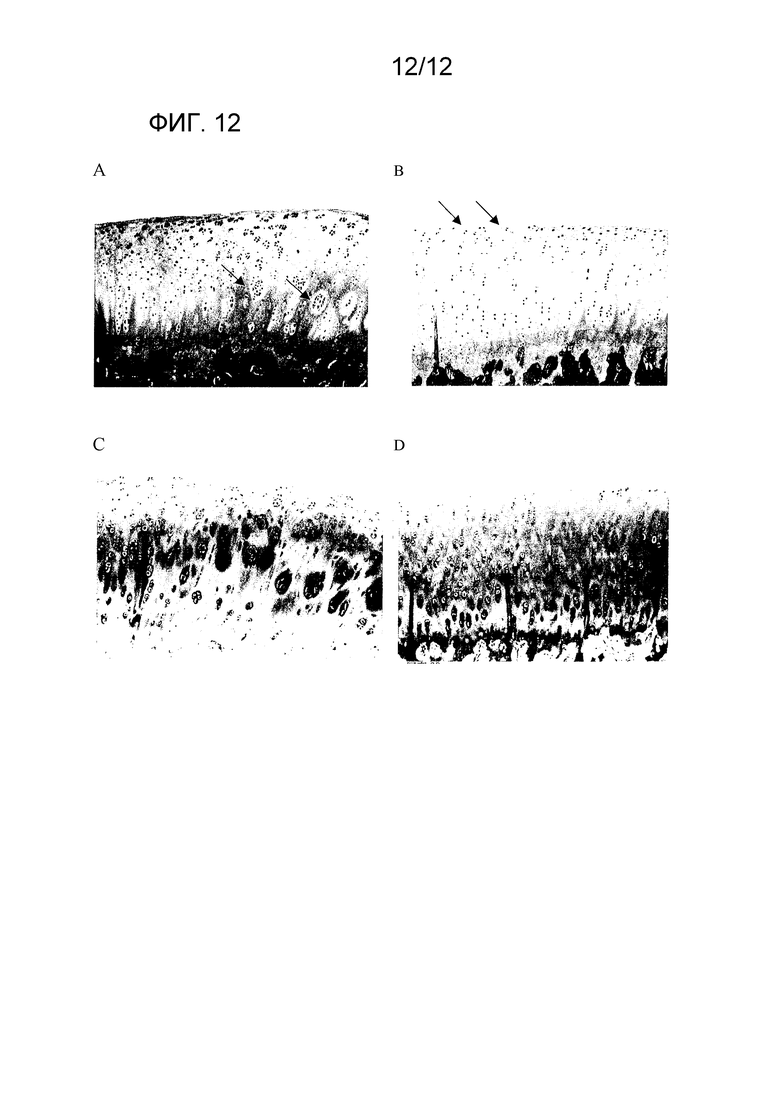
На фиг. 12 показаны патогистологические изображения характерных примеров. На изображении А показана группа, которой вводили носитель (№ животного 101), в которой в суставном хряще наблюдали дезорганизацию хондроцитов (показано стрелкой) и образование кластеров (показано стрелкой) (медиальная часть правого бедра, ГЭ окрашивание, увеличение ×200). На изображении В показана группа, которой вводили тестируемое вещество (№ животного 201), в которой наблюдали эрозию хряща (легкую) в суставном хряще (медиальная часть правого бедра, ГЭ окрашивание, увеличение ×200). На изображении С показана группа, которой вводили носитель (№ животного 101), в которой в суставном хряще наблюдали сниженное окрашивание протеогликана (легкое) (медиальная часть правого бедра, СО окрашивание, увеличение ×200). На изображении D показана группа, которой вводили тестируемое вещество (№ животного 201), в которой не наблюдали изменений суставного хряща (медиальная часть правого бедра, СО окрашивание, увеличение ×200).
Варианты осуществления изобретения
Далее в описании настоящее изобретение продемонстрировано более подробно.
Средство для лечения артроза по настоящему изобретению может быть использовано для лечения артроза, такого как остеоартрит, суставной ревматизм и ревматоидный полиартрит (и остеоартрит, в частности). Такие средства включают в качестве активного ингредиента циклическую фосфатидовую кислоту, карбоциклическую фосфатидовую кислоту или их соли. Любое соединение может быть использовано в качестве циклической фосфатидовой кислоты, карбоциклической фосфатидовой кислоты или их солей без определенного ограничения с условием, что такое соединение проявляет эффекты по настоящему изобретению. Предпочтительные примеры включают соединения, представленные формулой (I) ниже:
Формула 2
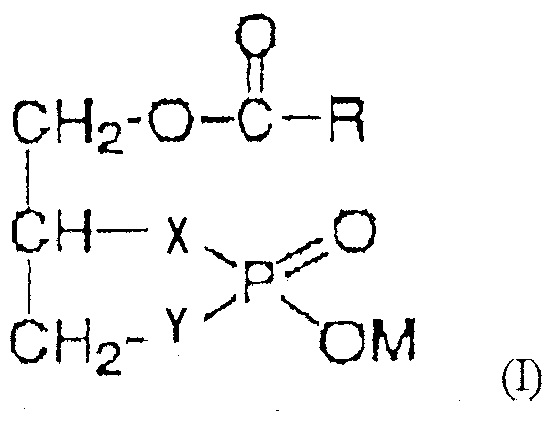
где R представляет собой линейную или разветвленную алкильную группу, имеющую от 1 до 30 атомов углерода, линейную или разветвленную алкенильную группу, имеющую от 2 до 30 атомов углерода, или линейную или разветвленную алкинильную группу, имеющую от 2 до 30 атомов углерода, которые могут содержать циклоалкановый или ароматический цикл; Х и Y каждый независимо представляет собой атом кислорода или метиленовую группу с условием, что Х и Y одновременно не являются метиленовой группой; и М представляет собой атом водорода или атом щелочного металла.
В формуле (I) специфические примеры линейных или разветвленных алкильных групп, имеющих от 1 до 30 атомов углерода, представленных заместителем R, включают метиловую группу, этиловую группу, пропиловую группу, бутиловую группу, пентиловую группу, гексиловую группу, гептиловую группу, октиловую группу, нониловую группу, дециловую группу, ундециловую группу, додециловую группу, тридециловую группу, тетрадециловую группу, пентадециловую группу, гексадециловую группу, гептадециловую группу, октадециловую группу, нонадециловую группу и эйкозиловую группу.
Специфические примеры линейных или разветвленных алкенильных групп, имеющих от 2 до 30 атомов углерода, представляющих заместитель R, включают аллильную группу, бутенильную группу, октенильную группу, деценильную группу, додекадиенильную группу и гексадекатриенильную группу. Их более специфические примеры включают 8-деценильную группу, 8-ундеценильную группу, 8-додеценильную группу, 8-тридеценильную группу, 8-тетрадеценильную группу, 8-пентадеценильную группу, 8-гексадеценильную группу, 8-гептадеценильную группу, 8-октадеценильную группу, 8-икозениловую группу, 8-докозенильную группу, гептадека-8,11-диенильную группу, гептадека-8,11,14 триенильную группу, нонадека-4,7,10,13-тетренильную группу, нонадека-4,7,10,13,16-пентенильную группу и геникоза-3,6,9,12,15,18-гексенильную группу.
Специфические примеры линейных или разветвленных алкинильных групп, имеющих от 2 до 30 атомов углерода, представляющих заместитель R, включают 8-децинильную группу, 8-ундецинильную группу, 8-додецинильную группу, 8-тридецинильную группу, 8-тетрадецинильную группу, 8-пентадецинильную группу, 8-гексадецинильную группу, 8-гептадецинильную группу, 8-октадецинильную группу, 8-икоцинильную группу, 8-докоцинильную группу и гептадека-8,11-диинильную группу.
Специфические примеры циклоалканового цикла, который может содержаться в вышеуказанной алкильной, алкенильной или алкинильной группе, включают циклопропановый цикл, циклобутановый цикл, циклопентановый цикл, циклогексановый цикл и циклооктановый цикл. Циклоалкановый цикл может содержать один или более гетероатомов и их примеры включают оксилановый цикл, оксетановый цикл, тетрагидрофурановый цикл и N-метилпиролидиновый цикл.
Специфические примеры ароматического цикла, который может содержаться в вышеописанной алкильной, алкенильной или алкинильной группе, включают бензольный цикл, нафталановый цикл, пиридиновый цикл, фурановый цикл и тиофеновый цикл.
Когда заместителем R является алкильная группа, замещенная циклоалкильным циклом, соответственно, специфические примеры включают циклопропилметиловую группу, циклогексилэтиловую группу и 8,9-метанопентадециловую группу.
Когда заместителем R является алкильная группа, замещенная ароматическим циклом, специфические примеры включают бензильную группу, фенетильную группу и п-пентилфенилоктиловую группу.
Предпочтительно R представляет собой линейную или разветвленную алкильную группу, имеющую от 9 до 17 атомов углерода, линейную или разветвленную алкенильную группу, имеющую от 9 до 17 атомов углерода, или линейную или разветвленную алкинильную группу, имеющую от 9 до 17 атомов углерода. Более предпочтительно R представляет собой линейную или разветвленную алкильную группу, имеющую 9, 11, 13, 15 или 17 атомов углерода, или линейную или разветвленную алкенильную группу, имеющую 9, 11, 13, 15 или 17 атомов углерода. Особенно предпочтительно R представляет собой линейную или разветвленную алкенильную группу, имеющую 9, 11, 13, 15 или 17 атомов углерода.
X и Y в соединениях, представленных формулой (I), каждый независимо представляет собой атом кислорода (-О-) или метиленовую группу (-СН2-) с условием, что X и Y одновременно не являются метиленовой группой. То есть комбинации X и Y включают следующие варианты:
(1) Х представляет собой атом кислорода и Y представляет собой атом кислорода;
(2) Х представляет собой атом кислорода и Y представляет собой метиленовую группу; или
(3) Х представляет собой метиленовую группу и Y представляет собой атом кислорода.
М в производном циклической фосфатидовой кислоты, представленном формулой (I), представляет собой атом водорода или атом щелочного металла. Примеры атомов щелочного металла включают литий, натрий и калий, натрий является особенно предпочтительным.
Специфически соединение, представленное формулой (I) в настоящем изобретении, является особенно предпочтительно производным циклической фосфатидовой кислоты или карбоциклической фосфатидовой кислоты, имеющей в качестве акриловой группы в положении 1 олеоиловую группу, в которой заместитель R представляет собой алкенильную группу, имеющую 17 атомов углерода (сокращенную как «С18:1»), или пальмитолеиловую группу, в которой заместитель R представляет собой алкенильную группу, имеющую 15 атомов углерода (сокращенную как «С16:1»).
Соединение, представленное формулой (I), может включать изомер, такой как позиционный изомер, геометрический изомер, таутомер или оптический изомер, в соответствии с типом его заместителя. Все возможные изомеры и смеси, включающие два или более типов таких изомеров в определенном соотношении, находятся в рамках настоящего изобретения.
Кроме того, соединение, представленное формулой (I), может находиться в форме аддукта, состоящего из соединения и воды или различных типов растворителей (гидраты или сольваты). Такой аддукт также находится в рамках настоящего изобретения. Более того, любые кристаллические формы соединения, представленного формулой (I), и его солей также находятся в рамках настоящего изобретения.
Соединение, представленное формулой (I), в котором X и Y представляют собой атомы кислорода, может быть химически синтезировано в соответствии с методом, описанным в, например, Японской патентной публикации (Kokai) # H05-230088 A (1993), H07-149772 A (1995), H07-258278 (1995) или H09-25235 (1997).
Также соединение, представленное формулой (I), в котором и X и Y представляют собой атомы кислорода, может быть синтезировано в соответствии с методом, описанным в Японской патентной публикации (Kokai) # 2001-178489 А путем возможной реакции фосфолипазы D с лизофосфолипидом. Лизофосфолипид, используемый в настоящем описании, особо не ограничен, пока он способен реагировать с фосфолипазой D. Известно множество типов лизофосфолипидов, известны молекулярные виды, содержащие различные типы жирных кислот или виниловых эфирных связей, и такие лизофосфолипиды являются коммерчески доступными. В качестве фосфолипазы D таковые, полученные из высших растений, таких как капуста или арахис, или таковые, происходящие от микроорганизмов, таких как Streptomyces chromofuscus или Actinomadula sp., являются коммерчески доступными в качестве реагентов, хотя циклическую фосфатидовую кислоту синтезируют ферментом, полученным от штамма Actinomadula sp. №362 очень селективным образом (Японская патентная публикация (Kokai) № Н11-367032 А (1999)). Реакцию между лизофосфолипидом и фосфолипазой D можно проводить в любых условиях, пока фермент способен осуществлять свое действие. Например, реакцию можно проводить в ацетатном буфере, содержащем хлорид кальция (рН около 5-6), при комнатной температуре или выше (предпочтительно 37°С) в течение 1-5 часов. Полученное производное циклической фосфатидовой кислоты может быть очищено в соответствии с обычной методикой посредством, например, экстракции, колоночной хроматографии или тонкослойной хроматографии (ТЖХ).
Соединение, представленное формулой (I), в которой Х представляет собой атом кислорода и Y представляет собой метиленовую группу, может быть синтезировано в соответствии с методом, описанным в литературе (Kobayashi S. et al. Tetrahedron Letters, 34, 4047-4050, 1993) или WO 2002/094286. Пример специфического пути синтеза показан ниже.
Формула 3
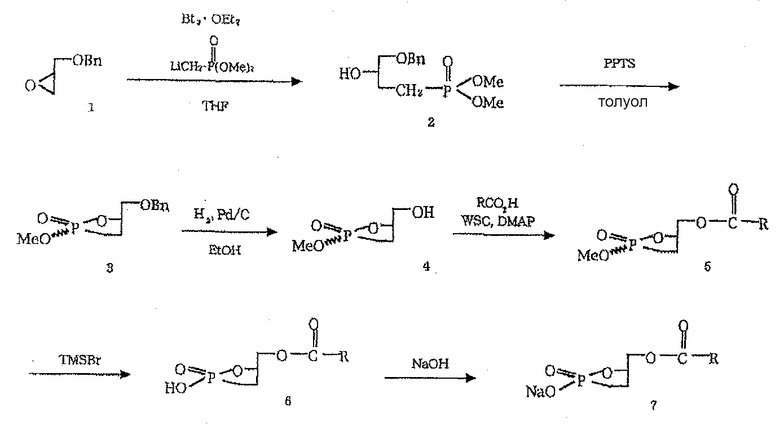
В вышеуказанных формулах, выше, коммерчески доступный (R)-бензилглицидиловый эфир (1) активируют с помощью BF3·Et2O, n-BuLi позволяют реагировать с диметилметилфосфонатом, и полученную литированную форму подвергают реакции для получения спирта (2).
Полученный спирт подвергают реакции в толуоле с использованием избыточного количества пиридиновой соли п-толуолсульфоновой кислоты при 80°С для получения циклизированной формы (3). Полученную циклизированную форму гидролизуют в атмосфере водорода с использованием 20% Pd(OH)2-C для проведения дебензилирования (4). Гидрохлориду 1-этил-3-(3-диметиламинопропил)карбодиимида, в качестве конденсатора, позволяют реагировать с жирной кислотой для получения связанной формы (5). Впоследствии бромтриметилсилан используют в качестве нуклеофила для исключительного удаления метиловой группы селективным образом по положению, таким образом, получая циклическую фосфоновую кислоту (6). Полученное вещество вводят в разделительную воронку с помощью эфира и к ним по каплям добавляют небольшое количество водного раствора 0,02Н гидроксида натрия для разделения жидкостей. Интересующее соединение экстрагируют и очищают в виде натриевой соли (7).
Соединение, представленное формулой (I), в которой Х представляет собой метиленовую группу и Y представляет собой атом кислорода, может быть синтезировано в соответствии с методом, описанным в Японской патентной публикации (Kokai) №2004-010582 А или Международной публикации WO 2003/104246.
Средство для лечения артроза по настоящему изобретению предпочтительно представлено в форме фармацевтической композиции, которая включает одну или более фармацевтически приемлемых добавок и соединение, представленное формулой (I), в качестве активного ингредиента.
Средство для лечения артроза по настоящему изобретению можно вводить в различных формах, и введение можно осуществлять перорально или парентерально (например, может использоваться внутривенное, внутримышечное, подкожное введение или внутрикожная инъекция, ректальное введение и введение через слизистые оболочки). Примеры лекарственных форм для фармацевтических композиций, подходящих для перорального введения, включают таблетку, гранулу, капсулу, порошок, раствор, суспензию и сироп. Примеры лекарственных форм для фармацевтических композиций, подходящих для парентерального введения, включают инъекции, инфузии, суппозиторий и средства, всасываемые через кожу. Лекарственная форма для средства по настоящему изобретению ими не ограничена. Более того, средство также может быть сделано в виде композиций отложенного высвобождения в соответствии с методами, известными в области техники.
Типы фармацевтических добавок, используемых для получения средства для лечения артроза, в соответствии с настоящим изобретением особо не ограничены, и специалист в области техники может выбрать адекватные добавки. Примеры добавок, которые могут быть использованы, включают вспомогательные вещества, дезинтегрирующие вещества или средства, способствующие дезинтеграции, вяжущие вещества, смазывающие вещества, оболочки, основания, растворители или солюбилизаторы, диспергирующие средства, суспендирующие средства, эмульгаторы, буферы, антиоксиданты, антисептики, изотонические средства, средства, регулирующие рН, растворяющие средства и стабилизаторы. Каждый специфический ингредиент, используемый для вышеуказанных целей, хорошо известен специалисту в области техники.
Примеры фармацевтических добавок, которые могут быть использованы для получения пероральных препаратов, включают: вспомогательные вещества, такие как глюкоза, лактоза, D-маннит, крахмал или кристаллическая целлюлоза; дезинтегрирующие вспомогательные средства, такие как карбоксиметилцеллюлоза, крахмал или карбоксиметилцеллюлоза кальция; вяжущие вещества, такие как гидроксипропилцеллюлоза, гидроксипропилметилцеллюлоза, поливинилпирролидон или желатин; смазывающие средства, такие как стеарат магния или тальк; средства для оболочки, такие как гидроксипропилметилцеллюлоза, белый сахар, полиэтиленгликоль или оксид титана; и основания, такие как вазелин, жидкий парафин, полиэтиленгликоль, желатин, каолин, глицерин, очищенная вода или твердый жир.
Примеры фармацевтических добавок, которые могут быть использованы для получения инъекционных или инфузионных препаратов, включают: растворитель или солюбилизатор, который может быть использован для водных инъекционных препаратов или инъекционных препаратов, растворяемых перед применением, таких как дистиллированная вода для инъекций, физиологический раствор, пропиленгликоль или поверхностно-активное вещество; изотоническое средство, такое как глюкоза, хлорид натрия, D-маннит или глицерин; и средство, регулирующее рН, такое как неорганическая кислота, органическая кислота, неорганическое основание или органическое основание.
Средство для лечения артроза по настоящему изобретению можно вводить млекопитающим, включая людей.
Доза средства для лечения артроза по настоящему изобретению должна увеличиваться или уменьшаться в соответствии с условиями, такими как возраст, пол, масса тела, симптомы пациента и путь введения. Доза активного ингредиента в сутки для взрослого обычно составляет 1 мкг/кг до 1000 мг/кг и предпочтительно от 10 мкг/кг до 100 мг/кг. Средство можно вводить в количествах, упомянутых выше, один или несколько раз в сутки (например, около 2-4 раз).
Настоящее изобретение описано более подробно со ссылками на следующие примеры, хотя настоящее изобретение не ограничено примерами.
ПРИМЕРЫ
Пример 1
(1) Метод
(1-1) Культура суставных хондроцитов и синовиоцитов
Использовали гиалиновый суставной хрящ, который забирали от пациента с коленным остеоартрозом в момент замены искусственным коленным суставом. Кусочки суставного хряща промывали и подвергали ферментативной обработке проназой и коллагеназой для разрушения матрицы хряща. После этого клетки получали, культивировали и затем криоконсервировали. Также забирали синовиоциты. В этом примере использовали такие суставные хондроциты и синовиоциты, полученные от пациента с остеоартритом, указанные клетки подвергали культивированию в монослое высокой плотности во избежание трансформации, и культивированные клетки затем подвергали эксперименту. Использовали среду, состоящую из DMEM, 10% FBS и 1% антибиотиков/противогрибковых средств, среду заменяли средой без сыворотки при достижении слияния и затем начинали эксперимент.
(1-2) Добавление циклической фосфатидовой кислоты или карбоциклической фосфатидовой кислоты (сРА)
В качестве циклической фосфатидовой кислоты и карбоциклической фосфатидовой кислоты использовали С16:1-сРА (сРА) и нативную сРА (NcPA) соответственно, и указанные вещества исследовали в отношении продукции гиалуроновой кислоты (НА), экспрессии ферментов, синтезирующих гиалуроновую кислоту (НА) (HAS1, HAS2 и HAS3), и ферментов, разрушающих гиалуроновую кислоту (НА) (HYAL1 и HYAL2), в концентрациях 0-50 нМ в течение 0-48 часов.
Химическая структура С16:1-сРА (указанная как «сРА» на чертеже) представлена ниже
Формула 4
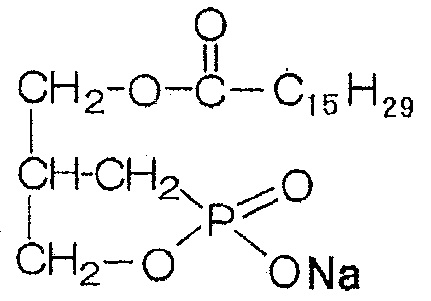
Нативную сРА (обозначенную как «NcPA» на чертеже) получали способом, описанным ниже (см. примеры 1 и 3 Японской патентной заявки №2011-126901).
Соевый фосфолипид (10 г; содержание лецитина: 70%) растворяли в 100 мл 1 М ацетатного буфера (рН 6,5), содержащего 0,3 М хлорида кальция, добавляли 6000 единиц фосфолипазы А2, полученной от Streptomyces, и смесь подвергали реакции при 40°С в течение 18 часов при перемешивании. Уровень рН реакционного раствора доводили до 2,5 для инактивации фермента, добавляли 100 мл хлороформа и 50 мл метанола и тщательно смешивали посредством перемешивания, и экстрагировали липидные компоненты. Слой хлороформа получали и отверждали досуха при пониженном давлении в ротационном испарителе. К твердым компонентам для осаждения фосфолипидов добавляли ацетон (100 мл) и удаляли свободные жирные кислоты. Осадок (5 г) растворяли в 40 мл хлороформа, к нему добавляли 10 мл 1 М ацетатного буфера (рН 5,5), дополнительно добавляли 1500 единиц фосфолипазы D, полученной от Actinomadura, и смесь подвергали реакции при 40°С в течение 18 часов при перемешивании. К реакционному раствору добавляли 20 мл 3 М раствора хлорида натрия и 20 мл 0,1 М раствора ЭДТА, и продукт реакции подвергали перемешиванию при 40°С в течение 1 часа. Далее добавляли 20 мл метанола, смесь тщательно перемешивали, и продукт реакции центрифугировали при 3000 об/мин в течение 5 минут для получения слоя хлороформа. Раствор отверждали досуха при пониженном давлении в ротационном испарителе и получали 3,8 г натриевой соли циклической фосфатидовой кислоты. Выход составил 54,3%, так как 3,8 г циклической фосфатидовой кислоты Na получали из соевого фосфолипида с содержанием лецитина 70% (т.е. 7 г лецитина в 10 г соевого фосфолипида). Чистоту натриевой соли циклической фосфатидовой кислоты анализировали с использованием силикагелевого планшета, образец распределяли на планшете с хлороформом:метанолом:уксусной кислотой:5% дисульфитом натрия (100:40:12:5, об./об.), и планшет погружали в смесь 5% ацетата меди, 8% фосфорной кислоты и 2% серной кислоты на короткий период времени. Планшет сушили на воздухе и нагревали при 180°С в течение около 10 минут, и образующиеся пятна изучали с использованием сканера (производимого ATTO Corporation). Специфически, контрольный продукт (чистота 97%) использовали в качестве контрольного образца, и пятна в тонкослойном хроматографе изучали с использованием денситометра с последующей количественной оценкой на основании соотношения площади. Чистота натриевой соли циклической фосфатидовой кислоты в продукте, полученном на вышеуказанной стадии, составила 54%.
Натриевую соль циклической фосфатидовой кислоты (500 мг) растворяли в 5 мл хлороформа, содержащего 10% метанола, наносили на силикагелевую колонку, распределяли с помощью растворителя, описанного выше, дополнительно распределяли с помощью хлороформа, содержащего 20% метанола, и фракционировали на фракции по 10 мл каждая. Фракции, содержащие натриевую соль циклической фосфатидовой кислоты, собирали в соответствии с методом ТЖХ, описанным выше, и отверждали досуха при пониженном давлении в ротационном испарителе. Таким образом, получали 320 мг порошка натриевой соли циклической фосфатидовой кислоты. Чистота натриевой соли циклической фосфатидовой кислоты в образце составила 95%.
(1-3) Измерение экспрессии фермента, синтезирующего НА, и экспрессии фермента, разрушающего НА
Культуре хондроцитов заменяли среду без сыворотки за 24 часа до начала эксперимента и добавляли сРА или N-сРА в различных концентрациях (0, 5, 10, 25 или 50 мкМ). Также культуре периостальных клеток заменяли среду без сыворотки за 24 часа до начала эксперимента и добавляли сРА в различных концентрациях (0, 10 или 25 мкМ). Общую РНК выделяли из культуры клеток через 0, 0,5, 1, 2 и 4 часа, синтезировали кДНК и уровень экспрессии HAS1, HAS2, HAS3, HYL1 и HYL2 оценивали количественно посредством ПЦР в реальном времени. Уровень экспрессии определяли относительно гена β-актина (т.е. контрольного гена) и представляли относительно контрольного значения без добавления сРА или N-сРА или значения до их добавления, которое нормализовали до 1.
Специфически, соотношение экспрессии определяли методом ΔΔCt, включающим сравнение различий в пороге количества циклов (значение Ct), полученного для мишени и контроля в образце с значением СТ, полученным для контрольного образца, как описано ниже.
1) ΔCt определяли с использованием Ct, полученного для соответствующего образца:
ΔCt = Ct (ген мишень) – Ct (контрольный ген);
2) ΔΔCt определяли:
ΔΔCt = ΔCt (ген мишень) – ΔCt (контрольный ген);
3) Уровень экспрессии целевого гена в целевом образце нормализовали:
2(-ΔΔCt);
4) изменения уровня экспрессии целевого гена определяли со ссылками на значение контрольного образца, нормализованное до 1.
(1-4) Измерение продукции гиалуроновой кислоты (НА).
Культуре хондроцитов заменяли среду без сыворотки за 48 часов до начала эксперимента и добавляли сРА и N-сРА в различных концентрациях (0, 10 или 50 мкМ). Надосадочную жидкость культуры забирали через 0, 6, 12, 24 и 48 часов. Посредством сэндвич анализа ELISA, включающего использование НА-связывающих белков, полученных из носового хряща быка (QnE Hyaluronic Acid (HA) ELISA Assay Kit; Biotech trading Partners, Inc), количественно оценивали продукцию НА.
(2) Результаты
(2-1) Результаты анализа экспрессии ферментов, синтезирующих НА, и ферментов, разлагающих НА
На каждой из фиг. 1-5 показаны результаты анализа экспрессии ферментов, синтезирующих НА, и ферментов, разрушающих НА в хондроцитах. Как показано на фиг. 1–5, С16:1-сРА (сРА) непрерывно индуцировала экспрессию HAS2 зависимо от концентрации. Тогда как экспрессия HAS1 и HAS3 транзиторно индуцировалась через 2 часа после добавления, уровень экспрессии снижался через 4 часа. NcPA давала похожие результаты. На экспрессию ферментов, разрушающих НА (HYL1, HYL2 и HYL3), не было выявлено влияния. Полученные результаты демонстрируют, что сРА и NcPA индуцируют экспрессию ферментов, синтезирующих НА. Также на фиг. 7 показаны результаты анализа экспрессии в синовиоцитах ферментов, синтезирующих НА, и на фиг. 8 показаны результаты анализа экспрессии в синовиоцитах ферментов, разрушающих НА.
(2-2) Результаты измерения продукции гиалуроновой кислоты (НА)
На фиг. 6 показаны результаты измерения продукции НА. Как показано на фиг. 6, С16:1-сРА (сРА) ускоряла синтез НА в хондроцитах с отсрочкой по времени и высвобождала НА из клеток. Через сорок восемь часов количество НА, продуцируемое в группе, которой добавляли сРА в количестве 50 нМ, было приблизительно в 3 раза больше, чем продуцируемое в группе, которой вводили носитель. NсРА давала сходные результаты. Полученные результаты демонстрируют, что С16:1-сРА (сРА) и NcPA ускоряют продукцию НА в суставных хондроцитах с остеоартритом (ОА).
(3) Заключение
Обнаружили, что циклическая фосфатидовая кислота или карбоциклическая фосфатидовая кислота, представленная формулой (I), индуцирует экспрессию ферментов, синтезирующих НА, и ускоряет продукцию НА в суставных хондроцитах человека с ОА, как в случае с фибробластами кожи.
Пример 2: Оценка эффектов ScPA в отношении остеоартрита колена кролика
(1) Метод
(1-1) Используемые животные и условия выращивания
Использовали двенадцать 11-12-недельных самцов кроликов (Kbs:NZW). Кроликов выращивали в отдельных клетках (один кролик на клетку) при 14,4°С–24,9°С при свете (12 часов с 7.00 утра до 7.00 вечера) с непрерывной вентиляцией. Кроликам позволяли потреблять 150 г корма (CR-3, CLEA Japan, Inc.) в сутки и пить водопроводную воду.
(1-2) Вводимые вещества
Использовали натриевую соль (2-гидрокси-2-оксид-1,2-оксафосфолан-4-ил)метилового эфира (9Z)-9-октадеценовой кислоты (С18:1-сРА; далее называемая как «ScPA»).
Формула 5
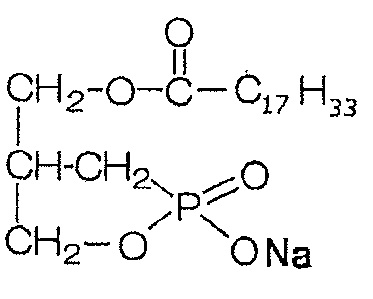
Физиологический раствор использовали в качестве растворителя.
(1-3) Получение модели остеоартрита
Волосы вокруг коленного сустава правой задней ноги кролика сбривали с использованием электрической машинки для стрижки под глубокой анестезией и побритую область дезинфицировали изодином. Наружную оболочку медиальной части правой задней конечности рассекали скальпелем, дополнительно рассекали границы между медиальной частью и капсулой сустава надколенно-бедренной связки и затем отсекали надколенно-бедренную связку. После этого суставную капсулу широко раскрывали, чтобы открыть медиальный мениск, который затем полностью удаляли. После удаления мениска ткани и эпидермис вокруг капсулы сустава зашивали. В момент ушивания область операции промывали физиологическим раствором (титр: 500 мг/20 мл), содержащим антибиотики (Вициллин, Meiji Seika Pharma Co., Ltd.).
В день хирургического лечения (день 0) кроликам позволяли свободно пить воду натощак. Пробуждение подтверждали посредством наблюдения спонтанных движений головы. Для предотвращения снижения температуры тела животных их подогревали, оборачивая их тела в полотенца до подтверждения пробуждения. Также положение тела адекватно меняли для предотвращения депонирования крови. С целью профилактики инфекции внутримышечно вводили антибиотик (вициллин: 3 ЕД/кг) один раз в сутки до 5 дней после лечения (день 5).
После получения модели животных их делили на две группы, каждая состоящая из 6 особей, при усреднении температуры тела (т.е. группа, которой вводили носитель, номера животных 101-106 и группа, которой вводили тестируемое вещество, номера животных 201-206).
(1-4) Введение тестируемого соединения и носителя в полость сустава
Тестируемое соединение и носитель вводили способом, описанным ниже.
Путь введения: в полость сустава
Место введения: правая задняя конечность (обработанная конечность)
Время введения: в дни 7, 11, 14, 18, 21, 25, 28, 32, 35 и 39
Дозировка: Тестируемое соединение: 10 мкг/кролика (объем: 0,2 мл)
Носитель: 0,2 мл/кролика
Средства введения: с использованием 1,0 мл шприца (Terumo Corporation) и инъекционной иглы 27G (Terumo Corporation)
(1-5) Оценка боли (распределение массы между обеими задними конечностями)
Частота измерений:
Измерения проводили всего семь раз: т.е. до лечения и через 1, 2, 3, 4, 5 и 6 недель после лечения.
Метод измерения:
Отдельно измеряли массу тела, нагруженную на правую заднюю конечность и левую заднюю конечность, с использованием массовой шкалы, и распределение массы на обработанную конечность (правая задняя конечность) определяли с использованием следующего уравнения:
Распределение массы (%) на обработанную конечность (правая задняя конечность) = [правая задняя конечность (кг)/правая задняя конечность (кг) + левая задняя конечность (кг)]×100
(1-6) Оценка отека (отек суставов обеих задних конечностей)
Частота измерений:
Измерения проводили 6 недель после лечения.
Метод измерения:
Наибольшую площадь суставов правой и левой задних конечностей измеряли с использованием цифровых циркулей и отек сустава, индуцированный остеоартритом, определяли с использованием следующего уравнения:
Отек (%) обработанной конечности (правая задняя конечность) = [(правая задняя конечность (мм) – левая задняя конечность (мм))/(левая задняя конечность (мм) + левая задняя конечность (мм))]×100
(1-7) Получение образцов биоматериалов (день 42) и обработка после взятия образцов
У животных отсекали четыре конечности под глубокой анестезией, вызывая их смерть от потери крови. После этого мыщелок бедра и мыщелок большеберцовой кости удаляли из коленного сустава обработанной конечности (правая задняя конечность) с последующей фиксацией в 10% растворе нейтрального буферного формалина.
(1-8) Получение патологических образцов и их патогистологическая оценка
Бедренную и большеберцовую кость, которые погружали и фиксировали в 10% растворе нейтрального буферного формалина, подвергали деминерализации EDTA. После завершения деминерализации окрашенные участки, идентифицированные ниже, погружали в парафин в соответствии с обычной методикой, и продукт нарезали на куски толщиной 4 мкм каждый. Срезы подвергали окрашиванию гематоксилином-эозином (ГЭ) и окрашиванию сафранином О (протеогликан) и гистологически оценивали под оптическим микроскопом (BX51TF; OLYMPUS). Степень дегенерации хряща патологических образцов оценивали в соответствии с критериями, показанными в таблице 1 ниже (Kikuchi T., Yoneda H. et al. Osteoarthritis cartilage, 4; p.99 и последующие страницы, 1996). Специфически образцы оценивали в отношении потери следующих 8 параметров в соответствии с пятибалльной оценкой (от 0 до +4): поверхностный слой; эрозия хряща; расслоение и/или трещины; снижение окрашивания протеогликана (окрашивание сафранином О); дезорганизация хондроцитов; потеря хондроцитов; обнажение субхондральной кости; и образование кластеров. Суммарный общий балл всех пунктов определяли как общий балл. Наблюдаемые пункты без специфических критериев определения в Таблице 1 оценивали в соответствии с критериями, показанными в таблице 2 ниже (Naoki Ishiguro et al., Journal of Surgery, 29: p.112 и последующие страницы, 2010).
Уменьшение клеток
обнажение кости
наблюдают на протяжении 1/3–2/3 площади
оцениваемого участка
(1-9) Обработка данных и статистический анализ
Отдельно определяли среднее для группы (среднее) и его стандартную ошибку (SE) для распределения массы между обеими задними конечностями и для отека суставов обеих задних конечностей. После этого для группы, которой вводили тестируемое вещество, и группы, которой вводили носитель, оценивали F-критерий. При отсутствии расхождений между образцами проводили оценку t-критерия Стьюдента. При наличии расхождения между образцами проводили оценку t-критерия Аспина-Уэлча. Относительно общих баллов оцениваемых параметров патогистологического исследования определяли среднее по группе (среднее) и его стандартную ошибку (SE) и затем различия между средними значениями для двух групп определяли посредством U-критерия Манн-Уитни. Двухсторонний уровень достоверности устанавливали как 5% и 1%.
(2) Результаты
(2-1) Оценка боли (распределение массы между обеими задними конечностями)
В таблице 3 и на фиг. 9 показаны изменения распределения массы между обеими задними конечностями со дня получения модели животных (день 0) до дня, в который забирали биоматериалы (день 42). В группе, которой вводили носитель, восстановление после хирургического вмешательства наблюдали до дня 14, остеоартрит индуцировали после этого, масса, нагружаемая на обработанную конечность (правая задняя конечность), снижалась из-за боли, вызванной остеоартритом, и масса снижалась до 28% ко дню, в который забирали образцы биоматериалов (день 42). В группе, которой вводили тестируемое вещество, наоборот, восстановление после хирургического вмешательства наблюдали к 14 дню, как в группе, которой вводили носитель, и после этого масса, нагружаемая на обработанную конечность (правая задняя конечность), сохранялась на более высоком уровне до дня, в который забирали образцы (день 42), по сравнению с группой, которой вводили носитель. Статистическую достоверность наблюдали как результат измерений в день 42 (р=0,0053).
Оценка боли (распределение массы по обеим задним конечностям)
(2-2) Оценка отека (отек суставов обеих задних конечностей)
В таблице 4 и на фиг. 10 показаны процентные значения отека суставов обеих задних конечностей в день, когда забирали образцы биоматериалов (день 42). Размеры сустава отдельного животного измеряли и определяли расхождение между группами. В результате отек суставов существеннее ингибировался в группе, которой вводили тестируемое вещество, по сравнению с группой, которой вводили носитель (р=0,0164).
Оценка отека (отек суставов обеих задних конечностей)
(2-3) Патогистологическое исследование
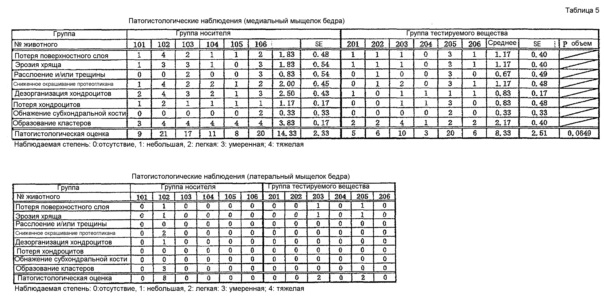
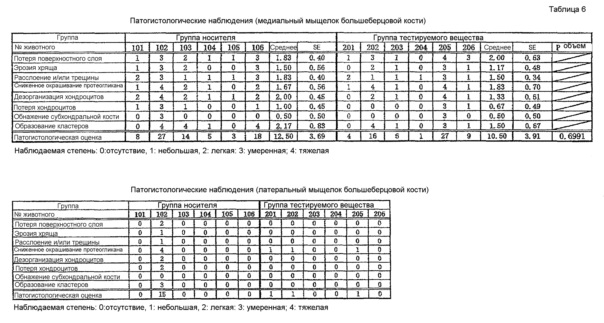
В таблице 5 и на фиг. 11 показано резюме результатов патогистологических исследований и на фиг. 12 показаны патогистологические изображения характерных примеров.
В группе, которой вводили носитель, и в группе, которой вводили тестируемое вещество, по существу не наблюдали повреждений в латеральных мыщелках бедренной кости или большеберцовой кости в результате получения модели остеоартроза.
Касательно медиального мыщелка бедренной кости, потерю поверхностного слоя суставного хряща, сниженную окрашиваемость протеогликана, дезорганизацию хондроцитов, потерю хондроцитов и образование кластеров наблюдали во всех 6 образцах в группе, которой вводили носитель, и эрозию хряща наблюдали в 5 из 6 образцов. Степень образования кластеров была особенно высокой во всех образцах (среднее = 2,50±0,43). Патогистологические оценки наблюдаемых показателей составили 9, 21, 17, 11, 8 и 20 (среднее 14,33±2,33), и в суставном хряще всех образцов наблюдали изменения от легких до тяжелых. Касательно медиального мыщелка бедренной кости, образование кластеров наблюдали во всех 6 образцах в группе, которой вводили тестируемое вещество, и потерю поверхностного слоя хряща, эрозию хряща и дезорганизацию хондроцитов наблюдали в 5 из 6 образцах. Патогистологические оценки составили 5, 6, 10, 3, 20 и 6 (среднее = 8,33±2,51), и такие изменения, наблюдаемые в 4 из 6 образцов, были меньше таковых, наблюдаемых в группе, которой вводили носитель в тех же областях. То есть патогистологические оценки группы, которой вводили тестируемое вещество, были ниже таковых группы, которой вводили носитель (р=0,0649).
Касательно медиального мыщелка большеберцовой кости, потерю поверхностного слоя суставного хряща, расслоение и/или трещины хряща и дезорганизацию хондроцитов наблюдали во всех 6 образцах группы, которой вводили носитель, и более низкую окрашиваемость протеогликана наблюдали в 5 из 6 образцов. Патогистологические оценки составили 8, 27, 14, 5, 3 и 18 (среднее = 12,50±3,69), и изменения суставного хряща от легких до тяжелых наблюдали в 4 из 6 образцов. В группе, которой вводили тестируемое вещество, расслоение и/или трещины хряща наблюдали во всех 6 образцах, и потерю поверхностного слоя хряща и сниженное окрашивание протеогликана наблюдали в 5 из 6 образцов. Патогистологические оценки составили 4, 16, 6, 1, 27 и 9 (среднее = 10,50±3,91).
Группа изобретений относится к лечению артроза. Терапевтическое средство при артрозе содержит в качестве активного ингредиента соединение, представленное формулой (I):
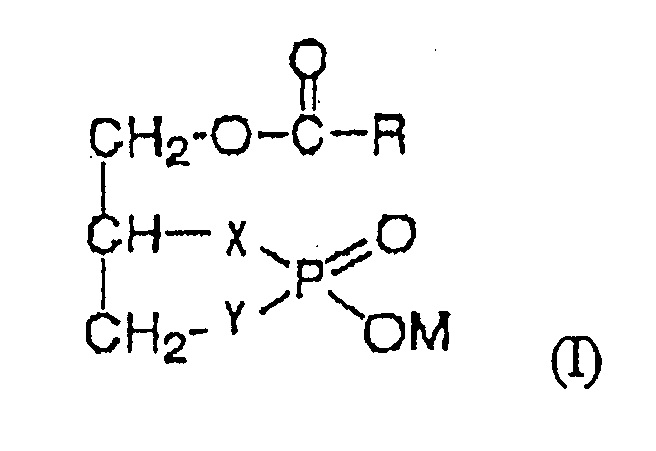
где R представляет собой линейную или разветвленную алкенильную группу, имеющую от 2 до 30 атомов углерода; X представляет собой атом кислорода или метиленовую группу, и Y представляет собой атом кислорода; и М представляет собой атом водорода или атом натрия. Также раскрыт способ лечения артроза, включающий введение соединения, представленного формулой (I), пациенту с артрозом. Группа изобретений позволяет достигнуть ингибирующего эффекта в отношении деструкции суставного хряща и выраженного терапевтического действия в отношении артроза за счет ускорения продукции гиалуроновой кислоты в хондроцитах. 2 н. и 3 з.п. ф-лы, 12 ил., 6 табл., 2 пр.
1. Терапевтическое средство при артрозе, которое содержит в качестве активного ингредиента соединение, представленное формулой (I):
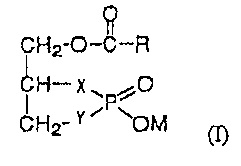
где R представляет собой линейную или разветвленную алкенильную группу, имеющую от 2 до 30 атомов углерода; X представляет собой атом кислорода или метиленовую группу, и Y представляет собой атом кислорода; и М представляет собой атом водорода или атом натрия.
2. Терапевтическое средство при артрозе по п. 1, где в формуле (I) X представляет собой атом кислорода.
3. Терапевтическое средство при артрозе по п. 1, где в формуле (I) X представляет собой метиленовую группу.
4. Терапевтическое средство при артрозе по п. 1 или 2, где соединение, представленное формулой (I), представляет собой карбоциклическую фосфатидовую кислоту, 1-олеил-циклическую фосфатидовую кислоту или 1-пальмитолеил циклическую фосфатидовую кислоту.
5. Способ лечения артроза, включающий введение соединения, представленного формулой (I), пациенту с артрозом:
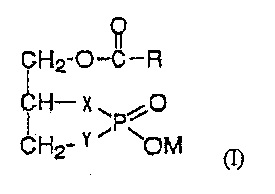
где R представляет собой линейную или разветвленную алкенильную группу, имеющую от 2 до 30 атомов углерода; X представляет собой атом кислорода или метиленовую группу, и Y представляет собой атом кислорода; и М представляет собой атом водорода или атом натрия.
| WO 2002094286 A1, 28.11.2002 | |||
| WO 2003104246 A1, 18.12.2003 | |||
| WO 2002083148 A1, 24.10.2002 | |||
| WO 2002083149 A1, 24.10.2002 | |||
| WO 2004091496 A2, 28.10.2002 | |||
| СРЕДСТВО "АРТРОВИТ" ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ АРТРИТОВ И АРТРОЗОВ | 2003 |
|
RU2240131C1 |
Авторы
Даты
2018-03-05—Публикация
2012-10-12—Подача