Это изобретение относится к новому применению композиции, содержащей полидезоксирибонуклеотиды (в дальнейшем ПДРН).
Композиция, применяемая в соответствии с изобретением, включает фракцию полимерных цепей ПДРН различной молекулярной массы, полученную из естественных источников, животного или растительного происхождения, таких как плацента и сперма рыб или растения.
Композиции на основе ПДРН, как определено выше, известны и коммерчески доступны.
FR 2676926 описывает фармацевтические композиции, содержащие в высокой степени полимеризированные полидезоксирибонуклеотиды, полученные из спермы рыб и используемые для лечения или предупреждения иммунных дефицитов; описаны композиции, содержащие полидезоксирибонуклеотиды в неионном растворителе, которые можно применять парентерально, особенно внутримышечно и/или внутривенно.
Процессы подготовки полидезоксирибонуклеотидов, полученных из плацент млекопитающих, описаны в EP 0226254.
Это изобретение относится к композициям на основе ПДРН, экстрагированных из естественных источников, для применения в терапевтическом лечении и/или в качестве терапевтического вспомогательного средства при лечении заболеваний костей и суставов, в частности, при остеоартрите, которые вводят внутрь сустава.
Другим объектом изобретения является применение ПДРН-композиции для производства медицинского устройства, пригодного в качестве вспомогательного средства при лечении дегенеративных заболеваний суставов.
В контексте изобретения используются вводимые внутрь суставов составы, содержащие высокоочищенную фракцию ПДРН, предпочтительно с чистотой более чем 95%, и более предпочтительно, больше чем 98%, предпочтительно полученную из спермы рыб.
Применяемые ПДРН предпочтительно обладают молекулярной массой от 20 кДальтонов до 2500 кДальтонов, более предпочтительно от 70 кДальтонов до 240 кДальтонов.
Как правило, в применяемых составах фракция ПДРН присутствует в концентрации от 0,1% до 10% по массе, предпочтительно от 0,5 до 3% по массе в водном солевом растворителе, указанная масса, относящаяся к общей массе состава.
Водный солевой растворитель предпочтительно содержит хлорид натрия и смесь дигидро фосфата натрия и гидро кислого фосфата натрия.
Применяемые ПДРН можно получить из животного или растительного источника, который богат ДНК, используя процессы, описанные в вышеупомянутой литературе; предпочтительным выбором является сперма рыб. Например, ПДРН, который может применяться в контексте изобретения, может быть получен путем процесса, включающего стадии:
1) ферментативный лизис белкового органического матрикса
2) осветляющая фильтрация образующегося раствора
3) осаждение четвертичными аммониевыми солями
4) декомплексирование преципитата
5) молекулярная селекция с использованием хроматографической колонки
6) осаждение элюата с использованием алкоголя.
В частности, вводимый продукт, лекарственное средство или медицинское устройство по изобретению предоставляется в форме пузырька или бутылки или в форме предварительно заполненного шприца, содержащего отмеренное количество ПДРН, например, от 1 мл до 4 мл (предпочтительно 2 мл) раствора ПДРН в концентрации от 1 мг/мл до 100 мг/мл (предпочтительно 5-30 и, в частности, приблизительно 20 мг/мл), с pH от 6,5 до 7,5 и имеющего вязкую консистенцию с увлажняющей, смазывающей и трофической функцией.
Композиция в соответствии с изобретением, в дальнейшем называемая CONDROTIDE, обладает следующими особенностями:
- внешний вид: прозрачный раствор
- цвет: бесцветный
- pH: 6,5-7,5
- объем, который можно выдавить из шприца: 2,00-2,05 мл
- осмолярность: 270-330 мОс/кг
- УФ-идентификация ПДРН: максимальное поглощение 258±2 нм
- УФ-измерение ПДРН: 18-22 мг/мл
- стерильность: стерильно (стерилизацию проводят при T>100, обычно при 120-121°C в течение предпочтительно 15 минут)
- бактериальный эндотоксин: <70 ЭЕд/мл.
Новое применение ПДРН-композиции, к которому относится изобретение, основано на следующих экспериментальных наблюдениях.
Экспериментальные фармакологические исследования in vitro проводили, когда разработка изобретения показала, что молекулы ПДРН, присутствующие в композициях по изобретению, обладают важным трофическим действием на первичные культуры синовиальных клеток, хондроцитов и хрящевых биопсий, это наблюдение согласуется с клиническим наблюдением, что результаты действия упомянутых композиций (CONDROTIDE) могут улучшаться и поддерживаться в течение долгого времени, в отличие от результатов, полученных для гиалуроновой кислоты.
В частности, было показано (путем цитофлуорометрического анализа и специфического окрашивания), что образование внеклеточного матрикса (коллагена II-го типа и аггрекана) значительно индуцируется в клеточных культурах, поддерживаемых в среде с добавлением 0,01% CONDROTIDE в течение двух недель; контрольные культуры, поддерживаемые в среде с добавлением 1% гиалуроновой кислоты, показали значительно меньшее образование клеточного матрикса.
Также были проведены гистологические исследования хрящевых биопсий, поддерживаемых в культуре в течение трех недель с использованием стандартной среды с добавлением гиалуроновой кислоты (1%) или CONDROTIDE (0,01%). Гистологическая проверка снова показала большее образование внеклеточного матрикса в образцах, обработанных CONDROTIDE, по сравнению с образцами, к которым была добавлена гиалуроновая кислота.
В частности то, о чем сообщено выше, является результатом следующих экспериментов.
Эксперимент 1: Хрящевые биопсии
Было выполнено исследование для оценки эффектов CONDROTIDE (состав, указанный выше) и гиалуроновой кислоты на ex vivo-фрагменты хрящевой ткани (в течение трех недель), сравнивая их с таковыми из стандартного раствора, обычно используемого в лаборатории для поддержания хрящевых биопсий.
Образец: хрящевые биопсии получение из хирургии.
Экспериментальные группы:
1. PN: биопсии, поддерживаемые в «хрящевой» среде + 0,01% CONDROTIDE,
2. НА: биопсии, поддерживаемые в «хрящевой» среде + 1% гиалуроновой кислоты,
3. CT: биопсии, поддерживаемые в «хрящевой» среде без добавок.
Конечная точка: Гистологический анализ.
Результаты
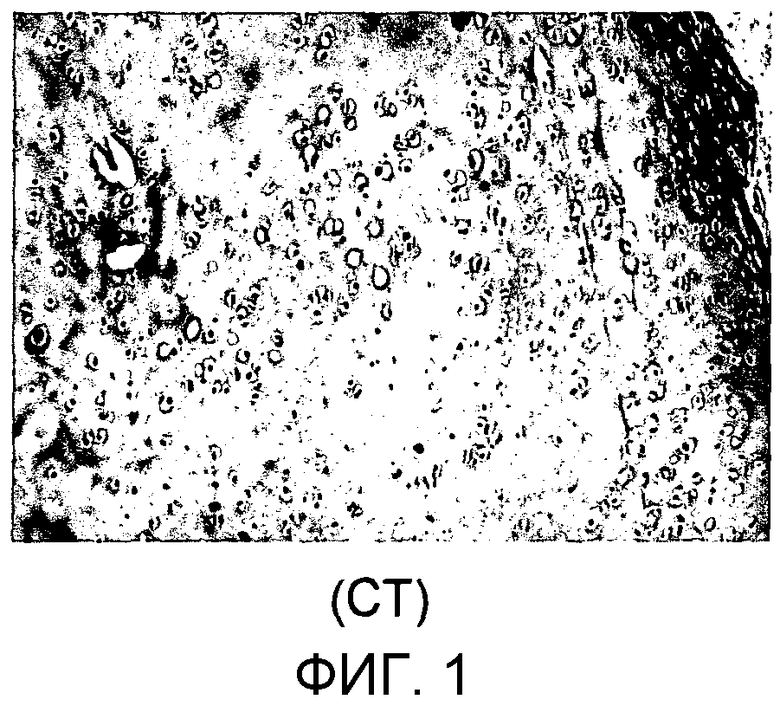
Результаты гистологического анализа биопсий приведены в Фиг.1-3, которые относятся к гематоксилин-эозиновым сечениям, полученным из хрящевых биопсий, фиксированных в формалине и пропитанных парафином, где:
Фиг.1: биопсия для контрольной группы (CT): можно видеть декальцинированный фрагмент суставного хряща, нормальный немного эозинофильный хрящевой матрикс и группу клеток, погруженную в хрящевой матрикс,
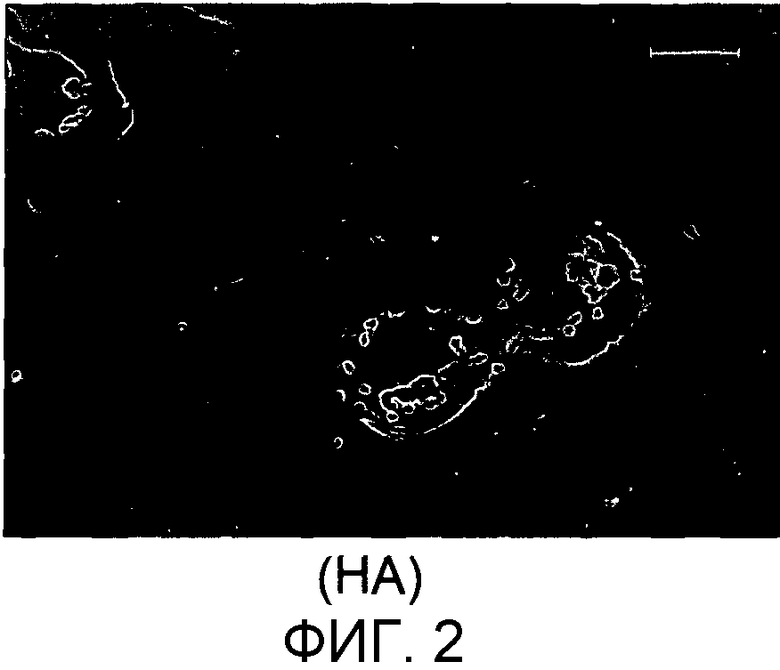
Фиг.2: биопсия для группы НА: можно видеть декальцинированный фрагмент хряща, присутствие ткани, подобной костной и отсутствие нормального хрящевого матрикса,
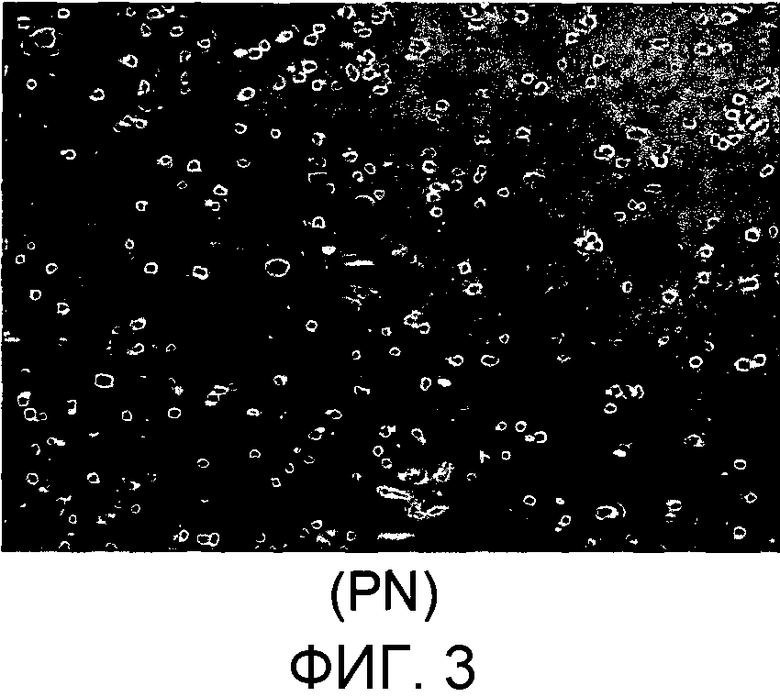
Фиг.3: биопсии после трех недель для группы PN: можно видеть декальцинированный фрагмент хряща, немного эозинофильный хрящевой матрикс и нормальный хрящевой матрикс, окружающий хондроциты.
Гистологический анализ для группы PN также указывает на положение, которое почти идентично таковому для положительного контроля CT, то есть поддерживаются фенотипические особенности, характерные для гиалинового суставного хряща. Наоборот группа, подвергавшаяся лечению НА, обнаруживала аномальные особенности, такие как формирование незрелых элементов кости и отсутствие нормального внеклеточного матрикса.
Эксперимент 2: Выделенные хрящевые клетки (хондроциты)
Было выполнено исследование, чтобы оценить эффекты состава по изобретению (CONDROTIDE) и гиалуроновой кислоты на выделенных хондроцитных клетках (двухнедельная культура), сравнивая их с таковыми для стандартной среды, обычно используемой в лаборатории для культуры хондроцитов.
Образец: Выделенные хондроциты человека.
Экспериментальные группы:
4. PN: клетки, поддерживаемые в «хрящевой» среде + 0,01% CONDROTIDE,
5. НА: клетки, поддерживаемые в «хрящевой» среде + 1% гиалуроновой кислоты,
6. CT: клетки, поддерживаемые в «хрящевой» среде без добавок.
Конечная точка: Иммуногистохимия, анализ FACS, окрашивание Alcian Blue.
Результаты
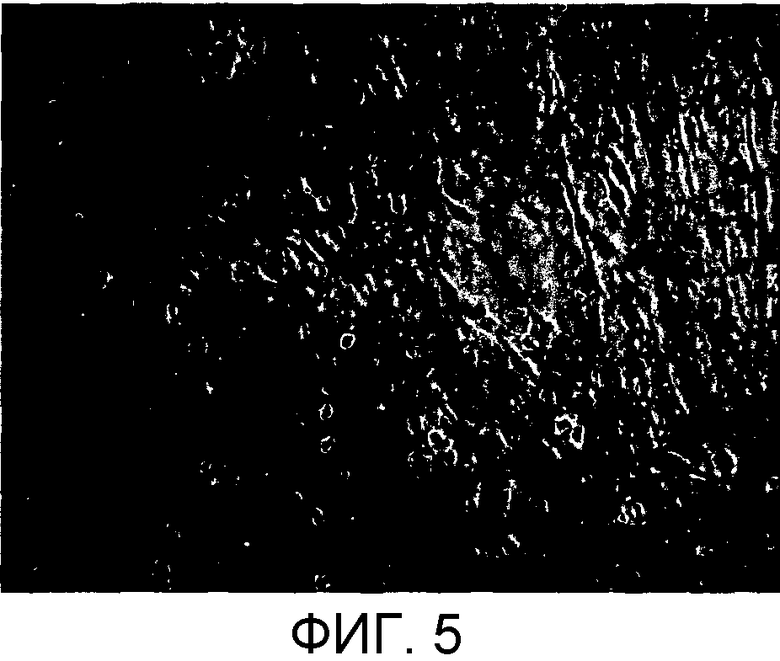
Иллюстрации 4 и 6 иллюстрируют результаты окрашивания Alcian Blue (что позволяет выявить присутствие внеклеточного матрикса):
Фиг.4: контрольная группа: высокоэкспрессируемый матрикс,
Фиг.5: группа НА: слабоэкспрессируемый матрикс,
Фиг.6: группа PN: высокоэкспрессируемый матрикс.
Сделано заключение, что 0,01% CONDROTIDE способен индуцировать образование внеклеточного матрикса в количествах, которые намного больше, чем для гиалуроновая кислота в выделенных культурах хондроцитов.
Эти данные были подтверждены анализом FACS и иммуногистохимическим анализом, который продемонстрировал, что профиль экспрессии и продуцирования аггрекана и коллагена II типа является значительно меньшим группе НА по сравнению с группами PN и CT.
Результаты предварительного исследования in vitro подтверждают наблюдение, что гиалуроновая кислота полезна только для улучшения симптомов в течение короткого периода времени, тогда как состав по изобретению (CONDROTIDE), как оказалось, являлся намного более активным при лечении заболеваний суставов, с устойчивыми результатами.
В подтверждение тестов in vitro, упомянутых выше, был выполнен эксперимент по проверке эффектов состава по изобретению, введенного внутрисуставно пациентам, страдающим от остеоартрита колена, с конкретной целью оценить эффективность, безопасность и переносимость этого состава (CONDROTIDE, медицинское устройство класса III).
Исследование было выполнено в соответствии с руководящими принципами Хельсинской Декларации 1974 и последующих обновлений и общих принципов «ICH согласованных трехсторонних руководящих принципов для качественной клинической практики (GCP)». Прежде чем начать исследования, было получено одобрение Комитета по этике биологических исследований Fondazione IRCCS поликлиники Сан Маттео университета Павии. Всем пациентам сообщили о клиническом испытании, и исследователи получили перед набором письменное согласие на основе полной информации от всех пациентов.
Структура исследования и контрольного клинического испытания в отношении гиалуроновой кислоты являлась «двойной-слепой» рандомизированной в параллельных группах.
Каждого пациента случайным образом определяли в одну из следующих групп лечения:
- группа A: ПДРН (вышеупомянутый состав CONDROTIDE),
- группа B: гиалуроновая кислота (SINOVIAL).
За каждый пациентом наблюдали в течение периода времени шестнадцать недель. Поскольку два различных лекарственных средства могли быть идентифицированы оператором в процессе инстилляции, применялась методика «слепой-наблюдатель» для поддержания «двойных-слепых» условий. Исследователь, вводящий продукт, отличался от исследователя, который исследовал пациента клинически и оценил эффективность и безопасность продукта. Таким образом, ни пациент, ни исследователь не знали о природе лечения.
Размер образца
Вычисление размера образца было основано на непарном t-тесте с уровнем вероятности 5%, стандартным отклонением 3 см и желательным порядком 80% детектирования различия в 1,6 см в уменьшении боли, измеренной путем VAS (Rheumatology 2002; 41:1240-1248). Полный размер образца 56 пациентов был вычислен, и вследствие этого было сделано условие для регистрирования, по крайней мере, 60 пациентов, 30 на группу.
Пациенты
Были набраны пациенты, страдающие от остеоартрита колена (в соответствии с классификации ACR - Arthritis Rheum. 1986; 29 (8): 1039-49). В частности, продукт, используемый в исследовании, обладал следующей композицией:
- полидезоксирибонуклеотиды: 20 мг
- хлорида натрия: 4 мг
- дигидро фосфат натрия дигидрат: 0,2 мг
- гидро фосфат натрия додекагидрат: 1 мг
- вода, подготовленная для инъекций: 1 мл q.s.
Раствор гиалуроновой кислоты под торговой маркой SINOVIAL, содержащий высокоочищенную натриевую соль гиалуроновой кислоты, имеющей молекулярную массу от 800 кДальтонов до 1200 кДальтонов, применялся в качестве контрольного продукта.
Композиция: Натриевая соль гиалуроновой кислоты: 0,8%, хлорид натрия, фосфат натрия и вода, подготовленная для USP (q.s).
Фармацевтическая форма: Шприцы, предварительно заполненные 16,0 мг гиалуроновой кислоты в 2 мл буферизованного соляного раствора хлорида натрия.
Дозировка и способ введения лекарства
Внутрисуставное лечение с гелем ПДРН включало пять инстилляций по 2 мл еженедельно.
Контрольную группу с гиалуроновой кислотой лечили внутрисуставными инстилляциями гиалуроната натрия (16,0 мг гиалуроновой кислоты в 2 мл). Этот раствор также применяли в качестве пяти инстилляций еженедельно.
Продукт (CONDROTIDE или SINOVIAL) вводили в суставную полость пораженного колена, используя стерильную иглу.
Продолжительность лечения
Лекарство вводили путем одной инстилляции в пораженное колено в неделю, в общей сложности пять инстилляций; время лечения поэтому составляло четыре недели, но каждый пациент наблюдался в течение в общей сложности шестнадцати недель.
Клинические оценки
Клинические оценки были сделаны для каждого пациента в начале исследования (Т0) и через одну (T1), две (T2), три (T3) и спустя четыре недели (T4) после начала исследования. T4 соответствует окончанию стадии лечения. Последующие клинические оценки были сделаны спустя один месяц после окончания лечения (T8) и спустя три месяца после окончания лечения (T16).
Главный параметр оценки (первичная конечная точка) представляет собой уровень боли, оцененный в покое, во время нагрузки и физической деятельности. Визуально-аналоговый масштаб (VAS в см от 0 до 10) применялся для оценки боли. Крепитацию при движении, ограничение суставной подвижности и суставного отека также оценивали, регистрировали со счетом от 0 до 3 (0 = отсутствие, 1 = слабая, 2 = умеренная, 3 = сильная) на каждой экспертизе.
Пациентами также была составлена анкета самооценок - результат оценок состояний коленей и остеоартрита - KOOS. KOOS представляет собой шкалу оценивания степени остеоартрита, разработанную как расширение индекса остеоартрита WOMAC (Западный университет Онтарио и Макмэстера) для создания полезного и принятого повсеместно инструмента для определения эффективности лечений при клинических испытаниях.
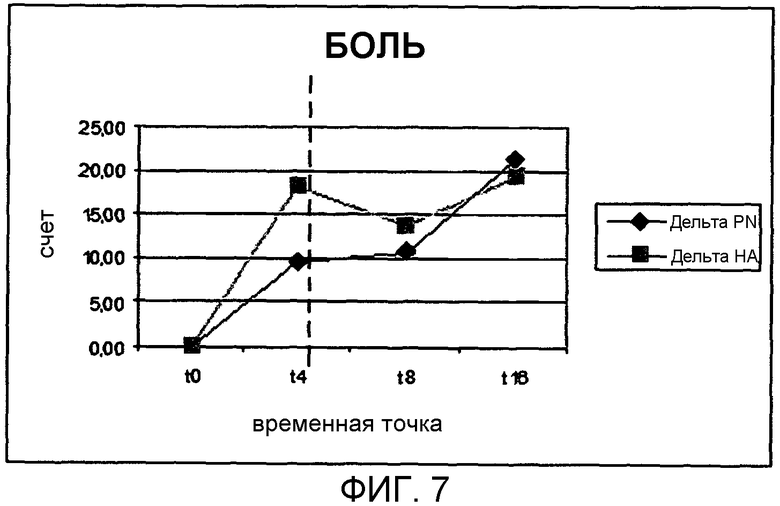
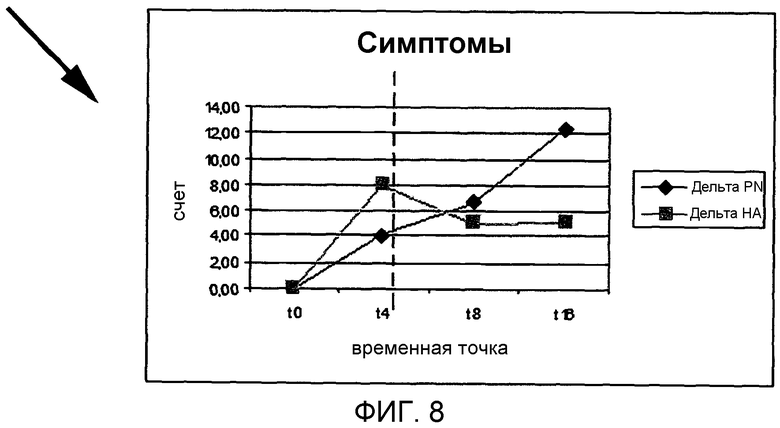
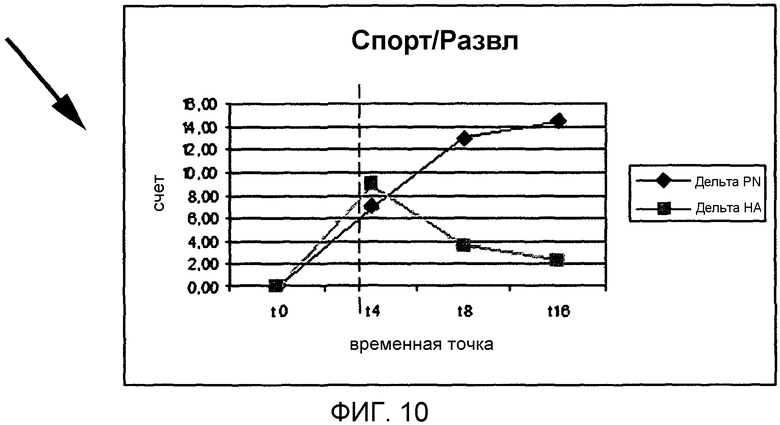
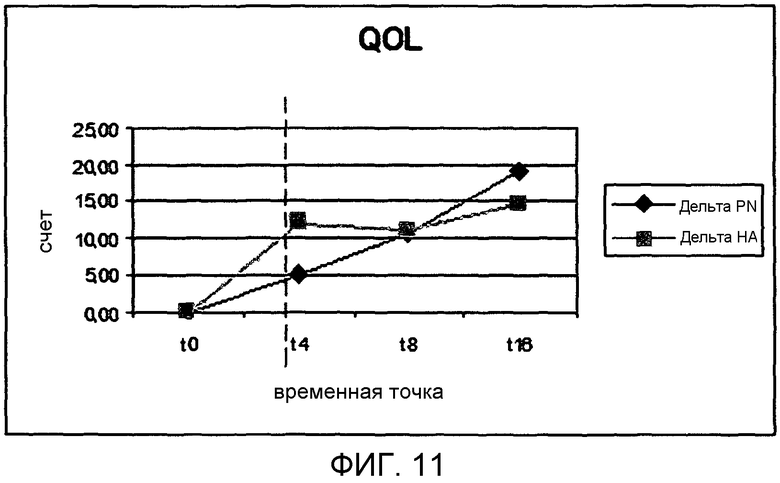
Этот анкетный опрос представляет собой определенный инструмент для оценки мнения пациентов относительно состояния их коленей. Анкетный опрос включает пять вспомогательных шкал (боль, Фиг.7), другие признаки (Фиг.8), функция суставов в повседневной жизни (ADL, Фиг.9), функция суставов при спортивных/развлекательный активностях (спорт/развл, Фиг.10) и качество жизни (КЖ, Фиг.11).
KOOS были составлены пациентами во время следующих экспертиз, Т0, T4, T8 и T 16, рассматривая неделю, предшествующую экспертизе, в своих ответах на вопросы. Пять вариантов ответа были предоставлены в анкете KOOS, каждый ответ получал счет от 0 до 4.
На основе статистического анализа данных полинуклеотиды, которые, как было подтверждено, имели статистически значимо больший эффект на боль в состоянии покоя, боль при нагрузке, крепитацию и уменьшение отека и ограничение подвижности сустава, чем контроль с гиалуроновой кислотой.
Эти данные показывают статистически существенно лучший эффект ПДРН по сравнению с гиалуроновой кислотой.
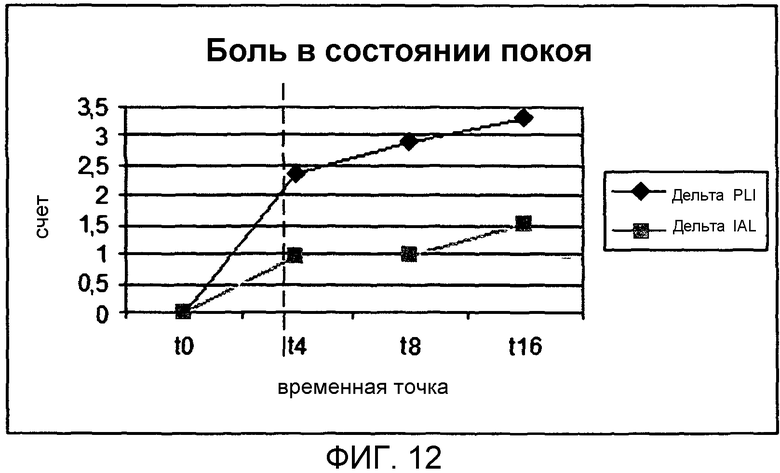
По мере рассмотрения данных, касающихся боли в состоянии покоя, путем анализа различия между базовыми значениями и их изменениями в ходе лечения (Дельта) были получены данные, иллюстрированные ниже, которые указывают на очевидную общую тенденцию со стороны ПДРН в достижении конечных значений, которые лучше значений, полученных для пациентов, подвергавшихся лечению гиалуроновой кислотой.
Результаты продемонстрированы в Фиг.12, где пунктирная вертикальная линия на графике делит каждую диаграмму на две части, соответствующих периоду лечения (левая половина) и последующему периоду наблюдения (правая половина).
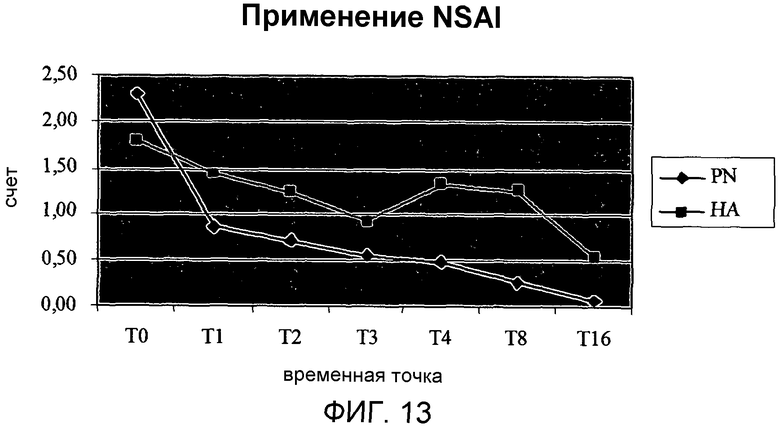
В ходе исследования пациентам разрешили в случае необходимости применять нестероидные противовоспалительные средства (NSAI), чтобы уменьшить болевые симптомы. Зарегистрированные данные, касающиеся применения NSAI (см. диаграмму в Фигуре 13), показывают очевидное большее потребление в начале испытания (TO) в группе подвергаемых лечению пациентов по сравнению с контролями, приводя к статистически достоверному различию в том, что в рассматриваемой группе наблюдалось уменьшение применения этих лекарственных средств, которые не были замечены в контрольной группе.
В дополнение к этому, поскольку лечение продолжалось, было отмечено и быстрое сокращение потребления NSAI в группе, подвергаемой лечению ПДРН, только после одной внутрисуставной инстилляции (Tl). В дополнение к этому было сохраняющееся меньшее применение NSAI в группе ПДРН во все последующее время, со специфическим различием между этими двумя лечениями в T4 и T8.
Как можно видеть из данных на Фиг.7-11, во время периода лечения проверенные продукты вызвали улучшение всех показателей KOOS; это улучшение было немного быстрее в контрольной группе. Однако, если изучить форму графиков в последующий период наблюдения, то можно заметить, что счет для группы гиалуроновой кислоты уменьшается или остается постоянным, в то время как счет для группы ПДРН продолжает увеличиваться.
Спустя три месяца после окончания лечения (T 16) счеты для группы ПДРН были во всех случаях выше, чем счеты для группы гиалуроновой кислоты; различие особенно очевидно для симптомов и вспомогательных признаков спорт/развл.
В последней шкале, которая представляет функционирование сустава в течение и после двигательной активности, контрольная группа (гиалуроновая кислота) вернулась к почти начальным значениям, в то время как группа, подвергаемая лечению ПДРН, показала наибольшее улучшение на 14,55 пунктов (не следует забывать, что улучшение по шкале KOOS является клинически значимым, если счет увеличивается на 8-10 пунктов в ходе лечении).
Полученные данные подтверждают применение состава по изобретению при терапевтическом лечении и в качестве терапевтического вспомогательного средства при лечении дегенеративных заболеваний суставов, таких как, в частности, при остеоартрите.
В настоящее время не существует никакого достаточно эффективного лечения этих заболеваний; предлагаемые лечения включают противовоспалительные средства, анальгезирующие средства, стероиды, физиотерапию и хирургическое вмешательство, а также добавление вязкости синовиальной жидкости путем внутрисуставной инстилляции гиалуроновой кислоты, используемой в контрольных тестах, описанных выше.
Следует принять во внимание, что лучший эффект, показанный составом ПДРН, включенным в состав по изобретению, происходит вследствие того, что ПДРН способны к связыванию заметного количества воды и реорганизации своей собственной структуры, ориентации и координирования водных модулей, с тем, чтобы сформировать подходящий гель.
Устройство в соответствии с изобретением, введенное внутрисуставно, обеспечивает вязкоупругое дополнение для синовиальной жидкости и может полностью смазывать суставные поверхности. В дополнение к этому можно предположить, что микромолекулы полидезоксирибонуклеотида в то же самое время подвергаются действию литических ферментов, которые постепенно высвобождают ПДРН все более меньшего размера в суставную полость.
Внутрисуставная инстилляция с использованием состава в соответствии с изобретением постепенно обогащает синовиальную жидкость, первоначально макромолекулами полинуклеотида, имеющими вязкоупругое действие, и со временем полинуклеотидами и нуклеотидами, которые используются тканями для улучшения клеточной активности и защиты и активизации физиологических механизмов регенерации суставного хряща.
Таким образом, вязкоупругое и смазочное действие продукта комбинируется с биостимулирующим и трофическим воздействием на суставный хрящ.
В результате делается заключение, что состав в соответствии с изобретением имеет общее применение для лечения причиняющих боль суставных заболеваний, которые могут быть приписаны к дегенеративным или посттравматическим состояниям или изменениям в суставах.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМБИНИРОВАННОЕ СРЕДСТВО ДЛЯ ВНУТРИСУСТАВНОГО ВВЕДЕНИЯ | 2017 |
|
RU2737380C2 |
| СХЕМА ПРИМЕНЕНИЯ СОЕДИНЕНИЯ FGF-18 | 2015 |
|
RU2700582C2 |
| КОМПОЗИЦИЯ ДЛЯ ПРОФИЛАКТИКИ, ОБЛЕГЧЕНИЯ ИЛИ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ ИЛИ СИМПТОМОВ, СВЯЗАННЫХ С ХРЯЩАМИ, ВКЛЮЧАЮЩАЯ HAPLN1 | 2019 |
|
RU2788162C2 |
| СХЕМА ПРИМЕНЕНИЯ СОЕДИНЕНИЯ FGF-18 | 2015 |
|
RU2691946C2 |
| КОМБИНАЦИЯ ДЛЯ ЛЕЧЕНИЯ ОСТЕОАРТРИТА | 2010 |
|
RU2560844C2 |
| КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ И ПРЕДУПРЕЖДЕНИЯ ОСТЕОАРТРИТА И ОСТЕОАРТРОЗА СУСТАВОВ | 2011 |
|
RU2509569C2 |
| КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ И ПРЕДУПРЕЖДЕНИЯ ОСТЕОАРТРИТА, ОСТЕОПОРОЗА И&NBSP;ОСТЕОАРТРОЗА СУСТАВОВ | 2013 |
|
RU2521227C1 |
| ХОНДРОИТИН ДЛЯ ПРИМЕНЕНИЯ В МЕДИЦИНЕ | 2013 |
|
RU2642964C2 |
| КОМБИНИРОВАННОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ АРТРОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2024 |
|
RU2827069C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ БЕСКЛЕТОЧНОГО ГИДРОГЕЛЯ ИЗ ВАРТОНОВА СТУДНЯ ПУПОВИНЫ ЧЕЛОВЕКА ДЛЯ ВНУТРИСУСТАВНОГО ПРИМЕНЕНИЯ | 2020 |
|
RU2745995C1 |



Описана фармацевтическая композиция на основе полидезоксирибонуклеотидов, экстрагированных из естественных источников. Композиция содержит фракцию полидезоксирибонуклеотидов, экстрагированных из спермы рыб, где указанные полидезоксирибонуклеотиды обладают полимерными цепями с различными молекулярными массами от 70 килодальтонов до 240 килодальтонов. Композиция пригодна для применения в качестве терапевтического средства при лечении костно-суставных патологий, особенно остеоартрита, путем внутрисуставной инъекции, обеспечивая необходимую вязкость синовиальной жидкости. 2 н. и 6 з.п. ф-лы, 13 ил.
1. Фармацевтическая композиция на основе полидезоксирибонуклеотидов, экстрагированных из естественных источников, для применения путем внутрисуставного введения при терапевтическом лечении дегенеративных или посттравматических состояний суставов, при этом композиция содержит фракцию полидезоксирибонуклеотидов, экстрагированных из спермы рыб, где указанные полидезоксирибонуклеотиды обладают полимерными цепями с различными молекулярными массами от 70 кДа до 240 кДа.
2. Композиция по п.1 в форме инъецируемого водного раствора, содержащего от 1 до 100 мг/мл, предпочтительно от 5 до 30 мг/мл полидезоксирибонуклеотидов в солевом водном растворителе.
3. Композиция по п.1 или 2 для лечения остеоартрита.
4. Композиция по п.1 или 2, обладающая pH от 6,5 до 7,5.
5. Композиция по п.4, содержащая соли хлорида натрия и фосфата натрия.
6. Композиция по п.1 для применения при лечении боли у пациента, страдающего от дегенеративного или посттравматического состояния суставов, причиняющего боль.
7. Применение композиции по любому из пп.1-5 для изготовления фармацевтического продукта или медицинского устройства, пригодных в качестве терапевтического средства при лечении костно-суставных патологий, особенно остеоартрита, путем внутрисуставной инъекции указанной композиции.
8. Применение по п.7, где указанный фармацевтический продукт или медицинское устройство для введения путем инъекции представлены в форме флакона, аптечного стеклянного сосуда или ампулы, или в форме предварительно заполненного шприца.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| ФОСФАТМОБИЛИЗУЮЩИЙ ШТАММ ПОЧВЕННЫХ БАКТЕРИЙ LELLIOTTIA NIMIPRESSURALIS CCM 32-3 И БИОПРЕПАРАТ НА ЕГО ОСНОВЕ ДЛЯ ОПТИМИЗАЦИИ МИНЕРАЛЬНОГО ПИТАНИЯ РАСТЕНИЙ, СТИМУЛЯЦИИ ИХ РОСТА И ПОВЫШЕНИЯ УРОЖАЙНОСТИ | 2018 |
|
RU2676926C1 |
| EP 0226254 A2, 24.06.1987 | |||
| Экономайзер | 0 |
|
SU94A1 |
| US 5712256 A, 27.01.1998. | |||
Авторы
Даты
2014-02-27—Публикация
2009-10-28—Подача