Область техники, к которой относится изобретение
Настоящее изобретение относится к области медицины, в частности к онкологии и молекулярной биологии, и может быть использовано для дифференциальной диагностики рака предстательной железы (РПЖ) и доброкачественной гиперплазии предстательной железы (ДГПЖ).
Уровень техники
Рак предстательной железы (РПЖ) является вторым по частоте и пятым по смертности среди злокачественных новообразований у мужчин в мире [Siegel R.L., Miller K.D., Jemal A. Cancer statistics, 2015. // CA. Cancer J. Clin. 2015. T. 65. №1. C. 5-29]. В Российской Федерации РПЖ также находится на втором месте по заболеваемости, а смертность от РПЖ стоит на третьем месте среди всех злокачественных опухолей мужчин [Алексеев Б.Я. Проблемы диагностики в онкоурологии. Взгляд хирурга // Российский электронный журнал лучевой диагностики. 2015. Т. 5. №3. С. 102-103; Каприн А.Д., Старинский В.В., Петрова Г.В. Состояние онкологической помощи населению России в 2014 году. - М.: МНИОИ им. П.А. Герцена - филиал ФГБУ «НМИРЦ» Минздрава России, 2015а. 236 с; Каприн А.Д., Старинский В.В., Петрова Г.В. Злокачественные новообразования в России в 2014 году (заболеваемость и смертность). - М.: МНИОИ им. П.А. Герцена - филиал ФГБУ «ФМИЦ им. П.А. Герцена» Минздрава России, 2016. 250 с.]. Одной из важных клинических проблем является вопрос дифференциальной диагностики доброкачественной гиперплазии предстательной железы (ДГПЖ) и РПЖ. ДГПЖ является распространенным заболеванием, проявляющимся в увеличении размера предстательной железы, что может оказывать значительное влияние на здоровье больного и требовать хирургического лечения при невосприимчивости к лекарственной терапии. ДГПЖ может развиваться и в 25 лет, однако гистологическое подтверждение чаще всего обнаруживается в возрасте примерно 50 лет, когда частота развития заболевания достигает 50% [Lokant М.Т., Naz R.K. Presence of PSA auto-antibodies in men with prostate abnormalities (prostate cancer/benign prostatic hyperplasia/prostatitis). // Andrologia. 2015. T. 47. №3. C. 328-32]. Ранняя дифференциальная диагностика ДГПЖ и РПЖ является очень важным моментом в плане улучшения исходов и выживаемости при РПЖ. Текущая скрининговая диагностика РПЖ включает метод ректального пальцевого исследования с чувствительностью около 37% [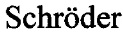 F.H. и др. Evaluation of the digital rectal examination as a screening test for prostate cancer. Rotterdam section of the European Randomized Study of Screening for Prostate Cancer. // J. Natl. Cancer Inst. 1998. T. 90. №23. C. 1817-23] и определение ПСА, уровень которого повышен как при РПЖ, так и при ДГПЖ, что делает дифференциальную диагностику относительно сложным процессом, особенно при значениях ПСА из «серой зоны» 4-10 нг/мл [Woolf S.H. The accuracy and effectiveness of routine population screening with mammography, prostate-specific antigen, and prenatal ultrasound: a review of published scientific evidence. // Int. J. Technol. Assess. Health Care. 2001. T. 17. №3. C. 275-304]. Еще одним способом диагностики РПЖ является трансректальная биопсия под контролем ультразвука [Каприн А.Д. и др. Современные методики биопсии предстательной железы в выявлении рака // Онкология. Журнал им. П.А. Герцена. 2014. Т. 2. №6. С. 59-62], однако данная методика имеет ограничения, связанные с техникой получения образцов, что в результате не позволяет обнаружить около 20% случаев РПЖ при первой процедуре [Djavan В. и др. Prospective evaluation of prostate cancer detected on biopsies 1, 2, 3 and 4: when should we stop? // J. Urol. 2001. T. 166. №5. C. 1679-83].
F.H. и др. Evaluation of the digital rectal examination as a screening test for prostate cancer. Rotterdam section of the European Randomized Study of Screening for Prostate Cancer. // J. Natl. Cancer Inst. 1998. T. 90. №23. C. 1817-23] и определение ПСА, уровень которого повышен как при РПЖ, так и при ДГПЖ, что делает дифференциальную диагностику относительно сложным процессом, особенно при значениях ПСА из «серой зоны» 4-10 нг/мл [Woolf S.H. The accuracy and effectiveness of routine population screening with mammography, prostate-specific antigen, and prenatal ultrasound: a review of published scientific evidence. // Int. J. Technol. Assess. Health Care. 2001. T. 17. №3. C. 275-304]. Еще одним способом диагностики РПЖ является трансректальная биопсия под контролем ультразвука [Каприн А.Д. и др. Современные методики биопсии предстательной железы в выявлении рака // Онкология. Журнал им. П.А. Герцена. 2014. Т. 2. №6. С. 59-62], однако данная методика имеет ограничения, связанные с техникой получения образцов, что в результате не позволяет обнаружить около 20% случаев РПЖ при первой процедуре [Djavan В. и др. Prospective evaluation of prostate cancer detected on biopsies 1, 2, 3 and 4: when should we stop? // J. Urol. 2001. T. 166. №5. C. 1679-83].
В течение многих лет было изучено множество возможных маркеров для диагностики и прогнозирования РПЖ. S. Sharma сформулировал основные требования к идеальному опухолевому маркеру: он должен быть высоко специфичен для конкретного типа опухоли и высоко чувствителен во избежание ложноположительных результатов, а также должен позволять проводить диагностику до клинических проявлений. Кроме того, желательно наличие корреляции с прогрессией и регрессией опухоли, короткого периода полураспада маркера для возможности повторных динамических измерений. Не последнюю роль играют стоимость и способ определения маркера и возможность предсказания метастазирования и его степени. Обнаружение идеального маркера представляется практически невозможным [Sharma S. Tumor markers in clinical practice: General principles and guidelines. // Indian J. Med. Paediatr. Oncol. 2009. T. 30. №1. C. 1-8]. Однако поиск маркеров РПЖ, максимально приближающихся к предъявленным требованиям, постоянно продолжается [Князев Е.Н. и др. Актуальные вопросы молекулярной диагностики рака предстательной железы // Онкоурология. 2014. №4. С. 14-22].
Простатический специфический антиген (ПСА) является одним из наиболее часто используемых маркеров РПЖ и до недавнего времени считался одним из самых надежных среди таковых [Алексеев Б.Я., Волкова М.И., Воробьев Н.В. Клиническая онкоурология. Монография. - М.: АБВ-пресс, 2011. 934 с.; Thompson I.M. PSA: a biomarker for disease. A biomarker for clinical trials. How useful is it? // J. Nutr. 2006. T. 136. №10. C. 2704S]. ПСА является сериновой протеазой из семейства калликреинов и был обнаружен в сыворотке крови в 1980 г. [Papsidero L.D. и др. A prostate antigen in sera of prostatic cancer patients. // Cancer Res. 1980. T. 40. №7. C. 2428-32].
Биологическая роль ПСА заключается в разжижении семенной жидкости [Lilja Н. и др. Seminal vesicle-secreted proteins and their reactions during gelation and liquefaction of human semen. // J. Clin. Invest. 1987. T. 80. №2. C. 281-5]. Ретроградное попадание ПСА в кровь ограничено примерно одной молекулой на миллион секретируемых в семенную жидкость молекул, что создает концентрацию ПСА в крови <4 нг/мл при концентрации в семенной жидкости на уровне 0,5-5 мг/мл, однако нарушение базальной мембраны эпителия предстательной железы может увеличивать концентрацию ПСА в кровотоке [Stenman U.H. Prostate-specific antigen, clinical use and staging: an overview. // Br. J. Urol. 1997. T. 79 Suppl 1. C. 53-60].
Изначальные исследования показали, что уровень свободного ПСА в сыворотке крови лучше предсказывает ДГПЖ, а более подходящим маркером РПЖ служит комплекс α1-антихимотрипсин-ПСА [Stenman U.H. и др. A complex between prostate-specific antigen and alpha 1-antichymotrypsin is the major form of prostate-specific antigen in serum of patients with prostatic cancer: assay of the complex improves clinical sensitivity for cancer. // Cancer Res. 1991. T. 51. №1. C. 222-6].
Однако повышенный ПСА обнаруживался только у 30-50% больных с ДГПЖ и только у 20% мужчин с РПЖ, в некоторых случаях РПЖ уровень ПСА оставался ниже 4,0 нг/мл, а также подвергался влиянию других факторов, таких как инфекция мочевыводящих путей, простатит, физическая травма, езда на велосипеде, пальцевое ректальное исследование и катетеризация [Andriole G.L. PSA screening and prostate cancer risk reduction. // Urol. Oncol. 2012. T. 30. №6. C. 936-7; Stamey T.A. и др. The prostate specific antigen era in the United States is over for prostate cancer: what happened in the last 20 years? // J. Urol. 2004. T. 172. №4 Pt 1. C. 1297-301]. Все это ведет к низкой специфичности и низкой положительной прогностической ценности уровня ПСА в предсказании РПЖ, особенно в «серой зоне» 2-10 нг/мл [Mistry K., Cable G. Meta-analysis of prostate-specific antigen and digital rectal examination as screening tests for prostate carcinoma. // J. Am. Board Fam. Pract. 2003. T. 16. №2. C. 95-101]. Среди случаев повышенного ПСА только четверть была связана с РПЖ, что натолкнуло ученых и практикующих врачей на мысль о необходимости учитывать помимо уровня ПСА дополнительные факторы, такие как соотношение свободного и связанного ПСА, возрастные изменения уровня ПСА, скорость прироста и время удвоения уровня ПСА, плотность ПСА переходной зоны, уровень предшественника ПСА [Schroder F.H. PSA screening-a review of recent studies. // Eur. J. Cancer. 2009. T. 45 Suppl 1. C. 402-4].
Еще одним маркером прогноза РПЖ может являться рецептор эпидермального фактора роста HER-2, или ErbB-2. HER-2 может активировать сигнальный путь андрогенового рецептора даже в отсутствие андрогенов [Craft N. и др. A mechanism for hormone-independent prostate cancer through modulation of androgen receptor signaling by the HER -2/neu tyrosine kinase. // Nat. Med. 1999. T. 5. №3. C. 280-5]. Это может обеспечивать возможность повышения жизнеспособности клеток РПЖ. Было обнаружено, что 25% не леченных первичных опухолей РПЖ, 59% локализованных и 78% метастатических опухолей после гормонального лечения гиперэкспрессируют HER-2 без амплификации гена, кроме того, HER-2 является перспективным предиктором развития резистентность к андроген-депривационной терапии [Signoretti S. и др. Her-2-neu expression and progression toward androgen independence in human prostate cancer. // J. Natl. Cancer Inst. 2000. T. 92. №23. C. 1918-25]. Уровень внеклеточного домена HER-2 в крови коррелирует с степенью прогрессии, рецидивами и метастазированием РПЖ [Siampanopoulou М. и др. Profiling serum HER-2/NEU in prostate cancer. // Hippokratia. 2013. T. 17. №2. C. 108-112].
В решении, представленном в международной заявке WO 2016145308, раскрыт способ обнаружения рака простаты в образце цельной крови пациента, включающий выделение РНК из образца, синтез кДНК и измерение уровня экспрессии по меньшей мере одной мРНК, выбранной из группы: KLK3, ACADL, GRHL2, НОХВ 13, HSD3B1, TMP.ERG, ARV3.7, ARV567, FOLH1, KLK2, HSD3B2, AGR2, AZGP1, STEAP2, KCNN2, GPX8, SLC01B3, TMEFF2, SPINK 1, SFRP4, NROB 1, FAM13C, HNFIA, CDH12, PGR, PITX2, MYBPC1, FOXA1, SRD5A2, COL1A1, NPY, UGT2B17, CLUL1, C9orfl52, FLNC, GPR39, RELN, THBS2, CYP17A1, CYP3A5, BRS3. SNAI2, CDH12, NKX3.1, LGR5, TRPM8, SLC01B3.
Несмотря на значительное количество исследований различных молекулярных биомаркеров, их практическая значимость зачастую остается противоречивой или имеет недостаточную доказательную базу для широкого применения в диагностике и прогнозировании РПЖ. Активное изучение наследственных и генетических факторов в развитии РПЖ натолкнуло исследователей на необходимость поиска молекулярно-генетических маркеров на уровне ДНК и РНК.
Одними из перспективных опухолевых маркеров являются молекулы микроРНК, которые представляют собой короткие некодирующие РНК со средней длиной 22 нуклеотида, способные осуществлять посттранскрипционную регуляцию экспрессии различных генов и проявлять как онкогенные, так и противоопухолевые свойства [Hamilton М.Р. и др. The Landscape of microRNA Targeting in Prostate Cancer Defined by AGO-PAR-CLIP. // Neoplasia. 2016. T. 18. №6. C. 356-70]. Появляется все больше информации о роли микроРНК при различных физиологических и патологических состояниях, поэтому исследование микроРНК при РПЖ является перспективным направлением развития науки и практической медицины.
Было обнаружено, что в качестве биомаркеров РПЖ могут выступать циркулирующие молекулы микроРНК [Гилязова И.Р. и др. Исследование роли генов биогенеза микроРНК в развитии рака почки и предстательной железы // Сборник трудов 3-й Всероссийской научно-практической конференции с международным участием «Медико-биологические аспекты мультифакториальной патологии». - Курск: 17-19 мая, 2016. С. 42; Кунсбаева Г.Б. и др. Роль микроРНК в развитии рака предстательной железы // Генетика. 2015. Т. 51. №7. С.737]. Данные молекулы выступают в роли посттрансляционных регуляторов, изменяя в конечном итоге экспрессию определенных генов [Ширшова А.Н. и др. МикроРНК при онкологических заболеваниях // Молекулярная медицина. 2015 с. №2. С. 4-12]. Существует множество подтверждений, что микроРНК могут быть гипер - или гипоэкспрессированы в различных злокачественных опухолях [Ширшова А.Н. и др. МикроРНК - новые перспективные биомаркеры опухолей и мишени химиотерапии. Часть 2. Исследование микроРНК в клинике онкологических заболеваний // Вопросы биологической, медицинской и фармацевтической химии. 2015d. №3. С. 35-47; Heneghan Н.М., Miller N., Kerin M.J. MiRNAs as biomarkers and therapeutic targets in cancer. // Curr. Opin. Pharmacol. 2010. T. 10. №5. C. 543-50]. Данные молекулы могут быть выделены из любых биологических жидкостей и определены даже при наличии в очень малых количествах, что делает их перспективными биомаркерами [Cortez М. А. и др. MicroRNAs in body fluids-the mix of hormones and biomarkers. // Nat. Rev. Clin. Oncol. 2011. T. 8. №8. C. 467-77]. Это делает актуальным изучение и разработку тест-систем на основе микроРНК для ранней малоинвазивной дифференциальной диагностики ДГПЖ и РПЖ.
Было обнаружено, что различные микроРНК и их сочетания коррелируют с наличием доброкачественных и злокачественных опухолей предстательной железы и их гистологическими характеристиками, прогнозом течения и чувствительностью к различным типам лечения. Однако на профили обнаруживаемых микроРНК может значительно влиять методика получения биологических образцов для анализа, например, способ получения сыворотки или плазмы крови для исследования циркулирующих микроРНК. Для получения маркеров с максимальной значимостью необходимо проведение анализа максимально широкого спектра известных микроРНК. Кроме того, профили микроРНК могут различаться в различных популяциях, что делает актуальными продолжающиеся исследования профиля микроРНК при патологиях предстательной железы и выработку новых диагностических панелей.
В заявке США №2015211077 раскрыт способ определения вероятности присутствия РПЖ, заключающийся в определении количества, по меньшей мере, одной диагностической микроРНК, из списка MIR-19a, MIR-19b, MIR-519c-5p и/или MIR-345 в биологическом образце пациента (крови или продукте крови), сравнение полученного результата с эталонным и расчет вероятности наличия патологии. Для оценки вероятности присутствия патологии принимаются во внимание возраст пациента, содержание ПСА и другие клинические показатели.
В патентном документе СА 2834187 раскрыт способ скрининга РПЖ, включающий измерение экспрессии микроРНК в исследуемом образце - моче пациента, сравнение уровня экспрессии с уровнем экспрессии микроРНК в нормальном образце, при избыточной экспрессии miR-1825 и пониженной экспрессии miR-484 делают вывод о раке простаты.
Наиболее близким к заявляемому является способ дифференциальной диагностики рака предстательной железы по измерению уровня экспрессии микроРНК hsa-miR-619-5p и hsa-miR-1184 с помощью микрочипов (Е.Н. Князев, К.А. Фомичева, Д.С. Михайленко, К.М. Нюшко, Т.Р. Саматов, Б.Я. Алексеев, М.Ю. Шкурников «Уровень hsa-miR-619-5p и hsa-miR-1184 в плазме крови различается при доброкачественной гиперплазии и раке предстательной железы», Бюллетень экспериментальной биологии и медицины, 2016, т. 161, №1, с. 124). Каждая из микроРНК hsa-miR-619-5p и hsa-miR-1184 является независимым клинико-лабораторным показателем для дифференциальной диагностики РПЖ и ДГПЖ. Однако чувствительность и специфичность одиночных микроРНК оказалась менее 70%, что требует поиска более чувствительного сочетания микроРНК.
Раскрытие изобретения
Задачей предлагаемого технического решения является разработка новых диагностических маркеров РПЖ, позволяющих с высокой степенью достоверности диагностировать РПЖ, а также разработка на их основе простого, чувствительного, надежного, применимого в условиях клинических или поликлинических медицинских учреждений способа диагностики РПЖ.
Техническим результатом является неинвазивная дифференциальная диагностика РПЖ и ДГПЖ, позволяющая с достоверностью и специфичностью более 80% установить диагноз, в том числе на ранних стадиях развития данных заболеваний
Поставленная задача решается способом диагностики РПЖ и дифференциальной диагностики РПЖ и ДГПЖ у человека определением уровня микроРНК в плазме крови пациента, включающим отделение плазмы крови, выделение тотальной РНК и количественную оценку представленности микроРНК в плазме крови пациента.
Настоящее изобретение относится к способу дифференциальной диагностики рака предстательной железы (РПЖ), включающему:
- получение образца периферической крови пациента;
- выделение плазмы крови из образца;
- выделение РНК из плазмы крови;
- измерение уровня экспрессии микроРНК hsa-miR-155-5p, hsa-miR-619-5p, hsa-miR-6777-5p с получением для каждого из перечисленных маркеров их количественных оценок представленности L1, L2 и L3, соответственно, с последующим определением вероятностного значения (F), характеризующего наличие риска РПЖ, по следующей формуле:
F=0,931×(L1-2,878)/2,064+0,960×(L2-3,059)/2,160+0,587×(L3-2,523)/0,689-0,515,
при этом пациента относят к группе высокого риска при получении значения F>0, при получении F≤0 - к группе низкого риска.
Предпочтительно выделение плазмы крови из образца проводить центрифугированием при режимах, обеспечивающих максимальную сохранность клеточных элементов крови и минимальное содержание тромбоцитов и мелких мембранных везикул.
Предпочтительно процесс центрифугирования проводить в два этапа по 10±1 минут каждый при температуре 25±2°С: первый - при 2000±100 RCF, с последующим переносом верхней фазы в новую пробирку, второй - при 4000±200 RCF, после этого отбирают всю плазму кроме 10±5% объема, находящегося у дна пробирки.
Предпочтительно использовать центрифугу с возможностью регулировки скорости разгона и торможения ротора и выставлять значения разгона и торможения на среднее значение между максимально быстрым и максимально медленным.
Предпочтительно выделение РНК из плазмы крови осуществлять с помощью набора реагентов miRNeasy Serum/Plasma Kit (Qiagen, ФРГ).
Предпочтительно для проведения микрочипового анализа использовать чипы GeneChip miRNA 4.0 Array (Affymetrix, США).
Краткое описание чертежей
На фиг. 1 представлена ROC-кривая для тройки микроРНК hsa-miR-155-5p, hsa-miR-619-5p, hsa-miR-6777-5p при диагностике РПЖ с указанием площади под кривой (AUC) и наилучшего сочетания чувствительности и специфичности.
Осуществление изобретения
Для диагностического скрининга осуществляют ректальное пальцевое исследование и/или определение уровня ПСА в сыворотке крови. Однако ректальное пальцевое исследование у пациентов с уровнем ПСА менее 2 нг/мл имеет положительную прогностическую ценность на уровне 5-30%. Поэтому поиск новых диагностических маркеров для диффернциальной диагностики РПЖ и ДГПЖ остается актуальным.
Существует подход к диагностике рака на основе микроРНК: используются не отдельные микроРНК со значимым отличием между группами пациентов, а сочетания микроРНК, которые могут не иметь индивидуальной диагностической ценности, однако в совокупности позволяют достоверно различать два состояния.
В изобретении представлены новые молекулярно-генетические маркеры для диагностики рака предстательной железы и дифференциальной диагностики РПЖ, доброкачественной гиперплазии предстательной железы и других патологий мочевыводящей системы, не затрагивающих предстательную железу. Функционал уровня представленности 3 микроРНК в плазме крови позволяет с высокой степенью достоверности диагностировать РПЖ.
Ниже представлено более подробное описание этапов осуществления изобретения, которое не ограничивает заявленный объем притязаний.
1. Забор крови с последующим отделением плазмы.
Проводят венепункцию периферической вены с забором крови в пробирку, содержащую антикоагулянта. В качестве антикоагулянта могут быть использованы любые известные из уровня техники антикоагулянты, например, ЭДТА. В течение 20±5 минут необходимо начать выделение плазмы. Режимы центрифугирования, а именно скорость разгона и торможения ротора центрифуги подбирают таким образом, чтобы обеспечить максимальную сохранность клеточных элементов крови и при минимальном содержании тромбоцитов и мелких мембранных везикул. Для центрифугирования необходимо использовать центрифугу, позволяющую поддерживать постоянную температуру на уровне 25±2°С.
Центрифугирование проводят при 2000±100 RCF (relative centrifugal force) в течение 10±1 минут при температуре 25±2°С, затем верхнюю прозрачную фазу аккуратно, чтобы не задеть среднюю белую фазу с ядерными клетками, отбирают в новую пробирку. Новую пробирку центрифугируют при 4000±200 RCF в течение 10±1 минут при температуре 25±2°С, затем медленно отбирают весь объем кроме 10% у самого дна пробирки, чтобы не потревожить осадок с остаточными клетками и клеточным детритом. Отобранную плазму используют для дальнейшего анализа.
2. Выделение тотальной РНК (выделение присутствующих в плазме РНК) из плазмы крови человека.
Выделение тотальной РНК из плазмы крови человека производят с помощью метода гуанидин тиоцианат-фенол-хлороформной экстракции по модифицированному протоколу [Turchinovich А. и др. Circulating miRNAs: cell-cell communication function? // Front. Genet. 2013. T. 4. C. 119] с добавлением преципитирующего агента с последующей сорбцией на кремниевой мембране и элюированием водой, свободной от ДНКаз и РНКаз.
Для этого на первом этапе в пробирке смешивают очищенную плазму с фенол-содержащим реагентом в объемном соотношении от 1:2 до 1:4, производят тщательное перемешивание на вортексе, затем в качестве преципитирующего агента добавляют гликоген из расчета 15±5 мкг на 1 мл смеси. После этого полученную смесь смешивают с хлороформом в соотношении от 4,5:1 до 5,5:1, производят тщательное перемешивание на вортексе и центрифугирование при ускорении от 14000 до 16000 RCF при температуре 4±2°С в течение 20±2 минут. Верхнюю прозрачную фазу аккуратно, чтобы не задеть осадок, переносят в чистую пробирку. Добавляют полуторакратный объем 100% этанола двойной перегонки, смесь перемешивают пипетированием без центрифугирования. Далее проводят выделение РНК на колонках с кремниевой мембраной, входящих в состав специальных наборов.
В качестве фенол-содержащего реагента может быть использован QIAzol Lysis Reagent (Qiagen), или TRI Reagent LS (Sigma) или TRIzol LS Reagent (Thermo Fisher Scientific).
В качестве преципитирующего агента добавляют гликоген, такой как GlycoBlue Coprecipitant (Thermo Fisher Scientific) или Glycogen (Affymetrix).
Для выделения на колонках с кремниевой мембраной может быть использован коммерческий набор miRNeasy Serum/Plasma Kit (Qiagen) или аналог.
3. Анализ профиля представленности микроРНК hsa-miR-6085, hsa-miR-6511b-5p, hsa-mir-6886 с помощью микрочипов.
Для анализа выбирают чипы, позволяющие анализировать все известные микроРНК из базы данных miRBase версии 20 или более поздних. Микрочипы должны содержать олигонуклеотидные пробы на специальной подложке, комплементарные к определяемым последовательностям микроРНК. МикроРНК должны метиться путем биотинилирования.
Уровни экспрессии (представленности) микроРНК могут быть проанализированы с помощью любого подходящего способа, известного в данной области, и не ограничивается использованием микрочипов. Уровни экспрессии микроРНК могут быть также проанализированы с помощью полимеразной цепной реакции (ПЦР) или блоттинга.
Уровни представленности L1, L2, L3 микроРНК hsa-miR-155-5p, hsa-miR-619-5p, hsa-miR-6777-5p проводят по стандартному протоколу производителя, описанному для используемых микрочипов. Уровни представленности берут в логарифмической шкале по чипам Affymetrix GeneChip miRNA 4.0, для этого CEL-файл обрабатывают в Affymetrix Expression Console (режим RMA+DABG-NO-NORM-Human_Only) и за L1 принимают уровень Probe Set ID 20501083, за L2 - уровень Probe Set ID 20504364, за L3 - уровень Probe Set ID 20525515.
4. Вычисляют нормированные уровни представленности N1, N2, N3 микроРНК hsa-miR-155-5p, hsa-miR-619-5p, hsa-miR-6777-5p по формулам:
N1=(L1-E1)/V1; N2=(L2-E2)/V2; N3=(L3-E3)/V3.
Константы E1, E2, Е3 и V1, V2, V3 при определении уровней представленности микроРНК по чипам Affymetrix GeneChip miRNA принимают следующие значения:
Е1=2,878, V1=2,064;
E2=3,059, V2=2,160;
Е3=2,523, V3=0,689.
5. Вычисляют значение F:
F=c1×N1+c2×N2+с3×10-ρ.
Значения коэффициентов c1, с2, с3 и порога ρ уже не зависят от технологии, используемой для определения уровня представленности микроРНК, и составляют соответственно 0,931,0,960, 0,587 и 0,515.
6. РПЖ определяют, когда F>0, в противном случае - диагностируют ДГПЖ. Поскольку окончательное подтверждение диагноза РПЖ производят с помощью высокоинвазивной процедуры биопсии предстательной железы, которая травматична для пациента и связана с риском осложнений, то еще одним преимуществом диагностики с помощью микроРНК становится возможность избежать проведения биопсии при попадании пациента в группу с низким риском РПЖ. Если же пациента относят к группе высокого риска, то рекомендовано проведение визуализирующих исследований и/или диагностической биопсии для гистологического подтверждения или опровержения диагноза.
Следует отметить, что отбор транскриптов осуществляли на основе анализа собственных данных о профиле микроРНК плазмы крови 188 пациентов с РПЖ и 57 здоровых добровольцев и пациентов с ДГПЖ или другими заболеваниями мочевыводящей системы, не затрагивающими предстательную железу, полученных на базе ФГБУ «НМИРЦ» Минздрава России. В основе отбора лежало построение бинарного (двухклассового) классификатора, различающего пациентов, у которых был диагностирован рак предстательной железы, и пациентов, у которых было диагностировано его отсутствие.
При фиксированном наборе транскриптов для построения классификатора, использующего в точности этот набор транскриптов, применяли однофакторный непарный дисперсионный анализ с поправкой Бенджамини-Хохберга на множественность сравнений.
Валидацию итогового набора микроРНК-маркеров осуществляли на валидационной выборке, образцы которой не были использованы при отборе транскриптов.
Изобретение поясняется следующими примерами осуществления.
Пример 1. Получение плазмы крови.
На профиль микроРНК в плазме крови может влиять разрушение различных клеточных элементов и высокий уровень остаточных фрагментов клеток, тромбоцитов и мелких мембранных везикул. Данные факторы в свою очередь зависят от таких моментов, как ускорение при центрифугировании и количество последовательных этапов центрифугирования, скорость разгона и торможения центрифуги, температура, поддерживаемая при выделении плазмы крови.
Была проведена оптимизация протокола центрифугирования плазмы. Кровь для исследования была получена от 41 пациента ФГБУ «НМИРЦ» Минздрава России.
Забор крови производили с использованием системы взятия венозной крови S-Monovette EDTA-KE/2,6 мл. От каждого пациента было получено три пробирки крови. После взятия крови пробирки несколько раз переворачивались для смешивания с ЭДТА. Выделение плазмы начинали не более, чем через 20 минут, и производили с помощью центрифуги 5810 R (Eppendorf), позволяющей поддерживать температуру от -9 до +40°С.
В каждом образце плазмы определяли содержание гемоглобина, микрочастиц и ДНК. Определение гемоглобина производили цианметгемоглобиновым методом с использованием набора реактивов Диагем Т и Диагем К (НПО Ренам) и спектрофотометра NanoDrop 2000.
В образцах определяли фракцию микрочастиц, содержащих фосфатидилсерин во внешнем слое цитоплазматической мембраны, с использованием аннексина V из набора Alexa Fluor 488 Annexin V/Dead Cell Apoptosis Kit (Life Technologies) и проточного цитометра с акустической фокусировкой Attune (Applied Biosystems).
Определение концентрации двухцепочечной ДНК производили непосредственно в образце плазмы с помощью набора Qubit dsDNA HS Assay Kit (Life Technologies) согласно протоколу производителя на флуориметре Qubit 2.0 (Life Technologies).
Результаты оценки воспроизводимости результатов измерения количества микрочастиц, уровня гемоглобина и ДНК в плазме показали, что для всех измерений коэффициент вариации не превышал 8%.
На данные показатели было оценено влияние ускорения, развиваемого центрифугой на первом и втором шаге центрифугирования (1000, 2000 или 4000 RCF), влияние температуры центрифугирования (4°С или 25°С), влияние скорости разгона ротора центрифуги для развития нужного ускорения и скорости последующего торможения в конце протокола (быстрые, средние или медленные значения разгона и торможения).
В результате оптимизации был разработан оптимальный протокол для получения плазмы крови с целью исследования профиля циркулирующих микроРНК. Предлагается производить центрифугирование в два этапа по 10±1 минут каждый: первый при 2000±100 RCF, с последующим переносом верхней фазы в новую пробирку, второй этап проводить при 4000±200 RCF, после этого отбирать всю плазму кроме 10±5% объема у дна пробирки. Все этапы должны проходить при 25±2°С, скорость разгона и торможения центрифуги устанавливается на средние значения.
Пример 2. Выделение тотальной РНК из плазмы крови
Выделение тотальной РНК из плазмы крови человека, полученной по Примеру 1, производили с помощью набора реагентов miRNeasy Serum/Plasma Kit (Qiagen) по модифицированному протоколу [Turchinovich, Weiz, Burwinkel, 2013] с добавлением GlycoBlue Coprecipitant 15 мг/мл (Thermo Fisher Scientific) по следующей методике.
1. Смешивали в отдельной пробирке 1,2 мл TRIzol LS Reagent (Life Techologies, США) и 400 мкл образца плазмы крови.
2. Тщательно перемешивали на вортексе в течение 15 секунд.
3. Инкубироватли при 25±2°С в течение 10 минут для полной диссоциации нуклеопротеиновых комплексов.
4. Добавляли в пробирку 1,6 мкл GlycoBlue Coprecipitant (15 мг/мл) для повышения эффективности выделения РНК.
5. Тщательно перемешивали на вортексе.
6. Добавляли 320 мкл хлороформа и тщательно перемешивали на вортексе 45 сек.
7. Устанавливали пробирку в штатив и инкубировали при 25±2°С 5 мин.
8. Устанавливали пробирку в центрифугу, предварительно охлажденную до 4±2°С, и центрифугировали в течение 20 мин при ускорении 16000 RCF при температуре 4±2°С.
9. Переносили верхнюю водную фазу в чистую пробирку на 2 мл, измеряли объем водной фазы и добавляли 1,5 объема 100% этанола (как правило, 800 и 1200 мкл соответственно). Хорошо перемешивали с помощью пипетки. Не центрифугировали.
10. Переносили 700 мкл образца, включая осадок, если он появился, на колонку RNeasy MinElute Spin. Центрифугировали 15 сек при 12000 RCF, затем удаляли раствор, прошедший через колонку.
11. Повторяли пункт 10 необходимое количество раз для оставшегося объема образца.
12. Наносили на колонку RNeasy MinElute Spin 700 мкл RWT-буфера, центрифугировали 15 сек при 12000 RCF. Удаляли раствор, прошедший через колонку.
13. Наносили на колонку RNeasy MinElute Spin 500 мкл буфера RPE, центрифугировали 15 сек при 12000 RCF. Удаляли раствор, прошедший через колонку.
14. Добавляли на колонку RNeasy MinElute Spin 500 мкл 80% этанола, центрифугировали 2 мин при 12000 RCF, чтобы высушить мембрану колонки.
15. Переносили колонку RNeasy MinElute Spin в чистую пробирку на 2 мл и центрифугировали 5 мин при максимальном ускорении и открытой крышке колонки, чтобы полностью удалить остатки жидкости.
16. Переносили колонку RNeasy MinElute Spin в чистую пробирку на 1,5 мл для элюции образца. Аккуратно наносили 20 мкл воды, свободной от РНКаз, непосредственно на мембрану колонки. Центрифугировали 1 мин при максимальном ускорении.
17. Вынимали из пробирки колонку, перемешивали элюированный раствор и осаждали на центрифуге. Хранили на льду до продолжения эксперимента или замораживали при минус 20°С для непродолжительного хранения либо при минус 80°С для длительного хранения.
Пример 3. Способ анализа уровней микроРНК с помощью микрочипов Affymetrix GeneChip miRNA 4.0
Анализ экспрессии микроРНК в образцах плазмы крови проводили в соответствии с протоколом производителя с небольшими модификациями. Для анализа брали 8 мкл тотальной РНК, выделенной из плазмы крови. На первой стадии проводили реакцию неспецифического синтеза поли-А олигонуклеотидов на 3'-конце молекул микроРНК с помощью поли-А-полимеразы. Для этого к 8 мкл РНК добавляли 2 мкл RNA Spike Control Oligos и 5 мкл Poly A Tailing Master Mix (Таблица 1, при приготовлении смеси сразу на несколько образцов необходимо увеличение объемов на 5% для учета потерь при пипетировании), аккуратно перемешивали и инкубировали 15 минут при 37°С.

Далее проводили стадию лигирования для мечения каждой молекулы РНК специальной Biotin-labeled3DNA меткой, содержащей биотин. Для этого после наращивания поли-А-концов к реакционной смеси добавляли 4 мкл 5х FlashTag Biotin HSR Ligation Mix, 2 мкл T4 DNA Ligase, аккуратно перемешивали и инкубировали 30 мин при 25°С, после чего останавливали реакцию, добавлением 2,5 мкл HSR Stop Solution. Затем из 23,5 мкл реакционной смеси отбирали по 2 мкл для анализа ELOSA QC Assay, оставшиеся 21,5 мкл использовали для гибридизации на микрочипе.
Анализ ELOSA QC Assay (Enzyme Linked Oligosorbent Assay) проводили для оценки качества проведенных реакций, поэтому этот анализ проводили до стадии гибридизации. ELOSA QC Assay проводили с тремя контролями: положительный контроль, содержащий ELOSA Positive Control (олигонуклеотиды, меченые биотином и проверенные на качество производителем); отрицательный контроль, содержащий все реагенты для мечения РНК, кроме RNA Spike Control Oligos; отрицательный контроль, содержащий все реагенты для мечения РНК, кроме RNA Spike Control Oligos и тотальной РНК. Для проведения анализа сначала разводили ELOSA Spotting Oligos в растворе 1х PBS: например, для трех образцов 4,5 мкл ELOSA Spotting Oligos растворяли в 220,5 мкл 1x PBS. Разведенные ELOSA Spotting Oligos добавляли по 75 мкл в каждую лунку на плашке для ELOSA. После этого плашку с ELOSA Spotting Oligos оставляли на ночь в холодильнике при 2-8°С. Затем плашку дважды промывали раствором 0,02% Tween-20 в 1x PBS, добавляли 150 мкл 5% BSA в 1x PBS в каждую лунку, после этого инкубировали плашку 1 час при 25±2°С. Раствор удаляли из плашки.
На следующем этапе готовили Hybridization Master Mix (Таблица 2) и заполняли 50,5 мкл этого раствора каждую лунку. Далее добавляли либо 2 мкл воды (для отрицательного контроля), либо 2 мкл ELOSA Positive Control (для положительного контроля), либо 2 мкл меченого образца. Плашку хорошо заклеивали и инкубировали 1 час при 25±2°С.
Далее проводили связывание с SA-HRP. Лунки промывали 3 раза 0,02% раствором Tween в 1x PBS, потом в каждую добавляли 75 мкл SA-HRP, разведенного в соотношении 1:4000 раствором 5% BSA в 1x PBS. Плашку заклеивали и инкубировали 1 час при 25±2°С.После этого лунки промывали 3 раза раствором 0,02% Tween в 1x PBS, добавляли 100 мкл ТМВ Substrate в каждую лунку, заклеивали плашку, заворачивали в фольгу и оставляли в темноте на 7 минут. Синий цвет раствора в лунке означал положительный результат: лунки с положительным контролем оказывались синими, а лунки с отрицательными контролями содержали неокрашенные растворы. Если раствор в лунках с образцами оказывался синим, то считали, что стадия мечения прошла успешно, и образцы использовали дальше для гибридизации на микрочип.
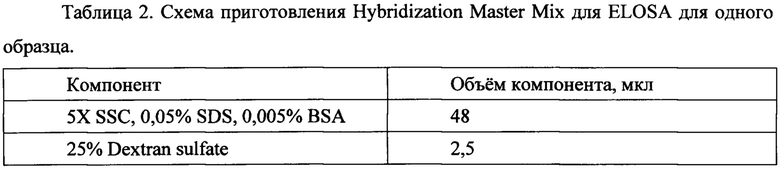
Для гибридизации готовили Hybridization Master Mix (Таблица 3, при приготовлении смеси на несколько образцов необходимо добавить 5% избыточного объема), при этом 20х Eukaryotic Hybridization Controls перед добавлением в реакционную смесь инкубировали 5 мин при 65°С. Готовый раствор Hybridization Master Mix добавляли по 110,5 мкл к 21,5 мкл меченого образца для составления Hybridization Cocktail. Полученный раствор инкубировали 5 мин при 99°С, а затем 5 мин при 45°С. Затем 130 мкл Hybridization Cocktail переносили в микрочип GeneChip miRNA 4.0. Чипы помещали в разогретую до 48°С гибридизационную печь Affymetrix Hybridization Oven 645 и оставляли в ней на 16 часов при скорости вращения 60 rpm.

По истечении 16 часов чипы вынимали из гибридизационной печи, удаляли из них гибридизационную смесь (при необходимости смесь можно сохранить и нанести на новый чип), заполняли чип буфером Array Holding Buffer и далее, следуя протоколу «GeneChip Expression Wash, Stain and Scan User Manual», промывали и прокрашивали с помощью GeneChipFluidics Station 450.
После промывки и прокрашивания чипы сканировали с помощью сканнера GeneChipScanner 3000 7G. В результате сканирования получали файлы с расширением «.CEL», в которых хранится информация об интенсивности свечения каждой точки на микрочипе. Для получения данных об экспрессии эти файлы подвергали статистическому анализу с помощью Affymetrix Expression Console.
Пример 4. Изучение профилей микроРНК в плазме крови пациентов с РПЖ и без РПЖ
Плазма крови для изучения профиля циркулирующих микроРНК больных с РПЖ и ДГПЖ была получена от 188 пациентов с РПЖ и 57 пациентов с ДГПЖ или отсутствием патологии предстательной железы в ФГБУ «НМИРЦ» Минздрава России (Таблица 4).

Для определения роли одиночных микроРНК в диагностике и дифференциальной диагностике ДГПЖ и РПЖ сравнение профилей экспрессии проводили с использованием программного обеспечения Transcriptome Analysis Console 3.0.0.466 (Affymetrix) с применением метода однофакторного непарного дисперсионного анализа. Среди всех микроРНК учитывали только те, log2-уровень экспрессии которых превышал 1,49 в плазме хотя бы одной из групп контроля или РПЖ. При этом значимым считалось 2-кратное и более изменение уровня микроРНК при уровне р-значения менее 0,05.
Для анализа роли сочетаний экспрессий нескольких микроРНК для диагностирования отсутствия РПЖ и наличия РПЖ использовали бинарный линейный классификатор. Входными данными этого классификатора являлись уровни циркулирующих в плазме крови человека микроРНК, результатом классификации - отнесение образца к одному из двух классов: РПЖ или отсутствие РПЖ.
На первом шаге методологии производили фильтрацию совокупности рассматриваемых микроРНК. Из анализа были исключены все микроРНК с представленностью ниже порога (3 квартиль на совокупной обучающей коллекции меньше 1,49). Дополнительно из анализа были исключены все микроРНК, которые коррелировали с уровнем гемоглобина (уровень статистической значимости, ассоциированный с коэффициентом корреляции Спирмана, меньше 0,05).
На втором шаге методологии из списка оставшихся в рассмотрении микроРНК отбирали микроРНК, по уровням которых осуществляли классификацию, и определяли (настраивали) параметры соответствующего классификатора. Осуществляли полный перебор двоек и троек микроРНК. Для каждой двойки и каждой тройки методом опорных векторов [Cortes С., Vapnik V. Support-Vector Networks // Mach. Learn. 1995. T. 20. №3. C. 273-297] с линейным ядром и штрафными коэффициентами, обратно пропорциональными размерам классов, по обучающей выборке настраивали бинарный классификатор. После настройки оценивали параметры достоверности классификации (чувствительность, специфичность, AUC -площадь под ROC-кривой). Двойки и тройки ранжировали по AUC, и рассматривали вопрос о включении в итоговую модель набора, ассоциированного с наибольшим значением AUC.
Рассчитывали уровни статистической значимости, соответствующие стандартной для биоинформатики модификации критерия Стьюдента -moderated t-statistics [Smyth G.K. Linear models and empirical bayes methods for assessing differential expression in microarray experiments. // Stat. Appl. Genet. Mol. Biol. 2004. Т. 3. C. Article3.], в качестве метода коррекции на множественность сравнений используютметод Бенжамини-Хохберга [Benjamini Y., Hochberg Y. Controlling the False Discovery Rate: a Practical and Powerful Approach to Multiple Testing // J.R. Stat. Soc. 1995. T. 57. №1. C. 289-300].
После исключения из анализа всех микроРНК с представленностью ниже порога (3 квартиль на совокупной обучающей коллекции меньше 1,49) и микроРНК, коррелирующих с уровнем гемоглобина, был произведен анализ всех пар и троек, составленных из оставшихся микроРНК.
Тройка, обеспечившая наилучшую диагностическую точность при определении наличия РПЖ, включала микроРНК hsa-miR-155-5p, hsa-miR-619-5p, hsa-miR-6777-5p. Наличию онкопатологии предстательной железы соответствует повышенный уровень в плазме крови всех трех микроРНК hsa-miR-155-5p, hsa-miR-619-5p, hsa-miR-6777-5p. Из всех возможных сочетаний по три микроРНК данная тройка обеспечивает существенно более высокое значение AUC по сравнению со всеми другими тройками. При сравнении с гистологически подтвержденным диагнозом чувствительность классификации на основе тройки микроРНК составила 78,9%, специфичность классификации - 80,8%, диагностическая точность - 79,4%, значение AUC - 0,850 (фиг. 1). Данные были получены в результате анализа в контрольной выборке, отличающейся от обучающей, построенной на основании анализа собственных данных о профиле микроРНК плазмы крови 68 пациентов с РПЖ и 69 здоровых добровольцев и пациентов с ДГПЖ или другими заболеваниями мочевыводящей системы, не затрагивающими предстательную железу, полученных на базе ФГБУ «НМИРЦ» Минздрава России.
Следует отметить, что эти значения соответствуют ситуации, когда набор образцов, соответствующих пациентам без онкопатологии предстательной железы, включал образцы, соответствующие пациентам с онкопатологиями других органов, а также пациентам с неонкологическими патологиями предстательной железы (доброкачественной гиперплазией). Это свидетельствует об отсутствии некорректности, связанной с возможным базированием классификатора на онкомаркерах, неспецифичных для предстательной железы, или же на маркерах патологий предстательной железы, свойственных не только онкопатологиям.
Также следует отметить, что при рассмотрении каждой отдельной микроРНК из входящих в построенную тройку микроРНК дифференциально представленной относительно двух сравниваемых классов является только hsa-miR-619-5p при стандартных критериях дифференциальной представленности, остальные две микроРНК по отдельности не имеют диагностической ценности. Однако чувствительность и специфичность при классификации на основе только hsa-miR-619-5p не превышают 70%, что говорит в пользу использования тройки микроРНК hsa-miR-155-5p, hsa-miR-619-5p, hsa-miR-6777-5p.
Пример 5. Исследование взаимосвязи уровней микроРНК в клеточной модели рака предстательной железы и плазме крови больных
МикроРНК могут выполнять свою функцию непосредственно в клетке, в которой они были синтезированы, однако было показано, что существуют определенные внутриклеточные механизмы сортировки, позволяющие секретировать во внеклеточное пространство рибонуклеопротеиновые комплексы микроРНК либо распределять микроРНК в экзосомы, которые затем поступают во внешнюю среду в виде везикул. При этом секреция микроРНК может быть неспецифической и напрямую зависеть от уровня микроРНК в клетках, либо определяться более специфическими регуляторными механизмами [Fritz J.V. и др. Sources and Functions of Extracellular Small RNAs in Human Circulation // Annu. Rev. Nutr. 2016. T. 36. №1. C. annurev-nutr-071715-050711].
МикроРНК из межклеточного пространства могут поступать непосредственно в системный кровоток. На сегодняшний день обнаружена корреляция целого ряда микроРНК в крови с наличием РПЖ, а также его характеристиками и прогнозом течения. На данный момент нет точного ответа, какие клетки являются источником циркулирующих микроРНК при РПЖ. Существует ряд гипотез их происхождения: клетки первичной опухоли и/или ее метастазов [Samatov T.R. и др. Modelling the metastatic cascade by in vitro microfluidic platforms // Prog. Histochem. Cytochem. 2015. T. 49. №4. C. 21-29], микроокружение опухоли, клетки иммунной системы [Makarova J.A. и др. Circulating microRNAs. // Biochem. Biokhimiia. 2015. Т. 80. №9. С. 1117-26]. Возможным подходом к изучению данного вопроса является моделирование in vitro. Был проведен анализ микроРНК в линии клеток РПЖ DU 145 и культуральной среде, в которой росли клетки, и сравнение выявленных профилей с профилями микроРНК плазмы крови больных с РПЖ.
Поскольку единственным источником увеличения уровня микроРНК в культуральной среде являются опухолевые клетки, можно утверждать, что прирост микроРНК достигается при разрушении погибших клеток и секреции из жизнеспособных клеток. Процесс накопления микроРНК в культуральной среде может служить моделью накопления микроРНК в области опухолевой ткани человека с РПЖ и попадания данных микроРНК в циркуляцию.
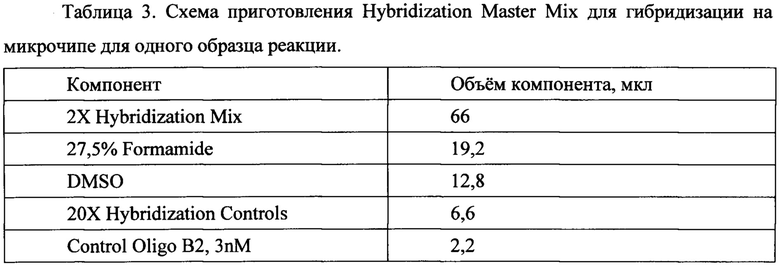
Был изучен уровень hsa-miR-155-5p, hsa-miR-619-5p, hsa-miR-6777-5p в клетках DU 145 и культуральной среде. Наличию онкопатологии предстательной железы соответствует повышенный уровень в плазме крове микроРНК hsa-miR-155-5p, hsa-miR-619-5р, hsa-miR-6777-5p. Таблица 5 отражает уровень данных микроРНК в культуральной среде и клетках РПЖ DU 145. Следует отметить, что уровень всех трех микроРНК был представлен выше порога в клетках и повышался в культуральной среде при росте клеток. Можно предположить, что повышение данных микроРНК в плазме крови при РПЖ связано с клетками опухоли.
Пример 6. Диагностика РПЖ
Пациент З-ч, 80 лет.
В марте 2015 г. проходил обследование в поликлинике НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина - филиале ФГБУ «НМИРЦ» Минздрава России с предварительным диагнозом гиперплазия предстательной железы. Жалобы на учащенное мочеиспускание.
Общий анализ мочи - норма. Лабораторная диагностика: ПСА=11,4 нг/мл. Пациенту было проведено исследование согласно заявляемому способу.
F=-2,98.
Так как F<0, было сделано заключение об отсутствии РПЖ.
В результате биопсии предстательной железы был поставлен диагноз доброкачественная гиперплазия предстательной железы.
Пример 7. Диагностика РПЖ
Пациент Р-в, 70 лет.
В июне 2015 г. проходил обследование в поликлинике НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина - филиале ФГБУ «НМИРЦ» Минздрава России с предварительным диагнозом гиперплазия предстательной железы. Жалобы на учащенное мочеиспускание.
Общий анализ мочи - норма. Лабораторная диагностика: ПСА=0,44 нг/мл.
Пациенту было проведено исследование согласно заявляемому способу.
F=0,32.
Так как F>0, было сделано заключение о наличии РПЖ.
В результате биопсии предстательной железы был поставлен диагноз рак предстательной железы (T2cN0M0).
Таким образом, преимуществами представленного изобретения являются возможность диагностики РПЖ и дифференциальной диагностики РПЖ и ДГПЖ даже на ранних стадиях развития рака (стадия I-II) с диагностической точностью выше, чем у существующих методов скрининговой диагностики; возможность избежать травматизирующей процедуры биопсии предстательной железы при отнесении пациента к группе низкого риска РПЖ; низкая инвазивность теста, поскольку определение микроРНК производится в образце венозной крови; высокая воспроизводимость метода диагностики.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ И ДОБРОКАЧЕСТВЕННОЙ ГИПЕРПЛАЗИИ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ | 2016 |
|
RU2647433C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ НА ОСНОВЕ АНАЛИЗА МИКРОРНК ПЛАЗМЫ КРОВИ | 2016 |
|
RU2618409C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ РИСКА ЗЛОКАЧЕСТВЕННОЙ ТРАНСФОРМАЦИИ КЛЕТОК ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ | 2022 |
|
RU2806518C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ | 2012 |
|
RU2521389C2 |
| Способ ранней диагностики опухолей предстательной железы | 2021 |
|
RU2756643C1 |
| Способ дифференциальной диагностики рака яичников, кистозных образований яичника и рака тела матки | 2024 |
|
RU2836527C1 |
| Тест-система "miR-M-SCREEN" для прогнозирования развития метастазов у больных колоректальным раком на основании уровня микро-РНК miR-26a и miR-143 в плазме крови | 2022 |
|
RU2786386C1 |
| СПОСОБ РАННЕЙ ДНК-ДИАГНОСТИКИ РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ | 2009 |
|
RU2405837C1 |
| МАРКЕР РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ | 2007 |
|
RU2360924C1 |
| Набор реагентов для определения малых рибонуклеиновых кислот (микроРНК) при диагностике множественной миеломы | 2024 |
|
RU2836054C1 |

Настоящее изобретение относится к области медицины, в частности к онкологии и молекулярной биологии, и может быть использовано для дифференциальной диагностики рака предстательной железы (РПЖ) и доброкачественной гиперплазии предстательной железы (ДГПЖ). Способ включает: получение образца периферической крови пациента; выделение плазмы крови из образца; выделение РНК из плазмы крови; измерение уровня экспрессии микроРНК hsa-miR-155-5р, hsa-miR-619-5p, hsa-miR-6777-5p с последующим определением вероятностного значения (F), характеризующего наличие риска РПЖ, по следующей формуле:
F=0,931×(L1-2,878)/2,064+0,960×(L2-3,059)/2,160+0,587×(L3-2,523)/0,689-0,515,
где L1, L2 и L3 - уровни экспрессии микроРНК hsa-miR-155-5p, hsa-miR-619-5p, hsa-miR-6777-5р соответственно. При получении значения F>0 диагностируют РПЖ, при получении F≤0 - ДГПЖ. Изобретение позволяет эффективно осуществлять диагностику рака предстательной железы и дифференциальную диагностику рака предстательной железы и доброкачественной гиперплазии предстательной железы, что позволяет начать своевременную и адекватную терапию. 6 з.п. ф-лы, 5 табл., 7 пр., 1 ил.
1. Способ дифференциальной диагностики рака предстательной железы (РПЖ) и доброкачественной гиперплазии предстательной железы (ДГПЖ), включающий получение образца периферической крови пациента; выделение плазмы крови из образца; выделение РНК из плазмы крови; измерение уровня экспрессии микроРНК hsa-miR-155-5р, hsa-miR-619-5p, hsa-miR-6777-5p с последующим определением вероятностного значения (F), характеризующего наличие риска РПЖ, по следующей формуле:
F=0,931×(L1-2,878)/2,064+0,960×(L2-3,059)/2,160+0,587×(L3-2,523)/0,689-0,515,
где L1, L2 и L3 - уровни экспрессии микроРНК hsa-miR-155-5p, hsa-miR-619-5p, hsa-miR-6777-5р соответственно,
и при получении значения F>0 диагностируют РПЖ, при получении F≤0 - ДГПЖ.
2. Способ по п. 1, характеризующийся тем, что выделение плазмы крови проводят центрифугированием образца крови.
3. Способ по п. 1, характеризующийся тем, что центрифугирование образца проводят при режимах, обеспечивающих максимальную сохранность клеточных элементов крови и минимальное содержание тромбоцитов и мелких мембранных везикул.
4. Способ по п. 3, характеризующийся тем, что центрифугирование проводят в два этапа по 10±1 мин каждый: первый - при 2000±100 RCF с последующим переносом верхней фазы в новую пробирку, второй этап проводится при 4000±200 RCF, после этого отбирают всю плазму кроме 10±5% объема у дна пробирки.
5. Способ по п. 3, характеризующийся тем, что все этапы проводят при 25±2°С.
6. Способ по п. 1, характеризующийся тем, что измерение уровня экспрессии микроРНК проводят с помощью микрочипового анализа.
7. Способ по п. 6, характеризующийся тем, что для проведения анализа используют чипы Affymetrix GeneChip miRNA 4.0.
| КНЯЗЕВ Е.Н | |||
| и др | |||
| ПРИСПОСОБЛЕНИЕ ДЛЯ УПРАЖНЕНИЙ НА МУНДШТУКЕ ДУХОВЫХ ИНСТРУМЕНТОВ | 1923 |
|
SU619A1 |
| Вага для выталкивания костылей из шпал | 1920 |
|
SU161A1 |
| Аппарат для радиометрической съемки | 1922 |
|
SU124A1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ | 2012 |
|
RU2521389C2 |
| US 2013053264 A1, 28.02.2013 | |||
| КУНИН И.С | |||
| и др | |||
| Молекулярные маркеры метастазирования аденокарциномы предстательной железы | |||
| Онкоурология | |||
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| САМСОНОВ Р.Б | |||
| и др | |||
| Выделение и анализ экзосомальной микро-РНК из мочи: новый метод диагностики рака предстательной железы | |||
| Экспериментальная и клиническая урология | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| http://ecuro.ru/article/vydelenie-i-analiz-ekzosomalnoi-mikro-rnk-iz-mochi-novyi-metod-diagnostiki-raka-predstatelno | |||
| KNYAZEV E.N | |||
| et al | |||
| ПРИСПОСОБЛЕНИЕ ДЛЯ УПРАЖНЕНИЙ НА МУНДШТУКЕ ДУХОВЫХ ИНСТРУМЕНТОВ | 1923 |
|
SU619A1 |
| Bull Exp Biol Med | |||
| Токарный резец | 1924 |
|
SU2016A1 |
| найдено в PubMed, PMID: 27265125. | |||
Авторы
Даты
2018-03-07—Публикация
2016-12-30—Подача