Изобретение относится к области биотехнологии и диагностической медицины и может быть использовано при разработке метода оценки риска рака предстательной железы (РПЖ), на этапе решения вопроса о целесообразности проведения диагностической биопсии или в ходе динамического наблюдения пациентов с пограничными значениями уровня концентрации сывороточного маркера ПСА. Рак предстательной железы (РПЖ) - это злокачественное образование, развивающиеся из эпителиальных клеток предстательной железы. Рак предстательной железы является четвертым в степени по распространенности среди других онкологических заболеваний, уступая раку молочной железы, легкого и прямой кишки. Первые этапы развития заболевания происходят бессимптомно, поэтому в большинстве случаев диагноз РПЖ ставится на стадии местного распространения процесса. Прогноз зависит от стадии и степени злокачественности заболевания. На первой стадии, при своевременном лечении десятилетняя выживаемость составляет более 90%, при второй - 80%, при третьей - 40%, при четвертой - 15%. Поэтому актуальными являются задачи скрининга и ранней диагностики РПЖ [1]. В настоящее время в основе диагностики РПЖ лежит комплекс исследований: определение уровня простатического специфического антигена (ПСА) в плазме или сыворотке крови, пальцевое ректальное исследование (ПРИ) и трансректальное ультразвуковое исследование предстательной железы (ТРУЗИ). В случае подозрения на РПЖ, на основании хотя бы одного из перечисленных исследований, комплекс диагностических подходов расширяется и может включать: биопсию предстательной железы с последующим гистологическим исследованием, эхо-допплерография предстательной железы, магнитно-резонансная томография (МРТ), компьютерная томография (КТ). Проблематичным аспектов является низкая диагностическая специфичность ПСА сыворотки, что ведет к необходимости проведения дополнительных, инвазивных и/или дорогостоящих, диагностических исследований. Для решения этой проблемы разрабатываются и внедряются в практику новые технологии «жидкостной биопсии». Например, Индекс здоровья простаты (Prostate health index - PHI) - разработанный компанией Beckman Coulter (Брея, США) тест: на основе определения в крови уровня общего ПСА, свободного ПСА и -2проПСА рассчитывается величина PHI, изменение которого может указывать на наличие РПЖ [2]. Схожая технология реализована компания ОРКО Health (Майами, США): расчет параметра 4k-score проводится по уровням четырех маркеров: общий ПСА, свободный ПСА, интактный ПСА и калликреин-2 (hK2) [3].
Внеклеточные нановезикулы (ВНВ) - являются новым перспективным классом онкомаркеров, который имеет перспективы применения для диагностики различных онкологических заболеваний [4], включая РПЖ [5]. ВНВ - это мембранные нано-везикулы (80-130 нм), которые секретируются всеми клетками многоклеточных организмов во внеклеточное пространство. В состав ВНВ входят факторы трансляции, ферменты метаболизма, протеолитические белки шапероны, различные типы нуклеиновых кислот. Некоторые белки, такие как белки теплового шока (HSP70 и HSP90) и тетраспанины (CD9, CD63, CD81) характерны для нановезикул, независимо от типа клеток, из которых они секретируются. Мембранные белки, белки клеточной адгезии и протеогликаны в составе везикулярной мембраны имеют состав аналогичный или близкий к составу клеток, секретирующих везикулы (клеток-продуцентов). Этот феномен позволяет установить клеточное происхождение специфических фракций ВНВ в составе общей популяции. Кроме того, состав молекул РНК (мРНК и/или микроРНК), которые попадают в везикулы в процессе их образования из клеточной цитоплазмы, также отражает тканевую принадлежность или состояние клеток-продуцентов.
МикроРНК - это класс малых регуляторных молекул РНК, которые выполняют функцию контроля стабильности информационных РНК и эффективности синтеза белковых молекул (трансляции) в клеточной цитоплазме. Состав (или «профиль» микроРНК в клетках различных тканей имеет характерные особенности, развитие различных патологических состояний (включая злокачественную трансформацию) сопровождается характерными изменениями состава внутриклеточных микроРНК. Этот феномен имеет очевидный диагностический потенциал, но предполагает получение и анализ биопсийного материала [6]. Внеклеточные функции микроРНК пока исследованы слабо, но различные типы этих молекул могут быть детектированы в биологических жидкостях в свободном виде (циркулирующие микроРНК), в составе комплексов с рибонуклеопротеинами (белки Argonaute, липопротеины высокой плотности) или в составе ВНВ. МикроРНК в составе ВНВ представляют интерес в качестве диагностических маркеров по двум основным причинам. Во-первых, микроРНК в составе ВНВ сохраняет биохимическую стабильность. Во-вторых, клеточные или тканевые особенности везикулярной поверхности позволяет выделить специфические (например, ткане-специфические) популяции ВНВ. Показано, что профиль микроРНК в составе специфической фракции ВНВ может отражать состав микроРНК соответствующий специфической популяции клеток [7-9]. Этот феномен определят высокий диагностический потенциал методов анализа микроРНК в составе ВНВ определенного происхождения. Так, выделение специфических популяций ВНВ, секретируемых специфическими клетками (например, злокачественными клетками или клетками предстательной железы), и последующий анализ биохимических компонентов этих ВНВ (например, микроРНК) является перспективным методом диагностики онкологических заболеваний, в частности, РПЖ.
Известно несколько примеров патентной защиты этой идеи или способов ее реализации, которые могут быть рассмотрены в качестве аналогов представленного способа.
US 7897356 B2 (Caris Life Sciences Switzerland Holdings GmbH): Методы и системы использования экзосом для определения фенотипа / Methods and systems of using exosomes for determining phenotypes - патент, зарегистрированный в 2012 на территории ряда стран (исключая РФ) охраняет приоритет использования определенного типа ВНВ, а именно экзосом, в рамках диагностики различных заболеваний (более 50 нозологий, включая РПЖ), путем выделения экзосом из всех типов биологических жидкостей (более 20 вариантов, включая плазму крови) и анализа различных биохимических компонентов (более 1000 конкретных молекул, включая микро-РНК miR-205-5p и miR-375-3р). В патенте не описано конкретных диагностических технологий, патент защищает право использования экзосом в качестве объекта анализа с целью медицинской диагностики в целом на территории ряда стран, исключая РФ.
Тест-система для диагностики или/и оценки риска развития/прогрессии РПЖ (Diagnostic Test: ExoDx Prostate - IntelliScore), основанная на выделении и анализе экзосом мочи, была разработана дочерней компанией Exosome Diagnostics GmbH. Тест-система проходила клинические испытания (ClinicalTrials.gov Identifier: NCT03235687). С учетом опубликованных данных, результат анализа может быть полезен при решении вопроса о (1) целесообразности проведения биопсии у пациентов, значение уровня ПСА плазмы которых незначительно повышено или соответствует так называемой «серой зоне» (2-10 нг/мл) [10] и/или (2) проведении хирургического лечения (радикальной простатэктомии) у пациентов с подтвержденным диагнозом РПЖ [11]. От разработанного способа технология ExoDx Prostate - IntelliScore отличается тем, что, во-первых, в качестве источника ВНВ используется моча (а не плазма); во-вторых, исследуемый образец представляет собой тотальную популяцию ВНВ (а не специфическую (PSMA(+)/AMACR(+)) фракцию везикул; в-третьих, проводится анализ трех молекул информационной РНК -продуктов транскрипции генов ERG, PCA3, SPDEF (а не двух молекул микроРНК miR-205-5p и miR-375-3р).
US 20130196355 A1 (Exosomics Siena SpA): Метод и набор для количественного и качественного анализа экзосом для диагностики рака предстательной железы и гиперплазии предстательной железы / Method and a kit to quantify and qualify exosomes for diagnosis of prostate cancer and prostate hyperplasia - патент, зарегистрированный в 2015 на территории ряда стран (исключая РФ) охраняет приоритет использования анализа экзосом плазмы в рамках диагностики РПЖ, путем полуколичественной оценки PSA-позитивных везикул с помощью проточной цитометрии или иммуно-ферментного анализа. Технология пока не была реализована в виде диагностической тест-системы. От разработанного способа технология отличается тем, что, результатом ее применения является полуколичественная оценка специфической популяции экзосом (а не выделение такой популяции и последующий анализа микроРНК), во-вторых, в качестве маркеров используются везикулярные белки Rab5 и PSA (а не PSMA и AMACR), в-третьих, в качестве молекул-лигандов используются антитела (а не ДНК-аптамеры).
US 10494676 В2 (Albert Ludwigs Universitaet Freiburg / Karlsruher Institut fuer Technologie KIT): Процесс диагностики рака с помощью экзосом / Process for the diagnosis of cancer by using exosomes - патент зарегистрированный в 2013 на территории ряда стран (исключая РФ) охраняет приоритет использования технологии анализа различных сплайсиг-форм мРНК (матричной РНК) гена ARG2 в образце экзосом, выделенных из плазмы крови или мочи, в рамках диагностики различных онкологических заболеваний, включая РПЖ. От разработанного способа технология отличается тем, что, во-первых, исследуемый образец представляет собой тотальную популяцию ВНВ мочи или плазмы (а не специфическую (PSMA(+)/AMACR(+)) фракцию везикул, во-вторых, технология предполагает анализа мРНК гена ARG2 (а не молекул микроРНК miR-205-5p и miR-375-3р).
Задачей изобретения являлось создания метода диагностики РПЖ на основе анализа микроРНК в простат-специфической фракции ВНВ плазмы.
Теоретической основой изобретения являлось предположение о том, что в состав мембраны ВНВ, секретируемых клетками предстательной железы, входят простат-специфические белки; а состав микроРНК в клетках предстательной железы и, соответственно в ВНВ, секретируемых этими клетками изменяется в случае злокачественной трансформации этих клеток, или развития РПЖ. Задача изобретения решалась путем разработки метода выделения фракции ВНВ, синтезируемой клетками предстательной железы, и последующего анализа молекул микроРНК, изменение экспрессии которых ассоциировано с развитием РПЖ.
В качестве технического прототипа способа выделения ВНВ может быть рассмотрена технология выделения тотальной популяции ВНВ плазмы с помощью супер-парамагнитных частиц (СПМЧ), поверхность которых «функционализирована» ДНК-аптамерами (патент РФ 2741638), аффинно связывающих маркер CD63, предположительно присутствующий на поверхности всех ВНВ (экзосом). В качестве идейных прототипов разработанного способа могут быть рассмотрены (а) метод выделения тироид-специфичных ВНВ и анализа маркерных микроРНК в выделенной популяции ВНВ с целью диагностики фолликулярного рака щитовидной железы [9], и (б) метод выделения простат-специфичных ВНВ и анализа маркерных микроРНК в выделенной популяции ВНВ с целью диагностики РПЖ [7, 8]. В первом примере в качестве молекулярного лиганда, связывающего специфические ВНВ, использовались антитела к тироид-специфичному белку ТРО (thyroid peroxidase). Во втором примере выделение простат-специфичных везикул проводилось с помощью ДНК-аптамера, для которого характерно аффинное взаимодействие с белком PSMA (prostate-specific membrane antigen). Недостатком представленных выше технологий являлось использование одного типа молекулы - лиганда, что не обеспечивало достаточной эффективности выделения специфических ВНВ и, соответственно, снижало диагностический потенциал метода в целом.
В отличии от прототипов, в разработанном способе суперпарамагнитные частицы «функционализированы» пятью типами ДНК-аптамеров, которые аффинно связывают различные эпитопы простат-специфичных мембранных белков PSMA (prostate specific membrane antigen) и AMACR (α-methyl acyl-CoA racemase). Это позволило эффективно «связывать» специфическую популяция ВНВ, секретируемых преимущественно клетками предстательной железы. Связь поверхности супер-парамагнитных частиц и ДНК - аптамеров (функционализация) осуществляется с помощью технологии «клик-химии» - реакции азид-алконового циклоприсоединения. Далее разработанный способ предполагает количественный анализ двух молекул микроРНК (miR-205-5p и miR-375-3р) в материале выделенных ВНВ с помощью последовательных реакций обратной транскрипции и ПНР.
Технический результат изобретения - способ уточняющей диагностики РПЖ - реализуется путем полуколичественного анализа двух молекул микроРНК (miR-205-5p и miR-375-3р) в материале простат-специфичных (PSMA(+) и AMACR(+)) ВНВ плазмы.
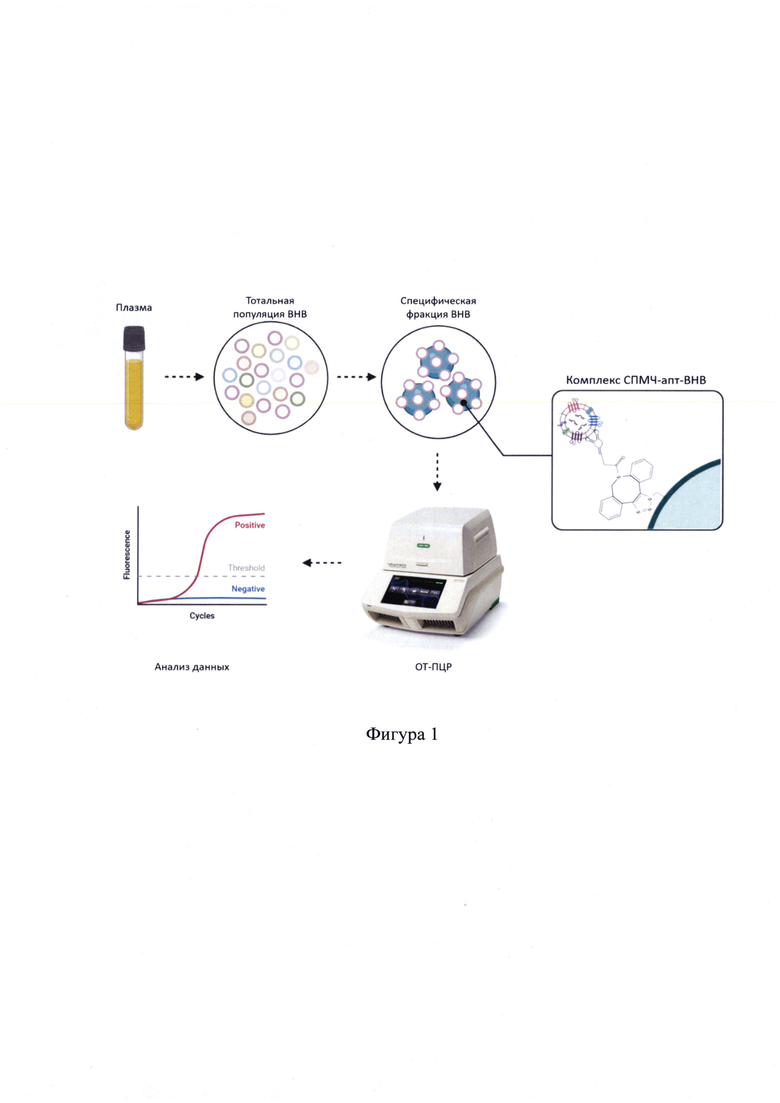
Поставленная задача достигается предлагаемым способом, схематично представленном на Фиг. 1:
1. Сбор венозной крови (5-6 мл) в вакутейнер с EDTA. Форменные элементы отделяются от плазмы центрифугированием 15 минут 1500g, плазма перемещается в чистую пробирку, из плазмы удаляется клеточный дебрис, фибриллы плазменных белков и крупные везикулы путем последовательного центрифугирования по 10 минут при ускорении 300g, 1500g, 2500g. Супернатант фильтруется через шприцевой фильтр с диаметром пор 0,22 мкм Minisart High Flow (Sartorius, Германия), после чего очищенная плазма перемещается в чистую пробирку.
2. Выделение тотальной популяции ВНВ плазмы объемом 1,5 мл может быть проведено любым способом, например, с помощью ультрацентрифугирования (патент RU 2556825 C1) или с помощью двухфазной полимерной системы (патент RU 2741776). Тотальную популяцию ВНВ, выделенных любым способом, ресуспендируют в 100 мкл фосфатно-солевого буфера.
3. Создание СПМЧ, поверхность которых функционализирована ДНК - аптамерами с помощью технологии «клик-химии» - реакции азид-алконового циклоприсоединения. Для этого используют СПМЧ размером 0,8-1 мкм, поверхность которых модифицирована азидными группами (-N3), например Azide Magnetic Beads (Click Chemistry Tools, США) и ДНК - аптамеры, последовательности которых представлены в Таблице 1, по 5' концу молекулы ДНК аптамеров модифицированы дибензоциклооктином (ДБЦО). Синтез ДНК - аптамеров проводится стандартным способом, очистка высокоэффективная жидкостная хроматография (ВЭЖХ).


Частицы (1 мг/мл) инкубируются с ДНК - аптамерами (100 пМоль) в 100 мкл фосфатно-солевого буфера 3 часа при комнатной температуре. Молекула ДБЦО на 5' конце аптамеров вступает в реакцию азид-алконового циклоприсоединения, промотируемого напряжением цикла с азидной группой на поверхности СПМЧ, благодаря чему образуется комплекс СПМЧ и аптамеров (СПМЧ-Апт), который способен связывать молекулы PSMA и AMACR в составе мембран везикул, секретируемых клетками предстательной железы. СПМЧ с функционализированной ДНК-аптамерами поверхностью отмываются дважды фосфатно-солевым буфером (ФСБ) с использованием магнитного штатива.
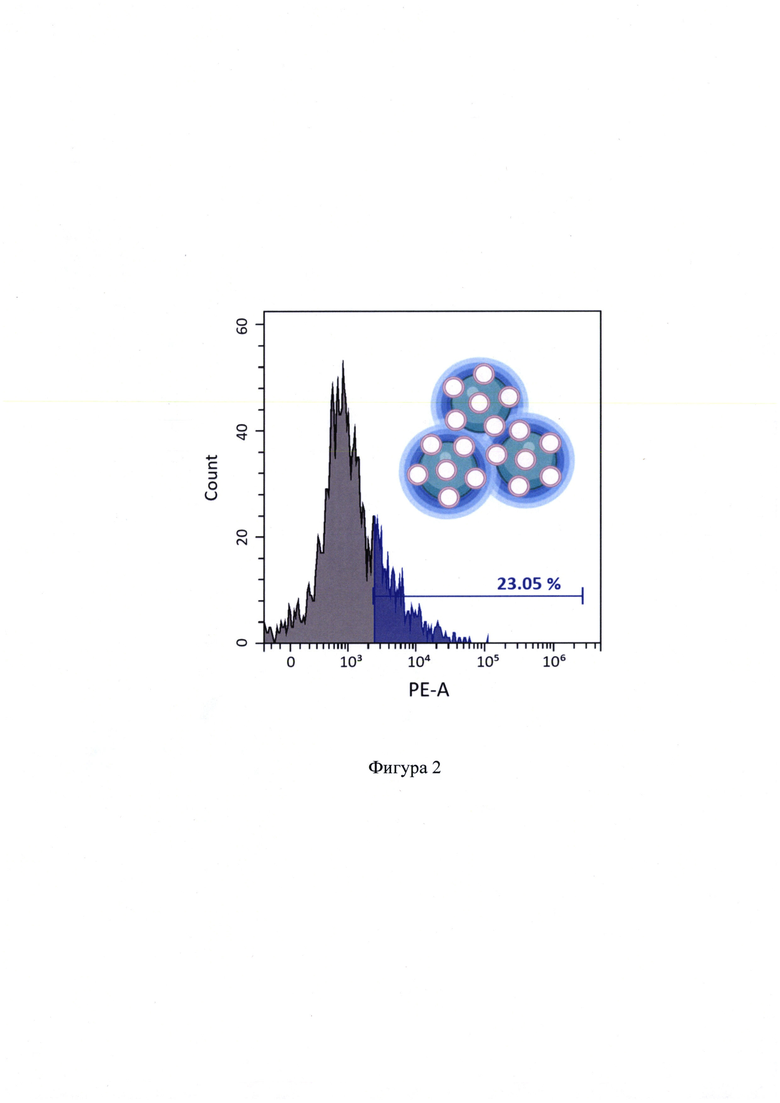
4. Для выделения простат-специфичной фракции везикул 5 мкл суспензии СПМЧ инкубируют в 200 мкл блокирующего буфера, например, 0.2% раствора I-Block™ (Invitrogen, США) 1 час при +4°С, при постоянном перемешивании, отмывают 3 раза в 200 мкл ФСБ и осаждают на магнитном штативе. К полученному осадку из функционализированных и блокированных СПМЧ добавляют 100 мкл выделенной ранее общей популяции ВНВ, инкубируют ночь при +4°С при постоянном перемешивании. Образовавшийся комплекс СПМЧ-Апт-ВНВ отмывают дважды в ФСБ и осаждают на магнитном штативе. Оценка эффективности связывания и выделения из тотальной популяции ВНВ плазмы фракции простат-специфических BHB-PSMA(+)/AMACR(+), может быть оценена с использованием проточной цитометрии. При этом фиксированные к поверхности СПМЧ везикулы окрашиваются с помощью, например, флуоресцентно-меченных антител к пан-везикулярным маркерам CD63 или CD9. Пример визуальной оценки BHB-PSMA(+)/AMACR(+), выделенных из тотальной популяции ВНВ плазмы здорового донора мужчины, представлен на Фиг. 2. Согласно полученным результатам, на поверхности 23% СПМЧ фиксированы ВНВ, интенсивность флуоресцентного сигнала отражает количество фиксированных везикул.
5. Выделение РНК и анализ микроРНК. Осадок используют для выделения микроРНК любым доступным способом, например, с помощью технологии протеолиза / липолиза (набор RNAGEM, производства компании MicroGEM, Новая Зеландия) или технологии твердофазной экстакции (Набор для выделения суммарной РНК и микроРНК из клеток и тканей, производства компании БиоЛабМикс, РФ) в соответствии с протоколами производителей. Выделенный раствор РНК используют для анализа концентрации маркерных молекул микроРНК miR-205-5p и miR-375-3р методом обратной транскрипции и последующий полимеразной цепной реакции (ОТ-ПЦР). Анализ может быть проведен любым доступным набором реагентов для анализа miR-205-5p и miR-375-3р, например, miRCURY LNA miRNA PCR Assays (Qiagen, США) или ALMIR (Альгимед Техно, Беларусь).
6. Анализ результатов проводится путем определения значений пороговых циклов (Ct) для двух молекул при фиксированной позиции «пороговой» линии, и расчета соотношения относительных концентраций miR-205-5p и miR-375-3р по формуле:
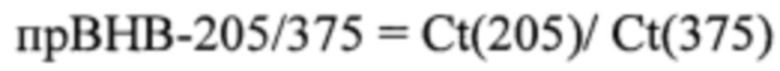
где Ct(205) - значение порогового цикла miR-205-5p
Ct(375) - значение порогового цикла miR-375-3р
Значение полученного показателя прВНВ-205/375 < 1 соответствует диагнозу РПЖ, значение полученного показателя прВНВ-205/375 ≥ 1 соответствует нормальному состоянию предстательной железы. Диагностическая чувствительность разработанного способа уточняющей диагностики - 97,22%, специфичность - 77,78%.
Способ подтверждается следующими примерами.
Пример 1. Анализа микроРНК (miR-205-5p и miR-375-3р) из специфической фракции ВНВ, секретируемых клетками предстательной железы, у пациентов к РПЖ и здоровых доноров.
Образцы плазмы были получены от 36 пациентов с гистологически верифицированным диагнозом рака предстательной железы. Средний возраст пациентов - 65 (диапазон 49-74 года), показатель Глисона - в диапазоне 6-9, уровень ПСА: 4,5-82,0 нг/мл. Образцы венозной крови были получены от 18 здоровых доноров, возрастом 20-54 года для формирования группы контроля. Плазма была приготовлена в соответствии с разработанным протоколом путем последовательного центрифугирования по 10 минут при ускорении 300g, 1500g, 2500g. Тотальная популяция ВНВ была выделена методом двухфазной полимерной системы [16]. Для этого в пробирку 2 мл добавили 0,0525 г Декстрана 450-650 кДа (Sigma-Aldrich, США) и 0,0255 г Полиэтиленгликоля 20 кДа (Sigma-Aldrich, США), внесли 1,5 мл плазмы, перемешали и растворили в течение часа при +4°С. Одновременно приготовили промывочный раствор путем растворения аналогичного количества полимеров в 1,5 мл ФСБ. Разделение смеси полимеров в плазме на две фазы провели центрифугированием 10 мин 1000g при 4°С, после чего верхнюю фазу удалили, а нижнюю фазу ресуспендировали в 1,4 мл ранее приготовленного промывочного раствора. Растворы перемешали и снова центрифугируют при 10 мин 1000g 4°С. Супернатант удалили и осадок ресуспендировали в 100 мкл ФСБ. В соответствии с разработанным способом приготовили СПМЧ-Апт и провели выделение простат-специфичной фракции ВНВ (BHB-PSMA(+)/AMACR(+)). РНК из BHB-PSMA(+)/AMACR(+) выделили стандартным методом с использованием коммерческого набора RNAGEM согласно протоколу производителя. В каждом полученном образце был проведен анализ концентрации mir-205-5p и mir-375-3р с помощью ОТ-ПЦР, для этого использовали соответствующие наборы реагентов серии ALMIR (Альгимед Техно, Минск). Расчет диагностического параметра прВНВ-205/375 для каждого биологического образца, включенного в исследование, провели по формуле прВНВ-205/375=Ct(205)/Ct(375).
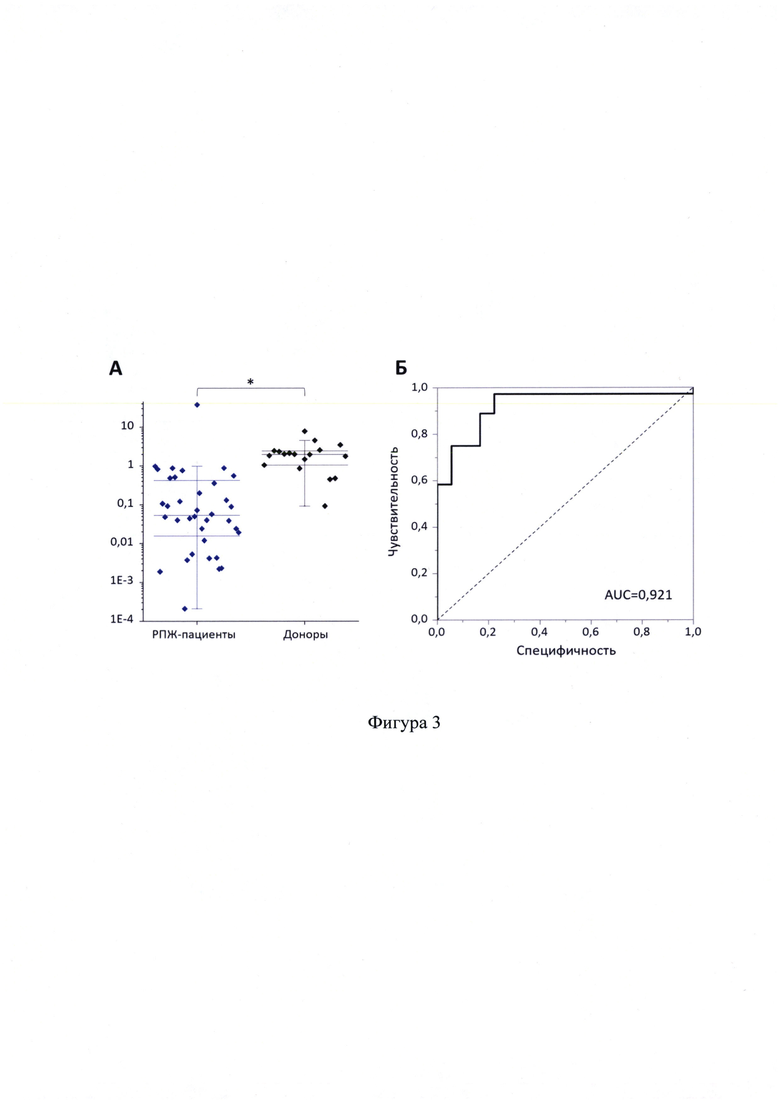
Для оценки параметров диагностической значимости разработанного способа в качестве референсного метода использовали гистологическое исследование. На Фиг. 3А представлены результаты оценки параметра прВНВ-205/375 в группах доноров (n. 18) и пациентов с РПЖ (n. 36). Статистическая значимость сравнения данных групп рассчитывалась методом Манна-Уитни (р<0,0005). На Фиг. 3Б приведен график ROC-кривой: площадь под кривой (area under curve, AUC - комплексный показатель диагностической значимости метода) = 0,921. Также были рассчитаны показатели диагностической значимости: чувствительность - 97,22%, специфичность - 77,78%, позитивное предиктивное значение - 89,47%, негативное предиктивное значение - 93,52%, общая точность - 90,61%.
Пример 2.
Анализа микроРНК (miR-205-5p и miR-375-3р) из специфической фракции ВНВ, секретируемых клетками предстательной железы, у пациента повышенным уровнем ПСА плазмы и отрицательным результатом диагностической биопсии.
Пациент С., 68 лет, жалоб нет, при профилактическом обследовании ПСА - 25 нг/мл, проведена диагностическая биопсия с последующим гистологическим исследованием материала (заключение: морфологические изменения, соответствующие картине доброкачественной гиперплазии предстательной железы).
Для оценки ситуации был определен параметр прВНВ-205/375, согласно заявленному методу. Полученный результат: прВНВ-205/375 = 1,32, что соответствует отсутствию признаков злокачественной трансформации клеток предстательной железы. Пациенту рекомендовано наблюдение у уролога и контроль уровня ПСА в динамике.
Пример 3.
Анализа микроРНК (miR-205-5p и miR-375-3р) из специфической фракции ВНВ, секретируемых клетками предстательной железы, у пациента уровнем ПСА - 5.5 нг/мл («серая зона»).
Пациент К., 54 года, жалоб нет, при профилактическом обследовании ПСА - 4.5 нг/мл, повторное исследование через 6 месяцев - 5,3 нг/мл. Заключение транс-уретрального ультразвукового исследования предстательной железы (ТРУЗИ): УЗИ признаков патологических изменений не выявлено.
Для решения вопроса о целесообразности проведения диагностической биопсии был определен параметр прВНВ-205/375, согласно заявленному методу. Полученный результат: прВНВ-205/375 = 0.91, что указывает на вероятность злокачественной трансформации клеток предстательной железы. Пациенту проведена диагностическая биопсия с последующим гистологическим исследованием материала (заключение: простатическая интраэпителиальная неоплазия (ПИН) высокой степени (high-grade prostatic intraepithelial neoplasia, HGPIN). Данное состояние ткани предстательной железы представляет собой предраковый процесс и является наиболее значимым прогностическим маркером развития РПЖ [17]. Пациенту рекомендована консультация онколога для определения тактики лечения.
Источники информации
1. Shieh, Y.; Eklund, М.; Sawaya, G.F.; Black, W.C.; Kramer, B.S.; Esserman, L.J. Population-based screening for cancer: Hope and hype. Nat. Rev. Clin. Oncol. 2016, 13.
2. Loeb, S.; Catalona, W.J. The Prostate Health Index: A new test for the detection of prostate cancer. Ther. Adv. Urol. 2014, 6.
3. Zappala, S.M.; Dong, Y.; binder, V.; Reeve, M; Sjoberg, D.D.; Mathur, V.; Roberts, R.; Okrongly, D.; Newmark, J.; Sant, G.; et al. The 4Kscore blood test accurately identifies men with aggressive prostate cancer prior to prostate biopsy with or without DRE information. Int. J. Clin. Pract. 2017, 71, doi:10.1111/ijcp.12943.
4. Czystowska-Kuzmicz, M.; Whiteside, T.L. The potential role of tumor-derived exosomes in diagnosis, prognosis, and response to therapy in cancer. Expert Opin. Biol. Ther. 2021, 21, 241-258, doi:10.1080/14712598.2020.1813276.
5. Samsonov, R.; Shtam, Т.; Burdakov, V.; Glotov, A.; Tsyrlina, E.; Berstein, L.; Nosov, A.; Evtushenko, V.; Filatov, M.; Malek, A. Lectin-induced agglutination method of urinary exosomes isolation followed by mi-RNA analysis: Application for prostate cancer diagnostic. Prostate 2016, 76, doi:10.1002/pros.23101.
6. Siddiqua, A.; Kousar, S.; Jamil, A.; Tabassum, R.; Mehmood, Т.; Shafiq, N. MicroRNA: A Signature for Cancer Diagnostics. In Current Cancer Treatment; IntechOpen, 2020.
7. Zabegina, L.; Nazarova, I.; Nikiforova, N.; Slyusarenko, M.; Sidina, E.; Knyazeva, M.; Tsyrlina, E.; Novikov, S.; Reva, S.; Malek, A. A New Approach for Prostate Cancer Diagnosis by miRNA Profiling of Prostate-Derived Plasma Small Extracellular Vesicles. Cells 2021, 10, 2372, doi:10.3390/cellsl0092372.
8. Zabegina, L.M.; Nikiforova, N.S.; Nazarova, I.V.; Knyazeva, M.S.; Tsyrlina, E.V.; Reva, S.A.; Nosov, A.K.; Malek, A.M. Analysis of miRNAs in the PSMA-positive fraction of plasma nano-sized extracellular vesicles in patients with prostate cancer. Cancer Urol. 2022, 17, 65-75, doi:10.17650/1726-9776-2021-17-4-65-75.
9. Zabegina, L.; Nazarova, I.; Knyazeva, M.; Nikiforova, N.; Slyusarenko, M.; Titov, S.; Vasilyev, D.; Sleptsov, I.; Malek, A. MiRNA let-7 from TPO(+) Extracellular Vesicles is a Potential Marker for a Differential Diagnosis of Follicular Thyroid Nodules. Cells 2020,9, 1917, doi:10.3390/cells9081917.
10. Tutrone, R.; Donovan, M J.; Torkler, P.; Tadigotla, V.; McLain, Т.; Noerholm, M.; Skog, J.; McKiernan, J. Clinical utility of the exosome based ExoDx Prostate(IntelliScore) EPI test in men presenting for initial Biopsy with a PSA 2-10 ng/mL. Prostate Cancer Prostatic Dis. 2020, 23, 607-614, doi:10.103 8/s41391-020-0237-z.
11. Kretschmer, A.; Tutrone, R.; Alter, J.; Berg, E.; Fischer, C.; Kumar, S.; Torkler, P.; Tadigotla, V.; Donovan, M.; Sant, G.; et al. Pre-diagnosis urine exosomal RNA (ExoDx EPI score) is associated with post-prostatectomy pathology outcome. World J. Urol. 2022, 40, 983-989, doi:10.1007/s00345-022-03937-0.
12. Li, В.; Liu, C.; Pan, W.; Shen, J.; Guo, J.; Luo, Т.; Feng, J.; Situ, В.; An, Т.; Zhang, Y.; et al. Facile fluorescent aptasensor using aggregation-induced emission luminogens for exosomal proteins profiling towards liquid biopsy. Biosens. Bioelectron. 2020, 168, doi:10.1016/j.bios.2020.112520.
13. Almasi, F.; Gargari, S.L.M.; Bitaraf, F.; Rasoulinejad, S. Development of a single stranded DNA aptamer as a molecular probe for LNCap cells using cell-SELEX. AvicennaJ. Med. Biotechnol. 2016, 8.
14. Jin, D.; Yang, F.; Zhang, Y.; Liu, L.; Zhou, Y.; Wang, F.; Zhang, G.J. ExoAPP: Exosome-Oriented, Aptamer Nanoprobe-Enabled Surface Proteins Profiling and Detection. Anal. Chem. 2018, 90, doi:10.1021/acs.analchem.8b03959.
15. Yang, D.K.; Chen, L.C.; Lee, M.Y.; Hsu, C.H.; Chen, C.S. Selection of aptamers for fluorescent detection of alpha-methylacyl-CoA racemase by single-bead SELEX. Biosens. Bioelectron. 2014, 62, doi:10.1016/j.bios.2014.06.027.
16. Slyusarenko, M.; Nikiforova, N.; Sidina, E.; Nazarova, I.; Egorov, V.; Garmay, Y.; Merdalimova, A.; Yevlampieva, N.; Gorin, D.; Malek, A. Formation and Evaluation of a Two-Phase Polymer System in Human Plasma as a Method for Extracellular Nanovesicle Isolation. Polymers (Basel). 2021, 13, 458, doi:10.3390/polym13030458.
17. Киселев, В.И.; Друх, В.М.; Кузнецов, И.Н.; Муйжнек, Е.Л. Андрианова, Е.А. Андреева, Ю.Ю.; Аллина, Д.О.; Лоран, О.Б.; Франк, Г.А. Морфологические изменения в ткани предстательной железы у пациентов с простатической интраэпителиальной неоплазией в процессе химиопрофилактики с помощью новой фармацевтической композиции дииндолилметана. Экспериментальная и клиническая урология 2015, 4, 54-58.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ И ДОБРОКАЧЕСТВЕННОЙ ГИПЕРПЛАЗИЕЙ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ | 2016 |
|
RU2646790C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ И ДОБРОКАЧЕСТВЕННОЙ ГИПЕРПЛАЗИИ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ | 2016 |
|
RU2647433C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ НА ОСНОВЕ АНАЛИЗА МИКРОРНК ПЛАЗМЫ КРОВИ | 2016 |
|
RU2618409C1 |
| СПОСОБ ВЫДЕЛЕНИЯ ЭКЗОСОМ ИЗ ПЛАЗМЫ КРОВИ | 2020 |
|
RU2741638C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ЦЕРВИКАЛЬНЫХ ДИСПЛАЗИЙ | 2021 |
|
RU2788860C1 |
| СПОСОБ ДИАГНОСТИКИ КОЛОРЕКТАЛЬНОГО РАКА | 2021 |
|
RU2772203C1 |
| Способ удаления внеклеточных нано-везикул из плазмы крови с помощью ковалентно иммобилизированных ДНК-аптамеров | 2022 |
|
RU2806434C1 |
| СПОСОБ ДИАГНОСТИКИ И МОНИТОРИНГА ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ С ИСПОЛЬЗОВАНИЕМ ЭКЗОСОМ КРОВИ | 2014 |
|
RU2571507C1 |
| СПОСОБ ВЫДЕЛЕНИЯ И АНАЛИЗА ЭКЗОСОМ | 2022 |
|
RU2788198C1 |
| СПОСОБ ДИАГНОСТИКИ ЛИМФОМЫ ХОДЖКИНА | 2021 |
|
RU2782326C1 |
Изобретение относится к медицине, а именно к медицинской диагностике, и может быть использовано для определения риска злокачественной трансформации клеток предстательной железы. Из плазмы крови выделяют простат-специфическую фракцию внеклеточных нановезикул (прВНВ). Проводят полуколичественный анализ концентраций mir-205-5p и mir-375-3р в материале выделенных прВНВ методом обратной транскрипции и полимеразной цепной реакции. Рассчитывают соотношение относительных концентраций mir-205-5p и mir-375-3р по формуле прВНВ-205/375=Ct(205)/Ct(375). При значении показателя прВНВ-205/375<1 определяют риск злокачественной трансформации клеток предстательной железы. При значении прВНВ-205/375>1 определяют отсутствие риска. Способ обеспечивает эффективное определение риска злокачественной трансформации клеток предстательной железы путем полуколичественного анализа mir-205-5p и mir-375-3р в материале прВНВ плазмы. 1 з.п. ф-лы, 3 ил., 1 табл., 3 пр.
1. Способ определения риска злокачественной трансформации клеток предстательной железы, основанный на последовательных процедурах выделения внеклеточных нановезикул (ВНВ) плазмы крови, выделения простат-специфической фракции ВНВ и полуколичественного анализа концентраций маркерных молекул микроРНК в материале выделенных ВНВ методом обратной транскрипции и полимеразной цепной реакции, включающего определение значений пороговых циклов (Ct) для двух молекул микроРНК: mir-205-5p и mir-375-3р и расчет соотношения относительных концентраций mir-205-5p и mir-375-3р по формуле
прВНВ-205/375=Ct(205)/Ct(375),
где Ct(205) - значение порогового цикла mir-205-5p,
Ct(375) - значение порогового цикла mir-375-3р,
и при значении полученного показателя прВНВ-205/375 < 1 определяют риск злокачественной трансформации клеток предстательной железы, при значении прВНВ-205/375 > 1 определяют отсутствие риска злокачественной трансформации клеток предстательной железы.
2. Способ по п. 1, отличающийся тем, что для выделения простат-специфической фракции ВНВ используют супер-парамагнитные микрочастицы (СПМЧ), функционализированные ДНК-аптамерами, которые связывают молекулы PSMA и AMACR на поверхности ВНВ, секретируемых клетками предстательной железы.
| ЭКЗОСОМАЛЬНЫЕ БИОМАРКЕРЫ | 2015 |
|
RU2712223C2 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ И ДОБРОКАЧЕСТВЕННОЙ ГИПЕРПЛАЗИИ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ | 2016 |
|
RU2647433C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ И ДОБРОКАЧЕСТВЕННОЙ ГИПЕРПЛАЗИЕЙ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ | 2016 |
|
RU2646790C1 |
| WO 2014193999 A2, 04.12.2014 | |||
| ZABEGINA L | |||
| et al | |||
| A New Approach for Prostate Cancer Diagnosis by miRNA Profiling of Prostate-Derived Plasma Small Extracellular Vesicles | |||
| Cells | |||
| Способ регенерирования сульфо-кислот, употребленных при гидролизе жиров | 1924 |
|
SU2021A1 |
Авторы
Даты
2023-11-01—Публикация
2022-11-16—Подача