Изобретение относится к медицине, а именно к препаратам для профилактики туберкулеза.
В настоящее время одной из основных причин смерти от инфекционных и паразитарных заболеваний является туберкулез [Татьков С.И., Дейнеко Е.В., Фурман Д.П. Перспективы создания противотуберкулезных вакцин нового поколения // Вавиловский Журнал Генетики и Селекции. 2011. Vol. 15, №11]. По данным Всемирной организации здравоохранения (ВОЗ) туберкулезом ежегодно заболевает в мире около 8 млн. человек, и около 3 млн. заболевших погибает. При этом по данным ФГБУ «ЦНИИОИЗ» Минздрава России в 2013 году в Российской Федерации по официальной статистике заболеваемость туберкулезом составила 63 случая на 100 тыс. населения, а смертность - 11,3 случаев на 100 тыс. населения [Hoang Т. et al. ESAT-6 (EsxA) and ТВ10.4 (EsxH) Based Vaccines for Pre- and Post-Exposure Tuberculosis Vaccination // PLoSONE / ed. Izzo A.A. 2013. Vol. 8, №12. P. e80579].
Возбудителем туберкулеза является патоген Mycobacterium tuberculosis (M. tuberculosis), реже - родственные ему виды М. bovis и М. africanum. Основным резервуаром и источником аэрогенной туберкулезной инфекции является бациллярный больной, выделяющий большое количество микобактерий с мокротой или слюной. Кроме того, заражение может происходить алиментарным путем - через употребление молока и молочнокислых продуктов от коров, пораженных М. bovis, или яиц от кур, инфицированных М. avium. В результате аэрогенного заражения туберкулезный процесс чаще возникает в органах дыхания, при алиментарном инфицировании могут поражаться почки, легкие, кости и суставы, периферические лимфоузлы, мочеполовые органы, глаза, центральная нервная система.
В зависимости от основных клинических проявлений различают легочную и нелегочные формы туберкулеза. Тем не менее, туберкулез легких остается наиболее распространенной и опасной формой. Без лечения более половины случаев в течение 5 лет заканчиваются смертью [Iem V. et al. Resistance of Mycobacterium tuberculosis to antibiotics in Lao PDR: first multicentric study conducted in 3 hospitals // BMC Infect. Dis. 2013. Vol. 13, №1. P. 275].
Если заболевание вызвано чувствительными к противотуберкулезным средствам штаммами микобактерий, правильно назначенное лечение практически всегда дает эффект. Однако в последние годы широкое распространение получили устойчивые к противотуберкулезным средствам штаммы микобактерий, лечение вызванного ими туберкулеза проходит крайне сложно. В связи с этим важным аспектом в борьбе с данным заболеванием является предупреждение развития заболевания, вакцинация.
В настоящее время для предупреждения туберкулеза широко используется вакцинирование новорожденных детей живой вакциной БЦЖ.
Вакцинация БЦЖ в детском возрасте эффективна в отношении заболевания милиарной формой туберкулеза легких и туберкулезным менингитом. Однако в последние годы усиливаются сомнения относительно ее универсальности и эффективности. Необходимо отметить, что развитие туберкулеза на сегодняшний день отмечается не только у некачественно вакцинированных или невакцинированных детей, но и у лиц, которым вакцина БЦЖ была введена правильно и своевременно [Стукова М.А. et al. Профилактика туберкулеза: современные подходы к разработке противотуберкулезных вакцин // Актуальные Вопросы Фтизиатрии Вестник РАМН. 2012. №11].
БЦЖ, подобно другим живым вакцинам, способна вызывать отрицательные побочные эффекты. Осложнения при вакцинации БЦЖ наблюдаются, в частности, у детей, инфицированных ВИЧ, еще до рождения. Принципиальным недостатком вакцины БЦЖ является постепенное (в течение 3-7 лет) снижение поствакцинального иммунитета. Согласно результатам контролируемых исследований, это приводит к практически полному отсутствию защитного эффекта уже через 10 лет после вакцинации [Russell D.G., Barry С.Е., Flynn J.L. Tuberculosis: what we don't know can, and does, hurt us // Science. 2010. Vol. 328, №5980. P. 852-856]. В то же время использование БЦЖ для ревакцинации, направленной на поддержание противотуберкулезного иммунитета, по данным экспертов ВОЗ, признается неэффективным [World Health Organization. BCG vaccine. WHO position paper //  Sect.
Sect.  Nations Wkly. Epidemiol. Rec. Health Sect. Secr. Leag. Nations. 2004. Vol. 79, №4. P. 27-38].
Nations Wkly. Epidemiol. Rec. Health Sect. Secr. Leag. Nations. 2004. Vol. 79, №4. P. 27-38].
Таким образом, к настоящему времени назрела необходимость разработки вакцин нового поколения как наиболее эффективных иммунопрофилактических средств борьбы с туберкулезом, в первую очередь с его легочной формой.
Одним из направлений разработки новых противотуберкулезных вакцин является создание субъединичных вакцин на основе рекомбинантных белков [Татьков С.И., Дейнеко Е.В., Фурман Д.П. Перспективы создания противотуберкулезных вакцин нового поколения // Вавиловский Журнал Генетики И Селекции. 2011. Vol. 15, №1].
Субъединичными называют вакцины, которые содержат только отдельные компоненты патогенного микроорганизма, содержащие эпитопы антигенов, активно распознаваемые иммунной системой хозяина. Достоинства субъединичных вакцин заключаются в том, что препарат, содержащий очищенный иммуногенный белок, стабилен и безопасен, его физико-химические свойства известны, в нем отсутствуют дополнительные белки и нуклеиновые кислоты, которые могли бы вызвать нежелательные эффекты в вакцинируемом организме [Калюкина А.С. Изучение возможности применения рекомбинантного белка HSP70 туберкулезной микобактерий в профилактике туберкулеза. Москва: Московская Медицинская Академия им. И.М. Сеченова, 2007]. Изучение генома М. tuberculosis штамма H37Rv показало, что он содержит 3995 открытых рамок считывания, но лишь для 52% из них удалось предсказать функциональную активность. Анализ протеома позволил выявить не менее 1800 клеточных и 800 секретируемых белков [Sharma А.K., Khuller G.K. Recombinant mycobacterial proteins future directions to improve protective efficacy // Indian J. Exp. Biol. 2001. Vol. 39, №12. P. 1214-1219].
К началу 2000 г. было получено несколько вариантов субъединичных вакцин, однако их протективный эффект при испытаниях оказался в ряде случаев непредсказуемым и сильно варьировался по эффективности [Sharma А.К., Khuller G.K. Recombinant mycobacterial proteins future directions to improve protective efficacy // Indian J. Exp. Biol. 2001. Vol. 39, №12. P. 1214-1219].
Наиболее широко используемой и близкой по достигаемому эффекту к заявляемому изобретению является вакцина туберкулезная для щадящей первичной иммунизации (БЦЖ-М) (Vaccinum tuberculosis (BCG-M) cryode-siccatum), содержащая в 1 дозе 0,025 мг микробных клеток БЦЖ живые микобактерий вакцинного штамма БЦЖ-1 и вспомогательные вещества, в частности, стабилизатор-натрия глутамата моногидрат в дозе 0,15 мг [http://www.rlsnet.ru/tn_index_id_8621.htm]. Препарат выпускается в комплекте с растворителем - 0,9% раствором натрия хлорида для инъекций, которым 1 доза вакцины разводится до объема 0,1 мл.
Недостатком вакцины наличие негативных побочных эффектов (к числу осложнений относятся "холодные" абсцессы, лимфадениты, остеомиелиты, хориоретиниты, сахарный диабет, а также возможность возникновения генерализованной БЦЖ-инфекции, приводящей к смерти [http://homeoint.ru/glossary/b001.htm].
Целью, решаемой в результате использования настоящего изобретения, являлось создание расширение спектра противотуберкулезных вакцин с целью получения более безопасной вакцины с эффективностью, не уступающей эффективности БЦЖ.
Технический результат достигался за счет введения в противотуберкулезную вакцину, содержащую активное начало и вспомогательные вещества, в качестве активного начала белков Tb10.4 М. tuberculosis (далее белок Tb10.4) и Ag85B М. tuberculosis (далее белок Ag85B) в соотношении от 2:1 до 1:2. при следующем соотношении ингредиентов, % масс:
Оптимальные результаты достигаются в том случае, когда белок Tb10.4 М. Tuberculosis и белок Ag85B M. tuberculosis содержатся в соотношении 1:1. В качестве вспомогательных веществ вакцина содержит белок на основе FHC Salmonella typhimurium (ФСТ) в концентрации 0,001-0,003% масс. и стабилизаторы, такие как маннитол, сукцинат натрия и твин-20. Последние могут вводится в вакцину как индивидуально, так и в виде смеси.
Композиция вакцины достигается смешением порошков ингредиентов в выбранных пропорциях с последующим их растворением водой в заданных объемах.
Использования белка на основе FliC Salmonella typhimurium в качестве компонента вакцины, нивелирует негативные эффекты и риски от использования живой, либо инактивированной вакцины, обеспечивая расширение спектра противотуберкулезных вакцин, а стабилизатор обеспечивает хранение вакцины в течение по крайней мере 6 месяцев при температуре +4C.
Заявляемая вакцина обладает эффективностью, превышающей эффективность аналогов при минимизации негативных побочных эффектов. Особенно эффективно использование заявляемой вакцины при противопоказаниях к применению аналогов, либо нежелании использовать аналоги ввиду их вышеописанных недостатков.
Указанные свойства предложенной вакцины подтверждены примерами.
Пример 1. Смещением ингредиентов были получены композиции 5 вакцин состав которых приведен в таблице 1 (вода - остальное).
Иммунизация субстанцией рекомбинантных белков
Осуществляли двукратную иммунизацию субстанцией рекомбинантных белков ТВ10.4 и Ag85B (интраназально, для композиции 1 также внутримышечно, по 6 мышей) с интервалом в 2 недели. Использовали дозу 50 мкг суммарного белка на мышь, вводили в объеме 100 мкл внутримышечно или 10 мкл - интраназально, по 5 мкл в каждую ноздрю. Для доведения требуемого объема использовали физиологический раствор.
Заражение осуществляли через 10 дней после последней вакцинации. Для моделирования туберкулеза использован стандартный тест-штамм М. tuberculosis Erdman. Микобактериальная суспензия для заражения мышей приготовлена ex tempore из трехнедельного штамма, культивируемого на среде Левенштейна-Йенсена. Заражающая доза - 106 колониеобразующих единиц (КОЕ)/мышь в 0,2 мл физраствора, путь введения - в латеральную хвостовую вену.
Мыши выведены из опыта через шесть недель после заражения путем эвтаназии в CO2-камере с последующим гильотинированием в соответствии с Методическими рекомендациями (см. п. 3).
Коэффициенты массы легких (КМЛ) и селезенки (KMC) рассчитывали по формуле, в условных единицах:

Индекс поражения легких (ИПЛ) устанавливали по совокупности экссудативных и продуктивных изменений в условных единицах - баллах.
Экссудативные изменения:
- легкие воздушны - 0
- единичные безвоздушные очаги - 0,25
- легкие безвоздушны на 1/2 - 0,5
- легкие безвоздушны на 2/3 - 0,75
- легкие безвоздушны на всем протяжении - 1,0
Продуктивные очаги:
- единичные субмилиарные очаги - 0,5
- многочисленные (не более 20) - 1,0
- многочисленные субмилиарные (более 20) - 1,5
- единичные милиарные - 1,75
- многочисленные сливающиеся субмилиарные и единичные милиарные - 2,0
- многочисленные милиарные (не более 10) - 2,25
- многочисленные милиарные, сливающиеся - 2,75
- появление мелких казеозных некротических фокусов - 3,0
- обширный казеоз - 4,0
- сплошное поражение легких - 5,0
Определяли показатели тяжести течения туберкулезной инфекции:
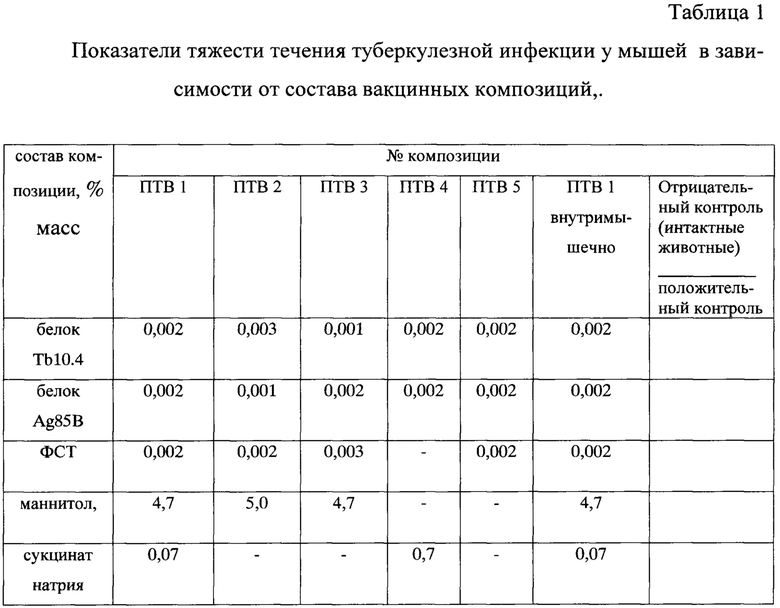
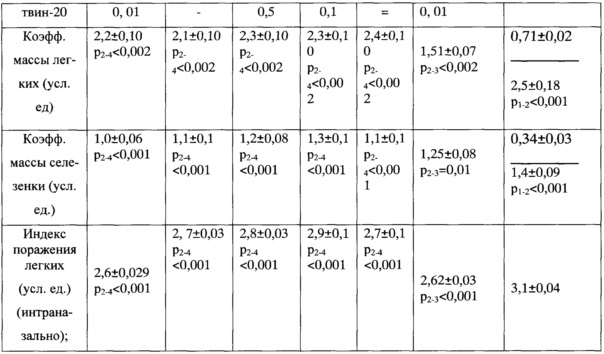
Результаты, приведенные на диаграммах, показывают, что кандидатная вакцина против туберкулеза на основе рекомбинантных белков ТВ10.4 и Ag85B M. tuberculosis проявляет протективную активность, причем как при внутримышечном, так и при интраназальном введении. Различия между группами достоверные.
Таким образом, продемонстрирована высокая эффективность противотуберкулезных вакцин на основе белка Tb10.4 M. tuberculosis, которая оказалась больше, чем таковая БЦЖ, в профилактической модели на лабораторных животных, по всем изученным показателям.
Также продемонстрирована безопасность предлагаемой вакцины: животные соответствующих групп выжили и были выведены из эксперимента принудительно, в процессе испытаний побочные эффекты не наблюдали.
| название | год | авторы | номер документа |
|---|---|---|---|
| Гибридный белок, ДНК, генетическая конструкция, рекомбинантная клетка, вакцина на основе гибридного белка для профилактики и лечения туберкулеза (варианты) | 2015 |
|
RU2615440C2 |
| Рекомбинантный штамм вируса гриппа A/PR8-NS124-TB10.4-2A-HspX и способ специфической профилактики туберкулеза легких с использованием вакцины мукозального применения на его основе | 2019 |
|
RU2726106C1 |
| ПОЛИАНТИГЕННАЯ ВАКЦИНА ДЛЯ ПРОФИЛАКТИКИ И ВСПОМОГАТЕЛЬНОГО ЛЕЧЕНИЯ ТУБЕРКУЛЕЗА | 2019 |
|
RU2724896C1 |
| РЕКОМБИНАНТНЫЕ ШТАММЫ ВИРУСА ГРИППА, ЭКСПРЕССИРУЮЩИЕ МИКОБАКТЕРИАЛЬНЫЙ ПРОТЕКТИВНЫЙ АНТИГЕН ESAT-6, И ИХ ИСПОЛЬЗОВАНИЕ ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ТУБЕРКУЛЕЗА | 2005 |
|
RU2318872C2 |
| ШТАММ Mycobacterium tuberculosis BN ДЛЯ МОДЕЛИРОВАНИЯ ЛАТЕНТНОЙ ТУБЕРКУЛЕЗНОЙ ИНФЕКЦИИ | 2021 |
|
RU2760751C1 |
| ВАКЦИНА РЕКОМБИНАНТНАЯ ПРОТИВОТУБЕРКУЛЕЗНАЯ И АДЪЮВАНТ ДЛЯ НЕЕ | 2017 |
|
RU2665817C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИММУНОГЕННОЙ КОМПОЗИЦИИ НА ОСНОВЕ ГИБРИДНОГО БЕЛКА Ag85A-DBD И ДЕКСТРАНА, РЕКОМБИНАНТНАЯ ПЛАЗМИДА pAg85A-DBD, ШТАММ Escherichia coli [pREP4, pAg85A-DBD], ХИМЕРНЫЙ БЕЛОК Ag85A-DBD | 2013 |
|
RU2520078C1 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДА pAg85A-CBD, ШТАММ Escherichia coli [pREP4, pAg85A-CBD], ХИМЕРНЫЙ БЕЛОК Ag85A-CBD И ИХ ПРИМЕНЕНИЕ | 2010 |
|
RU2429292C1 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДА, ШТАММ Escherichia coli, ХИМЕРНЫЙ БЕЛОК И ИХ ПРИМЕНЕНИЕ | 2010 |
|
RU2422524C1 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДА, ШТАММ Escherichia coli, ХИМЕРНЫЙ БЕЛОК И ИХ ПРИМЕНЕНИЕ | 2010 |
|
RU2422525C1 |
Изобретение относится к медицине, а именно к иммунологии, и может быть использовано для получения вакцины против туберкулеза. Вакцина содержит активное начало на основе микобактерий туберкулеза и вспомогательных веществ, при этом в качестве активного начала она содержит белок Tb10.4 M. tuberculosis и Ag85B M. tuberculosis в соотношении от 1:2 до 2:1 при следующем соотношении ингредиентов, мас.%: белок Tb10.4 M. tuberculosis 0,001-0,003; Ag85B M. tuberculosis 0,001-0,003; гибридный белок на основе FliC Salmonella typhimurium в концентрации 0,001-0,0030; вспомогательные вещества 4,5-5,5; вода - остальное. Использование в составе вакцины гибридного белка на основе FliC Salmonella typhimurium позволяет нивелировать побочные эффекты от использования живой вакцины, при этом полученная вакцина проявляет протективную активность как при внутримышечном, так и при интраназальном введении. 3 з.п. ф-лы, 1 пр., 1 табл.
1. Вакцина против туберкулеза, содержащая активное начало на основе микобактерий туберкулеза и вспомогательных веществ, содержащих воду для инъекций, отличающаяся тем, что в качестве активного начала она содержит белок Tb10.4 M. tuberculosis и Ag85B M. tuberculosis в соотношении от 1:2 до 2:1 при следующем соотношении ингредиентов, мас.%: белок Tb10.4 M.tuberculosis 0,001-0,003; Ag85B M.tuberculosis 0,001-0,003; гибридный белок на основе FliC Salmonella typhimurium в концентрации 0,001-0,0030; вспомогательные вещества 4,5-5,5; вода - остальное.
2. Вакцина против туберкулеза по п. 1, отличающаяся тем, что белок Tb10.4 М. tuberculosis и белок Ag85B M. tuberculosis содержатся в соотношении 1:1.
3. Вакцина против туберкулеза по п. 1, отличающаяся тем, что в качестве вспомогательного вещества она содержит стабилизаторы.
4. Вакцина против туберкулеза по п. 1, отличающаяся тем, что в качестве стабилизатора она содержит по крайне мере одно вещество, выбранное из группы, в которую входит маннитол, сукцинат натрия и твин-20.
| WO 2010006607 A1, 21.01.2010 | |||
| КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ СМЕСЬ ЭКСТРАКТОВ РАСТЕНИЙ ИЛИ СМЕСЬ МОЛЕКУЛ, СОДЕРЖАЩИХСЯ В УКАЗАННЫХ РАСТЕНИЯХ, И ПРИМЕНЕНИЕ ДЛЯ КОНТРОЛИРОВАНИЯ МЕТАБОЛИЗМА УГЛЕВОДОВ И/ИЛИ ЛИПИДОВ | 2015 |
|
RU2712625C2 |
| ЕА 201001820 А1, 30.08.2011 | |||
| ШТАММ БАКТЕРИЙ Escherichia coli - ПРОДУЦЕНТ РЕКОМБИНАНТНОГО ФЛАГЕЛЛИНА | 2012 |
|
RU2524133C2 |
| ГРЕБЕНЮК А.Н | |||
| и др | |||
| Получение различных вариантов рекомбинантного флагеллина и оценка их радиозащитной эффективности // Вестник Российской военно-медицинской академии, 2013, 3 (43), стр.75-80, рис.2. | |||
Авторы
Даты
2018-03-19—Публикация
2017-03-15—Подача