Область техники
Описаны способы и системы для выполнения разделения газов с использованием адсорбирующих материалов.
Уровень техники
Удаление загрязняющих веществ или примесей из газофазного потока обычно осуществляют при переработке нефти и природного газа. Например, большинство потоков природного газа содержат по меньшей мере некоторое количество СО2 помимо требуемого СН4. Дополнительно, во многих способах переработки нефти вырабатывают выходящий поток газовой фазы, который содержит множество соединений, таких как СН4 и СО2, которые являются газами при стандартных температуре и давлении. Выполнение разделения газофазного потока, содержащего СН4, может обеспечить удаление примеси и/или разбавителя, такого как CO2 или N2, при регулируемых условиях. Такую примесь или разбавитель затем можно направить в другие процессы, например направить на другое применение, в котором уменьшают утечку парниковых газов в окружающую среду.
В опубликованной заявке на патент US 2008/0282885 описаны системы и способы удаления CO2, N2 или H2S с использованием способа короткоцикловой адсорбции. Одним типом адсорбента, который можно использовать в способе короткоцикловой адсорбции, является цеолит с 8-членными кольцами, такой как цеолит типа DDR.
В патенте US 7255725 описана пористая неорганическая мембрана, содержащая углерод, и способ применения такой мембраны. Пористую неорганическую мембрану, не содержащую углерод (такую как цеолит), обрабатывают сырьем углеводородного типа при температурных условиях и в течение времени, которые подходят для осаждения углерода на неорганическую мембрану с помощью химической реакции. Углеродсодержащую мембрану затем поддерживают при температуре выше температуры осаждения в течение интервала времени до выполнения мембранного разделения. Описанная мембрана подходит для отделения неконденсируемых газов, таких как CO2, CH4 или Н2, от углеводородного сырья.
В международной публикации WO 2006/017557 описаны мембраны для высокоселективных разделений. После обжига мембрану типа молекулярного сита, такого как SAPO-34, обрабатывают модифицирующим агентом, таким как аммиак. Такая обработанная мембрана подходит для улучшения мембранного отделения СО2 от СН4), в котором понижают количество СН4 в пермеате, пошедшем через мембрану. Описаны и другие модифицирующие агенты, такие как силаны и/или амины, которые реагируют с кислыми центрами цеолитов, и полярные соединения, такие как этанол.
Краткое описание изобретения
В одном аспекте предложен способ выполнения разделения газов. Способ включает приведение адсорбента или мембраны, содержащих цеолит с 8-членными кольцами, или другой микропористый материал с 8-членными кольцами, в контакт с барьерным соединением при условиях, эффективных для селективации адсорбента или мембраны, причем барьерное соединение имеет минимальный размер, составляющий по меньшей мере примерно 4,05 Ангстрем, и максимальный размер, составляющий примерно 25 Ангстрем или менее; приведение селективированного адсорбента или мембраны в контакт с входящим потоком газа, содержащим первый компонент и второй компонент, с образованием первого потока газа, обогащенного первым компонентом по отношению к входящему потоку газа; и сбор второго потока газа, обогащенного вторым компонентом по отношению к входящему потоку газа.
В другом аспекте предложен способ выполнения разделения газов в устройстве короткоцикловой адсорбции. Способ включает приведение адсорбента, содержащего цеолит с 8-членными кольцами, или другой микропористый материал с 8-членными кольцами, в контакт с барьерным соединением в устройстве короткоцикловой адсорбции при условиях, эффективных для селективации адсорбента, причем цеолит с 8-членными кольцами представляет собой цеолит типа DDR, ZSM-58, Sigma-1 или их сочетание; приведение селективированного адсорбента в контакт с входящим потоком газа, содержащим первый компонент и второй компонент, с образованием выходящего потока газа, обогащенного первым компонентом по отношению к входящему потоку газа, при этом селективированный адсорбент адсорбирует по меньшей мере часть второго компонента в течение приведения в контакт; десорбцию по меньшей мере части адсорбированного второго компонента с образованием десорбированной части второго компонента; и сбор газового потока, содержащего по меньшей мере часть десорбированной второго части компонента, при этом газовый поток обогащен вторым компонентом по отношению к входящему потоку газа.
В еще одном аспекте предложен способ выполнения разделения газов в устройстве короткоцикловой адсорбции. Способ включает приведение адсорбента, содержащего микропористый материал, в контакт с барьерным соединением в устройстве короткоцикловой адсорбции при условиях, эффективных для селективации адсорбента, причем микропористый материал имеет поры, характеризующиеся первым размером наибольшей твердой сферы, которая может диффундировать вдоль любого направления в порах, а барьерное соединение имеет второй размер, представляющий собой минимальный размер соединения, причем второй размер больше первого размера на 10-60%; приведение селективированного адсорбента в контакт с входящим потоком газа, содержащим первый компонент и второй компонент, с образованием выходящего потока газа, обогащенного первым компонентом по отношению к входящему потоку газа, при этом селективированный адсорбент адсорбирует по меньшей мере часть второго компонента в течение приведения в контакт; десорбцию по меньшей мере части адсорбированного второго компонента с образованием десорбированной части второго компонента; и сбор газового потока, содержащего по меньшей мере часть десорбированной части второго компонента, при этом газовый поток обогащен вторым компонентом по отношению к входящему потоку газа.
Краткое описание чертежей
На Фиг. 1 и Фиг. 2 показаны результаты хроматографии с нулевой длиной для диффузии газов при различных условиях.
На Фиг. 3 показаны изотермы адсорбции СО2 при различных условиях.
На Фиг. 4 и Фиг. 5 показаны результаты хроматографии с нулевой длиной для диффузии газов при различных условиях.
На Фиг. 6 показаны изотермы адсорбции СО2 при различных условиях.
На Фиг. 7 показана зависимость от времени рабочей производительности для селективно пассивированного адсорбента по сравнению с равновесной адсорбцией для непассивированного адсорбента.
На Фиг. 8 показаны коэффициенты диффузии при 30°С для различных алканов.
Подробное описание воплощений изобретения
Обзор
В различных аспектах предложены способы и системы для улучшения разделения газофазных потоков с использованием адсорбента, такого как кинетически селективный адсорбент. В данном обсуждении термин «кинетически селективные адсорбенты» относится к адсорбентам с различными коэффициентами диффузии в отношении скорости переноса по меньшей мере первого соединения относительно по меньшей мере второго соединения. Примером подходящего адсорбента является цеолитовый адсорбент с 8-членными кольцами, такой как цеолит типа DDR. Подходящие газофазные потоки могут содержать по меньшей мере один углеводород, такой как метан или (газообразный) углеводород, содержащий по меньшей мере одну насыщенную углерод-углеродную связь, и по меньшей мере один дополнительный компонент, такой как СО2 или N2. Не связывая себя какой-либо конкретной теорией, полагают, что селективность адсорбента можно улучшить с помощью барьерных соединений, внедренных в (или по меньшей мере блокирующих) пористую структуру адсорбирующего материала. Поступая в (блокируя) пористую структуру, барьерные соединения могут влиять на эффективную площадь входного отверстия пор и/или объем пор, доступный для поступления потенциального адсорбируемого вещества в адсорбирующий материал. Таким образом, даже если два потенциальных адсорбируемых вещества могут иметь размеры, подходящие для адсорбции в сети пор адсорбента, присутствие барьерных соединений может изменять относительную способность различных потенциальных адсорбируемых веществ к поступлению в поры и/или к продвижению внутри пор адсорбента. В некоторых случаях барьерные соединения также могут вносить вклад в образование слоя на поверхности адсорбента. Такой возможный слой барьерных соединений также может изменять способность потенциальных адсорбируемых веществ поступать в (блокировать) поры адсорбирующего материала. Также следует отметить, что хотя приведенное выше описание относится к модифицированию кинетики поступления соединений в адсорбент, аналогичные способы можно использовать для модификации кинетики поступления соединений в мембрану, например, основанную на цеолитовой структуре с 8-членными кольцами.
В общем случае, подходящие адсорбенты для разделения газофазных потоков могут включать микропористые материалы (включая цеолиты), такие как материалы SAPO или другие типы структур, включающих атомы каркаса, отличные от Si и Al в каркасной структуре цеолитового типа. Дополнительно, микропористые материалы (включая цеолиты) с каркасами, имеющими другие размеры колец, могут образовывать подходящие адсорбенты, такие как цеолиты или другие микропористые материалы с 10-членными кольцевыми структурами, 12-членными кольцевыми структурами или структурами с другим числом атомов в кольце.
Предпочтительно, барьерные соединения могут изменять кинетику поступления молекулярных соединений в поры адсорбента (или мембраны), при этом оказывая пониженное или минимальное воздействие на адсорбцию (и/или перенос через мембрану) других целевых молекулярных соединений. Это может обеспечить поддержание скорости адсорбции требуемого адсорбируемого соединения, при этом улучшая селективность по отношению к адсорбции для адсорбции другого соединения. В других воплощениях кинетику поступления как требуемого адсорбируемого соединения, так и другого соединения (или соединений) можно изменять с помощью барьерных соединений с тем, что изменение кинетики для требуемого адсорбируемого соединения меньше, чем изменение кинетики для другого соединения (соединений), так что можно выгодно улучшить селективность преимущественной адсорбции требуемого адсорбируемого соединения. Например, СН4 и С2Н6 являются примерами соединений, на кинетику адсорбции которых может влиять присутствие определенных барьерных соединений. N2 и CO2 являются примерами соединений, для которых присутствие определенных барьерных соединений оказывают пониженное и/или минимальное воздействие на кинетику адсорбции. Таким образом, N2 и CO2 представляют собой потенциальные требуемые адсорбируемые соединения.
В способах короткоцикловой адсорбции и мембранного разделения селективация адсорбирующего материала с использованием барьерных соединений может улучшить селективность адсорбента для преимущественной адсорбции первого соединения относительно второго соединения. Например, это может обеспечить возможность повышения выхода требуемого углеводорода (такого как СН4 или С2Н6) в потоке продукта, а также повышения массового процентного содержания требуемого углеводорода по отношению к входящему потоку газа. Этого можно достичь путем преимущественного уменьшения кинетики адсорбции требуемого углеводорода относительно кинетики адсорбции одного или более других компонентов входящего потока газа (таких как N2 или СО2). Барьерные соединения, внедряемые в (блокирующие) сеть пор и/или образующие барьерный слой для улучшения разделения, можно использовать, например, в устройстве короткоцикловой адсорбции для выполнения газофазных разделений. Дополнительно, уменьшая скорость, при которой требуемый углеводород диффундирует в адсорбент, можно ослабить требования к продолжительности цикла для адсорбирующего слоя/материала. Это может обеспечить возможность выполнения циклов адсорбции и регенерации, которые могут быть более совместимы с интервалами времени, требуемыми для функционирования крупномасштабных клапанов и структурированных слоев адсорбента. При применении мембранного разделения присутствие барьерного соединения может увеличить относительную вероятность поступления компонента (такого как CO2 или N2) в мембрану и его диффузии через мембрану по сравнению с вероятностью поступления другого компонента (такого как СН4) в мембрану и его диффузии через мембрану.
Предпочтительно, барьерный слой не изменяет адсорбционную способность адсорбента (или требуемого проникающего компонента) в значительной степени. В предпочтительном воплощении присутствие барьерного слоя всего лишь уменьшает адсорбционную способность адсорбента на 40% или менее, например, менее чем на 20% или менее чем на 10%. Даже если адсорбционная способность может быть в некоторой степени снижена барьерным слоем, характеристика адсорбента может улучшиться из-за улучшений кинетической селективности.
Предпочтительно, барьерный слой можно образовать, используя соединение, которое медленно диффундирует через пористую структуру адсорбента. Это может обеспечить образование относительно стабильного слоя, который не требует частой регенерации или обновления. Путем образования барьерного слоя из медленно диффундирующего соединения, данный слой можно сконцентрировать в порах / среди пор вдали от центра адсорбента (то есть, в порах вблизи поверхности адсорбента). Наличие барьера, образованного в порах / среди пор вблизи/на поверхности адсорбента, может способствовать улучшению кинетической селективности путем немедленного блокирования или затруднения переноса и, следовательно, путем уменьшения кинетики адсорбции соединений, подлежащих кинетическому исключению из адсорбента. При температуре требуемого способа разделения коэффициент диффузии соединения, используемого для образования барьерного слоя, предпочтительно может составлять менее 10-15 м2/с, например менее 10-19 м2/с или менее 10-23 м2/с.
В некоторых предпочтительных воплощениях адсорбент может преимущественно адсорбировать второе соединение относительно первого соединения до (или без) применения барьерных соединений. В таких воплощениях применение барьерных соединений может дополнительно усилить селективность адсорбента в мембране или в способе короткоцикловой адсорбции. В других воплощениях барьерные соединения можно использовать для адсорбентов, которые иначе обладают небольшой адсорбционной селективностью для второго соединения относительно первого соединения или не обладают ею вообще. В таких других воплощениях применение барьерных соединений может привнести селективную адсорбцию в адсорбирующую систему.
В зависимости от воплощения блокирующее соединение можно ввести в адсорбент для образования барьерного слоя в различные моменты времени. Одним вариантом может быть введение блокирующего соединения после синтеза кристаллов адсорбента, но перед включением кристаллов в контактор или слоистую структуру. Другим вариантом может быть введение блокирующего соединения после образования адсорбирующего слоя, включающего кристаллы. Еще одним вариантом может быть введение блокирующего соединения после того как адсорбирующий слой, включающий кристаллы, использовали для создания контактора, такого как сосуд короткоцикловой адсорбции.
Удаление СО2 из потока, содержащего легкие углеводороды, может быть выгодным по ряду причин. Например, в потоке, используемом в качестве топлива для сгорания, СО2 может действовать как инертный разбавитель. Слишком большое количество CO2 в потоке топлива может подавлять реакцию горения. Природный газ для продажи в качестве топлива часто должен соответствовать техническим требованиям по максимальному количеству присутствующих разбавителей. В некоторых воплощениях количество инертных веществ, присутствующих в потоке природного газа, предпочтительно может составлять примерно 2 об.% или менее. Кроме того, любой CO2, который поступает в реакцию горения, может добавляться к парниковым газам, образующимся при реакции. Также может быть выгодным удалять N2 из содержащего метан потока (или другого потока, содержащего легкие углеводороды), так как N2 также может действовать как инертный разбавитель при горении. Помимо действия в качестве разбавителя в потоке топлива, высокие уровни CO2 и/или N2 могут увеличить сложность ожижения содержащего метан потока, такого как поток природного газа.
Способы разделения
Данное изобретение можно применять к мембранам, а также к способам короткоцикловой адсорбции. Мембраны можно образовать из адсорбирующих материалов. Например, в способах гидротермального синтеза можно получить цеолитовые мембраны. Цеолиты также можно внедрить в мембраны со смешанной матрицей. В способе мембранного разделения поток подаваемой смеси (обычно в газовой фазе) можно пропускать над одной стороной мембраны. Мембрана может селективно пропускать некоторые соединения к противоположной стороне мембраны, которая либо может находиться при пониженном давлении, либо может повергаться очистке. Соединение, преимущественно проходящее через мембрану, называют тяжелым компонентом, а соединение, преимущественно задерживаемое на стороне подачи, называют легким компонентом (независимо от их относительных молярных масс). Скорость переноса молекул через мембрану можно определить с помощью кинетики и равновесной адсорбции. Усиление кинетической селективности с помощью селективации может улучшить удерживание и, следовательно, извлечение, например, легкого компонента.
Все способы короткоцикловой адсорбции включают стадию адсорбции, на которой подаваемую смесь (обычно в газовой фазе) пропускают над адсорбентом, который преимущественно адсорбирует более легко адсорбируемый компонент по сравнению с менее легко адсорбируемым компонентом. Компонент может быть более легко адсорбируемым из-за кинетики или равновесных свойств адсорбента. Адсорбент обычно может быть заключен в контактор, который является частью установки короткоцикловой адсорбции. Контактор обычно может содержать сконструированный структурированный слой адсорбента или слой адсорбента, состоящий из частиц. Данный слой может содержать адсорбент и другие материалы, такие как другие адсорбенты, мезопористые наполняющие материалы и/или инертные материалы, используемые для уменьшения отклонений температуры, вызванных теплотой адсорбции и десорбции. Другие компоненты в установке короткоцикловой адсорбции могут включать (но не обязательно ограничиваются перечисленным) клапаны, трубы, баки и другие контакторы.
Способ регенерации адсорбента определяет тип способа короткоцикловой адсорбции. Способы адсорбции с перепадом давления (АПД) основаны на том факте, что газы под давлением стремятся быть адсорбированными внутри пористой структуры микропористых адсорбирующих материалов. Обычно чем выше давление, тем больше количество целевого газового компонента, которое будет адсорбировано. Когда давление понижают, адсорбированный целевой компонент обычно высвобождается или десорбируется. Способы АПД можно использовать для разделения газов из газовой смеси, так как различные газы стремятся заполнить микропористый или свободный объем адсорбента в различной степени, обусловленной либо равновесными, либо кинетическими свойствами адсорбента. Способы адсорбции с перепадом температуры (АПТ) также основаны на том факте, что газы под давлением стремятся быть адсорбированными внутри пористой структуры микропористых адсорбирующих материалов. Когда температуру адсорбента повышают, адсорбированный газ обычно высвобождается или десорбируется. Путем циклического изменения температуры адсорбирующих слоев способы АПТ можно использовать для разделения газов в смеси при использовании адсорбента, селективного для одного или более компонентов газовой смеси. В способах адсорбции с перепадом парциального давления (АППД) с вытеснением продувочным потоком адсорбент регенерируют продувочным потоком. В способах короткоцикловой адсорбции с частым циклом (ЧЦ) стадию адсорбции способа короткоцикловой адсорбции завершают за короткое время. Для кинетически селективных адсорбентов может быть предпочтительным использование способа короткоцикловой адсорбции с частым циклом. Если продолжительность цикла становится слишком длительной, кинетическая селективность может быть потеряна. Эти технологии короткоцикловой адсорбции можно выполнять по отдельности или в сочетании. Примерами способов, которые можно использовать в сочетании, являются АПДЧЦ (адсорбция с перепадом давления с частым циклом), АПТЧЦ (адсорбция с перепадом температуры с частым циклом), АПДТ (адсорбция с перепадом давления и температуры) и АППДТ (адсорбция с перепадом парциального давления и температуры). Селективацию можно использовать для улучшения характеристики всех способов короткоцикловой адсорбции.
Способы короткоцикловой адсорбции можно применять для удаления множества целевых газов из разнообразных газовых смесей. Используемый в данном документе термин «легкий компонент» относится к веществам или молекулярным компонентам, которые преимущественно не поглощаются адсорбентом на стадии адсорбции данного способа. Наоборот, используемый в данном документе термин «тяжелый компонент» относится к веществам или молекулярным компонентам, которые преимущественно поглощаются адсорбентом на стадии адсорбции данного способа.
Описанные в данном документе способы селективации могут обеспечить улучшение кинетически регулируемых способов короткоцикловой адсорбции и, например, могут увеличить извлечение легкого компонента. В кинетически регулируемых способах короткоцикловой адсорбции по меньшей мере часть (и предпочтительно большую часть) селективности можно придать, например, благодаря тому, что коэффициент диффузионного переноса в микропорах и свободный объем адсорбента для легких соединений меньше, чем для более тяжелых соединений. Также, в кинетически регулируемых способах короткоцикловой адсорбции с микропористыми адсорбентами, такими как цеолитовые адсорбенты с 8-членными кольцами, диффузионная селективность может быть обусловлена различиями диффузии в микропорах адсорбента и/или селективным диффузионным сопротивлением поверхности в кристаллах или частицах, которые составляют адсорбент. Кинетически регулируемые способы короткоцикловой адсорбции обычно противоположны равновесно регулируемым способам короткоцикловой адсорбции, в которых свойства равновесной адсорбции адсорбента регулируют селективность. Улучшение кинетической селективности может быть таким, что полное извлечение, например, введенного в способ легкого компонента, достигаемое в способе короткоцикловой адсорбции, может составлять более примерно 80 мол.%, например, более примерно 85 мол.%, более примерно 90 мол.% или более примерно 95 мол.%. Извлечение легкого компонента можно определить как средний по времени молярный расход легкого компонента в потоке продукта, деленный на средний по времени молярный расход легкого компонента в подаваемом потоке. Аналогично, извлечение тяжелого компонента можно определить как средний по времени молярный расход тяжелого компонента в потоке продукта, деленный на средний по времени молярный расход тяжелого компонента в подаваемом потоке.
Можно удалять два или более загрязняющих веществ одновременно, но для удобства компоненты, удаляемые путем селективной адсорбции, в данном документе обычно указаны в единственном числе как загрязняющее вещество или тяжелый компонент.
Описанные в данном документе способы селективации могут обеспечить улучшение кинетической селективности адсорбирующего материала, которое можно преобразовать посредством соответствующей схемы в улучшение извлечения требуемого компонента в кинетически регулируемом способе короткоцикловой адсорбции и/или в способе мембранного разделения.
Адсорбирующие контакторы и слои
Используемый в данном документе термин «адсорбирующий контактор» включает как структурированные, так и неструктурированные адсорбирующие контакторы. Адсорбирующий контактор является частью установки короткоцикловой адсорбции, в которой подаваемый газ приводят в контакт с адсорбентом. В способе АПТ контактор может содержать средства нагрева и охлаждения адсорбента, такие как нагревающие и охлаждающие каналы.Каждый контактор может содержать один или более адсорбирующих слоев. Слои являются секциями или частями контактора, которые содержат адсорбент. Каждый слой может содержать один адсорбент или смесь различных адсорбентов. Не обязательно, чтобы все слои в контакторе содержали один и тот же адсорбент.
В некоторых воплощениях слой в контакторе может включать насадку, содержащую по меньшей мере твердые инертные частицы и гранулы, содержащие адсорбент. Инертные частицы можно внедрить в слой, чтобы способствовать управлению теплотой адсорбции и десорбции. Гранулы, содержащие адсорбент, обычно могут включать частицы адсорбента, поры и связующее. Гранулы часто можно образовать в способах сушки распылением или экструзии. Инертные частицы обычно могут иметь размеры от примерно 100 мкм до примерно 10 см, но можно использовать любой подходящий размер частиц, в зависимости от конструкции. Гранулы, содержащие адсорбент, обычно могут иметь размеры от примерно 250 мкм до примерно 1 см, но также можно использовать любой подходящий размер частиц, в зависимости от конструкции. Перенос массы можно улучшить путем использования более мелких гранул, однако падение давления в слое может иметь тенденцию к возрастанию с уменьшением размера.
Одним примером разработанного адсорбирующего контактора является контактор с параллельными каналами, который может подходить для применения во множестве способов короткоцикловой адсорбции. Структура слоя адсорбирующего контактора, состоящего из контакторов с параллельными каналами, может включать закрепленные поверхности, на которых удерживают адсорбент или другой активный материал. Контакторы с параллельными каналами могут предоставить значительные преимущества по сравнению со стандартными способами разделения газов, такими как сосуды, содержащие адсорбирующие слои или экструдированные адсорбирующие частицы. «Контакторы с параллельными каналами» в данном документе определены как подгруппа адсорбирующих контакторов, включающих структурированные (сконструированные) адсорбенты в слоях с по существу параллельными проточными каналами. Эти проточные каналы можно образовать с помощью множества средств. Помимо адсорбирующего материала структура слоя может содержать один или более материалов, таких как (но не ограничиваясь перечисленным) материалы носителя, теплоотводящие материалы и уменьшающие пустоты компоненты.
В установке короткоцикловой адсорбции с контактором с параллельными каналами стенки каналов в слоях могут содержать адсорбент, например, одинакового размера цеолитовые кристаллы с 8-членными кольцами. Слои в контакторе могут при необходимости содержать теплоаккумулирующий (теплопередающий) материал, способствующий регулированию нагрева и охлаждения адсорбента в контакторе в течение стадий как адсорбции, так и десорбции способа адсорбции с перепадом давления. Нагрев в течение адсорбции может быть вызван теплотой адсорбции молекул, поступающих в адсорбент. Возможный теплоаккумулирующий материал также может способствовать охлаждению контактора в течение стадии десорбции. Теплоаккумулирующий материал можно внедрить в проточные каналы слоев в контакторе, внедрить в сам адсорбент и/или внедрить в виде части стенки проточных каналов. Когда он внедрен в адсорбент, он может представлять собой твердый материал, распределенный по всему слою адсорбента, и/или он может быть включен как слой внутри адсорбента. Когда он внедрен как часть стенки проточного канала, адсорбент может быть нанесен или образован на стенке. Любой подходящий материал можно использовать в качестве теплоаккумулирующего материала при практической реализации настоящего изобретения. Неограничивающие примеры таких материалов включают металлы, керамику и полимеры. Неограничивающие примеры предпочтительных металлов включают стальные, медные и алюминиевые сплавы. Неограничивающие примеры предпочтительной керамики включают диоксид кремния, оксид алюминия и диоксид циркония. Примером предпочтительного полимера, который можно использовать при практической реализации настоящего изобретения, является полиимид.
В зависимости от степени, до которой необходимо ограничить повышение температуры в течение стадии адсорбции, отношение массы используемого теплоаккумулирующего материала к массе микропористого адсорбента в контакторе может составлять от примерно 0,1 до примерно 25, например, от примерно 0,25 до 5, от примерно 0,25 до 2 или от примерно 0,25 до 1. В предпочтительном воплощении эффективное количество теплоаккумулирующего материала может быть внедрено в контактор. ффективное количество теплоаккумулирующего материала может быть количеством, достаточным для поддержания роста температуры адсорбента в течение стадии адсорбции до менее примерно 100°С, например, менее примерно 50°С или менее примерно 10°С.
Каналы в контакторе, также иногда называемые «проточными каналами» или «каналами газового потока», представляют собой пути в контакторе, через которые протекает газ. В целом, проточные каналы могут обеспечить относительно низкое гидродинамическое сопротивление наряду с относительно большой площадью поверхности. Длина проточного канала преимущественно может быть достаточной для обеспечения зоны переноса массы, при этом данная длина может по меньшей мере зависеть от скорости текучей среды и от отношения площади поверхности к объему канала. Каналы могут быть выполнены таким образом, чтобы минимизировать падение давления вдоль длины каналов. Во многих воплощениях фракция потока текучей среды, поступающая в канал на первом конце контактора, не находится в соединении с любой другой фракцией текучей среды, поступающей в другой канал на первом конце, до тех пор, пока эти фракции не объединятся после выхода на втором конце. В контакторах с параллельными каналами однородность каналов в слоях может быть важной для обеспечения эффективного использования (по существу всех) каналов и, по существу, равномерного заполнения зоны переноса массы. Как производительность, так и чистота газа может страдать, если существует избыточная несогласованность каналов. Если один проточный канал больше, чем соседний проточный канал, может произойти преждевременный прорыв продукта, что может привести к уменьшению чистоты получаемого газа, в некоторых случаях к неприемлемым уровням чистоты. Кроме того, для устройств, действующих при частотах цикла более примерно 50 циклов в минуту (ц/мин), может потребоваться большая однородность проточных каналов и меньшее падение давления, чем для устройств, действующих при более низких частотах цикла. Далее, если возникает слишком большое падение давления в слое, то трудно достичь более высоких частот цикла, таких как более чем примерно 3 ц/мин.
Размеры и геометрические формы слоев в контакторах с параллельными каналами могут быть любыми, подходящими для применения в оборудовании для осуществления способа короткоцикловой адсорбции. Неограничивающие примеры геометрических форм включают монолиты с различными формами, имеющие множество, по существу, параллельных каналов, проходящих от одного конца монолита до другого, множество трубчатых элементов, расположенные друг над другом слои адсорбирующих листов с промежутками и без промежутков между каждым листом, многослойные спиральные рулоны, пучки полых волокон, а также пучки по существу параллельных твердых волокон. Адсорбент может быть нанесен на эти геометрические формы или во многих случаях данные формы могут быть образованы непосредственно из адсорбирующего материала с подходящим связующим. Примером геометрической формы, образованной непосредственно из адсорбента/связующего, может быть экструзия композиционного материала цеолит/полимер в виде монолита. Другим примером геометрической формы, образованной непосредственно из адсорбента, могут быть экструдированные или скрученные полые волокна, изготовленные из композиционного материала цеолит/полимер. Примером геометрической формы, покрытой адсорбентом, может быть тонкий плоский стальной лист, покрытый микропористой адсорбирующей пленкой с небольшим содержанием мезопор, такой как цеолитовая пленка. Непосредственно образованный или покрытый адсорбентом слой может быть сам структурирован в виде множества слоев, состоящих либо из одинаковых, либо из различных адсорбирующих материалов. Структуры многослойных адсорбирующих листов описаны, например, в опубликованной патентной заявке US 2006/0169142, которая включена в данный документ путем ссылки.
Размеры проточных каналов можно рассчитать, учитывая падение давления вдоль проточного канала. Для проточных каналов может быть предпочтительным иметь ширину канала от примерно 5 мкм до примерно 1 мм, например от примерно 50 мкм до примерно 250 мкм. Используемый в данном документе термин «ширина канала» для проточного канала определен как длина линии поперек минимального размера проточного канала перпендикулярно пути потока. Например, если проточный канал является круглым в поперечном сечении, то ширина канала представляет собой внутренний диаметр круга. Однако, если проточный канал является прямоугольным в поперечном сечении, то ширина канала представляет собой длину перпендикулярной линии, связывающей две наиболее длинные стороны прямоугольника (то есть, длину наименьшей стороны прямоугольника). Также необходимо отметить, что проточные каналы могут иметь любую конфигурацию поперечного сечения. В некоторых предпочтительных воплощениях конфигурация поперечного сечения проточного канала может быть круглой, прямоугольной, квадратной или шестиугольной. Однако можно использовать любую геометрическую конфигурацию поперечного сечения, такую как (но не ограничиваясь перечисленным) эллипсы, овалы, треугольники, различные многоугольники или даже неправильные формы. В других предпочтительных воплощениях отношение объема адсорбента к объему проточного канала в адсорбирующем контакторе может составлять от примерно 0,5:1 до примерно 100:1, например от примерно 1:1 до примерно 50:1.
В некоторых применениях проточные каналы можно образовать путем наслаивания друг на друга листов адсорбента. Обычно, в применениях слоистого адсорбента длина проточного канала может составлять от примерно 0,5 см до примерно 10 м, например от примерно 10 см до примерно 1 м, а ширина канала от примерно 50 мкм до примерно 450 мкм. Каналы могут содержать разделитель или сетку, которая действует как разделитель. Для слоистых адсорбентов можно использовать разделители, которые являются конструкциями или материалами, которые определяют разделение между слоями адсорбента. Неограничивающие примеры типов разделителей, которые можно использовать в настоящем изобретении, включают те, которые состоят из таких материалов с точными размерами, как пластиковая, металлическая, стеклянная или углеродная сетка; пластиковая пленка или металлическая фольга; пластиковые, металлические, стеклянные, керамические или углеродные волокна и нити; керамические колонки; пластиковые, стеклянные, керамические или металлические сферы или диски; или их сочетания или смеси. Слоистые адсорбенты использовали в устройствах, действующих при частотах циклов АПД, составляющих до по меньшей мере примерно 150 ц/мин. Длина проточного канала может коррелировать со скоростью цикла. При более низких скоростях цикла, таких как от примерно 20 ц/мин до примерно 40 ц/мин, длина проточного канала может составлять один метр или более, даже до примерно 10 м. Для скоростей цикла больше примерно 40 ц/мин длину проточного канала обычно можно уменьшить и можно изменять, например, от примерно 10 см до примерно 1 м. Более длинные проточные каналы можно использовать для более медленных циклов АПД. Способы АПТЧЦ являются более медленными, чем способы АПДЧЦ и, в связи с этим, более длинные проточные каналы также можно использовать в способах АПТ.
В одном воплощении по меньшей мере один слой в контакторах в установке короткоцикловой адсорбции может содержать селективированный адсорбент. В других воплощениях большая часть адсорбента, содержащегося внутри слоя в контакторах, может быть селективированной.
Газовое сырье и адсорбирующие материалы
Способы разделения, описанные в данном документе, можно использовать для выполнения разделений многих видов газофазного сырья. Один пример газофазного сырья включает сырьевой природный газ или поток, такой как сырьевой природный газ, полученный на производственном участке по добыче нефти, или сырьевой природный газ или поток из газового месторождения или пласта сланцевого газа. Сырьевой природный газ обычно содержит метан, возможно некоторые высшие углеводороды, такие как С2-С4 углеводороды, СО2 и возможно один или более из дополнительных компонентов, таких как N2, H2S, H2O и меркаптаны. Сырьевой природный газ также может содержать одно или более веществ, введенных в процессе извлечения природного газа на производственном участке. Неограничивающие примеры таких веществ могут включать гликоли, такие как этиленгликоль, амины, такие как метилдиэтиламин, диметилдисульфид и их сочетания.
Улучшения в извлечении легкого компонента, вызванные селективацией адсорбентов или мембран, могут быть ценными для способов, используемых для удаления примесей из потоков природного газа, особенно потоков природного газа высокого давления. Может потребоваться излечение примесей, также называемых «тяжелым(и) компонентом(ами)», и обогащенного метаном продукта, также называемого «легким компонентом», при таком высоком давлении, как применяемое при эксплуатации при переработке природного газа. В зависимости от воплощения способ короткоцикловой адсорбции с использованием селективированного адсорбента можно использовать для достижения извлечения метана, составляющего более примерно 80 мол.%, например более примерно 85 мол.%, более примерно 90 мол.% или более примерно 95 мол.%, даже когда природный газ подают при относительно высоком давлении на входе, таком как более примерно 350 кПа изб. (примерно 50 фунтов на 1 кв. дюйм изб.), например, по меньшей мере примерно 1,0 МПа изб. (примерно 150 фунтов на 1 кв. дюйм изб.), по меньшей мере примерно 3,1 МПа изб. (примерно 450 фунтов на 1 кв. дюйм изб.), по меньшей мере примерно 4,1 МПа изб. (примерно 600 фунтов на кв. дюйм изб.) или по меньшей мере примерно 8,3 МПа изб. (примерно 1200 фунтов на кв. дюйм изб.). Состав потоков природного газа непосредственно из подземного месторождения (неочищенного природного газа) может изменяться от месторождения к месторождению. Чтобы получить газ, который можно вводить в трубопровод для продажи на бытовом и промышленном топливных рынках, необходимо удалить загрязняющие вещества, такие как N2, Hg, меркаптаны и кислые газы СО2 и H2S, до приемлемых уровней. Данные уровни и типы примесей изменяются от газового месторождения к газовому месторождению и в некоторых случаях могут включать большую часть молекул в добытом газе. Например, не является необычным для некоторых месторождений природного газа содержание CO2 от примерно 0 до примерно 90 мол.%, более типично от примерно 10 мол.% до примерно 70 мол.% СО2.
Другие примеры подходящего газофазного сырья могут включать топочный газ и/или топливный газ из способа перегонки нефти. Множество способов могут вырабатывать топочный газ и/или топливный газ, включающие СО2 и легкие углеводороды, такие как СН4. В зависимости от источника топочного/топливного газа, он/они также могут содержать H2S, Н2, N2, Н2О и/или другие компоненты, которые находятся в газовой фазе при стандартных условиях. Такие компоненты, как CO2 и N2, могут действовать как разбавители, уменьшая ценность таких потоков топочного газа и/или топливного газа.
Чтобы повысить ценность потока газовой фазы, можно выполнить разделение для выработки по меньшей мере двух потоков продукта. Первый поток продукта, соответствующий легкому компоненту, может быть обогащен требуемым продуктом, таким как СН4, и/или другими углеводородами, такими как другие углеводороды в целом, другие углеводороды, содержащие 4 или менее атомов углерода, или другие углеводороды, содержащие 3 или менее атомов углерода. Предпочтительно, другой углеводород может включать по меньшей мере одну насыщенную углерод-углеродную связь. Второй поток продукта, соответствующий тяжелому компоненту, может быть обогащен одним или более устраняемыми компонентами, такими как СО2 и/или N2.
Одним способом выполнения разделения может быть подвергание входящего потока воздействию адсорбирующего материала, который может преимущественно или селективно адсорбировать один или более компонентов газофазного потока. Различия в адсорбции могут быть обусловлены либо равновесием, либо кинетикой. Различия в равновесии могут отражаться в изотермах конкурирующей адсорбции и/или их можно оценить из изотерм одного компонента. Различия в кинетике могут отражаться в коэффициентах диффузии. Способы, в которых существенная часть селективности обусловлена различиями в кинетике, обычно называют кинетическими разделениями. Для кинетических разделений продолжительность стадии адсорбции предпочтительно может быть достаточно короткой для того, чтобы адсорбент не пришел в равновесие с потоком сырья. Например, катионные цеолиты с относительно большими порами (средний размер пор более 5 Å) могут обладать равновесной селективностью, позволяющей адсорбировать CO2 предпочтительнее, чем СН4, тогда как катионные цеолиты с относительно маленькими порами (средний размер пор менее 3,8 Å) могут обладать кинетической селективностью, позволяющей адсорбировать CO2 предпочтительнее, чем СН4. Контактор, изготовленный с использованием цеолитового адсорбента, можно использовать для селективной адсорбции CO2 из входящего потока газа, содержащего CO2 и СН4, что приводит к получению выходящего потока, обогащенного СН4. Для кинетического адсорбента продолжительность стадии адсорбции можно установить с помощью размера кристалла цеолита и коэффициента диффузии СН4. Регенерацию такого кинетического адсорбента можно выполнять с помощью изменения давления, изменения температуры, продувки и/или вытеснения. Использование кинетического адсорбента, который слабо адсорбирует CO2 (то есть, с относительно плоской изотермой адсорбции), может облегчить регенерацию. Цеолиты с высоким содержанием кремния (отношение Si/Al>~100) часто могут иметь такие типы слабых изотерм. Процесс регенерации обычно можно вырабатывать поток, обогащенный CO2 и обедненный углеводородами, такими как СН4.
Одним из факторов при выборе адсорбирующего цеолита (или другого адсорбирующего материала) может быть селективность для требуемого разделения. Если не указано другое, термин «селективность короткоцикловой адсорбции», используемый в данном документе, основан на бинарном (попарном) сравнении молярной концентрации компонентов в потоке сырья и полного количества молей этих компонентов, адсорбированных конкретным адсорбентом в течение стадии адсорбции технологического цикла при конкретных условиях функционирования системы и составе потока сырья. Такое определение селективности короткоцикловой адсорбции может подходить для технологического цикла, который является частью способа короткоцикловой адсорбции, такого как адсорбция с перепадом давления и/или адсорбция с перепадом температуры. Чтобы определить селективность, можно определить величины поглощения компонентов сырья. Для сырья, которое содержит по меньшей мере компоненты А и В, величины адсорбционного поглощения для компонентов А и В можно определить как: UA=(изменение полного количества молей А в адсорбенте в течение стадии адсорбции способа короткоцикловой адсорбции) / (молярная концентрация А в сырье), а UB=(изменение полного количества молей В в адсорбенте в течение стадии адсорбции способа короткоцикловой адсорбции) / (молярная концентрация В в сырье), где UA представляет собой адсорбционное поглощение компонента А, а UB представляет собой адсорбционное поглощение компонента В.
Для сырья, содержащего компонент А, компонент В и, возможно, один или более дополнительных компонентов, адсорбент, который имеет большую «селективность» для компонента А по сравнению с компонентом В, обычно может иметь в конце стадии адсорбции способа короткоцикловой адсорбции значение UA больше, чем UB. Таким образом, селективность можно определить как: Селективность Короткоцикловой Адсорбции = UA/UB (для UA>UB). Для адсорбентов, которые в основном являются кинетически селективными, селективность короткоцикловой адсорбции может зависеть от продолжительности цикла. В таких случаях длительная адсорбция и, следовательно, общие продолжительности циклов могут уменьшить селективность короткоцикловой адсорбции.
На основе вышеизложенного, подходящие адсорбенты можно эксплуатировать за времена циклов таким образом, чтобы иметь селективность короткоцикловой адсорбции более 1 для первого компонента (например, компонента А) относительно второго компонента (например, компонента В) в подходящем устройстве короткоцикловой адсорбции. Например, подходящий адсорбент для отделения СН4 от СО2 может иметь селективность короткоцикловой адсорбции более 1 для адсорбции CO2 (компонент А) относительно СН4 (компонент В). После селективации селективность короткоцикловой адсорбции для первого компонента по сравнению со вторым компонентом может составлять по меньшей мере примерно 5, например, по меньшей мере примерно 10. При некоторых селективациях селективность короткоцикловой адсорбции для первого компонента по сравнению со вторым компонентом может составлять по меньшей мере 25, например, по меньшей мере 100.
Примеры компонентов могут включать молекулярный азот (N2), диоксид углерода (СО2), сероводород (H2S) и метан (СН4). Согласно приведенным выше определениям, метан представляет собой компонент, соответствующий возможному «второму компоненту», при этом азот, диоксид углерода или их сочетание представляют собой возможные варианты «первого компонента». Одним вариантом может быть селективация адсорбента (и/или соответствующего подходящего устройства короткоцикловой адсорбции) так, чтобы селективность короткоцикловой адсорбции для CO2 по сравнению с СН4 составляла по меньшей мере 5, например, по меньшей мере 10, по меньшей мере 25 или по меньшей мере 100. Дополнительно или альтернативно, адсорбент можно селективировать так, чтобы он имел селективность короткоцикловой адсорбции для N2 по сравнению с СН4 по меньшей мере 5, например, по меньшей мере 10 или по меньшей мере 25. Также дополнительно или альтернативно, адсорбент можно селективировать так, чтобы он имел селективность короткоцикловой адсорбции для сочетания двух или более из указанных выше компонентов относительно СН4, составляющую по меньшей мере 5, например, по меньшей мере 10 или по меньшей мере 25 (например, в такой ситуации первый компонент можно выбрать из CO2, N2 или H2S, а второй компонент может представлять собой СН4). Во всех случаях селективация может преимущественно увеличивать селективность короткоцикловой адсорбции адсорбента.
Равновесную селективность также можно использовать как фактор при выборе адсорбента. В описанных в данном документе способах добавляют кинетическую селективность к равновесной селективности в способе, который может увеличить селективность короткоцикловой адсорбции адсорбента. Равновесную селективность можно охарактеризовать на основе долговременных измерений переноса или на основе характеристики медленного цикла. Например, для адсорбции СО2 при приблизительно 40°С с использованием цеолитового адсорбента типа DDR с 8-членными кольцами, СО2 может достигать равновесного уровня адсорбированных молекул за время (порядок величины), составляющее от примерно 0,5 секунд до примерно 10 секунд для кристаллов с размерами приблизительно 10 мкм. Для описания этого порядка величины достижение равновесного уровня адсорбции определено как достижение уровня, находящегося в пределах примерно 5% от равновесной концентрации адсорбции, например, в пределах примерно 2%. Для СН4 равновесный уровень адсорбированных молекул обычно может быть достигнут за время порядка десятков секунд. Другими словами, равновесной концентрации адсорбции можно достичь за время от примерно 2 секунд до примерно 200 секунд. В способе короткоцикловой адсорбции с относительно коротким временем цикла, таком как способ адсорбции с перепадом давления и/или температуры с быстрым циклом, продолжительность стадии адсорбции может быть сравнимой со временем (или, возможно, быть короче, чем время) достижения равновесного уровня адсорбированных молекул СН4. В результате, в способе короткоцикловой адсорбции со временем цикла порядка десятков секунд или менее на адсорбцию СО2 и СН4 могут влиять различные факторы, например, для DDR адсорбента с размером 10 мкм. Адсорбция CO2 может обладать характеристиками, более похожими на равновесную адсорбцию, когда время цикла короткоцикловой адсорбции может быть длиннее времени установления равновесия для адсорбции CO2. Наоборот, факторы кинетической адсорбции могут оказывать большее влияние на адсорбцию СН4, так как время способа короткоцикловой адсорбции может быть приблизительно сравнимо со временем достижения равновесия для СН4. В результате, селективацию можно использовать для увеличения кинетической селективности путем уменьшения адсорбции СН4 и для улучшения технологической гибкости способа (путем увеличения допустимых времен, затрачиваемых на стадию адсорбции). По аналогии с СО2, N2 может достигать равновесной адсорбции быстрее, чем СН4.
Для удаления CO2, N2 и/или H2S из природного газа или другого газового потока, который содержит метан и/или другие С2-С4 углеводороды, примеры подходящих адсорбирующих материалов могут включать цеолитовые материалы с 8-членными кольцами, которые обладают кинетической селективностью, которую можно улучшить с помощью селективации, для отделения СО2 и/или N2 от потока сырья. Примером подходящего цеолита с 8-членными кольцами в этом классе материалов, которые можно использовать в способах короткоцикловой адсорбции, является цеолит DDR. Другие примеры цеолитов с 8-членными кольцами включают Sigma-1 и ZSM-58, которые имеют каркасные структуры, изотипичные DDR. Цеолитовые материалы с 8-членными кольцами могут иметь отношение Si/Al от примерно 1:1 до примерно 10000:1, например, от примерно 10:1 до примерно 5000:1 или от примерно 50:1 до примерно 3000:1.
Цеолиты с 8-членными кольцами, подобные DDR, обычно могут иметь пористые каналы с размером отверстия (поры) порядка 3-4 Ангстрем. Например, размер отверстия (поры) цеолита типа DDR составляет примерно 3,65 Ангстрем. Молекулы с относительно линейной конфигурацией, такие как СО2 и/или N2, могут диффундировать более быстро в поре с таким размером отверстия по сравнению с более объемными молекулами, такими как метан. В качестве другого примера, минимальный размер молекулы метилдиэтиламина немного меньше 5 Ангстрем.
В некоторых воплощениях подходящие цеолитовые материалы с 8-членными кольцами могут обеспечить быстрое прохождение СО2 в цеолитовые кристаллы, при этом затрудняя перенос метана, что делает возможным селективное отделение СО2 от смеси СО2 и метана. С помощью селективации можно преимущественно улучшить селективность короткоцикловой адсорбции.
Цеолиты с 8-членными кольцами, подходящие для применения в данном документе, могут обеспечить доступ СО2 во внутреннюю пористую структуру через отверстия 8-членных колец таким образом, что отношение эффективных коэффициентов однокомпонентной диффузии CO2 и метана (то есть, DCO2/DCH4) может быть больше 10, например, больше примерно 50 или больше примерно 100. Другим учитываемым фактором для характеристик цикла при разделениях природного газа может являться абсолютный коэффициент диффузии метана, причем метан представляет собой легкий компонент в таких кинетически регулируемых разделениях. В сочетании с продолжительностью стадии адсорбции в способе короткоцикловой адсорбции абсолютный коэффициент диффузии метана может значительно влиять на извлечение метана в кинетически регулируемых разделениях газовых смесей, содержащих СО2 и СН4. Как упоминали ранее, может быть предпочтительной максимизация этого извлечения. Моделирование способа показало, что для цикла со стадией адсорбции, продолжающейся примерно 4 секунды, в контакторе, изготовленном с использованием кристаллов с размером примерно 15 мкм, эффективный коэффициент диффузии метана в кристаллах при рабочих условиях предпочтительно может составлять менее примерно 3×10-13 м2/с, чтобы избежать адсорбции слишком большого количества метана и вредного воздействия на извлекаемые целевые соединения. Для других продолжительностей циклов и/или кристаллов с другими размерами коэффициент диффузии метана DCH4 предпочтительно можно определить как
DCH4<3×10-13*[tadsorb/(4 с)]2 * [dcrystal/(15 мкм)]2 {в м2/с},
где tadsorb представляет собой продолжительность стадии адсорбции в секундах, a dcrystal представляет собой характеристический размер переноса через кристалл в микрометрах. Эти условия для коэффициента диффузии метана не всегда могут совпадать с сочетанием размеров кристаллов цеолитов с 8-членными кольцами, которые можно синтезировать, коэффициентом диффузии только что синтезированных кристаллов и размерами кристаллов, которые можно внедрить в контактор на практике. Селективация может обеспечить возможность снижения эффективного коэффициента диффузии метана до заданного диапазона для применяемого на практике контактора, при этом сохраняя и/или увеличивая отношение DCO2/DCH4. Доводы в пользу ограничения абсолютного коэффициента диффузии легкого компонента могут быть идентичны для кинетически регулируемых разделений других газовых смесей. Для обеспечения экспериментального измерения характеристики можно использовать эффективные коэффициенты диффузии (например, для СО2 и СН4) вместо коэффициентов диффузионного переноса, измеренных для чистого газа в режиме закона Генри изотермы адсорбции для адсорбента. Загрузка молекул в неселективированный адсорбент (например, цеолит) может быть низкой в режиме закона Генри и, в этом режиме, коэффициенты диффузии Фика и Стефана-Максвелла могут быть почти равны. Эффективный коэффициент диффузии пористого кристаллического материала для конкретного сорбата можно соответствующим образом измерить в показателях его постоянной времени диффузии, D/r2, где D представляет собой коэффициент диффузии Фика (м2/с), а величина "r" представляет собой радиус кристаллитов (м), характеризующий расстояние диффузии. В случаях, когда кристаллы неоднородны по размеру и геометрии, "r" представляет собой средний радиус, характерный для их соответствующих распределений. Одним из способов измерения постоянной времени и коэффициента диффузии может являться анализ стандартной кинетики адсорбции (то есть, гравиметрическое поглощение) с использованием способов, описанных в J. Crank "The Mathematics of Diffusion", 2nd Ed., Oxford University Press, Great Britain, 1975. Другим способом измерения постоянной времени и коэффициента диффузии может являться анализ данных хроматографии с нулевой длиной с использованием методов, описанных в D.М. Ruthven "Principles of Adsorption and Adsorption Processes", John Wiley, NY (1984) и J. Karger and D.M. Ruthven "Diffusion in Zeolites and Other Microporous Solids", John Wiley, NY (1992).
Другим способом получения коэффициентов диффузии может являться измерение постоянной времени для адсорбции и десорбции в устройстве циклической однокомпонентной адсорбции с перепадом давления. В таком устройстве адсорбент подвергают периодическому повышению и сбросу давления с чистым однокомпонентным газом. Каждый представляющий интерес компонент (например, СО2, СН4, N2 и Не) можно исследовать по отдельности. Измерения с Не часто используют для упрощения интерпретации собранных данных. Повышение давления можно выполнять путем переключения клапана для соединения сосуда высокого давления с ячейкой, содержащей адсорбент, и затем закрытия данного клапана. Сброс давления можно выполнять путем переключения другого клапана для соединения сосуда низкого давления с ячейкой, содержащей адсорбент, и затем закрытия данного клапана. Число молей вещества, адсорбированных образцом и десорбированных из образца, можно определить из измерений давления, объема и температуры в сосудах и ячейке. Непрерывный циклический процесс можно создать путем приведения в исходное состояние давлений в сосудах после стадий повышения и сброса давления. Постоянную времени для поглощения можно легко преобразовать в эффективный коэффициент диффузии, используя приближение линейной движущей силы (ЛДС). Например, если адсорбент рассматривают как изотропную среду с постоянным диаметром, то коэффициент переноса массы ЛДС (с-1) может представлять собой: τ (ЛДС) ≈ 16,2*Deffective*(dcrystal/2)2. Это приближение обычно используют для моделирования способов короткоцикловой адсорбции.
Дополнительно или альтернативно, описанные выше цеолиты с 8-членными кольцами можно селективировать для увеличения их кинетической селективности для отделения азота от метана, или, вообще, для отделения азота от С1-С4 или С1-С3 углеводородов в газовом потоке. Улучшенная кинетическая селективность подходящих материалов с 8-членными кольцами может обеспечить быстрое прохождение N2 в цеолитовые кристаллы, при этом затрудняя перенос метана (или других легких углеводородов), так что возможно селективно отделить N2 от смеси N2 и метана. Для удаления N2 отношение эффективных коэффициентов однокомпонентной диффузии N2 и метана (то есть, DN2/DCH4) в селективированном адсорбенте может быть больше 5, например, больше примерно 20, больше примерно 50 или больше примерно 100. В зависимости от воплощения, обсуждение абсолютной величины коэффициента диффузии метана может быть аналогичным рассмотренным выше соображениям.
Селективация адсорбирующих материалов
При различных приготовлениях адсорбирующий материал может иметь значительно отличающиеся коэффициенты диффузии. Даже при одинаковой технологии приготовления коэффициенты диффузии в некоторых случаях могут изменяться от партии к партии. Это особенно справедливо для цеолитов. Селективация может предоставить способ уменьшения изменений коэффициента диффузии легкого компонента, которые могли бы вредно влиять на извлечение указанного легкого компонента.
Способы селективации можно применять для многих адсорбирующих материалов. Способ селективации можно проиллюстрировать на цеолитовых адсорбентах, но необходимо понимать, что микропористые материалы с другими типами каркасных атомов и/или другими кольцевыми структурами также можно селективировать. Цеолиты представляют собой кристаллические материалы, которые обычно выращивают в способе гидротермального синтеза, в котором часто используют структурообразующий агент. После извлечения цеолитового кристаллического продукта из гидротермальной смеси для синтеза, его часто прокаливают для удаления темплата и других материалов, которые могут блокировать доступ в пористую структуру внутри кристаллических частиц. Способ селективации можно применять после того, как пористая структура адсорбента была открыта. В данном описании цеолитовые кристаллы, которые были подвергнуты прокаливанию для удаления структурообразующего агента, называют материалами «в только что синтезированной форме».
Для селективации адсорбентов были разработаны два различных класса технологий. Первый включает долговременное воздействие селективирующих молекул при более низких летучестях, тогда как второй включает воздействие при более высоких летучестях и температурах в течение более коротких промежутков времени. Не связывая себя какой-либо конкретной теорией, полагают, что селективации адсорбента можно достичь в результате того, что молекулы поступают в адсорбент и занимают положения внутри пор адсорбента. Селективирующие молекулы могут быть сконцентрированы во фронт адсорбции, который проходит внутрь от внешней поверхности адсорбента. Концентрация селективирующих молекул может сильно уменьшаться с расстоянием за пределами распространения фронта. Селективирующие молекулы могут действовать как барьерные соединения, изменяя способность потенциальных адсорбируемых веществ к поступлению в адсорбент и продвижению внутри адсорбента. Это может привести к увеличению кинетической селективности адсорбента. Например, селективация с помощью барьерных соединений может вызвать кинетическую селективность цеолита с 8-членными кольцами для увеличения газового отделения СО2 и/или N2 от СН4 или другого углеводорода. В некоторых случаях барьерные соединения также могут образовывать пассивирующий слой на поверхности адсорбента, что улучшает кинетическую селективность адсорбента.
Предпочтительно, барьерные соединения могут медленно диффундировать (коэффициент диффузии менее 10-15 м2/с) через пористую структуру адсорбента при рабочих условиях. Очень медленно диффундирующие молекулы (коэффициент диффузии менее 10-19 м2/с) могут концентрироваться в порах вдали от центра адсорбента (то есть, в порах вблизи поверхности адсорбента). В предельном случае сверхмедленной диффузии (менее 10-23 м2/с) молекулы могут располагаться в четко выраженном слое, который проходит внутрь от поверхности адсорбента. Наличие барьера, образованного в порах / среди пор вблизи/на поверхности адсорбента, может способствовать улучшению кинетической селективности в способе короткоцикловой адсорбции путем немедленного блокирования или замедления переноса и, следовательно, уменьшения скорости адсорбции соединений, подлежащих кинетическому исключению из адсорбента. Это может способствовать увеличению извлечения неулавливаемых молекулярных соединений, подлежащих извлечению в качестве продукта в течение стадии адсорбции. Для цеолитов с 8-членными кольцами примеры молекул в диапазоне от медленно диффундирующих до очень медленно диффундирующих молекул могут включать линейные алканы с более чем 4 атомами углерода в цепи и первичные линейные спирты с более чем 3 атомами углерода в цепи. Для цеолитов с 8-членными кольцами примеры молекул, которые могут включать от очень медленно диффундирующих до сверхмедленно диффундирующих молекул, могут включать моноразветвленные алканы, диразветвленные алканы, 2-октанол, вторичные спирты, многократно разветвленные алканы, разветвленные первичные спирты и их сочетания. Сверхмедленно диффундирующие молекулы могут включать триразветвленные парафины, такие как 2,2,4-триметилпентан. Медленно диффундирующие и сверхмедленно диффундирующие молекулы могут обеспечить образование относительно стабильного слоя селективации, который не требует частой регенерации или обновления.
Для образования эффективного барьера, который блокирует или замедляет перенос, максимальная загрузка блокирующего соединения в поры / среди пор вблизи поверхности адсорбента должна составлять по меньшей мере 10% от его насыщающей загрузки (qs, обычно выражают в ммоль/г). В других воплощениях максимальная загрузка блокирующего соединения в поры / среди пор вблизи поверхности адсорбента может составлять по меньшей мере 40% от его насыщающей загрузки, например, по меньшей мере 75% от его насыщающей загрузки. В других воплощениях загрузку можно ограничить относительно насыщающей загрузки, чтобы обеспечить по меньшей мере несколько открытых каналов. В таких воплощениях загрузка может составлять 20% от насыщающей загрузки или менее, например, 15% или менее. За область вблизи поверхности можно принять расстояние от поверхности в пределах 5% от диаметра или среднего размера частиц адсорбента. Эту максимальную загрузку можно оценить, исходя из летучести блокирующего соединения в паре, воздействию которого подвергают адсорбент. При данной оценке используют изотерму Ленгмюра для аппроксимации равновесного поглощения блокирующего соединения. Изотерма Ленгмюра может быть выражена в следующей математической форме:
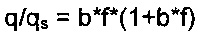 ,
,
где q представляет собой загрузку (ммоль/г) блокирующего соединения, qs представляет собой насыщающую загрузку (ммоль/г) блокирующего соединения, f представляет собой летучесть (бар) блокирующего соединения, а b представляет собой коэффициент Ленгмюра (1/бар). Этого условия можно достичь путем воздействия давлений паров барьерных соединений с молекулярной массой, составляющей по меньшей мере примерно 50 г/моль, например, по меньшей мере примерно 60 г/моль, при парциальных давлениях более примерно 10% от давления насыщенных паров. Более высоких максимальных загрузок можно достичь путем воздействия более высоких парциальных давлений барьерных соединений, таких как по меньшей мере примерно 25% от давления насыщенных паров, по меньшей мере примерно 50% или по меньшей мере примерно 90%. Для воздействия барьерных соединений при очень высоких парциальных давлениях можно образовать жидкую фазу и, соответственно, можно достичь подходящих высоких загрузок барьерных соединений. Примеры подходящих барьерных соединений могут включать (но не ограничиваются перечисленным) алканы (например, парафины), другие углеводороды, спирты, другие кислородсодержащие соединения, амины и серосодержащие соединения. Парафиновые соединения могут включать линейные парафины, моноразветвленные парафины, многократно разветвленные парафины, триразветвленные парафины и их сочетания. Спирты могут включать первичные и вторичные спирты. Кислородсодержащие соединения могут включать гликоли, такие как этиленгликоль и триэтиленгликоль. Примеры аминов могут включать метилдиэтиламин и диметилэтиламин. Одним из примеров серосодержащего соединения является диметилдисульфид. Селективация блокирующим соединением, имеющим величину "b" более 10/бар при характеристической температуре способа короткоцикловой адсорбции, может способствовать уменьшению потери блокирующего соединения после того, как оно было загружено в адсорбент. Применение блокирующих соединений с более высокими величинами b (такими как по меньшей мере 100/бар или по меньшей мере 100/бар при характеристической температуре способа короткоцикловой адсорбции) может дополнительно уменьшить потерю блокирующего соединения в течение действия способа короткоцикловой адсорбции или мембранного разделения.
Размер молекул может влиять как на прочность адсорбции (величина b), так и на коэффициент диффузии блокирующего соединения. Размеры молекул можно охарактеризовать максимальным и минимальным размером блокирующей молекулы. Например, для линейного парафина максимальный размер можно задать длиной вытянутой цепи, а минимальный размер можно задать диаметром цепи. Увеличение максимального размера блокирующей молекулы может увеличить величину b и снизить коэффициент диффузии. Когда максимальный размер блокирующей молекулы становится слишком большим, она не может эффективно селективно блокировать перенос одного молекулярного соединения, при этом обеспечивая быстрый перенос других соединений. Для цеолитовых адсорбентов с 8-членными кольцами максимальный размер блокирующего соединения может быть менее примерно 25 Ангстрем и более примерно 4 Ангстрем. Улучшенной характеристики можно достичь для цеолитовых адсорбентов с 8-членными кольцами, когда максимальный размер составляет менее примерно 15 Ангстрем и более примерно 6 Ангстрем. Молекулы с меньшими максимальными размерами, такие как СО2, H2S, метан, этан и Н2О, по-видимому, не улучшают кинетическую селективность адсорбентов. Минимальный размер блокирующей молекулы может определять ее способность к диффузии в цеолите. По мере того, как минимальный размер блокирующей молекулы возрастает, коэффициент диффузии может стремиться к уменьшению. Когда минимальный размер становится слишком большим, коэффициент диффузии может понизиться до такого значения, что соединение не сможет проходить во внутреннюю область цеолита за приемлемое время. Размер молекулы, которая может проходить в пористую структуру цеолита может быть больше того, который можно было бы предположить из базы данных цеолитовых структур, опубликованной International Zeolite Association (IZA), http://izasc.ethz.ch/fmi/xsl/IZA-SC/ft.xsl. Для каждого типа каркаса база данных дает размер твердой сферы, которая может диффундировать вдоль каждого направления в жестком цеолитовом каркасе. Из-за гибкости цеолитового каркаса, молекулы с минимальными размерами, которые значительно больше тех, которые можно предположить из базы данных IZA, могут проникать в пористую структуру цеолита. Для того чтобы можно было загружать блокирующие молекулы в цеолит, минимальный размер молекул может превышать размер IZA наибольшей твердой сферы, которая может диффундировать вдоль любого направления в жестком цеолитовом каркасе, не более чем на 2,0 Å. Для того чтобы можно было иметь более легкую загрузку блокирующих молекул в цеолит, минимальный размер их молекул может превышать размер IZA наибольшей твердой сферы, которая может диффундировать вдоль любого направления в жестком цеолитовом каркасе, не более чем на 1,5 Å. Чтобы иметь коэффициент диффузии, достаточно низкий для улавливания блокирующих молекул в цеолите, минимальный размер блокирующих молекул может превышать размер IZA наибольшей твердой сферы, которая может диффундировать вдоль любого направления в жестком цеолитовом каркасе, примерно на 0,4 Å. Улавливание блокирующих молекул можно усилить, если их минимальный размер примерно на 0,6 Å больше размера IZA наибольшей твердой сферы, которая может диффундировать вдоль любого направления в жестком цеолитовом каркасе. Дополнительно или альтернативно, различия в размерах можно выразить в процентах от размера наибольшей твердой сферы из базы данных IZA. В таких воплощениях минимальный размер молекул может превышать размер IZA наибольшей твердой сферы, которая может диффундировать вдоль любого направления в жестком цеолитовом каркасе, не более чем примерно на 60%, например, не более чем примерно на 55%, не более чем примерно на 50%, не более чем примерно на 45% или не более чем примерно на 40%. Дополнительно или альтернативно, в таких воплощениях минимальный размер молекул может быть по меньшей мере примерно на 10% больше размера IZA наибольшей твердой сферы, которая может диффундировать вдоль любого направления в жестком цеолитовом каркасе, например, по меньшей мере примерно на 15% больше, по меньшей мере примерно на 20% больше или по меньшей мере примерно на 25% больше.
Например, в базе данных IZA размер наибольшей твердой сферы, которая может диффундировать вдоль любого направления в жестком каркасе цеолита DDR, указан как 3,65 Å. Таким образом, предпочтительный минимальный размер подходящей блокирующей молекулы для DDR может составлять от примерно 4,05 до 5,65 Å. Чтобы облегчить загрузку блокирующих молекул в DDR, может быть предпочтительным, чтобы минимальный размер блокирующей молекул был менее примерно 5,15 Å. Чтобы усилить улавливание (то есть, долговременную стабильность) блокирующего соединения в DDR, может быть предпочтительным, чтобы минимальный размер блокирующей молекул был больше примерно 4,25 Å. Для селективации цеолита типа DDR примеры молекул, которые попадают в эти диапазоны размеров, могут включать (но не ограничиваются перечисленным) н-гексан, 2-метилпентан, 2-метилгексан, гексанол, 2-гексанол, 2-гептанол, 2-октанол, 2-метил-1-пентанол, 2-метил-1-гексанол. Для цеолита типа DDR примеры молекул, которые не попадают в этот диапазон размеров, включают толуол, циклогексиламин, бутиламин и н-метилпирролидон. Эксперименты показали, что при температурах около 100°С долговременное воздействие насыщенных паров этих молекул, которые не попадают в этот диапазон размеров, по-видимому, не приводит к значительному улучшению кинетической селективности.
Некоторые молекулы, используемые для селективации, могут реагировать с дефектами в цеолитовых каркасных структурах (такими как гидроксильные группы), образуя химические связи с ними внутри каркаса. Это может усилить стабильность селективации. Например, первичные и вторичные спирты могут диффундировать в структуру цеолита и впоследствии реагировать с гидроксильными группами и другими дефектами в структуре. Эта реакция может захватывать молекулы, так что они могут не поддаваться десорбции при нагревании до температур приблизительно 350°С или выше в инертной атмосфере (например, N2).
Множество способов можно использовать для введения барьерного соединения в адсорбент. Одним из вариантов может являться воздействие барьерного соединения на адсорбент до внедрения адсорбента в слой устройства короткоцикловой адсорбции. В этом случае частицы адсорбента можно обработать перед введением его в состав слоя. Технологии введения в состав могут включать образование гранул из селективированного адсорбента и связующего, отливку пленки из селективированного адсорбента и связующего, нанесение тонкого покрытия селективированного адсорбента и возможно связующего на носитель, такой как монолит. В одном воплощении адсорбент можно селективировать в течение от примерно 1 часа до примерно 150 часов, при давлениях от примерно 690 кПа изб. (100 фунтов на кв. дюйм изб.) до примерно 13,8 МПа изб. (2000 фунтов на кв. дюйм изб.), при температурах от примерно 155°С до примерно 350°С путем прямого воздействия высокой концентрации (более 90 мол.%) молекул, выбранных для изменения кинетической селективности адсорбента. Более низкие температуры могут замедлять диффузию молекул, выбранных для селективации, в адсорбент, тогда как температуры, которые являются слишком высокими, могут привести к термическому разложению барьерного соединения. Времена обработки можно уменьшить без термического разложения селективирующих молекул, например, используя температуры от примерно 250°С до примерно 310°С. Чтобы увеличить степень загрузки, может потребоваться использование настолько высокой летучести, насколько это возможно для обработки. Если селективирующие молекулы могут конденсироваться в жидкую фазу, то летучесть обычно не возрастает очень быстро с увеличением давления, и давление обработки можно понизить до значения, немного превышающего (выше более чем на 7 кПа (1 фунт на кв. дюйм)) давление, при котором происходит конденсация. Если фазовый переход в жидкость отсутствует, тогда может потребоваться использование такого давления, при котором летучесть (f) является такой, что произведение b*f больше 10 при температуре селективации. Это условие обычно выполняется, когда селективацию выполняют при давлениях более примерно 3,5 МПа изб. (примерно 500 фунтов на кв. дюйм изб.). Часто может потребоваться использование беспримесного (чистого) соединения для селективации. Когда это осуществляют, может быть предпочтительным, чтобы чистота соединения была выше примерно 95 мол. %, часто выше примерно 99 мол. %. Может быть предпочтительным, чтобы присутствующие примеси не влияли на загрузочные и селективирующие свойства соединения. Когда для селективации используют смесь соединений, может быть предпочтительным, чтобы более примерно 95 мол. % молекул в смеси представляли собой молекулы, предназначенные для загрузки в адсорбент, и чтобы чистота молекул в смеси была выше примерно 99 мол. %. Когда селективация происходит при повышенных давлении и температуре, адсорбент с блокирующим соединением можно загружать внутрь автоклава. Когда используют автоклав (или установку для порционной обработки), может потребоваться время для нагрева и охлаждения автоклава. Чтобы обеспечить свободу технологических действий, не жертвуя производительностью, может потребоваться время обработки в диапазоне от примерно 2 часов до примерно 20 часов. Если используют установку для обработки с высоким давлением / высокой температурой (например, установку для обработки с псевдоожиженным слоем высокого давления), можно достичь более коротких средних времен пребывания. После того как барьерное соединение загружено в адсорбент, адсорбент можно охладить для дополнительной обработки, которая может окончательно внедрить его в слой в контакторе. Так как полагают, что барьерное соединение по меньшей мере частично находится внутри пористой структуры адсорбента, барьерные соединения можно удерживать внутри/среди адсорбента в течение множества циклов короткоцикловой адсорбции. Улучшение кинетической селективности и уменьшение абсолютного коэффициента диффузии легкого компонента можно изменять в зависимости от точного выбора селективирующей молекулы, а также от сочетания условий времени, температуры и давления, выбранных в способе селективации. Таким образом, может потребоваться оптимизация выбора условий путем измерения коэффициента диффузии легкого компонента. Может потребоваться точное измерение этой величины, потому что извлечение легкого компонента может зависеть от абсолютного значения его эффективного коэффициента диффузии. Из-за того, что тяжелый компонент обычно быстро диффундирует, измерение его коэффициента диффузии должно быть достаточно точным для обеспечения достаточной кинетической селективности способа короткоцикловой адсорбции.
Альтернативно, перед внедрением адсорбирующей структуры в слой, адсорбент можно селективировать, подвергая его воздействию барьерного соединения в течение более 150 часов. Из-за более низкой производительности в производстве это представляет собой менее желательный способ изготовления селективированного адсорбента. При более длительном времени воздействия селективацию можно выполнять при более низких температурах и/или более низких давлениях.
Другим вариантом может быть воздействие барьерного соединения на адсорбент после того, как он был внедрен в слой или в компонент, который собирают в слой, используемый в контакторе внутри устройства короткоцикловой адсорбции. Когда слой образуют из содержащих адсорбент гранул, гранулы можно селективировать после того, как их образуют, используя ранее описанную процедуру селективации частиц адсорбента. Когда слои сконструированы для использования в контакторе с параллельными каналами, слои можно селективировать индивидуально, используя ранее описанные процедуры селективации частиц адсорбента. Например, слой в контакторе с параллельными каналами может представлять собой монолит, который был покрыт тонким слоем адсорбента. В таком случае монолит можно селективировать в автоклаве, используя процедуру, описанную для селективации частиц адсорбента. Во всех таких случаях слой можно селективировать перед внедрением в устройство короткоцикловой адсорбции.
Для селективации слоев, содержащих адсорбенты DDR, примеры подходящих барьерных соединений, которые можно нанести, используя описанные процедуры, могут включать (не ограничиваясь перечисленным) н-гексан, 2-метилпентан, 2-метилгексан, гексанол, 2-гексанол, 2-гептанол, 2-октанол, 2-метил-1-пентанол, 2-метил-1-гексанол и их сочетания.
Другим вариантом может являться воздействие барьерного соединения на адсорбент после того, как слои были установлены с образованием контактора. В этом случае может потребоваться возможность нагрева контактора до температуры более 100°С, например, более 150°С, и/или воздействия на контактор барьерного соединения (барьерных соединений) с молекулярной массой по меньшей мере примерно 50 г/моль, например, по меньшей мере примерно 60 г/моль, при более высоких парциальных давлениях, таких как парциальное давление, соответствующее по меньшей мере примерно 25%, например, по меньшей мере примерно 50% или по меньшей мере примерно 90% от давления насыщенного пара барьерного соединения (барьерных соединений). Если температура достаточно высока, так что не присутствует никакой жидкой фазы барьерного соединения (барьерных соединений), то может потребоваться проведение воздействия при давлениях больше примерно 690 кПа изб. (100 фунтов на кв. дюйм изб.) с по меньшей мере 10 мол. % (например, по меньшей мере 50 мол. %) барьерного соединения (барьерных соединений) в потоке. Времена воздействия могут составлять от часов до недель.
Другим вариантом может быть выполнение селективации после того, как контакторы были установлены внутри устройства короткоцикловой адсорбции. В этом случае селективацию можно выполнять, когда контактор находится внутри функционального устройства короткоцикловой адсорбции, с помощью барьерного соединения с молекулярной массой, составляющей по меньшей мере примерно 50 г/моль, например, по меньшей мере примерно 60 г/моль, которое вводят в подаваемый газ при парциальных давлениях больше примерно 10%, например, по меньшей мере примерно 25%, по меньшей мере примерно 50% или по меньшей мере примерно 90% от давления насыщенного пара. Выбор подходящих концентраций барьерного соединения может зависеть, в том числе, от выбора барьерного соединения, продолжительности цикла, температуры, при которой проводят процесс разделения, и продолжительности обработки. Времена обработки могут составлять от суток до месяцев. Способы, с помощью которых барьерные соединения можно ввести в поток газового сырья, могут включать непосредственное впрыскивание и/или использование испарителей, таких как барботеры. Может быть предпочтительным добавление барьерных соединений в поток сырья, даже если, в некоторых случаях, барьерные соединения уже могут присутствовать. По мере селективации адсорбента в результате воздействия барьерных соединений характеристика устройства короткоцикловой адсорбции может выгодно изменяться. Может потребоваться регулирование и планирование скорости изменения характеристики. После того, как характеристика достигла требуемого значения, концентрацию барьерного соединения в потоке сырья можно уменьшить. В некоторых случаях небольшой поддерживающий уровень барьерного соединения можно добавлять в сырье для улучшения долговременной стабильности селективации. Целью выбранных условий может быть обеспечение поступления барьерного соединения в сеть пор для улучшения кинетической селективности адсорбента, понижая таким образом коэффициент диффузии легкого компонента. Также может потребоваться поддержание селективации между циклами таким образом, который не вызывает избыточного накапливания барьерного соединения на поверхности адсорбента.
Другим вариантом селективации может быть включение барьерного соединения в отдельный газовый поток, проходящий через контактор после того, как он установлен внутри работающего устройства короткоцикловой адсорбции. Этот поток может отличаться от потока сырья; в этом случае устройство не должно действовать таким образом, чтобы производить разделение потока. В связи с этим, последовательность действий клапанов в устройстве не обязательно должна быть такой же, которую использовали для способа короткоцикловой адсорбции. Потоки, содержащие барьерное соединение, можно рециркулировать и отправить обратно через устройство, или их можно использовать однократно. Когда поток рециркулируют, барьерное соединение можно пополнить либо путем прямого впрыскивания, либо с использованием испарителей, таких как барботеры. Потоки, содержащие барьерное соединение, можно направить через устройство при температуре больше той, которую используют в способе короткоцикловой адсорбции. Аналогично, устройство можно нагревать, в то время как селективирующий поток направляют через устройство. В любом случае, может потребоваться воздействие селективирующих молекулярных соединений при температурах более 100°С, например, более 150°С. Концентрации барьерного соединения могут быть выше, чем в случае, когда его включают в подачу в устройство, выполняющее разделение. В таком случае, может быть предпочтительно, чтобы воздействие выполняли при более высоких парциальных давлениях барьерных соединений, таких как по меньшей мере примерно 25%, например, по меньшей мере примерно 50% или по меньшей мере примерно 90% от давления насыщенного пара. Если температура достаточно высока, так что не присутствует никакой жидкой фазы барьерного соединения, то может потребоваться провести воздействие при давлениях более примерно 690 кПа изб. (100 фунтов на кв. дюйм изб.) с по меньшей мере 10 мол. % (например, по меньшей мере 50 мол. %) барьерного соединения в потоке. Времена воздействия могут составлять от часов до недель.
Любые два или более вариантов можно по желанию поочередно объединять для обеспечения улучшенной селективности.
Другие воплощения
Дополнительно или альтернативно, настоящее изобретение может включать одно или более из следующих воплощений.
Воплощение 1. Способ выполнения разделения газов, включающий: приведение адсорбента или мембраны, содержащих цеолит с 8-членными кольцами или микропористый материал с 8-членными кольцами, в контакт с барьерным соединением при условиях, эффективных для селективации адсорбента или мембраны, где барьерное соединение имеет минимальный размер, составляющий от примерно 4,05 Å до примерно 5,65 Å, и максимальный размер, составляющий примерно 25 Å или менее, для цеолита с 8-членными кольцами или микропористого материала с 8-членными кольцами; приведение селективированного адсорбента или мембраны в контакт с входящим потоком газа, содержащим первый компонент и второй компонент, с образованием первого потока газа, обогащенного первым компонентом по отношению к входящему потоку газа; и сбор второго потока газа, обогащенного вторым компонентом по отношению к входящему потоку газа.
Воплощение 2. Способ по воплощению 1, в котором цеолит с 8-членными кольцами представляет собой цеолит типа DDR, Sigma-1, ZSM-58 или их сочетание.
Воплощение 3. Способ по любому из предшествующих воплощений, в котором барьерное соединение представляет собой гликоль, амин, спирт, алкан, серосодержащее соединение или их сочетание, причем барьерное соединение имеет молекулярную массу, составляющую по меньшей мере 50 г/моль.
Воплощение 4. Способ по любому из предшествующих воплощений, в котором барьерное соединение представляет собой этиленгликоль, триэтиленгликоль, метилдиэтиламин, диметилэтиламин, диметилдисилан, н-гексан, 2-октанол или их сочетание.
Воплощение 5. Способ по воплощению 1, в котором первый компонент содержит или представляет собой СН4.
Воплощение 6. Способ по любому из предшествующих воплощений, в котором второй компонент содержит или представляет собой СО2, N2 или их сочетание.
Воплощение 7. Способ по воплощению 1, в котором эффективные условия приведения адсорбента или мембраны в контакт с барьерным соединением включают температуру от примерно 50°С до примерно 350°С и полное давление от примерно 690 кПа изб. (примерно 100 фунтов на кв. дюйм изб.) до примерно 13,8 МПа изб. (примерно 2000 фунтов на кв. дюйм изб.), причем блокирующее соединение присутствует либо в виде жидкости, либо в виде газа с парциальным давлением блокирующего соединения, которое составляет по меньшей мере примерно 10% от давления насыщенного пара.
Воплощение 8. Способ по воплощению 7, в котором эффективные условия приведения адсорбента или мембраны в контакт с барьерным соединением включают температуру, составляющую по меньшей мере примерно 150°С, такую как по меньшей мере примерно 250°С.
Воплощение 9. Способ по любому из предшествующих воплощений, в котором приведение селективированного адсорбента в контакт с входящим потоком газа включает адсорбцию селективированным адсорбентом по меньшей мере части второго компонента в течение приведения в контакт, причем способ дополнительно включает десорбцию по меньшей мере части адсорбированного второго компонента с образованием десорбированной части второго компонента, причем поток второго газа содержит по меньшей мере часть десорбированной части второго компонента.
Воплощение 10. Способ по любому из предшествующих воплощений, дополнительно включающий десорбцию по меньшей мере части барьерного соединения в течение приведения селективированного адсорбента или мембраны в контакт с входящим потоком газа.
Воплощение 11. Способ по любому из предшествующих воплощений, в котором адсорбент является частью устройства короткоцикловой адсорбции, причем устройство короткоцикловой адсорбции представляет собой устройство адсорбции с перепадом давления или устройство адсорбции с перепадом температуры.
Воплощение 12. Способ по воплощению 11, в котором устройство короткоцикловой адсорбции представляет собой устройство адсорбции с перепадом давления с частым циклом или устройство адсорбции с перепадом температуры с частым циклом.
Воплощение 13. Способ по воплощению 11 или 12, дополнительно включающий повторение указанных приведения в контакт, десорбции и сбора в течение множества циклов.
Воплощение 14. Способ по любому из воплощений 1-8 или 10, в котором первый поток газа представляет собой поток ретентата, а второй поток газа представляет собой поток пермеата.
Воплощение 15. Способ по любому из предшествующих воплощений, в котором количество барьерного соединения, адсорбированного микропористым материалом, составляет примерно 20% или менее от насыщающей загрузки (qs).
Воплощение 16. Способ выполнения разделения газов в устройстве короткоцикловой адсорбции, включающий: приведение адсорбента, содержащего микропористый материал, в контакт с барьерным соединением в устройстве короткоцикловой адсорбции при условиях, эффективных для селективации адсорбента, причем микропористый материал имеет поры, характеризующиеся первым размером наибольшей твердой сферы, которая может диффундировать вдоль любого направления в порах, а барьерное соединение имеет второй размер, представляющий собой минимальный размер соединения, причем второй размер на 10-60% больше первого размера; приведение селективированного адсорбента в контакт с входящим потоком газа, содержащего первый компонент и второй компонент, с образованием выходящего потока газа, обогащенного первым компонентом по отношению к входящему потоку газа, при этом селективированный адсорбент адсорбирует по меньшей мере часть второго компонента в течение приведения в контакт; десорбцию по меньшей мере части адсорбированного второго компонента с образованием десорбированной части второго компонента; и сбор газового потока, содержащего по меньшей мере часть десорбированной части второго компонента, при этом газовый поток обогащен вторым компонентом по отношению к входящему потоку газа, и, возможно, включает объект изобретения по одному или более из воплощений 3-15.
Примеры
Пример 1. Селективация кристаллов DDR путем длительного воздействия паров барьерных соединений при температурах ниже 150°С
Селективация адсорбирующего материала может подавить адсорбцию более легкого компонента, такого как СН4, в большей степени, чем более тяжелого компонента, такого как СО2 и/или N2. Уменьшение величины коэффициента диффузии более легкого компонента может играть значительную роль в улучшении извлечения в способах мембранного разделения и короткоцикловой адсорбции. Таким образом, хотя адсорбция как более легкого, так и более тяжелого компонентов может быть снижена, может оказаться особенно выгодным снижение относительной скорости адсорбции СН4 (или другого более легкого компонента) в большей степени, чем для более тяжелого компонента.
Различие между адсорбцией СН4 и адсорбцией СО2 и/или N2 цеолитовыми адсорбентами с 8-членными кольцами можно видеть в различии на порядок величины (или больше) коэффициентов диффузии различных компонентов. Наблюдали, что цеолиты DDR с 8-членными кольцами, полученные в различных синтезах, могут иметь значительно отличающиеся коэффициенты диффузии для СН4, при этом сохраняя большое соотношение между коэффициентами диффузии для СО2 и СН4. В данном примере обсуждают перенос и селективацию, которые характерны для трех различных партий кристаллов DDR с высокими отношениями Si/Al (>~100), для которых было обнаружено, что они имеют сходные коэффициенты диффузионного переноса. Каждая партия кристаллов имеет относительно однородный размер частиц. Характеристический размер для партии с кристаллами наименьших размеров составлял ~2 мкм, а характеристический размер для партии с кристаллами наибольших размеров составлял ~30 мкм. Большая часть представленных результатов селективации получена для партии с характеристическим размером кристаллита (частицы) ~16 мкм. Полагают, что обсуждаемые в данном документе характеристики селективации также применимы для других приготовлений DDR материалов с различными коэффициентами диффузии СН4 в только что синтезированных кристаллах. Также полагают, что данные этого примера применимы для селективации других цеолитов.
В этом примере для цеолитов типа DDR с 8-членными кольцами было обнаружено, что коэффициенты диффузионного переноса для СН4 при температурах от примерно 50°С до примерно 100°С составляют от примерно 1×10-8 см2/с до менее чем 1×10-9 см2/с. Наоборот, было обнаружено, что в этом же температурном диапазоне коэффициенты диффузионного переноса для CO2 составляют от примерно 1×10-6 см2/с до примерно 1×10-7 см2/с. Коэффициент диффузионного переноса для N2 был такого же порядка величины, как и коэффициент диффузионного переноса для CO2, но меньше менялся с изменением температуры. В результате, диффузия CO2 и/или N2 в цеолитовом адсорбенте с 8-членными кольцами происходит за более короткое время по сравнению с намного более медленной диффузией СН4. Из-за более высоких скоростей диффузии на адсорбцию CO2 и/или N2 могут в большей степени влиять свойства равновесной диффузии, тогда как на адсорбцию СН4 могут в большей степени влиять свойства кинетической диффузии. Таким образом, метод подавления кинетической диффузии может скорее всего оказывать большее воздействие на адсорбцию СН4, чем на адсорбцию CO2 и/или N2.
Одной технологией исследования адсорбционных свойств адсорбента является хроматография с нулевой длиной. В хроматографии с нулевой длиной (ХНД) определяют коэффициенты диффузии из измерений скоростей, с которыми адсорбированные молекулы удаляются из образцов после быстрого переключения с условий адсорбции на условия десорбции. Анализ данных методов хроматографии с нулевой длиной описан, например, в D.М. Ruthven "Principles of Adsorption and Adsorption Processes", John Wiley, NY (1984) и в J. Karger and D.M. Ruthven "Diffusion in Zeolites and Other Microporous Solids", John Wiley, NY (1992). Пример данных хроматографии с нулевой длиной для чистого компонента на кристаллах DDR одинаковых размеров показан на Фиг. 1. Используемая в этом эксперименте установка ХНД была модифицирована по сравнению с традиционно используемой в литературе, так чтобы она вмещала и действовала с большим количеством образца, чем указано в литературе.
Данные, показанные на Фиг. 1, представляют собой диффузию этана из кристаллов DDR при ~50°С в поток Не с изменением потока через ячейку ХНД. Кристаллы DDR имели средний размер примерно 16 мкм. Поток через ХНД изменяли от ~5,2 мл/мин до ~26 мл/мин, как показано на чертеже. На Фиг. 1 на вертикальной оси показан логарифм отношения концентрации этана, диффундирующего из кристаллов DDR, к величине диффузии этана в нулевой момент времени. Таким образом, на Фиг. 1 показано изменение величины диффузии из кристаллов в зависимости от времени. Для каждой кривой на Фиг. 1 показаны как измеренные значения, так и модельные аппроксимации этих значений.
Как показано на Фиг. 1, модели, использующие процесс однокомпонентной диффузии через весь кристалл, по-видимому, соответствуют наборам данных, полученных для диффузии СН4, СО2 и С2Н6 в DDR. Для известного одинакового размера кристаллов модельные аппроксимации включали два параметра. Одним параметром был коэффициент диффузии, а вторым параметром была постоянная Генри для молекулярной адсорбции. В модельных аппроксимациях постоянную Генри приводили в соответствие с экспериментально определенной постоянной Генри с помощью независимых измерений равновесной адсорбции. Данную величину согласовывали с данными, также соответствующими постоянной Генри, полученной из теоретических расчетов. Модельные аппроксимации данных для СО2 и СН4 показывают, что для кристаллов DDR перенос массы в основном регулировался диффузией через объем кристалла.
Исследования ХНД также можно использовать для изучения диффузии из кристаллов, которые были подвергнуты воздействию одного или более барьерных соединений и/или загрязняющих веществ. В качестве начального испытания кристаллы DDR подвергали воздействию базовой газовой смеси, содержащей СО2, H2S, СН4 и, в некоторых случаях, небольшие количества С2-С7 компонентов, в течение ~1 месяца. Кристаллы DDR подвергали воздействию базовой газовой смеси при давлении примерно 5,9 МПа изб. (примерно 850 фунтов на кв. дюйм изб.) и температуре ~100°С. На Фиг. 2 показан набор данных ХНД для диффузии метана из кристаллов DDR после загрязняющего воздействия базовой смеси. В модельных аппроксимациях на Фиг. 2 использовали параметры, аналогичные параметрам для свежих кристаллов. Как показано на Фиг. 2, воздействие базовой газовой смеси привело к небольшому изменению или не привело к изменению измеренной диффузии метана по отношению к модели процесса однокомпонентной диффузии.
Воздействие базовой газовой смеси также, по-видимому, оказывает минимальное воздействие или не оказывает никакого воздействия на адсорбцию СО2. На Фиг. 3 показан пример изотерм адсорбции СО2 для кристаллов DDR в свежем состоянии и после воздействия некоторых типов базовых газов. Из-за более быстрой диффузии CO2 в DDR, изотерма адсорбции предоставляла ясное указание на различия в адсорбционной активности. Как показано на Фиг. 3, изотермы адсорбции для CO2 в кристаллах DDR, подвергнутых воздействию различных типов базовых газов, сравнимы с изотермой адсорбции для свежих кристаллов.
Данные на Фиг. 2 и Фиг. 3 показывают, что воздействие CO2, H2S и H2O, по-видимому, не оказывает значительного воздействия на адсорбционные характеристики кристаллов DDR. Этот вывод отличается от барьерных соединений по настоящему изобретению, которые изменяют характеристики переноса таких кристаллов.
Выполнили дополнительные ХНД исследования переноса СН4 в кристаллах DDR, в которых дополнительное одиночное барьерное соединение и/или загрязняющее вещество было включено в базовую газовую смесь. Условия воздействия в остальном были аналогичны упомянутым выше условиям воздействия базовых газов. Также были получены изотермы адсорбции CO2 для кристаллов DDR, подвергнутых воздействию базовых газов, включающих различные барьерные соединения и/или загрязняющие вещества, при давлении их насыщенного пара в базовой газовой смеси или вблизи него.
Помимо указанных выше исследований ХНД и изотерм адсорбции CO2, было показано изменение как адсорбции СН4, так и адсорбции CO2 для нескольких барьерных соединений. Барьерные соединения, которые влияли на адсорбционные характеристики, включали этиленгликоль, триэтиленгликоль, диметилдисульфид (ДМДС), гексан, метилдиэтиламин (МДЭА) и диметилэтиламин (ДМЭА). В отличие от этого, дополнительные исследования ХНД и изотерм адсорбции CO2 показали небольшое воздействие или не показали никакого воздействия на адсорбционные свойства DDR для некоторых загрязняющих веществ с характеристическим (минимальным) размером, превышающим размеры барьерных соединений. Например, кристаллы DDR, подвергнутые воздействию толуола, N-метилпирролидона, циклогексиламина и бутиламина, не показали какого-либо значительного изменения адсорбции СО2.
Изучали изменение кинетики переноса массы для образцов, селективированных ДМДС, МДЭА и ДМЭА. Полагали, что селективация частично обусловлена поступлением барьерных соединений в поры адсорбента, что приводит к пониженной вероятности диффузии СН4 в кристаллах. Для иллюстрации получили наглядный пример воздействия барьерного соединения на перенос СН4 путем селективации цеолитового адсорбента DDR с использованием МДЭА. В этом примере кристаллы цеолита DDR селективировали путем воздействия на кристаллы цеолита DDR в течение примерно одного месяца при температуре ~100°С базовой газовой смеси, которая изначально была приведена в контакт с резервуаром с жидким МДЭА. Жидкость не контактировала с адсорбентом и служила для насыщения базовой газовой смеси МДЭА. Количество МДЭА, содержащегося в резервуаре, более чем в 50 раз превышало количество молекул, требуемое для насыщения базовой газовой смеси. Насыщенный пар МДЭА в этом эксперименте имел концентрацию МДЭА в газовой фазе более чем в 5000 раз превышающую концентрации, ожидаемые при эксплуатации устройств короткоцикловой адсорбции при обработке природного газа.
На Фиг. 4 показаны исследования ХНД для кристаллов DDR после различных обработок. На Фиг. 4 график «базовой линии» показывает пример результатов измерений ХНД без внедрения адсорбирующего материала для улавливания метана. Кривая свежего образца показывает измеренную диффузию метана для кристаллов DDR до воздействия селективирующего агента. Кривая подвергнутого воздействию МДЭА образца соответствует кристаллам DDR, селективированным МДЭА, как описано выше. Как показано на Фиг. 4, диффузия метана из селективированных кристаллов DDR сначала была ниже, чем для неселективированных кристаллов. Однако диффузия из селективированных кристаллов DDR затем стабилизировалась и имела более пологий наклон по сравнению с неселективированными кристаллами.
На Фиг. 5 показаны дополнительные исследования ХНД при различных расходах СН4 для описанных выше кристаллов, селективированных МДЭА. Помимо величины диффузии, измеренной методом ХНД, на Фиг. 5 также показана аппроксимация части кривой с пологим наклоном с использованием модели диффузии с «поверхностным барьером». Как показано на Фиг. 5, модель поверхностного барьера предоставляет разумную аппроксимацию для длинного хвоста кривой диффузии. Это указывает на то, что воздействие МДЭА оказало влияние, аналогичное образованию поверхностного барьера на кристаллах DDR.
Помимо изменения характеристик диффузии СН4, МДЭА также изменяет характеристики адсорбции CO2. На Фиг. 6 показаны изотермы адсорбции СО2 как для неселективированных, так и для селективированных кристаллов DDR. Как показано на Фиг. 6, селективация МДЭА в присутствии или отсутствии воды приводила к сравнимым уровням селективации. Кристаллы DDR, подвергнутые воздействию МДЭА, показывали приблизительно 30%-ное уменьшение количества адсорбированного CO2 по сравнению с неселективированными кристаллами.
В качестве дополнительного исследования изучали степень селективации кристаллов DDR с использованием эксперимента по циклической селективации. В данном эксперименте N2 барботировали через барьерное соединение или загрязняющее вещество. Поток N2 затем проходил в ячейку, содержащую кристаллы DDR. Это подвергало кристаллы воздействию барьерного соединения. Периодически поток N2 останавливали и вводили газ, содержащий CO2, N2 и СН4. Продолжительность цикла установки составляла примерно 1-20 секунд. Рабочую производительность или адсорбцию кристаллов в течение длительного времени сравнивали с начальной адсорбцией кристаллов до воздействия барьерного соединения.
На Фиг. 7 показано изменение рабочей производительности кристаллов DDR со временем, по мере того как кристаллы циклически подвергали воздействию н-гексана. Как показано на Фиг. 7, рабочая производительность кристаллов для адсорбции N2 в течение всей процедуры составляла по меньшей мере примерно 70% от начальной рабочей производительности. Для CO2 рабочая производительность в течение всей процедуры составляла по меньшей мере примерно 80% от начальной рабочей производительности. Это показывает, что селективация гексаном оказывала умеренное воздействие на адсорбцию CO2 и N2 в течение циклов с продолжительностью примерно 1-20 секунд. Это не было неожиданным, так как время установления равновесия для СО2 и N2 составляет порядка 0,1 секунды, так что количество адсорбируемых CO2 и N2, по-видимому, приближалось к равновесным уровням в течение этих циклов. Наоборот, количество СН4, адсорбированное после начала циклического воздействия н-гексана, было значительно ниже. Как показано на Фиг. 7, количество СН4, адсорбированного селективированными кристаллами DDR, составляло менее примерно 20% от количества, адсорбированного неселективированными кристаллами. Это показывает, что н-гексан, по-видимому, селективировал кристаллы DDR, так что адсорбция СН4 была подавлена в большей степени, чем адсорбция CO2 и N2.
Аналогичные исследования циклического загрязнения или циклической селективации также выполняли с использованием метанола, толуола и воды в качестве загрязняющего вещества или барьерного соединения. Циклическое загрязнение проводили путем воздействия на кристаллы паров загрязняющего вещества при активности 50% от насыщения, при примерно 100°С, в потоке азота, давление которого изменяли от примерно 1,0 МПа изб. (примерно 150 фунтов на кв. дюйм изб.) до примерно 130 кПа изб. (примерно 20 фунтов на кв. дюйм изб.) каждые примерно 10-50 секунд. В этих дополнительных исследованиях циклического загрязнения было обнаружено, что воздействие метанола, толуола или воды в течение промежутков времени, больших одной недели, по-видимому, не влияло значительным образом на рабочую производительность кристаллов DDR.
Полагают, что резкое изменение рабочей производительности для СН4 и только умеренное изменение рабочих производительностей для CO2 и N2 обусловлено по меньшей мере частичным поступлением гексана в сеть пор адсорбента. Тот факт, что гексан действует как барьерное соединение, был установлен из измерений коэффициентов диффузии при примерно 30°С. Как показано на Фиг. 8, коэффициенты диффузии для алканов, содержащих 3 или более атомов углерода, были существенно меньше, чем коэффициенты диффузии для метана или этана.
В экспериментах по циклическому загрязнению, выполненных при примерно 100°С с н-гексаном при примерно 50% от его давления насыщенного пара, полагали, что сильный адсорбционный фронт продвигался в кристаллах DDR на расстояние менее (D*t)1/2. В силу низкого значения коэффициента диффузии гексана, максимальное расстояние проникновения при воздействии в течение примерно 350 часов составляло примерно 150 Ангстрем. Таким образом, полагают, что все изменения переноса были обусловлены тонким слоем адсорбированного гексана внутри сети пор кристаллов DDR вблизи поверхности. При продолжительности цикла, используемой в исследованиях загрязнения, кинетическая селективность DDR повышается по меньшей мере в 5 раз для разделений СО2/СН4 и по меньшей мере в 4 раза для разделений N2/CH4. Из-за относительно большой продолжительности цикла и характера описания экспериментов, ожидают, что в способах разделения короткоцикловой адсорбцией можно достичь повышения селективности в 5-10 раз.
Было проведено моделирование воздействия селективации на кинетически регулируемые способы короткоцикловой адсорбции, осуществляемые с DDR. Результаты моделирования показали, что при удалении большей части кислого газа или N2 селективация увеличивала извлечение метана путем понижения концентрации метана в богатом СО2 или N2 возвратном потоке. Селективация также может уменьшить загрязнение DDR молекулярными соединениями, такими как амины, ДМДС, этилен гликоль, триэтиленгликоль, МеОН, карбоновые кислоты и N-метилпирролидон. Полагают, что селективация поверхности кристаллов может подавить или минимизировать поступление загрязняющих веществ в поры кристаллов.
Пример 2. Селективация кристаллов DDR путем краткосрочного воздействия высоких концентраций моно- и диразветвленных алканов при температурах выше 250°С.
Размер моно- и диразветвленных алканов был таким, что не ожидали, что они могли бы войти в поры DDR, на основании опубликованного IZA размера твердой сферы, которая может проходить через поры. Однако фундаментальные молекулярные моделирования гибкости каркасов DDR указывают на то, что пористая структура иногда изгибается до размера, в который они могут поступать. Из моделирования гибкости каркаса все же не было ясно, могут ли они перемещаться в каркасе даже при высоких температурах.
Для испытания того, могут ли моно- и диразветвленные алканы диффундировать в DDR для того, чтобы в достаточной степени заполнить поры с образованием слоя селективации, выбрали процедуру высокотемпературной (~290°С) селективации, потому что ожидали, что диффузия стерически затрудненных молекул в DDR является высокоактивированным процессом, который должен происходить на порядки величины быстрее при температуре примерно 290°С, чем при комнатной температуре (примерно 20-25°С).
Для исследования селективации моно- и диразветвленными алканами использовали партию DDR, отличную от той, которую обсуждали в примере 1. Эта партия кристаллов DDR имела отношение Si/Al>250, и было обнаружено, что она имеет значительно более высокие коэффициенты диффузии для СН4, чем те, которые обсуждали в примере 1. Кристаллы в данной партии имели дискообразную форму и примерно одинаковый размер. Полагали, что двумерная структура связанных пор, обеспечивающая перенос молекул CO2 и СН4, находится в плоскости диска. Характеристический размер переноса в плоскости диска составлял примерно 7-9 мкм.
Для селективации четверть грамма образцов только что синтезированных кристаллов DDR загружали в ячейку, работающую под давлением, диаметром примерно 3 мм (~1/8 дюйма), соединенную с резервуаром под давлением, который был заполнен 25 граммами жидкой фазы моно- или диразветвленного алкана, выбранного для селективации. Чистота жидкостей, используемых в этих экспериментах, составляла более 99%. Для селективации ячейку, содержащую цеолит, заполняли жидкостью, повышали давление до примерно 4,8 МПа изб. (примерно 700 фунтов на кв. дюйм изб.), а затем нагревали до ~290°С. После того, как образцы выдерживали при данной температуре в течение намеченного периода времени, ячейку быстро охлаждали и извлекали селективированный порошок DDR. Перед проведением исследований переноса или ТГА (термогравиметрического анализа), избыток молекул удаляли, помещая порошок в продуваемую азотом печь при ~70°С в течение по меньшей мере ~2 часов, а затем помещая образец в вакуумную печь, поддерживаемую в диапазоне от ~60°С до ~70°С, в течение ~12 часов.
Для того чтобы определить, достаточное ли количество селективирующих молекул было захвачено в DDR, с помощью измерений ТГА определяли массовый процент селективирующих молекул, внедренных в цеолит. При ТГА селективированные порошки в количестве нескольких миллиграммов нагревали в потоке азота до ~120°С для удаления таких веществ, как вода и СО2, которые могли адсорбироваться в образце. Образцы затем выдерживали при ~120°С в течение приблизительно одного часа, чтобы убедиться в том, что масса образца была стабильна и что больше никакие соединения не продолжали десорбироваться. Затем температуру линейно повышали со скоростью ~6°С/мин до температуры ~600°С, выдерживали при этой температуре в течение ~1 часа, а затем быстро охлаждали до ~120°С. Разницы масс, зарегистрированные при ~120°С перед линейным повышением температуры и после него, использовали для оценки потери массы, которая происходила, когда образец нагревали и выдерживали при ~600°С. Полагали, что эта последовательность действий устраняет ошибки от эффекта плавучести при ТГА. В таблице ниже показана потеря массы при ТГА для селективации порошка DDR различными молекулами. По-видимому, эта потеря массы происходит как из-за десорбции селективирующих молекул при высокой температуре, так и из-за потери массы, связанной с изменениями в дефектах, таких как гидроксильные группы в кристаллической решетке DDR. Чтобы более точно оценить адсорбцию селективирующих молекул, образец обрабатывали без присутствия селективирующих молекул. Потерю массы этого образца использовали для определения потери массы, обусловленной изменениями в дефектах, таких как гидроксильные группы в кристаллической решетке DDR. С использованием его в качестве сравнительного образца, в таблице 1 ниже показано поглощение (в масс. %) селективирующих молекул в DDR. Если бы решетка DDR была полностью заполнена любой из этих молекул, то изменение массы составляло бы более 5 масс. %.
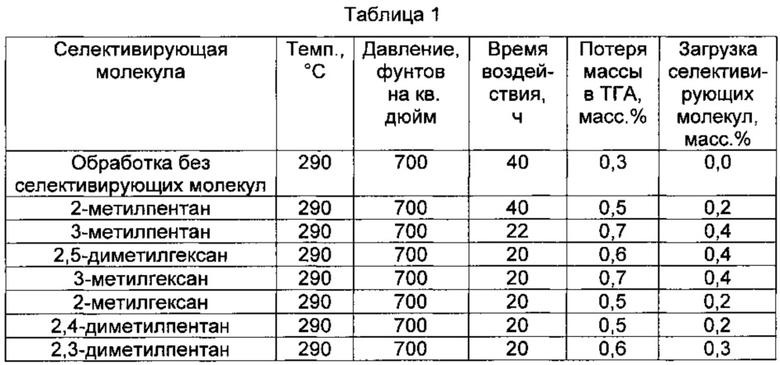
Чтобы продемонстрировать, что эти умеренные уровни загрузки селективирующих молекул могут значительно понизить коэффициент диффузии метана, провели эксперименты ХНД на трех селективированных образцах и на только что синтезированном DDR. Форма кривой ХНД для только что синтезированного материала не совпадала с ожидаемой теоретической формой, а аппроксимации различных участков кривой дали коэффициенты диффузии СН4 при ~30°С, составляющие от примерно 8×10-13 м2/с до примерно 50×10-13 м2/с. Аппроксимации этих участков кривой интерпретировали как описание того, как молекулы при различных загрузках выводятся из цеолита. Принимали, что средний по загрузке коэффициент диффузии СН4 этих аппроксимаций составляет ~15×10-13 м2/с. Исследования однокомпонентной АПД для пленки, изготовленной из этого цеолита, подтверждали более высокий средний коэффициент диффузии в диапазоне ~30*10-13 м2/с при условиях испытания АПД ~10,1 МПа изб. (~10 бар) и ~22°С. Для всех трех селективированных образцов форма кривой ХНД соответствовала ожидаемой теоретической форме. Образец, селективированный 2-метилпентаном, имел коэффициент диффузии СН4 при ~30°С, составляющий ~2,2×10-13 м2/с. Повторные измерения образца DDR, селективированного 3-метилпентаном, дали коэффициенты диффузии СН4 при ~30°С, составляющие ~2,2*10-13 м2/с и - 2,5×10-13 м2/с. Повторные измерения образца DDR, селективированного 2,5-диметилгексаном, дали коэффициенты диффузии СН4 при ~30°С, составляющие примерно 1,6×10-13 м2/с и примерно 1,9×10-13 м2/с.
Пример 3. Селективация пленок DDR путем краткосрочного воздействия высоких концентраций моноразветвленных алканов при температурах выше 250°С Пример 3 включает воздействие барьерного соединения на адсорбент после того, как адсорбент был включен в слой или в компонент, который можно собрать в слой и использовать в контакторе внутри устройства короткоцикловой адсорбции.
В данном примере использовали партию кристаллов DDR, отличающуюся от партий в примерах 1 и 2 тем, что эта партия кристаллов DDR имела более широкое распределение частиц по размерам. Эта партия кристаллов DDR также имела характеристический размер ~13 мкм и коэффициент диффузии СН4, измеренный с помощью ХНД при ~30°С, составляющий ~12×10-13 м2/с.
Пленки с толщиной приблизительно 200 мкм отливали из суспензии, состоящей из связующего, представляющего собой коллоидный диоксид кремния, и кристаллов DDR, с использованием ножевого устройства для нанесения их на плоскую полированную стальную пластину, которая предварительно была покрыта тонким (<25 мкм) слоем диоксида циркония для улучшения адгезии. После нанесения пластину нагревали до ~150°С для отверждения покрытия. Было установлено, что открытые поры занимали менее примерно 30 об.% отвержденной пленки, а масса DDR более чем в 15 раз превышала массу связующего. Стальная пластина имела ширину примерно 48 мм (~1,9 дюйма) и длину примерно 127 мм (~5 дюймов). В процессе профилирования края пластины были закрыты так, чтобы ширина пленки на пластине составляла примерно 40 мм (~1,6 дюйма). Непокрытые края пластины использовали для заделывания пластины в ячейку, которую можно было установить в устройство однокомпонентной адсорбции с перепадом давления. После того, как пластина была заделана в ячейку, толщина проточного канала, который был оставлен поверх пленки, составляла приблизительно 250 мкм.
Эксперименты по однокомпонентной адсорбции с перепадом давления сначала выполняли при комнатной температуре (примерно 20-25°С) и при ~50°С, чтобы охарактеризовать свойства переноса только что синтезированной пленки. При каждой температуре проводили отдельные эксперименты с СО2, СН4, N2 и Не. В каждом эксперименте адсорбент подвергали циклическому повышению давления до примерно 863 кПа изб. (примерно 125 фунтов на кв. дюйм изб.) и сбросу давления до примерно 170 кПа изб. (примерно 25 фунтов на кв. дюйм изб.). Измерения проводили после того, как был достигнут установившийся циклический режим работы. Повышение давления выполняли путем открывания клапана, соединяющего резервуар, находящийся под давлением ~1,0 МПа изб. (~150 фунтов на кв. дюйм изб.) и заполненный насадкой (уменьшающей изменения температуры), с ячейкой, содержащей адсорбент, при давлении ~170 кПа изб. (~25 фунтов на кв. дюйм изб.). Спустя примерно 0,25 секунды клапан закрывали, при этом давление в резервуаре падало до примерно 863 кПа изб. (примерно 125 фунтов на кв. дюйм изб.), а давление в ячейке возрастало до примерно 863 кПа изб. (примерно 125 фунтов на кв. дюйм изб.). Точные измерения действительного возрастания и падения давления в резервуаре и ячейке и температур использовали в сочетании с измерениями поведения системы с неадсорбируемым газом (то есть, Не) для получения количества перемещенных молей и количества молей, поглощенных адсорбентом. Ячейку герметизировали примерно на 30 секунд для наблюдения за любыми медленными процессами адсорбции, которые могли производить зависящие от времени изменения количества молей, поглощенных адсорбентом. Точные измерения изменений давления и температуры в герметизированной ячейке использовали в сочетании с измерениями поведения системы с неадсорбируемым газом (то есть, Не) для количественного определения зависящих от времени изменений загрузки. Затем использовали приближение ЛДФ (линейной дискриминантной функции) для преобразования любого наблюдаемого изменения в эффективный коэффициент диффузии. Наименьший временной промежуток, на котором можно проводить этот тип анализа, составляет примерно 0,25-0,5 секунды. Это предоставляет верхнюю границу эффективного коэффициента диффузии, который можно измерить. После поддержания ячейки в герметизированном состоянии в течение ~30 секунд, примерно на 10 секунд открывали клапан в резервуар пониженного давления, изначально находящийся при ~7 кПа изб. (~1 фунт на кв. дюйм изб.). В течение этого времени давление в ячейке и резервуаре пониженного давления выравнивалось до примерно 170 кПа изб. (примерно 25 фунтов на кв. дюйм изб.). После сброса давления длительностью ~10 секунд клапан между резервуаром пониженного давления и ячейкой закрывали, и ячейку герметизировали еще приблизительно на 10 секунд, ожидая начала нового цикла. Каждый последующий цикл имел такой же хронометраж действия клапанов, как и первый. Перед началом каждого цикла давления в питающем резервуаре и в резервуаре пониженного давления возвращали в исходное состояние.
В измерениях АПД CO2 и N2, по-видимому, полностью приходили в равновесие менее чем за 0,25 секунды. По существу, их коэффициенты диффузии были слишком большими для того, чтобы их можно было измерить, предоставляя нижнюю границу ~2×10-11 м2/с для эффективных коэффициентов диффузии CO2 и N2 в кристаллах DDR в только что синтезированной пленке. Для СН4 давление изменяли в ячейке таким образом, что можно было приблизительно подобрать коэффициент переноса массы, используя приближение ЛДФ. Эффективный коэффициент диффузии СН4, полученный приближением ЛДФ из результатов эксперимента при комнатной температуре, составлял приблизительно 35×10-13 м2/с. Это приблизительно в три раза больше, чем измерение методом ХНД при ~30°С. ХНД является измерением при низком давлении, и известно, что эффективные коэффициенты диффузии могут зависеть от давления.
После измерения коэффициентов диффузии в только что синтезированной пленке, пленку удаляли из устройства однокомпонентной АПД и селективировали 3-метилпентаном, используя процедуру, аналогичную той, которая описана в примере 2. Селективацию выполняли при ~4,8 МПа изб. (~700 фунтов на кв. дюйм изб.) и ~290°С в течение ~96 часов в автоклаве, который был достаточно большим, чтобы вмещать стальную пластину.
После селективации пленку повторно загружали в устройство однокомпонентной АПД и повторяли измерения. Было обнаружено, что CO2 и N2 полностью приходили в равновесие менее чем за 0,25 секунды аналогично тому, что наблюдали для только что синтезированной пленки. По существу, процесс селективации не привел к обнаруживаемым изменениям в кинетике для коэффициентов диффузии CO2 и N2. Коэффициент диффузии метана, определенный из аппроксимаций ЛДФ, понизился примерно в 4,2 раза как при комнатной температуре, так и при 50°С. При комнатной температуре эффективный коэффициент диффузии СН4 в DDR, селективированном 3-метилпентаном, составлял приблизительно 8×10-13 м2/с.
Пример 4. Селективация кристаллов DDR путем краткосрочного воздействия высоких концентраций линейных алканов при температурах выше 250°С В данном примере использовали материал DDR и способ селективации, описанные в примере 2. Было обнаружено, что селективация н-октаном при ~4,8 МПа изб. (~700 фунтов на кв. дюйм изб.) и ~290°С в течение ~3 часов обеспечивала загрузку н-октана в кристаллы DDR более 4 масс. %. Эта загрузка была больше ~75% от ожидаемой qs для н-октана и была нежелательно большой. Аналогичные результаты были обнаружены для селективации н-гексаном и н-гептаном для времен воздействия более ~2 часов. Чтобы продемонстрировать, что загрузку можно было уменьшить, сокращая время воздействия, селективацию выполняли н-гексаном при ~4,8 МПа изб. (~700 фунтов на кв. дюйм изб.) и ~290°С в течение ~0,75 часа. После селективации в течение ~0,75 часа было обнаружено, что загрузка составляла ~1,25 масс. %. На образце выполняли измерения методом ХНД, и было обнаружено, что коэффициент диффузии метана упал ниже уровня, который можно было обнаружить методом ХНД. Кривая ХНД была очень близка к разрешающей способности прибора, и оценили, что коэффициент диффузии СН4 упал ниже -10-14 м2/с.
Пример 5. Селективация кристаллов DDR путем краткосрочного воздействия высоких концентраций метил-разветвленных первичных спиртов при температурах выше 250°С
В данном примере использовали материал DDR и способ селективации, описанные в примере 2. Аналогично примеру 2, a priori не ожидали, что метил-разветвленный первичный спирт может диффундировать в DDR.
Результаты исследований методом ТГА адсорбции метил-разветвленных первичных спиртов в селективированных кристаллах DDR приведены в таблице 2 ниже. Во всех этих исследованиях методом ТГА преимущественная потеря массы происходила вблизи ~400°С. Это указывает на определенный тип химической связи между DDR и метил-разветвленными первичными спиртами. Предположили, что метил-разветвленные первичные спирты прореагировали с дефектами, связанными с гидроксильными группами, и другими дефектами в кристаллах DDR. ЯМР-исследования DDR и DDR, селективированного метил-разветвленным первичным спиртом, подтвердили эту гипотезу. Такая реакция усиливает стабильность селективации.
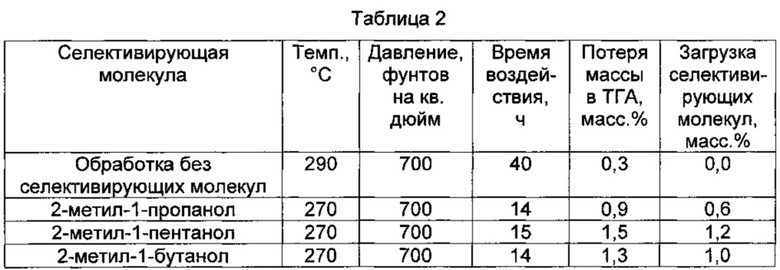
Чтобы определить воздействие селективации метил-разветвленным первичным спиртом на перенос СО2 и СН4, использовали баллистическую хроматографическую процедуру. В этом методе примерно 5-15 мг адсорбента загружали в ячейку диаметром ~1 мм и длиной ~1,5 см. Ячейку затем загружали в хроматограф таким образом, чтобы соединения с ячейкой не вызывали какого-либо значительного гидродинамического обратного смешения, когда газы протекали через ячейку с расходами примерно 5-40 см3/мин и с давлениями от ~100 кПа изб. (~1 бар изб.) до ~500 кПа изб. (~5 бар изб.). Чтобы можно было интерпретировать данные, поток через ячейку необходимо было считать по существу «поршневым потоком». Перед началом измерений адсорбент выдерживали при температуре от ~70°С до ~225°С либо в потоке гелия, либо в потоке азота.
Для определения переноса использовали масс-спектрометр, обладающий динамической характеристикой менее ~0,25 секунды, чтобы измерить изменения концентраций либо CO2, либо СН4, вытекающих из ячейки. Газы, используемые для изучения переноса, представляли собой смеси ~1-20% СН4 в Не или ~1-20% СО2 в Не. В этом примере пробные газы представляли собой ~10% СН4 в Не и ~10% СО2 в Не. В начале эксперимента через ячейку пропускали Не с расходом либо ~5 см3/мин, либо ~25 см3/мин. Клапан переключали, и через ячейку пропускали пробный газ с такой же скоростью, как и Не. После заранее заданного периода времени клапан снова переключали, и через ячейку пропускали гелий с первоначальным расходом. В конструкции оборудования было важно, чтобы скорость входящих потоков оставалась приблизительно постоянной, когда переключали клапан. Существовало несколько способов для выполнения этого, одним из которых является наличие впускного клапана, переключающего поток из ячейки в «холостой» путь, обладающий примерно таким же гидродинамическим сопротивлением, как и ячейка. В этом случае необходимо всегда пропускать Не и пробный газ и только переключаться между пропусканием через ячейку и пропусканием через «холостой» путь.
Большая часть анализа переноса СН4 поступила от наиболее коротких времен ~6 секунд, в течение которых пробный газ пропускали через ячейку. Другими продолжительностями времени, при которых изучали поток пробного газа через образец, были ~30 секунд, ~1 минута и ~2 минуты. Различие результатов при ~5 см3/мин и ~25 см3/мин использовали для оценки того, полностью ли СО2 пришел в равновесие с адсорбентом перед прохождением через ячейку. Анализ данных также основывался на регистрации динамической характеристики пустой ячейки.
Перенос через образец, селективированный 2-метил-1-пропанолом, сравнивали с переносом через базовый DDR, используя баллистическую хроматографию. Для СО2 существовал явный проскок, который был очень похож в образце, селективированном 2-метил-1-пропанолом, и в базовом DDR. Форму и положение фронта привели в соответствие с расходом таким образом, чтобы указать, что СО2 полностью пришел в равновесие с образцами даже при наиболее высоких расходах. Как ожидалось для полного равновесия, изменение времени, в течение которого газ пропускали через ячейку, от ~6 секунд до ~30 секунд не изменяет природу фронта проскока. Это показывает, что коэффициенты диффузии СО2 в образцах селективированного и базового DDR были больше 10-10 м2/с. Сравнение измерений СН4 для образцов селективированного и базового DDR дает оценку изменения диффузии СН4 из-за селективации. Как моделирование, так и непосредственное сравнение показали, что селективация 2-метил-1-пропанолом привела к уменьшению эффективного коэффициента диффузии СН4 по меньшей мере в 2,5 раза.
Аналогичные выводы были сделаны о воздействии селективации пленок DDR 2-метил-1-пропанолом с использованием способов и материалов, описанных в примере 3. Пленки, которые были селективированы 2-метил-1-пропанолом при ~4,8 МПа изб. (~700 фунтов на кв. дюйм изб.) и ~290°С в течение ~44 часов, имели примерно трехкратное уменьшение коэффициента диффузии СН4 без значительного воздействия на наблюдаемую кинетику CO2.
Пример 6. Селективация кристаллов DDR путем краткосрочного воздействия высоких концентраций вторичных спиртов при температурах выше 250°С В данном примере использовали материал DDR и способ селективации, описанные в примере 2. Результаты исследований методом ТГА адсорбции вторичных спиртов в селективированных кристаллах DDR приведены в таблице 3 ниже. Аналогично селективации метил-разветвленными первичными спиртами, основная потеря массы происходит вблизи ~400°С. Это указывает на определенный тип химической связи между DDR и вторичными спиртами.
Предположили, что вторичные спирты прореагировали с дефектами, связанными с гидроксильными группами, и другими дефектами в кристаллах DDR. Такая реакция, по-видимому, усиливает стабильность селективации.
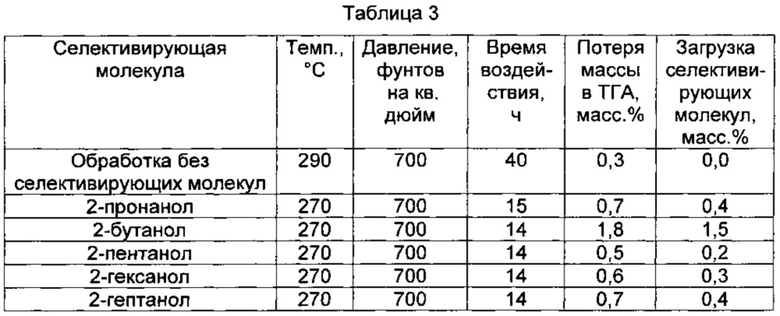
Перенос через образец, селективированный 2-гексанолом, сравнивали с переносом через базовый DDR, используя баллистическую хроматографию. Исследования показали, что эффективный коэффициент диффузии СН4 упал более чем в 10 раз, при этом перенос CO2 не показал почти никакого изменения.
Пример 7. Селективация пленок DDR путем краткосрочного воздействия высоких концентраций вторичных спиртов при температурах выше 250°С В данном примере использовали материал DDR и способ селективации, описанные в примере 3. Измерения однокомпонентной АПД использовали для оценки переноса в пленке DDR толщиной ~250 мкм до и после селективации 2-гексанолом в течение ~44 часов при ~4,8 МПа изб. (~700 фунтов на кв. дюйм изб.) и ~290°С. Сравнения измерений СО2, выполненных до и после селективации, не показали никакого обнаруживаемого изменения кинетики CO2. Анализ динамической характеристики АПД привел к значению нижней границы эффективного коэффициента диффузии CO2 на уровне ~2*10-11 м2/с для неселективированной и селективированной 2-гексанолом пленки DDR. Для СН4 давление в ячейке изменяли таким образом, чтобы можно было приблизительно аппроксимировать коэффициент переноса массы, используя приближение ЛДФ. Эффективный коэффициент диффузии СН4, полученный из анализа ЛДФ результатов эксперимента при комнатной температуре на пленке DDR, селективированной 2-гексанолом, составлял приблизительно 2×10-13 м2/с. Анализ ЛДФ показал, что эффективный коэффициент диффузии СН4 в пленке DDR, селективированной 2-гексанолом, был примерно в 15 раз меньше, чем в неселективированной пленке как при комнатной температуре, так и при 50°С.
Дополнительные измерения однокомпонентной АПД использовали для оценки переноса в пленке DDR толщиной ~250 мкм до и после селективации 2-октанолом в течение ~14 часов при ~4,8 МПа изб. (~700 фунтов на кв. дюйм изб.) и ~290°С. Сравнение измерений СО2, выполненных при комнатной температуре до и после селективации, не показало никакого обнаруживаемого изменения кинетики СО2. Анализ динамической характеристики АПД привел к значению нижней границы эффективного коэффициента диффузии СО2 на уровне ~2×10-11 м2/с для неселективированной и селективированной 2-октанолом пленки DDR. Для СН4 давление в ячейке изменяли таким образом, чтобы можно было приблизительно аппроксимировать коэффициент переноса массы, используя приближение ЛДФ. Эффективный коэффициент диффузии СН4 для DDR, полученный из анализа ЛДФ результатов эксперимента при комнатной температуре на пленке DDR, селективированной 2-октанолом, составлял ~0,3×10-13 м2/с. Анализ ЛДФ показал, что эффективный коэффициент диффузии СН4 в пленке DDR, селективированной 2-октанолом, был более чем в 100 раз меньше, чем в неселективированной пленке.
Хотя настоящее изобретение было описано с использованием конкретных воплощений, оно не ограничено ими. Подходящие изменения/модификации для действия в конкретных условиях должны быть понятны специалисту. Поэтому следует иметь в виду, что последующая формула изобретения охватывает все такие изменения/модификации как попадающие в истинную сущность / область защиты данного изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ разделения газов с использованием цеолитов типа DDR со стабилизированной адсорбционной активностью | 2013 |
|
RU2619788C2 |
| РАЗДЕЛЕНИЕ И ХРАНЕНИЕ ТЕКУЧИХ СРЕД С ИСПОЛЬЗОВАНИЕМ ITQ-55 | 2015 |
|
RU2672424C2 |
| Адсорбирующие материалы и способы их применения | 2015 |
|
RU2705340C2 |
| РАЗДЕЛЕНИЕ И ХРАНЕНИЕ ТЕКУЧИХ СРЕД С ИСПОЛЬЗОВАНИЕМ ITQ-55 | 2015 |
|
RU2674121C2 |
| РАЗДЕЛЕНИЕ И ХРАНЕНИЕ ТЕКУЧИХ СРЕД С ИСПОЛЬЗОВАНИЕМ ITQ-55 | 2015 |
|
RU2675874C2 |
| ИНТЕГРАЦИЯ АДСОРБЦИИ ПРИ ПЕРЕМЕННОМ ДАВЛЕНИИ С ЭНЕРГОУСТАНОВКОЙ ДЛЯ УЛАВЛИВАНИЯ/УТИЛИЗАЦИИ CO И ПРОИЗВОДСТВА N | 2013 |
|
RU2658406C2 |
| НАСТРАИВАЕМЫЕ АДСОРБЕНТЫ | 2018 |
|
RU2751716C2 |
| СТРУКТУРИРОВАННЫЙ СЛОЙ АДСОРБЕНТА, СПОСОБЫ ЕГО ПОЛУЧЕНИЯ И ЕГО ПРИМЕНЕНИЕ | 2015 |
|
RU2666849C1 |
| ФОРМОСЕЛЕКТИВНЫЙ ЦЕОЛИТОВЫЙ КАТАЛИЗАТОР И СПОСОБ КОНВЕРСИИ АРОМАТИЧЕСКИХ СОЕДИНЕНИЙ | 1996 |
|
RU2163506C2 |
| Способ обработки аминами для селективного отделения кислых газов | 2013 |
|
RU2618829C2 |
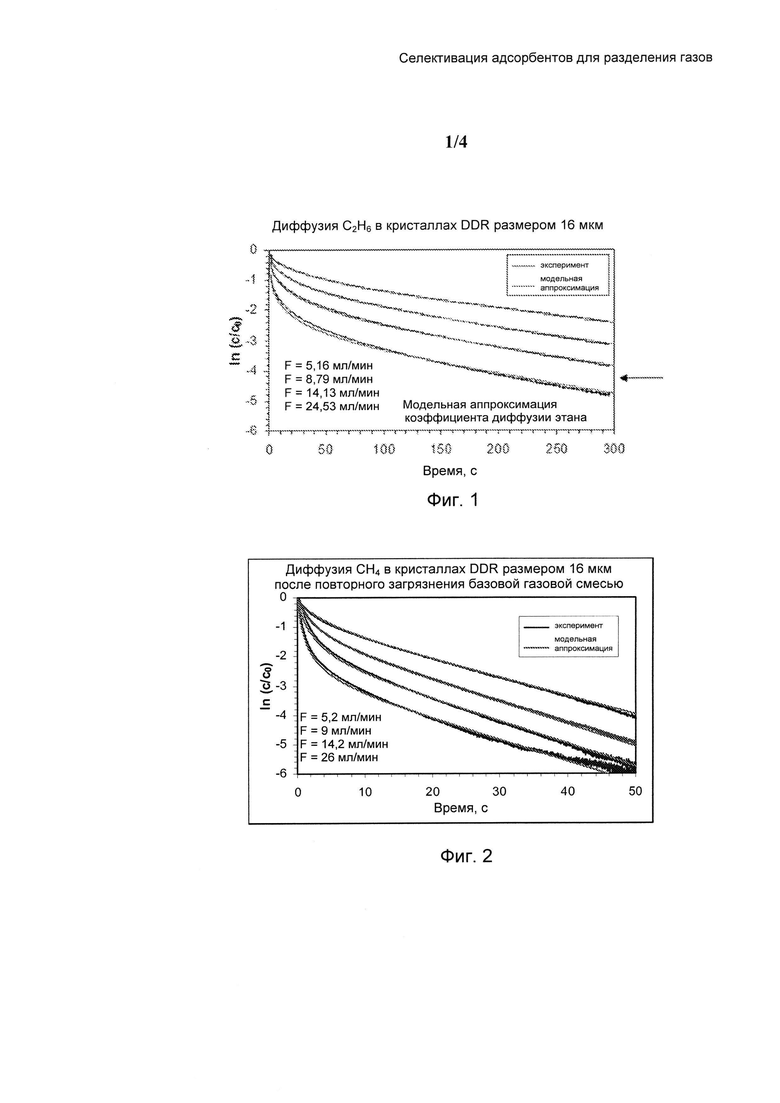
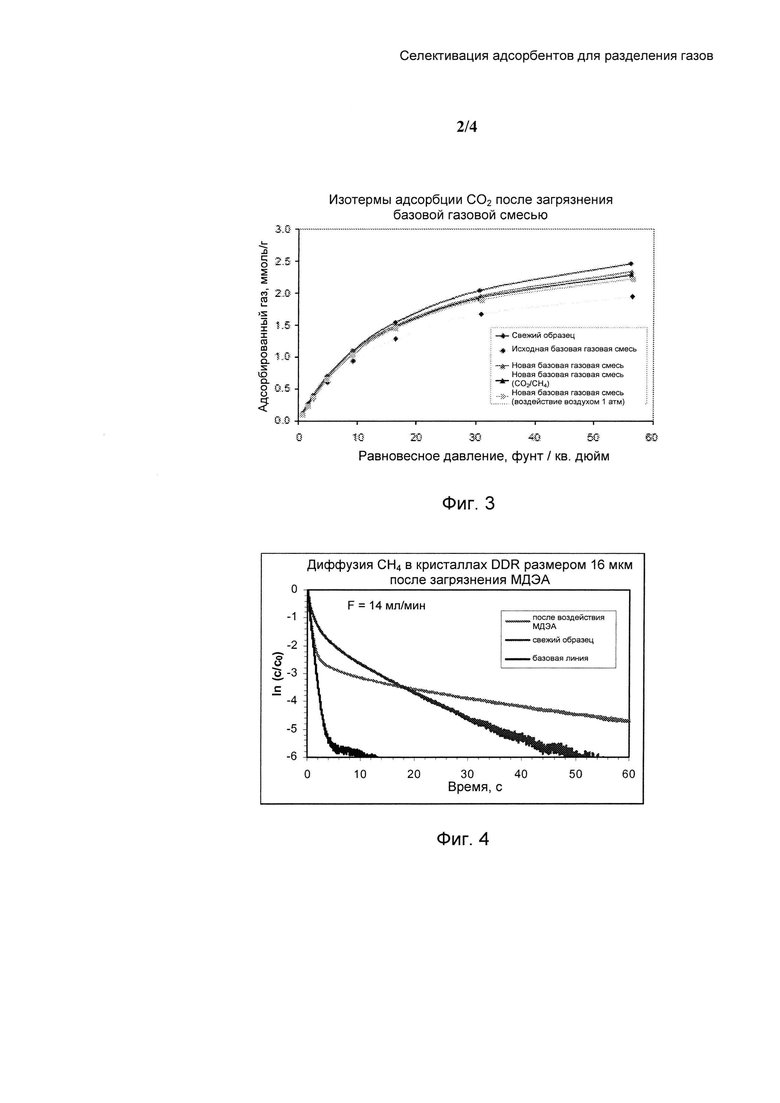
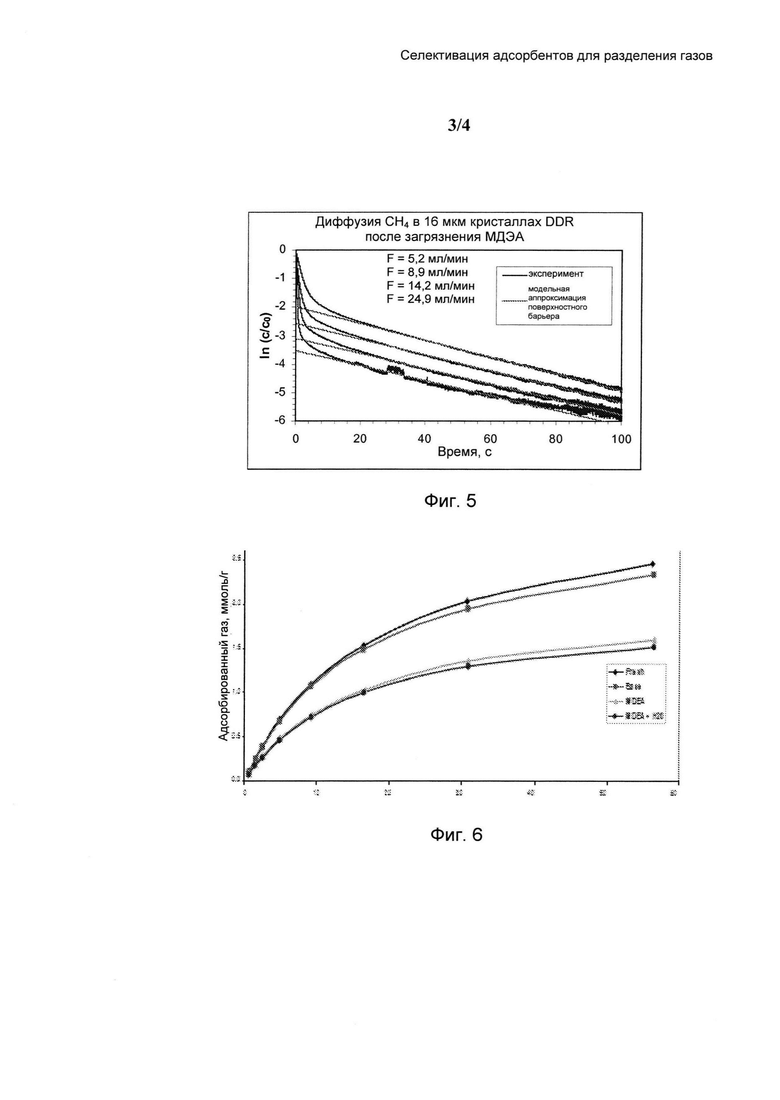
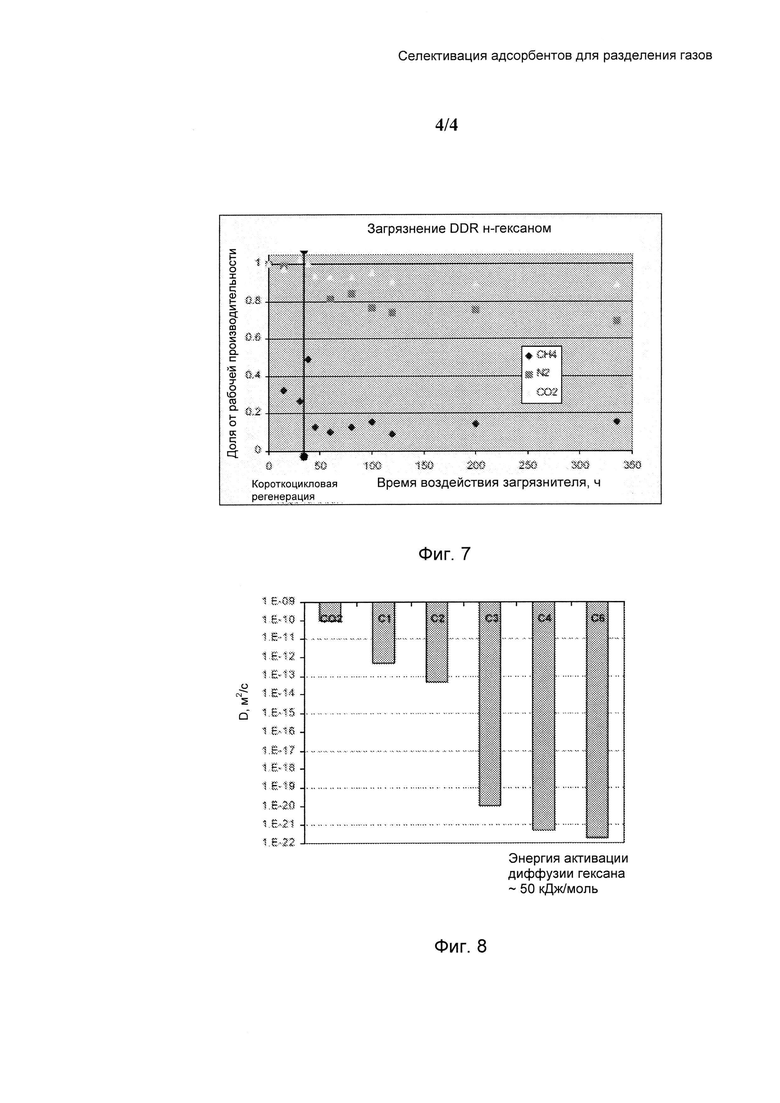
Изобретение относится к области селективации адсорбентов для разделения газов, в частности к способу разделения газов. Способ включает приведение адсорбента или мембраны, содержащих цеолит с 8-членными кольцами или микропористый материал с 8-членными кольцами, в контакт с барьерным соединением, при условиях, эффективных для селективации адсорбента или мембраны, включающие температуру от 50 до 350°C и полное давление от 690 до 13,8 МПа изб., где селективация адсорбента или мембраны включает диффузию молекулы барьерного соединения через пористую структуру микропористого материала с 8-членными кольцами, приведение селективированного адсорбента или мембраны в контакт с входящим потоком газа, содержащим первый компонент и второй компонент, с образованием первого потока газа, обогащенного первым компонентом по отношению к входящему потоку газа, и сбор второго потока газа, обогащенного вторым компонентом по отношению к входящему потоку газа. При этом барьерное соединение имеет минимальный размер молекулы, который на 0,4 Å превышает размер наибольшей твердой сферы, которая может диффундировать вдоль любого направления в адсорбенте, и максимальный размер, составляющий 25 Å или менее. Причем барьерное соединение присутствует либо в виде жидкости, либо в виде газа с парциальным давлением барьерного соединения 10% от давления насыщенного пара. Изобретение обеспечивает повышение селективности адсорбирующего материала. 2 н. и 13 з.п. ф-лы, 8 ил., 3 табл., 7 пр.
1. Способ выполнения разделения газов, включающий:
приведение адсорбента или мембраны, содержащих цеолит с 8-членными кольцами или микропористый материал с 8-членными кольцами, в контакт с барьерным соединением при условиях, эффективных для селективации адсорбента или мембраны, причем барьерное соединение имеет минимальный размер молекулы, который по меньшей мере на 0,4 Å превышает размер наибольшей твердой сферы, которая может диффундировать вдоль любого направления в адсорбенте, и максимальный размер, составляющий примерно 25 Å или менее, где эффективные условия приведения адсорбента или мембраны в контакт с барьерным соединением включают температуру от примерно 50°C до примерно 350°C и полное давление от примерно 690 кПа изб. (100 фунтов на 1 кв. дюйм изб.) до примерно 13,8 МПа изб. (примерно 2000 фунтов на 1 кв. дюйм изб.), причем барьерное соединение присутствует либо в виде жидкости, либо в виде газа с парциальным давлением барьерного соединения, которое составляет по меньшей мере примерно 10% от давления насыщенного пара, где селективация адсорбента или мембраны включает диффузию по меньшей мере одной молекулы барьерного соединения через пористую структуру микропористого материала с 8-членными кольцами;
приведение селективированного адсорбента или мембраны в контакт с входящим потоком газа, содержащим первый компонент и второй компонент, с образованием первого потока газа, обогащенного первым компонентом по отношению к входящему потоку газа, и
сбор второго потока газа, обогащенного вторым компонентом по отношению к входящему потоку газа.
2. Способ по п. 1, в котором цеолит с 8-членными кольцами представляет собой цеолит типа DDR, Sigma-1, ZSM-58 или их сочетание.
3. Способ по п. 1, в котором барьерное соединение представляет собой гликоль, амин, спирт, алкан, серосодержащее соединение или их сочетание, причем барьерное соединение имеет молекулярную массу, составляющую по меньшей мере 50 г/моль.
4. Способ по п. 1, в котором барьерное соединение представляет собой этиленгликоль, триэтиленгликоль, метилдиэтиламин, диметилэтиламин, диметилдисилан, н-гексан, 2-октанол или их сочетание.
5. Способ по п. 1, в котором первый компонент содержит или представляет собой СН4.
6. Способ по п. 1, в котором второй компонент содержит или представляет собой СО2, N2 или их сочетание.
7. Способ по п. 1, в котором эффективные условия приведения адсорбента или мембраны в контакт с барьерным соединением включают температуру, составляющую по меньшей мере примерно 150°C, такую как по меньшей мере примерно 250°C.
8. Способ по п. 1, в котором приведение селективированного адсорбента в контакт с входящим потоком газа включает адсорбцию селективированным адсорбентом по меньшей мере части второго компонента в течение приведения в контакт, причем способ дополнительно включает десорбцию по меньшей мере части адсорбированного второго компонента с образованием десорбированной части второго компонента, причем поток второго газа содержит по меньшей мере часть десорбированной части второго компонента.
9. Способ по п. 1, дополнительно включающий десорбцию по меньшей мере части барьерного соединения в течение приведения селективированного адсорбента или мембраны в контакт с входящим потоком газа.
10. Способ по п. 1, в котором адсорбент является частью устройства короткоцикловой адсорбции, причем устройство короткоцикловой адсорбции представляет собой устройство адсорбции с перепадом давления или устройство адсорбции с перепадом температуры.
11. Способ по п. 10, в котором устройство короткоцикловой адсорбции представляет собой устройство адсорбции с перепадом давления с частым циклом или устройство адсорбции с перепадом температуры с частым циклом.
12. Способ по п. 10 или 11, дополнительно включающий повторение указанных приведения в контакт, десорбции и сбора в течение множества циклов.
13. Способ по любому из пп. 1-7 или 9, в котором первый поток газа представляет собой поток ретентата, а второй поток газа представляет собой поток пермеата.
14. Способ по п. 1, в котором количество барьерного соединения, адсорбированного микропористым материалом, составляет примерно 20% или менее от насыщающей загрузки (qs).
15. Способ выполнения разделения газов в устройстве короткоцикловой адсорбции, включающий:
приведение адсорбента, содержащего микропористый материал, в контакт с барьерным соединением в устройстве короткоцикловой адсорбции при условиях, эффективных для селективации адсорбента, причем микропористый материал имеет поры, характеризующиеся первым размером наибольшей твердой сферы, которая может диффундировать вдоль любого направления в порах, а барьерное соединение имеет второй размер, представляющий собой минимальный размер соединения, причем второй размер на 10-60% больше первого размера;
приведение селективированного адсорбента в контакт с входящим потоком газа, содержащего первый компонент и второй компонент, с образованием выходящего потока газа, обогащенного первым компонентом по отношению к входящему потоку газа, при этом селективированный адсорбент адсорбирует по меньшей мере часть второго компонента в течение приведения в контакт;
десорбцию по меньшей мере части адсорбированного второго компонента с образованием десорбированной части второго компонента и
сбор газового потока, содержащего по меньшей мере часть десорбированной части второго компонента, при этом газовый поток обогащен вторым компонентом по отношению к входящему потоку газа, и, возможно, включающий содержание одного или более из пп. 3-14.
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| АДСОРБЕНТНЫЕ СТРУКТУРЫ ДЛЯ КИНЕТИЧЕСКОГО РАЗДЕЛЕНИЯ, РАЗРАБОТАННЫЕ НА НАУЧНОЙ ОСНОВЕ | 2006 |
|
RU2394631C2 |
Авторы
Даты
2018-03-22—Публикация
2013-11-08—Подача