Область техники
Способы обработки промышленных сточных вод имеют различные задачи, но в любом случае их основной целью является снижение количества органических и неорганических загрязняющих веществ. Потоки промышленных сточных вод часто содержат лишь несколько соединений, но в высокой концентрации, вследствие чего способ обработки должен быть весьма узкоспециализированным.
Глубина такой обработки зависит от правовых норм. Муниципальные власти обычно определяют нормативы сброса в канализационные сети, и государственные органы власти, такие как Управление охраны окружающей среды, обычно определяет нормы сброса в реки, озера и открытое море.
Отводимые потоки, содержащие высокие концентрации нитратов, также могут содержать большие количества других соединений, таких как хлориды (отходы рыбоконсервной промышленности, мокрого способа десульфуризации (обессеривания) извести и гипса и регенерационный раствор после регенерации ионообменных колонн) и сульфаты (отходы кожевенных заводов).
В частности, в способах, включающих ионный обмен, могут быть получены потоки сточных вод, сильно загрязненных неорганическими веществами. Например, при ионообменном превращении хлорида щелочного металла и нитрата кальция в нитрат щелочного металла и хлорид кальция образуются сточные воды с высоким содержанием солей и значительным загрязнением нитратами. Щелочным металлом при осуществлении такого способа ионного обмена может быть калий или натрий.
Способы обработки промышленных сточных вод могут представлять собой физическую (фильтрование, разделение, ионный обмен), химическую (флоккуляция, нейтрализация, окисление) или биохимическую обработку. Наиболее подходящий способ обработки выбирают в зависимости от токсичности и устойчивости соединений. Во многих случаях экономически выгодным является биохимический способ.
Для биохимической обработки промышленных сточных вод требуется:
- Выбрать вид организмов, способных разлагать целевое загрязняющее вещество;
- Создать условия, обеспечивающие оптимальный метаболизм выбранного вида;
- Обеспечить подачу веществ, необходимых для питания, а также обеспечить наличие источника углерода.
Денитрификация (удаление азота) представляет собой биохимический процесс, происходящий в природе, а также протекающий в системах обработки сточных вод. Осуществление такого способа в традиционных условиях очистки сточных вод рассмотрено, например, в Руководстве ATV-DVWK-A 131 (Bemessung von einstufigen Belebungsanlagen. Edition 05/2000. DWA. Germany. ISBN: 978-3-933707-41-3). В присутствии нитрата и отсутствии кислорода анаэробные бактерии способны использовать нитрат для окисления органических соединений, которое необходимо для поддержания их обмена веществ. Таким образом, в этом процессе происходит потребление нитратов и биодоступных органических соединений при сохранении и приращении биомассы и высвобождении CO2, N2 и воды.
Процесс денитрификации состоит из четырех этапов:
Нитрит, один из промежуточных продуктов этого процесса, токсичен для множества организмов. В частности, в случае накопления и полученной повышенной концентрации нитрит может стать критическим токсином для самих бактерий, восстанавливающих нитрат. В стандартных условиях восстановление нитрита происходит быстрее, чем восстановление нитрата, и, таким образом, в сбалансированных условиях накопления нитрита не происходит. Наличие высоких концентраций нитрата и легкоразлагаемого источника углерода, прежде всего, приводит к интенсивному высвобождению нитрита, и, следовательно, к прекращению восстановления нитрата из-за отравления нитритом.
Известно, что высокие концентрации солей в сточных водах отрицательно влияют на биологическую денитрификацию. Однако, в гиперсоленых водах были выявлены и идентифицированы несколько видов толерантных к содержанию галогенов и подходящих для проведения денитрификации бактерий. Чем выше соленость среды обитания, тем меньшим является количество специализированных бактериальных таксонов, которые могут выживать или полноценно жить в такой среде обитания. В экстремальном окружении, таком как кристаллизационный пруд «солнечных» солеварен (предприятий для добывания соли при испарении соленой воды на солнце), могут выживать лишь относительно редкие адаптированные виды галофильных (соленолюбивых) бактерий.
Кроме того, на скорость денитрификации большое влияние оказывает температура воды. До определенного предела активность микроорганизмов повышается при повышении температуры. Поскольку нитрат и нитрит, являясь акцепторами электронов, конкурируют за них с кислородом, для достижения оптимальных скоростей денитрификации следует избегать контакта среды с атмосферой, обогащенной кислородом. Таким образом, предпочтительно, биологическая денитрификация протекает при высокой температуре, которая, однако, ограничена максимальной температурой, при которой могут выжить соответствующие виды бактерий. С некоторыми исключениями, денитрификация представляет собой анаэробный процесс.
К настоящему времени авторами изобретения был открыт биохимический способ для денитрификации гиперсоленой композиции сточных вод, концентрация нитрата в которой составляет по меньшей мере 0,1% (масс./об.), и концентрация хлорида составляет по меньшей мере 5% (масс./об.), с применением галофильных и/или солеустойчивых бактерий.
Согласно настоящему изобретению, гиперсоленой композицией, такой как сточная вода, рассол и подобная среда, называют композицию, которая содержит по меньшей мере 5% (масс./об.) хлорид-ионов (Cl-).
Согласно настоящему изобретению, композиция с высокой концентрацией нитрата означает композицию, содержащую по меньшей мере 0,1% (масс./об.) нитрата (NO3-).
Согласно настоящему изобретению, упоминание "нитрата" или "хлорида" относится к общему количеству присутствующих "нитратных" или "хлоридных" соединений, независимо от того, находятся ли они в виде ионов или недиссоциированных соединений.
В настоящем описании, согласно Le Borgne с соавт. (Biodegradation of Organic Pollutants by Halophilic Bacteria and Archaea (Биоразложение органических загрязняющих веществ под действием галофильных бактерий и архебактерий), Journal of Molecular Microbiology and Biotechnology 2008; 15:74-922008), галофильные бактерии разделяют на слабогалофильные, которые активны при концентрации NaCl, составляющей от 2 до 5% (масс./об.) (средняя концентрация NaCl в морской воде составляет 3,5% (масс./об.)), умеренно галофильные, которые активны при концентрации NaCl, составляющей от 5 до 20% (масс./об.) и чрезвычайно галофильные, которые активны при концентрации NaCl, составляющей от 20 до 30% (масс./об.). Большая часть дополнительных бактерий согласно настоящему изобретению может быть отнесена к бактериям от умеренно галофильных до чрезвычайно галофильных. Однако, сообщество микроорганизмов, используемых в экспериментах согласно настоящему изобретению, представляло собой смесь галофильных, солеустойчивых и неспециализированных видов, полученную из смеси активированного ила, полученного на этапе денитрификации при плановой обработке муниципального сточных вод, и солесодержащего ила, полученного из кристаллизационного пруда «солнечной» солеварни. В отличие от солеустойчивых видов, для роста которых NaCl не требуется, но которые способны расти в солесодержащей среде, для роста галофильных видов присутствие NaCl необходимо.
Предшествующий уровень техники
В литературе указана специфичность целей биообработки и соответствующего выбора микроорганизмов, а также говорится о том, что каждая из целей биообработки требует установки определенной температуры, величины рН, подбора питательных микроэлементов и вида микроорганизмов.
В публикации Okeke с соавт. (Reduction of perchlorate and nitrate by salt-tolerant bacteria (Восстановление перхлората и нитрата солеустойчивыми бактериями). Environmental Pollution 118 (2002) 357-363)) рассмотрен способ биообработки сточных вод, оптимизированный для удаления перхлорат-ионов из сточных вод, содержащих 100 мг/л ClO4- (0,01% масс./об.) и 11,7 мг/л NO3- (0,001% масс./об.). Эффективность удаления нитрата составила 16,4% для совместной культуры солеустойчивой Citrobacter бактерии и несолеустойчивой бактерии, "perclace" как указано в источнике, и 15,6% для монокультуры Citrobacter в течение 7 суток. В качестве источника углерода использовали ацетат и экстракт дрожжей. Рекомендуемая температура для удаления ClO4- составила 30°С при содержании NaCl от 0 до 5%.
В публикации Cyplik Р. с соавт. (Effect of Macro/micro Nutrients and Carbon Source Over the Denitrification Rate of Haloferax Denitrificans Archaeon (Влияние макро/микропитательных веществ и источника углерода на скорость денитрификации Haloferax Denitrificans Archaeon), Enzyme and Microbial Technology 40, 2007, 212-220) рассмотрена денитрификация соленой воды под действием только солеустойчивых бактерий, в частности, Haloferax Denitrificans Archaeon. Цитируемое количество NaCl составляло от 2,5 до 3,5 М (от 14,5 до 20% (масс./об.)), и количество нитрата составляло от 100 до 1000 мг/л. Предпочтительными являются нейтральный рН и температура 37°С.
В публикации Foglar с соавт. (Nitrate Removal with Bacterial Cells Attached to Quartz Sand and Zeolite from Salty Wastewater (Удаление нитрата с помощью бактериальных клеток, закрепленных на кварцевом песке и цеолите, из соленых сточных вод), World J. Microbiol. Biotechnol. (2007) 23:1595-1603) рассмотрено исследование, в котором для удаления нитрата из соленой воды применяют смешанную бактериальную культуру. Используемое в экспериментах количество NaCl составляло 3% (масс./об.), а количество нитрата составляло 750 мг/л. В некоторых примерах добавляли источник углерода, температура составляла 37°С при нейтральном рН. Указанные бактерии включали Pseudomonas sp. и Paracoccus sp. В этом исследовании количество хлорида и количество нитрата было ниже, чем в настоящем изобретении, и снижение концентрации нитрата занимало больше времени (до 10 суток и более при 37°С), чем согласно настоящему изобретению.
В публикации Nair с соавт. (Biological denitrification of high strength nitrate waste using pre-adapted denitrifying sludge (Биологическая денитрификация отходов с высокой концентрацией нитратов с помощью предварительно адаптированного денитрифицирующего ила). Chemosphere 67 (2007) 1612-1617) показано, что удаление нитрата из сточных вод предприятия по производству удобрений может быть выполнено с использованием активированного ила. Испытания показали, что нитратсодержащий ил, в котором начальные концентрации NO3- составляют до 4%, может быть полностью обработан в течение 6 часов. Однако, в этом случае хлориды отсутствовали. Рекомендуемая температура для удаления NO3- составляла 37°С.
В публикации Le Borgne с соавт. (Biodegradation of Organic Pollutants by Halophilic Bacteria and Archaea, Journal of Molecular Microbiology and Biotechnology 2008; 15:74-922008) представлен обзор по биоразложению органических загрязняющих веществ под действием галофильных бактерий. Денитрификация не описана.
В публикации Osaka с соавт. (Effects of Carbon Source on Denitrification Efficiency and Microbial Community Structure in a Saline Wastewater Treatment Process (Влияние источника углерода на эффективность денитрификации и структуру микробного сообщества в способе обработки солесодержащих сточных вод), Water Research 42, 2008, 3709-3718) рассмотрено академическое исследование биологической денитрификации соленой воды, основной задачей которого являлся выбор подходящего источника углерода. Если концентрация NaCl составляет от 0 до 10%, то предпочтительным является ацетат. Бактериальную культуру получали из синтетического ила сточных вод, активированного NaCl в лабораторных условиях. Концентрация нитрата составляла 1,5 г/л. Указано, что в реакторах с загрузкой метанола или ацетата, применяемых для проведения денитрификации, использовали различные микробные виды (Azoarcus, Hyphomicrobium, Methylophage и Paracoccus для метанола и Azoarcus, Marinobacter и Halomonas для ацетата).
В публикации Tsang с соавт. (A novel sludge minimized biological nitrogen removal process for saline treatment (Новый способ биологического удаления азота при обработке солевого раствора при минимальном количестве ила). Water Science & Technology, т. 59, выпуск 10, 2009; стр. 1893-1899) рассмотрен способ многостадийной обработки солесодержащих сточных вод, содержащих некоторые количества сульфата (0,05% масс./об.), направленный на удаление органических загрязняющих веществ. Хлоридные соли не упоминаются.
В публикации Rezaee с соавт. (Denitrification of high salinity, high nitrate wastewater using clinoptilolite in с наполнителем bioreactor (Денитрификация сточных вод высокой солености с высоким содержанием нитратов с использованием клиноптилолита, находящегося в биореакторе с наполнителем). Journal of Environmental Research and Management. T. 3(2). стр. 031-036, март, 2012), в которой рассмотрена обработка сточных вод высокой солености (до 4% масс./об.) с высоким содержанием нитратов в биореакторе с наполнителем, в котором в качестве носителя применяли клиноптилолит, было показано, что может быть успешно обработан впускной поток, содержащий 500 мг/л (0,05% масс./об.) нитрата. Температура составляла 25°С.
В публикации Cyplik с соавт. (Biological Denitrification of High Nitrate Processing Wastewaters from Explosives Production Plant (Биологическая денитрификация технологических сточных вод с высоким содержанием нитратов предприятия, производящего взрывчатые вещества). Water Air Soil Pollution (2012) 223:1791-1800) рассмотрена биологическая денитрификация технологических сточных вод с высоким содержанием нитратов, получаемых на предприятии, производящем взрывчатые вещества, и показано, что нитраты могут быть удалены из сточных вод, имеющих высокую концентрацию загрязняющих нитратов. В течение 16 суток в присутствии нитроглицерина и низких концентраций хлоридов (21 мг/л) было удалено 3 г/л азота (из NO3-). Температура не указана, то есть можно предположить, что применяли стандартные лабораторные условия (20°С).
В патентной публикации US 4356092 (1982) рассмотрен биологический способ обработки сточных вод, но удаление нитрата не является его основной целью. Способ включает этапы культивирования нового штамма, Alcaligaenes faecalis HRL-1, и добавление культивированных к клеток к обрабатываемым сточным водам. Соленость не обсуждается.
Кроме того, в патентной публикации ЕР 2018417 В1 (2007) рассмотрен новый штамм Alcaligenes faecalis, CNCM 1-3448, способный превращать азот по Кьельдалю, азот аммиака и/или оксиды азота в газообразный азот, а также способный превращать углеродсодержащие вещества в диоксид углерода, причем оба эти превращения протекают в аэробных условиях. Соленость не обсуждалась.
В патентной публикации CN 101054232 А (2007) рассмотрен высокоэффективный биологический способ обработки гиперсоленых сточных вод, позволяющий получать аэробный гранулированный ил в реакторе последовательного получения без использования галофильных бактерий, то есть позволяющий проводить эффективную обработку гиперсоленых сточных вод и повышать устойчивость системы к солевому стрессу.
В патентной публикации WO 2010/076794 А1 (2010) рассмотрен способ денитрификации рассола посредством добавления солеустойчивых анаэробных бактерий. Денитрификацию проводят при нейтральном рН и добавлении источника углерода, при температуре, составляющей приблизительно 37°С. Способ осуществляют в биореакторе с псевдоожиженным слоем. Обрабатываемый рассол содержал лишь от 0,5 до 4% соли, 2 г/л хлорида и 0,05 г/л нитрата (в виде N), что гораздо ниже концентраций согласно настоящему изобретению.
Согласно предшествующему уровню техники не имеется биохимического способа, задачей которого является быстрое удаление нитрата в присутствии высокой концентрации хлоридов, предназначенного для обработки сточных вод, содержащих неорганические вещества, с помощью определенной комбинации бактерий.
Сведения, подтверждающие возможность осуществления изобретения
Изобретение относится к биохимическому способу денитрификации гиперсоленой композиции сточных вод, имеющей высокую концентрацию нитрата, в присутствии высокой концентрации хлорида.
Согласно изобретению, гиперсоленую композицию сточных вод, имеющую высокую концентрацию нитрата, подвергают биохимической обработке, в результате которой высокая концентрация нитрата, присутствующая наряду с высокой концентрацией хлорида, снижается до более низкой концентрации, предпочтительно в течение короткого периода времени, за счет воздействия на гиперсоленую композицию сточных вод галофильных и/или солеустойчивых бактерий.
Изобретение относится к биохимическому способу денитрификации гиперсоленой композиции сточных вод, концентрация нитрата в которой составляет по меньшей мере 0,1% (масс./об.) и концентрация хлорида составляет по меньшей мере 5% (масс./об.), где способ включает применение галофильных и/или солеустойчивых бактерий.
Один из примеров осуществления относится к биохимическому способу денитрификации гиперсоленой композиции сточных вод, получаемых при осуществлении способа ионного обмена, в которых концентрация нитрата составляет по меньшей мере 0,1% (масс./об.) и концентрация хлорида составляет по меньшей мере 5% (масс./об.), где способ включает применение галофильных и солеустойчивых бактерий.
Согласно одному из примеров осуществления, концентрация нитрата составляет по меньшей мере 0,20% (масс./об.), более предпочтительно 0,25% (масс./об.).
Обработку выполняют, используя сообщество бактерий, а не один вид бактерий. Учитывая высокую соленость, логично предположить, что все члены активного сообщества являются по меньшей мере солеустойчивыми, более вероятно, либо галофильными, либо солеустойчивыми, предпочтительно как галофильными, так и солеустойчивыми, и активное сообщество также необязательно содержит неспециализированные члены. Сообщество выбирали в течение некоторого времени из смеси ила, состоящей из обычного денитрифицирующего активированного ила, полученного на предприятии обработки муниципальных сточных вод, и солесодержащего осадочного ила, полученного из кристаллизационного пруда «солнечной» солеварни Ses Salines, Испания. Приблизительно от 85 до 95 масс. %, более предпочтительно приблизительно 90 масс. % ила состоит из активированного ила, получаемого на этапе денитрификации при плановой обработке муниципальных сточных вод. Приблизительно от 5 до 15 масс. %, более предпочтительно приблизительно 10 масс. % ила состоит из осадка, полученного из кристаллизационного пруда «солнечной» солеварни, включающего природные галофильные денитрифицирующие бактерии. Тип культивирования и способ выбирали, постепенно повышая с течением времени концентрации хлорида кальция и нитрата калия до требуемого уровня при постоянной температуре, составляющей от 35°С до 40°С, предпочтительно 37°С.
Несмотря на то, что большая часть (69 масс. %) бактерий «солнечной» солеварни оставалась неидентифицированными бактериями с короткими таксономными маркерными генами (V4-V6 SSU рДНК), секвенирование спаренных концов Illumina MySeq позволило точно отнести множество бактерий к следующим родам: Pseudomonas (численность (число особей на единицу пространства): 19 масс. %), Bacillus (число особей на единицу пространства: 4 масс. %) и Halomonas (число особей на единицу пространства: 3 масс. %), и необязательно менее распространенных (1 масс. % или менее) были обнаружены Rhodobacter, Arthrobacter, Flexibacter, Propionibacterium, Enterobacteriaceae, Flavobacterium, Bradyrhizobium, Hyphomicrobium, Lysobacter, Sinorhizobium, Azospirillum, Thiobacillus, Sphingobacter, Paracoccus, Aeromanas, Ochrobacterium, Nitrosomonas, Herbaspirillum, Janthinobacterium, Lactobacillus, Nitrobacter, Cellulomonas, Streptomycetes, Cytophaga, Thiomicrospira, Beggiatoa, Cellvibrio, Moraxella, Alteromonas, Kingella, Aquaspirillium, Norcadia и Azoarcus. Учитывая высокие концентрации солей, при которых происходила денитрификация, логично предположить, что все активные денитрифицирующие организмы были либо солеустойчивыми, либо галофильными.
Способ осуществляют при температуре, составляющей от 35°С до 40°С, предпочтительно приблизительно при 37°С, при которой наблюдали оптимальное функционирование.
Предпочтительно, в способе в качестве источника углерода используют ацетат калия, но также возможно использование метанола или этанола, хотя из-за их более высокой стоимости они менее предпочтительны для промышленного применения.
Питательные вещества в систему не добавляют, поскольку для специфично выбранных денитрифицирующих организмов в основном требуется нитрат. Следовые элементы, а также фосфаты, присутствуют в подаваемом иле в достаточном количестве. В крупномасштабном варианте осуществления, при постоянной обработке сточных вод и подаче ила лишь в начале для запуска процесса, может быть необходимым введение дополнительных следовых элементов и фосфата.
Было показано, что применение способа согласно изобретению позволяет снизить исходную концентрацию нитрата, составляющую от 1,5 до 3,0 г/л, до концентрации, составляющей приблизительно 0,001 г/л, в течение периода времени, составляющего от 24 до 48 часов, в частности, если применяемая смесь ила состоит на приблизительно от 85 до 95 масс. %, более предпочтительно приблизительно на 90 масс. %, из активированного ила, получаемого на этапе денитрификации при плановой обработке муниципальных сточных вод, и на приблизительно от 5 до 15 масс. %, более предпочтительно приблизительно на 10 масс. %, из солесодержащего ила, получаемого из кристаллизационного пруда «солнечной» солеварни.
Способ согласно изобретению осуществляют в биореакторе традиционным образом, известным специалисту в данной области техники. Биореактор может представлять собой либо реактор с суспендированным илом (осадком), либо реактор с плавающим слоем (англ. floating bed). В этом способе основным питательным веществом, необходимым для выполнения условий биохимического восстановления нитрата, является добавляемый источник углерода. Функционирование может быть как периодическим, так непрерывным.
Сточная вода, которая должна быть обработана, может быть получена на ионообменной установке. В процессе получения хлорид калия или хлорид натрия реагирует с нитратом кальция с образованием таких продуктов, как нитрат калия или нитрат натрия, и раствора хлорида кальция в качестве отхода. Поток сточной воды нуждается в специализированной обработке, поскольку концентрация загрязняющего нитрата слишком высока для сброса без очистки.
К настоящему описанию приложены следующие графические материалы:
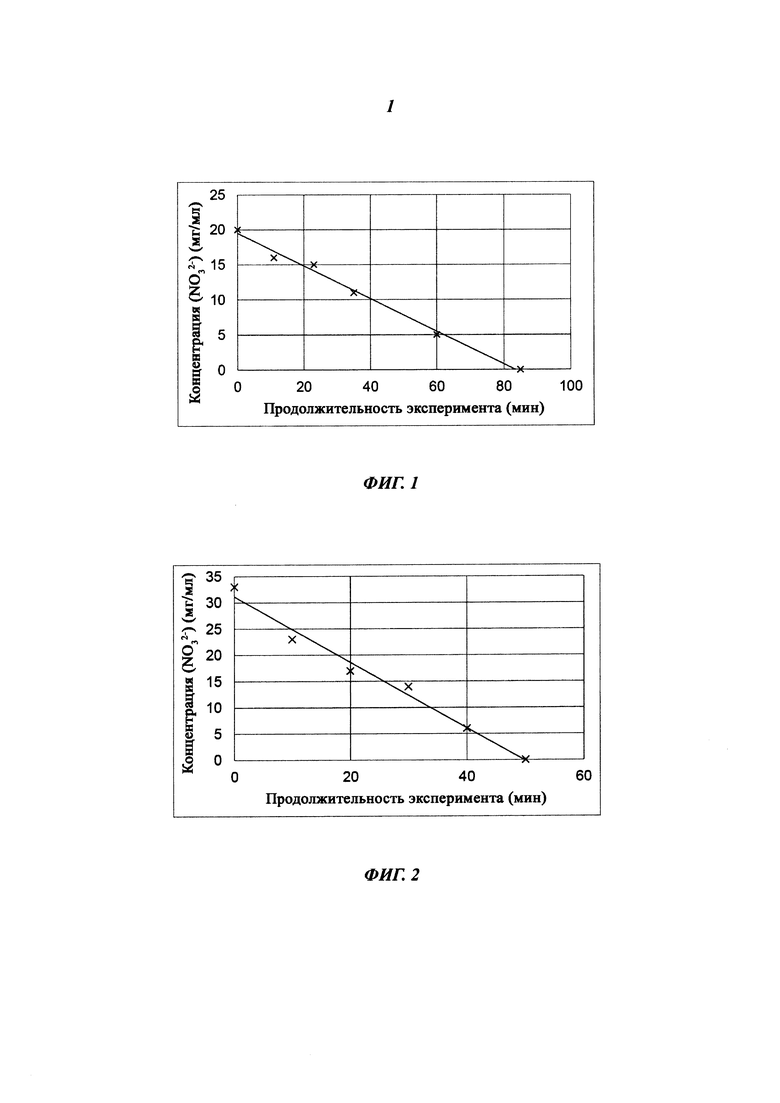
Фиг. 1: Денитрификация в стандартных условиях (без добавления источника углерода, комнатная температура) в рассмотренной (Эксперимент А) моделирующей установке емкостью 2 л.
Фиг. 2: Денитрификация в моделирующей установке емкостью 2 л с добавлением МеОН (10 мл/л) в качестве источника углерода при комнатной температуре (Эксперимент В).
Фиг. 3: Денитрификация в моделирующей установке емкостью 2 л при концентрации нитрата 260 мг/л (Эксперимент С).
Фиг. 4: Денитрификация в моделирующей установке емкостью 2 л при концентрации нитрата 2200 мг/л (Эксперимент D).
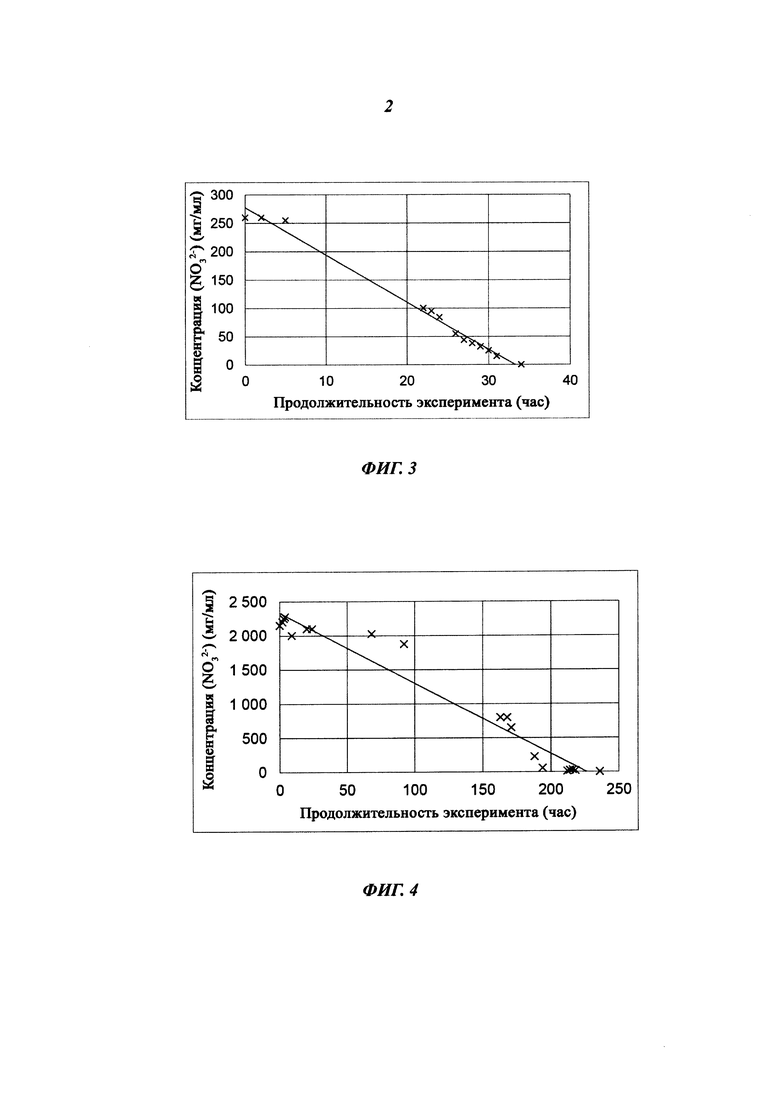
Фиг. 5: Влияние температуры на скорость денитрификации в экспериментальной 2-литровой моделирующей установке (Эксперимент Е).
Фиг. 6: Влияние KАс как источника углерода (Эксперимент F).
Фиг. 7: Денитрификация при высокой концентрации соли (Эксперимент G) в отсутствии значимого количества галофильных и/или солеустойчивых бактерий (не в соответствии с изобретением).
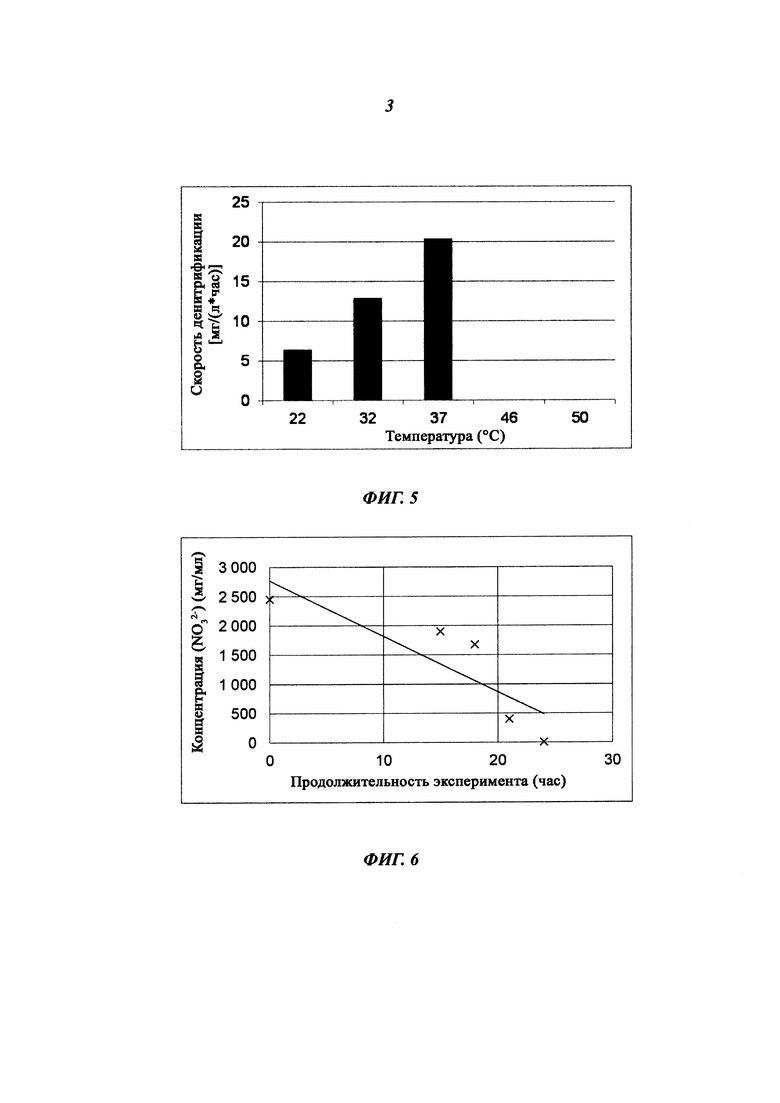
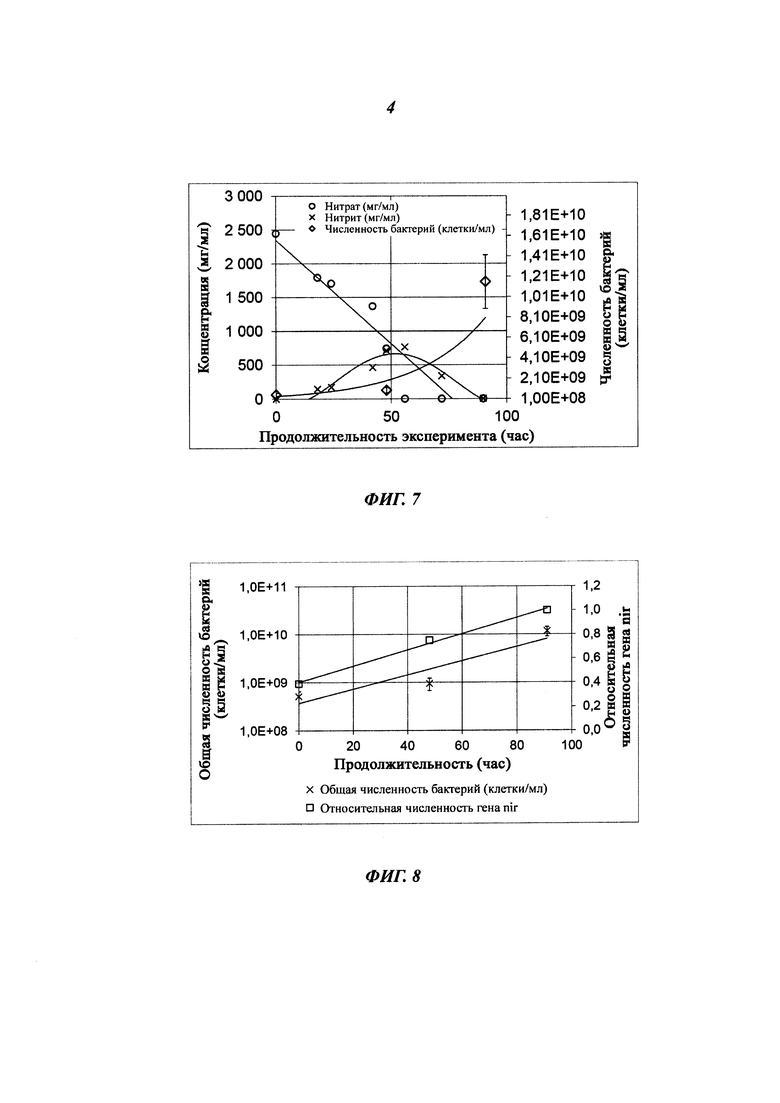
Фиг. 8: Общее число бактерий на единицу пространства (x) и относительное число денитрифицирующих бактерий на единицу пространства (□) в Эксперименте G, согласно фотометрическим измерениям (слева) и окрашиванию DAPI (сокращенно от англ. 4',6-diamidino-2-phenylindole, т.е. 4',6-диамидин-2-фенилиндол) (справа).
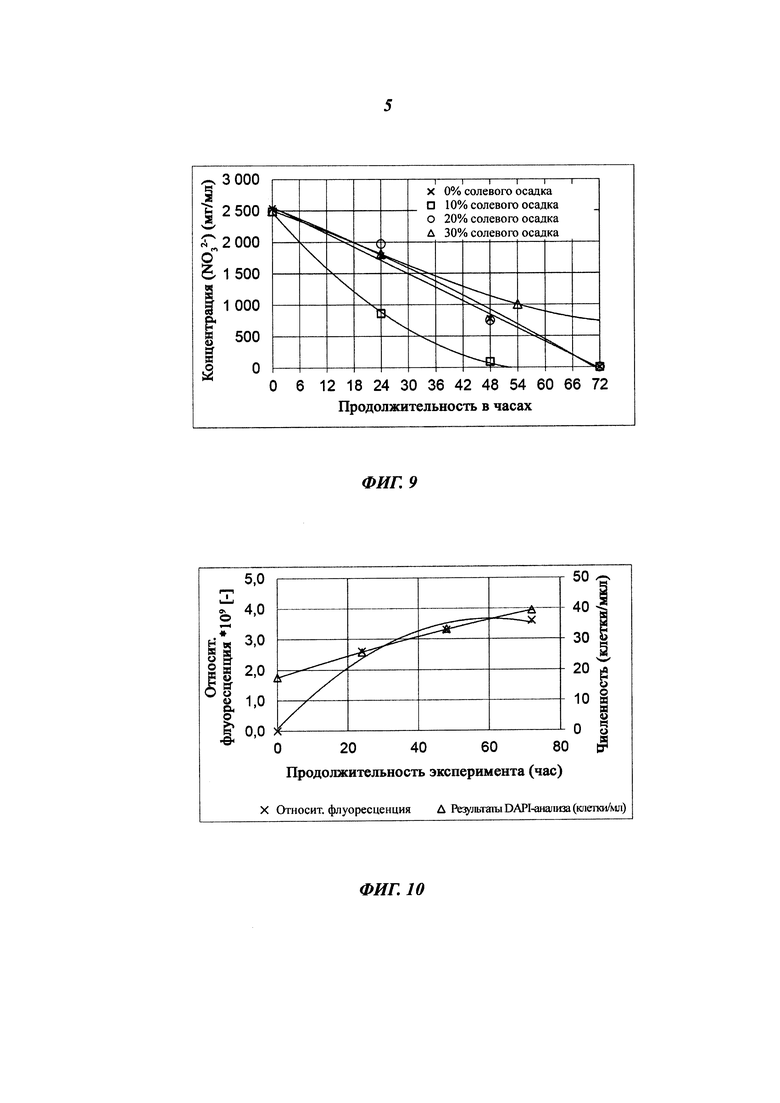
Фиг. 9: Скорости денитрификации при различных долях замещения осадка согласно изобретению (Эксперимент Н).
Фиг. 10: Общее число бактерий на единицу пространства (x) и число денитрифицирующих бактерий на единицу пространства (Δ) в Эксперименте Н, согласно фотометрическим измерениям (слева) и окрашиванию DAPI (справа).
Описание примеров осуществления изобретения
Общая часть
Нитрат калия получают ионным обменом из хлорида калия и нитрата кальция, получая при этом поток сточной воды, имеющий высокую соленость, благодаря присутствию хлорида кальция и высокой концентрации загрязняющего нитрата. Необходимо было определить способ биологической обработки этого потока сточной воды, приводящий к максимальной степени превращения нитрата в газообразный азот.
Целью этого эксперимента являлась оценка и обнаружение микробной среды, которая могла бы осуществлять полную денитрификацию при высоких концентрациях соли. Состав сточных вод включал 2,5 г нитрата/л сточной воды (0,25% масс./об.), 91 г CaCl2/ л сточной воды (5,7% масс./об. ионов Cl-), температура превышала 50°С, и подаваемые промышленные сточные воды не содержали источника углерода. В качестве дополнительного источника углерода добавляли ацетат калия в количестве 30 мл/л.
В методику проведения эксперимента входило создание закрытой регулируемой лабораторной системы (моделирующая установка емкостью 2 литра - далее 2-литровая моделирующая установка), в которой воспроизводили условия, имеющиеся в биореакторе с активированным илом. Экспериментальные возможности 2-литровой моделирующей установки включали возможность регулировать концентрации кислорода (обеспечивать недостаток кислорода), величину рН (для эффективной денитрификации обязателен диапазон от 6,5 до 8,5) и температуру. Таким образом, установка была оборудована постоянными датчиками, определяющими в режиме реального времени (онлайн) величины рН, содержания кислорода и температуры, перемешивающим устройством, доступом для отбора промежуточных образцов без кислородного загрязнения и вводом для продувки аргоном в случае непредвиденного окисления.
Для создания микробной среды использовали активированный ил, предоставленный предприятием по обработке сточных вод (сокращенно "ПОСВ") г. Кайзерслаутерн (Германия) (объемом 2,5 л в каждом эксперименте). В качестве осадка, содержащего природные галофильные денитрифицирующие бактерии, использовали осадок из кристаллизационного пруда «солнечной» солеварни Ses Salines, Испания.
В различные моменты времени во время проведения экспериментов отбирали образцы, в которых измеряли концентрации нитрата и нитрита (с помощью ионной хроматографии и фотометрии), общее число бактерий на единицу пространства (с помощью окрашивания DAPI), относительное количество генов нитритредуктазы (англ. сокращенно nir), которое определяет число денитрифицирующих бактерий на единицу пространства, и определяли молекулярный профиль микробного сообщества (Illumina секвенирование рибосомной РНК и статистический анализ структуры сообщества). При проведении экспериментов необходимо регулировать рН добавлением KОН, поскольку микробная среда имеет слабую тенденцию к закислению.
Концентрации нитрата измеряли фотометрическим способом при низких содержаниях соли и способом ионной хроматографии при высоких содержаниях соли.
Эксперимент А
Стандартная денитрификация без манипуляций с образцами в регулируемой 2-литровой моделирующей установке
Этот эксперимент служил контрольным для функционирования системы 2-литровой моделирующей установки в стандартных условиях при обычной (комнатной) температуре. Денитрификацию проводили в стандартных условиях (без добавления источника углерода, при комнатной температуре) в моделирующей установке емкостью 2 л. Добавляли 20 мг нитрата/л, что соответствует концентрациям нитратов, обычно имеющимся в сточной воде, подаваемой в ПОСВ.
Результаты представлены на Фиг. 1. При установленных экспериментальных условиях денитрификация сточной воды, содержащей 20 мг нитрата/л, прошла за 85 минут. Скорость денитрификации составила 14,1 мг/л/час.
Заключение: Экспериментальные условия идеально подходят для проведения экспериментов, поскольку денитрификация в моделирующей установке емкостью 2 л имеет ту же эффективность, что и в обычных условиях правильно функционирующего ПОСВ.
Эксперимент В
Добавление метанола (МеОН, 10 мл/л) в качестве дополнительного источника углерода для оценки влияния этого источника углерода на скорость денитрификации
Экспериментальные условия были такие же, как и в Эксперименте А, но с небольшим повышением концентрации нитратов (33 мг/л). Результаты представлены на Фиг. 2. Полная денитрификация 33 мг нитрата/л протекала за 50 минут. Наклон графика был несколько круче, чем в эксперименте в стандартных условиях (без добавления дополнительного источника углерода). Скорость денитрификации составляла 39,8 мг/л/час.
Заключение: Дополнительный источник углерода (метанол) заметно ускоряет денитрификацию. В последующих экспериментах изменение концентрации источника углерода не оказывала положительного влияния на скорость денитрификации.
Эксперимент С
Повышение концентрации нитрата до 260 мг/л (превышение концентраций, имеющихся в природных условиях, приблизительно в 10 раз)
Результаты представлены на Фиг. 3. Даже при такой повышенной концентрации нитрата полная денитрификация возможна. Однако, время, необходимое для полной денитрификации 260 мг нитрата/л, составляет до 34 часов. Скорость денитрификации составляла 7,4 мг/л/час.
Заключение: Способы микробной денитрификации при таких высоких концентрациях нитрата имеют гораздо более низкую скорость, чем в Эксперименте А, в котором концентрации нитрата близки к концентрациям в микробной среде. Вероятно, что численность встречающихся в природе бактерий в данных экспериментальных условиях слишком низка для эффективного протекания денитрификации.
Эксперимент D
Повышение концентрации нитрата до 2200 мг/л
Результаты представлены на Фиг. 4. Даже при такой повышенной концентрации нитрата полная денитрификация возможна. Однако, время, необходимое для полной денитрификации 2200 мг нитрата/л, составляет до 200 часов. Скорость денитрификации составляла 9,3 мг/л/час.
Заключение: Скорость денитрификации имела тот же порядок величины, что и в Эксперименте С, в котором концентрация нитрата была приблизительно в 10 раз ниже. Эта скорость слишком низка для стандартного применения в подходящем для ПОСВ способе удаления высокой концентрации нитрата. Из результатов этого эксперимента также понятно, что численность встречающихся в природе бактерий слишком низка для эффективной денитрификации в данных экспериментальных условиях. Таким образом, последующие эксперименты проводили с целью повышения численности и активности бактерий.
Эксперимент Е
Оценка влияния температуры на скорость денитрификации в экспериментальной 2-литровой моделирующей установке
Для оценки влияния температуры на скорость денитрификации в экспериментальной 2-литровой моделирующей установке было проведено несколько экспериментов с исходной концентрацией нитрата, составляющей приблизительно 1000 мг/л. Результаты представлены на Фиг. 5. Наивысшие скорости денитрификации были достигнуты при 37°С. Скорость денитрификации составляла 20,4 мг/л/час. При более высоких температурах скорость денитрификации снижалась.
Заключение: В экспериментальных условиях при температуре 37°С плотности и активности бактерий повышаются. Вследствие этого даже при чрезвычайно высоких концентрациях нитрата достигаются скорости денитрификации такого же порядка величины, что и в "стандартных условиях" (см. Эксперименты А и В). Однако, эти скорости все еще слишком низки для эффективного удаления таких высоких концентраций нитрата в промышленности. Были проведены дополнительные эксперименты.
Эксперимент F
Оценка влияния источника углерода
МеОН не подходит в качестве источника углерода для промышленного применения (по причинам высокой стоимости и низкой безопасности). Таким образом, для оценки ацетата калия (KАс) как альтернативного источника углерода проводили Эксперимент F. Во всех экспериментах KАс добавляли при определенном соотношении: C:N=1,5:1. Результаты представлены на Фиг. 6. Скорость денитрификации составляла 102 мг/л/час, в качестве источника углерода принимали KАс, температура составляла 37°С, концентрация нитрата была чрезвычайно высока.
Заключение: В этом эксперименте была достигнута наиболее высокая по сравнению с другими скорость денитрификации, которая значительно превышает стандартные скорости денитрификации на ПОСВ, имеющиеся в опубликованной литературе. Таким образом, можно заключить, что KАс в качестве источника углерода и оптимальная температура, составляющая 37°С, представляют собой подходящие условия для проведения эффективной микробной денитрификации.
Эксперимент G
Денитрификация при высоких концентрациях соли в отсутствии значительного количества галофильных и/или солеустойчивых бактерий (не в соответствии с изобретением)
Денитрификацию при высоких концентрациях солей проводили при концентрации CaCl2 91 г/л (5,7% масс./об. ионов Cl-), концентрации нитрата 2,5 г/л (0,25% масс./об.), KАс в качестве источника углерода и при температуре 37°С.
Результаты представлены на Фиг. 7. Скорость денитрификации составляла 43,7 мг/л/час. В течение эксперимента наблюдали значительное повышение численности бактерий и численности денитрифицирующих организмов в сточной воде. Это определяли с помощью количественной ПЦР (полимеразной цепной реакции) в режиме реального времени для гена nir (нитритредуктазы, см. Saggar с соавт. Sci. Total Environ.), кодирующего часть процесса денитрификации, и общее количество бактерий, определяемое анализом с использованием DAPI, вычисляли, проводя 5 определений одного образца. Результаты представлены на Фиг. 8. На Фиг. 8 показаны количественные (относительные) данные в условиях проведения Эксперимента G.
Заключение: В течение эксперимента биомасса специфических денитрифицирующих бактерий увеличилась в 2,5 раза.
Эксперимент Н
Замена активированного ила осадком из «солнечной» солеварни, включающим природные галофильные денитрифицирующие организмы
Активированный ил предприятия по обработке сточных вод (ПОСВ) г. Kaiserslautern (Германия) заменили осадком из кристаллизационного пруда «солнечной» солеварни Ses Saline, Испания, содержащим природные галофильные денитрифицирующие организмы. Результаты представлены на Фиг. 9. Замена 10% об. осадком, содержащим природные галофильные денитрифицирующие организмы, повышало скорость денитрификации по сравнению с Экспериментом G. Скорость денитрификации составила 51,8 мг/л/час. Неожиданно было обнаружено, что повышение относительной доли осадка, содержащего природные галофильные денитрифицирующие организмы (эксперименты проводили для 20% и 30% об., см. Фиг. 9) не повышало скорость денитрификации, а, напротив, значительно замедляло процесс денитрификации.
Кроме того, в течение эксперимента биомасса специфических денитрифицирующих бактерий увеличилась в 3,5 раза (см. Фиг. 10). Можно отметить, что применение способа согласно изобретению при использовании 10% солесодержащего осадка позволяет снижать исходную концентрацию нитрата, составляющую 2,5 г/л, до концентрации, приблизительно составляющей 1 г/л, в течение 24 часов, и до концентрации, приблизительно составляющей 0,001 г/л, в течение 48 часов.
| название | год | авторы | номер документа |
|---|---|---|---|
| Бактериальный препарат для нитрификации и денитрификации воды | 2022 |
|
RU2826455C2 |
| СПОСОБ ДЕНИТРИФИКАЦИИ ВОДЫ | 2001 |
|
RU2240986C2 |
| Способ биологической денитрификации сточных вод | 1984 |
|
SU1270738A1 |
| Штамм бактерий Virgibacillus halodenitrificans CHEL 4-5 ВКМ B-3472D для денитрификации с образованием нитрита | 2021 |
|
RU2774191C1 |
| Способ биологической денитрификации сточных вод | 1988 |
|
SU1664757A1 |
| СПОСОБ БИОЛОГИЧЕСКОЙ ОЧИСТКИ ВЫСОКОКОНЦЕНТРИРОВАННЫХ СТОЧНЫХ ВОД | 1997 |
|
RU2121461C1 |
| Способ биохимической очистки сточных вод от нитратов | 1978 |
|
SU789426A1 |
| Способ биологической очистки сточных вод от нитратов и органических соединений | 1984 |
|
SU1194851A1 |
| СПОСОБ ОКИСЛЕНИЯ АММОНИЯ И ТРУДНОДОСТУПНОГО ОРГАНИЧЕСКОГО ВЕЩЕСТВА СТОЧНЫХ ВОД В АЭРОБНО-АНОКСИДНЫХ УСЛОВИЯХ (ВАРИАНТЫ) | 2010 |
|
RU2492148C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ВЛИЯНИЯ ТОКСИЧНОСТИ СТОЧНЫХ ВОД НА ВОДНЫЕ СОЛЕНЫЕ СРЕДЫ | 2014 |
|
RU2541457C1 |
Изобретение относится к биохимической денитрификации гиперсоленых сточных вод. Биохимический способ денитрификации гиперсоленой композиции сточных вод, концентрация нитрата в которой составляет по меньшей мере 0,1% мас./об., а концентрация хлорида составляет по меньшей мере 5% (мас./об.), включает использование сообщества галофильных и/или солеустойчивых бактерий, где указанное сообщество выбрано из смеси ила, состоящей на от 85 до 95 мас.% из активированного ила, получаемого на этапе денитрификации при плановой обработке муниципальных сточных вод, и на приблизительно от 5 до 15 мас.% из солесодержащего ила, получаемого из кристаллизационного пруда «солнечной» солеварни. Ил включает бактерии по меньшей мере следующих родов: Pseudomonas, Bacillus и Halomonas. Изобретение позволяет быстро удалять нитраты в присутствии высокой концентрации хлоридов при обработке сточных вод, содержащих неорганические вещества, с помощью комбинации бактерий. 11 з.п. ф-лы, 10 ил.
1. Биохимический способ денитрификации гиперсоленой композиции сточных вод, концентрация нитрата в которой составляет по меньшей мере 0,1% (мас./об.) и концентрация хлорида составляет по меньшей мере 5% (мас./об.), включающий стадию, на которой для денитрификации указанных гиперсоленых сточных вод используют сообщество галофильных и/или солеустойчивых бактерий, также необязательно содержащее неспециализированные члены, где указанное сообщество выбрано из смеси ила, состоящей на от 85 до 95 мас.% из активированного ила, получаемого на этапе денитрификации при плановой обработке муниципальных сточных вод, и на приблизительно от 5 до 15 мас.% из солесодержащего ила, получаемого из кристаллизационного пруда «солнечной» солеварни, и где ил включает бактерии по меньшей мере следующих родов: Pseudomonas, Bacillus и Halomonas.
2. Способ по п. 1 для обработки гиперсоленых сточных вод, образующихся при осуществлении способа ионного обмена, в которых концентрация нитрата составляет по меньшей мере 0,1% (масс./об.) и концентрация хлорида составляет по меньшей мере 5% (масс./об.).
3. Способ по п. 1 или 2, где концентрация нитрата составляет по меньшей мере 0,20% (масс./об.), более предпочтительно 0,25% (мас./об.).
4. Способ по любому из пп. 1-3 для обработки гиперсоленых сточных вод, образующихся в процессе производства, в котором хлорид калия и нитрат кальция используются для получения хлорида кальция и потока сточной воды, содержащей нитрат.
5. Способ по любому из пп. 1-4 для обработки гиперсоленых сточных вод, образующихся в процессе производства, в котором хлорид натрия и нитрат кальция используются для получения хлорида кальция и потока сточной воды, содержащей нитрат.
6. Способ по любому из пп. 1-5, в котором указанное сообщество выбрано из смеси ила, состоящего на приблизительно 90 мас.% из активированного ила, получаемого на этапе денитрификации при плановой обработке муниципальных сточных вод, и на приблизительно 10 мас.% из солесодержащего ила, получаемого из кристаллизационного пруда «солнечной» солеварни.
7. Способ по любому из пп. 1-6, в котором галофильные бактерии выбраны из рода Pseudomonas (число особей на единицу пространства: 19 мас.%), Bacillus (число особей на единицу пространства 4 мас.%) и Halomonas (число особей на единицу пространства 3 мас.%), и необязательно менее распространенных (1 мас.% или менее) родов: Rhodobacter, Arthrobacter, Flexibacter, Propionibacterium, Enterobacteriaceae, Flavobacterium, Bradyrhizobium, Hyphomicrobium, Lysobacter, Sinorhizobium, Azospirillum, Thiobacillus, Sphingobacter, Paracoccus, Aeromanas, Ochrobacterium, Nitrosomonas, Herbaspirillum, Janthinobacterium, Lactobacillus, Nitrobacter, Cellulomonas, Streptomycetes, Cytophaga, Thiomicrospira, Beggiatoa, Cellvibrio, Moraxella, Alteromonas, Kingella, Aquaspirillium, Norcadia и Azoarcus.
8. Способ по любому из пп. 1-7, где способ осуществляют при температуре, составляющей от 35°C до 40°C, предпочтительно при приблизительно 37°C.
9. Способ по любому из пп. 1-8, в котором в качестве источника углерода используют ацетат калия.
10. Способ по любому из пп. 1-9, в котором исходную концентрацию нитрата, составляющую от 1,5 до 3,0 г/л, снижают до концентрации, составляющей приблизительно 0,001 г/л, в течение периода времени, составляющего от 24 до 48 часов.
11. Способ по любому из пп. 1-10, где способ осуществляют в биореакторе типа реактора с суспендированным осадком (илом).
12. Способ по любому из пп. 1-11, где способ осуществляют в биореакторе типа реактора с плавающим слоем.
| PEYTON BRENT M | |||
| et al., Nitrate Reduction with Halomonas campisalis: Kinetics of Denitrification at pH 9 and 12.5% NaCl, Water Research, Elsevier, Amsterdam, NL, 01.12.2001, vol | |||
| Скоропечатный станок для печатания со стеклянных пластинок | 1922 |
|
SU35A1 |
| ДИССОЦИАТОР ДЛЯ СЫРОЙ АММИАЧНОЙ ВОДЫ | 1925 |
|
SU4237A1 |
| СПОСОБ ДЕНИТРИФИКАЦИИ ВОДЫ | 2001 |
|
RU2240986C2 |
| KR 20130108763 A, 07.10.2013 | |||
| SHAPOVALOVA A.A | |||
| et al., Heterotrophic denitrification at extremly high salt and by haloalkaliphic gammaproteobacteria from hypersaline soda lakes, Extremophiles, 2008, 12, p | |||
| ПРИСПОСОБЛЕНИЕ ДЛЯ УПРАЖНЕНИЙ НА МУНДШТУКЕ ДУХОВЫХ ИНСТРУМЕНТОВ | 1923 |
|
SU619A1 |
| M | |||
| JOSE MARTINEZ-CANOVAS et al., Halomonas ventosae sp | |||
| nov., a moderately halophilic, denitrifyng, exopolysaccharide-producing bacterium, International Journal of Systematic and evolutionary microbiology, 2004, N54, p | |||
| ПРИБОР ДЛЯ СЪЕМКИ СЛОЖНЫХ ПРОФИЛЕЙ, ПРЕИМУЩЕСТВЕННО ГРЕБНЫХ ВОЗДУШНЫХ И ВОДЯНЫХ ВИНТОВ | 1922 |
|
SU733A1 |
Авторы
Даты
2018-03-28—Публикация
2015-05-13—Подача