Область, к которой относится изобретение
Изобретение относится к молекулярной биологии, биотехнологии, генной инженерии и медицине и может быть использовано для усиления защиты клеток различных органов и тканей, а также собственно органов и тканей человека от оксидативного стресса, в частности, в терапевтических целях.
Предшествующий уровень.
Оксидативный стресс клетки отражает дисбаланс между продукцией реактивных форм кислорода (азота) и антиоксидантной системой защиты. Он проявляется в мембранной дисфункции, повреждении ДНК, инактивации белкового синтеза. Оксидативный стресс приводит к образованию первичных и вторичных реактивных форм кислорода и азота, чаще известных как свободные радикалы.
Избыточная продукция свободных радикалов (O2⋅-, ОН⋅, NO:⋅), является фактором повреждения клеток организма, в частности они повреждают все компоненты клеточных структур, включая липиды мембран, белки и ДНК, что ведет к мутагенезу и высокому риску опухолеобразования. Избыточная активация реакций свободнорадикального окисления встречается при самых различных заболеваниях таких, как атеросклероз, болезни Паркинсона и Альцгеймера, диабет, катаракта, онкологические заболевания. Гиперпродукция свободных радикалов является также и характеристикой старения, что проявляется токсичностью на разных уровнях - органном, клеточном, генном.
Поэтому в клетке имеется естественная антиоксидантная система. Она представлена ферментами, среди которых наибольшее значение имеют Mn2+- и Cu2+-зависимые супероксиддисмутазы (гены SOD1 и SOD2), глютатионпероксидаза GPX, глютатионредуктаза и каталаза CAT. SOD преобразует супероксид-анионы в перекись водорода, которая затем трансформируется в воду другими ферментами, GPX и CAT. Ферментные антиоксиданты являются элементами внутриклеточной защиты, поскольку в плазме крови и в лимфе они обнаруживаются лишь в следовых количествах.
На активность антиоксидантных ферментов оказывают влияние возрастные изменения, которые выражаются в снижении их экспрессии. Стимуляция естественных антиоксидантных систем, привнесение экзогенных антиоксидантов - важный момент профилактики воспаления и раннего старения. В настоящее время для предотвращения или коррекции оксидативного стресса применяются препараты с генами антиоксидативных белков, которые обладают разной силой защитного ответа.
Так в патенте US 6045809 для нейтрализации токсического действия активных форм кислорода было предложено использовать фармацевтические композиции для перорального введения фермента - антиоксиданта супероксиддисмутазы в сочетании, по крайней мере, с одним из липидов (на примере керамидов) или белков (на примере проламинов). Недостаток данного подхода состоит в том, что при данном методе введения желаемый терапевтический эффект может оказаться недостигнутым, а также - при недостаточной степени очистки возможны побочные реакции.
В патенте US 8926965 было предложено использовать рекомбинантный модифицированный вариант супероксиддисмутазы-2. В ее аминокислотную последовательность путем создания мутаций в кодирующей нуклеотидной последовательности были внесены изменения по по сайтам К53 и К89 (степень идентичности модифицированного варианта белка и нативного белка не менее 95%). Нуклеотидная последовательность, кодирующая модифицированный белок, была введена в клетку-хозяин (эукариотические или прокариотические клетки, например бактериальные) с помощью рекомбинантного вектора экспрессии. Была показана трансляция белка модифицированной супероксиддисмутазы-2, и что его ферментативная активность более чем в 10 раз выше, чем у немодифицированного белка. Также было заявлено, что модифицированный пептид можно использовать для уменьшения оксидативного стресса и/или окислительного повреждения клетки как собственно лекарственное средство, так и в композиции с другими компонентами.
Недостатком данного подхода является высокая стоимость получения чистого рекомбинантного белка, а также - внесение модификаций в аминокислотную последовательность природного белка может привести к образованию структур, являющихся антигенными детерминантами.
За прототип авторами было принято решение по заявке WO 1988007541 А1, в котором предлагается использовать белок рекомбинантной глутатионпероксидазы человека для снижения оксидативного стресса в клетках, тканях и органах. Глутатионпероксидаза катализирует процесс разложения пероксида водорода и органических перекисей с одновременным окислением глутатиона, что и придает этому ферменту первоочередное значение в антиоксидатной защите организма.
Этот белок является одним из немногих белков, известных у высших позвоночных, который содержит селеноцистеин, который находится в активном центре глутатионпероксидазы. Обнаружены несколько изоформ фермента, которые образуются в результате альтернативного сплайсинга. Глутатионпероксидаза формирует высокоактивный интермедиант - селеновую кислоту, селеновая кислота при этом защищена белковым окружением от активных групп внутри самого белка. Механизм действия глутатионпероксидазы базируется на реакции селеновой кислоты с амидами или аминами другого белка, формируя селеноамидные связи.
Продукт гена GPX является фактором в развитии ишемической болезни сердца. Недостаток этого фермента может способствовать возникновению повреждений в эндотелиальной выстилке сосудов, что может привести к преждевременному старению эритроцитов. Снижение активности гена GPX может приводить к формированию катаракты. Глутатионпероксидаза помогает предотвратить нарушение функции сердца в результате реперфузионного синдрома при ишемии. Глутатионпероксидаза человека может быть использована для терапии различных расстройств, обусловленных появлением пероксидов как продуктов метаболизма клетки.
Изобретение по прототипу предлагает способ синтеза глутатионпероксидазы человека в большом количестве с использованием методов рекомбинантной ДНК. В патенте представлен полинуклеотид, с последовательностью кДНК гена GPX человека. Последовательность полинуклеотида или его модифицированные формы были встроены в векторы для экспрессии в эукариотических клетках рекомбинантных продуктов: глутатионпероксидаза человека, фрагменты глутатионпероксидазы человека, аналоги глутатионпероксидазы человека и аналоги фрагментов глутатионпероксидазы человека. Эти рекомбинантные полипептидные продукты имеют потенциальную терапевтическую пользу. Кроме того, они могут быть использованы для получения моноклональных и поликлональных антител к продукту гена GPX человека. Данные антитела применимы для диагностики недостатка продукта гена GPX у человека. Кроме того, аналог глутатионпероксидазы человека, активные фрагменты глутатионпероксидазы человека и моноклональные антитела к глутатионпероксидазе человека могут применяться для определения взаимодействия фермента с различными субстратами на основе взаимодействия фермента с гидрофильными и гидрофобными участками.
Недостатком данного подхода является высокая стоимость получения чистого рекомбинантного белка, более частое его введения при терапии (что увеличивает стоимость терапии и повышает риск побочных явлений) и сложность внутриклеточной доставки препарата. Также при создании терапевтического средства по прототипу не учтены индивидуальные характеристики пациента
Раскрытие изобретения
Задачей данного изобретения является создание линейки высокоэффективных биологически активных генно-терапевтических субстанций, способных препятствовать снижению антиоксидантной активности белка глутатионпероксидазы-3 в клетках органов и тканей и/или органах и тканях человека путем повышения уровня экспрессии гена GPX3 в клетках органов и тканей и/или органах и тканях человека, и/или повышения активности белка глутатионпероксидазы-3, ответственного за поддержание окислительно-восстановительного баланса в клетках органов и тканей и/или органах и тканях организма с учетом индивидуальных особенностей пациента.
Задача решается за счет того, что создана линейка биологически активных генно-терапевтических субстанций для коррекции патологических состояний клеток органов и тканей и/или органов и тканей человека, связанных с оксидативным стрессом, каждая из которых представляет собой генетическую конструкцию на основе векторной плазмиды, содержащей нативную кДНК гена GPX3 SEQ ID No: 1 или одну из модифицированных кДНК гена GPX3, и содержащей также регуляторные элементы, обеспечивающие транскрипцию этой последовательности в эукариотических клетках, в частности в клетках органов и тканей человека и способную обеспечить высокий уровень экспрессии гена GPX3 и увеличить активность белка глутатионпероксидазы-3 в клетках органов и тканей и/или органах и тканях человека, в частности, в гемопоэтических клетках, или гепатоцитах, или мезенхимальных стволовых клетках, или хондробластах, или клетках поджелудочной железы (например, в клетках панкреатических островков), или миоцитах или фибробластах кожи, или кератоцитах, или эпителиальных клетках роговицы, или в нейронах, ганглиях, Шванновских клетках, астроцитах, олигодендроцитах, микроглии, или в сперматозоидах, или в нефронах, или эндотелиальных клетках, или эпителиальных клетках в сочетании с транспортной молекулой или без нее при трансфекции этими биологически активными генно-терапевтическими субстанциями клеток органов и тканей человека и/или в органах и тканях человека в частности, в коже, суставах, печени, надпочечниках, почках, головном и спинном мозге, легких, сердце, сосудах, желудочно-кишечном тракте, простате, поджелудочной железе, глазе, роговице, слизистой оболочке, хрящевой ткани, мышечной ткани в сочетании с транспортной молекулой или без нее при введении этих биологически активных генно-терапевтических субстанций в органы и ткани человека. При этом генетическая конструкция с кДНК гена GPX3 содержит последовательность нуклеотидов, включающую в себя белок-кодирующую область кДНК гена GPX3, которая несет модификации, не затрагивающие структуру белка глутатионпероксидазы-3, а именно: делеции 5' нетранслируемых областей или делеции 3'-нетранслируемых областей, или нуклеотидные замены, не приводящие к аминокислотным заменам или обрыву аминокислотной цепи, или комбинации вышеперечисленных модификаций и, соответственно, не влияющие на кодируемую этой последовательностью аминокислотную последовательность. В качестве модифицированной кДНК гена GPX3 используют SEQ ID No: 2. Или в качестве модифицированной кДНК гена GPX3 используют SEQ ID No: 3. Или в качестве модифицированной кДНК гена GPX3 используют SEQ ID No: 4. Или в качестве модифицированной кДНК гена GPX3 используют SEQ ID No: 5. Или в качестве модифицированной кДНК гена GPX3 используют SEQ ID No: 6. Или в качестве модифицированной кДНК гена GPX3 используют SEQ ID No: 7. При этом в качестве транспортной молекулы используют липосомы, или дендримеры 5-го и выше поколений, или амфифильные блоксополимеры
Способ получения биологически активной генно-терапевтической субстанции для коррекции патологических состояний клеток органов и тканей и/или органов и тканей человека, связанных с оксидативным стрессом заключается в том, что получают кДНК гена GPX3, затем помещают кДНК в векторную плазмиду, способную обеспечить высокий уровень экспрессии этой кДНК в клетках различных органов и тканей человека, наращивают и выделяют необходимое количество генетической конструкции, затем комбинируют генетическую конструкцию с транспортной молекулой для трансфекции полученной биологически активной генно-терапевтической субстанцией клеток органов и тканей и/или введения полученной биологически активной генно-терапевтической субстанции в органы и ткани человека.
Или способ получения биологически активной генно-терапевтической субстанции для коррекции патологических состояний клеток различных органов и тканей человека, связанных с оксидативным стрессом заключается в том, что получают кДНК гена GPX3, модифицируют его по п.п. 3, или 4, или 5 или 6 или 7 или 8, затем помещают модифицированную кДНК в векторную конструкцию, способную обеспечить высокий уровень экспрессии этой кДНК в клетках различных органов и тканей человека, наращивают и выделяют необходимое количество генетической конструкции, затем комбинируют генетическую конструкцию с транспортной молекулой для трансфекции полученной биологически активной генно-терапевтической субстанцией клеток органов и тканей и/или введения полученной биологически активной генно-терапевтической субстанции в органы и ткани человека.
Способ использования каждой из созданных и представленных в линейке биологически активных генно-терапевтических субстанций для коррекции патологических состояний клеток органов и тканей и/или органов и тканей человека, связанных с оксидативным стрессом, заключается в трансфекции созданной биологически активной генно-терапевтической субстанцией, выбранной с учетом индивидуальных особенностей каждого конкретного пациента на основе предварительного эксперимента по определению наиболее эффективного варианта из созданных и представленных в линейке биологически активных генно-терапевтических субстанций, клеток органов и тканей человека.
Или способ использования каждой из созданных и представленных в линейке биологически активных генно-терапевтических субстанций для коррекции патологических состояний клеток органов и тканей и/или органов и тканей человека, связанных с оксидативным стрессом, заключается во введении одной из созданных биологически активных генно-терапевтической субстанций, выбранной именно для данного пациента на основе предварительного эксперимента по определению наиболее эффективного варианта из созданных и представленных в линейке биологически активных генно-терапевтических субстанций, в органы и ткани этого пациента, и/или во введении аутологичных клеток пациента, трансфицированных одной из созданных биологически активных генно-терапевтической субстанций, выбранной именно для данного пациента на основе предварительного эксперимента по определению наиболее эффективного варианта из созданных и представленных в линейке биологически активных генно-терапевтических субстанций, в органы и ткани этого пациента.
Перечень фигур
На фиг. 1
Представлена нуклеотидная последовательность немодифицированной кДНК гена GPX3, последовательность которой идентична приводимой в базе даных GenBank под номером NM_002084.3 - SEQ ID No: 1.
На фиг. 2
Представлена нуклеотидная последовательность модифицированной кДНК гена GPX3, SEQ ID No: 2, которая
содержит 1 нуклеотидную замену G→C в позиции 238 и 1 нуклеотидную замену G→T в позиции 277, не приводящие к изменениям в аминокислотной последовательности белка глутатионпероксидазы-3.
На фиг. 3
Представлена нуклеотидная последовательность модифицированной кДНК гена GPX3, SEQ ID No: 3, которая
содержит 1 нуклеотидную замену G→C в позиции 238; две нуклеотидных замены G→T в позициях 277, 301; 1 нуклеотидную замену А→С в позиции 325, не приводящие к изменениям в аминокислотной последовательности белка глутатионпероксидазы-3.
На фиг. 4
Представлена нуклеотидная последовательность модифицированной кДНК гена GPX3, SEQ ID No: 4, которая
содержит 1 нуклеотидную замену G→C в позиции 238; две нуклеотидных замены G→T в позициях 277, 301; 1 нуклеотидную замену А→С в позиции 325; 1 нуклеотидную замену G→A в позиции 445; 1 нуклеотидную замену A→G в позиции 472, не приводящие к изменениям в аминокислотной последовательности белка глутатионпероксидазы-3.
На фиг. 5
Представлена нуклеотидная последовательность модифицированной кДНК гена GPX3, SEQ ID No: 5, которая
содержит 1 нуклеотидную замену G→C в позиции 238; две нуклеотидных замены G→T в позициях 277, 301; 1 нуклеотидную замену А→С в позиции 325; 1 нуклеотидную замену G→А в позиции 445; 3 нуклеотидных замены A→G в позиции 472, 586, 673, не приводящие к изменениям в аминокислотной последовательности белка глутатионпероксидазы-3.
На фиг. 6
Представлена нуклеотидная последовательность модифицированной кДНК гена GPX3, SEQ ID No: 6, которая
содержит 2 нуклеотидных замены G→C в позициях 238, 826; три нуклеотидных замены G→T в позициях 277, 301, 697; 2 нуклеотидных замены А→С в позиции 325, 796; 1 нуклеотидную замену G→A в позиции 445; 3 нуклеотидных замены A→G в позиции 472, 586, 673, не приводящие к изменениям в аминокислотной последовательности белка глутатионпероксидазы-3.
На фиг. 7
Представлена нуклеотидная последовательность модифицированной кДНК гена GPX3, SEQ ID No: 7, которая
не содержит нетранслируемые 5' и 3' области гена и содержит 2 нуклеотидных замены G→C в позициях 238, 826; три нуклеотидных замены G→T в позициях 277, 301, 697; 2 нуклеотидных замены А→С в позиции 325, 796; 1 нуклеотидную замену G→A в позиции 445; 3 нуклеотидных замены A→G в позиции 472, 586, 673, не приводящие к изменениям в аминокислотной последовательности белка глутатионпероксидазы-3.
На фиг. 8
С целью последующего корректного определения генно-терапевтического эффекта после трансфекции фибробластов биологически активной генно-терапевтической субстанции с кДНК гена GPX3 проводили анализ эндогенной экспрессии гена GPX3 в культуре первичных фибробластов. На фигуре представлены графики накопления продуктов полимеразной цепной реакции (ПЦР), соответствующих:
1 - кДНК гена GPX3, фибробласты со сниженной экспрессией гена GPX3
2 - кДНК гена GPX3, фибробласты с нормальной экспрессией гена GPX3
3 - кДНК гена В2М, фибробласты со сниженной экспрессией гена GPX3
4 - кДНК гена В2М, фибробласты с нормальной экспрессией гена GPX3
В качестве референтного гена использовали ген В2М (Бета-2-микроглобулин) приведенного в базе данных GenBank под номером NM 004048.2.
На фиг. 9
С целью подтверждения увеличения экспрессии гена GPX3 в клеточной культуре фибробластов со сниженной экспрессией гена GPX3 при трансфекции данных клеток биологически активной генно-терапевтической субстанцией с кДНК гена GPX3 представлены графики накопления ПЦР-продуктов, соответствующих:
1 - кДНК гена GPX3 в фибробластах с нормальной экспрессией гена GPX3,
2 - кДНК гена GPX3 в фибробластах со сниженной экспрессией гена GPX3 до трансфекции БАГТС с кДНК гена GPX3.
3 - кДНК гена GPX3 в фибробластах со сниженной экспрессией гена GPX3 после трансфекции БАГТС с кДНК гена GPX3.
4 - кДНК гена GPX3 в фибробластах со сниженной экспрессией гена GPX3 после трансфекции вектором без кДНК гена GPX3.
5 - кДНК гена В2М в фибробластах с нормальной экспрессией гена GPX3.
6 - кДНК гена В2М в фибробластах со сниженной экспрессией гена GPX3 до трансфекции БАГТС с кДНК гена GPX3.
5 - кДНК гена В2М в фибробластах со сниженной экспрессией гена GPX3 после трансфекции БАГТС с кДНК гена GPX3.
8 - кДНК гена В2М в фибробластах со сниженной экспрессией гена GPX3 после трансфекции вектором без кДНК гена GPX3.
Из графиков следует, что в случае трансфекции вектором без вставки кДНК гена GPX3 уровень кДНК гена GPX3 в фибробластах не изменился, а в случае трансфекции вектором с кДНК GPX3-уровень кДНК фибробластов со сниженной экспрессией гена GPX3 многократно увеличился (до уровня выше, чем уровень кДНК гена GPX3 в нормальных фибробластах).
На фиг. 10
С целью подтверждения увеличения активности белка глутатионпероксидазы-3 в клеточной культуре фибробластов с нормальной экспрессией гена GPX3 при трансфекции данных клеток биологически активной генно-терапевтической субстанцией содержащим кДНК GPX3 представлен график изменения активности белка глутатионпероксидазы-3 в зависимости от разведения клеточного лизата немодифицированных фибробластов (культура А), трансфицированных вектором pCDNA 3.1 (+) не содержащим кДНК GPX3 (культура В) и трансфицированных биологически активной генно-терапевтической субстанцией на базе вектора pCDNA 3.1, содержащего GPX3 SEQ ID No: 1 (культура С). Из графика следует, что при трансфекции фибробластов биологически активной генно-терапевтической субстанцией с кДНК гена GPX3 происходит увеличение активности глутатионпероксидазы-3 в клеточном лизате.
Обозначения:
 культура А
культура А
 культура В
культура В
 культура С
культура С
На фиг. 11
С целью подтверждения увеличения активности глутатионпероксидазы-3 в коже человека при введении в кожу клеточной культуры фибробластов, трансфицированной биологически активной генно-терапевтической субстанцией представлен анализ изменения активности глутатионпероксидазы-3 в коже пациентов. При этом пациентам вводили три варианта культуры аутологичных фибробластов - нетрансфицированные (А), трансфицированные вектором pCMV6-XL5 (Б) и трансфицированные биологически активной генно-терапевтической субстанцией на базе pCMV6-GPX3 SEQ ID No: 7 (С) - в кожу предплечья. Также анализировали активность глутатионпероксидазы-3 в интактной коже. Показано повышение активности глутатионпероксидазы-3 в коже пациента в области введения фибробластов, трансфицированных биологически активной генно-терапевтической субстанцией кДНК гена GPX3.(C)
Обозначения:
 культура А
культура А
 культура В
культура В
 культура С
культура С
 контрольная биопсия
контрольная биопсия
На фиг. 12
С целью подтверждения увеличения активности глутатионпероксидазы-3 до различного индивидуального уровня в клеточных культурах фибробластов пациентов при трансфекции данных клеток биологически активными генно-терапевтическими субстанциями с модифицированными и нативной кДНК гена GPX3 в зависимости от наличия и типа в них той или иной модификации кДНК гена GPX3 представлен анализ изменения активности глутатионпероксидазы-3 в культурах фибробластов кожи человека в зависимости от наличия и типа модификаций в кДНК гена GPX3, используемой для трансфекции фибробластов.
Культуры фибробластов 23-х пациентов делили на 8 частей каждую с (А) по (Н); первые части (А) клеточных культур пациентов трансфицировали биологически активной генно-терапевтической субстанцией pCMV6-GPX3 SEQ ID No: 1, части (В) трансфицировали биологически активной генно-терапевтической субстанцией pCMV6-GPX3 SEQ ID No: 2, части (С) трансфицировали биологически активной генно-терапевтической субстанцией pCMV6-GPX3 SEQ ID No: 3, части (D) трансфицировали биологически активной генно-терапевтической субстанцией pCMV6-GPX3 SEQ ID No: 4, части (E) трансфицировали биологически активной генно-терапевтической субстанцией pCMV6-GPX3 SEQ ID No: 5, части (F) трансфицировали биологически активной генно-терапевтической субстанцией pCMV6-GPX3 SEQ ID No: 6, части (G) трансфицировали биологически активной генно-терапевтической субстанцией pCMV6-GPX3 SEQ ID No: 7, части (H) трансфицировали векторной плазмидой, не содержащей кДНК гена GPX3.
По итогам анализа уровня активности глутатионпероксидазы-3 выбрали показатели, касательно каждой части клеточной культуры от каждого пациента, продемонстрировавшие максимальные уровни активности глутатионпероксидазы-3 и объединили их в семь групп, исходя из следующего критерия:
В группе 1 максимальная активность глутатионпероксидазы-3 наблюдалась при трансфекции pCMV6-GPX3 SEQ ID No: 1.
В группе 2 максимальная активность глутатионпероксидазы-3 наблюдалась при трансфекции pCMV6-GPX3 SEQ ID No: 2.
В группе 3 максимальная активность глутатионпероксидазы-3 наблюдалась при трансфекции pCMV6-GPX3 SEQ ID No: 3.
В группе 4 максимальная активность глутатионпероксидазы-3 наблюдалась при трансфекции pCMV6-GPX3 SEQ ID No: 4.
В группе 5 максимальная активность глутатионпероксидазы-3 наблюдалась при трансфекции pCMV6-GPX3 SEQ ID No: 5.
В группе 6 максимальная активность глутатионпероксидазы-3 наблюдалась при трансфекции pCMV6-GPX3 SEQ ID No: 6.
В группе 7 максимальная активность глутатионпероксидазы-3 наблюдалась при трансфекции pCMV6-GPX3 SEQ ID No: 7.
Ни в одной из клеточных культур не наблюдалось того, что максимальная активность глутатионпероксидазы-3 присутствует при трансфекции вектором без вставки кДНК гена GPX3.
На фигуре 12 для каждой группы клеточных культур приведены диаграммы показателей ингибирования цветной реакции (усредненных в рамках группы, в случае, если в группу входит более одной клеточной культуры) применительно ко всем, участвующим в эксперименте активным генно-терапевтическим субстанциям, после трансфекции этих клеточных культур активными генно-терапевтическими субстанциями, содержащими модифицированные и нативную кДНК гена GPX3
Из фигуры следует, что достижение максимальной активности глутатионпероксидазы-3 в культурах фибробластов кожи различных пациентов при их трансфекции биологически активными генно-терапевтическими субстанциями, связано с индивидуальными особенностями пациентов и зависит от наличия и типа модификаций в кДНК гена GPX3, входящих в биологически активные генно-терапевтические субстанции.
Каждая биологически активная генно-терапевтическая субстанция из линейки биологически активных генно-терапевтических субстанций является эффективной в некоторой значительной группе пациентов. Следовательно для выбора наиболее эффективной биологически активной генно-терапевтической субстанции из линейки биологически активных генно-терапевтических субстанций для терапевтических целей необходимо предварительное персонализированное исследование пациента.
Обозначения:
 части клеточных культур, трансфицированных БАГТС GPX3 SEQ ID No: 1 (А)
части клеточных культур, трансфицированных БАГТС GPX3 SEQ ID No: 1 (А)
 части клеточных культур, трансфицированных БАГТС GPX3 SEQ ID No: 2 (В)
части клеточных культур, трансфицированных БАГТС GPX3 SEQ ID No: 2 (В)
 части клеточных культур, трансфицированных БАГТС GPX3 SEQ ID No: 3 (С)
части клеточных культур, трансфицированных БАГТС GPX3 SEQ ID No: 3 (С)
 части клеточных культур, трансфицированных БАГТС GPX3 SEQ ID No: 4 (D)
части клеточных культур, трансфицированных БАГТС GPX3 SEQ ID No: 4 (D)
 части клеточных культур, трансфицированных БАГТС GPX3 SEQ ID No: 5 (Е)
части клеточных культур, трансфицированных БАГТС GPX3 SEQ ID No: 5 (Е)
 части клеточных культур, трансфицированных БАГТС GPX3 SEQ ID No: 6 (F)
части клеточных культур, трансфицированных БАГТС GPX3 SEQ ID No: 6 (F)
 части клеточных культур, трансфицированных БАГТС GPX3 SEQ ID No: 7 (G)
части клеточных культур, трансфицированных БАГТС GPX3 SEQ ID No: 7 (G)
 части клеточных культур, трансфицированных плацебо (Н)
части клеточных культур, трансфицированных плацебо (Н)
На фиг. 13
С целью подтверждения увеличения экспрессии гена GPX3 в клеточной культуре кератоцитов и эпителиальных клеток глаза при трансфекции данных клеток биологически активной генно-терапевтической субстанцией с кДНК гена GPX3 приведены графики накопления ПЦР-продуктов, соответствующих:
1 - кДНК гена GPX3, кератоциты до трансфекции
2 - кДНК гена GPX3, эпителий роговицы до трансфекции
3 - кДНК гена GPX3, кератоциты после трансфекции
4 - кДНК гена GPX3, эпителий роговицы после трансфекции
5 - кДНК гена В2М, кератоциты до трансфекции
6 - кДНК гена В2М, эпителий роговицы до трансфекции
7 - кДНК гена В2М, кератоциты после трансфекции
6 - кДНК гена В2М, эпителий роговицы после трансфекции
Ген В2М использовали в качестве референтного.
Из фигуры следует, что в результате трансфекции уровень специфической кДНК гена GPX3 в культуре кератоцитов и в культуре эпителия многократно вырос.
На фиг. 14
С целью подтверждения увеличения экспрессии гена GPX3 в клеточной культуре хондробластов при трансфекции данных клеток биологически активной генно-терапевтической субстанцией с кДНК гена GPX3 приведены графики накопления ПЦР-продуктов, соответствующих:
1 - кДНК гена GPX3, до трансфекции
2 - кДНК гена GPX3, после трансфекции
3 - кДНК гена В2М, до трансфекции
4 - кДНК гена В2М, после трансфекции
Ген В2М использовали в качестве референтного.
Из фигуры следует, что в результате трансфекции уровень специфической кДНК гена GPX3 вырос многократно.
На фиг. 15
С целью подтверждения увеличения активности глутатионпероксидазы-3 в коже человека при введении в кожу биологически активной генно-терапевтической субстанции представлен анализ изменения активности глутатионпероксидазы-3 в коже. При этом пациенту вводили биологически активную генно-терапевтическую субстанцию, содержащую векторную плазмиду с кДНК гена GPX3 pCMV6-GPX3 SEQ ID No: 4 (В) и параллельно вводили плацебо, представляющее собой комбинацию векторной плазмиды pCMV-XL5 не содержащей кДНК гена GPX3 с транспортной молекулой (А) - в кожу предплечья. Показано увеличение активности глутатионпероксидазы-3 в биоптате кожи пациента 1В, которому вводились биологически активная генно-терапевтическая субстанция, содержащая генетическую конструкцию с кДНК гена GPX3, что говорит об эффективности биологически активной генно-терапевтической субстанции.
Обозначения:
 пациент 1А
пациент 1А
 пациент 1В
пациент 1В
 пациент 1В до введения БАГТС
пациент 1В до введения БАГТС
На фиг. 16
С целью подтверждения увеличения активности глутатионпероксидазы-3 в слизистой оболочке рта человека при введении в слизистую оболочку рта биологически активной генно-терапевтической субстанции представлен анализ изменения активности глутатионпероксидазы-3 в слизистой оболочке рта. При этом пациенту вводили биологически активную генно-терапевтическую субстанцию, содержащую векторную плазмиду с кДНК гена GPX3 pCDNA 3.1 GPX3 SEQ ID No: 5 (В) и параллельно вводили плацебо pCDNA 3.1(+), представляющее собой комбинацию векторной плазмиды не содержащей кДНК гена GPX3 с транспортной молекулой (А) - в слизистую оболочку рта.
Показано увеличение активности глутатионпероксидазы-3 в лизате биоптата слизистой оболочки рта пациента 1В, которому вводились биологически активная генно-терапевтическая субстанция, содержащая генетическую конструкцию с кДНК гена GPX3, что говорит об эффективности биологически активной генно-терапевтической субстанции.
Обозначения:
 пациент 1А
пациент 1А
 пациент 1В
пациент 1В
 пациент 1В до введения БАГТС
пациент 1В до введения БАГТС
На фиг. 17
С целью подтверждения увеличения активности глутатионпероксидазы-3 в мышечной ткани человека при введении в мышечную ткань биологически активной генно-терапевтической субстанции представлен анализ изменения активности глутатионпероксидазы-3 в мышечной ткани. При этом пациенту вводили биологически активную генно-терапевтическую субстанцию, содержащую векторную плазмиду с кДНК гена GPX3-pCMV6-Kan/Neo GPX3 SEQ ID No: 6 (В) и параллельно вводили плацебо pCMV6-Kan/Neo, представляющее собой комбинацию векторной плазмиды не содержащей кДНК гена GPX3 с транспортной молекулой (А) - в мышечную ткань в зоне предплечья. Показано увеличение активности глутатионпероксидазы-3 в биоптате мышечной ткани пациента 1В, которому вводились биологически активная генно-терапевтическая субстанция, содержащая генетическую конструкцию с кДНК гена GPX3, что говорит об эффективности биологически активной генно-терапевтической субстанции.
Обозначения:
 пациент 1А
пациент 1А
 пациент 1В
пациент 1В
 пациент 1В до введения БАГТС
пациент 1В до введения БАГТС
На фиг. 18
С целью подтверждения увеличения активности глутатионпероксидазы-3 до различного индивидуального уровня при введении в кожу пациентов биологически активных генно-терапевтических субстанций с модифицированными и нативной кДНК гена GPX3 анализировали уровень активности глутатионпероксидазы-3 в коже человека в зависимости от наличия и типа модификаций в кДНК гена GPX3.
Каждому из 21-го пациента, отобранных в случайном порядке, вводили в кожу предплечья 7 биологически активных генно-терапевтических субстанций pCMV6- SEQ ID No: 1, pCMV6- SEQ ID No: 2, pCMV6- SEQ ID No: 3, pCMV6- SEQ ID No: 4, pCMV6- SEQ ID No: 5, pCMV6- SEQ ID No: 6, pCMV6- SEQ ID No: 7, и плацебо pCMV6- XL5.
По итогам анализа уровня активности глутатионпероксидазы-3 в биоптатах выбрали показатели, касательно каждого биоптата от каждого пациента, продемонстрировавшие максимальные уровни активности глутатионпероксидазы-3 и объединили их в семь групп, исходя из следующего критерия:
В группе 1 максимальная активность глутатионпероксидазы-3 наблюдалась при введении pCMV6-GPX3 SEQ ID No: 1.
В группе 2 максимальная активность глутатионпероксидазы-3 наблюдалась при введении pCMV6-GPX3 SEQ ID No: 2.
В группе 3 максимальная активность глутатионпероксидазы-3 наблюдалась при введении pCMV6-GPX3 SEQ ID No: 3.
В группе 4 максимальная активность глутатионпероксидазы-3 наблюдалась при введении pCMV6-GPX3 SEQ ID No: 4.
В группе 5 максимальная активность глутатионпероксидазы-3 наблюдалась при введении pCMV6-GPX3 SEQ ID No: 5.
В группе 6 максимальная активность глутатионпероксидазы-3 наблюдалась при введении pCMV6-GPX3 SEQ ID No: 6.
В группе 7 максимальная активность глутатионпероксидазы-3 наблюдалась при введении pCMV6-GPX3 SEQ ID No: 7.
Ни в одном из биоптатов не наблюдалось того, что максимальная активность глутатионпероксидазы-3 присутствует в случае введения плацебо.
На фигуре 18 для каждой группы биоптатов приведены диаграммы показателей ингибирования цветной реакции (усредненных в рамках группы, в случае, если в группу входит более одного биоптата) применительно ко всем, участвующим в эксперименте активным генно-терапевтическим субстанциям, после введения пациентам этих активных генно-терапевтических субстанций, содержащих модифицированные и нативную кДНК гена GPX3.
Из данного примера следует, что достижение максимальной активности глутатионпероксидазы-3 в биоптатах кожи различных пациентов при введении им в кожу биологически активных генно-терапевтических субстанций, связано с индивидуальными особенностями пациентов и зависит от наличия и типа модификаций в кДНК гена GPX3, входящих в биологически активные генно-терапевтические субстанции.
Каждая биологически активная генно-терапевтическая субстанция из линейки биологически активных генно-терапевтических субстанций является эффективной в некоторой значительной группе пациентов. Следовательно, для выбора наиболее эффективной биологически активной генно-терапевтической субстанции из линейки биологически активных генно-терапевтических субстанций для терапевтических целей, необходимо предварительное персонализированное исследование пациента.
Обозначения:
 биоптаты пациентов после введения БАГТС GPX3 SEQ ID No: 1 (А)
биоптаты пациентов после введения БАГТС GPX3 SEQ ID No: 1 (А)
 биоптаты пациентов после введения БАГТС GPX3 SEQ ID No: 2 (В)
биоптаты пациентов после введения БАГТС GPX3 SEQ ID No: 2 (В)
 биоптаты пациентов после введения БАГТС GPX3 SEQ ID No: 3 (С)
биоптаты пациентов после введения БАГТС GPX3 SEQ ID No: 3 (С)
 биоптаты пациентов после введения БАГТС GPX3 SEQ ID No: 4 (D)
биоптаты пациентов после введения БАГТС GPX3 SEQ ID No: 4 (D)
 биоптаты пациентов после введения БАГТС GPX3 SEQ ID No: 5 (Е)
биоптаты пациентов после введения БАГТС GPX3 SEQ ID No: 5 (Е)
 биоптаты пациентов после введения БАГТС GPX3 SEQ ID No: 6 (F)
биоптаты пациентов после введения БАГТС GPX3 SEQ ID No: 6 (F)
 биоптаты пациентов после введения БАГТС GPX3 SEQ ID No: 7 (G)
биоптаты пациентов после введения БАГТС GPX3 SEQ ID No: 7 (G)
 биоптаты пациентов после введения плацебо (Н)
биоптаты пациентов после введения плацебо (Н)
На фиг. 19
С целью определения наиболее эффективной применительно к конкретному пациенту биологически активной генно-терапевтической субстанции анализировали активность глутатионпероксидазы-3 в клеточных лизатах фибробластов этого пациента, трансфицированных разными генетическими конструкциями, содержащими нативную или модифицированные кДНК гена GPX3.
По итогам анализа активности глутатионпероксидазы-3 в культуре фибробластов пациента выделили вариант биологически активной генно-терапевтической субстанции, при трансфекции которой происходит максимальное ингибирование в лизате клеточной культуры и соответственно наблюдается максимальная активность глутатионпероксидазы-3. В данном эксперименте максимальное ингибирование в лизате наблюдается при трансфекции биологически активной генно-терапевтической субстанцией на базе pCMV6 GPX3 SEQ ID No: 7, содержащей модифицированную кДНК GPX3, что показано на фигуре 19.
Таким образом, выбрана наиболее эффективная применительно к данному пациенту биологически активная генно-терапевтическая субстанция для последующей трансфекции клеток пациента в рамках терапевтической процедуры.
Обозначения:
1 - клеточный лизат после трансфекции БАГТС GPX3 SEQ ID No: 1 (А)
2 - клеточный лизат после трансфекции БАГТС GPX3 SEQ ID No: 2 (В)
3 - клеточный лизат после трансфекции БАГТС GPX3 SEQ ID No: 3 (С)
4 - клеточный лизат после трансфекции БАГТС GPX3 SEQ ID No: 4 (D)
5 - клеточный лизат после трансфекции БАГТС GPX3 SEQ ID No: 5 (Е)
6 - клеточный лизат после трансфекции БАГТС GPX3 SEQ ID No: 6 (F)
7 - клеточный лизат после трансфекции БАГТС GPX3 SEQ ID No: 7 (G)
8 - клеточный лизат после трансфекции плацебо (Н)
На фиг .20
С целью определения наиболее эффективной применительно к конкретному пациенту биологически активной генно-терапевтической субстанции анализировали активность глутатионпероксидазы-3 в лизатах биоптатов кожи этого пациента, после введения ему биологически активных генно-терапевтических субстанций, содержащих нативную или модифицированные кДНК гена GPX3.
По итогам анализа активности глутатионпероксидазы-3 в лизате биоптатов кожи пациента выделили вариант биологически активной генно-терапевтической субстанции, при введении которой происходит максимальное ингибирование в лизате биоптата кожи и соответственно наблюдается максимальная активность глутатионпероксидазы-3. В данном эксперименте максимальное ингибирование в лизате отмечено при введении биологически активной генно-терапевтической субстанции на базе pCMV6 GPX3 SEQ ID No: 3, содержащей модифицированную кДНК GPX3, что показано на фигуре 20.
Таким образом, выбрана наиболее эффективная применительно к данному пациенту биологически активная генно-терапевтическая субстанция для ее последующего введения пациенту в рамках терапевтической процедуры.
Обозначения:
1 - лизат биоптата после введения БАГТС GPX3 SEQ ID No: 1 (А)
2 - лизат биоптата после введения БАГТС GPX3 SEQ ID No: 2 (В)
3 - лизат биоптата после введения БАГТС GPX3 SEQ ID No: 1 (С)
4 - лизат биоптата после введения БАГТС GPX3 SEQ ID No: 4 (D)
5 - лизат биоптата после введения БАГТС GPX3 SEQ ID No: 5 (Е)
6 - лизат биоптата после введения БАГТС GPX3 SEQ ID No: 6 (F)
7 - лизат биоптата после введения БАГТС GPX3 SEQ ID No: 7 (G)
8 - лизат биоптата после введения плацебо (Н)
Реализация изобретения.
При снижении экспрессии генов, кодирующих белки окислительно-восстановительного баланса, например гена GPX3, происходит снижение антиоксидантной активности белка в организме.
Нокаутные по гену GPX3(-/-) мыши-гомозиготы демонстрировали снижение глутатионпероксидазной активности, повышение уровня селена в плазме, если мыши находятся на селен-обогащенной дитете, и снижение уровня селена в почках, независимо от получения дополнительного селена с пищей.
[PMID: 20015939], [PMID: 21518981]
Преимущества использования генетической конструкции с геном GPX3 для коррекции уровня активности белка глутатионпероксидазы-3 в клетках органов и тканей человека, по сравнению с использованием рекомбинантной глутатионпероксидазы по прототипу WO 1488007541 А1 следующие:
1) легче обеспечить более высокий и стабильный уровень белка в клетках,
2) не требуется сложная и дорогостоящая процедура рефолдинга и очистки белкового препарата,
3) обеспечивается транспортировка биологически активной генно-терапевтической субстанции в больший спектр клеток органов и тканей человека, а также более эффективная внутриклеточная транспортировка биологически активной генно-терапевтической субстанции,
4) учтены индивидуальные особенности пациентов.
Таким образом, для создания линейки биологически активных генно-терапевтических субстанций по данному изобретению был выбран ген GPX3, а не белок, кодируемый этим геном.
Для получения линейки биологически активных генно-терапевтических субстанций осуществляют следующие действия:
1. Получение нативной кДНК гена GPX3, содержащей белок-кодирующую область гена GPX3, клонирование ее в промежуточную плазмиду для дальнейших модификаций этой кДНК
2. Внесение в последовательность нуклеотидов кДНК гена GPX3 модификаций с целью создания линейки кДНК гена GPX3, обеспечивающих достаточный для борьбы с оксидативным стрессом уровень трансляции белка глутатионпероксидазы-3.
3. Клонирование нативной и модифицированных кДНК гена GPX3 в векторные плазмиды, способные обеспечить эффективную экспрессию этой кДНК в клетках органов и тканей человека.
4. Трансформация каждой из полученных генетических конструкций бактериальных клеток E.coli, анализ трансформированных клонов на предмет наличия, ориентации и копийности вставки кДНК и наращивание отобранных клонов для получения необходимого для дальнейшей работы количества вариантов плазмидной ДНК.
5. Выделение линейки генетических конструкций, содержащих модифицированные и нативную кДНК гена GPX3 для создания на ее базе линейки биологически активных генно-терапевтических субстанций.
6. Создание линейки биологически активных генно-терапевтических субстанций, каждая из которых включает генетическую конструкцию с модифицированной или нативной кДНК гена GPX3, или комбинацию такой конструкции с транспортной молекулой для эффективной трансфекции различных типов клеток органов и тканей и/или введения в органы и ткани человека.
Для доказательства эффективности созданных биологически активных генно-терапевтических субстанций, приводящих к увеличению экспрессии гена GPX3, проводят следующие исследования:
A) Выращивание культур различных типов клеток из биоптатов различных органов и тканей человека, например, фибробластов кожи человека, или хондробластов, или кератоцитов, или эпителиальных клеток роговицы.
B) Выделение РНК из культуры клеток, например, фибробластов кожи человека, или хондробластов, или кератоцитов, или эпителиальных клеток роговицы, и анализ транскрипции гена GPX3 из генома этих клеток.
C) Трансфекция культуры клеток, например, фибробластов кожи человека, или хондробластов, или кератоцитов, или эпителиальных клеток роговицы, биологически активными генно-терапевтическими субстанциями содержащими нативную и/или модифицированные кДНК гена GPX3 и параллельная трансфекция культуры этих же клеток векторной плазмидой, не содержащей кДНК гена GPX3 в различных комбинациях.
D) Сравнительный анализ изменения уровня кДНК и/или изменения активности белка глутатионпероксидазы-3, после трансфекции в различных комбинациях клеток, например, фибробластов кожи человека, или хондробластов, или кератоцитов, или эпителиальных клеток роговицы, биологически активными генно-терапевтическими субстанциями содержащими нативную и/или модифицированные кДНК гена GPX3 и параллельной трансфекции культуры этих же клеток векторной плазмидой, не содержащей кДНК гена GPX3. Данный анализ проводят, в частности, перед предполагаемой терапией с целью определения наиболее эффективной для пациента биологически активной генно-терапевтической субстанции.
E) Введение пациентам в органы и ткани культуры клеток с кДНК гена GPX3, например, введение, в кожу человека, аутологичных фибробластов, трансфицированных биологически активной генно-терапевтической субстанцией с кДНК гена GPX3 и параллельное введение пациентам в органы и ткани, например, в кожу культур этих же клеток не трансфицированных и трансфицированных вектором без вставки кДНК гена GPX3 и/или введение пациентам в органы и ткани биологически активных генно-терапевтических субстанций, например, введение в кожу человека биологически активных генно-терапевтических субстанций, содержащих нативную и/или модифицированные кДНК GPX3, а также плацебо в различных комбинациях.
F) Сравнительный анализ активности белка глутатионпероксидазы-3 в органах и тканях человека, в частности в коже человека, после введения клеток нетрансфицированных и трансфицированных биологически активными генно-терапевтическими субстанциями, содержащими кДНК гена GPX3 и векторными плазмидами, не содержащими кДНК гена GPX3 и/или биологически активных генно-терапевтических субстанций, содержащих нативную или модифицированные кДНК гена GPX3, а также плацебо.
G) Введение пациентам в органы и ткани, например, слизистую оболочку рта, или мышечную ткань биологически активных генно-терапевтических субстанций, содержащих нативную и/или модифицированные кДНК гена GPX3, а также плацебо.
H) Сравнительный анализ активности белка глутатионпероксидазы-3 в органах и тканях человека, в частности в слизистой оболочке рта, или мышечной ткани человека, после введения биологически активных генно-терапевтических субстанций, содержащих нативную и/или модифицированные кДНК GPX3 а также плацебо.
I) Введение пациентам в органы и ткани, например, введение в кожу пациента биологически активных генно-терапевтических субстанций, содержащих нативную и модифицированные кДНК гена GPX3.
J) Сравнительный анализ изменения активности белка глутатионпероксидазы-3 в органах и тканях пациента, в частности в коже, после введения биологически активных генно-терапевтических субстанций, содержащих нативную и модифицированные кДНК гена GPX3. Данный анализ проводят, в частности, перед предполагаемой терапией с целью выбора наиболее эффективной для пациента биологически активной генно-терапевтической субстанции из линейки биологически активных генно-терапевтических субстанций.
Пример 1
Получение нативной (немодифицированной) кДНК гена GPX3.
Немодифицированная кДНК гена GPX3 представляет собой последовательность нуклеотидов, идентичную приводимой в базе даных GenBank под номером NM_002084.3; нуклеотиды со 218 по 898 транслируются в аминокислотную последовательность, соответствующую приведенной в GenBank под номером NP_002075.2.
Суммарную РНК получают из клеток человеческой крови с помощью набора PAXGeneBlood RNA Kit (Qiagen, Germany) и используют для получения суммарной кДНК путем обратной транскрипции с помощью обратной транскриптазы RevertAid (ThermoScientific, USA) и случайных 9-нуклеотидных праймеров по методике производителя обратной транскриптазы. Затем, используя суммарную кДНК в качестве матрицы и специфичные, предварительно кинированные праймеры, комплементарные нуклеотидам 143-162 5' CCGGACACCTCAGACGGACG 3' (GPX3 F1) и 1022-1001 5' GGCTGGGGCCTTGAGTGATAGG 3' (GPX3 R1) из последовательности мРНК GPX3 (GenBank NM_002084.3), получают кДНК GPX3. Полимеразную цепную реакцию (ПЦР) проводят с помощью ДНК-полимеразы Phusion (ThermoScientific, USA), дающей продукты с тупыми концами. ПЦР проводят с помощью амплификатора Master CyclerGradient (Eppendorf, USA) в 50 мкл реакционной смеси, содержащей 0,5 мкл суммарной кДНК первой цепи, по 0,1 мкМ каждого праймера GPX3 F1 и GPX3 R1, 250 мкМ каждого дезоксинуклеотидтрифосфата (дАТФ, дЦТФ, дТТФ и дГТФ), 100 мМтрис-HCl (pH 8,85 при 20°С), 50 мМ сульфата аммония, 250 мМ хлористого калия, 0,01% Твин-20 и 5 ед. Pfu ДНК-полимеразы (PhusionThermoScientific, USA) при следующих условиях: первоначальная денатурация при +98°С в течение 30 сек, 35 циклов, включающих денатурацию при +98°С в течение 10 сек, отжиг праймеров при +64°С в течение 30 сек. и элонгацию при +68°С в течение 2 мин.
Продукт амплификации выделяют из агарозного геля с помощью набора QIAquickGelExtractionKit (Qiagen, Germany)
Амплифицированный фрагмент кДНК, несущий ген GPX3, клонируют в плазмидном векторе pUC19 (NEB, USA, кат номер N3041S). ДНК векторной плазмиды pUC19 (NEB, USA, кат. номер N3041S) гидролизуют рестриктазой Smal (NEB, USA), (или другой рестриктазой, дающей тупые концы) и обрабатывают щелочной фосфатазой. Амплифицированный фрагмент кДНК и линеаризованную плазмиду pUC19 лигируют с помощью ДНК-лигазы фага Т4 400000 ед./мл (NEB, USA, кат номер M0202S) из расчета 1 мкл фермента на 1 мкг ДНК. Лигирование проводят в объеме 20 мкл в присутствии 2 мМ АТФ, 50 мМ трис-HCl, pH 7,6, 10 мМ MgCl2, 10 мМ DTT в течение 10 ч при +16°C.
Полученной смесью трансформируют компетентные клетки E.coliTop10 (http://molbiol.ru/protocol/03_04.html), которые высевают на чашки Петри с L-агаром, содержащих 100 мкг/мл ампициллина и по 40 мкл на чашку растворов 100 мМ ИПТГ и 2% X-gal. Отдельные колонии анализируют на наличие вставки с помощью ПЦР с праймерами GPX3 F1 и GPX3 R1 и подтверждают секвенированием по методу Сэнгера, которое показывает наличие клонов с разной ориентацией целевого гена: EcoRI-5'NTR-кДНК GPX3-3'NTRHindIII и HindIII--5'NTR-кДНК GPX3-3'NTR-EcoRI
Полученная таким образом клонированная частичная (с 143 по 1022 н.п) нативная (немодифицированная) последовательность гена GPX3 длиной 880 н.п. в плазмиде pUC19-GPX3 SEQ ID No: 1 имеет первичную структуру, приведенную на фиг. 1.
Пример 2
Получение модифицированных кДНК гена GPX3.
Модификации проводят таким образом, чтобы не затрагивать первичную структуру белка глутатионпероксидазы-3, а именно, делеции 5' нетранслируемых областей или делеции 3'-нетранслируемых областей, или нуклеотидные замены, не приводящие к аминокислотным заменам или обрыву аминокислотной цепи, или комбинации вышеперечисленных модификаций и, соответственно, не влияющие на кодируемую этой последовательностью аминокислотную последовательность.
В частности для получения линейки кДНК гена GPX3 с целью повышения эффективности транскрипции и трансляции глутатионпероксидазы-3 в клетках тканей и органов человека в нативную последовательность кДНК GPX3, используя принцип оптимизации кодонов, вносят модификации путем замены минорных кодонов на синонимичные мажорные, а также проводят делеции 5' нетранслируемых областей или делеции 3'-нетранслируемых областей таким образом, чтобы замены не привели к изменениям в аминокислотной последовательности белка или обрыву аминокислотной цепи при трансляции, не ухудшили процессы транскрипции и трансляции.
Все модификации осуществляют в несколько этапов методом ПЦР мутагенеза набором QuikChange II XL kit или QuikChange Multi Site-Directed Mutagenesis Kit (AgilentTechNologies, USA,) согласно рекомендациям производителя.
http://www.agilent.com/cs/library/usermanuals/Public/200513.
К плазмидной ДНК pUC 19-GPX3 SEQ ID No: 1 по Примеру 1 (вариант pUC 19-GPX3 SEQ ID No: 1 с ориентацией целевого гена EcoRI-5'NTR-кДНК GPX3-3'NTRHindIII и вариант pUC 19-GPX3 SEQ ID No: 1 с ориентацией целевого гена HindIII--5'NTR-кДНК GPX3-3'NTR-EcoRI) в количестве 10-50 нг добавляют 50-100 нг праймера, содержащего необходимую замену, инсерцию или делецию длиной 25-45 н.п. и проводят ПЦР в буфере QuikChange Multi reaction buffer (AgilentTechNologies, USA) со смесью ферментов QuikChange Multi mix (AgilentTechNologies, USA) при следующих условиях: 95°C, 1 мин; далее от 30 до 35 циклов: 95°С 1 минута, 55°С 1 минута, 65°С 2 минуты/1000 н.п. После проведения ПЦР к амплификационной смеси добавляют 1-2 мкл рестриктазы Dpn I и инкубируют 1-2 часа при 37°С. Полученной смесью трансформируют компетентные клетки E.coliTop10 (http://molbiol.ru/protocol/03_04.html), которые высевают на чашки с L-агаром, содержащих 100 мкг/мл ампициллина. Трансформированнные колонии анализируют на содержание мутаций секвенированием плазмидной ДНК по методу Сэнгера.
Для получения модифицированной кДНК GPX3 SEQ ID No: 2 проводят последовательный ПЦР-мутагенез с праймерами, комплементарными участкам нативной кДНК GPX3 SEQ ID No: 1 (вариант pUC 19-GPX3 SEQ ID No: 1 с ориентацией целевого гена EcoRI-5'NTR-кДНК GPX3-3'NTRHindIII и вариант pUC 19-GPX3 SEQ ID No: 1 сориентацией целевого гена HindIII--5'NTR-кДНК GPX3-3'NTR-EcoRI), используемой в качестве матрицы:
1. GPX3 227-254 F:
5' CTGCTGCAGGCCTCCTGCCTGCTTTCCC 3',
комплементарный нуклеотидам 227-254, с заменой G→C в позиции 238
2. GPX3 266-288 F:
5' GGCTTCGTCTCTCAGAGCCGGGG 3',
комплементарный нуклеотидам 266-288, с заменой G→T в позиции 277.
Модифицированная таким образом нуклеотидная последовательность кДНК GPX3 SEQ ID No: 2 содержит 1 нуклеотидную замену G→C в позиции 238 и 1 нуклеотидную замену G→T в позиции 277, не приводящие к изменениям в аминокислотной последовательности белка глутатионпероксидазы-3 и имеет первичную структуру, приведенную на фиг. 2.
Для получения модифицированной кДНК GPX3 SEQ ID No: 3 проводят последовательный ПЦР-мутагенез с праймерами, комплементарными участкам нативной кДНК GPX3 SEQ ID No: 1 (вариант pUC 19-GPX3 SEQ ID No: 1 с ориентацией целевого гена EcoRI-5'NTR-кДНК GPX3-3'NTRHindIII и вариант pUC 19-GPX3 SEQ ID No: 1 сориентацией целевого гена HindIII--5'NTR-кДНК GPX3-3'NTR-EcoRI), используемой в качестве матрицы:
1. GPX3 227-254 F:
5' CTGCTGCAGGCCTCCTGCCTGCTTTCCC 3',
комплементарный нуклеотидам 227-254, с заменой G→C в позиции 238
2. GPX3 266-288 F:
5' GGCTTCGTCTCTCAGAGCCGGGG 3',
комплементарный нуклеотидам 266-288, с заменой G→T в позиции 277.
3. GPX3 289-318 F:
5' ACAAGAGAAGTCTAAGATGGACTGCCATGG 3',
Комплементарный нуклеотидам 289-318, с заменой G→T в позиции 301
4. GPX3 319-343 F:
5' TGGCATCAGTGGCACCATTTACGAG 3',
Комплементарный нуклеотидам 319-343, с заменой А→С в позиции 325.
Модифицированная таким образом нуклеотидная последовательность кДНК GPX3 SEQ ID No: 3 содержит 1 нуклеотидную замену G→C в позиции 238; две нуклеотидных замены G→T в позициях 277, 301; 1 нуклеотидную замену А→С в позиции 325, не приводящие к изменениям в аминокислотной последовательности белка глутатионпероксидазы-3 и имеет первичную структуру, приведенную на фиг 3.
Для получения модифицированной кДНК GPX3 SEQ ID No: 4 проводят последовательный ПЦР-мутагенез с праймерами, комплементарными участкам нативной кДНК GPX3 SEQ ID No: 1 (вариант pUC 19-GPX3 SEQ ID No: 1 с ориентацией целевого гена EcoRI-5'NTR-кДНК GPX3-3'NTRHindIII и вариант pUC 19-GPX3 SEQ ID No: 1 сориентацией целевого гена HindIII--5'NTR-кДНК GPX3-3'NTR-EcoRI), используемой в качестве матрицы:
1. GPX3 227-254 F:
5' CTGCTGCAGGCCTCCTGCCTGCTTTCCC 3',
Комплементарный нуклеотидам 227-254, с заменой G→C в позиции 238
2. GPX3 266-288 F:
5' GGCTTCGTCTCTCAGAGCCGGGG 3',
комплементарный нуклеотидам 266-288, с заменой G→T в позиции 277.
3. GPX3 289-318 F:
5' ACAAGAGAAGTCTAAGATGGACTGCCATGG 3',
комплементарный нуклеотидам 289-318, с заменой G→T в позиции 301
4. GPX3 319-343 F:
5' TGGCATCAGTGGCACCATTTACGAG 3',
Комплементарный нуклеотидам 319-343, с заменой А→С в позиции 325.
5. GPX3 435-460 F:
5' GAGGCCTGACAGGCCAGTACATTGAA 3',
Комплементарный нуклеотидам 435-460, с заменой G→A в позиции 445
6. GPX3 461-487 F:
5' CTGAATGCACTGCAGGAAGAGCTTGCA 3'
Комплементарный нуклеотидам 461-487, с заменой A→G в позиции 472.
Модифицированная таким образом нуклеотидная последовательность кДНК GPX3 SEQ ID No: 4 содержит 1 нуклеотидную замену G→C в позиции 238; две нуклеотидных замены G→T в позициях 277, 301; 1 нуклеотидную замену А→С в позиции 325; 1 нуклеотидную замену G→A в позиции 445; 1 нуклеотидную замену A→G в позиции 472, не приводящие к изменениям в аминокислотной последовательности белка глутатионпероксидазы-3 и имеет первичную структуру, приведенную на фиг 4.
Для получения модифицированной кДНК GPX3 SEQ ID No: 5 проводят последовательный ПЦР-мутагенез с праймерами, комплементарными участкам нативной кДНК GPX3 SEQ ID No: 1 (вариант pUC 19-GPX3 SEQ ID No: 1 с ориентацией целевого гена EcoRI-5'NTR-кДНК GPX3-3'NTRHindIII и вариант pUC 19-GPX3 SEQ ID No: 1 сориентацией целевого гена HindIII--5'NTR-кДНК GPX3-3'NTR-EcoRI), используемой в качестве матрицы:
1. GPX3 227-254 F:
5' CTGCTGCAGGCCTCCTGCCTGCTTTCCC 3',
Комплементарный нуклеотидам 227-254, с заменой G→C в позиции 238
2. GPX3 266-288 F:
5' GGCTTCGTCTCTCAGAGCCGGGG 3',
Комплементарный нуклеотидам 266-288, с заменой G→T в позиции 277.
3. GPX3 289-318 F:
5' ACAAGAGAAGTCTAAGATGGACTGCCATGG 3',
Комплементарный нуклеотидам 289-318, с заменой G→T в позиции 301
4. GPX3 319-343 F:
5' TGGCATCAGTGGCACCATTTACGAG 3',
Комплементарный нуклеотидам 319-343, с заменой А→С в позиции 325.
5. GPX3 435-460 F:
5' GAGGCCTGACAGGCCAGTACATTGAA 3',
Комплементарный нуклеотидам 435-460, с заменой G→A в позиции 445
6. GPX3 461-487 F:
5' CTGAATGCACTGCAGGAAGAGCTTGCA 3'
Комплементарный нуклеотидам 461-487, с заменой A→G в позиции 472.
7. GPX3 575-602 F:
5' AAGTATGTCCGGCCAGGTGGAGGCTTTG 3',
Комплементарный нуклеотидам 575-602, с заменой A→G в позиции 586
8. GPX3 666-695 F:
5' CTTTCCTGAAGAACTCCTGTCCTCCCACCT 3',
Комплементарный нуклеотидам 666-695, с заменой A→G в позиции 673.
Модифицированная таким образом нуклеотидная последовательность кДНК GPX3 SEQ ID No: 5 содержит 1 нуклеотидную замену G→C в позиции 238; две нуклеотидных замены G→T в позициях 277, 301; 1 нуклеотидную замену А→С в позиции 325; 1 нуклеотидную замену G→A в позиции 445; 3 нуклеотидных замены A→G в позиции 472, 586, 673, не приводящие к изменениям в аминокислотной последовательности белка глутатионпероксидазы-3 и имеет первичную структуру, приведенную на фиг 5.
Для получения модифицированной кДНК GPX3 SEQ ID No: 6 проводят последовательный ПЦР-мутагенез с праймерами, комплементарными участкам нативной кДНК GPX3 SEQ ID No: 1 (вариант pUC 19-GPX3 SEQ ID No: 1 с ориентацией целевого гена EcoRI-5'NTR-кДНК GPX3-3'NTRHindIII и вариант pUC 19-GPX3 SEQ ID No: 1 сориентацией целевого гена HindIII--5'NTR-кДНК GPX3-3'NTR-EcoRI), используемой в качестве матрицы:
1. GPX3 227-254 F:
5' CTGCTGCAGGCCTCCTGCCTGCTTTCCC 3',
Комплементарный нуклеотидам 227-254, с заменой G→C в позиции 238
2. GPX3 266-288 F:
5' GGCTTCGTCTCTCAGAGCCGGGG 3',
Комплементарный нуклеотидам 266-288, с заменой G→T в позиции 277.
3. GPX3 289-318 F:
5' ACAAGAGAAGTCTAAGATGGACTGCCATGG 3',
Комплементарный нуклеотидам 289-318, с заменой G→T в позиции 301
4. GPX3 319-343 F:
5' TGGCATCAGTGGCACCATTTACGAG 3',
Комплементарный нуклеотидам 319-343, с заменой А→С в позиции 325.
5. GPX3 435-460 F:
5' GAGGCCTGACAGGCCAGTACATTGAA 3',
Комплементарный нуклеотидам 435-460, с заменой G→A в позиции 445
6. GPX3 461-487 F:
CTGAATGCACTGCAGGAAGAGCTTGCA 3'
Комплементарный нуклеотидам 461-487, с заменой A→G в позиции 472.
7. GPX3 575-602 F:
5' AAGTATGTCCGGCCAGGTGGAGGCTTTG 3',
Комплементарный нуклеотидам 575-602, с заменой A→G в позиции 586
8. GPX3 666-695 F:
5' CTTTCCTGAAGAACTCCTGTCCTCCCACCT 3',
Комплементарный нуклеотидам 666-695, с заменой A→G в позиции 673.
9. GPX3 689-712 F:
5' CCCACCTCTGAGCTCCTGGGTACA 3',
Комплементарный нуклеотидам 689-712, с заменой G→T в позиции 697,
10. GPX3 781-813 F:
5' GGGGCCAGATGGTATCCCCATCATGCGCTGGCA 3',
Комплементарный нуклеотидам 781-813, с заменой А→С в позиции 796,
11. GPX3 814-842 F:
5' CCACCGGACCACCGTCAGCAACGTCAAGA 3',
Комплементарный нуклеотидам 814-842, с заменой G→C в позиции 826.
Модифицированная таким образом нуклеотидная последовательность кДНК GPX3 SEQ ID No:6 содержит 2 нуклеотидных замены G→C в позициях 238, 826; три нуклеотидных замены G→T в позициях 277, 301, 697; 2 нуклеотидных замены А→С в позиции 325, 796; 1 нуклеотидную замену G→A в позиции 445; 3 нуклеотидных замены A→G в позиции 472, 586, 673, не приводящие к изменениям в аминокислотной последовательности белка глутатионпероксидазы-3 и имеет первичную структуру, приведенную на фиг 6.
Для получения модифицированной кДНК GPX3 SEQ ID No: 7 проводят последовательный ПЦР-мутагенез с праймерами, комплементарными участкам нативной кДНК GPX3 SEQ ID No: 1 (вариант pUC 19-GPX3 SEQ ID No: 1 с ориентацией целевого гена EcoRI-5'NTR-кДНК GPX3-3'NTRHindIII и вариант pUC 19-GPX3 SEQ ID No: 1 сориентацией целевого гена HindIII--5'NTR-кДНК GPX3-3'NTR-EcoRI), используемой в качестве матрицы:
1. GPX3 227-254 F:
5' CTGCTGCAGGCCTCCTGCCTGCTTTCCC 3',
Комплементарный нуклеотидам 227-254, с заменой G→C в позиции 238
2. GPX3 266-288 F:
5' GGCTTCGTCTCTCAGAGCCGGGG 3',
Комплементарный нуклеотидам 266-288, с заменой G→T в позиции 277.
3. GPX3 289-318 F:
5' ACAAGAGAAGTCTAAGATGGACTGCCATGG 3',
Комплементарный нуклеотидам 289-318, с заменой G→T в позиции 301
4. GPX3 319-343 F:
5' TGGCATCAGTGGCACCATTTACGAG 3',
Комплементарный нуклеотидам 319-343, с заменой А→С в позиции 325.
5. GPX3 435-460 F:
5' GAGGCCTGACAGGCCAGTACATTGAA 3',
Комплементарный нуклеотидам 435-460, с заменой G→A в позиции 445
6. GPX3 461-487 F:
5' CTGAATGCACTGCAGGAAGAGCTTGCA 3'
Комплементарный нуклеотидам 461-487, с заменой A→G в позиции 472.
7. GPX3 575-602 F:
5' AAGTATGTCCGGCCAGGTGGAGGCTTTG 3',
Комплементарный нуклеотидам 575-602, с заменой A→G в позиции 586
8. GPX3 666-695 F:
5' CTTTCCTGAAGAACTCCTGTCCTCCCACCT 3',
Комплементарный нуклеотидам 666-695, с заменой A→G в позиции 673.
9. GPX3 689-712 F:
5' CCCACCTCTGAGCTCCTGGGTACA 3',
Комплементарный нуклеотидам 689-712, с заменой G→T в позиции 697,
10. GPX3 781-813 F:
5' GGGGCCAGATGGTATCCCCATCATGCGCTGGCA 3',
Комплементарный нуклеотидам 781-813, с заменой А→С в позиции 796,
11. GPX3 814-842 F:
5' CCACCGGACCACCGTCAGCAACGTCAAGA 3',
Комплементарный нуклеотидам 814-842, с заменой G→C в позиции 826.
12. а также для удаления 5'-нетранслируемой области гена GPX3 из последовательности с внесенными заменами с помощью ПЦР мутагенеза с праймером:
5' GACTCTAGAGGATCCCCGCCACCATGGCCCGGCTGCTGCAGG 3'
для варианта с ориентацией целевого гена HindIII--5'NTR-кДНК GPX3-3'NTR-EcoRI
13. а также для удаления 3'-нетранслируемой области гена GPX3 из последовательности с внесенными заменами с помощью ПЦР мутагенеза с праймером:
5' GGGGGTCAAGAGGAAGTAAGGGTACCGAGCTCGAATTCACTGG 3'
для варианта с ориентацией целевого гена HindIII--5'NTR-кДНК GPX3-3'NTR-EcoRI
14. а также для удаления 5'-нетранслируемой области гена GPX3 из последовательности с внесенными заменами с помощью ПЦР мутагенеза с праймером:
5' GAATTCGAGCTCGGTACCCGCCACCATGGCCCGGCTGCTGCAGG 3'
для варианта с ориентацией целевого гена EcoRI-5'NTR-кДНК GPX3-3'NTRHindIII
15. а также для удаления 3'-нетранслируемой области гена GPX3 из последовательности с внесенными заменами с помощью ПЦР мутагенеза с праймером:
5' GGGGGTCAAGAGGAAGTAAGGGGATCCTCTAGAGCGACCTG 3'
для варианта с ориентацией целевого гена EcoRI-5'NTR-кДНК GPX3-3'NTRHindIII
Модифицированная таким образом нуклеотидная последовательность кДНК GPX3 SEQ ID No: 7, не содержит нетранслируемые 5' и 3' области гена и содержит 2 нуклеотидных замены G→C в позициях 238, 826; три нуклеотидных замены G→T в позициях 277, 301, 697; 2 нуклеотидных замены А→С в позиции 325, 796; 1 нуклеотидную замену G→A в позиции 445; 3 нуклеотидных замены A→G в позиции 472, 586, 673, не приводящие к изменениям в аминокислотной последовательности белка глутатионпероксидазы-3 и имеет первичную структуру, приведенную на фиг 7.
Таким образом, получают линейку из 7 векторов на базе плазмиды pUC19, в которой клонированы кодирующие нативная и модифицированные нуклеотидные последовательности гена GPX3, (при этом каждый вектор из линейки получен в двух вариантах и содержит целевой ген с ориентацией EcoRI-5'NTR-кДНК GPX3-3'NTRHindIII и целевой ген с ориентацией HindIII--5'NTR-кДНК GPX3-3'NTR-EcoRI для создания генетических экспрессионных конструкций на базе разных векторов) для создания линейки биологически активных генно-терапевтических субстанций.
Пример 3
Создание генетических конструкций с модифицированными и нативной кДНК гена GPX3 для получения на их базе биологически активных генно-терапевтических субстанций.
Для экспрессии кДНК гена GPX3 в клетках органов и тканей человека полученные варианты кДНК GPX3 по Примеру 1 и Примеру 2 помещают в векторную плазмиду, при выборе которой используют следующие критерии выбора:
1) плазмида должна обязательно реплицироваться в E. coli, желательно с высокой копийностью;
2) в плазмиде должен быть бактериальный фактор селекции;
3) в векторе должно быть наличие эукариотических регуляторных элементов - обязательных промотора и терминатора (сигнала полиаденилирования), например, энхансер и интронный(е) элемент(ы);
4) наличие удобного полилинкера для клонирования. Примером такой плазмиды может быть pCMV6-XL5, pCMV6-Kan/Neo (OriGene, USA) или pCDNA 3.1(+) (ThermoFisherScientific, USA).
При клонировании кДНК гена GPX3 в pCDNA 3.1(+) кодирующая нуклеотидная последовательность помещается под контроль промотора цитомегаловируса человека CMV, эффективного в эукариотических клетках, и сигнала полиаденилирования гена бычьего гормона роста. Также данная плазмида обладает бактериальным фактором селекции - геном устойчивости к ампициллину, и эукариотическим фактором селекции - геном устойчивости к неомицину. При клонировании учитывают последовательность расположения сайтов HindIII и EcoRI в полилинкере pCDNA 3.1(+) и поэтому для клонирования в данный вектор используют HindIII-5'NTR-кДНК GPX3-3'NTR-EcoRI ориентированный фрагмент в pUC19 по примеру 1.
При клонировании кДНК гена GPX3 в pCMV6-XL5, pCMV6-Kan/Neo кодирующая нуклеотидная последовательность помещается под контроль промотора цитомегаловируса человека CMV, эффективного в эукариотических клетках, и сигнала полиаденилирования гена гормона роста человека. Также данная плазмида обладает бактериальным фактором селекции - геном устойчивости к ампициллину. При клонировании учитывают последовательность расположения сайтов EcoRI и HindIII в полилинкере pCMV6-XL5 (pCMV6-Kan/Neo) и поэтому для клонирования в данный вектор используют EcoRI-5'NTR-кДНК GPX3-3'NTR-HindIII ориентированный фрагмент в pUC19 по примеру 1.
Векторные плазмиды pUC19-GPX3 SEQ ID No: 1 с частичной нативной (немодифицированной) последовательностью гена GPX3 (с 143 по 1022 н.п.), pUC19-GPX3 SEQ ID No: 2, pUC19-GPX3 SEQ ID No: 3, pUC19-GPX3 SEQ ID No: 4, pUC19-GPX3 SEQ ID No: 5, pUC19-GPX3 SEQ ID No: 6, с частичной модифицированной путем замены оснований нуклеотидной последовательностью гена GPX3 (с 143 по 1022 н.п.) и pUC19-GPX3 SEQ ID No: 7 с модифицированной кДНК гена GPX3 и лишенной нетранслируемыех 5' и 3' областей данного гена, а также векторные плазмиды pCMV6-XL5, pCMV6-Kan/Neo и pCDNA 3.1(+) для дальнейшей экспрессии гена GPX3 в эукариотических клетках, гидролизуют рестриктазами EcoRI и HindIII (NEB, USA) при 37°С в соответствующем буфере (Маниатис Т., и др. Молекулярное клонирование. М., Мир, 1984).
Продукты рестрикции разделяют с помощью электрофореза в геле 1% агарозы, окрашивают раствором бромистого этидия и фрагменты ДНК, соответствующие гену-вставке HindIII-5'NTR-кДНК GPX3-3'NTR-EcoRI, либо EcoRI-5'NTR-кДНК GPX3-3'NTR-HindIII и линеаризованной плазмиде pCMV6-XL5 и pCMV6-Kan/Neo и pCDNA 3.1(+), вырезают, выделяют из геля с помощью набора для выделения из геля QIAquickGelExtractionKit из примера 1 и смешивают. Полученную смесь рестрикционных фрагментов лигируют с помощью ДНК-лигазы фага Т4. Лигирование проводят в течение 10-15 мин при комнатной температуре, а затем - при 12°С в течение 10 ч. Лигированную ДНК используют для трансформации клеток Е. coli по стандартной методике с использованием хлористого кальция. Трансформированные клетки отбирают на агаризованной среде LB с ампициллином (100 мкг/мл). Плазмидную ДНК из ампициллин-устойчивых колоний выделяют с помощью набора для выделения плазмид QiagenSpinMiniprepKit, анализируют с помощью гидролиза рестриктазами TEcoRI и HindIII и отбирают генетическую(ие) конструкцию(ии), содержащую
(ие) в своем составе кодирующую последовательность гена GPX3 под контролем промотора цитомегаловируса CMV, и сигналом полиаденилирования гена гормона роста, обозначаемую как pCMV6 GPX3 SEQ ID No: (1-7) или pCMV6-Kan/Neo GPX3 SEQ ID No: (1-7) или pCDNA 3.1GPX3 SEQ ID No: (1-7). Наличие вставки кДНК гена GPX3, ее последовательность и ориентацию также подтверждают с помощью секвенирования ДНК генетических конструкций по методу Сэнгера.
Бактерии, содержащие полученные генетические конструкции на базе векторов pCMV6-XL5, pCMV6-Kan/Neo и pCDNA 3.1(+), выращивают на жидкой среде LB с ампициллином, лизируют и выделяют плазмидную ДНК для трансфекции специальным набором для выделения плазмид QiagenMaxiKit для получения соответствующих биологически активных генно-терапевтических субстанций.
Полученные генетические экспрессионные конструкции используют для получения на их базе биологически активных генно-терапевтических субстанций, которые в дальнейшем применяют для трансфекции эукариотических клеток органов и тканей и/или введения в органы и ткани человека. В качестве контрольных плазмид используют исходный вектор pCMV6-XL5, (pCMV6-Kan/Neo) или pCDNA 3.1(+) без вставки кДНК гена GPX3.
Пример 4
Наращивание генетической конструкции в бактериальной культуре.
Для получения препаративных количеств векторной плазмиды, содержащей один из вариантов кДНК гена GPX3, полученными конструкциями по примеру 3 трансформируют бактериальные клетки E.coli (Маниатис Т., и др. Молекулярное клонирование. М., Мир, 1984) и выращивают полученные клоны бактерий, содержащие конструкцию, в присутствии бактериального фактора селекции - устойчивости к ампициллину.
Лигазную смесь по примеру 3 используют для трансформации компетентных клеток E.coli штамма XLblue. Предварительный отбор клонов, содержащих вставку кДНК гена GPX3 в правильной ориентации и единичной копии, осуществляют путем гидролиза плазмидной ДНК рестриктазами EcoRI и HindIII и анализа продуктов рестрикции путем электрофореза в 1.2% агарозном геле. Отобранные клоны используют для препаративного наращивания плазмидной ДНК с целью дальнейшей трансфекции в культуры фибробластов (хондробластов, кератоцитов и др.).
Для получения препаративных количеств генетических экспрессионных конструкций по Примеру 3 выращивали 20 мл ночной культуры E.coli в LB-среде с 150 мкг/мл ампициллина. Этой культурой инокулировали 500 мл LB-среды с 100 мкг/мл ампициллина, рост осуществляли в шейкере-инкубаторе в течение 16 часов при 37°С и 200 об/мин. Выделение плазмидной ДНК проводили с помощью набора EndoFreePlasmidMaxiKit (Qiagen, Germany). Выход составил 350 мкг ДНК.
Пример 5
Культивирование эукариотических клеток, например, фибробластов для последующих трансфекции биологически активной генно-терапевтической субстанцией и анализа экспрессии гена GPX3.
Для последующей трансфекции биологически активной генно-терапевтической субстанцией содержащей один из вариантов кДНК GPX3 по примеру 3, выращивают первичные культуры фибробластов человека из биоптатов кожи пациентов.
Используя устройство для взятия биопсии кожи Epitheasy 3.5 (MedaxSRL) берут образец биоптата кожи из зоны, защищенной от действия ультрафиолета, например за ушной раковиной или с боковой внутренней поверхности в зоне локтевого сустава, размером около 3 мм, массой - до 20 мг. Кожу пациента предварительно промывали стерильным физиологическим раствором и анестезировали раствором лидокаина. Выращивание первичной культуры клеток осуществляют на чашках Петри при 37°С в атмосфере, содержащей 5% CO2 в среде DMEM с 10% фетальной телячьей сывороткой и ампициллином 100 Ед/мл. Трипсинизацию и пересев производят каждые 5 дней, для трипсинизации клетки промывали раствором PBS и инкубировали 30 минут при 37°С в растворе, содержащем 0.05% трипсина и 1 мМ ЭДТА. Для нейтрализации трипсина к клеткам добавляли 5 мл культуральной среды и центрифугировали суспензию при 600 об/мин 5 минут. Рост культуры фибробластов после 4-5 пассажей осуществляли в культуральных флаконах емкостью 75 мл в среде, содержащей 10 г/л DMEM, 3.7 г/л Na2CO3, 2.4 г/л HEPES, 10% фетальной сыворотки и 100 Ед/мл ампициллина. Смену культуральной среды осуществляли каждые 2 дня. Общая продолжительность роста культуры не превышала 25-30 дней. Из культуры клеток отбирали аликвоту, содержащую 106 клеток.
Часть культуры фибробластов, предназначенную для выделения РНК с последующим анализом транскрипции гена GPX3, центрифугировали при 1000 об/мин 20 минут и дважды отмывали в буферном растворе PBS центрифугированием при 600 об/мин в течение 5 минут. Затем клетки ресуспендировали в 1.5 мл стабилизирующего реагента RNAlater и хранили при 4°С в течение 10 дней для последующего выделения РНК.
Выделение РНК проводили с помощью набора RNeasyMiniKit. (Qiagen, Germany). Выделенную РНК анализировали спектрофотометрически, измеряя соотношение оптической плотности при 260 и 280 нм, а также с помощью капиллярного электрофореза на приборе QIAxcel (Qiagen, Germany), используя картридж RNA Qiality Control. Для дальнейшей работы использовали только те образцы, для которых общее количество выделенной РНК было не менее 50 мкг РНК, соотношение D260 : D280 - не менее 1,8, а соотношение полос 28S: 18S на капиллярном электрофорезе - не ниже 1:1.
Синтез суммарной кДНК первой цепи проводили, используя обратную транскриптазу RevertAid (Thermo Scientific, USA), согласно рекомендациям изготовителя. 1-2 мкг суммарной РНК использовали в качестве матрицы для синтеза первой цепи кДНК. В реакционную смесь для проведения обратной транскрипции вносили 100-200 ед. обратной транскриптазы и 10 пМ случайного 9-нуклеотидного праймера.
Пример 6
Анализ эндогенной экспрессии гена GPX3 в культуре первичных фибробластов.
Анализ транскрипции гена GPX3 из генома фибробластов проводят с целью последующего корректного определения генно-терапевтического эффекта после трансфекции этих клеток генетическими конструкциями с кДНК гена GPX3.
Для анализа используют клеточные линии фибробластов кожи, фибробласты с низкой экспрессией гена GPX3 и фибробласты с нормальной экспрессией гена GPX3, из которых выделяют РНК по стандартной методике (Маниатис Т. и др. Молекулярное клонирование. М., Мир, 1984).
Выделенную. РНК анализируют методом ПЦР в режиме реального времени (SYBR GreenRealTimePCR). Для амплификации кДНК, специфичной для гена GPX3, используют прямой праймер:
GPX3FA1 5' TTACGAGTACGGAGCCCTCACC 3'
и обратный праймер:
GPX3-RA1 5' GAAAGCCCAGAATGACCAGACC 3'
Длина продукта амплификации - 179 нуклеотидов. В качестве референтного гена используют ген бета-2-микроглобулина В2М, уровень экспрессии которого в фибробластах сопоставим с таковым в норме для гена GPX3.
ПЦР-амплификацию проводят с помощью набора реагентов SYBR GreenQuantitect RT-PCR Kit (Qiagen, USA) или другого набора для ПЦР в режиме реального времени в 20 мкл амплификационной смеси, содержащей: 25 мкл QuantiTect SYBR Green RT-PCR MasterMix, 2,5 mM хлорида магния, по 0,5 мкМ каждого прймера, 5 мкл суммарной РНК. Реакцию осуществляют на амплификаторе CFX96 (Bio-Rad, USA) при следующих условиях: 1 цикл обратной транскрипции при 50°С 30 минут, денатурация 98°С - 15 мин, затем 40 циклов, включающих денатурацию 94°С - 15 сек, отжиг праймеров 55,8°С - 30 сек и элонгацию 72°С - 30 сек.
В качестве положительного контроля используют концентрацию ампликонов, получаемых при ПЦР на матрицах, представляющих собой плазмиды в известных концентрациях, содержащие последовательности кДНК генов GPX3 и В2М. Количество ПЦР продуктов - кДНК генов GPX3 и В2М, полученных в результате амплификации, оценивают в режиме реального времени с помощью программного обеспечения амплификатора Bio-RadCFXManager 2.1.ММ. В качестве отрицательного контроля используют деионизированную воду (кривые накопления ПЦР продуктов отрицательного и положительных контролей для упрощения визуализации на фигуре 8 не показаны).
По итогам анализа экспрессии гена GPX3 в разных культурах фибробластов (с низкой экспрессией гена GPX3 и с нормальной экспрессией гена GPX3) были отобраны клоны от пациентов одного возраста и одного типа старения, в которых количество ПЦР-продукта, соответствующего кДНК гена GPX3, была в 10-20 раз ниже таковой кДНК гена В2М. Кривые накопления специфических ПЦР-продуктов приведены на фигуре 8.
Пример 7
Трансфекция клеточной культуры фибробластов со сниженной экспрессией гена GPX3 биологически активной генно-терапевтической субстанцией с целью подтверждения увеличения экспрессии гена GPX3 в культуре данных клеток.
Для оценки эффективности биологически активной генно-терапевтической субстанции, содержащей немодифицированную кДНК гена GPX3 по примеру 3, этой биологически активной генно-терапевтической субстанцией трансфицируют первичную культуру фибробластов человека со сниженной экспрессией гена GPX3, отобранную по примеру 6.
Данную культуру фибробластов выращивают в культуральных флаконах (25 см2) до момента, когда клетки покрывают 50-70% поверхности флакона. Полученные клетки трансфицируют биологически активной генно-терапевтической субстанцией на основе pCMV6-GPX3 SEQ ID No: 1 в присутствии транспортной молекулы (например, дендримера) и вектором pCMV6-XL5 в качестве контроля.
6-луночный планшет с DMEM-средой с 10% фетальной телячьей сывороткой (1.6 мл в лунке) засевали фибробластами из расчета 1-4×105 клеток на лунку. Инкубировали клетки в течение 18 часов при 37°С и в атмосфере, содержащей 5% CO2. Затем 2 мкг плазмидной ДНК растворяли в среде DMEM без сыворотки с буфером Трис-HCl 20 мМ с 1 мМ ЭДТА, pH 7-8 (минимальная концентрация ДНК - 0.1 мкг/мкл). Конечный объем смеси составлял 100 мкл.
В качестве транспортной молекулы использовали раствор дендримера SuperFect Transfection Reagent 6-го поколения (Qiagen, Германия).
Приготовление комплекса ДНК-дендример проводили по методике производителя (QIAGEN, SuperFect Transfection Reagent Handbook, 2002) с некоторыми изменениями: к 15 мкл раствора дендримера (с концентрацией 3 мкг/мкл) добавляли 5 мкл (с концентрацией 0,5 мкг/мкл) раствора плазмидной ДНК и тщательно перемешивали. Затем инкубировали смесь ДНК с дендримером в течение 5-10 минут при температуре 15-25°С.
Из лунок планшета с клеточной культурой осторожно отбирали среду (не нарушая клеточного слоя) и промывали клетки 3 мл буфера PBS. К раствору, содержащему комплексы ДНК-дендример, добавляли 600 мкл среды DMEM с фетальной сывороткой и переносили эту смесь в лунки планшета с клетками. Клетки инкубировали с комплексами 2-3 часа при 37°С и в атмосфере, содержащей 5% CO2. Затем осторожно удаляли среду и промывали клеточный слой 3 мл буфера PBS. Затем добавляли культуральную среду и инкубировали 24-48 часов при 37°С и в атмосфере, содержащей 5% CO2, после чего оценивали уровень кДНК гена GPX3 и контрольной кДНК гена В2М с помощью амплификации в режиме реального времени как описано в примере 6. Результаты анализа приведены на фигуре 9.
Из графиков следует, что в случае трансфекции вектором без вставки кДНК гена GPX3 уровень кДНК гена GPX3 в фибробластах не изменился, а в случае трансфекции вектором с кДНК GPX3 - уровень кДНК фибробластов со сниженной экспрессией гена GPX3 многократно увеличился (до уровня выше уровня кДНК гена GPX3 в нормальных фибробластах).
Показано, что в клетках трансфицированных биологически активной генно-терапевтической субстанцией на основе pCMV6-GPX3 SEQ ID No: 1 наблюдается усиление экспрессии целевого гена GPX3.
Пример 8
Трансфекция клеточной культуры фибробластов с нормальной экспрессией гена GPX3 биологически активной генно-терапевтической субстанцией с кДНК гена GPX3 с целью подтверждения увеличения при этом активности белка глутатионпероксидазы-3 в культуре данных клеток.
Для оценки изменения уровня активности белка глутатионпероксидазы-3 в культуре фибробластов, использовали три варианта клеточной культуры - нетрансфицированные фибробласты, обработанные водным раствором дендримеров (А), трансфицированные векторной плазмидой, например, pCDNA 3.1(+), не содержащей кДНК гена GPX3 (В) и трансфицированные биологически активной генно-терапевтической субстанцией на основе той же самой векторной плазмиды, содержащей кДНК гена GPX3 - pCDNA 3.1 GPX3 SEQ ID No: 1(C). Трансфекцию клеток биологически активной генно-терапевтической субстанцией на основе pCDNA 3.1 GPX3 SEQ ID No: 1 и вектором pCDNA 3.1(+) в присутствии транспортных молекул (дендримеров) проводят как описано в примере 7.
Клеточный осадок, соответствующий 2×106 клеток промывали фосфатным буфером и ресуспендировали во льду в лизирующем буфере, содержащем 25 мМ ХЕПЕС pH 7.9, 100 мМ NaCl, 1 мМ ЭДТА, 1% Тритон Х-100, 10% глицерин и 1 мМ фенилметилсульфонилфторид. Лизат центрифугировали 5 минут при 14000 об/мин.
Активность белка глутатионпероксидазы-3 определяли непрямым колориметрическим методом с помощью набора Glutathione Peroxidase Cellular Activity Assay Kit, Catalog Number CGP1 (Sigma-Aldrich, USA). Принцип метода состоит в том, что глутатионпероксидаза воздействует на ферментативные реакции, в результате чего снижается концентрация NADPH (восстановленного никотинамидадениндинуклеотидфосфата), что в конечном итоге приводит к уменьшению оптической плотности раствора, которая измеряется при длине волны 340 нм. Анализ проводили по методике (Technocal Bulletin 2012), рекомендуемой производителем. Из графика, приведенного на фигуре 10, следует, что лизат культуры клеток, трансфицированных биологически активной генно-терапевтической субстанцией на основе pCDNA 3.1GPX3 SEQ ID No: 1, ингибирует цветную реакцию полностью без разведения и при разведении 1:10.
Таким образом показано, что транфекция фибробластов полученной биологически активной генно-терапевтической субстанцией, несущей кДНК гена GPX3, приводит к повышению активности глутатионпероксидазы-3 в клетках фибробластов.
Пример 9
Введение в кожу человека клеточной культуры фибробластов, трансфицированной биологически активной генно-терапевтической субстанцией с кДНК гена GPX3 с целью подтверждения увеличения после этого активности белка глутатионпероксидазы-3 в биоптате кожи человека.
С целью анализа изменения активности белка глутатионпероксидазы-3 в тканях человека пациентам в кожу предплечья вводили три варианта культуры аутологичных фибробластов - нетрансфицированных (А), трансфицированных вектором без вставки, например, pCMV6-XL5 (В) и трансфицированных биологически активной генно-терапевтической субстанцией на основе pCMV6-GPX3 SEQ ID No: 7(C) в комбинации с транспортными молекулами - липосомами TRANSFAST ТМ Transfection Reagent (PROMEGA, USA).
Приготовление суспензии липосом проводили по методике производителя (Promega, TransFast Transfection Reagent, Instruction for Use of Product, E2431) с некоторыми изменениями: к 0,4 мг порошка липосом добавляли 0,4 мл стерильной воды степени очистки Nuclease-Free. Суспензию хорошо перемешивали взбалтыванием. Полученный полупродукт суспензии липосом выдерживали в течение 18 часов при температуре - 20°С, затем оттаивали при комнатной температуре, ресуспендировали встряхиванием или на настольном миксере типа «ВОРТЕКС».
Для приготовления комплекса ДНК-липосомы к 400 мкл раствора липосом (с концентрацией 1 мг/мл) добавляли 400 мкл раствора плазмидной ДНК (с концентрацией 150 мкг/мл) и тщательно перемешивали. Затем инкубировали смесь ДНК с липосомами в течение 5-10 минут при температуре 15-25°С и использовали далее в качестве биологически активной генно-терапевтической субстанции.
Для последующей трансфекции биологически активной генно-терапевтической субстанцией выращивают первичные культуры фибробластов человека из биоптатов кожи пациентов по примеру 5.
Для трансфекции из лунок планшета с клеточной культурой осторожно отбирали среду (не нарушая клеточного слоя) и промывали клетки 3 мл буфера PBS. К раствору, содержащему комплексы ДНК-липосомы, добавляли 600 мкл среды DMEM с фетальной сывороткой и переносили эту смесь в лунки планшета с клетками. Клетки инкубировали с комплексами 2-3 часа при 37°С и в атмосфере, содержащей 5% CO2. Затем осторожно удаляли среду и промывали клеточный слой 3 мл буфера PBS. Затем добавляли культуральную среду и инкубировали 24-48 часов при 37°С в атмосфере, содержащей 5% CO2.
Часть клеточной культуры центрифугировали при 700 об/мин, дважды отмывали клетки физиологическим раствором, ресуспендировали в физиологическом растворе из расчета 1 млн клеток в 200 мкл и использовали для введения пациенту. Введение осуществляли тоннельным методом иглой 30G на глубину 3 мм. Очаги введения культур фибробластов располагались на расстоянии 3-5 см друг от друга. Активность глутатионпероксидазы-3 оценивали в лизатах биоптатов кожи пациента непрямым колориметрическим методом с помощью набора Glutathione Peroxidase Cellular Activity Assay Kit (Sigma-Aldrich, USA).) как описано в примере 8. Биопсийные образцы брали на 3 сутки после введения суспензии фибробластов. Взятие биопсии осуществляли из участков введения суспензии фибробластов, а также из интактной кожи, используя устройство для взятия биопсии кожи Epitheasy 3.5 (MedaxSRL). Кожу пациента предварительно промывали стерильным физиологическим раствором и анестезировали раствором лидокаина. Размер биопсийного образца был около 3 мм, масса - до 20 мг. Образец помещали в буферный раствор, содержащий 50 мМ Трис-HCl pH 7.6, 100 мМ NaCl, 1 мМ ЭДТА и 1 мМ фенилметилсульфонилфторид, и гомогенизировали до получения однородной суспензии. Полученную суспензию центрифугировали в течение 10 минут при 14000 об/мин.
Как видно из фигуры 11, в коже пациента в области введения фибробластов, трансфицированных биологически активной генно-терапевтической субстанцией на основе pCMV6-GPX3 SEQ ID No: 7, произошло увеличение активности белка глутатионпероксидазы-3, тогда как при введении контрольных культур фибробластов (трансфицированных и нетрансфицированных вектором без вставки кДНК гена GPX3 pCMV6-XL5) активность белка глутатионпероксидазы-3 в коже не изменялась.
Таким образом показана эффективность биологически активной генно-терапевтической субстанции, несущей модифицированную кДНК гена GPX3: трансфекция фибробластов полученной биологически активной генно-терапевтической субстанцией несущей модифицированную кДНК гена GPX3, приводит к повышению активности белка глутатионпероксидазы-3 в клетках фибробластов.
Пример 10.
Трансфекция культур фибробластов из биоптатов группы различных пациентов биологически активными генно-терапевтическими субстанциями, содержащими модифицированные и нативную кДНК GPX3.
С целью подтверждения индивидуального характера увеличения активности белка глутатионпероксидазы-3 до различного уровня при трансфекции клеточных культур фибробластов пациентов биологически активными генно-терапевтическими субстанциями с модифицированными и нативной кДНК гена GPX3 анализировали уровень активности белка глутатионпероксидазы-3 в клеточных лизатах фибробластов, трансфицированных разными биологически активными генно-терапевтическими субстанциями по примеру 3, содержащими модифицированные и нативную кДНК GPX3 в группе пациентов в зависимости от наличия и типа модификаций в кДНК гена GPX3.
Последовательность нативной кДНК GPX3 приведена на фигуре 1, SEQ ID No: 1., последовательности модифицированных кДНК GPX3 приведены на фигурах 2-7 (SEQ ID No: 2, SEQ ID No: 3, SEQ ID No: 4, SEQ ID No: 5, SEQ ID No: 6, SEQ ID No: 7).
Вырастили культуры фибробластов из однотипных биоптатов кожи, отобранных из зоны внутренней боковой поверхности в области локтевого сустава 23 пациентов, выбранных случайным образом по примеру 5, отобрали аликвоты и оценили уровень глутатионпероксидазы-3 в клеточных лизатах. Клеточный осадок, соответствующий 2×106 клеток, промывали фосфатным буфером и ресуспендировали во льду в лизирующем буфере, содержащем 25 мМ ХЕПЕС pH 7.9, 100 мМ NaCl, 1 мМ ЭДТА, 1% Тритон Х-100, 10% глицерин и 1 мМ фенилметилсульфонилфторид. Лизат центрифугировали 5 минут при 14000 об/мин, концентрацию белка в супернатанте определяли методом Брэдфорда ([Bradford М.М. (1976) Anal. Biochem. 72: 248-254.]).
Затем каждую из 23-ти культур фибробластов разделили на 8 частей. Одну часть, обозначенную (А), трансфицировали по примеру 7 биологически активной генно-терапевтической субстанцией на базе вектора pCMV6- SEQ ID No: 1, содержащей немодифицированную кДНК GPX3 (SEQ ID No: 1.) по примеру 3 в сочетании с транспортными молекулами - липосомами по примеру 9. Вторую часть, обозначенную (В), трансфицировали по примеру 7 биологически активной генно-терапевтической субстанцией на базе вектора pCMV6- SEQ ID No: 2, содержащей вариант 1 модифицированной кДНК GPX3 (SEQ ID No: 2.) по примеру 3 в сочетании с транспортными молекулами - липосомами по примеру 9. 3-ю часть, обозначенную (С), трансфицировали по примеру 7 биологически активной генно-терапевтической субстанцией на базе вектора pCMV6- SEQ ID No: 3, содержащей вариант 2 модифицированной кДНК GPX3 (SEQ ID No:3.) по примеру 3 в сочетании с транспортными молекулами - липосомами по примеру 9. 4-ю часть, обозначенную (D), трансфицировали по примеру 7 биологически активной генно-терапевтической субстанцией на базе вектора pCMV6- SEQ ID No: 4, содержащей вариант 3 модифицированной кДНК GPX3 (SEQ ID No: 4.) по примеру 3 в сочетании с транспортными молекулами - липосомами по примеру 9. 5-ю часть, обозначенную (Е), трансфицировали по примеру 7 биологически активной генно-терапевтической субстанцией на базе вектора pCMV6- SEQ ID No: 5, содержащей 4 вариант модифицированной кДНК GPX3 (SEQ ID No: 5.) по примеру 3 в сочетании с транспортными молекулами - липосомами по примеру 9. 6-ю часть, обозначенную (F), трансфицировали по примеру 7 биологически активной генно-терапевтической субстанцией на базе вектора pCMV6- SEQ ID No: 6, содержащей вариант 5 модифицированной кДНК GPX3 SEQ ID No: 6) по примеру 3 в сочетании с транспортными молекулами - липосомами по примеру 9. 7-ю часть, обозначенную (G), трансфицировали по примеру 7 биологически активной генно-терапевтической субстанцией на базе вектора pCMV6- SEQ ID No: 7, содержащей вариант 6 модифицированной кДНК GPX3 (SEQ ID No: 7) по примеру 3 в сочетании с транспортными молекулами - липосомами по примеру 9. 8-ю часть, обозначенную (Н), трансфицировали по примеру 7 векторной плазмидой pCMV6-XL5, не содержащей кДНК GPX3 по примеру 3 в сочетании с транспортными молекулами - липосомами по примеру 9.
Активность глутатионпероксидазы-3 определяли через 72 часа после трансфекции непрямым колориметрическим методом с помощью набора Glutathione Peroxidase Cellular Activity Assay Kit (Sigma-Aldrich, USA). Анализ проводили по методике, рекомендуемой производителем. Предварительно проводили оценку степени ингибирования цветной реакции в зависимости от концентрации чистого препарата глутатионпероксидазы-3. Исходя из данных предыдущих экспериментов, описанных в примере 8, лизат разводили в 5 раз.
По итогам анализа уровня активности глутатионпероксидазы-3 выбрали показатели, касательно каждой части клеточной культуры от каждого пациента, продемонстрировавшие максимальные уровни активности глутатионпероксидазы-3 и объединили их в семь групп, исходя из следующего критерия:
В группе 1 максимальное ингибирование в лизате, что соответствует максимальной активности глутатионпероксидазы-3, наблюдалось при трансфекции немодифицированной кДНК GPX3. В эту группу вошло 4 культуры из 23.
В группе 2 максимальное ингибирование в лизате, что соответствует максимальной активности глутатионпероксидазы-3, наблюдалось при трансфекции 1 вариантом модифицированной кДНК GPX3. В эту группу вошла 1 культура из 23
В группе 3 максимальное ингибирование в лизате, что соответствует максимальной активности глутатионпероксидазы-3, наблюдалось при трансфекции 2 вариантом модифицированной кДНК GPX3. В эту группу вошло 3 культуры из 23.
В группе 4 максимальное ингибирование в лизате, что соответствует максимальной активности глутатионпероксидазы-3 наблюдалось при трансфекции 3 вариантом модифицированной кДНК GPX3. В эту группу вошло 2 культуры из 23.
В группе 5 максимальное ингибирование в лизате, что соответствует максимальной активности глутатионпероксидазы-3, наблюдалось при трансфекции 4 вариантом модифицированной кДНК GPX3. В эту группу вошло 6 культур из 23.
В группе 6 максимальное ингибирование в лизате, что соответствует максимальной активности глутатионпероксидазы-3, наблюдалось при трансфекции 5 вариантом модифицированной кДНК GPX3. В эту группу вошли 4 культуры из 23.
В группе 7 максимальное ингибирование в лизате, что соответствует максимальной активности глутатионпероксидазы-3, наблюдалось при трансфекции 6 вариантом модифицированной кДНК GPX3. В эту группу вошло 3 культуры из 23.
Ни в одной из клеточных культур не наблюдалось того, что максимальное ингибирование в лизате, соответствующее максимальной активности глутатионпероксидазы-3, присутствует при трансфекции вектором, не содержащим кДНК гена GPX3.
На фигуре 12 для каждой группы клеточных культур приведены диаграммы показателей ингибирования цветной реакции (усредненных в рамках группы, в случае, если в группу входит более одной клеточной культуры) применительно ко всем, участвующим в эксперименте активным генно-терапевтическим субстанциям, после трансфекции этих клеточных культур активными генно-терапевтическими субстанциями, содержащими модифицированные и нативную кДНК гена GPX3.
Из данного примера следует, что достижение максимальной активности глутатионпероксидазы-3 в культурах фибробластов кожи различных пациентов при их трансфекции биологически активными генно-терапевтическими субстанциями, связано с индивидуальными особенностями пациентов и зависит от наличия и типа модификаций в кДНК гена GPX3, входящих в биологически активные генно-терапевтические субстанции.
Каждая биологически активная генно-терапевтическая субстанция из линейки биологически активных генно-терапевтических субстанций является эффективной в некоторой значительной группе пациентов. Следовательно, для выбора наиболее эффективной биологически активной генно-терапевтической субстанции из линейки биологически активных генно-терапевтических субстанций для терапевтических целей необходимо предварительное персонализированное исследование биоптатов пациента, либо клеток, выращенных из этих биоптатов на предмет максимальной эффективности терапевтического воздействия, созданных биологически активных генно-терапевтических субстанций в рамках линейки биологически активных генно-терапевтических субстанций.
Пример 11
Трансфекции клеточной культуры кератоцитов и эпителиальных клеток глаза биологически активной генно-терапевтической субстанцией без транспортной молекулы с целью подтверждения при этом увеличения экспрессии гена GPX3 в данных культурах клеток.
С целью выяснения эффективности биологически активной генно-терапевтической субстанции, содержащей кДНК GPX3, в различных типах клеток, трансфицировали кератоциты и эпителиальные клетки роговицы человека, без использования транспортных молекул.
Биопсийный материал из области лимба в виде круга диаметром 1-1.5 мм помещали в чашку Петри в сбалансированный солевой раствор Хэнкса, добавляли диспазу (20 мкл 25 ед/мл) и гентамицин и инкубировали 24 часа при +4. Затем отделяли эпителиальный слой от стромы и нарезали обе ткани кусочками 1-2 мм3.
Суспензию эпителиальных клеток получали путем инкубирования кусочков тканей в растворе Трипсин-ЭДТА в течение 15 минут при +37°С. Трипсинизацию останавливали добавлением соевого ингибитора трипсина в PBS. Клеточные суспензии отмывали центрифугированием при 700 об/мин и ресуспендировали в бессывороточной среде DMEM с гентамицином. Клетки растили в 25 см2 флаконах с 5 мл среды при 37°С и в атмосфере, содержащей 5% CO2. Через 24 часа среду с не прикрепившимися клетками удаляли и добавляли 5 мл свежей среды. Пересев производили каждые 7 дней в соотношении 1:2-1:3.
Суспензию кератоцитов получали путем инкубирования в среде RPMI-1640 с коллагеназой 300 ед/мл в течение 2 часов. Затем отмывали клетки и ресуспендировали в среде DMEM с 20% телячьей сывороткой и антибиотиком-антимикотиком. Клетки растили в 25 см2 флаконах с 1 мл среды при +37°С и в атмосфере, содержащей 5% CO2. Пересев производили каждые 7 дней в соотношении 1:4.
Поскольку эффективность трансфекции кератоцитов низкая, использовали биологически активную генно-терапевтическую субстанцию на основе плазмиды pCMV6-Kan/Neo GPX3 SEQ ID No: 2, содержащую дополнительный фактор селекции - ген neor, придающий устойчивость к антибиотику генетицину.
Биологически активную генно-терапевтическую субстанцию добавляли к клеткам и инкубировали клетки 1 час при 37°С. После инкубации добавляли бессывороточную среду DMEM к эпителиальным клеткам и среду DMEM, содержащую 10% фетальной телячьей сыворотки к кератоцитам и продолжали инкубировать 24 часа. После 24-часового инкубирования клетки высевали в новую среду DMEM, содержащую 400 μg/mL фактора селекции - антибиотика G418 (Geneticin). Выжившие клетки культивировали в течение 2 недель в 25 см3 флаконах с 5 мл среды с G418. Всего выращивали 24 образца культур эпителиальных клеток и 24 образца культур кератоцитов.
Каждые 24 часа из каждой культуры отбирали аликвоту по 500 мкл суспензии с целью выделения РНК и анализа уровня специфической кДНК. Выделение РНК проводили с помощью набора RNeasyMiniKit (Qiagen, Germany). Образцы РНК были сгруппированы в 3 группы по 8 образцов с близкой концентрацией и объединены. Анализ уровня специфической кДНК гена GPX3 проводили с помощью амплификации в режиме реального времени по методике и с праймерами по примеру 6, используя набор реагентов iTaqUniversalSYBRGreenSupermix (Bio-Rad, USA), амплификатор CFX96 (Bio-RadUSA) и программное обеспечение Bio-RadCFXManager 2.1. Максимальное увеличение экспрессии (транскрипции) гена GPX3 наблюдали на 3 сутки для эпителиальных клеток и на 5 сутки - для кератоцитов.
На фигуре 13 приведены кривые накопления специфического продукта амплификации, соответствующего кДНК гена GPX3, в кератоцитах и эпителиальных клетках роговицы.
Показано, что в кератоцитах и эпителиальных клетках роговицы человека, трансфицированных биологически активной генно-терапевтической субстанцией на основе pCMV6- Kan/Neo GPX3 SEQ ID No: 2, без транспортной молекулы, наблюдается усиление экспрессии целевого гена GPX3
Пример 12
Трансфекции клеточной культуры хондробластов биологически активной генно-терапевтической субстанцией с целью подтверждения при этом увеличения экспрессии гена GPX3 в данных культуре клеток.
С целью выяснения эффективности биологически активной генно-терапевтической субстанции, содержащей кДНК гена GPX3, в различных типах клеток, а также с целью оценки влияния транспортной молекулы на успешность трансфекции этой субстанцией - трансфицировали хондробласты человека, используя в качестве транспортной молекулы амфифильные блок-сополимеры.
Биоптаты хрящевой ткани массой 50-150 мг измельчали на фрагменты до 10 мм3 и инкубировали в буферном растворе с коллагеназой II, гиалуронидазой и трипсином в течение 48 часов при +37°С. Клетки отмывали бессывороточной средой DMEM, ресуспендировали в той же среде с гентамицином и выращивали при +37°С и в атмосфере, содержащей 5% CO2 во флаконах 75 см2 с 15 мл среды. Рост осуществлялся в бессыворотчной среде, так как в монослойной культуре хондроциты меняют форму и биохимические свойства. Пересев производили каждые 4 дня в соотношении 1:3, клетки снимали с поверхности флакона раствором трипсин-ЭДТА с 0.02% раствором Версена.
Для трансфекции клеток биологически активной генно-терапевтической субстанцией содержащей кДНК гена GPX3 использовали амфифильные блок-сополимеры. Применяли методику по (IntJPharm, 2012, 427, 80-87) или в (Macromol. Biosci. 2011, 11, 652-661), с некоторыми изменениями. Блок-сополимер синтезировали из смеси линейного полиэтиленимина (ПЭИ) (Polyscience Inc., США) и бифункционального полиэтиленгликоля (ПЭГ) N-гидроксисукцинимидил-75-N-(3-малеимидопропионил)-амидо-4, 7, 10, 13, 16, 19, 22, 25, 28, 31, 34, 37, 40, 43, 46, 49, 52, 55, 58, 61, 64, 67, 70, 73 - тетракосаоксапента-гептаконтаноата (MAL-dPEG™-NHS ester, Quanta BioDesign, Ltd., США) в боратном буфере. Полиплекс готовили за 1 час до введения в клетки, смешивая раствор блок-сополимера с ДНК генетической конструкции pCMV6- Kan/Neo GPX3 SEQ ID No: 3 с модифицированной кДНК GPX3 SEQ ID No: 3. Смесь для трансфекции добавляли к суспензии клеток в 1 мл культуральной среды DMEM с 10% фетальной сывороткой и ампициллином.
Так как для трансфекции использовали конструкцию, содержащую фактор селекции (устойчивость к генетицину), то клетки после трансфекции выращивали в 25 см3 флаконах с 5 мл среды с генетицином в течение 12 дней, меняя среду каждые 4 дня. Каждые 24 часа из каждой культуры отбирали аликвоту по 500 мкл суспензии с целью выделения РНК и анализа уровня специфической кДНК. Выделение РНК производили с помощью набора RNeasyMiniKit(Qiagen, Germany). Образцы РНК были сгруппированы в 3 группы по 8 образцов с близкой концентрацией и объединены. Анализ уровня специфической кДНК GPX3 проводили с помощью амплификации в режиме реального времени по методике и с праймерами по примеру 6, используя набор реагентов iTaqUniversalSYBRGreenSupermix (Bio-Rad, USA), амплификатор CFX96 (Bio-Rad, USA) и программное обеспечение Bio-RadCFXManager 2.1. Максимальное увеличение транскрипции GPX3 наблюдали на 5 сутки. На фигуре 14 приведены кривые накопления специфического продукта амплификации, соответствующего кДНК гена GPX3.
Показано, что в хондробластах трансфицированных биологически активной генно-терапевтической субстанцией на основе рCMV6-Kan/Neo GPX3 SEQ ID No: 3, используя в качестве транспортной молекулы амфифильные блок-сополимеры, наблюдается усиление экспрессии целевого гена GPX3
Пример 13
Введение в кожу человека биологически активной генно-терапевтической субстанции с кДНК гена GPX3 с целью подтверждения при этом увеличения активности глутатионпероксидазы-3 в коже человека.
С целью анализа изменения активности белка глутатионпероксидазы-3 пациентам вводили биологически активную генно-терапевтическую субстанцию, содержащую генетическую конструкцию с кДНК гена GPX3 (В) и параллельно вводили плацебо, представляющее собой комбинацию векторной плазмиды не содержащей кДНК гена GPX3 с транспортной молекулой (А) - в кожу предплечья.
В качестве транспортной молекулы использовали порошок липосом TRANSFAST ТМ Transfection Reagent (PROMEGA, USA) по примеру 9. Далее генетическую конструкцию pCMV6_GPX3 SEQ ID No: 4, которая содержит модифицированную кДНК гена GPX3 (SEQ ID No: 4), и плазмиду pCMV6-XL5, используемую в качестве плацебо - которая не содержит кДНК гена GPX3, каждую из которых растворяли в стерильной воде степени очистки Nuclease-Free. Для получения биологически активных генно-терапевтических субстанций готовили комплексы ДНК-липосомы по примеру 9.
Полученные биологически активную генно-терапевтическую субстанцию и плацебо использовали для введения пациенту. Введение осуществляли тоннельным методом иглой 30G на глубину 3 мм. Объем вводимого раствора биологически активной генно-терапевтической субстанции и плацебо - около 0,3 мл для каждого. Очаги введения биологически активной генно-терапевтической субстанции и плацебо располагались на расстоянии 3-5 см друг от друга.
Активность глутатионпероксидазы-3 оценивали в лизатах биоптатов кожи пациента непрямым колориметрическим методом с помощью набора Glutathione Peroxidase Cellular Activity Assay Kit (Sigma-Aldrich, USA), по примеру 8. Биопсийные образцы брали на 3 сутки после введения биологически активной генно-терапевтической субстанции. Взятие биопсии осуществляли из участков кожи в зоне введения биологически активной генно-терапевтической субстанции и плацебо, а также из интактной кожи, используя устройство для взятия биопсии Epitheasy 3.5 (Medax SRL) далее как описано в примере 9.
Показано, что в коже пациента в области введения биологически активной генно-терапевтической субстанции с кДНК гена GPX3, произошло увеличение активности глутатионпероксидазы-3, тогда как при введении плацебо активность глутатионпероксидазы-3 в коже не изменялась. Результаты отражены на фигуре 15
Пример 14
Введение в слизистую оболочку рта человека биологически активной генно-терапевтической субстанции с кДНК гена GPX3 с целью подтверждения при этом увеличения активности глутатионпероксидазы-3 в слизистой оболочке рта человека.
С целью анализа изменения активности белка глутатионпероксидазы-3 пациентам вводили биологически активную генно-терапевтическую субстанцию, содержащую генетическую конструкцию с кДНК гена GPX3 (В) и параллельно вводили плацебо, представляющее собой комбинацию векторной плазмиды не содержащей кДНК гена GPX3 с транспортной молекулой (А) - в слизистую оболочку рта.
В качестве транспортной молекулы использовали порошок липосом TRANSFAST ТМ Transfection Reagent (PROMEGA, USA) по примеру 9. Далее генетическую конструкцию pCDNA 3.1 GPX3 SEQ ID No: 5, которая содержит модифицированную кДНК гена GPX3 (SEQ ID No: 5), и плазмиду pCDNA 3.1(+), используемую в качестве плацебо, которая не содержит кДНК гена GPX3, каждую из которых растворяли в стерильной воде степени очистки Nuclease-Free. Для получения биологически активных генно-терапевтических субстанций готовили комплексы ДНК-липосомы по примеру 9.
Полученные биологически активную генно-терапевтическую субстанцию и плацебо использовали для введения пациенту. Введение осуществляли тоннельным методом иглой 30G на глубину 1-2 мм. Объем вводимого раствора биологически активной генно-терапевтической субстанции и плацебо - около 0,3 мл для каждого. Очаги введения биологически активной генно-терапевтической субстанции и плацебо располагались на расстоянии 2-4 см друг от друга.
Активность глутатионпероксидазы-3 оценивали в лизатах биоптатов слизистой оболочки рта пациента непрямым колориметрическим методом с помощью набора Glutathione Peroxidase Cellular Activity Assay Kit (Sigma-Aldrich, USA).
Биопсийные образцы брали на 3 сутки после введения биологически активной генно-терапевтической субстанции. Взятие биопсии осуществляли из участков слизистой оболочки рта в зоне введения биологически активной генно-терапевтической субстанции, а также из интактных участков и в зоне введения плацебо, используя устройство для взятия биопсии Epitheasy 3.5 (Medax SRL), далее по примеру 9.
Показано, что в слизистой оболочке рта пациента в области введения биологически активной генно-терапевтической субстанции с кДНК гена GPX3, произошло увеличение активности глутатионпероксидазы-3, тогда как при введении плацебо активность глутатионпероксидазы-3 в слизистой оболочке рта не изменялась. Результаты отражены на фигуре 16.
Пример 15
Введение в мышечную ткань человека биологически активной генно-терапевтической субстанции с кДНК гена GPX3 с целью подтверждения при этом увеличения активности глутатионпероксидазы-3 в мышечной ткани человека.
С целью анализа изменения активности белка глутатионпероксидазы-3 пациентам вводили биологически активную генно-терапевтическую субстанцию, содержащую векторную плазмиду с кДНК гена GPX3 (В) и параллельно вводили плацебо, представляющее собой комбинацию векторной плазмиды не содержащей кДНК гена GPX3 с транспортной молекулой (А) - в мышечную ткань икроножной мышцы.
В качестве транспортной молекулы использовали порошок липосом TRANS FAST ТМ Transfection Reagent (PROMEGA, USA) no примеру 9. Далее генетическую конструкцию pCMV6-Kan/Neo GPX3 SEQ ID No: 6, которая содержит модифицированную кДНК гена GPX3 (SEQ ID No: 6), и плазмиду pCMV6-Kan/Neo, используемую в качестве плацебо, которая не содержит кДНК гена GPX3, каждую из которых растворяли в стерильной воде степени очистки Nuclease-Free.
Для получения биологически активных генно-терапевтических субстанций готовили комплексы ДНК-липосомы по примеру 9.
Полученные биологически активную генно-терапевтическую субстанцию и плацебо использовали для введения пациенту. Введение осуществляли тоннельным методом иглой 30G на глубину 15-20 мм. Объем вводимого раствора биологически активной генно-терапевтической субстанции и плацебо - около 0,5 мл для каждого. Очаги введения биологически активной генно-терапевтической субстанции и плацебо располагались на расстоянии 5-7 см друг от друга Активность глутатионпероксидазы-3 оценивали в лизатах биоптатов мышечной ткани пациента непрямым колориметрическим методом с помощью набора Glutathione Peroxidase Cellular Activity Assay Kit (Sigma-Aldrich, USA).).
Биопсийные образцы брали на 3 сутки после введения биологически активной генно-терапевтической субстанции. Взятие биопсии осуществляли из участков мышечной ткани в зоне введения биологически активной генно-терапевтической субстанции, а также из интактных участков мышцы и в зоне введения плацебо, используя автоматическое устройство для взятия биопсии MAGNUM (компания BARD, USA), далее по примеру 9.
Показано, что, в мышечной ткани пациента в области введения биологически активной генно-терапевтической субстанции с кДНК гена GPX3, произошло увеличение активности глутатионпероксидазы-3, тогда как при введении плацебо активность глутатионпероксидазы-3 в мышечной ткани не изменялась. Результаты отражены на фигуре 17.
Пример 16.
Введение группе различных пациентов биологически активных генно-терапевтических субстанций содержащих модифицированные и нативную кДНК GPX3.
С целью подтверждения индивидуального характера увеличения активности белка глутатионпероксидазы-3 до различного уровня при введении в кожу пациентов биологически активных генно-терапевтических субстанций с модифицированными и нативной кДНК гена GPX3 анализировали уровень активности белка глутатионпероксидазы-3 в лизате биоптатов кожи группы пациентов в зависимости от наличия и типа модификаций в кДНК гена GPX3.
Последовательность нативной кДНК GPX3 приведена на фигуре 1, SEQ GPX3 ID No: 1, последовательности модифицированных кДНК GPX3 приведены на фигуре 2-7 (SEQ GPX3 ID No: 2, SEQ GPX3 ID No: 3, SEQ GPX3 ID No: 4, SEQ GPX3 ID No: 5, SEQ GPX3 ID No: 6, SEQ GPX3ID No: 7).
При этом генетические конструкции, одна из которых содержит нативную кДНК гена GPX3 (SEQ ID No: 1), вторая генетическая конструкция содержит модифицированную кДНК гена GPX3 (SEQ ID No: 2), третья генетическая конструкция содержит модифицированную кДНК гена GPX3 (SEQ ID No: 3), четвертая генетическая конструкция содержит модифицированную кДНК гена GPX3 (SEQ ID No: 4)), пятая генетическая конструкция содержит модифицированную кДНК гена GPX3 (SEQ ID No: 5), шестая генетическая конструкция содержит модифицированную кДНК гена GPX3 (SEQ ID No: 6), седьмая генетическая конструкция содержит модифицированную кДНК гена GPX3 (SEQ ID No: 7), восьмая генетическая конструкция (плацебо), представляет собой вектор pCMV6 XL5, растворяли в стерильной воде степени очистки Nuclease-Free. Для получения биологически активных генно-терапевтических субстанций готовили комплексы ДНК-дендример по примеру 7.
Полученные семь вариантов биологически активных генно-терапевтических субстанций и плацебо использовали для введения в кожу пациентам. Введение осуществляли тоннельным методом иглой 30G на глубину 3 мм. Объем вводимого раствора каждой биологически активной генно-терапевтической субстанции составлял около 0,3 мл. Очаги введения биологически активных генно-терапевтических субстанций и плацебо располагались на расстоянии 3-5 см друг от друга.
Каждому из 21-го пациента, отобранных в случайном порядке, вводили 7 биологически активных генно-терапевтических субстанций и плацебо в кожу предплечья.
Биопсийные образцы брали через 72 часа после введения биологически активных генно-терапевтических субстанций. Взятие биопсии осуществляли из участков введения биологически активных генно-терапевтических субстанций, плацебо, а также из интактной кожи, используя устройство для взятия биопсии кожи Epitheasy 3.5 (Medax SRL). Кожу пациента предварительно промывали стерильным физиологическим раствором и анестезировали раствором лидокаина. Размер каждого биопсийного образца был около 3 мм, масса - до 20 мг. Образец помещали в буферный раствор, содержащий 50 мМ Трис-HCl pH 7.6, 100 мМ NaCl, 1 мМ ЭДТА и 1 мМ фенилметилсульфонилфторид и гомогенизировали до получения однородной суспензии. Полученную суспензию центрифугировали в течение 10 минут при 14000 об/мин.
А - биоптат, полученный после введения биологически активной генно-терапевтической субстанции на базе pCMV6- SEQ ID No: 1, содержащий немодифицированную кДНК GPX3 (SEQ ID No: 1.) по примеру 3 в сочетании с транспортной молекулой-дендримером по примеру 7.
В - биоптат, полученный после введения биологически активной генно-терапевтической субстанции на базе pCMV6- SEQ ID No: 2, содержащий вариант 1 модифицированной кДНК GPX3 (SEQ ID No: 2.) по примеру 3 в сочетании с транспортной молекулой-дендримером по примеру 7.
С - биоптат, полученный после введения биологически активной генно-терапевтической субстанции на базе pCMV6- SEQ ID No: 3, содержащий вариант 2 модифицированной кДНК GPX3 (SEQ ID No: 3) по примеру 3 в сочетании с транспортной молекулой-дендримером по примеру 7.
D - биоптат, полученный после введения биологически активной генно-терапевтической субстанции на базе pCMV6- SEQ ID No: 4, содержащая вариант 3 модифицированной кДНК GPX3 (SEQ ID No: 4) по примеру 3 в сочетании с транспортной молекулой-дендримером по примеру 7.
Е - - биоптат, полученный после введения биологически активной генно-терапевтической субстанции на базе pCMV6- SEQ ID No: 5, содержащая 4 вариант модифицированной кДНК GPX3 (SEQ ID No: 5) по примеру 3 в сочетании с транспортной молекулой-дендримером по примеру 7.
F - биоптат, полученный после введения биологически активной генно-терапевтической субстанции на базе на базе pCMV6- SEQ ID No: 6, содержащая вариант 5 модифицированной кДНК GPX3 SEQ ID No: 6) по примеру 3 в сочетании с транспортной молекулой-дендримером по примеру 7.
G - биоптат, полученный после введения биологически активной генно-терапевтической субстанции на базе pCMV6- SEQ ID No: 7, содержащий вариант 6 модифицированной кДНК GPX3 (SEQ ID No: 7) по примеру 3 в сочетании с транспортной молекулой-дендримером по примеру 7.
Н - биоптат, полученный после введения векторной плазмиды pCMV6-XL5, не содержащая кДНК гена GPX3 по примеру 3 в сочетании с транспортной молекулой-дендримером по примеру 7.
Активность белка глутатионпероксидазы-3 определяли в девяти биоптатах кожи от каждого пациента (от А до Н и в биоптате интактной кожи) через 72 часа после введения биологически активных генно-терапевтических субстанций непрямым колориметрическим методом с помощью набора Glutathione Peroxidase Cellular Activity Assay Kit (Sigma-Aldrich, USA). Анализ проводили по методике, рекомендуемой производителем. Предварительно проводили оценку степени ингибирования цветной реакции в зависимости от концентрации чистого препарата глутатионпероксидазы-3 Исходя из данных предыдущих экспериментов, описанных в примере 8, лизат разводили в 5 раз.
По итогам анализа уровня активности глутатионпероксидазы-3 выбрали показатели, касательно каждого биоптата от каждого пациента, продемонстрировавшие максимальные уровни активности глутатионпероксидазы-3 и объединили их в семь групп, исходя из следующего критерия:
В группе 1 максимальное ингибирование в лизате биоптата, что соответствует максимальной активности
глутатионпероксидазы-3, наблюдалось при введении немодифицированной кДНК GPX3. В эту группу вошло 2 биоптата из 21.
В группе 2 максимальное ингибирование в лизате биоптата, что соответствует максимальной активности
глутатионпероксидазы-3, наблюдалось при введении 1 варианта модифицированной кДНК GPX3. В эту группу вошел 1 биоптат из 21.
В группе 3 максимальное ингибирование в лизате биоптата, что соответствует максимальной активности глутатионпероксидазы-3, наблюдалось при введении 2 варианта модифицированной кДНК GPX3. В эту группу вошло 3 биоптата из 21.
В группе 4 максимальное ингибирование в лизате биоптата, что соответствует максимальной активности глутатионпероксидазы-3, наблюдалось при введении 3 варианта модифицированной кДНК GPX3. В эту группу вошло 5 биоптатов из 21.
В группе 5 максимальное ингибирование в лизате биоптата, что соответствует максимальной активности глутатионпероксидазы-3, наблюдалось при введении 4 варианта модифицированной кДНК GPX3. В эту группу вошло 5 биоптатов из 21.
В группе 6 максимальное ингибирование в лизате биоптата, что соответствует максимальной активности глутатионпероксидазы-3, наблюдалось при введении 5 варианта модифицированной кДНК GPX3. В эту группу вошел 1 биоптат из 21.
В группе 7 максимальное ингибирование в лизате биоптата, что соответствует максимальной активности глутатионпероксидазы-3, наблюдалось при введении 6 варианта модифицированной кДНК GPX3. В эту группу вошло 4 биоптата из 21.
Ни в одном из биоптатов не наблюдалось того, что максимальное ингибирование цветной реакции, соответствующее максимальной активности глутатионпероксидазы-3, присутствует при введении плацебо - векторной плазмиды, не содержащей кДНК гена GPX3.
На фигуре 18 для каждой группы биоптатов приведены диаграммы показателей ингибирования цветной реакции (усредненных в рамках группы, в случае, если в группу входит более одного биоптата) применительно ко всем, участвующим в эксперименте активным генно-терапевтическим субстанциям, после введения пациентам этих активных генно-терапевтических субстанций, содержащих модифицированные и нативную кДНК гена GPX3.
Из данного примера следует, что достижение максимальной активности глутатионпероксидазы-3 в биоптатах кожи различных пациентов при введении им в кожу биологически активных генно-терапевтических субстанций, связано с индивидуальными особенностями пациентов и зависит от наличия и типа модификаций в кДНК гена GPX3, входящих в биологически активные генно-терапевтические субстанции.
Каждая биологически активная генно-терапевтическая субстанция из линейки биологически активных генно-терапевтических субстанций является эффективной в некоторой значительной группе пациентов. Следовательно для выбора наиболее эффективной биологически активной генно-терапевтической субстанции из линейки биологически активных генно-терапевтических субстанций для терапевтических целей необходимо предварительное персонализированное исследование биоптатов пациента, либо клеток, выращенных из этих биоптатов на предмет максимальной эффективности терапевтического воздействия, созданных биологически активных генно-терапевтических субстанций в рамках линейки биологически активных генно-терапевтических субстанций.
Пример 17
Трансфекция клеточной линии фибробластов пациента разными биологически активными генно-терапевтическими субстанциями, содержащими модифицированные и нативную кДНК GPX3 с целью персонализированного выбора из линейки биологически активных генно-терапевтических субстанций наиболее эффективной биологически активной генно-терапевтической субстанции применительно к данному пациенту для последующей трансфекции этой субстанцией клеток пациента в рамках терапевтической процедуры.
С целью определения наиболее эффективной применительно к конкретному пациенту биологически активной генно-терапевтической субстанции анализировали активность глутатионпероксидазы-3 в клеточных лизатах фибробластов этого пациента, трансфицированных разными биологически активными генно-терапевтическими субстанциями, содержащими нативную или модифицированные кДНК GPX3. Последовательность нативной кДНК GPX3 приведена на фигуре 1, SEQ ID No: 1, последовательности модифицированных кДНК GPX3 приведены на фигурах 2-7 (SEQ ID No: 2, SEQ ID No: 3, SEQ ID No: 4, SEQ ID No: 5, SEQ ID No: 6, SEQ ID No: 7).
Вырастили культуры фибробластов из биоптата пациента по примеру 5, отобрали аликвоты и провели клеточный лизис: клеточный осадок, соответствующий 2×106 клеток, промывали фосфатным буфером и ресуспендировали во льду в лизирующем буфере, содержащем 25 мМ ХЕПЕС pH 7.9, 100 мМ NaCl, 1 мМ ЭДТА, 1% Тритон Х-100, 10% глицерин и 1 мМ фенилметилсульфонилфторид. Лизат центрифугировали 5 минут при 14000 об/мин, концентрацию белка в супернатанте определяли методом Брэдфорда.
Активность глутатионпероксидазы-3 определяли непрямым колориметрическим методом с помощью набора Glutathione Peroxidase Cellular Activity Assay Kit (Sigma-Aldrich, USA). Анализ проводили по методике, рекомендуемой производителем. Предварительно проводили оценку степени ингибирования цветной реакции в зависимости от концентрации чистого препарата глутатионпероксидазы-3.
Затем культуру фибробластов пациента разделили на 8 частей. Одну часть, обозначенную (А), трансфицировали по примеру 7 биологически активной генно-терапевтической субстанцией на базе вектора pCMV6- SEQ ID No: 1, содержащей немодифицированную кДНК GPX3 (SEQ ID No: 1) по примеру 3 в сочетании с транспортными молекулами-липосомами по примеру 9. Вторую часть, обозначенную (В), трансфицировали по примеру 7 биологически активной генно-терапевтической субстанцией на базе вектора pCMV6- SEQ ID No: 2, содержащей вариант 1 модифицированной кДНК GPX3 (SEQ ID No: 2) по примеру 3 в сочетании с транспортными молекулами - липосомами по примеру 9. 3-ю часть, обозначенную (С), трансфицировали по примеру 7 биологически активной генно-терапевтической субстанцией на базе вектора pCMV6- SEQ ID No: 3, содержащей вариант 2 модифицированной кДНК GPX3 (SEQ ID No: 3) по примеру 3 в сочетании с транспортными молекулами-липосомами по примеру 9. 4-ю часть, обозначенную (D), трансфицировали по примеру 7 биологически активной генно-терапевтической субстанцией на базе вектора pCMV6- SEQ ID No: 4, содержащей вариант 3 модифицированной кДНК GPX3 (SEQ ID No: 4) по примеру 3 в сочетании с транспортными молекулами-липосомами по примеру 9. 5-ю часть, обозначенную (Е), трансфицировали по примеру 7 биологически активной генно-терапевтической субстанцией на базе вектора pCMV6- SEQ ID No: 5, содержащей 4 вариант модифицированной кДНК GPX3 (SEQ ID No: 5) по примеру 3 в сочетании с транспортными молекулами-липосомами по примеру 9. 6-ю часть, обозначенную (F), трансфицировали по примеру 7 биологически активной генно-терапевтической субстанцией на базе вектора pCMV6- SEQ ID No: 6, содержащей вариант 5 модифицированной кДНК GPX3 SEQ ID No: 6) по примеру 3 в сочетании с транспортными молекулами-липосомами по примеру 9. 7-ю часть, обозначенную (G), трансфицировали по примеру 7 биологически активной генно-терапевтической субстанцией на базе вектора pCMV6- SEQ ID No: 7, содержащей вариант 6 модифицированной кДНК GPX3 (SEQ ID No: 7) по примеру 3 в сочетании с транспортными молекулами-липосомами по примеру 9. 8-ю часть, обозначенную (Н), трансфицировали по примеру 7 векторной плазмидой pCMV6-XL5, не содержащей кДНК GPX3 по примеру 3 в сочетании с транспортными молекулами-липосомами по примеру 9.
Активность глутатионпероксидазы-3 определяли через 72 часа после трансфекции. Исходя из данных предыдущих экспериментов, описанных в примере 8, лизат разводили в 5 раз.
По итогам анализа активности глутатионпероксидазы-3 в культуре фибробластов пациента выделили вариант биологически активной генно-терапевтической субстанции, при трансфекции которой происходит максимальное ингибирование в лизате клеточной культуры и соответственно наблюдается максимальная активность глутатионпероксидазы-3. В данном эксперименте максимальное ингибирование в лизате отмечено при трансфекции биологически активной генно-терапевтической субстанцией на базе pCMV6 GPX3 SEQ ID No: 7, содержащей модифицированную кДНК GPX3, что показано на фигуре 19.
Таким образом, выбрана наиболее эффективная применительно к данному пациенту биологически активная генно-терапевтическая субстанция для последующей трансфекции клеток пациента в рамках терапевтической процедуры.
Пример 18
Введение в кожу пациента различных биологически активных генно-терапевтических субстанций, содержащих модифицированные и нативную кДНК гена GPX3 с целью персонализированного выбора из линейки биологически активных генно-терапевтических субстанций наиболее эффективной биологически активной генно-терапевтической субстанции применительно к данному пациенту для последующего введения этой субстанции пациенту в рамках терапевтической процедуры.
С целью определения наиболее эффективной применительно к конкретному пациенту биологически активной генно-терапевтической субстанции анализировали активность глутатионпероксидазы-3 в лизатах биоптатов кожи этого пациента, после введения ему в кожу биологически активных генно-терапевтических субстанций, содержащих нативную или модифицированные кДНК гена GPX3. Последовательность нативной кДНК GPX3 приведена на фигуре 1, SEQ ID No: 1., последовательности модифицированных кДНК GPX3 приведены на фигурах 2-7 (SEQ ID No: 2, SEQ ID No: 3, SEQ ID No: 4, SEQ ID No: 5, SEQ ID No: 6, SEQ ID No: 7)
Пациенту вводили 7 биологически активных генно-терапевтических субстанций и плацебо в кожу предплечья.
Первая биологически активная генно-терапевтическоая субстанция (А) на базе pCMV6- SEQ ID No: 1, содержащая немодифицированную кДНК GPX3 (SEQ ID No: 1) по примеру 3 в сочетании с транспортной молекулой-дендримером по примеру 7.
Вторая биологически активная генно-терапевтическая субстанция (В) на базе pCMV6- SEQ ID No: 2, содержащая вариант 1 модифицированной кДНК GPX3 (SEQ ID No: 2) по примеру 3 в сочетании с транспортной молекулой-дендримером по примеру 7.
3-я биологически активная генно-терапевтическая субстанция (C) на базе pCMV6- SEQ ID No: 3, содержащая вариант 2 модифицированной кДНК GPX3 (SEQ ID No: 3) по примеру 3 в сочетании с транспортной молекулой-дендримером по примеру 7.
4-я биологически активная генно-терапевтическая субстанция (D) на базе pCMV6- SEQ ID No: 4, содержащая вариант 3 модифицированной кДНК GPX3 (SEQ ID No: 4) по примеру 3 в сочетании с транспортной молекулой-дендримером по примеру 7.
5-я биологически активная генно-терапевтическая субстанция (Е) на базе pCMV6- SEQ ID No: 5, содержащая 4 вариант модифицированной кДНК GPX3 (SEQ ID No: 5) по примеру 3 в сочетании с транспортной молекулой-дендримером по примеру 7.
6-я биологически активная генно-терапевтическая субстанция (F) на базе pCMV6- SEQ ID No: 6, содержащая вариант 5 модифицированной кДНК GPX3 SEQ ID No: 6) по примеру 3 в сочетании с транспортной молекулой-дендримером по примеру 7.
7-я биологически активная генно-терапевтическая субстанция (G) на базе pCMV6- SEQ ID No: 7, содержащая вариант 6 модифицированной кДНК GPX3 (SEQ ID No: 7) по примеру 3 в сочетании с транспортной молекулой-дендримером по примеру 7.
8-я - векторная плазмида pCMV6-XL5, не содержащая кДНК GPX3 по примеру 3 в сочетании с транспортной молекулой-дендримером по примеру 7.
При этом генетические конструкции, одна из которых содержит нативную кДНК гена GPX3 (SEQ ID No: 1), вторая генетическая конструкция содержит модифицированную кДНК гена GPX3 (SEQ ID No: 2), третья генетическая конструкция содержит модифицированную кДНК гена GPX3 (SEQ ID No: 3), четвертая генетическая конструкция содержит модифицированную кДНК гена GPX3 (SEQ ID No: 4), пятая генетическая конструкция содержит модифицированную кДНК гена GPX3 (SEQ ID No: 5), шестая генетическая конструкция содержит модифицированную кДНК гена GPX3 (SEQ ID No: 6), седьмая генетическая конструкция содержит модифицированную кДНК гена GPX3 (SEQ ID No: 7), восьмая плазмида (плацебо), представляет собой вектор pCMV6 XL5, растворяли в стерильной воде степени очистки Nuclease-Free. Для получения биологически активных генно-терапевтических субстанций готовили комплексы ДНК-дендример по примеру 7.
Полученные семь вариантов биологически активных генно-терапевтических субстанций и плацебо использовали для введения пациенту. Введение осуществляли тоннельным методом иглой 30G на глубину 3 мм. Объем вводимого раствора каждой биологически активной генно-терапевтической субстанции составлял около 0,3 мл. Очаги введения биологически активных генно-терапевтических субстанций и плацебо располагались на расстоянии 3-5 см друг от друга.
Биопсийные образцы брали через 72 часа после введения биологически активных генно-терапевтических субстанций. Взятие биопсии осуществляли из участков введения биологически активных генно-терапевтических субстанций, плацебо, а также из интактной кожи используя устройство для взятия биопсии кожи Epitheasy 3.5 (Medax SRL). Кожу пациента предварительно промывали стерильным физиологическим раствором и анестезировали раствором лидокаина. Размер каждого биопсийного образца был около 3 мм, масса - до 20 мг. Образец помещали в буферный раствор, содержащий 50 мМ Трис-HCl pH 7.6, 100 мМ NaCl, 1 мМ ЭДТА и 1 мМ фенилметилсульфонилфторид и гомогенизировали до получения однородной суспензии. Полученную суспензию центрифугировали в течение 10 минут при 14000 об/мин.
Активность глутатионпероксидазы-3 определяли в девяти биоптатах кожи пациента через 72 часа после введения биологически активных генно-терапевтических субстанций непрямым колориметрическим методом с помощью набора Glutathione Peroxidase Cellular Activity Assay Kit (Sigma-Aldrich, USA). Анализ проводили по методике, рекомендуемой производителем. Предварительно проводили оценку степени ингибирования цветной реакции в зависимости от концентрации чистого препарата глутатионпероксидазы-3. Исходя из данных предыдущих экспериментов, описанных в примере 8, лизат разводили в 5 раз.
По итогам анализа активности глутатионпероксидазы-3 в лизате биоптатов кожи пациента выделили вариант биологически активной генно-терапевтической субстанции, при введении которой в кожу происходит максимальное ингибирование в лизате биоптата кожи и соответственно наблюдается максимальная активность глутатионпероксидазы-3. В данном эксперименте максимальное ингибирование в лизате биптатата кожи отмечено при введении биологически активной генно-терапевтической субстанции на базе pCMV6 GPX3 SEQ ID No: 3, содержащей модифицированную кДНК GPX3, что показано на фигуре 20.
Таким образом выбрана наиболее эффективная применительно к данному пациенту биологически активная генно-терапевтическая субстанция для ее последующего введения пациенту в рамках терапевтической процедуры.
Создана линейка биологически активных генно-терапевтических субстанций для коррекции патологических состояний клеток органов и тканей и/или органов и тканей человека, связанных с оксидативным стрессом вследствие недостаточной экспрессии гена GPX3, способ ее получения и использования.
Созданная линейка биологически активных генно-терапевтических субстанций с использованием одной из модифицированных или нативной кДНК гена GPX3 позволяет на практике использовать входящие в линейку биологически активные генно-терапевтические субстанции для повышения до необходимого уровня активности белка глутатионпероксидазы-3 в различных клетках органов и тканей и/или органах и тканях человека.
В результате проведения предварительных исследований биоптата пациента, либо клеток, выращенных из этих биоптатов, определяют, какой вариант биологически активной генно-терапевтической субстанции из созданной линейки биологически активных генно-терапевтических субстанций необходимо выбрать для данного пациента для того, чтобы повысить активность белка глутатионпероксидазы-3 клетках этих органов и тканей и/или органах и тканях до необходимого уровня применительно к конкретному пациенту. В тех случаях, когда использование биологически активной генно-терапевтической субстанции с нативной кДНК гена GPX3 не приводит к желаемому изменению уровня активности белка глутатионпероксидазы-3 в клетках органов и тканей и/или органах и тканях, необходимо применять субстанцию на основе модифицированной кДНК гена GPX3, приводящей к более эффективной экспрессии гена GPX3.
При использовании заявленной биологически активной генно-терапевтической субстанции не происходит встраивания экзогенного генетического материала в геном клетки.
Линейка биологически активных генно-терапевтических субстанций обеспечивает высокий уровень экспрессии гена GPX3, повышая активность белка глутатионпероксидазы-3 в клетках органов и тканей и/или органах и тканях человека в частности, в гемопоэтических клетках, или гепатоцитах, или мезенхимальных стволовых клетках, или хондробластах, или клетках поджелудочной железы (например, в клетках панкреатических островков), или миоцитах или фибробластах кожи, или кератоцитах, или эпителиальных клетках роговицы, или в нейронах, ганглиях, Шванновских клетках, астроцитах, олигодендроцитах, микроглии, или в сперматозоидах, или в нефронах, или эндотелиальных клетках, или эпителиальных клетках в сочетании с транспортной молекулой или без нее при трансфекции этими биологически активными генно-терапевтическими субстанциями клеток органов и тканей человека и/или в органах и тканях человека в частности, в коже, суставах, печени, надпочечниках, почках, головном и спинном мозге, легких, сердце, сосудах, желудочно-кишечном тракте, простате, поджелудочной железе, глазе, роговице, слизистой оболочке, хрящевой ткани, мышечной ткани в сочетании с транспортной молекулой или без нее при введении этих биологически активных генно-терапевтических субстанций в органы и ткани человека.
Таким образом, приведенные примеры подтверждают выполнение поставленной задачи, а именно, создание линейки биологически активных генно-терапевтических субстанций, при использовании которых применительно к клеткам органов и тканей и/или органам и тканям человека компенсируются дефекты гена GPX3, влияющие на экспрессию этого гена или на уровень активности белка глутатионпероксидазы-3, кодируемого этим геном, а также компенсируется недостаточная активность белка глутатионпероксидазы-3, вызванная факторами, влияющими на экспрессию гена GPX3.
Повышение эффективности коррекции уровня активности белка глутатионпероксидазы-3 в клетках органов и тканей человека достигают за счет того, что при недостаточной активности этого белка вследствие дефекта гена GPX3 используют не белок, а генетическую конструкцию с кДНК гена GPX3, кодирующую этот белок. При введении генетических конструкций в отличие от введения непосредственно белка, как в прототипе, снижается требуемая частота их введения в связи с пролонгированным действием, а также облегчается внутриклеточная доставка.
Промышленная применимость.
Все приведенные примеры по созданию и использованию созданной линейки биологически активных генно-терапевтических субстанций подтверждают ее промышленную применимость.
Перечень сокращений
ДНК - дезоксирибонуклеиновая кислота
кДНК - комплементарная дезоксирибонуклеиновая кислота
РНК - рибонуклеиновая кислота
мРНК - матричная рибонуклеиновая кислота
ПЦР - полимеразная цепная реакция
мл - миллилитр, мкл - микролитр
л - литр
мкг - микрограмм
мг - миллиграмм
г - грамм
мкМ - микромоль
мМ - миллимоль
об/мин - обороты в минуту
нм - нанометр
см - сантиметр
мВт - милливатт
о.е. ф-относительная единица флуоресценции
БАГТС - биологически активная генно-терапевтическая субстанция.







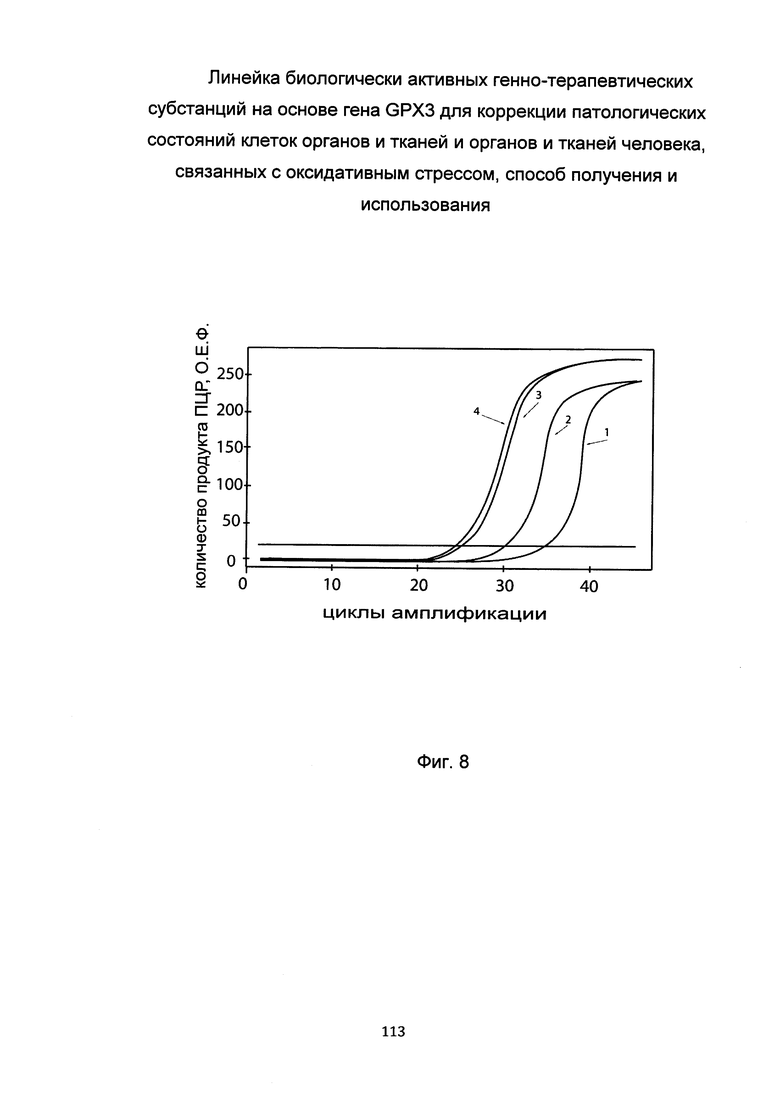
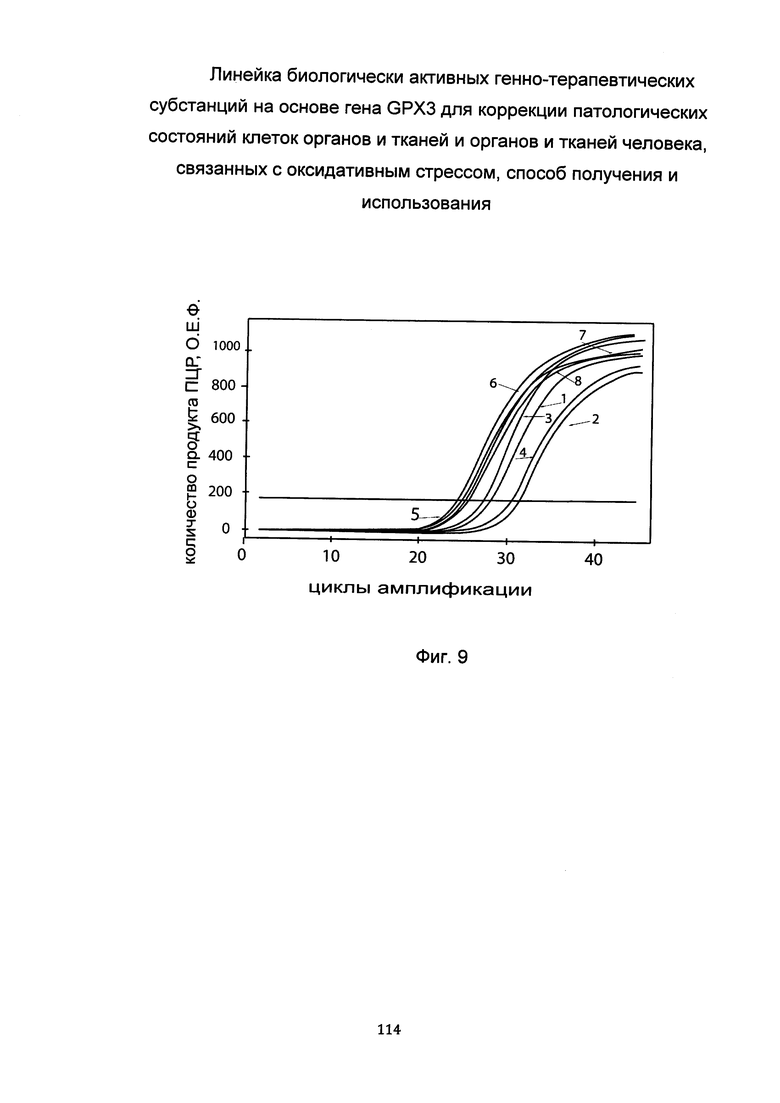
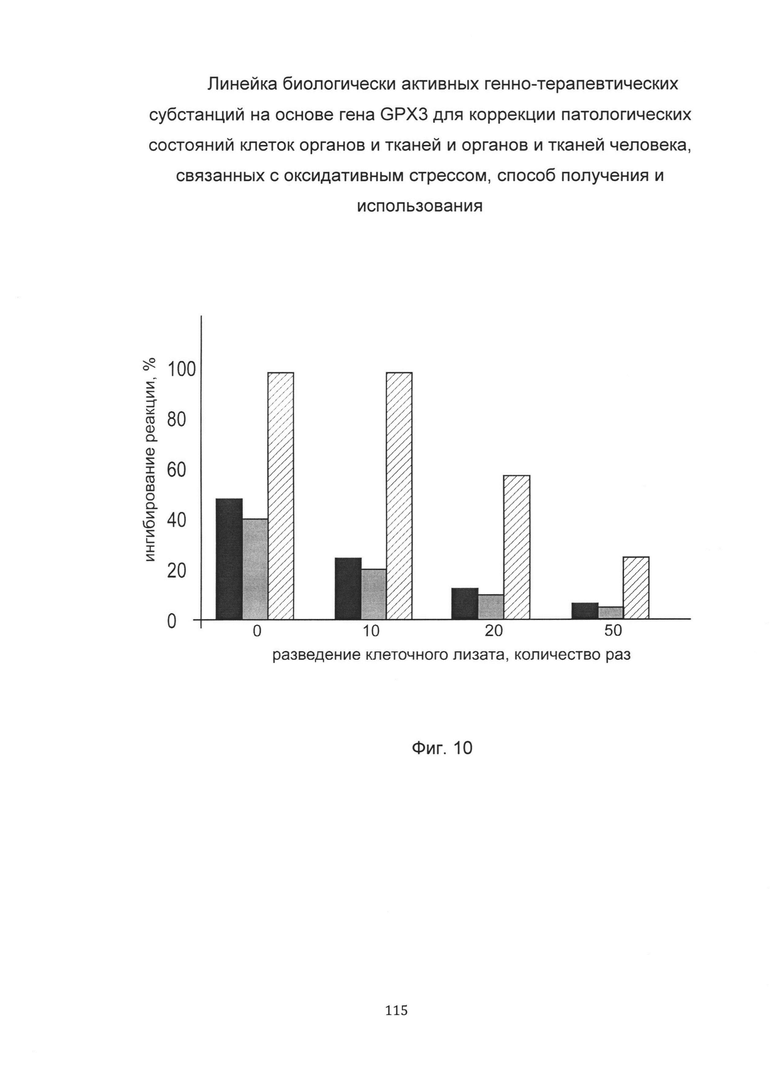
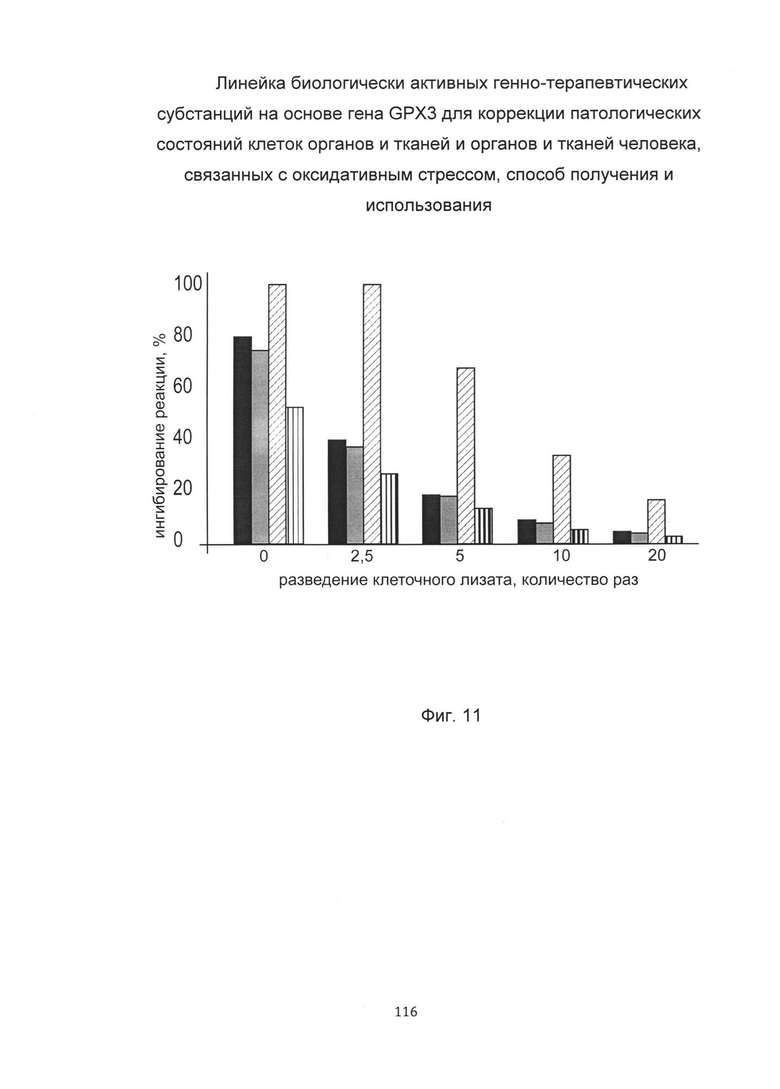
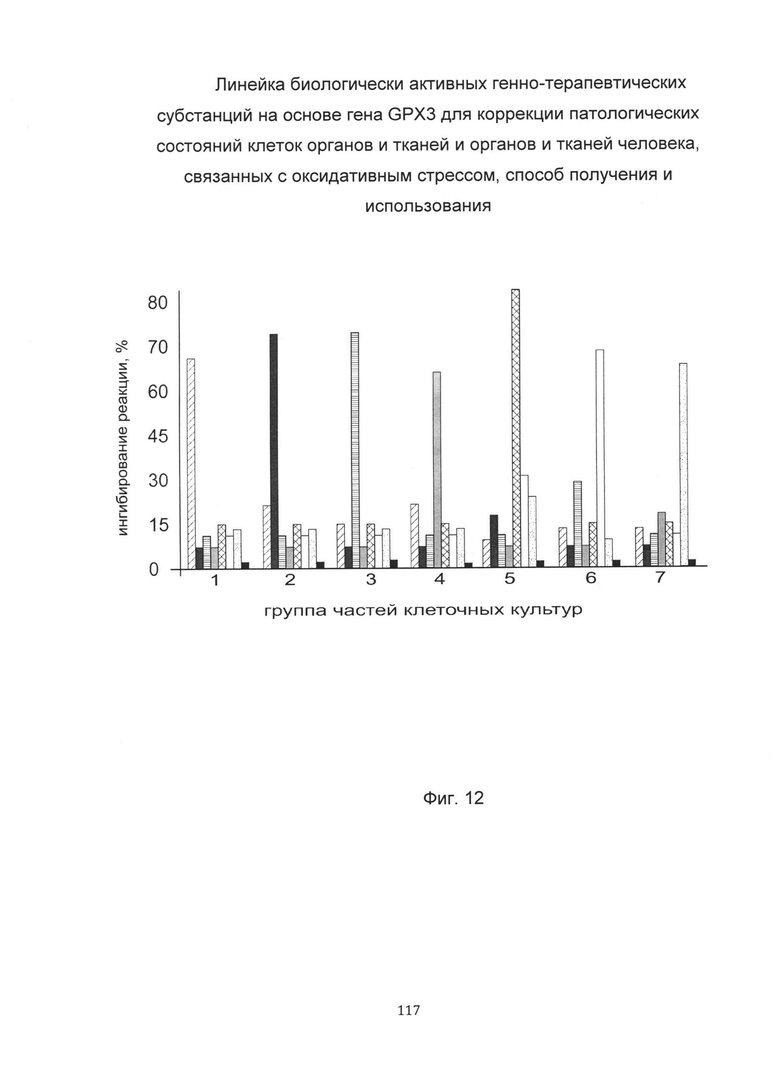
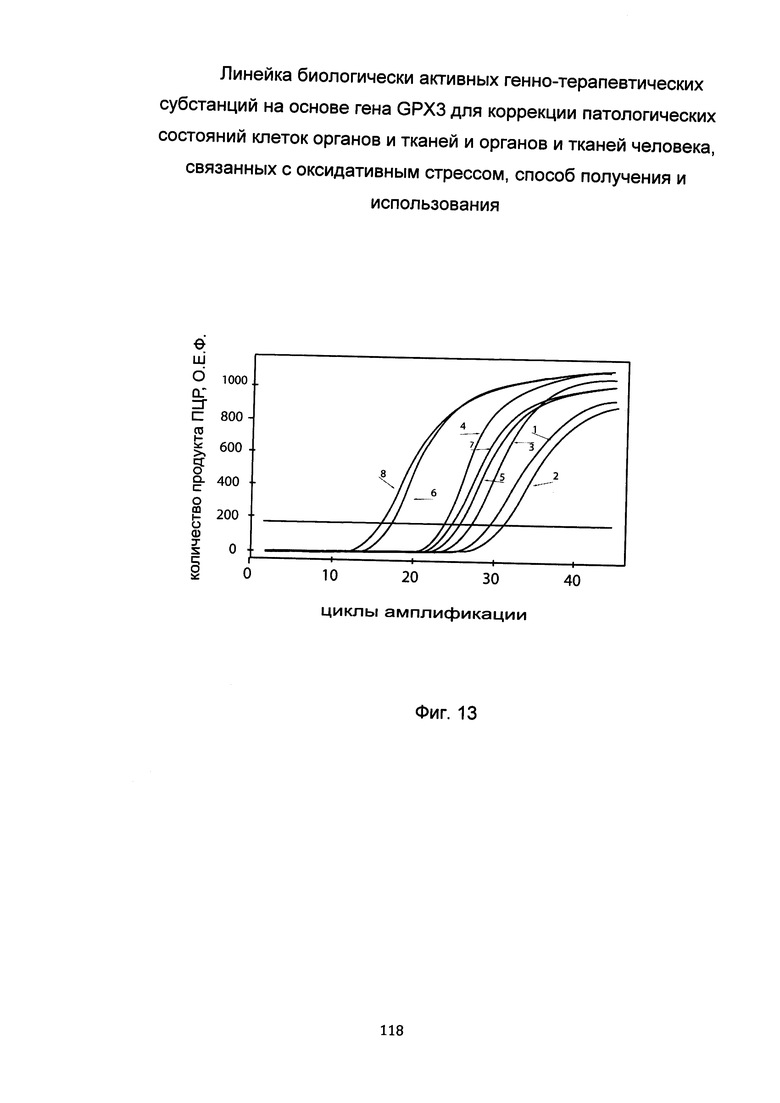
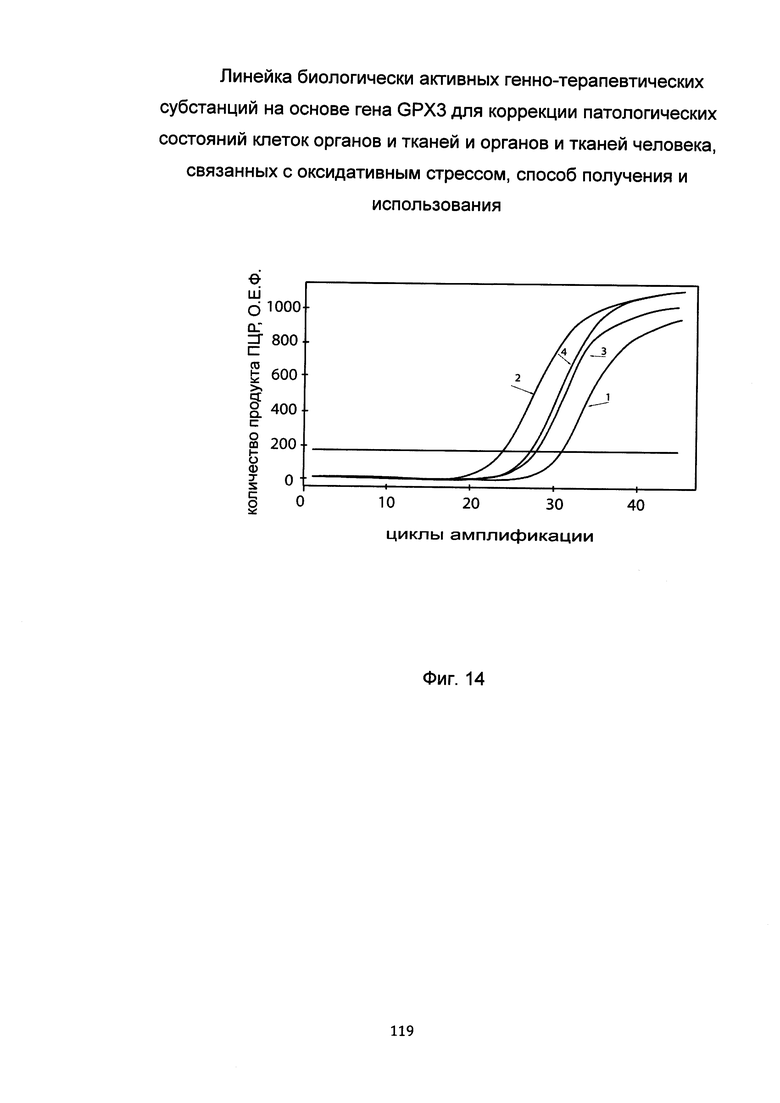
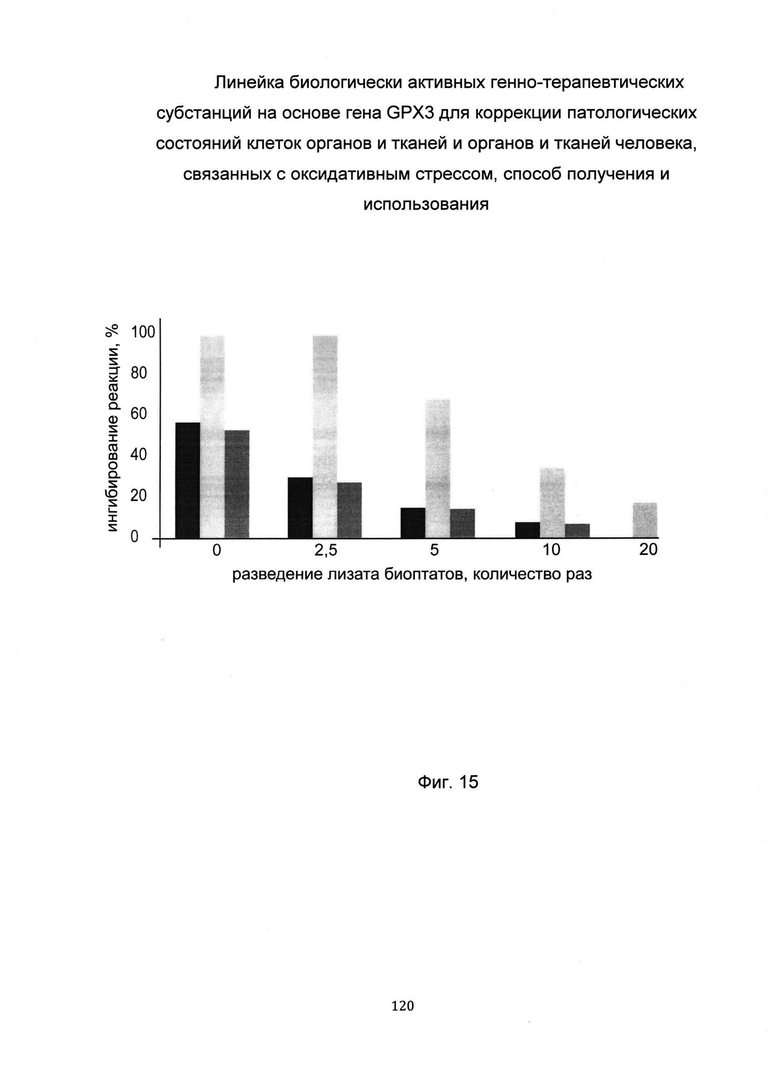
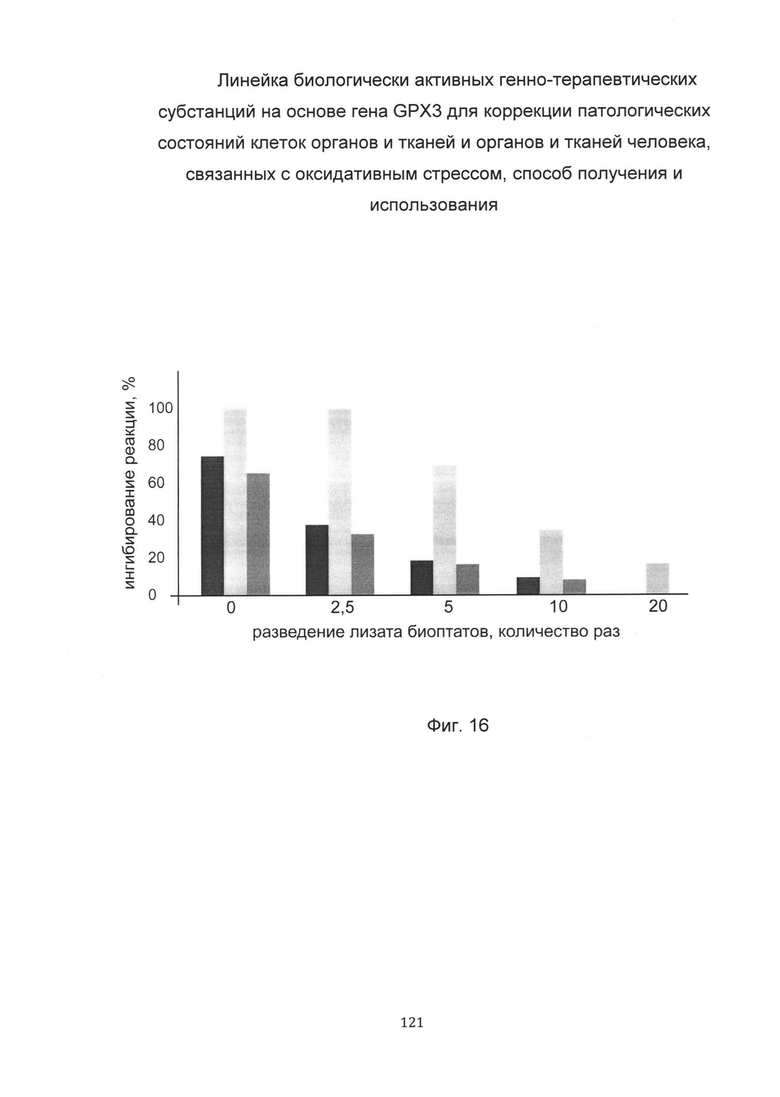
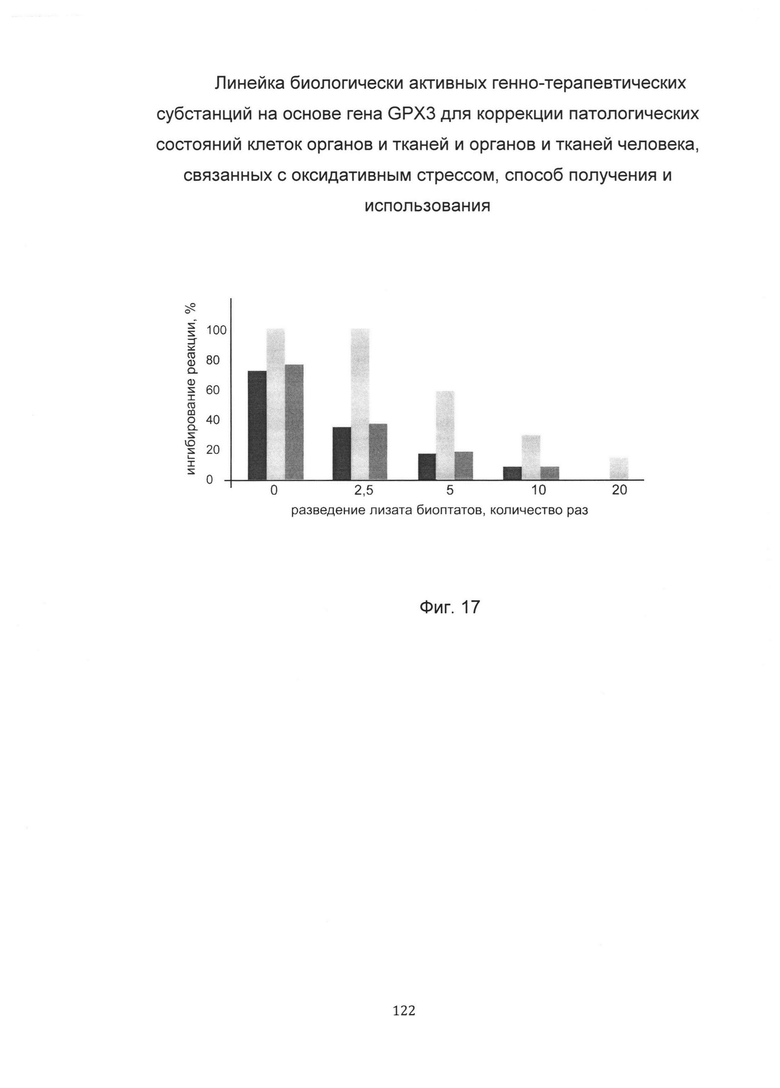
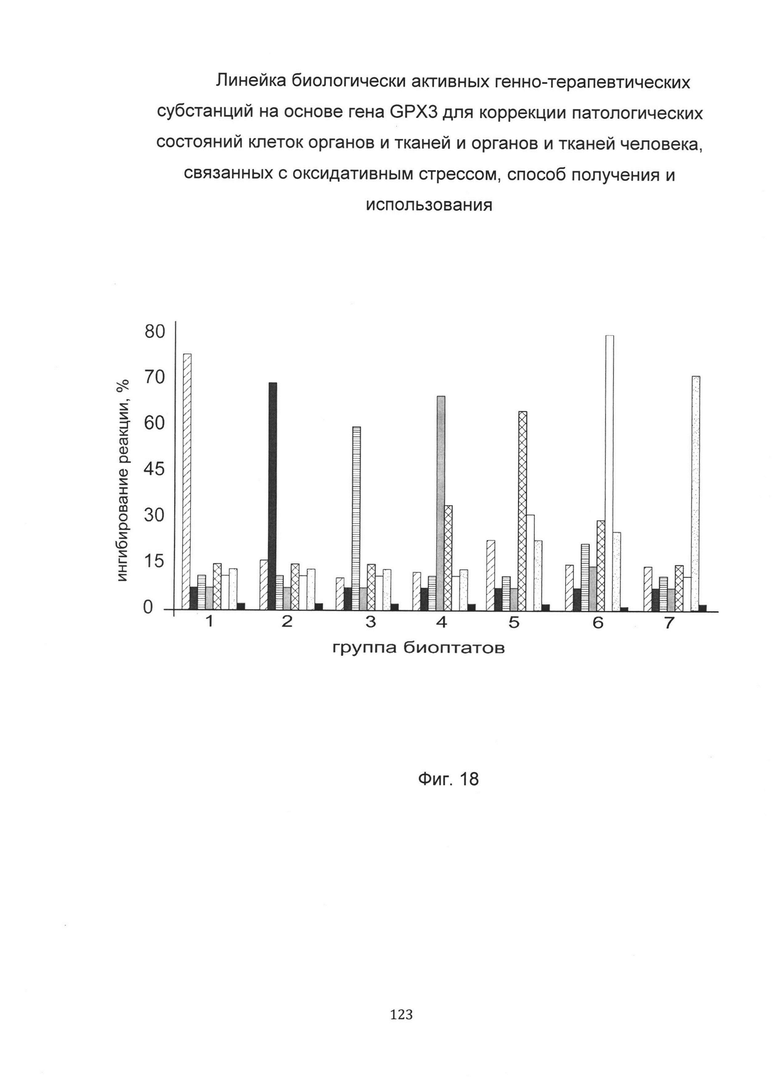
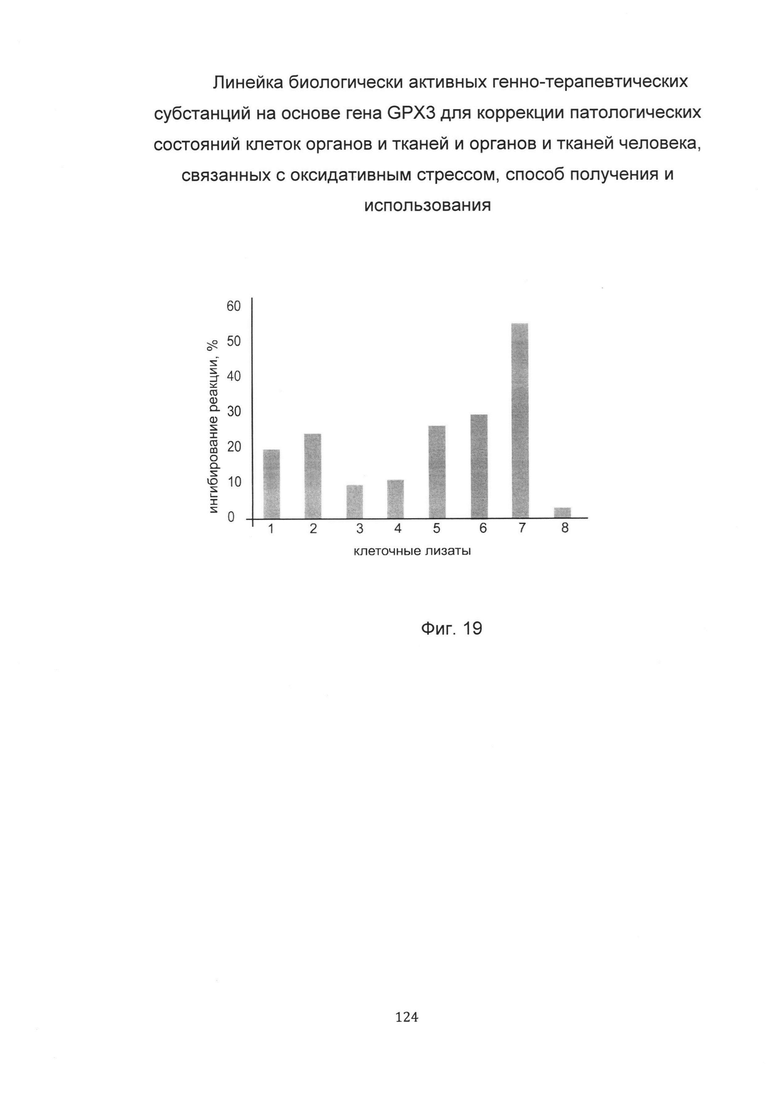
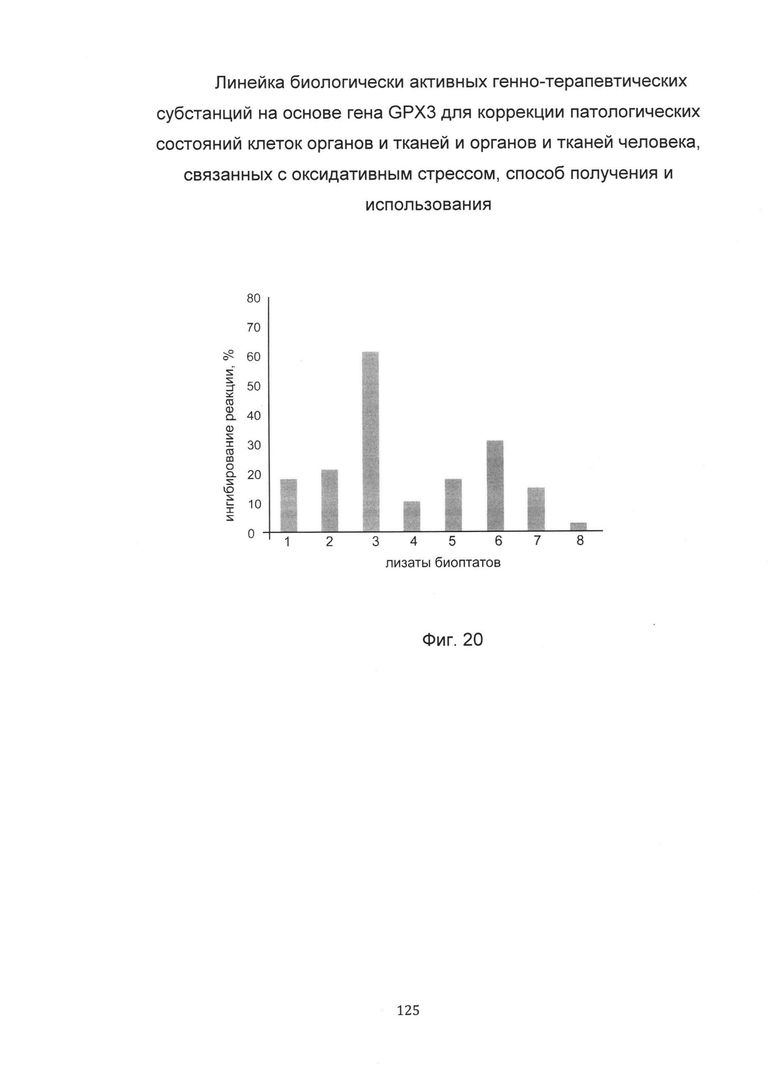
Группа изобретений относится к медицине и касается средства для коррекции патологических состояний клеток органов и тканей и/или органов и тканей человека, на основе гена GPX3, связанных с оксидативным стрессом, где клетки органов и тканей выбраны из клеток фибробластов, кератоцитов и эпителиальных клеток глаза, хондробластов; органы и ткани выбраны из кожи, слизистой оболочки рта человека или мышечной ткани человека, представляющего собой совокупность биологически активных генно-терапевтических субстанций, причем каждая из совокупности биологически активных генно-терапевтических субстанций представляет собой генетическую конструкцию на основе векторной плазмиды, включающую участок кДНК гена GPX3 и содержащую также регуляторные элементы, обеспечивающие транскрипцию этой последовательности в эукариотических клетках, а именно в клетках органов и тканей человека, в сочетании с транспортной молекулой или без нее. Группа изобретений также касается способа получения указанного средства для коррекции патологических состояний клеток органов и тканей и/или органов и тканей человека на основе гена GPX3, связанных с оксидативным стрессом; способа использования указанного средства для коррекции патологических состояний клеток органов и тканей и/или органов и тканей человека, на основе гена GPX3, связанных с количественным снижением белка GPX3. Группа изобретений обеспечивает высокий и стабильный уровень целевого белка в клетках. 3 н. и 2 з.п. ф-лы, 18 пр., 20 ил.
1. Средство для коррекции патологических состояний клеток органов и тканей и/или органов и тканей человека, на основе гена GPX3, связанных с оксидативным стрессом, где клетки органов и тканей выбраны из клеток фибробластов, кератоцитов и эпителиальных клеток глаза, хондробластов; органы и ткани выбраны из кожи, слизистой оболочки рта человека или мышечной ткани человека, представляющее собой совокупность биологически активных генно-терапевтических субстанций, причем каждая из совокупности биологически активных генно-терапевтических субстанций представляет собой генетическую конструкцию на основе векторной плазмиды, включающей участок кДНК гена GPX3, выбранный из нативной кДНК гена GPX3 SEQ ID No: 1, или модифицированной кДНК гена GPX3, при этом в качестве модифицированной кДНК гена GPX3, используют SEQ ID No: 2, или SEQ ID No: 3, или SEQ ID No: 4, или SEQ ID No: 5, или SEQ ID No: 6, или SEQ ID No: 7, или их сочетание и содержащей также регуляторные элементы, обеспечивающие транскрипцию этой последовательности в эукариотических клетках, а именно в клетках органов и тканей человека, в сочетании с транспортной молекулой или без нее.
2. Средство по п. 1, отличающееся тем, что каждая биологически активная генно-терапевтическая субстанция из совокупности биологически активных генно-терапевтических субстанций содержит генетическую конструкцию с кДНК гена GPX3 с последовательностью нуклеотидов, включающую в себя белок-кодирующую область кДНК гена GPX3, которая несет модификации, не затрагивающие структуру белка глутатионпероксидазы-3, а именно: делеции 5' нетранслируемых областей или делеции 3'-нетранслируемых областей, или нуклеотидные замены, не приводящие к аминокислотным заменам или обрыву аминокислотной цепи, или комбинации вышеперечисленных модификаций и, соответственно, не влияющие на кодируемую этой последовательностью аминокислотную последовательность.
3. Средство по п. 1, в котором каждая биологически активная генно-терапевтическая субстанция из совокупности биологически активных генно-терапевтических субстанций содержит в качестве транспортной молекулы липосомы или дендримеры 5-го и выше поколений.
4. Способ получения средства для коррекции патологических состояний клеток органов и тканей и/или органов и тканей человека на основе гена GPX3, связанных с оксидативным стрессом по п. 1, в котором каждую биологически активную генно-терапевтическую субстанцию из совокупности биологически активных генно-терапевтических субстанций получают следующим образом: получают кДНК гена GPX3, затем помещают кДНК в векторную плазмиду, наращивают и выделяют необходимое количество генетической конструкции, затем комбинируют генетическую конструкцию с транспортной молекулой для трансфекции полученной биологически активной генно-терапевтической субстанции клеток органов и тканей и/или введения полученной биологически активной генно-терапевтической субстанции в органы и ткани человека, при этом используют кДНК гена GPX3 SEQ ID No: 1, или SEQ ID No: 2, или SEQ ID No: 3, или SEQ ID No: 4, или SEQ ID No: 5, или SEQ ID N0: 6, или SEQ ID No: 7.
5. Способ использования средства для коррекции патологических состояний клеток органов и тканей и/или органов и тканей человека, на основе гена GPX3, связанных с количественным снижением белка GPX3 по п. 1, заключающийся в трансфекции, выбранной именно для данного пациента на основе предварительного эксперимента по определению наиболее эффективного варианта из созданных и представленных в совокупности биологически активных генотерапевтических субстанций, в органы и ткани пациента аутологичных клеток пациента, трансфицированных генно-терапевтической субстанцией, выбранной из совокупности созданных генно-терапевтических субстанций, и/или во введении в органы и ткани пациента генно-терапевтической субстанции или нескольких субстанций, выбранной/выбранных из группы созданных генно-терапевтических субстанций, или сочетанием обозначенных способов.
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| OTTAVIANO FG., et al., Regulation of the extracellular antioxidant selenoprotein plasma glutathione peroxidase (GPx-3) in mammalian cells.Mol Cell Biochem | |||
| Колосоуборка | 1923 |
|
SU2009A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| Колосоуборка | 1923 |
|
SU2009A1 |
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
| LEVINE RM., et al., Preparation and characterization of liposome-encapsulated plasmid DNA for gene delivery.Langmuir | |||
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
| WONG PT., et al., Multivalent dendrimer vectors with DNA intercalation motifs for gene delivery.Biomacromolecules | |||
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| ISHONINA OG., et al., [Comparative characteristics of antioxidant status in women with diabetes type 2 of different age groups].[Article in Russian]Adv Gerontol | |||
| Способ приготовления лака | 1924 |
|
SU2011A1 |
Авторы
Даты
2018-04-23—Публикация
2016-01-20—Подача