ССЫЛКА НА ПРИОРИТЕТНЫЙ ДОКУМЕНТ
[0001] По данной заявке испрашивается приоритет совместно рассматриваемой предварительной патентной заявки США с серийным № 61/719144, озаглавленной «Ophthalmic System for Sustained Release of Drug to Eye», которая подана 26 октября 2012 года. Настоящим претендуют на приоритет даты подачи и, таким образом, раскрытие предварительной патентной заявки включают посредством ссылки в полном объеме.
СВЯЗАННЫЕ ЗАЯВКИ
[0002] Эта заявка связана с (1) публикацией патента США № 2012/0136322, озаглавленной «ANTERIOR SEGMENT DRUG DELIVERY», которая подана 1 июня 2011 года; и (2) публикацией патента США № 2013/0144128, озаглавленной «OCULAR INSERT APPARATUS AND METHODS», которая подана 14 сентября 2012 года, обе включены в настоящий документ посредством ссылки в полном объеме.
ПРЕДПОСЫЛКИ
[0003] В настоящем документе описаны структуры, системы и способы для размещения глазного устройства на глаз, которые можно использовать для лечения глаза. Предоставлены различные реализации глазных устройств, используемых для доставки лекарственного средства, наряду со способами использования глазных устройств, расположенных на или около передней поверхности глаза. Устройства можно носить около передней поверхности глаза за пределами оптической зоны, и они могут доставлять терапевтически эффективные количества одного или нескольких терапевтических средств.
[0004] Различные офтальмологические и неофтальмологические состояния требуют введения различных лекарственных средств в глаз. Глазные капли и гели могут представлять собой эффективные носители для доставки лекарственного средства, но также могут иметь значительные недостатки. В частности, глазные капли смешиваются с текучим веществом в слезной пленке, и могут иметь время пребывания только 2-5 минут в слезной пленке. Может произойти локальная абсорбция всего лишь 5% лекарственного средства; часть или все остальное уносится из слезного мешка в слезный проток, что может иметь потенциально нежелательные эффекты. Следовательно, наибольшая часть лекарственного средства расходуется впустую, причем количества, менее идеальных, доставляют в ткань-мишень (целевую ткань). Также присутствие лекарственного средства в кровотоке может иметь потенциально опасные побочные эффекты. Гели могут более эффективно прилипать к глазу, но также могут замутнить зрение пациента. Как глазные капли, так и гели могут требовать частого повторного нанесения для некоторых видов терапии, и пациенты могут не вводить глазные капли или гели так часто, как указано, по меньшей мере, в некоторых случаях, так что количество доставляемого лекарственного средства может быть меньше идеального. Например, по меньшей мере в некоторых случаях существенное число пациентов может не заполнять свои предписания повторно после одного года, и в некоторых случаях существенное число пациентов может составлять вплоть до пятидесяти процентов. Альтернативы глазным каплям и гелям включают лечение, при котором вставные структуры, которые содержат или которые импрегнированны лекарственными средствами, помещают под веко глаза, в слезную точку или на роговицу, с использованием импрегнированных лекарственным средством контактных линз и т.п.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0005] Сохраняется потребность в усовершенствованной доставке лекарственного средства в глаз, которая имеет менее частое применение пользователем и обеспечивает усовершенствованную регулярность количества лекарственного средства, доставляемого в глаз.
[0006] В одном из аспектов раскрыто глазное устройств, выполненное с возможностью расположения на поверхности глаза по меньшей мере частично под по меньшей мере одним из верхнего и нижнего века глаза и за пределами роговицы глаза для доставки по меньшей мере одного терапевтического средства в глаз в течение продолжительного периода времени. Устройство содержит первую структуру, которая сформирована из первого материала, обеспечивающего первую форму глазного устройства перед расположением глазного устройства на поверхности глаза. Устройство содержит вторую структуру, которая сформирована из второго материала, который имеет трубчатую структуру и просвет, через который проходит первая структура. Второй материал отличается от первого материала. Устройство содержит по меньшей мере одно терапевтическое средство, диспергированное во втором материале второй структуры. Первая форма глазного устройства согласуется со второй, отличающейся форме после расположения глазного устройства на поверхности глаза. При удалении с глаза, глазное устройство сохраняет вторую форму или сменяет ее на третью форму. Третья форма отличается как от первой формы, так и от второй формы.
[0007] Трубчатая структура может иметь форму в поперечном сечении, которая является круглой, линзовидной, в форме восьмерки, подковообразной, овальной, продолговатой, скругленной прямоугольной, в форме звезды или зубчатого колеса. Первую структуру можно термически сплавлять в форму кольца после пронизывания через просвет второй структуры. Вторую структуру можно формировать из второго материала, формованного в две или более трубчатых структуры. Каждая из двух или более трубчатых структур может иметь просвет, через который проходит первая структура. Первую из двух или более трубчатых структур можно формировать с составом (формулировать) для того, чтобы высвобождать по меньшей мере одно терапевтическое средство, и вторую из двух или более трубчатых структур можно формировать с составом для того, чтобы высвобождать по меньшей мере одно терапевтическое средство или второе, отличающееся терапевтическое средство. Первая структура может определить первую форму, вторую форму и третью форму. Вторая форма может представлять собой форму по меньшей мере части конъюнктивы глаза, по меньшей мере части костной орбиты глаза или по меньшей мере часть костной орбиты глаза.
[0008] Глазное устройство может препятствовать отклонению от второй формы при удалении из глаза. Первая форма может представлять собой кольцевую форму, расположенную по существу в первой плоскости, а вторая и третья формы располагают по меньшей мере частично за пределами первой плоскости. Вторая форма может соответствовать поверхности седла. Вторая форма может иметь внешний контур, который соответствует внешнему контуру седла. Глазное устройство может менять первую форму на вторую форму в течение периода приблизительно от 20 минут приблизительно до 24 часов. Первый материал может включать материал, выполненный с возможностью повторно становиться пластичным под воздействием тепла, жидкости или давления. Первый материал может включать термопластичный материал. Первый материал может включать полипропилен. Второй материал может включать силиконовый материал. В некоторых реализациях только второй материал содержит по меньшей мере одно терапевтическое средство.
[0009] По меньшей мере одно терапевтическое средство может включать биматопрост, травопрост, латанопрост, тафлупрост, НПВС, стероид, антигистамин, ингибитор карбонангидразы (CAI), дорзоламид, циклоспорин, антибиотик, доксициклин, тетрациклин, азитромицин, жирную кислоту, длинноцепочечную жирную кислоту, жирный спирт, цетиловый спирт, стеариловый спирт, непроникающий стероид, свободную кислоту стероида, липид, кеторолак, силиконовое масло, олопатадин, простагландин, аналог простагландина, простамид, низкомолекулярный антагонист интегринов, лифитеграст, лотепреднол и фторметалон или их сочетание. По меньшей мере одно терапевтическое средство может включать аналог простагландина. Аналог простагландина может включать по меньшей мере один из биматопроста, латанопроста, травопроста и тафлупроста. По меньшей мере одно терапевтическое средство может быть предназначено для снижения внутриглазного давление в глазу. По меньшей мере одно терапевтическое средство может быть предназначено для лечения сухости глаз. По меньшей мере одно терапевтическое средство может включать по меньшей мере одно из циклоспорина, стероида, лотепреднола, фторметалона, непроникающего стероида, свободной кислоты стероида, нестероидного противовоспалительного средства, кеторолака, низкомолекулярного антагониста интегринов, лифитеграста, доксициклина, азитромицина, липида, жирного спирта, цетилового спирта, стеарилового спирта, жирной кислоты, длинноцепочечной жирной кислоты, масла или силиконового масла. По меньшей мере одно терапевтическое средство может включать стероид. Стероид может включать по меньшей мере один из лотепреднола или фторметалона.
[0010] Во взаимосвязанном аспекте раскрыто глазное устройство, выполненное с возможностью расположения на поверхности глаза по меньшей мере частично под по меньшей мере одним из верхнего и нижнего века глаза и за пределами роговицы глаза для доставки по меньшей мере одного терапевтического средства в глаз в течение продолжительного периода времени. Устройство содержит первую структуру, которая сформирована из первого материала, обеспечивающего первую форму глазного устройства перед расположением глазного устройства на поверхности глаза. Устройство содержит вторую структуру, которая сформирована из второго материала, который имеет трубчатую структуру с просветом, через который проходит первая структура. Второй материал отличается от первого материала. Устройство содержит по меньшей мере одно терапевтическое средство, диспергированное в первом материале первой структуры. Первая форма глазного устройства согласуется со второй, отличающейся формой после расположения глазного устройства на поверхности глаза. При удалении с глаза, глазное устройство сохраняет вторую форму или сменяет ее на третью форму. Третья форма отличается как от первой формы, так и от второй формы.
[0011] Во взаимосвязанном аспекте раскрыт способ изготовления глазного устройства, выполненного с возможностью расположения на поверхности глаза по меньшей мере частично под по меньшей мере одним из верхнего и нижнего века глаза и за пределами роговицы глаза для доставки по меньшей мере одного терапевтического средства в глаз в течение продолжительного периода времени. Способ включает формирование опорной структуры из отрезка первого материала, который имеет область первого конца и область второго конца, первой формы. Первая форма опорной структуры обеспечивает общую форму глазного устройства перед расположением глазного устройства на поверхности глаза. Способ включает диспергирование по меньшей мере одного терапевтического средства во втором материале для того, чтобы создавать матрицу лекарственного средства. Второй материал отличается от первого материала. Способ включает формование трубчатой структуры, которая имеет просвет, из матрицы лекарственного средства. Способ включает нанизывание трубчатой структуры на отрезок опорной структуры так, что опорная структура проходит через просвет трубчатой структуры. Первая форма согласуется со второй, отличающейся формой после расположения глазного устройства на поверхности глаза. При удалении с глаза, глазное устройство сохраняет вторую форму или меняет ее на третью форму. Третья форма отличается как от первой формы, так и от второй формы.
[0012] Способ дополнительно может включать сварку области первого конца отрезка с областью второго конца отрезка после того, как опорную структуру пронизывают через просвет трубчатой структуры. Сварка может включать термическое спаивание областей первого и второго концов вместе. Способ дополнительно может включать горячее формование отрезка первой формы посредством оборачивания отрезка вокруг сердечника, имеющего определенный диаметр. Диаметр может составлять по меньшей мере приблизительно 24 мм, по меньшей мере приблизительно 26 мм или по меньшей мере приблизительно 29 мм. Опорная структура может определять первую форму, вторую форму и третью форму глазного устройства. Первая форма может представлять собой кольцевую форму, расположенную по существу в первой плоскости, а вторую и третью формы располагают по меньшей мере частично за пределами первой плоскости. Глазное устройство может менять первую форму на вторую форму в течение периода приблизительно от 20 минут приблизительно до 24 часов. Первый материал может включать материал, выполненный с возможностью повторно становиться пластичным под воздействием тепла, жидкости или давления. Первый материал может включать термопластичный материал. Первый материал может включать полипропилен. Второй материал может включать силиконовый материал.
[0013] По меньшей мере одно терапевтическое средство может включать биматопрост, травопрост, латанопрост, тафлупрост, НПВС, стероид, антигистамин, ингибитор карбонангидразы (CAI), дорзоламид, циклоспорин, антибиотик, доксициклин, тетрациклин, азитромицин, жирную кислоту, длинноцепочечную жирную кислоту, жирный спирт, цетиловый спирт, стеариловый спирт, непроникающий стероид, свободную кислоту стероида, липид, кеторолак, силиконовое масло, олопатадин, простагландин, аналог простагландина, простамид, низкомолекулярный антагонист интегринов, лифитеграст, лотепреднол и фторметалон или их сочетание. Трубчатая структура может иметь форму сечения, в том числе круглую, линзовидную, в форме восьмерки, подковообразную, овальную, продолговатую, скругленную прямоугольную, в форме звезды или зубчатого колеса. Трубчатая структура может иметь диаметр сечения приблизительно 1 мм.
[0014] Способ дополнительно может включать высвобождение по меньшей мере одного терапевтического средства из матрицы лекарственного средства в глаз. Способ дополнительно может включать диспергирование по меньшей мере второго терапевтического средства во втором количестве второго материала для того, чтобы создавать второе количество матрицы лекарственного средства, и формование по меньшей мере второй трубчатой структуры, которая имеет второй просвет, из второго количества матрицы лекарственного средства. Способ дополнительно может включать нанизывание по меньшей мере второй трубчатой структуры на отрезок опорной структуры так, что опорная структура выходит через второй просвет по меньшей мере второй трубчатой структуры. Способ дополнительно может включать высвобождение по меньшей мере второго терапевтического средства из второго количества матрицы лекарственного средства. По меньшей мере второе терапевтическое средство может представлять собой то же, что и по меньшей мере первое терапевтическое средство. По меньшей мере второе терапевтическое средство может отличаться по меньшей мере от первого терапевтического средства. Матрица лекарственного средства может высвобождать по меньшей мере одно терапевтическое средство в глаз с первой скоростью элюирования, и второе количество матрицы лекарственного средства может высвобождать по меньшей мере второе терапевтическое средство в глаз со второй скоростью элюирования. Первая скорость элюирования и вторая скорость элюирования могут быть одинаковыми или различающимися.
[0015] Другие признаки и преимущества станут видны из следующего описания различных реализаций, которые иллюстрируют, в качестве примера, принципы изобретения.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0016] Эти и другие аспекты подробно описаны со ссылкой на следующие чертежи. Говоря в общем, фигуры не приведены с соблюдением абсолютного или относительного масштаба, а предназначены в качестве иллюстраций. Также относительное расположение признаков и элементов можно модифицировать с целью иллюстративной прозрачности.
[0017] На фиг. 1A представлен разборный вид реализации глазного устройства;
[0018] На фиг. 1B представлен перспективный вид в сборе глазного устройства с фиг. 1A;
[0019] На фиг. 1C представлен детализированный вид глазного устройства с фиг. 1B вдоль круга C;
[0020] На фиг. 1D представлен детализированный вид другой реализации глазного устройства;
[0021] На фиг. 1E представлен вид в поперечном разрезе глазного устройства с фиг. 1B;
[0022] На фиг. 1F представлены примеры формы в поперечном сечении глазных устройств, описанных в настоящем документе;
[0023] На фиг. 2A представлен вид в перспективе другой реализации глазного устройства;
[0024] На фиг. 2B представлен вид спереди глазного устройства с фиг. 2A;
[0025] На фиг. 3 представлена поверхность гиперболического параболоида;
[0026] На фиг. 4 представлен вид спереди дополнительной реализации глазного устройства;
[0027] На фиг. 5 представлен вид сбоку глазного устройства с фиг. 4;
[0028] На фиг. 6 представлен вид сбоку глазного устройства с фиг. 4;
[0029] На фиг. 7 представлен вид спереди другой реализации глазного устройства;
[0030] На фиг. 8 представлен увеличенный вид спереди части глазного устройства на фиг. 7;
[0031] На фиг. 9 представлен вид в перспективе другой реализации глазного устройства;
[0032] На фиг. 10 представлен вид сбоку глазного устройства с фиг. 9;
[0033] На фиг. 11 представлен вид сбоку глазного устройства с фиг. 9;
[0034] На фиг. 12 представлен схематический вид в разрезе для глаза, подходящего для введения глазного устройства;
[0035] На фиг. 13 представлен вид спереди глаза с фиг. 12;
[0036] На фиг. 14 представлен схематический вид сбоку в разрезе для глаза, содержащий конъюнктиву верхнего века и нижнего века;
[0037] На фиг. 15 представлен схематический вид сбоку в разрезе для верхнего века и складок конъюнктивы глаза;
[0038] На фиг. 16 представлена реализация устройства, расположенного на глазу;
[0039] На фиг. 17 представлен разборный вид для реализации устройства и упаковки.
[0040] Следует принимать во внимание, что чертежи в настоящем документе служат только в качестве примера и не выполнены с соблюдением масштаба.
ПОДРОБНОЕ ОПИСАНИЕ
[0041] В настоящем документе описаны различные реализации глазных устройств, которые выполнены с возможностью расположения на внешней, или передней, поверхности глаза для доставки терапевтического вещества в глаз. Глазные устройства, описанные в настоящем документе, объединены с терапевтическим веществом. В связи с этим, глазные устройства выполняют из терапевтического вещества, покрывают им, содержат его или иным образом объединяют с ним, как подробно описано далее. Глазные устройства имеют такие размеры и формы, что устройства выполнены с возможностью расположения на внешней поверхности глаза, причем по меньшей мере часть глазного устройства располагают под одним или обоими веками глаза таким образом, чтобы не контактировать с роговицей или не мешать.
[0042] Глазные устройства, описанные в настоящем документе, имеют такие размеры и формы, что глазное устройство поддерживает себя в целом в фиксированном положении на глазу с тем, чтобы избегать нежелательного движения после расположения на глазу. Глазные устройства можно выполнять многими способами и с возможностью фиксации на месте и/или небольшого движения, когда помещают на глаз, с тем, чтобы предоставить увеличенный комфорт пациенту. Фиксация и/или относительное движение глазных устройств может происходить относительно глазного яблока или относительно анатомической структуры(р), смежных с глазом, например, свода конъюнктивы.
[0043] Как описано далее более подробно, глазные устройства, описанные в настоящем документе, можно формировать in situ. В связи с этим, реализация глазного устройства имеет первую форму перед расположением в глазу. То есть, глазное устройство в обособленном состоянии имеет первую форму. После этого глазное устройство можно располагать на глазу так, что глазное устройство принимает вторую форму, которая отличается от первой формы. В отношении второй формы, можно формовать вторую форму глазного устройства и/или оно может пластически принимать вторую форму. Глазное устройство также можно активировать для того, чтобы оно принимало вторую форму, например, с использованием способности запоминать форму у материала, из которого глазное устройство можно изготавливать по меньшей мере частично. При удалении из глаза, глазное устройство может сохранять вторую форму. То есть, глазное устройство может поддерживать вторую форму, даже после удаления из глаза. Или, при удалении из глаза, глазное устройство может принимать третью форму, которая отличается от первой формы и/или второй формы. Изменение формы может происходить в двух или трех измерениях и может происходить по любой из осей x, y или z относительно глазного устройства.
[0044] В отношении перехода ко второй форме, глазное устройство выполнено с возможностью перехода к форме, которая согласуется с или дополняет форму анатомической структуры самого глаза и/или анатомической структуры вокруг глаза. Например, глазное устройство может соответствовать второй форме, которая соответствует контуру и размерам передней поверхности глаза. В другой реализации глазное устройство может соответствовать второй форме, которая соответствует форме анатомической структуры вокруг глаза или смежно с ним. Такая анатомическая структура может включать, например, веко(и) глаза, складки конъюнктивы, внутренний угол глаза, внешний угол глаза, верхнюю косую мышцу, трахею, слезную железу и т.д.
[0045] Переход от первой формы (за пределами глаза) ко второй форме (расположение на глазу) может происходить в течение определенного периода времени. Например, переход изначально может начинаться в пределах минут, суток или месяцев от момента изначального размещения глазного устройства на глазу. Переход ко второй форме может завершаться в течение периода меньше чем в минуту, одну или несколько минут, периода в сутки или периода в месяцы от момента изначального размещения глазного устройства на глазу, и его можно выбирать для того, чтобы отвечать одному или нескольким требованиям.
[0046] Глазное устройство, подлежащее расположению на глазу, можно выбирать из множества таких глазных устройств, где выбор по меньшей мере частично основан на полном размере глазного устройства по отношению к полному размеру глаза, на котором глазное устройство подлежит расположению, такому как диаметр глаза. В определенной реализации, глазное устройство, находясь в первой форме, имеет максимальный диаметр, который больше максимального диаметра глаза, на котором глазное устройство подлежит расположению.
[0047] Поскольку глазное устройство может соответствовать форме анатомической структуры глаза после имплантации или дополнять ее, не требуются никакие конкретные сведения о форме глаза пациента. Глазные устройства, описанные в настоящем документе, можно подгонять для того, чтобы они подходили к анатомической структуре глаза пациента in situ после размещения устройства на глазу пациента. Глазные устройства, описанные в настоящем документе, можно легко приспосабливать без приложения существенных усилий к анатомической структуре глаза, например, для того, чтобы возвращаться к первой форме перед имплантацией, что может снижать комфорт пациента и вести ощущению пациентом, что устройство находится в определенном положении. Однако глазные устройства, описанные в настоящем документе, не являются настолько мягкими, чтобы врач не мог легко обращаться с ними во время расположения и удаления.
[0048] Глазные устройства
[0049] Далее описано несколько реализаций глазного устройства.
[0050] На фиг. 1A представлен разборный вид, на фиг. 1B представлен вид в сборе, а на фиг. 1E представлен вид в поперечном разрезе для одной реализации глазного устройства 105. Глазное устройство 105 может иметь кольцевую конфигурацию, такая как овальная, круглая или тороидальная, с отверстием 130, которое может иметь размеры и форму для того, чтобы подходить для внешнего диаметра роговицы, когда располагают на передней поверхности глаза. Глазное устройство 105 может содержать одну или несколько корпусных структур 112, выполненных с возможностью окружать, покрывать или соединяться по меньшей мере с частью опорной структуры 135. В некоторых реализациях весь отрезок опорной структуры 135 окружают или покрывают одной или несколькими корпусными структурами 112. В некоторых реализациях опорная структура 135 представляет собой внутреннюю опорную структуру, которая проходит через внутренний канал или просвет 113 одной или нескольких корпусных структур 112 (см. фиг. 1E и фиг. 1F). Просвет 113 может иметь внутренний диаметр, выполненный с возможностью принимать или вмещать опорную структуру 135 так, что опорную структуру 135 можно продевать через просвет 113. Просвет 113, идущий через одну или несколько корпусных структур 112, может быть расположен центрально (так как показано на фиг. 1E) или смещен от центра (так, как в скругленной прямоугольной версии и в версии в форме восьмерки, представленных на фиг. 1F). Кроме того, одна или несколько корпусных структур 112 могут содержать одну или несколько канавок 116 на внешней поверхности так, что опорная структура 135 может быть соединена с или может проходить через канавки 116 одной или нескольких корпусных структур 112 вместо того, чтобы, или в дополнение к тому, чтобы быть продетой через внутренний просвет 113. Независимо от того, расположена ли опорная структура 135 внутри внутреннего просвета 113 или во внешней канавке 116 одной или нескольких корпусных структур 112, по меньшей мере часть одной или нескольких корпусных структур 112 может быть выполнена с возможностью контакта с передней внешней поверхностью глаза, когда глазное устройство 105 располагают на глазу.
[0051] Опорная структура 135 может иметь любые из множества материалов, форм и толщин. Опорная структура 135 может представлять собой материал, не подверженный эрозии, который может определять общую форму устройства 105. Опорная структура 135 может формировать тонкую, удлиненную структуру, которая по жесткости может быть похожа на проволоку и которая может формировать общую форму устройства, например, форму кольца или другую форму. Опорную структуру 135 можно формировать из какого-либо из множества материалов, включая в качестве неограничивающих примеров тонкую металлическую проволоку или проволоки, мононить или группу мононитей, твердую пластмассу, такую как нейлон, PMMA, поликарбонат, полиэтилентерефталат и/или другой полимер, полипропилен или другой синтетический шовный материал, способный обеспечивать структурную опору для устройства 105. В определенной реализации, опорная структура 135 представляет собой проволоку. В другой реализации, опорная структура 135 представляет собой полипропиленовую мононить или группу филаментов, сплавленных вместе терминальными концами для того, чтобы формировать кольцевую структуру. Опорная структура 135 посредством термической усадки может принимать форму кольца или другую форму. Опорная структура 135 может быть способна к активации после того, как глазное устройство 105 вставляют на глаз с тем, чтобы заставлять глазное устройство 105 приспосабливаться in situ. Например, материал опорной структуры можно активировать термически, например, теплом, которое глаз или веки глаза передают вставке. Дополнительные материалы можно рассматривать для одной или нескольких опорных структур 112, как предусмотрено в настоящем документе. Опорная структура 135 может содержать такой покрытый пластиковый или металлический материал, что покрытие содержит терапевтическое средство. Опорная структура 135 может иметь обработку поверхности, такую как плазменное травление или тому подобное, чтобы сделать возможным выполнение подходящего прикрепления к опорной структуре 135, например, такой как одна или несколько корпусных структур 112, как описано более подробно далее.
[0052] Также в отношении фиг. 1A-1E и как указано выше, одна или несколько корпусных структур 112 могут представлять собой трубчатые секции материала, который имеет такой внутренний просвет 113, что опорную структуру 135 можно пронизывать через просвет 113 перед сплавлением концов опорной структуры 135 вместе. В некоторых реализациях, можно формовать и отверждать корпусную структуру 112 конкретной формы, такой как трубчатая форма, которая имеет круглое или другое сечение. На фиг. 1C представлена реализация устройства 105, которое имеет две корпусные структуры 112a, 112b, вдоль круга C с фиг. 1B. Терминальный конец 111a первой корпусной структуры 112a может упираться в терминальный конец 111b второй корпусной структуры 112b. На фиг. 1D представлена другая реализация устройства 105, которое имеет две корпусные структуры 112a, 112b. В этой реализации, терминальные концы 111a, 111b отделяет друг от друга такое расстояние, что определенная область опорной структуры 135 остается обнаженной. Следует принимать во внимание, что в глазное устройство 105 может быть встроена одна корпусная структура 112 или больше чем две корпусные структуры 112.
[0053] Глазные устройства 105 могут иметь любую из множества форм сечения. В некоторых реализациях, устройство 105 и/или одна или несколько корпусных структур 112 могут быть круглыми в сечении, как в реализации, представленной на фиг. 1E. Устройство 105 и/или одна или несколько корпусных структур 112 также могут иметь сечение, которое является не круглым. Например, часть одной или нескольких корпусных структур 112 в контакте с глазом (например, с передней поверхностью глаза) может быть несколько уплощена. На фиг. 1F проиллюстрировано множество других форм сечения, включая круглую, линзовидную, в форме восьмерки, подковообразную, овальную, продолговатую, скругленную прямоугольную, в форме звезды или зубчатого колеса и т.д. В целом, края глазного устройства в сечении могут быть в целом скруглены. Следует принимать во внимание, что форма сечения может варьировать вдоль различных местоположений глазного устройства 105. В некоторых реализациях устройство 105 может иметь толщину в сечении между приблизительно 0,5 мм и до 1 мм. Кроме того, форму сечения можно выбирать для того, чтобы максимизировать или иным образом увеличивать количество площади поверхности глазного устройства 105, как рассмотрено более подробно далее. В некоторых реализациях, опорная структура 135 может иметь диаметр сечения между приблизительно 0,05 мм и приблизительно 0,35 мм, так что внутренний диаметр каждой корпусной структуры 112 может составлять между приблизительно 0,06 мм и приблизительно 0,36 мм, чтобы тем самым вмещать опорную структуру. В некоторых реализациях опорная структура 135 может быть между приблизительно 0,05 мм, 0,07 мм, 0,1 мм, 0,15 мм, 0,2 мм, 0,3 мм или 0,35 мм в диаметре. В некоторых реализациях, опорная структура 135 может представлять собой шовный материал из мононити, который имеет размер между размерами шовного материала приблизительно USP 0, 2-0, 3-0, 4-0, 5-0 или 6-0. Полный диаметр сечения в некоторых реализациях устройства может составлять приблизительно от 0,5 мм приблизительно до 1,5 мм.
[0054] Как указано выше, глазное устройство 105 может быть выполнено с возможностью приспосабливаться или формоваться in situ после расположения на поверхности глаза по конкретной анатомической форме глаза или форме анатомической структуры, окружающей глаз. Это делает возможной подгонку формы устройства “на лету”, что обеспечивает глазное устройство 105 с комфортной посадкой, которая минимизирует или элиминирует раздражение глаза или анатомической структуры, окружающей глаз, с использованием минимальной предварительно существующей информации о форме конкретного глаза пациента. Глазное устройство 105 может иметь начальную предшествующую вставке конфигурацию или форму перед расположением в глазу. Свойства материала опорной структуры 135, отдельно или в комбинации со свойствами материала одной или нескольких корпусных структур 112, могут определять предшествующую вставке форму глазного устройства 105. Можно повторно конфигурировать глазное устройство 105 от начальной, предшествующей вставке формы до второй, следующей за вставкой конфигурации или формы. Предшествующая вставке форма может иметь общую форму, которая является плоской или по существу плоской кольцевой или тороидальной формой. После наложения на поверхность глаза, предшествующая вставке форма может начать меняться в направлении второй, следующей за вставкой формы, например, через пластическую деформацию или тепловую активацию одного или нескольких компонентов глазного устройства 105. Следующая за вставкой форма может включать общую форму, которая в целом приспосабливается или формуется по передней поверхности глаза пациента, а также одному или нескольким компонентам окружающей анатомической структуры глаза, включая по меньшей мере часть конъюнктивы глаза и по меньшей мере часть костной орбиты. По существу, предшествующая вставке конфигурация имеет форму, которая отличается от формы следующей за вставкой конфигурации. Устройство 105 может поддерживать вторую следующую за вставкой конфигурацию даже после того, как устройство 105 удаляют из глаза. Альтернативно, устройство 105 может иметь третью следующую за удалением конфигурацию, которая имеет форму, отличную от одной или обеих из формы предшествующей вставке конфигурации и формы следующей за вставкой конфигурации.
[0055] При удалении с глаза, устройство 105 может препятствовать отклонению от формы конфигурации следующей за вставкой и/или следующей за удалением. Предшествующая вставке форма может представлять собой кольцевую форму, расположенную по существу в плоскости, и следующую за вставкой и/или следующую за удалением формы можно располагать по меньшей мере частично за пределами этой плоскости. В некоторых реализациях, опорная структура 135 может иметь автоматическое сопротивление отклонению, которое находится в пределах диапазона приблизительно от 0,01 Н/мм приблизительно до 1 Н/мм. В дополнительных реализациях опорная структура 135 может иметь первое автоматическое сопротивление отклонению между приблизительно 1 градусом и приблизительно 60 градусами. Автоматическое сопротивление отклонению опорной структуры 135 может включать угол отклонения между первой частью опорной структуры 135 и второй частью опорной структуры 135, когда первая часть имеет опору и удерживается на месте, а вес второй части отклоняет опорную структуру 135. Одну или несколько корпусных структур 112 можно формировать для того, чтобы также иметь автоматическое сопротивление отклонению. Автоматическое сопротивление отклонению одной или нескольких корпусных структур 112 может быть меньше, чем автоматическое сопротивление отклонению опорной структуры 135.
[0056] Устройства, описанные в настоящем документе, могут подвергаться изменению общей формы при расположении на глазу, например, от плоской или по существу плоской кольцевой формы до формы седла, описанной в настоящем документе. Устройство также может подвергаться более локализованным изменениям формы. Например, один или несколько компонентов устройств, описанных в настоящем документе, могут претерпевать изменение формы так, что форма сечения может меняться после имплантации и из-за контакта, образованного с определенной анатомической структурой глаза. Например, одну или несколько корпусных структур 112 можно формировать в целом из мягкого, формуемого материала, который формуют, чтобы он имел круглое сечение. В течение определенного периода времени после нахождения в контакте со структурой глаза, например, со сводом глаза, сечение корпусной структуры 112 может формоваться для того, чтобы более точно отражать или приспосабливаться к форме поверхности структуры глаза, с которой материал находится в контакте. Например, первая часть внешней поверхности корпусной структуры 112, такая как поверхность корпусной структуры 112, обращенная в направлении передней поверхности глаза или бульбарной конъюнктивы 344, может подвергаться локализованному изменению формы после определенного периода времени нахождения в контакте с этой анатомической структурой глаза. Аналогичным образом, вторая часть внешней поверхности корпусной структуры 112, такая как поверхность корпусной структуры 112, обращенная в направлении конъюнктивы 342 века на веке глаза, также может подвергаться локализованному изменению формы после определенного периода времени нахождения в контакте с этой анатомической структурой глаза. В некоторых реализациях, локализованное изменение формы частей внешней поверхности может быть от выпуклой сферической формы до вогнутой сферической формы. Форма сечения одной или нескольких корпусных структур 112 может меняться от круглой формы до линзовидной формы. В другой реализации, форма сечения одной или нескольких корпусных структур 112 может меняться от круглой формы до формы в форме восьмерки. В другой реализации, форма сечения одной или нескольких корпусных структур 112 может менять от круглой формы до формы конской подковы. Следует принимать во внимание, что внешняя поверхность корпусной структуры 112 может принимать или приспосабливаться к какой-либо из множества локальных форм в зависимости от формы структур глаза, с которыми внешняя поверхность корпусной структуры 112 образует контакт. Таким образом, устройства, описанные в настоящем документе, могут претерпевать изменение общей формы in situ, определяемое, в первую очередь, свойствами материала опорной структуры 135. Устройства, описанные в настоящем документе, также могут подвергаться локализованному изменению формы in situ, определяемому, в первую очередь, свойствами материала одной или нескольких корпусных структур 112. Конформация формы устройств, описанных в настоящем документе, по анатомической структуре глаза как в крупном масштабе, так и в локальном масштабе, вносит вклад в комфорт и удерживание устройства в глазу, которые испытывает пациент.
[0057] Как указано выше, глазные устройства, описанные в настоящем документе, могут содержать или могут быть связаны с одним или несколькими терапевтическими средствами с тем, чтобы высвобождать безопасное и терапевтически эффективное количество лекарственного средства(в) в глаз при имплантации в течение определенного периода времени. В некоторых реализациях, лекарственное средство диффундирует из силиконовой матрицы лекарственного средства по типу замедленного высвобождения через элюирование лекарственного средства. Высвобождение лекарственного средства из устройства может происходить любым из множества путей и не должно быть ограничено конкретным химическим механизмом или составом для высвобождения и введения лекарственного средства в глаз. Например, глазные устройства, описанные в настоящем документе, могут высвобождать лекарственное средство в глаз посредством элюирования лекарственного средства, диффузии лекарственного средства, биологического разложения, контролируемого высвобождения, замедленного высвобождения и т.п. В связи с этим, глазному устройству 105 можно придавать форму для получения большего или меньшего количества площади поверхности с тем, чтобы получать желаемый профиль высвобождения лекарственного средства. Например, увеличение площади поверхности одной или нескольких корпусных структур 112 может обеспечивать более высокий уровень высвобождения лекарственного средства для глазного устройства 105. В связи с этим, площадь поверхности в одном или нескольких конкретных местоположениях глазного устройства 105 можно выбирать для того, чтобы увеличивать, уменьшать или иным образом настраивать степень высвобождения лекарственного средства из конкретной области(ей) глазного устройства 105 по сравнению с другими областями глазного устройства 105. Это позволяет глазному устройству 105 иметь степень высвобождения в одном местоположении глазного устройства 105, которая отличается от степени высвобождения в другом местоположении глазного устройства 105.
[0058] Устройства, описанные в настоящем документе, можно формулировать для того, чтобы достигать различных целей высвобождения лекарственного средства. Например, устройства, описанные в настоящем документе, могут содержать лекарственное средство (такое как, например, внутри корпусной структуры 112), подлежащее высвобождению при конкретной степени высвобождения для того, чтобы получать первую дозу лекарственного средства в глазу. Устройства, описанные в настоящем документе, также могут содержать первое лекарственное средство в первом составе, такое как, например, в первой корпусной структуре 112, и первое лекарственное средство во втором составе, такое как, например, во второй корпусной структуре 112. Например, первый состав лекарственного средства может предусматривать более высокую дозу лекарственного средства, высвобождаемого в течение первого периода времени, и второй состав лекарственного средства может предусматривать более низкую дозу лекарственного средства, высвобождаемого в течение второго более длительного периода времени. Кроме того, устройства, описанные в настоящем документе, могут содержать первое лекарственное средство в первом составе и второе лекарственное средство во втором составе, что делает возможным единственное устройство для того, чтобы доставлять два (или больше, чем два) лекарственных средства одновременно. Например, устройство 105 может содержать первую корпусную структуру 112, которая содержит первое лекарственное средство, и вторую корпусную структуру 112, которая содержит второе лекарственное средство, и третью корпусную структуру 112, которая содержит третье лекарственное средство, и т.д. Также следует принимать во внимание, что устройства, описанные в настоящем документе, можно формулировать так, что единственная корпусная структура 112 (или другой компонент устройства) доставляет больше, чем одно лекарственное средство. Кроме того, следует принимать во внимание, что компоненты устройства, отличные от одной или нескольких корпусных структур 112, могут содержать лекарственное средство. Например, опорная структура 135 может быть выполнена с возможностью содержать лекарственное средство для высвобождения в глаз. Существуют различные пути, которыми устройства, описанные в настоящем документе, можно разрабатывать для того, чтобы получать определенный профиль высвобождения при доставке лекарственного средства, представляющий интерес. Одна или несколько корпусных структур 112, в частности, позволяют адаптировать лечение в соответствии с любой из множества комбинаций доз, степеней высвобождения и терапевтических средств, представляющих интерес.
[0059] Терапевтическое средство можно помещать на, встраивать, инкапсулировать или иным образом внедрять в матрицу для доставки. Матрица для доставки может содержаться в или на опорной структуре 135 или одной или нескольких корпусных структурах 112, или и там и там. Матрица для доставки, в свою очередь, может содержать биоразрушаемый или небиоразрушаемый материал. Матрица для доставки может содержать, несмотря на то, что не ограничена этим, полимер. Примеры биоразрушаемых полимеров включают белок, гидрогель, полигликолевую кислоту (PGA), полимолочную кислоту (PLA), поли(L-молочную кислоту) (PLLA), поли(L-гликолевую кислоту) (PLGA), полигликолид, поли-L-лактид, поли-D-лактид, поли(аминокислоты), полидиоксанон, поликапролактон, полиглюконат, сополимеры полимолочной кислоты-полиэтиленоксида, модифицированную целлюлозу, коллаген, сложные полиортоэфиры, полигидроксибутират, полиангидрид, полифосфоэфир, поли(α-оксикислоту) и их сочетания. Небиоразрушаемые полимеры могут включать силикон, NuSil Med 4810, силикон MED-4830, силиконовый материал, акрилаты, полиэтилены, полиуретан, полиуретан, гидрогель, сложный полиэфир (например, DACRON® из E. I. Du Pont de Nemours and Company, Wilmington, Del.), полипропилен, политетрафторэтилен (PTFE), вспененный PTFE (ePTFE), полиэфирэфиркетон (PEEK), нейлон, экструдированный коллаген, полимерную пену, силиконовый каучук, полиэтилентерефталат, ультравысокомолекулярный полиэтилен, поликарбонат уретан, полиуретан, полиимиды, нержавеющую сталь, никель-титановый сплав (например, Nitinol), титан, нержавеющую сталь, кобальт-хромовый сплав (например, ELGILOY® из Elgin Specialty Metals, Elgin, Ill.; CONICHROME® из Carpenter Metals Corp., Wyomissing, Pa.). В некоторых реализациях матрица для доставки представляет собой материал матрицы для замедленной доставки лекарственного средства из Ocular Therapeutix (Bedford, MA), в котором используют технологию гидрогелей, которые разрушаются с течением времени, высвобождая лекарственное средство, диспергированное в них. В определенной реализации, одну или несколько корпусных структур 112 можно формировать из матрицы для доставки, такой как силикон, в которой одно или несколько терапевтических средств можно диспергировать или примешивать в матрицу перед формованием и отверждением. В определенной реализации формованный силикон может иметь показания дюрометра в диапазоне приблизительно от 10 по Шору А приблизительно до 80 по Шору А. В некоторых реализациях, дюрометр показывает между силиконом 30 по Шору А и силиконом 50 по Шору А.
[0060] Следует принимать во внимание, что реализации глазных устройств, описанных и представленных на чертежах, являются примерами. Глазные устройства могут варьировать по форме, материалам и конфигурациям относительно того, что представлено. Например, глазные устройства, описанные в настоящем документе, не должны быть кольцевыми, но могут формировать лишь часть кольца. Например, глазные устройства по существу могут иметь форму буквы U или C. Также следует принимать во внимание, что глазные устройства, описанные в настоящем документе, могут содержать две или более отдельных структуры, которые совместно образуют глазное устройство 105. Однако, глазные устройства, описанные в настоящем документе, также могут представлять собой монолитные структуры, которые изготавливают из одного материала или комбинации материалов, при этом все еще обеспечивающих функциональные возможности доставки лекарственного средства и конформации формы.
[0061] Далее, на фиг. 2A и 2B представлена другая реализация глазного устройства 105. Как и в случае предыдущей реализации, глазное устройство 105 может иметь кольцевую конфигурацию, такую как овальная, круглая или тороидальная форма, с отверстием 130, которое может иметь размеры и форму для того, чтобы подходить снаружи к диаметру роговицы при расположении на глазу. Несмотря на то, что отверстие 130 может иметь размеры для того, чтобы минимизировать контакт с роговицей и/или ее повреждение, когда глазное устройство располагают на глазу, следует принимать во внимание, что глазное устройство 105 может иногда контактировать с роговицей, например, когда пациент смотрит вбок. Устройство 105 может содержать опорную структуру 135 (представленную штриховой линией), соединенную с корпусной структурой, расположенной вдоль всей опорной структуры 135 или вдоль ее части. Глазное устройство 105 может содержать внешнюю поверхность 110, а также внутреннюю поверхность 115, которая непосредственно контактирует с передней внешней поверхностью глаза, когда глазное устройство 105 располагают на глазу. Кроме того, глазное устройство 105 может содержать передний край 120, который ограничивает или окружает отверстие 130 глазного устройства 105. Задний край 125 может определять самый внешний контур глазного устройства 105. Каждый из заднего края 125 и переднего края 120 может определять схожую форму, например, круглую форму. Альтернативно, задний край 125 и передний край 120 могут иметь различные формы, например, передний край 120 может быть круглым, а задний край 125 может быть овальным или иметь некоторую другую форму. Отверстие 130 глазного устройства 105 может располагаться по центру или может быть смещено относительно центра устройства 105. В целом, однако, отверстие 130 предусматривает, что передний край 120 устройства остается за пределами оптической зоны глаза.
[0062] Также на фиг. 2A и 2B глазное устройство 105 в целом может содержать четыре области, в том числе носовую область NR, височную область TR, верхнюю область SR и нижнюю область IR. Носовая область NR в целом выполнена с возможностью расположения на носовой области глаза и височная область TR выполнена с возможностью расположения на височной области глаза. Аналогичным образом, верхняя область SR выполнена с возможностью расположения на верхней области глаза, тогда как нижняя область IR выполнена с возможностью расположения на нижней области глаза. Области NR, SR, TR и IR глазного устройства могут иметь конкретные размеры и форму для того, чтобы взаимодействовать с соответствующими областями глаза с тем, чтобы добиваться фиксации на глазу при минимальном раздражении глаза или без него. В связи с этим, заднему краю 125, который определяет внешний контур глазного устройства 105, можно придавать размеры и форму так, что каждая из областей идет на желаемое расстояние в заднем направлении вдоль внешней поверхности глаза, как описано более полно далее. Кроме того, области глазного устройства могут варьировать по геометрии, размеру, толщине, ширине и т.д. по отношению друг к другу. Любая одна из областей может содержать вырез или другую неровность поверхности.
[0063] Как указано выше, форма устройств, описанных в настоящем документе, может варьировать. В некоторых реализациях, форма глазного устройства 105 может варьировать, исходя из того, подлежит ли глазное устройство 105 расположению на правом глазу или на левом глазу. Области NR, SR, TR и IR не обязательно имеют аналогичные формы по сравнению друг с другом. Наоборот, области могут иметь различные формы и могут содержать один или несколько выступов, которые выполнены с возможностью увеличивать вероятность естественного удержания глазного устройства 105 на глазу в течение продолжительного периода времени.
[0064] В реализации с фиг. 2A и 2B, носовая область NR переднего края 120 имеет такую форму, что расстояние между передним краем 120 и задним краем 125 в целом уменьшено по отношению к остальной части глазного устройства 105. Другими словами, глазное устройство 105 имеет уменьшенную площадь поверхности в носовой области NR для реализации с фиг. 2A и 2B. Кроме того, височная область глазного устройства 105 может идти дальше в заднем направлении, чем остальная часть глазного устройства.
[0065] Задний край 125 может иметь форму, которая выполнена с возможностью удерживать глазное устройство 105 в относительно фиксированном положении при размещении на глазу с тем, чтобы уменьшать вероятность вращения или какого-либо другого движения глазного устройства 105 относительно глаза. В определенной реализации, задний край определяют поверхностью правильного или неправильного седла или гиперболического параболоида. На фиг. 3 представлена поверхность гиперболического параболоида 705. Контур 710 определяют посредством поверхности 705, и этот контур 710 может соответствовать контуру заднего края 125 реализации глазного устройства, такой как реализация с фиг. 2A и 2B. Поверхность 705 и/или контур 710 может иметь или может не иметь симметрию относительно оси x и y. Например, форма и/или контур может варьировать, исходя из того, располагают ли глазное устройство на левом глазу или на правом глазу. Следует принимать во внимание, что любые из реализаций глазного устройства 105, описанные в настоящем документе, могут иметь контур, который соответствует или по существу соответствует контуру 710, представленному на фиг. 3.
[0066] Как описано выше в отношении устройства, представленного на фиг. 1A-1E, любые реализации глазного устройства 105 можно деформировать, приспосабливать и/или формовать так, что общую форму устройства 105 сменяет in situ форма внешней поверхности глаза или окружающей анатомической структуры при размещении на глазу. Также со ссылкой на фиг. 3, глазные устройства 105 могут иметь такую достаточную жесткость, что задний край 125 приспосабливается к поверхности гиперболического параболоида, даже когда глазное устройство 105 не располагают на глазу, например, перед расположением на глазу или после удаления из глаза. Таким образом, в обособленном состоянии, задний край 125 глазного устройства 105 может приспосабливаться к поверхности гиперболического параболоида. В другой реализации, глазное устройство не приспосабливается к такой форме перед расположением на глазу. В такой реализации, глазное устройство может быть плоским или по существу плоским перед расположением на глазу. После этого может происходить пластическая деформация глазного устройства или его можно активировать для того, чтобы деформировать до другой формы после расположения на глазу в течение определенного периода времени. Следует принимать во внимание, что любые устройства, описанные в настоящем документе, можно реконфигурировать in situ от начальной, предшествующей вставке конфигурации до второй, следующей за вставкой конфигурации. Кроме того, эту следующую за вставкой конфигурацию можно сохранять даже после того, как устройство удаляют из глаза. Альтернативно, устройство может подвергаться дальнейшему изменению формы при удалении из глаза так, что оно принимает следующую за удалением конфигурацию, которая может представлять собой ту же или отличающуюся от предшествующей вставке конфигурации или следующей за вставкой конфигурации.
[0067] На фиг. 4, 5 и 6 представлена другая реализация глазного устройства 105. На фиг. 4 представлен вид спереди глазного устройства 105, тогда как на фиг. 5 и 6 представлен вид сбоку. Глазное устройство 105 может иметь в целом круглую форму, когда смотрят спереди, такую как овальная форма. Форму можно определять с помощью длинной оси L и короткой оси S. Как отмечено, форма может варьировать и она не обязана соответствовать овалу или кругу. Кроме того, глазное устройство может быть симметричным или асимметричным относительно длинной или короткой оси.
[0068] Как показано в виде сбоку на фиг. 5 и 6, глазное устройство 105 имеет такую форму, что оно выполнено с возможностью расположения на сферической или по существу сферической внешней поверхности глаза. Со ссылкой на фиг. 4, глазное устройство 105 может иметь пару увеличенных или расширенных областей, которые формируют клапаны 810 с увеличенной площадью поверхности, которые в целом располагают вдоль длинной оси L глазного устройства 105, хотя их положения можно варьировать. Клапаны 810 могут определять большую площадь поверхности, чем узкие области 815, которые в целом распложены вдоль короткой оси S глазного устройства 105. В реализации с фиг. 4-6, клапаны 810 могут постепенно сужаться или уменьшаться в размере, если идти от местоположения длинной оси L в направлении местоположения короткой оси S. Следует принимать во внимание, что переход размера при движении от клапанов 810 к относительно маленьким областям 815 может быть менее постепенным или может быть внезапным. Кроме того, конкретная форма клапанов 810, а также угол клапанов относительно оси, перпендикулярной к плоскости с фиг. 4, может варьировать для того, чтобы корректировать площадь поверхности клапанов, посадку на глазу, удержание и т.д.
[0069] На фиг. 7 представлена другая реализация глазного устройства 105. Если смотреть спереди, глазное устройство 105 может содержать в целом круглый корпус 1105, который образует круг, эллипс или другую кольцевую форму. По меньшей мере одну увеличенную область, такую как клапан 1110, можно располагать на корпусе 1105. Клапан 1110 может иметь любую из множества форм. В целом, клапан 1110 может иметь увеличенную толщину или ширину относительно локальной области корпуса 1105, где расположен клапан 1110.
[0070] В определенной реализации, каждый из клапанов 1110 расположен на определенном угловом расстоянии от другого клапана 1110, например, приблизительно 180 градусов, хотя относительные положения клапанов могут варьировать. Дополнительно может варьировать число клапанов 1110, включая 1, 2, 3, 4 или больше клапанов 1110. Каждый клапан 1110 необязательно содержит наружную область 1205, которая идет наружу относительно корпуса 1105. Каждый клапан также необязательно содержит внутреннюю область 1210, которая идет внутрь в направлении отверстия 130 корпуса 1105. Клапаны 1110 имеют размеры и формы для расположения на внешней, сферической поверхности глаза. Размер и форма, а также относительные положения клапанов 1110 можно выбирать для того, чтобы достигать желаемого профиля посадки, площади поверхности, удержания и т.д. Как отмечено, может варьировать форму реализации с фиг. 7. Например, корпус 1105 может иметь неправильную форму и может соответствовать контуру 710 с фиг. 3. Глазное устройство 105 также может содержать только корпус 1105 без клапанов 1110.
[0071] На фиг. 8 представлен увеличенный вид спереди для реализации одного из клапанов 1110. Как рассмотрено, клапаны 1110 могут содержать наружную область 1205 и внутреннюю область 1210. В проиллюстрированной реализации области 1205 и 1210 имеют по существу прямоугольную форму с закругленными краями, хотя следует принимать во внимание, что форма может варьировать. Поверхность клапана 1110 может содержать одно или несколько выпячиваний, которые выполнены с возможностью увеличения площади поверхности клапана 1110. Или клапан 1110 может иметь плоскую внешнюю поверхность. Кроме того, внутренняя область 1210 клапанов 1110 может иметь геометрию поверхности, которая соответствует поверхности сферы, как показано на фиг. 8.
[0072] На фиг. 9 представлен вид в перспективе еще одной другой реализации глазного устройства 105, которое имеет в целом кольцеобразный корпус 1305. На фиг. 10 и 11 представлен вид сбоку глазного устройства 105 с фиг. 9. Корпус 1305 можно формировать из тонкой кольцевой полосы, которая имеет в целом цилиндрическую внешнюю поверхность. Корпус 1305 может иметь пару клапанов 1310, которые могут идти под углом относительно плоскости, определяемой кругом корпуса 1305. Как показано на фиг. 10 и 11, клапаны 1310 могут находиться под углом 90 к плоскости корпуса 1305, хотя угол клапанов 1310 может варьировать. Клапаны 1310 могут быть ступенчатыми или зауженными по ширине относительно ширины корпуса 1305. Например, центральная область каждого клапана 1310 может быть шире, чем каждая из сторон, ограничивающих центральную область каждого клапана 1310. Сужение может быть постепенным или внезапным с тем, чтобы формировать одну или несколько ступенек в форме клапанов 1310.
[0073] Любая из реализаций устройств, описанных в настоящем документе, также может содержать один или несколько тактильных элементов, идущих радиально от структуры в форме кольца. Тактильные элементы также могут содержать по меньшей мере одно или несколько терапевтических средств.
[0074] Материалы и терапевтические средства
[0075] Глазными устройствами, описанными в настоящем документе, можно манипулировать относительно легко во время установки в глаз, а также удаления из глаза, при этом все еще делая возможно конформацию и формование in situ при имплантации на глаз для увеличенного комфорта и удержания на глазу.
[0076] Различные материалы могут вызывать изменение формы, описанное в настоящем документе. Один или несколько компонентов устройств, описанных в настоящем документе, можно формировать из множества материалов или встраивать их, таких как те, которые описаны в настоящем документе. Как указано выше, опорная структура 135 может вызывать изменение формы устройства. Опорную структуру 135 можно формировать из материала, обеспечивающего общую форму глазного устройства перед расположением устройства на поверхности глаза. Опорная структура 135 может определять форму устройства, когда устройство находится вне глаза перед имплантацией, форму устройства, которая соответствует in situ, а также форму устройства после удаления приспособленного устройства из глаза. Следует принимать во внимание, что изменение формы может происходить в течение различных периодов времени, например, от минут до периода в сутки или месяцы. В некоторых реализациях конформация формы от первой формы перед имплантацией на глаз до второй формы после имплантации на глаз происходит в течение периода приблизительно от 20 минут приблизительно до 24 часов.
[0077] Опорную структуру 135 можно формировать из одного или нескольких различных материалов, включая металлическую проволоку, нить или группу нитей, мононить, твердую пластмассу, такую как нейлон, PMMA, поликарбонат, полиэтилентерефталат и/или другой полимер, полипропилен или другой синтетический шовный материал или комбинации одного или нескольких указанных выше. Примеры материалов, которые могут растягиваться через пружинное действие, также рассматривают в настоящем документе для одного или нескольких компонентов устройства, в том числе платиновые сплавы, титановые сплавы, все сплавы нержавеющей стали и закаленные сплавы, различные плакированные металлы и изолированные провода. Глазное устройство можно по меньшей мере частично выполнять из материала с памятью формы. В неограничивающем примере можно использовать Nitinol, который позволит глазному устройству осуществлять смену на желаемую форму с использованием тепловой, магнитной или электромагнитной активации, из мартенситного в аустенитное состояние. Можно использовать другие примеры материалов с памятью формы, включая, например, полиуретаны с памятью формы, сшитый транс-полиоктиленовая резина, полинорборненовые полимеры, Nitinol, полиэтилен, PMMA, полиуретан, сшитый полиэтилен, сшитый полиизопрен, полициклооцетен, поликапролактон, сополимеры (олиго)капролактона, PLLA, сополимеры PL/DLA, сополимеры PLLA PGA, термопластические полимеры, такие как PEEK, сшитые блок-сополимеры полиэтилентерефталата (PET) и полиэтиленоксида (PEO), блок-сополимеры, содержащие полистирол и поли(1,4-бутадиен), и другие материалы памятью формы, общеизвестные специалистам в данной области. Материал также может представлять собой любой материал, выполненный с возможностью повторно становиться пластичным под воздействием тепла, жидкости и/или давления и затвердевать при охлаждении, высыхании и/или снятии давления.
[0078] В определенной реализации, одно или несколько глазных устройств, описанных в настоящем документе, могут расширяться по мере поглощения текучего вещества из слезной жидкости в глазу или могут растягиваться по механизму пружинного действия. Примеры материалов, которые могут набухать при установке в глазу, включают PVPE, PVA, полиуретановые гели и гидрогели других типов. Один или несколько компонентов устройств, описанных в настоящем документе, таких как опорная структура и/или корпусная структура, также можно формировать из одного или нескольких из множества материалов, в том числе биоразрушаемых или небиоразрушаемых материалов, таких как силикон. Терапевтическое средство можно помещать на, встраивать, инкапсулировать или иным образом внедрять в матрицу для доставки. Матрица для доставки, в свою очередь, может содержать или биоразрушаемый или небиоразрушаемый материал. Матрица для доставки может содержать, несмотря на то, что она не ограничен этим, полимер. Примеры биоразрушаемых полимеров включают белок, гидрогель, полигликолевую кислоту (PGA), полимолочную кислоту (PLA), поли(L-молочную кислоту) (PLLA), поли(L-гликолевую кислоту) (PLGA), полигликолид, поли-L-лактид, поли-D-лактид, поли(аминокислоты), полидиоксанон, поликапролактон, полиглюконат, сополимеры полимолочной кислоты-полиэтиленоксида, модифицированную целлюлозу, коллаген, сложные полиортоэфиры, полигидроксибутират, полиангидрид, полифосфоэфир, поли(α-оксикислоты) и их сочетания. Небиоразрушаемые полимеры могут включать силикон, силикон MED-4830, силиконовый материал, акрилаты, полиэтилены, полиуретан, полиуретан, гидрогель, сложный полиэфир (например, DACRON® из E. I. Du Pont de Nemours and Company, Wilmington, Del.), полипропилен, политетрафторэтилен (PTFE), вспененный PTFE (ePTFE), полиэфирэфиркетон (PEEK), нейлон, экструдированный коллаген, полимерную пену, силиконовый каучук, полиэтилентерефталат, ультравысокомолекулярный полиэтилен, поликарбонат уретан, полиуретан, полиимиды, нержавеющую сталь, никель-титановый сплав (например, Nitinol), титан, нержавеющую сталь, кобальт-хромовый сплав (например, ELGILOY© из Elgin Specialty Metals, Elgin, Ill.; CONICHROME® из Carpenter Metals Corp., Wyomissing, Pa.). В некоторых реализациях, матрица для доставки представляет собой материал матрицы для замедленной доставки лекарственного средства из Ocular Therapeutix (Bedford, MA), в котором используют технологию гидрогелей, которые разрушаются, с течением времени высвобождая лекарственное средство, диспергированное в нем. Устройства, описанные в настоящем документе, также могут содержать материал, который может изменять степень высвобождения лекарственного средства в глаз из устройства, в том числе материал, изменяющий скорость элюирования.
[0079] Для того чтобы предотвращать у пациента потенциальную аллергическую реакцию на глазное устройство, глазное устройство может содержать гипоаллергенный материал. Один или несколько компонентов устройств, описанных в настоящем документе, таких как опорная структура и/или корпусная структура, могут содержать материалы, такие как гидрогели, полиэтиленгликоль (PEG) или полиэтиленоксид (PEO), которые предотвращают адгезию белков и, таким образом, минимизируют вероятность развития аллергической реакции. Альтернативно, матрица для доставки лекарственного средства глазного устройства может содержать противоаллергенное и/или антигистаминное соединение для того, чтобы предотвращать аллергическую реакцию на глазное устройство. В определенных реализациях, матрица для доставки также может содержать другие материалы, известные в данной области. Глазное устройство также можно выполнять с возможностью уменьшения слизи.
[0080] Следует принимать во внимание, что эти материалы предоставлены в качестве примеров и не предназначены в качестве ограничения или полного списка материалов, выполненных с возможностью обеспечения изменения формы устройств и/или высвобождения лекарственного средства устройствами, описанными в настоящем документе.
[0081] В таблице 1 представлены примеры терапевтических средств, пригодных для использования с глазными устройствами, описанными в настоящем документе. Терапевтические средства можно использовать различными путями, и они могут включать одно или несколько из множества доставляемых терапевтических средств.
Неограничивающие примеры показаний и терапевтических средств
Стероид (например, лотепреднол, фторметалон)
Непроникающий стероид (например, свободные кислоты стероидов)
Нестероидные противовоспалистельные средства (например, кеторолак)
Низкомолекулярные антагонисты интегринов (например, лифитеграст)
Доксициклин или азитромицин
Нефармакологические средства (например, липид)
Жирный спирт (например, цетиловый спирт или стеариловый спирт)
Жирная кислота (например, длинноцепочечная жирная кислота)
Масло (например, силиконовое масло)
Антигистамин
Стероид (например, лотепреднол, фторметалон)
Нефармакологическое средство (например, липид)
Жирный спирт (например, цетиловый спирт или стеариловый спирт)
Жирная кислота (например, длинноцепочечная жирная кислота)
Масло (например, силиконовое масло)
[0082] Альтернативно или в комбинации с терапевтическими средствами в таблице 1 терапевтическое средство может включать одно или несколько из следующего: средство для снижения внутриглазного давления глаза, лекарственные средства против глаукомы, (например, адренергические агонисты, адренергические антагонисты (β-блокаторы), ингибиторы карбонангидраз (CAI, системные и местные), парасимпатомиметики, простагландины и гипотензивные липиды, а также их сочетания), противомикробные средства (например, антибиотик, противовирусное средство, антипаразитарное средство, противогрибковое средство и т.д.), кортикостероид или другое противовоспалительное средство (например, НПВС), противозастойное средство (например, сосудосуживающее средство), средство, которое предотвращает или модифицирует аллергический ответ (например, антигистамин, ингибитор цитокина, ингибитор лейкотриена, ингибитор IgE, иммуномодулирующий стабилизатор тучных клеток, мидриатик или тому подобное. Примеры состояний, которые можно лечить терапевтическим средством(ами), включают, но не ограничиваясь этим, глаукому, лечение до и после хирургического вмешательства, сухость глаз и аллергию. В некоторых реализациях терапевтическое средство может включать смазывающее средство или поверхностно-активное вещество, например, смазывающее средство для того, чтобы лечить сухость глаз.
[0083] Терапевтическое средство может включать аналог простагландина, подходящий для лечения глаукомы, как описано в настоящем документе. Аналог простагландина может включать, например, один или несколько из латанопроста (XALATAN®), биматопроста (LUMIGAN® или LATISSE®), карбопроста, унопростона, простамида, траватана, травопроста или тафлупроста. Терапевтическое средство также может включать стероид, антибиотик, нестероидное средство или «НПВС», лотепреднол, циклоспорин, дексаметезон, дипивефрин, олопатадин, эмедастин, антигистамин, моксифлоксацин, натамицин, противогрибковое средство, полимиксин, неомицин, непафенак, триамцинолон ацетонид, тобрамицин, преднизолон, римексолон, фторметолон, лодоксамид трометамин, лифлупреднат, бринзоламид, метипранолол, тимолол, апроклонидин, карбахол, пилокарпин, циклопентат, атропин, бетаксолол, бримонидин, недокромил, эпинастин, алкафтадин, кеторолак, лифитеграст, преднизолон, гатифлоксацин, бепотастин, бесифлоксацин, бромфенак, флуоцинолон, ганцикловир, тобрамицин, гидроксипропил целлюлозу, азитромицин, дорзоламид, левофлоксацин, офлоксацин, буназозин, унопростон, левокабастин, гиалуронат натрия, диквафозол, фторметолон, пиреноксин или латанопростин бунод.
[0084] Терапевтическое средство может включать одно или несколько из следующего или их эквиваленты, производные или аналоги: ингибиторы тромбина; антитромбогенные средства; тромболитические средства; фибринолитические средства; ингибиторы вазоспазма; сосудорасширяющие средства; антигипертензивные средства; противомикробные средства, такие как антибиотики (такие как тетрациклин, хлортетрациклин, бацитрацин, неомицин, полимиксин, грамицидин, цефалексин, окситетрациклин, хлорамфеникол, рифампицин, ципрофлоксацин, тобрамицин, гентамицин, эритромицин, пенициллин, сульфонамиды, сульфадиазин, сульфацетамид, сульфаметизол, сульфизоксазол, нитрофуразон, пропионат натрия), противогрибковые средства (такие как амфотерицин B и миконазол), и противовирусные средства (такие как идоксуридин трифтортимидин, ацикловир, ганцикловир, интерферон); ингибиторы поверхностных гликопротеиновых рецепторов; антитромбоцитарные средства; антимитотические средства; ингибиторы микротрубочек; антисекреторные средства; активные ингибиторы; ингибиторы ремоделирования; антисмысловые нуклеотиды; антиметаболиты; антипролиферативные средства (включая средства против ангиогенеза); химиотерапевтические средства против злокачественных опухолей; противовоспалительные средства (такие как гидрокортизон, гидрокортизона ацетат, дексаметезон 21-фосфат, флуоцинолон, медризон, метилпреднизолон, преднизолон 21-фосфат, преднизолон ацетат, фторметалон, бетаметазон, триамцинолон, триамцинолон ацетонид); нестероидные противовоспалительные средства (НПВС) (такие как салицилат, индометацин, ибупрофен, диклофенак, флурбипрофен, пироксикам индометацин, ибупрофен, наксопрен, пироксикам и набуметон). Противовоспалительные стероиды, предусмотренные для использования в реализациях описанных здесь способов, включают кортикостероиды, например, триамцинолон, дексаметезон, флуоцинолон, кортизон, преднизолон, флуметолон, лотепреднол и их производные); противоаллергические средства (такие как кромогликат натрия, антазолин, метаприллин, хлорфенирамин, цетиризин, пириламин, профенпиридамин); антипролиферативные средства (такие как 1,3-цис-ретиноевая кислота, 5-фторурацил, таксол, рапамицин, митомицин C и цисплатин); противозастойные средства (такие как фенилэфрин, нафазолин, тетрагидразолин); миотики и антихолинэстеразные средства (такие как пилокарпин, салицилат, карбахол, ацетилхолина хлорид, физостигмин, эзерин, диизопропил фторфосфат, фосфолин йод, демекарийбромид); антинеоплатические средства (такие как кармустин, цисплатин, фторурацил3; иммунологические лекарственные средства (такие как вакцины и иммуностимуляторы); гормональные средства (такие как эстрогены, эстрадиол, прогестативные средства, прогестерон, инсулин, кальцитонин, паратиреоидный гормон, пептидный и вазопрессиновый гипоталамический рилизинг-фактор); иммуносупрессорные средства, антагонисты гормона роста, факторы роста (такие как эпидермальный фактор роста, фактор роста фибробластов, тромбоцитарный фактор роста, трансформирующий фактор роста β, соматотропин, фибронектин); ингибиторы ангиогенеза (такие как ангиостатин, анекорвата ацетат, тромбоспондин, антитело против VEGF); агонисты дофамина; радиотерапевтические средства; пептиды; белки; ферменты; внеклеточный матрикс; компоненты; ингибиторы ACE; ловушки свободных радикалов; хелаторы; антиоксиданты; антиполимеразы; средства для фотодинамической терапии; средства для генной терапии; и другие терапевтические средства, такие как простагландины, антипростагландины, предшественники простагландинов, в том числе лекарственные средства против глаукомы, в том числе β-блокаторы, такие как тимолол, бетаксолол, левобунолол, атенолол, и аналоги простагландинов такие как биматопрост, травопрост, латанопрост, тафлупрост и т.п.; ингибиторы карбонангидраз, такие как ацетазоламид, дорзоламид, бринзоламид, метазоламид, дихлорфенамид, диамокс; и нейропротекторы, такие как лубезол, нимодипин и родственные соединения; и парасимпатомиметики, такие как пилокарпин, карбахол, физостигмин и т.п.
[0085] Следует принимать во внимание, что эти терапевтические средства предоставлены в качестве примеров и не предназначены в качестве ограничения или полного списка терапевтических средств, которые можно доставлять с использованием устройств, описанных в настоящем документе. Кроме того, следует принимать во внимание, что в настоящем документе предусмотрено множество нагрузок и доз лекарственных средств для различных терапевтических средств, такие как нагрузки и дозы лекарственных средств, описанные в публикации патента США № 2012/0136322, озаглавленной «ANTERIOR SEGMENT DRUG DELIVERY», которая подана 1 июня 2011 года; и публикации патента США № 2013/0144128, озаглавленной «OCULAR INSERT APPARATUS AND METHODS», которая подана 14 сентября 2012 года, каждая из которых включена в настоящий документ посредством ссылки.
[0086] Устройства, описанные в настоящем документе, можно изготавливать в соответствии с различными способами. В одной реализации, лекарственное средство можно смешивать с и диспергировать в матрице лекарственного средства, такой как силикон медицинских сортов, такой как силикон MED-4830, для того, чтобы формировать корпусную структуру 112 из материала из лекарственного средства и матрицы лекарственного средства. Материал из лекарственного средства и матрицы лекарственного средства корпусной структуры 112 можно формовать в желаемую форму и отверждать. Например, материал корпусной структуры 112 можно формовать и отверждать, как известно в данной области. В некоторых реализациях, корпусную структуру 112 можно формовать до удлиненной трубчатой структуры, которая имеет просвет 113, идущий через нее. Трубчатая структура может иметь различные формы сечения, как рассмотрено в настоящем документе, включая в качестве неограничивающих примеров круглую, линзовидную, в форме восьмерки, подковообразную, овальную продолговатую, скругленную прямоугольную, в форме звезды или зубчатого колеса и т.д. В некоторых реализациях, по меньшей мере часть корпусной структуры 112 может иметь толщину в сечении, которая составляет приблизительно 1 мм. Просвет 113, идущий через каждую из корпусных структур 112, может иметь внутренний диаметр, выполненный с возможностью вмещать опорную структуру 135. В некоторых реализациях, просвет 113 может иметь внутренний диаметр приблизительно 0,06 мм, 0,08 мм, 0,11 мм, 0,16 мм, 0,21 мм, 0,3 1 мм или 0,36 мм в диаметре. Каждая из корпусных структур 112 может варьировать по длине, такой как, например, по меньшей мере приблизительно 1 мм, 2, мм, 4 мм, 6 мм, 8 мм, 10 мм, 12 мм, 14 мм, 16 мм, 18 мм или более, вплоть до длины опорной структуры 135, на которую нанизывают корпусную структуру 112. Отрезок корпусных структур 112 может создавать дуговой отрезок опорной структуры 135. Например, одна корпусная структура 112 может создавать дуговой отрезок приблизительно от 5 градусов до 75 градусов приблизительно до 360 градусов, так что опорную структуру 135 полностью закрывает единственная корпусная структура 112. Глазное устройство 105 может иметь дуговой отрезок приблизительно от 5 градусов приблизительно до 75 градусов приблизительно до 175 градусов каждый, а также какой-либо отрезок между ними. Также следует принимать во внимание, что корпусную структуру 112 можно нанизывать на опорную структуру 135 так, что корпусную структуру 112 располагают на опорной структуре 135 в соответствии с одним из множества положений относительно опорной структуры 135 и относительно друг друга, если больше чем одна корпусная структура 112 содержится в устройстве 105.
[0087] Одну или несколько корпусных структур 112 можно нанизывать на опорную структуру 135. Напряжение с опорной структуры 135 можно снимать в печи и термически придавать форму кольца или другую форму, например, посредством оборачивания опорной структуры 135 вокруг сердечника, который имеет выбранный диаметр. Обладающую определенной формой опорную структуру 135 можно обрезать до желаемой длины, такой как, например 24 мм, 25 мм, 26 мм, 27 мм, 28 мм или 29 мм. Опорную структуру 135 можно термически усаживать на кольцо или другую форму до или после обрезки до желаемой длины. Одну или несколько корпусных структур 112 можно нанизывать на опорную структуру 135 перед термической сваркой концов опорной структуры 135 вместе. Когда одну или несколько корпусных структур 112 нанизывают на опорную структуру 135, свободные концы опорной структуры 135 можно сплавлять вместе, например, посредством их термической сварки для того, чтобы формировать полного кольца. Каждое устройство 105 можно помещать в упаковочный лоток и в конце стерилизовать электронным пучком.
[0088] Анатомическая структура глаза и способы использования
[0089] Глазные устройства, описанные в настоящем документе, в целом имеют размеры и формы, подлежащие расположению на внешней поверхности глаза, причем по меньшей мере часть глазного устройства располагают под одним или обоими веками глаза таким образом, чтобы не контактировать с роговицей или не мешать ей. Анатомическая структура глаза описана далее наряду с образцовыми способами имплантации и использования.
[0090] На фиг. 12 представлен глаз 300, подходящий для установки глазных устройств, описанных в настоящем документе. Глаз имеет светопропускающую роговицу 305 и светопропускающий хрусталик 312, который формирует изображение на светочувствительной сетчатке 314 с тем, чтобы человек мог видеть. Глаз 300 содержит светопропускающее стекловидное тело 316 между хрусталиком 312 и сетчаткой 314. Опорная ось A может включать одну или несколько известных осей глаза, таких как зрительная ось, линия взора, оптическая ось или другая ось глаза. Роговица 305 идет к лимбу 316 глаза, а лимб 316 соединяется со склерой 318 глаза. Глаз имеет радужку 320, которая может расширяться и сокращаться в ответ на свет. Глаз также содержит хориоид 322, расположенный между склерой 318 и сетчаткой 314. Кроме того, глаз содержит плоскую часть 326, расположенную вдоль части склеры глаза около лимба 316.
[0091] Со ссылкой на фиг. 12-15, глаз 300 содержит соединительнотканные структуры для того, чтобы защищать глаз и позволять глазу перемещаться. Веки выполнены с возможностью открываться для того, чтобы позволять глазу видеть, и закрываться для того, чтобы защищать глаз. Верхнее веко 336 идет по верхней части глаза и нижнее веко 338 идет по нижней части глаза. Веки глаза определяют глазную щель, которая идет между верхним веком 336 и нижним веком 338. Конъюнктива представляет собой свободную ткань, которая защищает глаз и позволяет глазу перемещаться внутри костной орбиты. Конъюнктива содержит часть века, содержащую конъюнктиву 342 века, и часть глазного яблока, содержащую бульбарную конъюнктиву 344. Конъюнктива 342 века выстилает внутреннюю поверхность верхнего и нижнего века глаза, которая контактирует с роговицей 305, когда веки глаза закрыты. Конъюнктива идет от конъюнктивы 342 века на каждом веке к бульбарной конъюнктиве 344, расположенной поверх склеры 318 глазного яблока. Бульбарная конъюнктива 344 соединяется с глазным яблоком около лимба 316. Конъюнктива идет от конъюнктивы 342 века к каждому веку глаза и возвращается для того, чтобы формировать мешок 346, содержащий дно 510 мешка и свод 360. Бульбарная конъюнктива 344 располагается поверх склеры 318 и прозрачна, так что белую склеру можно легко видеть.
[0092] На фиг. 13 представлен вид глаза спереди. Зрачок 364, радужку 320 и склеру 318 можно легко видеть на виде глаза спереди. Внутренний угол глаза расположен на носовом конце глазной щели, а внешний угол глаза расположен на латеральном конце глазной щели. Человеческий глаз, кроме того, содержит мясцо 366, которое расположено назально около внутреннего угла глаза. Складка бульбарной конъюнктивы 344, содержащей полулунную складку, может располагаться около мясца 366. Поскольку полулунная складка может двигаться с глазным яблоком, полулунная складка может двигаться назально под мясцо, когда пациент смотрит в сторону носа, и может становиться больше видна, когда пациент смотрит в сторону виска, чтобы поворачивать полулунную складку в сторону виска. Глаз может содержать дополнительные складки бульбарной конъюнктивы и конъюнктивы века, которые идут по окружности около глаза с тем, чтобы позволять глазу свободно вращаться внутри костной орбиты.
[0093] На фиг. 14 представлен вид сбоку в разрезе конъюнктивы верхнего века 338 и нижнего века 336 глаза. Бульбарная часть 344 конъюнктивы содержит множество складок 370F и часть 342 века конъюнктивы содержит множество складок 372F. Конъюнктива разворачивается назад между бульбарной конъюнктивой 344 и конъюнктивой 342 века у свода 360. Множество бульбарных складок 370F и множество складок 372F века могут идти по существу по окружности около по меньшей мере части глаза. Мешок 346 содержит дно 510 мешка, и дно 510 мешка содержит свод 360.
[0094] На фиг. 15 представлен вид в разрезе сбоку для верхнего века глаза и складок конъюнктивы. Бульбарная конъюнктива 344 верхнего века 338 имеет множество складок 370F вдоль конъюнктивы, идущих между лимбом и сводом 360. Конъюнктива 342 века на верхнем веке содержит множество складок 372F, идущих между сводом и нижним краем верхнего века 338 глаза. Бульбарная конъюнктива 344 нижнего века 336 имеет множество складок 370F вдоль конъюнктивы, идущих между лимбом и сводом 360, и конъюнктива 342 века на нижнем веке 336 содержит множество складок 372F, идущих между сводом и верхним краем нижнего века 336.
[0095] На фиг. 16 представлена реализация глазного устройства 105, вставленного на переднюю поверхность глаза и расположенную внутри верхнего и нижнего сводов 360. Устройство 105 можно устанавливать на глаз с использованием различных способов с использованием или без использования анестетика. В одной реализации, устройство 105 можно помещать после введения местного анестетика. Веки глаза можно аккуратно раздвигать и, используя тупоконечный инструмент или пальцы, устройство можно помещать в верхний и нижний своды. Например, устройство 105 можно вставлять сперва в верхний свод так, что устройство удерживается внутри верхнего свода, пока устройство размещают в нижнем своде. Следует принимать во внимание, что обратная процедура, в которой устройство сперва помещают в нижний свод перед установкой в верхний свод, рассмотрена в настоящем документе. После установки, глазное устройство 105 может удерживаться в положении на глазу в течение определенного периода времени без использования каких-либо механических крепежных элементов, которые идут в или через ткань глаза. Устройство может удерживаться естественным образом, например, посредством его взаимодействия с нормальной анатомической структурой глаза, которую дополняет конформация формы устройства, которая может произойти с течением времени. Находясь на месте, устройство в целом не видно при нормальном взгляде, возможно, за исключением маленького сегмента устройства, который может быть виден в носовой области глаза около мясца. Для того чтобы удалять устройство из глаза, необязательно можно наносить каплю анестетика на глаз перед захватом устройства в нижнем своде (обычно, с использованием тупоконечного инструмента), и аккуратно удалить устройство из глаза.
[0096] Устройство можно использовать для того, чтобы лечить глаз в течение определенного периода времени. Период времени, в течение которого глазное устройство 105 может располагаться на глазу для эффективного лечения, может варьировать, включая в качестве неограничивающих примеров по меньшей мере любой один из 1 суток, 5 суток, одной недели, одного месяца, двух месяцев, трех месяцев, четырех месяцев, шести месяцев или большего количества времени.
[0097] На фиг. 17 представлен разборный вид реализации глазного устройства 105 в упаковке 1701. Каждое глазное устройство 105 можно помещать в упаковочный лоток 1710 и в конце стерилизовать с помощью электронного пучка. Упаковочный лоток 1710 может содержать лунку 1715 комплементарной формы, выполненную с возможностью безопасного хранения глазного устройства 105 в лотке 1710, например, при вскрытии пакета 1720 из фольги при использовании. Глазное устройство 105 может располагаться внутри лотка 1710 погруженным в нетерапевтический раствор, например, физиологический раствор. Одно или несколько глазных устройств 105, описанных в настоящем документе, можно предоставлять в форме набора, содержащего упаковочный лоток 1710, который вмещает глазное устройство 105. В некоторых реализациях, набор дополнительно может содержать инструмент, выполненный с возможностью помогать при расположении устройства 105 в глазу, небольшое количество анестетика и инструкцию по использованию. В некоторых реализациях, набор может содержать множество глазных устройств 105. Например, один набор может содержать глазные устройства нескольких размеров, чтобы подходить к глазам различных размеров. Глазные устройства, описанные в настоящем документе, могут иметь общий диаметр приблизительно 24 мм, 25 мм, 26 мм, 27 мм, 28 мм или 29 мм, чтобы вмещать глаза различных размеров. Следует принимать во внимание, что содержание лекарственного средства в каждом устройстве может быть одним и тем же, независимо от размера. Альтернативно, один набор может содержать множество глазных устройств для лечения одного пациента в течение периода времени так, что когда одно устройство используют и удаляют, можно вставлять дополнительное устройство.
[0098] Несмотря на то, что это описание содержит много конкретного, это следует толковать не в качестве ограничения объема изобретения, которое заявлено, или того, что может быть заявлено, а скорее в качестве описания признаков, характерных для конкретных реализаций. Определенные признаки, которые описаны в этом описании в контексте отдельных реализаций, также можно реализовать в комбинации в одной реализации. Наоборот, различные признаки, которые описаны в контексте одной реализации, также можно реализовать во множестве реализаций отдельно или в любой подходящей подкомбинации. Кроме того, несмотря на то, что признаки могут быть описаны выше как действующие в определенных комбинациях и даже изначально заявлены как таковые, один или несколько признаков из заявленной комбинации может в некоторых случаях удален из комбинации, и заявленная комбинация может быть направлена на подкомбинацию или вариацию подкомбинации. Аналогичным образом, хотя операции приведены на рисунках в конкретном порядке, это не следует понимать как требование выполнять такие операции в конкретном представленном порядке или в последовательном порядке или что все проиллюстрированные операции должны быть выполнены, чтобы достичь желаемых результатов. Раскрыто только несколько примеров и реализаций. Вариации, модификации и улучшения в описанных примерах и реализациях и других реализация можно выполнять на основе того, что раскрыто.
| название | год | авторы | номер документа |
|---|---|---|---|
| ГЛАЗНОЕ ВКЛАДОЧНОЕ УСТРОЙСТВО И СПОСОБЫ | 2012 |
|
RU2618194C2 |
| ГЛАЗНОЕ ВКЛАДОЧНОЕ УСТРОЙСТВО И СПОСОБЫ | 2012 |
|
RU2740680C2 |
| РАСШИРЯЕМЫЕ УСТРОЙСТВА ДОСТАВКИ ЛЕКАРСТВЕННЫХ СРЕДСТВ И СПОСОБЫ ИСПОЛЬЗОВАНИЯ | 2015 |
|
RU2708958C2 |
| КОМПОЗИЦИИ ОМЕГА-3 ЖИРНЫХ КИСЛОТ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ, ВЫЗЫВАЮЩИХ ПОРАЖЕНИЕ НЕРВНОЙ СИСТЕМЫ | 2013 |
|
RU2667640C1 |
| ИЗОКСАЗОЛИНОВЫЕ ПАРАЗИТИЦИДНЫЕ СОСТАВЫ И СПОСОБЫ ЛЕЧЕНИЯ БЛЕФАРИТА | 2018 |
|
RU2840921C2 |
| СОСТАВ ДЛЯ ЭФФЕКТИВНОЙ ДОСТАВКИ ЛИПИДОВ В СЛЕЗНУЮ ПЛЕНКУ ЧЕЛОВЕКА С ИСПОЛЬЗОВАНИЕМ ЧУВСТВИТЕЛЬНОЙ К СОЛИ ЭМУЛЬСИОННОЙ СИСТЕМЫ | 2012 |
|
RU2772357C2 |
| ИЗОПРОПИЛОВЫЙ ЭФИР [(1R,2S,5R)-2-ИЗОПРОПИЛ-5-МЕТИЛЦИКЛОГЕКСАНКАРБОНИЛ)-АМИНО]-УКСУСНОЙ КИСЛОТЫ, РОДСТВЕННЫЕ СОЕДИНЕНИЯ И ИХ ПРИМЕНЕНИЕ В ТЕРАПИИ | 2011 |
|
RU2598644C2 |
| ЛЕЧЕНИЕ ДИСКОМФОРТА ГЛАЗ ПУТЕМ МЕСТНОГО ПРИМЕНЕНИЯ ОХЛАЖДАЮЩЕГО АГЕНТА НА НАРУЖНОЙ ПОВЕРХНОСТИ ВЕКА | 2010 |
|
RU2538696C2 |
| РАЗМЕЩЕНИЕ АВ EXTERNO ВНУТРИГЛАЗНОГО ШУНТА | 2016 |
|
RU2687764C1 |
| миРНК И ИХ ПРИМЕНЕНИЕ В СПОСОБАХ И КОМПОЗИЦИЯХ ДЛЯ ИНГИБИРОВАНИЯ ЭКСПРЕССИИ ГЕНА ORAI1 | 2014 |
|
RU2689607C2 |
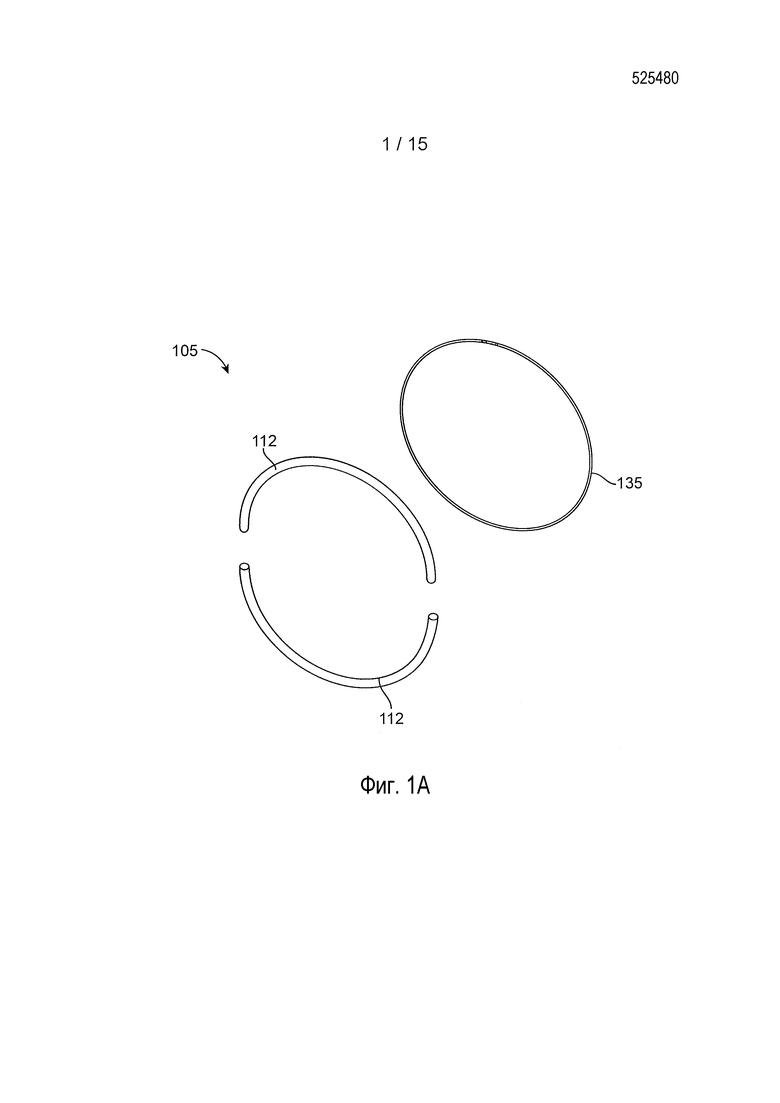
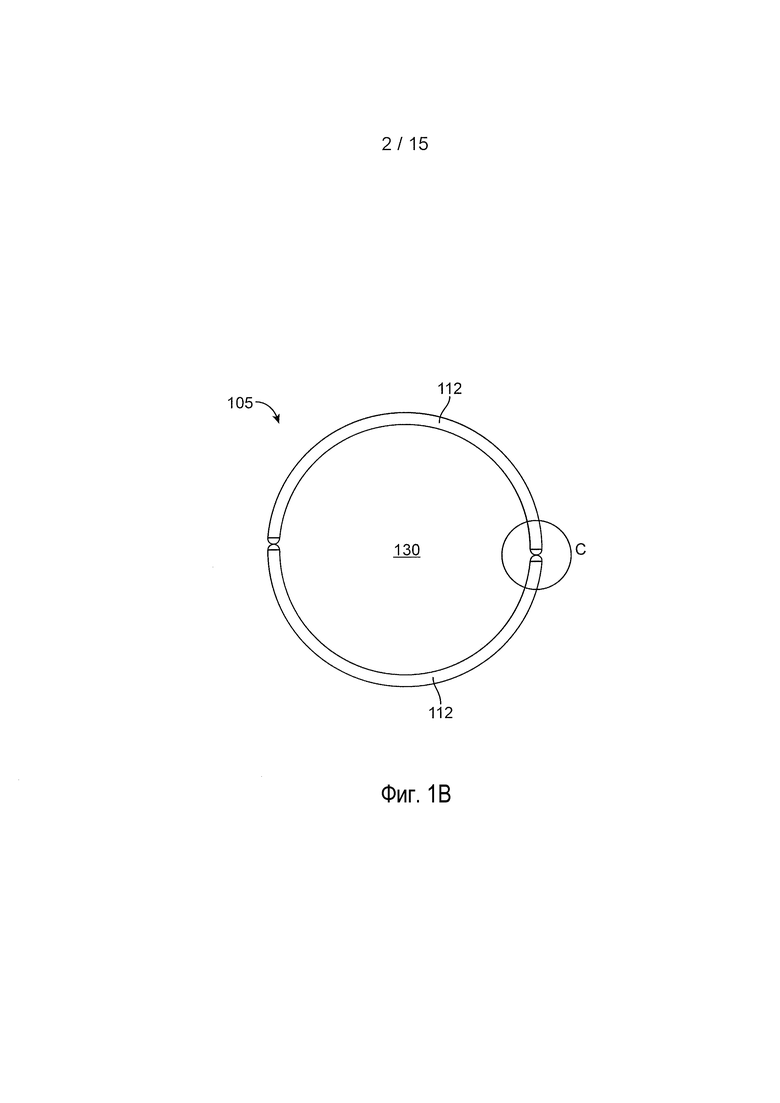
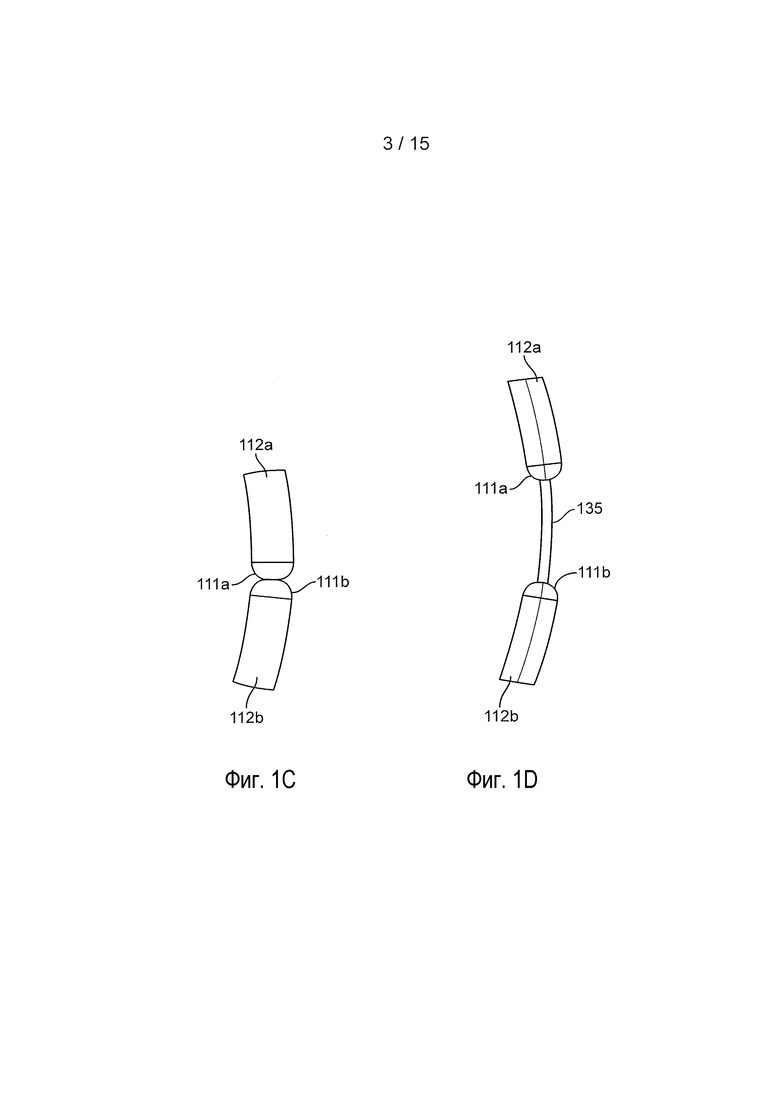
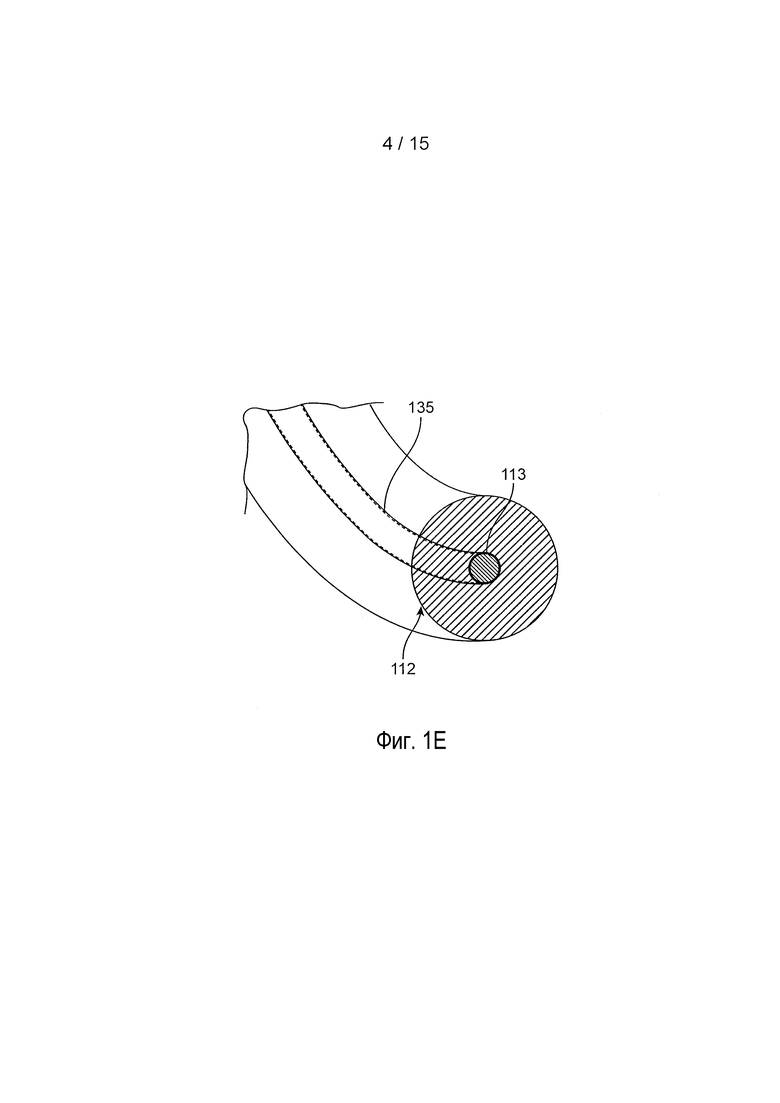
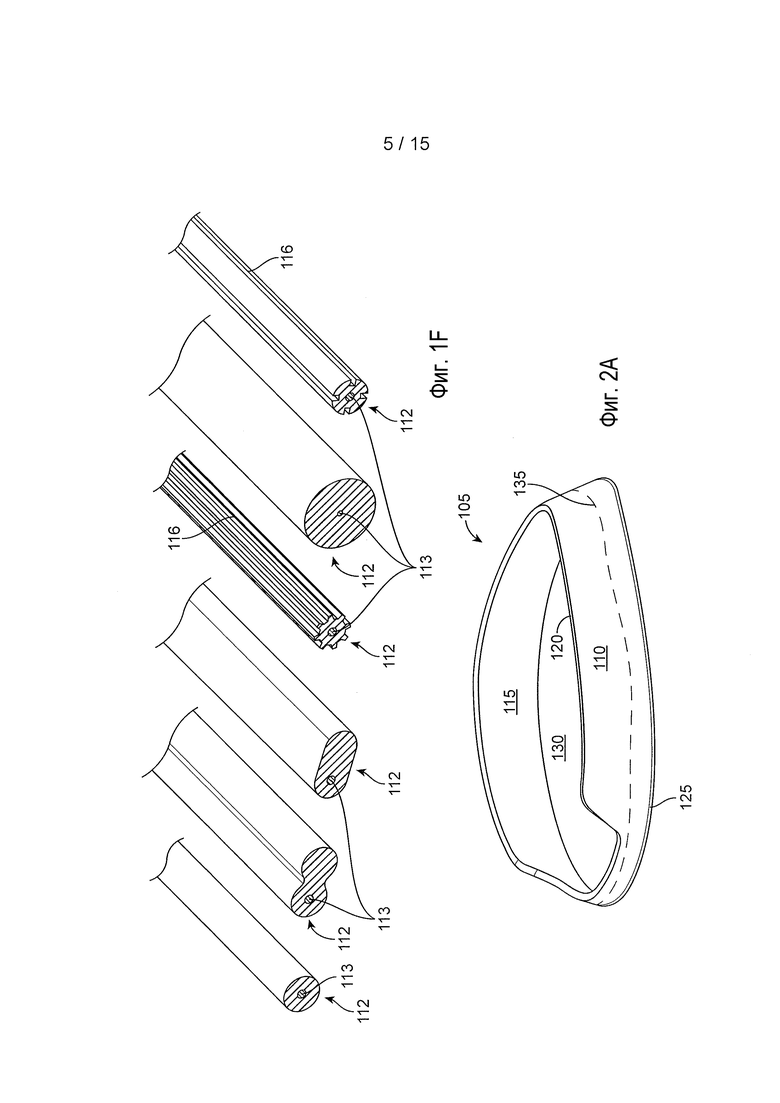
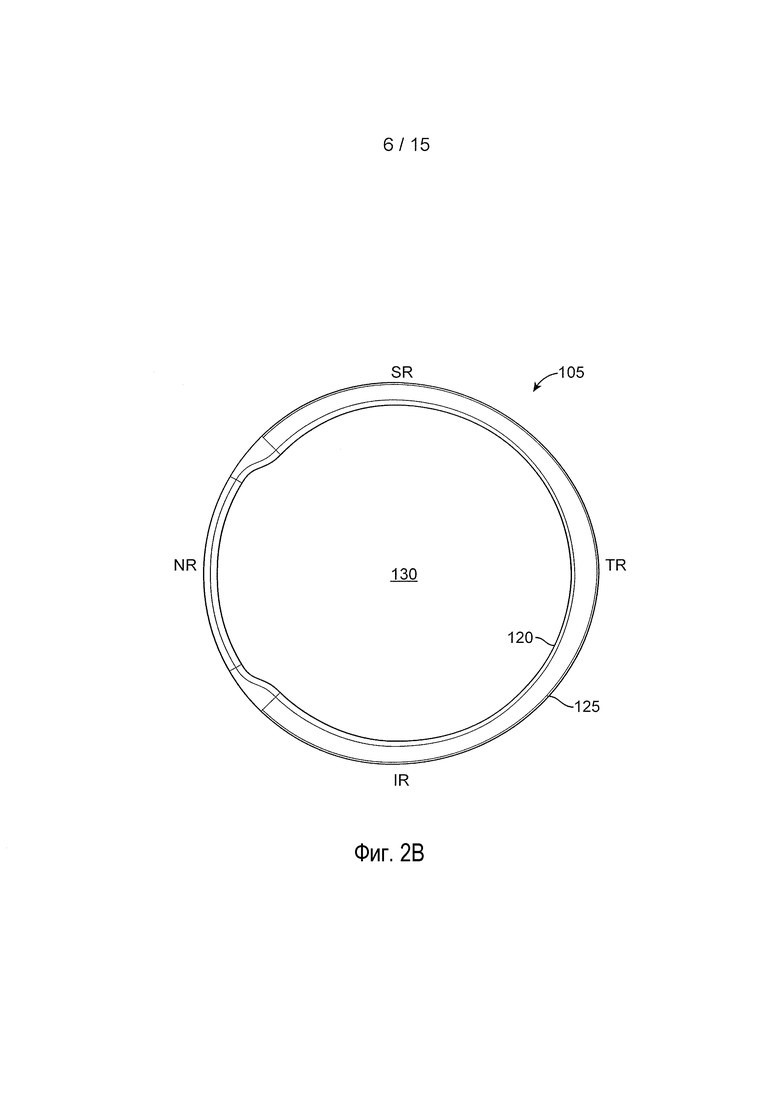
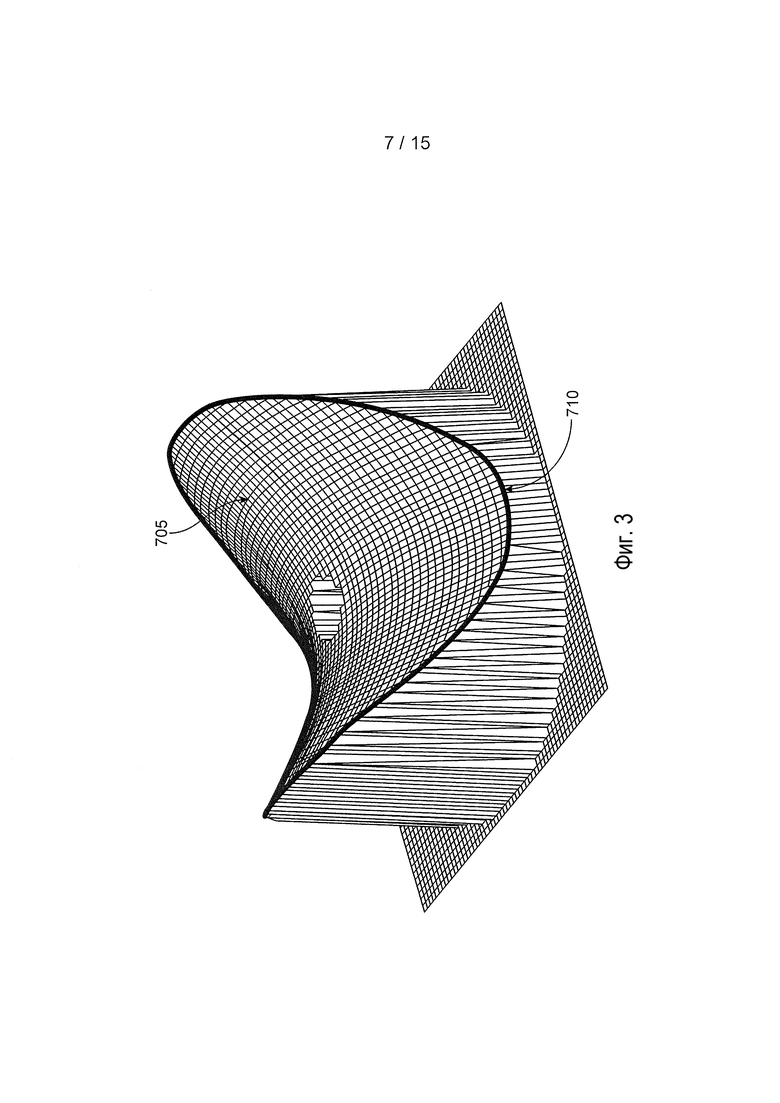
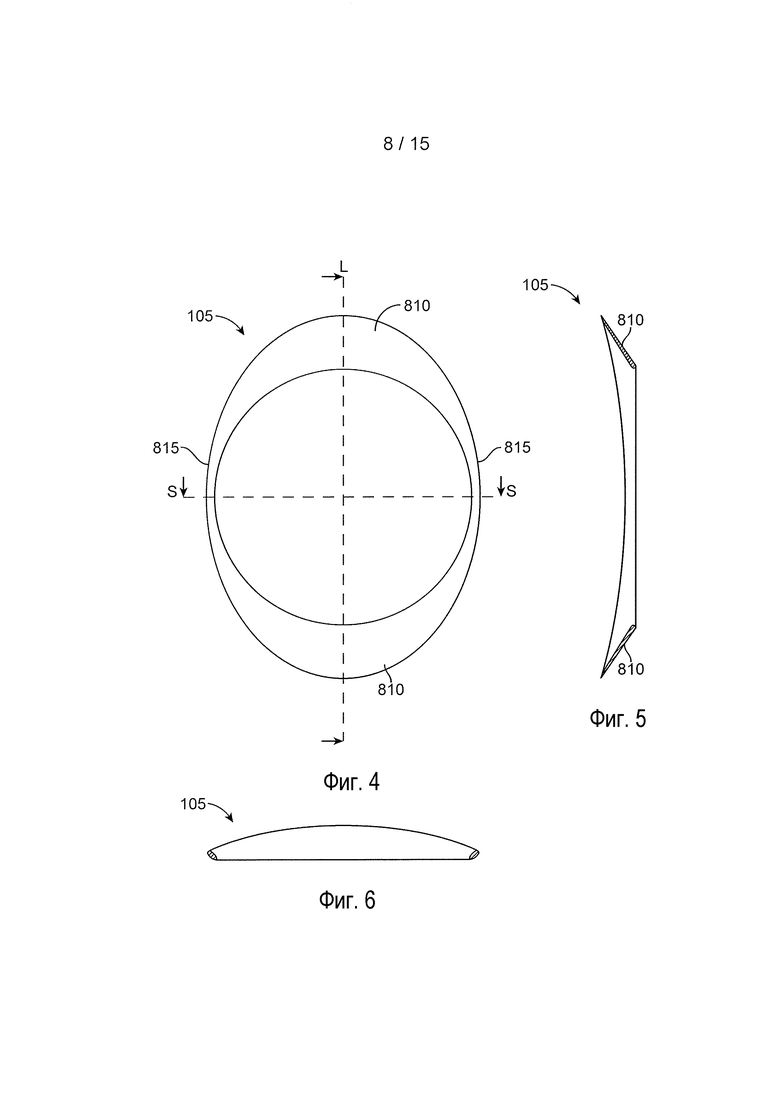
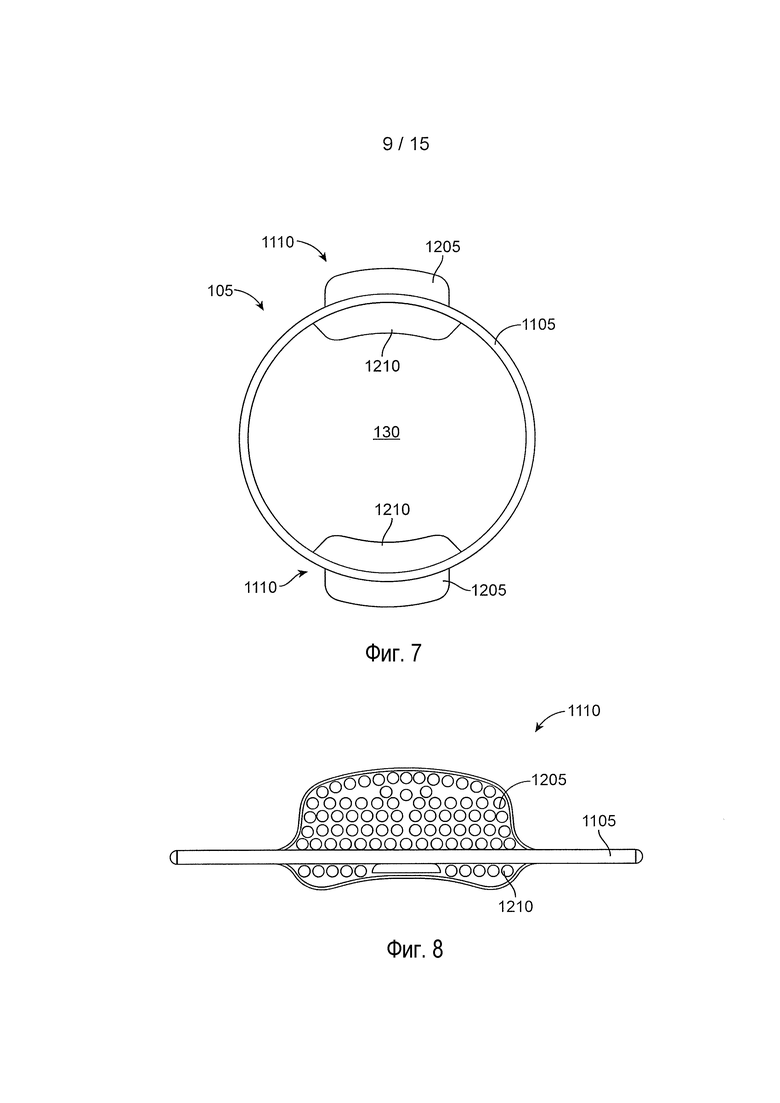
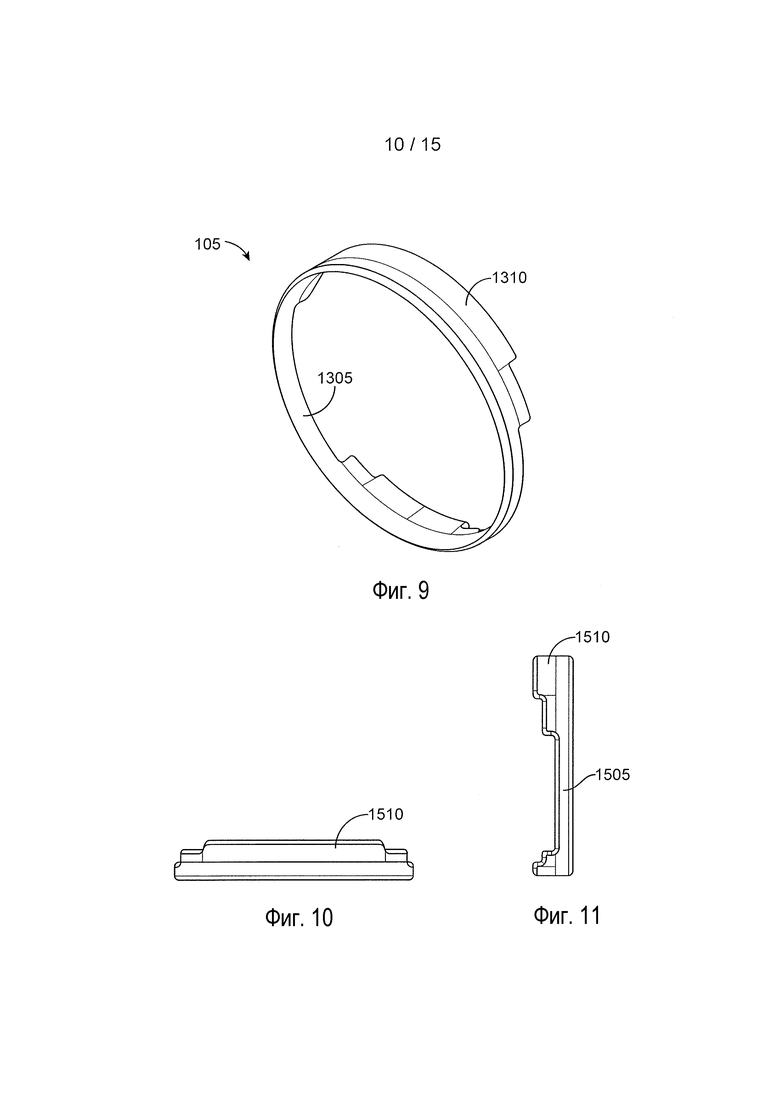
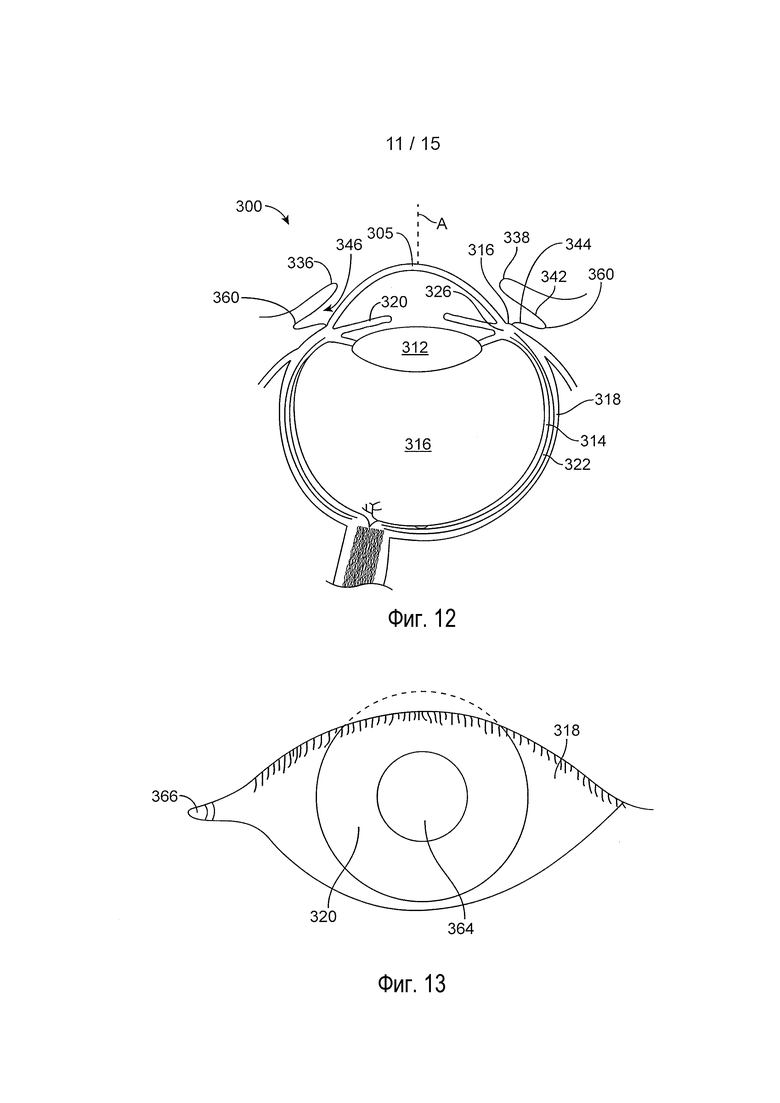
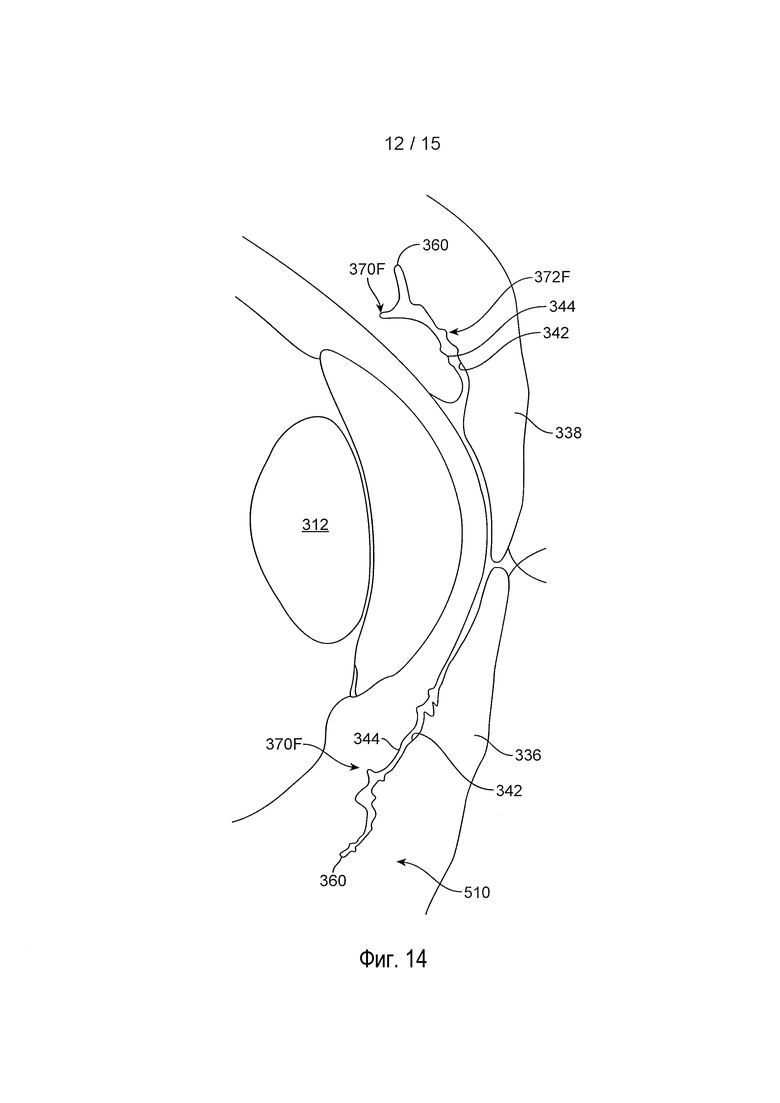
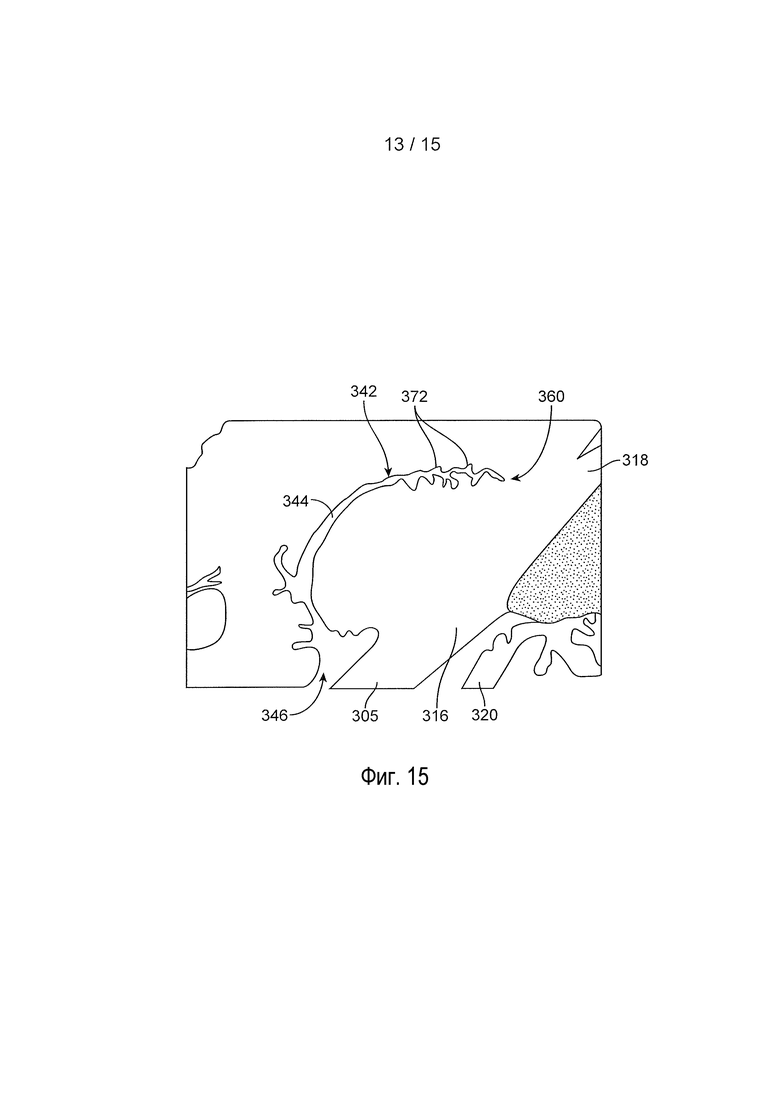
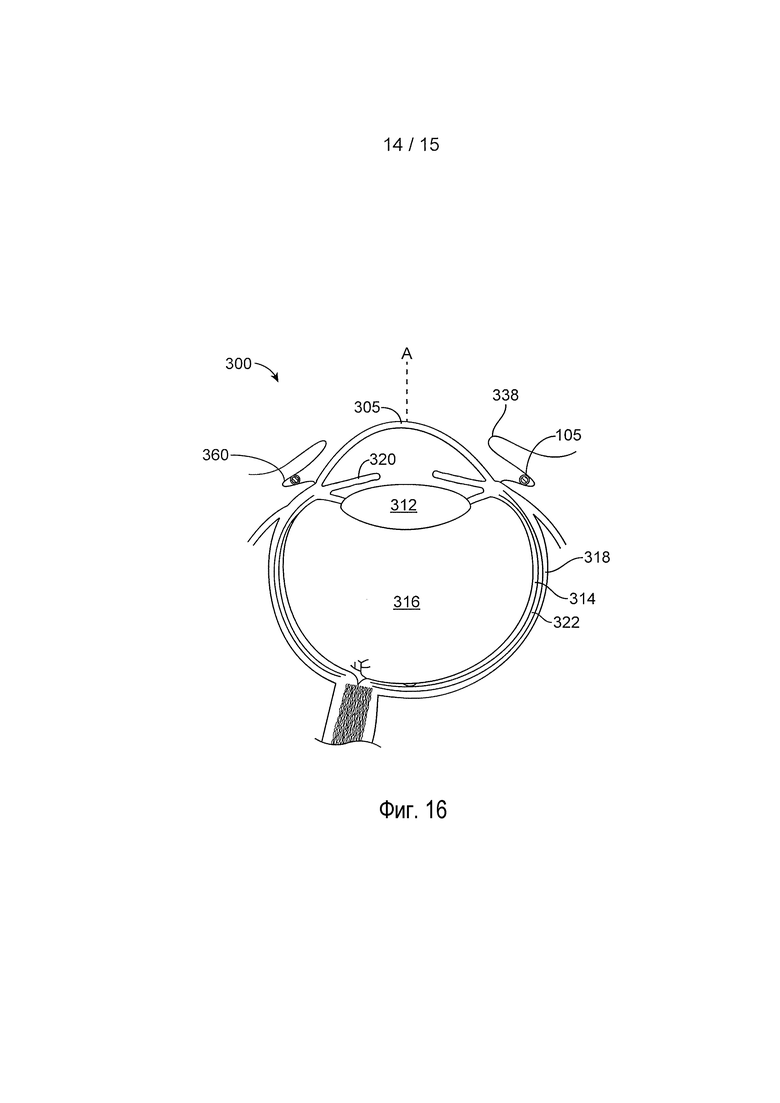
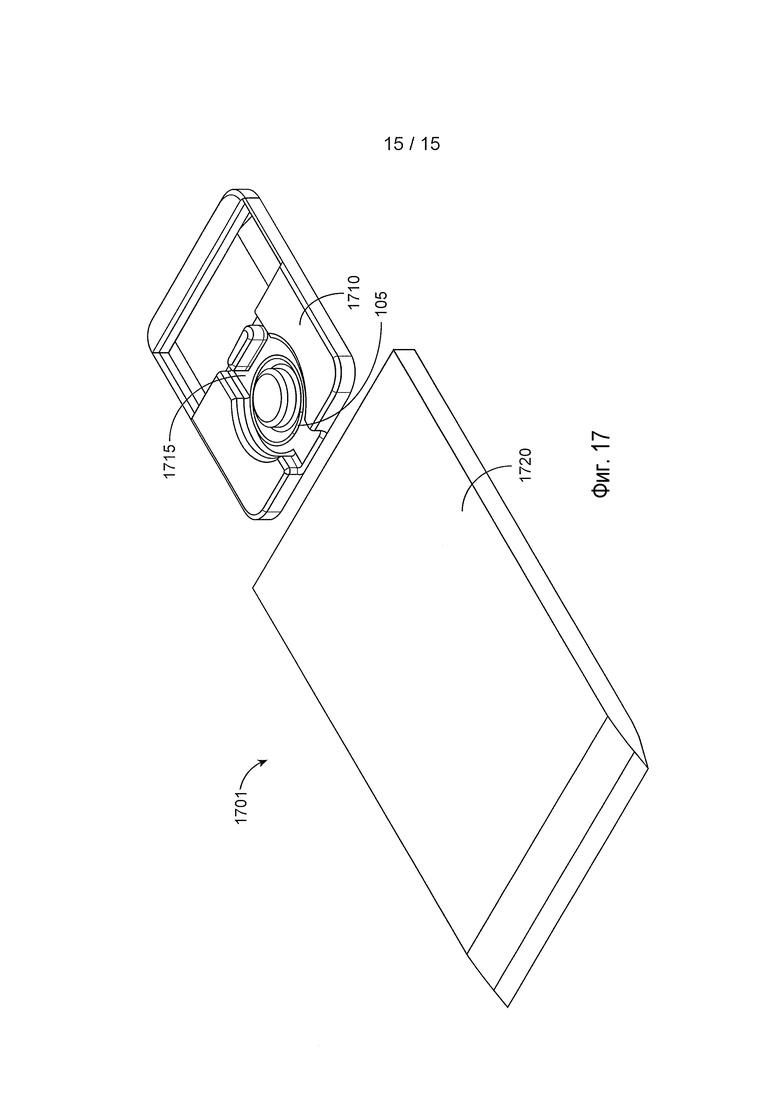
Изобретение относится к медицине. Глазное устройство, выполненное с возможностью расположения на поверхности глаза под по меньшей мере одним из верхнего и нижнего века глаза и за пределами роговицы глаза для доставки терапевтического средства в глаз в течение продолжительного периода времени. Устройство содержит тонкую, удлиненную, в виде мононитей первую структуру, которая сформирована из первого материала; вторую структуру, которая сформирована из второго материала, который имеет трубчатую структуру, сформированную из первой трубчатой корпусной структуры и второй трубчатой корпусной структуры, таким образом, что указанная первая структура идет через просвет, проходящий через указанные первую и вторую трубчатые корпусные структуры. Первый терминальный конец первой трубчатой корпусной структуры упирается во второй терминальный конец второй трубчатой корпусной структуры. Второй материал отличается от первого материала. Терапевтическое средство диспергировано в одном из первого материала первой структуры или второго материала второй структуры. Вторая структура имеет одну или более канавок, сформированных на внешней поверхности трубчатой структуры. Канавки проходят параллельно продольной оси трубчатой структуры и обеспечивают форму сечения для трубчатой структуры, когда сечение взято по продольной оси. 22 з.п. ф-лы, 17 ил., 1 табл.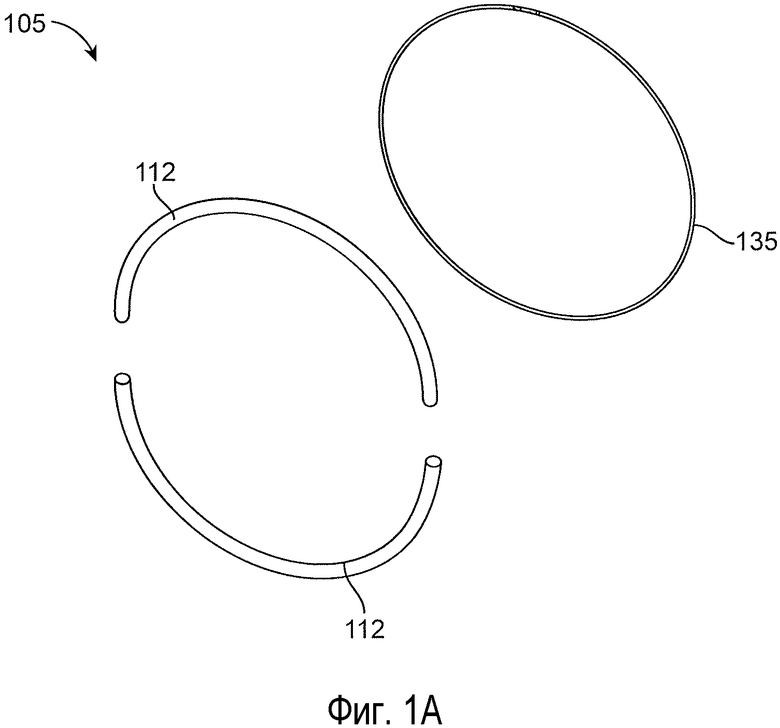
1. Глазное устройство, выполненное с возможностью расположения на поверхности глаза по меньшей мере частично под по меньшей мере одним из верхнего и нижнего века глаза и за пределами роговицы глаза для доставки по меньшей мере одного терапевтического средства в глаз в течение продолжительного периода времени, содержит:
тонкую, удлиненную, в виде мононитей первую структуру, которая сформирована из первого материала;
вторую структуру, которая сформирована из второго материала, который имеет трубчатую структуру, сформированную из по меньшей мере первой трубчатой корпусной структуры и второй трубчатой корпусной структуры таким образом, что указанная первая структура идет через просвет, проходящий через указанные первую и вторую трубчатые корпусные структуры, при этом первый терминальный конец первой трубчатой корпусной структуры упирается во второй терминальный конец второй трубчатой корпусной структуры, и второй материал отличается от первого материала; и
по меньшей мере одно терапевтическое средство, диспергированное по меньшей мере в одном из первого материала первой структуры или второго материала второй структуры,
при этом вторая структура имеет одну или более канавок, сформированных на внешней поверхности трубчатой структуры, при этом указанные канавки проходят параллельно продольной оси трубчатой структуры и обеспечивают форму сечения для трубчатой структуры, когда сечение взято по продольной оси.
2. Глазное устройство по п.1, в котором форму сечения выбирают из группы, состоящей из формы в виде восьмерки, подковообразной формы, формы звезды или зубчатого колеса.
3. Глазное устройство по п.1, в котором первую структуру термически сплавляют в форму кольца после пронизывания через просвет второй структуры.
4. Глазное устройство по п.1, в котором каждая из первой трубчатой корпусной структуры и второй трубчатой корпусной структуры имеет просвет, через который проходит первая структура.
5. Глазное устройство по п.4, в котором первую из первой и второй трубчатых корпусных структур формируют с составом для того, чтобы высвобождать по меньшей мере одно терапевтическое средство, и где вторую из первой и второй трубчатых корпусных структур формируют с составом для того, чтобы высвобождать по меньшей мере одно терапевтическое средство или по меньшей мере второе терапевтическое средство, диспергированное во втором материале второй структуры, где по меньшей мере одно терапевтическое средство и по меньшей мере второе терапевтическое средство представляют собой одинаковые или различающиеся терапевтические средства.
6. Глазное устройство по п.1, в котором первая структура обеспечивает первую форму глазного устройства перед расположением глазного устройства на поверхности глаза, и где первая форма глазного устройства соответствует второй отличающейся форме после расположения глазного устройства на поверхности глаза, и где при удалении с глаза глазное устройство вторую форму сохраняет или меняет на третью форму, где третья форма отличается как от первой формы, так и от второй формы, где первая структура определяет первую форму, вторую форму и третью форму.
7. Глазное устройство по п.6, в котором вторая форма представляет собой форму по меньшей мере части конъюнктивы глаза или по меньшей мере части костной орбиты глаза или соответствует поверхности седла.
8. Глазное устройство по п.6, где глазное устройство препятствует отклонению от второй формы при удалении из глаза.
9. Глазное устройство по п.6, где первая форма представляет собой кольцевую форму, расположенную, по существу, в первой плоскости, и вторую и третью формы располагают по меньшей мере частично за пределами первой плоскости.
10. Глазное устройство по п.6, где вторая форма соответствует поверхности седла.
11. Глазное устройство по п.6, в котором вторая форма имеет внешний контур, который соответствует внешнему контуру седла.
12. Глазное устройство по п.6, в котором глазное устройство меняет первую форму на вторую форму в течение периода приблизительно от 20 минут приблизительно до 24 часов.
13. Глазное устройство по п.1, в котором первый материал содержит материал, выполненный с возможностью повторно становиться пластичным под воздействием тепла, жидкости или давления.
14. Глазное устройство по п.1, в котором первый материал содержит термопластичный материал.
15. Глазное устройство по п.14, в котором первый материал содержит полипропилен.
16. Глазное устройство по п.1, в котором второй материал содержит силиконовый материал.
17. Глазное устройство по п.14, в котором по меньшей мере одно терапевтическое средство диспергируют только во втором материале второй структуры.
18. Глазное устройство по п.1, в котором по меньшей мере одно терапевтическое средство содержит средство, выбранное из группы, состоящей из биматопроста, травопроста, латанопроста, тафлупроста, НПВС, стероида, антигистамина, ингибитора карбонангидразы (CAI), дорзоламида, циклоспорина, антибиотика, доксициклина, тетрациклина, азитромицина, жирной кислоты, длинноцепочечной жирной кислоты, жирного спирта, цетилового спирта, стеарилового спирта, непроникающего стероида, свободной кислоты стероида, липида, кеторолака, масла, силиконового масла, олопатадина, простагландина, аналога простагландина, простамида, низкомолекулярного антагониста интегринов, лифитеграста, лотепреднола и фторметалона или их сочетания.
19. Глазное устройство по п.1, в котором по меньшей мере одно терапевтическое средство содержит аналог простагландина.
20. Глазное устройство по п.19, в котором аналог простагландина содержит по меньшей мере один из биматопроста, латанопроста, травопроста и тафлупроста.
21. Глазное устройство по п.1, в котором по меньшей мере одно терапевтическое средство предназначено для снижения внутриглазного давления в глазу.
22. Глазное устройство по п.1, в котором по меньшей мере одно терапевтическое средство предназначено для лечения сухости глаз.
23. Глазное устройство по п.22, в котором по меньшей мере одно терапевтическое средство содержит по меньшей мере одно из циклоспорина, стероида, лотепреднола, фторметалона, непроникающего стероида, свободной кислоты стероида, нестероидного противовоспалительного средства, кеторолака, низкомолекулярного антагониста интегринов, лифитеграста, доксициклина, азитромицина, липида, жирного спирта, цетилового спирта, стеарилового спирта, жирной кислоты, длинноцепочечной жирной кислоты, масла или силиконового масла.
| US 20120136322 A1, 31.05.2012 | |||
| US 20110009958 A1, 13.01.2011 | |||
| WO 2007083293 A1, 26.07.2007 | |||
| US 20120215184 A1, 23.08.2012 | |||
| US 20110184358 A1, 28.07.2011 | |||
| ИМПЛАНТАТЫ НАЗОЛАКРИМАЛЬНОЙ ДРЕНАЖНОЙ СИСТЕМЫ ДЛЯ МЕДИКАМЕНТОЗНОЙ ТЕРАПИИ | 2007 |
|
RU2414199C2 |
Авторы
Даты
2018-04-24—Публикация
2013-10-25—Подача