Область техники, к которой относится изобретение
Настоящее изобретение относится к области продуктов миРНК (малые интерферирующие РНК) и их применению в способах и композициях для лечения и/или предотвращения состояний глаза, и в частности, для лечения и/или предотвращения состояний глаза, таких как конъюнктивит и/или аллергические заболевания глаз, связанные с высоким уровнем экспрессии и/или активности ORAI1.
Уровень техники
РНК-интерференция представляет собой существующий в природе механизм посттрансляционной регуляции, присутствующий в большинстве эукариотических клеток, в котором малые двухцепочечные молекулы РНК (дцРНК) применяют для индукции гомологичного подавления экспрессии гена. Открытие РНК-интерференции Fire и Mello у червя C. elegans (Fire, 1998) было отмечено Нобелевской премией в 2006 г. Вскоре после этого первого описания показали, что РНК-интерференция также происходит в клетках млекопитающих, не посредством длинных дцРНК, а посредством малых двухцепочечных интерферирующих РНК (миРНК) длиной 21 нуклеотид (Elbashir, 2001).
Процесс РНК-интерференции считают эволюционно консервативным механизмом клеточной защиты, используемым для предотвращения экспрессии чужеродных генов и широко распространенным в разных таксономических группах и у растения, где его называют посттрансляционным подавлением экспрессии гена. После открытия механизма РНК-интерференции появилось огромное количество исследований, направленных на открытие новых соединений, способных селективно изменять экспрессию генов, в качестве нового способа лечения заболеваний человека, действующего на мишени, не поддающиеся медикаментозному лечению с помощью традиционных фармацевтических подходов с применением малых молекул или белков.
Согласно имеющимся знаниям механизм РНК-интерференции запускается при процессировании длинных двухцепочечных РНК РНКаза III-подобным белком, известным как Dicer. Белок Dicer, как правило, содержит N-концевой домен РНК-хеликазы, РНК-связывающий домен, так называемый Piwi/Argonaute/Zwille (PAZ), два домена РНКазы III и домен связывания двухцепочечной РНК (dsRBD, double-stranded RNA binding domain) (Collins, 2005), а его активность вызывает процессирование длинных двухцепочечных РНК до двухцепочечных миРНК длиной 21-24 нуклеотида с 2 неспаренными выступающими основаниями на 3'-конце, 5'-фосфатом и 3'-гидроксильной группой. Образующиеся в результате дуплексы миРНК затем встраиваются в эффекторный комплекс, называемый RISC (RNA-induced silencing complex, комплекс сайленсинга, индуцированный РНК), где антисмысловая или направляющая цепь миРНК обеспечивает узнавание и разрезание последовательности мРНК-мишени комплексом RISC (Elbashir, 2001) посредством аденозинтрифосфат (АТФ)-зависимого расплетания молекулы двухцепочечной миРНК за счет активности РНК-хеликазы (Nykanen, 2001). Каталитическая активность RISC, обеспечивающая деградацию мРНК, опосредована эндонуклеазой Argonaute 2 (AGO2) (Liu, 2004; Song, 2004). AGO2 относится к высококонсервативному семейству белков Argonaute. Белки Argonaute представляют собой ~100 кДа сильно основные белки, содержащие два общих домена, а именно домены PIWI и PAZ (Cerutti, 2000). Домен PIWI необходим для взаимодействия с Dicer и обладает нуклеазной активностью, обеспечивающей расщепление мРНК (Song, 2004). AGO2 использует одну цепочку дуплекса миРНК как направляющую для поиска матричных РНК, содержащих комплементарные последовательности, и расщепляет фосфодиэфирный остов между основаниями 10 и 11 относительно 5'-конца направляющей цепочки (Elbashir, 2001). Важной стадией при активации RISC является расщепление смысловой или «сопровождающей» цепи с помощью AGO2, высвобождающее эту цепочку из комплекса (Rand, 2005). Кристаллографические исследования, анализирующие взаимодействие направляющей цепи миРНК и домена PIWI, показывают, что только нуклеотиды со 2 по 8 составляют «затравочную последовательность», обеспечивающую узнавание целевой мРНК комплексом RISC, и что даже один неспаренный нуклеотид в этой последовательности может сильно нарушать способность молекулы подавлять экспрессию гена (Ma, 2005; Doench, 2004; Lewis, 2003). После расщепления мРНК из-за присутствия незащищенных концов РНК в фрагментах мРНК далее подвергается расщеплению и деградации внутриклеточными нуклеазами и больше не транслируется в белки (Orban, 2005), в то время как RISC повторно вступает в последующие циклы (Hutvagner, 2002). Это составляет каталитический процесс, приводящий к селективному уменьшению содержания конкретных молекул мРНК и соответствующих белков. Можно исследовать этот нативный механизм подавления экспрессии генов с целью регуляции любых выбранных генов (гена) посредством прямой доставки миРНК эффекторов в клетки или ткани, где они будут активировать RISC и обеспечивать сильное и специфичное подавление экспрессии целевой мРНК. РНК-интерференцию применяют в биомедицинских исследованиях, таких как лечение ВИЧ, вирусного гепатита, сердечно-сосудистых заболеваний и нарушений мозгового кровообращения, нарушения обмена веществ, нейродегенеративных заболеваний и рака (Angaji SA, et al., 2010).
Опубликовано много исследований, описывающих идеальные свойства, которыми должны обладать миРНК для достижения максимальной эффективности, в зависимости от длины, структуры, химического состава и последовательности. Исходные параметры создания миРНК были заданы Tuschl с соавторами в WO02/44321, хотя с тех пор было опубликовано много последующих исследований, алгоритмов и/или усовершенствований. Подходы к подбору миРНК усложнялись по мере появления новых подробностей механизма, дополнительно дальнейший анализ существующих и новых данных может предоставить дополнительную информацию, способствующую дальнейшему усовершенствованию данных подходов (Walton SP, et al., 2010). Альтернативно, в нескольких недавних исследованиях сообщили о создании и анализе новых индуцирующих РНК-интерференцию структур, отличающихся от классических «19+2» структур миРНК и не соответствующих основным свойствам классических миРНК, касающихся выступающих неспаренных оснований, длины или симметрии, что поднимает вопрос о пластичности аппарата РНК-интерференции в клетках млекопитающих (Chang CI, et al., 2011).
Также предпринято много попыток увеличения стабильности миРНК, поскольку она является основным препятствием терапии на основе миРНК из-за повсеместной распространенности РНКаз в биологических жидкостях. Другой свойственной молекулам миРНК проблемой является их иммуногенность, из-за которой миРНК, как было обнаружено, индуцируют неспецифичную активацию врожденного иммунитета. Нокдаун нецелевых генов (мРНК) является хорошо известным побочным эффектом подавления экспрессии гена посредством миРНК. Это происходит из-за частичной комплементарности миРНК и мРНК, отличающихся от целевой мРНК, и оказывает нецелевое действие на гены с последовательностью, комплементарной одной их двух цепей миРНК. Одной из основных стратегий увеличения стабильности и уменьшения нецелевых эффектов является применение модифицированных нуклеотидов, таких как 2'-O-метилнуклеотиды, 2'-аминонуклеотиды или нуклеотиды, содержащие 2'-О- или 4'-С-метиленовые мостики. Также описана модификация рибонуклеотидного остова, соединяющего соседние нуклеотиды, в основном посредством введения тиофосфатных нуклеотидов. По-видимому, увеличенная стабильность и/или снижение иммуногенности часто обратно пропорциональны эффективности [Parrish, 2000), и лишь определенное количество, положение и/или комбинации модифицированных нуклеотидов могут привести к образованию стабильного и неиммуногенного соединения для подавления экспрессии гена. Поскольку это представляет собой серьезное препятствие для терапии на основе миРНК, были опубликованы различные исследования, описывающие определенные профили модификации, демонстрирующие хорошие результаты, примеры таких исследований включают EP1527176, WO2008/050329, WO2008/104978 или WO2009/044392, хотя гораздо больше можно найти в литературе (Sanghvi YS. 2011; Deleavey, et al., 2012).
Аллергические заболевания характеризует повышенная реакция иммунной системы на чужеродное белковое вещество («аллерген»), которое поступает с пищей, с вдыхаемым воздухом в легкие, при инъекции или прикосновении. У аллергии есть генетический компонент. Если всего у одного из родителей есть аллергия любого типа, шансы, что у каждого ребенка будет аллергия, равны 1 к 3. Если аллергия есть у обоих родителей, гораздо вероятней (7 из 10), что у их детей будет аллергия. Аллергию невозможно вылечить, однако можно контролировать с помощью подходящей профилактики и лечения.
Около 30% людей по всему миру страдают от симптомов аллергии и 40-80% из них имеют глазные симптомы (Key B., 2001). Аллергические заболевания, затрагивающие глаз, или глазные аллергии составляют гетерогенную группу заболеваний с широким спектром клинических проявлений. Аллергическое заболевание глаз обычно развивается при взаимодействии конъюнктивы (мембраны, покрывающей глаз и выстилающей веко) с аллергеном. Аллергическое заболевание глаз может развиться независимо или в связи с другими симптомами аллергии (такими как ринит или астма).
Фундаментальные и клинические исследования способствуют пониманию того, какие клетки, медиаторы и иммунологические события участвуют в аллергических заболеваниях глаз. В глазу, в частности, в конъюнктиве, содержится большое число тучных клеток. При наличии аллергены могут связываться с иммуноглобулином IgE на рецепторах FcεRI на поверхности тучных клеток и индуцировать их активацию и высвобождение медиаторов аллергии (процесс, называемый дегрануляцией). При дегрануляции во внеклеточное окружение тучной клетки высвобождаются компоненты тучной клетки, включая гистамин, простагландины, триптазу и лейкотриены. Посредством разных механизмов эти компоненты вызывают признаки и симптомы аллергического заболевания глаз. Активацию тучных клеток аллергического воспаления часто называют острой фазой ответа или начальной фазой аллергического заболевания глаз. Ответ острой фазы может прогрессировать до ответа поздней фазы, характеризующегося привлечением клеток воспаления к очагу аллергического воспаления, например, проникновением эозинофилов и нейтрофилов в конъюнктиву.
Аллергическое заболевание глаз представляет собой одно из наиболее распространенных состояний, с которым сталкиваются аллергологи и офтальмологи. Аллергическое заболевание глаз обычно связано со следующими симптомами и признаками: конъюнктивитом, блефаритом, блефароконъюнктивитом или кератоконъюнктивитом. Глаз краснеет, начинает зудеть, появляется слезоточивость и выделения из глаз. В тяжелых случаях возникает ощущение жжения, боль и светобоязнь.
Аллергические заболевания, затрагивающие глаз, включают умеренные формы, такие как сезонный аллергический конъюнктивит и круглогодичный аллергический конъюнктивит; и более тяжелые проявления, такие как весенний кератоконъюнктивит; атопический кератоконъюнктивит и конъюнктивит с гиперплазией сосочков. Последние могут быть связаны с осложнениями, такими как повреждение роговицы, и могут вызывать потерю зрения. Сезонный аллергический конъюнктивит и круглогодичный аллергический конъюнктивит обычно представляют собой опосредованную IgE-тучными клетками реакцию гиперчувствительности к внешним аллергенами; в то время как атопический кератоконъюнктивит и весенний кератоконъюнктивит характеризует хроническое воспаление с участием нескольких типов иммунных клеток. Аллергены сезонного аллергического конъюнктивита и круглогодичного аллергического конъюнктивита с помощью антигенпрезентирующих клеток запускают иммунный ответ с преобладанием Th2, который индуцирует высвобождение IgE В-клетками. Активация аллергического ответа обычно включает инфильтрацию и дегрануляцию тучных клеток.
Сезонный аллергический конъюнктивит является наиболее частым аллергическим заболеванием глаз, обычно вызываемым аллергенами, такими как переносимая по воздуху пыльца, пыль и аллергены, содержащиеся в клетках кожи домашних животных. Признаки и симптомы, как правило, возникают в течение весны и лета и, как правило, ослабевают в зимние месяцы. Зуд, покраснение и отек конъюнктивы являются наиболее характерными симптомами, также симптомами являются слезоточивость, ощущение жжения и светобоязнь. В большинстве случаев сезонный аллергический конъюнктивит не является серьезным состоянием. Однако он может очень беспокоить пациентов, поскольку влияет на качество жизни и может иметь большое социоэкономическое значение (Kari O. And Saari KM, 2010).
Круглогодичный аллергический конъюнктивит является вторым по распространенности аллергическим заболеванием глаз, обычно вызываемым животными или клещами. Симптомы и признаки в основном такие же, как при сезонном аллергическом конъюнктивите, отличие в конкретных аллергенах, к которым у пациента есть аллергия, и то, что круглогодичный аллергический конъюнктивит может возникать на протяжении всего года при контакте с постоянными аллергенами. Круглогодичный аллергический конъюнктивит возникает во всех возрастных группах, но чаще в молодом или среднем возрасте у людей обоих полов. Кроме того, круглогодичный аллергический конъюнктивит часто связан с синдромом сухости глаз.
Сезонный аллергический конъюнктивит и круглогодичный аллергический конъюнктивит являются наиболее распространенными формами аллергических заболеваний глаз. Оценки варьируют, но считается, что эти типы аллергии поражают по меньшей мере 15-20% всей популяции. Сезонный аллергический конъюнктивит и круглогодичный аллергический конъюнктивит зачастую не диагностируют и, следовательно, не долечивают. При сезонном аллергическом конъюнктивите и круглогодичном аллергическом конъюнктивите индуцированное аллергеном локальное высвобождение IgE стимулирует дегрануляцию тучных клеток посредством Са2+-зависимого механизма. Активированные IgE тучные клетки высвобождают заранее образованные медиаторы воспаления, такие как гистамин и лейкотриен 4, являющиеся первыми медиаторами аллергической реакции. Эти медиаторы привлекают эозинофилы, которые проникают в очаг, усиливая аллергическую реакцию.
Весенний кератоконъюнктивит является относительно редким хроническим аллергическим воспалением окулярной поверхности которое в основном поражает детей и подростков. Основными симптомами являются зуд, покраснение, отек, выделения из глаз и светобоязнь. Наиболее характерным признаком является разрастание сосочков в верхней тарзальной конъюнктиве.
Атопический кератоконъюнктивит является билатеральным хроническим воспалительным заболеванием окулярной поверхности и века. Наиболее характерными признаками являются экзематозные зудящие очаги на веке. Нередко у пациентов в раннем возрасте была операция по удалению катаракты [Kari O. and Saari KM, 2010).
Конъюнктивит с гиперплазией сосочков является воспалительным заболеванием, характеризующимся гипертрофией сосочков верхней тарзальной конъюнктивы. Конъюнктивит с гиперплазией сосочков вызывают скорее инертные вещества, чем аллергены. При удалении этих раздражающих стимулов изменения сосочков конъюнктивы проходят. Отложение белков на поверхности контактных линз может стать антигенным и стимулировать образование IgE (La Rosa M. et al., 2013).
Современное лечение аллергического заболевания глаз включает нефармакологические и фармакологические стратегии. Избегание антигена является первичной модификацией поведения при всех типах аллергических заболеваний глаз. Искусственные заменители слезной жидкости выполняют барьерную функцию и помогают улучшить защиту первой линии на уровне слизи конъюнктивы. Если нефармакологические стратегии не обеспечивают адекватное уменьшение симптомов, можно применять фармакологическое лечение.
Главное направление контроля аллергического заболевания глаз включает применение противоаллергических терапевтических агентов, таких как противогистаминные, средства двойного действия или комбинированные средства и стабилизаторы тучных клеток. Местные противогистаминные средства (такие как эмедастин и левокабастин) конкурентно и обратимо блокируют гистаминовые рецепторы и ослабляют зуд и покраснение, но лишь на короткий период. Антигистаминные средства влияют на другие провоспалиительные медиаторы, которые остаются заингибированными. Ограниченная продолжительность действия требует частого введения, а местные антигистаминные средства могут раздражать глаз, особенно при длительном применении.
Комбинированное лечение с применением противоотечных средств (таких как оксиметазолин, тетрагидрозолин и нафазонлин) в комбинации с антигистаминными средствами действует как сосудосуживающее, но, известно, что оно может вызвать болезненность и жжение при инстилляции. Другие побочные явления включают расширение зрачка и реактивную гиперемию, что делает эти комбинированные средства более подходящими для краткосрочного применения. Кроме того, эти лекарственные средства не рекомендованы для применения у пациентов с закрытоугольной глаукомой. Стабилизаторы тучных клеток (такие как кромогликат, лодоксамид, недокромил) имеют неясный механизм действия. Они не облегчают существующие симптомы, и их можно применять только в профилактических целях для предотвращения дегрануляции тучных клеток при последующем контакте с аллергеном. Им требуется период нагрузки, в течение которого необходимо вводить их перед контактом с антигеном (La Rosa M. et al., 2013).
Если упомянутые выше противоаллергические лекарственные средства не обеспечивают адекватный контроль аллергического воспалительного процесса, применяют противовоспалительные агенты. Кортикостероиды остаются среди наиболее сильных фармакологических агентов, применяемых при более тяжелых вариантах аллергического заболевания глаз (La Rosa M. et al., 2013). Однако стероидные лекарственные средства обладают побочными эффектами, которые угрожают здоровью пациента в целом. Хроническое введение кортикостероидов может вызвать медикаментозный остеопороз за счет подавления всасывания кальция в кишечнике и ингибирования формирования кости. Другие побочные эффекты хронического введения кортикостероидов включают гипертензию, гипергликемию, гиперлипидемию (повышенные уровни триглицеридов) и гиперхолестеринемию (повышенные уровни холестерина) из-за действия этих лекарственных средств на метаболические процессы в организме. Также известно, что определенные кортикостероиды обладают большей способностью повышать внутриглазное давление, чем другие соединения этого класса. Например, известно, что преднизолон, являющийся очень сильным окулярным противовоспалительным агентом, обладает более выраженной способностью повышать внутриглазное давление, чем фторметолон, обладающий умеренной окулярной противовоспалительной активностью. Также известно, что риск повышения внутриглазного давления, связанного с местным офтальмологическим применением кортикостероидов, возрастает с течением времени. Другими словами, хроническое (т.е. продолжительное) применение этих агентов повышает риск значительного повышения внутриглазного давления. Таким образом, кортикостероиды могут не подходить для продолжительного лечения аллергических заболеваний глаз. Кроме того, хроническое применение кортикостероидов противопоказано из-за повышенного риска развития катаракты и глаукомы (Ono SJ, and Abelson MB, 2005).
Иммунотерапия аллергии полезна для снижения ответа на аллергены, но ее роль при аллергическом конъюнктивите не доказана. Основной целью такого лечения является индукция клинической толерантности по отношению к конкретному аллергену. Терапию проводят подкожно с постепенным увеличением доз для поддержания на уровне ниже порогового уровня клинической реакции. Сублингвальную иммунотерапию считают альтернативой подкожной иммунотерапии аллергии и вводят перорально под язык, но отдаленные результаты сублингвальной иммунотерапии еще не доступны. Большинство исследований этой формы терапии были исследованиями аллергического ринита. Как правило, иммунные ответы на введение аллергена не предсказывают эффективность терапии, а сама терапия может вызывать системные реакции, частота и тяжесть которых варьирует в зависимости от типа введенного аллергена (La Rosa M. et al., 2013).
Дополнительно, большинство новых офтальмологических противоаллергических агентов обладает ограниченной продолжительностью действия, и требует введения дозы дважды в день. Местный препарат с более продолжительным действием был бы предпочтительным, поскольку его можно было бы вводить в виде капель один раз в день. Таким образом, существует необходимость в новых видах терапии, предоставляющих преимущества в таких параметрах как эффективность и продолжительность действия, обладая при этом такими же профилями безопасности, как традиционные офтальмологические противоаллергические агенты.
Терапию на основе РНК-интерференции выделяют как способную удовлетворить нереализованные потребности в лечении аллергии (Popescu FD. 2005). Было показано, что системное введение миРНК к CD40 мышам, сенсибилизированным аллергеном, способно ослаблять назальные симптомы аллергии посредством ингибирования функций дендритных клеток и В-клеток и образования регуляторных Т-клеток (Suzuki M. et al., 2009). Кроме того, также разработали аллерген-специфичную терапию аллергического ринита на основе миРНК с помощью сенсибилизированных аллергеном дендритных клеток с подавленной экспрессией CD40 (Suzuki M et al., 2010).
Изменения концентрации свободного внутриклеточного кальция (Ca2+) в клетке регулируют многие биологические функции. Ca2+ сигналы образуются при контролируемом выходе Ca2+ из эндоплазматического ретикулума (ЭР), являющегося основным депо кальция в клетках. Выход кальция из ЭР активирует депо-управляемые Ca2+ каналы (SOC, store-operated) на плазматической мембране, индуцируя депо-управляемый вход Ca2+ в рамках входа внеклеточного кальция в цитоплазму. Недавние исследования подчеркивают важность данного механизма входа Ca2+ для ряда физиологических процессов, включая аллергию (Bergmeier W et al., 2013).
Депо-управляемый вход Ca2+ активируется в ответ на истощение запаса Ca2+ в ЭР.
Активация депо-управляемого входа Ca2+ индуцирует вход Ca2+ из внеклеточных компартментов, опосредованный Ca2+ каналами, регулируемыми высвобождением Ca2+ из депо (CRAC, store-operated Ca2+ release-activated Ca2+) (Hoth M. et al., 1992).
Каналы CRAC состоят из чувствительных к кальцию белков STIM (stromal interaction molecule, молекула стромального взаимодействия) и порообразующих субъединиц, называемых ORAI. В клетках млекопитающих содержатся три ORAI: ORAI1, ORAI2 и ORAI3; хотя ORAI2 и ORAI3 выполняют такую же роль, как и ORAI1, токи Ca2+, образованные этими белками, приблизительно в два-три раза меньше, чем токи, образованные ORAI1 (Smyth J.T. et al., 2006).
ORAI1 является активно экспрессирующимся 33 кДа белком плазматической мембраны с 4 трансмембранными доменами, который активируется кальциевым сенсором молекулой стромального взаимодействия 1 (STIM1, stromal interaction molecule 1), когда депо кальция истощены, и индуцирует вход внеклеточного кальция в цитоплазму через каналы CRAC. ORAI1 также называют модулятором CRAC 1, CRACM1 (CRAC Modulator 1), ORAT1, трансмембранным белком Transmembrane Protein 142A, TMEM142A (Transmembrane Protein 142А) или канальным белком CRAC 1. ORAI1 идентифицировали как основную субъединицу каналов CRAC (Wang Y. et al., 2012).
Растущее число фактов указывает на то, что краткосрочная и долгосрочная активация иммунных клеток при аллергической реакции опосредована входом Ca2+ в иммунные клетки из внеклеточного компартмента. Краткосрочный иммунный ответ включает дегрануляцию тучных клеток и активацию эффекторных цитотоксических Т-клеток. Действительно, дегрануляция тучных клеток, лишенных либо STIM1, либо ORAI1, сильно нарушена (Vig M. et al., 2008; Baba Y. et al 2008). Долгосрочные ответы включают модуляцию экспрессии генов, контролирующих пролиферацию и дифференцировку В- и Т-клеток (Parekh A.B. et al., 2005).
Также предполагают, что ORAI1 важен для эффекторной функции мышиных тучных клеток. Дегрануляция тучных клеток, полученных из лишенных ORAIl мышей, была сильно нарушена, а индукция опосредованного IgE пассивного анафилактического ответа in vivo также зависела от ORAI1. (Vig M, et al., 2008).
Исследовали нокдаун ORAI1 с помощью РНК-интерференции при аллергическом рините. Рекомбинантные лентивирусные векторы, кодирующие кшРНК (короткие шпилечные РНК) против ORAI1, введенные в ноздри сенсибилизированных овальбумином мышей вызывали симптомы аллергического ринита (количество чиханий и потираний носа) (Wang et al., 2012). Ринит развивается в результате назального раздражения или воспаления из-за заложенности. Аллергический ринит представляет собой аллергическое воспаление верхних отделов дыхательных путей, связанное с гиперчувствительностью нескольких типов иммунных клеток (Wang et al., 2012). Однако не все случаи ринита вызваны аллергическими реакциями. Ринит также развивается в ответ на химическое воздействие, в том числе на сигаретный дым, изменение температуры, инфекции и другие факторы.
В другом исследовании подавляли ORAI1 с помощью миРНК для ослабления опосредованной гистамином экспрессии COX-2 и активации NFkB, что указывает на важность опосредованной ORAI активации NFkB как сигнального пути, отвечающего за передачу гистаминовых сигналов, которые запускают воспалительные реакции при аллергическом ответе (Huang WC et al., 2011).
Таким образом, весьма вероятно, что значительная часть воспалительной реакции при аллергическом заболевании глаз опосредована активацией ORAI1.
Существуют патентные документы, ссылающиеся на миРНК для нокдауна ORAI1 для лечения аллергии. В W02010/099401 (Попечительский совет Университета Леланда Стэнфрода (младшего), The Board of Trustees of the Leland Stanford Junior University) описан способ модуляции активности канала CRAC в клетке, где канал CRAC контактирует с аминокислотным остатком домена STIM1, который связывается с ORAI1 и открывает канал CRAC. Среди поддающихся лечению состояний перечислены: аллергия или гиперчувствительность иммунной системы, включая гиперчувствительность замедленного типа и астму. В описании указано, что миРНК можно применять для нарушения экспрессии эндогенного гена для определения эффекта эндогенного гена на модулирование взаимодействия между белками STIM и ORAI.
В W02007/121186 (Королевский медицинский центр, The Queen's Medical Center) описано опосредованное миРНК подавление экспрессии человеческого CRACM1 (ORAI1) в клетках эмбриональной почки человека (HEK293). В этой заявке также указано, что агенты, модулирующие активность канала CRAC через взаимодействие с белком CRACM1 (ORAI1) или нарушение экспрессии CRACM1 (ORAI1) можно применять для модуляции аллергических реакций.
В W02009/095719 (ISIS INNOVATION LIMITED) описаны способы, применение и изделия для применения в лечении нарушений, связанных с активацией тучных клеток, включая комбинации агентов, ингибирующих белок CRACM1(ORAI1), которые могут быть миРНК, и агентов, ингибирующих лейкотриеновую активацию тучных клеток, для применения в лечении аллергических заболеваний, в частности, аллергического ринита.
В US2011/0112058 (Incozen Therapeutics Pvt. Ltd.) описан способ определения кандидатного агента для лечения рака легких, который предпочтительно ингибирует CRACM1/ORAI1. Этот документ также описывает применение миРНК для модуляции пути CRAC/STIM. Этот документ также указывает, что модуляторы канала CRAC, как было заявлено, полезны в лечении, предотвращении и/или облегчении заболеваний или нарушений, связанных с кальциевым каналом, активирующимся высвобождением кальция, включая аллергический ринит и аллергический конъюнктивит.
В US2012/0264231 (Hogan Patrick et al.) описаны способы и системы для идентификации агента, который может быть миРНК, модулирующей вход кальция через канал ORAI и/или регулирующей внутриклеточный кальций посредством канала ORAI, для лечения состояний и заболеваний, связанных с нарушением регуляции кальциевой передачи сигнала, включая аллергический ринит или аллергический конъюнктивит. Важная часть воспалительного ответа при аллергическом заболевании глаз, опосредованная ORAI1, не только является ключевой детерминантой воспалительного ответа, но также имеют отношение к клеточной пролиферации и клеточной миграции. Ингибирование ORAI1 с помощью миРНК в клетках пигментного эпителия сетчатки показало, что ORAI1 вовлечен в опосредованный эпидермальным фактором роста (EGF, epidermal growth factor) рост клеток. В этом исследовании предположили, что ORAI1 может быть потенциальной терапевтической мишенью лекарственных средств, направленных на лечение связанных с EGF нарушений, таких как пролиферативная витреоретинопатия (Yang et al 2013). Витреоретинопатия представляет собой заболевание, развивающееся как осложнение регматогенного отслоения сетчатки, во время которого жидкость из жидкой части стекловидного тела попадает в разрыв в сетчатке. Механизмы образования перфораций или разрывов сетчатки еще не полностью изучены. Скопление жидкости в субретинальном пространстве и тракционная сила стекловидного тела на сетчатке приводят к регматогенному отслоению сетчатки. Во время этого процесса слои клеток сетчатки контактируют с цитокинами стекловидного тела, которые стимулируют пролиферацию и миграцию пигментного эпителия сетчатки в процессе эпителиально-мезенхимального перехода и развивают способность мигрировать внутрь стекловидного тела. Во время этого процесса теряются контакты слоя клеток пигментного эпителия сетчатки с нейронами сетчатки и контакты клеток пигментного эпителия сетчатки с внеклеточным матриксом. Клетки пигментного эпителия сетчатки при миграции откладывают волокнистые мембраны, и эти мембраны сокращаются и тянут сетчатку. Все это в итоге приводит ко вторичной отслойке сетчатки после первичной хирургической отслойки сетчатки.
Краткое содержание изобретения
Настоящее изобретение представляет улучшенные продукты для уменьшения экспрессии ORAI1 и последующего окулярного воспаления при аллергических заболеваниях глаз. Преимуществом лечения аллергических заболеваниях глаз с помощью миРНК продуктов по сравнению с традиционными противоаллергическими терапевтическими агентами и противоаллергическими иммунотерапевтическими лекарственными средствами является то, что лечение на основе миРНК будет обладать более продолжительным эффектом. Это обусловлено тем, что отсутствие эффекторной молекулы вынуждает клетку заново синтезировать новые рецепторы, в то время как традиционные средства лечения оставляют содержание рецепторов на клеточной мембране неизменным.
Отмечается рост количества аллергических заболеваний глаз во всем мире. Особенно в промышленно развитых странах загрязнение окружающей среды считают основным фактором повышения чувствительности аллергиков. В дополнение к повышению выбросов в окружающую среду исследования также указывают на глобальное повышение уровня аллергенов в воздухе. Еще одним фактором является то, что жители бедных стран меньше обращаются за медицинской помощью для лечения аллергических заболеваний глаз, из-за чего частота зарегистрированных случаев заболевания в слаборазвитых странах может быть искусственно занижена.
По данным Американского фонда астмы и аллергии (Asthma and Allergy Foundation in America, AAFA), ежегодные затраты на лечение аллергии в США оценивают приблизительно в 14,5 млн долларов США. По их оценкам 50 миллионов американцев страдают от всех типов аллергии (1 из 5 американцев), включая аллергии на домашние/уличные, пищевые и лекарственные аллергены, латекс, насекомых, аллергические заболевания кожи и глаз. Распространение аллергии в США ускоряется с начала 1980х во всех возрастных, половых и расовых группах.
Несмотря на наличие географических особенностей, терапевты всего мира применяют общие критерии подбора подходящего курса лечения. Эти критерии включают эффективность, безопасность, удобство дозирования и удобство введения пациенту, согласно мнению специалистов из разных стран. Таким образом, на фоне увеличения по всему миру количества пациентов, жалующихся на ряд симптомов аллергических заболеваний глаз, выявление оптимального лечения с каждым днем становится все сложнее и интереснее.
ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фигура 1: показывает короткие фрагменты целевой последовательности гена ORAI1, выбранные в качестве целевых последовательностей миРНК настоящего изобретения.
Фигура 2: показывает олигонуклеотидные последовательности молекул миРНК настоящего изобретения, действующих на ORAI1, включенные в объем настоящего изобретения. SEQ ID NO, указанные на Фигуре, обозначают смысловую цепь (5'->3'); как правило, миРНК вводят в виде дцРНК, и они включают и смысловую, и комплементарную ей антисмысловую цепь. С SEQ ID NO. 112 по SEQ ID NO. 222 представляют собой миРНК, действующие на последовательности с SEQ ID NO. 1 по SEQ ID NO. 111, соответственно. Как правило, миРНК включает смысловую и антисмысловую цепи, а также может содержать неспаренные выступающие динуклеотиды на 3'-конце (например, dTdT). Однако это не является необходимым.
Фигура 3: модифицированные миРНК, действующие на ORAI1. Заданные SEQ ID NO обозначают смысловую (5'->3') цепь модифицированных миРНК ORAI1.
Фигура 4: Уровни экспрессии ORAI1 in vitro после трансфекции SEQ ID NO. 112 в разных клеточных линиях (человеческая A204, мышиная C2C12 и мышиная J744A.1).
Фигура 5: Уровни экспрессии ORAI1 in vitro после трансфекции миРНК, действующих на ORAI1 в мышиной клеточной линии C2C12.
Фигура 6: Уровни токсичности in vitro в разных клеточных линиях после трансфекции SEQ ID NO. 112 в разных клеточных линиях (человеческая A204 и мышиная C2C12).
Фигура 7: Уровни экспрессии человеческого ORAI1 in vitro после трансфекции SEQ ID NO. 112 и ее модифицированными вариантами, SEQ ID NO. 223, SEQ ID NO. 224, SEQ ID NO. 225, SEQ ID NO. 226, SEQ ID NO. 227, SEQ ID NO. 228 и SEQ ID NO. 229, в человеческих клетках A204.
Фигура 8: Уровни экспрессии мышиного ORAI1 in vitro после трансфекции SEQ ID NO. 112 и ее модифицированными вариантами, SEQ ID NO. 223, SEQ ID NO. 224, SEQ ID NO. 225, SEQ ID NO. 226, SEQ ID NO. 227, SEQ ID NO. 228 и SEQ ID NO. 229 в мышиных клетках C2C12.
Фигура 9: показывает дозозависимый эффект SEQ ID NO. 112 (SYL116011) и SEQ ID NO. 227 (SYL116011v8) в человеческих клетках. Трансфекции человеческих клеток A204 возрастающими дозами (от 0,001 до 100 нМ) SEQ ID NO. 112 (SYL116011) и SEQ ID NO. 227(SYL116011v8) и количественное определение % экспрессии гена ORAI1 в результате действия миРНК.
Фигура 10: показывает дозозависимый эффект SEQ ID NO. 112 (SYL116011) и SEQ ID NO. 227 (SYL116011v8) в мышиных клетках. Трансфекции мышиных клеток C2C12 возрастающими дозами (от 0,001 до 100 нМ) SEQ ID NO. 112 (SYL116011) и SEQ ID NO. 227(SYL116011v8) и количественное определение % экспрессии гена ORAI1 в результате действия миРНК.
Фигура 11: показывает экспрессию ORAI1 и его паралогов ORAI2 и ORAI3 после трансфекции SEQ ID NO. 112 (SYL116011) и SEQ ID NO. 227 (SYL116011v8) в человеческих клетках. Трансфекция SEQ ID NO. 112 и SEQ ID NO. 227 в человеческих клетках A204 и количественное определение % экспрессии генов ORAI1, ORAI2 и ORAI3 в результате действия миРНК.
Фигура 12: показывает экспрессию ORAI1 и его паралогов ORAI2 и ORAI3 после трансфекции SEQ ID NO. 112 (SYL116011) и SEQ ID NO. 227 (SYL116011v8) в мышиных клетках. Трансфекция SEQ ID NO. 112 и SEQ ID NO. 227 в мышиных клетках C2C12 и количественное определение % экспрессии генов ORAI1, ORAI2 и ORAI3 в результате действия миРНК.
Фигура 13: показывает выраженность возможных нецелевых эффектов после трансфекции SEQ ID NO. 112 (SYL116011) в человеческих клетках. Трансфекция SEQ ID NO. 112 в человеческих клетках A204 и количественное определение % экспрессии генов ORAI1, MSLN и OLFM12A в результате действия миРНК.
Фигура 14: показывает уровни экспрессии ORAI1 после трансфекции SEQ ID NO. 112 (SYL116011) в крысиных клеточных линиях. Трансфекция SEQ ID NO. 112 в крысиных клетках С6 и количественное определение % экспрессии гена ORAI1 в результате действия миРНК.
Фигура 15: показывает уровни экспрессии ORAI1 после трансфекции SEQ ID NO. 112 (SYL116011) в крысиных клеточных линиях. Трансфекция SEQ ID NO. 112 в крысиных клетках JTC-19 и количественное определение % экспрессии гена ORAI1 в результате действия миРНК
Фигура 16: показывает уровни экспрессии ORAI1 после трансфекции SEQ ID NO. 112 (SYL116011), SEQ ID NO. 233 (SYL116011v11) и SEQ ID NO. 235 (SYL116011v11) в человеческих, мышиных и крысиных клетках.
Фигура 17: Схема in vivo исследования.
Фигура 18: уровни мРНК ORAI1 в цельном глазу мышей в разное время после индукции аллергического заболевания глаз. АН: аллергии нет.
Фигура 19: уровни мРНК TLSP и Tnfrsf9 в мышиной модели аллергии, вызванной пыльцой амброзии. Уровни мРНК выражены как процент от уровней, наблюдаемых перед индукцией аллергии.
Фигура 20: Окулярные клинические признаки, свидетельствующие об аллергическом заболевании глаз. Мышей наблюдали через 1, 3, 6 и 24 ч после индукции аллергического заболевания глаз. Клинические признаки определяли, оценивая следующие параметры по шкале от 0 до 3: отек конъюнктивы и конъюнктивальная инъекция, гиперемия, отек века, выделения из глаза и слезоточивость. Данные выражены в процентах клинической оценки через 1 ч после индукции аллергии в обработанной фосфатно-солевым буфером группе и представляют собой среднее ± стандартная ошибка среднего для 8 животных в случае обработанной фосфатно-солевым буфером группы и для 15 животных в случае обработанной SEQ ID NO. 112 (SYL116011) группы.
Фигура 21: Отек конъюнктивы и слезоточивость в ответ на обработку разными дозами SEQ ID NO. 112 (SYL116011) в мышиной модели аллергии, вызванной пыльцой амброзии. Мышей наблюдали через 1, 3, 6 и 24 ч после индукции аллергического заболевания глаз A) Отек конъюнктивы и B) слезоточивость оценивали по шкале от 0 до 3. Данные выражены в процентах оценки через 1 ч после индукции аллергии в обработанной фосфатно-солевым буфером группе и представляют собой среднее для 8 животных в случае обработанной фосфатно-солевым буфером группы и для 15 животных в случае обработанной SEQ ID NO. 112 (SYL116011) группы.
Фигура 22: Инфильтрация тучных клеток в конъюнктиву века и в бульбарную конъюнктиву в ответ на обработку разными дозами SEQ ID NO. 112 (SYL116011) в мышиной модели аллергии, вызванной пыльцой амброзии. A) Инфильтрация тучных клеток в конъюнктиву века, выраженная как процент от числа тучных клеток, наблюдаемых в обработанных фосфатно-солевым буфером образцах через 3 ч после обработки. B) Инфильтрация тучных клеток в бульбарную конъюнктиву, выраженная как процент от числа тучных клеток, наблюдаемых в обработанных фосфатно-солевым буфером образцах через 3 ч после обработки.
Фигура 23: Инфильтрация эозинофилов в конъюнктиву века и в бульбарную конъюнктиву в ответ на обработку разными дозами SEQ ID NO. 112 (SYL116011) в мышиной модели аллергии, вызванной пыльцой амброзии. A) Инфильтрация эозинофилов в конъюнктиву века, выраженная как процент от числа тучных клеток, в обработанных фосфатно-солевым буфером образцах через 24 ч после обработки. B) Инфильтрация эозинофилов в бульбарную конъюнктиву, выраженная как процент от числа эозинофилов, наблюдаемых в обработанных фосфатно-солевым буфером образцах через 24 ч после обработки.
Фигура 24: Экспрессия TLSP и CD-137 в ответ на обработку разными дозами SEQ ID NO. 112 (SYL116011) в мышиной модели аллергии, вызванной пыльцой амброзии. A) Экспрессия TLSP; B) Экспрессия CD-137 (Tnfrsf9).
Фигура 25: Клинические симптомы, наблюдаемые в разных временных точках после индукции аллергии. Аллергию индуцировали введением окулярной дозы пыльцы амброзии мышам, предварительно обработанным фосфатно-солевым буфером, SEQ ID NO. 227 (SYL116011v8) или левокабастином. Данные представляют среднее для 10 животных в группе.
Фигура 26: Изменение последозовой гиперемии при профилактике SEQ ID NO. 112(SYL116011) по сравнению с Patanol® и профилактикой инертным носителем.
Фигура 27: Изменение последозового косоглазия при профилактике SEQ ID NO. 112 (SYL116011) по сравнению с Patanol® и профилактикой инертным носителем.
Фигура 28: Изменение последозового отека век при профилактике SEQ ID NO. 112 (SYL116011) по сравнению с Patanol® и профилактикой инертным носителем.
Фигура 29: Изменение последозового выделения из глаз при профилактике SEQ ID NO. 112 (SYL116011) по сравнению с Patanol® и профилактикой инертным носителем.
Подробное описание изобретения
В первом аспекте настоящее изобретение относится к получению молекулы миРНК для применения в качестве лекарственного средства в лечении и/или предотвращении состояния глаз, характеризующегося повышенной экспрессией и/или активностью ORAI1, где указанная молекула специфично действует на последовательность, выбранную из группы, состоящей из SEQ ID NO. 1 - SEQ ID NO. 111, и уменьшает экспрессию гена ORAI1 при попадании в клетку. Целевую последовательность предпочтительно выбирают из группы, состоящей из последовательностей SEQ ID NO. 1 - SEQ ID NO. 14, более предпочтительно, SEQ ID NO. 1 - SEQ ID NO. 8, и еще более предпочтительно, чтобы целевая последовательность содержала или состояла из SEQ ID NO. 1.
На ген «действует» миРНК в соответствии с настоящим изобретением когда, например, молекула миРНК селективно уменьшает или ингибирует экспрессию гена. Фраза «селективно уменьшает или ингибирует», как применяют в настоящей заявке, охватывает миРНК, которые нарушают экспрессию одного гена, в данном случае ORAI1. Альтернативно, миРНК действует на ген, когда (одна цепь) миРНК гибридизуется в строгих условиях с транскриптом гена, т.е. в его мРНК. Гибридизация «в строгих условиях» обозначает отжиг в целевой области мРНК в стандартных условиях, напр., при высокой температуре и/или низком содержании соли, которая обычно ухудшает гибридизацию. Подходящий протокол (с применением 0,1×SSC, 68°C в течение 2 часов) описан в Maniatis, T., et al., Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Laboratory, 1982, at pages 387-389.
Нуклеиновые кислоты, которые приведены в настоящей заявке, написаны в направлении от 5'- к 3'-концу, если иное не указано. Термин «нуклеиновая кислота» обозначает либо ДНК, либо РНК, либо их модифицированную форму, содержащую пуриновые или пиримидиновые основания, присутствующие в ДНК (аденин (A, adenine), цитозин (C, cytosine), гуанин (G, guanine), тимин (T, thymine)) или в РНК (аденин (A, adenine), цитозин (C, cytosine), гуанин (G, guanine), урацил (u, uracil)). Интерферирующие РНК, представленные в настоящей заявке, могут включать «Т» основания, например, на 3'-концах, даже несмотря на то, что основания «Т» не встречаются в РНК в природе. В некоторых случаях эти основания указаны как «dT», чтобы отличить дезоксирибонуклеотиды, присутствующие в цепочке рибонуклеотидов.
Целевая последовательность, как определено выше, описана как целевая последовательность ДНК, как применяют для определения вариантов транскриптов в базах данных, применяемых для создания миРНК, где конкретные применяемые соединения будут последовательностями РНК, определенными таким образом.
Специалист в данной области техники может получить доступ к любой последовательности целевого гена через базы данных общего пользования. Например, учетный номер в GenBank, соответствующий мРНК человеческого ORAI1, - это NM_032790 (Gene ID: 84876). Учетный номер гомолога в GenBank, соответствующий мРНК мышиного ORAI1, - это NM_175423 (Gene ID: 109305). Более того, в базе ENSEMBL (MBL-EBI/Wellcome Trust Sanger Institute) содержится следующие учетные номера человеческого и мышиного ORAI1: ENSG00000182500 и ENSMUSGO0000049686, соответственно. Общедоступные транскрипты мРНК человеческого ORAI1 - это ENST00000330079 и ENST00000537188.
Указанная предпочтительная целевая область, определенная настоящим изобретением, содержит или состоит из по меньшей мере одной последовательности, выбираемой из группы, состоящей из последовательностей с SEQ ID NO. 1 по SEQ ID NO. 111.
В предпочтительном варианте осуществления настоящего изобретения указанная предпочтительная целевая область содержит или состоит из по меньшей мере одной последовательности, выбираемой из группы, состоящей из последовательностей с SEQ ID NO. 1 по SEQ ID NO.14.
В другом предпочтительном варианте осуществления настоящего изобретения указанная предпочтительная целевая область содержит или состоит из по меньшей мере одной последовательности, выбираемой из группы, состоящей из последовательностей с SEQ ID NO. 1 по SEQ ID NO.8. Эти последовательности являются на 100% гомологичными в следующих видах: Homo sapiens, Mus musculus, Canis lupus familiaris и Rattus norvegicus.
В области РНК-интерференции после демонстрации в in vitro исследованиях отсутствия способности человеческих миРНК вызвать нокдаун гена модельного животного, синтезируют суррогатное соединение (активный в животных аналог) для анализа эффективности миРНК в соответствующей животной модели. Этот суррогат конструируют к той же области, за исключением нескольких нуклеотидов в зависимости от гомологии между человеческим и кроличьим целевым геном. Этот подход широко применяли для разработки других олигонуклеотидов, в частности для токсикологических исследований (Kornbrust D. et al., 2013).
В более предпочтительном варианте осуществления настоящего изобретения указанная предпочтительная целевая область содержит или состоит из SEQ ID NO. 1 (5'-TGATGAGCCTCAACGAGCA-3').
Следовательно, миРНК в соответствии с аспектами настоящего изобретения будет предпочтительно содержать двухцепочечную молекулу РНК, антисмысловая цепь которой будет содержать последовательность РНК, в основном комплементарную по меньшей мере одной последовательности, выбираемой из группы, состоящей из SEQ ID NO. 1 - SEQ ID NO. 111, а смысловая цепь будет содержать последовательность РНК, комплементарную антисмысловой цепи, где обе цепи гибридизуются посредством стандартного спаривания оснований нуклеотидов. Более предпочтительно, чтобы миРНК в соответствии с аспектами настоящего изобретения предпочтительно содержала двухцепочечную молекулу РНК, антисмысловая цепь которой содержит последовательность РНК, в основном комплементарную последовательности, выбираемой из группы, состоящей из SEQ ID NO. 1 - SEQ ID NO. 8, и еще предпочтительнее, состоящей из SEQ ID NO. 1.
Как определено настоящим изобретением, «в основном комплементарный» последовательности целевой мРНК можно также понимать как «в основном идентичный» указанной целевой последовательности. «Идентичность», как понимают специалисты в данной области техники, представляет собой степень родства последовательности нуклеотидных последовательностей, как определено при сопоставлении положения и идентичности нуклеотидов последовательностей. В одном варианте осуществления настоящего изобретения антисмысловую цепь миРНК, имеющую 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%,95%, 96%, 97%, 98% или 99% комплементарности последовательности целевой мРНК, считают в основном комплементарной, и ее можно применять в настоящем изобретении. Процент комплементарности описывает процент непрерывной последовательности нуклеотидов в первой молекуле нуклеиновой кислоты, которые могут образовывать пары по Уотсону-Крику с рядом непрерывных нуклеотидов во второй молекуле нуклеиновой кислоты. В предпочтительном варианте осуществления настоящего изобретения антисмысловая цепь миРНК является на 100% комплементарной целевой последовательности мРНК, а смысловая цепь миРНК является на 100% комплементарной антисмысловой на протяжении двухцепочечной части миРНК. Также миРНК может содержать выступающие неспаренные нуклеотиды на концах, например, выступающие неспаренные динуклеотиды на 3'-конце, предпочтительно, dTdT.
В предпочтительном варианте осуществления настоящего изобретения указанное состояние глаз, определенное настоящим изобретением, является аллергическим заболеванием глаз и/или окулярным конъюнктивитом. Более предпочтительно, чтобы указанное состояние глаз выбирали из сезонного аллергического конъюнктивита, круглогодичного аллергического конъюнктивита, весеннего кератоконъюнктивита, атопического кератоконъюнктивита, конъюнктивита с гиперплазией сосочков, синдрома сухости глаз и их комбинаций.
В соответствии с известным в данном уровне техники, было предложено множество разных структур для РНК-интерференции. Как правило, эти двухцепочечные молекулы составляют в длину приблизительно от 19 до приблизительно 25 нуклеотидов и содержат структуры с тупыми концами, а также с выступающими неспаренными концами. Было описано, что выступающие неспаренные концы являются преимуществом и могут присутствовать на 5'-концах или на 3'-концах любой из цепей, поскольку они снижают узнавание РНКазами и имитируют природный субстрат для Dicer. Некоторые авторы рекомендуют включать выступающие неспаренные концы на обоих 3'-концах молекул, в то время как другие считают достаточным один выступающий неспаренный конец. Другие описывают применение структур с тупыми концами со специфичными профилями модификаций (EP 1527176, WO 2005/062937, WO 2008/104978, EP 2322617, EP 2348133, US 2013/0130377 и многие другие).
Выступающие неспаренные концы могут состоять из от 1 до 5 нуклеотидов; как правило, выступающие неспаренные концы состоят из динуклеотидов. Классические молекулы, применяемые в данной области, содержат 19-нуклеотидную двухцепочечную молекулу, которая также содержит динуклеотидные выступающие неспаренные концы на 3'-конце, предпочтительно содержащие динуклеотиды, как описано в оригинальных исследованиях Tuschl (WO02/44321). Эти выступающие неспаренные концы еще больше увеличивают сопротивляемость деградации нуклеазами (РНКазой). Позднее Kim et al., 2005 описали, что 21-мерные продукты (содержащие динуклеотидные выступающие неспаренные концы) необходимы для связывания с RISC. Также Bramsen et al. 2009 описали, что введение возможных дестабилизирующих модификаций в выступающие неспаренные концы далее увеличивает эффективность подавления экспрессии.
Таким образом, предпочтительный вариант осуществления различных аспектов настоящего изобретения относится к молекулам миРНК, действующим по меньшей мере на одну последовательность, выбираемую из группы, состоящей из SEQ ID NO. 1 - SEQ ID NO.111, содержащую по меньшей мере один выступающий неспаренный конец. Предпочтительнее, чтобы указанные молекулы миРНК действовали по меньшей мере на одну последовательность, выбираемую из группы, состоящей из SEQ ID NO. 1 - SEQ ID NO.8, и еще предпочтительней, состоящей из SEQ ID NO. 1. Там, где настоящее изобретение относится к молекуле миРНК, действующей по меньшей мере на одну последовательность, выбираемую из группы, состоящей из SEQ ID NO. 1 - SEQ ID NO.111, миРНК будет включать антисмысловую цепь эквивалентной длины и комплементарную мишени и смысловую цепь эквивалентной длины и комплементарную антисмысловой цепи. Антисмысловая и смысловая цепи могут также содержать дополнительные основания, не комплементраные другой цепи или мишени и/или неспаренные в двухцепочечной части миРНК. Например, SEQ ID NO 1 является 19-нуклеотидной последовательностью; миРНК может включать двухцепочечный участок из 19 п.о. (пар оснований), соответствующий этой части последовательности и динуклеотидные выступающие неспаренные концы.
Предпочтительный вариант осуществления различных аспектов настоящего изобретения относится к молекулам миРНК, действующим по меньшей мере на одну последовательность, выбираемую из группы, состоящей из SEQ ID NO. 1 - SEQ ID NO.111, где каждая цепь двухцепочечной молекулы миРНК составляет приблизительно от 18 до приблизительно 28 или более (напр., около 18, 19, 20, 21, 22, 23, 24, 25, 26, 27 или 28 или более) нуклеотидов в длину.
Другой предпочтительный вариант осуществления различных аспектов настоящего изобретения относится к молекулам миРНК длиной 18-28 нуклеотидов или более, содержащих нуклеотидную последовательность, выбираемую из группы, состоящей из SEQ ID NO. 112 - SEQ ID NO. 229. Предпочтительнее, чтобы двухцепочечные молекулы миРНК были по меньшей мере 19 нуклеотидов в длину и, чтобы их выбирали из группы, состоящей из SEQ ID NO. 112 - SEQ ID NO. 229.
Другой альтернативный вариант осуществления различных аспектов настоящего изобретения относится к молекулам с тупыми концами.
Также предпочтительный вариант осуществления настоящего изобретения относится к миРНК, содержащей или состоящей из 19-нуклеотидной двухцепочечной структуры, действующей по меньшей мере на одну последовательность, выбираемую из группы, состоящей из SEQ ID NO. 1 - SEQ ID NO. 111. Предпочтительнее, чтобы миРНК содержала или состояла из 19-нуклеотидной двухцепочечной структуры, действующей по меньшей мере на одну последовательность, выбираемую из группы, состоящей из SEQ ID NO. 1 - SEQ ID NO. 8, и еще предпочтительнее, состоящей из SEQ ID NO. 1.
Частный вариант осуществления настоящего изобретения относится к 19-нуклеотидным двухцепочечным миРНК с тупыми концами, действующим по меньшей мере на одну последовательность, выбираемую из группы, состоящей из SEQ ID NO. 1 - SEQ ID NO. 111. Предпочтительнее, чтобы миРНК действовала по меньшей мере на одну последовательность, выбираемую из группы, состоящей из SEQ ID NO. 1 - SEQ ID NO. 8, и, еще предпочтительнее, состоящей из SEQ ID NO. 1. В следующем частном варианте осуществления настоящего изобретения данное соединение содержит или состоит из по меньшей мере одной последовательности, выбираемой из группы, состоящей из SEQ ID NO: 112 - SEQ ID NO. 229. В следующем предпочтительном варианте осуществления настоящего изобретения антисмысловая цепь этой миРНК является по меньшей мере на 80%, предпочтительно, по меньшей мере на 90% комплементарной по меньшей мере одной последовательности, выбираемой из группы, состоящей из SEQ ID NO. 1 - SEQ ID NO. 111.
В предпочтительном варианте осуществления настоящего изобретения данное соединение содержит или состоит из по меньшей мере одной последовательности, выбираемой из группы, состоящей из SEQ ID NO. 112 - SEQ ID NO. 119.
В более предпочтительном варианте осуществления настоящего изобретения данное соединение содержит или состоит из SEQ ID NO. 112 (5'- UGAUGAGCCUCAACGAGCA -3'), соответствующей смысловой цепи нашего контрольного соединения SYL1160011.
Более того, как описано в разделе «Предшествующий уровень техники», важной проблемой молекул миРНК является их нестабильность в биологических жидкостях из-за повсеместной распространенности РНКаз. Следовательно, было описано применение многих различных химических модификаций нуклеотидов с целью увеличения стабильности соединения.
Другой характерной проблемой молекул миРНК является их иммуногенность, из-за которой, как было обнаружено, миРНК вызывают неспецифичную активацию врожденного иммунитета, включая повышение уровня определенных цитокинов, напр., образования интерферона типа I и/или типа II, а также IL-12, IL-6 и/или TNF-α (Tumor Necrosis Factor alpha, фактор некроза опухоли альфа). Источником этих эффектов считают активацию Toll-подобных рецепторов, таких как TLR7, TLR8 и/или TLR3, посредством миРНК.
Также было описано, что оба эффекта, узнавание РНКазами и иммуногенность, зависят от последовательности.
Некоторые химические модификации, увеличивающие стабильность соединения за счет снижения чувствительности к РНКазам, также способны уменьшать индукцию иммунного распознавания в рамках последующего ответа. Однако введение химически модифицированных нуклеотидов в миРНК также может привести к снижению эффективности подавление экспрессии, как описано в предыдущем разделе, и, следовательно, применять его следует с осторожностью.
Следовательно, в предпочтительном варианте осуществления различных аспектов настоящего изобретения миРНК также включает по меньшей мере один нуклеотид с химической модификацией.
Предпочтительные химические модификации, увеличивающие стабильность и снижающие иммуногенные эффекты, включают 2'-O-метилнуклеотиды, 2'-фторнуклеотиды, 2'-аминонуклеотиды, 2'-дезоксинуклеотиды или нуклеотиды, содержащие 2'-0 или 4'-C-метиленовые мостики. Другие предпочтительные химические модификации для защиты от экзонуклеаз включают ExoEndoLight (EEL): модификацию всех пиримидинов в смысловой цепи до 2'-O-метиловых остатков и модификации всех пиримидинов в мотиве 5'-UA-3' или 5'-CA-3' в антисмысловой цепи. Дополнительно положение 1 смысловой цепи также можно заменить на 2'-O-метил, что предотвращает 5'-фосфорилирование смысловой цепи и таким образом увеличивает специфичность миРНК далее инактивируя смысловую цепь. Дополнительно смысловая цепь также может включать 2'-O-метиловую модификацию в положении 14, поскольку 2'-0-Me в этом положении далее инактивирует смысловую цепь и таким образом повышает специфичность миРНК. Дополнительно, другие предпочтительные модификации для защиты от экзонуклеаз включают метилфторовую защиту, при которой чередуются 2'-фторовые и 2'-O-метиловые модификации, начинающиеся (на 5'-конце) с 2'-F в смысловой цепи и начинающиеся с 2'-0-Me в антисмысловой цепи. Дополнительно, положение 1 в смысловой цепи также можно заменить 2'-0-Me, а положение 1 в антисмысловой цепи - 2'-F (поскольку его можно эффективно 5'-фосфорилировать). Также можно внести модификацию рибонуклеотидного остова, соединяющего соседние нуклеотиды, посредством введения модифицированных тиофосфатом нуклеотидов. Следующая предпочтительная модификация в объеме настоящего изобретения относится к замене урациловых рибонуклеотидов дезокситимидином (дезоксирибонуклеотидами). В другом предпочтительном варианте осуществления настоящего изобретения по меньшей мере один химически модифицированный нуклеотид содержится в смысловой цепи, в антисмысловой цепи или в обеих цепях миРНК.
Соответственно, в одном варианте осуществления настоящего изобретения миРНК содержит или состоит по меньшей мере из одной последовательности, выбираемой из группы, состоящей из SEQ ID NO. 223 - SEQ ID NO. 229.
Молекулы миРНК, как описано выше, можно доставлять внутрь клетки в виде нативных структур, применяя способы, известные в данной области техники. Например, при исследовании подавления экспрессии гена in vitro эти соединения вводят с помощью стандартных трансфекционных реагентов.
Для развития эффектов in vivo эти соединения также можно вводить сами по себе или с помощью агентов, способствующих доставке, таких как, например, липосомы, с помощью конъюгации со специфичной функциональной группой и т.п., хотя в данной области техники известно много разных вариантов, которые применяют по-разному в зависимости от локализации желаемой мишени в организме.
Альтернативно, молекулы миРНК различных аспектов настоящего изобретения можно экспрессировать в клетках с эукариотических промоторов. Рекомбинантные векторы, способные экспрессировать молекулы миРНК можно доставлять в клетки-мишени, где они могут сохраняться. Альтернативно, можно применять векторы, обеспечивающие транзиентную экспрессию молекул нуклеиновых кислот. Такие векторы по необходимости можно вводить повторно. После экспрессии молекула миРНК взаимодействует с целевой мРНК и запускает ответ по механизму РНК-интерференции. Молекулы миРНК, образующиеся таким способом, часто называют кшРНК (короткими шпилечными РНК), а их смысловая и антисмысловая цепи соединены небольшой петлей нуклеотидов. Доставка векторов, экспрессирующих молекулы миРНК, может быть системной, такой как внутривенное или внутримышечное введение, посредством введения в извлеченные из организма клетки-мишени и последующим введением обратно в организм или с помощью любых других способов, обеспечивающих введение в желаемую целевую клетку.
Следующий аспект настоящего изобретения относится к применению миРНК, действующей по меньшей мере на одну последовательность, выбираемую из группы, состоящей из SEQ ID NO. 1 - SEQ ID NO. 111, в препарате лекарственного средства для применения в способе лечения состояния глаза, характеризующегося повышенной экспрессией и/или активностью ORAI1. Предпочтительнее, чтобы указанную по меньшей мере одну последовательность выбирали из группы, состоящей из SEQ ID NO. 1 - SEQ ID NO. 8, и еще предпочтительнее, чтобы указанная по меньшей мере одна последовательность состояла из SEQ ID NO. 1. Способ включает ингибирование экспрессии ORAI1 у пациента. Термин «ингибирование» применяют для обозначения снижения или подавления экспрессии или активности. Предпочтительно, чтобы состояние глаза было аллергическим заболеванием глаз и/или конъюнктивитом. В одном варианте осуществления настоящего изобретения состояние глаза выбирают из группы, состоящей из сезонного аллергического конъюнктивита, круглогодичного аллергического конъюнктивита, весеннего кератоконъюнктивита, атопического кератоконъюнктивита, конъюнктивита с гиперплазией сосочков, синдрома сухости глаз и их комбинаций.
Также представлен способ лечения состояния глаза, характеризующегося повышенной экспрессией и/или активностью ORAI1. Способ включает ингибирование экспрессии ORAI1 у пациента. Способ может включать введение миРНК, действующей по меньшей мере на одну последовательность, выбираемую из группы, состоящей из SEQ ID NO. 1 - SEQ ID NO. 111. Предпочтительнее, чтобы указанную по меньшей мере одну последовательность выбирали из группы, состоящей из SEQ ID NO. 1 - SEQ ID NO. 8, и еще предпочтительнее, чтобы указанная по меньшей мере одна последовательность состояла из SEQ ID NO. 1.
В некоторых странах комбинация хронического аллергического конъюнктивита и синдрома сухости глаз является достаточно распространенной. Растущая проблема сухости глаз обусловлена распространенным искусственным кондиционированием воздуха, загрязняющими веществами в помещении и на улице и другими неизвестными причинами. Пациенты с синдромом сухости глаз большей степени подвержены аллергическим заболеваниям глаз, поскольку слезная пленка является важным барьером, препятствующим контактированию аллергенов с тучными клетками.
Ожидают, что терапевтическая обработка миРНК, действующими на мРНК ORAI1 будет обладать преимуществами по сравнению с малыми молекулами глазных капель для местного применения, увеличивая продолжительность эффекта, что позволяет уменьшить частоту дозирования и улучшить соблюдение пациентом схемы лечения. Это особенно важно в таких случаях, как аллергические заболевания глаз и/или конъюнктивит, включающий, но не ограничивающийся весенним кератоконъюнктивитом, атопическим кератоконъюнктивитом и конъюнктивитом с гиперплазией сосочков, поскольку часто они являются хроническими состояниями.
Принимая во внимание получение такого лекарственного средства, миРНК различных аспектов настоящего изобретения можно выпускать в виде фармацевтической композиции. Предпочтительно, чтобы композиции и составы указанных миРНК можно было вводить местно в заданный орган. В еще более предпочтительном варианте осуществления настоящего изобретения их можно составлять в форме для местного применения в глазах, предпочтительно, на поверхности роговицы глаза. Применение на поверхности роговицы глаза может быть, например, в форме глазных капель, геля, лосьона, крема или офтальмологических вкладок. Другие формы введения в глаз могут включать инъекцию в глаз.
Следующий предпочтительный вариант осуществления различных аспектов настоящего изобретения относится к миРНК, специфично действующей по меньшей мере на одну последовательность, выбираемую из группы, состоящей из SEQ ID NO. 1 - SEQ ID NO. 111, как описано в предыдущих параграфах, для применения в качестве лекарственного средства для лечения состояния глаза, характеризующегося повышенной экспрессией и/или активностью ORAI1. Предпочтительнее, чтобы указанную по меньшей одну последовательность выбирали из группы, состоящей из SEQ ID NO. 1 - SEQ ID NO. 8, и еще предпочтительнее, чтобы указанная по меньшей мере одна последовательность состояла из SEQ ID NO. 1. Как описано выше, это может быть миРНК, содержащая или состоящая из 19-нуклеотидной двухцепочечной структуры, действующая по меньшей мере на одну последовательность, выбираемую из группы, состоящей из SEQ ID NO. 1 - SEQ ID NO. 111. Эта мРНК может быть с тупыми концами. Предпочтительно, чтобы миРНК содержала или состояла из по меньшей мере одной последовательности, выбираемой из группы, состоящей из SEQ ID NO. 112 - SEQ ID NO. 229. Другие миРНК для применения в соответствии с настоящим изобретением содержат или состоят из по меньшей мере одной последовательности, выбираемой из группы, состоящей из SEQ ID NO. 223 - SEQ ID NO. 229.
В контексте настоящего изобретения для «специфичного действия» на последовательность миРНК настоящего изобретения, предпочтительно, содержит по меньшей мере такую же затравочную последовательность. Таким образом, любая последовательность в соответствии с настоящим изобретением, которая специфично действует по меньшей мере на одну последовательность, выбираемую из группы, состоящей из SEQ ID NO. 1 - SEQ ID NO. 111, предпочтительно, является идентичной в положениях 2-8 антисмысловой цепи. Предпочтительнее, чтобы указанную по меньшей мере одну последовательность выбирали из группы, состоящей из SEQ ID NO. 1 - SEQ ID NO. 8, и еще предпочтительнее, чтобы указанная по меньшей мере одна последовательность состояла из SEQ ID NO. 1.
Независимо от изложенного выше миРНК различных аспектов настоящего изобретения можно применять для подавления экспрессии ORAI1 в тканях, отличных от глаза. Следовательно, указанные миРНК необходимо составлять в соответствующей форме.
Например, молекула миРНК может содержать инертный носитель для доставки, включая липосомы, для введения субъекту. Носители, растворители и их соли могут присутствовать в виде фармацевтически приемлемых составов. Молекулы нуклеиновой кислоты можно вводить в клетки с помощью ряда способов, известных специалистам в данной области техники, включая, но не ограничиваясь энкапсулированием в липосомы, ионофорезом или включением в состав других инертных носителей, таких как биодеградируемые полимеры, гидрогели, циклодекстриновые поликислоты (сополимер молочной и гликолевой кислот (PLGA, poly (lactic-co-glycolic) acid)) и PLCA микросферы, биодеградируемые нанокапсулы и биоадгезивные микросферы, или посредством белковых векторов. В одном варианте осуществления настоящего изобретения молекулу миРНК доставляют с помощью клеточно-специфичного носителя миРНК, сочетающего компоненты вируса гепатита В и липосомы. В другом варианте осуществления настоящего изобретения молекулы нуклеиновых кислот настоящего изобретения также можно составлять в форме или в комплексе с полиэтиленимином и его производными, такими как полиэтиленимин-полиэтиленгликоль-N-ацетилгалактозаминовых (PEI-PEG-GAL, polyethyleneimine-polyethyleneglycol-N-acetylgalactosamine) или полиэтиленимин-полиэтиленгликоль-три-N-ацетилгалактозаминовых (PEI-PEG-triGAL, polyethyleneimine-polyethyleneglycol-tri-N-acetylgalactosamine) производных. Предпочтительными композициями настоящего изобретения являются водные растворы, в частности солевые растворы, такие как фосфатно-солевой буфер с диапазоном pH от приблизительно 7,0 до приблизительно 7,4, предпочтительно, с pH равным 7,2±0,5.
Молекула миРНК настоящего изобретения может образовывать комплекс с разрушающими мембрану агентами и/или молекулами катионных липидов или вспомогательных липидов.
Системы доставки, которые можно применять с настоящим изобретением включают, например, водные и неводные гели, крема, гетерогенные эмульсии, микроэмульсии, липосомы, мази, водные и неводные растворы, лосьоны, аэрозоли, углеводородные основы и порошки, и могут содержать эксципиенты, такие как солюбилизаторы, усилители проницаемости (напр., жирные кислоты, сложные эфиры жирных кислот, жирные спирты и аминокислоты) и гидрофильные полимеры (напр., поликарбофил и поливинилпиролидон). В одном варианте осуществления настоящего изобретения фармацевтически приемлемый носитель является липосомой или усилителем трансдермального проникновения.
Фармацевтический состав настоящего изобретения находится в форме, подходящей для введения, напр., системного или местного введения в клетку или в субъекта, включая, например, человека. Подходящие формы частично зависят от применения или способа введения, например, перорального, трансдермального или посредством инъекции. Другие факторы известны в данной области техники и включают такие особенности, как токсичность и формы, которые препятствуют проявлению эффекта композиции или состава.
Настоящее изобретение также включает композиции, полученные для хранения или введения, включающие фармацевтически эффективное количество заданных соединений в фармацевтически приемлемом носителе или растворителе. Приемлемые носители или растворители для терапевтического применения хорошо известны в фармацевтической области техники. Например, можно применять консерванты, стабилизаторы, красители и ароматизаторы. Такие агенты включают бензоат натрия, сорбиновую кислоту и сложные эфиры п-гидроксибензойной кислоты. Дополнительно, можно применять антиоксиданты и суспендирующие агенты.
Фармацевтически приемлемой дозой является доза, необходимая для предотвращения, ингибирования возникновения или для лечения (уменьшения симптома до некоторого уровня, предпочтительно, всех симптомов) болезненного состояния. Фармацевтически приемлемая доза, как правило, зависит от типа заболевания, применяемой композиции, способа введения, типа млекопитающего, подлежащего лечению, физических характеристик конкретного рассматриваемого млекопитающего, сопутствующей терапии и других факторов, известных специалистам в данной области техники.
Терапевтически эффективное количество также может обозначать количество миРНК, достаточное для задержки или минимизации начала окулярного нарушения, ассоциированного с аллергическим заболеванием глаз. Терапевтически эффективное количество также может обозначать количество терапевтического агента, оказывающее терапевтический эффект при лечении или контроле окулярного нарушения, ассоциированного с аллергическим заболеванием глаз. Также терапевтически эффективное количество в отношении миРНК настоящего изобретения обозначает количество только терапевтического агента или терапевтического агента в комбинации с другими лекарственными средствами, оказывающими терапевтический эффект при лечении или контроле окулярного нарушения, ассоциированного с аллергическим заболеванием глаз. При применении в связи с количеством миРНК настоящего изобретения данный термин может охватывать количество, которое улучшает терапию в целом, снижает или предотвращает нежелательные эффекты или увеличивает терапевтическую эффективность или оказывает синергическое действие с другим терапевтическим агентом.
Терапевтическим эффектом при лечении или контроле окулярного нарушения, такого как аллергическое заболевание глаз, является продолжительное уменьшение симптомов аллергии. Учитывая, что миРНК снизит уровень ORAI1 в клетке, после прекращения лечения клетке придется заново синтезировать новые белки. Таким образом, терапия на основе миРНК будет оказывать более продолжительное действие. Это считают существенным повышением терапевтической эффективности.
Дополнительным преимуществом применения миРНК является минимальная вероятность развития побочных эффектов или острой токсичности из-за присутствия в системном кровотоке, которые часто ассоциируются с различным лечением на основе глазных капель. Это обусловлено тем фактом, что при попадании в кровоток соединение быстро разрушается РНКазами, присутствующими в крови.
Вместе с тем, возможность выпуска молекул миРНК в однодозовых флаконах позволяет воздержаться от добавления в состав противомикробных консервантов. Консерванты присутствуют в большинстве составов, представленных на рынке на сегодняшний день. Эти консерванты могут вызвать развитие устойчивости у некоторых пациентов, что вынудит остановить лечение. Обе проблемы особенно важны, принимая во внимание тот факт, что состояния, такие как аллергические заболевания глаз и/или конъюнктивит, включающие, но не ограничивающиеся весенним кератоконъюнктивитом, атопическим кератоконъюнктивитом и конъюнктивитом с гиперплазией сосочков, часто являются хроническими, а значит, таковым является и лечение.
Одним из предпочтительных способов введения является местное, посредством инстилляции напрямую в глаз, предпочтительно, с помощью глазных капель. Как описано выше, терапевтическая обработка миРНК, действующими на мРНК ORAI1, как ожидают, будет обладать преимуществом по сравнению с малыми молекулами в глазных каплях для местного применения, увеличивая продолжительность эффекта, что позволяет уменьшить частоту дозирования и улучшить соблюдение пациентом схемы лечения.
Однако, как объяснено выше, также можно применять другие способы введения, помимо прямого введения в глаз. Точная дозировка и схема введения состава также будут зависеть от способа введения. Специалисту в данной области техники ясно, что точная дозировка и схема введения также зависят от степени тяжести заболевания, и подбирать их следует на основании клинической оценки практикующего врача и состояния каждого пациента. Также понятно, что конкретная величина дозы для любого конкретного субъекта зависит от ряда факторов, включая активность конкретного применяемого соединения, возраст, вес тела, общее состояние здоровья, пол, диету, время введения, способ введения и уровень выведения, комбинацию лекарственных средств и степень тяжести конкретного заболевания, подлежащего лечению.
Составы миРНК настоящего изобретения, описанные в настоящей заявке, можно вводить в дозированных лекарственных формах, содержащих стандартные нетоксичные фармацевтически приемлемые носители, адъюванты и/или инертные носители. Составы могут быть в форме, подходящей для перорального применения, например, в виде таблеток, пастилок, таблеток для рассасывания, водных или масляных суспензий, растворимых порошков или гранул, эмульсии, твердых или мягких капсул, сиропов или эликсиров. Композиции, предназначенные для перорального применения, можно получить в соответствии с любым известным в данной области техники способом получения фармацевтических композиций, и такие композиции могут содержать один или несколько подсластителей, ароматизаторов, красителей или консервантов для получения фармацевтически привлекательных и приятных на вкус препаратов. Таблетки содержат активный ингредиент в смеси с нетоксичными фармацевтически приемлемыми эксципиентами, подходящими для получения таблеток.
Такими эксципиентами могут быть, например, инертные растворители, такие как карбонат кальция, карбонат натрия, лактоза, фосфат кальция или фосфат натрия; гранулирующие и дезинтегрирующие агенты, такие как, кукурузный крахмал или альгиновая кислота; связывающие агенты, например, крахмал, желатин или камедь; и смазывающими агентами, например, стеаратом магния, стеариновой кислотой или тальком. Таблетки могут быть без оболочки или покрытые оболочкой с помощью известных техник. В некоторых случаях такие покрытия можно получить с помощью известных техник для задержки дезинтеграции и адсорбции в пищеварительном тракте, что обеспечивает более продолжительное действие. Например, можно применять замедляющие высвобождение материалы, такие как глицерилмоностеарат или глицерилдистеарат.
Составы для перорального применения также можно представлять в виде твердых желатиновых капсул, где активный ингредиент смешан с инертным твердым разбавителем, например, карбонатом кальция, фосфатом кальция или каолином, или в виде твердых желатиновых капсул, где активный ингредиент смешан с водной или масляной средой, например, с арахисовым маслом, парафиновым маслом или оливковым маслом.
Водные суспензии содержат активные вещества в смеси с эксципиентами, подходящими для получения водных суспензий. Такие эксципиенты являются суспендирующими агентами, например, карбоксиметилцеллюлозой натрия, метилцеллюлозой, гидропропилметилцеллюлозой, альгинатом натрия, поливинипирролидоном, трагакантовой камедью и аравийской камедью; диспергирующие или увлажняющие агенты могут быть встречающимся в природе фосфатидом, например, лецитином, или продуктами конденсации алкиленоксида с жирными кислотами, например, полиоксиэтиленстеаратом, или продуктами конденсации этиленоксида с алифатическими спиртами с длинной цепью., например, гептадекаэтиленоксиэтанолом, или продуктами конденсации этиленоксида с неполными эфирами, полученными из жирных кислот и гексита, такими как полиоксиэтиленсорбитолмоноолеат, или продуктами конденсации этиленоксида с неполными эфирами, полученными из жирных кислот и ангидридов гексита, например, полиэтиленсорбитанмоноолеатом. Водные суспензии могут также содержать один или несколько консервантов, например, этил или н-пропил п-гидроксибензоат, один или несколько красителей, один или несколько ароматизаторов и один или несколько подсластителей, таких как сахароза или сахарин.
Масляные суспензии можно выпускать, суспендируя активные ингредиенты в растительном масле, например, в арахисовом масле, оливковом масле, кунжутном масле или кокосовом масле, или в минеральном масле, таком как парафиновое масло. Масляные суспензии могут содержать загуститель, например, пчелиный воск, твердый парафин или цетиловый спирт. Подсластители и ароматизаторы можно добавлять для придания приятного вкуса пероральным препаратам. Эти композиции можно сохранить, добавляя антиоксидант, такой как аскорбиновая кислота.
Растворимые порошки и гранулы, подходящие для получения водной суспензии при добавлении воды, представляют активный ингредиент в смеси с диспергирующим или увлажняющим агентом, суспендирующим агентом и одним или несколькими консервантами. Примеры подходящих диспергирующих, увлажняющих агентов или суспендирующих агентов указаны выше. Также могут присутствовать дополнительные эксципиенты, например, подсластители, ароматизаторы и красители.
Фармацевтические композиции настоящего изобретения также могут быть в форме водомасляных эмульсий. Масляная фаза может быть растительным маслом или минеральным маслом или их смесью. Подходящие эмульгаторы могут быть встречающимися в природе камедями, например, аравийской камедью или трагакантовой камедью, встречающимися в природе фосфатидами, например, соевым лецитином и сложными или неполными эфирами, полученными из жирных кислот и гексита, ангидридами, например, сорбитанмоноолеатом, и продуктами конденсации указанных неполных эфиров с этиленоксидом, например, полиоксиэтиленсорбитанмоноолеатом. Эмульсии также могут содержать подсластители и ароматизаторы.
Сиропы и эликсиры можно составлять в форме с подсластителями, например, глицерином, пропиленгликолем, сорбитом, глюкозой или сахарозой. Такие составы также могут содержать смягчающее вещество, консервант, ароматизатор и краситель. Фармацевтические композиции или миРНК настоящего изобретения, описанные в настоящей заявке, могут быть в форме стерильной водной или масляной суспензии для инъекции.
Эту суспензию можно составлять в форме, соответствующей известному уровню техники, применяя подходящие диспергирующие или увлажняющие агенты и суспендирующие агенты, упомянутые выше.
Стерильный препарат для инъекции также может быть стерильным раствором или суспензией для инъекции в нетоксичном приемлемом для парентерального введения растворителе или разбавителе, например, в виде раствора в 1,3-бутандиоле. К приемлемым инертным носителям и растворителям, которые можно применять, относится вода, раствор Рингера и изотонический раствор хлорида натрия. Дополнительно, в качестве растворителя или суспендирующей среды традиционно применяют стерильные нелетучие масла. Для этой цели можно применять любое обычное нелетучее масло, включая моно- или диглицериды. Дополнительно, при получении препаратов для инъекции находят применение жирным кислотам, таким как олеиновая кислота.
В предпочтительных вариантах осуществления настоящего изобретения композиции настоящего изобретения составляют в форме раствора, предпочтительно буферного солевого раствора, такого как фосфатно-солевой буфер, или геля для местного введения в глаз, такого как, например, в форме глазных капель. В таких вариантах осуществления настоящего изобретения составы могут быть катионными эмульсиями и/или могут содержать биополимеры, включая, но не ограничиваясь сополимером молочной и гликолевой кислот, карбополом, гиалуроновой кислотой и полиакриловой кислотой.
Молекулы нуклеиновых кислот настоящего изобретения также можно вводить в форме суппозиторий, напр., для ректального введения лекарственного препарата. Эти композиции можно получить, смешивая лекарственное средство с подходящим не вызывающим раздражение эксципиентом, который находится в твердом состоянии при обычной температуре и в жидком состоянии при ректальной температуре и, таким образом, растворяется в прямой кишке, высвобождая лекарственное средство. Такие материалы включают масло какао и полиэтиленгликоли.
Молекулы нуклеиновых кислот настоящего изобретения можно вводить парентерально в стерильной среде. Лекарственное средство в зависимости от применяемого инертного носителя и концентрации можно либо суспендировать, либо растворять в инертном носителе. Эффективно можно растворять в инертном носителе адъюванты, такие как местные анестетики, консерванты и буферные агенты.
Таким образом следующий предпочтительный вариант осуществления настоящего изобретения относится к фармацевтической композиции, где указанная композиция содержит по меньшей мере миРНК, действующую по меньшей мере на одну последовательность, выбираемую из группы, состоящей из SEQ ID NO. 1 - SEQ ID NO. 111, как описано в предыдущих параграфах. Предпочтительнее, чтобы указанную по меньшей мере одну последовательность выбирали из группы, состоящей из SEQ ID NO. 1 - SEQ ID NO. 8, и еще предпочтительнее, чтобы указанная по меньшей мере одна последовательность состояла из SEQ ID NO. 1.
Молекулы нуклеиновых кислот настоящего изобретения также можно вводить субъекту в комбинации с другими терапевтическими соединениями для усиления общего терапевтического эффекта. Применение множества соединений для лечения по показаниям может усилить положительные эффекты на фоне уменьшения побочных эффектов.
Как применяют в настоящей заявке, термин «аллергическое заболевание глаз» обозначает аллергическое нарушение окулярной поверхности, вызванное повышенной экспрессией и/или активностью ORAI1. Его также можно называть аллергическим конъюнктивитом. Аллергическое заболевание глаз включает ряд патологических состояний, включая, но не ограничиваясь сезонным аллергическим конъюнктивитом, круглогодичным аллергическим конъюнктивитом, весенним кератоконъюнктивитом, атопическим кератоконъюнктивитом и конъюнктивитом с гиперплазией сосочков.
Как применяют в настоящей заявке, термин «конъюнктивит» обозначает воспаление конъюнктивы. В Индии его также называют «розовый глаз» или «глаз Мадраса». Обычно конъюнктивит вызывает инфекция (обычно вирусная, но иногда бактериальная) или аллергическая реакция.
«Клинические симптомы» аллергического заболевания глаз включают, но не ограничиваются окулярным зудом, покраснением глаз, отеком века, отеком конъюнктивы, слезоточивостью и назальным воспалением, заложенностью носа, насморком, назальным пруритом и ушным/небным пруритом и чиханием. Предпочтительно, чтобы настоящее изобретение лечило или предотвращало по меньшей мере два клинических симптома, предпочтительнее, по меньшей мере три, еще предпочтительнее более четырех.
Термин «пациент», как применяют в настоящей заявке, обозначает животных, включая млекопитающих, предпочтительно, человека.
Как применяют в настоящей заявке, термин «аллерген» обозначает любое антигенное вещество в окружающей среде, способное вызвать немедленное развитие гиперчувствительности (аллергии). Список известных аллергенов включает пыльцу растений, споры плесневых грибков, шерсть животных, домашняя пыль, пищевые продукты, перья, краски, мыла, детергенты, косметические средства, пластик и лекарственные средства. Аллергены могут попадать в организм при вдыхании, глотании, прикосновении или инъекции. Аллергены из воздуха являются аллергенами, достаточно легкими, чтобы переноситься потоком воздуха, например, пыльцой или спорами, но не ограничиваясь ими.
Под термином «аллергический конъюнктивит» в настоящем изобретении понимают воспаление конъюнктивы, вызванное аллергической реакцией. Конъюнктива является тонкой мембраной, покрывающей глаз. При раздражении конъюнктивы аллергеном обычно возникающие симптомы включают покраснение (в основном из-за вазодилатации малых периферических кровеносных сосудов), окулярный зуд, отек века, усиленную слезоточивость, светобоязнь, водянистое выделение из глаз и ощущение присутствия инородного тела (болезненное). Как правило, у пациентов усиливаются симптомы в теплую и сухую погоду, в то время как более низкая температура и дождь уменьшают симптомы.
Под термином «блефарит» в настоящем изобретении понимают хроническое воспаление века.
Под термином «блефароконъюнктивит» в настоящем изобретении понимают одновременное возникновение двух разных состояний глаза: блефарита и конъюнктивита. Блефарит затрагивает внешнюю часть века, в то время как конъюнктивит развивается в конъюнктиве.
Под термином «кератоконъюнктивит» в настоящем изобретении понимают воспаление роговицы и конъюнктивы.
Настоящее изобретение далее описывают следующие не ограничивающие примеры.
ПРИМЕРЫ
0. Материалы
Зонды для мышиного ORAI1: Taqman исследование экспрессии гена Mm00774349_ml.
Зонды для мышиного TLSP: Taqman исследование экспрессии гена Mm01157588_ml.
Зонды для мышиного TNFSR9: Taqman исследование экспрессии гена Mm00441899_ml.
18S эндогенный контроль: Taqman исследование экспрессии гена Hs99999901_sl.
Обратная транскриптаза Multiscribe 50 ед./мл (Applied Biosystems P/N 4311235).
Ингибитор РНКазы 20 ед./мл (Applied Biosystems P/N N8080119).
Универсальная 2× реакционная смесь TaqMan Master Mix.
Набор для нерадиоактивного исследования клеточной пролиферации (Promega, Mannheim, Germany).
Человеческие тучные клетки (HMC-1).
Кальциевая соль иономицина 1 мМ в ДМСО (Sigma Life Science
Каталожный номер 13909-lml).
Набор для детектирования с Аннексином V (Annexin-V detection kit) Life Technologies (Каталожный номер: V13241).
1. In vitro исследование
1.1 Уровни экспрессии ORAI1 после трансфекции миРНК настоящего изобретения в различных клеточных линиях.
Для демонстрации эффекта подавления экспрессии с помощью миРНК настоящего изобретения проводили измерение уровня экспрессии ORAI1 in vitro после трансфекции рядом миРНК настоящего изобретения в разных клеточных линиях. Человеческие клетки A204 и мышиные клетки C2C12 и J744A.1 трансфицировали 100 нМ SEQ ID NO. 112, 19 п.о. структурой дцРНК с тупыми концами, с помощью Transit TKO и Lipofectamine 2000 в качестве трансфектанта, соответственно. Все трансфекции проводили, следуя стандартным инструкциям производителя. В той же трансфекции рандомизированную последовательность миРНК применяли в качестве контроля специфичности интерференции. Осадки клеток собирали через 24, 48 и 72 часа после эксперимента по трансфекции и обрабатывали для оценки возможных вариаций уровней мРНК в результате действия миРНК. Количественное определение уровней РНК проводили с помощью ПЦР в режиме реального времени, применяя способ относительной количественной оценки, способ сравнения пороговых циклов (2-ΔΔ CT) (Livak and Schmittgen, 2001). Все эксперименты с количественной ПЦР в режиме реального времени проводили в трех повторах и повторяли в трех независимых экспериментах. Рассчитывали среднее и стандартное отклонение. Как показано на Фигуре 4, SEQ ID NO. 112 существенно снижала уровни мРНК ORAI1 приблизительно на 70-80% в клетках A204 и в клетках C2C12 и на 40% в J744A.1. SEQ ID NO. 113, SEQ ID NO. 115, SEQ ID NO. 116, SEQ ID NO. 117, SEQ ID NO. 118 и SEQ ID NO. 119, 19 п.о. структуры дцРНК с тупыми концами, также существенно снижали уровни экспрессии мРНК ORAI1 приблизительно на 40-80% (Фигура 5).
1.2 Жизнеспособность клеток различных клеточных линий после трансфекции миРНК настоящего изобретения.
Для демонстрации жизнеспособности клеток в присутствии миРНК настоящего изобретения измеряли уровни токсичности in vitro после трансфекции рядом миРНК настоящего изобретения в разных клеточных линиях. Человеческие клетки A204 и мышиные клетки C2C12 и J744A.1 трансфицировали 100 нМ SEQ ID NO. 112 (19 п.о. структурой дцРНК с тупыми концами) с помощью Transit TKO и Lipofectamine 2000 в качестве трансфектанта, соответственно. Все трансфекции проводили, следуя стандартным инструкциям производителя. В той же трансфекции рандомизированную последовательность миРНК применяли в качестве контроля специфичности интерференции. Осадки клеток собирали через 24, 48 и 72 часа после эксперимента по трансфекции и обрабатывали для оценки возможных вариаций уровня жизнеспособности клеток в результате трансфекции миРНК. Жизнеспособность клеток оценивали с помощью набора для нерадиоактивного исследования клеточной пролиферации CellTiter 96® (Promega). Этот способ основан на способности живых клеток (дегидрогеназных ферментов) восстанавливать соединение MTS тетразолиум (3-(4,5-dimethylthiazol-2-yl)-5-(3-carboxymethoxyphenyl)-2-(4-sulfophenyl)-2H-tetrazolium, http://www.multitran.ru/c/m.exe?t=6555991_2_13-(4,5-диметилтиазол-2-ил)-5-(3-карбоксиметоксифенил)-2-4-сульфофенилтетразолиум) до формазана, по данным измерения величины поглощения при 490 нм. Рассчитывали среднее и стандартное отклонение. Как показывает Фигура 6, не было обнаружено изменений жизнеспособности клеток для SEQ ID NO. 112. Таким образом, SEQ ID NO. 112 является нетоксичной и безопасной.
1.3 Уровни экспрессии ORAI1 после трансфекции немодифицированными и химически модифицированными миРНК настоящего изобретения в различных клеточных линиях.
Для улучшения стабильности миРНК настоящего изобретения и для обеспечения отсутствия иммуногенной активации вносили разные оптимизирующие миРНК химические модификации в каноническую последовательность SEQ ID NO. 112 (19 п.о. структурой дцРНК с тупыми концами); таким образом получали новые химически модифицированные соединения (SEQ ID NO. 223, SEQ ID NO. 224, SEQ ID NO. 225, SEQ ID NO. 226, SEQ ID NO. 227, SEQ ID NO. 228 и SEQ ID NO. 229) и трансфицировали их в человеческие и мышиные клетки, чтобы подтвердить их способность понижать уровень мРНК ORAI1. Химические модификации подробно описаны на Фигуре 3. Человеческие клетки A204 и мышиные клетки C2C12 и J744A.1 трансфицировали 100 нМ SEQ ID NO. 112, SEQ ID NO. 223, SEQ ID NO. 224, SEQ ID NO. 225, SEQ ID NO. 226, SEQ ID NO. 227, SEQ ID NO. 228 или SEQ ID NO. 229 (все эти структуры соответствуют 19 п.о. структуре дцРНК с тупыми концами) с помощью Transit TKO и Lipofectamine 2000 в качестве трансфектанта, соответственно. Все трансфекции проводили, следуя стандартным инструкциям производителя. В той же трансфекции рандомизированную последовательность миРНК применяли в качестве контроля специфичности интерференции. Осадки клеток собирали через 24, 48 и 72 часа после эксперимента по трансфекции и обрабатывали для оценки возможных вариаций уровня мРНК в результате обработки миРНК. Количественное определение уровней РНК проводили с помощью ПЦР в режиме реального времени, применяя способ относительной количественной оценки, способ сравнения пороговых циклов (2-ΔΔ CT) (Livak and Schmittgen, 2001). Все эксперименты с количественной ПЦР в режиме реального времени проводили в трех повторах и повторяли в трех независимых экспериментах. Рассчитывали среднее и стандартное отклонение. Как показано на Фигуре 7 и Фигуре 8 модифицированные миРНК демонстрировали высокую эффективность, сравнимую с SEQ ID NO. 112, как в человеческих, так и в мышиных клеточных линиях. Таким образом, химически модифицированные продукты SEQ ID NO. 223, SEQ ID NO. 224, SEQ ID NO. 225, SEQ ID NO. 226, SEQ ID NO. 227, SEQ ID NO. 228 и SEQ ID NO. 229 снижали уровни мРНК ORAI1 на 50% - 80%.
1.4 Дозозависимый эффект SEQ ID NO. 112 и SEQ ID NO. 227 в человеческих и мышиных клетках.
Человеческие клетки A204 и мышиные клетки C2C12 трансфицировали возрастающими дозами SEQ ID NO. 112 (19 п.о. структурой дцРНК с тупыми концами, SYL116011) и SEQ ID NO. 227 (19 п.о. структурой дцРНК с тупыми концами, SYL116011v8) (от 0,001 до 100 нМ) с помощью Transit TKO и Lipofectamine 2000 в качестве трансфектанта, соответственно. Все трансфекции проводили, соблюдая стандартные условия производителя. В той же трансфекции рандомизированную последовательность миРНК применяли в качестве контроля специфичности интерференции. Собирали осадки клеток и обрабатывали для оценки возможных вариаций уровня мРНК в результате действия миРНК. Количественное определение уровней РНК проводили с помощью ПЦР в режиме реального времени, применяя способ относительной количественной оценки, способ сравнения пороговых циклов (2-ΔΔ CT) (Livak and Schmittgen, 2001). Все эксперименты с количественной ПЦР в режиме реального времени проводили в трех повторах и повторяли в трех независимых экспериментах. Рассчитывали среднее и стандартную ошибку среднего. Как показано на Фигуре 9 существенное снижение уровней ORAI1 наблюдали в человеческих клетках при дозе 0,5 нМ. Наибольший эффект наблюдали в ответ на дозу 100 нМ как в случае SEQ ID NO. 112, так и SEQ ID NO. 227. Небольшие различия между SEQ ID NO. 112 и SEQ ID NO. 227 наблюдали при концентрациях от 10 до 50 нМ. SEQ ID NO. 227 снижала уровень мРНК ORAI1 на 60-80%, в то время как SEQ ID NO. 112 снижала уровень мРНК ORAI1 на 40-60%. Различий между концентрациями от 0,05 до 0,001 нМ не наблюдали.
Применяя эти данные, рассчитывали значение полумаксимальной ингибирующей концентрации (IC50, inhibitory concentration 50) равное 1,98 нМ для SEQ ID NO. 227 и 5,3 нМ для SEQ ID NO. 112.
Как показано на Фигуре 10, значительное снижение уровня ORAI1 также наблюдали в мышиных клетках C2C12 при дозе 2,5 нМ. Максимальный эффект наблюдали в ответ на дозу 50 нМ как SEQ ID NO. 112, так и SEQ ID NO. 227. Небольшие различия между SEQ ID NO. 112 и SEQ ID NO. 227 наблюдали при концентрациях от 5 до 100 нМ. Как SEQ ID NO. 112, так и SEQ ID NO. 227 снижали уровень мРНК ORAI1 на 70-80%. Различий между концентрациями от 0,1 до 0,001 нМ не наблюдали. Применяя эти данные, рассчитывали значение полумаксимальной ингибирующей концентрации (IC50, inhibitory concentration 50) равное 1,98 нМ для SEQ ID NO. 227 и 1,25 нМ для SEQ ID NO. 112.
1.5 Экспрессия ORAI1 и его паралогов ORAI2 и ORAI3 после трансфекции SEQ ID NO. 112 и SEQ ID NO. 227.
Чтобы продемонстрировать специфичный эффект подавления экспрессии миРНК настоящего изобретения проводили in vitro измерения уровня экспрессии ORAI1, ORAI2 и ORAI3 после трансфекции рядом миРНК настоящего изобретения в различных клеточных линиях. Исследовали эффект SEQ ID NO. 112 и SEQ ID NO. 227 на рецепторные каналы семейства ORAI, чтобы проанализировать их эффект на белки, структурно и функционально родственные каналу ORAI1. Уровни мРНК ORAI1, ORAI2 и ORAI3 оценивали в человеческих клетках A204 и в мышиных клетках C2C12 после обработки SEQ ID NO. 112 и SEQ ID NO. 227. Человеческие клетки A204 и мышиные клетки C2C12 трансфицировали 100 нМ SEQ ID NO 112 и SEQ ID NO 227 с помощью Transit TKO и Lipofectamine 2000 в качестве трансфектанта, соответственно. Все трансфекции проводили, соблюдая стандартные условия производителя. В той же трансфекции рандомизированную последовательность миРНК применяли в качестве контроля специфичности интерференции. Собирали осадки клеток через 24, 48 и 72 часа после эксперимента по трансфекции и обрабатывали для оценки возможных вариаций уровня мРНК в результате действия миРНК. Фигура 11 и Фигура 12 показывают, что SEQ ID NO. 112 и SEQ ID NO. 227 были способны селективно снижать уровни мРНК ORAI1, приблизительно на 70-80% в человеческих клетках, не оказывая существенного влияния на уровни мРНК ORAI2 или ORAI3 10 (Фигура 11), и на 60-70% в мышиных клетках (Фигура 12).
1.6 Проявление возможных нецелевых эффектов после трансфекции SEQ ID NO. 112 (SYL116011) в человеческих клетках.
Чтобы продемонстрировать специфичный эффект подавления экспрессии с помощью миРНК настоящего изобретения в отношении нежелательных целей, проводили in silico определение нецелевых эффектов SEQ ID NO. 112 в человеческих клеточных линиях. Измеряли уровни экспрессии MSLN и OLFM12A после трансфекции рядом миРНК настоящего изобретения в человеческих клеточных линиях. Анализировали эффект SEQ ID NO. 112 в отношении экспрессии генов MSLN и OLFM12A. Уровень мРНК MSLN и OLFM12A оценивали в человеческих клетках A204 после обработки 100 нМ SEQ ID NO. 112 с помощью Transit TKO в качестве трансфектанта. Все трансфекции проводили, соблюдая стандартные условия производителя, с положительным и отрицательным контролем. В той же трансфекции рандомизированную последовательность миРНК применяли в качестве контроля специфичности интерференции. Собирали осадки клеток через 24, 48 и 72 часа после эксперимента по трансфекции и обрабатывали для оценки возможных вариаций возможного нецелевого действия на уровни мРНК в результате действия SEQ ID NO. 112. Фигура 13 показывает, что SEQ ID NO. 112 не снижала уровень возможных нецелевых эффектов.
1.7 Уровень экспрессии ORAI1 после трансфекции SEQ ID NO. 112 в крысиных клеточных линиях
Чтобы продемонстрировать специфичный эффект подавления экспрессии SEQ ID NO. 112, проводили in vitro определение уровня экспрессии ORAI1 после трансфекции рядом миРНК настоящего изобретения в различных клеточных линиях. Крысиные клетки JTC-19 и C6 трансфицировали 100 нМ SEQ ID NO. 112 с помощью Transit IT2020 и Lipofectamine 2000 в качестве трансфектанта, соответственно. Все трансфекции проводили, соблюдая стандартные условия производителя, с отрицательным контролем. В той же трансфекции рандомизированную последовательность миРНК применяли в качестве контроля специфичности интерференции. Собирали осадки клеток через 24, 48 и 72 часа после эксперимента по трансфекции и обрабатывали для оценки возможных вариаций уровня мРНК в результате действия миРНК. Количественное определение уровней РНК проводили с помощью ПЦР в режиме реального времени, применяя способ относительной количественной оценки, способ сравнения пороговых циклов (2-ΔΔ CT) (Livak and Schmittgen, 2001). Все эксперименты с количественной ПЦР в режиме реального времени проводили в трех повторах и повторяли в трех независимых экспериментах. Рассчитывали среднее и стандартную ошибку среднего. Как показано на Фигуре 14 и на Фигуре 15, SEQ ID NO. 112 существенно снижала уровень мРНК ORAI1, приблизительно на 70% в клетках JTC-19 и на 40-70% в клетках C6. В случае SEQ ID NO. 112 уровень мРНК ORAI1 не восстанавливался полностью через 72 часа в клетках JTC-19, но не в клетках C6 (Фигура 14 и Фигура 15).
1.8 Уровни экспрессии гена ORAI1 после трансфекции SEQ ID NO. 112 (SYL116011), SEQ ID NO. 233 (SYL116011v11) и SEQ ID NO. 235 (SYL116011vll).
Человеческие клетки A204, мышиные клетки C2C12 и крысиные клетки JTC-19 трансфицировали 100 нМ SEQ ID NO. 112 (19 п.о. структура дцРНК с тупыми концами, SYL116011) и SEQ ID NO. 233 (19 п.о. структура дцРНК с тупыми концами, SYL116011v11) и SEQ ID NO. 235 (19 п.о. структура дцРНК с тупыми концами, SYL116011v12) с помощью Transit TKO, Lipofectamine 2000 и Mirus IT2020 в качестве трансфектанта, соответственно. Все трансфекции проводили, соблюдая стандартные условия производителя. В той же трансфекции рандомизированную последовательность миРНК применяли в качестве контроля специфичности интерференции. Собирали осадки клеток и обрабатывали для оценки возможных вариаций уровня мРНК в результате действия миРНК. Количественное определение уровней РНК проводили с помощью ПЦР в режиме реального времени, применяя способ относительной количественной оценки, способ сравнения пороговых циклов (2-ΔΔ CT) (Livak and Schmittgen, 2001). Как показано на Фигуре 16, существенное снижение уровня ORAI1 наблюдали в человеческих, мышиных и крысиных клетках. Уровень мРНК ORAI1 снижался на 70-80% в человеческих клетках в случае SEQ ID NO. 112 (SYL116O11), SEQ ID NO. 233 (SYL116O11v11) и SEQ ID NO. 235 (SYL116O11v11), а в мышиных клетках уровень мРНК ORAI1 уменьшался на 50% в случае SEQ ID NO. 112 (SYL116011), SEQ ID NO. 233(SYL116011vll) и SEQ ID NO. 235 (SYL116011v11), в то время как в крысиных уровень мРНК ORAI1 уменьшался на 50% в случае SEQ ID NO. 112 (SYL116011) и на 95% и 99% в случае SEQ ID NO. 233 (SYL116011v11) и SEQ ID NO. 235 (SYL116011v11), соответственно.
2. Исследование in vivo
2.1 In vivo анализ эффективности SEQ ID NO. 112 (SYL116011) и SEQ ID NO. 227 (SYL116011v8) в мышиной модели аллергического заболевания глаз, индуцированного пыльцой амброзии.
Целью настоящего исследования был анализ эффективности миРНК настоящего изобретения, созданных для подавления экспрессии ORAI1, в частности, SEQ ID NO. 112 (19 п.о. структуры дцРНК с тупыми концами, SYL116011) и SEQ ID NO. 227 (19 п.о. структуры дцРНК с тупыми концами, SYL116011v8), с целью уменьшения симптомов, ассоциированных с аллергическими заболеваниями глаз, в мышиной модели аллергического заболевания глаз, индуцированного пыльцой амброзии.
Амброзия представляет собой цветковое растение рода Амброзия (Ambrosia) семейства Сложноцветные (Asteraceae). Пыльца амброзии является очень аллергенной, как правило, ее считают самым сильным передающимся по воздуху аллергеном среди всех видов передающейся по воздуху пыльцы и основной причиной развития поллиноза по всему миру. Национальный институт изучения санитарного состояния окружающей среды (National Institute of Environmental Health Science, NIEHS) указывает на то, что амброзия и другая сорная трава, такая как щавель курчавый, марь белая, амарант, подорожник, щавель малый и полынь, являются самыми обильными источниками аллергенов пыльцы во всем мире. Эту пыльцу часто применяют в животных моделях исследования аллергического конъюнктивита (Bacsi A et al., 2005).
Целью данного анализа было определить, уменьшает ли подавление экспрессии ORAI1 при закапывании в глаза соединений настоящего изобретения (SEQ ID NO. 112 (SYL116011) и SEQ ID NO. 227 (SYL116011v8)) симптомы, вызванные индуцированным пыльцой амброзии аллергическим заболеванием глаз у мышей.
Проанализировали, экспрессируется ли ORAI1 в глазу мыши и повышается ли его экспрессия в ответ на индуцированное пыльцой амброзии аллергическое заболевание глаз. Также оценили эффект подавления экспрессии ORAI1 с помощью местного нанесения SEQ ID NO. 112 (SYL116011) или SEQ ID NO. 227 (SYL116011v8) на аллергический ответ в указанной выше мышиной модели. С этой целью анализировали следующие параметры:
клинические признаки в ответ на индукцию аллергии: типичные окулярные признаки аллергического конъюнктивита включают зуд, отек век, отек конъюнктивы (хемоз) и выделение слизи. Слизь, связанная с аллергическими заболеваниями глаз, обильная, вязкая и даже клейкая. Изменения конъюнктивы обычно придают бульбарной конъюнктиве «стеклянный» вид, а конъюнктива века становится более розовой, нежели красной, часто «молочного» вида.
Количество местных тучных клеток: в течение нескольких минут после аллергического раздражения конъюнктивы происходит дегрануляция тучных клеток; высвобождение медиаторов воспаления привлекает больше тучных клеток, которые мигрируют из более глубоких слоев конъюнктивы.
Местная инфильтрация эозинофилов: инфильтрация воспалительных клеток в конъюнктиву происходит через несколько часов после контакта с аллергеном и является частью долгосрочного ответа на аллергены. Хотя в конъюнктиву мигрируют несколько типов клеток, основными являются эозинофилы.
Изменения экспрессии биомаркеров, связанных с аллергией:
Тимусный стромальный лимфопоэтин (TLSP, thymic stromal lymphopoietin) является цитокином эпителиального происхождения, который активирует дендритные клетки, связываясь со своим специфичным рецептором TLSPR (TLSP receptor). Связывание TLSP с TLSPR индуцирует воспалительный ответ типа Th2. TLSP образуют в основном эпителиальные клетки, но также его могут образовывать тучные клетки, и его уровень может быть повышен в местах аллергического воспаления (Zheng X. et al., 2010).
Член суперсемейства рецепторов фактора некроза опухоли 9 (Tnfrsf9, tumor necrosis factor receptor superfamily, member 9) или CD-137 является костимулятором Т-клеток памяти. Этот костимулятор экспрессируется в активированных Т-клетках, NK клетках (natural killer, натуральные киллеры) и дендритных клетках, в то время как его лиганд CD137L (CD137 ligand) обнаруживают на зрелых дендритных клетках, активированных макрофагах и активированных В-клетках. CD-137 костимулирует активацию и пролиферацию Т-клеток, увеличивает выживаемость активированных Т-клеток и подавляет CD4+ T-хелперы. Было показано, что при аллергическом воспалении CD-137 опосредует зависящие от IL-4 Th2-ответы, и его уровень повышен в эозинофилах пациентов с опосредованной IgE аллергической реакцией.
A. Способы
a.1 Характеристика тестовой системы
Характеристика тестовой системы
Следующим преимуществом миРНК настоящего изобретения является то, что SEQ ID NO. 1 - SEQ ID NO. 8 соответствуют областям гена ORAI1, высоко консервативным среди последовательностей многих животных. Фактически, эти последовательности идентичны у человека и мыши, что делает эту животную модель особенно подходящей для исследования аллергических заболеваний глаз.
a.2 Индукция аллергии
Аллергический конъюнктивит индуцировали, иммунизируя животных смесью из 50 мкг пыльцы амброзии (Rw, ragweed) в 0,25 мл алюминиевых квасцов с помощью внутрибрюшинной инъекции в день 1. Раствор для иммунизации готовили непосредственно перед введением и на протяжении всего времени держали в защищенном от света месте. Через десять дней после иммунизации местно наносили 1,25 мг пыльцы Rw в виде глазных капель в каждый глаз. Проводили введение дозы в объеме 5 мкл/глаз. Эта процедура является адаптацией стандартного опубликованного ранее протокола, известного специалистам в данной области техники, и прошла проверку перед проведением оценки эффективности миРНК (Magone M. T. et al., 1998).
a.3 Введение тестируемого образца
Тестируемый образец вводили с помощью местного окулярного введения в оба глаза животных один раз в день на протяжении 5 дней, начиная с дня 6 (Фигура 4). Отдельной группе животных, служащей контролем, вводили инертный носитель (фосфатно-солевой буфер. Проводили введение дозы в объеме 5 мкл/глаз.
a.4 Клинические наблюдения и сбор образцов
Общее состояние здоровья животных контролировали ежедневно с момента первого введения до умерщвления. Мышей обследовали на предмет клинических признаков гиперчувствительности перед местной окулярной инстилляцией пыльцы и в разные временные точки вплоть до 24 ч после инстилляции пыльцы. Отек конъюнктивы и конъюнктивальную инъекцию, отек века, выделения из глаза и слезоточивость оценивали по шкале от 0 до 3. Клиническую оценку проводил наблюдатель, которому не были известны экспериментальные условия. Животных умерщвляли либо через 3, либо через 24 ч после индукции аллергии. Перед умерщвлением отбирали кровь для оценки присутствия IgE, IL-13, IL-10 и MCP-1 в плазме. После умерщвления извлекали глаза, селезенку и шейные лимфатические узлы и либо обрабатывали для последующего гистологического анализа, в дальнейшем сохраняли в виде РНК или обрабатывали для анализа уровня упомянутых выше цитокинов в конъюнктиве.
a.5 Гистопатология
Извлеченные глаза помещали в 10% формалин (1/20 объема) на 24 часа, затем формалин удаляли, несколько раз промывая 0,1 М фосфатным буфером и инкубировали в этом буфере на протяжении почти 24 ч. Образцы дегидратировали, инкубируя в возрастающих концентрациях этанола, а затем заключали в легкоплавкий парафин в гистопроцессоре (Leica TP 1020, каталожный номер - 0704 37101, Leica Microsystems, Nussloch, Germany). Готовили срезы образцов с помощью микротома для получения срезов толщиной 2 мкм, которые затем окрашивали либо толуидином синим для определения количества тучных клеток, либо гематоксилином-эозином для оценки инфильтрации эозинофилов.
a.6 Выделение РНК и обратная транскрипция
Общую РНК выделяли из цельных глаз, селезенки или лимфатических узлов с помощью набора для выделения РНК RNeasy (Invitrogen, CA, USA). 4 мкг общей РНК применяли для обратной транскрипции с помощью набора High-Capacity cDNA Archive kit (Applied Biosystems, Inc., Foster City, CA, USA) в соответствии с инструкциями производителя и IT-B-0003-01.
a.7 Количественная ПЦР
Количественную ПЦР проводили с применением системы детектирования Stepone plus (Applied Biosystems). 500 нанограмм каждого образца амплифицировали в универсальной 2× реакционной смеси TaqMan при следующих условиях: 95°C в течение 10 мин, затем 40 циклов (95°C в течение 15 с и 60°C в течение 1 мин). Все количественные ПЦР проводили в трех повторах и повторяли по меньшей мере в двух независимых экспериментах, всегда осуществляя контроль обратной транскрипции и контроль без матрицы. Уровни мРНК ORAI1, TLSP и Tnfrsf9 анализировали с помощью количественной ПЦР, применяя способ относительной количественной оценки ΔΔCT, применяя ген 18S в качестве внутреннего контроля (Livak K. J. and Schmittgen T. D., 2001).
a.8 Анализ IgE, IL-13, IL-10 и MCP-1 в плазме и конъюнктиве
Оценивали количество следующих цитокинов: IgE, IL-13, IL-10 и MCP-1 в плазме и конъюнктиве мышей с помощью следующих наборов в соответствии с инструкциями производителя.
B. Результаты
b.1 Экспрессия ORAI1 в глазах мышей и ее индукция в ответ на аллергическое заболевание глаз.
Экспрессию ORAI1 оценивали в глазах мышей в разные временные точки после индукции аллергии, как упомянуто в разделе «Способы». Фигура 17 показывает, что ORAI1 присутствует в глазу и что его экспрессия резко увеличивается в ответ на индукцию аллергии. Двукратное увеличение уровня мРНК ORAI1 наблюдали через 3-6 ч после введения пыльцы амброзии. Через 24 ч после индукции аллергии уровни ORAI1 составляли приблизительно 350% от исходного уровня.
b.2 Оценка экспрессии биомаркеров аллергии в ответ на аллергическое заболевание глаз.
Уровни мРНК TLSP и Tnfrsf9 исследовали в разные временные точки после индукции аллергического заболевания глаз посредством инстилляции пыльцы амброзии в заранее сенсибилизированных мышах. Через 3 ч после индукции аллергии наблюдали значительную индукцию как TLSP, так и Tnfrsf9. Через 24 ч после индукции уровни мРНК Tnfrsf9 были близки к исходному уровню, в то время как уровни мРНК TLSP все еще оставались приблизительно в 1,5 раза выше исходного уровня (Фигура 18).
b.3 Эффективность SEQ ID NO. 112 (SYL116011) в мышиной модели аллергического заболевания глаз
Трем группам животных внутрибрюшинно вводили дозу пыльцы амброзии, адсорбированной на алюминиевых квасцах, как указано в разделе «Способы». Через пять дней после внутрибрюшинной инъекции одной группе (A, n=8) проводили окулярную инстилляцию один раз в день фосфатно-солевым буфером на протяжении пяти дней, а вторая группа получала SEQ ID NO. 112 (SYL116011) в дозировке 150 мкг/глаз/день (низкая доза) (B, n=15) на протяжении такого же периода времени, в то время как третья группа получала SEQ ID NO. 112 (SYL116011) в дозировке 375 мкг/глаз/день (высокая доза) на протяжении 5 дней. Животных обследовали на предмет симптомов, связанных с аллергическим заболеванием глаз, через 1, 3, 6 и 24 ч после окулярной инстилляции пыльцы амброзии. Как показано на Фигуре 20, обработка любой дозой SEQ ID NO. 112 (SYL116011) существенно уменьшала немедленные клинические признаки аллергии. Дальнейший анализ клинических признаков показал, что обе дозы SEQ ID NO. 112 (SYL116011) оказывали специфичный эффект на два исследуемых параметра: хемоз (отек конъюнктивы) и слезоточивость (Фигура 21).
Инфильтрацию тучных клеток оценивали в конъюнктиве века и в бульбарной конъюнктиве через 3 ч после индукции аллергического заболевания глаз. SEQ ID NO. 112 (SYL116011), введенная в дозе 375 мкг/глаз/день, вызывала существенное снижение количества тучных клеток, приникающих как в конъюнктиву века, так и в бульбарную конъюнктиву (Фигура 22).
Инфильтрацию эозинофилов оценивали в конъюнктиве через 24 ч после индукции аллергии. Вновь наблюдали существенное уменьшение количества инфильтрующих эозинофилов в ответ на высокую дозу SEQ ID NO. 112 (SYL116011) в обеих зонах конъюнктивы и в ответ на низкую дозу в бульбарной конъюнктиве (Фигура 23).
Анализ биомаркера аллергии TLSP в цельном глазу показал дозозависимое снижение экспрессии этого маркера в ответ на SEQ ID NO. 112 (SYL116011). Экспрессия CD-137 (Tnfrsf9) также была существенно снижена в ответ на SEQ ID NO. 112 (SYL116011) через 3 ч после индукции аллергии. Как показано на Фигуре 11, этот маркер аллергии выраженно индуцирован через 3 ч после индукции аллергии (Фигура 24).
b.4 Эффективность SEQ ID NO. 227 (SYL116011v8) в мышиной модели аллергического заболевания глаз
Далее поставили другой in vivo эксперимент, в котором трем группам животных внутрибрюшинно вводили дозу пыльцы амброзии, адсорбированной на алюминиевых квасцах, как указано в разделе «Способы». Через пять дней после внутрибрюшинной инъекции одной группе (A, n=10) проводили окулярную инстилляцию один раз в день фосфатно-солевым буфером на протяжении пяти дней, а вторая группа получала другое соединение настоящего изобретения (SEQ ID NO. 227 (SYL116011v8)) в дозировке 450 мкг/глаз/день (B, n=10) на протяжении такого же периода времени, в то время как третья группа получала 2 мкл 0,5 мг/мл левокабастина на протяжении 5 дней. Левокабастин является антагонистом рецептора H1 второго поколения, доступный в настоящее время на рынке для лечения аллергических заболеваний глаз. Животных обследовали на предмет симптомов, связанных с аллергическим заболеванием глаз, через 0,5, 1, 3, 6 и 24 ч после окулярной инстилляции пыльцы амброзии. Как показано на Фигуре 25, обработка SEQ ID NO. 227 (SYL116011v8) существенно уменьшала клинические признаки аллергии; уменьшение клинических признаков было сильнее выражено в ответ на левокабастин. Дальнейший анализ клинических симптомов показал, что SEQ ID NO. 227 (SYL116011v8) улучшает все исследуемые параметры по сравнению с обработанными фосфатно-солевым буфером животными. Таким образом, было доказано, что данное соединение является эффективным терапевтическим средством при аллергических заболеваниях глаз.
2.2 Оценка эффектов in vivo SEQ ID NO. 112 (SYL116011) в мышиной модели экспериментального аллергического конъюнктивита.
Целью настоящего исследования была оценка эффектов миРНК настоящего изобретения, созданных для подавления экспрессии ORAI1, для уменьшения симптомов аллергии, таких как гиперемия, косоглазие, выделения из глаз и отек века, ассоциированных с аллергическим конъюнктивитом, в мышиной модели.
Задачей настоящего исследования было оценить, уменьшает ли подавление экспрессии ORAI1 при окулярной инстилляции SEQ ID NO. 112 (19 п.о. структуры дцРНК с тупыми концами, SYL116011) симптомы аллергии (гиперемию, косоглазие, выделения из глаз и отек века) в мышиной модели аллергического конъюнктивита. В качестве положительного контроля применяли распространенное лекарственное средство противоаллергический Patanol®. Patanol® (0,1% олопатадин) является антигистаминным средством/стабилизатором тучных клеток двойного действия, вводимым в виде глазных капель. Patanol® блокирует эффекты гистамина и предотвращает высвобождение химических соединений, отвечающих за симптомы аллергии, из тучных клеток. Местное введение фосфатно-солевого буфера (инертного носителя) применяли в качестве отрицательного контроля.
A. Способы
В данном исследовании самок мышей Balb/C сенсибилизировали амброзией, смешанной с гидроксидом алюминия в день 0. В день 18 мышей местно сенсибилизировали амброзией в сбалансированном солевом растворе перед местной обработкой, чтобы удалить мышей, считающихся не отвечающими на индукцию аллергии. Не отвечающими считали мышей, у которых гиперемия не изменялась по меньшей мере на 2 единицы по сравнению с исходным уровнем. Из-за малого числа отвечающих мышей снова проводили сенсибилизацию мышей в день 21. В день 24 повторяли процедуру дня 18 для идентификации отвечающих мышей. Для исследования отобрали 48 мышей и рандомизировали их в 6 групп, по 8 мышей в группе. Группы профилактической обработки получали соответствующие местные лекарственные средства в дни 25-27 (один раз в день ежедневно для групп 2, 3 и 5; четыре раза ежедневно для группы 6). В дни 28-31 мышей местно нагружали аллергеном амброзии дважды в день на фоне введения соответствующего лекарственного средства (один раз в день всем группам, за исключением группы Patanol®, которая получала три доза ежедневно). Животных оценивали на предмет гиперемии, косоглазия, выделения из глаз и отека века, проводя оценку после первой, четвертой, шестой и восьмой нагрузки антигеном.
a.1 Животные
Мышей содержали в поликарбонатных клетках на подстилке (ALPHA-dri®). Клетки соответствовали стандартам, заданным Законом о благополучии животных (AWA, Animal Welfare Act) и Руководством по Уходу и применению лабораторных животных. Рекомендации по предоставлению пространства для животных соответствовали требованиям Службы здравоохранения (PHS, Public Health Service) и AWA. Наполнитель и подстилку в клетках животных меняли по мере необходимости, поддерживая сухость и чистоту.
Животные имели свободный доступ к свежему, аппетитному и сбалансированному корму. Животные имели свободный доступ к чистой питьевой незагрязненной воде. Контроль состояния окружающей среды был настроен на поддержание температуры равной 22±4°C (68±5°F) и относительной влажности равной 50±20%. Поддерживали 12-часовой светотемновой цикл. Животных адаптировали в течение по меньшей мере 5 дней после поступления в виварий перед проведением исходной оценки. Помощь ветеринара не требовалась на протяжении всего исследования.
a.2 Сенсибилизация аллергеном
Способ введения: подкожно, в подколенные области обеих задних конечностей.
Частота: в день 0 и день 21 во всех группах.
Процедура: при каждой сенсибилизации животные, получавшие амброзию (SRW), получали 100 мкг амброзии в 0,65 мг гидроксида алюминия в 50 мкл.
a.3 Введение доз
Местную обработку SEQ ID NO. 112 (SYL116011), Patanol® в качестве положительного контроля или инертным носителем в качестве контроля проводили всем группам, как указано. Мышам дозы вводили местно в роговицу с помощью откалиброванной микропипетки, 3 мкл каплю в каждый глаз. Во время профилактической обработки (дни 25-27) животным из группы Patanol® вводили дозу четыре раза в день ежедневно приблизительно в 9.00, 12.00, 14.00 и 17.00. Все время указано как ± 60 минут, а точное время введения дозы регистрировали в папке с материалами исследования. Животные в группах 2, 3, 5 и 6 получали местные дозы приблизительно в 13.00±60 минут. В дни нагрузки антигеном (дни 28-31) мышам из группы Patanol® вводили дозу трижды в день ежедневно в дни нагрузки антигеном приблизительно в 9.00, 13.00, 16.00, однако, время введения дозы указано как ±90 минут. Всем остальным группам вводили дозу приблизительно в 13.00. Снова точное время введения дозы регистрировали в папке с материалами исследования.
a.4 Нагрузка аллергеном
Способ введения: окулярное введение, в оба глаза.
Частота: в день 18 проводили скрининг нагрузки амброзией для идентификации отвечающих животных. Мышей оценивали в исходный период, перед нагрузкой амброзией. Затем через 18±1 минут после нагрузки снова проводили оценку животных. Из-за отсутствия отвечающих животных исследование задерживали. Вторую сенсибилизацию проводили в день 21 и повторяли скрининг нагрузкой амброзией в день 24. В дни 25-27 начинали соответствующую профилактическую обработку в группах 2, 3, 5 и 6. В дни 28-31 нагрузку два раза в день проводили приблизительно через 30 минут после 1й ежедневной дозы Patanol® и после 3й ежедневной дозы Patanol®. В дни 28-31 после местного введения дозы 1 в день 28 и после введения третьей местной дозы в дни 29-31, оценивали животных через 30 минут после введения местной дозы Patanol®, а затем нагружали ~3 минуты после оценки и снова оценивали через 18 минут после нагрузки (нагрузка после местного нанесения 1, 4, 6 и 8).
Процедура: мышей нагружали местными дозами 150 мкг амброзии (3 мкл 50 мг/мл) суспензии в 3 мкл сбалансированного солевого раствора в каждый глаз. Животных рандомизировали на основании изменений гиперемии в день 24 по сравнению с исходным уровнем.
a.5 Сбор тканей
Животных умерщвляли и, удостоверившись в их смерти, извлекали правый глаз и окружающие придатки глаза и хранили в фиксаторе Дэвидсона в течение 24 часов. После 24 часов фиксации ткань переносили в 70% этанол для длительного хранения. Глаза заключали в парафин и готовили 1 окрашенный гематоксилином-эозином, 1 окрашенный толуидином синим и 1 неокрашенный препарат для каждого глаза.
a.6 Статистические способы
Данные анализировали с помощью двухфакторного дисперсионного анализа с поправкой Бонферрони для сравнения различий клинических признаков между группами.
B. Результаты
Данные по гиперемии, косоглазию, отеку века и выделениям из глаз представляют собой среднее ± стандартную ошибку среднего для N=8 глаз. Тот же наблюдатель, не имеющей информации о кодах обработки, оценивал мышей при нагрузке 1, 4, 6 и 8, проведенной в дни исследования 28, 29, 30 и 31, соответственно. В случае гиперемии, косоглазия и выделения из глаз животных оценивали по шкале тяжести 0-4 (при этом 0 считали нормой, а 4 наиболее тяжелой степенью). В случае отека века мышей оценивали по шкале 0-2. Для каждой конечной точки животных оценивали через 30 минут после введения дозы (только для Patanol®) или в исходный период перед нагрузкой в тот день (для всех других групп). Все группы анализировали с помощью двухфакторного дисперсионного анализа с поправкой Бонферрони, и любую статистическую значимость по сравнению с инертным носителем отмечали звездочкой.
b.1 Изменение последозовой гиперемии - профилактика SEQ ID NO. 112 (SYL116011) по сравнению с Patanol® и профилактикой инертным носителем.
Данные представляют собой среднее ± стандартная ошибка среднего для n=8 глаз в группе. Patanol® демонстрировал статистически меньший ответ после первой нагрузки в день 28 (p<0,01). Профилактические дозы SEQ ID NO. 112 (SYL116011) демонстрировали схожую с Patanol® тенденцию, но статистическая значимость не обнаружена (см. Фигуру 26).
b.2 Изменение последозового косоглазия - профилактика SEQ ID NO. 112 (SYL116011) по сравнению с Patanol® и профилактикой инертным носителем.
Данные представляют собой среднее ± стандартная ошибка среднего для n=8 глаз в группе (см. Фигуру 27). Статистическая значимость не обнаружена.
b.3 Изменение последозового отека века - профилактика SEQ ID NO. 112 (SYL116011) по сравнению с Patanol® и профилактикой инертным носителем.
Данные представляют собой среднее ± стандартная ошибка среднего для n=8 глаз в группе (см. Фигуру 28). Статистическая значимость не обнаружена.
b.4 Изменение последозового выделения из глаз - профилактика SEQ ID NO. 112 (SYL116011) по сравнению с Patanol® и профилактикой инертным носителем.
Данные представляют собой среднее ± стандартная ошибка среднего для n=8 глаз в группе (см. Фигуру 29). Статистическая значимость не обнаружена.
C. Выводы
По итогам исследования представляется, что хотя профилактика SEQ ID NO. 112 (SYL116011) сохраняла ту же тенденцию снижения гиперемии, отека века и выделения из глаз (см. Фигуры 26-29), однако она не была статистически значимой при анализе этих данных с помощью двухфакторного дисперсионного анализа с поправкой Бонферрони из-за малого N, применяемого в данном исследовании.
Примечательно то, что при оценке эффектов SEQ ID NO. 112 (SYL116011) настоящего изобретения, созданных для подавления экспрессии ORAI1, результаты показали схожую тенденцию дозозависимого ответа в группе SEQ ID NO. 112 (SYL116011), что и в группе, обработанной Patanol®, известным противоаллергическим лекарственным средством, в настоящее время представленным на рынке, уменьшая в обоих случаях симптомы аллергии, ассоциированные с аллергическим конъюнктивитом, в мышиной модели. Ожидают, что при более высоких значениях N анализ данных будет статистически значимым.
ССЫЛКИ
Angaji S.A, Hedayati S.S, Poor R.H, et al. "Application of RNA interference in treating human diseases" J Genet. 2010. Vol. 89. 4. 527-37.
Baba Y, Nishida K, Fujii Y, Hirano T, et al. "Essential function for the calcium sensor STIM1 in mast cell activation and anaphylactic responses". Nat Immunol. 2008;9:81-88.
Bacsi A, Dharajiya N, Choudhury BK, et al. "Effect of pollen-mediated oxidative stress on immediate hypersensitivity reactions and late-phase inflammation in allergic conjunctivitis." J Allergy Clin Immunol. 2005 Oct; 116 (4):836-43.
Baumann TK & Martenson ME. "Extracellular protons both increase the activity and reduce the conductance of capsaicin-gated channels." J Neuroscl. 2000. 20:RC80.
Bergmeier W, Weidinger C, Zee I, Feske S. "Emerging roles of store-operated Ca (2+) entry through STIM and ORAI proteins in immunity, hemostasis and cancer" Channels (Austin). 2013 Mar 19;7(4).
Bramsen J.B., Laursen M.B., Nielsen A. F., et al. 2009 "A large-scale chemical modification screen identifies design rules to generate siRNAs with high activity, high stability and low toxicity" Nucleic Acids Res Vol. 37 Issue: 9 Pages:25 2867-81.
Caterina et al. "The capsaicin receptor: a heat-activated ion channel in the pain pathway." Nature. 1997 389(6653):816-24.
Caterina et al. "The vanilloid receptor: a molecular gateway to the pain pathway." Annual Rev Neuroscl. 2001 24:487-517.
Cerutti, L., N. Mian, et al. "Domains in gene silencing and cell differentiation proteins: the novel PAZ domain and redefinition of the Piwi domain." Trends Biochem Scl. 2000 25(10):481-2.
Collins, R. E. and X. Cheng. "Structural domains in RNAi." FEBS Lett 2005 579(26): 5841-9.
Chang C.I, Kim H.A, Dua P, et al. "Structural Diversity Repertoire of Gene Silencing Small Interfering RNAs" Nucleic Acid Ther. 2011. Vol. 21. 3. 125-31.
Deleavey G.F and Damha M.J. "Designing chemically modified oligonucleotides for targeted gene silencing". Chem Biol. 2012 Vol.19.8. 937-54.
Doench, J.G. Sharp, P.A. "Specificity of microRNA target selection in translational repression" Genes Dev. 2004 18, 504-511.
Elbashir, S. M., W. Lendeckel, et al. "RNA interference is mediated by 21- and 22-nucleotide RNAs." Genes Dev. 2001 15(2): 188-200.
Fire, A., S. Xu, et al. "Potent and specific genetic interference by double-stranded RNA in Caenorhabditis elegans." Nature. 1998 391(6669): 806-11.
Gonzalez, G. G., Garcia, P. et al. "Reduction of capsacin- induced ocular pain and neurogenic inflammation by calcium antagonists." Invest Ophthalmol Vis Scl. 1993 34 (12) :3329-3335.
Hoth M, Penner R. "Depletion of intracellular calcium stores activates a calcium current in mast cells". Nature. 1992;355:353-356.
Huang WC, Chai CY, Chen WC, et al. "Histamine regulates cyclooxygenase 2 gene activation through Orail-mediated NFkB activation in lung cancer cells" Cell Calcium. 2011 Jul; 50 (1):27-35
Hutvagner, G. and P. D. Zamore. "A microRNA in a multiple-turnover RNAi enzyme complex." Science. 2002.297(5589):2056-60.
Kari O. and Saari KM. "Updates in the treatment of ocular allergies". Journal of Asthma and Allergy 2010:3 149-158.
Key B. Allergy and allergic diseases. Part I. N. Engl J Med. 2001; 344:30-37.
Kim D.H., Behlke M.A., Rose S.D., et al. "Synthetic dsRNA Dicer substrates enhance RNAi potency and efficacy" Nat Biotechnol 2005. Vol. 23 Issue: 2 Pages: 222-6.
Kornbrust D, Cavagnaro J, Levin A, et al. "Oligo safety working group exaggerated pharmacology subcommittee consensus document" Nucleic Acid Ther 2013 Vol. 23, 1, Pag: 21-8.
La Rosa M, Lionetti E, Reibaldi M, et al. "Allergic conjunctivitis: a comprehensive review of the literature" Italian Journal of Pediatrics 2013, 39:18.
Lewis, B.P., Shih I. et al. "prediction of mammalian micro RNA targets." Cell. 2003 115:787-798.
Liu, J., M. A. Carmell, et al. "Argonaute2 is the catalytic engine of mammalian RNAi." Science. 2004 305 (5689):1437-41.
Livak K. J. and Schmittgen T. D., "Analysis of relative gene expression data using real-time quantitative PCR and the 2(-Delta Delta C(T)) Method" Methods. 2001; Vol: 25, Issue: 4, Pages: 402-8.
Ma, J. B., Y. R. Yuan, et al. "Structural basis for 5'-end-specific recognition of guide RNA by the A. fulgidus Piwi protein." Nature. 2005 434(7033): 666-70.
Magone MT, Chan CC, Rizzo LV, Kozhich AT, Whitcup SM. "A novel murine model of allergic conjunctivitis". Clin Immunol Immunopathol. 1998;87:75-84.
Maniatis, T., et al., "Molecular Cloning: A Laboratory Manual". Cold Spring Harbor Laboratory, 1982, at pages 387-389.
Montell et al. "Short hairpin RNAs (shRNAs) induce sequence-specific silencing in mammalian cells." Genes Dev. 2002 16 (8):948-58.
Nykanen, A., B. Haley, et al. "ATP requirements and small interfering RNA structure in the RNA interference pathway." Cell 2001 107 (3):309-21.
Ono SJ, Abelson MB. "All ergic conjunctivitis: update on pathophysiology and prospects for future treatment" J. Allergy Clin. Immunol. 2005, 75(1), 1 18-122.
Orban, T. I. and E. Izaurralde. "Decay of mRNAs targeted by RISC requires XRN1, the Ski complex, and the exosome." Rna. 2005 11(4):459-69.
Parekh AB, Putney JW, Jr. "Store-operated calcium channels". Physiol Rev 2005; 85:757-810.
Parrish, S., J. Fleenor, et al. "Functional anatomy of a dsRNA trigger: differential requirement for the two trigger strands in RNA interference." Mol Cell. 2000 6(5): 1077-87.
Popescu FD. "Antisense- and RNA interference-based therapeutic strategies in allergy" J Cell Mol Med. 2005 Oct-Dec;9(4):840-53.
Rand, T. A., S. Petersen, et al. "Argonaute2 cleaves the anti-guide strand of siRNA during RISC activation." Cell. 2005 123 (4):621-9.
Reynolds, A., Leake, D., et al. "Rational siRNA design for RNA interference" Nat Biotechnol. 2004 22(3):326-30.
Sanghvi Y.S. "A status update of modified oligonucleotides for chemotherapeutics applications" Curr Protoc Nucleic Acid Chem. 2011 Vol. 4. 41 1-22.
Schubert, S. et al. "Local RNA target structure influences siRNA efficacy: systematic analysis of intentionally designed binding regions." J Mol Biol. 2005 348:883-893.
Smyth JT, Dehaven WI, Jones BF, et al. "Emerging perspectives in store-operated Ca2+ entry: roles of Orai, Stim and TRP". Blochlm Blophys Acta 2006;1763:1147-1160.
Song, J. J., S. K. Smith, et al. "Crystal structure of Argonaute and its implications for RISC slicer activity." Science. 2004 305(5689): 1434-7.
Suzuki M, Zheng X, Zhang X, et al. "Inhibition of allergic responses by CD40 gene silencing" Allergy. 2009 Mar;64(3):387-97.
Suzuki M, Zheng X, Zhang X, et al. "A novel allergen- specific therapy for allergy using CD40-silenced dendritic cells" J Allergy Clin Immunol. 2010 Mar;125(3):737-43.
Ui-Tei, K., Naito, Y., et al. "Guidelines for the selection of highly effective siRNA sequences for mammalian and chick RNA interference." Nucleic Acids Res. 2004 32(3): 936-48.
Vig M, DeHaven WI, Bird GS, et al. "A major defect in mast cell effector functions in CRACM1-/- mice" Nat Immunol. 2008 Jan;9(1):89-96.
Walton S.P, Wu M, Gredell J.A and Chan C. "Designing highly active siRNAs for therapeutic applications" FEBS J. 2010. Vol. 277. 23. 4806-13.
Wang Y, Lin L, Zheng C. "Downregulation of Orail expression in the airway alleviates murine allergic rhinitis" Exp Mol Med. 2012 Mar 31; 44 (3):177-90.
Yang I-H, Tsai Y-T et al. "Involvement of STIM1 and ORAI1 in EGF-mediated cell growth in retinal pigment epithelial cells" Journal of Biomedical Science. 2013; 20:41.
Zheng X, Ma P, de Paiva CS, et al. TSLP and downstream molecules in experimental mouse allergic conjunctivitis. Invest Ophthalmol Vis Scl 2010;51:3076-3082.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ лечения аллергической бронхиальной астмы, основанный на подавлении экспрессии генов цитокинов IL-4 и IL-13 с использованием молекул миРНК | 2016 |
|
RU2615463C1 |
| СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ БРОНХИАЛЬНОЙ АСТМЫ, ОСЛОЖНЯЮЩИХ ЕЕ РЕСПИРАТОРНЫХ ВИРУСНЫХ ИНФЕКЦИЙ И ДРУГИХ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ ДЫХАТЕЛЬНЫХ ПУТЕЙ | 2012 |
|
RU2526146C2 |
| КИРНК И ИХ ИСПОЛЬЗОВАНИЕ В СПОСОБАХ И КОМПОЗИЦИЯХ ДЛЯ ИНГИБИРОВАНИЯ ЭКСПРЕССИИ ГЕНА NRARP | 2016 |
|
RU2738971C2 |
| АНТИСМЫСЛОВЫЕ ОЛИГОНУКЛЕОТИДЫ ДЛЯ ЛЕЧЕНИЯ АЛЛЕРГИИ И ПРОЛИФЕРАЦИИ НЕОПЛАСТИЧЕСКИХ КЛЕТОК | 2005 |
|
RU2416412C2 |
| КОМПОЗИЦИЯ ДЛЯ ПОДАВЛЕНИЯ ЭКСПРЕССИИ ГЕНА ЦИТОКИНА ИНТЕРЛЕЙКИНА-4 | 2014 |
|
RU2563989C1 |
| ОЛИГОНУКЛЕОТИДНЫЕ ПОСЛЕДОВАТЕЛЬНОСТИ, НАЦЕЛЕННЫЕ НА ТРАНСКРИПЦИОННЫЙ ФАКТОР TSC22D4, ДЛЯ ЛЕЧЕНИЯ РЕЗИСТЕНТНОСТИ К ИНСУЛИНУ | 2016 |
|
RU2723091C2 |
| ТЕРАПЕВТИЧЕСКИЕ КОМПОЗИЦИИ И СПОСОБЫ ПРОТИВ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ С МОЛЕКУЛАМИ РНКИ, НАПРАВЛЕННЫМИ ПРОТИВ HSP47 | 2015 |
|
RU2756253C2 |
| КОМБИНИРОВАННАЯ ТЕРАПИЯ ГЕПАТОЦЕЛЛЮЛЯРНОЙ КАРЦИНОМЫ НА ОСНОВЕ СОРАФЕНИБА | 2022 |
|
RU2800071C1 |
| ИНГИБИРОВАНИЕ STAT-1 | 2002 |
|
RU2311910C2 |
| iPHK-ОПОСРЕДОВАННОЕ ИНГИБИРОВАНИЕ СВЯЗАННЫХ С ФАКТОРОМ НЕКРОЗА ОПУХОЛИ АЛЬФА СОСТОЯНИЙ | 2007 |
|
RU2469090C2 |






























































































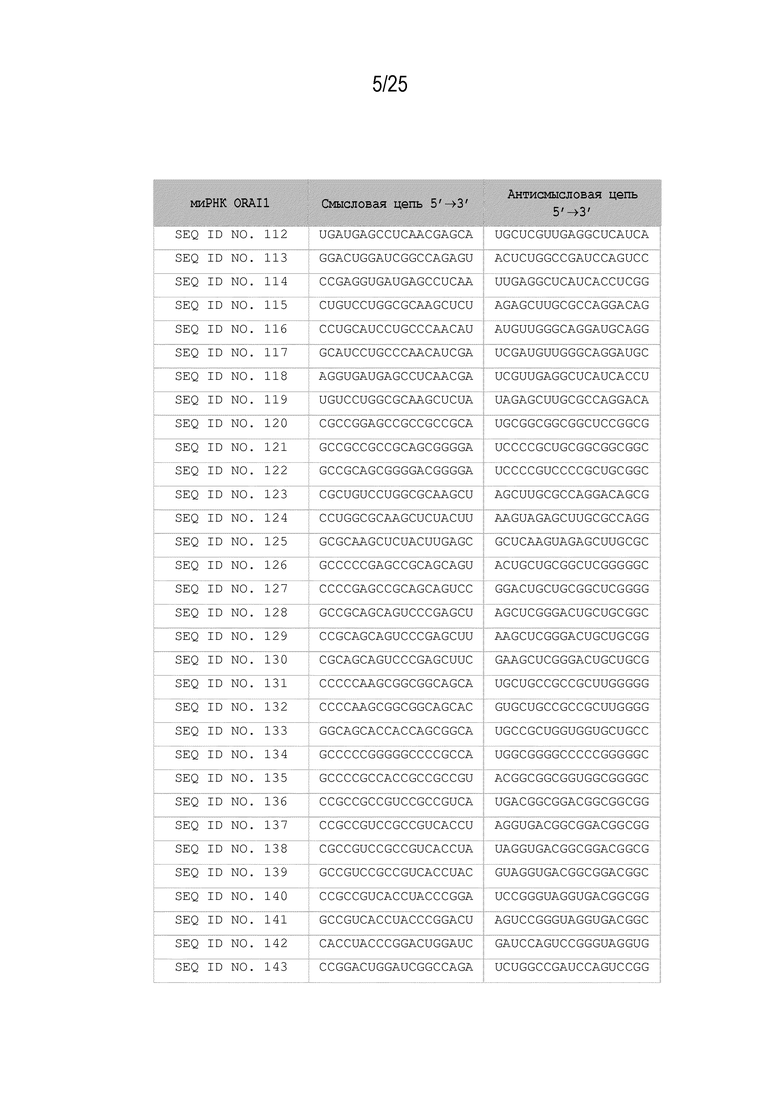



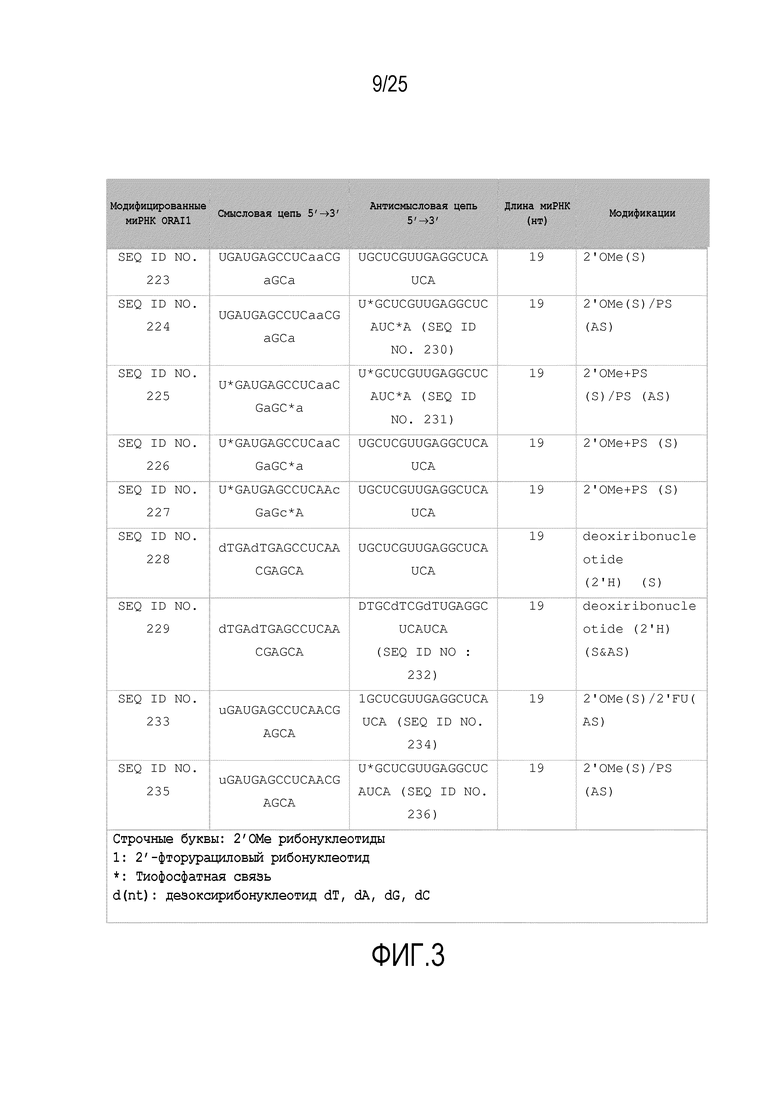
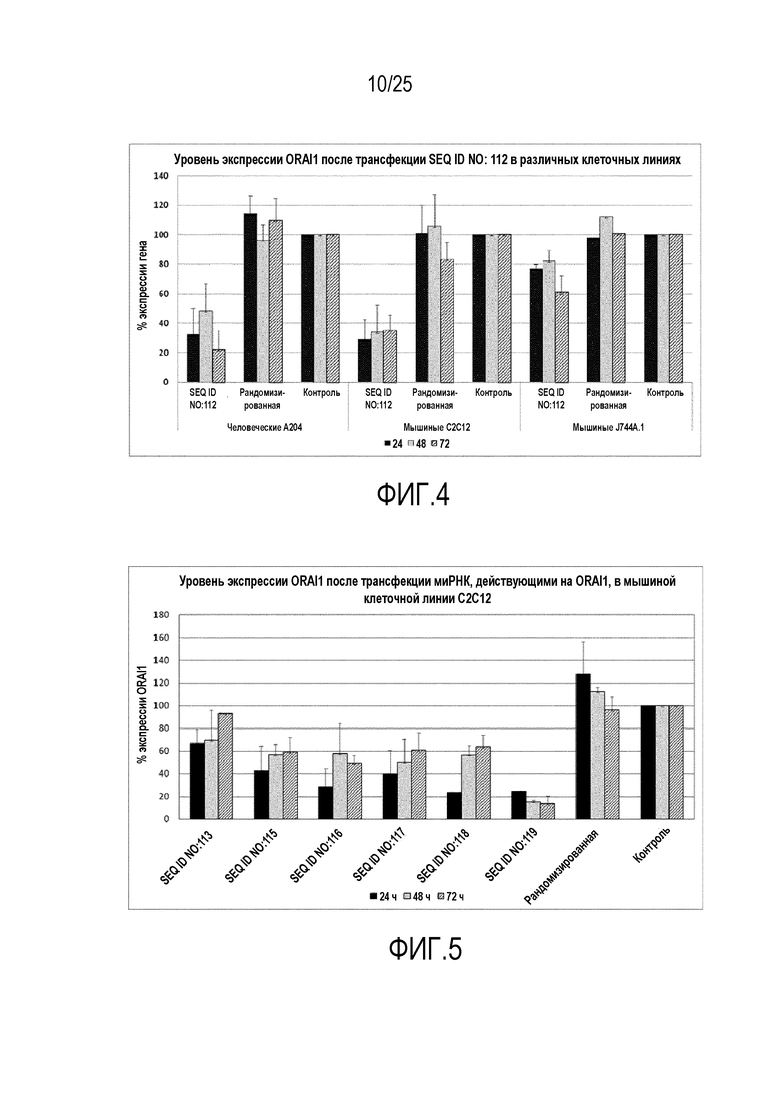
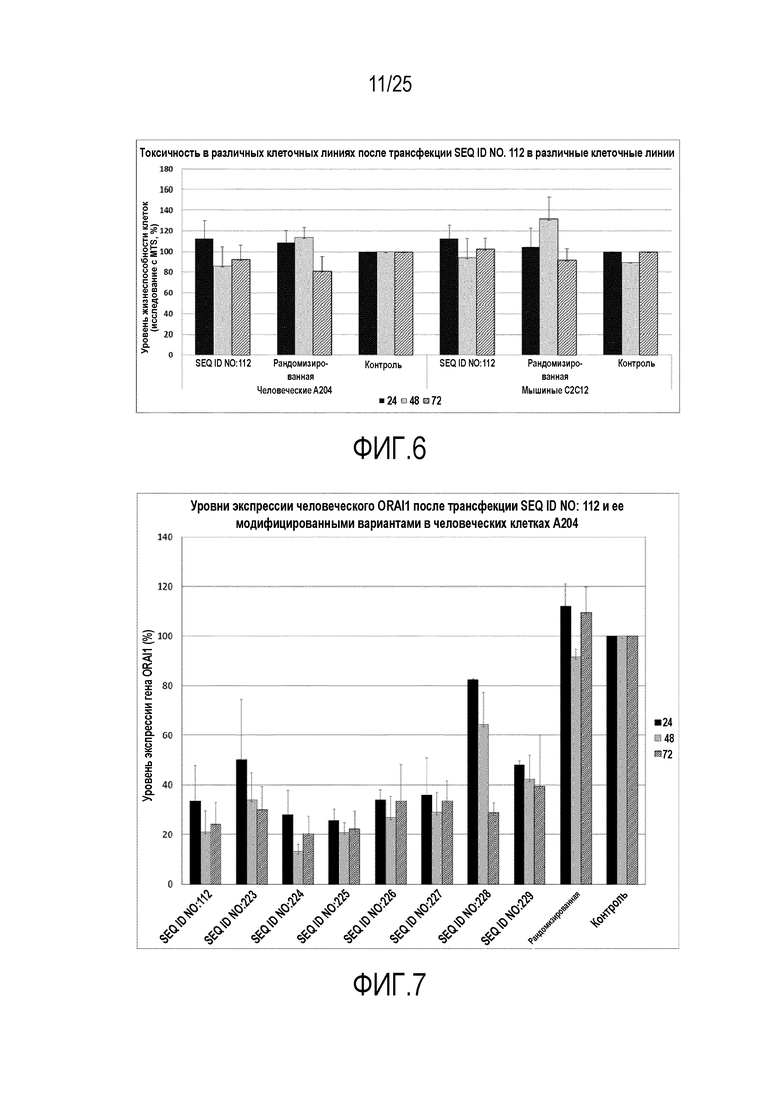
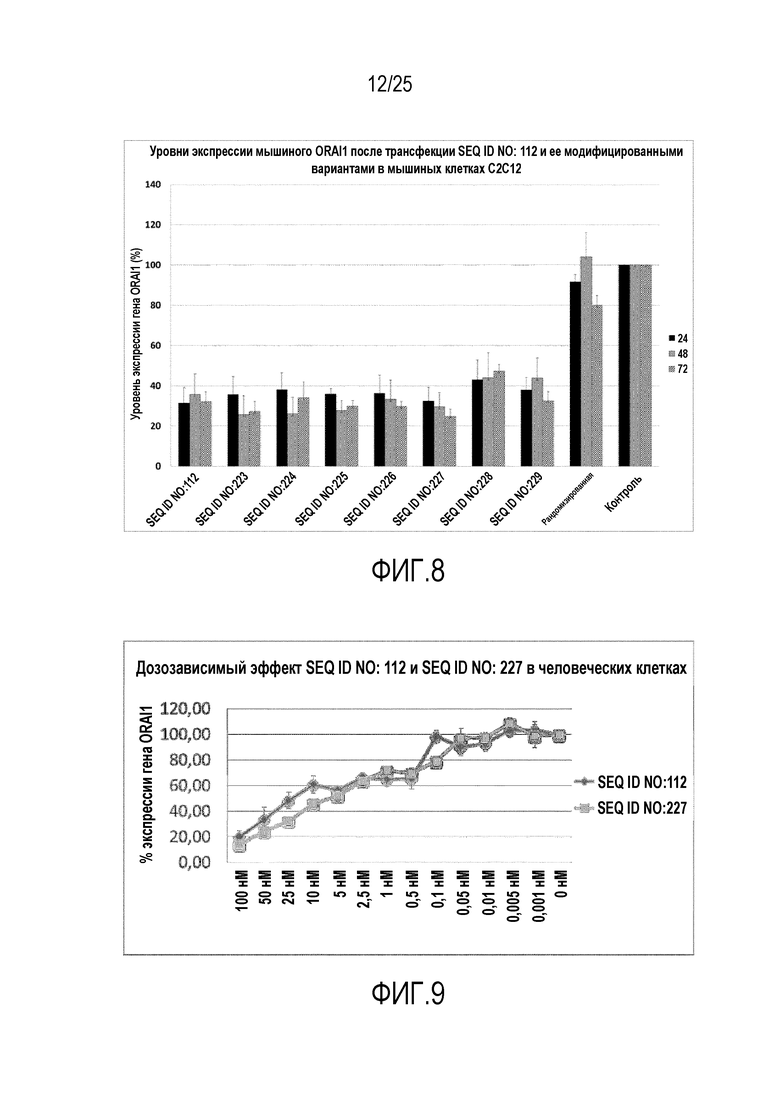
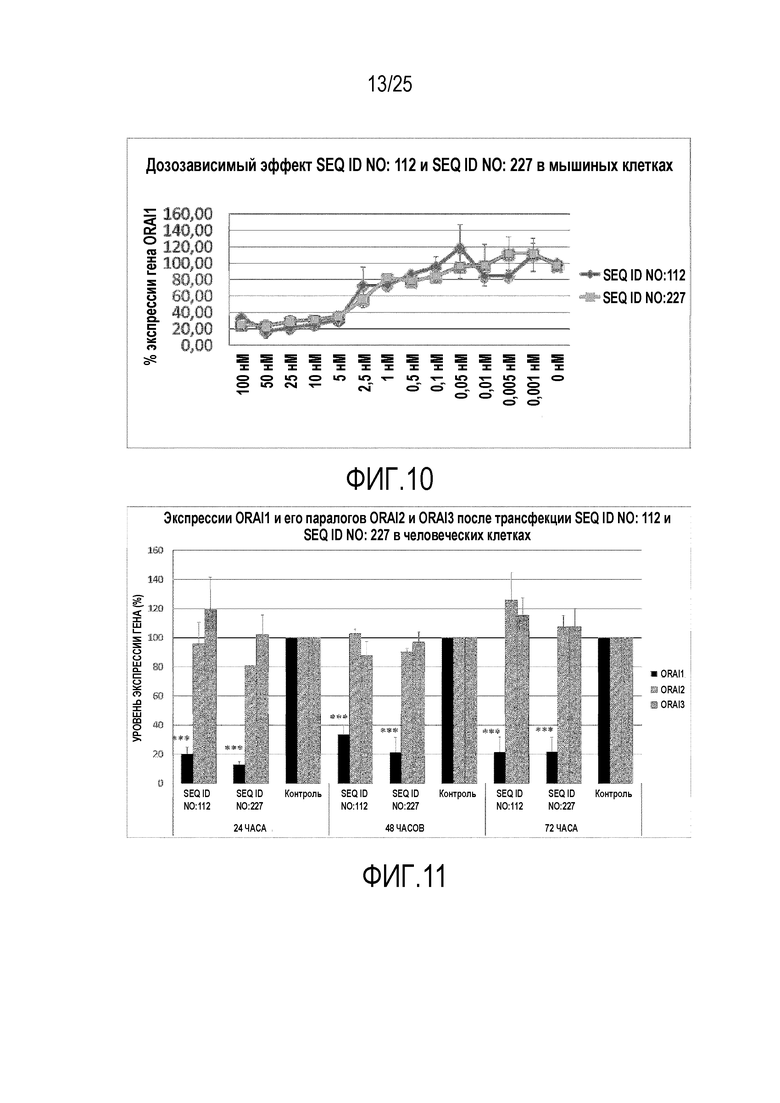
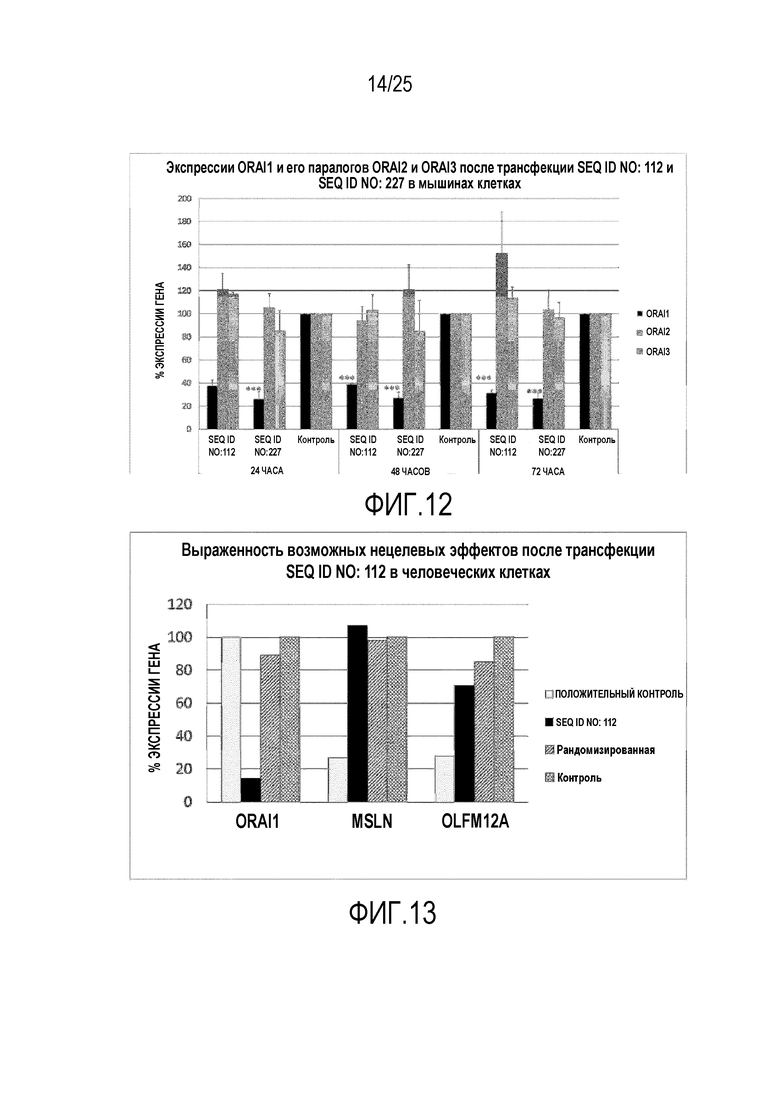
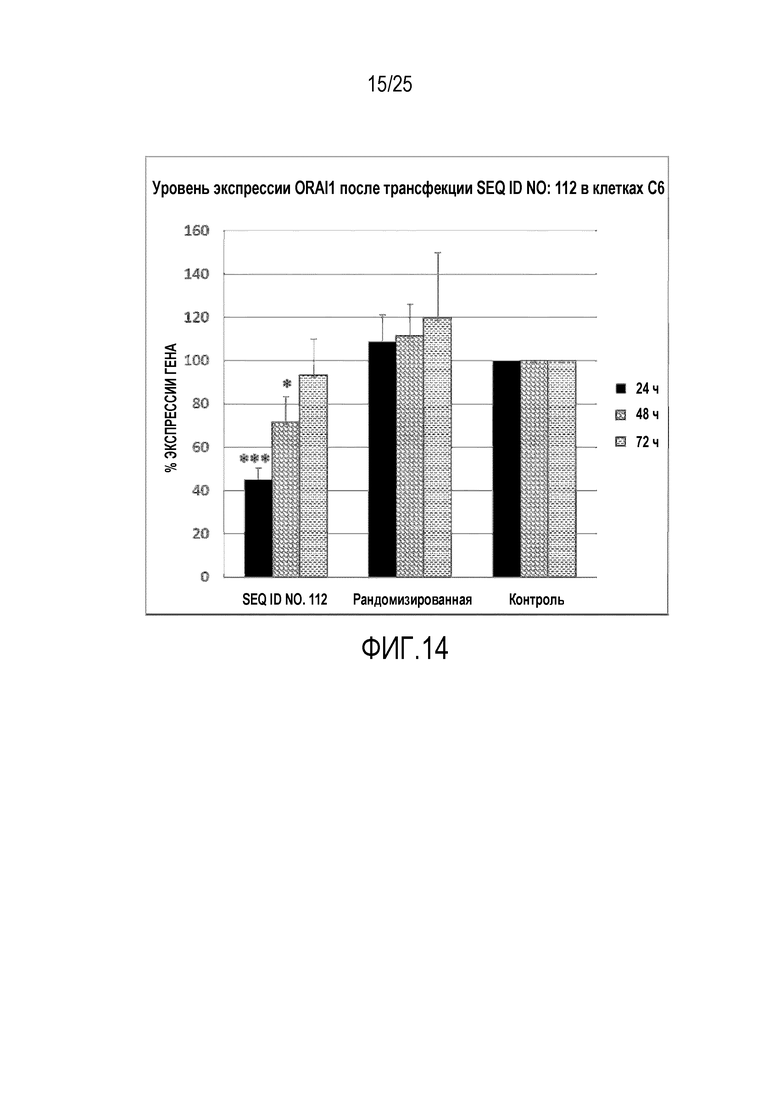
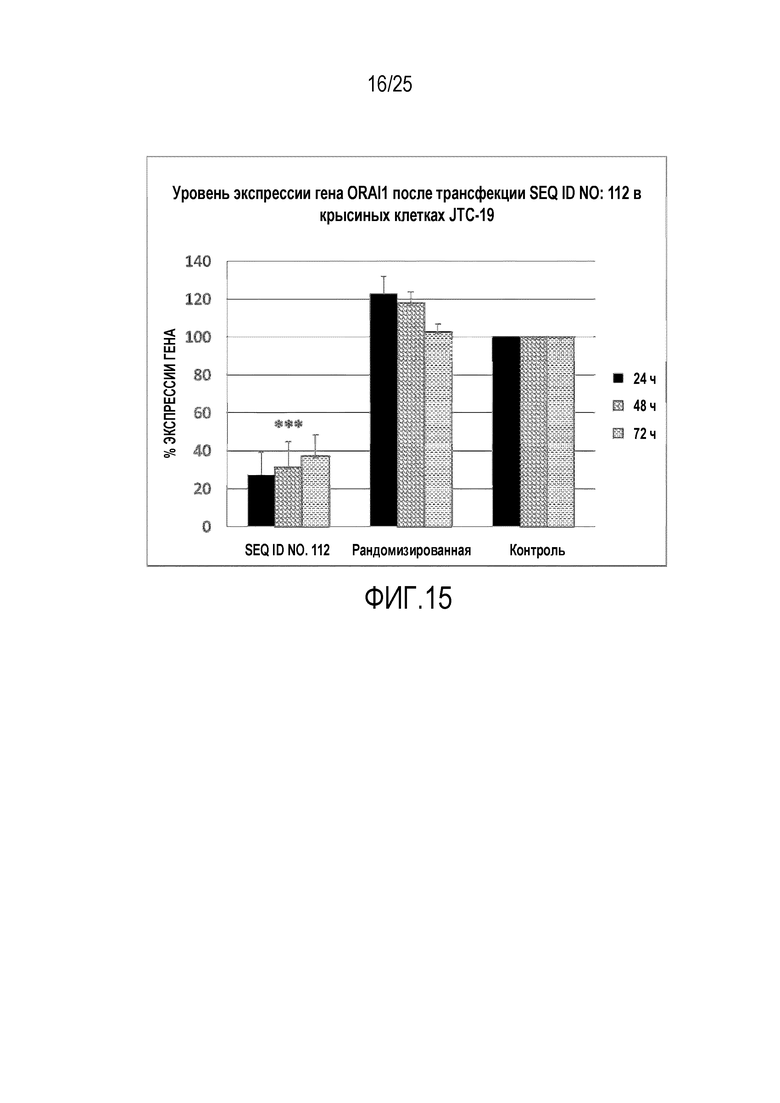
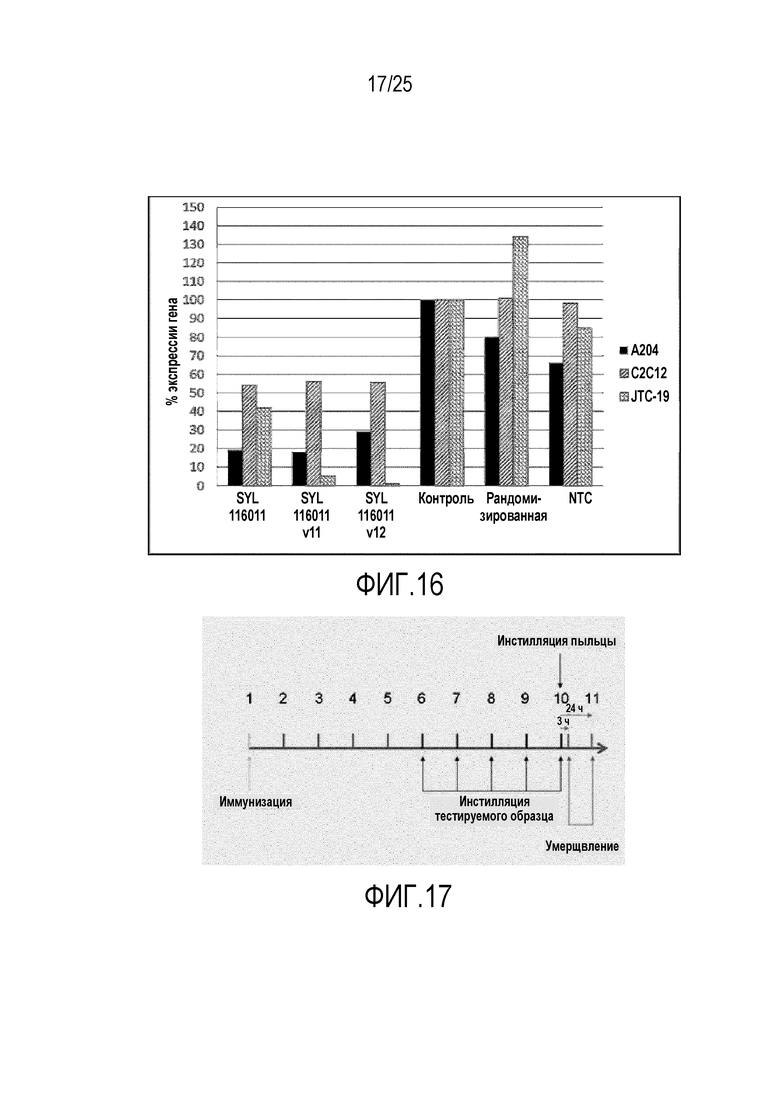
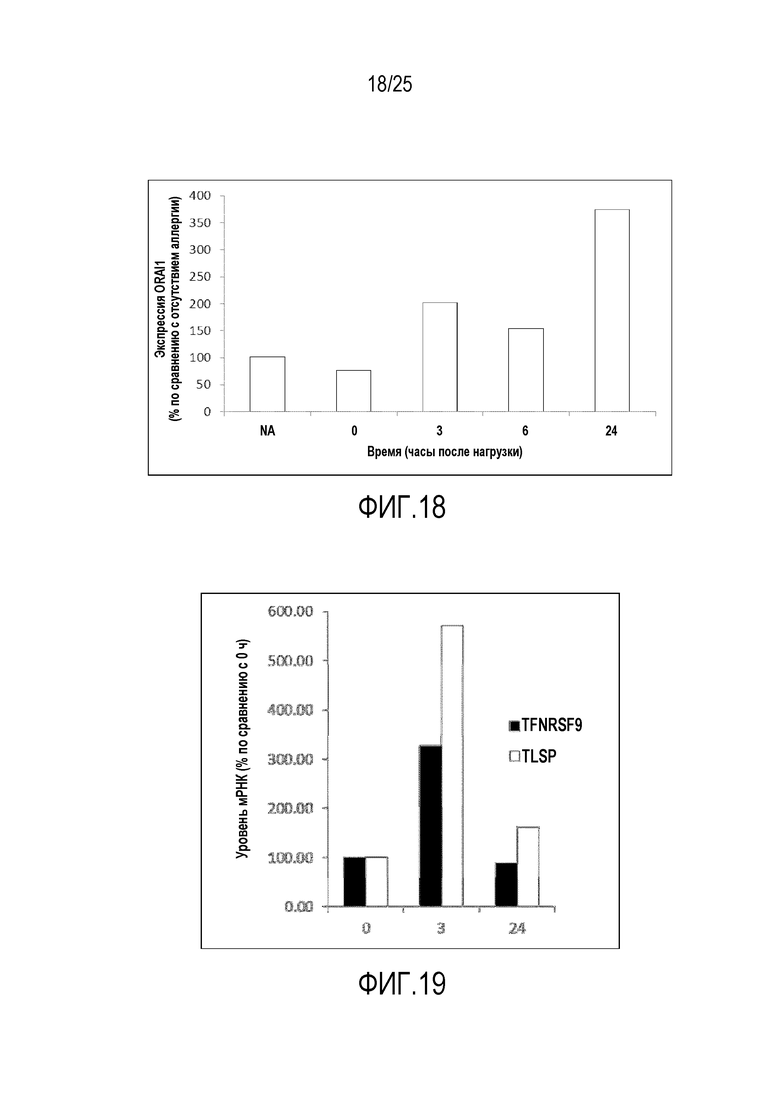
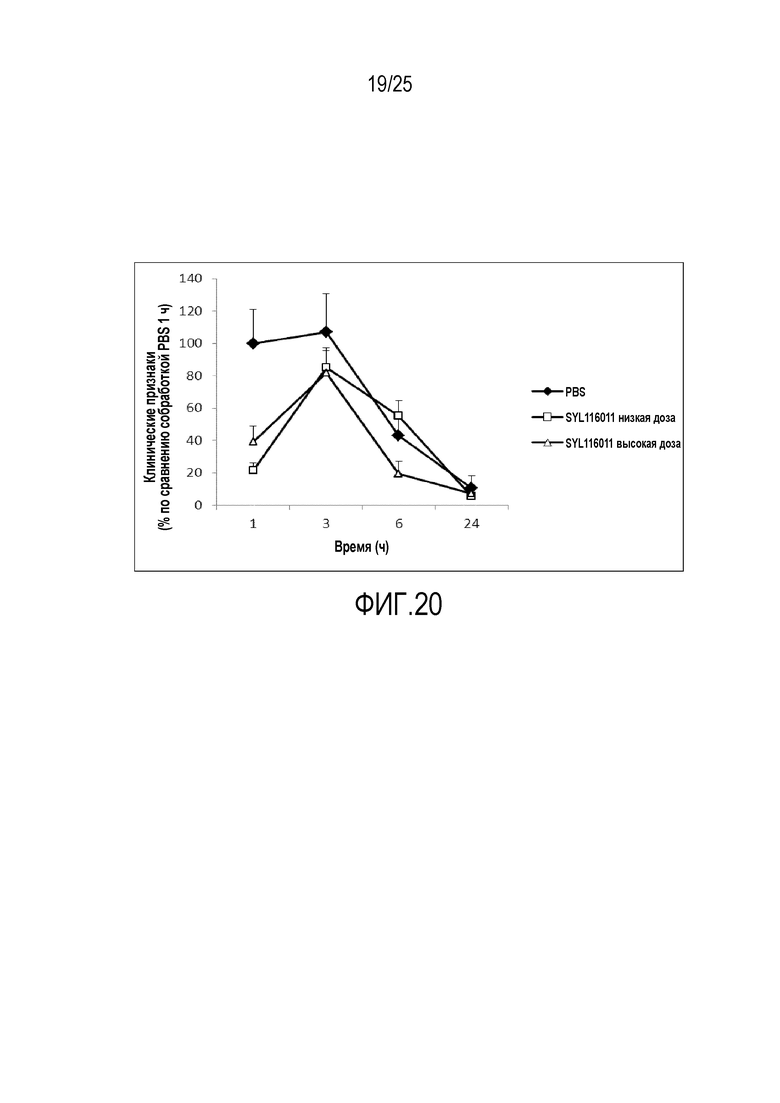
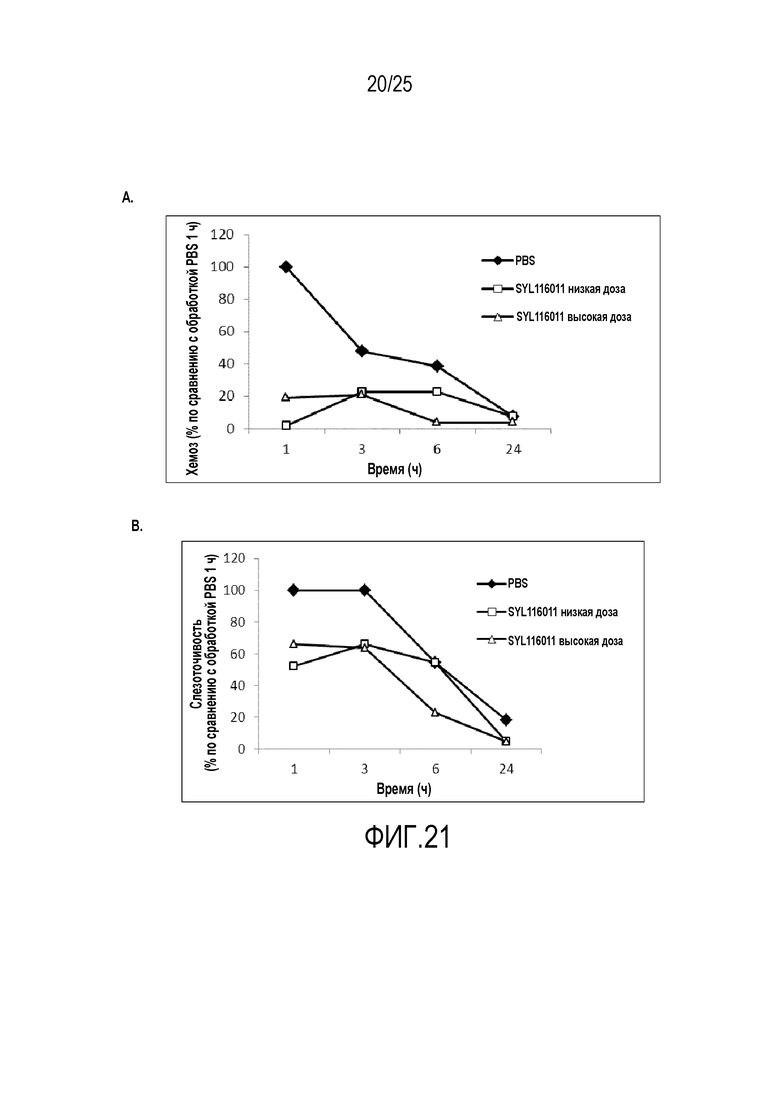
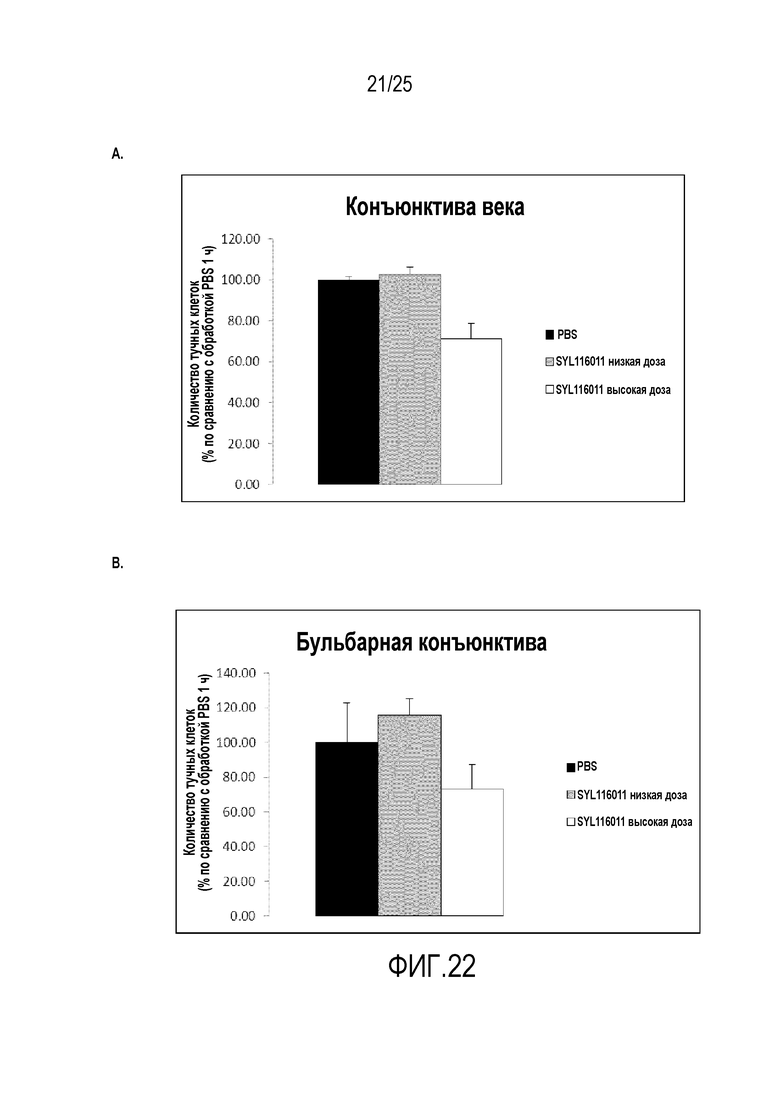
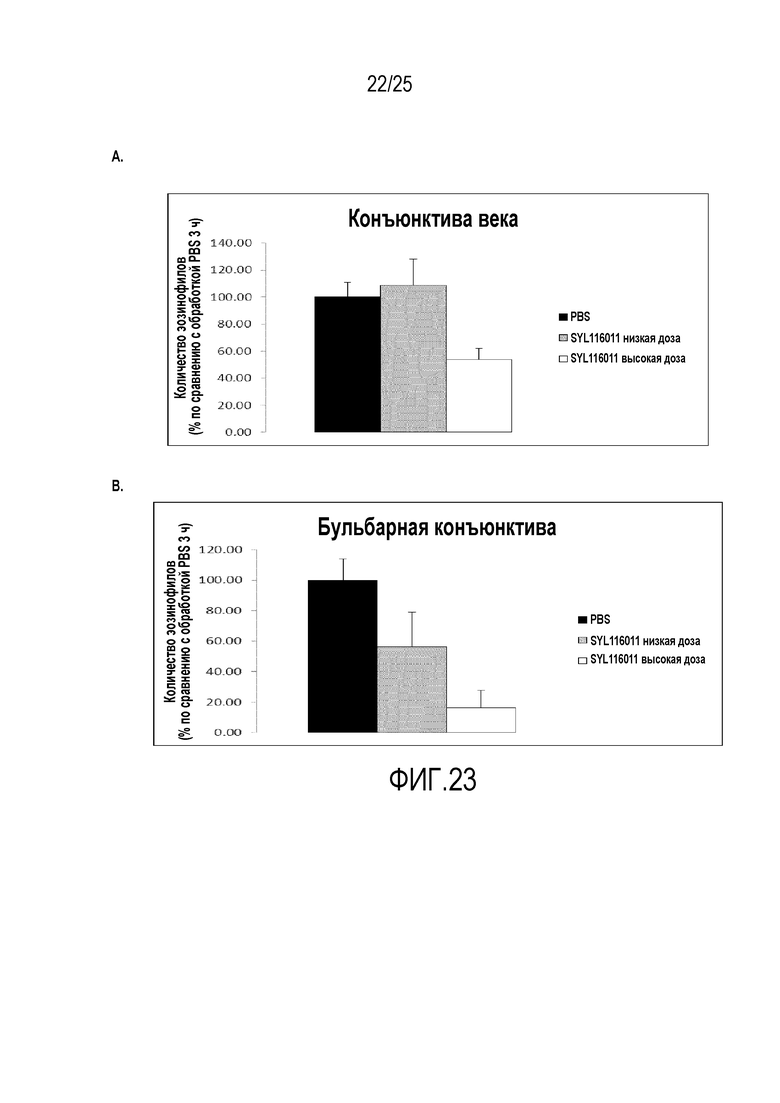

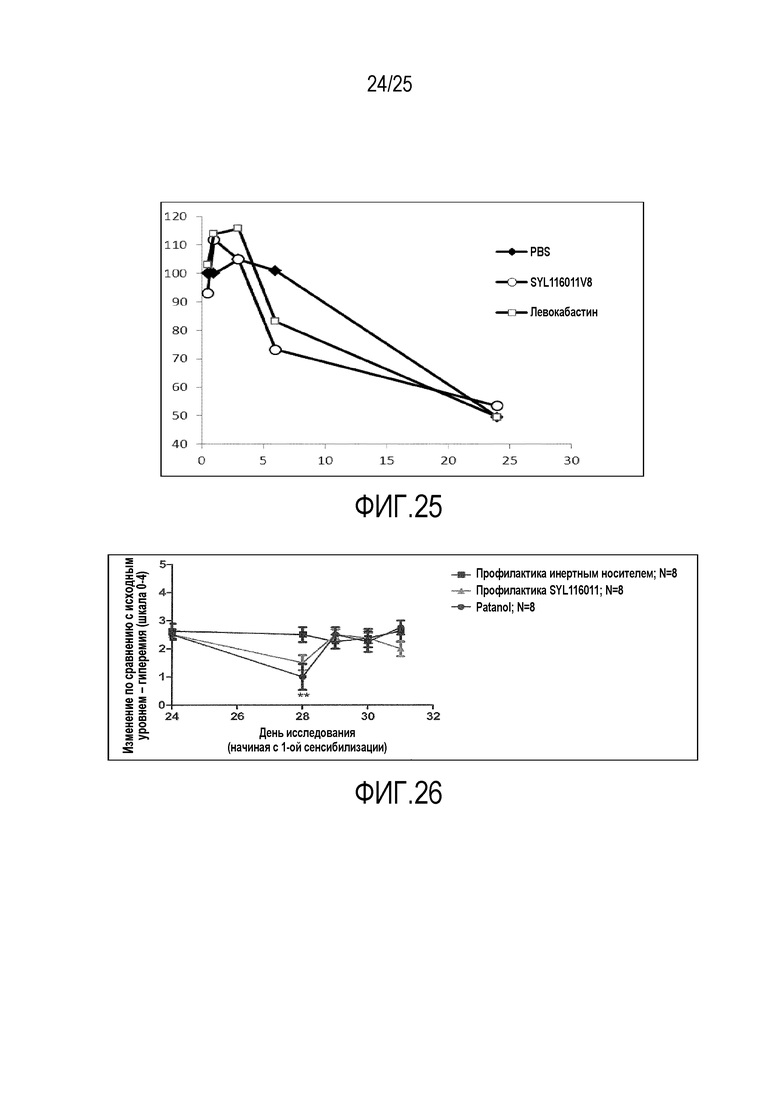
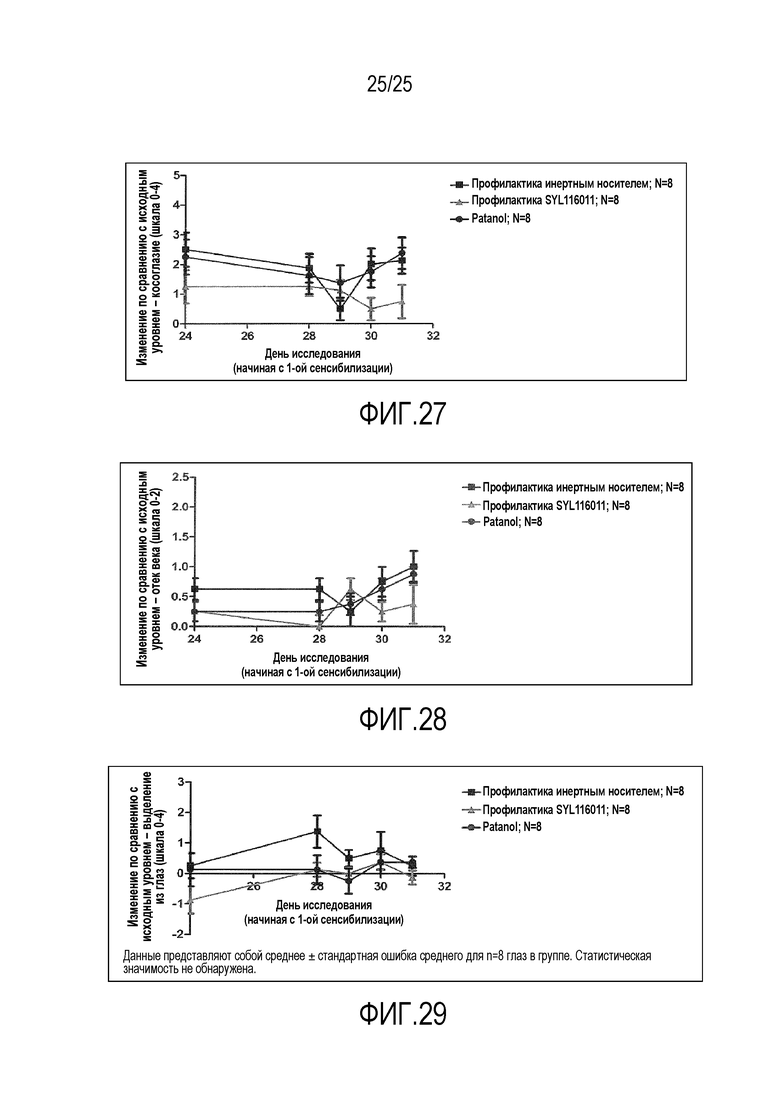
Изобретение относится к области биохимии. Описана группа изобретений, включающая молекулу миРНК, которая снижает экспрессию гена ORAI1 при введении в клетку, применение вышеуказанной молекулы миРНК в получении лекарственного средства для лечения состояния глаза, характеризующегося повышенной экспрессией или активностью гена ORAI1, и фармацевтическую композицию, содержащую вышеуказанную молекулу миРНК, для лечения и/или предотвращения состояния глаза, характеризующегося повышенной экспрессией или активностью ORAI1. В одном из вариантов изобретения молекула миРНК содержит 19-нуклеотидную двухцепочечную область. Изобретение расширяет арсенал средств для специфичного воздействия на ген ORAI1. 3 н. и 7 з.п. ф-лы, 29 ил., 1 табл., 32 пр.
1. Молекула миРНК, где указанная молекула специфично действует по меньшей мере на одну последовательность, выбранную из группы, состоящей из SEQ ID NO. 1 - SEQ ID NO. 111, и снижает экспрессию гена ORAI1 при введении в клетку, и где указанная миРНК содержит или состоит из по меньшей мере одной последовательности, выбранной из группы, состоящей из SEQ ID NO. 112, SEQ ID NO. 113, SEQ ID NO. 115-119, SEQ ID NO. 223-229, SEQ ID NO. 233 и SEQ ID NO. 235, и где указанная миРНК содержит 19-нуклеотидную двухцепочечную область.
2. Молекула миРНК по п.1, где указанная миРНК имеет тупые концы.
3. Молекула миРНК по п.1, где по меньшей мере один нуклеотид содержит химическую модификацию.
4. Молекула миРНК по п.3, где указанная химическая модификация нуклеотида выбрана из 2'-O-метилирования и замены урацилрибонуклеотидов дезокситимидиновыми нуклеотидами и их комбинаций.
5. Молекула миРНК по п.3, где указанная химическая модификация расположена в смысловой цепи, в антисмысловой цепи или в обеих цепях.
6. Молекула миРНК по п.3, где указанная миРНК выбрана по меньшей мере одной последовательности из группы, состоящей SEQ ID NO. 223 - SEQ ID NO. 229, SEQ ID NO. 233 и SEQ ID NO. 235.
7. Применение молекулы миРНК по п. 1 в получении лекарственного средства для лечения состояния глаза, характеризующегося повышенной экспрессией или активностью ORAI1.
8. Применение по п.7, где указанное состояние глаза является аллергическим заболеванием глаз и/или конъюнктивитом.
9. Применение по п.7, где указанное состояние глаза выбрано из сезонного аллергического конъюнктивита, круглогодичного аллергического конъюнктивита, весеннего кератоконъюнктивита, атопического кератоконъюнктивита, конъюнктивита с гиперплазией сосочков, синдрома сухости глаз и их комбинаций.
10. Фармацевтическая композиция для лечения и/или предотвращения состояния глаза, характеризующегося повышенной экспрессией или активностью ORAI1, где указанная композиция содержит по меньшей мере молекулу миРНК, описанную в п. 1, в фармацевтически эффективном количестве.
| I-HUI YANG et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| RU 2010122640 A (НОВАРТИС АГ) 10.12.2011. | |||
Авторы
Даты
2019-05-28—Публикация
2014-10-21—Подача