Область техники
Настоящее изобретение относится к производным пиразолопиридина, которые представляют собой блокаторы натриевых каналов и имеют множество терапевтических применений, в частности, при лечении боли.
Уровень техники
Производные пиразолопиридина по настоящему изобретению представляют собой блокаторы натриевых каналов и имеют множество терапевтических применений, в частности, при лечении боли.
Более конкретно, производные пиразолопиридина по изобретению представляют собой избирательные чувствительные к тетродотоксину (TTX-S) блокаторы. В нижеследующем обсуждении изобретение проиллюстрировано с помощью ссылки на ингибирование канала NaV1.3 или NaV1.7 в качестве TTX-S каналов. Они демонстрируют аффинность к каналу NaV1.3 или NaV1.7, которая значительно больше их аффинности к каналу NaV1.5, в качестве устойчивых к тетродотоксину (TTX-R) натриевых каналов. Производные пиразолопиридина по изобретению демонстрируют хорошую избирательность к каналу NaV1.3 или NaV1.7 по сравнению с каналом NaV1.5.
Канал NaV1.3 крысы и канал NaV1.3 человека клонировали в 1988 г., 1998 г., 2000 г., соответственно (NPL 1, NPL 2 и NPL 3). Канал NaV1.3 ранее был известен как натриевый канал головного мозга III типа. NaV1.3 присутствует на относительно высоких уровнях в нервной системе эмбрионов крыс, но едва поддается обнаружению у взрослых крыс. При лигатуре спинального нерва (SNL), хроническом констрикционном повреждении (CCI) и в моделях диабетической нейропатии (NPL 4, NPL 5, NPL 6 и NPL 7) после аксотомии возникает повышающая регуляция NaV1.3. Повышающая регуляция канала NaV1.3 вносит вклад в натриевый ток быстрой переподготовки в малых нейронах ганглия заднего корешка (DRG) (NPL 3). Эти наблюдения позволяют предположить, что NaV1.3 может вносить ключевой вклад в гипервозбудимость нейронов.
Для того чтобы подтвердить вклад натриевого канала NaV1.3 в болевые состояния, в моделях боли на животных использовали специфичные антисмысловые олигонуклеотиды (ASO). Обработка натриевого канала NaV1.3 с использованием ASO значительно ослабляла связанное с болью поведение после операции CCI (NPL 8). Эти находки позволяют предположить, что антагонист натриевого канала NaV1.3 можно использовать для того, чтобы лечить нейропатические болевые состояния.
Канал NaV1.7, по-видимому, является лучшей «подтвержденной» болевой мишенью. Наиболее впечатляющие находки в отношении NaV1.7 пришли из исследований генетики человека. Cox et al. (NPL 9) обнаруживали мутации SCN9A, которые вызывают потерю функции NaV1.7 в трех семействах из Пакистана. Их наблюдения связывают потерю функции NaV1.7 с врожденной неспособностью испытывать боль, вдобавок к доказательству, указывающему на канал NaV1.7 в качестве важного участника в ноцицепции человека.
В отличие от этого, также описаны мутации с приобретением функции, которые ведут к усиленной боли, например, первичная эритермалгия в одном случае и пароксизмальное экстремальное болевое нарушение в другом. Эти мутации с приобретением функции у пациентов ведут к различным типам изменений порогового тока в натриевых токах NaV1.7 и, что интересно, к различным степеням эффективности специфичных лекарственных средств, блокирующих натриевые каналы. Смысл этих находок заключается в том, что избирательный NaV1.7 блокатор может представлять собой эффективное лечение боли у человека.
Известно, что местный анестетик лидокаин и летучий анестетик галотан действуют как на TTX-R, так и на TTX-S натриевые каналы с низкой избирательностью и низкой активностью (значения IC50 находятся в диапазоне от 50 мкМ до 10 мМ). Эти анестетики в высоких системных концентрациях могут вызывать разрушительные побочные эффекты, например, паралич и остановку сердца. Однако системное введение лидокаина в низких концентрациях является эффективным при лечении хронической боли (NPL 10). У крыс применение очень низкой дозы TTX в DRG поврежденного сегмента спинномозгового нерва L5 значительно снижает механическое аллодиническое поведение (NPL 11). Это позволяет предположить, что TTX-S подтипы натриевых каналов играют важную роль в поддержании аллодинического поведения в животной модели нейропатической боли.
Канал NaV1.5 также является членом TTX-устойчивых натриевых каналов. Канал NaV1.5 почти исключительно экспрессирует ткань сердца, и показано, что он лежит в основании различных аритмий сердца и нарушений проводимости.
Список цитируемой литературы
Непатентная литература
{NPL 1} FEBS Lett. 228 (1), 187-194, 1988.
{NPL 2} J. Mol. Neurosci., 10 (1), 67-70, 1998.
{NPL 3} Eur. J. Neurosci. 12 (12), 4281-4289, 2000.
{NPL 4} J Neurophysiol 82, 2776-2785, 1999. J. A. Black et al.
{NPL 5} Ann Neurol 52, 786-792, 2002. M.J. Cranner et al.
{NPL 6} J Biol Chem 279, 29341-29350, 2004. S. Hong et al.
{NPL 7} Mol Brain Res 95, 153-161, 2001. C.H. Kim et al.
{NPL 8} J. Neurosci. 24, 4832-4839, 2004, Hains, B.C. et al.
{NPL 9} Nature 444, 894-898, 2006.
{NPL 10} Trends in Pharm. Sci 22, 27-31, 2001, Baker, M.D. et al.
{NPL 11} Brain Res 871, 98-103, 2000, Lyu, Y.S. et al.
Сущность изобретения
Техническая проблема
Цель изобретения состоит в том, чтобы предоставить новые TTX-S блокаторы, которые можно использовать в качестве лекарственных средств. Предпочтительные соединения должны эффективно связываться с TTX-S каналами (NaV1.3 и/или NaV1.7), при этом демонстрируя низкую аффинность к другим натриевым каналам, в частности, к каналу NaV1.5. Они должны хорошо абсорбироваться из желудочно-кишечного тракта, обладать метаболической стабильностью и иметь благоприятные фармакокинетические свойства. Они должны быть нетоксичными и демонстрировать незначительные побочные эффекты. Кроме того, идеальное лекарственное средство существует в физической форме, которая стабильна, не гигроскопична и которую легко формулировать.
В частности, производные пиразолопиридина по настоящему изобретению избирательны к TTX-S каналам относительно канала NaV1.5, что ведет к улучшению профиля побочных эффектов.
Следовательно, производные пиразолопиридина по настоящему изобретению можно использовать в лечении широкого диапазона нарушений, в частности, боли, острой боли, хронической боли, нейропатической боли, воспалительной боли, висцеральной боли, ноцицептивной боли, включая боль после хирургического вмешательства, и смешанных типов боли, включая боль во внутренних органах, желудочно-кишечном тракте, структурах черепа, скелетно-мышечной системе, спинном мозге, урогенитальной системе, сердечно-сосудистой системе и ЦНС, включая боль при злокачественной опухоли, в спине, орофациальную боль и боль, вызванную химиотерапией.
Другие состояния, которые можно лечить производными пиразолопиридина по настоящему изобретению, включают рассеянный склероз, нейродегенеративные нарушения, синдром раздраженной кишки, остеоартрит, ревматоидный артрит, нейропатологические нарушения, функциональные нарушения кишечника, воспалительные заболевания кишечника, боль, связанную с дисменореей, боль в тазу, цистит, панкреатит, мигрень, кластерные и тензионные головные боли, диабетическую нейропатию, периферичесую нейропатическую боль, ишиас, фибромиалгию, болезнь Крона, эпилепсию или эпилептические состояния, биполярную депрессию, тахиаритмии, нарушение настроения, биполярное нарушение, психиатрические нарушения, такие как тревога и депрессия, миотонию, аритмию, нарушения движения, нейроэндокринные нарушения, атаксию, недержание, висцеральную боль, невралгию тройничного нерва, герпетическую невралгию, общую невралгию, постгерпетическую невралгию, корешковую боль, ишиас, позвоночную боль, боль в голове или шее, острую или некупируемую боль, прорывную боль, боль после хирургического вмешательства, инсульт, боль при злокачественной опухоли, эпилепсию, и каузалгию.
Соединения демонстрировали активность по отношению к каналу NaV1.3 или NaV1.7. Дополнительно они демонстрировали избирательность к каналу NaV1.3 или NaV1.7 по сравнению с каналом NaV1.5.
Решение проблемы
По отношению к другим соединениям, раскрытым в данной области, соединения по настоящему изобретению могут демонстрировать меньшую токсичность, хорошую абсорбцию и распределение, хорошую растворимость, меньшее связывание с белками плазмы, меньшее взаимодействие между лекарственными средствами, хорошую метаболическую стабильность, сниженную ингибирующую активность в отношении канала HERG и/или сниженное удлинение QT.
[1] Данное изобретение предусматривает соединение следующей формулы (I):
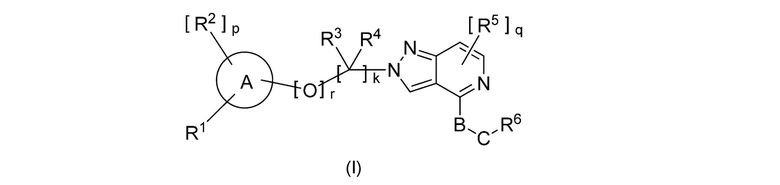 ,
,
в которой:
A представляет собой арил; предпочтительно, арил представляет собой пиридил, фенил, пиразинил, пиридазинил, пиразол, триазолил, индолил, бензимидазолил, или изохинолинил; более предпочтительно арил представляет собой пиридил, фенил, пиразинил, или пиридазинил; наиболее предпочтительным арилом является пиридил или фенил;
B выбран из группы, состоящей из химической связи, -C1-6 алкилена-, -C1-6 алкилен-NR2-, -NR2- и -(C=O)-;
C выбран из группы, состоящей из химической связи, -(C=O)- и -NR2-;
R1 независимо выбран из группы, состоящей из: (1) водорода, (2) -On-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (3) -On-C3-7 циклоалкила, где циклоалкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (4) -On-арила, где арил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (5) -S-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (6) -S-арила, где арил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (7) -NH-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, и (8) -NH-арила, где арил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11;
предпочтительно, R1 независимо выбран из группы, состоящей из: (2) -On-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (3) -On-C3-7 циклоалкила, где циклоалкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (4) -On-арила, где арил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, и (7) -NH-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11;
где n независимо равен 0 или 1, когда n равен 0, химическая связь присутствует вместо -On-;
R2 независимо выбран из группы, состоящей из: (1) водорода, (2) галогена, (3) гидроксила, (4) -On-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R7, (5) -On-C3-6 циклоалкила, где циклоалкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R7, (6) -On-C2-4 алкенила, где алкенил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R7, (7) -On-фенила или -On-нафтила, где фенил или нафтил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R7, (8) -On-гетероциклила, где гетероциклил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R7, (9) -(C=O)-NR8R9, (10) -NR8R9, (11) -S(O)2-NR8R9, (12) -NR8-S(O)2R9, (13) -S(O)t-R9, где t равно 0, 1 или 2, (14) -NR8(C=O)R9, (15) -CN и (16) -NO2;
где n независимо равен 0 или 1, когда n равен 0, химическая связь присутствует вместо -On-; предпочтительно, R2 независимо выбран из группы, состоящей из: (1) водорода, (2) галогена, (3) гидроксила и (4) -On-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R7; более предпочтительно R2 независимо выбран из группы, состоящей из: (1) водорода, (2) галогена, (3) метила и (4) метокси;
p равен 1, 2, 3 или 4; когда p равен двум или более чем двум, R2 могут быть одинаковыми или различными; предпочтительно р равно 1;
R3 и R4 независимо представляют собой водород или C1-6 алкил, который является незамещенным или замещенным одним или более заместителями, независимо выбранными из галогена, гидроксила и -O-C1-6 алкила; или R3 образует 3-7-членное кольцо с R4, который может содержать атом азота, атом кислорода, атом серы или двойную связь, где 3-7-членное кольцо необязательно замещено 1-6 заместителями, независимо выбранными из группы, состоящей из: (1) водорода, (2) гидроксила, (3) галогена, (4) C1-6 алкила, который является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (5) C3-6 циклоалкила, который является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (6) -O-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, и (7) -O-C3-6 циклоалкила, где циклоалкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11; предпочтительно, R3 представляет собой водород; предпочтительно R4 обозначает водород или C1-6 алкил; более предпочтительно R4 обозначает водород или метил;
R5 независимо выбран из группы, состоящей из: (1) водорода, (2) галогена, (3) -On-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R7, (4) -On-C3-6 циклоалкила, где циклоалкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R7, и (5) -On-C2-4 алкенила, где алкенил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R7;
где n независимо равен 0 или 1, когда n равен 0, химическая связь присутствует вместо -On-; предпочтительно, R5 представляет собой водород или C1-6 алкил; более предпочтительно R5 обозначает водород или метил;
R5 может быть в любом положении в пиразолопиридиновом кольце;
q равен 1, 2 или 3; когда q равен двум или более чем двум, R5 могут быть одинаковыми или различными; предпочтительно q равно 1;
R6 независимо представляет собой водород, C1-6 алкил, C1-6 алкокси, C2-6 алкенил, C3-7 циклоалкил, -NR8R9, гетероциклил, арил, арил-C1-6 алкил или гетероциклил-C1-6 алкил, где C1-6 алкил, C1-6 алкокси, C2-6 алкенил, C3-7 циклоалкил, гетероциклил, арил, арил-C1-6 алкил или гетероциклил-C1-6 алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из галогена, гидроксила, C1-6 алкила, -O-C1-6 алкила, -C3-7 циклоалкила, -O-C3-7 циклоалкила, гидроксил-C1-6 алкокси, -CN, -NR8R9, -(C=O)-R8, -(C=O)-NR8R9, -NR8-(C=O)-R9, -NR8-(C=O)-NR9R10, -NR8-(C=O)-OR9, -NR8-S(O)2-R9, -NR8-S(O)2-NR9R10 и -S(O)2-R8;
когда B представляет собой -NR2-, и C представляет собой -(C=O)-, R6 может образовывать 4-7-членное кольцо с R2;
предпочтительно R6 независимо представляет собой водород, C1-6 алкил, C3-7 циклоалкил, гетероциклил или арил, где алкил C1-6, C3-7 циклоалкил, гетероциклил, арил или, незамещенный или замещенный одним или несколькими заместителями, независимо выбран из галогена, гидроксила, C1-6 алкила, -O- C1-6 алкила, -CN, -NR8R9, и -NR8-(C=O)-R9; более предпочтительно R6 выбран из группы, состоящей из метила, этила, изопропила, и циклопропил, гетероциклил или арил, который является незамещенным или замещен одним или несколькими заместителями, независимо выбранными из галогена, гидроксила, C1-6 алкила, -О-C1-6 алкила, -CN;
более предпочтительно R6 также выбран из группы, состоящей из метила, этила, пропила, и циклопропил, который не замещен или замещен одним или несколькими заместителями, независимо выбранными из галогена, гидроксила, C1-6 алкила, -O-C1-6 алкила, -CN, -NR8R9 и-NR8-(C=O)-R9;
R7 выбран из группы, состоящей из: (1) водорода, (2) галогена, (3) гидроксила, (4) -(C=O)m-Ol-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (5) -Ol-(C1-3)перфторалкила, (6) -(C=O)m-Ol-C3-6 циклоалкила, где циклоалкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (7) -(C=O)m-Ol-C2-4 алкенила, где алкенил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (8) -(C=O)m-Ol-фенила или -(C=O)m-Ol-нафтила, где фенил или нафтил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (9) -(C=O)m-Ol-гетероциклила, где гетероциклил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (10) -(C=O)-NR8R9, (11) -NR8R9, (12) -S(O)2-NR8R9, (13) -S(O)t-R8, где t равен 0, 1 или 2, (14) -CO2H, (15) -CN и (16) -NO2;
где l равен 0 или 1, и m равен 0 или 1; когда l равен 0 или m равен 0, химическая связь присутствует вместо -Ol- или -(C=O)m, и когда l равен 0, и m равен 0, химическая связь присутствует вместо -(C=O)m-Ol-;
предпочтительно, R7 обозначает водород;
R8, R9 и R10 независимо представляют собой водород, C1-6 алкил, C2-6 алкенил, C3-7 циклоалкил или арил, который является незамещенным или замещенным одним или более заместителями, независимо выбранными из галогена, гидроксила, C1-6 алкила, -O-C1-6 алкила, C3-7 циклоалкила и -O-C3-7 циклоалкила; или R8 образует 4-7-членное кольцо с R9, которое может содержать атом азота, атом кислорода, атом серы или двойную связь, где 4-7-членное кольцо необязательно замещено 1-6 заместителями, независимо выбранными из группы, состоящей из: (1) водорода, (2) гидроксила, (3) галогена, (4) C1-6 алкила, который является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (5) C3-6 циклоалкила, который является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (6) -O-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, и (7) -O-C3-6 циклоалкила, где циклоалкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11;
предпочтительно, R8, R9 и R10 независимо представляют собой водород, C1-6 алкил или C3-7 циклоалкил;
R11 независимо выбран из группы, состоящей из: (1) водорода, (2) гидроксила, (3) галогена, (4) -C1-6 алкила, который является незамещенным или замещенным одним или более галогенами, (5) -C3-6 циклоалкила, (6) -O-C1-6 алкила, где алкил является незамещенным или замещенным одним или более галогенами, (7) -O(C=O)-C1-6 алкила, (8) -NH-C1-6 алкила, (9) фенила, (10) гетероциклила, (11) -CN и (12) -Si(C1-6 алкил)3; предпочтительно R11 обозначает галоген или -C3-6 циклоалкил;
k равен 1 или 2; предпочтительно k равно 1;
r равен 0 или 1, когда r равен 0, химическая связь присутствует вместо -[O]r-; предпочтительно r равно 0;
или его пролекарство или его фармацевтически приемлемая соль.
[2] Данное изобретение предусматривает соединение, представленное выше формулой (I), согласно [1],
где:
k равен 1;
r равен 0;
или его пролекарство или его фармацевтически приемлемая соль.
[3] Предпочтительные соединения по данному изобретению представлены следующей формулой (II):
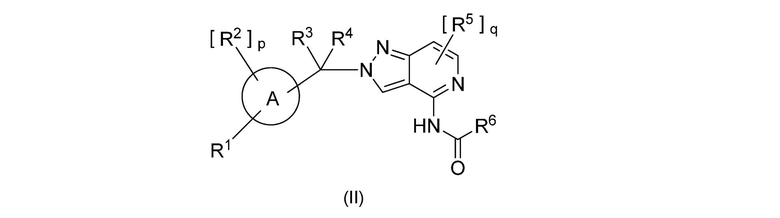 ,
,
в которой:
A представляет собой арил; предпочтительно, арил представляет собой пиридил, фенил, пиразинил, пиридазинил, пиразол, триазолил, индолил, бензимидазолил или изохинолинил; более предпочтительно арил представляет собой пиридил, фенил, пиразинил или пиридазинил; наиболее предпочтительным арилом является пиридил или фенил;
R1 независимо выбран из группы, состоящей из: (1) водорода, (2) -On-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (3) -On-C3-7 циклоалкила, где циклоалкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (4) -On-арила, где арил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (5) -S-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (6) -S-арила, где арил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11; (7) -NH-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, и (8) -NH-арила, где арил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11;
предпочтительно, R1 независимо выбран из группы, состоящей из: (2) -On-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (3) -On-C3-7 циклоалкила, где циклоалкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (4) -On-арила, где арил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, и (7) -NH-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11;
где n независимо равен 0 или 1, когда n равен 0, химическая связь присутствует вместо -On-;
R2 независимо выбран из группы, состоящей из: (1) водорода, (2) галогена, (3) гидроксила, (4) -On-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R7, (5) -On-C3-6 циклоалкила, где циклоалкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R7, (6) -On-C2-4 алкенила, где алкенил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R7, (7) -On-фенила или -On-нафтила, где фенил или нафтил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R7, (8) -On-гетероциклила, где гетероциклил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R7, (9) -(C=O)-NR8R9, (10) -NR8R9, (11) -S(O)2-NR8R9, (12) -NR8-S(O)2R9, (13) -S(O)t-R9, где t равен 0, 1 или 2, (14) -NR8(C=O)R9, (15) -CN и (16) -NO2;
где n независимо равен 0 или 1, когда n равен 0, химическая связь присутствует вместо -On-;
предпочтительно, R2 независимо выбран из группы, состоящей из: (1) водорода, (2) галогена, (3) гидроксила и (4) -On-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R7; более предпочтительно R2 независимо выбраны из группы, состоящей из: (1) водорода, (2) галогена, (3) метила и (4) метокси;
p равен 1, 2, 3 или 4; когда p равен двум или более чем двум, R2 могут быть одинаковыми или различными; предпочтительно р равно 1;
R3 и R4 независимо представляют собой водород или C1-6 алкил, который является незамещенным или замещенным одним или более заместителями, независимо выбранными из галогена, гидроксила и -O-C1-6 алкила; или R3 образует 3-7-членное кольцо с R4, которое может содержать атом азота, атом кислорода, атом серы или двойную связь, где 3-7-членное кольцо необязательно замещено 1-6 заместителями, независимо выбранными из группы, состоящей из: (1) водорода, (2) гидроксила, (3) галогена, (4) C1-6 алкила, который является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (5) C3-6 циклоалкила, который является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (6) -O-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, и (7) -O-C3-6 циклоалкила, где циклоалкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11;
предпочтительно, R3 представляет собой водород; предпочтительно R4 обозначает водород или C1-6 алкил; более предпочтительно R4 обозначает водород или метил;
R5 независимо выбран из группы, состоящей из: (1) водорода, (2) галогена, (3) -On-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R7, (4) -On-C3-6 циклоалкила, где циклоалкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R7, и (5) -On-C2-4 алкенила, где алкенил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R7;
где n независимо равен 0 или 1, когда n равен 0, химическая связь присутствует вместо -On-;
предпочтительно, R5 представляет собой водород или C1-6 алкил; более предпочтительно R5 обозначает водород или метил;
R5 может быть в любом положении в пиразолопиридиновом кольце;
q равен 1, 2 или 3; когда q равен двум или более чем двум, R5 могут быть одинаковыми или различными;
предпочтительно q равно 1;
R6 независимо представляет собой водород, C1-6 алкил, C1-6 алкокси, C2-6 алкенил, C3-7 циклоалкил, гетероциклил, арил, арил-C1-6 алкил или гетероциклил-C1-6 алкил, где C1-6 алкил, C1-6 алкокси, C2-6 алкенил, C3-7 циклоалкил, гетероциклил, арил, арил-C1-6 алкил или гетероциклил-C1-6 алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из галогена, гидроксила, C1-6 алкила, -O-C1-6 алкила, -C3-7 циклоалкила, -O-C3-7 циклоалкила, гидроксил-C1-6 алкокси, -CN, -NR8R9, -(C=O)-R8, -(C=O)-NR8R9, -NR8-(C=O)-R9, -NR8-(C=O)-NR9R10, -NR8-(C=O)-OR9, -NR8-S(O)2-R9, -NR8-S(O)2- NR9R10 и -S(O)2-R8;
предпочтительно R6 независимо представляет собой водород, C1-6 алкил, C3-7 циклоалкил, гетероциклил или арил, где алкил C1-6, C3-7 циклоалкил, гетероциклил, арил или незамещенный или замещенный одним или несколькими заместителями, независимо выбран из галогена, гидроксила, C1-6 алкила, -O- C1-6 алкила, -CN, -NR8R9, и -NR8-(C=O)-R9; более предпочтительно R6 выбран из группы, состоящей из метила, этила, изопропила, и циклопропил, гетероциклил или арил, который является незамещенным или замещен одним илинесколькими заместителями, независимо выбранными из галогена, гидроксила, C1-6 алкила, -О-C1-6 алкил, -CN;
R7 выбрано из группы, состоящей из: (1) водорода, (2) галогена, (3) гидроксила, (4) -(C=O)m-Ol-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (5) -Ol-(C1-3)перфторалкила, (6) -(C=O)m-Ol-C3-6 циклоалкила, где циклоалкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (7) -(C=O)m-Ol-C2-4 алкенила, где алкенил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (8) -(C=O)m-Ol-фенила или -(C=O)m-Ol-нафтила, где фенил или нафтил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (9) -(C=O)m-Ol-гетероциклила, где гетероциклил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (10) -(C=O)-NR8R9, (11) -NR8R9, (12) -S(O)2-NR8R9, (13) -S(O)t-R8, где t равен 0, 1 или 2, (14) -CO2H, (15) -CN и (16) -NO2;
где l равен 0 или 1 и m равен 0 или 1; когда l равен 0, или m равен 0, химическая связь присутствует вместо -Ol- или -(C=O)m-, и когда l равен 0, и m равен 0, химическая связь присутствует вместо -(C=O)m-Ol-;
предпочтительно, R7 обозначает водород;
R8, R9 и R10 независимо представляют собой водород, C1-6 алкил, C2-6 алкенил, C3-7 циклоалкил или арил, который является незамещенным или замещенным одним или более заместителями, независимо выбранными из галогена, гидроксила, C1-6 алкила, -O-C1-6 алкила, C3-7 циклоалкила и -O-C3-7 циклоалкила; или R8 образует 4-7-членное кольцо с R9, которое может содержать атом азота, атом кислорода, атом серы или двойную связь, где 4-7-членное кольцо необязательно замещено 1-6 заместителями, независимо выбранными из группы, состоящей из: (1) водорода, (2) гидроксила, (3) галогена, (4) C1-6 алкила, который является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (5) C3-6 циклоалкила, который является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (6) -O-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, и (7) -O-C3-6 циклоалкила, где циклоалкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11;
предпочтительно, R8, R9 и R10 независимо представляют собой водород, C1-6 алкил или C3-7 циклоалкил;
R11 независимо выбран из группы, состоящей из: (1) водорода, (2) гидроксила, (3) галогена, (4) -C1-6 алкила, который является незамещенным или замещенным одним или более галогенами, (5) -C3-6 циклоалкила, (6) -O-C1-6 алкила, где алкил является незамещенным или замещенным одним или более галогенами, (7) -O(C=O)-C1-6 алкила, (8) -NH-C1-6 алкила, (9) фенила, (10) гетероциклила, (11) -CN и (12) -Si(C1-6 алкил)3;
предпочтительно R11 обозначает галоген или -C3-6 циклоалкил;
или его пролекарство или его фармацевтически приемлемая соль.
[4] Более предпочтительны соединения, описанные в [3], где:
R2 независимо выбран из группы, состоящей из: (1) водорода, (2) галогена, (3) метила и (4) метокси;
p равен 1;
R3 представляет собой водород;
R4 представляет собой водород или метил;
R6 выбран из группы, состоящей из метила, этила, изопропила и циклопропила, гетероциклила или арила, который является незамещенным или замещенным одним или более заместителями, независимо выбранными из галогена, гидроксила, C1-6 алкила, -O-C1-6 алкила, -CN;
или его пролекарство или его фармацевтически приемлемая соль.
[5] Предпочтительные соединения по данному изобретению представлены следующей формулой (III):
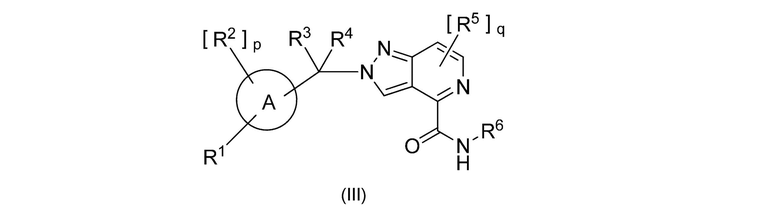 ,
,
в которой:
A представляет собой арил; предпочтительно, арил представляет собой пиридил, фенил, пиразинил, пиридазинил, пиразол, триазолил, индолил, бензимидазолил или изохинолинил; более предпочтительно арил представляет собой пиридил, фенил, пиразинил или пиридазинил; наиболее предпочтительным арилом является пиридил или фенил;
R1 независимо выбран из группы, состоящей из: (1) водорода, (2) -On-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (3) -On-C3-7 циклоалкила, где циклоалкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (4) -On-арила, где арил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (5) -S-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (6) -S-арила, где арил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11; (7) -NH-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, и (8) -NH-арила, где арил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11;
предпочтительно, R1 независимо выбран из группы, состоящей из: (2) -On-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (3) -On-C3-7 циклоалкила, где циклоалкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (4) -On-арила, где арил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, и (7) -NH-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11;
где n независимо равен 0 или 1, когда n равен 0, химическая связь присутствует вместо -On-;
R2 независимо выбран из группы, состоящей из: (1) водорода, (2) галогена, (3) гидроксила, (4) -On-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R7, (5) -On-C3-6 циклоалкила, где циклоалкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R7, (6) -On-C2-4 алкенила, где алкенил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R7, (7) -On-фенила или -On-нафтила, где фенил или нафтил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R7, (8) -On-гетероциклила, где гетероциклил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R7, (9) -(C=O)-NR8R9, (10) -NR8R9, (11) -S(O)2-NR8R9, (12) -NR8-S(O)2R9, (13) -S(O)t-R9, где t равен 0, 1 или 2, (14) -NR8(C=O)R9, (15) -CN и (16) -NO2;
где n независимо равен 0 или 1, когда n равен 0, химическая связь присутствует вместо -On-; предпочтительно, R2 независимо выбран из группы, состоящей из: (1) водорода, (2) галогена, (3) гидроксила и (4) -On-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R7; более предпочтительно R2 независимо выбран из группы, состоящей из: (1) водорода, (2) галогена, (3) метила и (4) метокси;
p равен 1, 2, 3 или 4; когда p равен двум или более чем двум, R2 могут быть одинаковыми или различными; предпочтительно р равно 1;
R3 и R4 независимо представляют собой водород или C1-6 алкил, который является незамещенным или замещенным одним или более заместителями, независимо выбранными из галогена, гидроксила и -O-C1-6 алкила; или R3 образует 3-7-членное кольцо с R4, которое может содержать атом азота, атом кислорода, атом серы или двойную связь, где 3-7-членное кольцо необязательно замещено 1-6 заместителями, независимо выбранными из группы, состоящей из: (1) водорода, (2) гидроксила, (3) галогена, (4) C1-6 алкила, который является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (5) C3-6 циклоалкила, который является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (6) -O-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, и (7) -O-C3-6 циклоалкила, где циклоалкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11;
предпочтительно, R3 представляет собой водород; предпочтительно R4 обозначает водород или C1-6 алкил; более предпочтительно R4 обозначает водород или метил;
R5 независимо выбран из группы, состоящей из: (1) водорода, (2) галогена, (3) -On-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R7, (4) -On-C3-6 циклоалкила, где циклоалкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R7, и (5) -On-C2-4 алкенила, где алкенил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R7;
где n независимо равен 0 или 1, когда n равен 0, химическая связь присутствует вместо -On-;
предпочтительно, R5 представляет собой водород или C1-6 алкил; более предпочтительно R5 обозначает водород или метил;
R5 может быть в любом положении в пиразолопиридиновом кольце;
q равен 1, 2 или 3; когда q равен двум или более чем двум, R5 могут быть одинаковыми или различными; предпочтительно q равно 1;
R6 независимо представляет собой водород, C1-6 алкил, C1-6 алкокси, C2-6 алкенил, C3-7 циклоалкил, гетероциклил, арил, арил-C1-6 алкил или гетероциклил-C1-6 алкил, где C1-6 алкил, C1-6 алкокси, C2-6 алкенил, C3-7 циклоалкил, гетероциклил, арил, арил-C1-6 алкил или гетероциклил-C1-6 алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из галогена, гидроксила, C1-6 алкила, -O-C1-6 алкила, -C3-7 циклоалкила, -O-C3-7 циклоалкила, гидроксил-C1-6 алкокси, -CN, -NR8R9, -(C=O)-R8, -(C=O)-NR8R9, -NR8-(C=O)-R9, -NR8-(C=O)-NR9R10, -NR8-(C=O)-OR9, -NR8-S(O)2-R9, -NR8-S(O)2- NR9R10 и -S(O)2-R8; предпочтительно R6 независимо представляет собой водород, C1-6 алкил, C3-7 циклоалкил, гетероциклил или арил, где C1-6 алкил, C3-7 циклоалкил, гетероциклил, арил или незамещенный или замещенный одним или несколькими заместителями, независимо выбран из галогена, гидроксила, C1-6 алкила, -O- C1-6 алкила, -CN, -NR8R9 и -NR8-(C=O)-R9; более предпочтительно R6 также выбран из группы, состоящей из метила, этила, пропила, и циклопропил, который не замещен или замещен одним или несколькими заместителями, независимо выбранными из галогена, гидроксила, C1-6 алкила, -O-C1-6 алкила, -CN, -NR8R9 и-NR8-(C=O)-R9;
R7 выбрано из группы, состоящей из: (1) водорода, (2) галогена, (3) гидроксила, (4) -(C=O)m-Ol-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (5) -Ol-(C1-3)перфторалкила, (6) -(C=O)m-Ol-C3-6 циклоалкила, где циклоалкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (7) -(C=O)m-Ol-C2-4 алкенила, где алкенил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (8) -(C=O)m-Ol-фенила или -(C=O)m-Ol-нафтила, где фенил или нафтил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (9) -(C=O)m-Ol-гетероциклила, где гетероциклил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (10) -(C=O)-NR8R9, (11) -NR8R9, (12) -S(O)2-NR8R9, (13) -S(O)t-R8, где t равен 0, 1 или 2, (14) -CO2H, (15) -CN и (16) -NO2;
где l равен 0 или 1 и m равен 0 или 1; когда l равен 0, или m равен 0, химическая связь присутствует вместо -Ol- или -(C=O)m-, и когда l равен 0, и m равен 0, химическая связь присутствует вместо -(C=O)m-Ol-;
предпочтительно, R7 обозначает водород;
R8, R9 и R10 независимо представляют собой водород, C1-6 алкил, C2-6 алкенил, C3-7 циклоалкил или арил, который является незамещенным или замещенным одним или более заместителями, независимо выбранными из галогена, гидроксила, C1-6 алкила, -O-C1-6 алкила, C3-7 циклоалкила и -O-C3-7 циклоалкила; или R8 образует 4-7-членное кольцо с R9, которое может содержать атом азота, атом кислорода, атом серы или двойную связь, где 4-7-членное кольцо необязательно замещено 1-6 заместителями, независимо выбранными из группы, состоящей из: (1) водорода, (2) гидроксила, (3) галогена, (4) C1-6 алкила, который является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (5) C3-6 циклоалкила, который является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (6) -O-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, и (7) -O-C3-6 циклоалкила, где циклоалкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11;
предпочтительно, R8, R9 и R10 независимо представляют собой водород, C1-6 алкил или C3-7 циклоалкил;
R11 независимо выбран из группы, состоящей из: (1) водорода, (2) гидроксила, (3) галогена, (4) -C1-6 алкила, который является незамещенным или замещенным одним или более галогенами, (5) -C3-6 циклоалкила, (6) -O-C1-6 алкила, где алкил является незамещенным или замещенным одним или более галогенами, (7) -O(C=O)-C1-6 алкила, (8) -NH-C1-6 алкила, (9) фенила, (10) гетероциклила, (11) -CN и (12) -Si(C1-6 алкил)3;
предпочтительно R11 обозначает галоген или -C3-6 циклоалкил;
или его пролекарство или его фармацевтически приемлемая соль.
[6] Более предпочтительны соединения, описанные в [5], где:
R2 независимо выбран из группы, состоящей из:
(1) водорода, (2) галогена, (3) метила и (4) метокси;
p равен 1;
R3 представляет собой водород;
R4 представляет собой водород или метил;
R6 выбран из группы, состоящей из метила, этила, изопропила, пропила или бутила, который является незамещенным или замещенным одним или более заместителями, независимо выбранными из гидроксила, C1-6 алкила, C3-7 циклоалкила, -O-C1-6 алкила, -CN и -NR8-(C=O)-R9, в котором каждый из R8 и R9 имеет значение, как в указано выше;
или его пролекарство или его фармацевтически приемлемая соль.
[7] Подходящие отдельные соединения по изобретению представляют собой:
N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
2-гидрокси-2-метил-N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразол[4,3-c]пиридин-4-ил)пропанамида;
N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)ацетамида;
N-(2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)ацетамида;
N-(2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропионамида;
N-(2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанкарбоксамида;
N-(2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-гидрокси-2-метилпропанамида;
N-(2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)ацетамида;
N-(2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропионамида;
N-(2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)тетрагидро-2H-пиран-4-карбоксамида;
N-(2-((6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-хлор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-хлор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропионамида;
N-(2-((5-хлор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)тетрагидро-2H-пиран-4-карбоксамида;
N-(2-((5-хлор-6-(2,2-дифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)ацетамида;
N-(2-((5-хлор-6-(2,2-дифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропионамида;
N-(2-((5-хлор-6-(2,2-дифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-хлор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)ацетамида;
N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)тетрагидро-2H-пиран-4-карбоксамида;
N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)оксазол-5-карбоксамида;
1,1-диметил-3-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)мочевины;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-амина;
3-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)оксазолидин-2-она;
этил (2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)карбамата;
N-(2-((6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)ацетамида;
N-(2-((6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропионамида;
4-метокси-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридина;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((6-(2,2-дифторэтокси)-5-фторпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((6-(2,2-дифторэтокси)-5-фторпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((6-(2,2,2-трифторэтокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((6-(2,2,2-трифторэтокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)ацетамида;
N-(2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропионамида;
N-(2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)тетрагидро-2H-пиран-4-карбоксамида;
N-(2-((5-фтор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропионамида;
N-(2-((5-фтор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((5-фтор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пиваламида;
N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)никотинамида;
1-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пирролидин-2-она;
1-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)имидазолидин-2-она;
4-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)морфолина;
N-(1-метил-1H-пиразол-3-ил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-амина;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(пиримидин-2-ил)-2H-пиразоло[4,3-c]пиридин-4-амина;
N-(2-((6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)тетрагидро-2H-пиран-4-карбоксамида;
3-(2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-1,1-диметилмочевины;
N-(2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пиваламида;
N-(2-(4-(2,2,2-трифторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-(4-(2,2,2-трифторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-4-(1H-пиразол-5-ил)-2H-пиразоло[4,3-c]пиридина;
N-(2-((6-(2,2,3,3,3-пентафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((6-(2,2,3,3,3-пентафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-(4-(трифторметокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(тетрагидрофуран-3-ил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-циклопропил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-циклобутил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(циклопропилметил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-((тетрагидро-2H-пиран-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-метоксиэтил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-N-(1-гидроксипропан-2-ил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-метил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропионамида;
N-(3-метил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-(1-(6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-(2-(6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((6-(4-фторфенокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((6-(4-фторфенокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-метил-N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
(S)-N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)тетрагидрофуран-2-карбоксамида;
(S)-N-(2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)тетрагидрофуран-2-карбоксамида;
N-(2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)никотинамида;
(R)-2-гидрокси-N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-с]пиридин-4-ил)пропанамида;
(S)-2-гидрокси-N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пирролидин-1-карбоксамида;
1-ацетил-N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пиперидин-4-карбоксамида;
N-изопропил-2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-пропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изобутил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-этоксиэтил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(цианометил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-((тетрагидрофуран-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(диметиламино)этил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(пиридин-3-илметил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-((5-метил-1,2,4-оксадиазол-3-ил)метил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(пиридин-3-ил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)тетрагидрофуран-2-карбоксамида;
(R)-N-(2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)тетрагидрофуран-2-карбоксамида;
N-(3-метоксипропил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-((1-гидроксициклогексил)метил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(6-метил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропионамида;
N-(6-метил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(6-метил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
2-гидрокси-2-метил-N-(6-метил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
N-(7-метил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропионамида;
N-(7-метил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
1-изобутирил-N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пиперидин-4-карбоксамида;
N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)1-(метилсульфонил)пиперидин-4-карбоксамида;
(S)-1-ацетил-N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пирролидин-2-карбоксамида;
(R)-1-ацетил-N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пирролидин-2-карбоксамида;
N-метил-N-(2-((2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)амино)-2-оксоэтил)ацетамида;
(S)-2-метокси-N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
(S)-N-(2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-метоксипропанамида;
(R)-N-(2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-гидроксипропанамида;
(S)-N-(2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-гидроксипропанамида;
2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-циклопропил-2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(циклопропилметил)-2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-N-(2-(диметиламино)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(2-морфолиноэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-(пиридин-2-ил)ацетамида;
N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-(пиридин-3-ил)ацетамида;
N-изопропил-2-((6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-циклопропил-2-((6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(циклопропилметил)-2-((6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-(пиридин-4-ил)ацетамида;
N-(цианометил)-2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-N-пропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-цианопропан-2-ил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидрокси-2-метилпропил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-(диметиламино)пропил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-аминоэтил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(оксетан-3-ил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-((4-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((4-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-(пиридин-4-ил)ацетамида;
2-(пиридин-4-ил)-N-(2-((6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)ацетамида;
N-(2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-(пиридин-3-ил)ацетамида;
2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((4-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
2-гидрокси-2-метил-N-(2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
N-метил-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-метил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)2-(2-метилтиазол-4-ил)ацетамида;
N-(2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-(пиридин-3-ил)ацетамида;
N-(2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-(пиридин-4-ил)ацетамида;
2-(3,5-диметилизоксазол-4-ил)-N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)ацетамида;
N-изопропил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-N-(2-гидроксипропил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(2-гидроксипропил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(2,3-дигидроксипропил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
2-гидрокси-2-метил-N-(2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
N-метил-2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(1-гидроксипропан-2-ил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-амино-2-оксоэтил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(2-(метилсульфонамидо)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-цианоэтил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-цианоэтил)-2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
2-((5-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((5-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((5-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((5-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(2-гидроксиэтокси)этил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-этил-2-((5-фтор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-фтор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2-дифторэтокси)пиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2-дифторэтокси)пиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2-дифторэтокси)пиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2-дифторэтокси)пиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-N-(2,3-дигидроксипропил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-(4-(2,2,2-трифторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(4-фторфенокси)-5-метилпиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((6-(2,2,3,3,3-пентафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-((6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(1-амино-1-оксопропан-2-ил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(2-(метиламино)-2-оксоэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-амино-3-оксопропил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидрокси-2,2-диметилпропил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(4-гидроксибутил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-(3-метил-4-(2,2,2-трифторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-ацетамидопропил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(3-(метилсульфонамидо)пропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторэтокси)-3-метилбензил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторэтокси)-3-метилбензил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2-дифторэтокси)пиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-(4-(2,2,2-трифторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((2-метил-6-(2,2,2-трифторэтокси)пиридин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((2-метил-6-(2,2,2-трифторэтокси)пиридин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(3-гидроксипропил)-2-(3-метил-4-(2,2,2-трифторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((5-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-фтор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(4-фторфенокси)-5-метилпиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((6-(2,2,3,3,3-пентафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-((2-метил-6-(2,2,2-трифторэтокси)пиридин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((2-метил-6-(2,2,2-трифторэтокси)пиридин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((2-метил-6-(2,2,2-трифторэтокси)пиридин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((2-метил-6-(2,2,2-трифторэтокси)пиридин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((2-метил-6-(2,2,2-трифторэтокси)пиридин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((6-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((6-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
(S)-N-(2-гидроксипропил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-N-(2-гидроксипропил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(2,3-дигидроксипропил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-N-(2,3-дигидроксипропил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(2,3-дигидроксипропил)-2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((1-(5-(трифторметил)пиридин-2-ил)-1H-пиразол-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((1-(5-(трифторметил)пиридин-2-ил)-1H-пиразол-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((1-(5-(трифторметил)пиридин-2-ил)-1H-пиразол-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-((1-(5-(трифторметил)пиридин-2-ил)-1H-пиразол-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((1-(5-(трифторметил)пиридин-2-ил)-1H-пиразол-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(2-гидроксипропил)-2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-N-(2-гидроксипропил)-2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(1-гидроксипропан-2-ил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(1-гидроксипропан-2-ил)-2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-цианоэтил)-2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-цианоэтил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-амино-2-оксоэтил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-метоксиэтил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-метил-6-(2-(2,2,2-трифторэтокси)этокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-метил-6-(2-(2,2,2-трифторэтокси)этокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
2-гидрокси-2-метил-N-(2-((5-метил-6-(2-(2,2,2-трифторэтокси)этокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
N-(2-((2-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((2-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-гидроксиэтил)-2-((5-метил-6-(2-(2,2,2-трифторэтокси)этокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((5-метил-6-(2-(2,2,2-трифторэтокси)этокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-((5-метил-6-(2-(2,2,2-трифторэтокси)этокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((5-метил-6-(2-(2,2,2-трифторэтокси)этокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((2-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((2-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((2-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((2-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((5-метил-6-(2-(2,2,2-трифторэтокси)этокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((2-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-(2-(4-(трифторметил)фенокси)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-(2-(4-(трифторметил)фенокси)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-(2-(4-(трифторметил)фенокси)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-(2-(4-(трифторметил)фенокси)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-(2-(4-(трифторметил)фенокси)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((6-метил-5-(2,2,2-трифторэтокси)пиразин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((6-метил-5-(2,2,2-трифторэтокси)пиразин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-гидрокси-2-метилпропанамида;
2-(2-((3-хлор-5-(трифторметил)пиридин-2-ил)окси)этил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(2-((3-хлор-5-(трифторметил)пиридин-2-ил)окси)этил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(2-((3-хлор-5-(трифторметил)пиридин-2-ил)окси)этил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(2-((3-хлор-5-(трифторметил)пиридин-2-ил)окси)этил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(2-((3-хлор-5-(трифторметил)пиридин-2-ил)окси)этил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-циклопропил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-циклопропил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-циклопропил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-циклопропил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-циклопропил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-((6-метил-5-(2,2,2-трифторэтокси)пиразин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((6-метил-5-(2,2,2-трифторэтокси)пиразин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((6-метил-5-(2,2,2-трифторэтокси)пиразин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((6-метил-5-(2,2,2-трифторэтокси)пиразин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(4-хлор-1H-пиразол-1-ил)-5-метилпиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(4-хлор-1H-пиразол-1-ил)-5-метилпиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-((5-метил-2-фенил-2H-1,2,3-триазол-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-метоксиэтил)-2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(4-хлор-1H-пиразол-1-ил)-5-метилпиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(4-хлор-1H-пиразол-1-ил)-5-метилпиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
2-гидрокси-2-метил-N-(2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
N-(2-((5-метил-2-фенил-2H-1,2,3-триазол-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((6-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((6-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((6-(циклопропилметокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((6-(циклопропилметокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((6-(циклопропилметокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)2-гидрокси-2-метилпропанамида;
N,6-диметил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-6-метил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((5-метил-6-((2,2,2-трифторэтил)амино)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((5-метил-6-((2,2,2-трифторэтил)амино)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((5-метил-6-((2,2,2-трифторэтил)амино)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((5-метил-6-((2,2,2-трифторэтил)амино)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(циклопропилметокси)-5-метилпиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-((6-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((6-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((6-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((6-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(циклопропилметокси)-5-метилпиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(циклопропилметокси)-5-метилпиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(циклопропилметокси)-5-метилпиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(циклопропилметокси)-5-метилпиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-(3-метил-4-(трифторметокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-(3-метил-4-(трифторметокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-(3-метил-4-(трифторметокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-(3-метил-4-(трифторметокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((2-(2,2,2-трифторэтокси)пиридин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-фенил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-метил-2-(3-метил-4-(трифторметокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(4-хлор-1H-пиразол-1-ил)-5-метилпиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((2-(2,2,2-трифторэтокси)пиридин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(4-фторфенокси)-5-метилпиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((6-(4-фторфенокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-6-метил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-6-метил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-N-(3-(метилсульфонил)пропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-((1-(2,2,2-трифторэтокси)изохинолин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((1-(2,2,2-трифторэтокси)изохинолин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((1-(2,2,2-трифторэтокси)изохинолин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((1-(2,2,2-трифторэтокси)изохинолин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((1-(2,2,2-трифторэтокси)изохинолин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-(4-((2,2,2-трифторэтокси)метил)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-(4-((2,2,2-трифторэтокси)метил)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-(4-((2,2,2-трифторэтокси)метил)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-4-гидрокси-1-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пирролидин-2-она;
2-((5-(2,2-дифторэтокси)-4-метилпиридин-2-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(2,2-дифторэтокси)-4-метилпиридин-2-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-((1-метил-5-(трифторметокси)-1H-индол-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((1-метил-5-(трифторметокси)-1H-индол-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((1-метил-5-(трифторметокси)-1H-индол-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((1-метил-5-(трифторметокси)-1H-индол-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(3-хлор-4-(2,2-дифторэтокси)бензил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(3-хлор-4-(2,2-дифторэтокси)бензил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-метил-6-((2,2,2-трифторэтокси)метил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(3-(метилсульфонил)пропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((5-метил-6-((2,2,2-трифторэтокси)метил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((5-метил-6-((2,2,2-трифторэтокси)метил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((5-метил-6-((2,2,2-трифторэтокси)метил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((5-метил-6-((2,2,2-трифторэтокси)метил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((1-метил-5-(трифторметокси)-1H-индол-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-метил-6-((2,2,2-трифторэтокси)метил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((5-(2,2-дифторэтокси)-4-метилпиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-(2,2-дифторэтокси)-4-метилпиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((5-(2,2-дифторэтокси)-4-метилпиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-гидрокси-2-метилпропанамида;
N-(2-(3-(трифторметокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-(3-(трифторметокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
2-гидрокси-2-метил-N-(2-(3-(трифторметокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
N-(2-(2-((3-фтор-5-(трифторметил)пиридин-2-ил)окси)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-(2-((3-фтор-5-(трифторметил)пиридин-2-ил)окси)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-метил-2-(3-(трифторметокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-(3-(трифторметокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-(3-(трифторметокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-(3-(трифторметокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-(2-((3-фтор-5-(трифторметил)пиридин-2-ил)окси)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(2-((3-фтор-5-(трифторметил)пиридин-2-ил)окси)этил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(2-((3-фтор-5-(трифторметил)пиридин-2-ил)окси)этил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-(2,2,3,3,3-пентафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-(2,2,3,3,3-пентафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-гидроксиэтил)-2-(4-(1,1,2,2-тетрафторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-(4-(1,1,2,2-тетрафторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((5-(2,2,3,3,3-пентафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((5-(2,2,3,3,3-пентафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((5-(2,2,3,3,3-пентафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(2,2-дифторэтокси)-4-метилпиридин-2-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(2,2-дифторэтокси)-4-метилпиридин-2-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(2,2-дифторэтокси)-4-метилпиридин-2-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((5-(2,2,3,3-тетрафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((5-(2,2,3,3-тетрафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((5-(2,2,3,3-тетрафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-гидрокси-2-метилпропанамида;
N-(2-((5-(2,2,3,3-тетрафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-ацетамидоэтил)-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(2-гидроксипропил)-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(2,3-дигидроксипропил)-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(3-(трифторметил)бензил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-(3-(трифторметил)бензил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-метил-2-(3-(трифторметил)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-(3-(трифторметил)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-(3-(трифторметил)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-(3-(трифторметил)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамид;
(R)-N-(2-гидроксипропил)-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-N-(2,3-дигидроксипропил)-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(3-хлор-4-(2,2-дифторэтокси)бензил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-(4-(1,1,2,2-тетрафторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(3-хлор-4-(2,2-дифторэтокси)бензил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-(4-(1,1,2,2-тетрафторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-((S)-2-гидроксипропил)-2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-((5-метил-6-(3,3,3-трифторпропил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((5-метил-6-(3,3,3-трифторпропил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((5-метил-6-(3,3,3-трифторпропил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((5-метил-6-(3,3,3-трифторпропил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((5-метил-6-(3,3,3-трифторпропил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-((4-метил-5-(3,3,3-трифторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((4-метил-5-(3,3,3-трифторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((4-метил-5-(3,3,3-трифторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((4-метил-5-(3,3,3-трифторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-N-(2,3-дигидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-N-(2,3-дигидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-N-(1-гидроксипропан-2-ил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
2-гидрокси-2-метил-N-(2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
N-метил-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((4-метил-5-(3,3,3-трифторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((4-метил-5-(3,3,3-трифторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((5-метил-6-(3,3,3-трифторпропил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((5-метил-6-(3,3,3-трифторпропил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
2-((5-хлор-6-(2,2-дифторпропокси)пиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2-дифторпропокси)пиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2-дифторпропокси)пиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2-дифторпропокси)пиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2-дифторпропокси)пиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(1-гидроксипропан-2-ил)-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-хлор-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-хлор-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((5-хлор-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)2-гидрокси-2-метилпропанамида;
N-(2-((1-метил-5-(трифторметил)-1H-бензо[d]имидазол-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((1-метил-5-(трифторметил)-1H-бензо[d]имидазол-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
2-((5-хлор-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(3-хлор-4-(2,2-дифторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-(3-хлор-4-(2,2-дифторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-метил-2-((1-метил-5-(трифторметил)-1H-бензо[d]имидазол-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((1-метил-5-(трифторметил)-1H-бензо[d]имидазол-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((1-метил-5-(трифторметил)-1H-бензо[d]имидазол-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((1-метил-5-(трифторметил)-1H-бензо[d]имидазол-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((1-метил-5-(трифторметил)-1H-бензо[d]имидазол-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(4-(2,2-дифторэтокси)-3-метилбензил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-(4-(2,2-дифторэтокси)-3-метилбензил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-(4-(2,2-дифторэтокси)-3-метилбензил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-гидрокси-2-метилпропанамида;
2-гидрокси-2-метил-N-(2-(3-метил-4-(2,2,2-трифторэтокси)бензил)-2H-пиразоло[4,3-c]пиримидин-4-ил)пропанамида;
2-гидрокси-2-метил-N-(2-(3-метил-4-(трифторметокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
2-гидрокси-2-метил-N-(2-(2-(4-(трифторметил)фенокси)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
N-(2-((6-(4-хлор-1H-пиразол-1-ил)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-гидрокси-2-метилпропанамида;
2-(4-(2,2-дифторэтокси)-3-метилбензил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторэтокси)-3-метилбензил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-хлор-6-(2,2-дифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((5-хлор-6-(2,2-дифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(2-пропионамидоэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-изобутирамидоэтил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(циклопропанкарбоксамидо)этил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
этил (2-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамидо)этил)карбамата;
N-(2-бензамидоэтил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(2-гидрокси-2-метилпропанамидо)этил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(2-(N-метилацетамидо)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-бутирамидоэтил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(циклобутанкарбоксамидо)этил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(циклогексанкарбоксамидо)этил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(3-этилуреидо)этил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((5-хлор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((6-(циклопропилметокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-(3-метил-4-(трифторметокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-(3-метил-4-(2,2,2-трифторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-(4-(2,2-дифторэтокси)-3-метилбензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((5-хлор-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((1-метил-5-(трифторметокси)-1H-индол-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-гидрокси-2-метил-N-(2-((4-метил-5-(3,3,3-трифторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(2-(пиколинамидо)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(2-(никотинамидо)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(изоникотинамидо)этил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(1-гидроксициклогексанкарбоксамидо)этил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-(3-хлор-4-(2,2,2-трифторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((4-метил-5-(2,2,3,3-тетрафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
2-гидрокси-2-метил-N-(2-((4-метил-5-(2,2,3,3-тетрафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
N-(2-((5-хлор-6-(циклопропилметокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-хлор-6-(циклопропилметокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((5-хлор-6-(циклопропилметокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-гидрокси-2-метилпропанамида;
N-метил-2-((4-метил-5-(2,2,3,3-тетрафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((4-метил-5-(2,2,3,3-тетрафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((4-метил-5-(2,2,3,3-тетрафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((4-метил-5-(2,2,3,3-тетрафторпропокси)пиридин-2-ил)метил)-2H-пирaзоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((4-метил-5-(2,2,3,3-тетрафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((4-метил-5-(2,2,3,3-тетрафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((2-метил-6-(2,2,2-трифторэтокси)пиридин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-(2-(4-(трифторметил)фенокси)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((6-(4-хлор-1H-пиразол-1-ил)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((1-(2,2,2-трифторэтокси)изохинолин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-(4-(1,1,2,2-тетрафторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((2-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((6-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
2-((5-хлор-6-(циклопропилметокси)пиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(циклопропилметокси)пиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((5-хлор-6-(циклопропилметокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(циклопропилметокси)пиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(циклопропилметокси)пиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(циклопропилметокси)пиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((6-((4-фторбензил)окси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((6-((4-фторбензил)окси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((6-((4-фторбензил)окси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-гидрокси-2-метилпропанамида;
2-((6-((4-фторбензил)окси)-5-метилпиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((6-((4-фторбензил)окси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((6-((4-фторбензил)окси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-((4-фторбензил)окси)-5-метилпиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-((4-фторбензил)окси)-5-метилпиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-((4-фторбензил)окси)-5-метилпиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((6-циклобутокси-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((6-циклобутокси-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((6-циклобутокси-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-гидрокси-2-метилпропанамида;
N-(2-((4-метил-5-(2,2,3,3-тетрафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
2-((6-циклобутокси-5-метилпиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-циклобутокси-5-метилпиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((6-циклобутокси-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-циклобутокси-5-метилпиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-циклобутокси-5-метилпиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-циклобутокси-5-метилпиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-(циклопропилметокси)-4-метилпиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-(циклопропилметокси)-4-метилпиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((5-(циклопропилметокси)-4-метилпиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-гидрокси-2-метилпропанамида;
2-((5-(циклопропилметокси)-4-метилпиридин-2-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(циклопропилметокси)-4-метилпиридин-2-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((5-(циклопропилметокси)-4-метилпиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(циклопропилметокси)-4-метилпиридин-2-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(циклопропилметокси)-4-метилпиридин-2-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(циклопропилметокси)-4-метилпиридин-2-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-(2,2-дифторпропокси)-4-метилпиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-(2,2-дифторпропокси)-4-метилпиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
2-((5-(2,2-дифторпропокси)-4-метилпиридин-2-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(2,2-дифторпропокси)-4-метилпиридин-2-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((5-(2,2-дифторпропокси)-4-метилпиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(2,2-дифторпропокси)-4-метилпиридин-2-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(2,2-дифторпропокси)-4-метилпиридин-2-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(2,2-дифторпропокси)-4-метилпиридин-2-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-(2,2-дифторпропокси)-4-метилпиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-гидрокси-2-метилпропанамида;
(R)-2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-N-(1-гидроксипропан-2-ил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-N-(2,3-дигидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-N-(2,3-дигидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-цианоэтил)-2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(4-(2,2-дифторпропокси)-3-метилбензил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-(4-(2,2-дифторпропокси)-3-метилбензил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-(4-(2,2-дифторпропокси)-3-метилбензил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-гидрокси-2-метилпропанамида;
2-(4-(2,2-дифторпропокси)-3-метилбензил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторпропокси)-3-метилбензил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-(4-(2,2-дифторпропокси)-3-метилбензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторпропокси)-3-метилбензил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторпропокси)-3-метилбензил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторпропокси)-3-метилбензил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)оксазол-5-карбоксамида;
2-гидрокси-2-метил-N-(2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
(S)-2-(4-(2,2-дифторэтокси)-3-метилбензил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-2-(4-(2,2-дифторэтокси)-3-метилбензил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(1-(4-(2,2-дифторэтокси)-3-метилфенил)этил)-N-((R)-2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-2-(4-(2,2-дифторэтокси)-3,5-диметилбензил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-2-(3-(2,2-дифторэтокси)-4-метилбензил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(1-(4-(2,2-дифторпропокси)-3-метилфенил)этил)-N-((R)-2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(1-(4-(2,2-дифторэтокси)-3-метилфенил)этил)-N-((R)-2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-2-(4-(2,2-дифторпропокси)-3-метилбензил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-2-(4-(2,2-дифторпропокси)-3-метилбензил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(1-(4-(2,2-дифторэтокси)-3-метилфенил)этил)-N-((S)-2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-2-(4-(2,2-дифторэтокси)-3,5-диметилбензил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-2-(3-(2,2-дифторэтокси)-4-метилбензил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(1-(4-(2,2-дифторпропокси)-3-метилфенил)этил)-N-((S)-2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(1-(4-(2,2-дифторэтокси)-3-метилфенил)этил)-N-((S)-2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-2-(1-(4-(2,2-дифторэтокси)-3-метилфенил)этил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторэтокси)-3,5-диметилбензил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(3-(2,2-дифторэтокси)-4-метилбензил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(1-(4-(2,2-дифторпропокси)-3-метилфенил)этил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(1-(4-(2,2-дифторэтокси)-3-метилфенил)этил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(1-(4-(2,2-дифторэтокси)-3-метилфенил)этил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторэтокси)-3,5-диметилбензил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(3-(2,2-дифторэтокси)-4-метилбензил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(1-(4-(2,2-дифторпропокси)-3-метилфенил)этил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(1-(4-(2,2-дифторэтокси)-3-метилфенил)этил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторпропокси)-3-метилбензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(дифторметокси)-3-метилбензил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(дифторметокси)-3-метилбензил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-(4-(дифторметокси)-3-метилбензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(дифторметокси)-3-метилбензил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(дифторметокси)-3-метилбензил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-2-(4-(дифторметокси)-3-метилбензил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-2-(4-(дифторметокси)-3-метилбензил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
и
2-(4-(дифторметокси)-3-метилбензил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
или его пролекарство или его фармацевтически приемлемая соль.
[8] Более подходящие отдельные соединения по изобретению представляют собой:
N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
2-гидрокси-2-метил-N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
N-(2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-хлор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)ацетамида;
N-метил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)ацетамида;
N-(2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)тетрагидро-2H-пиран-4-карбоксамида;
N-(2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пиваламида;
N-этил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-метоксиэтил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-пропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(диметиламино)этил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-гидрокси-2-метил-N-(6-метил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
2-гидрокси-2-метил-N-(2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
N-изопропил-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-метил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-N-(2-гидроксипропил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(2-гидроксипропил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(2,3-дигидроксипропил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-метил-2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-цианоэтил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-цианоэтил)-2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-этил-2-((5-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(2-гидроксиэтокси)этил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
2-((5-хлор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2-дифторэтокси)пиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2-дифторэтокси)пиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-N-(2,3-дигидроксипропил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((6-(2,2,3,3,3-пентафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(4-гидроксибутил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-(3-метил-4-(2,2,2-трифторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-ацетамидопропил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(3-(метилсульфонамидо)пропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторэтокси)-3-метилбензил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторэтокси)-3-метилбензил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((2-метил-6-(2,2,2-трифторэтокси)пиридин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(3-гидроксипропил)-2-(3-метил-4-(2,2,2-трифторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-((2-метил-6-(2,2,2-трифторэтокси)пиридин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((2-метил-6-(2,2,2-трифторэтокси)пиридин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((2-метил-6-(2,2,2-трифторэтокси)пиридин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((2-метил-6-(2,2,2-трифторэтокси)пиридин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((2-метил-6-(2,2,2-трифторэтокси)пиридин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(2-гидроксипропил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-N-(2-гидроксипропил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(2,3-дигидроксипропил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-N-(2,3-дигидроксипропил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((1-(5-(трифторметил)пиридин-2-ил)-1H-пиразол-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((1-(5-(трифторметил)пиридин-2-ил)-1H-пиразол-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(2-гидроксипропил)-2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(1-гидроксипропан-2-ил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-цианоэтил)-2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-цианоэтил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((5-метил-6-(2-(2,2,2-трифторэтокси)этокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((2-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((2-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((2-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((2-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-(2-(4-(трифторметил)фенокси)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-(2-(4-(трифторметил)фенокси)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((6-метил-5-(2,2,2-трифторэтокси)пиразин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-гидрокси-2-метилпропанамида;
2-(2-((3-хлор-5-(трифторметил)пиридин-2-ил)окси)этил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-с]пиридин-4-карбоксамида;
2-((5-циклопропил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-циклопропил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-циклопропил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((6-метил-5-(2,2,2-трифторэтокси)пиразин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((6-метил-5-(2,2,2-трифторэтокси)пиразин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(4-хлор-1H-пиразол-1-ил)-5-метилпиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(4-хлор-1H-пиразол-1-ил)-5-метилпиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(4-хлор-1H-пиразол-1-ил)-5-метилпиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(4-хлор-1H-пиразол-1-ил)-5-метилпиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((6-(циклопропилметокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-гидрокси-2-метилпропанамида;
N,6-диметил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-6-метил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((5-метил-6-((2,2,2-трифторэтил)амино)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((5-метил-6-((2,2,2-трифторэтил)амино)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(циклопропилметокси)-5-метилпиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(циклопропилметокси)-5-метилпиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(циклопропилметокси)-5-метилпиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(циклопропилметокси)-5-метилпиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(циклопропилметокси)-5-метилпиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-(3-метил-4-(трифторметокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-(3-метил-4-(трифторметокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(4-хлор-1H-пиразол-1-ил)-5-метилпиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((6-(4-фторфенокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-6-метил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-6-метил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-N-(3-(метилсульфонил)пропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-((1-(2,2,2-трифторэтокси)изохинолин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((1-(2,2,2-трифторэтокси)изохинолин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((1-(2,2,2-трифторэтокси)изохинолин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((1-(2,2,2-трифторэтокси)изохинолин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(3-хлор-4-(2,2-дифторэтокси)бензил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-метил-6-((2,2,2-трифторэтокси)метил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(3-(метилсульфонил)пропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((1-метил-5-(трифторметокси)-1H-индол-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-(2,2-дифторэтокси)-4-метилпиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-(2,2-дифторэтокси)-4-метилпиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-гидроксиэтил)-2-(3-(трифторметокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-(2,2,3,3,3-пентафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-этил-2-((5-(2,2,3,3,3-пентафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(2,2-дифторэтокси)-4-метилпиридин-2-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(2,2-дифторэтокси)-4-метилпиридин-2-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(2,2-дифторэтокси)-4-метилпиридин-2-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((5-(2,2,3,3-тетрафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-гидрокси-2-метилпропанамида;
N-(2-((5-(2,2,3,3-тетрафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-ацетамидоэтил)-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(2-гидроксипропил)-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(2,3-дигидроксипропил)-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-(3-(трифторметил)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-N-(2-гидроксипропил)-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-N-(2,3-дигидроксипропил)-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(3-хлор-4-(2,2-дифторэтокси)бензил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(3-хлор-4-(2,2-дифторэтокси)бензил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-(4-(1,1,2,2-тетрафторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-((S)-2-гидроксипропил)-2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-((5-метил-6-(3,3,3-трифторпропил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((5-метил-6-(3,3,3-трифторпропил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((5-метил-6-(3,3,3-трифторпропил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((5-метил-6-(3,3,3-трифторпропил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((5-метил-6-(3,3,3-трифторпропил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-((4-метил-5-(3,3,3-трифторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((4-метил-5-(3,3,3-трифторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((4-метил-5-(3,3,3-трифторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((4-метил-5-(3,3,3-трифторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-N-(1-гидроксипропан-2-ил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
2-гидрокси-2-метил-N-(2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
N-метил-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((4-метил-5-(3,3,3-трифторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((5-метил-6-(3,3,3-трифторпропил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
2-((5-хлор-6-(2,2-дифторпропокси)пиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2-дифторпропокси)пиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2-дифторпропокси)пиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2-дифторпропокси)пиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-с]пиридин-4-карбоксамида;
(S)-N-(1-гидроксипропан-2-ил)-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((1-метил-5-(трифторметил)-1H-бензо[d]имидазол-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((1-метил-5-(трифторметил)-1H-бензо[d]имидазол-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-гидрокси-2-метил-N-(2-(3-метил-4-(2,2,2-трифторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
2-гидрокси-2-метил-N-(2-(3-метил-4-(трифторметокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
2-(4-(2,2-дифторэтокси)-3-метилбензил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторэтокси)-3-метилбензил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((6-(циклопропилметокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-(3-метил-4-(2,2,2-трифторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-(4-(2,2-дифторэтокси)-3-метилбензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-гидрокси-2-метил-N-(2-((4-метил-5-(3,3,3-трифторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
N-этил-2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
2-((5-хлор-6-(циклопропилметокси)пиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(циклопропилметокси)пиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(циклопропилметокси)пиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(циклопропилметокси)пиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(циклопропилметокси)пиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-((4-фторбензил)окси)-5-метилпиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((6-циклобутокси-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-гидрокси-2-метилпропанамида;
2-((6-циклобутокси-5-метилпиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((6-циклобутокси-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-циклобутокси-5-метилпиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-циклобутокси-5-метилпиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-циклобутокси-5-метилпиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-(циклопропилметокси)-4-метилпиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-гидрокси-2-метилпропанамида;
2-((5-(циклопропилметокси)-4-метилпиридин-2-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(циклопропилметокси)-4-метилпиридин-2-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(циклопропилметокси)-4-метилпиридин-2-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(циклопропилметокси)-4-метилпиридин-2-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-(2,2-дифторпропокси)-4-метилпиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
2-((5-(2,2-дифторпропокси)-4-метилпиридин-2-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(2,2-дифторпропокси)-4-метилпиридин-2-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(2,2-дифторпропокси)-4-метилпиридин-2-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(2,2-дифторпропокси)-4-метилпиридин-2-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(2,2-дифторпропокси)-4-метилпиридин-2-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-цианоэтил)-2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторпропокси)-3-метилбензил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторпропокси)-3-метилбензил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторпропокси)-3-метилбензил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторпропокси)-3-метилбензил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторпропокси)-3-метилбензил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-2-(4-(2,2-дифторэтокси)-3-метилбензил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(1-(4-(2,2-дифторэтокси)-3-метилфенил)этил)-N-((R)-2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-2-(4-(2,2-дифторэтокси)-3,5-диметилбензил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(1-(4-(2,2-дифторпропокси)-3-метилфенил)этил)-N-((R)-2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-2-(4-(2,2-дифторпропокси)-3-метилбензил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-2-(4-(2,2-дифторпропокси)-3-метилбензил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(1-(4-(2,2-дифторэтокси)-3-метилфенил)этил)-N-((S)-2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-2-(4-(2,2-дифторэтокси)-3,5-диметилбензил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(1-(4-(2,2-дифторпропокси)-3-метилфенил)этил)-N-((S)-2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-2-(1-(4-(2,2-дифторэтокси)-3-метилфенил)этил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторэтокси)-3,5-диметилбензил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(1-(4-(2,2-дифторпропокси)-3-метилфенил)этил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(1-(4-(2,2-дифторэтокси)-3-метилфенил)этил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторэтокси)-3,5-диметилбензил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(1-(4-(2,2-дифторпропокси)-3-метилфенил)этил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторпропокси)-3-метилбензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(дифторметокси)-3-метилбензил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
и
2-(4-(дифторметокси)-3-метилбензил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
или его пролекарство или его фармацевтически приемлемая соль.
[9] Настоящее изобретение предусматривает фармацевтическую композицию, которая содержит соединение или его пролекарство или его фармацевтически приемлемую соль, как описано в любом из [1]-[8], и фармацевтически приемлемый носитель.
[10] Настоящее изобретение предусматривает фармацевтическую композицию, как описано в [9], которая содержит другое фармакологически активное средство.
[11] Настоящее изобретение предусматривает способ лечения состояния или нарушения, в котором используют блокаторы TTX-S каналов, у животного, включая человека, который включает введение животному, нуждающемуся в таком лечении, терапевтически эффективного количества соединения или его пролекарства или его фармацевтически приемлемой соли, как описано в любом из [1]-[8].
[12] Настоящее изобретение предусматривает способ, как описано в [11], где указанное состояние или нарушение выбирают из группы, состоящей из: боли, острой боли, хронической боли, нейропатической боли, воспалительной боли, висцеральной боли, ноцицептивной боли, рассеянного склероза, нейродегенеративного нарушения, синдрома раздраженной кишки, остеоартрита, ревматоидного артрита, нейропатологических нарушений, функциональных нарушений кишечника, воспалительных заболеваний кишечника, боли, связанной с дисменореей, боли в тазу, цистита, панкреатита, мигрени, кластерных и тензионных головных болей, диабетической нейропатии, периферической нейропатической боли, ишиаса, фибромиалгии, болезни Крона, эпилепсии или эпилептических состояний, биполярной депрессии, тахиаритмий, нарушения настроения, биполярного нарушения, психиатрических нарушений, включая тревогу и депрессию, миотонии, аритмии, нарушений движения, нейроэндокринных нарушений, атаксии, недержания, висцеральной боли, невралгии тройничного нерва, герпетической невралгии, общей невралгии, постгерпетической невралгии, корешковой боли, ишиаса, позвоночной боли, боли в голове или шее, острой или некупируемой боли, прорывной боли, боли после хирургического вмешательства, инсульта, боли при злокачественной опухоли, эпилепсии и каузалгии;
и их комбинаций.
[13] Настоящее изобретение предусматривает применение соединения, описанного в любом из [1]-[8], или его фармацевтически приемлемой соли, пролекарства, сольвата или композиции для получения лекарственного средства для лечения состояния или нарушения, в котором используют блокаторы TTX-S каналов.
[14] Настоящее изобретение предусматривает применение, как описано в [13], где указанное состояние или нарушение выбирают из группы, состоящей из: боли, острой боли, хронической боли, нейропатической боли, воспалительной боли, висцеральной боли, ноцицептивной боли, рассеянного склероза, нейродегенеративного нарушения, синдрома раздраженной кишки, остеоартрита, ревматоидного артрита, нейропатологических нарушений, функциональных нарушений кишечника, воспалительных заболеваний кишечника, боли, связанной с дисменореей, боли в тазу, цистита, панкреатита, мигрени, кластерных и тензионных головных болей, диабетической нейропатии, периферической нейропатической боли, ишиаса, фибромиалгии, болезни Крона, эпилепсии или эпилептических состояний, биполярной депрессии, тахиаритмий, нарушения настроения, биполярного нарушения, психиатрических нарушений, включая тревогу и депрессию, миотонии, аритмии, нарушений движения, нейроэндокринных нарушений, атаксии, недержания, висцеральной боли, невралгии тройничного нерва, герпетической невралгии, общей невралгии, постгерпетической невралгии, корешковой боли, ишиаса, позвоночной боли, боли в голове или шее, острой или некупируемой боли, прорывной боли, боли после хирургического вмешательства, инсульта, боли при злокачественной опухоли, эпилепсии, каузалгии и боли, вызванной химиотерапией;
и их комбинаций.
[15] Настоящее изобретение предусматривает соединение, описанное в любом из [1]-[8], или пролекарство или фармацевтически приемлемую соль для использования в лечении состояния или нарушения, в котором используют блокаторы TTX-S каналов.
[16] Настоящее изобретение предусматривает способ получения фармацевтической композиции, который включает смешивание соединения, описанного в любом из [1]-[8], или его пролекарства или его фармацевтически приемлемой соли и фармацевтически приемлемого носителя или эксципиента.
Полезные эффекты изобретения
Производные пиразолопиридина по настоящему изобретению представляют собой блокаторы натриевых каналов и имеют множество терапевтических применений, в частности, при лечении боли.
Более конкретно, производные пиразолопиридина по изобретению представляют собой избирательные чувствительные к тетродотоксину (TTX-S) блокаторы. В нижеследующем обсуждении изобретение проиллюстрировано с помощью ссылки на ингибирование канала NaV1.3 или NaV1.7 в качестве TTX-S каналов.
Они демонстрируют аффинность к каналу NaV1.3 или NaV1.7, которая значительно больше, чем их аффинность к каналу NaV1.5 в качестве устойчивых к тетродотоксину (TTX-R) натриевых каналов.
Производные пиразолопиридина по изобретению демонстрируют хорошую избирательность к каналу NaV1.3 или NaV1.7 по сравнению с каналом NaV1.5.
В частности, производные пиразолопиридина по настоящему изобретению избирательны к TTX-S каналам относительно канала NaV1.5, что ведет к улучшению в профиле побочных эффектов.
Следовательно, производные пиразолопиридина по настоящему изобретению можно использовать в лечении широкого диапазона нарушений, в частности, боли, острой боли, хронической боли, нейропатической боли, воспалительной боли, висцеральной боли, ноцицептивной боли, включая боль после хирургического вмешательства, и смешанные типы боли, включая боль во внутренних органах, желудочно-кишечном тракте, структурах черепа, скелетно-мышечной системе, спинном мозге, мочеполовой системе, сердечно-сосудистой системе и ЦНС, включая боль при злокачественной опухоли, боль в спине, орофациальную боль и боль, вызванную химиотерапией.
Другие состояния, которые можно лечить производными пиразолопиридина по настоящему изобретению, включают рассеянный склероз, нейродегенеративные нарушения, синдром раздраженной кишки, остеоартрит, ревматоидный артрит, нейропатологические нарушения, функциональные нарушения кишечника, воспалительные заболевания кишечника, боль, связанную с дисменореей, боль в тазу, цистит, панкреатит, мигрень, кластерные и тензионные головные боли, диабетическую нейропатию, периферическую нейропатическую боль, ишиас, фибромиалгию, болезнь Крона, эпилепсию или эпилептические состояния, биполярную депрессию, тахиаритмии, нарушение настроения, биполярное нарушение, психиатрические нарушения, такие как тревога и депрессия, миотонию, аритмию, нарушения движения, нейроэндокринные нарушения, атаксию, недержание, висцеральную боль, невралгию тройничного нерва, герпетическую невралгию, общую невралгию, постгерпетическую невралгию, корешковую боль, ишиас, позвоночную боль, боль в голове или шее, острую или некупируемую боль, прорывную боль, боль после хирургического вмешательства, инсульт, боль при злокачественной опухоли, эпилепсию и каузалгию.
Описание вариантов осуществления
Примеры состояний или нарушений, опосредованных TTX-S каналами, включают, но не ограничиваясь этим, связанные с TTX-S каналами заболевания. Соединения по настоящему изобретению демонстрируют блокирующую TTX-S каналы активность. Соединения по настоящему изобретению могут демонстрировать меньшую токсичность, хорошую абсорбцию и распределение, хорошую растворимость, меньшую аффинность связывания с белками, отличными от TTX-S каналов, меньшее взаимодействие между лекарственными средствами, хорошую метаболическую стабильность, сниженную ингибирующую активность в отношении канала HERG и/или уменьшенное удлинение QT.
Специалисты в данной области примут во внимание, что «галоген» или «гало», как используют в настоящем документе, подразумевает включение фтора, хлора, брома и йода. Аналогичным образом, 1-6, как в C1-6, определяют для того, чтобы идентифицировать число, имеющее значение 1, 2, 3, 4, 5 или 6. Согласно определению, например, C1-6, как в C1-6 алкиле, определяют для того, чтобы идентифицировать алкильная группа, которая имеет 1, 2, 3, 4, 5 или 6 атомов углерода. Аналогичным образом, C2-6 алкенил определяют для того, чтобы идентифицировать алкенильную группу, которая имеет 2, 3, 4, 5 или 6 атомов углерода. Группа, которую обозначают как независимо замещенную заместителями, можно независимо замещать множеством таких заместителей.
Термин «алкил», как используют в настоящем документе, обозначает линейный насыщенный одновалентный углеводородный радикал с одним до шести углеродных атомов или разветвленный насыщенный одновалентный углеводородный радикал с тремя до шести углеродных атомов, например, метил, этил, пропил, 2-пропил, бутил (включая все изомерные формы), пентил (включая все изомерные формы) и т.п.
Термин «алкокси», как используют в настоящем документе, обозначает -O-алкил такой как, но не ограничиваясь этим, метокси, этокси, пропокси или 2-пропокси, бутокси (включая все изомерные формы), и т.п.
Термин «алкилтио», как используют в настоящем документе, обозначает -S-алкил такой как, но не ограничиваясь этим, метилтио, этилтио, и т.п.
Термин «алкиламино», как используют в настоящем документе, обозначает -NH-алкил такой как, но не ограничиваясь этим, метиламино, этиламино, пропиламино, 2-пропиламино и т.п.
Термин «алкенил», как используют в настоящем документе, обозначает углеводородный радикал, который имеет по меньшей мере одну двойную связь, которая может быть E- или Z-конфигурации, включая в качестве неограничивающих примеров этенил, пропенил, 1-бутенил, 2-бутенил и т.п.
Термин «циклоалкил», как используют в настоящем документе, обозначает моно- или бициклическое кольцо такое как, но не ограничиваясь этим, циклопропильная, циклобутильная, циклопентильная, циклогексильная, циклогептильная, норборанильная, адамантильная группы и т.п.
Термин «алкилен», как используют в настоящем документе, обозначает линейный насыщенный двухвалентный углеводородный радикал с одним до шести углеродных атомов или разветвленный насыщенный двухвалентный углеводородный радикал с тремя до шести углеродных атомов, если не указано иное, например, но не ограничиваясь этим, метилен, этилен, пропилен, 1-метилпропилен, 2-метилпропилен, бутилен, пентилен и т.п.
Термин «циклоалкилен», как используют в настоящем документе, обозначает моно- или бициклическое кольцо такое как, но не ограничиваясь этим, циклопропилен, циклобутилен, циклопентилен, циклогексилен, циклогептилен и т.п.
Термин «арил», как используют в настоящем документе, обозначает моно- или бикарбоциклическое или моно- или бигетероциклическое кольцо, которое может содержать от 0 до 4 гетероатомов, выбранных из O, N и S, таких как, но не ограничиваясь этим, фенил, нафтил, бензофуранил, бензофуразанил, бензимидазолонил, бензоимидазолил, бензоизотиазолил, бензоизоксазолил, бензотиадиазолил, бензотиазолил, бензоксадиазолил, бензоксазолонил, бензоксазолил, бензотиофенил, бензотриазолил, карбазолил, карболинил, хроманил, циннолинил, 2,3-диоксоиндолил, фуранил, фуразанил, фуропиридил, фуропирролил, имидазолил, имидазопиразинил, имидазопиридинил, имидазопиримидинил, имидазотиазолил, индазолил, индолазинил, индолинил, индолил, изобензофуранил, изохроманил, изоиндолил, изохинолил, изоксазолопиридил, изоксазолинил, изоксазолил, изотиазолил, нафтиридинил, оксазолинил, оксадиазолил, оксазолил, оксетанил, 2-оксоиндолил, фталазил, пиразолопиридил, пиразолопиримидинил, пиразолил, пиразинил, пиридил, пиримидил, пиридазинил, пиридопиримидинил, пирролопиридил, пирролил, хиназолинил, хинолил, хиноксалинил, тетразолопиридил, тетразолил, тиадиазолил, тиазолил, тиофенил, тиенопиразинил, тиенопиразолил, тиенопиридил, тиенопирролил, триазолопиримидинил, триазолил, 4-оксо-1,4-дигидрохинолил, 2-оксо-1,2-дигидропиридил, 4-оксо-1,4-дигидропиримидил, 2-оксо-1,2-дигидрохинолил, 4-оксо-4H-пиридо[1,2-a]пиримидил, 4-оксо-1,4-дигидро-1,8-нафтиридил и их N-оксиды.
Термин «гетероциклил», как используют в настоящем документе, включает как ненасыщенные, так и насыщенные гетероциклические фрагменты; где ненасыщенные гетероциклические фрагменты (т.е. «гетероарил») включают, но не ограничиваясь этим, бензофуранил, бензофуразанил, бензимидазолонил, бензоимидазолил, бензоизотиазолил, бензоизоксазолил, бензотиадиазолил, бензотиазолил, бензоксадиазолил, бензоксазолонил, бензоксазолил, бензотиофенил, бензотриазолил, карбазолил, карболинил, хроманил, циннолинил, 2,3-диоксоиндолил, фуранил, фуразанил, фуропиридил, фуропирролил, имидазолидинонил, имидазолил, имидазопиразинил, имидазопиридинил, имидазопиримидинил, имидазотиазолил, индазолил, индолазинил, индолинил, индолил, изобензофуранил, изохроманил, изоиндолил, изохинолил, изоксазолопиридил, изоксазолинил, изоксазолил, изотиазолил, нафтиридинил, оксазинанонил, оксазолидинонил, оксазолинил, оксадиазолил, оксазолил, оксетанил, 2-оксоиндолил, оксоизоиндолил, фталазил, пиразолил, пиразолопиридил, пиразолопиримидинил, пиразинил, пиридил, пиримидил, пиридазинил, пиридопиримидинил, пирролопиридил, пирролил, хиназолинил, хинолил, хиноксалинил, тетразолопиридил, тетразолил, тиадиазолил, тиазолил, тиофенил, тиенопиразинил, тиенопиразолил, тиенопиридил, тиенопирролил, триазолопиримидинил, триазолил, 4-оксо-1,4-дигидрохинолил, 2-оксо-1,2-дигидропиридил, 4-оксо-1,4-дигидропиримидил, 2-оксо-1,2-дигидрохинолил, 4-оксо-4H-пиридо[1,2-a]пиримидил, 4-оксо-1,4-дигидро-1,8-нафтиридил и их N-оксиды; и где насыщенные гетероциклические фрагменты включают азетидинил, 1,4-диоксанил, гексагидроазепинил, пиперазинил, пиперидинил, пиридин-2-онил, пирролидинил, морфолинил, тетрагидрофуранил, тетрагидропиранил, тиоморфолинил, триазолопиримидил, тетрагидротиенил, пирролидинонил, 3,4-дигидро-2H-пиридо[3,2-b][1,4]оксазинил, 2-оксо-2,5,6,7-тетрагидро-1H-циклопентапиридил, 4,5,6,7-тетрагидроиндазолил, 5,6,7,8-тетрагидро-1,6-нафтиридил, и их N-оксиды и их S-оксиды.
Термин «C0», как используют в настоящем документе, обозначает непосредственную связь.
Термин «защитная группа», как используют в настоящем документе, обозначает защитную гидрокси- или аминогруппу, которую выбирают из типичных защитных гидрокси- или аминогрупп, описанных в Protective Groups in Organic Synthesis под редакцией T. W. Greene et al. (John Wiley & Sons, 2007).
Термин «лечение», как используют в настоящем документе, включает препятствование, сдерживание, замедление, остановку или обращение прогрессирования или тяжести существующего симптома или нарушения. Как используют в настоящем документе, термин «предотвращение» или «для того, чтобы предотвращать» включает препятствование, сдерживание или подавление заболеваемости или возникновения симптома или нарушения.
Как используют в настоящем документе, форма единственного числа относится как к единственному, так и к множественному числу объекта, на который она указывает, если не указано иное.
В объем «соединений по изобретению» включены все соли, сольваты, гидраты, комплексы, полиморфы, пролекарства, радиоактивномеченные производные, стереоизомеры и оптические изомеры соединений формулы (I).
Соединения формулы (I) могут формировать их кислотно-аддитивные соли. Следует принимать во внимание, что для использования в медицине соли соединений формулы (I) должны быть фармацевтически приемлемыми. Подходящие фармацевтически приемлемые соли очевидны специалистам в данной области и включают те, что описаны в J. Pharm. Sci., 1977, 66, 1-19, такие как кислотно-аддитивные соли, сформированные с неорганическими кислотами, например, но не ограничиваясь этим, соляной, бромистоводородной, серной, азотной или фосфорной кислотой; и органическими кислотами, например, но не ограничиваясь этим, янтарной, малеиновой, муравьиной, уксусной, трифторуксусной, пропионовой, фумаровой, лимонной, винной, бензойной, п-толуолсульфоновой, метансульфоновой или нафталинсульфоновой кислотой. Определенные из соединений формулы (I) могут формировать кислотно-аддитивные соли с одним или несколькими эквивалентами кислоты. Объем настоящего изобретения включает все возможные стехиометрические и нестехиометрические формы. Кроме того, определенные соединения, содержащие кислую функцию, такую как карбокси, можно выделять в форме их неорганической соли, в которой противоион можно выбирать из натрия, калия, лития, кальция, магния и т.п., а также из органических оснований, таких как холин, аргинин, бензатин, диэтиламин, глицин, лизин, меглумин, оламин, 2-амино-2-метилпропан-1-ол, бенетамин, трет-бутиламин, гидроксиэтилпирролидин (epolamine), этилендиамин, гидрабамин, морфолин, пиперазин, прокаин, триэтаноламин, диэтаноламин, моноэтаноламин, триизопропаноламин и трометамин.
Также в объем изобретения входят так называемые «пролекарства» соединений формулы (I). Таким образом, определенные производные соединений формулы (I), которые сами могут иметь небольшую или нулевую фармакологическую активность, при введении в или на организм можно превращать в соединения формулы (I), обладающие желаемой активностью, например, посредством гидролитического расщепления. Такие производные обозначают как «пролекарства». Дополнительню информацию об использовании пролекарств можно найти в Pro-drugs as Novel Delivery Systems, Vol. 14, ACS Symposium Series (T Higuchi and W Stella) и Bioreversible Carriers in Drug Design, Pergamon Press, 1987 (ed. E B Roche, American Pharmaceutical Association).
Термин «животное», как используют в настоящем документе, включает субъект-млекопитающее или субъект-немлекопитающее. Примеры подходящего субъекта-млекопитающего могут включать, без ограничения, человека, грызунов, домашних животных, сельскохозяйственных животных и приматов. Подходящие грызуны могут включать, но не ограничиваясь этим, мышей, крыс, хомяков, песчанок и морских свинок. Подходящие домашние животные могут включать, но не ограничиваясь этим, кошек, собак, кроликов и хорьков. Подходящие сельскохозяйственные животные могут включать, но не ограничиваясь этим, лошадей, коз, овец, свиней, крупный рогатый скот, лам и альпак. Подходящие приматы могут включать, но не ограничиваясь этим, шимпанзе, лемуров, макак, игрунок, паукообразных обезьян, беличьих обезьян и зеленых мартышек. Примеры подходящего субъекта-немлекопитающего могут включать, без ограничения, птиц, рептилий, амфибий и рыб. Неограничивающие примеры птиц включают куриц, индеек, уток и гусей. Предпочтительным субъектом-млекопитающим является человек.
Пролекарства в соответствии с изобретением, например, можно получать посредством замены подходящих функциональностей, присутствующих в соединениях формулы (I), на определенные фрагменты, известные специалистам в данной области в качестве «профрагментов», как описано, например, в Design of Prodrugs by H. Bundgaard (Elsevier, 1985). Некоторые примеры пролекарств в соответствии с изобретением включают:
(i) когда соединение формулы (I) содержит спиртовую функциональность (-OH), соединения, где гидроксигруппу заменяют на фрагмент, который может быть превращен в гидроксигруппу in vivo. Указанный фрагмент, который может быть превращен в гидроксигруппу in vivo, обозначает фрагмент, который может быть трансформирован в гидроксильную группу in vivo посредством, например, гидролиза и/или посредством фермента, например, эстеразы. Примеры указанного фрагмента включают, но не ограничиваясь этим, сложноэфирные и простые эфирные группы, которые можно легко гидролизовать in vivo. Предпочтительными являются фрагменты, которые заменили водород гидроксигруппы на ацилоксиалкил, 1-(алкоксикарбонилокси)алкил, фталидил и ацилоксиалкилоксикарбонил, такой как пивалоилоксиметилоксикарбонил; и
(ii) когда соединение формулы (I) содержит аминогруппу, в качестве примера пролекарства приведено производное пиразолопиридина, полученное посредством реакции с подходящим галогенангидридом или подходящим ангидридом кислоты. Особенно предпочтительным производным пиразолопиридина в качестве пролекарства является -NHCO(CH2)2OCH3, -NHCOCH(NH2)CH3 или тому подобное.
Дополнительные примеры замещающих групп в соответствии с приведенными выше примерами и примерами пролекарств других типов можно найти в указанных выше литературных источниках.
Соединения формулы (I) и их соли можно получать в кристаллической или некристаллической форме, и, если в кристаллической, их необязательно можно гидратировать или сольватировать. Объем этого изобретения включает стехиометрические гидраты или сольваты, а также соединения, содержащие переменные количества воды и/или растворителя.
Соли и сольваты, имеющие фармацевтически неприемлемые противоионы или ассоциированные растворители, входят в объем настоящего изобретения, например, для применения в качестве промежуточных соединений при получении других соединений формулы (I) и их фармацевтически приемлемых солей.
Соединения формулы (I) могут иметь полиморфы в кристаллической форме, которые входят в объем настоящего изобретения.
Дополнительно, соединения формулы (I) можно вводить в качестве пролекарств. Как используют в настоящем документе, «пролекарство» соединения формулы (I) представляет собой функциональное производное соединения, которое, при введении пациенту, в конечном итоге высвобождает соединение формулы (I) in vivo. Введение соединения формулы (I) в качестве пролекарства может позволять специалисту в данной области выполнять одно или несколько из следующего: (a) модифицировать начало действия соединения in vivo; (b) модифицировать длительность действия соединения in vivo; (c) модифицировать транспортировку или распределение соединения in vivo; (d) модифицировать растворимость соединения in vivo; и (e) преодолеть побочный эффект или другую сложность, связанную с соединением. Типичные функциональные производные, используемые с получением пролекарства, включают модификации соединения, которые химически или ферментативно отщепляют in vivo. Такие модификации, которые включают получение фосфатов, амидов, сложных эфиров, сложных тиоэфиров, карбонатов и карбаматов, хорошо известны специалистам в данной области.
В определенных соединениях формулы (I) может присутствовать один или несколько хиральных углеродных атомов. В таких случаях соединения формулы (I) существуют в виде стереоизомеров. Изобретение распространяется на все оптические изомеры, такие как стереоизомерные формы соединений формулы (I), включая энантиомеры, диастереоизомеры и их смеси, такие как рацематы. Различные стереоизомерные формы можно разделять или разрешать друг от друга стандартными способами, или какой-либо заданный изомер можно получать с помощью стандартного стереоселективного или асимметричного синтеза.
Определенные соединения в настоящем документе могут существовать в различных таутомерных формах, и следует понимать, что данное изобретение относится ко всем таким таутомерным формам.
Изобретение также включает меченные изотопами соединения, которые идентичны тем, что описаны в настоящем документе, но с учетом того факта, что один или несколько атомов заменяют на атом, который имеет атомную массу или массовое число, отличное от атомной массы или массового числа, которое обычно находят в природе. Примеры изотопов, которые могут быть встроены в соединения по изобретению, включают изотопы водорода, углерода, азота, кислорода, фосфора, фтора, йода и хлора, такие как 2H, 3H, 11C, 13C, 14C, 18F, 123I и 125I. Соединения по изобретению, которые содержат указанные выше изотопы и/или другие изотопы других атомов, входят в объем настоящего изобретения. Меченные изотопами соединения по настоящему изобретению, например, те, в которые встроены радиоактивные изотопы, такие как 3H, 14C, можно использовать в анализе распределения лекарственного средства и/или субстрата в тканях. Изотопы тритий, т.е. 3H, и углерод-14, т.е. 14C, являются особенно предпочтительными из-за легкости их получения и возможности обнаружения. Изотопы 11C и 18F, в частности, можно использовать в PET (позитронно-эмиссионная томография), а изотопы 123I, в частности, можно использовать в SPECT (однофотонной эмиссионной компьютерной томографии), все можно использовать при визуализации головного мозга. Кроме того, замещение более тяжелыми изотопами, такими как дейтерий, т.е. 2H, может давать определенные терапевтические преимущества, являющиеся результатом более высокой метаболической стабильности, например, увеличенное время полужизни in vivo или сниженные требования к дозе, и, таким образом, может быть предпочтительным в некоторых случаях. Меченные изотопами соединения по изобретению обычно можно получать посредством осуществления процедур, раскрытых ниже в схемах и/или в примерах, с последующим замещением немеченного изотопами реактива легкодоступным меченным изотопами реактивом.
В отношении других соединений, раскрытых в данной области, определенные соединения проявляют неожиданные свойства, например, в отношении длительности действия и/или метаболизма, такие как увеличенная метаболическая стабильность, увеличенная пероральная биодоступность или абсорбция и/или сниженные взаимодействия между лекарственными средствами.
Соединения формулы (I), представляющие собой блокаторы канала NaV1.3 и/или NaV1.7, потенциально можно использовать при лечении определенного спектра нарушений. Лечение боли, в частности, хронической, воспалительной, нейропатической, ноцицептивной и висцеральной боли, является предпочтительным использованием.
Физиологическая боль представляет собой важный защитный механизм, выработанный для того, чтобы предупреждать об опасности потенциально вредоносных стимулов из внешней среды. Система работает через особый набор первичных сенсорных нейронов, и ее активируют болевые стимулы через механизмы периферической трансдукции (см. Millan, 1999, Prog. Neurobiol., 57, 1-164, обзор). Эти сенсорные волокна известны как болевые рецепторы и представляют собой аксоны характерно малого диаметра с низкими скоростями проведения. Болевые рецепторы кодируют интенсивность, длительность и качество болевого стимула и, в соответствии с их топографически организованной проекцией на спинной мозг, местоположение стимула. Болевые рецепторы находят на ноцицептивных нервных волокнах, среди которых имеет место два основных типа, A-дельта волокна (миелинизированные) и C волокна (безмиелиновые). Активность, генерируемая с помощью входного сигнала болевого рецептора, переносится, после комплексной обработки в заднем роге, или непосредственно или через переключательные ядра ствола мозга, в вентробазальный таламус и после этого в кору, где возникает ощущение боли.
Боль обычно можно классифицировать как острую или хроническую. Острая боль начинается внезапно и непродолжительна (обычно двенадцать недель или меньше). Она обычно связана с конкретной причиной, такой как конкретное повреждение, и часто является острой и сильной. Боль этого типа может возникать после конкретных повреждений, являющихся результатом хирургического вмешательства, лечения зубов, растяжения или вывиха. Острая боль обычно не ведет к какой-либо персистирующей физиологической реакции. В отличие от этого, хроническая боль представляет собой длительную боль, типично персистирующую в течение больше чем трех месяцев и ведущую к значительным физиологическим и эмоциональным проблемам. Обыкновенные примеры хронической боли представляют собой нейропатическую боль (например, болевую диабетическую нейропатию, постгерпетическую невралгию), синдром запястного канала, позвоночную боль, головную боль, боль при злокачественной опухоли, артритическую боль и хроническую боль после хирургического вмешательства.
Когда в ткани организма наблюдается существенное повреждение вследствие заболевания или травмы, происходит изменение характеристик активации болевого рецептора и имеет место повышение чувствительности, на периферии локально около повреждения и центрально, где заканчиваются болевые рецепторы. Эти эффекты ведут к повышенному ощущению боли. При острой боли эти механизмы могут быть полезны, при содействии протективному поведению, которое может лучше способствовать тому, чтобы процессы восстановления имели место. Обычно ожидают, что чувствительность нормализуется после заживления повреждения. Однако при многих хронических болевых состояниях, гиперчувствительность сохраняется долго после процесса заживления и часто обусловлена повреждением нервной системы. Это повреждение часто ведет к аномалиям в чувствительных нервных волокнах, связанным с недостаточной адаптацией и аберрантной активностью (Woolf & Salter, 2000, Science, 288, 1765-1768).
Клиническая боль имеет место, когда дискомфорт и анормальная чувствительность выделяются среди симптомов у пациента. Пациенты обычно бывают достаточно гетерогенными и могут давать различные болевые симптомы. Такие симптомы включают: 1) спонтанную боль, которая может быть тупой, жгучей или колющей; 2) увеличенную болевую реакцию на болевые стимулы (гипералгезия); и 3) боль, вызываемую обычно безопасными стимулами (аллодиния - Meyer et al., 1994, Textbook of Pain, 13-44). Несмотря на то, что пациенты, страдающие различными формами острой и хронической боли, могут иметь схожие симптомы, лежащие в основе механизмы могут быть различны и, следовательно, могут требовать различных стратегий лечения. Следовательно, боль также делят на множество различных подтипов согласно отличающейся патофизиологии, включая ноцицептивную, воспалительную и нейропатическую боль.
Ноцицептивную боль вызывает повреждение ткани или интенсивные стимулы с потенциалом вызвать повреждение. Болевые афференты активируются посредством трансдукции стимулов болевыми рецепторами в месте повреждения и активируют нейроны в спинном мозге на уровне, где они заканчиваются. Затем происходит их переключение на восходящие проводящие пути спинного мозга к головному мозгу, где происходит восприятие боли (Meyer et al., 1994, Textbook of Pain, 13-44). Активация болевых рецепторов активирует афферентные нервные волокна двух типов. Миелинизированные A-дельта волокна передают быстро и отвечают за ощущения острой и колющей боли, тогда как безмиелиновые C волокна передают с более низкой скоростью и переносят тупую или ноющую боль. Острая ноцицептивная боль от умеренной до острой является значимым признаком боли от травмы центральной нервной системы, растяжений/вывихов, ожогов, инфаркта миокарда и острого панкреатита, послеоперационной боли (боли после хирургической процедуры любого типа), посттравматической боли, почечной колики, боли при злокачественной опухоли и позвоночной боли. Боль при злокачественной опухоли может представлять собой хроническую боль, такую как боль, связанная с опухолью, (например, боль в костях, головная боль, лицевая боль или висцеральная боль) или боль, связанная с терапией злокачественной опухоли (например, постхимиотерапевтический синдром, синдром хронической боли после хирургического вмешательства или постлучевой синдром). Боль при злокачественной опухоли также может возникать в ответ на химиотерапию, иммунотерапию, гормональную терапию или лучевую терапию. Позвоночная боль может возникать из-за грыжевых или разорванных межпозвоночных дисков или аномалий люмбальных фасеточных суставов, крестцово-подвздошных сочленений, паравертебральных мышц или задней продольной связки. Позвоночная боль может разрешаться естественным путем, но у некоторых пациентов, когда она длится более 12 недель, она становится хроническим состоянием, которое может быть чрезвычайно изнуряющим.
Нейропатическую боль в настоящее время определяют как боль, которую инициирует или обуславливает первичное повреждение или нарушение функции нервной системы. Повреждение нервов может быть обусловлено травмой и заболеванием, и, таким образом, термин «нейропатическая боль» охватывает многие нарушения с различной этиологией. Они включают, но не ограничиваясь этим, периферическую нейропатию, диабетическую нейропатию, постгерпетическую невралгию, невралгию тройничного нерва, позвоночную боль, нейропатию при злокачественной опухоли, ВИЧ-нейропатию, боль в фантомной конечности, синдром запястного канала, центральную постинсультную боль и боль, связанную с хроническим алкоголизмом, гипотиреоидизм, уремию, рассеянный склероз, повреждение спинного мозга, болезнь Паркинсона, эпилепсию и недостаточность витаминов. Нейропатическая боль является патологической, поскольку она не играет защитной роли. Она часто присутствует долго после исчезновения исходной причины, обыкновенно длится в течение лет, значительно снижая качество жизни пациента (Woolf and Mannion, 1999, Lancet, 353, 1959-1964). Симптомы нейропатической боли сложно лечить, поскольку они часто являются гетерогенными, даже среди пациентов с одним и тем же заболеванием (Woolf & Decosterd, 1999, Pain Supp., 6, S141-S147; Woolf and Mannion, 1999, Lancet, 353, 1959-1964). Они включают спонтанную боль, которая может быть непрерывной, и пароксизмальную или анормальную спровоцированную боль, такую как гипералгезия (повышенная чувствительность к болевому стимулу) и аллодиния (чувствительность к обычно безопасному стимулу).
Воспалительный процесс представляет собой сложную последовательность биохимических и клеточных событий, активируемых в ответ на повреждение ткани или присутствие инородных веществ, результатом чего является отек и боль (Levine and Taiwo, 1994, Textbook of Pain, 45-56). Артритическая боль представляет собой наиболее распространенную воспалительную боль. Ревматоидная болезнь представляет собой одно из наиболее распространенных хронических воспалительных состояний в развитых странах и ревматоидный артрит является обыкновенной причиной нетрудоспособности. Точная этиология ревматоидного артрита не известна, но современные гипотезы предполагают, что могут быть важны как генетические, так и микробиологические факторы (Grennan & Jayson, 1994, Textbook of Pain, 397-407). По оценкам, почти 16 миллионов американцев имеют симптоматический остеоартрит (OA) или дегенеративное заболевание суставов, большинство из которых в возрасте более 60 лет, и ожидается увеличение до 40 миллионов с увеличением возраста популяции, чудовищно увеличивая эту проблему здравоохранения (Houge & Mersfelder, 2002, Ann Pharmacother., 36, 679-686; McCarthy et al., 1994, Textbook of Pain, 387-395). Большинство пациентов с остеоартритом нуждаются в медицинском обслуживании в связи со связанной болью. Артрит имеет значительное влияние на психосоциальную и физическую функцию, и известно, что он является ведущей причиной нетрудоспособности в старческом возрасте. Анкилозирующий спондилит также представляет собой ревматическое заболевание, которое вызывает артрит позвоночника и крестцово-подвздошных сочленений. Он варьирует от прерывистых эпизодов позвоночной боли, которые возникают на всем протяжении жизни, до тяжелого хронического заболевания, которое атакует позвоночник, периферические сосуды и другие органы тела.
Другой тип воспалительной боли представляет собой висцеральную боль, которая включает боль, связанную с воспалительным заболеванием кишечника (IBD). Висцеральная боль представляет собой боль, связанную с внутренними органами, которые охватывают органы брюшной полости. Эти органы включают половые органы, селезенку и часть пищеварительной системы. Боль, связанную с внутренними органами, можно разделить на боль органов пищеварительной системы и боль органов не пищеварительной системы. Обыкновенно встречающиеся нарушения желудочно-кишечного тракта (ЖКТ), которые вызывают боль, включают функциональные нарушения кишечника (FBD) и воспалительное заболевание кишечника (IBD). Эти нарушения ЖКТ включают широкий диапазон состояний заболеваний, которые в настоящее время контролируют лишь умеренно, включая, в отношении FBD, желудочно-пищеводный рефлюкс, диспепсию, синдром раздраженной кишки (IBS) и синдром функциональной абдоминальной боли (FAPS), и в отношении IBD, болезнь Крона, илеит и язвенный колит, которые все регулярно вызывают висцеральную боль. Другие типы висцеральной боли включают боль, связанную с дисменореей, циститом и панкреатитом, и боль в тазу.
Следует отметить, что некоторые типы боли имеют множество этиологий, и, таким образом, их можно классифицировать в больше чем одной области, например, позвоночная боль и боль при злокачественной опухоли имеют как ноцицептивные, так и нейропатические компоненты.
Другие типы боли включают:
(i) боль, являющуюся результатом скелетно-мышечных нарушений, включая миалгию, фибромиалгию, спондилит, серонегативные (неревматоидные) артропатии, несуставной ревматизм, дистрофинопатию, гликогенолиз, полимиозит и пиомиозит;
(ii) сердечную и сосудистую боль, включая боль, обусловленную стенокардией, инфарктом миокарда, митральным стенозом, перикардитом, феноменом Рейно, склередему и ишемию скелетных мышц;
(iii) головную боль, такую как мигрень (включая мигрень с аурой и мигрень без ауры), кластерная головная боль, тензионная головная боль, смешанная головная боль и головная боль, связанная с сосудистыми нарушениями; и
(vi) орофациальную боль, включая зубную боль, ушную боль, синдром жжения полости рта и височно-нижнечелюстную миофасциальную боль.
Также ожидают, что соединения формулы (I) можно использовать при лечении рассеянного склероза.
Изобретение также относится к терапевтическому использованию соединений формулы (I) в качестве средств для лечения или облегчения симптомов нейродегенеративных нарушений. Такие нейродегенеративные нарушения включают, например, болезнь Альцгеймера, болезнь Хантингтона, болезнь Паркинсона и амиотрофический боковой склероз. Настоящее изобретение также охватывает лечение нейродегенеративных нарушений, называемых острым мозговым повреждением. Они включают, но не ограничиваясь этим, инсульт, травму головы и асфиксию. Инсульт относится к церебральному сосудистому заболеванию, и также его можно обозначать как церебральное сосудистое нарушение (CVA), и он включает острый тромбоэмболический инсульт. Инсульт включает как очаговую, так и общую ишемию. Также включены временные церебральные ишемические приступы и другие церебральные сосудистые проблемы, сопровождаемые ишемией головного мозга. Эти сосудистые нарушения могут возникать у пациента, подвергающегося конкретно каротидной эндартерэктомии или другим цереброваскулярным или сосудистым хирургическим процедурам в целом или диагностическим сосудистым процедурам, включая церебральную ангиографию и т.п. Другие нарушения представляют собой травму головы, травму спинного мозга или повреждение от общей аноксии, гипоксии, гипогликемии, гипотензии, а также схожих повреждений, наблюдаемых во время процедур, от эмболии, гиперфузии и гипоксии. Настоящее изобретение можно использовать в определенном спектре нарушений, например, во время сердечного коронарного шунтрирования, при внутричерепных геморрагических нарушениях, при перинатальной асфиксии, при остановке сердца и эпилептическом статусе.
Опытный врач будет способен определять ситуацию, в которой субъекты восприимчивы к или имеют риск, например, инсульта, а также страдают инсультом, подходящую для введения посредством способов по настоящему изобретению.
TTX-S натриевые каналы вовлечены в широкий диапазон биологических функций. Это предполагает возможную роль этих рецепторов в различных патологических процессах у человека или других видов. Соединения по настоящему изобретению имеют полезность при лечении, предотвращении, улучшении, управлении или снижении риска различных неврологических и психиатрических нарушений, связанных с TTX-S натриевыми каналами, включая одно или несколько из следующих состояний или заболеваний: боль, острая боль, хроническая боль, нейропатическая боль, воспалительная боль, висцеральная боль, ноцицептивная боль, рассеянный склероз, нейродегенеративное нарушение, синдром раздраженной кишки, остеоартрит, ревматоидный артрит, нейропатологические нарушения, функциональные нарушения кишечника, воспалительные заболевания кишечника, боль, связанная с дисменореей, боль в тазу, цистит, панкреатит, мигрень, кластерные и тензионные головные боли, диабетическая нейропатия, периферическая нейропатическая боль, ишиас, фибромиалгия, болезнь Крона, эпилепсия или эпилептические состояния, биполярная депрессия, тахиаритмии, нарушение настроения, биполярное нарушение, психиатрические нарушения, такие как тревога и депрессия, миотония, аритмия, нарушения движения, нейроэндокринные нарушения, атаксия, недержание, висцеральная боль, невралгия тройничного нерва, герпетическая невралгия, общая невралгиая, постгерпетическая невралгия, корешковая боль, ишиас, позвоночная боль, боль в голове или шее, острая или некупируемая боль, прорывная боль, боль после хирургического вмешательства, инсульт, боль при злокачественной опухоли, эпилепсия, каузалгия и боль, вызванная химиотерапией.
Дозировка активного ингредиента в композициях по данному изобретению может варьировать, однако, необходимо, чтобы количество активного ингредиента было таким, что получают подходящую дозированную форму. Активный ингредиент можно вводить пациентам (животным и человеку), нуждающимся в таком лечении, в дозах, которые обеспечат оптимальную фармацевтическую эффективность.
Выбранная доза зависит от желаемого терапевтического эффекта, пути введения и длительности лечения. Доза будет варьировать от пациента к пациенту в зависимости от природы и тяжести заболевания, массы пациента, особой диеты, которой после этого придерживается пациент, сопутствующего лечения и других факторов, которые известны специалистам в данной области.
Для введения пациентам-людям общая суточная доза соединений по изобретению типично находится в диапазоне от 0,1 мг до 1000 мг, конечно, в зависимости от способа введения. Например, пероральное введение может требовать общей суточной дозы от 1 мг до 1000 мг, тогда как внутривенная доза может требовать только от 0,1 мг до 100 мг. Общую суточную дозу можно вводить одной или разделенными дозами, и она может, по усмотрению врача, выходить за пределы типичного диапазона, данного в настоящем документе.
Эти дозы основаны на среднем субъекте-человеке, который имеет массу приблизительно от 60 кг до 70 кг. Врач без труда будет способен определять дозы для субъектов, масса которых выходит из этого диапазона, таких как дети и престарелые люди.
В одном из вариантов осуществления диапазон доз будет составлять приблизительно от 0,5 мг до 500 мг на пациента в сутки; в другом варианте осуществления приблизительно от 0,5 мг до 200 мг на пациента в сутки; в другом варианте осуществления приблизительно от 1 мг до 100 мг на пациента в сутки; и в другом варианте осуществления приблизительно от 5 мг до 50 мг на пациента в сутки; в еще одном другом варианте осуществления приблизительно от 1 мг до 30 мг на пациента в сутки. Фармацевтические композиции по настоящему изобретению можно предоставлять в твердом дозированном составе, например, содержащем приблизительно от 0,5 мг до 500 мг активного ингредиента или содержащем приблизительно от 1 мг до 250 мг активного ингредиента. Фармацевтическую композицию можно предоставлять в твердом дозированном составе, который содержит приблизительно 1 мг, 5 мг, 10 мг, 25 мг, 50 мг, 100 мг, 200 мг или 250 мг активного ингредиента. Для перорального введения композиции можно предоставлять в форме таблеток, содержащих от 1,0 до 1000 миллиграммов активного ингредиента, например, 1, 5, 10, 15, 20, 25, 50, 75, 100, 150, 200, 250, 300, 400, 500, 600, 750, 800, 900 и 1000 миллиграммов активного ингредиента, для симптоматической корректировки дозы для пациента, подлежащего лечению. Соединения можно вводить по схеме от 1 до 4 раз в сутки, например, один или два раза в сутки.
Соединения по настоящему изобретению можно использовать в комбинации с одним или несколькими другими лекарственными средствами при лечении, предотвращении, управлении, уменьшении интенсивности или снижении риска заболеваний или состояний, для которых соединения по настоящему изобретению или другие лекарственные средства могут иметь полезность, где комбинация лекарственных средств вместе безопаснее или более эффективна, чем любое лекарственное средство отдельно. Такое другое лекарственное средство(а), таким образом, можно вводить путем и в количестве, широко используемых, одновременно или последовательно, с соединением по настоящему изобретению. Когда соединение по настоящему изобретению используют одновременно с одним или несколькими другими лекарственными средствами, предполагают фармацевтическую композицию в стандартной дозированной форме, которая содержит такие другие лекарственные средства и соединение по настоящему изобретению. Однако комбинированное лечение также может включать терапию, в которой соединение по настоящему изобретению и одно или несколько других лекарственных средств вводят по различным перекрывающимся схемам. Также предусмотрено, что когда используют в комбинации с одним или несколькими другими активными ингредиентами, соединения по настоящему изобретению и другие активные ингредиенты можно использовать в более низких дозах, чем когда каждое используют по отдельности.
Соответственно, фармацевтические композиции по настоящему изобретению включают те, которые содержат один или несколько других активных ингредиентов, в дополнение к соединению по настоящему изобретению. Приведенные выше комбинации включают комбинации соединения по настоящему изобретению не только с одним другим активным соединением, но также с двумя или более другими активными соединениями.
Аналогичным образом, соединения по настоящему изобретению можно использовать в комбинации с другими лекарственными средствами, которые используют при предотвращении, лечении, управлении, уменьшении интенсивности или снижении риска заболеваний или состояний, для которых можно использовать соединения по настоящему изобретению. Такие другие лекарственные средства, таким образом, можно вводить посредством пути и в количестве, широко используемых, одновременно или последовательно с соединением по настоящему изобретению. Когда соединение по настоящему изобретению используют одновременно с одним или несколькими другими лекарственными средствами, предполагают фармацевтическую композицию, содержащую такие другие лекарственные средства в дополнение к соединению по настоящему изобретению. Соответственно, фармацевтические композиции по настоящему изобретению включают те, которые также содержат один или несколько других активных ингредиентов, в дополнение к соединению по настоящему изобретению.
Массовое соотношение соединения по настоящему изобретению и второго активного ингредиента может варьировать и будет зависеть от эффективной дозы каждого ингредиента. Обычно используют эффективную дозу каждого. Таким образом, например, когда соединение по настоящему изобретению объединяют с другим средством, массовое соотношение соединения по настоящему изобретению и другого средства обычно будет варьировать от приблизительно 1000:1 до приблизительно 1:1000, включая от приблизительно 200:1 до приблизительно 1:200. Комбинации соединения по настоящему изобретению и других активных ингредиентов обычно также будут в пределах указанного выше диапазона, но в каждом случае будут использовать эффективную дозу каждого активного ингредиента. В таких комбинациях соединение по настоящему изобретению и другие активные средства можно вводить отдельно или вместе. Кроме того, введение одного элемента может быть до, параллельно или после введения другого средства(средств).
Блокатор TTX-S натриевых каналов можно эффективно объединять с другим фармакологически активным соединением или с двумя или более другими фармакологически активными соединениями, в частности, при лечении воспалительной боли и урологических заболеваний или нарушений. Например, блокатор TTX-S натриевых каналов, в частности, соединение формулы (I) или его пролекарство или его фармацевтически приемлемую соль или сольват, как определено выше, можно вводить одновременно, последовательно или отдельно в комбинации с одним или несколькими средствами, выбранными из следующего:
- опиоидный анальгетик, например, морфин, героин, гидроморфон, оксиморфон, леворфанол, леваллорфан, метадон, меперидин, фентанил, кокаин, кодеин, дигидрокодеин, оксикодон, гидрокодон, пропоксифен, налмефен, налорфин, налоксон, налтрексон, бупренорфин, буторфанол, налбуфин или пентазоцин;
- нестероидное противовоспалительное лекарственное средство (НПВС), например, аспирин, диклофенак, дифлузинал, этодолак, фенбуфен, фенопрофен, флуфенизал, флурбипрофен, ибупрофен, индометацин, кетопрофен, кеторолак, меклофенамовая кислота, мефенамовая кислота, мелоксикам, набуметон, напроксен, нимесулид, нитрофлурбипрофен, олсалазин, оксапрозин, фенилбутазон, пироксикам, сульфасалазин, сулиндак, толметин или зомепирак;
- барбитуратное успокоительное, например, амобарбитал, апробарбитал, бутабарбитал, бутабитал, мефобарбитал, метарбитал, метогекситал, пентобарбитал, фенобартитал, секобарбитал, талбутал, теамилал или тиопентал;
- бензодиазепин, который обладает седативным действием, например, хлордиазэпоксид, клоразепат, диазепам, флуразепам, лоразепам, оксазепам, темазепам или триазолам;
- H1 антагонист, который обладает седативным действием, например, дифенгидрамин, пириламин, прометазин, хлорфенирамин или хлорциклизин;
- успокоительное, такое как глютетимид, мепробамат, метаквалон или дихлоралфеназон;
- релаксант скелетных мышц, например, баклофен, карисопродол, хлорзоксазон, циклобензаприн, метокарбамол или орфренадин;
- антагонист NMDA рецептора, например, декстрометорфан ((+)-3-гидрокси-N-метилморфинан) или его метаболит декстрорфан ((+)-3-гидрокси-N-метилморфинан), кетамин, мемантин, пирролохинолин хинин, цис-4-(фосфонометил)-2-пиперидинкарбоновая кислота, будипин, EN-3231 (MorphiDexTM, комбинированный состав морфина и декстрометорфана), топирамат, нерамексан или перзинфотел, включая антагонист NR2B, например, ифенпродил, траксопродил или (-)-(R)-6-{2-[4-(3-фторфенил)-4-гидрокси-1-пиперидинил]-1-гидроксиэтил-3,4-дигидро-2(1H)-хинолинон;
- альфа-адренергическое средство, например, доксазозин, тамсулозин, клонидин, гуанфацин, дексмедетомидин, модафинил или 4-амино-6,7-диметокси-2-(5-метан-сульфонамидо-1,2,3,4-тетрагидроизохинол-2-ил)-5-(2-пиридил)хиназолин;
- трициклический антидепрессант, например, десипрамин, имипрамин, амитриптилин или нортриптилин;
- антиконвульсант, например, карбамазепин, ламотригин, топиратмат или вальпроат;
- тахикининовый (NK) антагонист, в частности антагонист NK-3, NK-2 или NK-1, например, альфаR,9R)-7-[3,5-бис(трифторметил)бензил]-8,9,10,11-тетрагидро-9-метил-5-(4-метилфенил)-7H-[1,4]диазоцино[2,1-g][1,7]-нафтиридин-6-13-дион (TAK-637), 5-[[(2R,3S)-2-[(1R)-1-[3,5-бис(трифторметил)фенил]этокси-3-(4-фторфенил)-4-морфолинил]метил]-1,2-дигидро-3H-1,2,4-триазол-3-он (MK-869), апрепитант, ланепитант, дапитант или 3-[[2-метокси-5-(трифторметокси)фенил]метиламино]-2-фенилпиперидин (2S,3S);
- мускариновый антагонист, например, оксибутинин, толтеродин, пропиверин, троспия хлорид, дарифенацин, солифенацин, темиверин и ипратропий;
- избирательный ингибитор ЦОГ-2, например, целекоксиб, рофекоксиб, парекоксиб, валдекоксиб, деракоксиб, эторикоксиб, или люмиракоксиб;
- анальгетик из дегтя, в частности парацетамол;
- нейролептик, такой как дроперидол, хлорпромазин, галоперидол, перфеназин, тиоридазин, мезоридазин, трифлуоперазин, флуфеназин, клозапин, оланзапин, рисперидон, зипрасидон, кветиапин, сертиндол, арипипразол, сонепипразол, блонансерин, илоперидон, пероспирон, раклоприд, зотепин, бифепрунокс, азенапин, луразидон, амисульприд, балаперидон, палиндор, эпливанзерин, озанетант, римонабант, меклинертант, МираксионTM или саризотан;
- агонист (например, ресинифератоксин) или антагонист (например, капсазепин) рецептора ваниллоида;
- агонист или антагонист катионного канала с транзиторным рецепторным потенциалом подтипа V1, V2, V3, V4, M8, M2, A1;
- бета-адренергическое средство, такое как пропранолол;
- местный анестетик, такой как мексилетин;
- кортикостероид, такой как дексаметезон;
- агонист или антагонист 5-HT рецептора, в частности, агонист 5-HT1B/1D, такой как элетриптан, суматриптан, наратриптан, золмитриптан или ризатриптан;
- антагонист 5-HT2A рецептора, такой как R(+)-альфа-(2,3-диметокси-фенил)-1-[2-(4-фторфенилэтил)]-4-пиперидинметанол (MDL-100907);
- холинергический (никотиновый) анальгетик, такой как изпрониклин (TC-1734), (E)-N-метил-4-(3-пиридинил)-3-бутен-1-амин (RJR-2403), (R)-5-(2-азетидинилметокси)-2-хлорпиридин (ABT-594) или никотин;
- ТрамадолTM;
- PDEV ингибитор, такой как 5-[2-этокси-5-(4-метил-1-пиперазинилсульфонил)фенил]-1-метил-3-N-пропил-1,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-он (силденафил), (6R,12aR)-2,3,6,7,12,12a-гексагидро-2-метил-6-(3,4-метилендиоксифенил)пиразино[2',1':6,1]пиридо[3,4-b]индол-1,4-дион (IC-351 или тадалафил), 2-[2-этокси-5-(4-этилпиперазин-1-ил-сульфонил)фенил]-5-метил-7-пропил-3H-имидазо[5,1-f][1,2,4]триазин-4-он (варденафил), 5-(5-ацетил-2-бутокси-3-пиридинил)-3-этил-2-(1-этил-3-азетидинил)-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-он, 5-(5-ацетил-2-пропокси-3-пиридинил)-3-этил-2-(1-изопропил-3-азетидинил)-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-он, 5-[2-этокси-5-(4-этилпиперазин-1-илсульфонил)пиридин-3-ил]-3-этил-2-[2-метоксиэтил]-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-он, 4-[(3-хлор-4-метоксибензил)амино]-2-[(2S)-2-(гидроксиметил)пирролидин-1-ил]-N-(пиримидин-2-илметил)пиримидин-5-карбоксамид, 3-(1-метил-7-оксо-3-пропил-6,7-дигидро-1H-пиразоло[4,3-d]пиримидин-5-ил)-N-[2-(1-метилпирролидин-2-ил)этил]-4-пропоксибензолсульфонамид;
- альфа-2-дельта лиганд, такой как габапентин, прегабалин, 3-метилгабапентин, (3-(аминометил)бицикло[3.2.0]гепт-3-ил)уксусная кислота, (3S,5R)-3-(аминометил)-5-метилгептановая кислота, (3S,5R)-3-амино-5-метилгептановая кислота, (3S,5R)-3-амино-5-метилоктановая кислота, (2S,4S)-4-(3-хлорфенокси)пролин, (2S,4S)-4-(3-фторбензил)пролин, [(1R,5R,6S)-6-(аминометил)бицикло[3.2.0]гепт-6-ил]уксусная кислота, 3-((1-(аминометил)циклогексил)метил)-4H-[1,2,4]оксадиазол-5-он, C-[1-((1H-тетразол-5-ил)метил)циклогептил]метиламин, (3S,4S)-(1-(аминометил)-3,4-диметилциклопентил)уксусная кислота, (3S,5R)-3-(аминометил)-5-метилоктановая кислота, (3S,5R)-3-амино-5-метилнонановая кислота, (3S,5R)-3-амино-5-метилоктановая кислота, (3R,4R,5R)-3-амино-4,5-диметилгептановая кислота и (3R,4R,5R)-3-амино-4,5-диметилоктановая кислота;
- каннабиноид;
- антагонист метаботропного рецептора глутамата подтипа 1 (mGluR1);
- ингибитор обратного захвата серотонина, такой как сертралин, метаболит сертралина деметилсертралин, флуоксетин, норфлуоксетин (дезметиловый метаболит флуоксетина), флувоксамин, пароксетин, циталопрам, метаболит циталопрам дезметилциталопрам, эсциталопрам, d,l-фенфлурамин, фемоксетин, ифоксетин, цианодотиепин, литоксетин, дапоксетин, нефазодон, церикламин и тразодон;
- ингибитор обратного захвата норадреналина (норэпинефрина), такой как мапротилин, лофепрамин, миртазапин, оксапротилин, фезоламин, томоксетин, миансерин, бупроприон, метаболит бупроприона гидроксибупроприон, номифензин и вилоксазин (ВиваланTM), в частности избирательный ингибитор обратного захвата норадреналина, такой как ребоксетин, в частности (S,S)-ребоксетин;
- двойной ингибитор обратного захвата серотонина-норадреналина, такой как венлафаксин, метаболит венлафаксина O-дезметилвенлафаксин, кломипрамин, метаболит кломипрамина дезметилкломипрамин, дулоксетин, милнаципран и имипрамин;
- ингибитор индуцибельной синтазы оксида азота(II) (iNOS), такой как S-[2-[(1-иминоэтил)амино]этил]-L-гомоцистеин, S-[2-[(1-иминоэтил)амино]этил]-4,4-диоксо-L-цистеин, S-[2-[(1-иминоэтил)амино]этил]-2-метил-L-цистеин, (2S,5Z)-2-амино-2-метил-7-[(1-иминоэтил)амино]-5-гептеновая кислота, 2-[[(1R,3S)-3-амино-4-гидрокси-1-(5-тиазолил)бутил]тио]-5-хлор-3-пиридинкарбонитрил; 2-[[(1R,3S)-3-амино-4-гидрокси-1-(5-тиазолил)бутил]тио]-4-хлорбензонитрил, (2S,4R)-2-амино-4-[[2-хлор-5-(трифторметил)фенил]тио]-5-тиазолбутанол, 2-[[(1R,3S)-3-амино-4-гидрокси-1-(5-тиазолил)бутил]тио]-6-(трифторметил)-3 пиридинкарбонитрил, 2-[[(1R,3S)-3-амино-4-гидрокси-1-(5-тиазолил)бутил]тио]-5-хлорбензонитрил, N-[4-[2-(3-хлорбензиламино)этил]фенил]тиофен-2-карбоксамидин или гуанидиноэтилдисульфид;
- ингибитор ацетилхолинэстеразы, такой как донепезил;
- антагонист простагландина E2 подтипа 4 (EP4), такой как N-[({2-[4-(2-этил-4,6-диметил-1H-имидазо[4,5-c]пиридин-1-ил)фенил]этил}амино)карбонил]-4-метилбензолсульфонамид или 4-[(1S)-1-({[5-хлор-2-(3-фторфенокси)пиридин-3-ил]карбонил}амино)этил]бензойная кислота;
- антагонист лейкотриена B4; такой как 1-(3-бифенил-4-илметил-4-гидроксихроман-7-ил)циклопентанкарбоновая кислота (CP-105696), 5-[2-(2-карбоксиэтил)-3-[6-(4-метоксифенил)-5E-гексенил]оксифенокси]валериановая кислота (ONO-4057) или DPC-11870,
- ингибитор 5-липоксигеназы, такой как зилейтон, 6-[(3-фтор-5-[4-метокси-3,4,5,6-тетрагидро-2H-пиран-4-ил])феноксиметил]-1-метил-2-хинолон (ZD-2138) или 2,3,5-триметил-6-(3-пиридилметил),1,4-бензохинон (CV-6504);
- блокатор натриевого канала, такой как лидокаин;
- блокатор кальциевого канала, такой как зиконотид, зонизамид, мибефрадил;
- 5-HT3 антагонист, такой как ондансетрон;
- химиотерапевтическое лекарственное средство, такое как оксалиплатин, 5-фторурацил, лейковорин, паклитаксел;
- антагонист пептида, связанного с геном кальцитонина (CGRP);
- антагонист брадикинина (BK1 и BK2);
- блокатор потенциал-зависимых натриевых каналов (NaV1.3, NaV1.7, Nav1,8);
- блокатор потенциал-зависимого кальциевого канала (N-типа, T-типа);
- антагонист P2X (рецептор ионного канала АТФ типа);
- антагонист чувствительного к кислоте ионного канала (ASIC1a, ASIC3);
- антагонист ангиотензина AT2;
- антагонист рецептора хемокина CCR2B;
- ингибитор катепсина (B, S, K);
- агонист или антагонист рецептора сигма1;
и их фармацевтически приемлемые соли и сольваты.
В терапии такие комбинации дают значительные преимущества, включая синергическую активность.
Фармацевтическую композицию по изобретению, которую можно получать смешиванием, соответственно, при температуре окружающей среды и атмосферном давлении, обычно адаптируют для перорального, парентерального или ректального введения, и, по существу, она может быть в форме таблеток, капсул, пероральных жидких препаратов, порошков, гранул, пастилок, восстанавливаемых порошков, инъецируемых или вливаемых растворов или суспензий или суппозиториев. Перорально вводимые композиции обычно являются предпочтительными. Таблетки и капсулы для перорального введения могут быть в форме стандартной дозы и могут содержать стандартные эксципиенты, такие как связывающие средства (например, прежелатинизированный кукурузный крахмал, поливинилпирролидон или гидроксипропилметилцеллюлоза); наполнители (например, лактоза, микрокристаллическая целлюлоза или вторичный кислый фосфат кальция); смазывающие средства для таблетирования (например, стеарат магния, тальк или диоксид кремния); разрыхлители (например, картофельный крахмал или крахмал гликолят натрия); и приемлемые увлажняющие средства (например, лаурилсульфат натрия). Таблетки можно покрывать в соответствии со способами, хорошо известными в обычной фармацевтической практике.
Пероральные жидкие препараты могут быть в форме, например, водной или масляной суспензии, растворов, эмульсий, сиропов или крепких настоев, или могут быть в форме сухого продукта для восстановления водой или другим подходящим наполнителем перед использованием. Такие жидкие препараты могут содержать стандартные добавки, такие как суспендирующие средства (например, сорбитовый сироп, производные целлюлозы или гидрогенизированные съедобные жиры), эмульгирующие средства (например, лецитин или камедь), неводные наполнители (которые могут включать съедобные масла, например, миндальное масло, маслянистые сложные эфиры, этиловый спирт или фракционированные растительные масла), консерванты (например, метил- или пропил-п-гидроксибензоаты или сорбиновая кислота), и, при желании, стандартные ароматизаторы или красящие вещества, буферные соли и подсластители, в зависимости от ситуации. Препараты для перорального введения можно соответствующим образом формулировать, чтобы обеспечивать контролируемое высвобождение активного соединения или его фармацевтически приемлемой соли.
Для парентерального введения текучие стандартные дозированные формы получают с использованием соединения формулы (I) или его фармацевтически приемлемой соли и стерильного наполнителя. Составы для инъекции можно представлять в стандартной дозированной форме, например, в ампулах или в множестве доз, с использованием соединения формулы (I) или его фармацевтически приемлемой соли и стерильного наполнителя, необязательно, с дополнительным консервантом. Композиции могут принимать такие формы, как суспензии, растворы или эмульсии в маслянистых или водных наполнителях, и могут содержать вспомогательные средства, такие как суспендирующие, стабилизирующие и/или диспергирующие средства. Альтернативно, активный ингредиент может быть в порошкообразной форме для разбавления перед использованием подходящим наполнителем, например, стерильной апирогенной водой. Соединение, в зависимости от используемых наполнителя и концентрации, можно или суспендировать или растворять в наполнителе. При получении растворов соединение можно растворять для инъекции и стерильно фильтровать перед заполнением подходящего сосуда или ампулы и закупориванием. Благоприятно, адъюванты, такие как местный анестетик, консерванты и буферные средства, растворяют в наполнителе. Чтобы повысить стабильность, после заполнения сосуда можно заморажитать композицию и под вакуумом удалять воду. Парентеральные суспензии получают по существу тем же образом, за исключением того, что вместо растворения соединение суспендируют в наполнителе и нельзя выполнять стерилизацию фильтрованием. Соединение можно стерилизовать посредством воздействия этиленоксидом перед суспензией в стерильном наполнителе. Благоприятно, поверхностно-активное вещество или увлажняющее средство включают в композицию для того, чтобы содействовать однородному распределению соединения.
С использованием водной или масляной основы можно формулировать лосьоны, и в целом они также будут содержать одно или несколько эмульгирующих средств, стабилизирующих средств, диспергирующих средств, суспендирующих средств, загустителей или красителей. С использованием водной или неводной основы можно формулировать капли, которые также содержат одно или несколько диспергирующих средств, стабилизирующих средств, растворителей или суспендирующих средств. Они также могут содержать консервант.
Соединения формулы (I) или их фармацевтически приемлемые соли также можно формулировать в ректальные композиции, такие как суппозитории или удерживающие клизмы, например, содержащие стандартные основы суппозиториев, такие как кокосовое масло или другие глицериды.
Соединения формулы (I) или фармацевтически приемлемые соли также можно формулировать в виде препаратов депо. Такие длительно действующие составы можно вводить посредством имплантации (например, подкожно или внутримышечно) или посредством внутримышечной инъекции. Таким образом, например, соединения формулы (I) или фармацевтически приемлемые соли можно формулировать с подходящими полимерными или гидрофобными материалами (например, в виде эмульсии в приемлемом масле) или ионообменными смолами, или в виде умеренно растворимых производных, например, в виде умеренно растворимой соли.
Для интраназального введения соединения формулы (I) или их фармацевтически приемлемые соли можно формулировать в виде растворов для введения через подходящее устройство отмеренных или стандартных доз или, альтернативно, в виде смеси порошка с подходящим носителем для введения с использованием подходящего устройства доставки. Таким образом, соединения формулы (I) или их фармацевтически приемлемые соли можно формулировать для перорального, трансбуккального, парентерального, топического (включая глазное и назальное), введения депо или ректального введения или в форме, подходящей для введения посредством ингаляции или инсуфляции (через рот или через нос). Соединения формулы (I) и их фармацевтически приемлемые соли можно формулировать для топического введения в форме мазей, кремов, гелей, лосьонов, пессариев, аэрозолей или капель (например, глазных, ушных или назальных капель). Мази и кремы можно формулировать, например, с использованием водной или масляной основы с добавлением подходящих загустителей и/или гелеобразующих средств. Мази для введения в глаз можно изготавливать стерильно с использованием стерилизованных компонентов.
Общий синтез
На всем протяжении данной заявки используют следующие сокращения в следующих значениях:
Термин «основание» аналогичным образом не накладывает конкретного ограничения на свойства используемых оснований, и любое основание, обычно используемое в реакциях этого типа, можно здесь использовать в равной мере. Примеры таких оснований включают, но не ограничиваясь этим: гидроксиды щелочных металлов, такие как гидроксид лития, гидроксид натрия, гидроксид калия, фосфат калия и гидроксид бария; гидриды щелочных металлов, такие как гидрид лития, гидрид натрия и гидрид калия; алкоксиды щелочных металлов, такие как метоксид натрия, этоксид натрия и трет-бутоксид калия; карбонаты щелочных металлов, такие как карбонат лития, карбонат натрия, карбонат калия и карбонат цезия; гидрокарбонаты щелочных металлов, такие как гидрокарбонат лития, гидрокарбонат натрия и гидрокарбонат калия; амины, такие как N-метилморфолин, триэтиламин, трипропиламин, трибутиламин, диизопропилэтиламин, N-метилпиперидин, пиридин, 4-пирролидинопиридин, пиколин, 2,6-ди(трет-бутил)-4-метилпиридин, хинолин, N,N-диметиланилин, N,N-диэтиланилин, 1,5-диазабицикло[4,3.0]нон-5-ен (DBN), 1,4-диазабицикло[2.2.2]октан (DABCO), 1,8-диазабицикло[5.4.0]ундец-7-ен (DBU), лутидин и колидин; амиды щелочных металлов, такие как амид лития, амид натрия, амид калия, диизопропиламид лития, диизопропиламид калия, диизопропиламид натрия, бис(триметилсилил)амид лития и бис(триметилсилил)амид калия. Среди них триэтиламин, диизопропилэтиламин, DBU, DBN, DABCO, пиридин, лутидин, колидин, карбонат натрия, гидрокарбонат натрия, гидроксид натрия, карбонат калия, гидрокарбонат калия, гидроксид калия, фосфат калия, гидроксид бария и карбонат цезия являются предпочтительными.
Реакции обычно и предпочтительно осуществляют в присутствии инертного растворителя. Нет конкретного ограничения свойств растворителя, подлежащего использованию, при условии, что он не оказывает нежелательного эффекта на реакцию или участвующие реактивы и что он может растворять реактивы, по меньшей мере, в определенной степени. Примеры подходящих растворителей включают, но не ограничиваясь этим: галогенированные углеводороды, такие как DCM, хлороформ, тетрахлорид углерода и дихлорэтан; простые эфиры, такие как диэтиловый эфир, диизопропиловый эфир, THF и диоксан; ароматические углеводороды, такие как бензол, толуол и нитробензол; амиды, такие как DMF, DMA и гексаметилфосфорный триамид; амины, такие как N-метилморфолин, триэтиламин, трипропиламин, трибутиламин, диизопропилэтиламин, N-метилпиперидин, пиридин, 4-пирролидинопиридин, N,N-диметиланилин и N,N-диэтиланилин; спирты, такие как метанол, этанол, пропанол, изопропанол и бутанол; нитрилы, такие как MeCN и бензонитрил; сульфоксиды, такие как диметилсульфоксид (DMSO) и сульфолан; кетоны, такие как ацетон и диэтилкетон. Среди этих растворителей, предпочтительные включают, но без ограничения, DMF, DMA, DMSO, THF, диэтиловый эфир, диизопропиловый эфир, диметоксиэтан, ацетонитрил, DCM, дихлорэтан и хлороформ.
Примеры
Изобретение проиллюстрировано в следующих неограничивающих примерах, в которых, если не установлено иное: все реактивы коммерчески доступны, все операции осуществляют при комнатной температуре или температуре окружающей среды, то есть в диапазоне приблизительно 18-25°C; испарение растворителя осуществляют с использованием роторного испарителя при пониженном давлении при температуре бани до приблизительно 60°C; мониторинг реакций осуществляют с помощью тонкослойной хроматографии (TLC), а времена реакций приведены только в качестве иллюстрации; структуру и чистоту всех выделенных соединений подтверждают с помощью по меньшей мере одного из следующих способов: TLC (пластины для TLC Merck, предварительно покрытые силикагелем 60 F254, или пластины для HPTLC Merck, предварительно покрытые NH2 F254), масс-спектрометрия или ЯМР. Выход приводят только для иллюстративных целей. Колоночную флэш-хроматографию осуществляют с использованием силикагеля 60 Merck (230-400 меш ASTM), Fuji Silysia Chromatorex (зарегистрированная торговая марка) DU3050 (Amino Type), Wako Wakogel C300-HG, диоксида кремния Biotage KP-Sil, колонки Yamazen Hi-FLASH, YMC DispoPack-SIL или аминосвязанного диоксида кремния Biotage KP-NH. Очистку соединений с использованием ВЭЖХ (препаративная LC-MS) осуществляют с помощью следующего аппарата и условий.
Аппарат: система Waters MS-trigger AutoPurification (торговая марка).
Колонка: Waters XTerra C18, 19×50 мм, частица 5 микрометров.
Условие A: MeOH или MeCN/0,01% (об./об.) водный раствор аммиака.
Условие B: MeOH или MeCN/0,05%(об./об.) водный раствор муравьиной кислоты.
Данные масс-спектрометрии низкого разрешения (ESI) получают с помощью следующего аппарата и условий: аппарат: система Waters Alliance HPLC на масс-спектрометре ZQ или ZMD и УФ-детектор. Данные ЯМР определяют при 270 МГц (спектрометр JEOL JNM-LA 270) или 300 МГц (JEOL JNM-LA300) с использованием дейтерированного хлороформа (99,8% D) или диметилсульфоксида (99,9% D) в качестве растворителя, если не указано иное, относительно тетраметилсилана (TMS) в качестве внутреннего стандарта в миллионных долях (м.д.); используемые стандартные сокращения: с = синглет, д = дублет, т = триплет, к = квартет, м = мультиплет,
ушир. = уширенный и т.д. Химические символы имеют свои обычные значения; M (моль(и) на литр), л (литр(ы)), мл (миллилитр(ы)), г (грамм(ы)), мг (миллиграмм(ы)), моль (моли), ммоль (миллимоли).
Каждое полученное соединение обычно называют в соответствии ChemBioDraw (Ultra, версия 12.0, CambridgeSoft).
Условия для определения времени удержания при ВЭЖХ:
Способ: QC1.
Аппарат: Waters ACQUITY Ultra Performance LC с TUV-детектором и масс-спектрометром ZQ.
Колонка: Waters ACQUITY C18, 2,1×100 мм, размер частицы 1,7 микрометра.
Температура колонки: 60°C.
Скорость потока: 0,7 мл/мин.
Время прохождения: 3 мин.
УФ обнаружение: 210 нм.
MS обнаружение: ESI положительный/отрицательный режим.
Подвижные фазы:
A1: 10 мМ ацетат аммония.
B1: MeCN.
Программа градиентов: (КК нейтральный полный 3 мин).
Способ: QC2.
Прибор: Waters 2795 Alliance ВЭЖХ с ZQ2000 масс-спектрометром и 2996 PDA.
Детектор
Колонка: XBridge C18, 2,1×50 мм, размер частиц 3,5 микрометра.
Температура колонки: 45°C.
Скорость потока: 1,2 мл/мин.
Продолжительность цикла: 4,5 мин.
УФ детектирование: 210-400 нм скан.
MS детектирование: ESI положительный/отрицательный режим.
Подвижные фазы:
A: вода.
10 B: MeCN.
C: 1% водный раствор HCOOH.
D: 1% водный раствор NH3.
Программа градиента:
Все из пиразолопиридиновых производных формулы (I) можно получить способами, описанными в общих способах, представленных ниже, или конкретными способами, описанными в части примеров получения и части получения промежуточных соединений, или их стандартными модификациями. Настоящее изобретение также включает любой один или более из данных способов получения пиразолопиридиновых производных формулы (I), в добавление к любым новым промежуточным соединениям, применяемым в настоящем изобретении.
В следующих общих способах, дескрипторы представляют собой, как определено ранее для пиразолопиридиновых производных формулы (I), если не указано иначе.
Схема A
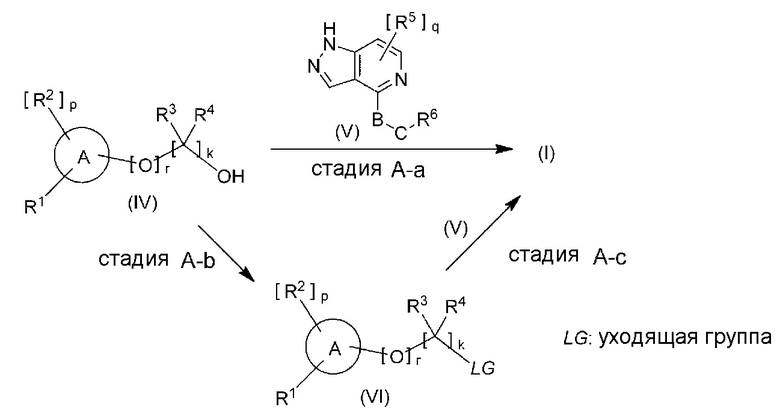
На стадии A-a, соединение формулы (I) можно получить из соединения формулы (IV) реакцией Мицунобу с соединением формулы (V), применяя подходящий реагент в органическом растворителе в присутствии конденсирующего реагента, такого как, но не ограничиваясь, диэтилазодикарбоксилат/трифенилфосфин, диизопропилазодикарбоксилат/трифенилфосфин, ди-трет-бутилазодикарбоксилат/трифенилфосфин и цианометилентрибутилфосфоран.
Примеры подходящего органического растворителя включают растворители, такие как THF, 1,4-диоксан, DMF, MeCN и толуол. Реакцию можно проводить при температуре от приблизительно -20 до 180°C, более предпочтительно от приблизительно 20 до 150°C. Продолжительность реакции в общем составляет от приблизительно 30 минут до 48 часов, более предпочтительно от приблизительно 30 минут до 24 часов.
Когда LG представляет собой группу, такую как O-трифторметансульфонат, O-тозилат, O-мезилат, йодид, бромид и хлорид, на стадии A-b, соединение формулы (VI) можно получить сульфонилированием или замещением галогеном соединения формулы (IV), например, в известных условиях сульфонилирования или известных условиях галогенирования в инертном растворителе. В случае сульфонилирования, реакцию можно проводить в присутствии основания в инертном растворителе. Предпочтительное основание выбрано из, например, но не ограничиваясь: гидроксида, алкоксида, карбоната, галогенида или гидрида щелочного или щелочноземельного металла, такого как гидроксид натрия, гидроксид калия, метоксид натрия, этоксид натрия, трет-бутоксид калия, карбонат натрия, карбонат калия, фторид калия, гидрид натрия или гидрид калия; или амина, такого как TEA, трибутиламин, диизопропилэтиламин, 2,6-лутидин, пиридин или диметиламинопиридин. Примеры подходящих инертных водных или неводных органических растворителей включают: спирты, такие как метанол или этанол; эфиры, такие как THF или 1,4-диоксан; ацетон; DMF; галогенированные углеводороды, такие как DCM, 1,2-дихлорэтан или хлороформ; и пиридин; или их смеси. Реакцию можно проводить при температуре в диапазоне от приблизительно -10°C до 200°C, предпочтительно в диапазоне от приблизительно 20 до 100°C. Продолжительность реакции обычно составляет от приблизительно 10 минут до 4 дней, предпочтительно от приблизительно 10 минут до 24 часов. В случае галогенирования, примером источника галогена является источник, такой как тионилхлорид, N-бромсукцинимид, N-хлорсукцинимид, йод, бром, трихлорид фосфора, трибромид фосфора, тетрахлорид углерода или тетрабромид углерода. В случае реакции галогенирования, реакцию можно проводить в присутствии восстанавливающего реагента, такого как трифенилфосфин. Примеры подходящего органического растворителя включают растворители, такие как THF, 1,4-диоксан, DCM, 1,2-дихлорэтан, тетрахлорид углерода, толуол и DMF.
На стадии A-c, соединение формулы (I) можно получить из соединения формулы (VI) и формулы (V) в присутствии подходящего основания в инертном растворителе. Примеры подходящего основания включают, но не ограничиваются, основания, такие как гидрид натрия, карбонат калия, бикарбонат калия, карбонат цезия, карбонат натрия, бикарбонат натрия, фосфат трикалия, трет-бутоксид калия, триэтиламин, N,N-диизопропилэтиламин и дициклогексиламин. Примеры подходящего органического растворителя включают растворители, такие как THF, 1,4-диоксан, DMF, MeCN, DMA и толуол. Реакцию можно проводить при температуре от приблизительно -20 до 150°C, более предпочтительно от приблизительно 0 до 100°C. Продолжительность реакции в общем составляет от приблизительно 30 минут до 48 часов, более предпочтительно от приблизительно 30 минут до 24 часов.
Схема B
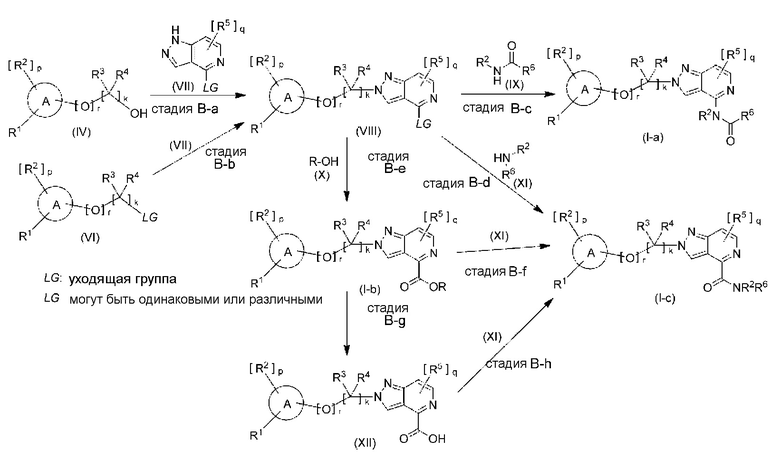
На стадии B-a, соединение формулы (VIII) можно получить из соединения формулы (IV) и соединения формулы (VII) реакцией Мицунобу, как описано на стадии A-a.
На стадии B-b, соединение формулы (VIII) можно получить из соединения формулы (VI) и соединения формулы (VII), как описано на стадии A-c.
Когда -B-C-R6 компонента формулы (I) представляет собой -NHR2-(C=O)-R6, на стадии B-c, соединение (I-a) можно получить конденсацией формулы (VIII) с подходящим реагентом формулы (IX) в условиях конденсации в подходящих органических растворителях в присутствии подходящего катализатора, содержащего переходный металл, и в присутствии или отсутствии основания. Примеры подходящих катализаторов, содержащих переходный металл, включают, но не ограничиваются: тетракис(трифенилфосфин)палладий(0), хлорид бис(трифенилфосфин)палладия(II), медь (0), ацетат меди (I), бромид меди (I), хлорид меди (I), йодид меди(I), оксид меди (I), трифторметансульфонат меди (II), ацетат меди (II), бромид меди (II), хлорид меди(II), йодид меди (II), оксид меди (II), трифторметансульфонат меди (II), ацетат палладия (II), хлорид палладия (II), бис(ацетонитрил)дихлорпалладий (II), бис(дибензилиденацетон)палладий (0), трис(дибензилиденацетон)дипалладий (0) и дихлорид [1,1'-бис(дифенилфосфино)ферроцен]палладия (II). Предпочтительные катализаторы представляют собой тетракис(трифенилфосфин)палладий (0), хлорид бис(трифенилфосфин)палладия (II), ацетат палладия(II), хлорид палладия (II), бис(ацетонитрил)дихлорпалладий (0), бис(дибензилиденацетон)палладий (0), трис(дибензилиденацетон)дипалладий (0) и дихлорид [1,1-бис(дифенилфосфино)ферроцен]палладия (II). Примеры подходящего карбоксамида, представленного формулой (IX), включают, но не ограничиваются, карбоксамиды, такие как ацетамид, пропионамид, изобутирамид и циклопропанкарбоксамид. Примеры подходящего органического растворителя включают: THF; 1,4-диоксан; DMF; MeCN; спирты, такие как метанол или этанол; галогенированные углеводороды, такие как DCM, 1,2-дихлорэтан, хлороформ или тетрахлорид углерода; и диэтиловый эфир; в присутствии или отсутствии основания, такого как фосфат трикалия, бикарбонат натрия, карбонат натрия или карбонат калия. Данную реакцию можно проводить в присутствии подходящей добавки.
Примеры данной добавки включают, но не ограничиваются: 4,5-бис(дифенилфосфино)-9,9-диметилксантен, трифенилфосфин, три-трет-бутилфосфин, 1,1'-бис(дифенилфосфино)ферроцен, три-2-фурилфосфин, три-o-толилфосфин, 2-(дихлоргексилфосфино)бифенил и трифениларсин. Реакцию можно проводить при температуре от приблизительно 50 до 200°C, более предпочтительно от приблизительно 80 до 150°C. Продолжительность реакции обычно составляет от приблизительно 5 минут до 48 часов, более предпочтительно от приблизительно 30 минут до 24 часов.
В альтернативном случае реакцию можно проводить в микроволновой системе. Реакцию можно проводить при температуре в диапазоне от приблизительно 100 до 200°C, предпочтительно в диапазоне от приблизительно 120 до 180°C. Продолжительность реакции обычно составляет от приблизительно 10 минут до 3 часов, предпочтительно от приблизительно 15 минут до 1 часа.
Когда -B-C-R6 компонента формулы (I) представляет собой -(C=O)-NR2R6 на стадии B-d соединение (I-c) можно получить из соединения формулы (VIII) и соединения формулы (XI) реакцией внедрения CO в подходящих органических растворителях в присутствии подходящего катализатора, содержащего переходный металл, в присутствии или отсутствии основания в атмосфере монооксида углерода.
Пример подходящих катализаторов, содержащих переходный металл, включает, но не ограничивается: металлический палладий, палладий-углерод, ацетат палладия (II), трис(дибензилиденацетон)дипалладий-хлороформ, дихлорид [1,2-бис(дифенилфосфино)этан]палладия, дихлорид бис(три-o-толуилфосфин)палладия, дихлорид бис(трифенилфосфин)палладия, тетракис(трифенилфосфин)палладий, дихлор[1,1'-бис(дифенилфосфино)ферроцен]палладий или катализатор, полученный в растворе добавлением лиганда в данный реакционный раствор. Лиганд, добавляемый в реакционный раствор, может представлять собой содержащий фосфор лиганд, такой как 1,1'-бис(дифенилфосфино)ферроцен, бис(2-дифенилфосфинофениловый)эфир, 2,2'-бис(дифенилфосфино)-1,1'-бинафтор, 1,3-бис(дифенилфосфино)пропан, 1,4-бис(дифенилфосфино)бутан, три-о-толуилфосфин, трифенилфосфин, 2-дифенилфосфино-2'-метокси-1,1'-бинафтил или 2,2-бис(дифенилфосфино)-1,1'-бинафтил. Примеры подходящего органического растворителя включают: THF; 1,4-диоксан; DMF; DMA; MeCN; толуол; галогенированные углеводороды, такие как DCM, 1,2-дихлорэтан, хлороформ или тетрахлорид углерода; и диэтиловый эфир; в присутствии или отсутствии основания, такого как триэтиламин, N,N-диизопропилэтиламин, фосфат трикалия, бикарбонат натрия, карбонат натрия или карбонат калия. Данную реакцию можно проводить в присутствии подходящей добавки. Примеры данных добавок включают: 4,5-бис(дифенилфосфино)-9,9-диметилксантен, трифенилфосфин, три-трет-бутилфосфин, 1,1'-бис(дифенилфосфино)ферроцен, три-2-фурилфосфин, три-o-толилфосфин, 2-(дихлоргексилфосфино)бифенил и трифениларсин. Реакцию можно проводить при температуре от приблизительно 50 до 200°C, более предпочтительно от приблизительно 60 до 150°C. Продолжительность реакции обычно составляет от приблизительно 5 минут до 48 часов, более предпочтительно от приблизительно 30 минут до 24 часов. Вместо монооксида углерода, можно применять другие источники монооксида углерода, такие как гексакарбонил молибдена и DMF/трет-бутоксид калия.
В альтернативном случае реакцию можно проводить в микроволновой системе. Реакцию можно проводить при температуре в диапазоне от приблизительно 100 до 200°C, предпочтительно в диапазоне от приблизительно 120 до 180°C. Продолжительность реакции обычно составляет от приблизительно 10 минут до 3 часов, предпочтительно от приблизительно 15 минут до 1 часа.
На стадии B-e, соединение формулы (I-b) можно получить из соединения формулы (VIII) и спирта формулы (X) реакцией внедрения CO, как описано на стадии B-d.
Альтернативно, реакцию можно проводить с другим источником монооксида углерода, таким как фенилформиат/триэтиламин и гексакарбонил молибдена.
На стадии B-f, соединение формулы (I-c) можно получить из соединения формулы (I-b) и формулы (XI) в подходящих растворителях. Примеры подходящих растворителей включают, но не ограничиваются: THF, 1,4-диоксан, DMF, MeCN, MeOH, EtOH и воду. Реакцию можно осуществлять при температуре от приблизительно 0 до 200°C, более предпочтительно от приблизительно 20 до 150°C. Продолжительность реакции обычно составляет от приблизительно 5 минут до 48 часов, более предпочтительно от приблизительно 30 минут до 24 часов.
На стадии B-g, соединение формулы (XII) можно получить гидролизом эфирного соединения формулы (I-b). Гидролиз можно проводить общепринятыми способами. В стандартном способе гидролиз осуществляют в основных условиях, например, в присутствии гидроксида натрия, гидроксида калия или гидроксида лития. Подходящие растворители включают, например, но не ограничиваются: воду, спирты, такие как метанол, этанол, пропанол, бутанол, 2-метоксиэтанол и этиленгликоль; эфиры, такие как THF, DME и 1,4-диоксан; амиды, такие как DMF и триамид гексаметилфосфорной кислоты; и сульфоксиды, такие как DMSO. Предпочтительные растворители представляют собой воду, метанол, этанол, пропанол, THF, DME, 1,4-диоксан, DMF и DMSO. Данную реакцию можно проводить при температуре в диапазоне от приблизительно 20 до 100°C в течение от приблизительно 30 минут до 24 часов.
На стадии B-h, соединение формулы (I-c) можно получить из соединения формулы (XII) амидированием соединением формулы (XI), применяя подходящий конденсирующий агент, такой как HBTU и EDC-HOBT, предпочтительно в присутствии основания, такого как триэтиламин и N,N-диизопропилэтиламин, в подходящем растворителе, таком как DMF, DMA и DCM, при температуре от приблизительно 5 до 60°C в течение приблизительно 1-24 часов. Кроме того, соединение формулы (I-c) можно также получить из соединения формулы (III) амидированием галогенангидридом карбоновой кислоты, полученной из соединения формулы (XII), применяя тионилхлорид или оксалилхлорид, предпочтительно в присутствии основания, такого как триэтиламин, пиридин и N,N-диизопропилэтиламин, в подходящем растворителе, таком как DCM, при температуре от приблизительно 5 до 40°C в течение приблизительно 1-24 часов.
Схема C
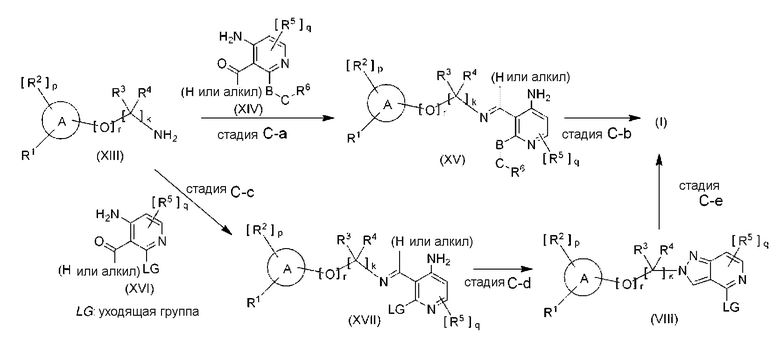
На стадии C-a, соединение формулы (XV) можно получить из амина формулы (XIII) и соединения формулы (XIV) в подходящих растворителях, таких как толуол, THF, диоксан, диэтиловый эфир, DCM, 1,2-дихлорэтан, хлороформ, гексан, MeOH и EtOH. Реакцию можно осуществлять в присутствии подходящей добавки. Примеры данных добавок включают, но не ограничиваются, изопропоксид титана (IV), этоксид титана (IV), молекулярные сита, сульфат магния, сульфат меди (II), хлористоводородную кислоту, уксусную кислоту, п-толуолсульфокислоту, трифторметансульфокислоту и 10-камфорсульфокислоту. Данную реакцию можно проводить при температуре в диапазоне от приблизительно 0 до 150°C в течение от приблизительно 30 минут до 48 часов.
На стадии C-b, соединение формулы (I) можно получить из соединения формулы (XV) в присутствии подходящего реагента, такого как триэтилфосфит и диацетат йодбензола, в инертном растворителе или без растворителя. Предпочтительный растворитель выбран из DMF, DMA, MeOH, EtOH, DCM, 1,2-дихлорэтана и толуола. Данную реакцию можно проводить при температуре в диапазоне от приблизительно 0 до 150°C в течение от приблизительно 30 минут до 48 часов.
На стадии C-c, соединение формулы (XVII) можно получить из соединения формулы (XIII) и соединения формулы (XVI), как описано на стадии C-a.
На стадии C-d, соединение формулы (VIII) можно получить из соединения формулы (XVII), как описано на стадии C-b.
На стадии C-e, соединение формулы (I) можно получить из соединения формулы (VIII) способом, аналогичным B-c, B-d, B-e, B-f, B-g и B-h на схеме B.
Схема D
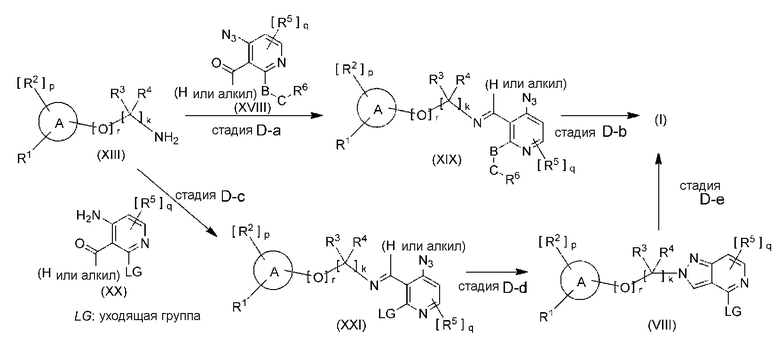
На стадии D-a, соединение формулы (XIX) можно получить из соединения формулы (XIII) и соединения формулы (XVIII), как описано на стадии C-a.
На стадии D-b, соединение формулы (I) можно получить из соединения формулы (XIX) с или без подходящей добавки в подходящем растворителе. Примеры подходящей добавки включают, но не ограничиваются, добавки, такие как йодид меди(I)/N,N,N',N'-тетраметилэтилендиамин.
Примеры подходящего растворителя включают, но не ограничиваются, растворители, такие как толуол, 1,2-дихлорбензол, DMF, DMA, THF, 1,4-диоксан, DCM и 1,2-дихлорэтан. Реакцию можно проводить при температуре от приблизительно 20 до 180°C. Продолжительность реакции обычно составляет от приблизительно 30 минут до 48 часов.
На стадии D-c, соединение формулы (XXI) можно получить из соединения формулы (XIII) и соединения формулы (XX), как описано на стадии C-a.
На стадии D-d, соединение формулы (VIII) можно получить из соединения формулы (XXI), как описано на стадии D-b.
На стадии D-e, соединение формулы (I) можно получить из соединения формулы (VIII) способом, аналогичным B-c, B-d, B-e, B-f, B-g и B-h на схеме B.
Схема E
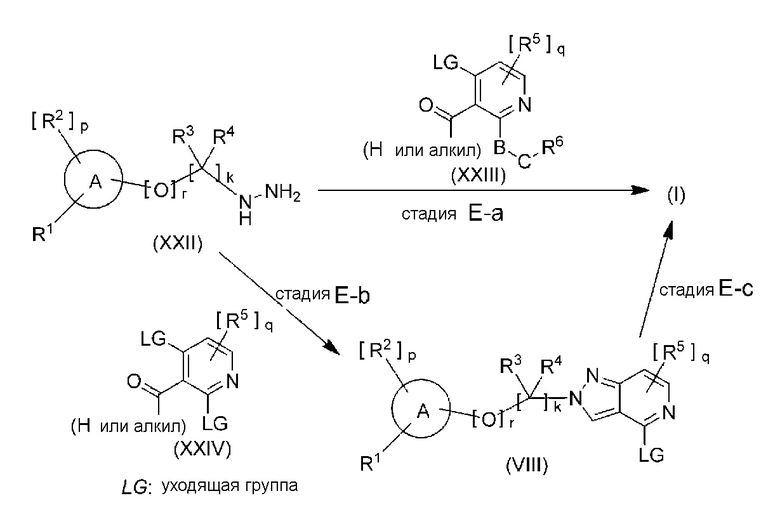
На стадии E-a, соединение формулы (I) можно получить из соединения формулы (XXII) и соединения формулы (XXIII) в подходящем органическом растворителе. Примеры подходящего органического растворителя включают, но не ограничиваются, растворители, такие как MeOH, EtOH, толуол, THF, 1,4-диоксан, DMF, MeCN, 1,2-дихлорэтан и толуол. Реакцию можно осуществлять при температуре от приблизительно 20 до 180°C, более предпочтительно от приблизительно 50 до 150°C. Продолжительность реакции обычно составляет от приблизительно 30 минут до 48 часов, более предпочтительно от приблизительно 30 минут до 24 часов.
На стадии E-b, соединение формулы (VIII) можно получить из соединения формулы (XXII) и соединения формулы (XXIV), как описано на стадии E-a.
На стадии E-c, соединение формулы (I) можно получить из соединения формулы (VIII) способом, аналогичным B-c, B-d, B-e, B-f, B-g и B-h на схеме B.
Ключевые промежуточные амины формулы (XIII) можно получить следующим общим путем получения схемы F и G.
Схема F
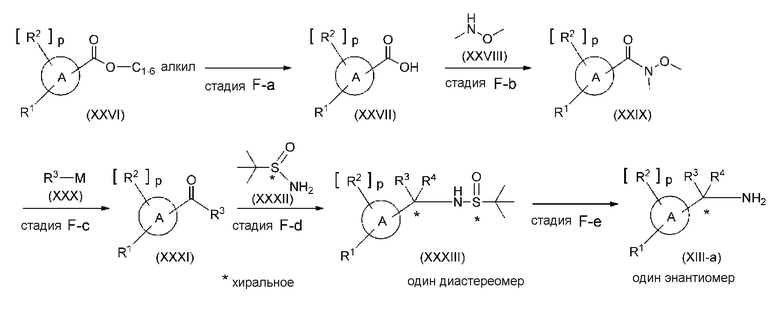
Когда -(O)r-(CR3R4)k-NH2 компонента формулы (XIII) представляет собой -(CR3R4)-NH2, соединение формулы (XIII-a) можно получить согласно схеме F и G.
На стадии F-a, соединение формулы (XXVII) можно получить гидролизом эфирного соединения формулы (XXVI), как описано на стадии B-g.
На стадии F-b, соединение формулы (XXIX) можно получить из кислоты формулы (XXVII) и N,O-диметилгидроксиламина (XXVIII) амидированием (образование амида Вейнреба), как описано на стадии B-h.
На стадии F-c, соединение формулы (XXXI) можно получить из соединения формулы (XXIX) обработкой подходящим алкилметаллическим реагентом (XXX) в инертном растворителе.
Примеры подходящего алкилметаллического реагента включают, но не ограничиваются, реагенты, такие как метиллитий, этиллитий, хлорид метилмагния, бромид метилмагния и йодид метилмагния. Примеры инертного растворителя включают, но не ограничиваются, растворители, такие как THF, диэтиловый эфир, DME и 1,4-диоксан. Реакцию можно проводить при температуре от приблизительно -40 до 100°C, более предпочтительно от приблизительно 0 до 50°C. Продолжительность реакции обычно составляет от приблизительно 5 минут до 48 часов, более предпочтительно от приблизительно 30 минут до 24 часов.
На стадии F-d, соединение формулы (XXXIII) можно получить в виде одного диастереомера из карбонильного соединения формулы (XXXI) и хирального трет-бутансульфинамида (XXXII) общепринятыми способами, известными специалисту в данной области техники (Pure Appl. Chem., 75, 39-46, 2003; Tetrahedron Lett., 45, 6641-6643, 2004). В следующих разделах промежуточных соединений и примеров, название соединения формулы (XXXIII) описано как (R) или (S) изомер, которое представляет собой конфигурацию атома серы.
На стадии F-e, соединение формулы (XIII-a) можно получить в виде одного энантиомеры из соединения формулы (XXXIII) обработкой в кислых условиях общепринятыми способами, известными специалисту в данной области техники (Pure Appl. Chem., 75, 39-46, 2003; Tetrahedron Lett., 45, 6641-6643, 2004).
Схема G
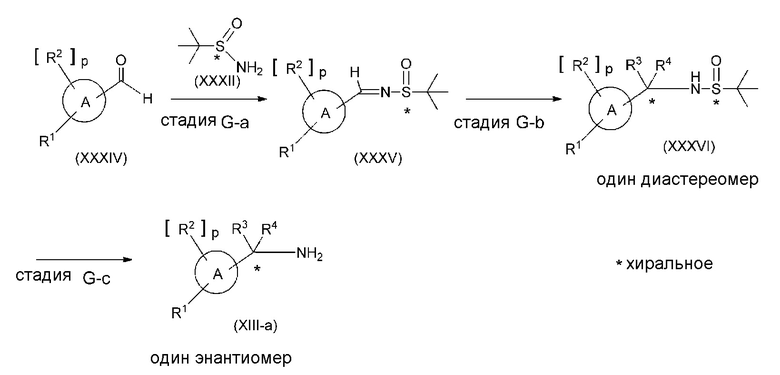
На стадии G-a, соединение формулы (XXXV) можно получить из альдегида формулы (XXXIV) и хирального трет-бутансульфинамида (XXXII) общепринятыми способами, известными специалисту в данной области техники (Pure Appl. Chem., 75, 39-46, 2003; Tetrahedron Lett., 45, 6641-6643, 2004).
На стадии G-b, соединение (XXXVI) можно получить в виде одного диастереомера из хирального сульфинилимина формулы (XXXV) и алкилметаллического реагента или гидридного реагента общепринятыми способами, известными специалисту в данной области техники (Pure Appl. Chem., 75, 39-46, 2003; Tetrahedron Lett., 45, 6641-6643, 2004). В следующих разделах промежуточных соединений и примеров, название соединения формулы (XXXVI) описано как (R) или (S) изомер, которое представляет собой конфигурацию атома серы.
На стадии G-c, соединение формулы (XIII-a) можно получить в виде одного энантимера из соединения формулы (XXXVI) обработкой в кислых условиях общепринятыми способами, известными специалисту в данной области техники (Pure Appl. Chem., 75, 39-46, 2003; Tetrahedron Lett., 45, 6641-6643, 2004).
Когда -(O)r-(CR3R4)k-OH компонента ключевых промежуточных спиртов формулы (IV) представляет собой -(CR3R4)-OH, соединение формулы (IV-a) можно получить следующим общим способом получения схемы H.
Ключевые промежуточные спирты формулы (IV-a) можно получить следующим общим способом получения схемы H.
Схема H
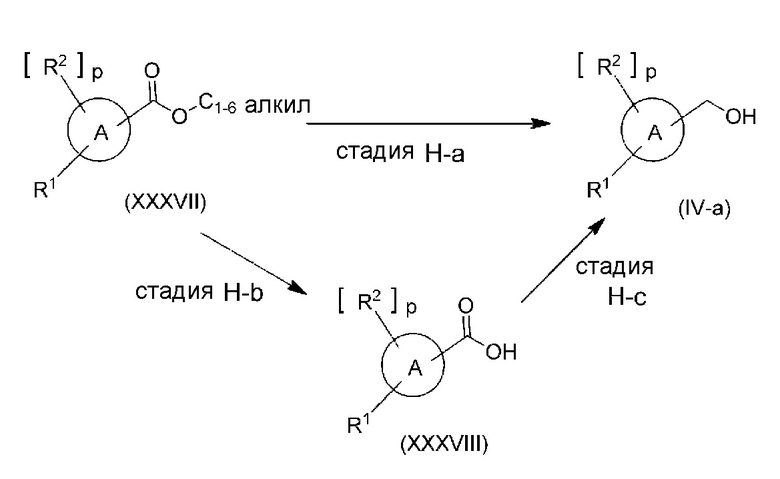
На стадии H-a, соединение формулы (IV-a) можно получить восстановлением соединения формулы (XXXVII). Восстановление можно осуществлять в присутствии подходящего восстанавливающего реагента в инертном растворителе или без растворителя. Предпочтительный восстанавливающий агент выбран из, например, но не ограничиваясь, агентов, таких как боргидрид натрия, литийалюмогидрид, боргидрид лития, борановый комплекс и диизобутилалюмогидрид. Температуры реакции обычно находятся в диапазоне от приблизительно -78 до 100°C, предпочтительно в диапазоне от приблизительно -70 до 60°C. Продолжительность реакции обычно составляет от приблизительно 30 минут до одного дня.
Примеры подходящих растворителей включают, но не ограничиваются: THF; 1,4-диоксан; DMF; MeCN; спирты, такие как MeOH или EtOH, и галогенированные углеводороды, такие как DCM, 1,2-дихлорэтан, хлороформ или тетрахлорид углерода.
На стадии H-b, соединение формулы (XXXVIII) можно получить гидролизом эфирного соединения формулы (XXXVII), как описано на стадии B-g.
На стадии H-c, соединение формулы (IV-a) можно получить восстановлением карбоновой кислоты формулы (XXXVIII), как описано на стадии H-a.
Ключевой промежуточный пиразолопиридин формулы (V) и (VII) можно получить следующим общим способом получения схемы J.
Схема J
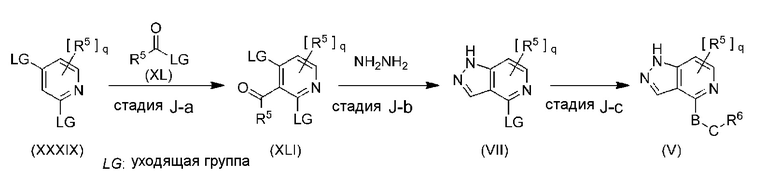
На стадии J-a, соединение формулы (XLI) можно получить металлированием соединения формулы (XXXIX) и захватом карбонильным соединением формулы (XL). Металлирование можно осуществлять в присутствии основания, такого как н-бутиллитий, втор-бутиллитий, трет-бутиллитий и диизопропиламид лития. Примеры карбонильного соединения формулы (XL) включают, но не ограничиваются, соединения, такие как DMF, ацетилхлорид, пропионилхлорид и бензоилхлорид.
Примеры подходящего органического растворителя включают растворители, такие как THF, диэтиловый эфир, 1,4-диоксан и гексан. Реакцию можно проводить при температуре от приблизительно -78 до 20°C.
Продолжительность реакции обычно составляет от приблизительно 30 минут до 24 часов.
На стадии J-b, соединение формулы (VII) можно получить из карбонильного соединения формулы (XLI) и гидразина, как описано на стадии E-a.
На стадии J-c, соединение формулы (V) можно получить из соединения формулы (VII) способом, аналогичным B-c, B-d, B-e, B-f, B-g и B-h на схеме B.
Ключевые промежуточные формулы (XVI) можно получить следующим общим способом получения схемы K.
Схема K
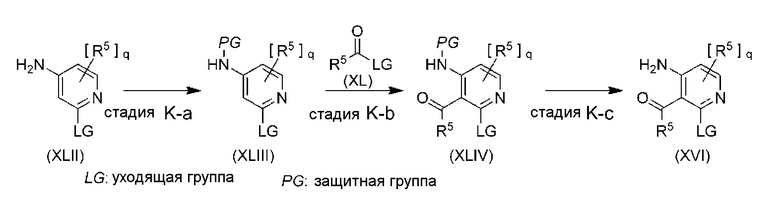
На стадии K-a, защитную группу можно ввести общепринятыми способами, известными специалисту в данной области техники (стандартные амино защитные группы описаны в "Protective Groups in Organic Synthesis Forth Edition" под редакцией T. W. Greene et al. (John Wiley & Sons, 2007)).
На стадии K-b, соединение формулы (XLIV) можно получить из соединения формулы (XLIII) и соединения формулы (XL), как описано на стадии J-a.
На стадии K-c, соединение формулы (XVI) можно получить деблокированием соединения формулы (XLIV) общепринятыми способами, известными специалисту в данной области техники (стандартные амино защитные группы описаны в "Protective Groups in Organic Synthesis Forth Edition" под редакцией T. W. Greene et al. (John Wiley & Sons, 2007)).
Все исходные соединения и промежуточные соединения в следующих синтезах могут быть имеющимися в продаже, или их можно получить общепринятыми способами, известными специалисту в данной области техники, иначе указано в части получения промежуточных соединений.
Часть получения промежуточных соединений
Промежуточные соединения получали следующим образом.
Промежуточное соединение-A1: (5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метанол
Стадия-1: 5-метил-6-(2,2,2-трифторэтокси)никотиновая кислота
К перемешиваемой смеси гидрида натрия (9,28 г, 232 ммоль, 60% в масле, промытого гексаном перед применением) в DMA (60 мл) добавляли 2,2,2-трифторэтанол (6,68 мл, 93 ммоль) при 0°C и перемешивали при комнатной температуре в течение 20 минут. К смеси добавляли раствор 6-фтор-5-метилникотиновой кислоты (12,0 г, 77 ммоль) в DMA (160 мл) при комнатной температуре, и полученную в результате смесь перемешивали при 70°C в течение 6 часов и продолжали перемешивание при комнатной температуре в течение ночи. Реакционную смесь разбавляли водой (800 мл) и подкисляли добавлением 2 M хлористоводородной кислоты. Белый осадок собирали фильтрованием, промывали водой и гексаном, и сушили в вакууме при 50°C в течение 3 часов, получая 15,1 г (83% выход) заявленного в заголовке соединения в виде белого твердого остатка.
Символ «δ» далее обозначен как «дельта».
1H-ЯМР (300 MГц, CDCl3) дельта 8,72 (1H, с), 8,10 (1H, с), 4,84 (2H, к, J=8,8 Гц), 2,30 (3H, с) (сигнал COOH не наблюдали), MS (ESI) m/z: 234 (M-H)-.
Стадия-2: (5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метанол
К перемешиваемому раствору 5-метил-6-(2,2,2-трифторэтокси)никотиновой кислоты (15,0 г, 63,8 ммоль, стадия-1) в THF (120 мл) добавляли порциями алюмогидрид лития (3,20 г, 84 ммоль) при 0°C. Реакционную смесь перемешивали при комнатной температуре в течение 2 часов. Реакционную смесь гасили насыщенным водным раствором хлорида аммония при 0°C. Полученную в результате суспензию фильтровали через слой целита и промывали EtOAc (100 мл×4). Объединенный фильтрат промывали водой и соляным раствором, сушили над сульфатом натрия, затем фильтровали и концентрировали, получая 13,51 г (96% выход) заявленного в заголовке соединения в виде бледно-желтого твердого остатка.
1H-ЯМР (300 MГц, CDCl3) дельта 7,93 (1H, с), 7,51 (1H, с), 4,76 (2H, к, J=8,8 Гц), 4,63 (2H, ушир.), 2,24 (3H, с) (сигнал COOH не наблюдали)
Промежуточное соединение-A2: (6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метанол
Стадия-1: 6-(2,2-дифторэтокси)-5-метилникотиновая кислота
Заявленное в заголовке соединение получали с выходом 94% (6,57 г, белый твердый остаток) из 6-фтор-5-метилникотиновой кислоты (5,00 г, 32,2 ммоль) и 2,2-дифторэтанола (5,29 г, 64,5 ммоль) способом, аналогичным стадии-1 промежуточного соединения-A1.
1H-ЯМР (300 MГц, DMSO-d6) дельта 13,09 (1H, ушир. с), 8,56 (1H, д, J=2,2 Гц), 8,07 (1H, д, J=2,2 Гц), 6,42 (1H, тт, J=54,3, 3,7 Гц), 4,66 (2H, тд, J=14,7, 3,7 Гц), 2,21 (3H, с), MS (ESI) m/z: 218 (M+H)+.
Стадия-2: метил 6-(2,2-дифторэтокси)-5-метилникотинат
К смеси 6-(2,2-дифторэтокси)-5-метилникотиновой кислоты (3,19 г, 14,7 ммоль, стадия-1) и карбонату калия (4,06 г, 29,4 ммоль) в DMF (37 мл) добавляли йодметан (1,4 мл, 22 ммоль), и смесь перемешивали при комнатной температуре в течение 1 часа. Смесь выливали в воду (300 мл), и водный слой экстрагировали EtOAc (300 мл). Отделенный органический слой промывали водой (100 мл), сушили над сульфатом натрия и концентрировали в вакууме.
Остаток очищали хроматографией на силикагеле, элюируя н-гексаном/EtOAc (10:1-4:1), получая 2,99 г (88% выход) заявленного в заголовке соединения в виде белого твердого остатка.
1H-ЯМР (300 MГц, CDCl3) дельта 8,64 (1H, д, J=1,8 Гц), 8,03 (1H, д, J=1,8 Гц), 6,15 (1H, тт, J=55,8, 4,4 Гц), 4,61 (2H, тд, J=13,2, 4,4 Гц), 3,91 (3H, с), 2,25 (3H, с), MS (ESI) m/z: 232 (M+H)+.
Стадия-3: (6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метанол
Заявленное в заголовке соединение получали с количественным выходом (2,62 г, бесцветное масло) из метил 6-(2,2-дифторэтокси)-5-метилникотината (2,99 г, 12,9 ммоль, стадия-2) способом, аналогичным стадии-2 промежуточного соединения-A1.
1H-ЯМР (300 MГц, CDCl3) дельта 7,92 (1H, д, J=1,8 Гц), 7,48 (1H, д, J=1,8 Гц), 6,14 (1H, тт, J=55,8, 4,0 Гц), 4,62-4,49 (4H, м), 2,22 (3H, с), 1,80 (1H, т, J=5,9 Гц), MS (ESI) m/z: 204 (M+H)+.
Промежуточное соединение-A3: (5-хлор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метанол
Стадия-1: 5-хлор-6-(2,2,2-трифторэтокси)никотиновая кислота
К суспензии гидрида натрия (5,00 г, 60% в масле, 125 ммоль) в DMA добавляли 2,2,2-трифторэтанол (5,8 мл, 94 ммоль) при 0°C. После перемешивания при 0°C в течение 20 минут к смеси добавляли 5,6-дихлорникотиновую кислоту (12,0 г, 62,5 ммоль), и ее перемешивали при 90°C в течение 2 часов. После охлаждения до комнатной температуры, смесь выливали в 0,3 M хлористоводородную кислоту (700 мл). Образовавшийся белый осадок собирали фильтрованием и промывали водой и гексаном, получая 16,6 г (количественный выход) заявленного в заголовке соединения в виде белого твердого остатка. Его применяли в следующей стадии без дополнительной очистки.
1H-ЯМР (300 MГц, DMSO-d6) дельта 8,66 (1H, д, J=2,2 Гц), 8,32 (1H, д, J=2,2 Гц), 5,15 (2H, к, J=8,8 Гц), MS (ESI) m/z: 256 (M+H)+.
Стадия-2: (5-хлор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метанол
К перемешиваемому раствору 5-хлор-6-(2,2,2-трифторэтокси)никотиновой кислоты (5,00 г, 19,5 ммоль, стадия-1) в THF (50 мл) добавляли N,N'-карбонилдиимидазол (4,76 г, 29,3 ммоль) при комнатной температуре. После перемешивания при комнатной температуре в течение 2 часов, медленно добавляли к смеси раствор боргидрида натрия (3,70 г, 98,0 ммоль) в воде (50 мл) при 0°C. После перемешивания при 0°C в течение 15 минут, добавляли к смеси при 0°C 2 M хлористоводородную кислоту (50 мл). Через 30 минут смесь аккуратно выливали в насыщенный раствор бикарбоната натрия (100 мл). Ее экстрагировали EtOAc (200 мл), и органический слой сушили над сульфатом натрия. После удаления органического растворителя, остаток очищали колоночной хроматографией на силикагеле, элюируя н-гексаном/EtOAc (2:1), получая 4,63 г (98% выход) заявленного в заголовке соединения в виде бледно-желтого твердого остатка.
1H-ЯМР (300 MГц, CDCl3) дельта 8,00 (1H, д, J=2,2 Гц), 7,76 (1H, д, J=2,2 Гц), 4,82 (2H, к, J=8,8 Гц), 4,66 (2H, с), MS (ESI) m/z: 242 (M+H)+.
Промежуточное соединение-A4: (5-хлор-6-(2,2-дифторэтокси)пиридин-3-ил)метанол
Стадия-1: 5-хлор-6-(2,2-дифторэтокси)никотиновая кислота
Заявленное в заголовке соединение получали с выходом 83% (4,12 г, белый твердый остаток) из 5,6-дихлорникотиновой кислоты (4,00 г, 20,8 ммоль) и 2,2-дифторэтанола способом, аналогичным стадии-1 промежуточного соединения-A3.
1H-ЯМР (300 MГц, DMSO-d6) дельта 13,4 (1H, ушир. с), 8,65 (1H, д, J=1,8 Гц), 8,28 (1H, д, J=1,8 Гц), 6,44 (1H, тт, J=54,3, 3,3 Гц), 4,73 (2H, тд, J=15,0, 3,3 Гц), MS (ESI) m/z: 236 (M-H)-.
Стадия-2: метил 5-хлор-6-(2,2-дифторэтокси)никотинат
К раствору 5-хлор-6-(2,2-дифторэтокси)никотиновой кислоты (1,5 г, 6,31 ммоль, стадия-1) в MeOH (100 мл) добавляли по каплям тионилхлорид (1,38 мл, 18,9 ммоль) при 0°C. Затем, реакционную смесь кипятили с обратным холодильником при перемешивании в течение 2 часов. После удаления растворителя получали 1,57 г (количественный выход) заявленного в заголовке соединения в виде белого твердого остатка.
1H-ЯМР (300 MГц, DMSO-d6) дельта 8,68 (1H, д, J=2,2 Гц), 8,33 (1H, д, J=2,2 Гц), 6,44 (1H, тт, J=54,3, 3,3 Гц), 4,74 (2H, тд, J=14,7, 3,3 Гц), 3,86 (3H, с), MS (ESI) m/z: 252 (M+H)+.
Стадия-3: (5-хлор-6-(2,2-дифторэтокси)пиридин-3-ил)метанол
Заявленное в заголовке соединение получали с выходом 62% (0,87 г, бесцветное масло) из метил 5-хлор-6-(2,2-дифторэтокси)никотината (1,57 г, 6,25 ммоль, стадия-2) способом, аналогичным стадии-2 промежуточного соединения-A1.
1H-ЯМР (300 MГц, CDCl3) дельта 7,99 (1H, д, J=2,2 Гц), 7,74 (1H, д, J=2,2 Гц), 6,16 (1H, тт, J=55,4, 4,4 Гц), 4,65 (2H, д, J=5,5 Гц), 4,60 (2H, тд, J=13,2, 4,0 Гц), сигнал OH не наблюдали, MS (ESI) m/z: 224 (M+H)+.
Промежуточное соединение-A5: (5-фтор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метанол
Стадия-1: 2-хлор-5-фтор-6-(2,2,2-трифторэтокси)никотиновая кислота
Смесь 2,6-дихлор-5-фторникотиновой кислоты (25,0 г, 119 ммоль), 2,2,2-трифторэтанола (17,1 мл, 238 ммоль) и гидроксида натрия (14,3 г, 357 ммоль) в воде (600 мл) перемешивали при 80°C в течение 40 часов. После охлаждения до 0°C, смесь подкисляли концентрированной хлористоводородной кислотой (pH 2). Полученный в результате белый осадок собирали фильтрованием и сушили, получая 32,2 г заявленного в заголовке соединения в неочищенном виде. Его применяли в следующей стадии без дополнительной очистки. MS (ESI) m/z: 274 (M+H)+.
Стадия-2: 5-фтор-6-(2,2,2-трифторэтокси)никотиновая кислота
Смесь 2-хлор-5-фтор-6-(2,2,2-трифторэтокси)никотиновой кислоты (32,2 г, 118 ммоль, стадия-1), триэтиламина (23 мл, 165 ммоль) и 10% Pd-C (12,5 г) в EtOH перемешивали при комнатной температуре в течение 5 часов в атмосфере водорода. Затем, смесь фильтровали через слой целита, и фильтрат концентрировали в вакууме. Остаток растворяли в воде (300 мл), и раствор подкисляли концентрированной хлористоводородной кислотой. Образовавшийся белый осадок собирали фильтрованием, получая 21,0 г (75%) заявленного в заголовке соединения в виде белого твердого остатка.
1H-ЯМР (300 MГц, DMSO-d6) дельта 13,40 (1H, ушир.), 8,55 (1H, д, J=1,8 Гц), 8,13 (1H, дд, J=10,3, 1,8 Гц), 5,16 (2H, к, J=9,2 Гц), MS (ESI) m/z: 238 (M-H)-.
Стадия-3: (5-фтор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метанол
Заявленное в заголовке соединение получали с выходом 91% (1,11 г, коричневое масло) из 5-фтор-6-(2,2,2-трифторэтокси)никотиновой кислоты (1,29 г, 5,39 ммоль, стадия-2) способом, аналогичным стадии-2 промежуточного соединения-A1.
1H-ЯМР (300 MГц, CDCl3) дельта 7,88 (1H, с), 7,48 (1H, дд, J=9,9, 1,5 Гц), 4,84 (2H, к, J=8,4 Гц), 4,68 (2H, д, J=5,9 Гц), 1,76 (1H, м), MS (ESI) m/z: 226 (M+H)+.
Промежуточное соединение-A6: (6-(3,3,3-трифторпропокси)пиридин-3-ил)метанол
Стадия-1: метил 6-(3,3,3-трифторпропокси)никотинат
трет-Бутоксид калия (2,45 г, 21,9 ммоль) добавляли к раствору 3,3,3-трифторпропан-1-ола (1,67 мл, 18,9 ммоль) в THF (30 мл) и перемешивали в течение 5 минут. Затем, добавляли к нему метил 6-хлорникотинат (2,5 г, 14,6 ммоль) и перемешивали в течение 2 часов. Реакционную смесь выливали в воду, экстрагировали EtOAc. Органический слой сушили над сульфатом натрия и концентрировали в вакууме, получая 2,21 г (61% выход) заявленного в заголовке соединения в виде бесцветного масла. Данный материал применяли в следующей реакции (стадия-2) без дополнительной очистки.
1H-ЯМР (300 MГц, CDCl3) дельта 8,81 (1H, д, J=2,2 Гц), 8,17 (1H, дд, J=8,8, 2,2 Гц), 6,79 (1H, д, J=8,8 Гц), 4,62 (2H, т, J=6,2 Гц), 3,91 (3H, с), 2,63 (2H, м), MS (ESI) m/z: 250 (M+H)+.
Стадия-2: 6-(3,3,3-трифторпропокси)никотиновая кислота
К раствору метил 6-(3,3,3-трифторпропокси)никотината (1,37 г, 5,50 ммоль, стадия-1) в MeOH (30 мл) добавляли 2 M гидроксид натрия (5 мл) и перемешивали в течение 2 часов при 60°C. После удаления растворителя остаток растворяли в воде (30 мл) и подкисляли концентрированной хлористоводородной кислотой (pH 2). Полученный в результате белый осадок собирали фильтрованием и сушили, получая 1,11 г (86% выход) заявленного в заголовке соединения в виде белого твердого остатка.
1H-ЯМР (300 MГц, CDCl3) дельта 8,90 (1H, д, J=2,2 Гц), 8,23 (1H, дд, J=8,8, 2,2 Гц), 6,83 (1H, д, J=8,8 Гц), 4,65 (2H, т, J=6,2 Гц), 2,65 (2H, м), MS (ESI) m/z: 236 (M+H)+.
Стадия-3: (6-(3,3,3-трифторпропокси)пиридин-3-ил)метанол
Заявленное в заголовке соединение получали с выходом 91% (858 мг, 4,25 ммоль, коричневое масло) из 6-(3,3,3-трифторпропокси)никотиновой кислоты (1,00 г, 4,25 ммоль, стадия-2) способом, аналогичным стадии-2 промежуточного соединения-A1.
1H-ЯМР (300 MГц, CDCl3) дельта 8,11 (1H, д, J=2,2 Гц), 7,64 (1H, дд, J=8,4, 2,6 Гц), 6,77 (1H, д, J=8,1 Гц), 4,64 (2H, с), 4,55 (2H, т, J=6,6 Гц), 2,70-2,54 (2H, м), 1,67 (1H, ушир. с), 1H-ЯМР (300 MГц, CDCl3) дельта 8,11 (1H, д, J=2,2 Гц), 7,64 (1H, дд, J=8,4, 2,6 Гц), 6,77 (1H, д, J=8,1 Гц), 4,64 (2H, с), 4,55 (2H, т, J=6,6 Гц), 2,70-2,54 (2H, м), 1,67 (1H, ушир. с), MS (ESI) m/z: 222 (M+H)+.
Промежуточное соединение-A7: гидрохлорид 1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этанамина (один энантиомер; антипод промежуточного соединения-A27)
Стадия-1: N-метокси-N,5-диметил-6-(2,2,2-трифторэтокси)никотинамид
Смесь 5-метил-6-(2,2,2-трифторэтокси)никотиновой кислоты (2,27 г, 9,67 ммоль, стадия-1 промежуточного соединения-A1), гидрохлорида N,O-диметилгидроксиламина (1,04 г, 10,64 ммоль), HBTU (5,50 г, 14,51 ммоль) и триэтиламина (5,39 мл, 38,7 ммоль) в DCM (30 мл) перемешивали при комнатной температуре в течение 1,5 часов. Реакционную смесь выливали в насыщенный водный раствор гидрокарбоната натрия (300 мл) и экстрагировали DCM (500 мл). Органический слой промывали насыщенным водным гидрокарбонатом натрия (300 мл×2) и сушили над сульфатом натрия, и концентрировали в вакууме. Остаток очищали колоночной хроматографией на силикагеле, элюируя н-гексаном/EtOAc (4:1), получая 2,03 г (76% выход) заявленного в заголовке соединение в виде бесцветного масла.
1H-ЯМР (300 MГц, CDCl3) дельта 8,43 (1H, д, J=2,2 Гц), 7,86 (1H, м), 4,82 (2H, к, J=8,4 Гц), 3,60 (3H, с), 3,38 (3H, с), 2,26 (3H, с), MS (ESI) m/z: 279 (M+H)+.
Стадия-2: 1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этанон
К раствору N-метокси-N,5-диметил-6-(2,2,2-трифторэтокси)никотинамида (2,03 г, 7,31 ммоль, стадия-1) в THF (25 мл) добавляли по каплям раствор бромида метилмагния в THF (1,12 M, 13,1 мл, 14,6 ммоль) при 0°C. После перемешивания при комнатной температуре в течение 1,5 часов реакцию гасили насыщенным водным раствором бикарбоната натрия (150 мл), и водный слой экстрагировали EtOAc (150 мл×2). Объединенный органический слой сушили над сульфатом натрия и концентрировали в вакууме. Остаток промывали гексаном, получая 1,47 г (86% выход) заявленного в заголовке соединения в виде белого твердого остатка.
1H-ЯМР (300 MГц, CDCl3) дельта 8,59 (1H, д, J=2,0 Гц), 8,03 (1H, д, J=2,2 Гц), 4,84 (2H, к, J=8,4 Гц), 2,57 (3H, с), 2,27 (3H, с), MS (ESI) m/z: 234 (M+H)+.
Стадия-3: (R)-2-метил-N-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)пропан-2-сульфинамид (один диастереомер)
К смеси 1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этанона (1,47 г, 6,32 ммоль, стадия-2) и (R)-2-метилпропан-2-сульфинамида (1,15 г, 9,48 ммоль) в THF (10 мл) добавляли этоксид титана (IV) (1,99 мл, 9,48 ммоль), и смесь перемешивали при 70°C в течение 22 часов. После охлаждения до 0°C, добавляли к смеси боргидрид натрия (717 мг, 19,0 ммоль). После перемешивания при 0°C в течение 1 часа, реакцию гасили насыщенным водным раствором бикарбоната натрия (150 мл), и водный слой экстрагировали EtOAc (150 мл). Отделенный органический слой промывали водой, сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали колоночной хроматографией на силикагеле, элюируя н-гексаном/EtOAc (4:1-1:1,5), получая 1,70 г (79%) заявленного в заголовке соединения в виде бесцветного масла.
1H-ЯМР (300 MГц, CDCl3) дельта 7,94 (1H, д, J=2,2 Гц), 7,45 (1H, д, J=2,2 Гц), 4,76 (2H, к, J=8,8 Гц), 4,56-4,43 (1H, м), 3,32 (1H, д, J=2,6 Гц), 2,24 (3H, с), 1,51 (3H, д, J=6,6 Гц), 1,23 (9H, с), MS (ESI) m/z: 339 (M+H)+.
Стадия-4: гидрохлорид 1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этанамина (один энантиомер; антипод промежуточного соединения-A27)
Смесь (R)-2-метил-N-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)пропан-2-сульфинамида (один диастереомер, стадия-3) (1,70 г, 5,01 ммоль) и 8 M HCl-MeOH (10 мл) перемешивали при комнатной температуре в течение 1 часа. После удаления растворителя, остаток кристаллизовали из EtOAc/гексана, получая 1,27 г (94%) заявленного в заголовке соединения в виде белого твердого остатка.
1H-ЯМР (300 MГц, DMSO-d6) дельта 8,56 (2H, ушир. с), 8,16 (1H, д, J=2,0 Гц), 7,87 (1H, д, J=2,0 Гц), 5,03 (2H, к, J=9,2 Гц), 4,50-4,28 (1H, м), 2,20 (3H, с), 1,50 (3H, д, J=7,0 Гц), MS (ESI) m/z: 235 (M+H)+.
Промежуточное соединение-A8: (6-(2,2-дифторэтокси)-5-фторпиридин-3-ил)метанол
Стадия-1: 2-хлор-6-(2,2-дифторэтокси)-5-фторникотиновая кислота
Заявленное в заголовке соединение получали с выходом 55% (6,76 г, белый твердый остаток) из 2,6-дихлор-5-фторникотиновой кислоты (10,0 г, 47,6 ммоль) и 2,2-дифторэтанола способом, аналогичным стадии-1 промежуточного соединения-A5.
1H-ЯМР (300 MГц, CDCl3) дельта 8,10 (1H, д, J=9,5 Гц), 6,17 (1H, тт, J=55,0, 4,1 Гц), 4,68 (2H, тд, J=12,8, 4,1 Гц) (сигнал COOH не наблюдали), MS (ESI) m/z: 256 (M+H)+.
Стадия-2: 6-(2,2-дифторэтокси)-5-фторникотиновая кислота
Заявленное в заголовке соединение получали с выходом 55% (2,1 г, белый твердый остаток) из 2-хлор-6-(2,2-дифторэтокси)-5-фторникотиновой кислоты (4,5 г, 17,6 ммоль, стадия-1) способом, аналогичным стадии-2 промежуточного соединения-A5.
1H-ЯМР (300 MГц, DMSO-d6) дельта 8,55 (1H, д, J=2,2 Гц), 8,08 (1H, дд, J=12,5, 2,2 Гц), 6,44 (1H, тт, J=54,3, 3,3 Гц), 4,75 (2H, тд, J=15,0, 3,3 Гц) (сигнал COOH не наблюдали), MS (ESI) m/z: 220 (M-H)-.
Стадия-3: метил 6-(2,2-дифторэтокси)-5-фторникотинат
Заявленное в заголовке соединение получали с выходом 71% (1,6 г, белый твердый остаток) из 6-(2,2-дифторэтокси)-5-фторникотиновой кислоты (2,1 г, 9,7 ммоль, стадия-2) способом, аналогичным стадии-2 промежуточного соединения-A4.
1H-ЯМР (300 MГц, CDCl3) дельта 8,59 (1H, с), 7,95 (1H, д, J=11,1 Гц), 6,18 (1H, тт, J=55,4, 4,0 Гц), 4,68 (2H, тд, J=13,2, 3,7 Гц), 3,94 (3H, с), MS (ESI) m/z: 236 (M+H)+.
Стадия-4: (6-(2,2-дифторэтокси)-5-фторпиридин-3-ил)метанол
Заявленное в заголовке соединение получали с выходом 88% (1,24 г, бесцветное масло) из метил 6-(2,2-дифторэтокси)-5-фторникотината (1,6 г, 6,8 ммоль, стадия-3) способом, аналогичным стадии-2 промежуточного соединения-A1.
1H-ЯМР (300 MГц, CDCl3) дельта 7,87 (1H, с), 7,45 (1H, д, J=10,3 Гц), 6,16 (1H, тт, J=55,4, 4,4 Гц), 4,66 (2H, д, J=5,9 Гц), 4,60 (2H, тд, J=13,2, 3,7 Гц) (сигнал OH не наблюдали), MS (ESI) m/z: 208 (M+H)+, 206 (M-H)-.
Промежуточное соединение-A9: (6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метанол
Заявленное в заголовке соединение получали с выходом 78% (12,6 г, желтый полутвердый остаток) из 6-(2,2,3,3-тетрафторпропокси)никотиновой кислоты (1,29 г, 5,39 ммоль) способом, аналогичным стадии-2 промежуточного соединения-A1.
1H-ЯМР (300 MГц, CDCl3) дельта 8,13 (1H, д, J=2,2 Гц), 7,69 (1H, дд, J=8,8, 2,2 Гц), 6,84 (1H, д, J=8,8 Гц), 6,02 (1H, тт, J=53,1, 4,6 Гц), 4,78-4,66 (4H, м), 1,69 (1H, т, J=5,9 Гц), MS (ESI) m/z: 240 (M+H)+.
Промежуточное соединение-A10: (6-(2,2,3,3,3-пентафторпропокси)пиридин-3-ил)метанол
Стадия-1: метил 6-(2,2,3,3,3-пентафторпропокси)никотинат
К перемешиваемой суспензии гидрида натрия (3,85 г, 96 ммоль, 60% в масле) в DMA (120 мл) добавляли по каплям 2,2,3,3,3-пентафторпропан-1-ол (6,4 мл, 64 ммоль) при 0°C. После перемешивания в течение 10 минут добавляли по каплям при 0°C раствор метил 6-хлорникотината (5,5 г, 32 ммоль) в DMA (40 мл), и смесь перемешивали в течение 30 минут при комнатной температуре. Затем, смесь перемешивали при 90°C в течение 2 часов. После охлаждения до комнатной температуры добавляли 2 M водный гидроксид натрия (pH приблизительно составляет 6). Смесь экстрагировали н-гексаном/EtOAc (1:2, 200 мл). Органический слой промывали водой, соляным раствором, сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали колоночной хроматографией на NH-геле, элюируя н-гексаном/EtOAc (30:1), получая 3,07 г (34% выход) заявленного в заголовке соединения в виде коричневого масла.
1H-ЯМР (300 MГц, CDCl3) дельта 8,12 (1H, д, J=2,2 Гц), 8,24 (1H, дд, J=8,4, 2,6 Гц), 6,90 (1H, д, J=8,1 Гц), 4,90 (2H, т, J=12,5 Гц), 3,93 (3H, с), MS (ESI) m/z: 286 (M+H)+.
Стадия-2: (6-(2,2,3,3,3-пентафторпропокси)пиридин-3-ил)метанол
Заявленное в заголовке соединение получали с выходом 83% (2,31 г, коричневое масло) из метил 6-(2,2,3,3,3-пентафторпропокси)никотината (3,07 г, 10,8 ммоль, стадия-1) способом, аналогичным стадии-2 промежуточного соединения-A1.
1H-ЯМР (300 MГц, CDCl3) дельта 8,13 (1H, д, J=1,5 Гц), 7,69 (1H, дд, J=8,8, 2,2 Гц), 6,87 (1H, д, J=8,8 Гц), 4,84 (2H, т, J=12,8 Гц), 4,66 (2H, д, J=5,1 Гц), 1,73 (1H, т, J=5,1 Гц), MS (ESI) m/z: 258 (M+H)+.
Промежуточное соединение-A11: гидрохлорид (+)-1-(6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)этанамина (один энантиомер)
Стадия-1: 6-(2,2-дифторэтокси)-N-метокси-N,5-диметилникотинамид
Заявленное в заголовке соединение получали с выходом 98% (1,20 г, белый твердый остаток) из 6-(2,2-дифторэтокси)-5-метилникотиновой кислоты (1,02 г, 4,70 ммоль, стадия-1 промежуточного соединения-A2) способом, аналогичным стадии-1 промежуточного соединения-A7.
1H-ЯМР (300 MГц, CDCl3) дельта 8,43 (1H, д, J=2,2 Гц), 7,84 (1H, ушир. с), 6,16 (1H, тт, J=55,8, 4,4 Гц), 4,60 (2H, тд, J=13,2, 4,4 Гц), 3,58 (3H, с), 3,37 (3H, с), 2,25 (3H, с), MS (ESI) m/z: 261 (M+H)+.
Стадия-2: 1-(6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)этанон
Заявленное в заголовке соединение получали с количественным выходом (0,99 г, белый твердый остаток) из 6-(2,2-дифторэтокси)-N-метокси-N,5-диметилникотинамида (1,20 г, 4,61 ммоль, стадия-1) способом, аналогичным стадии-2 промежуточного соединения-A7.
1H-ЯМР (270 MГц, CDCl3) дельта 8,58 (1H, д, J=2,0 Гц), 8,01-8,00 (1H, м), 6,16 (1H, тт, J=55,4, 4,0 Гц), 4,63 (2H, тд, J=13,2, 4,0 Гц), 2,57 (3H, с), 2,26 (3H, с), MS (ESI) m/z: 216 (M+H)+.
Стадия-3: (R)-N-(1-(6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)этил)-2-метилпропан-2-сульфинамид (один диастереомер)
Заявленное в заголовке соединение получали с выходом 82% (1,22 г, бесцветное масло) из 1-(6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)этанона (0,99 г, 4,61 ммоль, стадия-2) и (R)-2-метилпропан-2-сульфинамида способом, аналогичным стадии-3 промежуточного соединения-A7.
1H-ЯМР (300 MГц, CDCl3) дельта 7,97 (1H, д, J=2,2 Гц), 7,43 (1H, ушир. с), 6,14 (1H, тт, J=55,8, 4,4 Гц), 4,59-4,46 (3H, м), 3,32 (1H, ушир. с), 2,22 (3H, с), 1,50 (3H, д, J=6,6 Гц), 1,23 (9H, с), MS (ESI) m/z: 321 (M+H)+.
Стадия-4: гидрохлорид (+)-1-(6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)этанамина (один энантиомер)
Заявленное в заголовке соединение получали с выходом 94% (0,91 г, белый твердый остаток) из (R)-N-(1-(6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)этил)-2-метилпропан-2-сульфинамида (один диастереомер) (1,22 г, 3,80 ммоль, стадия-3) способом, аналогичным стадии-4 промежуточного соединения-A7.
1H-ЯМР (270 MГц, DMSO-d6) дельта 8,58 (2H, ушир. с), 8,13 (1H, д, J=2,0 Гц), 7,82 (1H, ушир. с), 6,40 (1H, тт, J=54,7, 3,3 Гц), 4,60 (2H, тд, J=15,2, 3,3 Гц), 4,42-4,36 (1H, м), 2,19 (3H, с), 1,52 (3H, д, J=6,6 Гц), [α]D=+3,09 (c=1,18, метанол).
Промежуточное соединение-A12: (6-(4-фторфенокси)-5-метилпиридин-3-ил)метанол
Стадия-1: метил 6-(4-фторфенокси)-5-метилникотинат
Смесь метил 6-фтор-5-метилникотината (2,40 г, 14,2 ммоль), 4-фторфенола (2,39 г, 21,3 ммоль) и карбоната калия (3,92 г, 28,4 ммоль) в DMF (45 мл) перемешивали при 90°C в течение 3 часов. После охлаждения до комнатной температуры смесь фильтровали через слой целита и промывали EtOAc (200 мл). Фильтрат промывали водой (200 мл) и соляным раствором (200 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали хроматографией на силикагеле, элюируя н-гексаном/EtOAc (20:1), получая 3,46 г (93% выход) заявленного в заголовке соединения в виде белого твердого остатка.
1H-ЯМР (300 MГц, CDCl3) дельта 8,59 (1H, д, J=2,2 Гц), 8,12 (1H, д, J=2,2 Гц), 7,15-7,06 (4H, м), 3,90 (3H, с), 2,40 (3H, с), MS (ESI) m/z: 262 (M+H)+.
Стадия-2: 6-(4-фторфенокси)-5-метилникотиновая кислота
Заявленное в заголовке соединение получали с выходом 91% (2,98 г, белый твердый остаток) из метил 6-(4-фторфенокси)-5-метилникотината (3,46 г, 13,2 ммоль, стадия-1) способом, аналогичным стадии-2 промежуточного соединения-A6.
1H-ЯМР (300 MГц, CDCl3) дельта 8,67 (1H, д, J=2,2 Гц), 8,16 (1H, д, J=2,2 Гц), 7,18-7,06 (4H, м), 2,40 (3H, с) (сигнал COOH не наблюдали), MS (ESI) m/z: 248 (M+H)+.
Стадия-3: (6-(4-фторфенокси)-5-метилпиридин-3-ил)метанол
Заявленное в заголовке соединение получали с выходом 98% (417 мг, белый твердый остаток) из 6-(4-фторфенокси)-5-метилникотиновой кислоты (450 мг, 1,82 ммоль, стадия-2) способом, аналогичным стадии-2 промежуточного соединения-A3.
1H-ЯМР (300 MГц, CDCl3) дельта 7,93 (1H, с), 7,59 (1H, с), 7,15-7,03 (4H, м), 4,62 (2H, д, J=5,5 Гц), 2,36 (3H, с), 1,65 (1H, т, J=5,5 Гц), MS (ESI) m/z: 234 (M+H)+.
Промежуточное соединение-A13: (5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метанол
Стадия-1: 5-метил-6-(3,3,3-трифторпропокси)никотиновая кислота
К раствору гидрида натрия (0,844 г, 21,1 ммоль) в THF (10 мл), добавляли при 0°C 3,3,3-трифторпропан-1-ол (1,61 г, 14,1 ммоль) в THF (10 мл) и перемешивали в течение 5 минут. Затем, добавляли по каплям к реакционной смеси метил 6-фтор-5-метилникотинат (1,19 г, 7,04 ммоль) в THF (10 мл), и полученную в результате смесь перемешивали при комнатной температуре в течение 2 часов. Реакционную смесь разбавляли водой (30 мл) и перемешивали в течение ночи. После удаления THF, смесь подкисляли 2 M хлористоводородной кислотой (11 мл). Полученный в результате белый осадок собирали фильтрованием и сушили, получая 1,76 г (количественный выход) заявленного в заголовке соединения в виде белого твердого остатка. Данный материал применяли в следующей реакции (стадия-2) без дополнительной очистки. MS (ESI) m/z: 250 (M+H)+.
Стадия-2: (5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метанол
Заявленное в заголовке соединение получали с выходом 95% (2,43 г, белый твердый остаток) из 5-метил-6-(3,3,3-трифторпропокси)никотиновой кислоты (2,71 г, 10,9 ммоль, стадия-1) способом, аналогичным стадии-2 промежуточного соединения-A3.
1H-ЯМР (270 MГц, CDCl3) дельта 7,94 (1H, с), 7,47 (1H, с), 4,62-4,54 (4H, м), 2,71-2,56 (2H, м), 2,19 (3H, с), 1,62 (1H, т, J=5,9 Гц), MS (ESI) m/z: 236 (M+H)+.
Промежуточное соединение-A14: (5-метил-6-(2,2,2-трифторэтокси)пиридазин-3-ил)метанол
Стадия-1: Смесь 6-хлор-4-метил-3-(2,2,2-трифторэтокси)пиридазина и 3-хлор-4-метил-6-(2,2,2-трифторэтокси)пиридазина (2:1)
К перемешиваемому раствору 2,2,2-трифторэтанола (2,03 г, 20,2 ммоль), DMF (20 мл) и THF (10 мл) аккуратно добавляли 60% гидрид натрия (0,78 г, 20,2 ммоль) при 0°C. После перемешивания при комнатной температуре в течение 1 часа, данный раствор медленно добавляли к раствору 3,6-дихлор-4-метилпиридазина (3,00 г, 18,4 ммоль) в DMF (20 мл) при 0°C. Полученную в результате смесь перемешивали при комнатной температуре в течение 1 часа. Смесь выливали в ледяную воду и экстрагировали EtOAc (200 мл). Органический слой промывали водой (200 мл×2) и сушили над сульфатом натрия. После удаления органического растворителя, остаток очищали колоночной хроматографией на силикагеле, элюируя н-гексаном/EtOAc (9:1), получая 3,40 г смеси заявленного в заголовке соединения (81% выход) в виде белого твердого остатка. MS (ESI) m/z: 227 (M+H)+.
Стадия-2: этил 5-метил-6-(2,2,2-трифторэтокси)пиридазин-3-карбоксилат и этил 4-метил-6-(2,2,2-трифторэтокси)пиридазин-3-карбоксилат
Смесь 6-хлор-4-метил-3-(2,2,2-трифторэтокси)пиридазина и 3-хлор-4-метил-6-(2,2,2-трифторэтокси)пиридазина (3,40 г, 15,0 ммоль, стадия-1), ацетата палладия (II) (0,34 г, 1,50 ммоль), 1,3-бис(дифенилфосфино)пропана (1,24 г, 3,00 ммоль), триэтиламина (6,27 мл, 45,0 ммоль), DMF (40 мл) и EtOH (20 мл) перемешивали при 80°C в атмосфере монооксида углерода (1 атм) в течение 20 часов. После охлаждения до комнатной температуры, смесь разбавляли EtOAc (200 мл). Ее промывали водой (200 мл×2), и органический слой сушили над сульфатом натрия. После удаления органического растворителя, остаток очищали колоночной хроматографией на силикагеле, элюируя н-гексаном/EtOAc (8:1-5:1), получая 2,15 г этил 5-метил-6-(2,2,2-трифторэтокси)пиридазин-3-карбоксилата (54% выход, более полярный продукт) в виде грязно-белого твердого остатка и 0,63 г этил 4-метил-6-(2,2,2-трифторэтокси)пиридазин-3-карбоксилата (16% выход, менее полярный продукт) в виде бледно-желтого масла.
Этил 5-метил-6-(2,2,2-трифторэтокси)пиридазин-3-карбоксилат (более полярный)
1H-ЯМР (300 MГц, CDCl3) дельта 7,99 (1H, д, J=1,5 Гц), 5,02 (2H, к, J=8,1 Гц), 4,50 (2H, к, J=7,3 Гц), 2,36 (3H, с), 1,46 (3H, т, J=7,3 Гц), MS (ESI) m/z: 265 (M+H)+.
Этил 4-метил-6-(2,2,2-трифторэтокси)пиридазин-3-карбоксилат (менее полярный)
1H-ЯМР (300 MГц, CDCl3) дельта 7,00 (1H, с), 4,99 (2H, к, J=8,1 Гц), 4,49 (2H, к, J=7,3 Гц), 2,58 (3H, с), 1,46 (3H, т, J=7,3 Гц), MS (ESI) m/z: 265 (M+H)+.
Стадия-3: (5-метил-6-(2,2,2-трифторэтокси)пиридазин-3-ил)метанол
Заявленное в заголовке соединение получали с выходом 30% (373 мг, коричневое масло) из этил 5-метил-6-(2,2,2-трифторэтокси)пиридазин-3-карбоксилата (1,5 г, 5,7 ммоль, стадия-2) способом, аналогичным стадии-2 промежуточного соединения-A1.
1H-ЯМР (300 MГц, CDCl3) дельта 7,31 (1H, с), 4,93 (2H, к, J=8,1 Гц), 4,86 (2H, с), 2,31 (3H, с) (сигнал OH не наблюдали), MS (ESI) m/z: 223 (M+H)+.
Промежуточное соединение-A15: (4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метанол
Стадия-1: 2-хлор-4-метил-5-(2,2,2-трифторэтокси)пиридин
К смеси 6-хлор-4-метилпиридин-3-ола (2,00 г, 13,9 ммоль) и карбоната цезия (6,81 г, 20,9 ммоль) в DMF (40 мл) добавляли по каплям 2,2,2-трифторэтил трифторметансульфонат (3,56 г, 15,3 ммоль) при 0°C. После перемешивания при комнатной температуре в течение 1 часа, смесь выливали в воду (300 мл). Водный слой экстрагировали EtOAc (300 мл). Отделенный органический слой промывали водой (200 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали колоночной хроматографией на силикагеле, элюируя н-гексаном/EtOAc (9:1), получая 3,00 г (95% выход) заявленного в заголовке соединения в виде белого твердого остатка.
1H-ЯМР (300 MГц, CDCl3) дельта 7,90 (1H, с), 7,17 (1H, с), 4,43 (2H, к, J=7,3 Гц), 2,28 (3H, с), MS (ESI) m/z: 226 (M+H)+.
Стадия-2: этил 4-метил-5-(2,2,2-трифторэтокси)пиколинат
Заявленное в заголовке соединение получали с выходом 90% (3,14 г, белый твердый остаток) из 2-хлор-4-метил-5-(2,2,2-трифторэтокси)пиридина (3,00 г, 13,3 ммоль, стадия-1) способом, аналогичным стадии-2 промежуточного соединения-A14.
1H-ЯМР (300 MГц, CDCl3) дельта 8,24 (1H, с), 8,00 (1H, с), 4,57-4,42 (4H, м), 2,35 (3H, с), 1,44 (3H, т, J=6,6 Гц), MS (ESI) m/z: 264 (M+H)+.
Стадия-3: (4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метанол
Заявленное в заголовке соединение получали с выходом 72% (913 мг, бледно-желтый твердый остаток) из этил 4-метил-5-(2,2,2-трифторэтокси)пиколината (1,50 г, 5,7 ммоль, стадия-2)способом, аналогичным стадии-2 промежуточного соединения-A1.
1H-ЯМР (300 MГц, CDCl3) дельта 8,09 (1H, с), 7,09 (1H, с), 4,68 (2H, д, J=3,7 Гц), 4,44 (2H, к, J=8,1 Гц), 3,44 (1H, ушир. с), 2,30 (3H, с), MS (ESI) m/z: 222 (M+H)+.
Промежуточное соединение-A16: (3-метил-4-(2,2,2-трифторэтокси)фенил)метанол
Стадия-1: 3-метил-4-(2,2,2-трифторэтокси)бензойная кислота
К перемешиваемому раствору 4-гидрокси-3-метилбензойной кислоты (10 г, 65,7 ммоль) и карбоната цезия (64,2 г, 197 ммоль) в DMF (150 мл) добавляли 2,2,2-трифторэтилтрифторметансульфонат (33,6 г, 145 ммоль) при 0°C. Смесь перемешивали при 0°C в течение 10 минут, затем перемешивали при комнатной температуре в течение 2 дней. К смеси добавляли воду (150 мл) и гранулы NaOH (15 г), и полученную в результате смесь перемешивали в течение 20 часов при комнатной температуре. Смесь разбавляли водой (100 мл), промывали эфиром (100 мл×2) и водный слой подкисляли концентрированной хлористоводородной кислотой (pH 4) при 0°C, получая белый твердый остаток. Твердый остаток собирали фильтрованием, промывали последовательно водой и н-гексаном и сушили в вакууме при 50°C, получая 14,8 г (96 % выход) заявленного в заголовке соединения в виде белого твердого остатка.
1H-ЯМР (300 MГц, CDCl3) дельта 7,98-7,90 (2H, м), 6,83 (1H, д, J=8,0 Гц), 4,43 (2H, к, J=7,3 Гц), 2,31 (3H, с) (сигнал COOH не наблюдали), MS (ESI) m/z: 233 (M-H)-.
Стадия-2: (3-метил-4-(2,2,2-трифторэтокси)фенил)метанол
Заявленное в заголовке соединение получали с выходом 80% (5,26 г, белый твердый остаток) из 3-метил-4-(2,2,2-трифторэтокси)бензойной кислоты (7,00 г, 29,9 ммоль, стадия-1) способом, аналогичным стадии-2 промежуточного соединения-A1.
1H-ЯМР (300 MГц, CDCl3) дельта 7,19-7,16 (2H, м), 6,78 (1H, д, J=8,4 Гц), 4,62 (2H, д, J=5,9 Гц), 4,35 (2H, к, J=8,7 Гц), 2,27 (3H, с) (сигнал OH не наблюдали), MS (ESI) m/z: наблюдали положительный ион сигнала фрагмента 203.
Промежуточное соединение-A17: (4-(2,2-дифторэтокси)-3-метилфенил)метанол
Стадия-1: метил 4-(2,2-дифторэтокси)-3-метилбензоат
К перемешиваемому раствору метил 4-гидрокси-3-метилбензоата (1,5 г, 9,0 ммоль), 2,2-дифторэтанола (0,90 г, 10,8 ммоль), трифенилфосфина (3,6 г, 13,5 ммоль) в THF (40 мл) добавляли по каплям диэтилазодикарбоксилат (4,9 мл, 10,8 ммоль, 40% раствор в толуоле) при 0°C. Смесь перемешивали при комнатной температуре в течение 30 минут. Затем реакционную смесь перемешивали при 60°C в течение 2 часов. После охлаждения до комнатной температуры, смесь концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле, элюируя н-гексаном/EtOAc (18:1), получая 1,9 г (90% выход) заявленного в заголовке соединения в виде белого твердого остатка.
1H-ЯМР (300 MГц, CDCl3) дельта 7,90-7,85 (2H, м), 6,79 (1H, д, J=8,8 Гц), 6,13 (1H, тт, J=54,9, 4,4 Гц), 4,24 (2H, тд, J=12,5, 3,7 Гц), 3,89 (3H, с), 2,27 (3H, с).
Стадия-2: (4-(2,2-дифторэтокси)-3-метилфенил)метанол
Заявленное в заголовке соединение получали с количественным выходом (712 мг, бесцветное масло) из метил 4-(2,2-дифторэтокси)-3-метилбензоата (750 мг, 3,3 ммоль, стадия-1) способом, аналогичным стадии-2 промежуточного соединения-A1.
1H-ЯМР (300 MГц, CDCl3) дельта 7,18-7,15 (2H, м), 6,78 (1H, д, J=8,1 Гц), 6,11 (1H, тт, J=54,9, 4,2 Гц), 4,61 (2H, д, J=5,9 Гц), 4,19 (2H, тт, J=13,0, 4,2 Гц), 2,25 (3H, с) (сигнал OH не наблюдали).
Промежуточное соединение-A18: (5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метанол
Стадия-1: 5-метил-6-(2,2,3,3-тетрафторпропокси)никотиновая кислота
Заявленное в заголовке соединение получали с количественным выходом (3,7 г, белый твердый остаток) из 6-фтор-5-метилникотиновой кислоты (2,0 г, 12,9 ммоль) и 2,2,3,3-тетрафторпропан-1-ола (3,4 г, 25,8 ммоль) способом, аналогичным стадии-1 промежуточного соединения-A1.
1H-ЯМР (300 MГц, CDCl3) дельта 8,74 (1H, д, J=2,2 Гц), 8,09 (1H, д, J=2,2 Гц), 6,00 (1H, тт, J=52,7, 3,7 Гц), 4,84 (2H, т, J=12,5 Гц), 2,28 (3H, с), сигнал COOH не наблюдали, MS (ESI) m/z: 268 (M+H)+.
Стадия-2: (5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метанол
Заявленное в заголовке соединение получали с выходом 98% (0,93 г, желтое масло) из 5-метил-6-(2,2,3,3-тетрафторпропокси)никотиновой кислоты (1,00 г, 3,74 ммоль) способом, аналогичным стадии-2 промежуточного соединения-A1.
1H-ЯМР (300 MГц, DMSO-d6) дельта 7,93 (1H, с), 7,57 (1H, с), 6,68 (1H, тт, J=52,0, 5,9 Гц), 5,19 (1H, т, J=5,9 Гц), 4,84 (2H, т, J=13,9 Гц), 4,43 (2H, д, J=5,9 Гц), 2,18 (3H, с), MS (ESI) m/z: 254 (M+H)+.
Промежуточное соединение-A19: (2-метил-6-(2,2,2-трифторэтокси)пиридин-4-ил)метанол
Стадия-1: этил 2-метил-6-(2,2,2-трифторэтокси)изоникотинат
Заявленное в заголовке соединение получали с выходом 83% (2,42 г, бесцветное масло) из этил 2-гидрокси-6-метилизоникотината (2,0 г, 11,0 ммоль) и 2,2,2-трифторэтилтрифторметансульфоната (2,82 г, 12,1 ммоль) способом, аналогичным стадии-1 промежуточного соединения-A15.
1H-ЯМР (270 MГц, CDCl3) дельта 7,36 (1H, с), 7,23 (1H, с), 4,78 (2H, к, J=8,6 Гц), 4,38 (2H, к, J=7,3 Гц), 2,50 (3H, с), 1,39 (3H, т, J=7,3 Гц), MS (ESI) m/z: 264 (M+H)+.
Стадия-2: (2-метил-6-(2,2,2-трифторэтокси)пиридин-4-ил)метанол
Заявленное в заголовке соединение получали с выходом 90% (753 мг, бесцветное масло) из этил 2-метил-6-(2,2,2-трифторэтокси)изоникотината (1,00 г, 3,8 ммоль, стадия-1) способом, аналогичным стадии-2 промежуточного соединения-A1.
1H-ЯМР (300 MГц, CDCl3) дельта 6,80 (1H, с), 6,66 (1H, с), 4,76 (2H, д, J=8,8 Гц), 4,67 (2H, к, J=5,9 Гц), 2,43 (3H, с), 1,81 (1H, т, J=5,9 Гц), MS (ESI) m/z: 222 (M+H)+.
Промежуточное соединение-A20: (1-(5-(трифторметил)пиридин-2-ил)-1H-пиразол-3-ил)метанол
Заявленное в заголовке соединение получали с выходом 92% (1,04 г, бесцветное масло) из 1-(5-(трифторметил)пиридин-2-ил)-1H-пиразолe-3-карбоновой кислоты (1,2 г, 4,7 ммоль) способом, аналогичным стадии-2 промежуточного соединения-A3.
1H-ЯМР (300 MГц, CDCl3) дельта 8,66 (1H, с), 8,56 (1H, д, J=2,2 Гц), 8,08-8,00 (2H, м), 6,50 (1H, д, J=2,9 Гц), 4,81 (2H, д, J=5,8 Гц), MS (ESI) m/z: 244 (M+H)+.
Промежуточное соединение-A21: (6-(циклопропилметокси)-5-метилпиридин-3-ил)метанол
Стадия-1: 6-(циклопропилметокси)-5-метилникотиновая кислота
К суспензии гидрида натрия (2,04 г, 60% в масле, 53,2 ммоль) в THF (30 мл) добавляли циклопропилметанол (3,84 г, 53,2 ммоль) и метил 6-фтор-5-метилникотинат (1,50 г, 8,9 ммоль), и смесь перемешивали при 0°C в течение 1 часа. Затем, добавляли 1 M водный раствор гидроксида натрия (20 мл), EtOH (10 мл) и THF (10 мл), и смесь перемешивали при 60°C в течение 1 часа. После охлаждения до комнатной температуры, смесь подкисляли 2 M хлористоводородной кислотой (pH 4), и водный слой экстрагировали EtOAc (100 мл). Органический слой сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали колоночной хроматографией на силикагеле, элюируя DCM/MeOH (20:1), получая 1,72 г заявленного в заголовке соединения (содержащего приблизительно 20% 6-метокси-5-метилникотиновой кислоты) в виде белого твердого остатка. Его применяли в следующей стадии без дополнительной очистки. MS (ESI) m/z: 206 (M-H)-.
Стадия-2: (6-(циклопропилметокси)-5-метилпиридин-3-ил)метанол
Заявленное в заголовке соединение получали с выходом 68% (1,10 г, белый твердый остаток) из 6-(циклопропилметокси)-5-метилникотиновой кислоты (1,72 г, 8,30 ммоль, стадия-1) способом, аналогичным стадии-2 промежуточного соединения-A1.
1H-ЯМР (300 MГц, CDCl3) дельта, 7,92 (1H, с), 7,45 (1H, с), 4,59 (2H, д, J=5,9 Гц), 4,15 (2H, д, J=6,6 Гц), 2,22 (3H, с), 1,54 (1H, т, J=5,9 Гц), 1,35-1,24 (1H, м), 0,62-0,55 (2H, м), 0,37-0,32 (2H, м), MS (ESI) m/z: 194 (M+H)+.
Промежуточное соединение-A22: (2-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метанол
Стадия-1: метил 2-метокси-6-(2,2,2-трифторэтокси)никотинат
Заявленное в заголовке соединение получали с выходом 54% (1,79 г, бесцветное масло) из метил 6-хлор-2-метоксиникотината (2,5 г, 12,4 ммоль) и 2,2,2-трифторэтанола (2,78 г, 24,8 ммоль) способом, аналогичным стадии-1 промежуточного соединения-A6.
1H-ЯМР (300 MГц, CDCl3) дельта 8,21 (1H, д, J=8,0 Гц), 6,47 (1H, д, J=8,0 Гц), 4,79 (2H, к, J=8,8 Гц), 4,07 (3H, с), 3,87 (3H, с), MS (ESI) m/z: 266 (M+H)+.
Стадия-2: (2-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метанол
Заявленное в заголовке соединение получали с выходом 74% (1,19 г, белый твердый остаток) из метил 2-метокси-6-(2,2,2-трифторэтокси)никотината (1,79 г, 6,75 ммоль, стадия-1) способом, аналогичным стадии-2 промежуточного соединения-A1.
1H-ЯМР (300 MГц, CDCl3) дельта 7,54 (1H, д, J=8,0 Гц), 6,41 (1H, д, J=8,0 Гц), 4,72 (2H, к, J=8,8 Гц), 4,59 (2H, с), 3,97 (3H, с), 2,10 (1H, ушир. с), MS (ESI) m/z: 238 (M+H)+.
Промежуточное соединение-A23: (6-метил-5-(2,2,2-трифторэтокси)пиразин-2-ил)метанол
Стадия-1: метил 6-метил-5-(2,2,2-трифторэтокси)пиразин-2-карбоксилат
Смесь метил 5-хлор-6-метилпиразин-2-карбоксилата (3,00 г, 16,1 ммоль), 2,2,2-трифторэтанола (32,2 г, 322 ммоль) и карбоната калия (3,33 г, 24,1 ммоль) в DMF (30 мл) перемешивали при 60°C в течение 2 часов. После охлаждения до комнатной температуры смесь отфильтровывали, и фильтрат разбавляли EtOAc (300 мл). Органический слой промывали водой (100 мл×3), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали колоночной хроматографией на силикагеле, элюируя EtOAc, получая 3,91 г (97% выход) заявленного в заголовке соединения в виде белого твердого остатка. MS (ESI) m/z: 251 (M+H)+.
Стадия-2: 6-метил-5-(2,2,2-трифторэтокси)пиразин-2-карбоновая кислота
Заявленное в заголовке соединение получали с выходом 66% (2,44 г, белый твердый остаток) из метил 6-метил-5-(2,2,2-трифторэтокси)пиразин-2-карбоксилата (3,91 г, 15,6 ммоль, стадия-1) способом, аналогичным стадии-2 промежуточного соединения-A6.
1H-ЯМР (300 MГц, DMSO-d6) дельта 13,36 (1H, ушир. с), 8,67 (1H, с), 5,11 (2H, к, J=8,8 Гц), 2,48 (3H, с), MS (ESI) m/z: 235 (M-H)-.
Стадия-3: (6-метил-5-(2,2,2-трифторэтокси)пиразин-2-ил)метанол
Заявленное в заголовке соединение получали с количественным выходом (1,9 г, белый твердый остаток) из 6-метил-5-(2,2,2-трифторэтокси)пиразин-2-карбоновой кислоты (2,0 г, 8,5 ммоль, стадия-2) способом, аналогичным стадии-2 промежуточного соединения-A3.
1H-ЯМР (300 MГц, DMSO-d6) дельта 8,07 (1H, с), 5,46 (1H, т, J=1,5 Гц), 5,08-4,99 (2H, м), 4,54 (2H, д, J=5,8 Гц), 2,42 (3H, с), MS (ESI) m/z: 223 (M+H)+.
Промежуточное соединение-A24: (6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метанол
Стадия-1: 6-(2,2-дифторпропокси)-5-метилникотиновая кислота
Заявленное в заголовке соединение получали с выходом 87% (2,14 г, белый твердый остаток) из метил 6-фтор-5-метилникотината (1,80 г, 10,6 ммоль) и 2,2-дифторпропан-1-ола (1,13 г, 11,7 ммоль) способом, аналогичным стадии-1 промежуточного соединения-A21.
1H-ЯМР (300 MГц, DMSO-d6) дельта 8,56 (1H, д, J=1,5 Гц), 8,07 (1H, д, J= 1,5 Гц), 4,64 (2H, т, J=13,2 Гц), 2,22 (3H, с), 1,75 (3H, т, J=19,1 Гц) (сигнал COOH не наблюдали), MS (ESI) m/z: 230 (M-H)-.
Стадия-2: (6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метанол
Заявленное в заголовке соединение получали с выходом 93% (1,31 г, бесцветное масло) из 6-(2,2-дифторпропокси)-5-метилникотиновой кислоты (1,5 г, 6,5 ммоль, стадия-1) способом, аналогичным стадии-2 промежуточного соединения-A3.
1H-ЯМР (300 MГц, DMSO-d6) дельта 7,91 (1H, с), 7,55 (1H, с), 5,17 (1H, т, J=5,8 Гц), 4,54 (2H, т, J=13,2 Гц), 4,41 (2H, д, J=5,8 Гц), 2,17 (3H, с), 1,73 (3H, т, J=19,1 Гц), MS (ESI) m/z: 218 (M+H)+.
Промежуточное соединение-A25: (5-циклопропил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метанол
Стадия-1: метил 5-циклопропил-6-(2,2,2-трифторэтокси)никотинат
Смесь метил 5-бром-6-(2,2,2-трифторэтокси)никотината (1,00 г, 3,18 ммоль), циклопропилбороновой кислоты (821 мг, 9,6 ммоль), ацетата палладия (II) (36 мг, 0,16 ммоль), трициклогексилфосфина (15% толуольный раствор, 595 мг, 0,32 ммоль) и фосфата калия (1,69 г, 7,96 ммоль) в смеси толуол-вода (10:1, 11 мл) кипятили с обратным холодильником при перемешивании в течение 12 часов. После охлаждения до комнатной температуры, смесь фильтровали через слой целита. Фильтрат концентрировали в вакууме. Остаток очищали хроматографией на силикагеле, элюируя н-гексаном/EtOAc (20:1), получая 854 мг (97% выход) заявленного в заголовке соединения в виде белого твердого остатка.
1H-ЯМР (300 MГц, CDCl3) дельта 8,59-8,57 (1H, м), 7,76-7,74 (1H, м), 4,90-4,79 (2H, м), 3,91 (3H, с), 2,12-2,06 (1H, м), 1,04-0,98 (2H, м), 0,78-0,74 (2H, м), MS (ESI) m/z: 276 (M+H)+.
Стадия-2: (5-циклопропил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метанол
Заявленное в заголовке соединение получали с выходом 86% (657 мг, белый твердый остаток) из метил 5-циклопропил-6-(2,2,2-трифторэтокси)никотината (850 мг, 3,09 ммоль, стадия-1) способом, аналогичным стадии-2 промежуточного соединения-A1.
1H-ЯМР (300 MГц, CDCl3) дельта 7,88 (1H, д, J=2,2 Гц), 7,23 (1H, д, J=2,2 Гц), 4,78 (2H, к, J=8,0 Гц), 4,60 (2H, д, J=5,9), 2,13-2,04 (1H, м), 1,71 (1H, ушир. с), 1,02-0,95 (2H, м), 0,73-0,68 (2H, м), MS (ESI) m/z: 248 (M+H)+.
Промежуточное соединение-A26: (6-(4-хлор-1H-пиразол-1-ил)-5-метилпиридин-3-ил)метанол
Стадия-1: метил 6-(4-хлор-1H-пиразол-1-ил)-5-метилникотинат
Смесь метил 6-фтор-5-метилникотината (800 мг, 4,73 ммоль), 4-хлор-1H-пиразола (509 мг, 4,97 ммоль) и карбоната цезия (3,08 г, 9,46 ммоль) в DMF (16 мл) перемешивали при 60°C в течение 1 часа. После охлаждения до комнатной температуры, смесь разбавляли EtOAc (150 мл) и промывали водой (100 мл×3). Органическую фазу фильтровали через силикагель, и фильтрат концентрировали, получая 1,19 г (количественный выход) заявленного в заголовке соединения в виде белого твердого остатка.
1H-ЯМР (300 MГц, CDCl3) дельта 8,88 (1H, д, J=1,5 Гц), 8,43 (1H, с), 8,26 (1H, с), 7,68 (1H, с), 3,97 (3H, с), 2,68 (3H, с), MS (ESI) m/z: 252 (M+H)+.
Стадия-2: 6-(4-хлор-1H-пиразол-1-ил)-5-метилникотиновая кислота
Заявленное в заголовке соединение получали с выходом 80% (904 мг, белый твердый остаток) из метил 6-(4-хлор-1H-пиразол-1-ил)-5-метилникотината (1,19 г, 4,7 ммоль, стадия-1) способом, аналогичным стадии-2 промежуточного соединения-A6.
1H-ЯМР (300 MГц, DMSO-d6) дельта 8,81 (1H, с), 8,69 (1H, с), 8,36 (1H, с), 7,99 (1H, с), 2,56 (3H, с) (сигнал COOH не наблюдали), MS (ESI) m/z: 236 (M-H)-.
Стадия-3: (6-(4-хлор-1H-пиразол-1-ил)-5-метилпиридин-3-ил)метанол
Заявленное в заголовке соединение получали с выходом 96% (791 мг, белый твердый остаток) из 6-(4-хлор-1H-пиразол-1-ил)-5-метилникотиновой кислоты (880 мг, 3,70 ммоль, стадия-2) способом, аналогичным стадии-2 промежуточного соединения-A3.
1H-ЯМР (300 MГц, CDCl3) дельта 8,28 (1H, ушир. с), 8,21 (1H, с), 7,70 (1H, ушир. с), 7,65 (1H, с), 4,76 (2H, д, J=5,3 Гц), 2,56 (3H, с), 1,93 (1H, т, J=5,3 Гц), MS (ESI) m/z: 224 (M+H)+.
Промежуточное соединение-A27: гидрохлорид 1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этанамина (один энантиомер; антипод промежуточного соединения-A7)
Стадия-1: (S)-2-метил-N-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)пропан-2-сульфинамид (один диастереомер)
Заявленное в заголовке соединение получали с выходом 83% (0,79 г, бесцветное масло) из 1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этанона (0,66 г, 2,81 ммоль, стадия-2 промежуточного соединения-A7) и (S)-2-метилпропан-2-сульфинамида способом, аналогичным стадии-3 промежуточного соединения-A7.
1H-ЯМР (300 MГц, CDCl3) дельта 7,93 (1H, д, J=1,84 Гц), 7,44 (1H, с), 4,76 (2H, к, J=8,4 Гц), 4,54-4,46 (1H, м), 3,32 (1H, д, J=2,6 Гц), 2,24 (3H, с), 1,51 (3H, д, J=6,6 Гц), 1,23 (9H, с), MS (ESI) m/z: 339 (M+H)+.
Стадия-2: гидрохлорид 1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этанамина (один энантиомер; антипод промежуточного соединения-A7)
Заявленное в заголовке соединение получали с выходом 88% (0,56 г, белый твердый остаток) из (S)-2-метил-N-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)пропан-2-сульфинамида (один диастереомер) (0,79 г, 2,33 ммоль, стадия-1) способом, аналогичным стадии-4 промежуточного соединения-A7.
1H-ЯМР (300 MГц, DMSO-d6) дельта 8,41 (2H, ушир. с), 8,13 (1H, д, J=2,2 Гц), 7,82 (1H, д, J=1,8 Гц), 5,02 (2H, к, J=9,2 Гц), 4,44-4,37 (1H, м), 2,19 (3H, с), 1,50 (3H, д, J=7,0 Гц), MS (ESI) m/z: 235 (M+H)+.
Промежуточное соединение-A28: (5-метил-6-(2-(2,2,2-трифторэтокси)этокси)пиридин-3-ил)метанол
Стадия-1: 5-метил-6-(2-(2,2,2-трифторэтокси)этокси)никотиновая кислота
Заявленное в заголовке соединение получали с выходом 73% (1,95 г, белый твердый остаток) из метил 6-фтор-5-метилникотината (1,60 г, 9,46 ммоль) и 2-(2,2,2-трифторэтокси)этанола (1,64 г, 11,4 ммоль) способом, аналогичным стадии-1 промежуточного соединения-A21.
1H-ЯМР (300 MГц, DMSO-d6) дельта 12,98 (1H, ушир. с), 8,55 (1H, с), 8,01 (1H, с), 4,52-4,49 (2H, м), 4,16 (2H, к, J=9,5 Гц), 3,98-3,95 (2H, м), 2,19 (3H, с), MS (ESI) m/z: 278 (M-H)-.
Стадия-2: (5-метил-6-(2-(2,2,2-трифторэтокси)этокси)пиридин-3-ил)метанол
Заявленное в заголовке соединение получали с выходом 85% (0,97 г, бесцветное масло) из 5-метил-6-(2-(2,2,2-трифторэтокси)этокси)никотиновой кислоты (1,2 г, 4,3 ммоль, стадия-1) способом, аналогичным стадии-2 промежуточного соединения-A3.
1H-ЯМР (300 MГц, DMSO-d6) дельта 7,89 (1H, с), 7,49 (1H, с), 5,12 (1H, т, J=5,8 Гц), 4,41-4,38 (4H, м), 4,13 (2H, к, J=9,5 Гц), 3,92 (2H, т, J=4,4 Гц), 2,14 (3H, с), MS (ESI) m/z: 266 (M+H)+.
Промежуточное соединение-A29: (5-метил-6-((2,2,2-трифторэтил)амино)пиридин-3-ил)метанол
Стадия-1: 5-метил-6-((2,2,2-трифторэтил)амино)никотиновая кислота
Смесь метил 6-фтор-5-метилникотината (2,00 г, 11,8 ммоль) и 2,2,2-трифторэтанамина (9,37 г, 95 ммоль) в N-метилпирролидоне (24 мл) перемешивали при 220°C в течение 2,5 часов при микроволновом облучении. Смесь разбавляли MeOH (30 мл) и добавляли к смеси 2 M водный раствор гидроксида натрия (15 мл). После перемешивания при 50°C в течение 1 часа, смесь подкисляли 2 M хлористоводородной кислотой и экстрагировали EtOAc/гексан (100 мл×3). Объединенный органический слой промывали водой (100 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток кристаллизовали из диизопропилового эфира, получая 884 мг (32%) заявленного в заголовке соединения в виде бледно-розового твердого остатка.
1H-ЯМР (300 MГц, DMSO-d6) дельта 8,49 (1H, с), 7,78 (1H, с), 7,17 (1H, т, J=6,6 Гц), 4,35-4,21 (2H, м), 2,14 (3H, с) (сигнал COOH не наблюдали), MS (ESI) m/z: 233 (M-H)-.
Стадия-2: (5-метил-6-((2,2,2-трифторэтил)амино)пиридин-3-ил)метанол
Заявленное в заголовке соединение получали с выходом 85% (623 мг, белый твердый остаток) из 5-метил-6-((2,2,2-трифторэтил)амино)никотиновой кислоты (780 мг, 3,3 ммоль, стадия-1), способом аналогичным стадии-2 промежуточного соединения-A3.
1H-ЯМР (300 MГц, CDCl3) дельта 7,99 (1H, ушир. с), 7,36 (1H, ушир. с), 4,56 (2H, д, J=5,5 Гц), 4,46-4,30 (1H, м), 4,30-4,21 (2H, м), 2,15 (3H, с), 1,51 (1H, т, J=5,5 Гц), MS (ESI) m/z: 221 (M+H)+.
Промежуточное соединение-A30: (3-метил-4-(трифторметокси)фенил)метанол
Стадия-1: этил 3-метил-4-(трифторметокси)бензоат
Заявленное в заголовке соединение получали с выходом 88% (1,72 г, бесцветное масло) из 4-бром-2-метил-1-(трифторметокси)бензола (2,00 г, 7,84 ммоль) способом, аналогичным стадии-2 промежуточного соединения-A14.
1H-ЯМР (300 MГц, CDCl3) дельта 7,95-7,88 (2H, м), 7,26-7,24 (1H, м), 4,38 (2H, к, J=7,3 Гц), 2,36 (3H, с), 1,40 (3H, т, J=7,3 Гц).
Стадия-2: (3-метил-4-(трифторметокси)фенил)метанол
Заявленное в заголовке соединение получали с выходом 93% (620 мг, бесцветное масло) из этил 3-метил-4-(трифторметокси)бензоата (0,80 г, 3,22 ммоль, стадия-1) способом, аналогичным стадии-2 промежуточного соединения-A1.
1H-ЯМР (300 MГц, CDCl3) дельта 7,35-7,15 (3H, м), 4,67 (2H, д, J=5,6 Гц), 2,32 (3H, с), 1,74 (1H, т, J=5,6 Гц).
Промежуточное соединение-A31: (2-(2,2,2-трифторэтокси)пиридин-4-ил)метанол
Заявленное в заголовке соединение получали с выходом 87% (816 мг, бесцветное масло) из 2-(2,2,2-трифторэтокси)изоникотиновой кислоты (1,00 г, 4,5 ммоль) способом, аналогичным стадии-2 промежуточного соединения-A3.
1H-ЯМР (300 MГц, CDCl3) дельта 8,10 (1H, д, J=5,1 Гц), 6,95 (1H, д, J=5,1 Гц), 6,88 (1H, с), 4,77 (2H, к, J=8,6 Гц), 4,72 (2H, д, J=5,8 Гц), 1,91 (1H, т, J=5,8 Гц), MS (ESI) m/z: 208 (M+H)+.
Промежуточное соединение-A32: (5-фенил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метанол
Стадия-1: метил 5-фенил-6-(2,2,2-трифторэтокси)никотинат
Смесь метил 5-бром-6-(2,2,2-трифторэтокси)никотината (2,00 г, 6,37 ммоль), фенилбороновой кислоты(932 мг, 7,64 ммоль), тетракис(трифенилфосфин)палладия (0) (368 мг, 0,32 ммоль) и бикарбоната натрия (1,07 г, 12,7 ммоль) в смеси диоксан-вода (10:1, 22 мл) кипятили с обратным холодильником при перемешивании в течение 18 часов. После охлаждения до комнатной температуры смесь выливали в воду (30 мл), и водный слой экстрагировали EtOAc (30 мл×3). Объединенный органический слой сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали колоночной хроматографией на силикагеле, элюируя н-гексаном/EtOAc (10:1), получая 1,99 г (количественный выход) заявленного в заголовке соединения в виде белого твердого остатка.
1H-ЯМР (300 MГц, CDCl3) дельта 8,78 (1H, д, J=2,2 Гц), 8,31 (1H, д, J=2,2 Гц), 7,57 (2H, д, J=6,6 Гц), 7,48-7,40 (3H, м), 4,88 (2H, к, J=8,0 Гц), 3,95 (3H, с), MS (ESI) m/z: 312 (M+H)+.
Стадия-2: (5-фенил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метанол
Заявленное в заголовке соединение получали с выходом 73% (1,26 г, белый твердый остаток) из метил 5-фенил-6-(2,2,2-трифторэтокси)никотината (1,90 г, 6,10 ммоль) способом, аналогичным стадии-2 промежуточного соединения-A1.
1H-ЯМР (300 MГц, CDCl3) дельта 8,10 (1H, д, J=2,2 Гц), 7,76 (1H, д, J=2,2 Гц), 7,6-7,3 (5H, м), 4,83 (2H, к, J=8,1 Гц), 4,72 (2H, с), 1,81 (1H, ушир. с), MS (ESI) m/z: 284 (M+H)+.
Промежуточное соединение-A33: (1-(2,2,2-трифторэтокси)изохинолин-4-ил)метанол
Стадия-1: метил 1-(2,2,2-трифторэтокси)изохинолин-4-карбоксилат
Заявленное в заголовке соединение получали с выходом 88% (1,14 г, белый твердый остаток) из метил 1-хлоризохинолин-4-карбоксилата (1,00 г, 4,5 ммоль) способом, аналогичным стадии-1 промежуточного соединения-A10.
1H-ЯМР (300 MГц, CDCl3) дельта 8,97 (1H, д, J=8,8 Гц), 8,77 (1H, с), 8,35 (1H, д, J=8,1 Гц), 7,87-7,81 (1H, м), 7,65 (1H, т, J=8,1 Гц), 5,01 (2H, к, J=8,1 Гц), 3,99 (3H, с), MS (ESI) m/z: 286 (M+H)+.
Стадия-2: (1-(2,2,2-трифторэтокси)изохинолин-4-ил)метанол
Заявленное в заголовке соединение получали с количественным выходом (0,88 г, белый твердый остаток) из метил 1-(2,2,2-трифторэтокси)изохинолин-4-карбоксилата (0,98 г, 3,4 ммоль, стадия-1) способом, аналогичным стадии-2 промежуточного соединения-A1.
1H-ЯМР (300 MГц, CDCl3) дельта 8,33 (1H, д, J=8,2 Гц), 8,12 (1H, д, J=8,2 Гц), 7,97 (1H, с), 7,83-7,78 (1H, м), 7,68-7,60 (1H, м), 5,02 (2H, д, J=5,9 Гц), 4,95 (2H, к, J=8,4 Гц), 1,68 (1H, т, J=5,9 Гц), MS (ESI) m/z: 258 (M+H)+.
Промежуточное соединение-A34: (5-(2,2-дифторэтокси)-4-метилпиридин-2-ил)метанамин
Стадия-1: 2-хлор-5-(2,2-дифторэтокси)-4-метилпиридин
Заявленное в заголовке соединение получали с выходом 95% (4,14 г, белый твердый остаток) из 6-хлор-4-метилпиридин-3-ола (3,0 г, 20,9 ммоль) и 2,2-дифторэтилтрифторметансульфоната (4,92 г, 23,0 ммоль) способом, аналогичным стадии-1 промежуточного соединения-A15.
1H-ЯМР (300 MГц, CDCl3) дельта, 7,89 (1H, с), 7,14 (1H, с), 6,11 (1H, тт, J=54,3, 4,4 Гц), 4,26 (2H, тд, J=13,2, 4,4 Гц), 2,26 (3H, с), MS (ESI) m/z: 208 (M+H)+.
Стадия-2: этил 5-(2,2-дифторэтокси)-4-метилпиколинат
Заявленное в заголовке соединение получали с выходом 87% (4,24 г, белый твердый остаток) из 2-хлор-5-(2,2-дифторэтокси)-4-метилпиридина (4,14 г, 19,9 ммоль, стадия-1) способом, аналогичным стадии-2 промежуточного соединения-A14.
1H-ЯМР (300 MГц, CDCl3) дельта, 8,24 (1H, с), 7,99 (1H, с), 6,14 (1H, тт, J=55,0, 4,4 Гц), 4,49-4,32 (4H, м), 2,32 (3H, с), 1,44 (3H, т, J=6,6 Гц), MS (ESI) m/z: 246 (M+H)+.
Стадия-3: (5-(2,2-дифторэтокси)-4-метилпиридин-2-ил)метанол
Смесь этил 5-(2,2-дифторэтокси)-4-метилпиколината (2,0 г, 8,2 ммоль, стадия-2) и хлорида кальция (3,62 г, 32,6 ммоль) в THF-EtOH (1:1, 60 мл) перемешивали при комнатной температуре в течение 30 минут. Затем, смесь охлаждали до 0°C, и добавляли порциями к ней боргидрид натрия (771 мг, 20,4 ммоль). После перемешивания в течение 1 дня, реакцию гасили насыщенным водным раствором хлорида аммония (200 мл), и водный слой экстрагировали DCM (200 мл×2). Объединенный органический слой сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали колоночной хроматографией на силикагеле, элюируя н-гексаном/EtOAc (10:1, затем только EtOAc), получая 1,61 г (97% выход) заявленного в заголовке соединения в виде белого твердого остатка.
1H-ЯМР (300 MГц, DMSO-d6) дельта 8,18 (1H, с), 7,26 (1H, с), 6,41 (1H, тт, J=54,2, 3,7 Гц), 5,31 (1H, т, J=5,9 Гц), 4,47-4,37 (4H, м), 2,21 (3H, с), MS (ESI) m/z: 204 (M+H)
Стадия-4: 2-((5-(2,2-дифторэтокси)-4-метилпиридин-2-ил)метил)изоиндолин-1,3-дион
Заявленное в заголовке соединение получали с выходом 74% (720 мг, белый твердый остаток) из (5-(2,2-дифторэтокси)-4-метилпиридин-2-ил)метанола (594 мг, 2,92 ммоль, стадия-3) и фталимида (473 мг, 3,22 ммоль) способом, аналогичным стадии-1 промежуточного соединения-A17.
1H-ЯМР (300 MГц, CDCl3) дельта 8,05 (1H, с), 7,91-7,86 (2H, м), 7,78-7,70 (2H, м), 7,12 (1H, с) 6,08 (1H, тт, J=54,9, 4,5 Гц), 4,93 (2H, с), 4,27-4,17 (2H, м), 2,23 (3H, с), MS (ESI) m/z: 333 (M+H)+.
Стадия-5: (5-(2,2-дифторэтокси)-4-метилпиридин-2-ил)метанамин
К суспензии 2-((5-(2,2-дифторэтокси)-4-метилпиридин-2-ил)метил)изоиндолин-1,3-диона (720 мг, 2,17 ммоль, стадия-4) в MeOH (30 мл) добавляли гидразингидрат (0,32 мл, 6,50 ммоль), и смесь перемешивали при 60°C в течение 5 часов. После удаления растворителя, к остатку добавляли 1 M водный раствор гидроксида натрия (100 мл), и водный слой экстрагировали DCM (100 мл), сушили над сульфатом натрия, фильтровали и концентрировали, получая 307 мг (70% выход) заявленного в заголовке соединения в виде бесцветного масла.
1H-ЯМР (300 MГц, DMSO-d6) дельта 8,19 (1H, с), 7,25 (1H, с), 6,40 (1H, тт, J=54,2, 3,6 Гц), 4,41 (тд, 1H, J=14,7 Гц, 3,6 Гц), 3,69 (2H, с), 2,19 (3H, с) (сигнал NH2 не наблюдали), MS (ESI) m/z: 203 (M+H)+.
Промежуточное соединение-A35: (1-метил-5-(трифторметокси)-1H-индол-2-ил)метанол
Стадия-1: этил 1-метил-5-(трифторметокси)-1H-индол-2-карбоксилат
Заявленное в заголовке соединение получали с выходом 99% (1,01 г, коричневое масло) из этил 5-(трифторметокси)-1H-индол-2-карбоксилата (975 мг, 3,6 ммоль, стадия-1) способом, аналогичным стадии-2 промежуточного соединения-A2.
1H-ЯМР (300 MГц, CDCl3) дельта 7,52 (1H, ушир. с), 7,40-7,34 (1H, м), 7,32-7,18 (2H, м), 4,39 (2H, к, J=7,0 Гц), 4,09 (3H, с), 1,42 (3H, т, J=7,0 Гц), MS (ESI) m/z: 288 (M+H)+.
Стадия-2: (1-метил-5-(трифторметокси)-1H-индол-2-ил)метанол
Заявленное в заголовке соединение получали с количественным выходом (0,88 г, белый твердый остаток) из этил 1-метил-5-(трифторметокси)-1H-индол-2-карбоксилата (0,96 г, 3,3 ммоль, стадия-1) способом, аналогичным стадии-2 промежуточного соединения-A1.
1H-ЯМР (300 MГц, CDCl3) дельта 7,44 (1H, с), 7,35-7,24 (1H, м), 7,20-7,05 (1H, м), 6,47 (1H, с), 4,81 (2H, д, J=5,6 Гц), 3,82 (3H, с), 1,63 (1H, т, J=5,6 Гц), MS (ESI) m/z: 246 (M+H)+.
Промежуточное соединение-A36: (3-хлор-4-(2,2-дифторэтокси)фенил)метанол
Стадия-1: метил 3-хлор-4-(2,2-дифторэтокси)бензоат
Заявленное в заголовке соединение получали с выходом 98% (2,0 г, белый твердый остаток) из метил 3-хлор-4-гидроксибензоата (1,5 г, 8,0 ммоль) способом, аналогичным стадии-1 промежуточного соединения-A17.
1H-ЯМР (300 MГц, CDCl3) дельта 8,09 (1H, д, J=2,2 Гц), 7,94 (1H, дд, J=8,8, 2,2 Гц), 6,94 (1H, д, J=8,0 Гц), 6,18 (1H, тт, J=54,9, 4,4 Гц), 4,30 (2H, тд, J=12,5, 4,4 Гц), 3,91 (3H, с).
Стадия-2: (3-хлор-4-(2,2-дифторэтокси)фенил)метанол
Заявленное в заголовке соединение получали с количественным выходом (860 мг, прозрачное бесцветное масло) из метил 3-хлор-4-(2,2-дифторэтокси)бензоата (930 мг, 3,7 ммоль, стадия-1) способом, аналогичным стадии-2 промежуточного соединения-A1.
1H-ЯМР (300 MГц, CDCl3) дельта 7,42 (1H, д, J=2,2 Гц), 7,22 (1H, дд, J=8,1, 2,2 Гц), 6,93 (1H, д, J=8,8 Гц), 6,15 (1H, тт, J=54,9, 4,4 Гц), 4,63 (2H, д, J=5,1 Гц), 4,24 (2H, тд, J=12,8, 4,4 Гц), 1,75-1,65 (1H, м).
Промежуточное соединение-A37: гидрохлорид 5-(хлорметил)-3-метил-2-((2,2,2-трифторэтокси)метил)пиридина
Стадия-1: диэтил 3-метилпиридин-2,5-дикарбоксилат
Заявленное в заголовке соединение получали с выходом 72% (2,05 г, желтое масло) из 2,5-дибром-3-метилпиридина (3,00 г, 12,0 ммоль) способом, аналогичным стадии-2 промежуточного соединения-A14.
1H-ЯМР (300 MГц, CDCl3) дельта 9,10 (1H, д, J=1,5 Гц), 8,21 (1H, с), 4,52-4,39 (4H, м), 2,62 (3H, с), 1,48-1,40 (6H, м), MS (ESI) m/z: 238 (M+H)+.
Стадия-2: этил 6-(гидроксиметил)-5-метилникотинат
Заявленное в заголовке соединение получали с выходом 74% (1,25 г, бледно-желтый твердый остаток) из диэтил 3-метилпиридин-2,5-дикарбоксилата (2,05 г, 8,6 ммоль) способом, аналогичным стадии-3 промежуточного соединения-A34.
1H-ЯМР (300 MГц, CDCl3) дельта 9,02 (1H, с), 8,08 (1H, с), 4,74 (2H, с), 4,42 (2H, к, J=7,3 Гц), 2,28 (3H, с), 1,42 (3H, т, J=7,3 Гц), MS (ESI) m/z: 196 (M+H)+.
Стадия-3: гидрохлорид этил 6-(хлорметил)-5-метилникотината
К раствору этил 6-(гидроксиметил)-5-метилникотината (1,25 г, 6,40 ммоль) в DCM (25 мл) добавляли тионилхлорид (0,93 мл, 12,8 ммоль) при 0°C. После перемешивания при комнатной температуре в течение 1 часа растворитель удаляли в вакууме, получая 1,37 г (количественный выход) заявленного в заголовке соединения в виде бледно-желтого твердого остатка.
MS (ESI) m/z: 214 (M+H)+.
Стадия-4: 5-метил-6-((2,2,2-трифторэтокси)метил)никотиновая кислота
К смеси 2,2,2-трифторэтанола (3,84 г, 38,4 ммоль) и карбоната цезия (8,33 г, 25,6 ммоль) в DMF (20 мл) добавляли гидрохлорид этил 6-(хлорметил)-5-метилникотината (1,37 г, 6,39 ммоль). После перемешивания при 40°C в течение 20 часов добавляли к смеси 2 M водный раствор гидроксида натрия (20 мл), воду (20 мл), THF (20 мл) и EtOH (20 мл). После перемешивания при 60°C в течение 3 часов, смесь подкисляли 2 M хлористоводородной кислотой (pH 4). Органический растворитель удаляли упариванием, и оставшийся водный слой экстрагировали EtOAc/гексаном. Отделенный органический слой промывали водой, сушили над сульфатом натрия и концентрировали в вакууме. Остаток кристаллизовали из гексана, получая 1,06 г (66%) заявленного в заголовке соединения в виде белого твердого остатка.
1H-ЯМР (300 MГц, DMSO-d6) дельта 8,85 (1H, д, J=1,5 Гц), 8,11 (1H, с), 4,84 (2H, с), 4,22-4,12 (2H, м), 2,40 (3H, с) (сигнал COOH не наблюдали), MS (ESI) m/z: 248(M-H)-.
Стадия-5: (5-метил-6-((2,2,2-трифторэтокси)метил)пиридин-3-ил)метанол
Заявленное в заголовке соединение получали с выходом 86% (843 мг, бесцветное масло) из 5-метил-6-((2,2,2-трифторэтокси)метил)никотиновой кислоты (1,04 г, 4,17 ммоль, стадия-4) способом, аналогичным стадии-2 промежуточного соединения-A3.
1H-ЯМР (300 MГц, CDCl3) дельта 8,37 (1H, д, J=1,4 Гц), 7,56 (1H, д, J=1,4 Гц), 4,82 (2H, с), 4,72 (2H, с), 3,88 (2H, к, J=8,8 Гц), 2,42 (3H, с), 2,21-2,02 (1H, м), MS (ESI) m/z: 236 (M+H)+.
Стадия-6: гидрохлорид 5-(хлорметил)-3-метил-2-((2,2,2-трифторэтокси)метил)пиридина
Заявленное в заголовке соединение получали с количественным выходом (830 мг, белый твердый остаток) из (5-метил-6-((2,2,2-трифторэтокси)метил)пиридин-3-ил)метанола (693 мг, 2,95 ммоль, стадия-5) способом, аналогичным стадии-3.
1H-ЯМР (300 MГц, CDCl3) дельта 8,71 (1H, с), 8,23 (1H, с), 5,28 (2H, с), 4,72 (2H, с), 4,17 (2H, к, J=8,4 Гц), 2,63 (3H, с), MS (ESI) m/z: 254 (M+H)+.
Промежуточное соединение-A38: 2-((3-фтор-5-(трифторметил)пиридин-2-ил)окси)этанол
Заявленное в заголовке соединение получали с выходом 64% (785 мг, бесцветное масло) из 2,3-дифтор-5-(трифторметил)пиридина (1,00 г, 5,46 ммоль) и этан-1,2-диола (678 мг, 10,9 ммоль) способом, аналогичным стадии-1 промежуточного соединения-A10.
1H-ЯМР (300 MГц, CDCl3) дельта 8,22 (1H, с), 7,57 (1H, дд, J=9,5, 1,5 Гц), 4,62-4,59 (2H, м), 4,05-4,00 (2H, м), 2,49 (1H, т, J=5,9 Гц), MS (ESI) m/z: 226 (M+H)+.
Промежуточное соединение-A39: (5-(2,2,3,3,3-пентафторпропокси)пиридин-2-ил)метанол
Стадия-1: 2-бром-5-(2,2,3,3,3-пентафторпропокси)пиридин
Заявленное в заголовке соединение получали с количественным выходом (2,11 г, желтый твердый остаток) из 6-бром-4-метилпиридин-3-ола (1,20 г, 6,90 ммоль) и трифторметансульфоната 2,2,3,3,3-пентафторпропила (13,8 ммоль) способом, аналогичным стадии-1 промежуточного соединения-A15.
1H-ЯМР (300 MГц, CDCl3) дельта 8,13 (1H, д, J=3,4 Гц), 7,45 (1H, д, J=8,8 Гц), 7,19 (1H, дд, J=8,8, 3,4 Гц), 4,46 (2H, т, J=11,4 Гц), MS (ESI) m/z: 306 (M+H)+.
Стадия-2: этил 5-(2,2,3,3,3-пентафторпропокси)пиколинат
Заявленное в заголовке соединение получали с выходом 72% (1,89 г, бледно-оранжевый твердый остаток) из 2-бром-5-(2,2,3,3,3-пентафторпропокси)пиридина (2,11 г, 6,9 ммоль) способом, аналогичным стадии-2 промежуточного соединения-A14.
1H-ЯМР (300 MГц, CDCl3) дельта 8,47 (1H, д, J=2,9 Гц), 8,16 (1H, д, J=8,6 Гц), 7,34 (1H, дд, J=8,6, 2,9 Гц), 4,60-4,40 (4H, м), 1,45 (3H, т, J=7,0 Гц), MS (ESI) m/z: 300 (M+H)+.
Стадия-3: (5-(2,2,3,3,3-пентафторпропокси)пиридин-2-ил)метанол
Заявленное в заголовке соединение получали с выходом 80% (847 мг, бесцветное масло) из этил 5-(2,2,3,3,3-пентафторпропокси)пиколината (1,23 г, 4,10 ммоль) способом, аналогичным стадии-3 промежуточного соединения-A34.
1H-ЯМР (300 MГц, CDCl3) дельта 8,31 (1H, д, J=2,6 Гц), 7,36-7,21 (2H, м), 4,74 (2H, д, J=4,9 Гц), 4,49 (2H, т, J=12,1 Гц), 3,34 (1H, т, J=4,9 Гц), MS (ESI) m/z: 258 (M+H)+.
Промежуточное соединение-A40: (4-(1,1,2,2-тетрафторэтокси)фенил)метанол
Заявленное в заголовке соединение получали с выходом 82% (464 мг, бесцветное масло) из 4-(1,1,2,2-тетрафторэтокси)бензойной кислоты (600 мг, 2,52 ммоль) способом, аналогичным стадии-2 промежуточного соединения-A3.
1H-ЯМР (300 MГц, CDCl3) дельта 7,39 (2H, д, J=8,4 Гц), 7,21 (2H, д, J=8,4 Гц), 5,91 (1H, тт, J=52,9, 2,9 Гц), 4,71 (2H, д, J=5,7 Гц), 1,74 (1H, т, J=5,7 Гц).
Промежуточное соединение-A41: (5-(2,2,3,3-тетрафторпропокси)пиридин-2-ил)метанол
Стадия-1: 2-бром-5-(2,2,3,3-тетрафторпропокси)пиридин
Заявленное в заголовке соединение получали с количественным выходом (2,25 г, желтый твердый остаток) из 6-бромпиридин-3-ола (1,30 г, 7,47 ммоль) и 2,2,3,3-тетрафторпропан-1-ола (3,94 г, 14,9 ммоль) способом, аналогичным стадии-1 промежуточного соединения-A15.
1H-ЯМР (300 MГц, CDCl3) дельта 8,12 (1H, д, J=2,9 Гц), 7,44 (1H, д, J=8,8 Гц), 7,16 (1H, дд, J=8,8, 2,9 Гц), 6,03 (1H, тт, J=52,7, 4,4 Гц), 4,40 (2H, т, J=11,7 Гц), MS (ESI) m/z: 288 и 290 (M+H)+.
Стадия-2: этил 5-(2,2,3,3-тетрафторпропокси)пиколинат
Заявленное в заголовке соединение получали с выходом 94% (2,07 г, бледно-желтый твердый остаток) из 2-бром-5-(2,2,3,3-тетрафторпропокси)пиридина (2,25 г, 7,81 ммоль, стадия-1) способом, аналогичным стадии-2 промежуточного соединения-A14.
1H-ЯМР (300 MГц, CDCl3) дельта 8,46 (1H, д, J=2,9 Гц), 8,16 (1H, д, J=8,8 Гц), 8,33 (1H, дд, J=8,8, 2,9 Гц), 6,06 (1H, тт, J=52,7, 4,4 Гц), 4,52-4,44 (4H, м), 1,45 (3H, т, J=6,6 Гц), MS (ESI) m/z: 282 (M+H)+.
Стадия-3: (5-(2,2,3,3-тетрафторпропокси)пиридин-2-ил)метанол
Заявленное в заголовке соединение получали с выходом 91% (717 мг, белый твердый остаток) из этил 5-(2,2,3,3-тетрафторпропокси)пиколината (923 мг, 3,28 ммоль, стадия-2) способом, аналогичным стадия-3 промежуточного соединения-A34.
1H-ЯМР (300 MГц, DMSO-d6) дельта 8,29 (1H, с), 7,57-7,40 (2H, м), 6,70 (1H, тт, J=52,0, 5,9 Гц), 5,37 (1H, т, J=5,9 Гц), 4,68 (2H, т, J=13,9 Гц), 4,50 (2H, д, J=5,9 Гц), MS (ESI) m/z: 240 (M+H)+.
Промежуточное соединение-A42: (5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метанол
Стадия-1: 5-хлор-6-(2,2,3,3-тетрафторпропокси)никотиновая кислота
Заявленное в заголовке соединение получали с выходом 97% (7,29 г, бледно-коричневый твердый остаток) из 5,6-дихлорникотиновой кислоты (5,00 г, 26,0 ммоль) и 2,2,3,3-тетрафторпропан-1-ола (5,16 г, 39,1 ммоль) способом, аналогичным стадии-1 промежуточного соединения-A3.
1H-ЯМР (300 MГц, CDCl3) дельта 8,77 (1H, д, J=1,5 Гц), 8,34 (1H, д, J=2,2 Гц), 6,08 (1H, тт, J=52,8, 4,5 Гц), 4,88 (2H, т, J=12,5 Гц) (сигнал COOH не наблюдали), MS (ESI) m/z: 286 (M-H)-.
Стадия-2: (5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метанол
Заявленное в заголовке соединение получали с выходом 96% (2,49 г, белый твердый остаток) из 5-хлор-6-(2,2,3,3-тетрафторпропокси)никотиновой кислоты (2,49 г, 8,66 ммоль, стадия-1) способом, аналогичным стадии-2 промежуточного соединения-A3.
1H-ЯМР (300 MГц, CDCl3) дельта 8,02 (1H, д, J=2,0 Гц), 7,71 (1H, д, J=2,0 Гц), 6,09 (1H, тт, J=52,9, 4,8 Гц), 4,78 (2H, тт, J=12,2, 1,5 Гц), 4,67 (2H, д, J=5,3 Гц), 1,80 (1H, т, J=5,3 Гц), MS (ESI) m/z: 274 (M+H)+.
Промежуточное соединение-A43: гидрохлорид 1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этанамина (один энантиомер)
Стадия-1: 4-метил-5-(2,2,2-трифторэтокси)пиколиновая кислота
Заявленное в заголовке соединение получали с выходом 92% (2,72 г, белый твердый остаток) из этил 4-метил-5-(2,2,2-трифторэтокси)пиколината (3,30 г, 12,5 ммоль, стадия-2 промежуточного соединения-A15) способом, аналогичным стадии-2 промежуточного соединения-A6.
1H-ЯМР (300 MГц, CDCl3) дельта 8,12 (1H, с), 8,09 (1H, с), 4,55 (2H, к, J=7,6 Гц), 2,39 (3H, с), сигнал COOH не наблюдали, MS (ESI) m/z: 236 (M+H)+, 234 (M-H)-.
Стадия-2: N-метокси-N,4-диметил-5-(2,2,2-трифторэтокси)пиколинамид
Заявленное в заголовке соединение получали с количественным выходом (1,6 г, грязно-белый твердый остаток) из 4-метил-5-(2,2,2-трифторэтокси)пиколиновой кислоты (1,0 г, 4,3 ммоль, стадия-1) способом, аналогичным стадии-1 промежуточного соединения-A7.
1H-ЯМР (300 MГц, CDCl3, добавляли 1 каплю DMSO-d6) дельта 8,14 (1H, с), 7,58 (1H, ушир. с), 4,51 (2H, к, J=8,1 Гц), 3,76 (3H, с), 3,41 (3H, с), 2,32 (3H, с), MS (ESI) m/z: 279 (M+H)+.
Стадия-3: 4-метил-5-(2,2,2-трифторэтокси)пиколинальдегид
Заявленное в заголовке соединение получали с выходом 95% (1,2 г, бледно-коричневый твердый остаток) из N-метокси-N,4-диметил-5-(2,2,2-трифторэтокси)пиколинамида (1,6 г, 5,8 ммоль, стадия-2) и алюмогидрида лития (80 мг, 2,9 ммоль) способом, аналогичным стадии-2 промежуточного соединения-A1.
1H-ЯМР (300 MГц, CDCl3) дельта 9,98 (1H, с), 8,29 (1H, с), 7,85 (1H, с), 4,57 (2H, к, J=8,1 Гц), 2,36 (3H, с), MS (ESI) m/z: 220 (M+H)+.
Стадия-4: (R,E)-2-метил-N-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метилен)пропан-2-сульфинамид (один энантиомер)
Смесь 4-метил-5-(2,2,2-трифторэтокси)пиколинальдегида (1,6 г, 7,3 ммоль, стадия-3), (R)-2-метилпропан-2-сульфинамида (1,33 г, 11,0 ммоль) и тетраэтоксида титана (2,50 г, 11,0 ммоль) в THF (30 мл) кипятили с обратным холодильником при перемешивании в течение 2 часов. После охлаждения до 0°C, добавляли к смеси воду (30 мл) и EtOAc (80 мл), и ее фильтровали через слой целита. Фильтрат промывали последовательно водой и соляным раствором, сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали колоночной хроматографией на силикагеле, элюируя н-гексаном/EtOAc (4:1-2:1), получая 1,14 г (48% выход) заявленного в заголовке соединения в виде бледно-желтого твердого остатка.
1H-ЯМР (300 MГц, CDCl3) дельта 8,62 (1H, с), 8,25 (1H, с), 7,88 (1H, с), 4,53 (2H, к, J=8,0 Гц), 2,36 (3H, с), 1,28 (9H, с), MS (ESI) m/z: 323 (M+H)+.
Стадия-5: (R)-2-метил-N-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)пропан-2-сульфинамид (один диастереомер)
К раствору (R,E)-2-метил-N-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метилен)пропан-2-сульфинамида (1,1 г, 3,4 ммоль, стадия-4) в DCM (50 мл) добавляли по каплям раствор метилмагнийбромида в THF (0,97 M, 7,0 мл, 6,8 ммоль) при -78°C. После перемешивания при -78°C в течение 1 часа, реакцию гасили насыщенным водным раствором хлорида аммония (100 мл). Водный слой экстрагировали DCM (100 мл×2). Объединенный органический слой промывали водой (100 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали колоночной хроматографией на силикагеле, элюируя н-гексаном/EtOAc (1:3), получая 1,09 г (94% выход) заявленного в заголовке соединения в виде бесцветного масла.
1H-ЯМР (300 MГц, CDCl3) дельта 8,08 (1H, с), 7,12 (1H, с), 4,65 (1H, д, J=5,4 Гц), 4,54-4,46 (1H, м), 4,42 (2H, к, J=7,9 Гц), 2,28 (3H, с), 1,48 (3H, д, J=6,6 Гц), 1,25 (9H, с), MS (ESI) m/z: 337 (M-H)-.
Стадия-6: гидрохлорид 1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этанамина (один энантиомер)
Заявленное в заголовке соединение получали с количественным выходом (1,1 г, белый твердый остаток) из (R)-2-метил-N-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)пропан-2-сульфинамида (1,1 г, 3,3 ммоль, стадия-5) способом, аналогичным стадии-4 промежуточного соединения-A7.
1H-ЯМР (300 MГц, DMSO-d6) дельта 8,42 (2H, ушир. с), 8,38 (1H, с), 7,43 (1H, с), 4,95 (2H, к, J=8,8 Гц), 4,50-4,38 (1H, м), 2,22 (3H, с), 1,45 (3H, д, J=6,6 Гц), MS (ESI) m/z: 235 (M+H)+.
Промежуточное соединение-A44: (5-метил-6-(3,3,3-трифторпропил)пиридин-3-ил)метанол
Стадия-1: метил 6-хлор-5-метилникотинат
Заявленное в заголовке соединение получали с выходом 93% (2,02 г, белый твердый остаток) из 6-хлор-5-метилникотиновой кислоты (2,00 г, 11,7 ммоль) способом, аналогичным стадии-2 промежуточного соединения-A2.
1H-ЯМР (300 MГц, CDCl3) дельта 8,83 (1H, с, J=2,2 Гц), 8,16 (1H, с), 3,95 (3H, с), 2,44 (3H, с), MS (ESI) m/z: 186 (M+H)+.
Стадия-2: метил 5-метил-6-(3,3,3-трифторпропил)никотинат
К суспензии порошкового цинка (2,49 г, 38,1 ммоль) в THF (15 мл) добавляли 1,2-дибромэтан (0,21 г, 1,1 ммоль) и триметилсилилхлорид (0,12 г, 1,1 ммоль). После перемешивания при комнатной температуре в течение 20 минут добавляли 1,1,1-трифтор-3-йодпропан (6,10 г, 27,2 ммоль), и смесь перемешивали при 55°C в течение 1 часа, получая раствор (3,3,3-трифторпропил)цинкйодида в THF. К смеси метил 6-хлор-5-метилникотината (2,02 г, 10,9 ммоль, стадия-1) и тетракис(трифенилфосфин)палладия (0) (1,01 г, 0,87 ммоль) в DMF (15 мл) добавляли цинковый реагент, и смесь перемешивали при 55°C в течение 12 часов. После охлаждения до комнатной температуры, смесь выливали в воду (100 мл), и водный слой экстрагировали EtOAc (30 мл×2).
Объединенный органический слой сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали колоночной хроматографией на силикагеле, элюируя н-гексаном/EtOAc (5:1 - только EtOAc), получая 2,32 г (86% выход) заявленного в заголовке соединения в виде оранжевого твердого остатка.
1H-ЯМР (300 MГц, CDCl3) дельта 8,97 (1H, д, J=1,5 Гц), 8,05 (1H, д, J=1,5 Гц), 3,94 (3H, с), 3,10-3,04 (2H, м), 2,76-2,62 (2H, м), 2,38 (3H, с), MS (ESI) m/z: 248 (M+H)+.
Стадия-3: (5-метил-6-(3,3,3-трифторпропил)пиридин-3-ил)метанол
Заявленное в заголовке соединение получали с количественным выходом (1,16 г, бледно-желтый твердый остаток) из метил 5-метил-6-(3,3,3-трифторпропил)никотината (1,30 г, 5,26 ммоль, стадия-2) способом, аналогичным стадии-2 промежуточного соединения-A1.
1H-ЯМР (300 MГц, CDCl3) дельта 8,31 (1H, с), 7,49 (1H, с), 4,67 (2H, д, J=5,9 Гц), 3,03-2,98 (2H, м), 2,68-2,51 (2H, м), 2,33 (4H, с), MS (ESI) m/z: 220 (M+H)+.
Промежуточное соединение-A45: (4-метил-5-(3,3,3-трифторпропокси)пиридин-2-ил)метанол
Стадия-1: 2-хлор-4-метил-5-(3,3,3-трифторпропокси)пиридин
Заявленное в заголовке соединение получали с количественным выходом (3,64 г, бледно-желтый твердый остаток) из 6-хлор-4-метилпиридин-3-ола (3,00 г, 20,9 ммоль) и 3,3,3-трифторпропан-1-ола (5,72 г, 50,1 ммоль) способом, аналогичным стадии-1 промежуточного соединения-A17.
1H-ЯМР (300 MГц, CDCl3) дельта, 7,87 (1H, с), 7,12 (1H, с), 4,27 (2H, т, J=6,6 Гц), 2,78-2,59 (2H, м), 2,22 (3H, с), MS (ESI) m/z: 240 (M+H)+.
Стадия-2: этил 4-метил-5-(3,3,3-трифторпропокси)пиколинат
Заявленное в заголовке соединение получали с выходом 93% (3,92 г, бледно-желтый твердый остаток) из 2-хлор-4-метил-5-(3,3,3-трифторпропокси)пиридина (3,64 г, 15,2 ммоль, стадия-1) способом, аналогичным стадии-2 промежуточного соединения-A14.
1H-ЯМР (300 MГц, CDCl3) дельта, 8,24 (1H, с), 7,97 (1H, с), 4,49-4,36 (4H, м), 2,78-2,62 (2H, м), 2,29 (3H, с), 1,44 (3H, т, J=6,6 Гц), MS (ESI) m/z: 278 (M+H)+.
Стадия-3: (4-метил-5-(3,3,3-трифторпропокси)пиридин-2-ил)метанол
Заявленное в заголовке соединение получали с выходом 93% (807 мг, белый твердый остаток) из этил 4-метил-5-(3,3,3-трифторпропокси)пиколината (1,0 г, 3,6 ммоль, стадия-2) способом, аналогичным стадии-3 промежуточного соединения-A34.
1H-ЯМР (300 MГц, DMSO-d6) дельта 8,16 (1H, с), 7,26 (1H, с), 5,28 (1H, т, J=5,8 Гц), 4,45 (2H, д, J=5,8 Гц), 4,30 (2H, т, J=5,8 Гц), 2,89-2,74 (2H, м), 2,17 (3H, с), MS (ESI) m/z: 236 (M+H)+.
Промежуточное соединение-A46: (5-хлор-6-(2,2-дифторпропокси)пиридин-3-ил)метанол
Стадия-1: 5-хлор-6-(2,2-дифторпропокси)никотиновая кислота
Заявленное в заголовке соединение получали с выходом 85% (1,12 г, бесцветное масло) из 5,6-дихлорникотиновой кислоты (1,00 г, 5,21 ммоль) и 2,2-дифторпропан-1-ола (0,50 г, 5,21 ммоль) способом, аналогичным стадии-1 промежуточного соединения-A3.
1H-ЯМР (300 MГц, CDCl3) дельта 8,77 (1H, д, J=2,2 Гц), 8,31 (1H, д, J=2,2 Гц), 4,64 (2H, т, J=11,7 Гц), 1,80 (3H, т, J=18,3 Гц), (сигнал COOH не наблюдали), MS (ESI) m/z: 252 (M+H)+.
Стадия-2: (5-хлор-6-(2,2-дифторпропокси)пиридин-3-ил)метанол
Заявленное в заголовке соединение получали с выходом 73% (689 мг, бесцветное масло) из 5-хлор-6-(2,2-дифторпропокси)никотиновой кислоты (1,00 г, 3,97 ммоль, стадия-1) способом, аналогичным стадии-2 промежуточного соединения-A3.
1H-ЯМР (300 MГц, CDCl3) дельта 8,00 (1H, с), 7,74 (1H, д, J=1,5 Гц), 4,65 (2H, т, J=5,9 Гц), 4,55 (2H, д, J=11,7 Гц), 1,78 (3H, т, J=19,1 Гц), 1,6-1,5 (1H, м), MS (ESI) m/z: 238(M+H)+.
Промежуточное соединение-A47: (5-хлор-6-(3,3,3-трифторпропокси)пиридин-3-ил)метанол
Стадия-1: 5-хлор-6-(3,3,3-трифторпропокси)никотиновая кислота
1H-ЯМР (300 MГц, CDCl3) дельта 8,77 (1H, д, J=2,2 Гц), 8,29 (1H, д, J=1,5 Гц), 4,72 (2H, т, J=6,6 Гц), 2,78-2,63 (2H, м) (сигнал COOH не наблюдали), MS (ESI) m/z: 270 (M+H)+.
Стадия-2: (5-хлор-6-(3,3,3-трифторпропокси)пиридин-3-ил)метанол
1H-ЯМР (300 MГц, CDCl3) дельта 8,00 (1H, д, J=1,8 Гц), 7,72 (1H, д, J=1,8 Гц), 4,75-4,55 (4H, м), 2,76-2,56 (2H, м), 1,80 (1H, ушир. с), MS (ESI) m/z: 256 (M+H)+.
Промежуточное соединение-A48: 1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этанол
К раствору 1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этанона (3,41 г, 14,6 ммоль, стадия-2 промежуточного соединения-A7) в MeOH (70 мл) добавляли боргидрид натрия (1,11 г, 29,2 ммоль) при 0°C, и смесь перемешивали при комнатной температуре в течение 3 часов. Затем, реакцию гасили водой, и смесь фильтровали через слой целита. Фильтрат экстрагировали EtOAc, сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали колоночной хроматографией на силикагеле, элюируя EtOAc, получая 3,39 г (99%) заявленного в заголовке соединения в виде бесцветного масла.
1H-ЯМР (300 MГц, CDCl3) дельта 7,93 (1H, с), 7,52 (1H, с), 4,93-4,83 (1H, м), 4,76 (2H, к, J=8,8 Гц), 2,24 (3H, с), 1,49 (3H, д, J=5,9 Гц), MS (ESI) m/z: 236 (M+H)+.
Промежуточное соединение-A49: гидрохлорид (4-метил-5-(2,2,3,3-тетрафторпропокси)пиридин-2-ил)метанамина
Стадия-1: 2-хлор-4-метил-5-(2,2,3,3-тетрафторпропокси)пиридин
К смеси 6-хлор-4-метилпиридин-3-ола (5,00 г, 34,8 ммоль) и карбоната цезия (34,0 г, 104 ммоль) в DMF (140 мл) добавляли 1,1,2,2-тетрафтор-3-йодпропан (16,9 г, 69,7 ммоль), и смесь перемешивали при 90°С в течение 19 часов. После охлаждения до комнатной температуры, смесь выливали в воду (500 мл), и водный слой экстрагировали EtOAc/гексаном (3:1, 500 мл). Отделенный органический слой промывали водой (300 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали хроматографией на силикагеле, элюируя н-гексаном/EtOAc (20:1-4:1), получая 7,97 г (89% выход) заявленного в заголовке соединения в виде бледно-желтого твердого остатка.
1H-ЯМР (300 MГц, CDCl3) дельта 7,91 (1H, с), 7,16 (1H, с), 6,02 (1H, тт, J=53,1, 4,0 Гц), 4,43 (2H, т, J=11,7 Гц), 2,26 (3H, с), MS (ESI) m/z: 258 (M+H)+.
Стадия-2: этил 4-метил-5-(2,2,3,3-тетрафторпропокси)пиколинат
Заявленное в заголовке соединение получали с выходом 90% (5,55 г, белый твердый остаток) из 2-хлор-4-метил-5-(2,2,3,3-тетрафторпропокси)пиридина (5,39 г, 20,9 ммоль, стадия-1) способом, аналогичным стадии-2 промежуточного соединения-A14.
1H-ЯМР (300 MГц, CDCl3) дельта 8,26 (1H, с), 8,00 (1H, с), 6,04 (1H, тт, J=53,1, 4,0 Гц), 4,60-4,35 (4H, м), 2,32 (3H, с), 1,44 (3H, т, J=7,1 Гц), MS (ESI) m/z: 296 (M+H)+.
Стадия-3: (4-метил-5-(2,2,3,3-тетрафторпропокси)пиридин-2-ил)метанол
Заявленное в заголовке соединение получали с выходом 80% (1,36 г, бесцветное масло) из этил 4-метил-5-(2,2,3,3-тетрафторпропокси)пиколината (2,00 г, 6,77 ммоль, стадия-2) способом, аналогичным стадии-3 промежуточного соединения-A34.
1H-ЯМР (300 MГц, CDCl3) дельта 8,10 (1H, с), 7,10 (1H, с), 6,05 (1H, тт, J=53,0, 4,4 Гц), 4,68 (2H, с), 4,45 (2H, т, J=11,7 Гц), 3,58 (1H, ушир. с), 2,28 (3H, с), MS (ESI) m/z: 254 (M+H)+.
Стадия-4: 2-((4-метил-5-(2,2,3,3-тетрафторпропокси)пиридин-2-ил)метил)изоиндолин-1,3-дион
Заявленное в заголовке соединение получали с выходом 82% (1,70 г, белый твердый остаток) из (4-метил-5-(2,2,3,3-тетрафторпропокси)пиридин-2-ил)метанола (1,36 г, 5,39 ммоль, стадия-3) и фталимида (873 мг, 5,93 ммоль) способом, аналогичным стадии-1 промежуточного соединения-A17.
1H-ЯМР (300 MГц, CDCl3) дельта 8,06 (1H, с), 7,93-7,83 (2H, м), 7,79-7,70 (2H, м), 7,14 (1H, с), 6,02 (1H, тт, J=53,1, 4,4 Гц), 4,93 (2H, с), 4,39 (2H, т, J=11,7 Гц), 2,28 (3H, с), MS (ESI) m/z: 383 (M+H)+.
Стадия-5: гидрохлорид (4-метил-5-(2,2,3,3-тетрафторпропокси)пиридин-2-ил)метанамина
Заявленное в заголовке соединение получали с выходом >99% (1,35 г, белый твердый остаток) из 2-((4-метил-5-(2,2,3,3-тетрафторпропокси)пиридин-2-ил)метил)изоиндолин-1,3-диона (1,70 г, 4,44 ммоль, стадия-4) способом, аналогичным стадии-5 промежуточного соединения-A34.
1H-ЯМР (300 MГц, DMSO-d6) дельта 8,45 (3H, ушир. с), 8,41 (1H, с), 7,43 (1H, с), 6,74 (1H, тт, J=51,6, 5,5 Гц), 4,80 (2H, т, J=13,2 Гц), 4,15-4,03 (2H, м), 2,25 (3H, с), MS (ESI) m/z: 253 (M+H)+.
Промежуточное соединение-A50: гидрохлорид (5-хлор-6-(циклопропилметокси)пиридин-3-ил)метанамина
Стадия-1: 5-хлор-6-(циклопропилметокси)никотиновая кислота
Заявленное в заголовке соединение получали с выходом 98% (4,65 г, белый твердый остаток) из 5,6-дихлорникотиновой кислоты (4,00 г, 20,8 ммоль) и циклопропилметанола (2,25 г, 31,3 ммоль) способом, аналогичным стадии-1 промежуточного соединения-A3.
1H-ЯМР (300 MГц, DMSO-d6) дельта 8,63 (1H, д, J=2,2 Гц), 8,22 (1H, д, J=2,2 Гц), 4,28 (2H, д, J=7,3 Гц), 1,38-1,20 (1H, м), 0,63-0,54 (2H, м), 0,42-0,34 (2H, м), (сигнал COOH не наблюдали), MS (ESI) m/z: 226 (M-H)-.
Стадия-2: (5-хлор-6-(циклопропилметокси)пиридин-3-ил)метанол
Заявленное в заголовке соединение получали с выходом 80% (1,50 г, бесцветное масло) из 5-хлор-6-(циклопропилметокси)никотиновой кислоты (2,00 г, 8,79 ммоль, стадия-1) способом, аналогичным стадии-2 промежуточного соединения-A3.
1H-ЯМР (300 MГц, CDCl3) дельта 7,98 (1H, д, J=2,2 Гц), 7,70 (1H, д, J=2,2 Гц), 4,62 (2H, д, J=5,5 Гц), 4,22 (2H, д, J=7,0 Гц), 1,71 (1H, т, J=5,6 Гц), 1,42-1,20 (1H, м), 0,66-0,51 (2H, м), 0,47-0,33 (2H, м), MS (ESI) m/z: 214 (M+H)+.
Стадия-3: 2-((5-хлор-6-(циклопропилметокси)пиридин-3-ил)метил)изоиндолин-1,3-дион
Заявленное в заголовке соединение получали с выходом 74% (1,79 г, белый твердый остаток) из (5-хлор-6-(циклопропилметокси)пиридин-3-ил)метанола (1,50 г, 7,00 ммоль, стадия-2) и фталимида (1,13 г, 7,70 ммоль) способом, аналогичным стадии-1 промежуточного соединения-A17.
1H-ЯМР (300 MГц, CDCl3) дельта 8,12 (1H, д, J=2,2 Гц), 7,90-7,80 (2H, м), 7,76-7,70 (3H, м), 4,76 (2H, с), 4,19 (2H, д, J=7,4 Гц), 1,35-1,24 (1H, м), 0,69-0,50 (2H, м), 0,43-0,31 (2H, м), MS (ESI) m/z: 343 (M+H)+.
Стадия-4: гидрохлорид (5-хлор-6-(циклопропилметокси)пиридин-3-ил)метанамина
Заявленное в заголовке соединение получали с выходом 86% (1,12 г, белый твердый остаток) из 2-((5-хлор-6-(циклопропилметокси)пиридин-3-ил)метил)изоиндолин-1,3-диона (1,79 г, 5,23 ммоль, стадия-3) способом, аналогичным стадии-5 промежуточного соединения-A34.
1H-ЯМР (300 MГц, DMSO-d6) дельта 8,33 (3H, ушир. с), 8,19 (1H, д, J=1,8 Гц), 8,07 (1H, д, J=1,8 Гц), 4,20 (2H, д, J=7,3 Гц), 4,05-3,94 (2H, м), 1,32-1,20 (1H, м), 0,61-0,51 (2H, м), 0,39-0,31 (2H, м), MS (ESI) m/z: 213 (M+H)+.
Промежуточное соединение-A51: гидрохлорид 1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этанамина (один энантиомер) (антипод промежуточного соединения-A43)
Заявленное в заголовке соединение получали согласно способу промежуточного соединения-A43, применяя (S)-2-метилпропан-2-сульфинамид вместо (R)-2-метилпропан-2-сульфинамида.
Промежуточное соединение-A52: гидрохлорид (3-хлор-4-(2,2,2-трифторэтокси)фенил)метанамина
Стадия-1: (3-хлор-4-(2,2,2-трифторэтокси)фенил)метанол
Заявленное в заголовке соединение получали с выходом 69% (767 мг, бесцветное масло) из 3-хлор-4-(2,2,2-трифторэтокси)бензойной кислоты (1,18 г, 4,63 ммоль) способом, аналогичным стадии-2 промежуточного соединения-A3.
1H-ЯМР (300 MГц, CDCl3) дельта 7,43 (1H, д, J=2,2 Гц), 7,26-7,22 (1H, м), 6,97 (1H, д, J=8,1 Гц), 4,65 (2H, д, J=5,9 Гц), 4,41 (2H, к, J=8,1 Гц), 1,71 (1H, т, J=5,5 Гц).
Стадия-2: 2-(3-хлор-4-(2,2,2-трифторэтокси)бензил)изоиндолин-1,3-дион
Заявленное в заголовке соединение получали с выходом 77% (894 мг, белый твердый остаток) из (3-хлор-4-(2,2,2-трифторэтокси)фенил)метанола (760 мг, 3,16 ммоль, стадия-1) способом, аналогичным стадии-1 промежуточного соединения-A17.
1H-ЯМР (300 MГц, CDCl3) дельта 7,89-7,73 (2H, м), 7,74-7,71(2H, м), 7,50 (1H, д, J=2,2 Гц) 7,33 (1H, дд, J=8,1, 2,2 Гц), 6,91 (1H, д, J=8,1 Гц), 4,78 (2H, с), 4,36 (2H, к, J=8,1 Гц).
Стадия-3: гидрохлорид (3-хлор-4-(2,2,2-трифторэтокси)фенил)метанамина
Заявленное в заголовке соединение получали с выходом 89% (593 мг, грязно-белый твердый остаток) из 2-(3-хлор-4-(2,2,2-трифторэтокси)бензил)изоиндолин-1,3-диона (890 мг, 2,41 ммоль, стадия-2) способом, аналогичным стадии-5 промежуточного соединения-A34.
1H -ЯМР (300 MГц, DMSO-d6) дельта 8,47 (3H, ушир. с), 7,68 (1H, с), 7,48 (1H, д, J=8,8 Гц), 7,33 (1H, д, J=8,8 Гц), 4,91 (2H, к, J=8,8 Гц), 3,98 (2H, д, J=5,1 Гц), MS (ESI) m/z: наблюдали положительный ион сигнала фрагмента 223.
Промежуточное соединение-A53: гидрохлорид (6-((4-фторбензил)окси)-5-метилпиридин-3-ил)метанамина
Стадия-1: 6-((4-фторбензил)окси)-5-метилникотиновая кислота
Заявленное в заголовке соединение получали с выходом 69% (4,26 г, белый твердый остаток) из метил 6-фтор-5-метилникотината (4,00 г, 23,7 ммоль) способом, аналогичным стадии-1 промежуточного соединения-A21.
1H-ЯМР (300 MГц, CDCl3/DMSO-d6) дельта 8,69 (1H, д, J=2,2 Гц), 8,01 (1H, д, J=2,2 Гц), 7,45 (2H, дд, J=8,0, 5,1 Гц), 7,06 (2H, т, J=8,8 Гц), 5,43 (2H, с), 2,24 (3H, с), (сигнал COOH не наблюдали), MS (ESI) m/z: 260 (M-H)-.
Стадия-2: (6-((4-фторбензил)окси)-5-метилпиридин-3-ил)метанол
Заявленное в заголовке соединение получали с выходом 91% (1,30 г, белый твердый остаток) из 6-((4-фторбензил)окси)-5-метилникотиновой кислоты (1,50 г, 5,74 ммоль, стадия-1) способом, аналогичным стадии-2 промежуточного соединения-A3.
1H-ЯМР (300 MГц, CDCl3) дельта 7,96 (1H, д, J=1,9 Гц), 7,51-7,38 (3H, м), 7,12-7,01 (2H, м), 5,37 (2H, с), 4,60 (2H, д, J=2,2 Гц), 2,23 (3H, с), 1,68 (1H, ушир. с), MS (ESI) m/z: 248 (M+H)+.
Стадия-3: 2-((6-((4-фторбензил)окси)-5-метилпиридин-3-ил)метил)изоиндолин-1,3-дион
Заявленное в заголовке соединение получали с выходом 74% (1,46 г, белый твердый остаток) из (6-((4-фторбензил)окси)-5-метилпиридин-3-ил)метанола (1,30 г, 5,25 ммоль, стадия-2) способом, аналогичным стадии-1 промежуточного соединения-A17.
1H-ЯМР (300 MГц, CDCl3) дельта 8,03 (1H, д, J=2,2 Гц), 7,83-7,70 (2H, м), 7,68-7,60 (2H, м), 7,44 (1H, д, J=1,4 Гц), 7,38-7,30 (2H, м), 7,02-6,90 (2H, м), 5,26 (2H, с), 4,68 (2H, с), 2,11 (3H, с), MS (ESI) m/z: 377 (M+H)+.
Стадия-4: гидрохлорид (6-((4-фторбензил)окси)-5-метилпиридин-3-ил)метанамина
Заявленное в заголовке соединение получали с выходом 92% (1,01 г, бледно-желтый твердый остаток) из 2-((6-((4-фторбензил)окси)-5-метилпиридин-3-ил)метил)изоиндолин-1,3-диона (1,46 г, 3,88 ммоль, стадия-3) способом, аналогичным стадии-5 промежуточного соединения-A34.
1H-ЯМР (300 MГц, DMSO-d6) дельта 8,24 (3H, ушир. с), 8,07 (1H, д, J=1,8 Гц), 7,70 (1H, д, J=1,8 Гц), 7,55-7,43 (2H, м), 7,26-7,15 (2H, м), 5,38 (2H, с), 3,99-3,90 (2H, м), 2,19 (3H, с), MS (ESI) m/z: 247 (M+H)+.
Промежуточное соединение-A54: гидрохлорид (6-циклобутокси-5-метилпиридин-3-ил)метанамина
Стадия-1: 6-циклобутокси-5-метилникотиновая кислота
Заявленное в заголовке соединение получали с выходом 88% (1,18 г, белый твердый остаток) из 6-фтор-5-метилникотиновой кислоты (1,00 г, 6,45 ммоль) и циклобутанола (837 мг, 11,6 ммоль) способом, аналогичным стадии-1 промежуточного соединения-A1.
1H-ЯМР (300 MГц, DMSO-d6) дельта 8,50 (1H, с), 7,97 (1H, с), 5,21 (1H, квинтeт, J=7,3 Гц), 2,48-2,35 (2H, м), 2,16 (3H, с), 2,15-1,99 (2H, м), 1,84-1,57 (2H, м), (сигнал COOH не наблюдали), MS (ESI) m/z: 208 (M+H)+.
Стадия-2: (6-циклобутокси-5-метилпиридин-3-ил)метанол
Заявленное в заголовке соединение получали с выходом 87% (2,22 г, белый твердый остаток) из 6-циклобутокси-5-метилникотиновой кислоты (2,74 г, 13,2 ммоль, стадия-1) способом, аналогичным стадии-2 промежуточного соединения-A3.
1H-ЯМР (300 MГц, CDCl3) дельта 7,91 (1H, с), 7,43 (1H, с), 5,21 (1H, квинтeт, J=7,3 Гц), 4,57 (2H, д, J=5,1 Гц), 2,58-2,41 (2H, м), 2,32-2,04 (3H, м), 2,19 (3H, с), 1,91-1,58 (2H, м), MS (ESI) m/z: 194 (M+H)+.
Стадия-3: 2-((6-циклобутокси-5-метилпиридин-3-ил)метил)изоиндолин-1,3-дион
Заявленное в заголовке соединение получали с выходом 83% (3,07 г, белый твердый остаток) из (6-циклобутокси-5-метилпиридин-3-ил)метанола (2,22 г, 11,5 ммоль, стадия-2) способом, аналогичным стадии-1 промежуточного соединения-A17.
1H-ЯМР (300 MГц, CDCl3) дельта 8,05 (1H, д, J=1,8 Гц), 7,92-7,78 (2H, м), 7,74-7,68 (2H, м), 7,46 (1H, д, J=1,8 Гц), 5,17 (1H, квинтeт, J=7,3 Гц), 4,73 (2H, с), 2,49-2,36 (2H, м), 2,20-2,00 (2H, м), 2,14 (3H, с), 1,86-1,56 (2H, м), MS (ESI) m/z: 323 (M+H)+.
Стадия-4: гидрохлорид (6-циклобутокси-5-метилпиридин-3-ил)метанамина
Заявленное в заголовке соединение получали с выходом 96% (2,10 г, белый твердый остаток) из 2-((6-циклобутокси-5-метилпиридин-3-ил)метил)изоиндолин-1,3-диона (3,07 г, 9,52 ммоль, стадия-3) способом, аналогичным стадии-5 промежуточного соединения-A34.
1H-ЯМР (300 MГц, DMSO-d6) дельта 8,21 (3H, ушир. с), 8,02 (1H, с), 7,65 (1H, с), 5,15 (1H, квинтeт, J=7,0 Гц), 4,00-3,88 (2H, м), 2,48-2,33 (2H, м), 2,14 (3H, с), 2,11-1,95 (2H, м), 1,84-1,55 (2H, м), MS (ESI) m/z: 193 (M+H)+.
Промежуточное соединение-A55: гидрохлорид (5-(циклопропилметокси)-4-метилпиридин-2-ил)метанамина
Стадия-1: 2-хлор-5-(циклопропилметокси)-4-метилпиридин
Заявленное в заголовке соединение получали с выходом 86% (3,57 г, бесцветное масло) из 6-хлор-4-метилпиридин-3-ола (3,00 г, 20,9 ммоль) и (бромметил)циклопропана (3,39 г, 25,1 ммоль) способом, аналогичным стадии-1 промежуточного соединения-A15.
1H-ЯМР (300 MГц, CDCl3) дельта 7,84 (1H, с), 7,10 (1H, с), 3,88 (2H, д, J=6,6 Гц), 2,25 (3H, с), 1,37-1,22 (1H, м), 0,72-0,62 (2H, м), 0,43-0,33 (2H, м), MS (ESI) m/z: 198 (M+H)+.
Стадия-2: этил 5-(циклопропилметокси)-4-метилпиколинат
Заявленное в заголовке соединение получали с выходом 52% (2,21 г, белый твердый остаток) из 2-хлор-5-(циклопропилметокси)-4-метилпиридина (3,57 г, 18,1 ммоль, стадия-1) способом, аналогичным стадии-2 промежуточного соединения-A14.
1H-ЯМР (300 MГц, CDCl3) дельта 8,21 (1H, с), 7,95 (1H, с), 4,44 (2H, к, J=6,6 Гц), 3,99 (2H, д, J=6,6 Гц), 2,31 (3H, с), 1,43 (3H, т, J=6,6 Гц), 1,39-1,23 (1H, м), 0,72-0,63 (2H, м), 0,45-0,36 (2H, м), MS (ESI) m/z: 236 (M+H)+.
Стадия-3: (5-(циклопропилметокси)-4-метилпиридин-2-ил)метанол
Заявленное в заголовке соединение получали с выходом 73% (597 мг, бесцветное масло) из этил 5-(циклопропилметокси)-4-метилпиколината (1,00 г, 4,25 ммоль, стадия-2) способом, аналогичным стадии-3 промежуточного соединения-A34.
1H-ЯМР (300 MГц, CDCl3) дельта 8,05 (1H, с), 7,03 (1H, с), 4,62 (2H, с), 3,90 (2H, д, J=6,6 Гц), 2,27 (3H, с), 1,35-1,20 (1H, м), 0,69-0,60 (2H, м), 0,41-0,32 (2H, м), MS (ESI) m/z: 194 (M+H)+.
Стадия-4: 2-((5-(циклопропилметокси)-4-метилпиридин-2-ил)метил)изоиндолин-1,3-дион
Заявленное в заголовке соединение получали с выходом 77% (767 мг, белый твердый остаток) из (5-(циклопропилметокси)-4-метилпиридин-2-ил)метанола (597 мг, 3,09 ммоль, стадия-3) и фталимида (500 мг, 3,40 ммоль) способом, аналогичным стадии-1 промежуточного соединения-A17.
1H-ЯМР (300 MГц, CDCl3) дельта 8,03 (1H, с), 7,90-7,82 (2H, м), 7,78-7,65 (2H, м), 7,09 (1H, с), 4,91 (2H, с), 3,85 (2H, д, J=6,6 Гц), 2,22 (3H, с), 1,39-1,18 (1H, м), 0,68-0,55 (2H, м), 0,38-0,28 (2H, м), MS (ESI) m/z: 323 (M+H)+.
Стадия-5: гидрохлорид (5-(циклопропилметокси)-4-метилпиридин-2-ил)метанамина
Заявленное в заголовке соединение получали с выходом >99% (581 мг, белый твердый остаток) из 2-((5-(циклопропилметокси)-4-метилпиридин-2-ил)метил)изоиндолин-1,3-диона (767 мг, 2,38 ммоль, стадия-4) способом, аналогичным стадии-5 промежуточного соединения-A34.
1H-ЯМР (300 MГц, DMSO-d6) дельта 8,39 (3H, ушир. с), 8,27 (1H, с), 7,43 (1H, с), 4,18-4,01 (2H, м), 4,00 (2H, д, J=6,9 Гц), 2,24 (3H, с), 1,30-1,19 (1H, м), 0,64-0,53 (2H, м), 0,41-0,30 (2H, м), MS (ESI) m/z: 193 (M+H)+.
Промежуточное соединение-A56: (5-метил-6-(2,2,3,3-тетрафторпропокси)пиридазин-3-ил)метанол
Стадия-1: Смесь 6-хлор-4-метил-3-(2,2,3,3-тетрафторпропокси)пиридазина и 3-хлор-4-метил-6-(2,2,3,3-тетрафторпропокси)пиридазина (приблизительно 1,5:1)
Заявленное в заголовке соединение получали с выходом 85% (5,42 г, бесцветное масло) из 3,6-дихлор-4-метилпиридазина (4,00 г, 24,5 ммоль) и 2,2,3,3-тетрафторпропан-1-ола (3,56 г, 27,0 ммоль) способом, аналогичным стадии-1 промежуточного соединения-A14. MS (ESI) m/z: 259 (M+H)+.
Стадия-2: этил 5-метил-6-(2,2,3,3-тетрафторпропокси)пиридазин-3-карбоксилат
Заявленное в заголовке соединение получали с выходом 27% (1,66 г, желтый твердый остаток) из смеси 6-хлор-4-метил-3-(2,2,3,3-тетрафторпропокси)пиридазина и 3-хлор-4-метил-6-(2,2,3,3-тетрафторпропокси)пиридазина (приблизительно 1,5:1) (5,40 г, 20,9 ммоль, стадия-1) способом, аналогичным стадии-2 промежуточного соединения-A14.
1H-ЯМР (300 MГц, CDCl3) дельта 7,99 (1H, с), 6,02 (1H, тт, J=53,1, 3,7 Гц), 5,04 (2H, т, J=12,5 Гц), 4,50 (2H, к, J=7,3 Гц), 2,34 (3H, с), 1,46 (3H, т, J=7,3 Гц), MS (ESI) m/z: 297 (M+H)+.
Стадия-3: 5-метил-6-(2,2,3,3-тетрафторпропокси)пиридазин-3-карбоновая кислота
Заявленное в заголовке соединение получали с выходом >99% (909 мг, белый твердый остаток) из смеси этил 5-метил-6-(2,2,3,3-тетрафторпропокси)пиридазин-3-карбоксилата (980 мг, 3,31 ммоль, стадия-2) способом, аналогичным стадии-2 промежуточного соединения-A5.
1H-ЯМР (300 MГц, DMSO-d6) дельта 8,00 (1H, с), 6,75 (1H, тт, J=51,2, 5,1 Гц), 5,01 (2H, т, J=13,1 Гц), 2,26 (3H, с), (сигнал COOH не наблюдали), MS (ESI) m/z: 267 (M-H)-.
Стадия-4: (5-метил-6-(2,2,3,3-тетрафторпропокси)пиридазин-3-ил)метанол
Заявленное в заголовке соединение получали с выходом 88% (670 мг, белый твердый остаток) из 5-метил-6-(2,2,3,3-тетрафторпропокси)пиридазин-3-карбоновой кислоты (800 мг, 2,98 ммоль, стадия-3) способом, аналогичным стадии-2 промежуточного соединения-A3.
1H-ЯМР (300 MГц, CDCl3) дельта 7,32 (1H, с), 6,00 (1H, тт, J=52,7, 3,7 Гц), 4,91 (2H, т, J=12,4 Гц), 4,85 (2H, с), 3,62 (1H, ушир. с), 2,28 (3H, с), MS (ESI) m/z: 255 (M+H)+.
Промежуточное соединение-A57: гидрохлорид (5-(2,2-дифторпропокси)-4-метилпиридин-2-ил)метанамина
Стадия-1: 2-хлор-5-(2,2-дифторпропокси)-4-метилпиридин
Заявленное в заголовке соединение получали с выходом 98% (4,52 г, бледно-желтое масло) из 6-хлор-4-метилпиридин-3-ола (3,00 г, 20,9 ммоль) и 2,2-дифторпропилтрифторметансульфоната (11,9 г, 52,2 ммоль) способом, аналогичным стадии-1 промежуточного соединения-A15.
1H-ЯМР (270 MГц, CDCl3) дельта 7,88 (1H, с), 7,14 (1H, с), 4,18 (2H, т, J=11,2 Гц), 2,27 (3H, с), 1,80 (3H, т, J=18,5 Гц), MS (ESI) m/z: 222 (M+H)+.
Стадия-2: этил 5-(2,2-дифторпропокси)-4-метилпиколинат
Заявленное в заголовке соединение получали с выходом 92% (5,35 г, бледно-желтый твердый остаток) из 2-хлор-5-(2,2-дифторпропокси)-4-метилпиридина (4,99 г, 22,5 ммоль, стадия-1) способом, аналогичным стадии-2 промежуточного соединения-A14.
1H-ЯМР (300 MГц, CDCl3) дельта 8,23 (1H, с), 7,99 (1H, с), 4,46 (2H, к, J=7,3 Гц), 4,28 (2H, т, J=11,0 Гц), 2,33 (3H, с), 1,81 (3H, т, J=19,1 Гц), 1,44 (3H, т, J=7,3 Гц), MS (ESI) m/z: 260 (M+H)+.
Стадия-3: (5-(2,2-дифторпропокси)-4-метилпиридин-2-ил)метанол
Заявленное в заголовке соединение получали с выходом 62% (1,05 г, бесцветное масло) из этил 5-(2,2-дифторпропокси)-4-метилпиколината (2,00 г, 7,71 ммоль, стадия-2) способом, аналогичным стадии-3 промежуточного соединения-A34.
1H-ЯМР (300 MГц, CDCl3) дельта 8,07 (1H, с), 7,07 (1H, с), 4,68 (2H, с), 4,20 (2H, т, J=11,3 Гц), 2,28 (3H, с), 1,81 (3H, т, J=18,7 Гц), (сигнал OH не наблюдали), MS (ESI) m/z: 218 (M+H)+.
Стадия-4: 2-((5-(2,2-дифторпропокси)-4-метилпиридин-2-ил)метил)изоиндолин-1,3-дион
Заявленное в заголовке соединение получали с выходом 34% (1,05 г, белый твердый остаток) из (5-(2,2-дифторпропокси)-4-метилпиридин-2-ил)метанола (1,05 г, 4,81 ммоль, стадия-3) и фталимида (779 мг, 4,81 ммоль) способом, аналогичным стадии-1 промежуточного соединения-A17.
1H-ЯМР (300 MГц, CDCl3) дельта 8,04 (1H, с), 7,92-7,83 (2H, м), 7,79-7,70 (2H, м), 7,13 (1H, с), 4,93 (2H, с), 4,14 (2H, т, J=11,0 Гц), 2,24 (3H, с), 1,77 (3H, т, J=18,7 Гц), MS (ESI) m/z: 347 (M+H)+.
Стадия-5: гидрохлорид (5-(2,2-дифторпропокси)-4-метилпиридин-2-ил)метанамина
Заявленное в заголовке соединение получали с выходом >99% (1,35 г, белый твердый остаток) из 2-((5-(2,2-дифторпропокси)-4-метилпиридин-2-ил)метил)изоиндолин-1,3-диона (1,70 г, 4,44 ммоль, стадия-4) способом, аналогичным стадии-5 промежуточного соединения-A34.
1H-ЯМР (300 MГц, DMSO-d6) дельта 8,33 (1H, с), 8,31 (3H, ушир. с), 7,36 (1H, с), 4,47 (2H, т, J=12,6 Гц), 4,08 (2H, к, J=5,5 Гц), 2,23 (3H, с), 1,77 (3H, т, J=19,4 Гц), MS (ESI) m/z: 217 (M+H)+.
Промежуточное соединение-A58: гидрохлорид (4-(2,2-дифторпропокси)-3-метилфенил)метанамина
Стадия-1: метил 4-(2,2-дифторпропокси)-3-метилбензоат
Заявленное в заголовке соединение получали с выходом 76% (2,09 г, белый твердый остаток) из метил 4-гидрокси-3-метилбензоата (1,86 г, 11,2 ммоль) и 2,2-дифторпропилтрифторметансульфоната (6,37 г, 27,9 ммоль) способом, аналогичным стадии-1 промежуточного соединения-A15.
1H-ЯМР (300 MГц, CDCl3) дельта 7,92-7,85 (2H, м), 6,79 (1H, д, J=8,1 Гц), 4,16 (2H, т, J=11,0 Гц), 3,89 (3H, с), 2,28 (3H, с), 1,81 (3H, т, J=19,1 Гц), MS (ESI) m/z: 245 (M+H)+.
Стадия-2: (4-(2,2-дифторпропокси)-3-метилфенил)метанол
Заявленное в заголовке соединение получали с выходом >99% (805 мг, белый твердый остаток) из метил 4-(2,2-дифторпропокси)-3-метилбензоата (900 мг, 3,68 ммоль, стадия-1) способом, аналогичным стадии-2 промежуточного соединения-A1.
1H-ЯМР (300 MГц, CDCl3) дельта 7,23-7,12 (2H, м), 6,77 (1H, д, J=8,0 Гц), 4,61 (2H, д, J=5,9 Гц), 4,11 (2H, т, J=11,0 Гц), 2,26 (3H, с), 1,80 (3H, т, J=19,1 Гц), 1,56 (1H, т, J=5,9 Гц).
Стадия-3: 2-(4-(2,2-дифторпропокси)-3-метилбензил)изоиндолин-1,3-дион
Заявленное в заголовке соединение получали с выходом 85% (1,10 г, белый твердый остаток) из (4-(2,2-дифторпропокси)-3-метилфенил)метанола (805 мг, 3,72 ммоль, стадия-2) и фталимида (603 мг, 4,10 ммоль) способом, аналогичным стадии-1 промежуточного соединения-A17.
1H-ЯМР (300 MГц, CDCl3) дельта 7,91-7,80 (2H, м), 7,78-7,65 (2H, м), 7,32-7,23 (2H, м), 6,71 (1H, д, J=8,8 Гц), 4,76 (2H, с), 4,06 (2H, т, J=11,4 Гц), 2,21 (3H, с), 1,76 (3H, т, J=18,7 Гц), MS (ESI) m/z: 346 (M+H)+.
Стадия-4: гидрохлорид (4-(2,2-дифторпропокси)-3-метилфенил)метанамина
Заявленное в заголовке соединение получали с выходом >99% (796 мг, белый твердый остаток) из 2-(4-(2,2-дифторпропокси)-3-метилбензил)изоиндолин-1,3-диона (1,10 г, 3,17 ммоль, стадия-3) способом, аналогичным стадии-5 промежуточного соединения-A34.
1H-ЯМР (300 MГц, DMSO-d6) дельта 8,20 (3H, ушир. с), 7,32-7,22 (2H, м), 7,04 (1H, д, J=8,8 Гц), 4,30 (2H, т, J=12,5 Гц), 3,92 (2H, к, J=5,9 Гц), 2,18 (3H, с), 1,76 (3H, т, J=19,1 Гц), MS (ESI) m/z: 216 (M+H)+.
Промежуточное соединение-A59: гидрохлорид 1-(4-(2,2-дифторэтокси)-3-метилфенил)этанамина (один энантиомер)
Стадия-1: метил 4-(2,2-дифторэтокси)-3-метилбензоат
К перемешиваемому раствору метил 4-гидрокси-3-метилбензоата (1,5 г, 9,0 ммоль), 2,2-дифторэтанола (0,90 г, 10,8 ммоль), трифенилфосфина (3,6 г, 13,5 ммоль) в THF (40 мл) добавляли по каплям диэтилазодикарбоксилат (4,9 мл, 10,8 ммоль, 40 % раствор в толуоле) при 0°C. Смесь перемешивали при комнатной температуре в течение 30 минут. Затем реакционную смесь перемешивали при 60°C в течение 2 часов. После охлаждения до комнатной температуры, смесь концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле, элюируя н-гексаном/EtOAc (18:1), получая 1,9 г (90 % выход) заявленного в заголовке соединения в виде белого твердого остатка.
1H-ЯМР (300 MГц, CDCl3) дельта 7,90-7,85 (2H, м), 6,79 (1H, д, J=8,8 Гц), 6,13 (1H, тт, J=54,9, 4,4 Гц), 4,24 (2H, тд, J=12,5, 3,7 Гц), 3,89 (3H, с), 2,27 (3H, с).
Стадия-2: 4-(2,2-дифторэтокси)-3-метилбензойная кислота
Заявленное в заголовке соединение получали с выходом >99 % (1,1 г, белый твердый остаток) из метил 4-(2,2-дифторэтокси)-3-метилбензоата (1,0 г, 4,3 ммоль, стадия-1) способом, аналогичным стадии-2 промежуточного соединения-A6.
1H-ЯМР (300 MГц, CDCl3) дельта 7,97-7,90 (2H, м), 6,83 (1H, д, J=8,1 Гц), 6,14 (1H, тт, J=54,9, 4,4 Гц), 4,26 (2H, тд, J=12,5, 4,4 Гц), 2,28 (3H, с), (сигнал COOH не наблюдали), MS (ESI) m/z: 215 (M-H)-.
Стадия-3: 4-(2,2-дифторэтокси)-N-метокси-N,3-диметилбензамид
Заявленное в заголовке соединение получали с выходом 94 % (900 мг, прозрачное бесцветное масло) из 4-(2,2-дифторэтокси)-3-метилбензойной кислоты (800 мг, 3,7 ммоль, стадия-2) способом, аналогичным стадии-1 промежуточного соединения-A7.
1H-ЯМР (300 MГц, CDCl3) дельта 7,60-7,50 (2H, м), 6,78 (1H, д, J=8,0 Гц), 6,13 (1H, тт, J=54,9, 4,4 Гц), 4,23 (2H, тд, J=12,4, 3,7 Гц), 3,56 (3H, с), 3,35 (3H, с), 2,26 (3H, с), MS (ESI) m/z: 260 (M+H)+.
Стадия-4: 1-(4-(2,2-дифторэтокси)-3-метилфенил)этанон
Заявленное в заголовке соединение получали с выходом 98% (730 мг, бледно-желтое масло) из 4-(2,2-дифторэтокси)-N-метокси-N,3-диметилбензамида (900 мг, 3,4 ммоль, стадия-3) способом, аналогичным стадии-2 промежуточного соединения-A7.
1H-ЯМР (300 MГц, CDCl3) дельта 7,84-7,80 (2H, м), 6,81 (1H, д, J=8,0 Гц), 6,14 (1H, тт, J=54,9, 3,7 Гц), 4,25 (2H, тд, J=12,5, 3,7 Гц), 2,82 (3H, с), 2,28 (3H, с), MS (ESI) m/z: 215 (M+H)+.
Стадия-5: (R)-N-(1-(4-(2,2-дифторэтокси)-3-метилфенил)этил)-2-метилпропан-2-сульфинамид (один диастереомер)
Заявленное в заголовке соединение получали с выходом 47 % (520 мг, прозрачное бесцветное масло) из 1-(4-(2,2-дифторэтокси)-3-метилфенил)этанона (750 мг, 3,5 ммоль, стадия-4) и (R)-2-метилпропан-2-сульфинамида способом, аналогичным стадии-3 промежуточного соединения-A7.
1H-ЯМР (300 MГц, CDCl3) дельта 7,14 (2H, ушир.), 6,75 (1H, д, J=8,8 Гц), 6,10 (1H, тт, J=54,9, 4,4 Гц), 4,50-4,40 (1H, м), 4,17 (2H, тд, J=13,2, 4,4 Гц), 3,33 (1H, ушир. с), 2,24 (3H, с), 1,47 (3H, д, J=6,6 Гц), 1,23 (9H, с).
Стадия-6: гидрохлорид 1-(4-(2,2-дифторэтокси)-3-метилфенил)этанамина (один энантиомер)
Заявленное в заголовке соединение получали с выходом 96% (390 мг, белый твердый остаток) из (R)-N-(1-(4-(2,2-дифторэтокси)-3-метилфенил)этил)-2-метилпропан-2-сульфинамида (один диастереомер) (750 мг, 3,5 ммоль, стадия-5) способом, аналогичным стадии-4 промежуточного соединения-A7.
1H-ЯМР (300 MГц, DMSO-d6) дельта 8,23 (2H, ушир. с), 7,31-7,25 (2H, м), 7,06 (1H, д, J=8,8 Гц), 6,40 (1H, тт, J=54,2, 2,9 Гц), 4,33 (2H, тд, J=14,7, 3,7 Гц), 2,18 (3H, с), 1,47 (3H, д, J=6,6 Гц), (сигнал CHNH2 (бензильный протон) не наблюдали).
Промежуточное соединение-A60: гидрохлорид 1-(4-(2,2-дифторпропокси)-3-метилфенил)этанамина (один энантиомер)
Заявленное в заголовке соединение получали из 2,2-дифторпропан-1-ола вместо 2,2-дифторэтанола способом, аналогичным промежуточному соединению-A59.
1H-ЯМР (300 MГц, DMSO-d6) дельта 8,24 (3H, ушир. с), 7,32-7,26 (2H, м), 7,03 (1H, д, J=8,4 Гц), 4,35-4,20 (3H, м), 2,18 (3H, с), 1,74 (3H, т, J=19,1 Гц), 1,45 (3H, д, J=6,6 Гц), MS (ESI) m/z: 230 (M+H)+.
Промежуточное соединение-A61: гидрохлорид 1-(4-(2,2-дифторэтокси)-3-метилфенил)этанамина (один энантиомер, антипод промежуточного соединения-A59)
Заявленное в заголовке соединение получали из (S)-2-метилпропан-2-сульфинамида вместо (R)-2-метилпропан-2-сульфинамида способом, аналогичным промежуточному соединению-A59.
Следующие промежуточные соединения являются имеющимися в продаже, или их получали известными способами.
Промежуточное соединение B1: 4-хлор-1H-пиразоло[4,3-c]пиридин
Промежуточное соединение B2: 4-хлор-6-метил-1H-пиразоло[4,3-c]пиридин
Промежуточное соединение B3: 4-хлор-7-метил-1H-пиразоло[4,3-c]пиридин
Промежуточное соединение B4: 4-хлор-3-метил-1H-пиразоло[4,3-c]пиридин
Промежуточное соединение B5: соль 4-амино-2-хлорникотинальдегида и 2,2,2-трифторуксусной кислоты
Репрезентативный способ для способа A
Следующий способ получения промежуточного соединения-1a представляет способ A.
Промежуточное соединение-1a:
4-хлор-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин
К раствору 4-хлор-2H-пиразоло[4,3-c]пиридина (1,50 г, 9,77 ммоль, промежуточное соединение-B1), (5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метанола (2,38 г, 10,7 ммоль, промежуточное соединение-A1) и трифенилфосфина (3,84 г, 14,7 ммоль) В THF (40 мл) добавляли 2,2M толуольный раствор диэтилазодикарбоксилата (5,33 мл, 11,7 ммоль) при 0°C. После перемешивания при комнатной температуре в течение 16 часов, реакционную смесь разбавляли EtOAc (200 мл) и промывали водой (200 мл). Органический слой сушили над сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле, элюируя гексаном/EtOAc (5:1-4:1), получая 1,30 г (37% выход) заявленного в заголовке соединения в виде бледно-желтого твердого остатка и 1,62 г (46% выход) его региоизомера (4-хлор-1-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-1H-пиразоло[4,3-c]пиридина) в виде бледно-желтого твердого остатка.
1H-ЯМР (300 MГц, CDCl3) дельта 8,09 (1H, с), 8,06-8,04 (2H, м), 7,48-7,45 (2H, м), 5,53 (2H, с), 4,77 (2H, к, J=8,6 Гц), 2,28 (3H, с), MS (ESI) m/z: 357 (M+H)+.
Репрезентативный способ для способа B
Следующий способ получения промежуточного соединения-52a представляет способ B.
Промежуточное соединение-52a:
4-хлор-2-((5-метил-6-((2,2,2-трифторэтокси)метил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин
Смесь 4-хлор-2H-пиразоло[4,3-c]пиридина (457 мг, 2,97 ммоль, промежуточное соединение-B1), 5-(хлорметил)-3-метил-2-((2,2,2-трифторэтокси)метил)пиридина (830 мг, 3,27 ммоль, промежуточное соединение-A37) и карбоната калия (1,65 г, 11,9 ммоль) в DMF (20 мл) перемешивали при 60°C в течение 17 часов. После охлаждения до комнатной температуры смесь выливали в воду (200 мл). Водный слой экстрагировали EtOAc (200 мл). Отделенный органический слой промывали водой (100 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали колоночной хроматографией на силикагеле, элюируя гексаном/EtOAc (3:1 - EtOAc только), получая 242 мг (22% выход) заявленного в заголовке соединения в виде белого твердого остатка и 557 мг (51% выход) его региоизомера в виде белого твердого остатка.
1H-ЯМР (270 MГц, DMSO-d6) дельта 9,00 (1H, с), 8,47 (1H, с), 7,99 (1H, д, J=5,9 Гц), 7,65 (1H, с), 7,56 (1H, д, J=5,9 Гц), 5,74 (2H, с), 4,75 (2H, с), 4,13 (2H, к, J=10,0 Гц), 2,31 (3H, с), MS (ESI) m/z: 371 (M+H)+.
Репрезентативный способ для способа C
Следующий способ получения промежуточного соединения-1a представляет способ C.
Промежуточное соединение-1a:
4-хлор-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин
Стадия-1: 2-хлор-3-((((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)имино)метил)пиридин-4-амин
К перемешиваемому раствору трифторацетата 4-амино-2-хлорникотинальдегида (1,00 г, 3,70 ммоль) и гидрохлорида (5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метанамина (1,14 г, 4,43 ммоль) в THF (10 мл) добавляли тетраизопропоксид титана (4,33 мл, 14,8 ммоль) при комнатной температуре. Полученную в результате смесь кипятили с обратным холодильником в течение 2 часов. После охлаждения до комнатной температуры, реакционную смесь выливали в перемешиваемый раствор 2 M водного гидроксида натрия (100 мл) при комнатной температуре. Затем, смесь разбавляли EtOAc (100 мл) и фильтровали через слой целита и промывали EtOAc (100 мл). Фильтрат промывали соляным раствором (200 мл), и органический слой сушили над сульфатом натрия. Затем органическую фракцию разбавляли гексаном (100 мл). Данный раствор фильтровали через стеклянный фильтр, заполненный силигелем, и промывали гексаном/EtOAc (1:1). Фильтрат концентрировали при пониженном давлении, получая 1,29 г (97% выход) заявленного в заголовке соединения в виде бледно-желтого твердого остатка.
1H-ЯМР (300 MГц, CDCl3) дельта 9,00 (1H, с), 7,93 (1H, с), 7,87 (1H, д, J=5,9 Гц), 7,39 (1H, с), 6,46 (1H, д, J=5,9 Гц), 4,81-4,72 (4H, м), 2,24 (3H, с), (сигналы NH2 не наблюдали), MS (ESI) m/z: 359 (M+H)+.
Стадия-2: 4-хлор-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин
Смесь 2-хлор-3-((((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)имино)метил)пиридин-4-амина (1,29 г, 3,59 ммоль, стадия-1), диацетата йодбензола (4,63 г, 14,4 ммоль) и DMF (30 мл) перемешивали при 80°C в течение 2 часов. После охлаждения до комнатной температуры, смесь выливали в воду (150 мл) и экстрагировали EtOAc (150 мл×2). Объединенную органическую фракцию промывали водой (200 мл) и сушили над сульфатом натрия. После удаления растворителя, остаток очищали колоночной хроматографией на силикагеле, элюируя н-гексаном/EtOAc (3:1-1:1), получая 0,59 г (46% выход) заявленного в заголовке соединения в виде белого твердого остатка.
1H-ЯМР и МС данные были аналогичными данным, показанным в способе A.
Репрезентативный способ для способа D
Следующий способ получения промежуточного соединения-1d представляет способ D.
Промежуточное соединение-1d:
4-хлор-6-метил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-с]пиридин
К THF (5 мл) раствору 4-хлор-6-метил-1H-пиразоло[4,3-c]пиридина (0,320 г, 1,91 ммоль) добавляли (5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метанол (0,507 г, 2,3 ммоль) и (цианометилен)трибутилфосфоран (0,80 мл, 3,05 ммоль) при комнатной температуре. Полученную в результате смесь перемешивали при 60°C в течение 20 часов в атмосфере азота. Реакционную смесь концентрировали досуха. Неочищенный продукт реакции очищали колоночной хроматографией на силикагеле, элюируя гексаном/EtOAc (5:1-1:2), получая 284 мг (40% выход) заявленного в заголовке соединения в виде белого твердого остатка.
1H-ЯМР (300 MГц, CDCl3) дельта 8,04-8,02 (2H, м), 7,45 (1H, ушир. с), 7,27-7,25 (1H), 5,48 (2H, с), 4,77 (2H, к, J=8,3 Гц), 2,58 (3H, с), 2,22 (3H, с), MS (ESI) m/z: 371 (M+H)+.
Следующие промежуточные соединения получали, применяя способ A, B, C или D из исходных соединений, показанных в таблицах 3-1 - 3-5. Спектральные данные промежуточных соединений показаны в таблице 4-1 - 4-6.
метилпиридин-3-ил)метил)-2Н-пиразоло[4,3-с]пиридин
Репрезентативный способ для способа E
Следующий способ получения промежуточного соединения-1b представляет способ E.
Промежуточное соединение-1b: этил 2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксилат
К раствору 4-хлор-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридина (6,31 г, 17,7 ммоль, промежуточное соединение-1a) в DMF/EtOH (2:1, 180 мл) добавляли ацетат палладия (II) (1,19 г, 5,31 ммоль), 1,3-бис(дифенилфосфино)пропан (2,19 г, 5,31 ммоль) и триэтиламин (7,4 мл, 53,1 ммоль). Смесь нагревали при 80°C в течение 3 часов в атмосфере газообразного CO. Реакционную смесь разбавляли EtOAc (400 мл) и промывали водой (200 мл). Органический слой сушили над сульфатом натрия, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле, элюируя гексаном/EtOAc (4:1-1:4), получая 5,13 г (74% выход) заявленного в заголовке соединения в виде бледно-желтого твердого остатка.
1H-ЯМР (300 MГц, CDCl3) дельта 8,64 (1H, с), 8,48 (1H, д, J=5,9 Гц), 8,07 (1H, с), 7,75 (1H, д, J=6,6 Гц), 7,48 (1H, с), 5,58 (2H, с), 4,77 (2H, к, J=8,6 Гц), 4,54 (2H, к, J=7,3 Гц), 2,21 (3H, с), 1,49 (3H, т, J=7,3 Гц), MS (ESI) m/z: 395 (M+H)+.
Промежуточное соединение-1c: 2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоновая кислота
Заявленное в заголовке соединение получали с выходом 96% (183 мг, бледно-желтый твердый остаток) из этил 2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксилата (205 мг, 0,52 ммоль, промежуточное соединение-1b) способом, аналогичным стадии-2 промежуточного соединения-A6.
MS (ESI) m/z: 365 (M-H)-.
Промежуточное соединение-1h: гидрохлорид N-(2-аминоэтил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида
Стадия 1. трет-бутил (2-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамидо)этил)карбамат
Заявленное в заголовке соединение получали с выходом >99% (278 мг, бесцветный сироп) из 2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4 -карбоновой кислоты (200 мг, 0,55 ммоль, промежуточное соединение-1c) и трет-бутил (2-аминоэтил)карбамата (131 мг, 0,82 ммоль) способом, аналогичным стадии-1 промежуточного соединения-A7.
1H-ЯМР (300 MГц, CDCl3) дельта 8,81 (1H, с), 8,35 (1H, ушир. с), 8,25 (1H, д, J=5,1 Гц), 8,07 (1H, с), 8,02 (1H, с), 7,69 (1H, д, J=5,1 Гц), 7,46 (1H, с), 5,56 (2H, с), 4,76 (2H, к, J=8,8 Гц), 3,70-3,58 (2H, м), 3,50-3,38 (2H, м), 2,20 (3H, с), 1,42 (9H, с), MS (ESI) m/z: 509 (M+H)+.
Стадия 2. гидрохлорид N-(2-аминоэтил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида
Смесь трет-бутил (2-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамидо)этил)карбамата (278 мг, 0,55 ммоль, стадия-1) и 4 M хлороводорода в диоксановом растворе (10 мл) перемешивали при комнатной температуре в течение 1 часа. После удаления растворителя, остаток промывали диизопропиловым эфиром-гексаном, получая 243 мг (>99%) заявленного в заголовке соединения в виде белого твердого остатка.
MS (ESI) m/z: 409 (M+H)+.
Репрезентативный способ для способа F
Следующий способ получения промежуточного соединения-36b представляет способ F.
Промежуточное соединение-36b: фенил 2-(2-((3-хлор-5-(трифторметил)пиридин-2-ил)окси)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксилат
Смесь 4-хлор-2-(2-((3-хлор-5-(трифторметил)пиридин-2-ил)окси)этил)-2H-пиразоло[4,3-c]пиридина (310 мг, 0,82 ммоль), фенилформиата (201 мг, 1,64 ммоль), ацетата палладия (II) (5 мг, 0,03 ммоль), Xantphos (57 мг, 0,10 ммоль) и триэтиламина (0,23 мл, 1,64 ммоль) в MeCN кипятили с обратным холодильником при перемешивании в течение 12 часов. После охлаждения до комнатной температуры, растворитель удаляли в вакууме. Остаток очищали колоночной хроматографией на силикагеле, элюируя н-гексаном/EtOAc (1:1-1:3), получая 152 мг (40% выход) заявленного в заголовке соединения в виде желтого твердого остатка.
1H-ЯМР (270 MГц, DMSO-d6) дельта 8,85 (1H, с), 8,57 (1H, д, J=5,9 Гц), 8,28 (1H, с), 7,84-7,82 (2H, м), 7,51-7,45 (2H, м), 7,35-7,29 (3H, м), 4,96 (4H, с), MS (ESI) m/z: 463 (M+H)+.
Следующие промежуточные соединения получали, применяя способ E или F из исходных соединений, показанных в таблице 5-1 - 5-4. Спектральные данные промежуточных соединений показаны в таблице 6-1 - 6-6.
Часть получения примеров
Примерные соединения (пример-1 - 649) получали следующим способом.
Репрезентативный способ для способа G
Следующий способ получения примера 1 представляет способ G.
Пример 1: N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамид
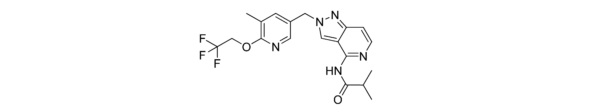
Смесь 4-хлор-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридина (20 мг, 0,056 ммоль, промежуточное соединение-1a), изобутирамида (15 мг, 0,17 ммоль), трис(дибензилиденацетон)дипалладия (0) (1 мг, 1 микромоль), 4,5-бис(дифенилфосфино)-9,9-диметилксантена (2 мг, 3 микромоль) и фосфата трикалия (18 мг, 0,084 ммоль) в диоксане (2 мл) перемешивали при 170°C в течение 20 минут при микроволновом облучении. После охлаждения до комнатной температуры, полученную в результате смесь фильтровали через короткую колонку NH-gel, элюируя EtOAc, и фильтрат концентрировали. Остаток очищали сильным катионнообменным картриджем (BondElute (зарегистрированная торговая марка) SCX, 1 г/6 мл, Varian Inc.) и затем препаративной LC-MS, получая 9,3 мг (40% выход) заявленного в заголовке соединения.
Репрезентативный способ для способа H
Следующий способ получения примера 33 представляет способ H.
Пример 33: N-изопропил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамид
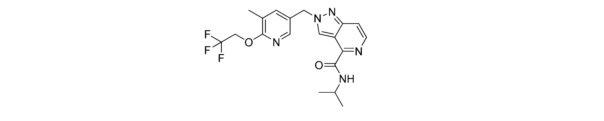
К смеси 2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоновой кислоты (16 мг, 0,044 ммоль, промежуточное соединение-1c) и триэтиламина (0,06 мл, 0,4 ммоль) в DMF (1 мл) добавляли HBTU (33 мг, 0,087 ммоль). После перемешивания при комнатной температуре в течение 10 минут добавляли к смеси изопропиламин (0,022 мл, 0,26 ммоль). После перемешивания при 60°C в течение 1 часа, смесь разбавляли EtOAc (3 мл). Органический слой промывали водой (3 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток фильтровали через NH-gel, элюируя EtOAc, и фильтрат концентрировали в вакууме. Остаток очищали препаративной LC-MS, получая 4,6 мг (26% выход) заявленного в заголовке соединения.
Репрезентативный способ для способа J
Следующий способ получения примера 289 представляет способ J.
Пример 289: 2-(2-((3-хлор-5-(трифторметил)пиридин-2-ил)окси)этил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамид
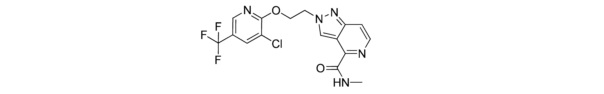
Смесь фенил 2-(2-((3-хлор-5-(трифторметил)пиридин-2-ил)окси)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксилата (15 мг, 0,032 ммоль, промежуточное соединение-36b) и 40% водного раствора метиламина (0,1 мл) в THF (1 мл) перемешивали при 80°C в течение 2 часов. После удаления растворителя, остаток очищали препаративной LC-MS, получая 8,6 мг (66% выход) заявленного в заголовке соединения.
Репрезентативный способ для способа K
Следующий способ получения примера 143 представляет способ K.
Пример 143: N-метил-2-((4-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамид
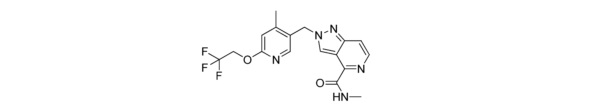
Смесь этил 2-((4-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксилата (15 мг, 0,038 ммоль, промежуточное соединение-20b) и 40% водного раствора метиламина (2 мл) перемешивали при 60°C в течение 30 минут. После охлаждения до комнатной температуры, смесь разбавляли EtOAc (2 мл) и промывали водой (2 мл). Органический слой сушили над сульфатом натрия и концентрировали. Остаток очищали сильным катионнообменным картриджем (BondElute (зарегистрированная торговая марка) SCX, 1 г/6 мл, Varian Inc.), и затем препаративной LC-MS, получая 6,0 мг (42% выход) заявленного в заголовке соединения.
Репрезентативный способ для способа L
Следующий способ получения примера 141 представляет способ L.
Пример 141: N-(2-гидроксиэтил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамид
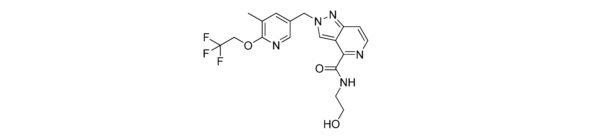
Смесь этил 2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксилата (1,10 г, 2,79 ммоль, промежуточное соединение-1b) и 2-аминоэтанола (3,41 г, 55,8 ммоль) в EtOH (20 мл) перемешивали при 60°C в течение 3 часов. После упаривания растворителя, остаток разбавляли EtOAc (200 мл) и промывали водой (100 мл) и соляным раствором (100 мл). Органический слой сушили над сульфатом натрия и концентрировали в вакууме. Остаток промывали диизопропиловым эфиром-EtOAc, получая 1,13 г (99% выход) заявленного в заголовке соединения в виде белого порошка.
Репрезентативный способ для способа М
Следующий способ получения примера 30 представляет способ M.
Пример 30: 4-метокси-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин
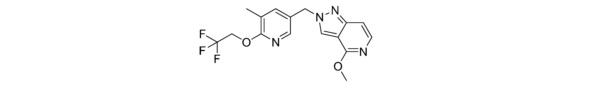
Заявленное в заголовке соединение получали с выходом 41% (72 мг, желтое масло) из 4-хлор-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридина (180 мг, 0,51 ммоль, промежуточное соединение-1a), применяя MeOH в качестве растворителя, способом, аналогичным стадии-2 промежуточного соединения-A14.
Репрезентативный способ для способа N
Следующий способ получения примера 55 представляет способ N.
Пример 55: 4-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)морфолин
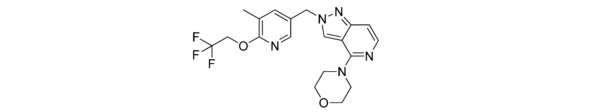
Смесь 4-хлор-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридина (20 мг, 0,056 ммоль, промежуточное соединение-1a), морфолина (49 мг, 0,56 ммоль) и карбоната калия (47 мг, 0,34 ммоль) в DMA (1,5 мл) перемешивали при 120°C в течение 3 часов. После охлаждения до комнатной температуры, смесь разбавляли EtOAc (5 мл) и промывали водой (5 мл). Органический слой сушили над сульфатом натрия и концентрировали. Остаток очищали картриджем с сильной катионнообменной смолой (BondElute (зарегистрированная торговая марка) SCX, 1 г/6 мл, Varian Inc.), и затем препаративной LC-MS, получая 8,5 мг (37% выход) заявленного в заголовке соединения.
Репрезентативный способ для способа P
Следующий способ получения примера 64 представляет способ P.
Пример 64: 2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-4-(1H-пиразол-5-ил)-2H-пиразоло[4,3-c]пиридин
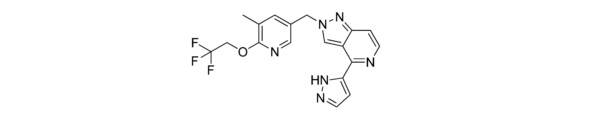
Смесь 4-хлор-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридина (25 мг, 0,070 ммоль, промежуточное соединение-1a), гидрата (1H-пиразол-5-ил)бороновой кислоты (27 мг, 0,21 ммоль), трис(дибензилиденацетон)дипалладия (0) (13 мг, 0,014 ммоль), 2-дициклогексилфосфино-2',6'-диметоксибифенила (12 мг, 0,028 ммоль) и фосфата калия (45 мг, 0,21 ммоль) в DMF (1 мл) перемешивали при 100°C в течение 16 часов. После охлаждения до комнатной температуры смесь разбавляли EtOAc (5 мл) и промывали водой (5 мл). Органический слой сушили над сульфатом натрия и концентрировали. Остаток очищали картриджем с сильной катионнообменной смолой (BondElute (зарегистрированная торговая марка) SCX, 1 г/6 мл, Varian Inc.), и затем препаративной LC-MS, получая 2,9 мг (11% выход) заявленного в заголовке соединения.
Следующие примеры получали, применяя способ G, H, J, K, L, M, или N, из исходных соединений и реагентов, показанных в таблице 7-1 - 7-55 и таблице 8-1 - 8-15. Время удерживания и наблюдаемый MS (положительный или отрицательный режим LC-MS всех примеров описаны в таблице 9-1 - 9-5. 1H-ЯМР данные примера 1, 2, 69, 141, 149, 158, 166, 172, 174, 179, 183, 199, 220, 222, 223, 288, 301, 343, 462 и 518 описаны в таблице 10-1 - 10-2.
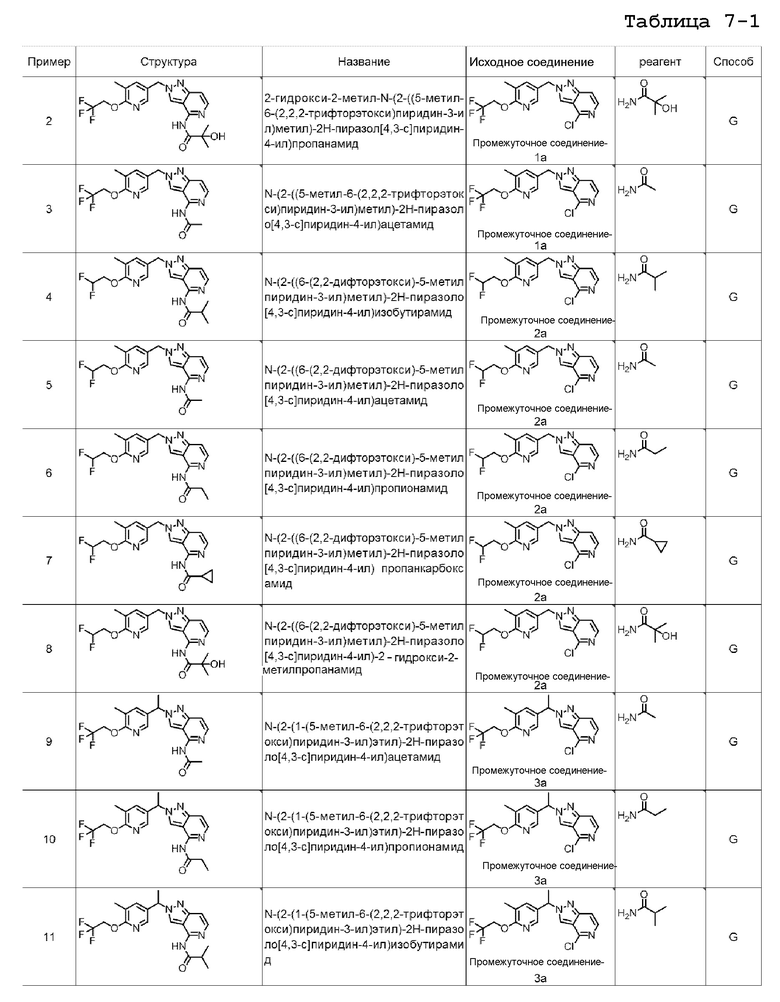
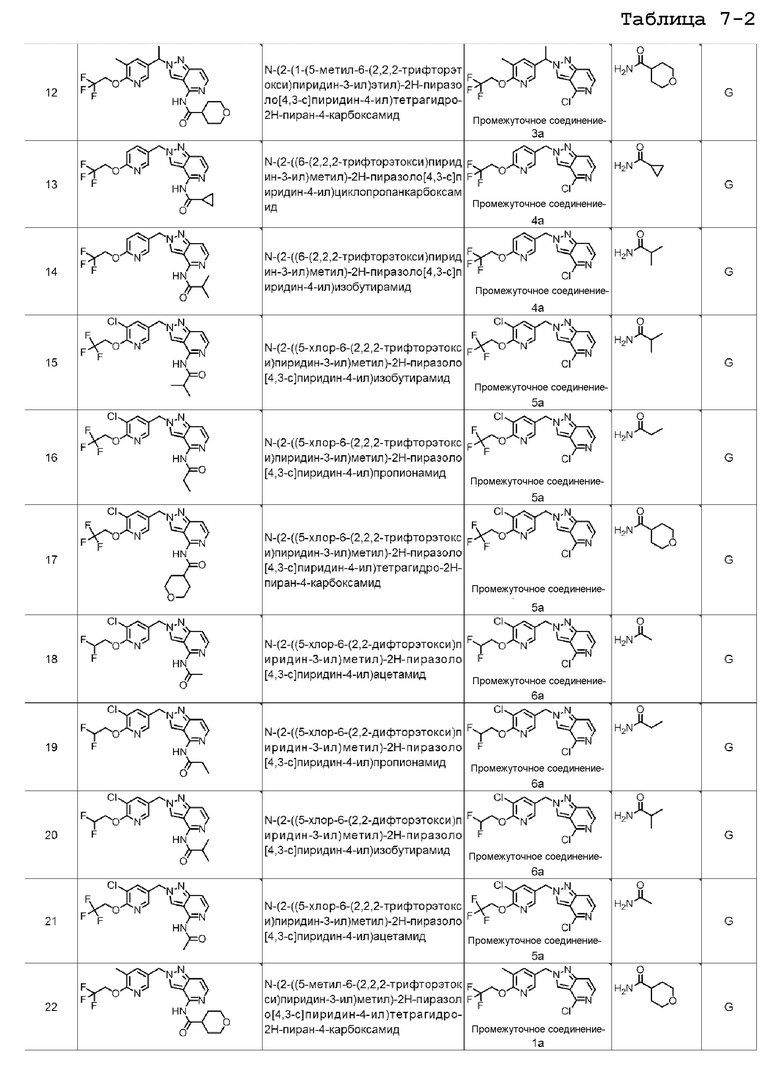
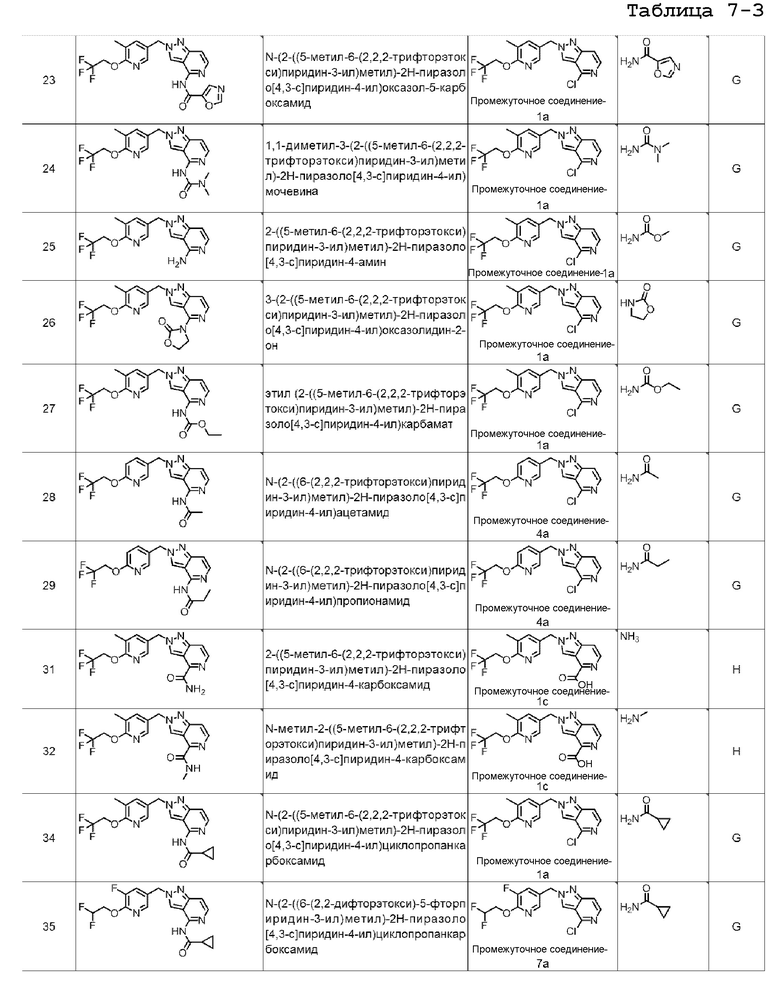

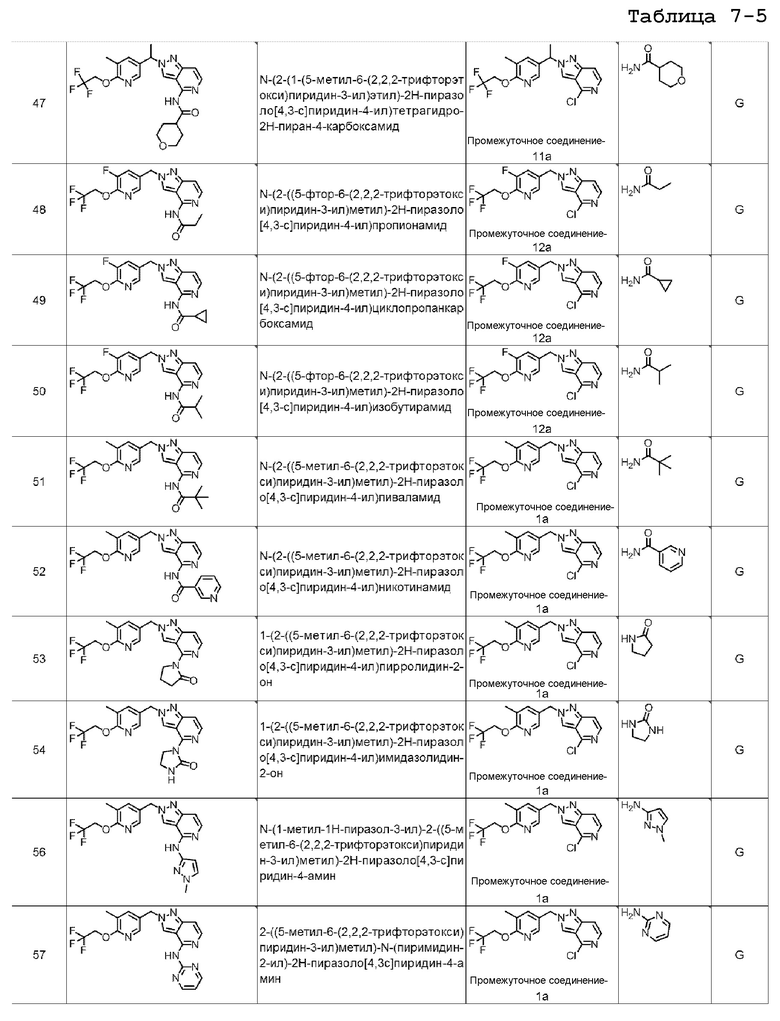
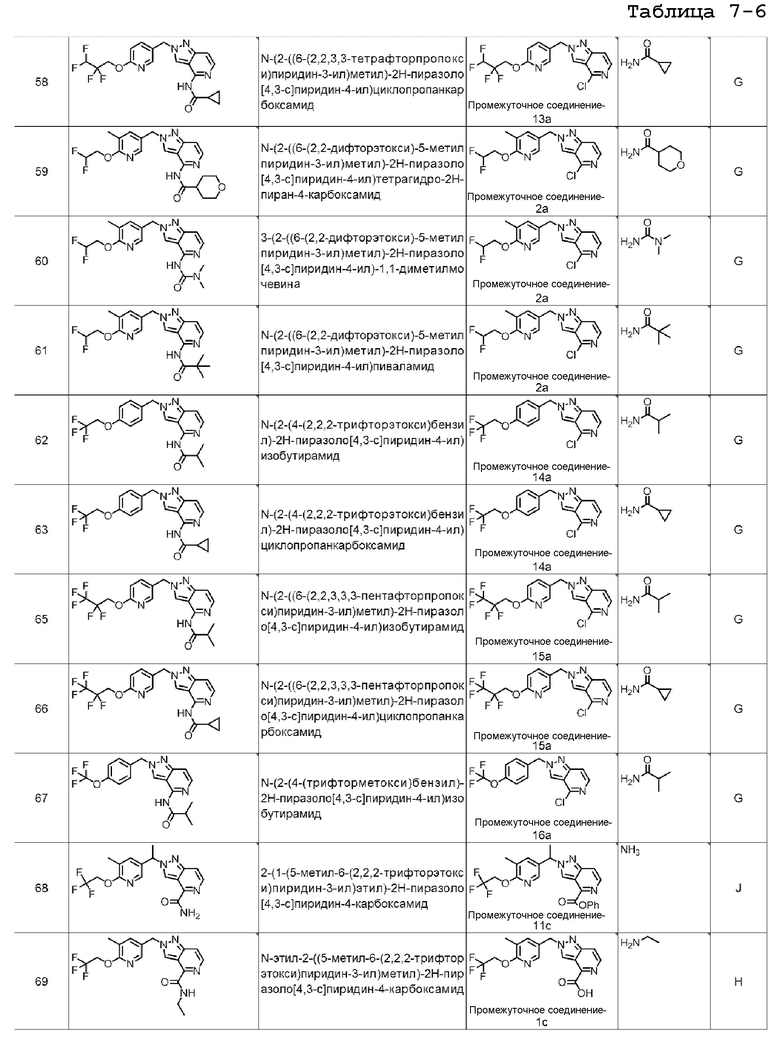
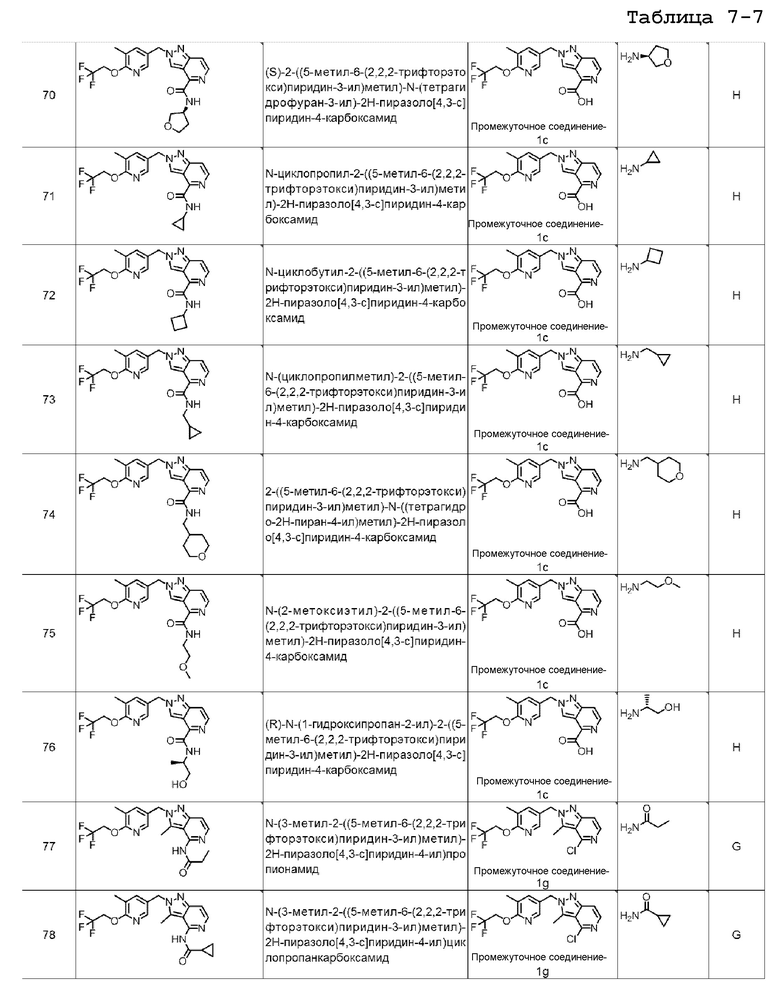
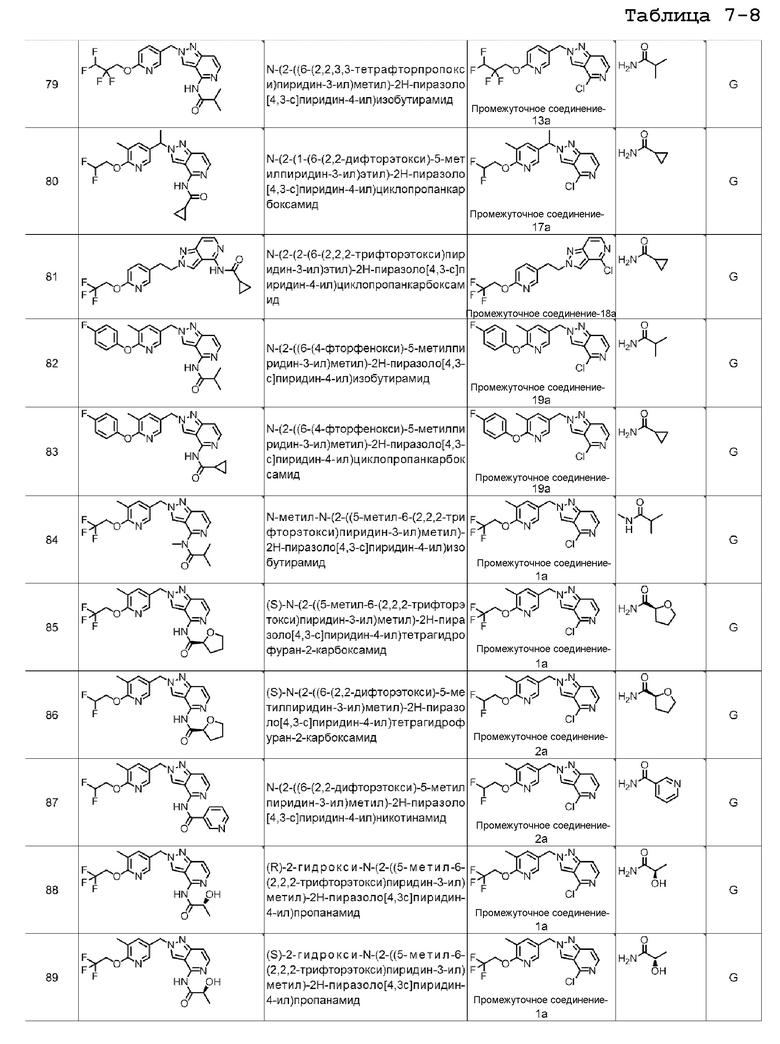
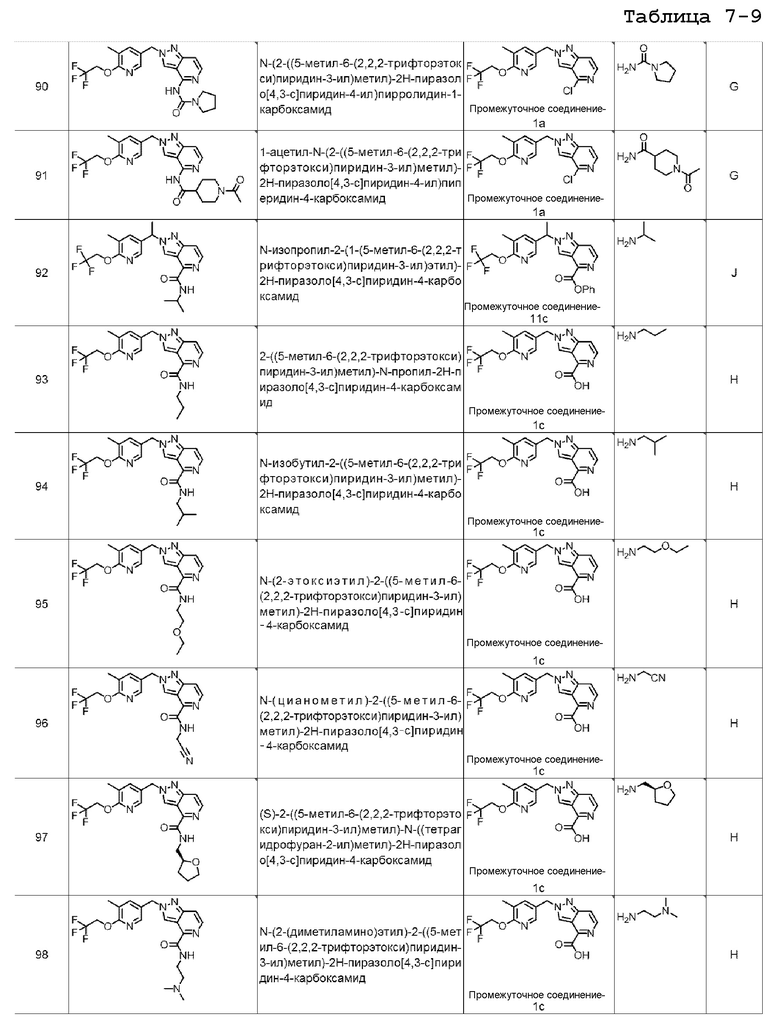
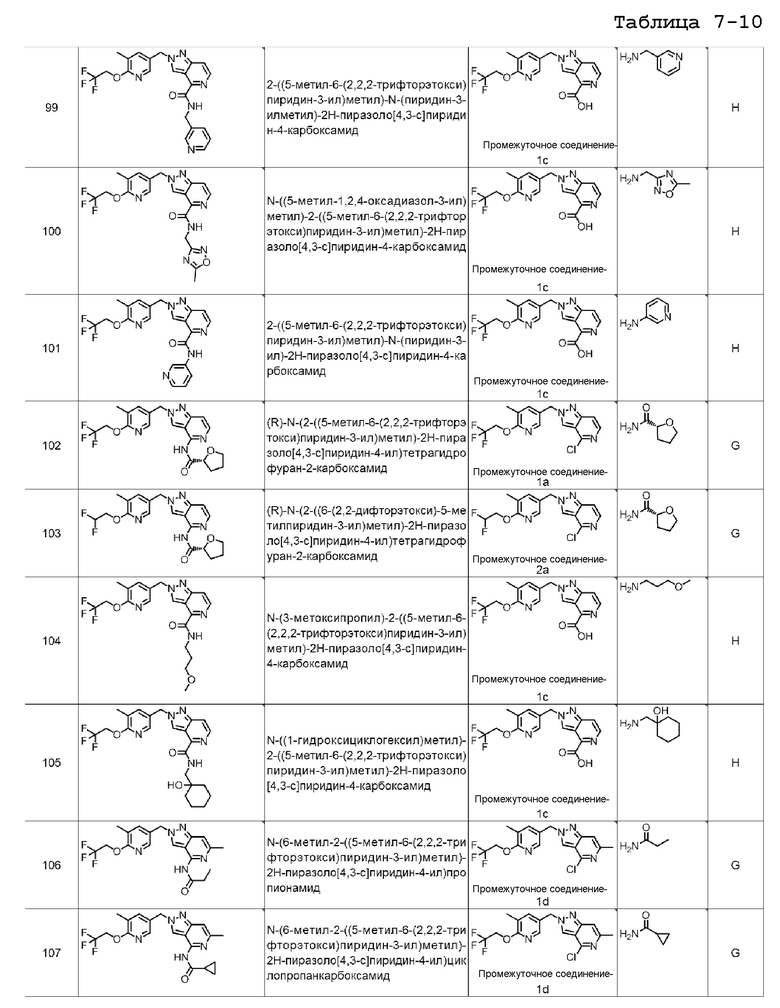
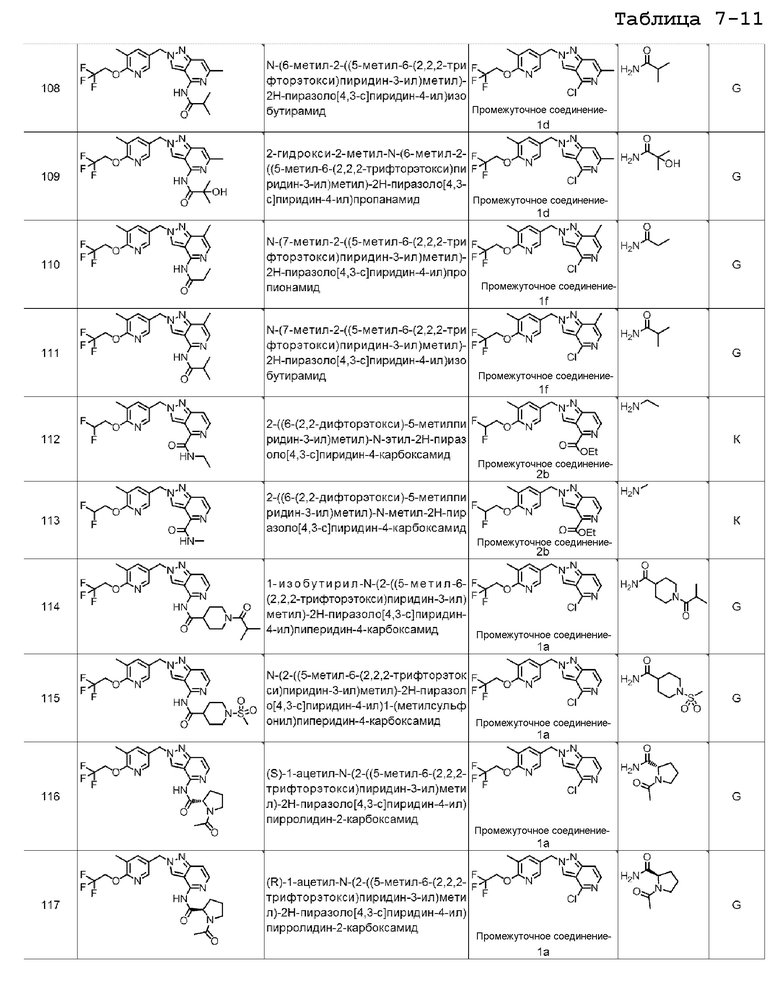

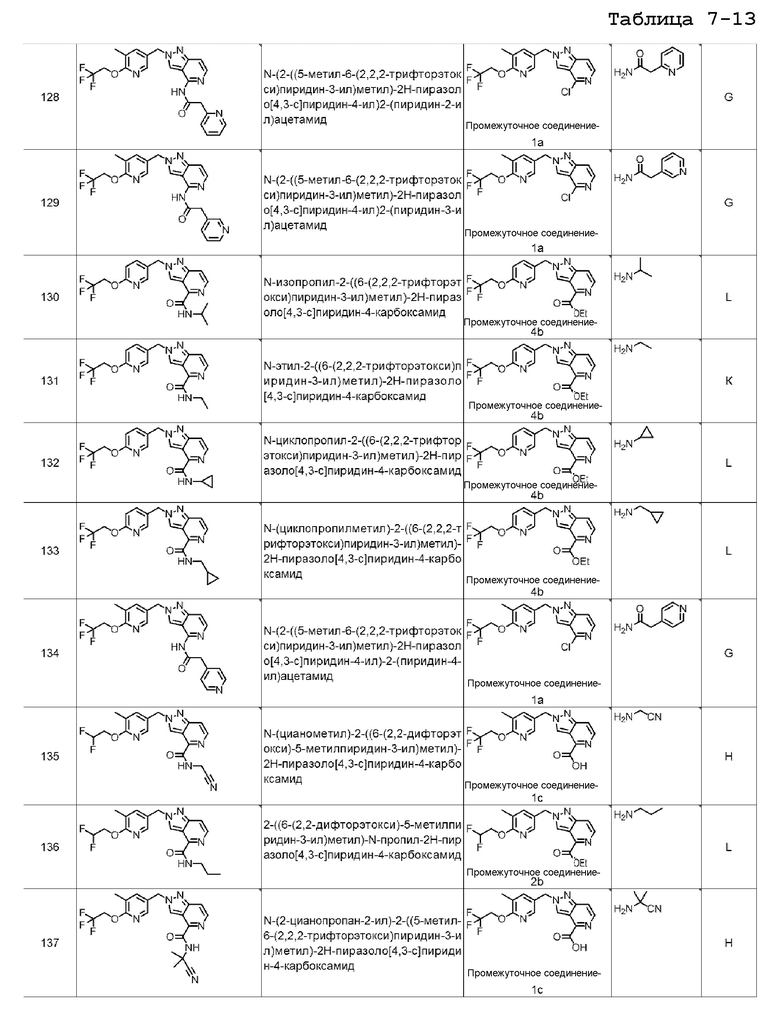
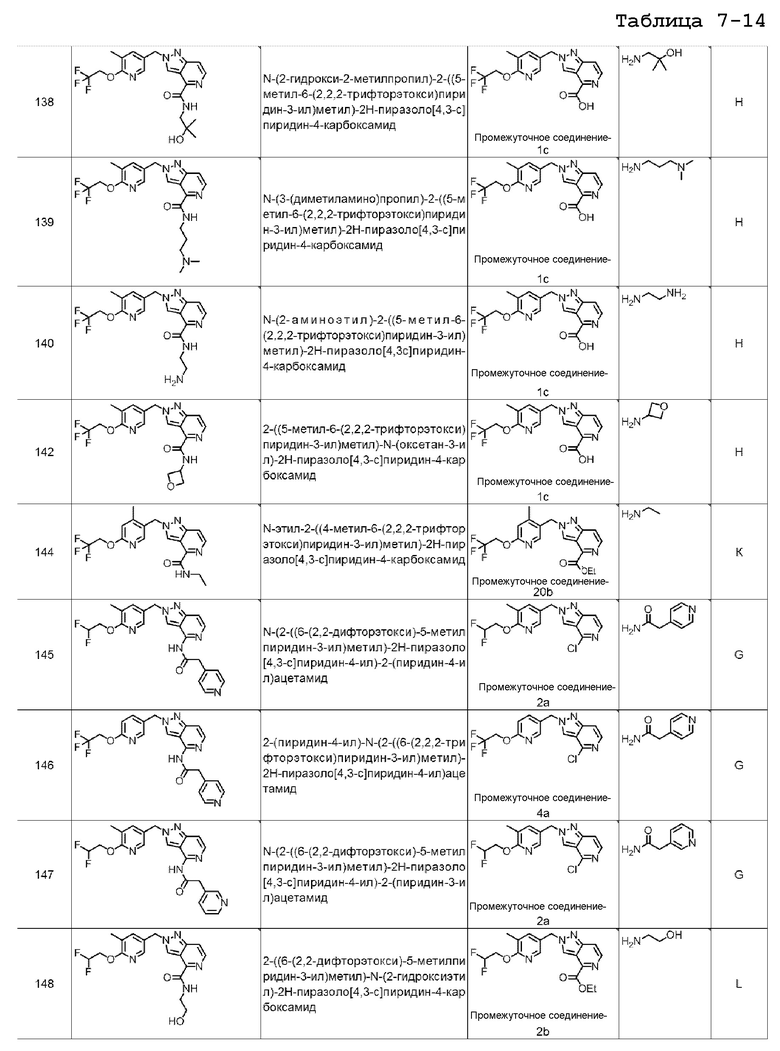
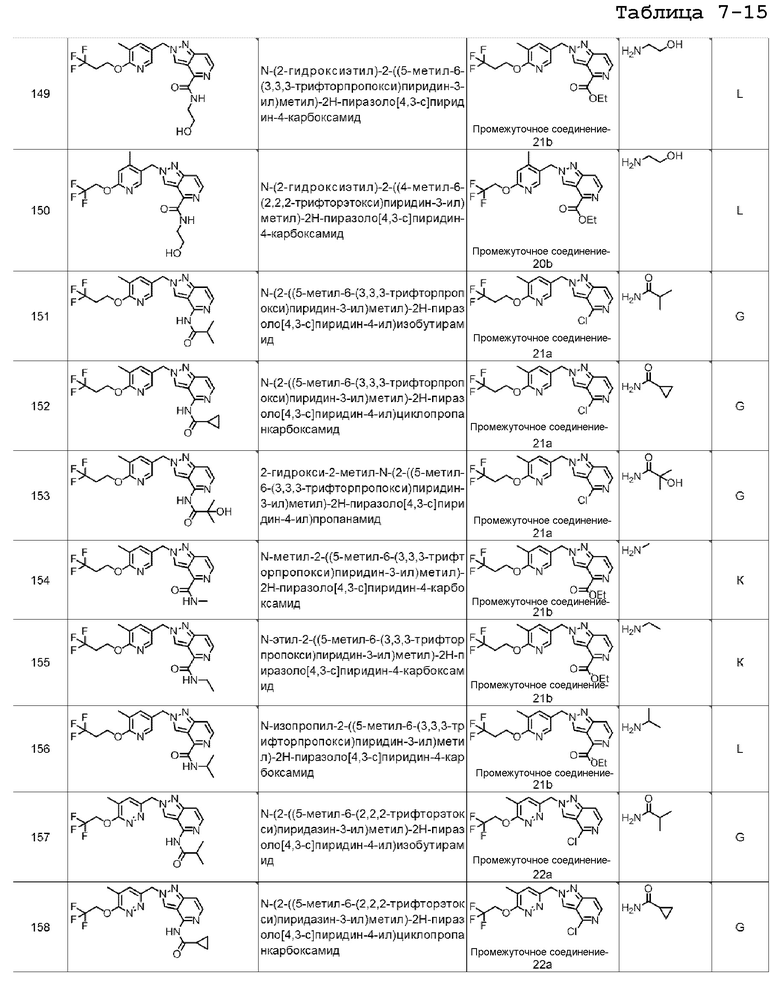
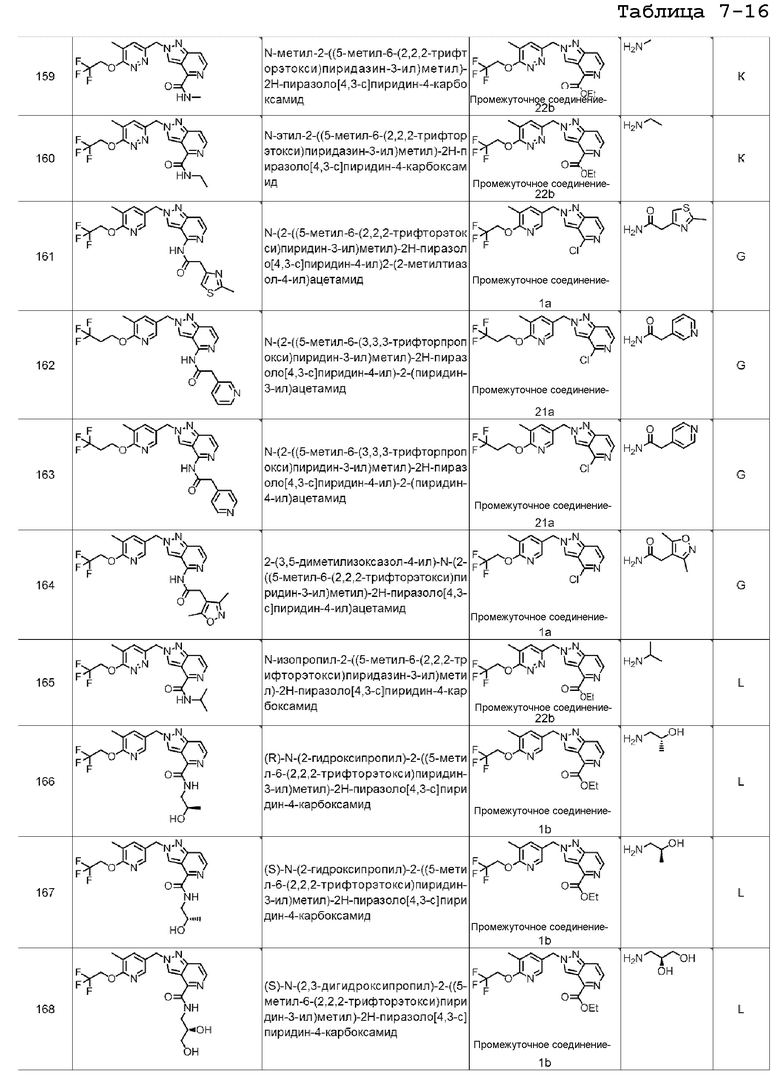
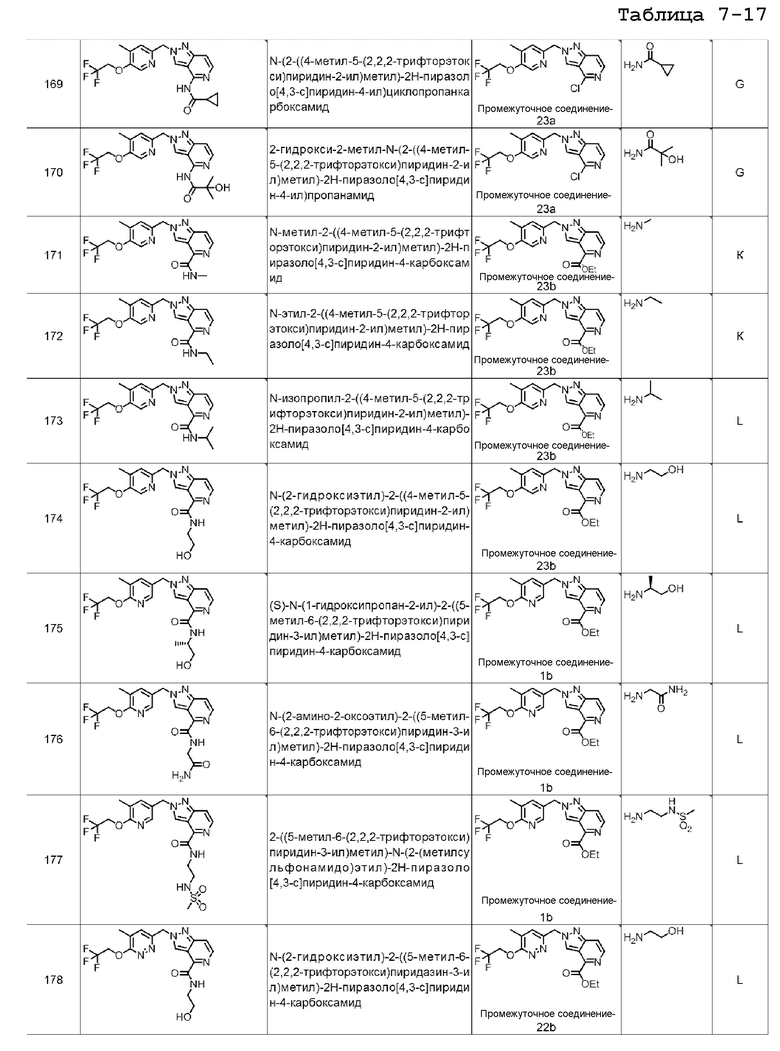
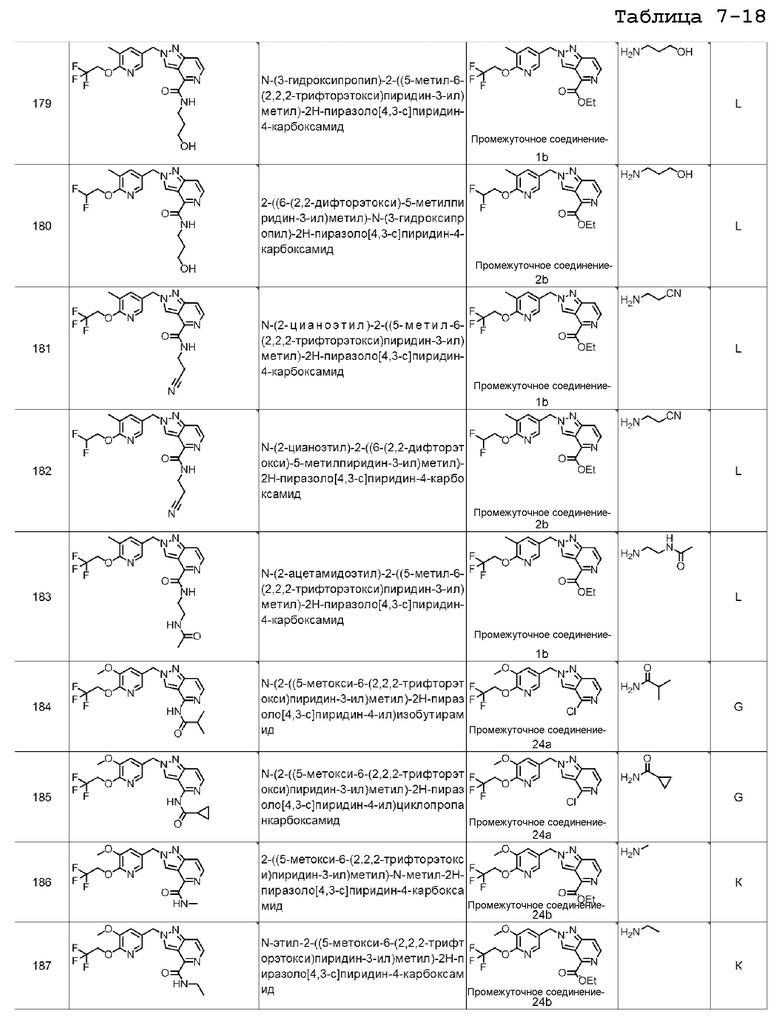
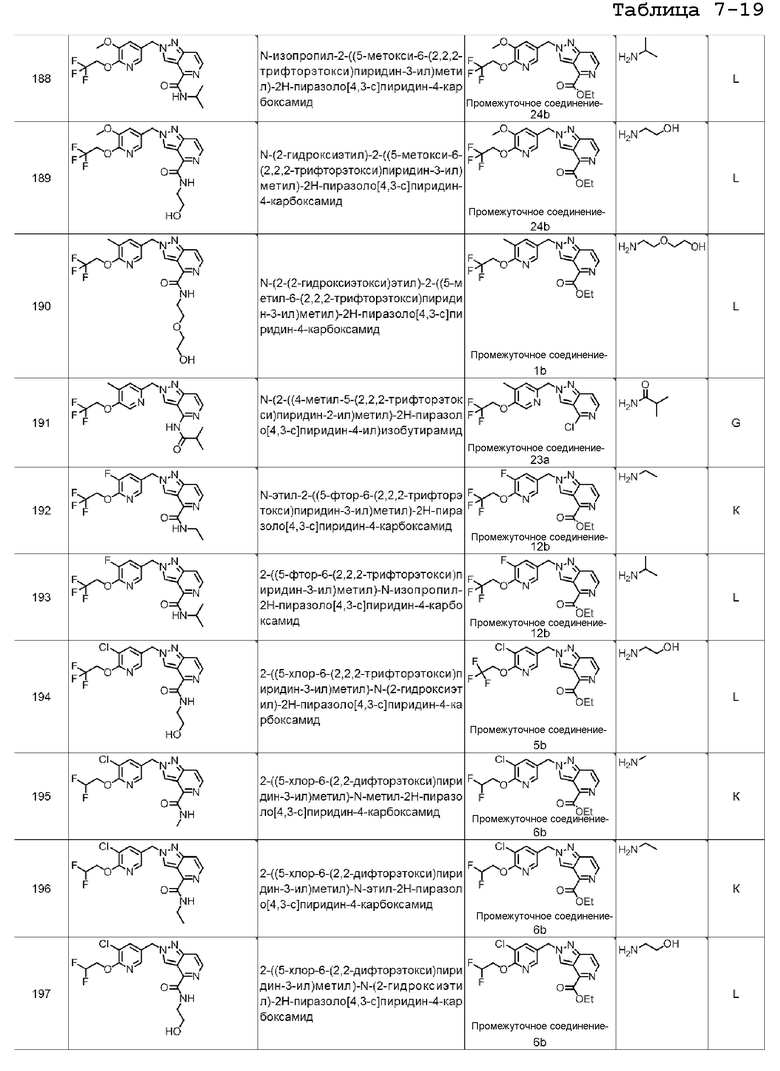
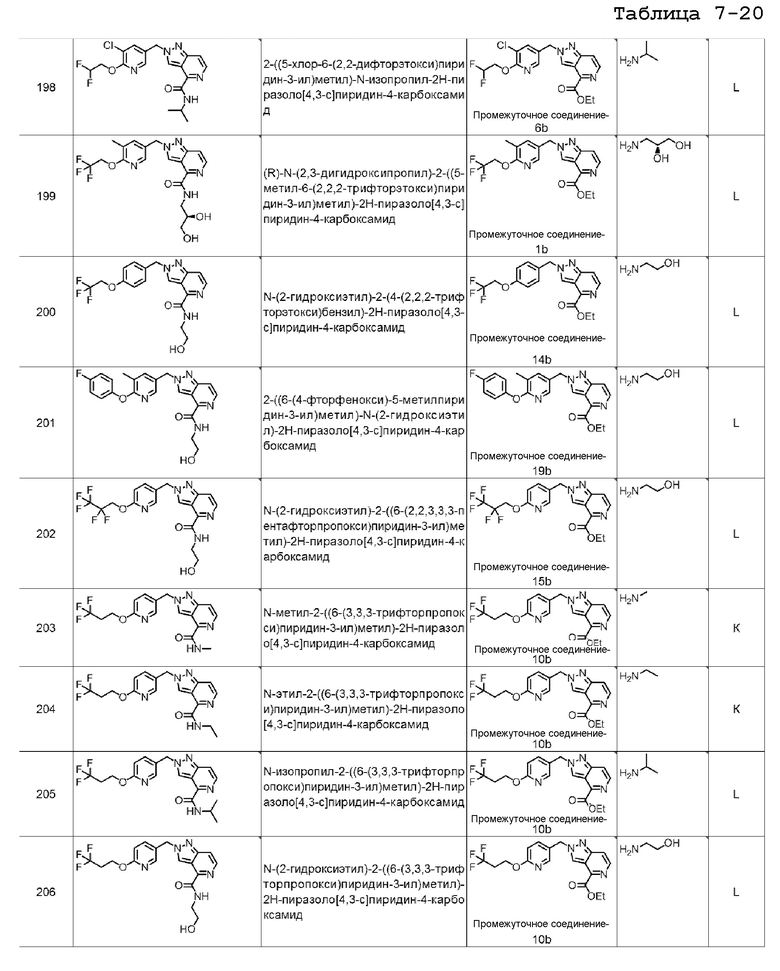
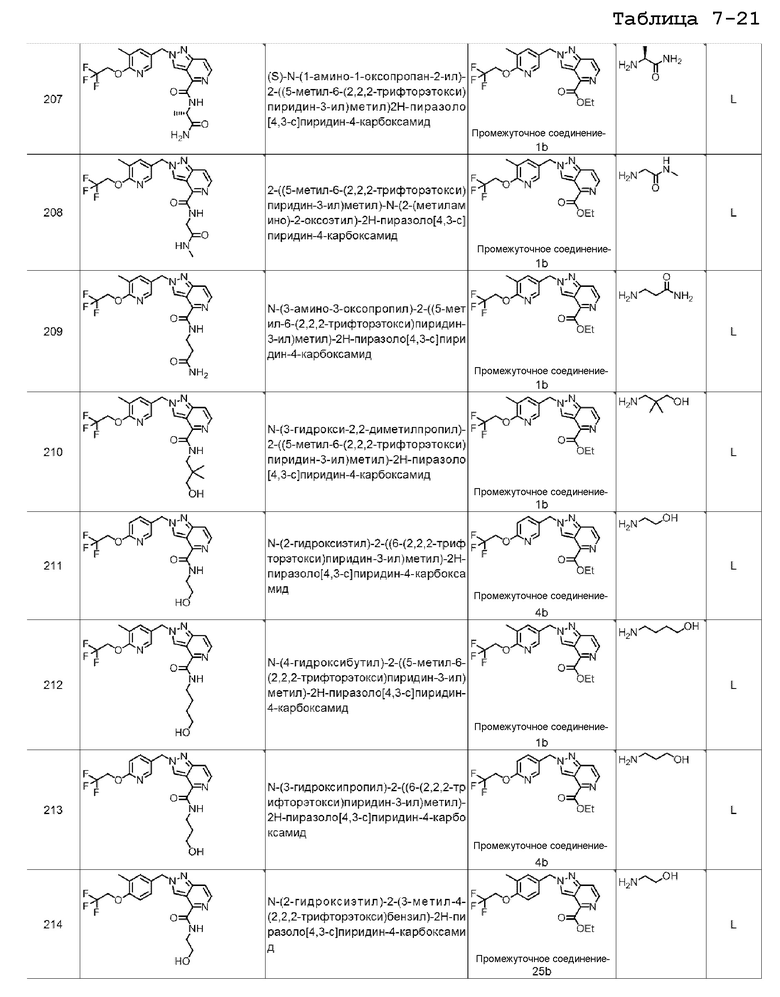
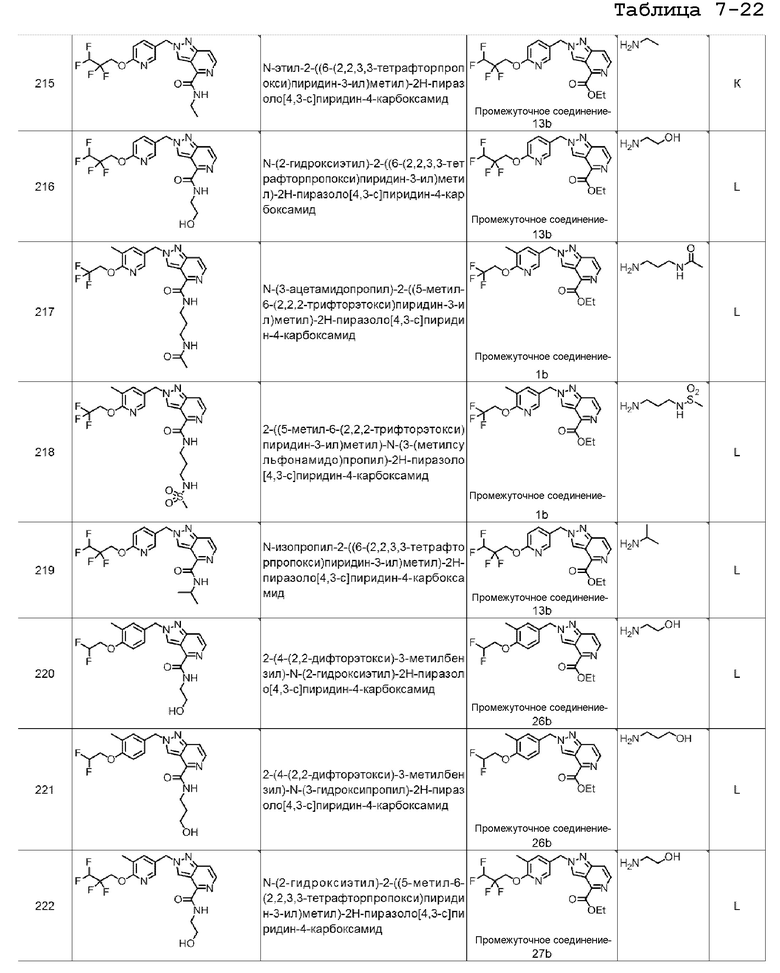
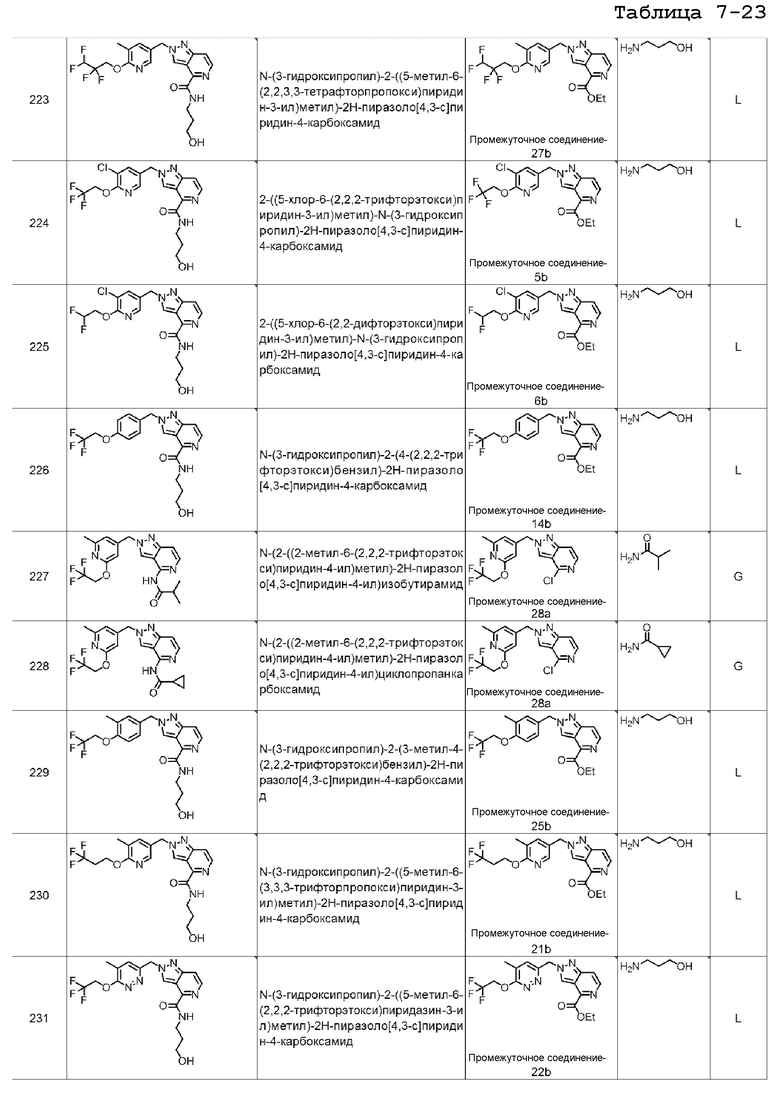
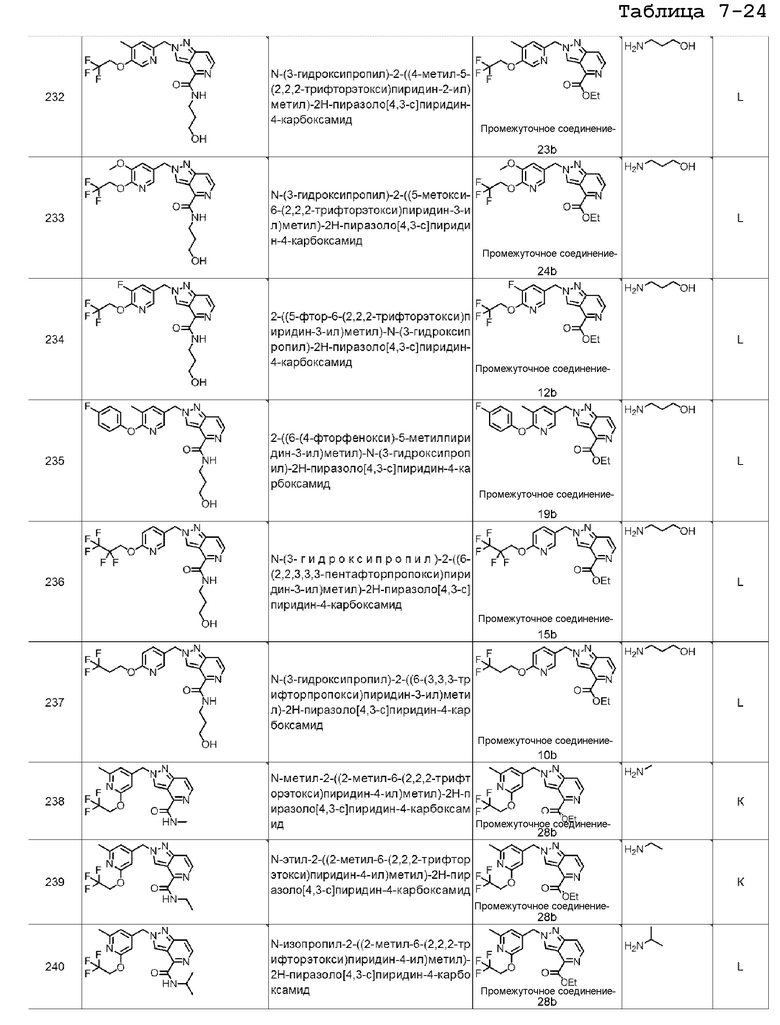
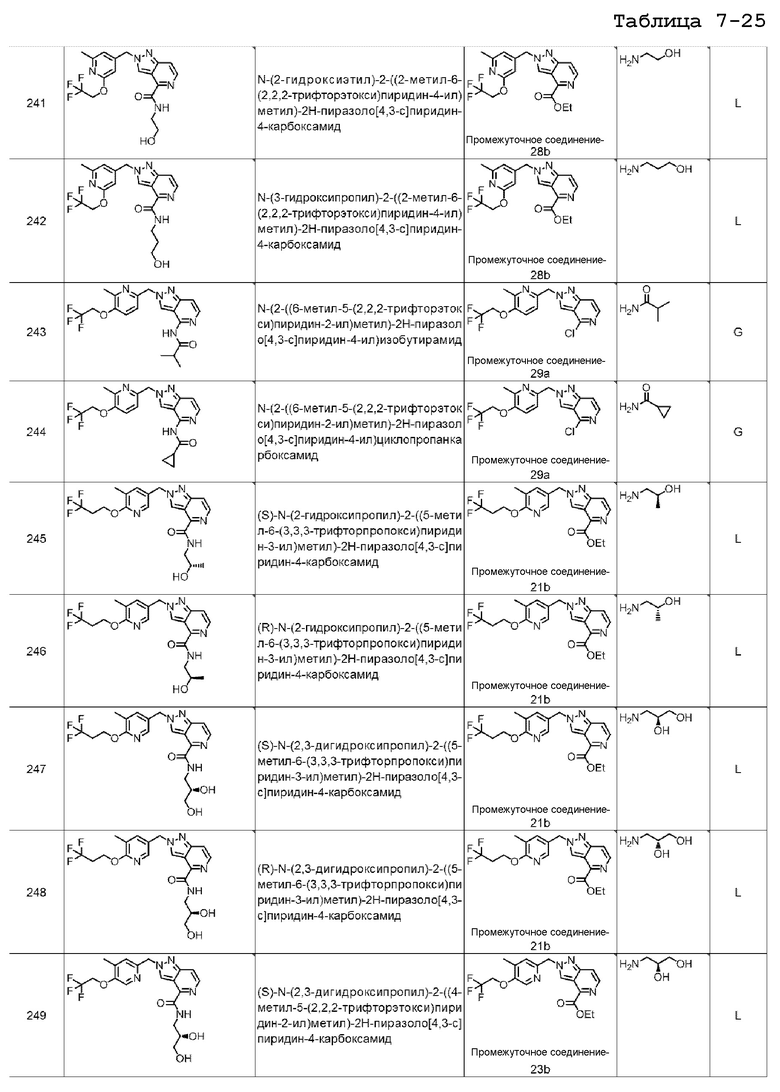
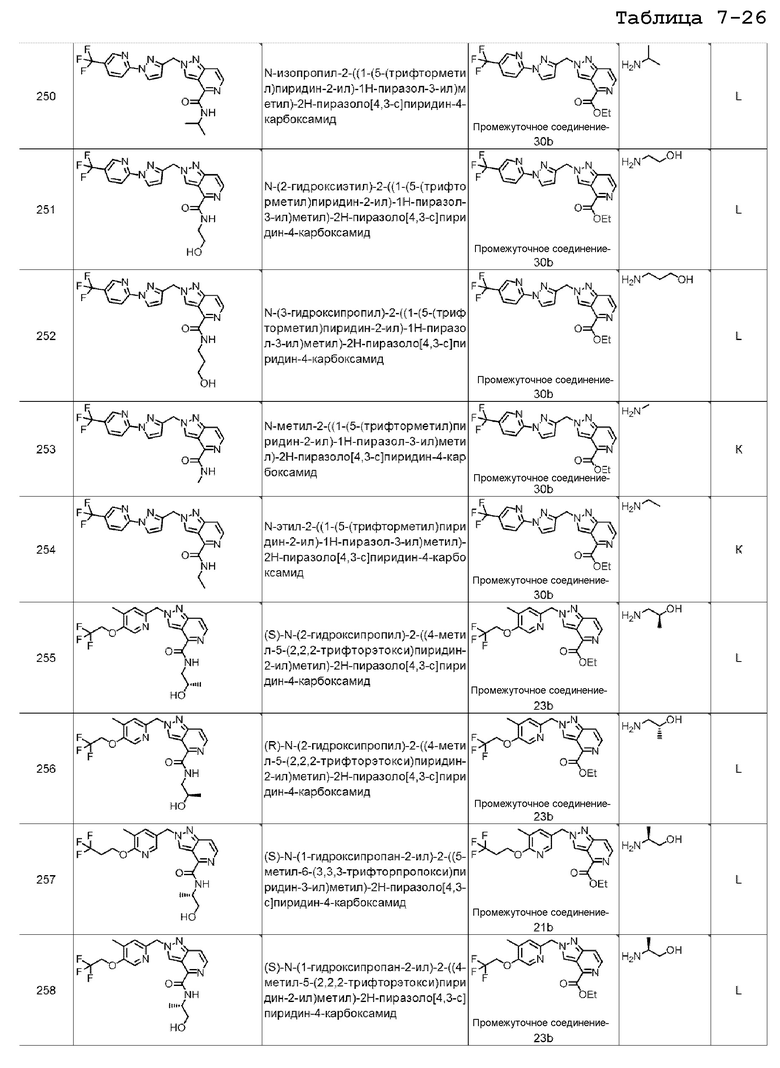
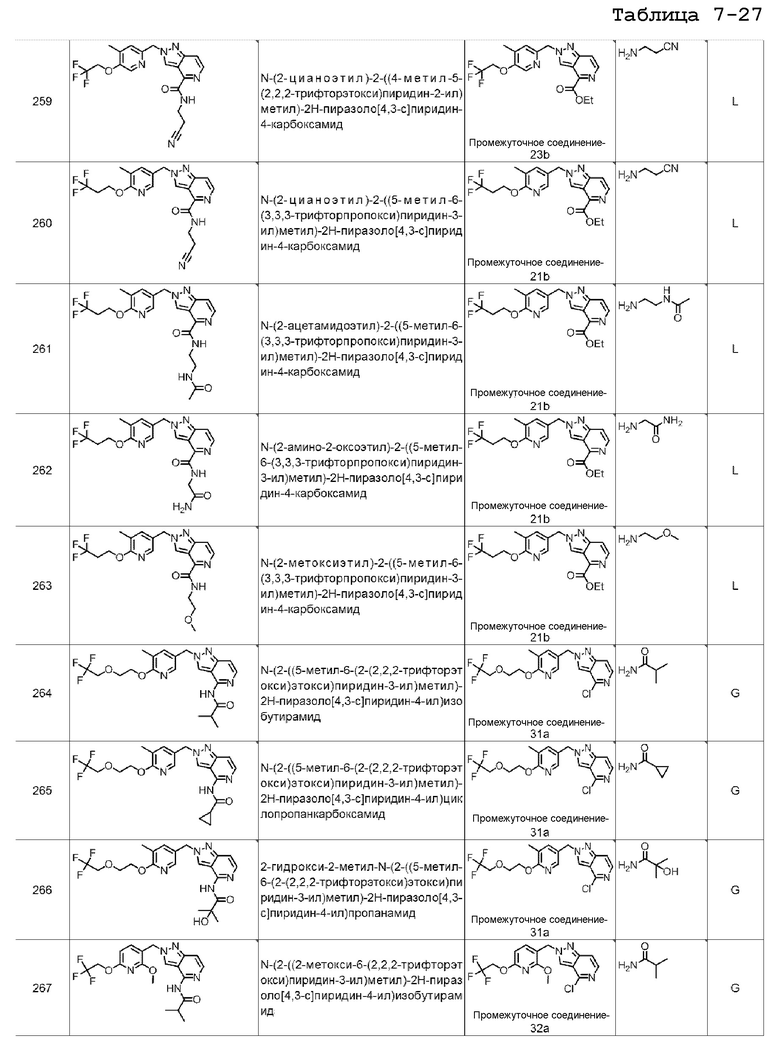
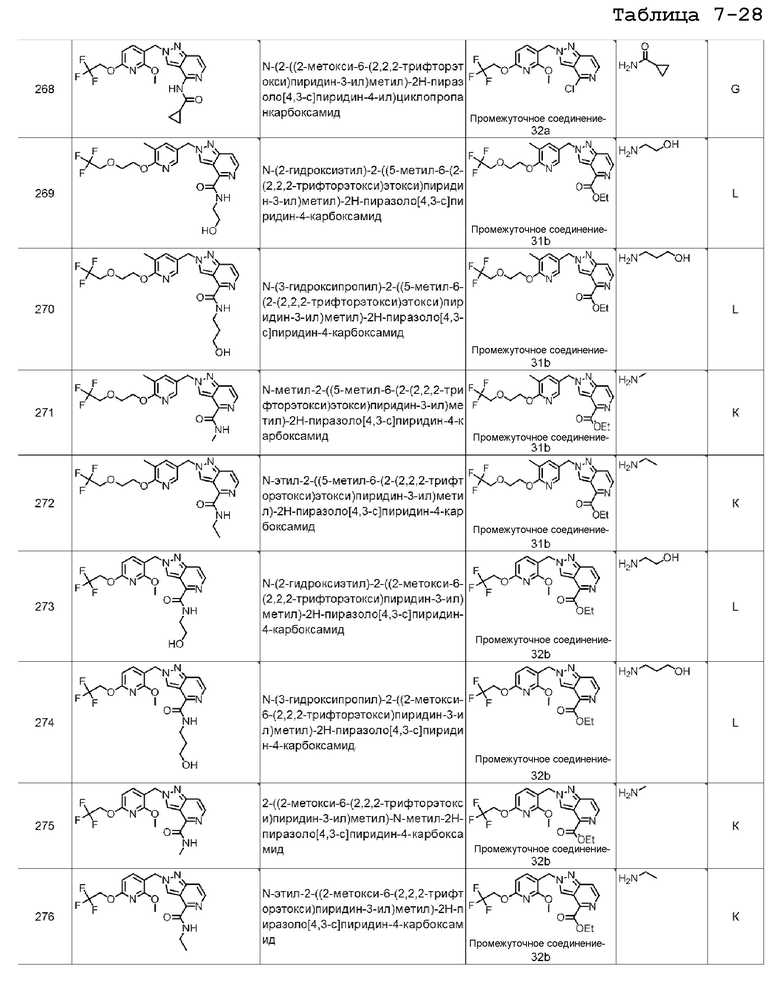
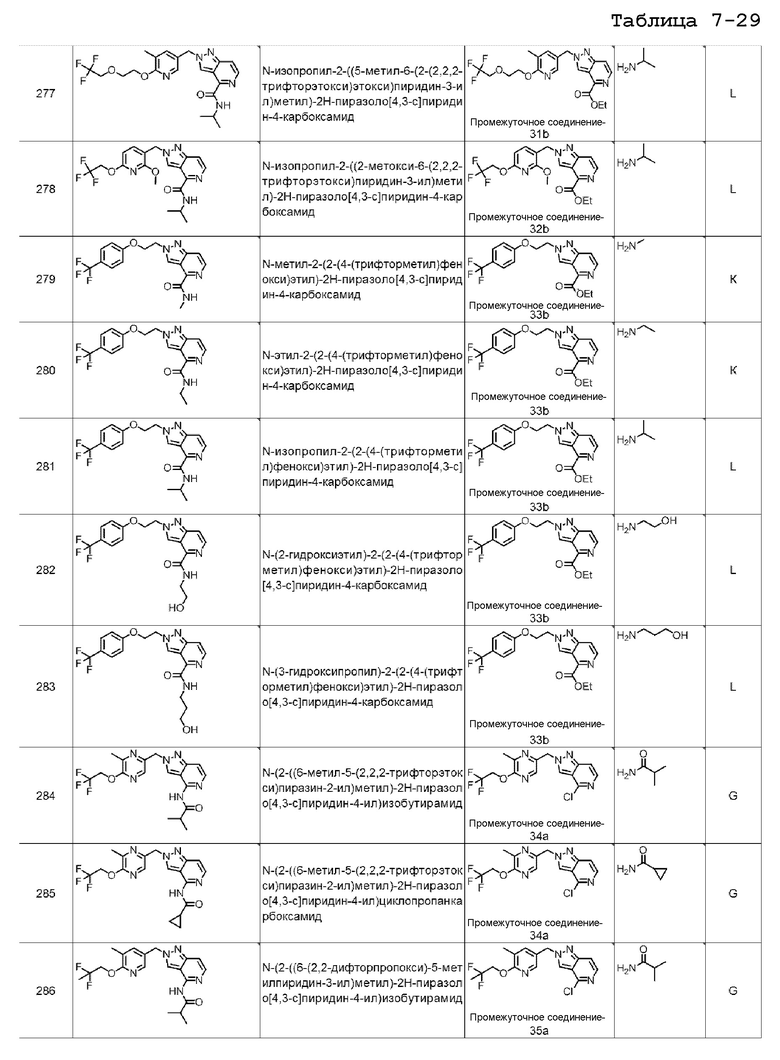
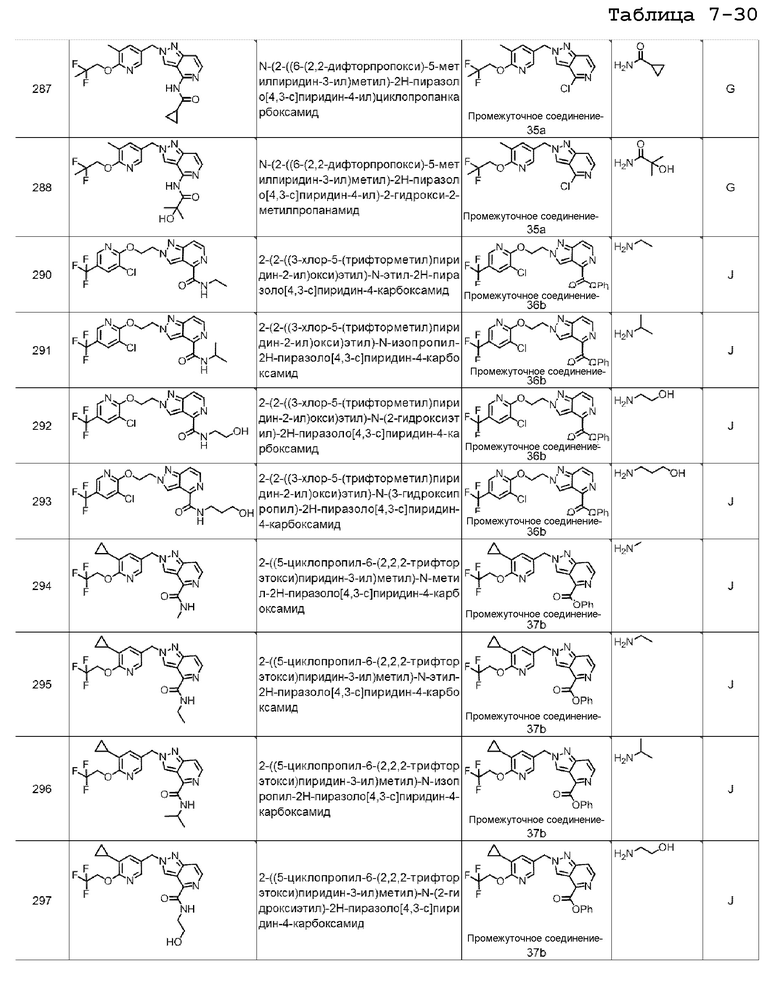
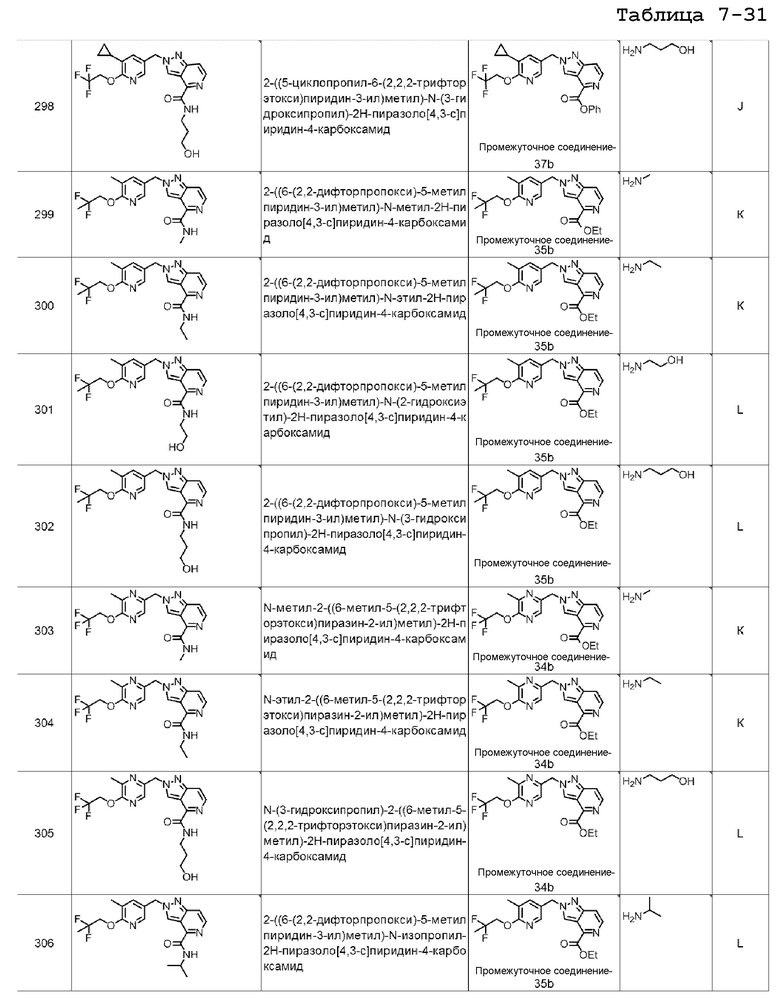
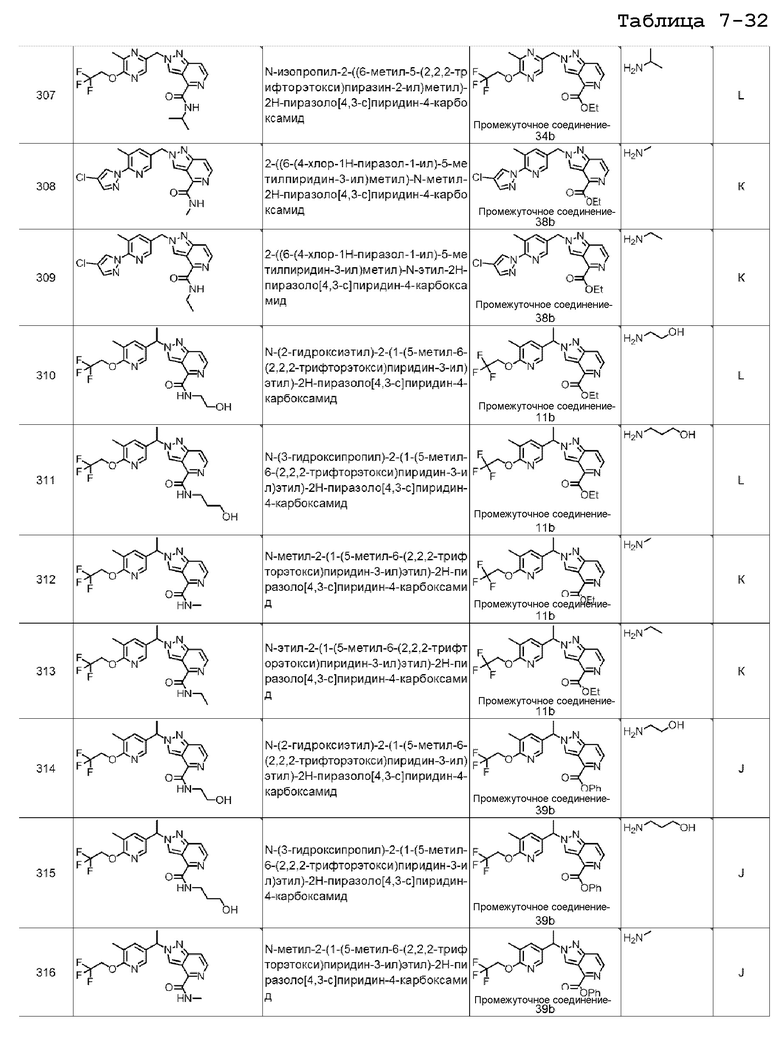
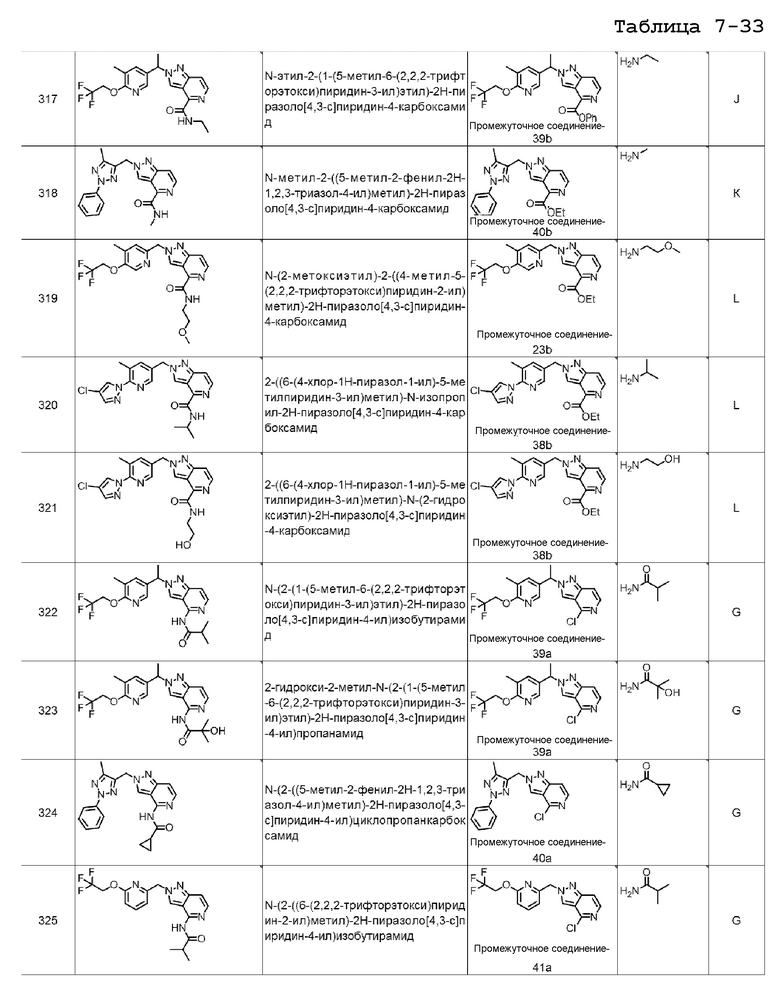
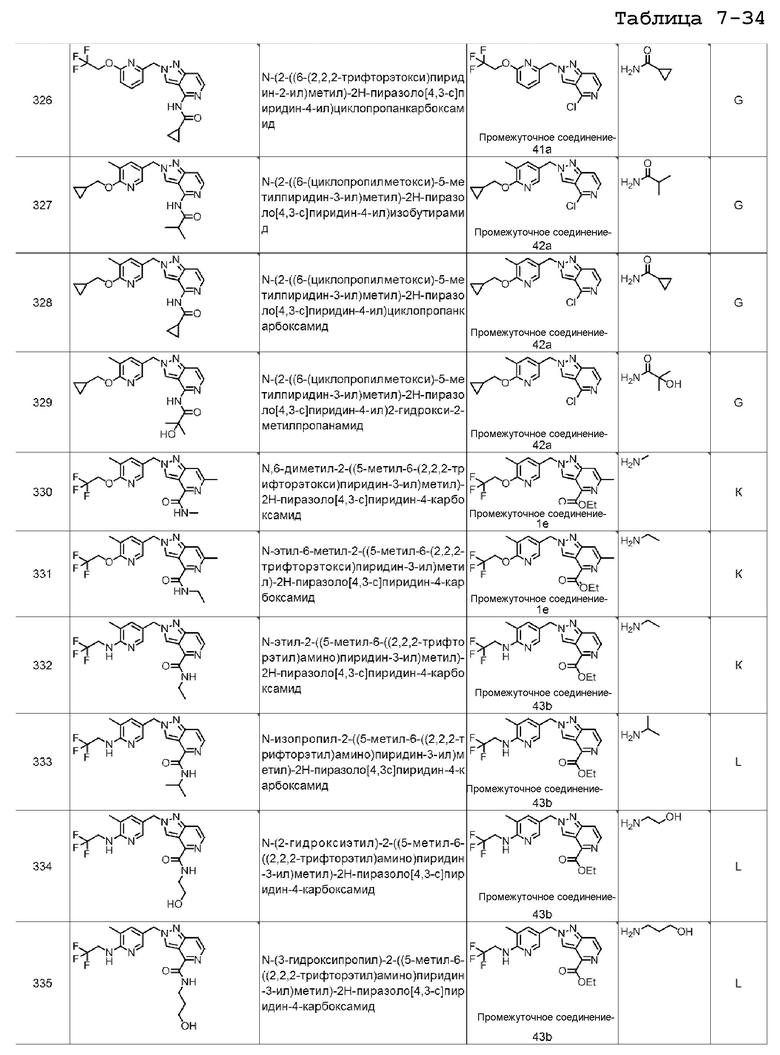
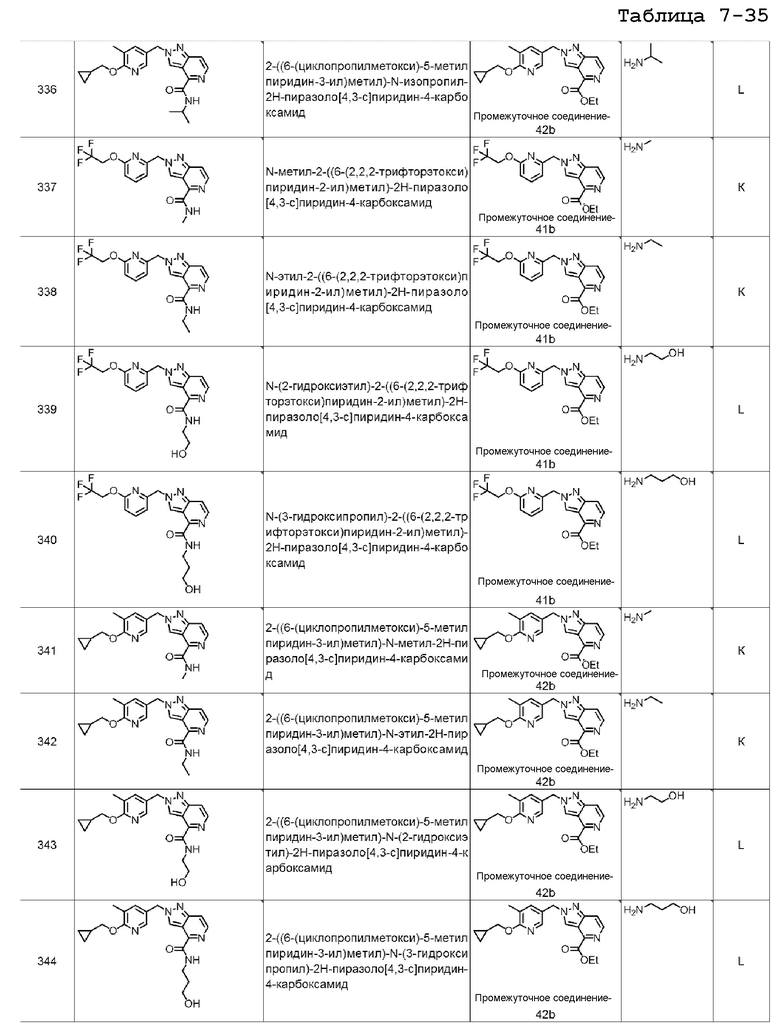
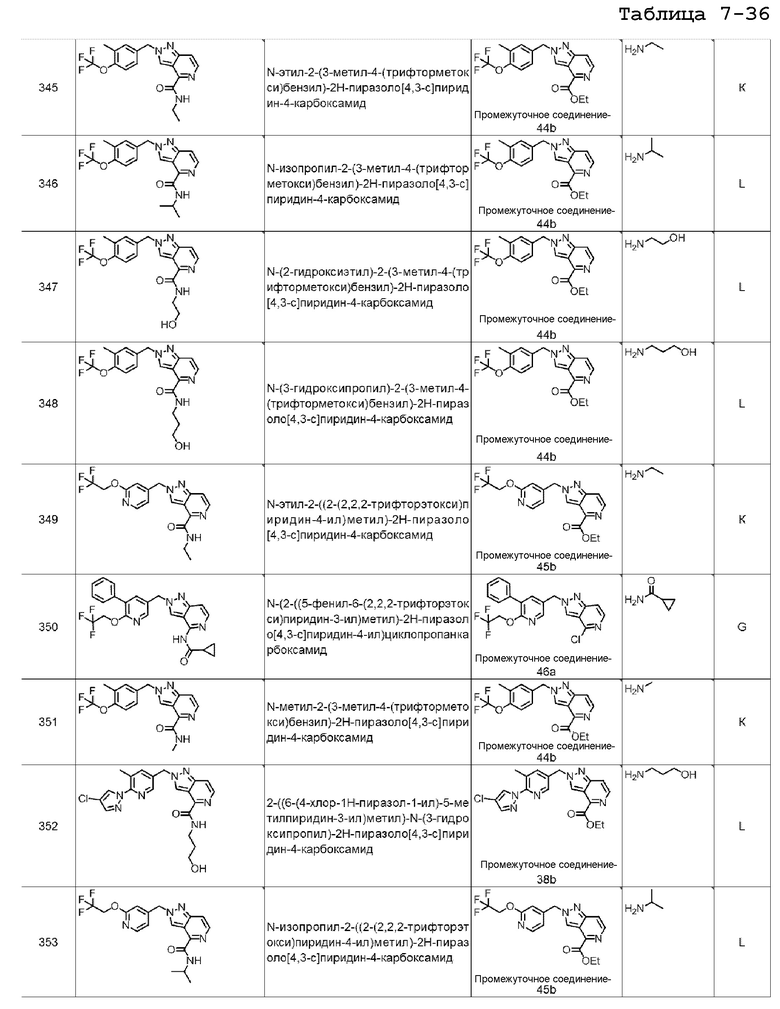
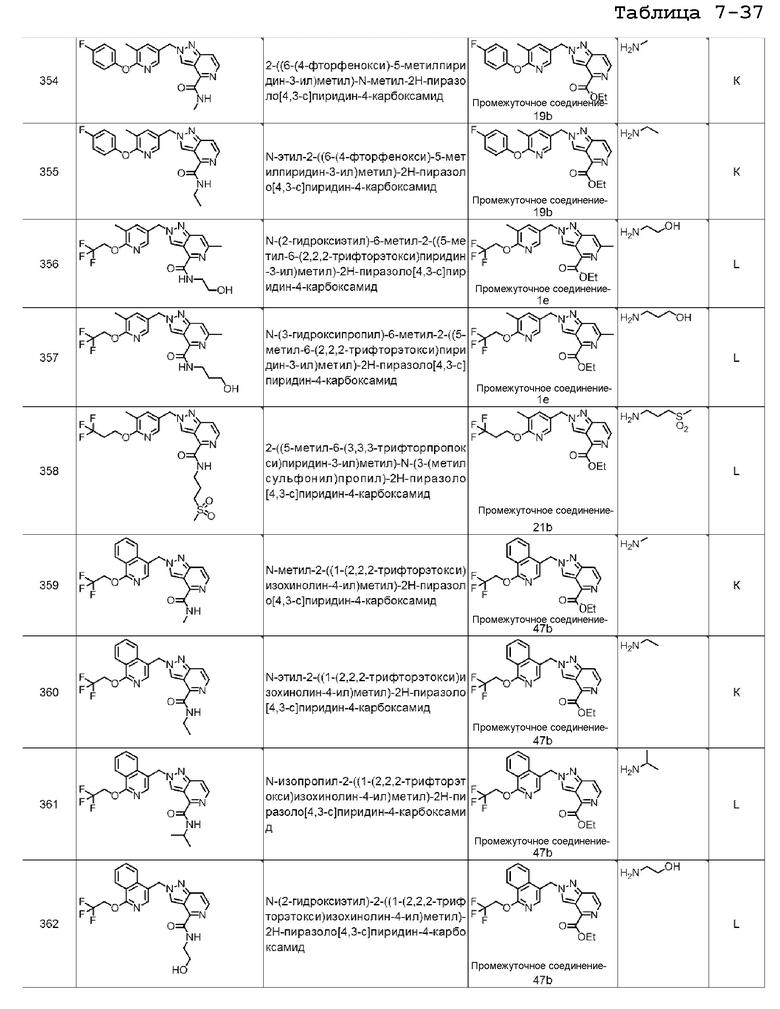
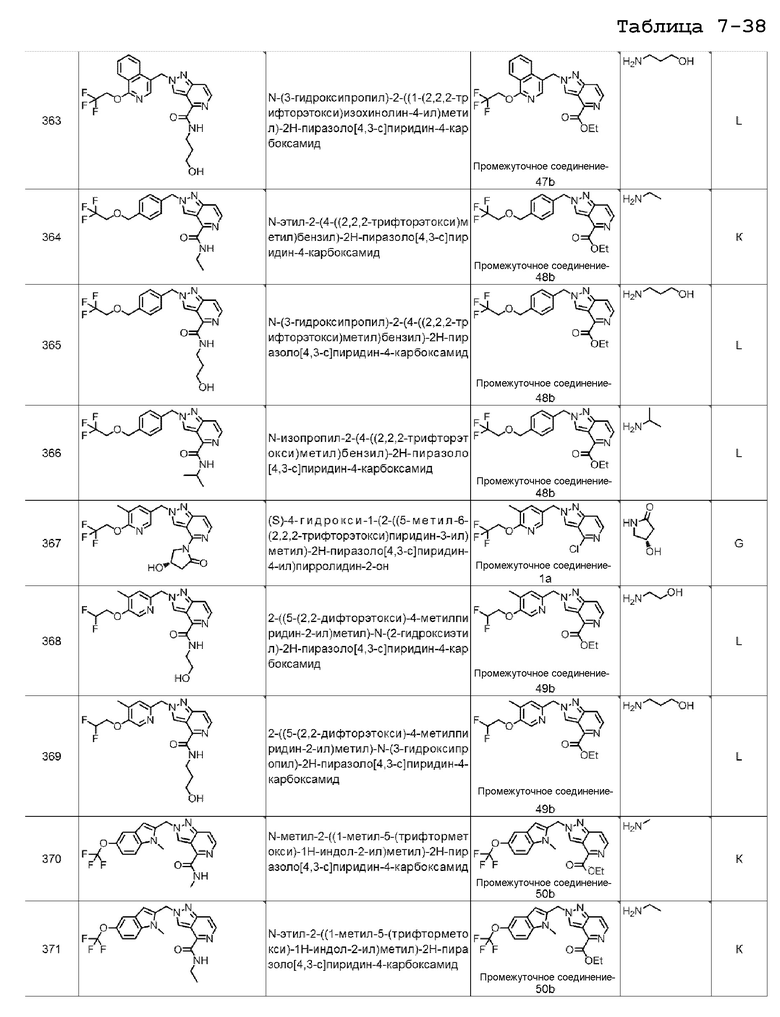
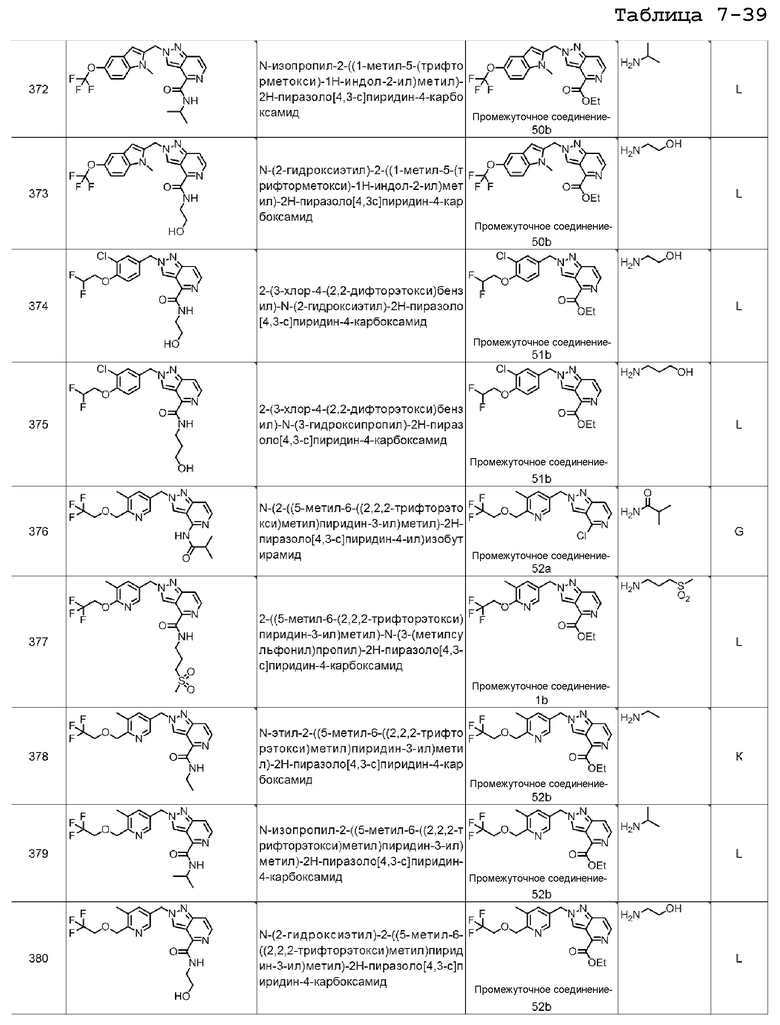
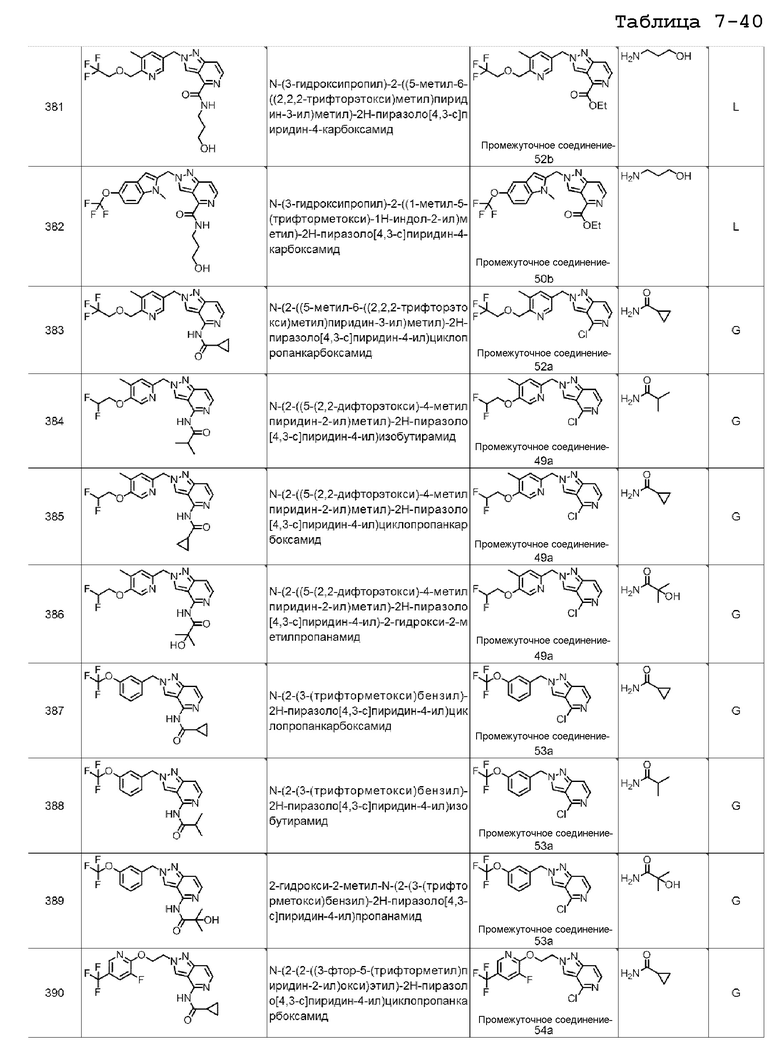
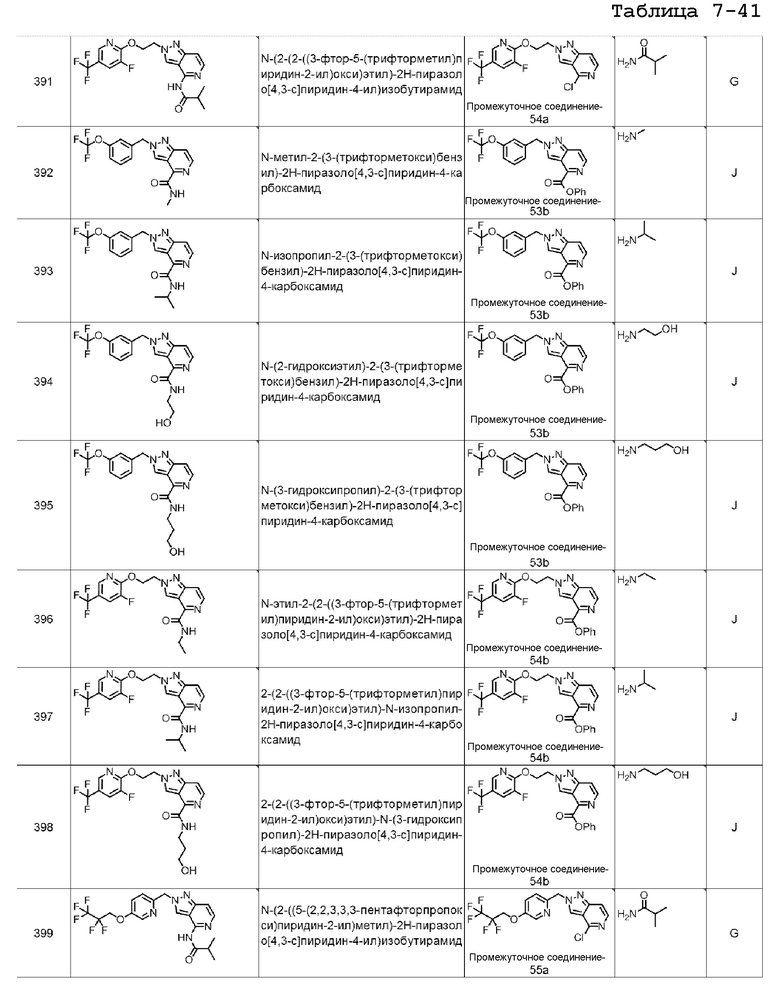
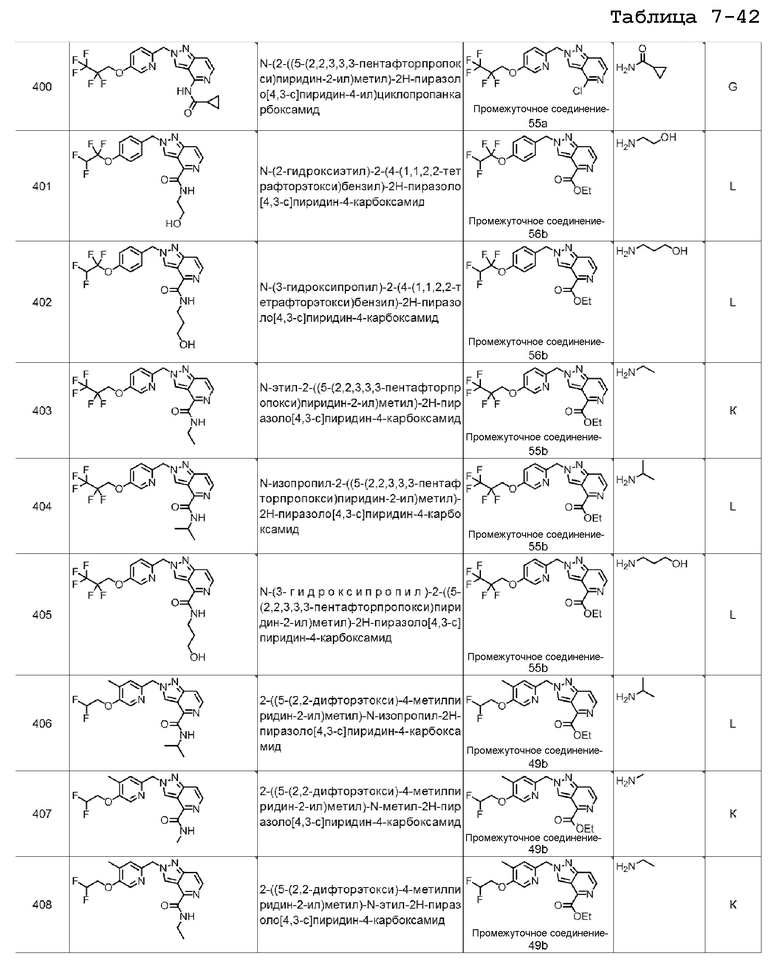
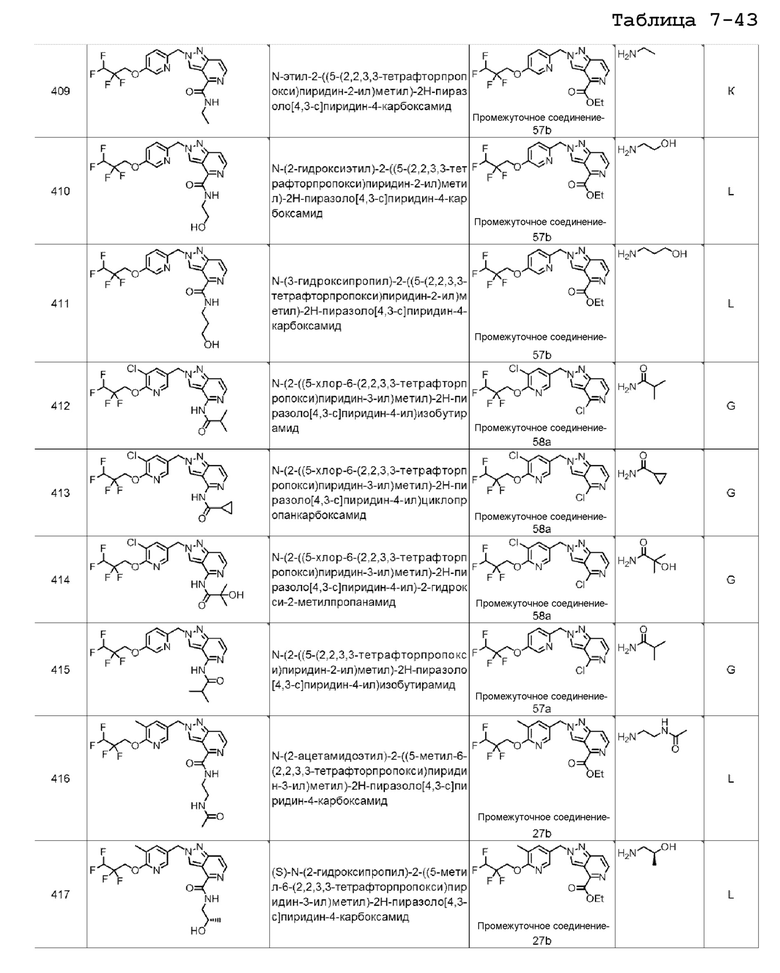

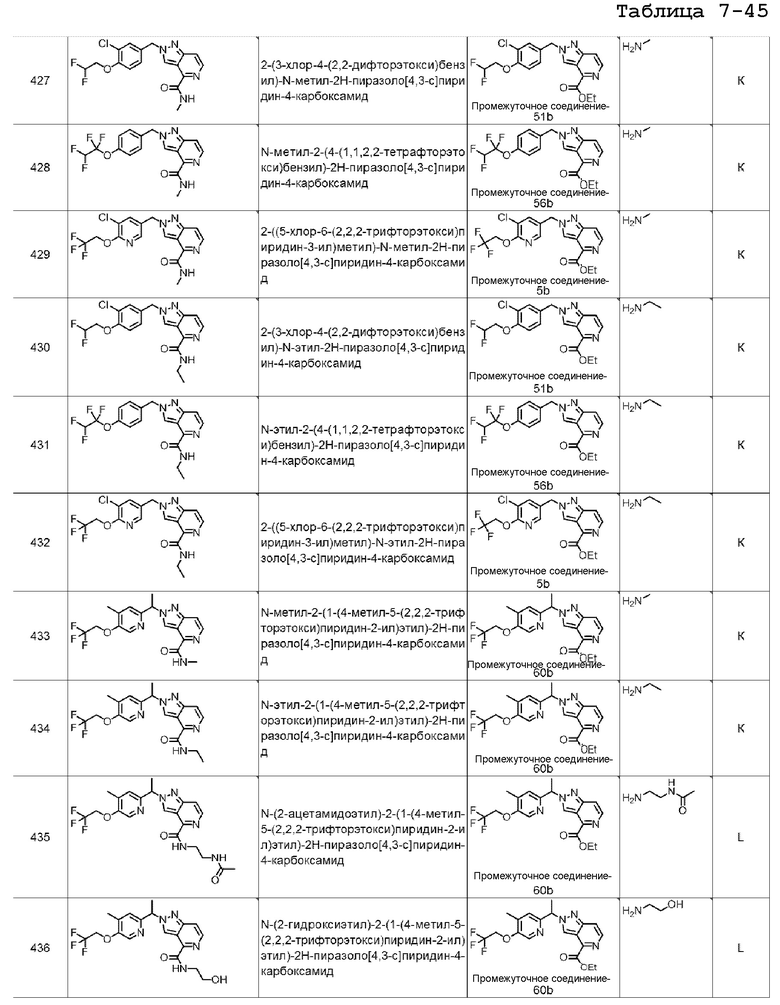
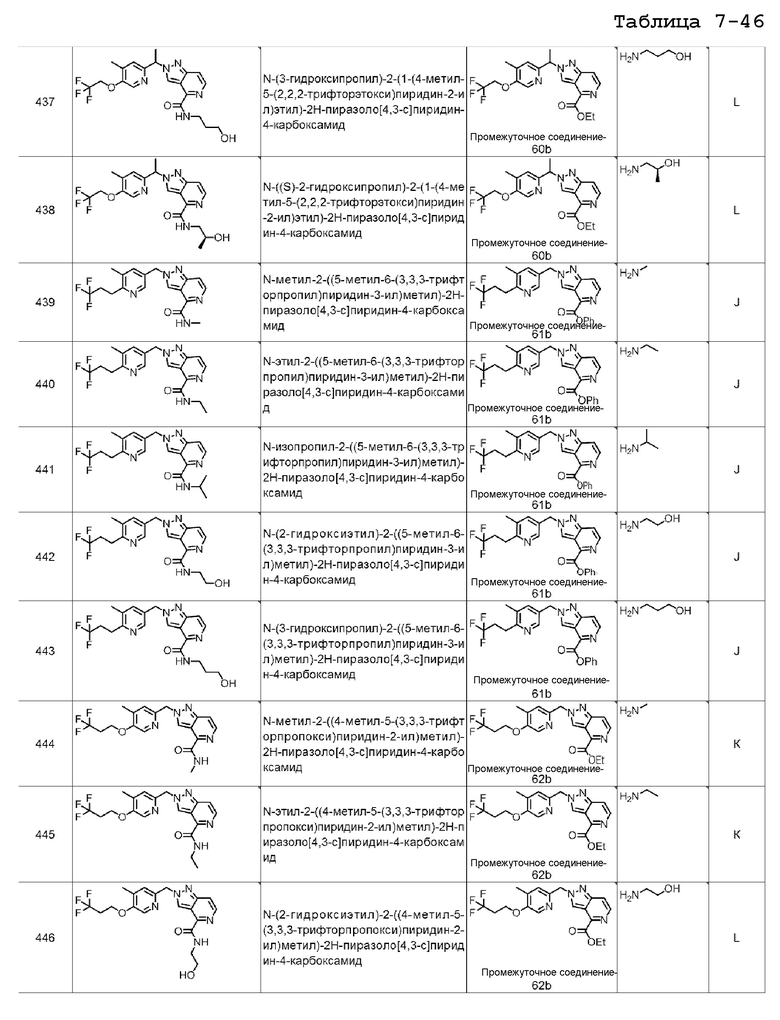
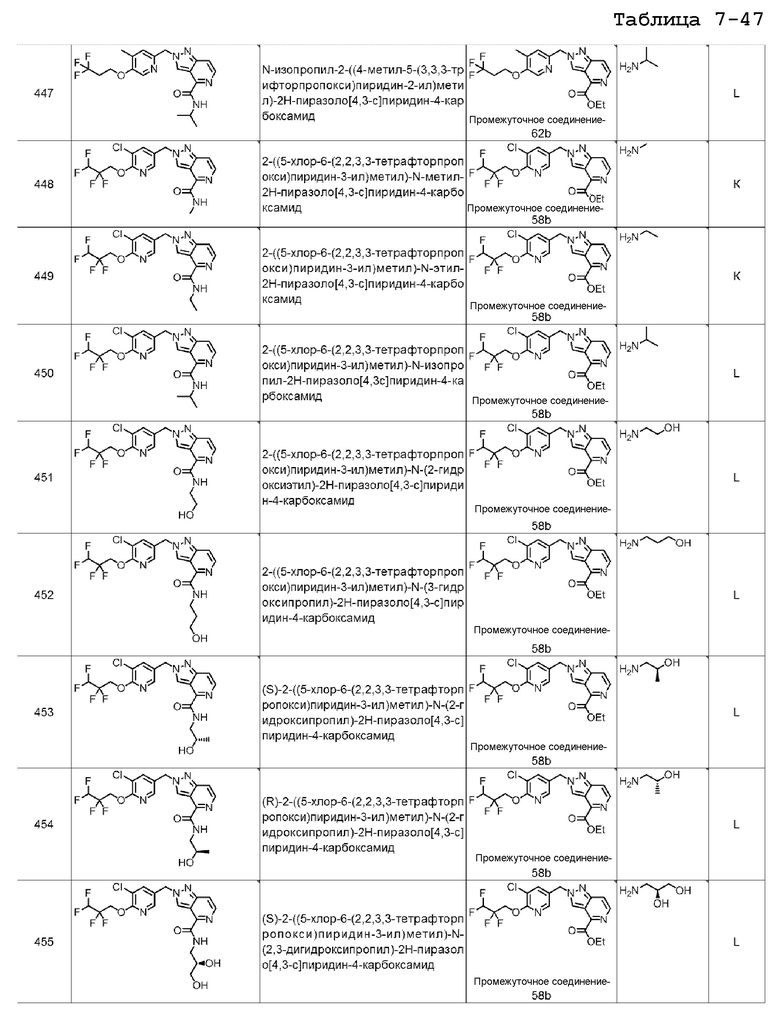
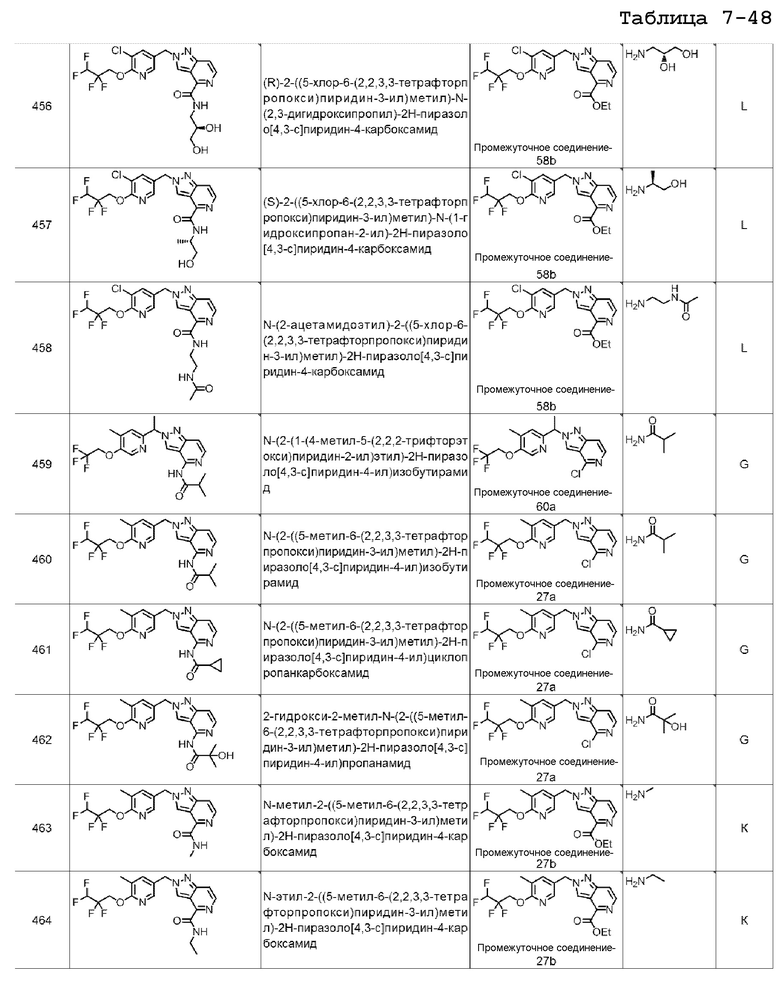
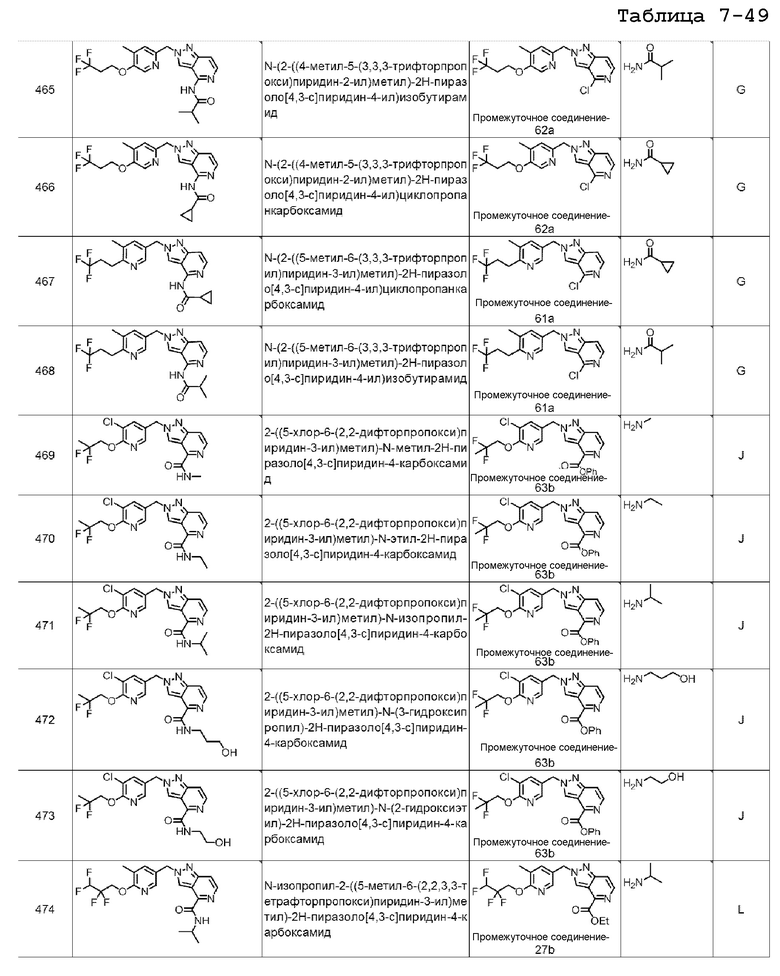
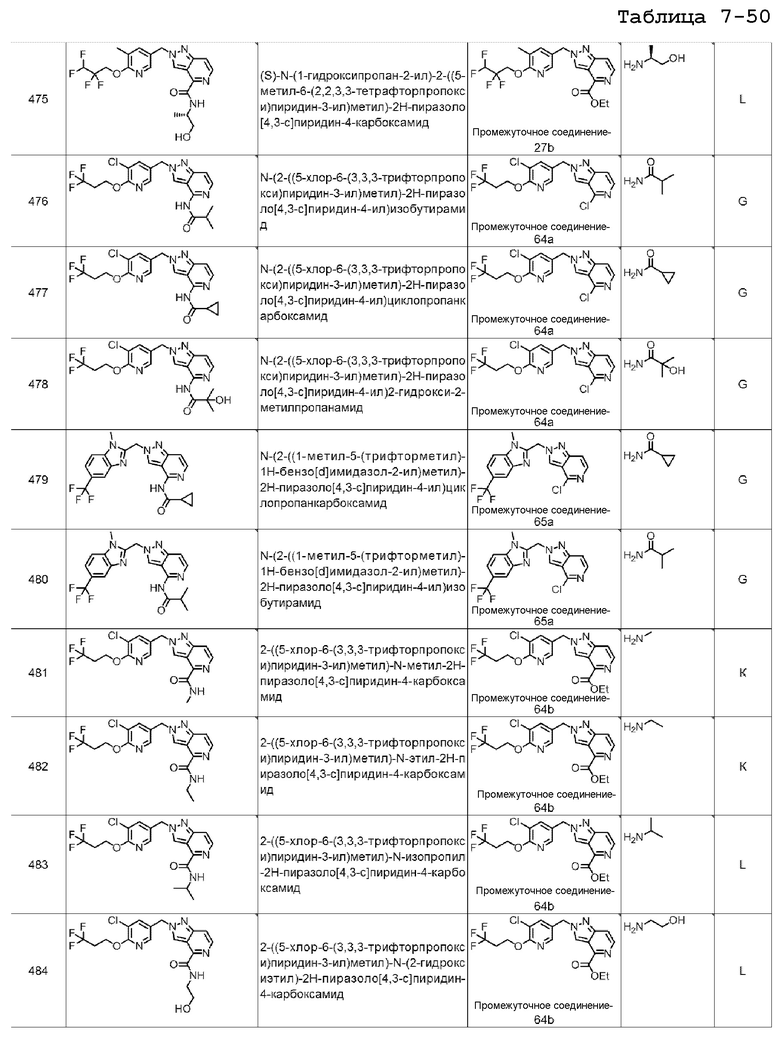
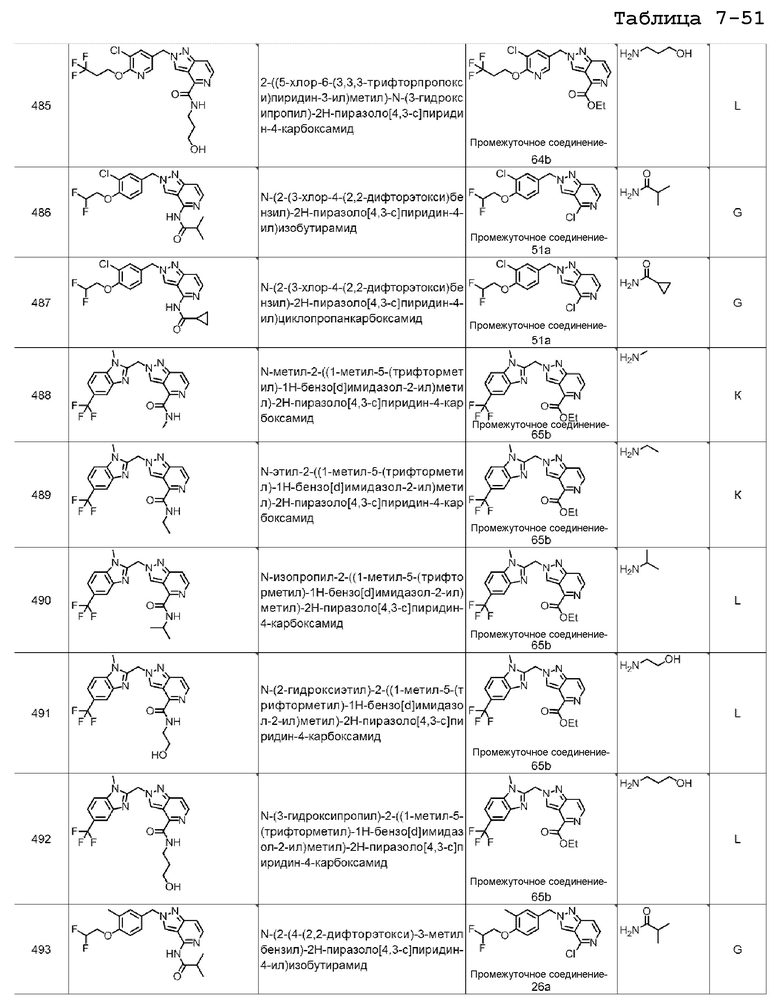
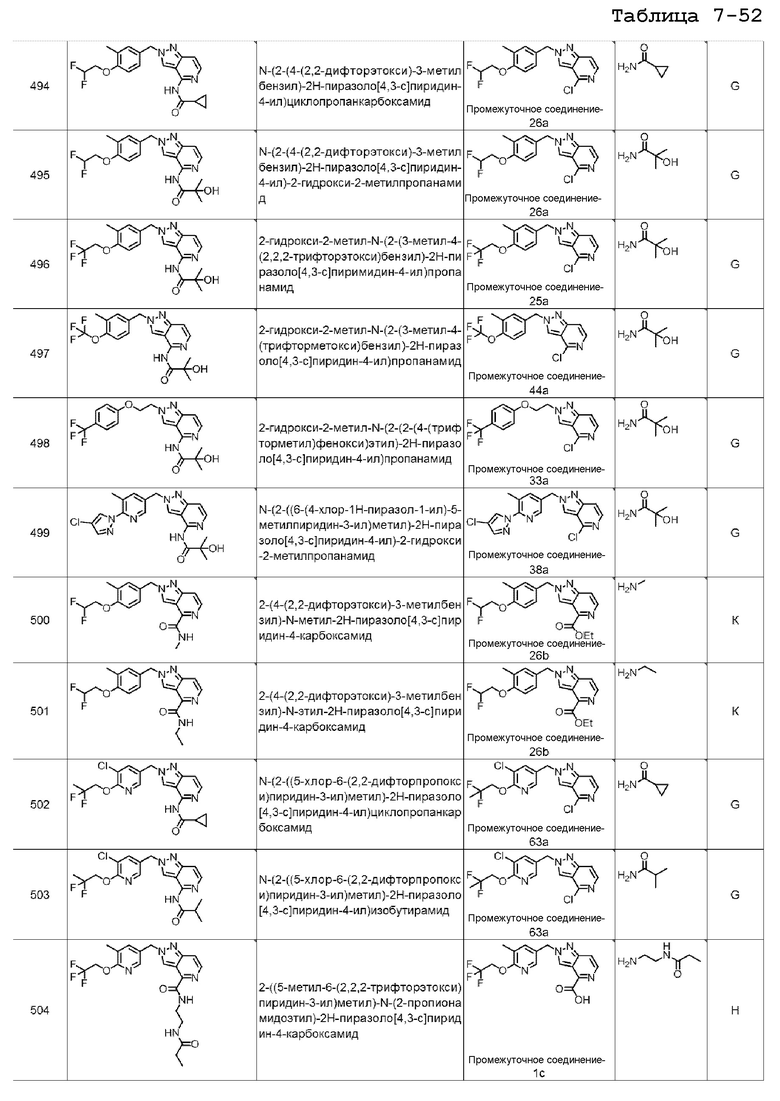
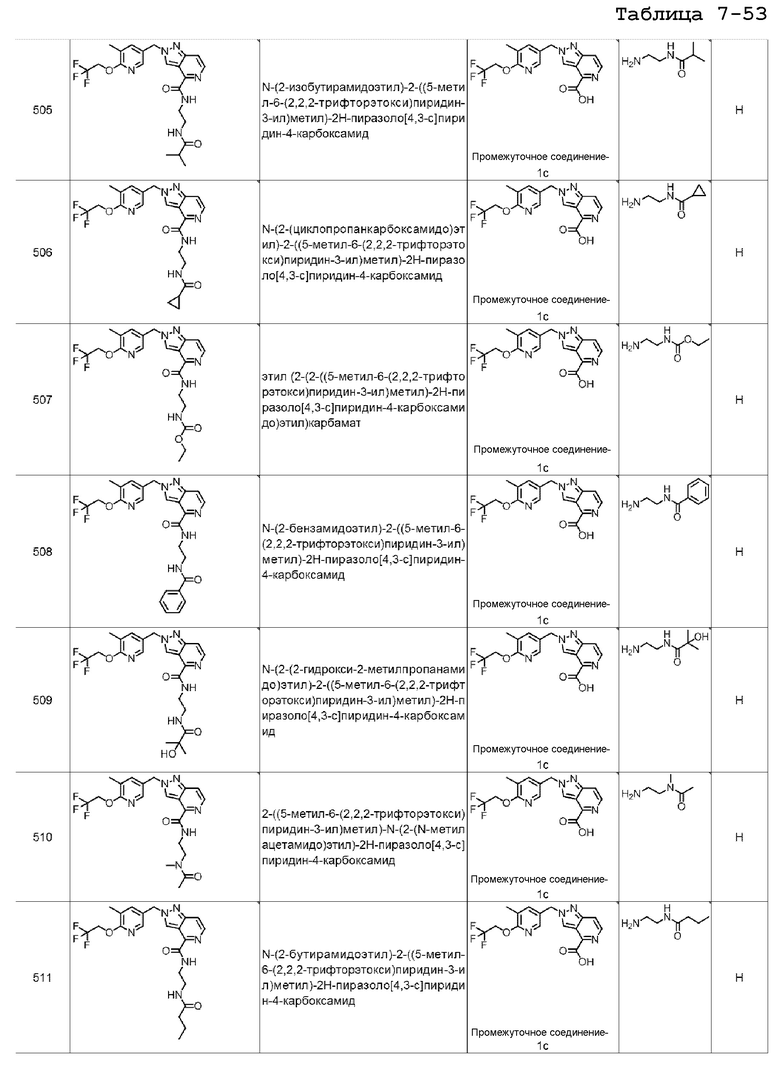
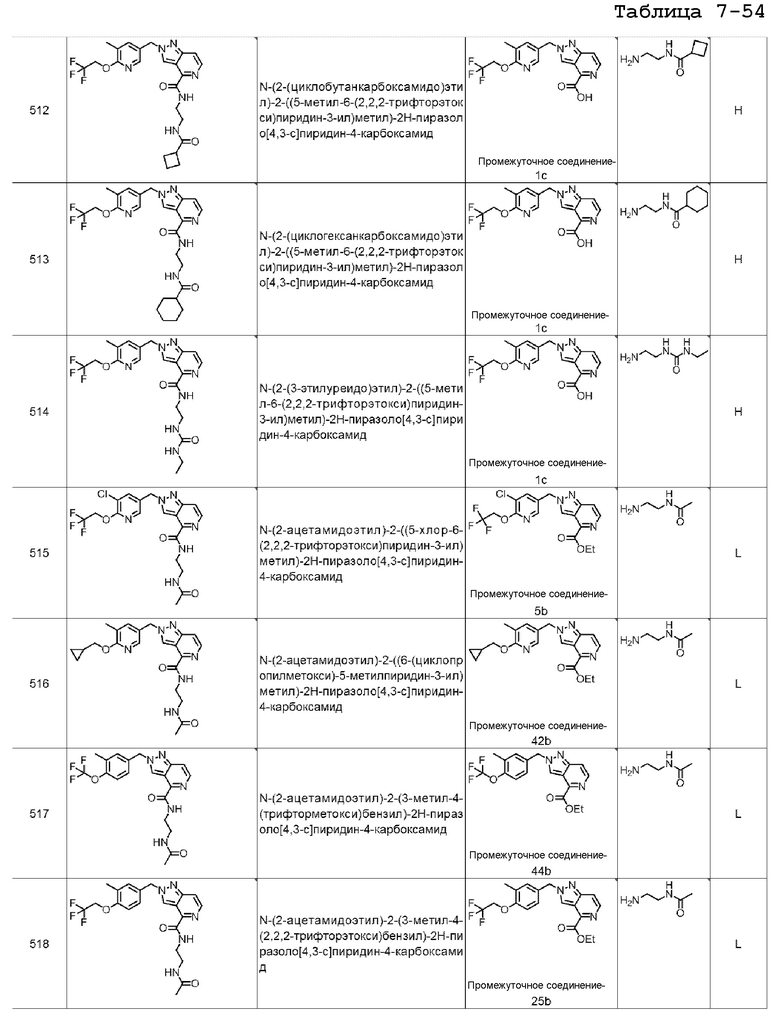
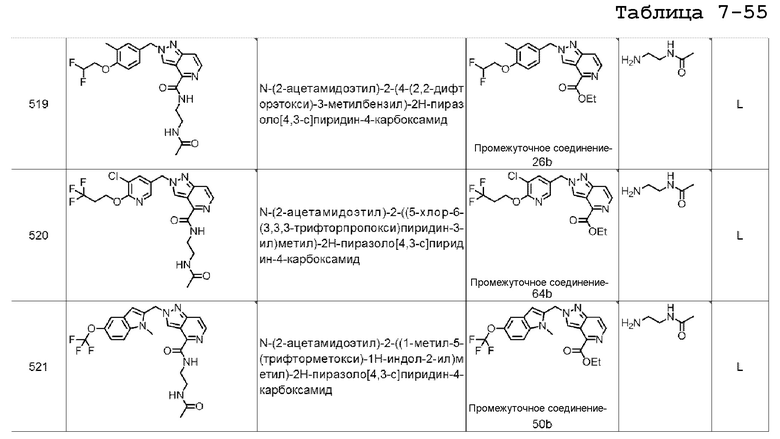
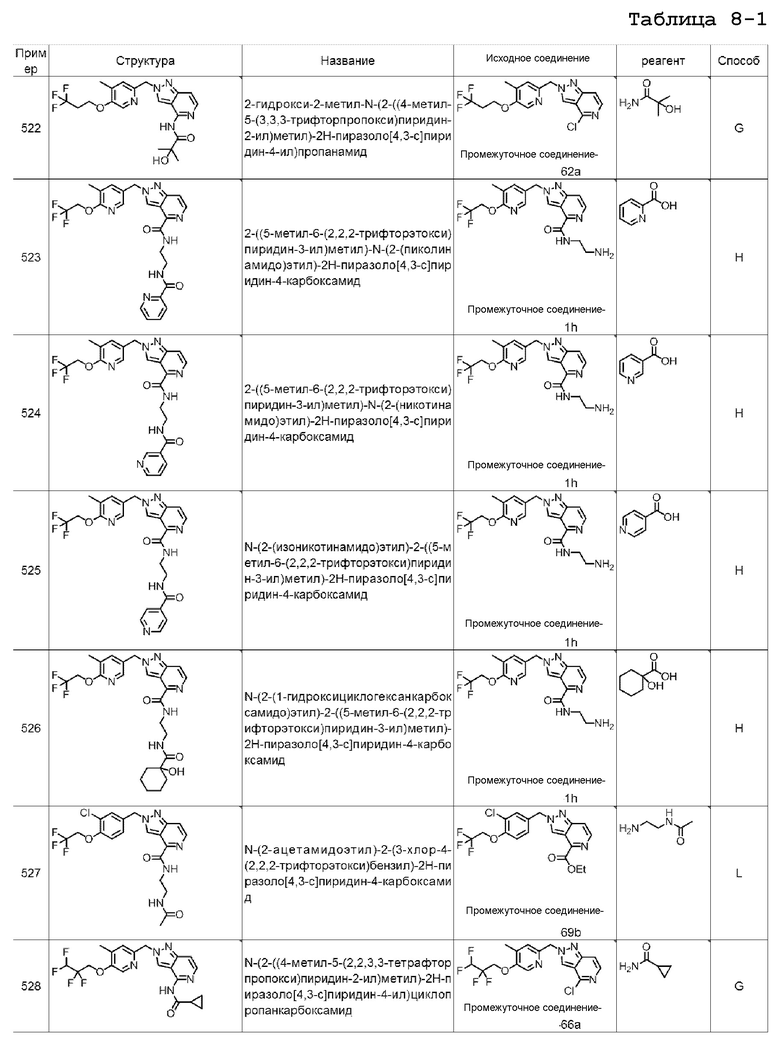
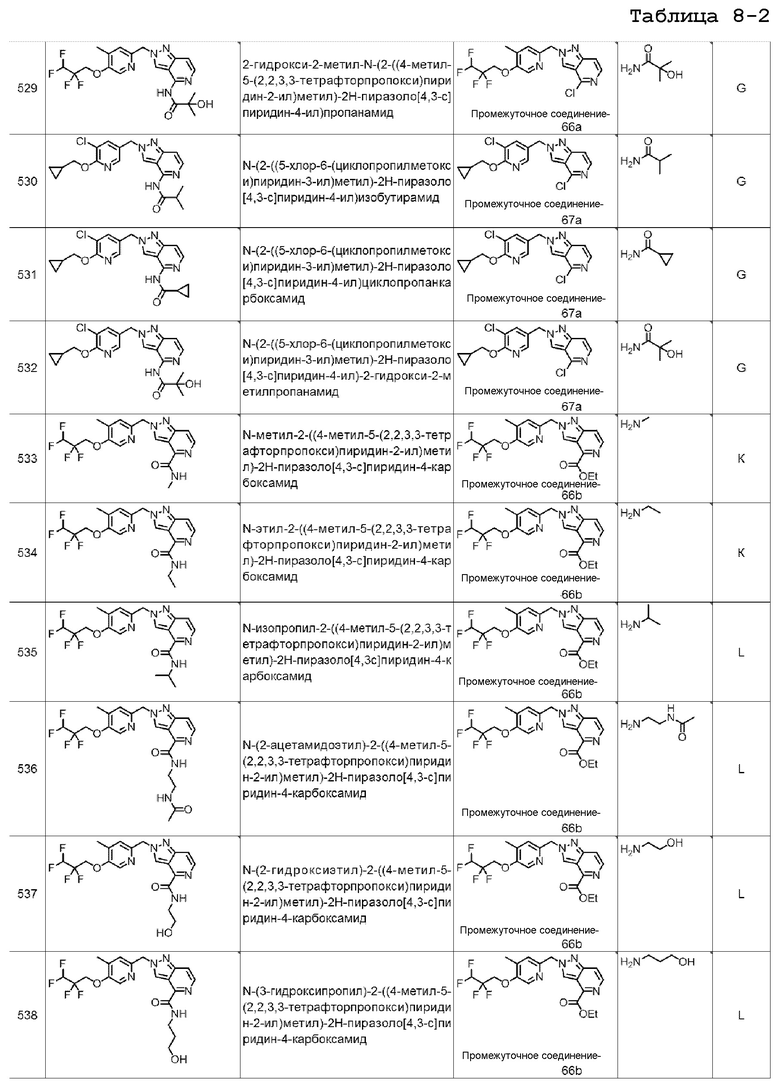
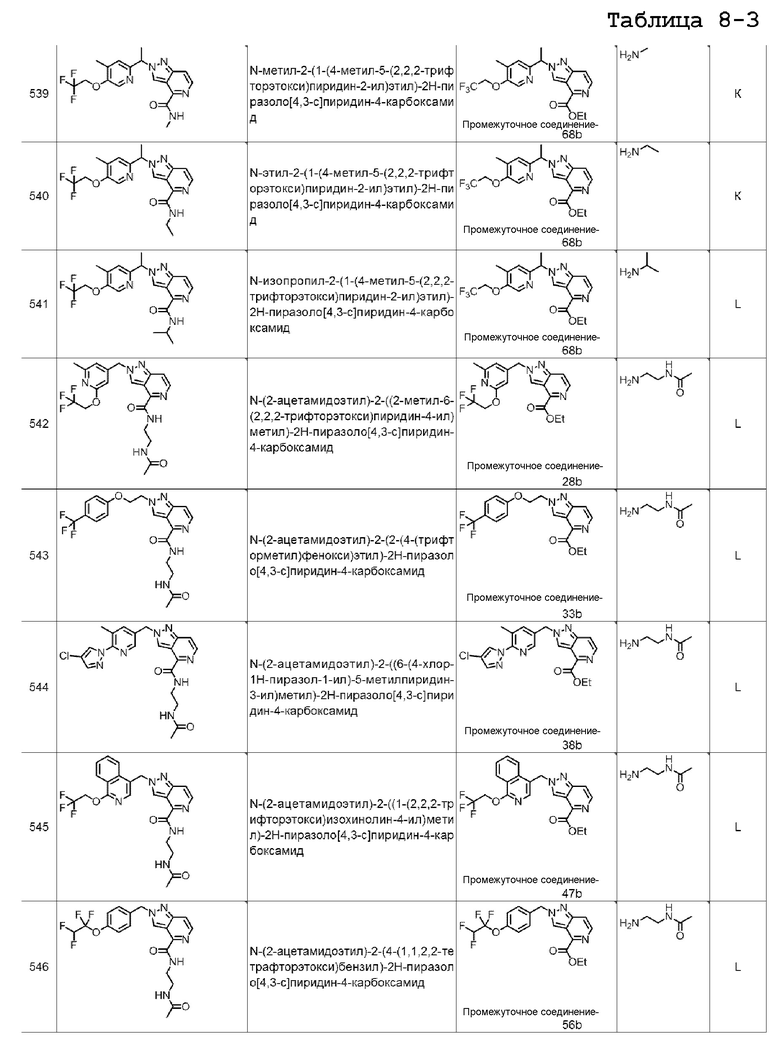
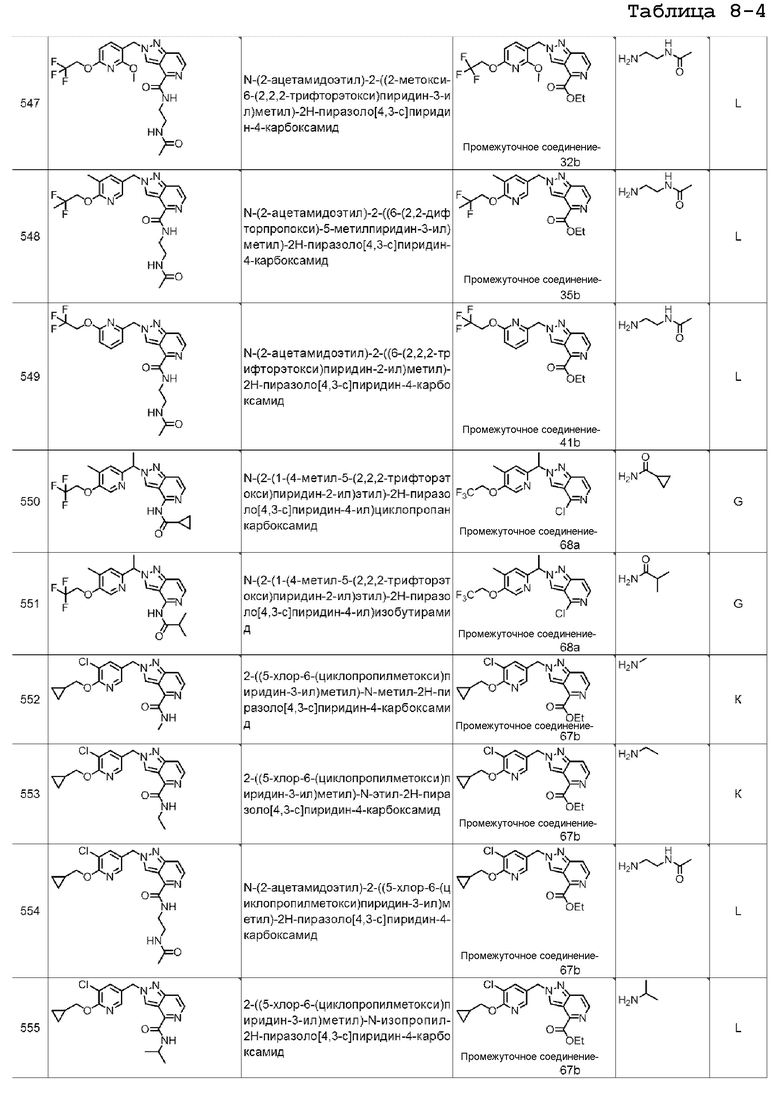
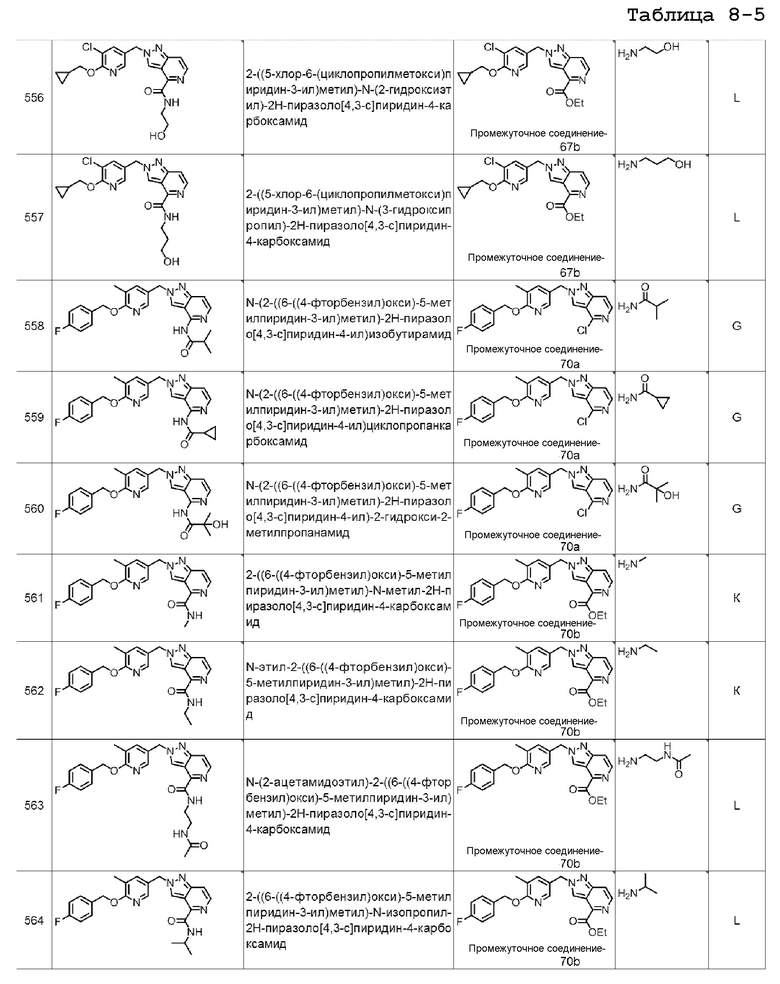
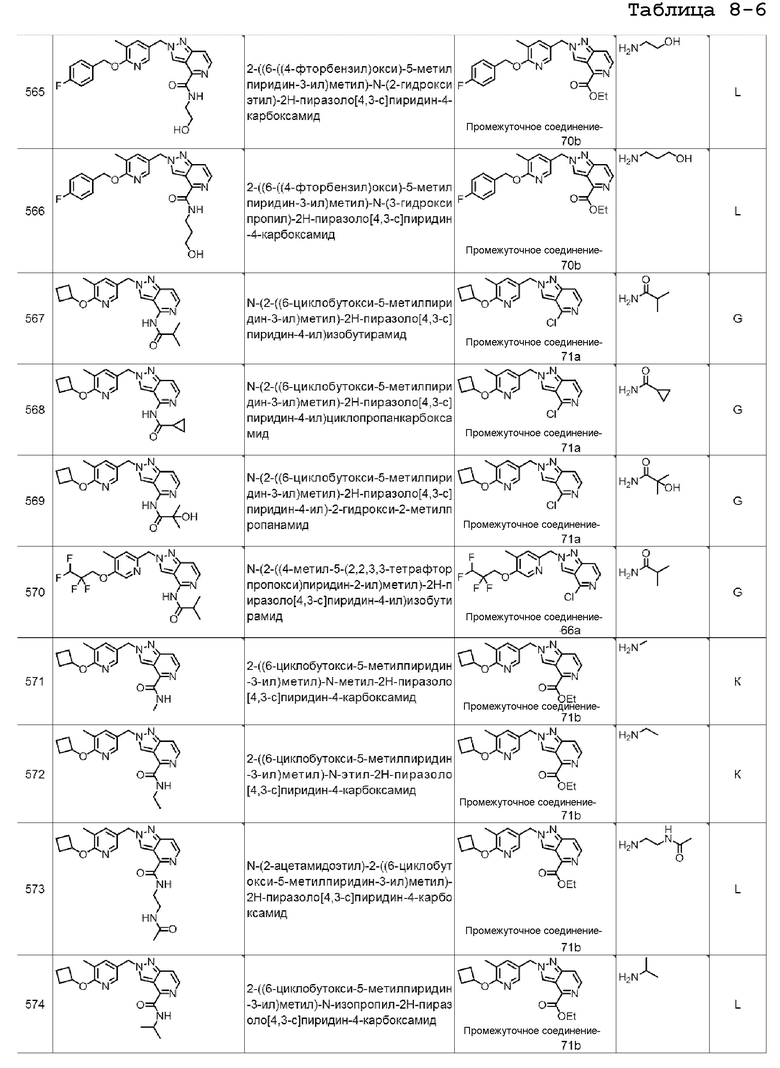
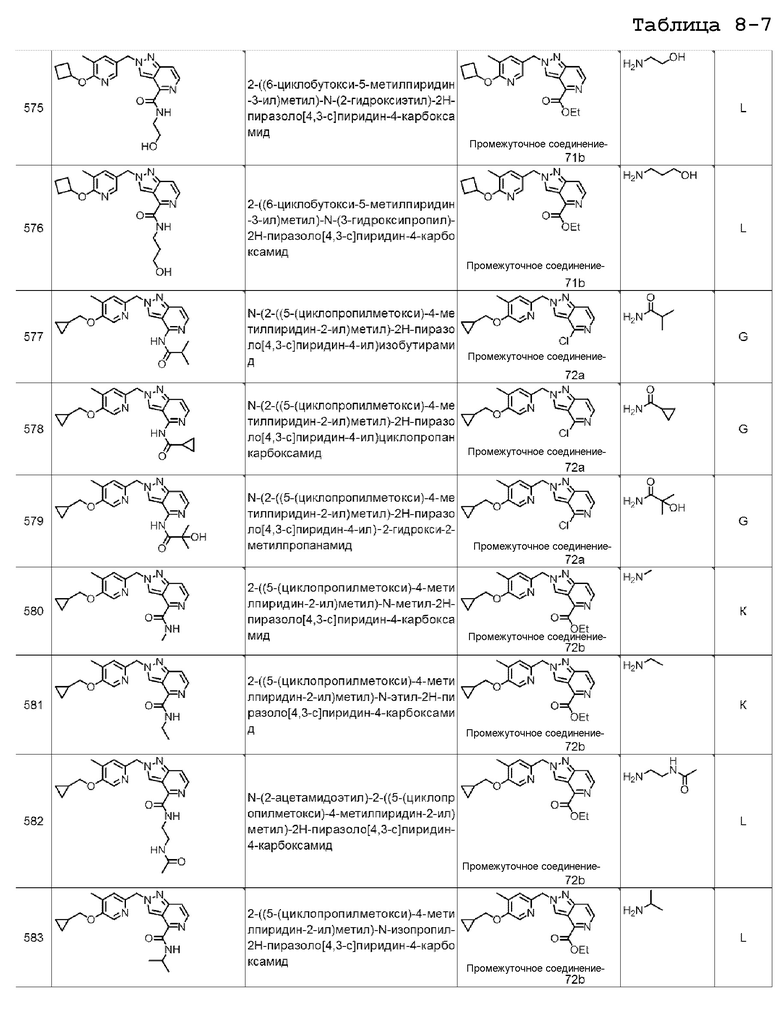
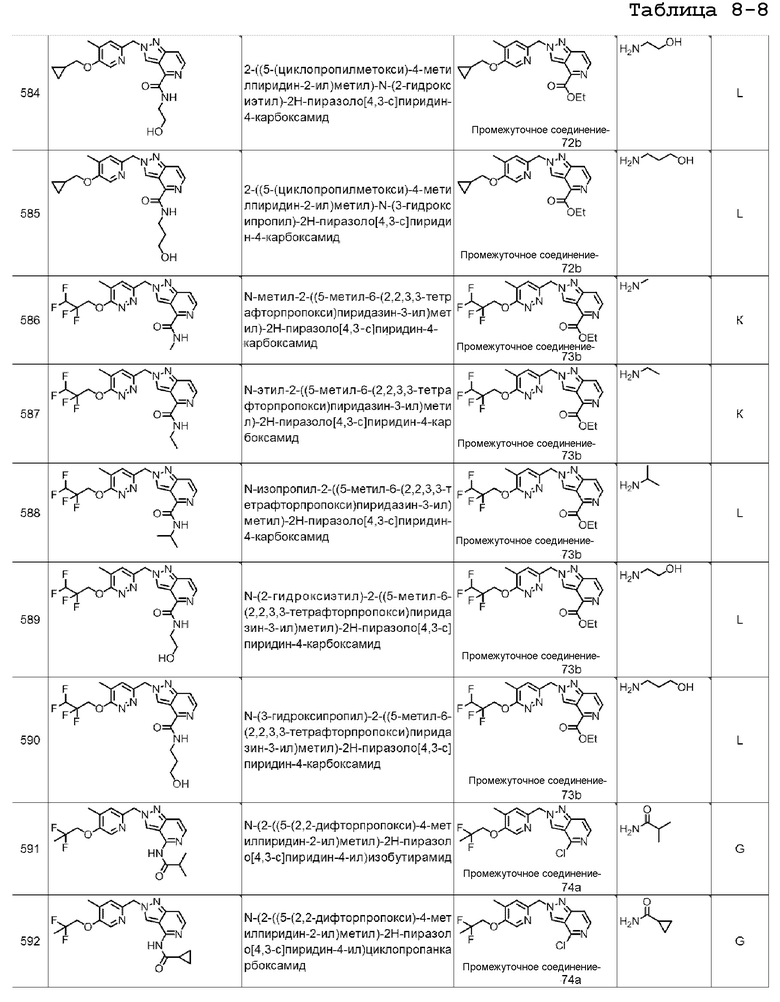
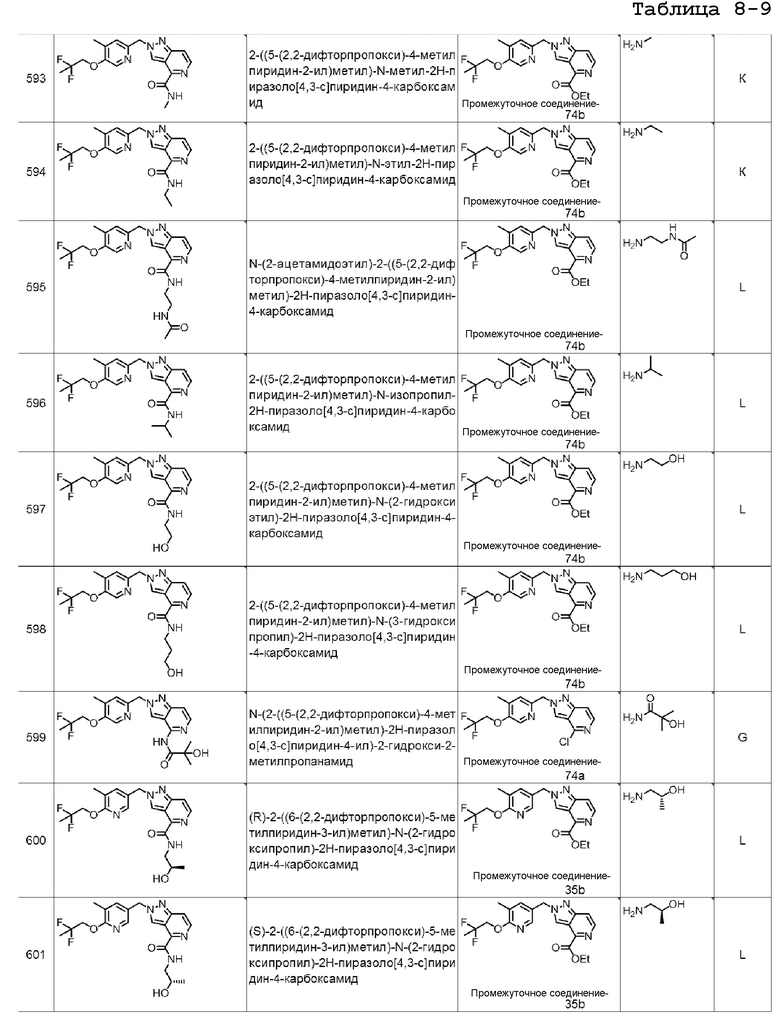
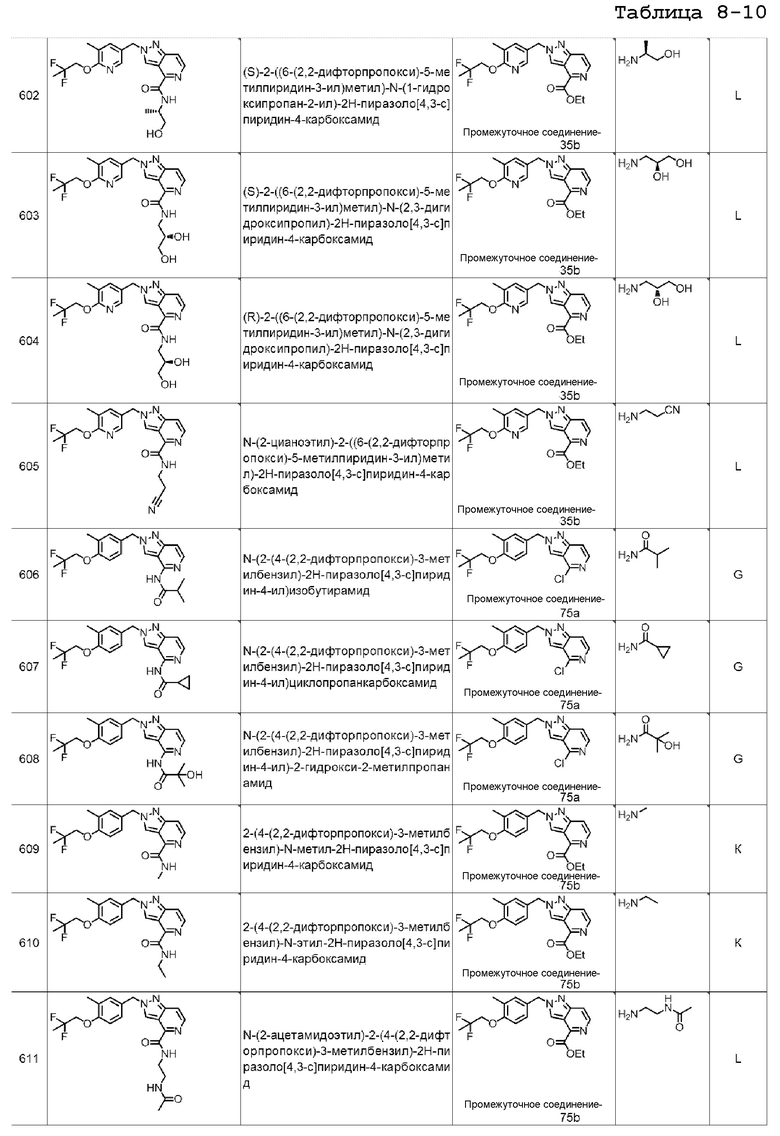
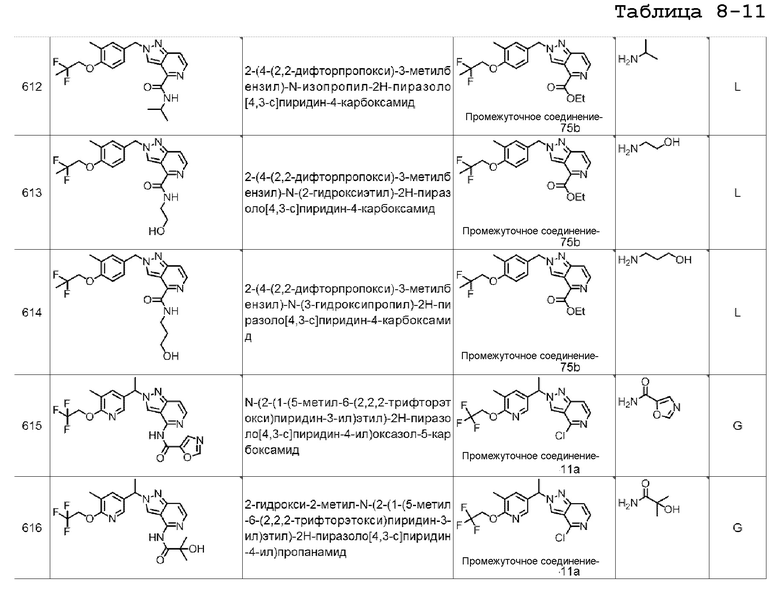
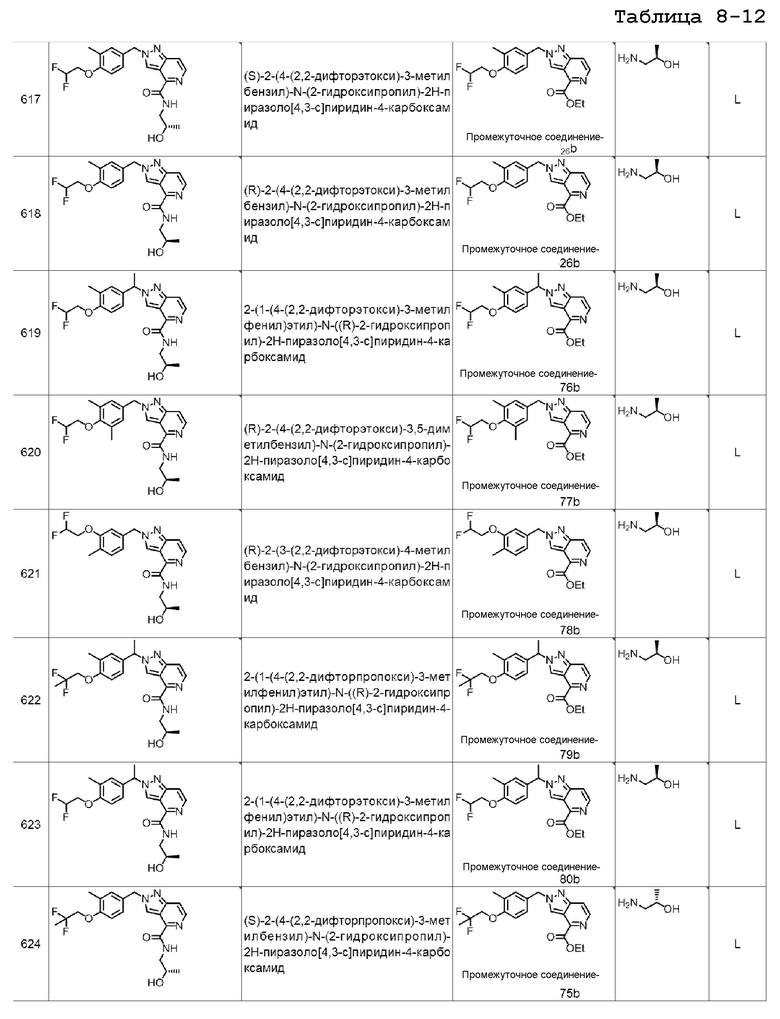
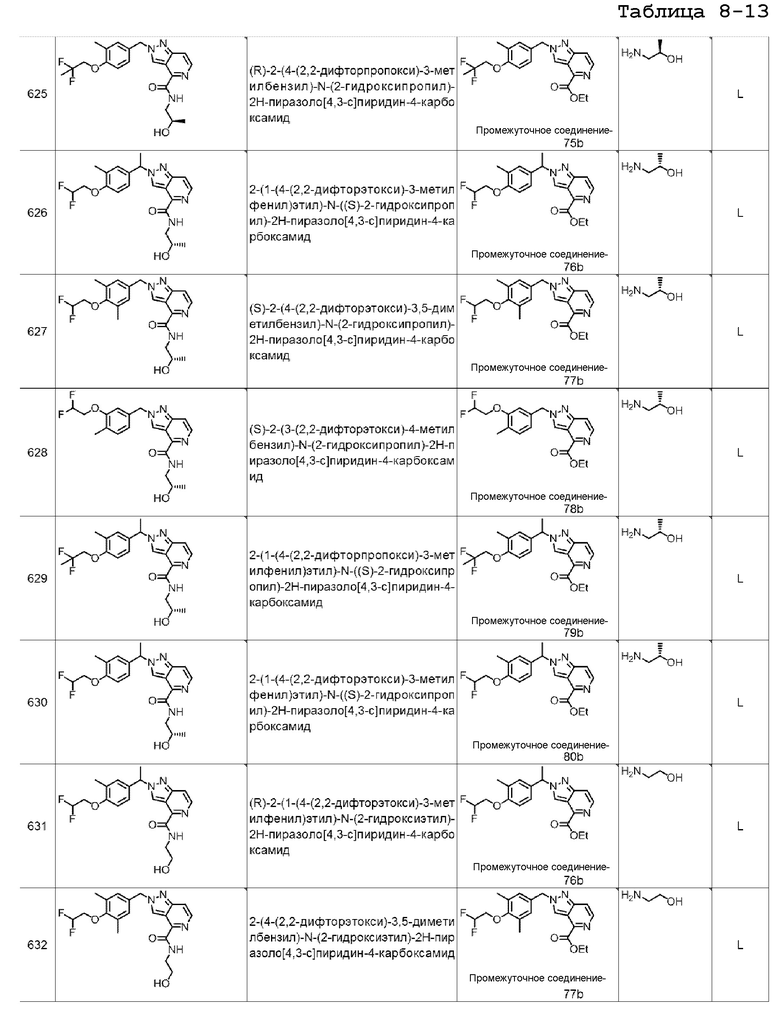
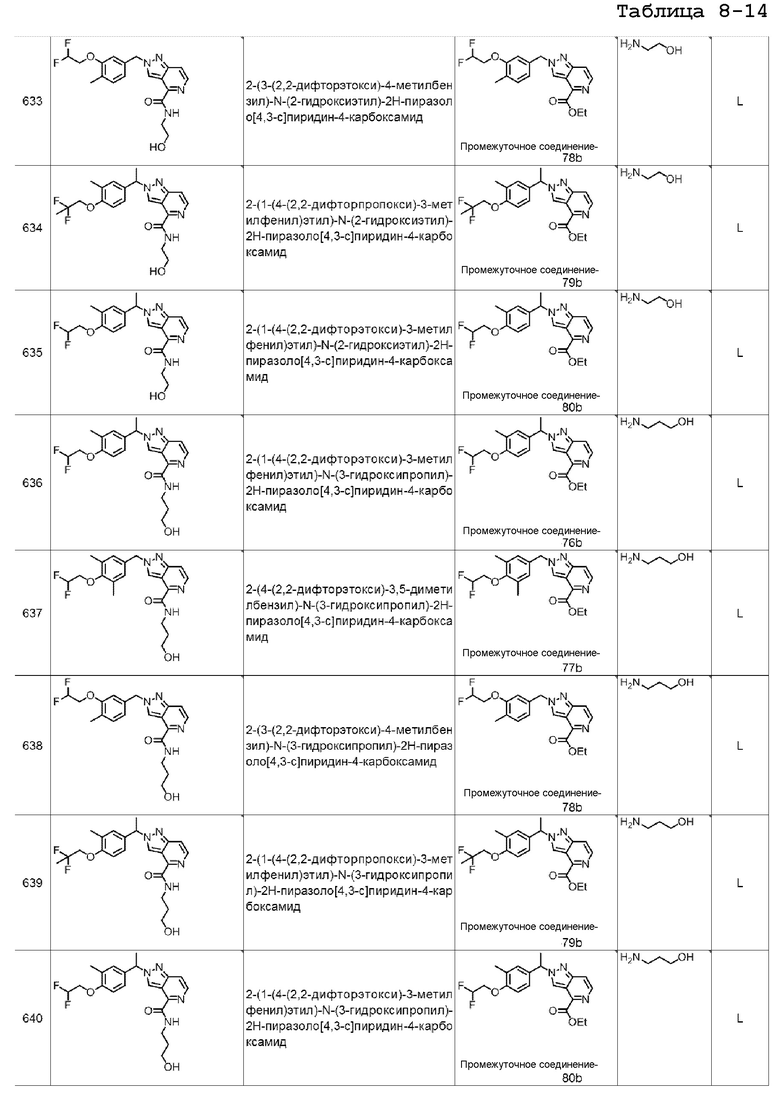
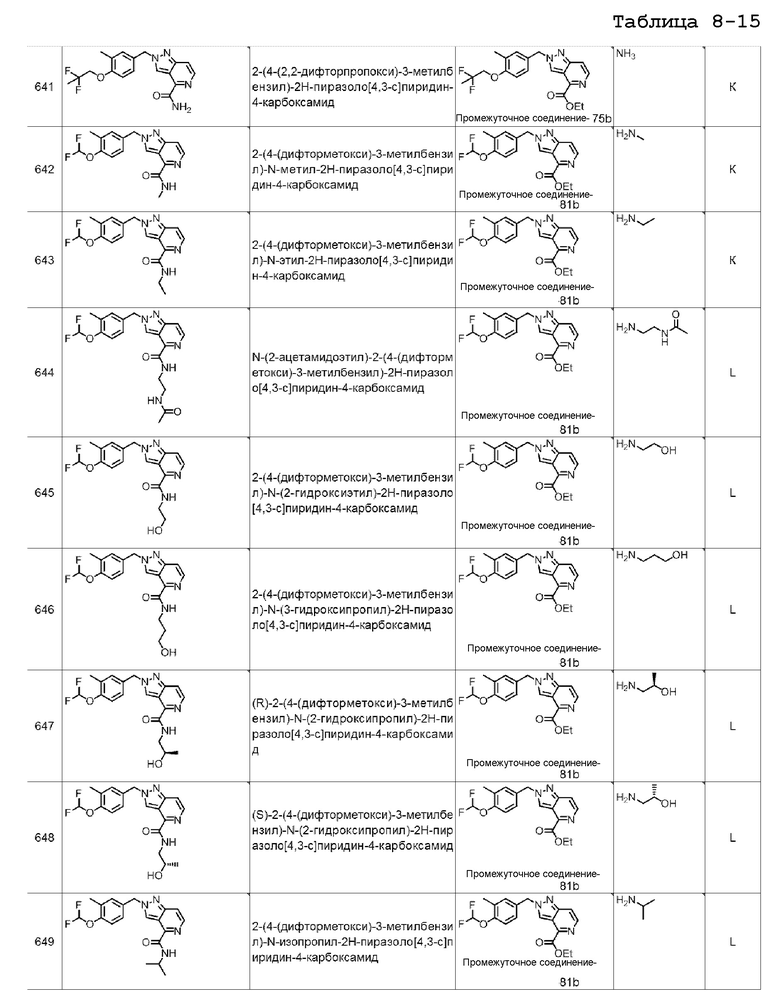
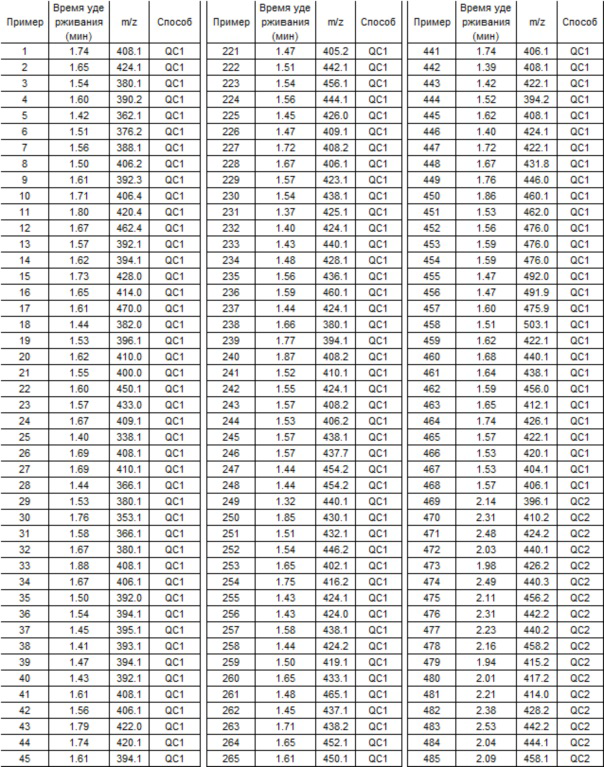
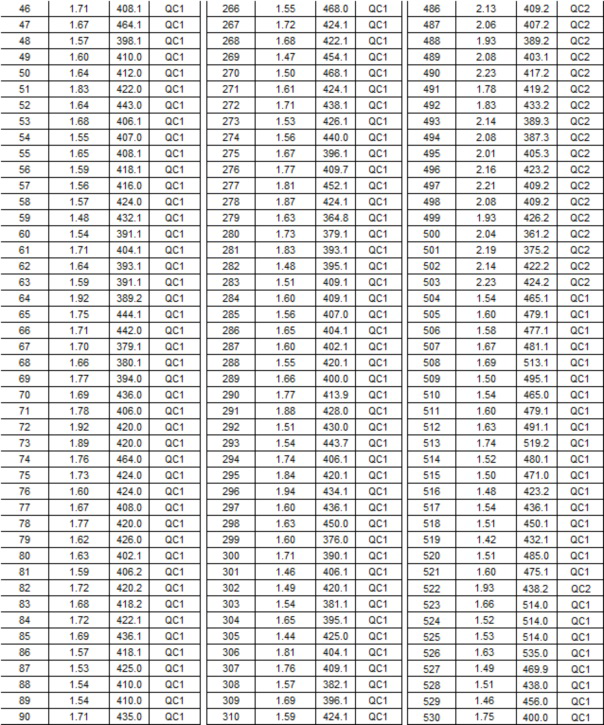
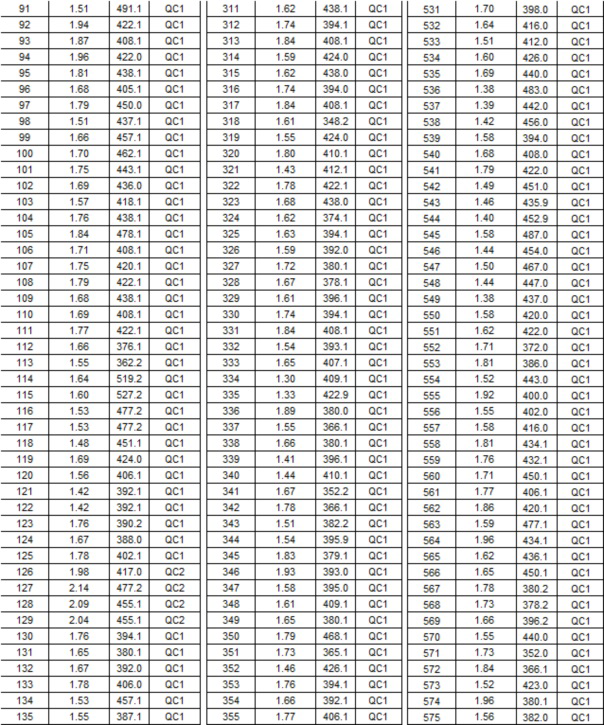
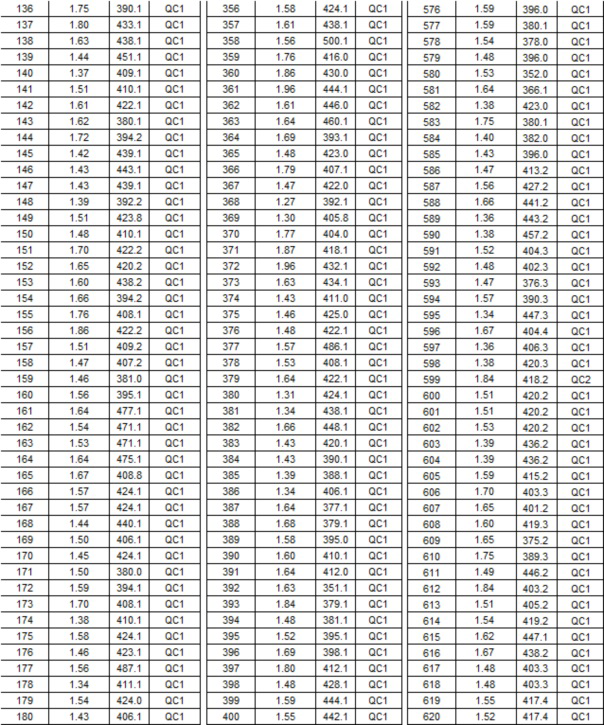
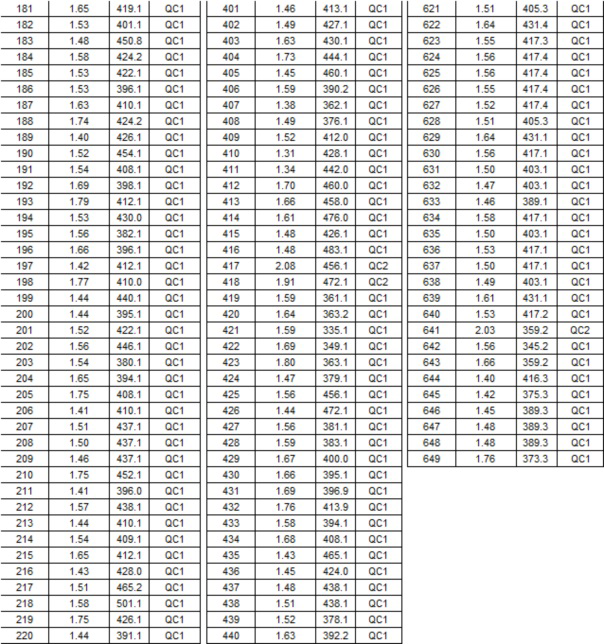
Фармакологические анализы
Активность потенциал-зависимых натриевых каналов человека in vitro
Ингибирующие активности соединений в отношении потенциал-зависимых натриевых каналов определяют способами, хорошо известными в данной области.
Способность производных пиразолопиридина формулы (I) ингибировать каналы NaV1.3, NaV1.7 и NaV1.5 измеряют посредством анализа резонансного переноса энергии флуоресценции (FRET) и электрофизиологического анализа, описанных ниже.
Анализ FRET
Этот скрининг используют для того, чтобы определять эффекты соединений в отношении каналов NaV1.3 человека, NaV1.7 человека и NaV1.5 человека, используя систему стимуляции электрическим полем (EFS) в формате 96-луночного планшета на платформе FDSS (Hamamatsu Photonics). Мониторинг изменения мембранного потенциала осуществляют с использованием пары FRET красителей, оксонол (DiSBAC2(3)) и кумарин (CC2-DMPE).
Поддержание клеток:
Все клетки HEK293, экспрессирующие каналы NaV1.3 человека, и клетки HEK293, экспрессирующие каналы NaV1.5 человека, растили в колбах T225, в 5% CO2 увлажненном инкубаторе приблизительно до смыкания 80%. Композиция сред состоит из модифицированной Дульбекко среды Игла (высокая глюкоза), 10% FCS, пенициллина 100 ед./мл, стрептомицина 100 мкг/мл и генетицина 500 мкг/мл.
Клетки CHO, экспрессирующие каналы NaV1.7 человека, растят в колбах T225, в 5% CO2 увлажненном инкубаторе приблизительно до смыкания 80%. Композиция сред состоит из HAM/F12 с GlutaMAX I, 10% FCS, пенициллина 100 ед./мл и гигромицина 100 мкг/мл.
Протокол:
- Высеять все клеточные линии (1×105 клеток/лунка) в покрытые поли-D-лизином 96-луночные планшеты перед экспериментом.
- Инкубировать при 37°C в 5% CO2 в течение 24 часов.
- Промыть каждую лунку буфером для анализа (140 мМ NaCl, 4,5 мМ KCl, 10 мМ D-глюкоза, 2 мМ CaCl2, 1 мМ MgCl2, 10 мМ HEPES, pH 7,4, скорректированный с использованием NaOH) два раза.
- Добавить 1-ый загружающий раствор, который содержит 10 мкМ CC2-DMPE и 0,06% Pluronic F-127 в буфере для анализа.
- Инкубировать планшет при комнатной температуре в темноте в течение 1 часа.
- Удалить 1-ый загружающий раствор и добавить 2-ой загружающий раствор, который содержит 15 мкМ DiSBAC2(3), 0,555 мМ VABSC-1 и 0,004% Pluronic F-127 в буфере для анализа.
- Поместить планшет в темноту при комнатной температуре на 25 минут.
- Добавить растворы соединений в планшет для анализа.
- Установить планшет для анализа в FDSS и поместить EFS устройство на планшет.
- Измерить EFS-индуцированный флуоресцентный ответ с помощью FDSS.
Данные анализируют и представляют в виде нормализованных отношений интенсивностей, измеряемых при 440 нм. Процесс вычисления этих соотношений осуществляют следующим образом:
FIR = отношение интегрированной флуоресценции = интеграл отношения, нормализованного к базовому уровню (перед EFS)
Этот анализ осуществляют с использованием специальной компьютерной программы, разработанной для генерируемых FDSS данных. Значения отношения флуоресценции наносят на график с использованием XLfit для того, чтобы определять значение IC50 для каждого соединения.
Все тестированные соединения демонстрируют IC50 меньше чем приблизительно 3 мкМ в отношении NaV1.3 и/или NaV1.7 в анализах выше. Предпочтительные соединения демонстрируют IC50 меньше чем приблизительно 1 мкМ в отношении NaV1.7 и/или NaV1.3 в анализах выше.
Соединениями с IC50 в отношении NaV1.7<1 мкМ и/или NaV1.3<1 мкМ являются:
Примеры 1, 2, 3, 4, 6, 7, 9, 10, 11, 14, 15, 16, 18, 19, 20, 21, 22, 25, 27, 32, 33, 34, 38, 41, 42, 43, 44, 45, 46, 47, 51, 52, 61, 65, 69, 71, 75, 80, 82, 85, 88, 89, 92, 93, 96, 98, 103, 104, 106, 107, 108, 109, 112, 113, 119, 120, 125, 126, 128, 129, 134, 139, 141, 145, 147, 148, 149, 151, 153, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 187, 190, 191, 194, 195, 196, 197, 199, 201, 202, 203, 204, 207, 209, 212, 214, 215, 216, 217, 218, 219, 220, 221, 222, 223, 224, 227, 228, 229, 230, 231, 232, 238, 239, 240, 241, 242, 245, 246, 247, 248, 251, 252, 254, 255, 256, 257, 258, 259, 260, 261, 262, 264, 265, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 280, 281, 282, 283, 284, 285, 286, 287, 288, 289, 290, 292, 293, 294, 295, 296, 297, 298, 299, 300, 301, 302, 304, 306, 307, 308, 309, 310, 311, 312, 313, 314, 315, 316, 317, 320, 321, 322, 326, 327, 328, 329, 330, 331, 332, 333, 335, 336, 337, 338, 341, 342, 343, 344, 345, 347, 348, 349, 350, 351, 352, 355, 356, 357, 358, 359, 360, 362, 363, 364, 367, 369, 370, 371, 372, 373, 374, 375, 376, 377, 378, 380, 382, 383, 384, 385, 386, 387, 391, 392, 394, 395, 399, 400, 401, 402, 403, 406, 407, 408, 409, 412, 413, 414, 415, 416, 417, 418, 420, 422, 423, 424, 425, 426, 427, 428, 429, 430, 431, 432, 433, 434, 435, 436, 437, 438, 439, 440, 441, 442, 443, 444, 445, 446, 447, 448, 449, 450, 451, 452, 453, 454, 455, 456, 457, 458, 459, 460, 461, 462, 463, 464, 465, 466, 467, 468, 469, 470, 471, 472, 473, 474, 475, 476, 477, 478, 479, 480, 481, 482, 483, 484, 485, 486, 487, 489, 492, 493, 494, 495, 496, 497, 500, 501, 502, 503, 504, 506, 507, 508, 512, 513, 515, 516, 517, 518, 519, 521, 522, 523, 524, 525, 527, 528, 529, 530, 531, 532, 533, 534, 535, 537, 538, 540, 545, 548, 549, 551, 552, 553, 554, 555, 556, 557, 558, 559, 560, 561, 562, 563, 564, 565, 566, 567, 568, 569, 570, 571, 572, 573, 574, 575, 576, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 596, 597, 598, 599, 600, 602, 603, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 616, 617, 618, 619, 620, 622, 624, 625, 626, 627, 629, 631, 632, 633, 634, 636, 637, 639, 640, 641, 642, 643, 645, 646 и 649.
Что касается всех тестированных соединений, отношение активностей для NaV1.5 против NaV1.3 или NaV1.7 составляет больше чем три. Например, активности из примера 2 в отношении NaV1.5 и NaV1.7 составляют больше чем 30 мкМ и 0,38 мкМ, соответственно.
Электрофизиологический анализ для Nav
Запись фиксации потенциала целой клетки используют для того, чтобы оценивать эффективность или избирательность блокатора Na-каналов в отношении клеток HEK293, экспрессирующих NaV1.3 человека (hSCN3A), или клеток CHO, экспрессирующих NaV1.7 человека (hSCN9A). Клетки HEK293, экспрессирующие NaV1.3 человека, растят в средах для выращивания, которые содержат: фосфатно-солевой буфер Дульбекко (DMEM), 10% термоинактивированную эмбриональную телячью сыворотку (FBS) (Hyclone Laboratories Inc), пенициллин 100 мкг/мл/стрептомицин 100 ед./мл, ЗеоцинTM 150 мкг/мл и генетицин 3 мкг/мл. Клетки CHO, экспрессирующие NaV1.7 человека, растят в средах для выращивания, которые содержат: HAM/F-12, 9% термоинактивированную FBS (Hyclone Laboratories Inc) и 100 мкг/мл пенициллин/100 ед./мл стрептомицин и гигромицин 100 мкг/мл.
Клетки, экспрессирующие Na-каналы, диссоциируют с помощью 0,05% трипсин-ЭДТА и затем высевают на покровное стекло на 24-48 ч.
Стеклянные пипетки вытягивают до диаметра кончика от 1 до 2 микрометров на вытягивателе пипеток. Пипетки заполняют внутриклеточным раствором и вдоль ее длины вставляют хлорированный серебряный провод, который затем соединяют с головкой усилителя с фиксацией уровня напряжения (Axon Instruments или HEKA elektronik). Внеклеточный регистрирующий раствор состоит из (мМ): 140 NaCl, 5 KCl, 2 CaCl2, 1 MgCl2, 10 HEPES и 10 глюкозы, pH 7,4, скорректированный с использованием NaOH. Внутренний раствор состоит из (мМ): 120 CsF, 15 NaCl, 10 EGTA и 10 HEPES, pH 7,2, скорректированный с использованием CsOH. После введения кончика пипетки в ванночку, отмечают сопротивление пипетки (приемлемый диапазон находится между 1-3 МОм). Контактную разность потенциалов между растворами пипетки и ванночки обнуляют на усилителе. После установления полноклеточной конфигурации, раствору пипетки позволяют приходить в равновесие внутри клетки приблизительно в течение 10 минут перед началом регистрации. Для токов выполняют фильтрацию низких частот между 2-5 кГц и цифровую дискретизацию на 10 кГц.
Нормализованную кривую инактивации в установившемся состоянии строят, используя 2 сек (для наполнителя) или 60 сек для кондиционирующего импульса (для лекарственных средств) для различных потенциалов, за которыми незамедлительно следует тестовый импульс до -10 мВ. Строят графики пиковых токов в виде доли максимального тока при кондиционирующих потенциалах в диапазоне от -120 мВ до -40 мВ для NaV1.3 и от -130 мВ до -60 мВ для NaV1.7. Значения V1/2 или k оценивают по больцмановской аппроксимации. Аффинность лекарственных средств к состоянию покоя Na-каналов (Kresting или Kr) оценивают посредством 30 мсек тестового импульса от отрицательного исходного -120 или -130 мВ, где фактически все каналы находятся в состоянии покоя. Значение Kr вычисляют с помощью стандартной модели связывания 1:1:
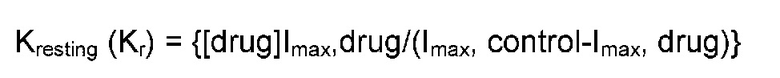 ,
,
где Kresting (=Kr) представляет собой константу диссоциации для состояния покоя и [drug] представляет собой концентрацию соединения. Imax,control и Imax,drug представляют собой пиковые токи в отсутствии и в присутствии соединения, соответственно.
Аффинность лекарственного средства инактивированному состоянию Na каналов (Kinact или Ki) оценивают по сдвигу кривой доступности соединению. Взаимодействие соединения с каналом в инактивированном состоянии оценивают с помощью следующего уравнения:
 ,
,
где kinact (=ki) представляет собой константу диссоциации в инактивтрованном состоянии.  представляет собой индуцированный соединением сдвиг напряжения на половину максимального напряжения кривой Больцмана, и k представляет собой коэффициент наклона в присутствии соединения.
представляет собой индуцированный соединением сдвиг напряжения на половину максимального напряжения кривой Больцмана, и k представляет собой коэффициент наклона в присутствии соединения.
Все тестированные соединения по изобретению демонстрируют высокие активности в этой модели. Например, активности (Ki) из примера 2 в отношении NaV1.3 и NaV1.7 составляют 0,57 мкМ и 0,34 мкМ, соответственно.
Анализ in vivo
Индуцированная хроническим констрикционным повреждением (CCI) статическая аллодиния у крыс
Самцов крыс Sprague-Dawley в возрасте 7 недель приобретают в Charles River Japan Inc. и содержат группами по две на клетку в 12-часовом цикле свет/темнота (свет включают в 07:00) с доступом к пище и воде ad libitum. Индуцированную CCI статическую аллодинию оценивают посредством теста шерсти по фон Фрею (VFH). Хирургическое вмешательство осуществляют согласно способу Bennett GJ and Xie YK (Pain 1988, 33: 87-107). Животным выполняют анестезию с использованием интраперитонеальной инъекции пентобарбитала натрия. Левый общий седалищный нерв обнажают на уровне середины бедра, освобождают от прилегающей ткани, и туго накладывают четыре лигатуры вокруг него, используя шелковую нить 4-0. На разрез накладывают швы, и крысам позволяют восстанавливаться в их клетках с мягкой подстилкой. Имитацию операции осуществляют аналогичным образом, за исключением наложения лигатуры на седалищный нерв. Животных индивидуально помещают в тестовую камеру из плексигласа на поднятой решетке для акклиматизации перед сутками тестирования. В послеоперационные сутки (POD) 14-28 осуществляют оценку с использованием серии калиброванных VFH (монофиламенты Семмеса-Винштейна) с усилием 0,4, 0,6, 1, 2, 4, 6, 8 и 15 г. VFH, начиная с усилия 2 г, применяют восходящим или нисходящим образом согласно модифицированному способу вверх-вниз по Диксону, который описан Chaplan SR et al. (J Neurosci Methods 1994, 53: 55-63). Каждую VFH подносят к подошвенной поверхности оперированной задней лапы с постоянным давлением, направленным вверх, пока не происходит сгибание в течение приблизительно 6 секунд. В отсутствии отдергивания лапы подносят более сильный стимул. В случае отдергивания лапы выбирают следующий более слабый стимул. После начального изменения от положительного к отрицательному, или наоборот, применяют еще 4 стимуляции. 6-оценочный паттерн из положительных и отрицательных реакций превращают в 50% порог отдергивания лапы (PWT) с использованием следующей формулы:
50% PWT (g) = (10[Xf+κδ])/10000,
где Xf представляет собой значение (в логарифмических единицах) конечной использованной VFH, κ представляет собой табличное значение для паттерна положительных/отрицательных реакций и δ представляет собой среднюю разность между стимулами в логарифмических единицах (здесь 0,224).
В случае, когда непрерывные положительные или отрицательные реакции наблюдают на всем протяжении до конца спектра стимулов, присваивают значения 0,25 и 15 г, соответственно. Животных, демонстрирующих статическую аллодинию (<4 г для 50% PWT) посредством CCI хирургического вмешательства, отбирают для оценки и рандомизируют, чтобы было приблизительно одинаковое среднее 50% PWT на протяжении всех групп. Соединения по изобретению или их наполнители вводят системно. Крыс знакомят с камерой в течение по меньшей мере 20 минут перед измерением. 50% PWT измеряют в подходящий момент после введения соединения. Статистический анализ осуществляют посредством критерия Стьюдента для одной выборки или однофакторного дисперсионного анализа (ANOVA) с апостериорным критерием Дуннетта в сравнении с группой наполнителя.
Все тестированные соединения по изобретению демонстрируют высокие активности в этой модели.
Индуцированная полным адъювантом Фрейнда (CFA) термическая гипералгезия у крыс
Самцов крыс Sprague-Dawley в возрасте 6 недель приобретают в Charles River Japan Inc. и содержат группами по две на клетку в 12-часовом цикле свет/темнота (свет включают в 07:00) с доступом к пище и воде ad libitum. CFA-индуцированную термическую гипералгезию оценивают с использованием аппарата для подошвенного теста (Ugo Basile), как описано Hargreaves K et al. (Pain 1988, 32: 77-88). Животных помещают в аппарат, состоящий из индивидуального тестового ящика на поднятом стеклянном столе, и позволяют аклиматизироваться в течение по меньшей мере 10 минут. После ознакомления передвижной источник лучистого тепла помещают под столом, и к подошвенной поверхности правой задней лапы применяют тепловую стимуляцию. Время ожидания до удаления своей задней лапы определяют как время ожидания отдергивания лапы (PWL) в секундах. Точку отсечения устанавливают на 30 сек для того, чтобы предотвращать повреждение тканей. CFA получают в концентрации Mycobacterium tuberculosis H37 RA от 2-3 мг/мл в жидком парафине. После дезинфекции 70% этанолом, крысам инъецируют внутрь подошвы 100 мкл CFA (200-300 мкг) в правую заднюю лапу. Через двое суток после инъекции CFA, PWL измеряют аналогичным образом, как указано выше. Животных, демонстрирующих снижение PWL (гипералгезия) посредством инъекции CFA, отбирают для оценки и рандомизируют, чтобы было приблизительно одинаковое среднее PWL на протяжении всех групп. Соединения по изобретению или их наполнители вводят системно. Крыс знакомят с аппаратом в течение по меньшей мере 10 минут перед каждым измерением. PWL измеряют в подходящий момент после введения соединения. Статистический анализ осуществляют посредством критерия Стьюдента для одной выборки или ANOVA с апостериорным критерием Дуннетта в сравнении с группой наполнителя.
Все тестированные соединения по изобретению демонстрируют высокие активности в этой модели.
CFA-индуцированная недостаточность весовой нагрузки у крыс
Самцов крыс Sprague-Dawley в возрасте 7 недель приобретают в Charles River Japan Inc. и содержат группами по две на клетку в 12-часовом цикле свет/темнота (свет включают в 07:00) с доступом к пище и воде ad libitum. CFA-индуцированную недостаточность весовой нагрузки (WB) оценивают с использованием устройства для тестирования неспособности (Linton Instrumentation). Животных знакомят с пластмассовым ящиком, который идет с устройством для тестирования неспособности, за сутки до инъекции CFA. В день инъекции CFA распределение веса каждой задней лапы измеряют 3 раза у каждой крысы с использованием устройства для тестирования, и разность распределения веса, вес на правой (с инъекцией) лапе минус вес на левой (без инъекции) лапе, определяют как значение недостаточности WB в г. Длительность каждого измерения корректируют до 3 секунд. CFA получают в концентрации Mycobacterium tuberculosis H37 RA от 2-3 мг/мл в жидком парафине. После дезинфекции 70% этанолом, крысам инъецируют внутрь подошвы 100 мкл CFA (200-300 мкг) в правую заднюю лапу. Через двое суток после инъекции CFA распределение веса каждой задней лапы измеряют и вычисляют значение недостаточности WB аналогичным образом, как указано выше. Животных, демонстрирующих снижение недостаточности WB (>30%) посредством инъекции CFA, отбирают для оценки и рандомизируют, чтобы было приблизительно одинаково на протяжении всех групп. Соединения по изобретению или их наполнители вводят системно. Распределение веса каждой задней лапы измеряют в подходящий момент после введения соединения, и значение недостаточности WB вычисляют, как объяснено ранее. Статистический анализ осуществляют посредством критерия Стьюдента для одной выборки или ANOVA с апостериорным критерием Дуннетта в сравнении с группой наполнителя.
Все тестированные соединения по изобретению демонстрируют высокие активности в этой модели.
Индуцированная рассечением лапы статическая аллодиния у крыс
Самцов крыс Sprague-Dawley в возрасте 7 недель приобретают в Charles River Japan Inc. и содержат группами по две на клетку в 12-часовом цикле свет/темнота (свет включают в 07:00) с доступом к пище и воде ad libitum. Индуцированную рассечением лапы статическую аллодинию оценивают с помощью VFH теста. Хирургическое вмешательство осуществляют согласно процедуре, описанной Brennan et al. (Pain 1996, 64: 493-501). Животным изначально делают анестезию смесью от 3 до 4% изофлурана/O2 в анестетической камере и поддерживают с использованием от 2 до 3%, которые доставляют через носовой конус. Подошвенную поверхность правой задней лапы стерилизуют 7,5% раствором повидон-йода. Выполняют 1-см продольное рассечение лезвием номер 11, через кожу и фасцию подошвенной стороны лапы, начиная с 0,5 см от проксимального края пятки и продолжая в направлении пальцев. Подошвенную мышцу поднимают, используя щипцы, и отводят. Место крепления мышцы и вставку оставляют интактными. После остановки кровотечения мягким надавливанием, кожу сближают двумя швами из нейлона 5-0. Место раны покрывают мазью террамицинTM, и крысам позволяют восстанавливаться в своих клетках с мягкой подстилкой. Животных индивидуально помещают в тестовую камеру из плексигласа на поднятую решетку для акклиматизации в течение 1 часа перед сутками хирургического вмешательства. На POD1 осуществляют оценку с использованием серии калиброванных VFH (0,008, 0,02, 0,04, 0,07, 0,16, 0,4, 0,6, 1, 1,4, 2, 4, 6, 8, 10, 15 и 26 г). Начиная с усилия 0,16 г, восходящим или нисходящим образом, каждую VFH подносят к проксимальному концу раны рядом с латеральной частью пятки при постоянном направленном вверх давлении, пока не происходит сгибание в течение приблизительно 6 секунд. В отсутствии отдергивания лапы (отрицательная реакция), подносят более сильный стимул. В случае отдергивания лапы (положительная реакция), выбирают следующий более слабый стимул. Наименьшее количество усилия, требуемое для того, чтобы вызвать две положительные реакции, определяют как PWT в г. В случае, когда непрерывные положительные или отрицательные реакции наблюдают на всем протяжении до конца спектра стимулов, присваивают значения 0,008 и 26 г, соответственно. Животных, демонстрирующих PWT с помощью хирургического вмешательства для рассечения <1,4 г, отбирают для оценки и рандомизируют, чтобы было приблизительно одинаковое среднее PWT на протяжении всех групп. Соединения по изобретению или их наполнители вводят системно. Крыс знакомят с камерой в течение по меньшей мере 20 минут перед измерением. PWT измеряют в подходящий момент после введения соединения. Статистический анализ осуществляют с помощью U-критерия Манна-Уитни или Краскела-Уоллиса с апостериорным критерием Дуннетта в сравнении с группой наполнителя.
Все тестированные соединения по изобретению демонстрируют высокие активности в этой модели.
Индуцированная паклитакселом статическая аллодиния у крыс
Самцов крыс Sprague-Dawley в возрасте 7 недель приобретают в Charles River Japan Inc. и содержат группами по две на клетку в 12-часовом цикле свет/темнота (свет включают в 07:00) с доступом к пище и воде ad libitum. Индуцированную паклитакселом статическую аллодинию оценивают с помощью VFH теста. Обработку паклитакселом осуществляют согласно способу Polomano RC et al. (Pain 2001, 94: 293-304). Паклитаксел (2 мг) инъецируют интраперитонеально в четверо чередующихся суток (сутки 1, 3, 5 и 7) в объеме 1 мл/кг. Накопленная доза составляет 8 мг/кг. В группе симуляции наполнителем (смесь 16,7% Cremophor EL и 16,7% этанола в физиологическом растворе) обрабатывают по той же схеме. Животных индивидуально помещают в тестовую камеру из плексигласа на поднятую решетку для акклиматизации перед сутками тестирования. На сутки 15-29 оценку осуществляют с использованием серии калиброванных VFH с усилием 0,4, 0,6, 1, 2, 4, 6, 8 и 15 г. VFH, начиная с усилия 2 г, прикладывают восходящим или нисходящим образом согласно модифицированному способу вверх-вниз по Диксону, который описан Chaplan SR et al. (J Neurosci Methods 1994, 53: 55-63). Каждую VFH прикладывают к подошвенной поверхности оперированной задней лапы с постоянным направленным вверх давлением, пока не происходит сгибание в течение приблизительно 6 секунд. В отсутствии отдергивания лапы прикладывают более сильный стимул. В случае отдергивания лапы, выбирают следующий более слабый стимул. После начального изменения с положительной на отрицательную или наоборот, применяют 4 дополнительные стимуляции. 6-оценочный паттерн положительных и отрицательных реакций превращают в 50% PWT с использованием следующей формулы:
50% PWT (g) = (10[Xf+κδ])/10000,
где Xf представляет собой значение (в логарифмических единицах) конечной использованной VFH, κ представляет собой табличное значение для паттерна положительных/отрицательных реакций и δ представляет собой среднюю разность между стимулами в логарифмических единицах (здесь 0,224).
В случае, когда непрерывные положительные или отрицательные реакции наблюдают на всем протяжении до конца спектра стимулов, присваивают значения 0,25 и 15 г, соответственно. Животных, демонстрирующих статическую аллодинию (50% PWT <4 г) посредством обработки паклитакселом, отбирают для оценки и рандомизируют, чтобы было приблизительно равное среднее 50% PWT на протяжении всех групп. Соединения по изобретению или их наполнители вводят системно. Крыс знакомят с камерой в течение по меньшей мере 20 минут перед измерением. 50% PWT измеряют в подходящий момент после введения соединения. Статистический анализ осуществляют посредством критерия Стьюдента для одной выборки или ANOVA с апостериорным критерием Дуннетта в сравнении с группой наполнителя.
Все тестированные соединения по изобретению демонстрируют высокие активности в этой модели.
Индуцированное формалином ноцицептивное поведение у крыс
Самцов крыс Sprague-Dawley в возрасте 6 недель приобретают в Charles River Japan Inc. и содержат группами по две на клетку в 12-часовом цикле свет/темнота (свет включают в 07:00) с доступом к пище и воде ad libitum. Тест с формалином осуществляют во время светового цикла. Животные акклиматизируются к тестовой камере в течение по меньшей мере 30 минут перед инъекцией формалина. Зеркало помещают позади и/или под камерой, чтобы способствовать наблюдению. 50 мкл 5% раствора формалина инъецируют подкожно в подошвенную поверхность правой задней лапы. Незамедлительно после инъекции, крыс индивидуально помещают в камеру и регистрируют связанное с болью поведение. После тестирования, время, проведенное за лизанием и/или кусанием лапы, в которую выполняли инъекцию, подсчитывают по 5-минутным интервалам в течение 45 минут после обработки формалином. Сумму времени, проведенного за лизанием/кусанием, в секундах от времени 0 до 5 минут считают ранней фазой, тогда как позднюю фазу получают как сумму времени, проведенного за лизанием/кусанием, типично от 15 до 45 минут. Соединения по изобретению или их наполнители вводят системно в подходящий момент времени перед инъекцией формалина. Статистический анализ осуществляют посредством критерия Стьюдента для одной выборки или ANOVA с апостериорным критерием Дуннетта в сравнении с группой наполнителя.
Все тестированные соединения по изобретению демонстрируют высокие активности в этой модели.
Анализ связывания дофетилида у человека
Клетки HEK293S, трансфицированные HERG человека, получают и растят в пределах организации. Собранные клетки суспендируют в 50 мМ Трис-HCl (pH 7,4 при 4°C) и гомогенизируют с использованием ручного разрушителя Polytron PT 1200, установленного на полную мощность, в течение 20 с на льду. Гомогенаты центрифугируют при 48000×g при 4°C в течение 20 мин. Затем осадки ресуспендируют, гомогенизируют и центрифугируют еще раз аналогичным образом. Конечные осадки ресуспендируют в подходящем объеме 50 мМ Трис-HCl, 10 мМ KCl, 1 мМ MgCl2 (pH 7,4 при 4°C), гомогенизируют, делят на аликвоты и хранят при -80°C, пока не используют. Аликвоты мембранных фракций используют для определения концентрации белка с использованием BCA Protein Assay Kit (PIERCE) и считывателя планшетов ARVOsx (Wallac). Анализ связывания проводят в общем объеме 30 мкл в 384-луночных планшетах. Активность измеряют посредством PHERAstar (BMG LABTECH), используя технологию флуоресцентной поляризации. 10 мкл тестируемых соединений инкубируют с 10 мкл флуоресцентного лиганда (6 нМ меченое Cy3B производное дофетилида) и 10 мкл мембранного гомогената (6 мкг белка) в течение 120 минут при комнатной температуре. Неспецифическое связывание определяют с помощью 10 мкМ E4031 в конечной концентрации.
Все тестированные соединения по изобретению демонстрируют более высокие значения IC50 при связывании дофетилида у человека, чем значения IC50 в FRET анализе NaV1.3 или NaV1.7. Высокие значения IC50 в активностях связывания дофетилида человека ведут к снижению риска сердечно-сосудистых нежелательных явлений.
Анализ метаболической стабильности
Время полужизни в микросомах печени человека (HLM)
Тестируемые соединения (1 мкМ) инкубируют с 3,3 мМ MgCl2 и 0,78 мг/мл HLM (HL101) или 0,74 мг/мл HLM (Gentest UltraPool 150) в 100 мМ калий-фосфатном буфере (pH 7,4) при 37°C в планшете с 96 глубокими лунками. Реакционную смесь делят на две группы, группу не P450 и группу P450. NADPH (Никотинамидадениндинуклеотидфосфат) добавляют только в реакционную смесь группы P450. (Также вместо NADPH используют генерирующую NADPH систему.) Аликвоту образцов группы P450 собирают в момент времени 0, 10, 30 и 60 мин, где момент времени 0 мин показывает время, когда в реакционную смесь группы P450 добавляют NADPH. Аликвоту образцов группы P450 собирают в момент времени -10 и 65 мин. Собранные аликвоты экстрагируют с MeCN раствором, содержащим внутренний стандарт. Преципитированный белок осаждают в центрифуге (2000 об./мин, 15 мин). Концентрацию соединения в супернатанте измеряют с помощью системы LC/MS/MS.
Значение времени полужизни получают посредством построения графика натурального логарифма площади пика отношения соединения/внутренний стандарт в зависимости от времени. Наклон линии наилучшего соответствия через точки дает скорость метаболизма (k). Его преобразуют в значение времени полужизни с использованием следующих уравнений: Время полужизни = ln 2/k.
Соединения по данному изобретению демонстрируют предпочтительную стабильность, которая показывает указанное выше практическое использование.
Анализ взаимодействия между лекарственными средствами
Этот способ по существу включает определение процента ингибирования формирования метаболитов из зондов (такрин (Sigma A3773-1G) 2 мкМ, декстрометорфан (Sigma D-9684) 5 мкМ, диклофенак (Sigma D-6899-10G) 5 мкМ и мидазолам (ULTRAFINE UC-429) 2 мкМ) по 3 мкМ каждого соединения.
Более конкретно, анализ осуществляют следующим образом. Соединения (60 мкМ, 10 мкл) предварительно инкубируют в 170 мкл смеси, содержащей 0,1 мг белка/мл микросом печени человека, 100 мМ калий-фосфатный буфер (pH 7,4), 1 мМ MgCl2 и зонды в качестве субстрата, в течение 5 мин. Реакцию начинают посредством добавления 20 мкл 10 мМ NADPH (также используют 20 мкл генерирующей NADPH системы, которая состоит из 10 мМ NADP+, 50 мМ DL-изолимонной кислоты и 10 Ед./мл изолимонной дегидрогеназы). Планшет для анализа инкубируют при 37°C. MeCN добавляют для того, чтобы инкубировать раствор в подходящее время (например, 8 мин).
Концентрацию метаболитов в супернатанте измеряют с помощью системы LC/MS/MS.
Степень взаимодействия между лекарственными средствами интерпретируют на основе % образования метаболитов в присутствии или в отсутствии тестируемого соединения.
Соединения по данному изобретению демонстрируют предпочтительные результаты, которые показывают указанное выше практическое использование.
Анализ связывания белков плазмы
Связывание белков плазмы тестируемым соединением (1 мкМ) измеряют с помощью способа равновесного диализа, используя оборудование под 96-луночные планшеты. HTD96aTM, регенерированные целлюлозные мембраны (отсечение по молекулярной массе 12000-14000, 22 мм×120 мм) вымачивают в течение ночи в дистиллированной воде, затем в течение 15 минут в 30% этаноле и наконец в течение 20 минут в диализном буфере (фосфатно-солевой буфер Дульбекко, pH7,4). Используют замороженную плазму человека, крыс Sprague-Dawley и собак Beagle. Собирают оборудование для диализа и добавляют 150 мкл плазмы, обогащенной соединением, на одну сторону каждой лунки и 150 мкл диализного буфера на другую сторону каждой лунки. После 4 часов инкубации при 37°C на 150 об./мин, берут аликвоты образцов плазмы и буфера. Соединение в плазме и буфере экстрагируют в 300 мкл MeCN, содержащего соединения внутреннего стандарта для анализа. Концентрацию соединения определяют с использованием анализа LC/MS/MS.
Фракцию несвязанного соединения вычисляют с помощью следующих уравнений (A) или (B):
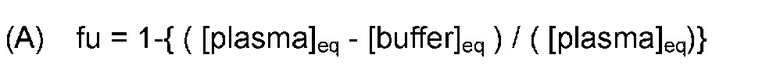 ,
,
где [plasma]eq и [buffer]eq представляют собой концентрации соединения в плазме и буфере, соответственно.
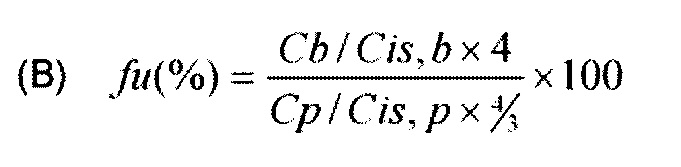 ,
,
где Cp представляет собой площадь пика соединения в образце плазмы;
Cis,p представляет собой площадь пика внутреннего стандарта в образце плазмы;
Cb представляет собой площадь пика соединения в образце буфера;
Cis,b представляет собой площадь пика внутреннего стандарта в образце буфера;
4 и 4/3 представляют собой обратное значение степени разведения в плазме и буфере, соответственно.
Соединения по данному изобретению демонстрируют предпочтительное связывание белков плазмы, которое показывает указанное выше практическое использование.
Исследование равновесной водной растворимости
Раствор DMSO (2 мкл, 30 мМ) каждого соединения распределяют в каждую лунку 96-луночного планшета со стеклянным дном. Калий-фосфатный буферный раствор (50 мМ, 198 мкл, pH 6,5) добавляют в каждую лунку, и смесь инкубируют при 37°C при вращающем встряхивании в течение 24 часов. После центрифугирования при 2000g в течение 5 минут, супернатант фильтруют через поликарбонатную мембрану Isopore. Концентрацию образцов определяют с помощью общего способа градиентной ВЭЖХ (J. Pharm. Sci. 2006, 95, 2115-2122).
Все публикации, включая в качестве неограничивающих примеров, выданные патенты, патентные заявки и статьи в журналах, цитированные в этой заявке, включены в настоящий документ посредством ссылки в полном объеме. Несмотря на то, что изобретение описано выше со ссылкой на раскрытые варианты осуществления, специалисты в данной области легко поймут, что конкретные детализированные эксперименты являются только иллюстрациями изобретения. Следует понимать, что различные модификации можно выполнять, не отступая от сущности изобретения. Соответственно, изобретение ограничено только следующей формулой изобретения.
Промышленная применимость
Производные пиразолопиридина по настоящему изобретению можно использовать при лечении широкого диапазона нарушений, в частности, боли, такой как острая боль, хроническая боль, нейропатическая боль, воспалительная боль, висцеральная боль, ноцицептивная боль, включая боль после хирургического вмешательства, и смешанные типы боли, в которые вовлечены внутренние органы, желудочно-кишечный тракт, структуры черепа, скелетно-мышечная система, спинной мозг, мочеполовая система, сердечно-сосудистая система и ЦНС, включая боль при злокачественной опухоли, позвоночную боль, орофациальную боль и боль, вызванную химиотерапией.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ АРИЛАМИДОВ В КАЧЕСТВЕ БЛОКАТОРОВ TTX-S | 2011 |
|
RU2535671C1 |
| ПРОИЗВОДНЫЕ ПИРРОЛОПИРИДИНОНА В КАЧЕСТВЕ TTX-S БЛОКАТОРОВ | 2013 |
|
RU2646754C2 |
| АМИДОПРОИЗВОДНЫЕ КАК БЛОКАТОРЫ TTX-S | 2013 |
|
RU2632899C2 |
| НОВЫЕ СОЕДИНЕНИЯ И КОМПОЗИЦИИ ДЛЯ ИНГИБИРОВАНИЯ NAMPT | 2011 |
|
RU2617988C2 |
| ПРОИЗВОДНОЕ N-(АЗААРИЛ)ЦИКЛОЛАКТАМ-1-КАРБОКСАМИДА, МЕТОД ЕГО ПОЛУЧЕНИЯ И ЕГО ПРИМЕНЕНИЕ | 2018 |
|
RU2765785C2 |
| БЕНЗОКСАЗЕПИНОВЫЕ ИНГИБИТОРЫ PI3K И СПОСОБЫ ПРИМЕНЕНИЯ | 2010 |
|
RU2600927C2 |
| ФАРМАЦЕВТИЧЕСКИЕ СОЕДИНЕНИЯ | 2020 |
|
RU2840815C2 |
| АРИЛ-ЗАМЕЩЕННЫЕ КАРБОКСАМИДНЫЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ БЛОКАТОРОВ КАЛЬЦИЕВЫХ ИЛИ НАТРИЕВЫХ КАНАЛОВ | 2010 |
|
RU2575168C2 |
| ГИДРОКСИПУРИНОВЫЕ СОЕДИНЕНИЯ И ИХ ПРИМЕНЕНИЕ | 2016 |
|
RU2685417C1 |
| БЕНЗОКСЕПИНОВЫЕ ИНГИБИТОРЫ PI3 И СПОСОБЫ ПРИМЕНЕНИЯ | 2010 |
|
RU2557658C2 |
Настоящее изобретение относится к пиразолопиридиновым производным формулы (I), в которой А представляет собой арил, выбранный из группы, состоящей из пиридила, фенила, пиразинила, пиридазинила, пиразола, триазола, индолила, бензимидазолила и изохинолинила; -В-С представляет собой -NR2-(C=O) или -(C=O)-NR2-, и остальные силволы и радикалы имеют значения, указанные в формуле изобретения. Данные соединения обладают активностью, блокирующей потенциалозависимые натриевые каналы, такие как TTX-S каналы, являются пригодными для лечения или предотвращения расстройства и заболевания, в котором участвуют потенциалзависимые натриевые каналы. Настоящее изобретение также относится к фармацевтической композиции, содержащей данные соединения, и применению данных соединений и композиций в предотвращении или лечении заболеваний, в которых участвуют потенциалзависимые натриевые каналы. 8 н. и 7 з.п. ф-лы, 10 табл., 649 пр.
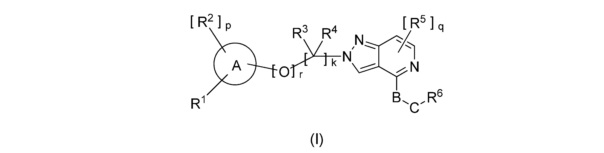
1. Соединение следующей формулы (I):
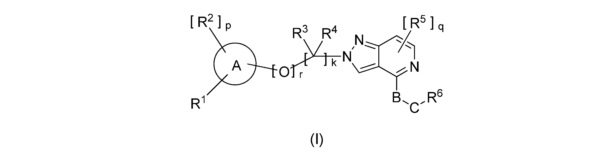 ,
,
в которой:
A представляет собой арил, выбранный из группы, состоящей из пиридила, фенила, пиразинила, пиридазинила, пиразола, триазолила, индолила, бензимидазолила и изохинолинила;
-B-C- представляет собой -NR2-(C=O)- или -(C=O)-NR2-, где R2 представляет собой водород или C1-6 алкил;
R1 независимо выбран из группы, состоящей из: (1) водорода, (2) -On-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (3) -On-C3-7 циклоалкила, где циклоалкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (4) -On-фенила, -On-пиридила или -On-пиразолила, где фенил, пиридил или пиразолил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, и (7) -NH-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11;
где n независимо равен 0 или 1, когда n равен 0, химическая связь присутствует вместо -On-;
R2 независимо выбран из группы, состоящей из: (1) водорода, (2) галогена, (3) гидроксила, (4) -On-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R7, (5) -On-C3-6 циклоалкила, где циклоалкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R7, и (7) -On-фенила, где фенил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R7;
где n независимо равен 0 или 1, когда n равен 0, химическая связь присутствует вместо -On-;
p равен 1 или 2;
R3 и R4 независимо представляют собой водород или C1-6 алкил, который является незамещенным;
R5 независимо выбран из группы, состоящей из: (1) водорода и (3) C1-6 алкила, где алкил является незамещенным;
R5 может быть в любом положении в пиразолопиридиновом кольце;
q равен 1;
R6 независимо представляет собой водород, C1-6 алкил, C1-6 алкокси, C3-7 циклоалкил, -NR8R9, гетероциклил, арил, арил-C1-6 алкил или гетероциклил-C1-6 алкил, где C1-6 алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из группы, состоящей из гидроксила, -O-C1-6 алкила, -C3-7 циклоалкила, который является незамещенным или замещенным гидроксилом, гидроксил-C1-6 алкокси, -CN, -NR8R9, -(C=O)-NR8R9, -NR8-(C=O)-R9, -NR8-(C=O)-NR9R10, -NR8-(C=O)-OR9, -NR8-S(O)2-R9, -NR8-S(O)2-NR9R10 и -S(O)2-R8;
где гетероциклил или гетероциклил-C1-6 алкил является незамещенным или замещенным -(C=O)-R8 или -S(O)2-R8;
где гетероциклил представляет собой 4-6-членный насыщенный гетероциклил, содержащий один или два гетероатома, которые независимо выбраны из O, N и S;
где арил или арил-C1-6 алкил является незамещенным или замещенным одним или двумя заместителями, которые представляют собой или независимо выбраны из C1-6 алкила;
когда B представляет собой -NR2-, и C представляет собой -(C=O)-, R6 может образовывать 5-членное кольцо с R2, необязательно содержащее дополнительный гетероатом O или N;
R7 выбран из группы, состоящей из: (1) водорода, (2) галогена, (5) -Ol-(C1-3)перфторалкила, (6) -(C=O)m-Ol-C3-6 циклоалкила, и (8) -Ol-фенила, где фенил является незамещенным или замещенным одним или более галогенами;
где l равен 0 или 1, и m равен 0; когда l равен 0, химическая связь присутствует вместо -Ol-, и когда l равен 0, и m равен 0, химическая связь присутствует вместо -(C=O)m-Ol-;
R8, R9 и R10 независимо представляют собой водород, C1-6 алкил, который является незамещенным или замещенным одним или более гидроксилами, C3-7 циклоалкил, который является незамещенным или замещенным гидроксилом, или арил, выбранный из фенила или пиридила; или R8 образует 4-6-членное кольцо с R9, которое может содержать атом азота или атом кислорода;
R11 независимо выбран из группы, состоящей из: (1) водорода, (3) галогена, (4) -C1-6 алкила, который является незамещенным или замещенным одним или более галогенами, (5) -C3-6 циклоалкила, (6) -O-C1-6 алкила, где алкил является незамещенным или замещенным одним или более галогенами, и (9) фенила, который является незамещенным или замещенным галогеном;
k равен 1 или 2;
r равен 0 или 1, когда r равен 0, химическая связь присутствует вместо -[O]r-;
или его фармацевтически приемлемая соль.
2. Соединение по п. 1, где
k равен 1;
r равен 0;
или фармацевтически приемлемая соль.
3. Соединение следующей формулы (II)
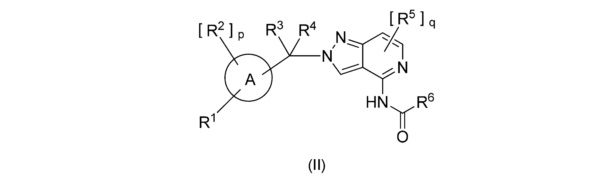 ,
,
в которой:
A выбирают из группы, состоящей из пиридила, фенила, пиразинила, пиридазинила, триазолила и бензимидазолила;
R1 независимо выбран из группы, состоящей из: (1) водорода, (2) -On-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (3) -On-C3-7 циклоалкила, где циклоалкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, и (4) -On-фенила, -On-пиридила или -On-пиразолила, где фенил, пиридил или пиразолил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11;
где n независимо равен 0 или 1, когда n равен 0, химическая связь присутствует вместо -On-;
R2 независимо выбран из группы, состоящей из: (1) водорода, (2) галогена, (3) гидроксила, (4) -On-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R7, (5) -On-C3-6 циклоалкила, где циклоалкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R7, и (7) -On-фенила, где фенил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R7;
где n независимо равен 0 или 1, когда n равен 0, химическая связь присутствует вместо -On-;
p равен 1 или 2;
R3 и R4 независимо представляют собой водород или C1-6 алкил, который является незамещенным;
R5 независимо выбран из группы, состоящей из: (1) водорода, и (3) -C1-6 алкила, где алкил является незамещенным;
R5 может быть в любом положении в пиразолопиридиновом кольце;
q равен 1;
R6 независимо представляет собой водород, C1-6 алкил, C1-6 алкокси, C3-7 циклоалкил, -NR8R9, гетероциклил, арил, арил-C1-6 алкил или гетероциклил-C1-6 алкил, где C1-6 алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из группы, состоящей из гидроксила, C1-6 алкила, -O-C1-6 алкила, -C3-7 циклоалкила, -CN, -(C=O)-NR8R9, -NR8-(C=O)-R9, и -S(O)2-R8;
где гетероциклил или гетероциклил-C1-6 алкил является незамещенным или замещенным -(C=O)-R8 или -S(O)2-R8;
где гетероциклил представляет собой 4-6-членный насыщенный гетероциклил, содержащий один или два гетероатома, которые независимо выбраны из O, N и S;
где арил или арил-C1-6 алкил является незамещенным или замещенным одним или двумя заместителями, которые представляют собой или независимо выбраны из C1-6 алкила;
R7 выбран из группы, состоящей из: (1) водорода, (2) галогена, (5) -Ol-(C1-3)перфторалкила, (6) -(C=O)m-Ol-C3-6 циклоалкила, и (8) -Ol-фенила, где фенил является незамещенным или замещенным одним или более галогенами;
где l равен 0 или 1, и m равен 0; когда l равен 0, химическая связь присутствует вместо -Ol-, и когда l равен 0, и m равен 0, химическая связь присутствует вместо -(C=O)m-Ol-;
R8, R9 и R10 независимо представляют собой водород, C1-6 алкил, который является незамещенным или замещенным одним или более гидроксилами, или C3-7 циклоалкил, который является незамещенным или замещенным гидроксилом; или R8 образует 4-6-членное кольцо с R9, которое может содержать атом азота или атом кислорода;
R11 независимо выбран из группы, состоящей из: (1) водорода, (3) галогена, (5) -C3-6 циклоалкила, (6) -O-C1-6 алкила, где алкил является незамещенным или замещенным одним или более галогенами, (9) фенила, который является незамещенным или замещенным галогеном;
или его фармацевтически приемлемая соль.
4. Соединение по п. 3, в котором:
R2 независимо выбран из группы, состоящей из: (1) водорода, (2) галогена, (3) метила и (4) метокси;
p равен 1;
R3 представляет собой водород;
R4 представляет собой водород или метил;
R6 выбран из группы, состоящей из метила, этила, изопропила, циклопропила, гетероциклила и арила, где метил, этил или изопропил является незамещенным или замещенным одним или более заместителями, независимо выбранными из группы, состоящей из гидроксила, C1-6 алкила, -O-C1-6 алкила, и -CN;
где гетероциклил является незамещенным или замещенным -(C=O)-R8 или -S(O)2-R8;
где арил является незамещенным или замещенным одним или двумя заместителями, которые представляют собой или независимо выбраны из C1-6 алкила; или его фармацевтически приемлемая соль.
5. Соединение следующей формулы (III)
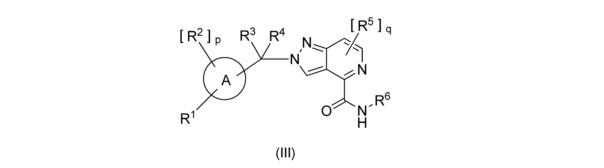 ,
,
в которой:
A выбирают из группы, состоящей из пиридила, фенила, пиразинила, пиридазинила, пиразола, триазолила, индолила, бензимидазолила, и изохинолинила;
R1 независимо выбран из группы, состоящей из: (1) водорода, (2) -On-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (3) -On-C3-7 циклоалкила, где циклоалкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, (4) -On-фенила, -On-пиридила или -On-пиразолила, где фенил, пиридил или пиразолил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11, и (7) -NH-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R11;
где n независимо равен 0 или 1, когда n равен 0, химическая связь присутствует вместо -On-;
R2 независимо выбран из группы, состоящей из: (1) водорода, (2) галогена, (3) гидроксила, (4) -On-C1-6 алкила, где алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R7, (5) -On-C3-6 циклоалкила, где циклоалкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R7, и (7) -On-фенила, где фенил является незамещенным или замещенным одним или более заместителями, независимо выбранными из R7;
где n независимо равен 0 или 1, когда n равен 0, химическая связь присутствует вместо -On-;
p равен 1 или 2;
R3 и R4 независимо представляют собой водород или C1-6 алкил, который является незамещенным;
R5 независимо выбран из группы, состоящей из: (1) водорода, и (3) C1-6 алкила, где алкил является незамещенным;
R5 может быть в положении 6 или 7 в пиразолопиридиновом кольце, где R5 представляет собой C1-6 алкил;
q равен 1;
R6 независимо представляет собой водород, C1-6 алкил, C1-6 алкокси, C3-7 циклоалкил, гетероциклил, арил, арил-C1-6 алкил или гетероциклил-C1-6 алкил, где C1-6 алкил является незамещенным или замещенным одним или более заместителями, независимо выбранными из группы, состоящей из гидроксила, -O-C1-6 алкила, -C3-7 циклоалкила, который является незамещенным или замещенным гидроксилом, гидроксил-C1-6 алкокси, -CN, -NR8R9, -(C=O)-NR8R9, -NR8-(C=O)-R9, -NR8-(C=O)-NR9R10, -NR8-(C=O)-OR9, -NR8-S(O)2-R9, -NR8-S(O)2- NR9R10 и -S(O)2-R8;
где гетероциклил или гетероциклил-C1-6 алкил является незамещенным или замещенным -(C=O)-R8 или -S(O)2-R8;
где гетероциклил представляет собой 4-6-членный насыщенный гетероциклил, содержащий один или два гетероатома, которые независимо выбраны из O, N и S;
где арил или арил-C1-6 алкил является незамещенным или замещенным одним или двумя заместителями, которые представляют собой или независимо выбраны из C1-6 алкила;
R7 выбрано из группы, состоящей из: (1) водорода, (2) галогена, (5) -Ol-(C1-3)перфторалкила, (6) -(C=O)m-Ol-C3-6 циклоалкила, и (8) -Ol-фенила, где фенил является незамещенным или замещенным одним или более галогенами;
где l равен 0 или 1 и m равен 0; когда l равен 0, химическая связь присутствует вместо -Ol-, и когда l равен 0, и m равен 0, химическая связь присутствует вместо -(C=O)m-Ol-;
R8, R9 и R10 независимо представляют собой водород, C1-6 алкил, который является незамещенным или замещенным одним или более гидроксилами, C3-7 циклоалкил, который является незамещенным или замещенным гидроксилом, или арил, выбранный из фенила или пиридила; или R8 образует 4-6-членное кольцо с R9, которое может содержать атом азота, атом кислорода или атом кислорода;
R11 независимо выбран из группы, состоящей из: (1) водорода, (3) галогена, (4) -C1-6 алкила, который является незамещенным или замещенным одним или более галогенами, (5) -C3-6 циклоалкила, (6) -O-C1-6 алкила, где алкил является незамещенным или замещенным одним или более галогенами, и (9) фенила, который является незамещенным или замещенным галогеном;
или его фармацевтически приемлемая соль.
6. Соединение по п. 5, в котором:
R2 независимо выбран из группы, состоящей из: (1) водорода, (2) галогена, (3) метила и (4) метокси;
p равен 1;
R3 представляет собой водород;
R4 представляет собой водород или метил;
R6 выбран из группы, состоящей из: метила, этила, изопропила, пропила и бутила, который является незамещенным или замещенным одним или более заместителями, независимо выбранными из группы, состоящей из: гидроксила, C3-7 циклоалкила, который является незамещенным или замещенным гидроксилом, -O-C1-6 алкила, -CN и -NR8-(C=O)-R9, в котором каждый из R8 и R9 имеет значение, как в п. 5;
или его фармацевтически приемлемая соль.
7. Соединение, которое выбрано из:
N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
2-гидрокси-2-метил-N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразол[4,3-c]пиридин-4-ил)пропанамида;
N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)ацетамида;
N-(2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)ацетамида;
N-(2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропионамида;
N-(2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанкарбоксамида;
N-(2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-гидрокси-2-метилпропанамида;
N-(2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)ацетамида;
N-(2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропионамида;
N-(2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)тетрагидро-2H-пиран-4-карбоксамида;
N-(2-((6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-хлор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-хлор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропионамида;
N-(2-((5-хлор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)тетрагидро-2H-пиран-4-карбоксамида;
N-(2-((5-хлор-6-(2,2-дифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)ацетамида;
N-(2-((5-хлор-6-(2,2-дифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропионамида;
N-(2-((5-хлор-6-(2,2-дифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-хлор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)ацетамида;
N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)тетрагидро-2H-пиран-4-карбоксамида;
N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)оксазол-5-карбоксамида;
1,1-диметил-3-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)мочевины;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-амина;
3-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)оксазолидин-2-она;
этил (2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)карбамата;
N-(2-((6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)ацетамида;
N-(2-((6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропионамида;
4-метокси-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридина;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((6-(2,2-дифторэтокси)-5-фторпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((6-(2,2-дифторэтокси)-5-фторпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((6-(2,2,2-трифторэтокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((6-(2,2,2-трифторэтокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)ацетамида;
N-(2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропионамида;
N-(2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)тетрагидро-2H-пиран-4-карбоксамида;
N-(2-((5-фтор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропионамида;
N-(2-((5-фтор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((5-фтор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пиваламида;
N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)никотинамида;
1-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пирролидин-2-она;
1-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)имидазолидин-2-она;
4-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)морфолина;
N-(1-метил-1H-пиразол-3-ил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-амина;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(пиримидин-2-ил)-2H-пиразоло[4,3-с]пиридин-4-амина;
N-(2-((6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)тетрагидро-2H-пиран-4-карбоксамида;
3-(2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-1,1-диметилмочевины;
N-(2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пиваламида;
N-(2-(4-(2,2,2-трифторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-(4-(2,2,2-трифторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-4-(1H-пиразол-5-ил)-2H-пиразоло[4,3-c]пиридина;
N-(2-((6-(2,2,3,3,3-пентафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((6-(2,2,3,3,3-пентафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-(4-(трифторметокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(тетрагидрофуран-3-ил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-циклопропил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-циклобутил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(циклопропилметил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-((тетрагидро-2H-пиран-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-метоксиэтил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-N-(1-гидроксипропан-2-ил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-метил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропионамида;
N-(3-метил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-(1-(6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-(2-(6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((6-(4-фторфенокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((6-(4-фторфенокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-метил-N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
(S)-N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)тетрагидрофуран-2-карбоксамида;
(S)-N-(2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)тетрагидрофуран-2-карбоксамида;
N-(2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)никотинамида;
(R)-2-гидрокси-N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
(S)-2-гидрокси-N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пирролидин-1-карбоксамида;
1-ацетил-N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пиперидин-4-карбоксамида;
N-изопропил-2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-пропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изобутил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-этоксиэтил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(цианометил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-((тетрагидрофуран-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(диметиламино)этил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(пиридин-3-илметил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-((5-метил-1,2,4-оксадиазол-3-ил)метил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(пиридин-3-ил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)тетрагидрофуран-2-карбоксамида;
(R)-N-(2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)тетрагидрофуран-2-карбоксамида;
N-(3-метоксипропил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-((1-гидроксициклогексил)метил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(6-метил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропионамида;
N-(6-метил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(6-метил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
2-гидрокси-2-метил-N-(6-метил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
N-(7-метил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропионамида;
N-(7-метил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
1-изобутирил-N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пиперидин-4-карбоксамида;
N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-1-(метилсульфонил)пиперидин-4-карбоксамида;
(S)-1-ацетил-N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пирролидин-2-карбоксамида;
(R)-1-ацетил-N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пирролидин-2-карбоксамида;
N-метил-N-(2-((2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)амино)-2-оксоэтил)ацетамида;
(S)-2-метокси-N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
(S)-N-(2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-метоксипропанамида;
(R)-N-(2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-гидроксипропанамида;
(S)-N-(2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-гидроксипропанамида;
2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-циклопропил-2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(циклопропилметил)-2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-N-(2-(диметиламино)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(2-морфолиноэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)2-(пиридин-2-ил)ацетамида;
N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)2-(пиридин-3-ил)ацетамида;
N-изопропил-2-((6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-циклопропил-2-((6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(циклопропилметил)-2-((6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-(пиридин-4-ил)ацетамида;
N-(цианометил)-2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-N-пропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-цианопропан-2-ил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидрокси-2-метилпропил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-(диметиламино)пропил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-аминоэтил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(оксетан-3-ил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-((4-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((4-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-(пиридин-4-ил)ацетамида;
2-(пиридин-4-ил)-N-(2-((6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)ацетамида;
N-(2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-(пиридин-3-ил)ацетамида;
2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((4-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
2-гидрокси-2-метил-N-(2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
N-метил-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-метил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)2-(2-метилтиазол-4-ил)ацетамида;
N-(2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-(пиридин-3-ил)ацетамида;
N-(2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-(пиридин-4-ил)ацетамида;
2-(3,5-диметилизоксазол-4-ил)-N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)ацетамида;
N-изопропил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-N-(2-гидроксипропил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(2-гидроксипропил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(2,3-дигидроксипропил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
2-гидрокси-2-метил-N-(2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
N-метил-2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(1-гидроксипропан-2-ил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-амино-2-оксоэтил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(2-(метилсульфонамидо)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-цианоэтил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-цианоэтил)-2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
2-((5-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((5-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((5-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((5-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(2-гидроксиэтокси)этил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-этил-2-((5-фтор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-фтор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2-дифторэтокси)пиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2-дифторэтокси)пиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2-дифторэтокси)пиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2-дифторэтокси)пиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-N-(2,3-дигидроксипропил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-(4-(2,2,2-трифторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(4-фторфенокси)-5-метилпиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((6-(2,2,3,3,3-пентафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-((6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(1-амино-1-оксопропан-2-ил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(2-(метиламино)-2-оксоэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-амино-3-оксопропил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидрокси-2,2-диметилпропил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(4-гидроксибутил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-(3-метил-4-(2,2,2-трифторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-ацетамидопропил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(3-(метилсульфонамидо)пропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторэтокси)-3-метилбензил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторэтокси)-3-метилбензил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2-дифторэтокси)пиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-(4-(2,2,2-трифторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((2-метил-6-(2,2,2-трифторэтокси)пиридин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((2-метил-6-(2,2,2-трифторэтокси)пиридин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(3-гидроксипропил)-2-(3-метил-4-(2,2,2-трифторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((5-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-фтор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(4-фторфенокси)-5-метилпиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((6-(2,2,3,3,3-пентафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-((2-метил-6-(2,2,2-трифторэтокси)пиридин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((2-метил-6-(2,2,2-трифторэтокси)пиридин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((2-метил-6-(2,2,2-трифторэтокси)пиридин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((2-метил-6-(2,2,2-трифторэтокси)пиридин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((2-метил-6-(2,2,2-трифторэтокси)пиридин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((6-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((6-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
(S)-N-(2-гидроксипропил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-N-(2-гидроксипропил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(2,3-дигидроксипропил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-N-(2,3-дигидроксипропил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(2,3-дигидроксипропил)-2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((1-(5-(трифторметил)пиридин-2-ил)-1H-пиразол-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((1-(5-(трифторметил)пиридин-2-ил)-1H-пиразол-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((1-(5-(трифторметил)пиридин-2-ил)-1H-пиразол-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-((1-(5-(трифторметил)пиридин-2-ил)-1H-пиразол-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((1-(5-(трифторметил)пиридин-2-ил)-1H-пиразол-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(2-гидроксипропил)-2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-N-(2-гидроксипропил)-2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(1-гидроксипропан-2-ил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(1-гидроксипропан-2-ил)-2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-цианоэтил)-2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-цианоэтил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-амино-2-оксоэтил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-метоксиэтил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-метил-6-(2-(2,2,2-трифторэтокси)этокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-метил-6-(2-(2,2,2-трифторэтокси)этокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
2-гидрокси-2-метил-N-(2-((5-метил-6-(2-(2,2,2-трифторэтокси)этокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
N-(2-((2-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((2-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-гидроксиэтил)-2-((5-метил-6-(2-(2,2,2-трифторэтокси)этокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((5-метил-6-(2-(2,2,2-трифторэтокси)этокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-((5-метил-6-(2-(2,2,2-трифторэтокси)этокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((5-метил-6-(2-(2,2,2-трифторэтокси)этокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((2-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((2-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((2-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((2-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((5-метил-6-(2-(2,2,2-трифторэтокси)этокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((2-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-(2-(4-(трифторметил)фенокси)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-(2-(4-(трифторметил)фенокси)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-(2-(4-(трифторметил)фенокси)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-(2-(4-(трифторметил)фенокси)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-(2-(4-(трифторметил)фенокси)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((6-метил-5-(2,2,2-трифторэтокси)пиразин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((6-метил-5-(2,2,2-трифторэтокси)пиразин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-гидрокси-2-метилпропанамида;
2-(2-((3-хлор-5-(трифторметил)пиридин-2-ил)окси)этил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(2-((3-хлор-5-(трифторметил)пиридин-2-ил)окси)этил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(2-((3-хлор-5-(трифторметил)пиридин-2-ил)окси)этил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(2-((3-хлор-5-(трифторметил)пиридин-2-ил)окси)этил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(2-((3-хлор-5-(трифторметил)пиридин-2-ил)окси)этил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-циклопропил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-циклопропил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-циклопропил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-циклопропил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-циклопропил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-((6-метил-5-(2,2,2-трифторэтокси)пиразин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((6-метил-5-(2,2,2-трифторэтокси)пиразин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((6-метил-5-(2,2,2-трифторэтокси)пиразин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((6-метил-5-(2,2,2-трифторэтокси)пиразин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(4-хлор-1H-пиразол-1-ил)-5-метилпиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(4-хлор-1H-пиразол-1-ил)-5-метилпиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-((5-метил-2-фенил-2H-1,2,3-триазол-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-метоксиэтил)-2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(4-хлор-1H-пиразол-1-ил)-5-метилпиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(4-хлор-1H-пиразол-1-ил)-5-метилпиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
2-гидрокси-2-метил-N-(2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
N-(2-((5-метил-2-фенил-2H-1,2,3-триазол-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((6-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((6-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((6-(циклопропилметокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((6-(циклопропилметокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((6-(циклопропилметокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)2-гидрокси-2-метилпропанамида;
N,6-диметил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-6-метил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((5-метил-6-((2,2,2-трифторэтил)амино)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((5-метил-6-((2,2,2-трифторэтил)амино)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((5-метил-6-((2,2,2-трифторэтил)амино)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((5-метил-6-((2,2,2-трифторэтил)амино)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(циклопропилметокси)-5-метилпиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-((6-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((6-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((6-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((6-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(циклопропилметокси)-5-метилпиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(циклопропилметокси)-5-метилпиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(циклопропилметокси)-5-метилпиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(циклопропилметокси)-5-метилпиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-(3-метил-4-(трифторметокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-(3-метил-4-(трифторметокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-(3-метил-4-(трифторметокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-(3-метил-4-(трифторметокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((2-(2,2,2-трифторэтокси)пиридин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-фенил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-метил-2-(3-метил-4-(трифторметокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(4-хлор-1H-пиразол-1-ил)-5-метилпиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((2-(2,2,2-трифторэтокси)пиридин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(4-фторфенокси)-5-метилпиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((6-(4-фторфенокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-6-метил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-6-метил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-N-(3-(метилсульфонил)пропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-((1-(2,2,2-трифторэтокси)изохинолин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((1-(2,2,2-трифторэтокси)изохинолин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((1-(2,2,2-трифторэтокси)изохинолин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((1-(2,2,2-трифторэтокси)изохинолин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((1-(2,2,2-трифторэтокси)изохинолин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-(4-((2,2,2-трифторэтокси)метил)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-(4-((2,2,2-трифторэтокси)метил)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-(4-((2,2,2-трифторэтокси)метил)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-4-гидрокси-1-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пирролидин-2-она;
2-((5-(2,2-дифторэтокси)-4-метилпиридин-2-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(2,2-дифторэтокси)-4-метилпиридин-2-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-((1-метил-5-(трифторметокси)-1H-индол-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((1-метил-5-(трифторметокси)-1H-индол-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((1-метил-5-(трифторметокси)-1H-индол-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((1-метил-5-(трифторметокси)-1H-индол-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(3-хлор-4-(2,2-дифторэтокси)бензил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(3-хлор-4-(2,2-дифторэтокси)бензил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-метил-6-((2,2,2-трифторэтокси)метил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(3-(метилсульфонил)пропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((5-метил-6-((2,2,2-трифторэтокси)метил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((5-метил-6-((2,2,2-трифторэтокси)метил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((5-метил-6-((2,2,2-трифторэтокси)метил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((5-метил-6-((2,2,2-трифторэтокси)метил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((1-метил-5-(трифторметокси)-1H-индол-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-метил-6-((2,2,2-трифторэтокси)метил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((5-(2,2-дифторэтокси)-4-метилпиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-(2,2-дифторэтокси)-4-метилпиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((5-(2,2-дифторэтокси)-4-метилпиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-гидрокси-2-метилпропанамида;
N-(2-(3-(трифторметокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-(3-(трифторметокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
2-гидрокси-2-метил-N-(2-(3-(трифторметокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
N-(2-(2-((3-фтор-5-(трифторметил)пиридин-2-ил)окси)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-(2-((3-фтор-5-(трифторметил)пиридин-2-ил)окси)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-метил-2-(3-(трифторметокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-(3-(трифторметокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-(3-(трифторметокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-(3-(трифторметокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-(2-((3-фтор-5-(трифторметил)пиридин-2-ил)окси)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(2-((3-фтор-5-(трифторметил)пиридин-2-ил)окси)этил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(2-((3-фтор-5-(трифторметил)пиридин-2-ил)окси)этил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-(2,2,3,3,3-пентафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-(2,2,3,3,3-пентафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-гидроксиэтил)-2-(4-(1,1,2,2-тетрафторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-(4-(1,1,2,2-тетрафторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((5-(2,2,3,3,3-пентафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((5-(2,2,3,3,3-пентафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((5-(2,2,3,3,3-пентафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(2,2-дифторэтокси)-4-метилпиридин-2-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(2,2-дифторэтокси)-4-метилпиридин-2-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(2,2-дифторэтокси)-4-метилпиридин-2-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((5-(2,2,3,3-тетрафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((5-(2,2,3,3-тетрафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((5-(2,2,3,3-тетрафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-гидрокси-2-метилпропанамида;
N-(2-((5-(2,2,3,3-тетрафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-ацетамидоэтил)-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(2-гидроксипропил)-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(2,3-дигидроксипропил)-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(3-(трифторметил)бензил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-(3-(трифторметил)бензил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-метил-2-(3-(трифторметил)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-(3-(трифторметил)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-(3-(трифторметил)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-(3-(трифторметил)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамид;
(R)-N-(2-гидроксипропил)-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2Hпиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-N-(2,3-дигидроксипропил)-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(3-хлор-4-(2,2-дифторэтокси)бензил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-(4-(1,1,2,2-тетрафторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(3-хлор-4-(2,2-дифторэтокси)бензил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-(4-(1,1,2,2-тетрафторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-((S)-2-гидроксипропил)-2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-((5-метил-6-(3,3,3-трифторпропил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((5-метил-6-(3,3,3-трифторпропил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((5-метил-6-(3,3,3-трифторпропил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((5-метил-6-(3,3,3-трифторпропил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((5-метил-6-(3,3,3-трифторпропил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-((4-метил-5-(3,3,3-трифторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((4-метил-5-(3,3,3-трифторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((4-метил-5-(3,3,3-трифторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((4-метил-5-(3,3,3-трифторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-N-(2,3-дигидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-N-(2,3-дигидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-N-(1-гидроксипропан-2-ил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
2-гидрокси-2-метил-N-(2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
N-метил-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((4-метил-5-(3,3,3-трифторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((4-метил-5-(3,3,3-трифторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((5-метил-6-(3,3,3-трифторпропил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((5-метил-6-(3,3,3-трифторпропил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
2-((5-хлор-6-(2,2-дифторпропокси)пиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2-дифторпропокси)пиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2-дифторпропокси)пиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2-дифторпропокси)пиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2-дифторпропокси)пиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(1-гидроксипропан-2-ил)-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-хлор-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-хлор-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((5-хлор-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)2-гидрокси-2-метилпропанамида;
N-(2-((1-метил-5-(трифторметил)-1H-бензо[d]имидазол-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((1-метил-5-(трифторметил)-1H-бензо[d]имидазол-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
2-((5-хлор-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(3-хлор-4-(2,2-дифторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-(3-хлор-4-(2,2-дифторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-метил-2-((1-метил-5-(трифторметил)-1H-бензо[d]имидазол-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((1-метил-5-(трифторметил)-1H-бензо[d]имидазол-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((1-метил-5-(трифторметил)-1H-бензо[d]имидазол-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((1-метил-5-(трифторметил)-1H-бензо[d]имидазол-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((1-метил-5-(трифторметил)-1H-бензо[d]имидазол-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(4-(2,2-дифторэтокси)-3-метилбензил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-(4-(2,2-дифторэтокси)-3-метилбензил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-(4-(2,2-дифторэтокси)-3-метилбензил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-гидрокси-2-метилпропанамида;
2-гидрокси-2-метил-N-(2-(3-метил-4-(2,2,2-трифторэтокси)бензил)-2H-пиразоло[4,3-c]пиримидин-4-ил)пропанамида;
2-гидрокси-2-метил-N-(2-(3-метил-4-(трифторметокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
2-гидрокси-2-метил-N-(2-(2-(4-(трифторметил)фенокси)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
N-(2-((6-(4-хлор-1H-пиразол-1-ил)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-гидрокси-2-метилпропанамида;
2-(4-(2,2-дифторэтокси)-3-метилбензил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторэтокси)-3-метилбензил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-хлор-6-(2,2-дифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((5-хлор-6-(2,2-дифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(2-пропионамидоэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-изобутирамидоэтил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(циклопропанкарбоксамидо)этил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
этил (2-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамидо)этил)карбамата;
N-(2-бензамидоэтил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(2-гидрокси-2-метилпропанамидо)этил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(2-(N-метилацетамидо)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-бутирамидоэтил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(циклобутанкарбоксамидо)этил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(циклогексанкарбоксамидо)этил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(3-этилуреидо)этил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((5-хлор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((6-(циклопропилметокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-(3-метил-4-(трифторметокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-(3-метил-4-(2,2,2-трифторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-(4-(2,2-дифторэтокси)-3-метилбензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((5-хлор-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((1-метил-5-(трифторметокси)-1H-индол-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-гидрокси-2-метил-N-(2-((4-метил-5-(3,3,3-трифторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(2-(пиколинамидо)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(2-(никотинамидо)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(изоникотинамидо)этил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(1-гидроксициклогексанкарбоксамидо)этил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-(3-хлор-4-(2,2,2-трифторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((4-метил-5-(2,2,3,3-тетрафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
2-гидрокси-2-метил-N-(2-((4-метил-5-(2,2,3,3-тетрафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
N-(2-((5-хлор-6-(циклопропилметокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-хлор-6-(циклопропилметокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((5-хлор-6-(циклопропилметокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-гидрокси-2-метилпропанамида;
N-метил-2-((4-метил-5-(2,2,3,3-тетрафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((4-метил-5-(2,2,3,3-тетрафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((4-метил-5-(2,2,3,3-тетрафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((4-метил-5-(2,2,3,3-тетрафторпропокси)пиридин-2-ил)метил)-2H-пирaзоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((4-метил-5-(2,2,3,3-тетрафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((4-метил-5-(2,2,3,3-тетрафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((2-метил-6-(2,2,2-трифторэтокси)пиридин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-(2-(4-(трифторметил)фенокси)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((6-(4-хлор-1H-пиразол-1-ил)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((1-(2,2,2-трифторэтокси)изохинолин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-(4-(1,1,2,2-тетрафторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((2-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((6-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
2-((5-хлор-6-(циклопропилметокси)пиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(циклопропилметокси)пиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((5-хлор-6-(циклопропилметокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(циклопропилметокси)пиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(циклопропилметокси)пиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(циклопропилметокси)пиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((6-((4-фторбензил)окси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((6-((4-фторбензил)окси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((6-((4-фторбензил)окси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-гидрокси-2-метилпропанамида;
2-((6-((4-фторбензил)окси)-5-метилпиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((6-((4-фторбензил)окси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((6-((4-фторбензил)окси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-((4-фторбензил)окси)-5-метилпиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-((4-фторбензил)окси)-5-метилпиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-((4-фторбензил)окси)-5-метилпиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((6-циклобутокси-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((6-циклобутокси-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((6-циклобутокси-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-гидрокси-2-метилпропанамида;
N-(2-((4-метил-5-(2,2,3,3-тетрафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
2-((6-циклобутокси-5-метилпиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-циклобутокси-5-метилпиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((6-циклобутокси-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-циклобутокси-5-метилпиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-циклобутокси-5-метилпиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-циклобутокси-5-метилпиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-(циклопропилметокси)-4-метилпиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-(циклопропилметокси)-4-метилпиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((5-(циклопропилметокси)-4-метилпиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)2-гидрокси-2-метилпропанамида;
2-((5-(циклопропилметокси)-4-метилпиридин-2-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(циклопропилметокси)-4-метилпиридин-2-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((5-(циклопропилметокси)-4-метилпиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(циклопропилметокси)-4-метилпиридин-2-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(циклопропилметокси)-4-метилпиридин-2-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(циклопропилметокси)-4-метилпиридин-2-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-(2,2-дифторпропокси)-4-метилпиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-(2,2-дифторпропокси)-4-метилпиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
2-((5-(2,2-дифторпропокси)-4-метилпиридин-2-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(2,2-дифторпропокси)-4-метилпиридин-2-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((5-(2,2-дифторпропокси)-4-метилпиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(2,2-дифторпропокси)-4-метилпиридин-2-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(2,2-дифторпропокси)-4-метилпиридин-2-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(2,2-дифторпропокси)-4-метилпиридин-2-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-(2,2-дифторпропокси)-4-метилпиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-гидрокси-2-метилпропанамида;
(R)-2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-N-(1-гидроксипропан-2-ил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-N-(2,3-дигидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-N-(2,3-дигидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-цианоэтил)-2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(4-(2,2-дифторпропокси)-3-метилбензил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-(4-(2,2-дифторпропокси)-3-метилбензил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-(4-(2,2-дифторпропокси)-3-метилбензил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-гидрокси-2-метилпропанамида;
2-(4-(2,2-дифторпропокси)-3-метилбензил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторпропокси)-3-метилбензил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-(4-(2,2-дифторпропокси)-3-метилбензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторпропокси)-3-метилбензил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторпропокси)-3-метилбензил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторпропокси)-3-метилбензил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)оксазол-5-карбоксамида;
2-гидрокси-2-метил-N-(2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
(S)-2-(4-(2,2-дифторэтокси)-3-метилбензил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-2-(4-(2,2-дифторэтокси)-3-метилбензил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(1-(4-(2,2-дифторэтокси)-3-метилфенил)этил)-N-((R)-2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-2-(4-(2,2-дифторэтокси)-3,5-диметилбензил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-2-(3-(2,2-дифторэтокси)-4-метилбензил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(1-(4-(2,2-дифторпропокси)-3-метилфенил)этил)-N-((R)-2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(1-(4-(2,2-дифторэтокси)-3-метилфенил)этил)-N-((R)-2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-2-(4-(2,2-дифторпропокси)-3-метилбензил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-2-(4-(2,2-дифторпропокси)-3-метилбензил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(1-(4-(2,2-дифторэтокси)-3-метилфенил)этил)-N-((S)-2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-2-(4-(2,2-дифторэтокси)-3,5-диметилбензил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-2-(3-(2,2-дифторэтокси)-4-метилбензил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(1-(4-(2,2-дифторпропокси)-3-метилфенил)этил)-N-((S)-2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(1-(4-(2,2-дифторэтокси)-3-метилфенил)этил)-N-((S)-2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-2-(1-(4-(2,2-дифторэтокси)-3-метилфенил)этил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторэтокси)-3,5-диметилбензил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(3-(2,2-дифторэтокси)-4-метилбензил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(1-(4-(2,2-дифторпропокси)-3-метилфенил)этил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(1-(4-(2,2-дифторэтокси)-3-метилфенил)этил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(1-(4-(2,2-дифторэтокси)-3-метилфенил)этил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторэтокси)-3,5-диметилбензил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(3-(2,2-дифторэтокси)-4-метилбензил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(1-(4-(2,2-дифторпропокси)-3-метилфенил)этил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(1-(4-(2,2-дифторэтокси)-3-метилфенил)этил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторпропокси)-3-метилбензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(дифторметокси)-3-метилбензил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(дифторметокси)-3-метилбензил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-(4-(дифторметокси)-3-метилбензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(дифторметокси)-3-метилбензил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(дифторметокси)-3-метилбензил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-2-(4-(дифторметокси)-3-метилбензил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-2-(4-(дифторметокси)-3-метилбензил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
и
2-(4-(дифторметокси)-3-метилбензил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
или его фармацевтически приемлемая соль.
8. Соединение по п. 7, которое выбрано из:
N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
2-гидрокси-2-метил-N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
N-(2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-хлор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)ацетамида;
N-метил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)ацетамида;
N-(2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)тетрагидро-2H-пиран-4-карбоксамида;
N-(2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пиваламида;
N-этил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-метоксиэтил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-пропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(диметиламино)этил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-гидрокси-2-метил-N-(6-метил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
2-гидрокси-2-метил-N-(2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
N-изопропил-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-метил-6-(2,2,2-трифторэтокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-метил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-N-(2-гидроксипропил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(2-гидроксипропил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(2,3-дигидроксипропил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-метил-2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-цианоэтил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-цианоэтил)-2-((6-(2,2-дифторэтокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-этил-2-((5-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(2-гидроксиэтокси)этил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
2-((5-хлор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2-дифторэтокси)пиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2-дифторэтокси)пиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-N-(2,3-дигидроксипропил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((6-(2,2,3,3,3-пентафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(4-гидроксибутил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-(3-метил-4-(2,2,2-трифторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-ацетамидопропил)-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(3-(метилсульфонамидо)пропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторэтокси)-3-метилбензил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторэтокси)-3-метилбензил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((2-метил-6-(2,2,2-трифторэтокси)пиридин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(3-гидроксипропил)-2-(3-метил-4-(2,2,2-трифторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-((2-метил-6-(2,2,2-трифторэтокси)пиридин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((2-метил-6-(2,2,2-трифторэтокси)пиридин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((2-метил-6-(2,2,2-трифторэтокси)пиридин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((2-метил-6-(2,2,2-трифторэтокси)пиридин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((2-метил-6-(2,2,2-трифторэтокси)пиридин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(2-гидроксипропил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-N-(2-гидроксипропил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(2,3-дигидроксипропил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-N-(2,3-дигидроксипропил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((1-(5-(трифторметил)пиридин-2-ил)-1H-пиразол-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((1-(5-(трифторметил)пиридин-2-ил)-1H-пиразол-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(2-гидроксипропил)-2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(1-гидроксипропан-2-ил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2Hпиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-цианоэтил)-2-((4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-цианоэтил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((5-метил-6-(2-(2,2,2-трифторэтокси)этокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((2-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((2-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((2-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((2-метокси-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-(2-(4-(трифторметил)фенокси)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-(2-(4-(трифторметил)фенокси)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((6-метил-5-(2,2,2-трифторэтокси)пиразин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-гидрокси-2-метилпропанамида;
2-(2-((3-хлор-5-(трифторметил)пиридин-2-ил)окси)этил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-с]пиридин-4-карбоксамида;
2-((5-циклопропил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-циклопропил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-циклопропил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((6-метил-5-(2,2,2-трифторэтокси)пиразин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((6-метил-5-(2,2,2-трифторэтокси)пиразин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(4-хлор-1H-пиразол-1-ил)-5-метилпиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(4-хлор-1H-пиразол-1-ил)-5-метилпиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(4-хлор-1H-пиразол-1-ил)-5-метилпиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(4-хлор-1H-пиразол-1-ил)-5-метилпиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(1-(5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((6-(циклопропилметокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-гидрокси-2-метилпропанамида;
N,6-диметил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-6-метил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((5-метил-6-((2,2,2-трифторэтил)амино)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((5-метил-6-((2,2,2-трифторэтил)амино)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(циклопропилметокси)-5-метилпиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(циклопропилметокси)-5-метилпиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(циклопропилметокси)-5-метилпиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(циклопропилметокси)-5-метилпиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(циклопропилметокси)-5-метилпиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-(3-метил-4-(трифторметокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-(3-метил-4-(трифторметокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-(4-хлор-1H-пиразол-1-ил)-5-метилпиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((6-(4-фторфенокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-6-метил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-6-метил-2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-метил-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-N-(3-(метилсульфонил)пропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-((1-(2,2,2-трифторэтокси)изохинолин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((1-(2,2,2-трифторэтокси)изохинолин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((1-(2,2,2-трифторэтокси)изохинолин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((1-(2,2,2-трифторэтокси)изохинолин-4-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(3-хлор-4-(2,2-дифторэтокси)бензил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-метил-6-((2,2,2-трифторэтокси)метил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
2-((5-метил-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-(3-(метилсульфонил)пропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((1-метил-5-(трифторметокси)-1H-индол-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-(2,2-дифторэтокси)-4-метилпиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-((5-(2,2-дифторэтокси)-4-метилпиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-гидроксиэтил)-2-(3-(трифторметокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-(2,2,3,3,3-пентафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-этил-2-((5-(2,2,3,3,3-пентафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(2,2-дифторэтокси)-4-метилпиридин-2-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(2,2-дифторэтокси)-4-метилпиридин-2-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(2,2-дифторэтокси)-4-метилпиридин-2-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((5-(2,2,3,3-тетрафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-гидрокси-2-метилпропанамида;
N-(2-((5-(2,2,3,3-тетрафторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
N-(2-ацетамидоэтил)-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(2-гидроксипропил)-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2Hпиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-N-(2,3-дигидроксипропил)-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-(3-(трифторметил)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-N-(2-гидроксипропил)-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-N-(2,3-дигидроксипропил)-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(3-хлор-4-(2,2-дифторэтокси)бензил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(3-хлор-4-(2,2-дифторэтокси)бензил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-(4-(1,1,2,2-тетрафторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2,2-трифторэтокси)пиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-((S)-2-гидроксипропил)-2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-((5-метил-6-(3,3,3-трифторпропил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((5-метил-6-(3,3,3-трифторпропил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((5-метил-6-(3,3,3-трифторпропил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((5-метил-6-(3,3,3-трифторпропил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((5-метил-6-(3,3,3-трифторпропил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-((4-метил-5-(3,3,3-трифторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((4-метил-5-(3,3,3-трифторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-гидроксиэтил)-2-((4-метил-5-(3,3,3-трифторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((4-метил-5-(3,3,3-трифторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-N-(1-гидроксипропан-2-ил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((5-хлор-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
2-гидрокси-2-метил-N-(2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
N-метил-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((4-метил-5-(3,3,3-трифторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
N-(2-((5-метил-6-(3,3,3-трифторпропил)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)циклопропанкарбоксамида;
2-((5-хлор-6-(2,2-дифторпропокси)пиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2-дифторпропокси)пиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2-дифторпропокси)пиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(2,2-дифторпропокси)пиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-изопропил-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-с]пиридин-4-карбоксамида;
(S)-N-(1-гидроксипропан-2-ил)-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(3,3,3-трифторпропокси)пиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((1-метил-5-(трифторметил)-1H-бензо[d]имидазол-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((1-метил-5-(трифторметил)-1H-бензо[d]имидазол-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-гидрокси-2-метил-N-(2-(3-метил-4-(2,2,2-трифторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
2-гидрокси-2-метил-N-(2-(3-метил-4-(трифторметокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
2-(4-(2,2-дифторэтокси)-3-метилбензил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторэтокси)-3-метилбензил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((6-(циклопропилметокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-(3-метил-4-(2,2,2-трифторэтокси)бензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-(4-(2,2-дифторэтокси)-3-метилбензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-гидрокси-2-метил-N-(2-((4-метил-5-(3,3,3-трифторпропокси)пиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)пропанамида;
N-этил-2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-(1-(4-метил-5-(2,2,2-трифторэтокси)пиридин-2-ил)этил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
2-((5-хлор-6-(циклопропилметокси)пиридин-3-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(циклопропилметокси)пиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(циклопропилметокси)пиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(циклопропилметокси)пиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-хлор-6-(циклопропилметокси)пиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-((4-фторбензил)окси)-5-метилпиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((6-циклобутокси-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-гидрокси-2-метилпропанамида;
2-((6-циклобутокси-5-метилпиридин-3-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-ацетамидоэтил)-2-((6-циклобутокси-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-циклобутокси-5-метилпиридин-3-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-циклобутокси-5-метилпиридин-3-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((6-циклобутокси-5-метилпиридин-3-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-(циклопропилметокси)-4-метилпиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)-2-гидрокси-2-метилпропанамида;
2-((5-(циклопропилметокси)-4-метилпиридин-2-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(циклопропилметокси)-4-метилпиридин-2-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(циклопропилметокси)-4-метилпиридин-2-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(циклопропилметокси)-4-метилпиридин-2-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-метил-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-этил-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(3-гидроксипропил)-2-((5-метил-6-(2,2,3,3-тетрафторпропокси)пиридазин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-((5-(2,2-дифторпропокси)-4-метилпиридин-2-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-ил)изобутирамида;
2-((5-(2,2-дифторпропокси)-4-метилпиридин-2-ил)метил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(2,2-дифторпропокси)-4-метилпиридин-2-ил)метил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(2,2-дифторпропокси)-4-метилпиридин-2-ил)метил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(2,2-дифторпропокси)-4-метилпиридин-2-ил)метил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-((5-(2,2-дифторпропокси)-4-метилпиридин-2-ил)метил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
N-(2-цианоэтил)-2-((6-(2,2-дифторпропокси)-5-метилпиридин-3-ил)метил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторпропокси)-3-метилбензил)-N-метил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторпропокси)-3-метилбензил)-N-этил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторпропокси)-3-метилбензил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторпропокси)-3-метилбензил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторпропокси)-3-метилбензил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-2-(4-(2,2-дифторэтокси)-3-метилбензил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(1-(4-(2,2-дифторэтокси)-3-метилфенил)этил)-N-((R)-2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-2-(4-(2,2-дифторэтокси)-3,5-диметилбензил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(1-(4-(2,2-дифторпропокси)-3-метилфенил)этил)-N-((R)-2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-2-(4-(2,2-дифторпропокси)-3-метилбензил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-2-(4-(2,2-дифторпропокси)-3-метилбензил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(1-(4-(2,2-дифторэтокси)-3-метилфенил)этил)-N-((S)-2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(S)-2-(4-(2,2-дифторэтокси)-3,5-диметилбензил)-N-(2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(1-(4-(2,2-дифторпропокси)-3-метилфенил)этил)-N-((S)-2-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
(R)-2-(1-(4-(2,2-дифторэтокси)-3-метилфенил)этил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторэтокси)-3,5-диметилбензил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(1-(4-(2,2-дифторпропокси)-3-метилфенил)этил)-N-(2-гидроксиэтил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(1-(4-(2,2-дифторэтокси)-3-метилфенил)этил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторэтокси)-3,5-диметилбензил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(1-(4-(2,2-дифторпропокси)-3-метилфенил)этил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(2,2-дифторпропокси)-3-метилбензил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
2-(4-(дифторметокси)-3-метилбензил)-N-(3-гидроксипропил)-2H-пиразоло[4,3-c]пиридин-4-карбоксамида; и
2-(4-(дифторметокси)-3-метилбензил)-N-изопропил-2H-пиразоло[4,3-c]пиридин-4-карбоксамида;
или его фармацевтически приемлемая соль.
9. Фармацевтическая композиция, блокирующая активность TTX-S, содержащая соединение или его фармацевтически приемлемую соль по любому из пп. 1-8, и фармацевтически приемлемый носитель.
10. Способ лечения заболевания или расстройства, в которое вовлечены блокаторы каналов TTX-S, у животного, включая человека, включающий введение нуждающемуся в лечении млекопитающему терапевтически эффективного количества соединения или его фармацевтически приемлемой соли по любому из пп. 1-8.
11. Способ по п. 10, где указанное заболевание или состояние выбрано из группы, состоящей из: боли, острой боли, хронической боли, невропатической боли, воспалительной боли, висцеральной боли, ноцицептивной боли, рассеянного склероза, нейродегенеративного расстройства, синдрома раздраженного кишечника, остеоартрита, ревматоидного артрита, невропатологических нарушений, функциональных расстройств кишечника, воспалительного заболевания кишечника, боли, связанной с дисменореей, боли в области таза, цистита, панкреатита, мигрени, кластерной и головной боли, диабетической нейропатии, периферической невропатической боли, пояснично-крестцового радикулита, фибромиалгии, болезни Крона, эпилепсии или эпилептического состояния, биполярной депрессии, тахиаритмии, нарушения настроения, биполярного расстройства, психических расстройств, таких как тревожность и депрессия, миотонии, аритмии, двигательных расстройств, нейроэндокринных нарушений, атаксии, недержания мочи, висцеральной боли, невралгии тройничного нерва, герпетической невралгии, общей невралгии, постгерпетической невралгии, радикулярной боли, ишиалгии, боли в спине, боли в шее или голове, тяжелой или неустранимой боли, «прорывной» боли, послеоперационной боли, инсульта, боли при раке, эпилепсии, каузалгии и химио-индуцированной боли; и их комбинаций.
12. Применение соединения по любому из пп. 1-8 или его фармацевтически приемлемой соли, или композиции для получения лекарственного средства для лечения заболевания или расстройства, в котором участвуют блокаторы каналов TTX-S.
13. Применение по п. 12, где указанное заболевание или состояние выбрано из группы, состоящей из: боли, острой боли, хронической боли, невропатической боли, воспалительной боли, висцеральной боли, ноцицептивной боли, рассеянного склероза, нейродегенеративного расстройства, синдрома раздраженного кишечника, остеоартрита, ревматоидного артрита, невропатологических нарушений, функциональных расстройств кишечника, воспалительного заболевания кишечника, боли, связанной с дисменореей, боли в области таза, цистита, панкреатита, мигрени, кластерной и головной боли, диабетической нейропатии, периферической невропатической боли, пояснично-крестцового радикулита, фибромиалгии, болезни Крона, эпилепсии или эпилептического состояния, биполярной депрессии, тахиаритмии, нарушения настроения, биполярного расстройства, психических расстройств, таких как тревожность и депрессия, миотонии, аритмии, двигательных расстройств, нейроэндокринных нарушений, атаксии, недержания мочи, висцеральной боли, невралгии тройничного нерва, герпетической невралгии, общей невралгии, постгерпетической невралгии, радикулярной боли, ишиалгии, боли в спине, боли в шее или голове, тяжелой или неустранимой боли, «прорывной» боли, послеоперационной боли, инсульта, боли при раке, эпилепсии, каузалгии и химио-индуцированной боли; и их комбинаций.
14. Соединение по любому из пп. 1-8 или фармацевтически приемлемая соль для применения в лечении заболевания или состояния, в котором участвуют блокаторы каналов TTX-S.
15. Способ получения фармацевтической композиции, блокирующей активность TTX-S, включающий смешение соединения или его фармацевтически приемлемой соли по любому из пп. 1-8, и фармацевтически приемлемого носителя или вспомогательного вещества.
| Колосоуборка | 1923 |
|
SU2009A1 |
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| J.-D BOURZAT ET AL, SUR UNE NOUVELLE METODE DE SYNTHESE PYRAZOLO [4,3-c] PYRIDINES, TETRAHEDRON, vol | |||
| Солесос | 1922 |
|
SU29A1 |
| Кинематографический аппарат | 1918 |
|
SU441A1 |
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| Картотека | 1929 |
|
SU15952A1 |
Авторы
Даты
2018-04-25—Публикация
2013-10-31—Подача