Права правительства
[1] Правительство Соединенных Штатов обладает правами на настоящее изобретение согласно контракту № DE-AC36-08GO28308 между Министерством энергетики США и ООО «Альянс по устойчивой энергетике», которое руководит и управляет Национальной лабораторией возобновляемой энергии.
[2] Настоящее изобретение было осуществлено при поддержке правительства согласно соглашению по оказанию помощи Министерства энергетики США № DE-AR0000350, № CFDA (Catalog of Federal Domestic Assistance, каталога федеральной поддержки) 81,135. Правительство обладает определенными правами на настоящее изобретение.
Область техники
[3] Настоящее изобретение относится к способу получения по меньшей мере одного продукта из сырья, содержащего метан. Данный способ включает подачу газообразного субстрата, содержащего СН4 и O2, в биореактор, который содержит культуру по меньшей мере одного метанотрофного микроорганизма в жидкой питательной среде, для получения по меньшей мере одного продукта, такого как липиды и аминокислоты.
Уровень техники
[4] Глобальный энергетический кризис вызвал повышенный интерес к альтернативным подходам для производства топлива. Различные виды биотоплива для нужд транспорта являются привлекательной заменой бензину и быстро выходят на топливные рынки в виде слабоконцентрированных смесей. Производство биотоплива на основе биомассы стало основным подходом к увеличению производства альтернативной энергии и сокращению выбросов парниковых газов. Производство биотоплива из биомассы обеспечивает энергетическую независимость. Также было показано, что производство биотоплива усиливает как развитие сельскохозяйственных районов, так и устойчивое экономическое развитие.
[5] В традиционных жидких видах биотоплива применяют углеводное сырье, такое как крахмал, тростниковый сахар, кукуруза, рапс, соя, пальмовое и растительные масла. Сырье первого поколения характеризуется множеством значительных проблем. На стоимость данного углеводного сырья влияет его ценность в качестве пищи для человека или корма для животных, тогда как культивирование сельскохозяйственных культур, источников крахмала или сахарозы, для получения этанола является экономически нецелесообразным во всех регионах. Постоянное использование данного сырья в качестве источника для получения различных видов биотоплива неизбежно окажет большую нагрузку на пахотные земли и источники воды. Вследствие этого интерес представляет разработка технологий для преобразования менее дорогостоящих и/или более многочисленных углеродных ресурсов в топливо.
[6] Виды биотоплива второго поколения получают из целлюлозы и водорослей. Водоросли были выбраны для получения липидов благодаря высоким скоростям роста и способности водорослей потреблять диоксид углерода и образовывать кислород.
[7] Также было продемонстрировано, что различные виды биотоплива можно получить в результате микробиологической конверсии синтетического газа, содержащего монооксид углерода (синтез-газа). Ацетогенные бактерии, такие как бактерии родов Acetobacterium, Moorella, Clostridium, Ruminococcus, Acetobacterium, Eubacterium, Butyribacterium, Oxobacter, Methanosarcina, Methanosarcina и Desulfotomaculum, можно использовать для получения уксусной кислоты, ацетата и других продуктов, таких как этанол, посредством анаэробной ферментации монооксида углерода и/или водорода и диоксида углерода. Данные бактерии преобразуют синтез-газ в продукты посредством метаболического пути Вуда-Льюнгдаля, ключевым ферментом которого является ацетил-Ко-А-синтаза. Например, различные штаммы Clostridium Ijungdahlii, которые образуют ацетат и этанол из синтез-газа, описаны в публикациях WO 00/68407, ЕР 117309, патентах США №№5,173,429, 5,593,886 и 6,368,819, публикациях WO 98/00558 и WO 02/08438.
[8] Областью, в которой наблюдалась увеличенная активность, является микробиологический синтез липидов, включающий исходные материалы, необходимые для получения биотоплива. Многочисленные исследования продемонстрировали способность накапливать липиды посредством применения жировых дрожжей и различных субстратов, таких как промышленный глицерол, уксусная кислота, канализационный ил, фильтрат сыворотки, меласса сахарного тростника и гидролизат стеблей риса. Данные технологии получения биотоплива второго поколения также столкнулись с проблемами в связи с высокими производственными затратами и затратами, связанными с транспортированием и хранением сырья.
[9] Метан представляет собой второй наиболее распространенный парниковый газ, выделяемый в Соединенных Штатах в результате деятельности человека. Хотя период жизни метана значительно короче, чем диоксида углерода, метан более эффективно улавливает радиационное излучение, чем диоксид углерода, и вследствие этого сравнительный вклад метана в изменение климата в течение 20 лет более чем в 70 раз превышает вклад диоксида углерода. Системы на основе природного газа и нефти представляют собой наибольшие промышленные источники метана, за которыми следует образование метана в процессе сельского хозяйства и свалки отходов. Современные стратегии утилизации метана/сокращения выбросов сфокусировались на применении метана из природного газа и метана, который образуется в ходе множества промышленных процессов, в качестве рентабельного источника топлива.
[10] В природе известны различные метанотрофные бактерии, которые в аэробных условиях способны объединять кислород и метан с образованием формальдегида благодаря ферментам метанмонооксигеназе и метанолдегидрогеназе. Затем формальдегид включается в органические соединения посредством пути RuMP (ribulose monophosphate pathway, путь монофосфата рибулозы) (метанотрофы I типа) или пути серина (метанотрофы II типа). Были определены одиннадцать родов метанотрофов, а именно Methylococcus, Methylomonas, Methylomicrobium, Methylobacter, Methylocaldum, Methylovulum, Methylomarinum, Methylomahnovum, Methylothermus, Methylocystis и Methylosinus.
[11] На сегодняшний день коммерческое применение метанотрофных бактерий ограничено. В публикации Semrau, J.D. (2011) обсуждается применение метанотрофов для биологической очистки загрязненных территорий, например, разрушения хлорированных углеводородов, таких как трихлорэтилен. В публикации WO 09/154683 описано применение метанотрофов в топливных элементах, в которых метан окисляется микроорганизмами в топливном элементе для получения электронов. В публикации патента США №2005/0221465 и в патенте США №7,799,550 описано применение гидролизированной гомогенизированной биомассы метанотрофных бактерий в качестве питательного сырья для ферментации. В патенте ЕР 1641475 описано применение липидов из метанотрофных бактерий для восстановления холестерола. В публикации патента США №2003/0138878 и в патенте EP 1320579 В1 описано применение биомассы метанотрофных бактерий в качестве источника белка. В публикации патента США №2006/0057726 описан набор генетических инструментов для положительной селекции хромосомных мутаций С1-метаболизирующих бактерий посредством гомологичной рекомбинации. В обзоре Kalyuzhnaya et al. (2011) описаны биотехнологические аспекты метанотрофных бактерий и изложены перспективы использования усваивающих метан микроорганизмов для получения эктоина. В исследовании, проведенном Shoda et al. (1975), приведены оптимальные парциальные давления кислорода и метана для культивирования усваивающих метан бактерий в периодической культуре.
[12] В данной области техники сохраняется потребность в получении ценных продуктов, таких как различные виды биотоплива, из газообразных субстратов, содержащих метан. Целью настоящего изобретения является обеспечение новых процессов для получения полезных продуктов, таких как липиды и аминокислоты, из газообразных субстратов, содержащих метан, и предоставление общественности новых способов уменьшения выбросов метана в атмосферу или по меньшей мере предоставление общественности полезного выбора.
Краткое описание изобретения
[13] В настоящем изобретении предложен ответ на потребность, существующую в данной области техники. Согласно первому аспекту в настоящем изобретении предложен способ получения по меньшей мере одного продукта посредством микробиологической конверсии газообразного субстрата, включающий:
(а) обеспечение газообразного субстрата, содержащего СН4 и O2, в биореактор, который содержит культуру по меньшей мере одного метанотрофного микроорганизма в жидкой питательной среде; и
(b) микробиологическое преобразование газообразного субстрата в условиях ферментации в по меньшей мере один продукт в биомассе клеток, который выбран из группы, включающей липиды, белки, аминокислоты и комбинации указанных соединений и выделяемые жирные кислоты.
[14] Согласно конкретным вариантам реализации первого аспекта настоящего изобретения в результате осуществления данного способа образуются липиды или аминокислоты или комбинации указанных соединений. Согласно конкретным вариантам реализации настоящего изобретения липиды могут включать, но не ограничены указанными, жирные кислоты, гликолипиды, сфинголипиды, сахаролипиды, поликетиды, стероидные липиды, гопаноиды, фосфолипиды и пренольные липиды или комбинации указанных липидов. Согласно конкретным вариантам реализации настоящего изобретения аминокислоты могут включать, но не ограничены ими, пролин, 5-оксопролин, аланин, аспартат, глутамин и глутамат или комбинации указанных аминокислот.
[15] Согласно конкретным вариантам реализации настоящего изобретения липиды, полученные в результате данного способа, можно преобразовать в по меньшей мере одно химическое соединение, топливо или компонент топлива. Например, липиды можно преобразовать в соединения, которые выбраны из группы, включающей возобновляемое дизельное топливо, биодизельное топливо, дизельное топливо, компоненты дизельного топлива, сложные метиловые эфиры жирных кислот (FAME, fatty acid methyl esters) и сложные этиловые эфиры жирных кислот (FAEE, fatty acid ethyl esters), посредством способов, хорошо известных в данной области техники.
[16] Согласно второму аспекту в настоящем изобретении предложен процесс получения по меньшей мере одного продукта посредством микробиологической конверсии газообразного субстрата, включающий:
(a) обеспечение газообразного субстрата, содержащего СН4 и O2, в биореактор, который содержит жидкую питательную среду и культуру по меньшей мере одного метанотрофного микроорганизма;
(b) микробиологическое преобразование газообразного субстрата для получения по меньшей мере одного продукта в биомассе клеток микроорганизма; и
(c) экстракцию по меньшей мере одного продукта из биомассы клеток микроорганизма.
[17] Согласно конкретным вариантам реализации настоящего изобретения жидкую питательную среду подают в реактор непрерывно. Согласно конкретным вариантам реализации настоящего изобретения жидкую питательную среду насыщают O2 перед подачей в биореактор. Согласно конкретным вариантам реализации настоящего изобретения в жидкой питательной среде повышают давление, и среду насыщают O2 перед подачей в биореактор.
[18] Согласно конкретным вариантам реализации настоящего изобретения по меньшей мере часть не вступившего в реакцию газообразного субстрата и/или любого газа, образованного микроорганизмом, покидает биореактор через газоотвод. Согласно конкретным вариантам реализации настоящего изобретения по меньшей мере часть выходящего газа поступает обратно в биореактор для последующего преобразования. Согласно конкретным вариантам реализации настоящего изобретения по меньшей мере часть выходящего газа используется в качестве топлива.
[19] Согласно конкретным вариантам реализации настоящего изобретения культура по меньшей мере одного микроорганизма суспендирована в жидкой питательной среде. Согласно конкретным вариантам реализации настоящего изобретения значение pH жидкой питательной среды поддерживают в диапазоне от приблизительно 6 до приблизительно 11. Согласно предпочтительным вариантам реализации настоящего изобретения значение pH жидкой питательной среды поддерживают в диапазоне от приблизительно 8 до приблизительно 9,5. Согласно конкретным вариантам реализации настоящего изобретения температуру жидкой питательной среды поддерживают в диапазоне от приблизительно 5 до приблизительно 60°С. Согласно предпочтительным вариантам реализации настоящего изобретения температуру жидкой питательной среды поддерживают в диапазоне от приблизительно 25 до приблизительно 35°С.
[20] Согласно конкретным вариантам реализации настоящего изобретения один или несколько микроорганизмов представляют собой метанотрофные бактерии, которые выбраны из группы, включающей Methylococcus, Methylomonas, Methylomicrobium, Methylobacter, Methylosarcina, Methylocaldum, Methylomarinum, Methylomarinovum, Methylothermus, Methylovulum, Methylocystis и Methylosinus. Согласно конкретным вариантам реализации настоящего изобретения метанотрофную бактерию выбирают из Methylococcus capsulatus, Methylomonas methanica, Methylomonas sp., Methylosinus trichosporium, Methylobacter marinus, Methylobacter luteus, Methylomicrobium alcaliphilum и Methylomicrobium buryatense. Согласно предпочтительным вариантам реализации настоящего изобретения метанотрофная бактерия представляет собой Methylomicrobium buryatense.
[21] Согласно конкретным вариантам реализации настоящего изобретения метанотрофная бактерия представляет собой штамм, существующий в природе. Согласно альтернативным вариантам реализации настоящего изобретения метанотрофная бактерия представляет собой штамм, полученный генно-инженерным способом. Согласно конкретным вариантам реализации настоящего изобретения метанотрофная бактерия представляет собой выбранный штамм. Согласно конкретным вариантам реализации настоящего изобретения выбранный метанотрофный штамм представляет собой штамм 5GB1 Methylomicrobium.
[22] Согласно конкретным вариантам реализации настоящего изобретения данный процесс включает этап экстракции по меньшей мере одного продукта из клеточной мембраны по меньшей мере одного микроорганизма. Согласно конкретным вариантам реализации настоящего изобретения этап экстракции включает процедуру влажной экстракции. Согласно конкретным вариантам реализации настоящего изобретения этап экстракции происходит в реакторе и отделен от этапа конверсии. Согласно конкретным вариантам реализации настоящего изобретения поток продукта, содержащий по меньшей мере один продукт и/или по меньшей мере один микроорганизм, поступает из реактора в модуль для экстракции.
[23] Согласно конкретным вариантам реализации настоящего изобретения этап экстракции включает этап разрушения клеток с применением гомогенизации под высоким давлением, химической или физической предварительной обработки, такой как (но не ограничиваясь ими) предварительная обработка биомассы кислотой или щелочью и нагревание до температур, превышающих температуры денатурации белка (от приблизительно 50°С до приблизительно 200°С, предпочтительно от приблизительно 75°С до приблизительно 90°С). Согласно конкретным вариантам реализации настоящего изобретения этап экстракции также включает этап экстракции растворителем. Согласно конкретным вариантам реализации настоящего изобретения на этапе экстракции растворителем поток продукта разделяется на легкую фазу, содержащую один или несколько продуктов и растворитель, и тяжелую фазу, содержащую отработанную биомассу.
[24] Согласно конкретным вариантам реализации настоящего изобретения растворитель представляет собой неполярный алкан или короткоцепочечный спирт или любую комбинацию указанных соединений. Согласно предпочтительным вариантам реализации настоящего изобретения растворитель представляет собой гексан или альтернативные короткоцепочечные алканы (например, пентан, гептан) или короткоцепочечные спирты, например, бутанол, изобутанол, трет-бутанол, пентанол или любой другой растворитель (или комбинации системы растворителей), совместимый с составом микробиологических липидов. В случае более полярной природы доступных продуктов жизнедеятельности микроорганизмов следует выбрать систему с более полярным растворителем.
[25] Согласно конкретным вариантам реализации настоящего изобретения по меньшей мере один экстрагируемый продукт дополнительно поступает в модуль процессинга продукта. Согласно конкретным вариантам реализации настоящего изобретения по меньшей мере один экстрагируемый продукт преобразуют в возобновляемое дизельное топливо, биодизельное топливо, дизельное топливо, компоненты дизельного топлива, среднецепочечные углеводороды и стероидные и изопреноидные производные, сложные метиловые эфиры жирных кислот (FAME) и сложные этиловые эфиры жирных кислот (FAEE).
[26] Согласно конкретным вариантам реализации настоящего изобретения по меньшей мере часть тяжелой фазы, содержащей отработанную биомассу с этапа экстракции растворителем, поступает в анаэробный ферментер, в котором по меньшей мере часть тяжелой фазы преобразуется в биогаз. По меньшей мере часть биогаза, образованного в анаэробном ферментере, может поступать в биореактор. Согласно альтернативным вариантам реализации настоящего изобретения по меньшей мере часть биогаза, образованного в анаэробном ферментере, поступает на газовую турбину для получения энергии. Энергию, полученную на газовой турбине, можно использовать для снабжения энергией любого этапа способа согласно настоящему изобретению, описанного в настоящей заявке.
[27] Согласно конкретному варианту реализации настоящего изобретения белковую часть клеточной биомассы можно отделить и использовать для получения гранул белка, которые можно применять в качестве белка для корма животных.
[28] Согласно третьему аспекту в настоящем изобретении предложен способ получения по меньшей мере одного продукта посредством микробиологической конверсии газообразного субстрата, включающий:
(a) обеспечение субстрата, содержащего кислород и по меньшей мере одно соединение, которое выбрано из СН4, СН3ОН и их комбинации, в биореактор, который содержит жидкую питательную среду и культуру по меньшей мере одного метанотрофного микроорганизма; и
(b) Микробиологическое преобразование газообразного субстрата в по меньшей мере один продукт, который выбран из липидов и аминокислот, в биомассе клеток микроорганизма; и
(с) Экстракцию по меньшей мере одного продукта из клеточной мембраны микроорганизма.
[29] Согласно конкретным вариантам реализации третьего аспекта настоящего изобретения субстрат содержит СН4, СН3ОН и O2. Согласно альтернативным вариантам реализации настоящего изобретения субстрат по существу содержит СН3ОН и O2. Согласно конкретным вариантам реализации настоящего изобретения субстрат, содержащий СН4, смешивают с СН3ОН перед подачей в биореактор. Согласно альтернативным вариантам реализации настоящего изобретения СН4 преобразуют в СН3ОН перед подачей в биореактор.
[30] Согласно четвертому аспекту в настоящем изобретении предложена система для фиксации углерода, причем указанная система содержит:
(i) реактор, содержащий жидкую питательную среду и культуру по меньшей мере метанотрофного микроорганизма;
(ii) по меньшей мере один подвод газа, спроектированный таким образом, чтобы направлять подачу газообразного субстрата, содержащего СН4 и O2, в реактор; и
(iii) по меньшей мере один газоотвод, спроектированный таким образом, чтобы позволить газу покинуть реактор; и
(iv) по меньшей мере один газоотвод, спроектированный таким образом, чтобы позволить газу покинуть биореактор.
[31] Согласно конкретным вариантам четвертого аспекта настоящего изобретения данную систему используют в способе, описанном в первом, втором и третьем аспектах. Согласно конкретным вариантам реализации настоящего изобретения систему используют в способе микробиологической конверсии субстрата, содержащего кислород и по меньшей мере одно соединение из СН4, СН3ОН, в по меньшей мере один продукт, который выбран из липидов, белков, аминокислот и комбинаций указанных соединений.
[32] Согласно конкретным вариантам реализации настоящего изобретения реактор спроектирован таким образом, чтобы по существу стимулировать рост одного или нескольких микроорганизмов и/или получить один или несколько продуктов. Согласно альтернативным вариантам реализации настоящего изобретения система может содержать первый реактор для роста и второй реактор для синтеза продукта.
[33] Согласно конкретным вариантам реализации настоящего изобретения данная система содержит средства для подачи по меньшей мере части газа, покидающего биореактор, обратно к по меньшей мере одному подводу газа реактора.
[34] Согласно конкретным вариантам реализации настоящего изобретения данная система также содержит зону экстракции для экстракции одного или нескольких продуктов, полученных из биомассы. Согласно конкретным вариантам реализации настоящего изобретения система содержит средства для прохождения потока, содержащего по меньшей мере один продукт и/или по меньшей мере один микроорганизм, из реактора в зону экстракции.
[35] Согласно конкретным вариантам реализации настоящего изобретения зона экстракции содержит несколько блоков экстракции. Согласно конкретным вариантам реализации настоящего изобретения зона экстракции содержит первый, второй, третий и четвертый блоки экстракции. Согласно конкретным вариантам реализации настоящего изобретения первый блок экстракции спроектирован для химической или физической обработки влажной биомассы, например, гомогенизации под высоким давлением, разрушения клеточной мембраны под действием термической обработки и/или под действием кислоты или щелочи. Согласно конкретным вариантам реализации настоящего изобретения второй блок экстракции спроектирован для экстракции растворителем. Согласно конкретным вариантам реализации настоящего изобретения третий блок экстракции спроектирован для разделения продукта/растворителя и отработанной биомассы посредством центрифугирования. Согласно конкретным вариантам реализации настоящего изобретения система содержит средство для прохождения продуктов, растворителя и/или биомассы между блоками экстракции.
[36] Согласно конкретным вариантам реализации настоящего изобретения система также включает зону процессинга продукта. Согласно конкретным вариантам реализации настоящего изобретения зона процессинга продукта содержит блок гидрообработки. Согласно конкретным вариантам реализации настоящего изобретения система содержит средство для подачи по меньшей мере части потока продукта из зоны экстракции в зону процессинга продукта.
[37] Согласно конкретным вариантам реализации настоящего изобретения система также содержит зону анаэробной ферментации. Согласно конкретным вариантам реализации настоящего изобретения система содержит средство для подачи по меньшей мере части отработанной биомассы в зону анаэробной ферментации.
[38] Настоящее изобретение также включает части, элементы и характеристики, указанные или обозначенные в описании настоящей заявки, индивидуально или в совокупности, в любой или во всех комбинациях из двух или более указанных частей, элементов или характеристик, и, если в настоящей заявке указаны конкретные числа, которые имеют известные эквиваленты в данной области, к которой относится изобретение, такие известные эквиваленты считают включенными в настоящую заявку, как если бы такие эквиваленты были указаны в настоящей заявке индивидуально.
Краткое описание чертежей
[39] Ниже настоящее изобретение будет подробно описано со ссылкой на прилагаемые фигуры, где:
[40] На фигуре 1 представлен стехиометрический график, иллюстрирующий диапазон возможной стехиометрии потребления микроорганизмами СН4.
[41] На фигуре 2 представлен стехиометрический график, иллюстрирующий диапазон возможной стехиометрии потребления микроорганизмами СН4 при эксплуатации с воздухом.
[42] На фигуре 3 представлен стехиометрический график, иллюстрирующий диапазон возможной стехиометрии потребления микроорганизмами СН4 в пользу образования липидов при эксплуатации с ограниченным доступом O2.
Подробное описание изобретения
Определения
[43] Если не указано обратное, в настоящей спецификации используются следующие термины, как определено ниже:
[44] Термин «реактор» и/или «биореактор» включает любое устройство для микробиологической конверсии, состоящее из одного или нескольких сосудов и/или колонн или трубопроводов, такое как реактор с иммобилизованными клетками, газлифтный реактор, барботажный колоночный реактор (bubble column reactor, BCR), реактор с циркуляционной петлей, мембранный реактор, такой как мембранный биореактор с системой полых волокон (Hollow Fibre Membrane Bioreactor, HFM BR) или реактор с орошаемым слоем (trickle bed reactor, TBR).
[45] Термин «газообразный субстрат» включает любой газ, содержащий соединение или элемент, используемый микроорганизмом в качестве источника углерода и необязательно источника энергии при микробиологической конверсии. Газообразный субстрат, как правило, будет содержать значительную часть СН4 и O2. Аналогично, термин «субстрат» включает любой газ и/или жидкость, содержащую соединение или элемент, используемый микроорганизмом в качестве источника углерода и необязательно источника энергии при микробиологической конверсии. Примеры жидких субстратов включают метанол.
[46] Термин «биодизельное топливо» относится к полученному из липидов дизельному топливу, состоящему из длинноцепочечных алкиловых эфиров. Биодизельное топливо, как правило, получают в результате химической реакции липидов со спиртом для получения сложных эфиров жирных кислот.
[47] Термин «возобновляемое дизельное топливо» относится к полученному из липидов дизельному топливу, состоящему из длинноцепочечных алкильных соединений, не содержащих кислород или другие гетероатомы, такие как азот или сера. Возобновляемое дизельное топливо, как правило, получают в результате каталитической гидрогенизации, деоксигенации и денитрогенации липидов необязательно с последующим каталитическим крекингом и изомеризацией длинноцепочечных углеводородов до алканов с длиной цепи от 8 до 14 углеродов.
[48] Термин «выходящий газ» включает любой газ, который покидает реактор через один или несколько газоотводов. Выходящий газ будет, как правило, содержать СН4, O2 и CO2.
[49] Термин «жидкая питательная среда» и/или «среда» включает жидкую среду, содержащую питательные вещества, подходящие для микробиологической конверсии с применением одного или нескольких микроорганизмов. Жидкая питательная среда содержит витамины и/или минералы, достаточные для роста используемого микроорганизма или микроорганизмов.
[50] Термин «массоперенос» в настоящей заявке означает перенос газообразных субстратов в жидкую среду, в которой развиваются микроорганизмы.
[51] Термин «влажная экстракция», как правило, относится к процедуре экстракции, при которой продукты непосредственно экстрагируют из микроорганизма без необходимости в удалении воды и сушке.
[52] Как правило, в способах влажной экстракции используют суспензии влажной биомассы, содержащие менее 40% твердых веществ (предпочтительно от 10 до 20% твердых веществ), что позволяет проводить экстракцию в перемешиваемом реакторе периодического действия в присутствии растворителя, при этом обеспечивая максимальную скорость массопереноса растворитель - биомасса для увеличения эффективности экстракции продукта. Фракционирование влажной биомассы с применением химического разрушения клеток известно для водорослей (Czartoski et al., WO 2010/104922, "Algae Biomass Fractionation"). Примеры способов включают способы, описанные Czartoski et al., в которых обработка кислотой предшествует экстракции липидов с последующим процессом экстракции неполярным растворителем. Однако процесс экстракции адаптирован конкретно для водорослей, в особенности для неполярных липидов, и не предполагает использование биомассы бактерий или метанотрофов или экстракцию полярных липидов (полученных из значительной фракции бактериальной мембраны в биомассе микроорганизмов и бактерий). Существующий уровень техники процедур экстракции не включает адаптацию полярности растворителя для экстракции к составу и полярности липидов, которые будут экстрагированы, и такая адаптация является новизной в системах экстракции, описанных в настоящем изобретении.
[53] Термин «легкая фаза» в настоящей заявке означает часть разделенного вещества после процедуры экстракции, которая, главным образом, содержит экстрагированный продукт и растворитель.
[54] Термин «тяжелая фаза» в настоящей заявке означает часть разделенного вещества после процедуры экстракции, которая, главным образом, содержит воду, отработанную биомассу и любой остаток продукта/растворителя.
[55] Термин «анаэробный ферментер» в настоящей заявке относится к реактору, который спроектирован для анаэробной конверсии органических отходов в биогаз. Как правило, реактор будет содержать ацидогенные бактерии, ацетогенные бактерии и/или метанобразующие бактерии. Ацидогенные бактерии используют для конверсии органических полимеров и аминокислот в CO2, Н2, NH3 и органические кислоты. Ацетогенные бактерии преобразуют полученные в результате органические полимеры в уксусную кислоту вместе с дополнительными CO2, Н2 и NH3. Метанобразующие бактерии преобразуют полученную уксусную кислоту в СН4 и СО. Реакторы, подходящие для анаэробной ферментации, могут включать, но не ограничены ими, ферментеры на основе закрытого анаэробного бассейна, ферментеры с поршневым течением потока, ферментеры полного смешения и сухие ферментеры.
[56] Если контекст не диктует обратное, фразы «микробиологическая конверсия» или «микробиологическая реакция» и т.п. в настоящей заявке охватывают как фазу роста, так и фазу биосинтеза продукта согласно способу.
[57] Метанотрофный белок одноклеточных организмов (SCP, single cell protein) представляет собой хорошо известный источник белка для корма животных (Anthony, 1982). Белок цельных клеток, как правило, обрабатывают для удаления нуклеиновых кислот и других соединений фосфора (наподобие фосфолипидов). Авторы настоящего изобретения предлагают собирать белки клеток после экстракции липидов и применять их в качестве источника аминокислот для корма животных.
[58] Термин «условия ферментации» в настоящей заявке представляет собой условия, необходимые для осуществления микробиологической конверсии, и включает, без ограничения, температуру жидкой питательной среды, состав жидкой питательной среды и концентрацию отдельных компонентов среды, давление в реакторе, коэффициент массопереноса используемой смеси газов в реакторе, соотношение СН4 и O2 в смешанном газе, скорость потока смешанного газа, количество инокулюма, перемешивание биореактора и pH жидкой питательной среды.
[59] Термин «влажная биомасса» в настоящей заявке означает биомассу, которую отцентрифугировали для удаления по меньшей мере некоторой части воды, присутствующей в биомассе. Влажная биомасса, как правило, содержит по меньшей мере приблизительно 30 масс. % воды.
[60] Термин «сухая биомасса» в настоящей заявке означает биомассу, которую сначала отцентрифугировали, а затем высушили, например, с применением лиофилизатора, для удаления приблизительно 100% воды.
[61] Известны способы получения липидов из источников углерода, таких как глюкоза, ксилоза, лактоза, глицерол и этанол (Chi et al., "Oleaginous yeast Cryptococcus curvatus culture with dark fermentation hydrogen production effluent as feedstock for microbial lipid production" International Journal of Hydrogen Energy, Vol 36, 2011, pp 9542-9550.) Примеры таких способов включают способы, описанные, например, в публикации Chi et al. Более того, известно множество микроводорослей, способных осуществлять микробную конверсию сахаров в липиды, такие как водоросли рода Chlorella species. Однако метан не использовали в качестве источника углерода для микробиологического получения липидов. [62] Способ согласно первому аспекту настоящего изобретения включает микробиологическую конверсию метана и кислорода в биореакторе, снабжаемом газом, для получения липидов, белков и аминокислот. Согласно определенным вариантам реализации настоящего изобретения данный способ также включает экстракцию продуктов на основе липидов, полученных из биомассы бактерий.
Микроорганизмы
[63] Необходимой частью способа согласно настоящему изобретению является по меньшей мере одна метанотрофная бактерия, способная к микробиологическому преобразованию СН4 и O2 в продукты, такие как липиды и аминокислоты. Любые метанотрофные бактерии, способные к микробиологическому преобразованию СН4 и O2 в липиды и/или аминокислоты, можно использовать согласно настоящему изобретению. Метанотрофная бактерия представляет собой бактерию, которая выбрана из группы, включающей Methylococcus, Methylomonas, Methylomicrobium, Methylobacter, Methylocaldum, Methylomarinum, Methylovulum, Methylomarinovum, Methylothermus, Methylocystis, Methylosinus и комбинации указанных бактерий. Согласно конкретным вариантам реализации настоящего изобретения метанотрофную бактерию выбирают из Methylococcus capsulatus, Methylomonas methanica, Methylomonas spp., Methylosinus trichosporium, Methylomarinum vadi, Methylobacter marinus, Methylomarinum vadi, Methylomicrobium alcaliphilum и Methylomicrobium buryatense.
[64] Согласно следующим вариантам реализации настоящего изобретения метанотрофную бактерию выбирают из рода Methylomicrobium. Метанотрофные бактерии данного рода представляют собой типичные метанотрофы группы I, использующие для ассимиляции углерода путь рибулозы монофосфата (RuMP).
[65] Согласно предпочтительным вариантам реализации настоящего изобретения метанотрофная бактерия представляет собой Methylomicrobium buryatense. Данный вид является мезофильным, хотя и способен расти при температуре 10°С-45°С. В периодической культуре рост происходит при pH 6-11, предпочтительно pH 8,0-9,5, и при концентрации NaCl 0,1-8%, предпочтительно 0,75% NaCl. Данный вид содержит связанную с мембранами метанмонооксигеназу (корпускулярную) (particulate methane monooxygenase, pMMO) и растворимую метанмонооксигеназу (soluble methane monooxygenase, sMMO) (Kaluzhnaya et al., 2001).
[66] Метанотрофная бактерия может представлять собой бактерию, существующую в природе, или штамм, полученный генно-инженерным способом. Например, метанотрофная бактерия представляет собой полученный генно-инженерным способом штамм Methylomicrobium, который обладает улучшенными характеристиками роста по сравнению с родительским штаммом. Согласно конкретным вариантам реализации настоящего изобретения метанотрофная бактерия представляет собой выбранный штамм Methylomicrobium. Пример выбранного штамма, подходящего для использования согласно настоящему изобретению, представляет собой штамм 5GB1 Methylomicrobium buryatense, который является вариантом дикого типа, устойчивым к рифамицину, и содержит мутацию в гене rpoS (MBURv2_50058), содержащем вставку 309 пар оснований, которая приводит к появлению стоп-кодона через 218 АК (аминокислот) (за пределами 327 АК дикого типа). Согласно определенным вариантам реализации настоящего изобретения улучшенный штамм обладает специфической скоростью роста приблизительно 0,24 (время удвоения культуры 3 ч) в оптимизированной среде роста (см. пример 1).
Сырье
[67] Независимо от используемой в способе согласно настоящему изобретению метанотрофной бактерии согласно настоящему изобретению, такой бактерии требуется источник углерода и источник кислорода для получения липидов и/или аминокислот. Источники углерода включают, без ограничения, метан, метанол и их комбинации. Метан может быть получен из источника, который выбран из группы, включающей, но не ограниченной ими, природный газ, синтетический природный газ, гидраты природного газа, труднодоступный природный газ, сланцевый газ, сжигаемый газ, метан угольных пластов, метан угольных шахт, метан, полученный в результате каталитического крекинга олефинов или органических веществ, газ, образующийся при разложении отходов, биогаз, нефтяной попутный газ, метан, полученный в процессе сельского хозяйства, и метан, полученный как нежелательный продукт в результате гидрогенизации СО и реакций гидролиза, таких как процесс Фишера-Тропша. Наибольшим источником СН4 в мировом масштабе являются системы природного газа и нефти.
[68] Метанол может быть получен в результате каталитической конверсии монооксида углерода и водорода. В качестве альтернативы, СН3ОН получают в результате каталитической конверсии СН4. Согласно конкретным вариантам реализации настоящего изобретения поток газа, содержащего СН4, каталитическим способом преобразуют в СН3ОН перед поступлением в реактор. Согласно некоторым вариантам реализации настоящего изобретения способ согласно настоящему изобретению объединен с процессом синтеза СН3ОН. Например, по меньшей мере часть СН3ОН из способа синтеза СН3ОН, такого как способ, осуществляемый на заводе по производству метанола, может быть направлена в реактор утилизации в способе согласно настоящему изобретению.
[69] Согласно различным вариантам реализации настоящего изобретения метанол и метан могут быть перемешаны и поданы в биореактор
[70] Вторым компонентом, необходимым для роста метанотрофной бактерии и образования липидов и/или аминокислот, является кислород или источник кислорода. Типичные источники кислорода включают, но не ограничены ими, воздух, обогащенный воздух, O2 от фракционной перегонки, адсорбцию при переменном давлении, концентратор кислорода, электролиз и жидкий O2. Соотношение источника кислорода к источнику углерода можно варьировать для улучшения образования желаемых продуктов или для оптимизации эффективности микробной реакции и в конечном итоге для улучшения образования или улучшения роста. Соотношение O2 к СН4 в газообразном субстрате может варьировать от приблизительно 5:1 до приблизительно 1:1. Согласно конкретным вариантам реализации настоящего изобретения газообразный субстрат, который поступает в биореактор, содержит O2 и СН4 в соотношении, которое варьирует от приблизительно 2,5:1 до приблизительно 1:1. Согласно конкретным вариантам реализации настоящего изобретения газообразный субстрат, который поступает в биореактор, содержит O2 и СН4 в соотношении, которое варьирует от приблизительно 1,5:1 до приблизительно 1:1. Стехиометрия реакции между СН4 и O2 будет варьировать в зависимости от пути, который используется микроорганизмом (микроорганизмами). Диапазон возможной стехиометрии потребления СН4 микроорганизмами проиллюстрирован на фигуре 1.
[71] Как показано на фигуре 1, исходя из стехиометрии, может потребоваться эксплуатация реактора, при которой объемы СН4 и O2 вводят в диапазоне воспламеняемости (1). Предпочтительно, что реактор функционирует, когда в реакторе наблюдаются условия невоспламенения, и вследствие этого 96% или более конверсии СН4 необходимо при функционировании при соотношении O2 к СН4 во входящем газе 1,8:1 с целью создать в реакторе условия невоспламенения.
[72] Согласно конкретным вариантам реализации настоящего изобретения газообразный субстрат, используемый в данном способе, содержит воздух как альтернативу O2. При функционировании с воздухом вместо O2 условия эксплуатации в реакторе можно поддерживать за пределами диапазона воспламеняемости в зависимости от конверсии СН4 в реакторе. Диапазон стехиометрии при эксплуатации с воздухом проиллюстрирован на фигуре 2, где (1) представляет собой диапазон воспламеняемости, (2) представляет собой диапазон стехиометрии, (3) представляет собой состав входящего газа и (4) представляет собой воздушный канал. Согласно определенным вариантам реализации настоящего изобретения конверсия СН4 более чем на 40% приведет к созданию условий невоспламенения в реакторе с применением соотношения O2 к СН4 во входящем газе 1,8:1, что упрощает конструкцию реактора с точки зрения уменьшения источника воспламенения.
[73] Когда источник углерода представляет собой метанол, концентрация СН3ОН в среде роста может варьировать от приблизительно 1% (об./об.) до приблизительно 5% (об./об.). Согласно конкретным вариантам реализации настоящего изобретения соотношение может составлять от 1:1,2 до приблизительно 1:1,5. Для оптимального использования метанола штамм необходимо выращивать в полностью аэробных условиях. Согласно конкретным вариантам реализации настоящего изобретения субстрат, содержащий СН3ОН, вводят в реактор на начальных стадиях способа с целью оптимизировать рост микроорганизмов. После установления оптимальной скорости роста одного или нескольких микроорганизмов субстрат можно заменить субстратом, содержащим СН4 и O2.
[74] Источник углерода и источник кислорода могут поступать в биореактор в одном потоке или в виде отдельных потоков. Например, поток природного газа можно смешать с потоком, содержащим кислород, например, воздухом, для обеспечения желаемого соотношения O2:СН4.
[75] Согласно другому варианту реализации настоящего изобретения субстрат, содержащий метан и метанол, может поступать в реактор, и поток, содержащий кислород, может отдельно поступать реактор. Жидкий поток метанола может поступать отдельно от газообразного потока метана.
[76] Потоки смешанных газов могут также обладать дополнительными преимуществами, в особенности в тех случаях, когда поток газа, содержащего СН4 или СН4 и O2, является прерывающимся по своей природе. Например, прерывающийся поток газа, содержащего СН4 или СН4 и O2, можно смешать с по существу непрерывным потоком, содержащим СН4 или СН4 и O2, и ввести в реактор. Согласно конкретным вариантам реализации настоящего изобретения состав и скорость по существу непрерывного потока можно варьировать в соответствии с прерывающимся потоком с целью поддержания снабжения потоком субстрата по существу непрерывного состава и поддержания скорости потока, поступающего в ферментер.
[77] Вне зависимости от соотношения источник кислорода: источник углерода, которое поступает в реактор, важно, чтобы достаточное количество кислорода было растворено в жидкой питательной среде для облегчения потребления бактериями. Как правило, содержание растворенного кислорода должно варьировать от приблизительно 0,1% до приблизительно 100% насыщения воздухом при атмосферном давлении. Согласно некоторым вариантам реализации настоящего изобретения содержание растворенного кислорода находится в диапазоне от приблизительно 0,1 до приблизительно 40% насыщения воздухом при атмосферном давлении. Как правило, желательно, чтобы содержание растворенного кислорода составляло менее чем приблизительно 1 мМ/л O2.
[78] Способ согласно настоящему изобретению можно объединить с другим способом, включающим синтез продуктов из газообразных субстратов. Пример таких способов включает получение спиртов и/или кислот посредством анаэробной ферментации газообразных субстратов, содержащих СО, CO2 и/или Н2. Примеры способов включают способы, описанные, например, в публикациях WO 2007/117157 и WO 2008/115080, а также в патентах США №№6,340,581, 6,136,577, 5,593,886, 5,807,722 и 5,821,111, каждый из которых включен в настоящую заявку посредством ссылки. Согласно таким вариантам реализации настоящего изобретения потоки газа, содержащие СН4 вместе с СО, CO2 и/или Н2, например, природный газ или газ, образующийся при разложении отходов, можно подвергать любому способу разделения газа, известному в данной области техники, с целью разделения компонентов или элементов газа. Разделенный СН4 можно затем использовать в способе согласно настоящему изобретению, тогда как СО, CO2 и/или Н2 можно использовать в способе анаэробной ферментации.
Реактор
[79] Культивирование микроорганизма (микроорганизмов) и микробиологическую конверсию метана в один или несколько продуктов можно проводить в любом подходящем биореакторе, таком как реактор с иммобилизованными клетками, газлифтный реактор, барботажный колоночный реактор (BCR), реактор с циркуляционной петлей, мембранный реактор, такой как мембранный биореактор с системой полых волокон (HFM BR) или реактор с орошаемым слоем (TBR). Также согласно некоторым вариантам реализации настоящего изобретения биореактор может содержать первый реактор для роста, в котором культивируется микроорганизм (микроорганизмы), и второй реактор для синтеза продукта, в который может поступать бульон из реактора для роста и в котором можно получить различные продукты (например, кислоты).
[80] Биореактор содержит жидкую питательную среду, содержащую необходимые бактерии, и в биореактор будет подаваться газообразный субстрат, содержащий СН4 и O2. Согласно конкретным вариантам реализации настоящего изобретения жидкую питательную среду подают в реактор непрерывно. Согласно конкретным вариантам реализации настоящего изобретения жидкую питательную среду насыщают O2 перед подачей в реактор. Согласно конкретным вариантам реализации настоящего изобретения в жидкой питательной среде повышают давление, и среду насыщают O2 перед подачей в реактор.
[81] Жидкая питательная среда содержит питательные вещества, подходящие для микробиологической конверсии с применением желаемой бактерии, и будет также содержать витамины и/или минералы, достаточные для роста используемого микроорганизма или микроорганизмов. Среды, подходящие для культивирования усваивающих метан бактерий, известны в данной области техники. Например, подходящие среды описаны в публикациях Kaluzhnaya et al., 2001 и Ojala et al., 2011. Согласно конкретным вариантам реализации настоящего изобретения среда представляет собой минимальную смесь солей. Состав может варьировать по содержанию соли. Типичные составы питательной среды приведены в таблице 1.
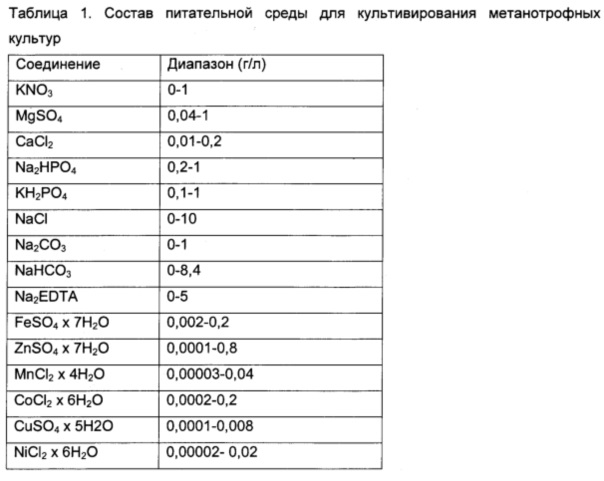

[82] Согласно некоторым вариантам реализации настоящего изобретения среда, используемая для роста штамма 5GB1 М. buryatense, содержит культуральную среду NMS. Согласно следующим вариантам реализации настоящего изобретения среда, используемая для роста штамма 5GB1 М. buryatense, содержит MgSO4 * 7H2O, содержание которого варьирует от приблизительно 0,04 г/л до приблизительно 1 г/л, CaCI2 * 6H2O, содержание которого варьирует от приблизительно 0,007 г/л до приблизительно 0,2 г/л, NaCl, KH2PO4, Na2CO3, Na2- EDTA, FeSO4 * 7H2O, ZnSO4 * 7H2O, MnCl2 * 4H2O, H3BO3, содержание которых варьирует от приблизительно 0,02 г/л до приблизительно 0,03 г/л, CoCl2 * 6H2O, содержание которого варьирует от приблизительно 0,02 г/л до приблизительно 0,2 г/л, CuCl2 * 2H2O, NiCl2 * 6H2O и Na2MoO4 * 2H2O, содержание которых варьирует от приблизительно 0,003 г/л до приблизительно 0,05 г/л.
[83] Согласно некоторым вариантам реализации настоящего изобретения среда, используемая для роста штамма 5GB1 М. buryatense, содержит по меньшей мере один источник азота, такой как KNO3, NaNO3, NH4Cl, (NH4)2SO4, мочевина или комбинации указанных соединений. Согласно следующим вариантам реализации настоящего изобретения среда, используемая для роста штамма 5GB1 М. buryatense, содержит по меньшей мере один источник азота, содержащий KNO3, NaNO3 или комбинации указанных соединений.
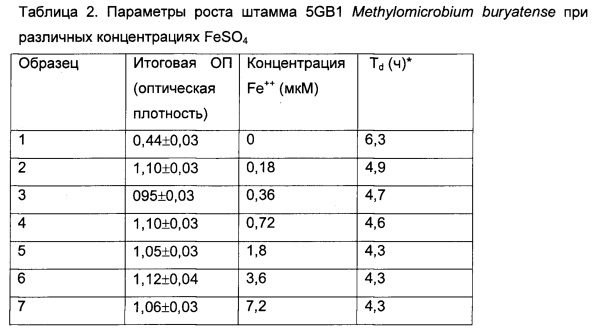
[84] Было установлено, что некоторые питательные вещества при их добавлении влияют на скорость роста и количество липидов, образуемое конкретной бактерией. В частности, желательно, чтобы потребление Cu++составляло по меньшей мере 7,5 мкмоль/гСМК (грамм сухой массы клеток). Поскольку количество меди может со временем стать ядовитым для бактерий, желательно, чтобы концентрация Cu++находилась в диапазоне от приблизительно 7 мкМ до приблизительно 20 мкМ. Аналогично желательно, чтобы концентрация Fe++находилась в диапазоне от приблизительно 5 мкМ до приблизительно 15 мкМ (таблица 2). Аналогично потребление NO3- должно варьировать от приблизительно 5 ммоль/гСМК до приблизительно 8 ммоль/гСМК. Дополнительно концентрация PO4-3 должна варьировать от приблизительно 1,4 ммоль/гСМК до приблизительно 2 ммоль/гСМК.
[85] Биореактор спроектирован таким образом, чтобы обеспечивать достаточный массоперенос, позволяющий микроорганизму (микроорганизмам) получить доступ к СН4 (и или СН3ОН) и O2. Длительные времена пребывания газа приводят к высокому потреблению газа микроорганизмом (микроорганизмами). Согласно конкретным вариантам реализации настоящего изобретения реактор представляет собой реактор с циркуляционной петлей, содержащий вертикальный сегмент и выпускной сегмент, через которые циркулируют газообразный субстрат и жидкая среда. Реактор может дополнительно содержать широкий диапазон подходящих контактных модулей газ/жидкость, которые могут обеспечить эффективный массоперенос газообразного субстрата, необходимый для улучшения микробиологической конверсии. Контактный модуль обеспечивает уникальное геометрическое окружение, которое позволяет газу и жидкости смешиваться надлежащим образом вдоль пути течения потока, в результате чего поступивший газ растворяется в жидкости более равномерно. В качестве примера данные контактные модули включают, но не ограничены ими, матрицу структурированной гофрированной металлической укладки, неупорядоченную укладку, ситчатые пластинки и статические смесители, все из которых характеризуются диапазоном хорошо известных типов и плотностей и широко доступны из коммерческих источников.
[86] В соответствии с конкретными вариантами реализации настоящего изобретения скорость массопереноса газообразного субстрата к культуре микроорганизмов можно контролировать таким образом, что культура микроорганизмов снабжается субстратом при оптимальной скорости подачи или при скорости, приближенной к оптимальной скорости подачи. В реакторах скорость массопереноса можно контролировать посредством контроля парциального давления газообразного субстрата и/или посредством контроля скорости потока жидкости или задержки подачи газа. Согласно конкретным вариантам реализации настоящего изобретения массоперенос контролируют посредством контроля парциального давления газообразного субстрата, поступающего в реактор.
[87] Согласно конкретным вариантам реализации настоящего изобретения pH среды поддерживают при значении от приблизительно 6 до приблизительно 11. Более конкретно, pH варьирует от приблизительно 8,0 до приблизительно 9,5. pH можно контролировать посредством добавления карбоната или бикарбоната или посредством добавления кислот и оснований к среде в соответствии с требованиями. Согласно конкретным вариантам реализации настоящего изобретения температуру жидкой питательной среды поддерживают от приблизительно 5 до приблизительно 65°С, предпочтительно от приблизительно 20 до приблизительно 40°С и наиболее предпочтительно от приблизительно 25 до приблизительно 35°С.
Получение продуктов
[88] Способ согласно настоящему изобретению позволяет получить продукты на основе липидов в результате микробиологической конверсии СН4 метанотрофными микроорганизмами в биореакторе. Согласно различным вариантам реализации настоящего изобретения липиды содержатся в мембранной фракции биомассы бактерий. Липидная фракция от общего объема биомассы будет определяться условиями роста в реакторе. Согласно конкретным вариантам реализации настоящего изобретения липиды, которые содержатся в мембранной фракции биомассы бактерий, составляют приблизительно по меньшей мере 5% от сухой массы бактерий. Согласно конкретным вариантам реализации настоящего изобретения липиды, которые содержатся в мембранной фракции биомассы бактерий, составляют по меньшей мере приблизительно 20% или по меньшей мере приблизительно 40% от сухой массы бактерий. Одним из побочных газов, образующихся в процессе микробиологической конверсии, является CO2. CO2 может оставаться с любыми не вступившими в реакцию газами в газовой фазе, или некоторая его часть может содержаться в жидком бульоне. Количество, которое остается в газовой фазе, по сравнению с количеством, которое поступает в жидкий бульон, зависит от pH бульона, причем более высокие значения pH способствуют нахождению CO2 в жидком бульоне.
[89] Согласно конкретным вариантам реализации настоящего изобретения ограниченное поступление O2 в реактор будет способствовать образованию липидов микроорганизмом (микроорганизмами). Надлежащее снабжение СН4 с ограниченным поступлением O2 может привести к более высокой скорости роста и увеличенному образованию липидов культурой. Вследствие этого согласно конкретным вариантам реализации настоящего изобретения газообразный субстрат, содержащий избыток СН4, вводят в реактор для образования культурой липидного продукта. Согласно конкретным вариантам реализации настоящего изобретения ограниченное поступление СН4 в реактор будет способствовать образованию микроорганизмом (микроорганизмами) липидов. Надлежащее снабжение O2 с ограниченным поступлением СН4 может привести к более высокой скорости роста и к увеличенному образованию культурой липидов. Вследствие этого согласно конкретным вариантам реализации настоящего изобретения газообразный субстрат, содержащий избыток O2, вводят в реактор для образования культурой липидного продукта. Согласно конкретным вариантам реализации настоящего изобретения для способствования образованию липидов поглощение бактериями газообразного субстрата находится в соотношении O2 к СН4, которое варьирует от приблизительно 1:1 до приблизительно 2,5:1. Согласно предпочтительным вариантам реализации настоящего изобретения для способствования образованию липидов поглощение O2 и СН4 находится в соотношении, которое варьирует от приблизительно 1,3:1 до приблизительно 1:1. Желательно, чтобы скорость роста бактерий составляла по меньшей мере 0,08 ч-1, или по меньшей мере 0,12 ч-1, или по меньшей мере 0,2 ч-1 или по меньшей мере 0,4 ч-1. Диапазон стехиометрии при использовании ограничения O2 и способствования продукции липидов проиллюстрирован на фигуре 3, где (1) представляет собой диапазон воспламеняемости.
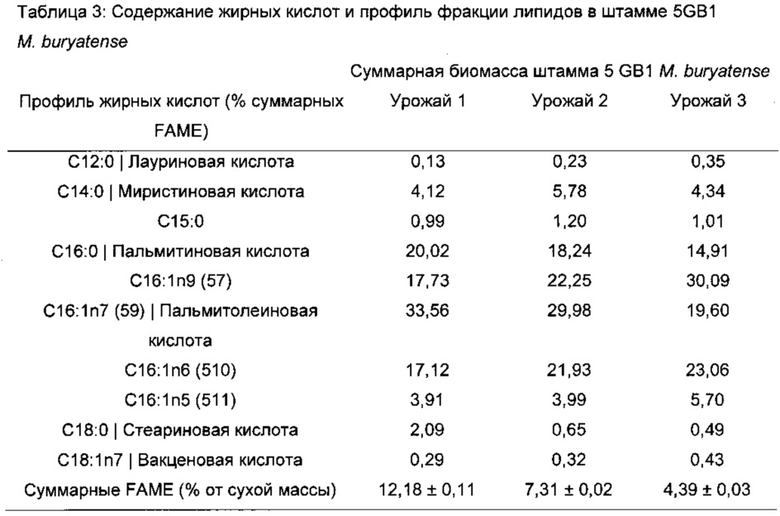
[90] Согласно конкретным вариантам реализации настоящего изобретения в результате осуществления способа образуются липиды, включая жирные кислоты, гликолипиды, сфинголипиды, сахаролипиды, поликетиды, стероидные липиды, гопаноиды, фосфолипиды и пренольные липиды с жирной кислотой (и образующимся углеводородом) с длиной цепей приблизительно от 12 до 20 атомов углерода. Конкретные примеры липидов включают, но не ограничены ими, лауриновую кислоту, миристиновую кислоту, пальмитиновую кислоту, пальмитолеиновую кислоту, стеариновую кислоту, вакценовую кислоту, фосфатидилхолин, триглицерины, глицеролы и комбинации указанных липидов. Конкретное содержание жирной кислоты показано в примере 1, таблица 3.
[91] Помимо получения липидов, в результате осуществления способа согласно настоящему изобретению можно также получить аминокислоты. Согласно конкретным вариантам реализации настоящего изобретения аминокислоты, образуемые микроорганизмом, включают, но не ограничены ими, эктоин, пролин, 5-оксопролин, аланин, аспартат, глутамин и глутамат. Пример образования аминокислоты представлен в таблице 3, которая приведена в примере 3. Образование аминокислот микроорганизмом может являться результатом культивирования при высоком содержании соли (3-8% NaCl).
[92] Реактор желательно эксплуатировать в условиях, соответствующих прохождению микробиологической конверсии газа в желаемые продукты. Условия реакции, которые следует принимать во внимание, включают давление, температуру, скорость потока газа, скорость потока жидкости, pH среды, окислительно-восстановительный потенциал среды, скорость перемешивания (при использовании реактора непрерывного действия с механическим перемешиванием), содержание инокулюма, максимальные концентрации субстрата для обеспечения того, что СН4, СН3ОН или O2 в жидкой фазе не становятся лимитирующими, и максимальные концентрации продукта во избежание ингибирования продуктом.
[93] Согласно определенным вариантам реализации настоящего изобретения может иметь преимущество процесс при увеличенном парциальном давлении. Более высокое давление в реакторе может повлиять на образование липидов и рост микроорганизмов. Согласно конкретным вариантам реализации настоящего изобретения реактор поддерживают при давлении от приблизительно атмосферного до приблизительно 3000 кПа. Согласно другим вариантам реализации настоящего изобретения давление может составлять от приблизительно 20 кПа до приблизительно 2000 кПа.
[94] Согласно определенным вариантам реализации настоящего изобретения концентрация натрия в среде может оказывать эффект на рост и скорости продукции метанотрофных микроорганизмов. Согласно конкретным вариантам реализации настоящего изобретения концентрацию натрия в среде доводят до желаемого уровня с применением соли, предпочтительно NaCl. В таких случаях pH среды контролируют с применением кислот и оснований, которые не содержат натрия. Согласно предпочтительным вариантам реализации настоящего изобретения концентрацию натрия поддерживают от приблизительно 120 до приблизительно 210 мМ (в форме катиона).
[95] Согласно различным вариантам реализации настоящего изобретения состав газа по способу определяют с применением газовой хроматографии посредством регуляторного отбора проб входящего и выходящего газа. Данный подход позволяет контролировать СН4, CO2, O2 и инертные соединения, такие как азот, в газе, а также водород, образованный в результате метаболизма бактерий. Согласно конкретным вариантам реализации настоящего изобретения уровень O2 в реакторе также контролируют посредством применения датчика растворенного кислорода, который измеряет концентрацию O2 в бульоне реактора. Согласно конкретным вариантам реализации настоящего изобретения измерения, полученные с применением датчика кислорода, используют для контроля скорости подачи входящего O2 или воздуха.
[96] Согласно конкретным вариантам реализации настоящего изобретения по меньшей мере часть неиспользованного газа и/или газа, образуемого микроорганизмом (микроорганизмами), покидает реактор через газоотвод. Данный выходящий газ, как правило, содержит непотребленные СН4 и O2 вместе с CO2, образуемым микроорганизмом. Согласно конкретным вариантам реализации настоящего изобретения по меньшей мере часть выходящего газа возвращается в биореактор для последующего преобразования. Согласно таким вариантам реализации настоящего изобретения выходящий газ может сначала подвергаться любому способу разделения газа, известному в данной области техники, для удаления одного или нескольких нежелательных компонентов из потока выходящего газа, например, CO2. В качестве альтернативы, по меньшей мере часть выходящего газа можно использовать в качестве топлива.
Экстракция
[97] Согласно различным вариантам реализации настоящего изобретения липидные продукты содержатся в клетке или в клеточной мембране. В данных случаях липидные продукты необходимо экстрагировать из биомассы бактерий. Вследствие этого после процесса микробиологической конверсии в реакторе биомасса поступает в зону экстракции.
[98] Зона экстракции может содержать несколько блоков экстракции для различных стадий способа экстракции. На первой стадии биомасса может поступать в блок разрушения клеток при концентрации твердых веществ, пригодной для закачивания биомассы (менее 40% твердых веществ и предпочтительно от 1 до 10% твердых веществ) для предварительной обработки перед экстракцией липидов. Этап предварительной обработки может состоять из химической или физической обработки клеточной биомассы, предпочтительно гомогенизации под высоким давлением, инкубации при высокой температуре (от приблизительно 50°С до приблизительно 200°С, предпочтительно от приблизительно 75°С до приблизительно 90°С) или предварительной обработки кислотой или щелочью (в предпочтительных концентрациях от приблизительно 1 до приблизительно 10% H2SO4 или NaOH, предпочтительно от приблизительно 2 до приблизительно 4% H2SO4 или NaOH) или любой комбинации указанных способов.
[99] Согласно следующим вариантам реализации настоящего изобретения разрушенные клетки могут сначала подвергаться этапу обезвоживания (удаления воды) для удаления некоторого количества воды, содержащейся в ферментативном бульоне, перед тем, как поступят на процесс экстракции растворителем. Удаление воды может включать, например, но не ограничиваясь ими, центрифугирование, фильтрацию, выпаривание или комбинации указанных способов. Удаление воды может привести к тому, что часть биомассы, содержащая разрушенные клетки, будет характеризоваться меньшим содержанием воды, чем содержание воды в исходном ферментативном бульоне. Согласно некоторым вариантам реализации настоящего изобретения содержание воды в биомассе, содержащей разрушенные клетки и липиды, после удаления воды может варьировать от приблизительно 10 масс. % воды до приблизительно 60 масс. % воды.
[100] Затем разрушенные клетки можно подвергать процессу экстракции растворителем в соотношении влажная биомасса: растворитель от приблизительно 100:1 и приблизительно 1:100, или в соотношении от приблизительно 10:1 до приблизительно 1:10, или в соотношении от приблизительно 5:1 до приблизительно 1:5 или в соотношении от приблизительно 2:1 до приблизительно 1:2. Предпочтительный растворитель для использования на данной стадии представляет собой растворитель с полярностью, совместимой с полярностью липидной фракции, и с достаточно низкой температурой кипения для более легкого удаления растворителя; предпочтительные растворители представляют собой растворители на основе короткоцепочечного спирта для высокополярной липидной фракции в метанотрофных биомассах, например, бутанол или пентанол, или растворители на основе короткоцепочечных алканов для микробиологических неполярных липидов, например, гексан или гептан, или комбинацию полярного и неполярного растворителя. Другие примеры растворителей, которые можно использовать в способе согласно настоящему изобретению, выбраны из группы, включающей метанол, этанол, 1-пропанол, н-бутанол, изобутанол, изоамиловый спирт, 2-метил-1-бутанол, фенетиловый спирт, 1-пентанол, 1-гексанол, 1-гептанол, 1-октанол, 1-нонанол, 1-деканол, триптофол, изопропанол, 2-бутанол, 2-пентанол, 2-гексанол, циклогексанол, трет-бутиловый спирт, трет-амиловый спирт, 2-метил-2-пентанол, 2-метилгексан-2-ол, 2-метилгептан-2-ол, 3-метил-3-пентанол, 3-метилактан-3-ол, циклопентан, циклогексан, бензол, толуол, диэтиловый эфир, дихлорметан, тетрагидрофуран, этилацетат, ацетон, диметилформамид, ацетонитрил, диметилсульфоксид и комбинации указанных растворителей. Согласно конкретным вариантам реализации настоящего изобретения продукт процесса экстракции дополнительно разделяют на легкую фазу, главным образом, содержащую экстрагированные липиды и растворитель, и тяжелую фазу, главным образом, содержащую воду, отработанную биомассу и остаток липида/растворителя. Согласно некоторым вариантам реализации настоящего изобретения разделение легкой фазы и тяжелой фазы можно осуществлять гравиметрическими методами, включая, но не ограничиваясь ими, центрифугирование и фазовые разделители. Согласно конкретным вариантам реализации настоящего изобретения на стадии разделения применяют центрифугу с коническими перегородками в роторе.
[101] Согласно некоторым вариантам реализации настоящего изобретения этап экстракции растворителем можно завершать при температуре, которая варьирует от приблизительно 0°С до приблизительно 100°С. Согласно некоторым вариантам реализации настоящего изобретения этап экстракции растворителем можно завершать при температуре, которая варьирует от приблизительно 20°С до приблизительно 50°С. Согласно следующим вариантам реализации настоящего изобретения этап экстракции растворителем можно завершать при температуре приблизительно 0°С, приблизительно 10°С, приблизительно 20°С, приблизительно 30°С, приблизительно 40°С, приблизительно 50°С, приблизительно 60°С, приблизительно 70°С, приблизительно 80°С, приблизительно 90°С или приблизительно 100°С.
[102] Согласно некоторым вариантам реализации настоящего изобретения этап экстракции растворителем можно проводить при давлении, которое варьирует от приблизительно 35 кПа (5 фунт-сила/дюйм2) до приблизительно 13790 кПа (2000 фунт-сила/дюйм2), или от приблизительно 690 кПа (100 фунт-сила/дюйм2) до приблизительно 6900 кПа (1000 фунт-сила/дюйм2), или от приблизительно 6900 кПа (1000 фунт-сила/дюйм2) до приблизительно 13790 кПа (2000 фунт-сила/дюйм2), или от 97 кПа (14 фунт-сила/дюйм2) до приблизительно 172 кПа (25 фунт-сила/дюйм2).
[103] Согласно некоторым вариантам реализации настоящего изобретения этап экстракции растворителем может быть выполнен в период времени, варьирующий от приблизительно 1 минут до приблизительно 24 часов. Согласно некоторым следующим вариантам реализации настоящего изобретения этап экстракции растворителем может быть выполнен в период времени, варьирующий от приблизительно 1 минуты до приблизительно 60 минут. Согласно следующим вариантам реализации настоящего изобретения этап экстракции растворителем может быть выполнен в период времени приблизительно 1 минуту, приблизительно 10 минут, приблизительно 20 минут, приблизительно 30 минут, приблизительно 40 минут, приблизительно 50 минут или приблизительно 60 минут. Согласно следующим вариантам реализации настоящего изобретения этап экстракции растворителем может быть выполнен в период времени, варьирующий от приблизительно 1 часа до приблизительно 24 часов. Согласно следующим вариантам реализации настоящего изобретения этап экстракции растворителем может быть выполнен в период времени приблизительно 1 час, приблизительно 2 часа, приблизительно 3 часа, приблизительно 4 часа, приблизительно 5 часов, приблизительно 6 часов, приблизительно 7 часов, приблизительно 8 часов, приблизительно 9 часов, приблизительно 10 часов, приблизительно 11 часов, приблизительно 12 часов, приблизительно 13 часов, приблизительно 14 часов, приблизительно 15 часов, приблизительно 16 часов, приблизительно 17 часов, приблизительно 18 часов, приблизительно 19 часов, приблизительно 20 часов, приблизительно 21 час, приблизительно 22 часа, приблизительно 23 часа или приблизительно 24 часа.
[104] После разделения растворитель можно выделить из липидного продукта посредством перегонки и направить обратно в зону экстракции, оставляя поток по существу чистых липидов. Согласно конкретным вариантам реализации настоящего изобретения тяжелая фаза, содержащая отработанную биомассу, поступает в модуль анаэробной ферментации. В качестве альтернативы, отработанную биомассу можно использовать для получения белка одноклеточных организмов.
[105] Согласно конкретным вариантам реализации настоящего изобретения липиды, экстрагированные из биомассы, можно подвергнуть дополнительной обработке для получения топлива или других химических веществ. Например, по меньшей мере фракцию потока липидного продукта можно направить в блок гидрообработки, в котором липиды можно преобразовать в дизельное топливо или компоненты дизельного топлива.
[106] Согласно другому варианту реализации настоящего изобретения липиды можно преобразовать в по меньшей мере одно химическое соединение, топливо или компонент топлива, которые выбраны из группы, включающей возобновляемое дизельное топливо, биодизельное топливо, углеводороды, сложные метиловые эфиры жирных кислот (FAME) и сложные этиловые эфиры жирных кислот (FAEE), посредством способов, хорошо известных в данной области техники. В различных производных химических веществ, таких как чистящие средства и средства личной гигиены, используются компоненты, например, поверхностно-активные вещества, жирные спирты и жирные кислоты, для всех из которых липиды или производные липидов могут использоваться в качестве заместителя. Также из липидов можно получить различные продукты переработки масел.
[107] Согласно конкретным вариантам реализации настоящего изобретения по меньшей мере часть тяжелой фазы, содержащей отработанную биомассу с этапа экстракции растворителем, направляют в блок анаэробного ферментера. В блоке анаэробного ферментера компоненты тяжелой фазы преобразуются в биогаз посредством анаэробной ферментации. Блок анаэробного ферментера может содержать ацидогенные бактерии, ацетогенные бактерии и/или метанобразующие бактерии. В типичном способе анаэробной ферментации ацидогенные бактерии сначала преобразуют органические полимеры и аминокислоты в CO2, Н2, NH3 и органические кислоты. Затем ацетогенные бактерии преобразуют полученные в результате органические полимеры в уксусную кислоту вместе с дополнительным CO2, Н2 и NH3. Наконец, метанобразующие бактерии преобразуют полученную уксусную кислоту в СН4 и CO2.
[108] Согласно конкретным вариантам реализации настоящего изобретения по меньшей мере часть биогаза, образованного в анаэробном ферментере, вносят в биореактор, причем метан используют для последующей микробиологической конверсии метанотрофными бактериями в один или несколько продуктов. Согласно альтернативным вариантам реализации настоящего изобретения по меньшей мере часть биогаза, образованного в анаэробном ферментере, поступает на газовую турбину для получения энергии. Энергию, полученную на газовой турбине, можно использовать для снабжения энергией любого этапа способа согласно настоящему изобретению, описанного в настоящей заявке.
Примеры
Пример 1
В данном примере представлена общая процедура проведения следующих экспериментов. Жидкую среду готовили в биореакторе посредством растворения следующих реактивов в 1000 мл деионизированной воды.
0,2 г MgSO4×7H2O
0,02 г CaCl2×6H2O
1,00 г KNO3
7,5 г NaCl
Затем биореактор автоклавировали при температуре 121°С в течение 20 минут, после чего охлаждали до температуры 30°С. В биореактор вводили датчик растворенного кислорода (РК) и датчик pH, оба из которых подсоединяли к контролеру. Затем воздух барботировали через среду со скоростью 100 сксм/м (стандартный кубический сантиметр) в течение 12 часов. Добавляли микроэлементы, карбонатный и фосфатный буферы (2 мл, 25 мл и 20 мл, соответственно).
Состав микроэлементов:
1,0 г Na2-EDTA
2,0 г FeSO4×7H2O
0,8 г ZnSO4×7H2O
0,03 г MnCl2×4H2O
0,03 г Н3ВО3
0,2 г CoCl2×6H2O
0,6 г CuCl2×2H2O
0,02 г NiCl2×6H2O
0,05 г Na2MoO×2H2O
Довести до 1000 мл
Фосфатный раствор:
5,44 г KH2PO4
10,73 г Na2HPO4
Довести до 1000 мл
Карбонатный раствор:
1 М NaHCO3 700 мл
1 М Na2CO3 300 мл
Контроль основности (3 М NaOH) присоединяли и устанавливали для поддержания pH 8,8.
Поток воздуха заменяли конкретным газом, исследование которого проводили, и образцы для анализа методом газовой хроматографии отбирали каждые 45 минут с применением автоматического отбора проб во время анализа. Наконец, добавляли 50 мл инокулюма.
Пример 2.
Метанотрофным бактериям для роста, окисления метанола, а также дыхания необходимо железо. Было показано, что метанотрофы могут образовывать Fe-хелатирующее соединение (Yoon et al., 2010; Matsen et al., 2013), и вследствие этого могут расти при очень низких концентрациях металла. Авторы настоящего изобретения обнаружили, что скорость роста штамма 5GB1 зависит от наличия железа. Максимальный рост наблюдается при высоком содержании железа - 14,4 мкМ. Культуры штамма 5GB1 Methylomicrobium buryatense росли в 50 мл минеральной среды в закрытых флаконах объемом 250 мл с добавлением 50 мл метана и различных концентраций Fe++, добавляемых в форме FeSO4.

Пример 3
Клетки выращивали в периодической культуре с использованием различных условий роста. Урожай 1 получали от клеток, которые росли при неограниченном поступлении СН4 и O2; Урожай 2 получали от клеток, которые росли в условиях ограничения O2; и Урожай 3 получали от клеток, которые росли в условиях ограничения СН4. Переэтерификацию целых клеток использовали для количественного определения жирных кислот в виде сложных метиловых эфиров жирных кислот (суммарные FAME) и для определения профиля жирных кислот клеточных липидов. Содержание липидов в клетках и профили жирных кислот варьировали в зависимости от условий роста.
Пример 4
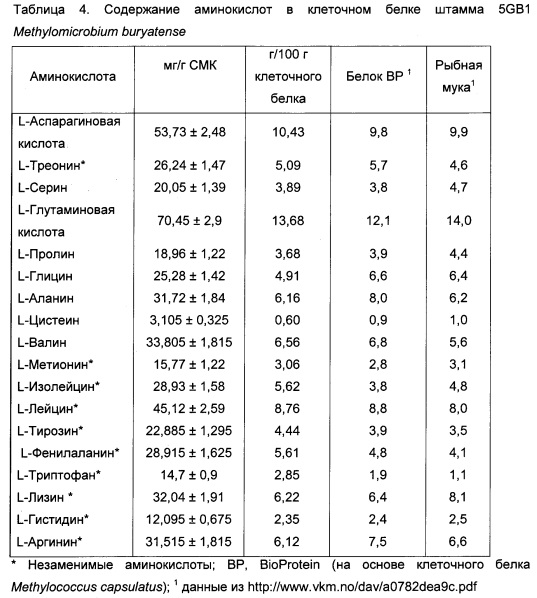
Культуры штамма 5GB1 Methylomicrobium buryatense выращивали в 250 мл минеральной среды, описанной выше, в сосудах объемом 1 л с добавлением 750 мл метана. Клетки собирали посредством центрифугирования, лиофилизировали и направляли на анализ аминокислот в AminoAcids (https://www.aminoacids.com) для составления профиля суммарных аминокислот. Состав аминокислот белка, полученного из Methylomicrobium, представлен в таблице 4. Было продемонстрировано, что содержание изолейцина и метионина в клеточном белке штамма 5GB1 аналогично содержанию таковых в рыбной муке и превышает содержание данных аминокислот в белке BP. Более того, в отличие от биомассы Methylococcus capsulatus, которая содержит 15% нуклеиновых кислот, биомасса штамма 5GB1 Methylomicrobium buryatense содержит всего 3-5% нуклеиновых кислот.
Пример 5
В данном примере описаны некоторые параметры ферментации, установленные в ходе культивирования с подпиткой и непрерывного культивирования. При культивировании с подпиткой исходную среду и установку реактора, описанную в примере 1, использовали до достижения стационарной фазы роста и уменьшения потребления газа. Газ на входе в реактор и на выходе из реактора измеряли каждый час с целью определить потребление газа, и оптическую плотность культуры также многократно измеряли для определения условий роста.
Для культивирования с подпиткой при использовании метанола применяли процедуру, аналогичную примеру 1, с целью проведения эксперимента с метанолом вместо метана в качестве источника углерода. Перед инокуляцией к стандартной среде NMS2 добавляли 0,5% об./об. метанола. Вместо предварительно смешанной смеси газов через среду барботировали воздух со скоростью 100 сксм/м. Контроль pH и отбор проб для газовой хроматографии оставались без изменений. Конкретные скорости поглощения СН4 и O2, достигавшие максимума при наибольшей скорости роста, обобщены в таблице 5 ниже.
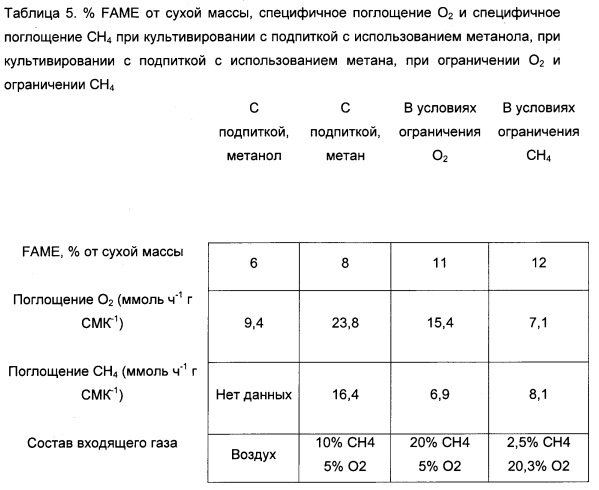
В аналогичном эксперименте культуру с подпиткой переключали на непрерывное питание средой с компонентами среды, разделенными на различные растворы. Данной системе позволяли достичь равновесия. Скорости потока компонентов среды в реактор изменяли до тех пор, пока не было обнаружено, что один из компонентов стал лимитирующим. Специфичные требования к NO3 и PO4 для биомассы определяли на основании равновесной концентрации биомассы, поддерживаемой ограничением потока питательных веществ.

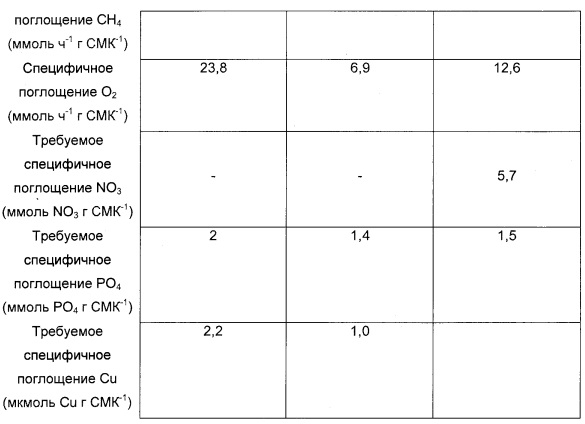
Пример 6
Хорошо известно, что медь играет ключевую роль в физиологии и активности аэробных метанотрофных бактерий. Рост штаммов, содержащих только конкретный вид метанмонооксигеназы, в большой степени зависит от наличия металла. Культуры с растворимой ММО могут расти без добавления меди, однако демонстрируют уменьшенную скорость роста. Штамм 5GB1 был способен переключаться с sMMO после ограничения поступления меди и рос в широком диапазоне содержания меди (0-20 мкМ). Скорость роста штамма без меди составляла 0,115 ч-1 (по сравнению с 0,24 ч-1 при оптимальном содержании меди). Было установлено, что оптимальные концентрации меди составляют 12 мкМ (добавлены в форме CuSO4). При концентрации меди более 24 мкМ рост штамма не наблюдался. Количество накопленных липидов было выше в культурах, росших с медью, как описано в таблице ниже.

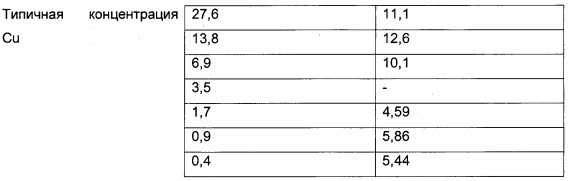
Пример 7
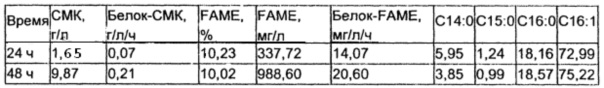
В данном примере описана культура с высокой плотностью клеток микроорганизма согласно настоящему изобретению при периодическом культивировании в биореакторе объемом 0,5 л. Культуральная среда, используемая для данной культуры, была модифицирована и содержала 8Х источник азота, 2Х фосфатный раствор и 4Х раствор микроэлементов в жидкой среде, описанной в примере 1. Соотношение СН4 и O2 в смешанном газе составляло 1:0,8. pH культуры в биореакторе контролировали и поддерживали на значении pH 8,8. Максимальная плотность клеток 22 г/л была достигнута при данном культивировании в течение 48 ч и приведена ниже.
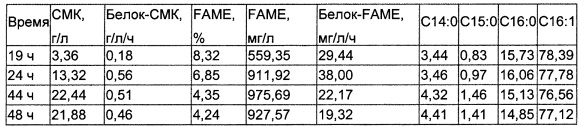
Пример 8
В данном примере описана периодическая культура, которую выращивали в биореакторе объемом 5 л. Для данной культуры использовали ту же культуральную среду, смешанный газ и рН культуры, что и в примере 7. Из данной культуры, культивируемой в течение 72 ч, получали 10 г/л СМК, что составило лишь половину от максимальной СМК, которая была достигнута в примере 7. Данный факт можно объяснить более низкой скоростью перемешивания, осуществляемой в данном биореакторе. Однако содержание FAME в ходе всего данного культивирования составило приблизительно 10%.

Пример 8. Совместимость растворителя с типами липидов
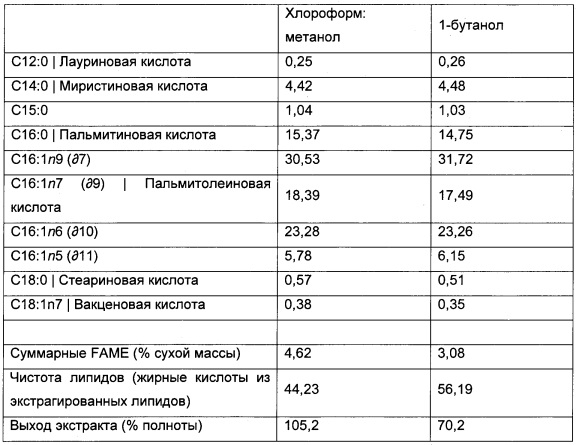
Селективное разделение полярных и неполярных интактных липидов в полярных и неполярных растворителях было продемонстрировано на чистых компонентах. Бутанол выбирали как типичный низкокипящий растворитель на основе короткоцепочечного спирта, образующий более легкую фазу с водной суспензией клеток, и проводили сравнение с гексаном как традиционным растворителем для экстракции липидов в случае липидов на основе триглицеридов. С использованием фосфатидилхолина как типичного полярного липида и чистого канолового масла как типичного неполярного липида - триглицерида, сравнение эффективности экстракции после растворения липидов в воде и последующей экстракции этиленгексаном или бутанолом (в соотношении 1:1) продемонстрировало экстракцию 2,7% полярных липидов в гексане с достаточным образованием эмульсии, ингибирующей разделение фаз, необходимое для экстракции, тогда как в бутаноле наблюдалось извлечение 70%, с извлечением нейтральных липидов 61-72% при использовании обоих типов растворителей. Разделение бутанолом было чистым и эффективным для полярной экстракции липидов.

Подтверждение полноты экстракции липидов из сухой биомассы, которую определяли посредством измерения соответствующих для получения топлива жирных кислот, продемонстрировало, что 1-бутанол был таким же эффективным растворителем, как более токсичная система растворителей хлороформ: метанол (2:1), которую используют для общих аналитических экстракций и, как правило, считают полной. Систему для ускоренной экстракции растворителем (accelerated solvent extractor, ASE, Dionex) использовали для экстракции из высушенной биомассы под давлением с применением следующих параметров: 75 мг сухой биомассы, экстрагированной при 50°С при 1500 фунт/дюйм2, для трех последовательных экстракций. Растворитель с экстрагированными липидами выпаривали досуха в потоке азота при температуре 40°С. Хлороформ: метанол стабильно экстрагировали 100% липидов, бутанол экстрагировал 70% липидов.
Профиль жирных кислот оставался неизменным, типичные жирные кислоты присутствовали в липидах, экстрагированных бутанолом, и представлены ниже.
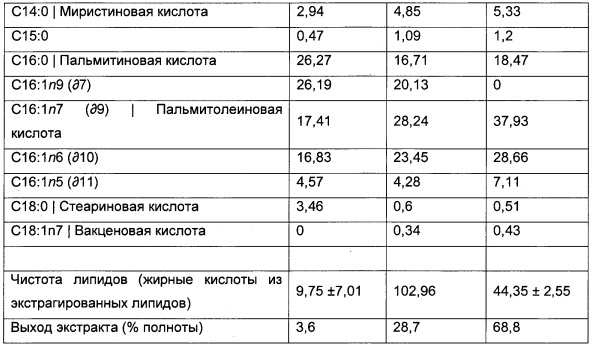
Пример 9. Подтверждение увеличенной эффективности экстракции при термической обработке суспензии клеток 1-10% суспензию клеток при инкубации нагревали в течение 15 мин. при температуре 85°С с последующей экстракцией в течение 1 ч при комнатной температуре с применением выхода биомассы от 4 до 28% экстрагируемости жирных кислот при использовании гексана, тогда как при использовании бутанола полнота экстракции составляла 70%. Было установлено, что термическая обработка является эффективным способом разрушения клеток, позволяющим проводить экстракцию и разделение полярных и неполярных липидов. Потенциальные механизмы, благодаря которым тепло может помочь индуцировать разрушение клеток, включают денатурацию белков и разрушение слоя протеогликанов клеток, что делает липиды более доступными для экстракции растворителем.

[109] Варианты реализации настоящего изобретения описаны в качестве примера. Однако следует понимать, что конкретные этапы или стадии, необходимые в одном варианте реализации, могут не являться необходимыми в другом. И наоборот, этапы или стадии, включенные в описание конкретного варианта реализации, могут необязательно преимущественно использоваться в вариантах реализации, в которых такие этапы и стадии конкретно не упоминаются.
[110] Несмотря на то, что настоящее изобретение в общих чертах описано со ссылкой на любой тип потока, который может перемещаться по системе или поблизости от системы (систем) посредством любого известного способа переноса, согласно определенным вариантам реализации настоящего изобретения поток субстрата и/или выходящих веществ является газообразным. Специалисты в данной области техники понимают, что конкретные стадии можно объединить посредством подходящих трубопроводов или т.п., сконструированных для получения или пропускания потоков через систему. Для облегчения доставки потоков на конкретные стадии можно применять насос или компрессор. Более того, компрессор можно использовать для увеличения давления газа, который подается на одну или несколько стадий, например, в биореактор. Как обсуждается в настоящей заявке выше, давление газов в биореакторе может влиять на эффективность реакции ферментации, осуществляемой согласно настоящему изобретению. Вследствие этого, давление можно откорректировать для улучшения эффективности ферментации. Подходящие величины давления для общепринятых реакций известны в данной области техники.
[111] Кроме того, системы или способы согласно настоящему изобретению могут необязательно включать способы регулирования и/или контроля других параметров для улучшения общей эффективности способа. Для регулирования и/или контроля конкретных параметров процесса в систему можно ввести один или несколько процессоров. Например, конкретные варианты реализации настоящего изобретения могут включать определение способов мониторинга состава потока (потоков) субстрата и/или выходящих веществ. Кроме того, конкретные варианты реализации настоящего изобретения могут включать способы контроля доставки потока (потоков) субстрата на конкретные стадии или элементы в пределах конкретной системы, если с помощью средств для определения было установлено, что данный поток содержит состав, подходящий для конкретной стадии. Например, в случаях, когда поток газообразного субстрата содержит низкие уровни O2 или высокие уровни СН4, которые могут пагубно сказаться на микробиологической реакции, поток субстрата может быть отклонен от биореактора. Согласно конкретным вариантам реализации настоящего изобретения система включает средства для мониторинга и контроля места назначения потока субстрата и/или скорости потока, так что поток с желаемым или подходящим составом может быть доставлен на конкретную стадию.
[112] Кроме того, может быть необходимо нагреть или охладить конкретные компоненты системы или поток (потоки) субстрата перед или в течение одной или нескольких стадий в способе. В таких случаях можно использовать известные способы для нагревания или охлаждения. Например, для нагрева или охлаждения потоков субстрата можно применять теплообменники.
[113] Более того, система может включать один или несколько этапов предварительной/последующей обработки для улучшения функционирования или эффективности конкретной стадии. Например, этап предварительной обработки может включать средства для удаления конкретного вещества и/или длинноцепочечных углеводородов или смол из потока газообразного субстрата. Другие операции предварительной или последующей обработки, которые можно проводить, включают разделение желаемого продукта (продуктов) из конкретных стадий, таких как, например, стадии получения в биореакторе.
[114] Настоящее изобретение было описано в настоящей заявке со ссылкой на предпочтительные варианты реализации с целью облегчить читателю реализацию настоящего изобретения на практике без чрезмерного экспериментирования. Специалисты в данной области техники понимают, что настоящее изобретение может быть реализовано на практике в большом количестве вариантов и модификаций, отличных от тех, которые были конкретно описаны в настоящей заявке. Следует понимать, что настоящее изобретение включает все такие варианты и модификации. Более того, заголовки, названия разделов или т.п.приведены для облечения читателю понимания настоящего документа, и их не следует истолковывать как ограничивающие объем настоящего изобретения.
[115] Более конкретно, как понимает специалист в данной области техники, осуществление вариантов реализации настоящего изобретения могут включать один или несколько дополнительных элементов. Только элементы, необходимые для понимания настоящего изобретения в его различных аспектах, могут быть показаны в конкретном примере или в описании. Однако объем настоящего изобретения не ограничен описанными вариантами реализации и включает системы и/или способы, включающие один или несколько дополнительных этапов и/или один или несколько замененных этапов, и/или системы и/или способы, позволяющие избежать одного или нескольких этапов.
[116] Ссылка на любой предшествующий уровень техники в данной спецификации не является признанием или любой формой указания на то, что данный предшествующий уровень техники образует часть всеобщего обобщенного знания в данной области в стране, и данную ссылку не следует считать таковой.
[117] По всей данной спецификации и в любом пункте прилагаемой формулы изобретения, если контекст не диктует обратное, слова «содержит», «содержащий», «включает», «включающий» и т.п. следует истолковывать как имеющие включающий, а не исключающий смысл, то есть в смысле «включая, но не ограничиваясь ими».
| название | год | авторы | номер документа |
|---|---|---|---|
| МИКРООРГАНИЗМЫ ДЛЯ ПОВЫШЕННОГО ПРОДУЦИРОВАНИЯ АМИНОКИСЛОТ И СВЯЗАННЫЕ С НИМИ СПОСОБЫ | 2015 |
|
RU2688486C2 |
| СИСТЕМА, СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ БИОПЕРЕРАБОТКИ | 2013 |
|
RU2723620C2 |
| РЕАКТОРЫ, СИСТЕМЫ И СПОСОБЫ ФЕРМЕНТАЦИИ С ПОДАЧЕЙ ГАЗА С ПРИМЕНЕНИЕМ ЗОНЫ ВЕРТИКАЛЬНОГО ПОТОКА | 2018 |
|
RU2761409C2 |
| РЕАКТОРЫ, СИСТЕМЫ И ПРОЦЕССЫ ФЕРМЕНТАЦИИ С ПОДАЧЕЙ ГАЗА, ИСПОЛЬЗУЮЩИЕ ЕМКОСТИ РАЗДЕЛЕНИЯ ГАЗА/ЖИДКОСТИ | 2018 |
|
RU2769130C2 |
| УСОВЕРШЕНСТВОВАННОЕ УЛАВЛИВАНИЕ УГЛЕРОДА ПРИ ФЕРМЕНТАЦИИ | 2020 |
|
RU2778024C2 |
| УСОВЕРШЕНСТВОВАННОЕ УЛАВЛИВАНИЕ УГЛЕРОДА ПРИ ФЕРМЕНТАЦИИ | 2014 |
|
RU2735100C2 |
| СИСТЕМА И СПОСОБ (ВАРИАНТЫ) ИНТЕНСИФИКАЦИИ ПРОИЗВОДСТВА БИОМАССЫ | 2017 |
|
RU2747305C2 |
| СИСТЕМЫ ФЕРМЕНТАЦИИ С ПОДАЧЕЙ ГАЗА | 2013 |
|
RU2639542C2 |
| УСОВЕРШЕНСТВОВАННОЕ УЛАВЛИВАНИЕ УГЛЕРОДА ПРИ ФЕРМЕНТАЦИИ | 2022 |
|
RU2800360C1 |
| СПОСОБ И СИСТЕМА ДЛЯ ПОЛУЧЕНИЯ ПРОДУКТОВ, ВКЛЮЧАЮЩИХ СПИРТЫ И/ИЛИ КИСЛОТЫ, ПРИ МИКРОБИОЛОГИЧЕСКОЙ ФЕРМЕНТАЦИИ | 2008 |
|
RU2539027C2 |
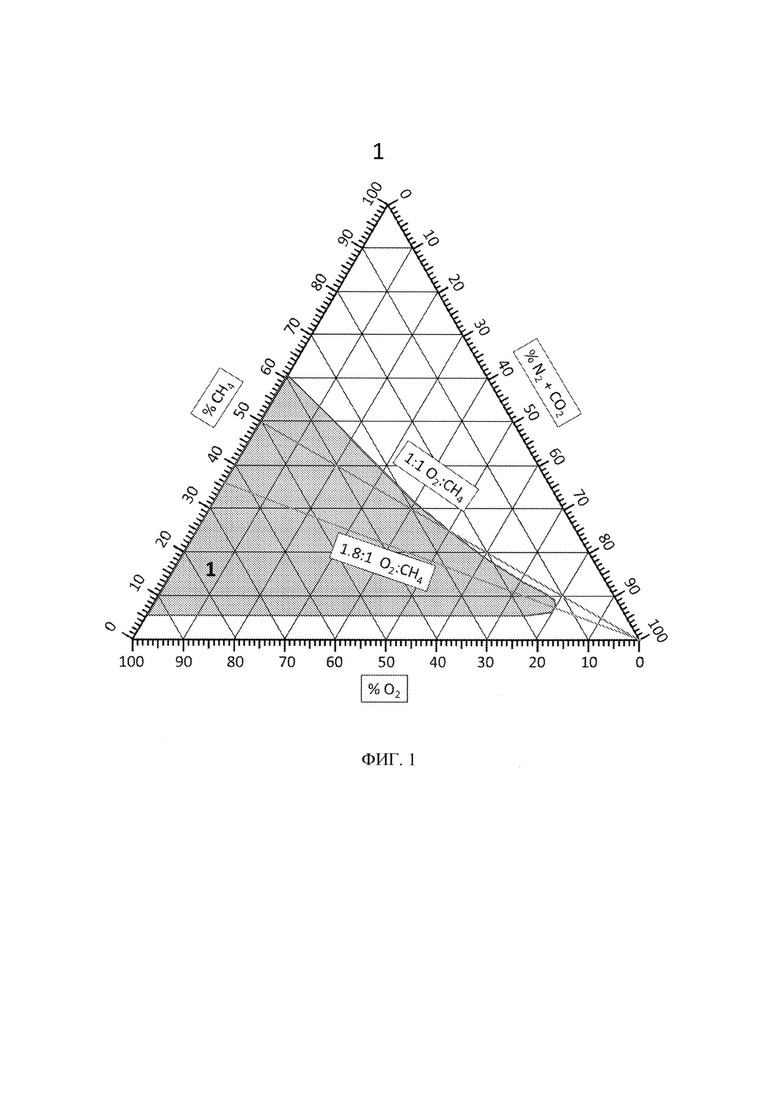
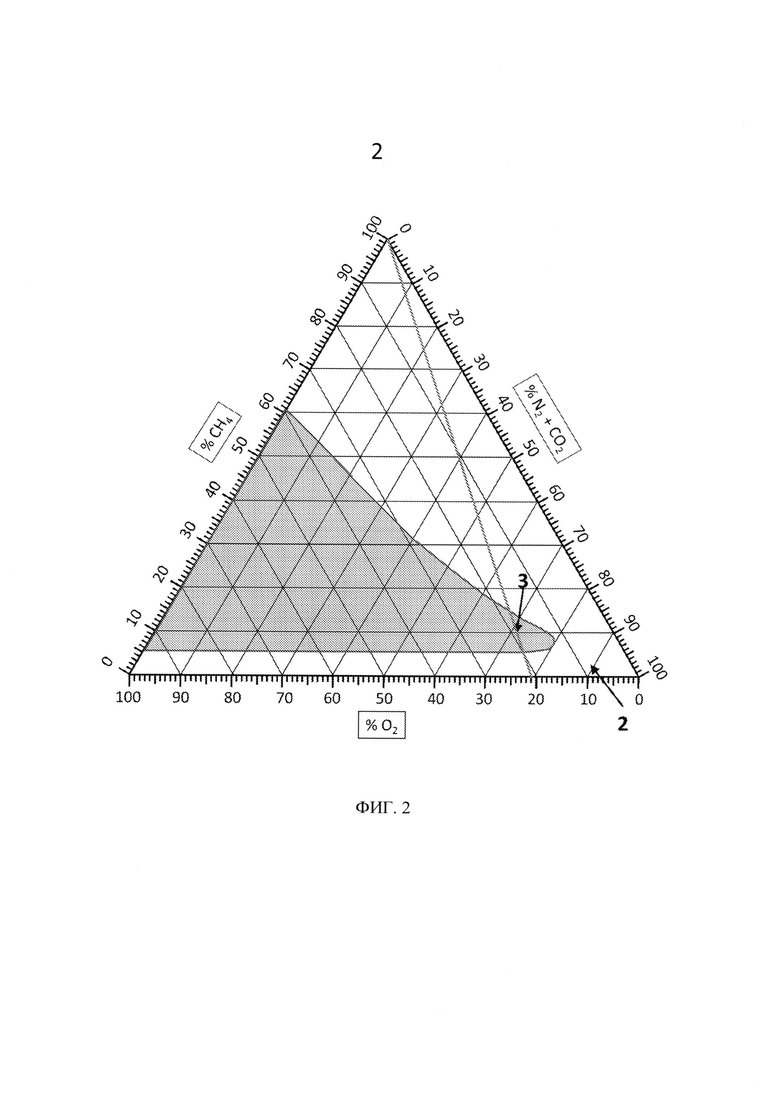
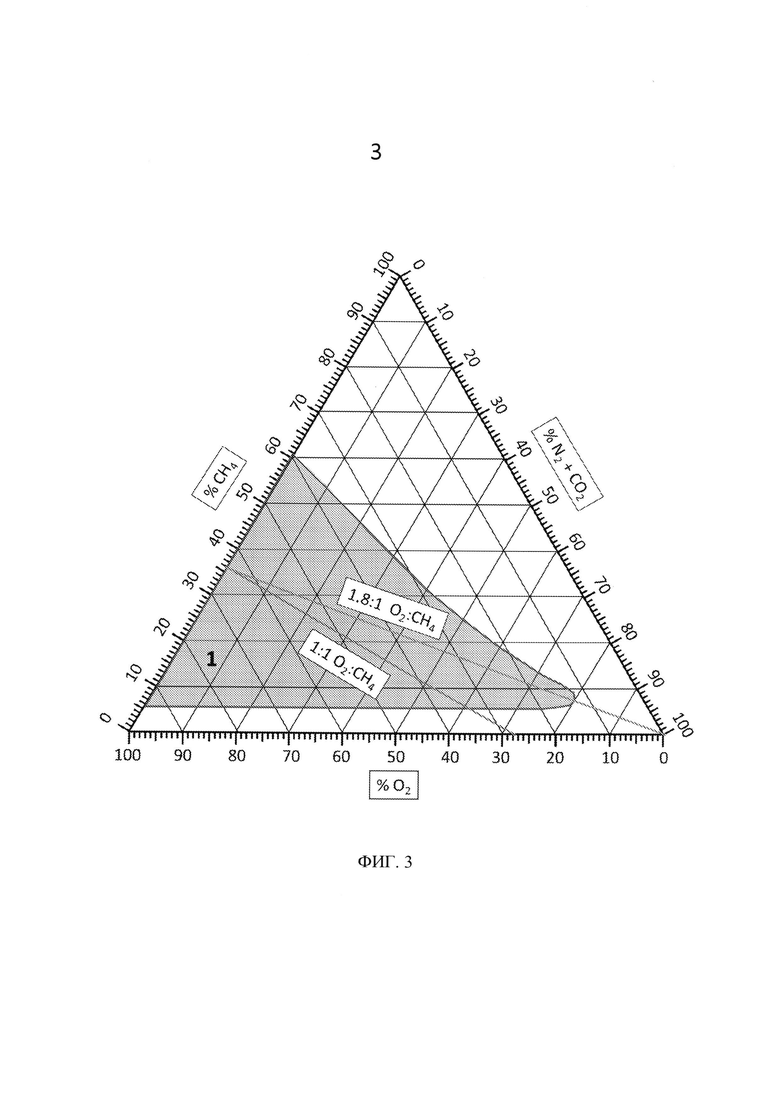
Группа изобретений относится к области биохимии. Предложен способ получения липидного продукта посредством микробиологической конверсии газообразного субстрата (варианты). В одном варианте способ включает обеспечение газообразного субстрата в содержащем культуру одного метанотрофного микроорганизма в жидкой питательной среде биореакторе, микробиологическое преобразование газообразного субстрата в условиях ферментации в липидный продукт в клеточной мембране метанотрофного микроорганизма и выделение липидного продукта из клеточной мембраны метанотрофного микроорганизма. Причём газообразный субстрат содержит СН4 и O2 в соотношении O2:СН4 от 5:1 до 0,9:1. В другом варианте способ включает подачу субстрата в содержащий жидкую питательную среду и культуру одного метанотрофного микроорганизма биореактор, микробиологическое преобразование субстрата для получения липидного продукта и выделение липидного продукта из клеточной мембраны микроорганизма. Причём субстрат содержит O2 и одно соединение из СН4, СН3ОН или их комбинации. Изобретения обеспечивают получение липидов из содержащих метан газообразных субстратов, а также уменьшение выброса метана в атмосферу. 2 н. и 24 з.п. ф-лы, 3 ил., 7 табл., 9 пр.
.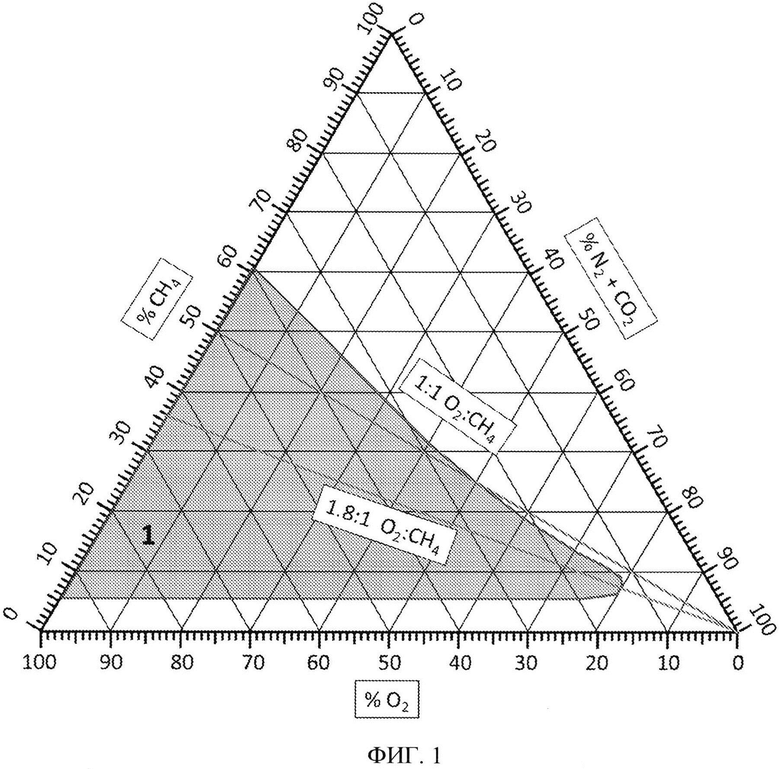
1. Способ получения по меньшей мере одного липидного продукта посредством микробиологической конверсии газообразного субстрата, включающий:
(a) обеспечение газообразного субстрата, содержащего СН4 и O2 в соотношении O2:СН4, которое варьируют от 5:1 до 0,9:1, в биореактор, который содержит культуру по меньшей мере одного метанотрофного микроорганизма в жидкой питательной среде; и
(b) микробиологическое преобразование газообразного субстрата в условиях ферментации в по меньшей мере один липидный продукт в клеточной мембране метанотрофного микроорганизма;
(c) выделение по меньшей мере одного липидного продукта из клеточной мембраны метанотрофного микроорганизма,
где указанный по меньшей мере один липидный продукт выбран из группы, состоящей из жирных кислот, гликолипидов, сфинголипидов, сахаролипидов, поликетидов, стероидных липидов, гопаноидов, фосфолипидов и пренольных липидов или их смесей.
2. Способ по п. 1, отличающийся тем, что способом дополнительно получают по меньшей мере один продукт, выбранный из группы, состоящей из белков, аминокислот и выделяемых жирных кислот.
3. Способ по п. 1 или 2, отличающийся тем, что указанные липиды дополнительно преобразуют в соединения, которые выбраны из группы, состоящей из возобновляемого дизельного топлива, биодизельного топлива, дизельного топлива, компонентов дизельного топлива сложных метиловых эфиров жирных кислот и сложных этиловых эфиров жирных кислот.
4. Способ по п. 1 или 2, отличающийся тем, что указанный газообразный субстрат содержит O2 и СН4 в соотношении O2:СН4 от 1,3:1 до 0,9:1.
5. Способ по п. 1 или 2, отличающийся тем, что указанный микроорганизм поглощает СН4 и O2 в соотношении O2 к СН4 от 1:1 до 2,5:1.
6. Способ по п. 1 или 2, отличающийся тем, что указанная питательная среда содержит от 7 до 20 мкМ/гСМК Cu++.
7. Способ по п. 1 или 2, отличающийся тем, что указанная питательная среда содержит от 5 до 8 ммоль/гСМК NO3-.
8. Способ по п. 1 или 2, отличающийся тем, что указанная питательная среда содержит от 1,4 до 2 ммоль/гСМК PO4-3.
9. Способ по п. 1 или 2, отличающийся тем, что указанная культура по меньшей мере одного метанотрофного микроорганизма выбрана из группы, состоящей из родов Methylococcus, Methylomonas, Methylomicrobium, Methylobacter, Methylocaldum, Methylosphaera, Methylocystis и Methylosinus или комбинации указанных родов.
10. Способ по п. 1 или 2, отличающийся тем, что указанная культура включает Methylomicrobium buryatense.
11. Способ по п. 1 или 2, отличающийся тем, что по меньшей мере часть не вступившего в реакцию газообразного субстрата и/или любого газа, образованного микроорганизмом, покидает биореактор, не вступив в реакцию, через газоотвод и поступает обратно в биореактор для последующего преобразования и/или используется в качестве топлива.
12. Способ по п. 1 или 2, дополнительно включающий поддержание рН жидкой питательной среды в диапазоне от 6 до 11.
13. Способ по п. 1 или 2, дополнительно включающий поддержание температуры жидкой питательной среды в диапазоне от 5 до 50°С.
14. Способ получения по меньшей мере одного липидного продукта посредством микробиологической конверсии субстрата, включающий:
(a) подачу субстрата, содержащего O2 и по меньшей мере одно соединение, которое выбрано из СН4, СН3ОН и комбинации указанных соединений, в биореактор, который содержит жидкую питательную среду и культуру по меньшей мере одного метанотрофного микроорганизма;
(b) микробиологическое преобразование субстрата для получения по меньшей мере одного липидного продукта, который выбран из группы, состоящей из жирных кислот, гликолипидов, сфинголипидов, сахаролипидов, поликетидов, стероидных липидов, гопаноидов, фосфолипидов и пренольных липидов или их смесей, в клеточной мембране метанотрофного микроорганизма; и
(c) выделение по меньшей мере одного липидного продукта из клеточной мембраны микроорганизма.
15. Способ по п. 14, отличающийся тем, что способом дополнительно получают по меньшей мере один продукт, выбранный из группы, состоящей из белков, аминокислот и выделяемых жирных кислот.
16. Способ по п. 14 или 15, отличающийся тем, что указанный субстрат содержит O2 и СН4 и СН3ОН и соотношение O2:СН4 варьируют от 5:1 до 0,5:1.
17. Способ по п. 15, отличающийся тем, что указанный микроорганизм поглощает СН4 и O2 в соотношении O2 к СН4 от 1:1 до 2,5:1.
18. Способ по п. 14 или 15, дополнительно включающий смешивание СН4 с СН3ОН перед поступлением в биореактор.
19. Способ по п. 14 или 15, отличающийся тем, что указанную культуру по меньшей мере одного метанотрофного микроорганизма выбирают из родов, включающих Methylococcus, Methylomonas, Methylomicrobium, Methylobacter, Methylocaldum/Methylothermus, Methylomarinum, Methylomarinovum, Methylocystis и Methylosinus или комбинаций указанных родов.
20. Способ по п. 14 или 15, отличающийся тем, что указанная культура содержит Methylomicrobium buryatense.
21. Способ по п. 14 или 15, отличающийся тем, что указанный этап выделения включает этап разрушения клеток и этап выделения растворителем.
22. Способ по п. 21, отличающийся тем, что в результате указанного этапа выделения растворителем образуется легкая фаза, содержащая по меньшей мере один продукт, и тяжелая фаза, содержащая отработанную биомассу.
23. Способ по п. 22, отличающийся тем, что по меньшей мере часть отработанной биомассы используют для получения белка одноклеточных организмов.
24. Способ по п. 22, дополнительно включающий поступление по меньшей мере части тяжелой фазы в анаэробный ферментер, в котором по меньшей мере часть тяжелой фазы преобразуется в биогаз.
25. Способ по п. 24, отличающийся тем, что по меньшей мере часть образованного биогаза подается в биореактор.
26. Способ по п. 14 или 15, дополнительно включающий преобразование по меньшей мере части выделенного продукта в по меньшей мере одно соединение, которое выбрано из группы, состоящей из возобновляемого дизельного топлива, биодизельного топлива, дизельного топлива, производных дизельного топлива, сложных метиловых эфиров жирных кислот и сложных этиловых эфиров жирных кислот.
| US 5397473 A, 14.03.1995 | |||
| KALUZHNAYA M., KHMELENINA V | |||
| and et al., Taxonomic Characterization of New Alkaliphilic and Alkalitolerant Methanotrophs from Soda Lakes of the Southeastern Transbaikal Region and description of Methylomicrobium buryatense sp.nov | |||
| // Systematic and Applied Microbiology, 2001, 24, стр.166-176 | |||
| Biotech Bacteria Could Convert Methane to Liquid Diesel // Environment News Service, 04.01.2013 | |||
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| WO 2012122343 A2, 13.09.2012 | |||
| SU 1040797 A1, 27.05.1995. | |||
Авторы
Даты
2018-06-21—Публикация
2014-10-20—Подача