Изобретение относится к области медицины и может быть использовано для диагностики Т- и В-линейных острых лимфобластных лейкозов (ОЛЛ) с использованием световой микроскопии в сочетании с компьютерной обработкой данных.
ОЛЛ представляют собой гетерогенную группу опухолевых заболеваний системы кроветворения. Они характеризуются поражением костного мозга и крови патологическими бластами. Диагностика острых лейкозов (ОЛ) базируется на комплексной характеристике бластов. При этом применяются морфологические, цитохимические и иммунофенотипические методы изучения клеток [Френкель М.А., в кн. «Клиническая онкогематология» под редакцией проф. М.А. Волковой, Москва, «Медицина», 2007 г., стр. 306-319, Тупицын Н.Н., в кн. «Клиническая онкогематология» под редакцией проф. М.А. Волковой, Москва, «Медицина», 2007 г., стр. 338-370]. Каждый из этих подходов характеризует отдельные особые свойства бластов. Совокупность полученных данных является основанием для диагностики ОЛЛ и их вариантов.
Морфологический метод исследования заключается в изучении окрашенных препаратов крови и костного мозга с подсчетом числа бластов в процентах к общему числу клеток. В крови подсчитывается 200 клеток, в костном мозге 500 клеток двумя независимыми экспертами. При этом учитываются размер и форма клеток, очертания ядер, особенности структуры хроматина, ядерно-цитоплазматическое отношение и наличие включений в цитоплазму. Морфологический подход не дает возможности во многих случаях установить природу бластов в связи с их значительной гетерогенностью.
Цитохимическое исследование включает анализ маркеров гранулоцитарного и моноцитарного рядов гемопоэза. Они позволяют отдифференцировать ОЛЛ от миелоидных лейкозов. Однако этот метод не является адекватным в части случаев лейкозов.
Иммунофенотипическое исследование основано на изучении антигенной структуры бластов с помощью проточной цитофлюорометрии. Использование широкого набора диагностических антител позволяет определить направленности дифференцировки и установить стадию созревания бластов. Анализ результатов иммунофенотипирования, с учетом морфологических и цитохимических показателей дает основание определить гистогенез и этап дифференцировки бластов при ОЛЛ.
Делаются попытки расширить характеристику клеток крови и костного мозга при лейкозах с помощью автоматических систем. Однако ошибки достигают уровня 30-40%. Отсутствуют достоверные данные по возможности одновременной морфологической и иммунофенотипической характеристики бластов на окрашенных мазках с целью диагностики вариантов ОЛЛ.
Известен «Способ распознавания изображения текстуры клеток» [Патент РФ №2385494]. Данный способ анализа изображения текстуры объекта для выявления патологии, включающий определение текстурных признаков объекта, которое состоит в том, что осуществляют предобработку полученных изображений объекта посредством сегментации на основе анализа в цветовом пространстве информативных с точки зрения текстурных признаков областей изображения объекта, определяемых выбранным размером окна, шагом и направлением просмотра изображения объекта, производят вычисления значений для текстурных признаков и формирования матриц чисел и осуществляют идентификацию и классификацию объекта, при этом текстурные признаки определяют для изображений клеток крови, предобработку полученных изображений объекта посредством сегментации осуществляют на основе кластерного анализа в цветовом пространстве, в качестве информативных с точки зрения текстурных признаков областей изображения объекта используют выделение изображений ядер клеток, наиболее информативные признаки для классификации определяют автоматически на основе обучающих выборок из предварительно созданных баз изображений, классифицированных экспертами и содержащих клетки каждого типа (бластные, лимфоциты), на основе которых производят идентификацию и классификацию, преобразуют пиксели изображения в различные цветовые пространства, вычисляют матрицу пространственной смежности, после чего на основании вычисленных значений текстурных признаков осуществляют классификацию (распределение по общим признакам) в пространстве текстурных признаков: энергия, момент инерции, максимальная вероятность, локальная однородность, энтропия, след НМПС, среднее значение яркости, корреляция значений яркости изображения.
Однако указанный способ не обеспечивает в условиях близких кластеров описания лейкоцитов с различным иммунологическим статусом, актуализации баз данных и пополнения данными экспертов, повышения доли заболеваний, выявляемых на ранней стадии, что является одной из приоритетных задач онкологии в условиях совершенствования современных видов диагностики и терапии с контролем их эффективности.
Известен метод компьютерного распознавания и классификации аномальных клеток крови и программное обеспечение для его реализации [Патент ES 2428215 А1]. В решении предложен метод, который выполняет классификацию клеток на основе методов автоматизированной обработки и анализа проб крови, что включает получение цифровых изображений аномальных клеток крови из мазков крови. Сегментация этих цифровых изображений аномальных клеток включает регионы ядра, цитоплазмы и внешней области фона вокруг клетки. По ним вычисляются внутренние морфологические характеристики каждого из этих регионов ядра, цитоплазмы и внешней области клетки. Автоматическое распознавание и классификация аномальных клеток крови проводится на основе характеристик, рассчитанных для этих регионов. Такие аномальные клетки классифицируются для помощи в диагностике при гематологических заболеваниях. Предложенное изобретение включает компьютерные программы, адаптированные для выполнения некоторых этапов изобретения.
В решении рассмотрены методы предобработки. Соответствующие процедуры не увеличивают информацию, присутствующую в данных, но увеличивают динамический диапазон свойств изображения для облегчения обработки. Некоторые методы предварительной обработки, которые могут использоваться, включают фильтрацию изображений путем применения фильтров: Гаусса, медианного, Винера, с целью уменьшения уровня шума. В рассматриваемом подходе применяются препараты, окрашенные по методике Май-Грюнвальд-Гимза. Окраска препарата позволяет лучше определить цвет для определения лучших компонент для сегментации. В решении при сегментации используется два варианта: первый - сегментация контуров методом обнаружения контуров по компоненте Н цветового пространства HSV, второй - группировка и преобразование. Процедура описания аномальных клеток осуществляется по текстурным характеристикам в цветовом пространстве Lab. Классификация осуществляется на основе метода главных компонент. Доля клеток, неправильно классифицированных, составила 1,93%.
Однако предложенное решение не обеспечивает выявления наличия лейкемических клеток, морфологически сходных с лимфобластами в крови или костном мозге, для проведения дифференциальной диагностики с другими лимфопролиферативными заболеваниями, установление взаимосвязи морфологических и текстурных характеристик изображений клеток крови и костного мозга с экспрессией ключевых антигенов острых лимфобластных лейкозов при первичной диагностике, в рецидиве, в ремиссии и в ходе анализа минимального числа опухолевых клеток при остаточной болезни в онкологии.
По мнению заявителя, наиболее близких аналогов заявленного решения нет.
Технический результат предлагаемого изобретения заключается в получении дополнительных независимых объективных критериев при дифференциальной диагностике острого лимфобластного лейкоза, установлении корреляций между структурой бластов и их иммунофенотипическим статусом, определение взаимосвязи между результатами морфологического исследования и данными проточной цитометрии, при установлении иммуноподвариантов острого лимфобластного лейкоза. Это обеспечит уточнение методов первичной диагностики, выявление рецидивов, что позволит персонифицировать подходы к терапии онкологических больных, тем самым повысить качество медицинского обслуживания населения.
Указанный технический результат заявленного решения достигается в способе распознавания структуры ядер бластов крови и костного мозга с применением световой микроскопии в сочетании с компьютерной обработкой данных для определения В- и Т-линейных острых лимфобластных лейкозов за счет получения компьютерным анализатором цветного изображения с мазков, последующего выделения на изображении лейкоцитов и получения бинарного изображения, на котором последовательным сканированием изображения проводят процедуру заполнения пустот, определяют области бинарного изображения, соответствующие областям лейкоцитов на цветном изображении, по полученным областям измеряется пространственно-яркостное распределение пикселей изображения и рассчитываются текстурные индексы для представлений цветовых моделей, на основе которых формируют матрицу числовых индексов, для классификации полученные индексы сравнивают с индексами, формируемыми на основе данных морфоцитохимических и иммунофенотипических исследований, проведенных по мазкам, и данных компьютерного анализа, проведенных для эталонных объектов, полученные индексы заносят в базу знаний, по результатам которых определяют индекс структуры ядра для сопоставления данных компьютерного анализа и иммунофеннотипа при дифференциальной диагностике острого лейкоза.
В частном случае цветное изображение получают с мазков крови или костного мозга. Изображение, полученное с препарата крови может, свидетельствовать о возможности наличия заболевания острый лейкоз, а изображение, получаемое с препаратов костного мозга, служит для подтверждения диагноза острый лейкоз.
Также для выделения изображений лейкоцитов осуществляют расчет по гистограмме в автоматическом режиме с последующим анализом выделенных областей и разделением их с использованием трансформации расстояний и роста регионов. Предложенное решение позволяет автоматизировать анализ и уменьшить время вычислений для снижения трудоемкости анализа.
Кроме того, для поиска пустот внутри границы клеток крови осуществляют процедуру заполнения пустот внутри области изображения лейкоцита по бинарной картинке с использованием медианного фильтра. Данная процедура необходима для восстановления целостности клеток и расчета характеристик по ядрам лейкоцитов, т.к. наличие пустот приводит к ложным расчетам.
Также процедуру заполнения пустот внутри области лейкоцита осуществляют на основе анализа связанных областей.
Расчет текстурных индексов осуществляется для всех компонент цветовых моделей из ряда RGB, XYZ, HSL, Lab, Luv, LHC, HLS, HSV, YUV, YIQ, YCbCr, CMY. Предложенный набор цветовых компонент позволяет выбрать наиболее оптимальные цветовые компоненты для нахождения текстурных индексов, характеризующих структуру ядра.
Для каждой цветовой компоненты проводят расчет текстурных индексов по матрицам пространственной смежности, матрицам длин серий и вейвлет-характеристикам для определения оптимальных индексов структуры ядра в условиях близких кластеров.
Классификацию изображений лейкоцитов осуществляют по сформированным двумерным матрицам, где по столбцам располагаются значения индексов, а по строкам изображения лейкоцитов. Предложенный подход позволяет визуализировать результаты классификации лейкоцитов и при необходимости провести экспертное уточнение их типа. В качестве эталонов использовались данные по типу лейкоцитов, полученные по результатам морфоцитохимических и иммунофенотипических исследований и по оценкам экспертов. Это позволило выполнить оценку эффективности заявленного способа.
Ниже приведен пример конкретной реализации предложенного способа. Компьютерная микроскопия в системе «АТЛАНТ» проводилась на окрашенных мазках костного мозга 38 больных ОЛЛ. По результатам морфоцитохимических и иммунофенотипических исследований у 17 больных был установлен Т-ОЛЛ, у 21 больных установлен В-ОЛЛ. Морфоцитохимическое и иммунофенотипическое исследования были проведены в лаборатории иммунологии гемопоэза РОНЦ им. Н.Н, Блохина (заведующий лабораторией профессор д.м.н. Н.Н. Тупицын). Получены изображения клеток в цветовой модели RGB на основе измерений функции яркости в трех спектральных диапазонах, соответствующих красному (R), зеленому (G) и синему (В) участкам спектра видимого электромагнитного излучения (автоматизированный микроскоп Olympus ВХ43 со спектрозональной камерой Imperx IPX-4M1ST-GCFB). Изображения сохранялись в формате BMP, с цветовой кодировкой RGB24 (свыше 16 млн цветов).
В ходе исследования получено 4930 изображения лимфобластов костного мозга, из них 2048 изображений клеток у больных с Т-ОЛЛ, 2882 изображений клеток у больных с В-ОЛЛ. Для полученных изображений рассчитывались текстурные и вейвлет-характеристики по цветовым компонентам полутоновых изображений цветовых моделей RGB, XYZ, HSL, Lab, Luv, LHC, HLS, HSV, YUV, YIQ, YCbCr, CMY. При этом расчет текстурных характеристик проводился для областей на изображениях лимфобластов размером 45×45 пикселей, вписанных в изображения ядер клеток. Для разделения клеток разных типов рассчитывалось 513 текстурных характеристик для каждой из рассматриваемых клеток, затем определялись средние значения для выборки клеток в препарате каждого из пациентов.
По полученным средним значениям характеристик проводилось распознавание типа ОЛЛ, с применением линейного классификатора с функциями расстояния Евклида, Манхеттена и Чебышева в двумерном пространстве признаков. Для анализа были использованы все возможные пары признаков из рассчитанных 513 типов текстурных характеристик.
По результатам сравнения результатов классификации типов ОЛЛ для различных пар текстурных признаков была определена пара признаков MENT, MRENGE-1, при которой распознавание типа ОЛЛ происходило с минимальной ошибкой. Индекс «ENT» соответствует текстурному признаку «энтропия», рассчитанного в цветовом пространстве RGB для координаты R (красный цвет), а индекс «RENGE-1» соответствует значению вейвлет-признака «относительный диапазон», рассчитанного в цветовом пространстве YUV для цветоразностной компоненты U.
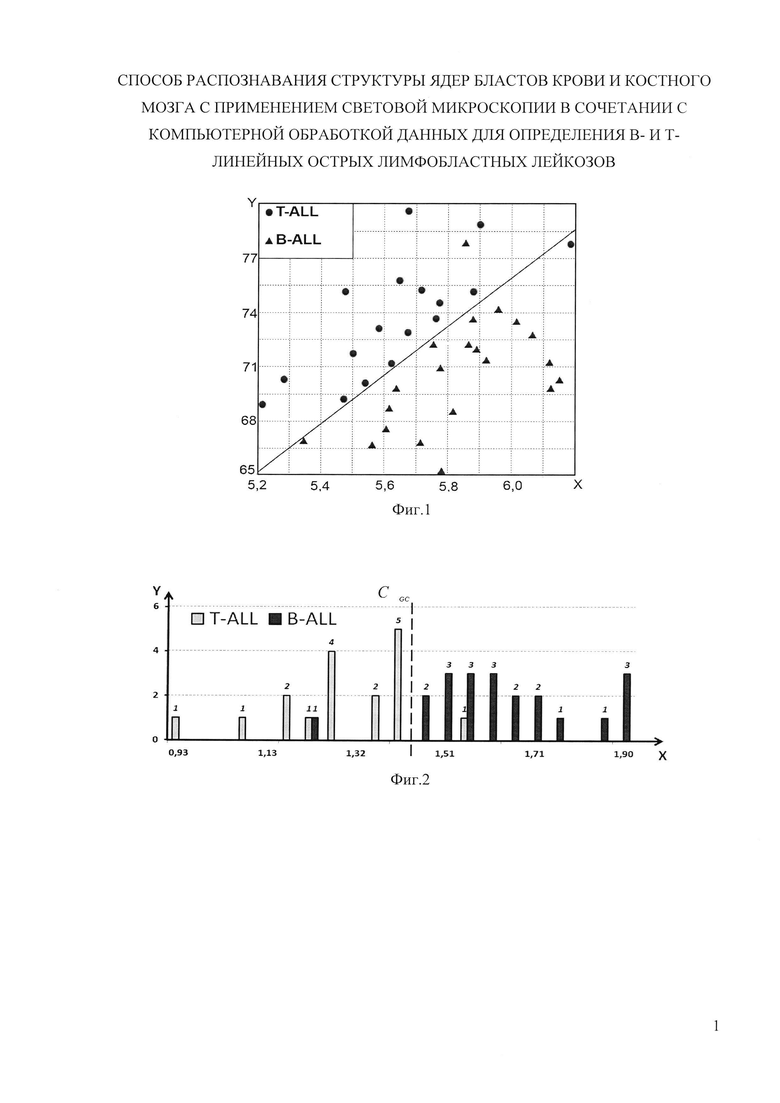
Графическое представление распределения двух классов (Т-ОЛЛ и В-ОЛЛ) в двумерном пространстве признаков представлено на фиг. 1. По координатным осям отложены признаки: по оси абсцисс отложен первый признак Х=MENT, по оси ординат второй признак Y=MRENGE-1.
Таким образом, по указанным признакам можно судить о варианте ОЛЛ (Т- или В- типа). Использование сочетания текстурных признаков на основе вейвлет-характеристик и матрицы пространственной смежности позволило достичь точности в 95%.
Для практической оценки типа клетки предложен обобщенный критерий, рассчитываемый с использованием найденных признаков. Значение этого критерия рассчитывается по формуле 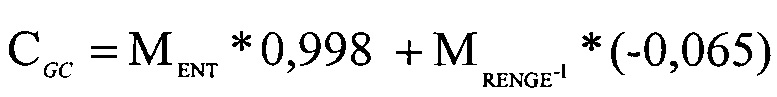 .
.
Гистограмма распределения признака CGC для двух классов пациентов (с Т и В типами ОЛЛ) представлен на фиг. 2
Используя в качестве критерия значение признака CGC, равное 1,405, можно проводить диагностику вариантов острого лимфобластного лейкоза по правилу: если значение критерия CGC больше значения 1,405, то принимается решение, что клетки соответствующего препарата принадлежат В-ОЛЛ типу, если меньше, то Т-ОЛЛ типу.
Таким образом, предложенный способ распознавания структуры ядер лейкоцитов крови и костного мозга при определении Т- и В-вариантов острого лимфобластного лейкоза с применением систем компьютерной микроскопии показал его применимость для установления Т-ОЛЛ и В-ОЛЛ варианта острого лимфобластного лейкоза.
Анализ данных полученных при исследованиях бластов с помощью автоматизированных систем на окрашенных мазках костного мозга при ОЛЛ позволяет выявить закономерную взаимосвязь между строением ядер бластов и их антигенным статусом. Полученные параметры были формализованы. В результате работы был разработан метод дифференциальной диагностики В- и Т-линейных ОЛЛ. Этот подход позволяет уточнить вариант заболевания и ускорить диагностический процесс. Использование световой микроскопии в сочетании с компьютерной обработкой данных может способствовать быстрому принятию клинических решений и адекватному подбору терапевтических схем у пациентов с ОЛЛ.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ распознавания структуры ядер бластов крови и костного мозга | 2021 |
|
RU2785607C1 |
| Способ диагностики онкологического заболевания крови | 2022 |
|
RU2803281C1 |
| Способ детализации структурных элементов медико-биологических объектов исследования | 2023 |
|
RU2803277C1 |
| СПОСОБ АВТОМАТИЗИРОВАННОГО АНАЛИЗА КЛЕТОК КРОВИ ПОСРЕДСТВОМ ОПИСАНИЯ ЛЕЙКОЦИТОВ НА ОСНОВЕ ОПТИЧЕСКИХ ОСОБЕННОСТЕЙ СТРУКТУРЫ ЯДЕР | 2014 |
|
RU2612007C2 |
| СПОСОБ МИКРОСКОПИЧЕСКОГО ИССЛЕДОВАНИЯ ОБРАЗЦА, СОДЕРЖАЩЕГО МИКРООБЪЕКТЫ С РАЗНОРОДНЫМИ ЗОНАМИ | 2006 |
|
RU2308745C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ОСТРЫХ ЛЕЙКОЗОВ С ПОМОЩЬЮ КЛЕТОЧНОГО БИОЧИПА | 2017 |
|
RU2681651C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТЕЧЕНИЯ ОСТРЫХ ЛЕЙКОЗОВ | 2010 |
|
RU2416795C1 |
| Способ обнаружения и классификации цветных изображений ядросодержащих клеток крови и костного мозга при формировании диагностического заключения в онкогематологии | 2024 |
|
RU2837299C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ХАРАКТЕРА ТЕЧЕНИЯ ОСТРОГО ЛИМФОБЛАСТНОГО ЛЕЙКОЗА У ДЕТЕЙ | 1999 |
|
RU2152028C1 |
| Способ прогнозирования эффективности лечения больных острыми миелобластными лейкозами противоопухолевыми препаратами даунорубицином и цитозин-арабинозидом | 2019 |
|
RU2702657C1 |
Изобретение относится к области медицины, а именно к медицинской диагностике, и может быть использовано для распознавания структуры ядер бластов крови и костного мозга с применением световой микроскопии в сочетании с компьютерной обработкой данных для диагностики В- и Т-линейных острых лимфобластных лейкозов. Получают компьютерным анализатором цветное изображения с мазков. Осуществляют выделение на изображении лейкоцитов и получают бинарное изображение, на котором последовательным сканированием изображения проводят процедуру заполнения пустот внутри границы клетки. Измеряют пространственно-яркостное распределение пикселей изображения. Определяют значение текстурных индексов, характеризующих структуру ядра, для представлений цветовых моделей лейкоцитов. На основе индексов формируют матрицу числовых текстурных индексов структуры ядра, где по столбцам располагают значения индексов, а по строкам изображения лейкоцитов, для распознавания структуры ядер бластов. Способ обеспечивает проведение дифференциальной диагностики В- и Т-линейных ОЛЛ за счет сочетания световой микроскопии с компьютерной обработкой данных. 6 з.п. ф-лы, 2 ил.
.
1. Способ распознавания структуры ядер бластов крови и костного мозга с применением световой микроскопии в сочетании с компьютерной обработкой данных для диагностики В- и Т-линейных острых лимфобластных лейкозов, заключающийся в получении компьютерным анализатором цветного изображения с мазков, последующем выделении на изображении лейкоцитов и получении бинарного изображения, на котором последовательным сканированием изображения проводят процедуру заполнения пустот внутри границы клетки, измеряют пространственно-яркостное распределение пикселей изображения и определяют значение текстурных индексов, характеризующих структуру ядра, для представлений цветовых моделей лейкоцитов, на основе которых формируют матрицу числовых текстурных индексов структуры ядра, где по столбцам располагают значения индексов, а по строкам изображения лейкоцитов, для распознавания структуры ядер бластов.
2. Способ по п. 1, в котором цветное изображение получают с мазков крови или костного мозга.
3. Способ по п. 1, в котором выделение изображений лейкоцитов осуществляют по гистограмме в автоматическом режиме с последующим анализом выделенных областей и разделением их с использованием трансформации расстояний и роста регионов.
4. Способ по п. 1, в котором процедуру заполнения пустот внутри области изображения лейкоцита осуществляют по бинарному изображению с использованием медианного фильтра.
5. Способ по п. 1, в котором процедуру заполнения пустот внутри области изображения лейкоцита осуществляют на основе анализа связанных областей.
6. Способ по п. 1, в котором расчет текстурных индексов осуществляется для всех компонент цветовых моделей из ряда RGB, XYZ, HSL, Lab, Luv, LHC, HLS, HSV, YUV, YIQ, YCbCr, CMY.
7. Способ по п. 1, в котором расчет текстурных индексов рассчитывают по матрице пространственной смежности, матрицы длин серий и вейвлет-характеристик.
| УСТРОЙСТВО КОРПУСА ЗАЩИТНОГО ПРИСПОСОБЛЕНИЯ | 2007 |
|
RU2428215C2 |
| СПОСОБ РАСПОЗНАВАНИЯ ИЗОБРАЖЕНИЯ ТЕКСТУРЫ КЛЕТОК | 2008 |
|
RU2385494C1 |
| RU 2052199 C1, 10.01.1996 | |||
| СПОСОБ ДИАГНОСТИКИ ФОРМ ХРОНИЧЕСКОГО ЛИМФОЛЕЙКОЗА | 1992 |
|
RU2068995C1 |
| WO 2004055731 A2, 01.07.2004 | |||
| НИКИТАЕВ В.Г | |||
| и др | |||
| Модель автоматизации морфологического анализа клеток для диагностики и обучения | |||
| Успехи современного естествознания, 2008, N8, с.141-142. | |||
Авторы
Даты
2018-06-28—Публикация
2017-12-12—Подача