Изобретение относится к области медицины - стоматология/детская стоматология и микробиология/бактериология, и может быть использовано для неспецифической профилактики и входить в комплексное лечение кариеса молочных зубов воздействием на кариесогенные Streptococcus mutans в составе микробиома языка и зубного налета язычной поверхности зубов у детей раннего возраста.
Кариес - инфекционное заболевание, не угрожающее жизни, но значительно влияющее на функциональные свойства организма, рост ребенка и снижающее качество его жизни (American Academy of Pediatric Dentistry. Symposium on the prevention of oral disease in children and adolescents. Chicago. 2005: Conference papers. Pediatr Dent 2006. 196-198).
Несмотря на меры, направленные на снижение уровня кариеса у детей, распространенность и тяжесть кариозного процесса в различных регионах нашей страны остается на высоком уровне (Кисельникова Л.П., Токарева А.В. Кариес раннего детского возраста и его осложнения. 9-th Congress of the European Academy of Pediatric Dentistry, Croatia, Dubrovnik, 2008, p. - 107.; Скрипкина Г.И., Смирнов С.И. Модель развития кариозного процесса у детей // Стоматология детского возраста и профилактика. 2012. №3. С. 3-7). При этом практически в 2,5-3 раза увеличилось поражаемость кариесом молочных зубов среди детей раннего и дошкольного возраста (Харитонова Т.Л., Лебедева С.Н., Казакова Л.Н. Ранняя профилактика кариеса зубов у детей // Саратовский научно-медицинский журнал. 2011. Том 7 №1. Приложение. С. 260.; Шаковец Н.В. и др. Факторы риска возникновения раннего детского кариеса по результатам трех стран // Стоматология детского возраста и профилактика стоматологических заболеваний: Сб. трудов VII научно-практической конференции с международным участием / Москва, Санкт-Петербург, 16 мая 2011 года, под редакцией проф. Кисельниковой Л.П., Дроботько Л.Н. С. 213-215). По данным зарубежных авторов, наибольший рост распространенности и интенсивности кариеса наблюдается в возрастной категории от 2 до 5 лет (Borutta A., Wagner М., Kneist S. Early Childhood Caries: A Multi-Factorial Disease // OHDMBSC; Splieth С.H., Treuner A., Berndt C. Oral health in toddlers. und Gesundheits
und Gesundheits  derung. 2009. 4. P. 119-123).
derung. 2009. 4. P. 119-123).
В связи с высокой распространенностью данной патологии предложен специальный термин: «Early Childhood Caries», характеризующий наличие одной или более кариозной, удаленной по поводу осложненного кариеса или запломбированной, поверхности в любом временном зубе у детей в возрасте 71 месяца и ранее (Milnes A. R. Description and epidemiology of nursing caries. J Public Health Dent 1996; 56:38-50; Tinanoff N, Kaste L M, Corbin SB. Early childhood caries:positive beginning. Comm Dent Oral Epidemiol 1998; 26: 117-119). Кариес раннего возраста уже давно признан клиническим синдромом, описанным Belterami в 1930-е годы как "Les dents noire de tout-petits / "черные зубы самых маленьких" (Belterami G. Les dents noires de tout-petits. 
 In Belterami G (ed). La
In Belterami G (ed). La  infantile. Marseille: Leconte 1952).
infantile. Marseille: Leconte 1952).
При кариесе раннего детского возраста временные зубы поражаются практически сразу после их прорезывания. Кариозный процесс характеризуется быстротой течения, распространением в ширину, множественным поражением зубов в порядке их прорезывания, кроме резцов нижней челюсти. Редкое поражение нижних резцов объясняется лучшим самоочищением из-за положения языка и обильного омывания их слюной (Кузьмина Э.М. Профилактика стоматологических заболеваний. - М.: Медицина. 2001. 32 с.). Зубы ребенка особенно нуждаются в бережном и эффективном уходе в течение первого года после прорезывания, а также в период минерального созревания эмали, от 2 до 5 лет (Харитонова Т.Л., Лебедева С.Н., Казакова Л.Н. Ранняя профилактика кариеса зубов у детей // Саратовский научно-медицин. журнал. 2011. Т. 7, №1 прил. С. 260-262).
Прорезавшиеся или подвергшиеся профессиональной гигиене зубы в течение нескольких минут покрываются слоем белков и гликопротеинов слюны / пелликулой. Именно эта пленка, а не эмаль зуба является субстратом для адгезии бактерий (Asikainen S, Chen С: Oral ecology and person to person transmission of Aa and Pg. Periodontology 2000). В современной трактовке бактериальный налет называют «биопленкой», которая является специализированной бактериальной экосистемой, обеспечивающей жизнеспособность и сохранение составляющих ее видов микроорганизмов и увеличение общей популяции (Caufield P. W., Cutter G. R., Dasanayake А. Р.: Initial a cquisition of mutans streptococci by infants: evidence for a discrete window of infectivity. J DentRes 1993, Леус П.А. Коммунальная стоматология, 2000). Согласно концептуальной модели зубной биопленки по Jill S. Nield-Gehrig (2003) она состоит из бактерий; микроколоний, агрегатов микроколоний бактерий, экстрацеллюлярного полисахаридного матрикса EPS-субстанции, эпителиоцитов, компонентов слюны, пищи и клеток крови. Биопленка, ассоциируемая с состоянием здоровья зубов и пародонта / Health-associated dental plaque. Микробиологический портрет здоровой пленки: S. sanguinis, S. mitis, S. orates, S. salivarium, Veillonella, Actinomycetaceae, Haemophilus, Bacteroides. Биопленка, ассоциируемая с кариесом, пародонтитом, периимплантитом / Disease-associated dental plaque представлена нарушением микробного гомеостаза: доминирование ацидогенных и ацидотолерантных Streptococcus spp. и Lactobacillus spp., утрата доминирования основной симбионтной и увеличение роли транзиторной микрофлоры (О.С. Гилева, конференция «Опережая будущее», Москва, 2012, Эндодонтия тудэй. - 02.2012).
Патогенные бактерии не проявляют агрессивности против организма хозяина до тех пор, пока количество и степень их вирулентности не достигает необходимого уровня, чтобы эффективно преодолеть защиту организма хозяина. In vitro резистентность биопленки антибиотикам в 500-1000 раз превышает аналогичную способность отдельных колоний бактерий (Allais G. Биопленка полости рта, Новое в стоматологии. 2006).
Микрофлора как важнейшая структурно-составная часть многокомпонентной системы полости рта - индикатор стоматологического и системного здоровья, состояния окружающей среды (О.С. Гилева, конференция «Опережая будущее», Москва, Эндодонтия тудэй. 2012). Нормальная флора полости рта принимает участие в формировании зубной бляшки / зубного налета. Известно, что более 800 видов изученных микроорганизмов населяют полость рта здорового человека, сохраняя экосистему и не нарушая гомеостаз (Slavkin, 1999, Чайковская И.В., 2002, Зеленова Е.Г. и др., 2004, Тец В.В., 2008). На сегодняшний день доказана ведущая роль микрофлоры в возникновении кариозного процесса (Кнайст С., Маслак Е., Царе Р., Берзина С., Скривеле С., Терехова Т., Шаковец Н., Вагнер М., де Мура-Зибер В., де Мура Р., Берутта А. Биологические и социальные факторы риска возникновения раннего детского кариеса // Современная стоматология. 2011. №1. С. 62-65). Гипотеза о роли стрептококков в развитии кариеса была принята в США для практического руководства с 1960 года после исследований, проводившихся в стране с 40-х годов XX века (Shafer W. G., A textbook of oral pathology, 1974).
Грамположительные стрептококки вида Streptococcus mutans, инициируют формирование зубного налета / биологической пленки на поверхности зуба и обеспечивают, за счет коадгезии, накопление других представителей патогенной флоры (Кузнецов Е.А., Царев В.Н. и др., 1996; Burt and Pai, 2001; Чайковская И.В., 2002; Berkowitz R., J.Causes. 2003, Тец В.В., 2008, Скрипкина Г.И., 2014; Хавкин А.И., Ипполитов Ю.А., Алешина Е.О., Микробиота и болезни полости рта, 2015. 78-81). Стрептококки составляют значительную долю микрофлоры зубной бляшки, до 80% от общего количества микроорганизмов полости рта (Weiilherell I.А. Composition of dental enamel // Brit. Med. Bull. 1975. - Vol. 31, №2. P. 1415-1420; Максимовский Ю.M. и др., 2009). Наиболее важным фактором вирулентности Streptococcus mutans является их процветание в кислой среде (Овруцкий Г.Д., Леонтьев В.К., 2010). В результате брожения углеводов бактерии кариесогенного зубного налета производят органические кислоты, воздействующие на восприимчивую эмаль зубов, и в результате развивается кариес (Seow KW. Biological mechanisms of early childhood caries. Community Dent Oral Epidemiol. 1998. 26. 1 Suppl: 8-27). Эти свойства позволяют стрептококкам первыми заселять различные биотопы полости рта ребенка (В.С. Крамарь с соавт., 1992)
Основными биотопами полости рта являются слизистые оболочки, спинка языка, десневая борозда, ротовая жидкость и зубной налет (Зеленова Е.Г. Заславская М.И., Салина Е.В., Рассанов С П. Микрофлора полости рта: норма и патология: Учебное пособие. Н. Новгород: Изд. НГМА, 2004. 158 с.) По обсемененности стрептококками отдельных биотопов имеются разноречивые данные (Зеленова Е.Г. и др., 2004, Скрипкина Г.И., 2014). Различные виды оральных стрептококков избирательно колонизируют определенные участки: S. mitior - буккальные эпителиоциты слизистой оболочки; S. mutans - адсорбируется на твердой поверхности зубов. Частота обнаружения S. mutans в слюне и зубодесневых карманах составляет 100%, в 1 мл слюны - 1,5⋅105. Численность оральных стрептококков, вариабельна, но является информативным показателем, отражая степень гомеостатических нарушений (Разживин, А.П. Дисбиотические состояния у детей: клиника, диагностика и лечение: уч. пособие. Н. Новгород: НГМА. 1999. 123 с.).
Инфицирование кариесогенными видами S. mutans и их колонизация в бороздках языка, возможны еще до прорезывания зубов (Berkowitz 2003), что подтверждает путь передачи Streptococcus mutans от матери к ребенку (Кузьмина Э.М. Профилактика стоматологических заболеваний: учебное пособие. Москва, 2001; Кузьмина Э.М. Профилактика кариеса зубов как важнейший аспект сохранения стоматологического здоровья детей. // Рос. педиатр. Журн. - 2006. - №6). Исследования, проведенные (Thorhild I, Lindau-Johnson В, Twetman S, 2002, Berkowitz, 2003, Шаковец H.В., 2009, Caufield, Ratanapridakul et al, 1988, Loveren, Buijsetal, 2000; Кузьмина Э.M., И.И. Лысенкова, Профилактика кариеса зубов как важнейший аспект сохранения стоматологического здоровья детей, // Рос. педиатр. Журн. 2006. №6; Кисельникова Л.П. Индивидуальная профилактика кариеса у детей школьного возраста / Клинич. Стоматология. 2006). Дети, посещающие один детский сад, имеют идентичные штаммы бактерий в слюне (Berkowitz, 2003), и дети, которые находятся на домашнем воспитании, имеют идентичные штаммы стрептококков и их титр с матерью и отцом, что подтверждает горизонтальный путь передачи кариесогенных стрептококков (Seow K W., Biological mechanisms of early childhood caries. Community Dent Oral Epidemiol. 1998; 26:8-27; Caufield P. W, Griffen A L. Dental Caries. An infectious and transmissible disease. Pediatr Clin North Am. 2000; 47:1001-19). Чем раньше полость рта заселяется 5. mutans, тем выше распространенность кариеса к 4 годам жизни ребенка (American Association of Pediatric Dentistry (AAPD). Dental care for your baby. 2009). Возраст, в котором ребенок инфицируется S. mutans, очень важен и определяет риск развития у него кариеса. Исторически сложилось представление о том, что инфицирование ребенка происходит между 19 и 31 мес. в так называемое дискретное окно инфекции. Однако в настоящее время уже доказано, что этот вид инфекции может встречаться и в более раннем возрасте. Так, выявление S. mutans у годовалых детей было наиболее эффективным прогностическим критерием кариеса, диагностированного у тех же детей 3,5 лет. По современным представлениям, средний возраст инфицирования составляет 15,7-16,0 мес.; к этому сроку 84% детей имеют высокий уровень колонизации полости рта S. mutans. Клинические исследования, проведенные в последние годы, показали, что S. mutans обнаруживаются в полости рта беззубых младенцев до 6 мес. Их экологическая ниша располагается в бороздках спинки языка.
Бактериологические исследования показали, что у детей с ранним кариесом S. mutans составляют 30% культивируемой флоры зубной бляшки. Такая высокая плотность обсемененности поверхностей зубов этим видом бактерий ассоциируется с кариозными поражениями, меловыми пятнами и неповрежденными поверхностями зубов, соседствующими с кариозно измененными участками. В противовес этому, в зубной бляшке детей с низкой активностью кариеса, S. mutans обычно составляют менее 0,1% микрофлоры. В.Г. Корчагин в своем исследовании, проведенном на пациентах 12-14 лет, достоверно показал, что у детей с более высокой обсемененностью зубного налета S. mutans отмечается высокая интенсивность кариеса 6,57±0,63, в то время как у детей с низкой интенсивностью кариеса 3,30±0,66 - S. mutans в зубной бляшке меньше. Уровень обсемененности зубного налета бактериальной микрофлорой автор связывает с резистентностью организма. Исследования Alaluusua S. и Renkonen О. показали, что дети, зубная бляшка у которых в 2 года уже содержала S. mutans, к 4 годам страдали активными формами кариеса, со значениями кпу 10,6, в то время как у детей, у которых колонизация полости рта произошла позднее, индекс кпу был в пределах 3,4. Аналогичные данные представлены В. Kohler и соавт.
Отсюда следует вывод о том, что чем раньше полость рта ребенка колонизируется S. mutans, тем выше шанс покрытия незрелой эмали недавно прорезавшихся зубов зубным налетом, свойства которого будут очень сильно зависеть от потребляемой пищи, особенно если в ней есть легко ферментируемые углеводы. Из всех углеводов сахароза наиболее значимый агрессивный фактор, так как преобразует некариесогенные / anticariogenic продукты в кариесогенные. Сахароза способствует увеличению пропорции Streptococcus mutans и лактобактерий и одновременно снижается уровень Streptococcus sanguini. (Douglass J.M. Response to Tinan off and Palmer: Dietary determinants of dental caries and dietary recommendations for preschool children. J Public Health Dent 2000; 207-209; Paes Leme, H. Koo, С.M. Bellato, G. The Role of Sucrose in Cariogenic Dental Biofilm Formation - New Insight. J Dent Res 2006, 878-887).
Для такого многофакторного заболевания как кариес зубов, проведение стереотипных профилактических мероприятий не гарантирует высокий конечный результат. Необходимо отказаться от шаблонного подхода к профилактике кариеса зубов и определять индивидуальную предрасположенность человека к этому заболеванию (Пузикова О.Ю. Прогнозирование развития кариеса зубов с учетом интегрированных показателей и математического моделирования: дис. канд. мед. наук. Омск, 1999. 183 с.). Важно проводить профилактику, базирующуюся на донозологической диагностике и прогнозировании заболевания (Laurisch L. ZWR., 1990; Мельник А.И. автореф. дис. 1991; Li Y., W. Wang J. Dent. Res., 2002.; M. Fontana et al., J. Dent. Res., 2011; Профилактика кариеса сегодня/Новое в стоматологии. 2011. №6. 178. С 6-15.; Slayton R. Оценка риска развития кариеса // Маэстро стоматологии. 2007. №25. С 23-26; J. Tsubonchi et al. A study of dental caries and risk factors among Native American infants / // J Dent Child. - 1995. - Vol. 62. - P. 283-287).
Донозологическое состояние - переход от нормы к патологии, получившее название «донозологической диагностики», является основой формирования групп здоровья и выработки первичных профилактических мероприятий (Risik of aktoren ftir das Nursingottle-yndrome / Ch. Hirsh et al. // Oralprophylaxe. 2000. Vol. 22. P. 103-107; Robko F. J. Haufigkeit der Nuckelflaschen karies beiVorschulkindern in einer westdeutschen Grobstadt / F. J. Robko, M. Buitkamp // Oralprophylaxe. 2002.Vol.24. P. 59-65; Sellmann H. H. Kariesrisikotest jetzt auch als DNSSonden-Test // Dental Spigel. 2003. Vol. 1. P. 44-45; van Palenstein Helderman W.H., W. Soe, M.A. van't H о Rise factors of early childhood caries in a Southeast Asian population. J. Dent. Res. 2006. Vol. 85, №1. P. 85-88; Горбунова И.Л. Использование ДНК технологий для раннего выявления предрасположенности к кариесу. Стоматология. 2006. №4. С. 18-19). Массовая донозологическая диагностика должна явиться одним из важнейших элементов в системе охраны здоровья детей, так как направлена не на поиск болезни, а на установление уровня здоровья (Сунцов В.Г., Стоматологическая профилактика у детей, Москва, 2001. 344 с.). Раннее выявление, устранение или ослабление факторов риска уменьшают прирост кариеса у детей. Профилактика кариеса зубов является залогом стоматологического здоровья на всю жизнь. Сохранение здоровых временных зубов до физиологической смены позволит избежать многих проблем в будущем.
Таким образом, вопрос профилактики риска развития раннего детского кариеса и разработка индивидуального подхода к лечебно-профилактическим методам коррекции и, собственно лечению, весьма актуален.
Лечебный контроль за неспецифической биопленкой является простым и обычным эффективным средством в лечении кариеса и заболеваний пародонта (Кузьмина Э. М. Профилактика стоматологических заболеваний: учебное пособие. Москва, 2001., Socranssky S. S., Haffajee A.D.: Dental Biofilms: difficult the rapeutictargets. Periodontology 2002). Лечение должно охватывать всю поверхность полости рта и прилегающей поверхности глотки, а не только область зубов и пародонта (Theilade Е. Factors controlling the microflora of the healthy mouth. In: Human microbial ecology. Hill M.J., Marsh P.D. Boca Raton, F L, CRC Press 1990).
В связи с вышеизложенным, наши исследования посвящены мерам неспецифической донозологической профилактики, лечения и лечебного контроля за наиболее уязвимой группой риска развития кариеса - детей раннего возраста путем уменьшения титра бактерий Streptococcus mutans в биотопах полости рта, их адгезивной и коадгезивной способности в наиболее обсемененных кариесогенными микроорганизмами биотопах - микробиоме спинки языка и зубном налете язычной поверхности молочных зубов.
В нашем исследовании, проводившимся в период с 2013 по 2015 г.г., использовались готовые к применению сертифицированные препараты коллоидного серебра, содержащие наночастицы Ag+. Наш выбор препаратов для неспецифической профилактики и лечения кариеса зубов у детей раннего возраста был обусловлен уникальностью молекул Ag+. Наиболее кратко свойства серебра как антисептика изложены в статье по ссылке в Интернет-ресурсе: http://www.o8ode.ru/article/tawa/bacterios.htm. Бактерицидные свойства серебра известны с глубокой древности, поскольку оно, как и золото, встречалось в самородном состоянии и его не приходилось выплавлять из руды. Еще в Древней Индии с его помощью обеззараживали воду, а персидский царь Кир хранил воду в серебряных сосудах. Люди издавна ели с серебряных ложек, хранили молоко и воду в ведрах из серебра. В религиозных индусских книгах написано об обеззараживании воды путем кратковременного погружения в нее раскаленного серебра. В настоящее время обеззараживание воды с помощью серебра производят электрохимическим методом.
Серебро является очень редким химическим элементом на нашей планете. Среднее содержание этого серебра в земной коре составляет около 70 мг/т. Даже в глинистых сланцах, где его концентрация считается максимальной, содержание серебра едва достигает 1 г/т. Химическая активность серебра выше золота, его концентрация в водах Мирового океана в 10 раз выше, чем у золота, и составляет около 0,04 мкг/л.
Серебро обладает бактерицидным, противовирусным, выраженным противогрибковым и антисептическим действием и служит высокоэффективным обеззараживающим средством в отношении патогенных микроорганизмов, вызывающих острые инфекции. Действие ионов серебра распространяется более чем на 650 видов бактерий. Для сравнения - спектр действия любого антибиотика 5-10 видов бактерий.
Эффективность бактерицидного действия ионов серебра объясняется их способностью подавлять работу фермента, с помощью которого обеспечивается кислородный обмен у простейших организмов. Как только на поверхности микробной клетки сорбируются ионы серебра, они проникают внутрь клетки и ингибируют ферменты - дыхательной цепи, разобщая процессы окисления и окислительного фосфорилирования в микробных клетках, в результате чего клетка гибнет. Имеются данные, свидетельствующие об образовании комплексов нуклеиновых кислот ионами серебра, вследствие чего нарушается стабильность ДНК и жизнеспособность бактерий. Одной из причин широкого противомикробного действия ионов серебра является ингибирование трансмембранного транспорта Na+ и Са++.
Серебро обладает более мощным антимикробным эффектом, чем пенициллин, биомицин и другие антибиотики, и оказывает губительное действие на антибиотикоустойчивые штаммы бактерий. На золотистый стафилококк, вульгарный протей, синегнойную и кишечную палочки, представляющие особый интерес для клиницистов, ионы серебра оказывают различное противомикробное действие - от бактерицидного до бактериостатического. См. дополнительные материалы, в которых представлены документированные данные эксперимента по воздействию ионов серебра препаратов «Елена» и «Князь серебряный» на несколько видов АТСС штаммов условно-патогенных бактерий из числа микрофлоры тела человека. Серебро превосходит антибиотики, в отношении золотистого стафилококка и большинства кокков (Брызгунов В.С, Липин В.Н., Матросова В.Р. Сравнительная оценка бактерицидных свойств серебряной воды и антибиотиков на чистых культурах микробов и их ассоциациях. Научн. тр. Казанского мед. ин-та. 1964. Т 14. 121-123). Рядом исследователей установлено, что ионы серебра обладают выраженной способностью инактивировать вирусы осповакцины, гриппа штаммов А-1, В, некоторых энтеро- и аденовирусов, и даже вирус ВИЧ (Валихова С.С., Вольский Н.Н. и др. Способ лечения вич-инфицированных больных. Росс. Патент. 2192870).
Эффект уничтожения бактерий препаратами серебра чрезвычайно велик. Он в 1750 раз сильнее действия той же концентрации карболовой кислоты и в 3,5 раза сильнее действия сулемы. Всего 1 мг/л серебра в течение 30 минут вызывает полную инактивацию вирусов гриппа А, В, Митре и Сендай. Уже при концентрации 0,1 мг/л серебро обладает выраженным фунгицидным действием. При микробной нагрузке 100000 клеток на один литр гибель грибов Candida albicans наступает через 30 минут после контакта с серебром (Голубович В.Н., Работнова И.Л. Кинетика подавления роста Candida udlus ионами серебра. Микробиология. 1974. 43).
Скорость уничтожения зависит от концентрации ионов серебра в растворе: так, кишечная палочка погибает через 3 мин при концентрации 1 мг/л, через 20 мин - при 0,5 мг/л, через 50 мин - при 0,2 мг/л, через 2 ч - при 0,05 мг/л. При этом обеззараживающая способность серебра выше, чем у карболовой кислоты, сулемы и даже таких сильных окислителей, как хлор, хлорная известь, гипохлорид натрия.
При применении допустимых концентраций ионы серебра, убивая всю патогенную и условно-патогенную флору организма, остаются безопасными для собственной полезной флоры организма / сапрофитов. Интересный факт: если при лечении инфекции из-за образования антибиотико-устойчивых форм бактерий приходиться менять препарат каждый 5 дней, то к ионам серебра ни одна бактерия или вирус не образуют устойчивых форм. Ионы серебра оказывают губительное действие на антибиотикоустойчивые формы (Белеванцев В.И., Бондарчук. И.В. Институт неорганической химии СО РАН. Очерк свойств серебра и его соединений. Применение препаратов серебра в медицине. Новосибирск, 1994).
Установлено, что растворы серебра являются самым эффективным средством при непосредственном соприкосновении с поверхностями, гноящимися и воспаленными вследствие бактериального заражения. Результаты применения серебряной воды свидетельствуют об эффективности ее действия при желудочно-кишечных заболеваниях, холециститах, инфекционных гепатитах, холангитах, панкреатитах, дуоденитах, любых кишечных инфекциях без опасения погубить собственную полезную микрофлору и вызвать дисбактериоз. С успехом лечится язвенная болезнь желудка и 12 п.к., так как уничтожаются бактерии хеликобактер - пилори и кампилобактер, постоянно живущие на слизистых оболочках желудка и кишечника и активно поддерживающие эрозивные и язвенные процессы в ЖКТ.
Типичные наночастицы серебра имеют размеры 25 нм. Они имеют чрезвычайно большую удельную площадь поверхности, что увеличивает область контакта серебра с бактериями или вирусами, значительно улучшая его бактерицидные действия.
При этом серебро не просто металл, способный убивать бактерии, но и микроэлемент, являющийся необходимой составной частью тканей любого живого организма. В суточном рационе человека должно содержаться в среднем 80 мкг серебра. При употреблении ионных растворов серебра не только уничтожаются болезнетворные бактерии и вирусы, но и активизируются обменные процессы в организме человека, повышается иммунитет.
Ионы серебра принимают участие в обменных процессах организма. В зависимости от концентрации, его катионы могут как стимулировать, так и угнетать активность ряда ферментов. Под влиянием серебра в два раза усиливается интенсивность окислительного фосфорилирования в митохондриях головного мозга, а также увеличивается содержание нуклеиновых кислот, что улучшает функцию головного мозга. Серебро в разных лекарственных формах применяется в хирургической практике: при поражении костей, мышц, суставов, лимфатических узлов, обусловленном стрепто-стафило-пневмококковой инфекцией, туберкулезной палочкой; в офтальмологии, в ЛОР-практике (Безлепко А.В. Эффективность и безопасность применения колларгола в лечении неатопической бронхиальной астмы. Дисс.… канд. мед. наук, М. 1999. в педиатрии). Применяют серебро / серебряную воду для купания детей, при дерматозах, детской экземе, ожогах. Используют в практике внутренних заболеваний: при лечении гастрита, вирусных энтерита и колита, при эндокринологических заболеваниях и нарушении обмена веществ: сахарная болезнь, диатезы; в практике инфекционных заболеваний: при лечении дизентерии, брюшного тифа, скарлатины, дифтерии; в акушерско-гинекологической практике: при лечении различных воспалительных процессов слизистой оболочки гинекологической сферы и трещин сосков, см. Росс. патент 2411951, 2011 г.; практике кожных заболеваний: при лечении фурункулеза и грибковых поражений кожи; в стоматологической практике: при лечении стоматита, гингивита и других заболеваний полости рта; наружное применение: гнойные раны, гнойничковые заболевания кожи, ожоги, дерматозы, экзема. Бытовое применение серебра / серебряной воды: консервирование напитков, соков, компотов, обеззараживание питьевой воды в эпидемиологически неблагоприятных районах; полив комнатных растений для обеззараживания земли от микроорганизмов, плесени, грибков, дезинфекция посуды, овощей, фруктов, дезинфекция нательного и постельного белья.
На сайте фирмы Faberlic интернет-ресурс: http://shop.faberlic.com/index.php?option=com_catalog&view=goods&id=1000142308855&idcategory=1000111369973; предлагаются к применению зубные щетки с ионами серебра, которые предотвращает размножение бактерий на щетине.
На сайте фирмы «Коралловый клуб» размещены препараты коллоидного серебра в виде раствора «Colloidal silver», 118 мл. Рядом помещен следующий текст. Коллоидное серебро представляет собой новый раствор серебра, который совершенно безопасен для человеческого организма. Данный раствор обладает мощным антибактериальным действием, поэтому его можно использовать в борьбе с бактериями и с дрожжами. Коллоидное серебро использовали для проведения клинических исследований ученые кафедры микробиологии Молодежного университета Бригхема. Они пришли к выводу, что данный раствор является превосходным антисептиком, которому присуще мощное противогрибковое действие, его можно использовать как внутрь, так и наружно, причем в больших дозировках, так как в его составе нет токсических веществ. Данный раствор можно использовать и для профилактики многочисленных заболеваний. Источник: http://www.tiensmed.ru/news/post_new7409.html
Сайт «Здоровый образ жизни» ссылка: https://zdips.ru/, и далее: https://zdips.ru/zdorovoe-pitanie/mineraly/1652-serebro-v-organizme-heloveka.html. Серебро (Ag) - это химический элемент с атомным номером 47. В элементарном виде серебро представляет собой серебристо-белый металл. Серебро пластично, ковко, довольно устойчиво к коррозии и поэтому относится к благородным металлам. Его плотность 10,5 г/см3, что примерно в полтора раза больше, чем у железа.
Ионы серебра пагубно воздействуют на болезнетворные микроорганизмы, оно используется для обеззараживания воды. Нитрат серебра (ляпис, "адский камень") - мощнейший антисептик, способный защитить человека даже от заражения крови в результате попадания в рану трупного яда. Главное при этом - как можно быстрее обработать рану. Нитрат серебра и его коллоидные растворы применяются как вяжущее средство. Серебро используется в качестве пищевой добавки и имеет маркер Е174. Серебро содержится во многих живых организмах. В тканях млекопитающих его концентрация составляет около 0,02 мг/кг веса. Биологическая роль серебра в организме человека до конца не изучена. Самая высокая его концентрация обнаружена в головном мозгу, точнее, в ядрах нейронов - до 0,08% от сухого вещества.
О свойствах серебра пишет автор по ссылке в интернет - ресурсе: http://forum.guns.ru/forummessage/15/4669.html. Действующими - наиболее активными элементами серебра являются ионы, которые благодаря функциональным особенностям электронов пяти уровневых орбит атома серебра вступают в постоянно неустойчивую связь с фрагментами молекулы воды, в результате чего молекулы воды образуют вокруг иона серебра устойчивую оболочку, сохраняющую активное состояние иона серебра в виде стабилизированного гидратированного комплекса. Под защитой водной оболочки ионы серебра легко проникают в ткани живого организма и свободно циркулируют в кровотоке и жидких средах тканей, встречаясь с патогенными микробами, вирусами и грибками, легко проникают через их внешнюю оболочку, а затем соединяются с дыхательным ферментом и, блокируя дыхательную функцию, приводят к их гибели. При этом патогенные микроорганизмы не могут выработать устойчивости к губительному действию ионов серебра, как по отношению к антибиотикам. Полезную флору кишечника ионы серебра не затрагивают, помогая бороться с дисбактериозом, стимулируя рост бактерий, работающих на человека.
Основным путем поступления ионов серебра в организм человека остается кишечник. Известны способы введения серебряной воды внутривенно, через кожу. Поэтому любые контакты с серебром уже обогащают организм человека ионами серебра и на этом основана полезность серебряных украшений.
Благодаря высокой активности бактерицидных свойств серебряной воды, только ее пьют отечественные и американские космонавты, моряки на подводных лодках, при дальних плаваниях и при других экстремальных ситуациях. А лечебные концентрации ионов серебра, которые на порядки превышают их концентрацию в серебряной воде, оказались способными уничтожить даже вирусы СПИДа, метастазы рака и тяжелейшие инфильтраты туберкулеза. Уже установлено, что количество серебра в тканях нашего организма достигает 20 мкг на 100 г сухого вещества. Больше всего серебра содержится в головном мозге человека, в ядрах нервных клеток, в железах эндокринной системы, радужной оболочке глаз и в костях. Следовательно, серебро является необходимым структурным элементом тканей нашего организма. Также отмечено стимулирующее действие ионов серебра на кроветворные органы с усилением окислительных процессов головного мозга в два раза, что улучшает его функцию. Участвуя в обменных процессах организма, серебро расходуется и для восполнения требуется его дополнительное поступление извне, при этом, суточная потребность человека достигает 88 мкг серебра. Сегодня серебро рассматривается как необходимый микроэлемент, обеспечивающий здоровье нашего организма за счет пополнения структурных запасов серебра в организме и бактерицидных свойств серебра, защищающих нас от инфекции. Появляются сообщения, и о противовоспалительных свойствах серебра, которые проявляются подобно мощным иммуномодуляторам, сравнимым со стероидными гормонами. Под влиянием серебра повышается количество иммуноглобулинов классов А, М, G, увеличивается процентное содержание абсолютного количества Т-лимфоцитов. Ионы серебра активно участвуют в имуннозащитой функции организма и могут повышать иммунитет. Однако издавна отмечали, что одному человеку серебро реально помогает за неделю, другому - не поможет и за месяцы, а у третьего может вызвать аллергическую реакцию.
В связи с чем во многих странах были выработаны допустимые нормативы содержания серебра в питьевой воде. ВОЗ допускает до 0,1 мг/л, Евро-Стандарт и в России 0,01 мг/л. При этом, общеизвестные серебросодержащие лекарства (коллоидное серебро, азотнокислое серебро) применяемые в медицине более ста лет, содержат серебра на 3-4 порядка больше, учитывая, что время их применения недлительное.
В лекарственных препаратах серебро оказывает уничтожающее действие на микробы при концентрации ионов более 150 мкг/л. Это токсично для человека. Для антибактериального эффекта так много не требуется. Информация на сайте Центр Соколинского, интернет-pecypc: https://www.pobedi2.ru/natural_products/imunitet/kolloidnoe-serebro/. Ионы серебра находятся в воде во взвешенном состоянии, образуя гель с мельчайшими частицами. 95% частиц наносеребра имеет размеры 3-5 нм. Концентрация обычного наносеребра 10 ppm, соответственно у наносеребра 30-30 ppm. Концентрированное вещество применяется наружно и для ингаляций на заднюю стенку глотки, в нос. Коллоидный раствор наносеребра иммуномодулирующий 10 мг/л - Насизоль 10 ppm, 100 мл, с высокой стабильностью состава и способностью проникать в ткани, разработан сотрудниками Физико-технического института в Санкт-Петербурге и внедрен в практику (центр «Рецепты здоровья» Владимира Соколинского. Производитель ООО «Медицинские системы», г. Санкт-Петербург). Может использоваться наружно и внутрь. Применение взрослым внутрь по 1 чайной ложке 1 раз в день, желательно натощак; детям до 6 лет по 2-3 капли 2 раза в день не более 3-х недель подряд, перерыв 1 месяц. Имеется также антисептик для наружного и внутреннего применения «NASiSOL», 30 в виде спрея, антисептический раствор коллоидного серебра с содержанием частиц серебра 30 ppm, то есть 30 мг/л. Насизоль 30 ppm - концентрированное вещество только для наружного применения и на слизистые: при ангине, гайморите, парадонтозе, кольпите, грибковых поражениях кожи. Более активного натурального противомикробного средства не найти. Его можно сравнить только со 100% маслом чайного дерева. Но масло труднее использовать у детей из-за сильного запаха. Сделать ингаляцию наносеребра легко. Флакон снабжен распылителем. В одном флаконе содержится 100 мл безопасного коллоидного серебра.
Нами сначала использовалось наносеребро в форме геля, для наружного применения, «NAno SILver SOL» клининг gel, 30 ppm, производитель ООО «Рэсбио» г. Санкт-Петербург, по заказу НПО «Звезда» г. Санкт-Петербург для детей 3-х лет. Согласно инструкции, гель может применяться для антисептической обработки рук.
Позднее НПО «Звезда» г. Санкт-Петербург расширила свой ассортимент различных форм, содержащих наночастицы серебра: Септик Дентамин гель, с наносеребром, 15 ppm, 30 мл. Гель Дентамин содержит наночастицы серебра концентрацией 15 ppm, размерностью 2-5 нм (85% всех частиц) и нейтральные, неионные гелеобразующие вещества, разрешенные к применению на коже и слизистых оболочках. Обладает местным иммуномодулирующим, антисептическим, противовирусным, противовоспалительным, онкопротекторным действием. Доказанно препятствует размножению S. mutans, стрептококку, которому отводят основную роль в развитии кариеса. По инструкции применяется местно при эрозиях / повреждениях слизистой оболочки полости рта, афтозном стоматите, при заболеваниях десен, неприятном запахе изо рта, профилактике кариеса (при использовании в капах). Наносить на пораженные участки слизистой 3-6 раз в день до достижения результата. Для профилактики кариеса и плохого запаха изо рта - наполнить гелем капы (индивидуальные или купленные в аптеке) - проводить аппликации на ночь, после чистки зубов, перед сном в течение часа (продолжительность курса не ограничена). Гель с наносеребром подавляет деятельность «плохих» бактерий S. mutans, покрывающих зубную эмаль в виде тончайших биопленок и вырабатывающих кислоты, разъедающие эмаль и вызывающие кариес. Однако имеется существенный недостаток в инструкции по применению: предлагается использование геля в капах для профилактики кариеса, что неприемлемо для детей раннего возраста, которые активно сопротивляются нахождению в полости рта посторонних, инородных предметов, кроме того, предполагается большой расход геля для использования по всему объему капы.
Известен способ профилактики и лечения кариеса детей как общегигиенический/санологический метод - регулярная чистка зубов. Главной целью механического удаления налета является уменьшение общего количества бактерий и модификация состава биопленки.
Известны следующие способы профессиональной профилактики кариеса. Реминерализующая профилактика кариеса зубов. Направленное использование эффекта реминерализации для повышения резистентности эмали зубов. Проникновение и оседание в различных слоях эмали кальция, фосфата и фтора ведет к постепенной нормализации проницаемости за счет образования новых кристаллов гидроксиапатита (Johanson, 1965; Silverstone, 1972; Кочержинский В.В., 1973). Работами ряда авторов (Lenz, 1967; Frank, 1967; Vahl, 1968; Watherell et al., 1974; Woltgens et al, 1976) отмечено, что в процессе реминерализации происходит заполнение межкристаллических пространств новыми кристаллами, отличными от здоровой эмали (Gustafson, Sundstrom, 1975). Основными компонентами таких смесей должны быть соли кальция, фосфаты и фториды в ионизированной форме (Боровский Е.В., Леус П.А., 1972; Прохончуков А.А., 1977; Пахомов Г.Н., 1982; Леонтьев В.К., 1984). Создание таких препаратов наталкивается на серьезные технологические трудности, связанные с химической несовместимостью указанных ионов в одном растворе они быстро взаимодействуют друг с другом и выпадают в осадок. Для реминерализации эмали были предложены искусственно созданные растворы (Andersen, 1921). По данным Pigman er al. (1964) раствор Sobel, содержащий в ммоль/литр Ca - 2,5; фосфат - 1,6; натрий - 97; К - 5; НСО, - 22; при pH 7,3 и температуре 37°С, при реминерализации не вызывает полного затвердевания эмали без дополнительной обработки фтором. Эти данные были подтверждены при исследованиях Muhlemann et al. (1964). В 1960 году Koulourides, Pigman описали метастабильный раствор фосфата кальция для восстановления эмали, размягченной кислотой. Однако, при проверке этого раствора Levine (1980) были отмечены существенные недостатки: неустойчивость при хранении и низкая минерализующая способность из-за трудно растворимости фосфата кальция. В экспериментальных исследованиях (Silverstone, 1971) был использован раствор, содержащий 200 ммоль/л хлорида натрия, 1,8-,9 -фосфата и 1- кальция (Са/Р -1,63). Добавление хлорида натрия предотвращало спонтанную преципитацию реминерализующего раствора. При исследованиях было выявлено, что для реминерализации в экспериментальных условиях существенное значение имеет не только присутствие и оптимальное соотношение ионов Са и Р в растворе, но и величина pH (Koulourides et al, 1965; Gonzales et al., 1975; Silverstone, 1977). В отечественной практике был предложен реминерализующий раствор, содержащий в своем составе соединения кальция, фосфата, фтора, цинка и магния (Боровский Е.В., Леус П.А., 1972). Используя последовательно аппликации 10% раствора глюконата кальция (5-10 мин) и 2% водного раствора фторида натрия, Е.В. Боровский, П.А. Леус (1976) получили хороший терапевтический эффект при лечении кариеса в стадии белого пятна. Ими отмечен положительный результат лечения в 88,4% случаев после 15-20 аппликаций. Поверхность эрозий приобретает мелкозернистый рельеф, стойкость структуры сохраняется в течение 12 прослеженных месяцев. Использование метода Е.В. Боровского с профилактическими целями у детей г. Москвы (Боровский Е.В., Леус П.А. и др., 1977; Боровский Е.В., Терентьева Т.Е. и др., 1978; Боровский Е.В., Кузьмина Э.М., Васина С.А., 1980) позволило снизить прирост кариеса постоянных зубов на 29-44%. Недостатком этого метода является неудобство в применении (два раствора) для детей раннего возраста, кроме того, глюконат кальция трудно диссоциирует на ионы, что ослабляет лечебный и профилактический эффект. Применение для лечения очаговой деминерализации эмали (Аксамит Л.А., 1978) только раствора глюконата кальция положительного эффекта не дает.
Реминерализующий состав, известный под названием «Ремодент», был предложен Г.Н. Пахомовым (1974), содержит минеральные вещества, извлеченные из костей и зубов при их химической обработке. Применение «Ремодента» для ранней терапии очаговой деминерализации эмали (Пахомов Г.Н., Леус П.А., 1979) позволило добиться исчезновения пятен при медленнотекущей форме в 75% случаев. После экспериментальной и клинической проверки ряда модификаций препарата, начат промышленный выпуск «Ремодента» в виде зубной пасты и порошка на основе синтетического раствора (Лусте А.Я., Ласовский И.И., 1984). Однако способ применения «Ремодента» в виде аппликаций трудоемок, требует большой затраты времени врача и пациента, в его составе неизбежно большое количество посторонних ионов, чужеродных антигенов, и снижен реминерализующий потенциал за счет осаждения Ca или Р при приготовлении, что неприменимо для детей раннего возраста.
Омской школой стоматологов (Леонтьев В.К., 1978; Сунцов В.Г., 1987) на протяжении длительного времени разрабатывался новый класс реминерализующих средств. В качестве средств профилактики и лечения начального кариеса были использованы реминерализующие кальций-фосфатсодержащие гели (а.с. 1114221), моделирующие по фосфорнокальциевому коэффициенту и степени перенасыщенности Ca и Р эмаль и слюну здорового человека и имеющие различные показатели pH. Гели перенасыщены ионами кальция и фосфата относительно их концентрации в слюне. Это увеличение повышает минерализующий потенциал средств профилактики и лечения по сравнению с потенциалом здоровой слюны во много раз. Для профилактики кариеса зубов у детей назначается чистка гелями курсами 2-3 раза в год по 10-15 дней на курс. Однако дети раннего возраста не чистят зубы самостоятельно, и дозировка ионов на них не рассчитана.
Фторпрофилактика. Препараты фтора являются одним из основных средств профилактики кариеса зубов, хотя в механизме кариесстатического действия остается много неясного. Большое количество работ, посвященных раскрытию механизмов действия фтора (Пахомов Г.Н., Леус П.А., 1972); Федоров Ю.А. с соавт., 1974; Palazzi, 1975; Gulzov, 1976) позволяет выделить три главных направления. Во-первых, фтор, взаимодействуя с гидроксиапатитом эмали, замещает гидроксильную или карбонатную группу с образованием менее растворимой формы - гидроксифторапатита (Wefel, Harless, 1981; Ogaard et al., 1983). Во-вторых, фториды оказывают угнетающее влияние на рост и обмен веществ микрофлоры полости рта путем активного ингибирующего действия на фосфоэнолпируваткиназу, в результате чего снижается интенсивность расщепления углеводов и кислотопродукция (Hardwick, 1963; Edgar et al., 1970; Myers, Handelman, 1971). Полоскания фторидами воздействуют на колонизацию бактерий на поверхности эмали (Tinanoff et al., 1976) путем изменения адгезии. В-третьих, работами (Brudevold et al., 1961; Колесника А.Г., 1967; Silverstone, 1971; Gonsales et al., 1975) доказано действие фтора, наряду с минеральной, на белковую фазу эмали, что влияет на формирование зубов и на их устойчивость к кариесу. В зубах, обработанных фторсодержащей пастой, отмечается усиление интенсивности включения радиоактивного Ca и Р (Колесник А.Г., 1964; Пахомов Г.Н. с соавт., 1971; Максимовская Л.Н., Шерман Л.В., 1980). Для профилактики кариеса применяются различные соединения фтора, которые обычно подразделяются на группы неорганических и органических веществ. Чаще всего используется фтористый натрий и калий (Ибрагимов A.M., 1981), фтористое олово (Сватун Б., 1981; Tinanoff et al., 1983), аминофторид (Кюнцель В., 1980; Pipa, 1982), монофторфосфат (Ekstrand, 1979), фтористый цирконий (Horowitz, Bitler, 1976). Многочисленные исследования по выявлению наиболее активного в противокариозном отношении соединения фтора не позволили с достоверностью ответить на этот вопрос. Большинство соединений обладает близким по показателям противокариозным эффектом, хотя данные довольно противоречивы. Вместе с тем, однозначно для практического применения фторидов выявлены оптимальные концентрации фтора для местного применения: не более 1-2% в расчете на ион фтора, так как дальнейшее повышение содержания этого элемента на эффективность профилактики не влияет (Driscol et al., 1982). При подборе фтористых средств и композиций необходимо учитывать возможность связывания фторидов, например с кальцием, в результате чего они могут терять свою активность (Пахомов Г.Н. с соавт., 1975; Морозова Н.В., Морозова Л.В., 1975; Hesselgren, 1980). Фториды для профилактики кариеса зубов должны назначаться в зависимости от содержания фтора в питьевой воде и продуктах питания, иначе их применение будет неэффективным (Пашаев К.П., Воронина Л.А., 1984). Формы применения соединений фтора для профилактики кариеса зубов разнообразны. В местностях, где содержание фтора ниже 0,7 мг/л, для массовой профилактики применяется фторирование питьевой воды (Габович Р.Д., Минх А.А., 1979; Петрикас А.Ш., 1981; Тимонов М.А., 1985) путем повышения концентрации фтора до 0,8-1,2 мг/л. Имеются данные о выраженном профилактическом эффекте (редукция кариеса до 50%) при использовании у детей фторированной соли (Regolati, 1975; Toth, 1977; Toth et al., 1980). молока в Закарпатье, Смоленске и других городах страны (П.И. Горзов, А.Г. Колесник, А.Г. Шаргородский и др., 1995). Для коллективной и индивидуальной профилактики кариеса используются полоскания 0,02-0,2% растворами фторидов (Смоляр Н.И., Масный З.П., 1985), аппликации 1-2% растворов и гелей фтора (Морозова Н. В., 1975; Колесник Л.Г. с соавт., 1975; Леонтьев В.К. с соавт., 1977; Прохончуков А.А., 1977; Чекмезова И.В., 1983), чистка зубов фторосодержащими пастами (Пахомов Г.Н., 1975; Морозова Н.В., 1975; Климм В., 1980), введение фторидов с помощью электрофореза (Opalko et al., 1978), нанесение фтористого лака (Лагутина Н.Я., Степанов А.В., 1980; Синицин Р.Г. с соавт., 1980; Косенко К.Н. с соавт., 1984; Боровский Е.В. с соавт., 1985), разжевывание фтористых таблеток (Driscoll, 1974, 1978; Horowitz, 1979, 1984; Weatherell et al., 1984), дача внутрь таблеток фторида натрия (Berner et al., 1975; Ahrens, 1976; Anke, 1979; Driscoll et al., 1979; Klimek, 1982) и витафтора (Пашаев К.П., 1981; Петрушенко О.Е., Жедик А.Н., 1985). Анализ эффективности перечисленных видов фторпрофилактики кариеса зубов показывает, что редукция кариеса в преобладающем большинстве случаев не превышает 50%. Действие фтора не длительно, что, вероятно, связано с вымыванием его из эмали (Алкалаев К.К., 1964; Brudevold et al., 1965; Mechin, 1975). Однако современные исследования идентифицируют фтор как яд при его применении в воде и соли, в этом случае применение этих устаревших - методов неприменимо для детей раннего возраста и является существенным недостатком.
Методика применения фтористых лаков: «Duraphat» (Woelm) «Duraphat» (Colgate) «Fluor Protector» «Stand-Gard» «Фторлак» «Радогель F» (ВладМиВа) «Радуга» (Радуга-Р) «Флурадент» (Радуга-Р). Проводится профессиональная гигиена полости рта; изоляция зубов, высушиваются теплым воздухом; на все поверхности зубов кисточкой или деревянной палочкой тонким слоем наносится фтористый лак, избегая попадания препарата на слизистую оболочку полости рта. В течение 3-5 минут лак высушивается, пациент сидит с открытым ртом. После пациенту рекомендуется в течение 2 часов не есть, на протяжении суток употреблять только жидкую и мягкую пищу, в течение 12-24 не следует чистить зубы. Рекомендуется 3-х кратное покрытие зубов с интервалом 1-2 дня.
Глубокое фторирование - это образование субмикроскопических кристаллов (50A) CaF2 и MgF2, имеющего еще большую растворимость, чем CaF2, в порах разрыхленной зоны твердой субстанции зуба. Препараты для глубокого фторирования: «Эмаль-герметизирующий ликвид», «Глуфторед». Глубокое фторирование происходит в результате последовательного смачивания эмали слабокислым раствором магниево-фтористого силиката (MgSiF6) и последующего туширования щелочной суспензией гидроокиси меди-кальция. Растворы проникают глубоко в воронки эмали и реакция протекает как на поверхности эмали, так и внутри воронок / дентинных канальцев. В результате образуются фториды кальция и магния, а также кремниевая кислота MgSiF6 + 2Са(ОН)2=2 CaF2 + MgF2 + Si(OH)4. Образующаяся кремниевая кислота превращается в гель. В результате возникает щелочная гелеобразная субстанция с включениями микрокристаллов фторидов кальция, меди и магния. При избытке Са(ОН)2 реакция протекает без образования MgF2: MgSiF6 + 3Са(ОН)2=2 CaF2 + Mg(OH)2 + Si(OH)4. Нанофториды сохраняются в воронках от 0,5 до 2 лет, постепенно выделяя фтор.
Методика проведения «глубокого фторирования» препаратом «Эмаль-герметизирующий ликвид». С зубов тщательно снимают зубной налет, в том числе и в межзубном пространстве, высушивают в течение 0,5-1,0 минуты, зубы обильно смачивают ватным тампоном, пропитанным жидкостью для первого туширования, которая представляет собой фтористый силикат магния, в течение 30 секунд, обдувая при этом теплым воздухом; далее поверхность зубов предварительно взболтанным препаратом №1. После этого, не производя промежуточного полоскания рта, эмаль зуба тщательно смачивают предварительно взболтанным препаратом №2. Только после этого пациент может прополоскать рот через 1-2 минуты. После двукратного повторения через 1-3 недели, процедуру в последующем проводят 1-2 раза в год. Следует иметь в виду, что при случайном проглатывании большого количества эмаль-герметизирующей жидкости (более 5 мл) рекомендуется выпить большое количество воды или молока. Во врачебном кабинете может быть рекомендовано в качестве антидота использовать жидкое гипсовое молоко: 1 чайная ложка на 1 стакан воды.
Методика проведения «глубокого фторирования» препаратом «Глуфторед». С зубов тщательно снимают зубной налет, в том числе и в межзубном пространстве и высушивают; зубы обильно смачивают ватным тампоном, пропитанным жидкостью для первого туширования, которая представляет собой фтористый силикат магния в течение 1 минуты, обдувая при этом теплым воздухом; далее поверхность зубов смачивают взвесью гидроокиси меди-кальция в воде в течение 1 минуты; проводится полоскание водой. Существенным недостатком является трудоемкость обеих методик, большие временные затраты, большая вероятность заглатывания препаратов фтора, что трудно предотвратить при работе с детьми раннего возраста.
Возможны аппликации фторидов. Для этой цели используются 1-2% растворы фтористого натрия или фтористые гели. Применяются они в виде зубо-десневых аппликаций. Поверхности зубов перед аппликацией тщательно очищаются путем чистки гигиеническими зубными пастами, изолируются от слюны и высушиваются. Наносится раствор на ватных тампонах на 3-4 минуты или в виде кап. Заглатывать раствор фторидов нельзя. Наличие чужеродных предметов и большая временная экспозиция исключают использование приведенных выше методик у детей до 3-х лет.
Профессором В.К. Леонтьевым для аппликации предложен 1-2% гель фторида натрия на 3% агаре. Перед применением после чистки зубов разогретый на спиртовке гель кисточкой наносится на зубы, где он при соприкосновении с ними застывает в виде тонкой пленки. После этого пациента отпускают домой с рекомендацией в течение 3 часов не принимать пищу. Данные способ также трудоемок и малоприменим для детей раннего возраста, что в данном случае снижает его ценность.
В стоматологической практике известно применение антисептиков. Типичными и наиболее исследованными средствами являются хлоргексидин, алексидин, диацид (Трыковски Я., 1981; Петрикас А.Ш., Румянцев В.А., 1984). Эти вещества в малых концентрациях (0,1-0,2% растворы) обладают сильным и специфичным антимикробным действием, подавляя рост и развитие микрофлоры. Хлоргексидин как наиболее широко применяемое средство для профилактики кариеса (Giermo, 1975; Сватун Б.И др., 1981) используется в виде полосканий и зубной пасты. При его применении на 80-90% уменьшается количество микрофлоры, индуцирующей кариес в полости рта, снижается образование налета. Для полосканий используется 0,05-0,2% раствор 1-2 раза в день после приема пищи. Раствор имеет горьковатый вкус, может изменяться цвет языка (чернеет), при длительном назначении способствует десквамации эпителия в полости рта, изменению вкусовой чувствительности. Существенным недостатком является неумение детьми раннего возраста полоскать рот и горький на вкус препарат. Кроме того, имеются сведения, что при длительном применении могут образовываться в полости рта коканцерогены, поэтому используются только свежеприготовленные растворы хлоргексидина.
Метод серебрения (Сафорайт, Япония), приостанавливающий развитие кариеса посредством химической модификации кариозных тканей. Метод заключается в последовательном нанесении на кариозные ткани раствора серебра и препарата-восстановителя (аскорбиновой кислоты, гидрохинона). После чего серебро переходит в металлическую форму и осаждается на поверхности в виде мелкодисперсных кристаллов. Метод способствует окраске тканей зубов в черный цвет, что не нравится родителям и может способствовать социальной дезадаптации ребенка. Этот метод лишает ребенка эстетичной улыбки.
Эти способы и применяемые для его реализации средства приняты в качестве наиболее близких аналогов-прототипов. Однако у всех выше перечисленных способов есть существенные недостатки. Все они малоприменимы для непосредственного воздействия на кариесогенную флору у детей раннего возраста, от момента рождения и до 3-х лет, не дают доступной, безопасной, точной и простой в применении методики донозологической профилактики и, одновременно, лечения кариеса зубов, с применением/аппликацией препаратов коллоидного серебра в бактериологически идентифицированных, наиболее активных биотопах как модельной системе для донации/источника кариесогенных S. mutans, с целью подавления их роста и/или уменьшения титра с помощью современных сертифицированных и безопасных в применении, безвкусных и прозрачных гелей, содержащих наночастицы серебра. Также недостатком вышеперечисленных аналогов-прототипов является: временные затраты, длительная манипуляция, высокая затрата специализированого труда. В связи с особенностями психо-соматического статуса детей раннего возраста, их неусидчивостью, выполнение осмотра специалистом и применение сложных манипуляций неудобно. В этой связи необходимо выбрать оптимальный способ, который предполагает минимальные временные затраты для выполнения профилактических и лечебных процедур, удобен, безвреден, легкодоступен у детей раннего возраста. Кроме того, предлагаемый способ легко осваивают родители или люди, осуществляющие уход за детьми.
В доступной научной литературе не имеется указаний на взаимосвязь между высокой обсемененностью кариесогенной флорой биотопов слизистой оболочки спинки языка и зубного налета с язычных поверхностей зубов у детей раннего возраста и возможностью прямого воздействия на нее коллоидного серебра непосредственно в этих биотопах.
В процессе нашего исследования выявлено, что плотность обсемененности кариесогенной флорой язычной поверхности зубов и слизистой оболочки спинки языка статистически достоверно одинаковы, в то же время их обсемененность значительно выше всех других биотопов полости рта, где возможно обнаружение Streptococcus mutans.
В настоящее время для исследований микробного состава полости рта и слюны используются методики, являющиеся простыми и удобными у детей при применении непосредственно в стоматологическом кабинете. Для проведения микробиологического тестирования на Steptococcus mutans нами использовались диагностические тесты in vitro у детей: «Dentocult SM Strip mutans» (фирма «Vivadent», Лихтенштейн).
Для проведения экспресс-теста «Dentocult SM Strip mutans» шероховатая поверхность тест-полоски с закругленным концом прижимается к языку ребенка, на котором присутствует слюна. Тест-полоски с квадратным концом имеют шероховатую поверхность, на которую наносят зубной налет с эмали зубов. Затем полоски помещаются в селективную питательную слюну во флакон с предварительно растворенным диском антибиотика бацитрацина, который задерживает рост бактерий, кроме S. mutans. Флакон помещается в инкубатор на 48 часов при температуре 37°С. После проведения инкубации наличие бактерий выявляется по росту на шероховатой поверхности тест-полоски колоний, имеющих цвет, варьирующий от темно-синего до голубого. Количественный состав характеризуется плотностью их прикрепления и сравнивается с эталонной картой/схемой в инструкции по применению.
Анализ плотности колонизации слюны, различных поверхностей зубов, межзубного промежутка и слизистой спинки языка патогенными стрептококками, представлен на Фиг. 1, он показал преобладание Streptococcus mutans на язычной поверхности зубов и слизистой оболочке спинки языка, с наименьшей концентрацией микроорганизмов на вестибулярной поверхности зубов (р<0,01).
Задача изобретения: предложить способ неспецифической донозологической профилактики и лечения кариеса зубов у детей раннего возраста для уменьшения обсемененности кариесогенными микроорганизмами Streptococcus mutans зубного налета молочных зубов и спинки языка путем применения коллоидного серебра, и его непосредственного воздействия на слизистую оболочку спинки языка и язычную поверхность молочных зубов как наиболее активных биотопов-донаторов, с использованием готовых препаратов наносеребра, лишенный выше перечисленных недостатков.
Технический результат состоит в том, что выполняется щадящая и безболезненная профилактическая или лечебная процедура детям раннего возраста, с возможностью непосредственного влияния активными в отношении кариесогенных бактерий ионами наночастиц серебра Ag+ на самые высоко обсемененные Streptococcus mutans биотопы полости рта у детей раннего возраста как наиболее значимые источники инфекта, а также уменьшения количества/титра патогенных кариесогенных микроорганизмов S. mutans, из числа индигенной микрофлоры полости рта человека, в доступных для обработки слизистой оболочки спинки языка, язычных поверхностей молочных зубов как областей с вероятной функцией донации, применяя незаявляемые препараты коллоидного серебра с концентрацией ионов Ag+ 30 ppm в форме геля.
Повышается качество неспецифической донозологической профилактики и лечения кариеса с появлением возможности неоднократной быстрой обработки биотопов слизистых оболочек спинки языка и язычной поверхности зубов у детей как способа прямого бактерицидного воздействия на кариесогенные бактерии Streptococcus mutans в биотопах, возможностью неоднократного бактериологического контроля за результатами проводимой профилактики и лечения. Разработка индивидуальной программы профилактики кариеса зубов путем увеличения или уменьшения дозы, кратности приема и/или курса профилактики и лечения с возможностью коррекции этих процедур у детей. Отсутствие препятствий доступа к поверхности языка и язычных поверхностей зубов на приеме у стоматолога или другого специалиста, позволяет широко использовать предлагаемый способ воздействия наночастиц серебра Ag+ на патогенную флору в составе микробиома языка и язычных поверхностей зубов непосредственно, в разных концентрациях активного вещества на модель донации/источника Streptococcus mutans, достоверно препятствующих как их размножению, так и распространению в другие биотопы полости рта у детей раннего возраста. Ранняя неспецифическая профилактика кариеса у детей играет важную роль в сохранении стоматологического здоровья.
Технический результат достигается тем, что перед началом профилактических и лечебных мероприятий от родителей получено информированное согласие в соответствии со ст. 20, №323 - ФЗ от 21.11.2011 г. Всем детям проводят комплексное стоматологическое исследование: оценка кпу зубов, гигиенический индекс (ГИ) и кариесогенность зубного налета (КЗН). Интенсивность поражения зубов кариесом определяют с помощью индекса кпу: число кариозных, пломбированных и удаленных по поводу осложненного кариеса временных зубов. Для расчета гигиенического состояния полости рта используется индекс для детей раннего возраста по Э.М. Кузьминой, 2000. Определяют кариесогенность ЗН по методике Hardwick J.L., Manley E.В. в модификации Недосеко В.Б. Проводится микробиологическое тестирование детей раннего возраста, определяют наличие и плотность обсеменения бактериями Streptococcus mutans слизистой оболочки дорсальной поверхности/ спинки языка и всех исследуемых поверхностей молочных зубов. Забор осуществляется с интактного/некариозного участка эмали зубов нижней челюсти и со всей поверхности слизистой оболочки средней трети спинки языка ребенка стерильным тупфером. Степень колонизации стрептококками мутанс оценивается по наличию и количественному содержанию Streptococcus mutans с использованием незаявляемого микробиологического теста «Dentocult SM Strip Mutans» производства «Vivadent», Лихтенштейн. Тест основан на применении селективной питательной среды для кариесогенных стрептококков и тест-полоски с квадратным концом и шероховатой поверхностью, основанный на естественной способности бактерий Streptococcus mutans к адгезии.
Полоска с нанесенным биологическим материалом погружается, согласно инструкции производителя, в селективный для Streptococcus mutans питательный бульон с антибиотиком бацитрацином, к которому резистентны S. mutans. Флакон инкубируют 48 часов при температуре 37°С. После проведения инкубации наличие бактерий выявляется по плотности роста колоний, возвышающихся на шероховатой поверхности тест-полоски в виде мелких синих шариков, диаметром 0,1-0,5 мм. Оценка результатов проводится по прилагаемой типовой схеме в инструкции по применению, отражающей количество/плотность колоний Streptococcus mutans, титр относили к одному из четырех классов: 0-й класс соответствует менее чем 10000 колоний (КОЕ<104/мл), 1-й класс, менее 100000 колоний (КОЕ<105/мл), 2-й класс - от 100000 до 1000000 (КОЕ105/мл - КОЕ106/мл), 3-ий класс -> 1000000 колоний (КОЕ>106/мл). Результаты регистрируют в журнале учета выделенных штаммов. Количество/плотность/обсемененность/титр выявленных в микробиоме слизистой спинки языка S. mutans статистически достоверно соответствует титру Streptococcus mutans в зубном налете наиболее обсемененного ими биотопа язычной поверхности молочных зубов нижней челюсти. Данные представлены в таблице 1. Следовательно, полученные данные могут использоваться в качестве прогностической модели для определения биотопов, наиболее обсемененных кариесогенными бактериями Streptococcus mutans твердых тканей молочных зубов у детей раннего возраста с целью дальнейшей их обработки коллоидным серебром.
После определения кпу, ИГ, КЗН, детей распределили в две клинические группы: с низкой активностью и интенсивностью кариеса 15 детей 3-х лет, и высокой активностью и интенсивностью кариозного процесса 20 детей 3-х лет, которые/обе группы наряду с разработанной нами профилактикой получали препараты коллоидного серебра. Третья контрольная группа имела среднюю и высокую активность кариеса, где 18 детям проводилась разработанная нами схема профилактики, но они не получали препараты серебра. Технический результат по предлагаемому способу непосредственно достигается тем, что детям до 3-х лет из клинических групп на фоне предложенной нами для всех обследуемых схемы профилактики дополнительно проводили аппликацию коллоидным серебром в форме геля с концентрацией наночастиц серебра Ag+ 30 ppm по схеме в течение 6 месяцев. Через 3 месяца и через 6 месяцев, после окончания курса, проводили текущее и контрольное стоматологическое и микробиологическое исследование детей до 3-х лет во всех группах. Гель для наружного применения, «NAno SILver SOL» клининг gel, 30 ppm, производитель ООО «Рэсбио» г. Санкт-Петербург, по заказу НПО «Звезда» г. Санкт-Петербург, применяли для 35 детей до 3-х лет из 2-х опытных групп с острым и хроническим течением кариеса. Курс аппликации геля непосредственно в биотопопы-источники Streptococcus mutans проводился вискозным тампоном-аппликатором в количестве 2 капель: первая капля геля выдавливалась из флакона диаметром 2,5-3 мм, сначала наносилась на язычные поверхности зубов нижней челюсти слева и, затем, справа, вторая капля апплицировалась на слизистую оболочку средней трети спинки языка круговыми движениями слева направо, захватывая всю поверхность слизистой оболочки средней трети спинки языка от центра к периферии. Вся процедура занимала не более 30-40 секунд. Курс лечения проводился следующим образом. Аппликация коллоидного серебра с наночастицами Ag+ в концентрации 30 ppm проводилась родителями 2 раза в день утром и вечером. Рекомендовано утром натощак предварительно провести гигиеническую чистку зубов, дать ребенку 30,0-50,0 мл чистой воды и через 5-7 минут проводить последовательную обработку биотопов язычной поверхностей зубов и спинки языка, нанося незаявляемый гель с наночастицами Ag+ в концентрации 30 ppm. Принимать пищу можно не ранее, чем через 20-30 минут, Рекомендовано вечером перед сном, предварительно провести гигиеническую чистку зубов, дать ребенку 30,0-50,0 мл чистой воды и через 5-7 минут проводить последовательную обработку биотопов язычной поверхностей зубов нижней челюсти и спинки языка, нанося незаявляемый гель с наночастицами Ag+ в концентрации 30 ppm. Проводить аппликацию можно не ранее, чем через час после приема пищи и/или напитков. Схема рассчитана на два курса в течение 6 месяцев. Базовый курс включает аппликацию коллоидным серебром 2 раза в день в течение 7 дней, следующие 7 дней перерыв, всего 3 месяца. Поддерживающий курс включает аппликацию коллоидным серебром 1 раз в день перед сном в течение 14 дней, следующие 14 дней перерыв, всего 3 месяца.
После проведения предложенной нами схемы лечебно-профилактических мероприятий, включающих: санацию полости рта, нормализацию характера и режима питания с устранением углеводного фактора, аппликацию фторидов местно 1 раз в 3 месяца, консультацию у педиатра. После демонстрации образцов с выросшими колониями патогенных бактерий для повышения мотивации, родителей обучали гигиене полости рта с использованием зубной нити. В трех группах получены статистически значимые результаты по уменьшению образования зубного налета на поверхностях зубов, уменьшению титра кариесогенных Streptococcus mutans в исследованных биотопах полости рта. Прироста кпу в 1 опытной группе не произошло, во 2 группе - незначительно, в контрольной группе на фоне разработанной нами профилактики имел место прирост кпу у 7 детей из 18. Динамика индекса кпу зубов у детей 3-х лет при проведении профилактических мероприятий (М±m) представлены в таблице 2
Преимуществами предлагаемого способа являются:
- безвредность, уменьшение временных затрат, экономичность;
- доступность биотопов язычной поверхности зубов нижней челюсти и биотопа спинки языка у детей;
- щадящая диагностическая процедура для детей раннего возраста; простота и скорость использования;
- возможность опосредованного неспецифического лечения и профилактики кариеса зубов, уменьшения кариесогенности зубного налета у детей раннего возраста, влияния на кариесогенные микроорганизмы, из числа индигенной микрофлоры полости рта человека, Streptococcus mutans, слизистой оболочки спинки языка и мягкого налета твердых язычных поверхностей зубов непосредственно в их биотопах-источниках;
- повышение качества донозологической профилактики и лечения, с появлением возможности неоднократного бактериологического контроля за обсемененностью слизистых оболочек спинки языка и язычной поверхности зубов нижней челюсти как ориентировочного способа выявления кариесогенности зубного налета в результате проводимого комплекса профилактических мероприятий;
- профилактика кариеса зубов у детей раннего возраста путем применения коллоидного серебра с иммуномодулирующими свойствами;
- повышение качества лечения/профилактических мероприятий и возможность коррекции лечебно-профилактических процедур безопасными препаратами с наночастицами серебра детям раннего возрста;
- отсутствие препятствий доступа к поверхности спинки языка на приеме у стоматолога, или другого специалиста, позволяет широко использовать предлагаемый способ снижения титра кариесогенной флоры в составе микробиома корня и твердых тканей зубов на модели донации кариесогенных бактерий в другие биотопы полости рта у детей раннего возраста;
- после окончания курса комплекса лечебно-профилактических мероприятий при отсутствии противопоказаний можно провести повторный курс аппликации коллоидного серебра на поверхность спинки языка и язычной поверхности зубов на усмотрение лечащего врача;
- устойчивость к серебру у кариесогенных бактерий не обнаружена;
- высокая комплаентность родителей к предлагаемому способу профилактики и лечения
Пример 1
Ребенок А., 2 года 11 месяцев, при первичном обращении выявлены: отсутствие санации - кпу зубов составило 7, плохая гигиена полости рта / ГИ - 0,74 и выраженный кариесогенный зубной налет - 2 балла. В полости рта: 53, 52, 51, 61, 62, 63, 64 зубы: острое течение кариеса, декомпенсация: кариозные полости глубокие, дентин влажный, светлый. Ребенок обследован микробиологически, согласно предлагаемого способа. Забор биоматериала производили из 4-х биотопов: налет с вестибулярной и язычной поверхностей зубов, межзубного промежутка и со слизистой оболочки спинки языка. Выявили, что обсемененность слизистой спинки языка и язычной поверхности зубов кариесогенными бактериями Streptococcus mutans соответствует 3-у классу / КОЕ>106/мл; статистически значимых различий не выявлено. Обсемененность вестибулярной поверхности зуба - 1 класс / КОЕ<105/мл, межзубного промежутка - 2 класс, что соответствует КОЕ 105/мл - КОЕ 106/мл. Таким образом, при первичном обследовании выявлена высокая обсемененность кариесогенными бактериями. Высокий титр патогенной микрофлоры обусловлен отсутствием санации, плохой гигиеной полости рта и выраженным кариесогенным зубным налетом. Был назначен комплекс лечебно - профилактических мероприятий, включающий: санацию полости рта, нормализацию характера и режима питания с устранением углеводного фактора, аппликация фторидов местно 1 раз в 3 месяца, консультацию у педиатра. После демонстрации образцов с выросшими колониями патогенных бактерий для повышения мотивации, родителей обучали гигиене полости рта с использованием зубной нити и аппликациям коллоидного серебра с наночастицами Ag+ в концентрации 30 ppm по ниже приведенной схеме.
Аппликация коллоидного серебра с наночастицами Ag+ в концентрации 30 ppm проводилась родителями 2 раза в день утром и вечером. Утром натощак после предварительной гигиенической чистки зубов, давали ребенку 30,0-50,0 мл чистой воды и через 5-7 минут проводили последовательную обработку биотопов язычной поверхностей зубов и спинки языка, наносили незаявляемый гель с наночастицами Ag+ в концентрации 30 ppm. Принимали пищу не ранее, чем через 20-30 минут. Вечером перед сном, предварительно проводили гигиеническую чистку зубов, давали ребенку 30,0-50,0 мл чистой воды и через 5-7 минут проводили последовательную обработку биотопов язычной поверхностей зубов нижней челюсти и спинки языка, наносили незаявляемый гель с наночастицами Ag+ в концентрации 30 ppm. Проводили аппликацию не ранее, чем через час после приема пищи и/или напитков. Схему выполняли двумя курсами в течение 6 месяцев. Базовый курс включал аппликацию коллоидным серебром 2 раза в день в течение 7 дней, следующие 7 дней перерыв, всего 3 месяца. Поддерживающий курс включал аппликацию коллоидным серебром 1 раз в день перед сном в течение 14 дней, следующие 14 дней перерыв, всего 3 месяца.
Через 3 месяца, после проведения комплекса лечебно-профилактических мероприятий с использованием геля с коллоидным серебром повторно оценивали стоматологический статус и класс обсемененности кариесогенными микроорганизмами. По всем показателям получили достоверное улучшение. Значение кпу осталось прежним - 7, но в структуре индекса изменился компонент «к» - «0», «п» - 7. Анализ полученных результатов показал достоверное уменьшение ГИ - 0,24, значения кариесогенности зубного налета улучшились до 1 балла. Выявили, что обсемененность слизистой спинки языка и язычной поверхности зубов кариесогенными бактериями Streptococcus mutans соответствует 1-у классу / КОЕ<105/мл; статистически значимых различий не выявили. Обсемененность вестибулярной поверхности зуба - 1 класс / КОЕ<105/мл, межзубного промежутка - 1 классу, что соответствует КОЕ<105/мл. В течение диспансерного наблюдения новых очагов кариозного поражения зубов у ребенка выявлено не было.
Пример 2
Ребенок С., 2 года 4 месяца, кпу зубов составило 0. Гигиена полости рта / ГИ - 0,18, значение кариесогенного зубного налета - 1 балл. Ребенка обследовали микробиологически, согласно предлагаемого способа. Взят биоматериал из 4-х биотопов: налет с вестибулярной и язычной поверхностей зубов, межзубного промежутка и со слизистой оболочки спинки языка. Выявили, что обсемененность слизистой спинки языка и язычной поверхности зубов кариесогенными бактериями Streptococcus mutans составила - 2 класс, что соответствует КОЕ 105/мл - КОЕ 106/мл; статистически значимых различий не выявлено. Обсемененность вестибулярной поверхности зуба - 0 класс, что соответсвует КОЕ<104/мл, межзубного промежутка - 1 класс / КОЕ<105/мл. Осуществляли разработанный нами комплекс лечебно - профилактических мероприятий, включающий: санацию полости рта, нормализацию характера и режима питания с устранением углеводного фактора, аппликацию фторидов местно 1 раз в 3 месяца, консультацию у педиатра. После демонстрации образцов с выросшими колониями патогенных бактерий для повышения мотивации, родителей обучали гигиене полости рта с использованием зубной нити и аппликациям коллоидного серебра с наночастицами Ag+ в концентрации 30 ppm по ниже приведенной схеме.
Аппликация коллоидного серебра с наночастицами Ag+ в концентрации 30 ppm проводилась родителями 1-2 раза в день утром и вечером. Утром натощак предварительно проводили гигиеническую чистку зубов, давали ребенку 30,0-50,0 мл чистой воды и через 5-7 минут проводили последовательную обработку биотопов язычной поверхностей зубов и спинки языка, нанося незаявляемый гель с наночастицами Ag+ в концентрации 30 ppm. Принимали пищу не ранее, чем через 20-30 минут, вечером перед сном, предварительно проводили гигиеническую чистку зубов, давали ребенку 30,0-50,0 мл чистой воды и через 5-7 минут проводили последовательную обработку биотопов язычной поверхностей зубов нижней челюсти и спинки языка, наносили незаявляемый гель с наночастицами Ag+ в концентрации 30 ppm. Проводили аппликацию не ранее, чем через час после приема пищи и/или напитков. Схема состояла из двух курсов в течение 6 месяцев. Базовый курс включал аппликацию коллоидным серебром 2 раза в день в течение 7 дней, следующие 7 дней перерыв, так поочередно, всего 3 месяца. Поддерживающий курс включал аппликацию коллоидным серебром 1 раз в день перед сном в течение 14 дней, следующие 14 дней перерыв, всего 3 месяца.
Через 3 месяца, после проведения комплекса лечебно-профилактических мероприятий с использованием геля с коллоидным серебром повторно оценивали стоматологический статус и класс обсемененности кариесогенными микроорганизмами. По всем показателям получили достоверное улучшение. Значение кпу осталось прежним - 0. Анализ полученных результатов показал прежнее значение ГИ - 0,1, и кариесогенности зубного налета до 0 баллов. Выявили, что обсемененность слизистой спинки языка и язычной поверхности зубов кариесогенными бактериями Streptococcus mutans соответствует 0-у классу КОЕ<104/мл; статистически значимых различий не выявлено. Обсемененность вестибулярной поверхности зуба - 0 класс, что соответствует КОЕ<104/мл, межзубного промежутка - 0 класс, что соответствует КОЕ<104/мл. В течение диспансерного наблюдения новых очагов кариозного поражения зубов у ребенка выявлено не было.
Пример 3
Ребенок О., 2 года 9 месяцев, кпу зубов равно 1. Хорошая гигиена полости рта / ГИ - 0,14, значение кариесогенного зубного налета - 0 баллов. В полости рта: 64 зуб - хроническое течение кариеса, компенсация: кариозная полость средних размеров, дентин плотный, пигментированный. Ребенок обследован микробиологически, согласно предлагаемого способа. Забор биоматериала производили из 4-х биотопов: налет с вестибулярной и язычной поверхностей зубов, межзубного промежутка и со слизистой оболочки спинки языка. Выявили, что обсемененность слизистой спинки языка и язычной поверхности зубов кариесогенными бактериями Streptococcus mutans по 2-му классу, что соответствует КОЕ<105/мл; статистически значимых различий не выявлено. Обсемененность вестибулярной поверхности зуба - 2 класс / КОЕ<105/мл, межзубного промежутка - 2 класс, что соответствует КОЕ<105/мл. Был назначен комплекс лечебно - профилактических мероприятий, включающий: санацию полости рта, нормализацию характера и режима питания с устранением углеводного фактора, аппликация фторидов местно 1 раз в 3 месяца, консультация у педиатра. После демонстрации образцов с выросшими колониями патогенных бактерий для повышения мотивации, родителей обучали гигиене полости рта с использованием зубной нити и аппликациям коллоидного серебра с наночастицами Ag+ в концентрации 30 ppm по ниже приведенной схеме.
Аппликация коллоидного серебра с наночастицами Ag+ в концентрации 30 ppm проводилась родителями 2 раза в день утром и вечером. Утром натощак после предварительной гигиенической чистки зубов, давали ребенку 30,0-50,0 мл чистой воды и через 5-7 минут проводили последовательную обработку биотопов язычной поверхностей зубов и спинки языка, наносили незаявляемый гель с наночастицами Ag+ в концентрации 30 ppm. Принимали пищу не ранее, чем через 20-30 минут. Вечером перед сном, предварительно проводили гигиеническую чистку зубов, давали ребенку 30,0-50,0 мл чистой воды и через 5-7 минут проводили последовательную обработку биотопов язычной поверхностей зубов нижней челюсти и спинки языка, наносили незаявляемый гель с наночастицами Ag+ в концентрации 30 ppm. Проводили аппликацию не ранее, чем через час после приема пищи и/или напитков. Схему выполняли двумя курсами в течение 6 месяцев. Базовый курс включал аппликацию коллоидным серебром 2 раза в день в течение 7 дней, следующие 7 дней перерыв, всего 3 месяца. Поддерживающий курс включал аппликацию коллоидным серебром 1 раз в день перед сном в течение 14 дней, следующие 14 дней перерыв, всего 3 месяца. После проведения комплекса лечебно-профилактических мероприятий с использованием геля с коллоидным серебром, показатели стоматологического статуса улучшились. Значение кпу осталось прежним - 1, но в структуре индекса изменился компонент «к» -«0», «п» - 1. Анализ полученных результатов показал прежнее значение ГИ - 0,14, и кариесогенности зубного налета до 0 баллов. Выявили, что обсемененность слизистой спинки языка и язычной поверхности зубов кариесогенными бактериями Streptococcus mutans соответствует 1-у классу КОЕ<105/мл.; статистически значимых различий не выявлено. Обсемененность вестибулярной поверхности зуба - 0 класс, что соответствует КОЕ<104/мл., межзубного промежутка - 1 класс, что соответствует КОЕ<105/мл. В течение диспансерного наблюдения новых очагов кариозного поражения зубов у ребенка выявлено не было.
Пример 4
Ребенок С., 2 года 10 месяцев, кпу зубов равно 8. Плохая гигиена полости рта / ГИ - 0,68, значение кариесогенного зубного налета - 2 балла. В полости рта: 54, 53, 52, 51, 61, 62, 63, 64 зубы: острое течение кариеса, декомпенсация: кариозные полости глубокие, дентин влажный, светлый. Ребенок обследован микробиологически, согласно предлагаемого способа. Забор биоматериала осуществляли из 4-х биотопов: налет с вестибулярной и язычной поверхностей зубов, межзубного промежутка и со слизистой оболочки спинки языка. Выявили, что обсемененность слизистой спинки языка и язычной поверхности зубов кариесогенными бактериями Streptococcus mutans составила - 3 класс, что соответствует КОЕ>106/мл; статистически значимых различий не выявлено. Обсемененность вестибулярной поверхности зуба - 3 класс КОЕ>106/мл, межзубного промежутка - 3 класс, что соответствует КОЕ>106/мл. В данном клиническом случае мы не назначали аппликации коллоидного серебра с наночастицами Ag+ в концентрации 30 ppm. Ребенку провели разработанный нами комплекс лечебно-профилактических мероприятий, включающий в себя: санацию полости рта, нормализацию характера и режима питания с устранением углеводного фактора, аппликацию фторидов местно 1 раз в 3 месяца, консультацию у педиатра. После демонстрации образцов с выросшими колониями патогенных бактерий для повышения мотивации, родителей обучали гигиене полости рта с использованием зубной нити. После проведения комплекса лечебно-профилактических мероприятий без использования геля с коллоидным серебром, показатели стоматологического статуса также улучшились, обсемененность кариесогенными бактериями уменьшилась. Значение кпу осталось прежним - 8, но в структуре индекса изменился компонент «к» - «0», «п» - 8. Анализ полученных результатов показал достоверное уменьшение ГИ - 0,28, значения кариесогенности зубного налета улучшились до 1 балла. Выявили, что обсемененность слизистой спинки языка и язычной поверхности зубов кариесогенными бактериями S. mutans соответствует 1-у классу / КОЕ<105 /мл; статистически значимых различий не выявлено. Обсемененность вестибулярной поверхности зуба - 1 класс / КОЕ<105/мл, межзубного промежутка - 1 класс, что соответствует КОЕ<105/мл. В течение диспансерного наблюдения выявили прирост одного очага кариозного поражения зубов.
Пример 5
Ребенок Р., 2 года 11 месяцев, кпу зубов равно 4. Плохая гигиена полости рта / ГИ - 0,62 и выраженный кариесогенный зубной налет - 2 балла. В полости рта: 52, 51, 61, 62 зубы - хроническое течение кариеса, компенсация: кариозные полости выполненные плотным, пигментированным дентином. Ребенок обследован микробиологически, согласно предлагаемого способа. Взят биоматериал из 4-х биотопов: налет с вестибулярной и язычной поверхностей зубов, межзубного промежутка и со слизистой оболочки спинки языка. Выявили, что обсемененность слизистой спинки языка и язычной поверхности зубов кариесогенными бактериями Streptococcus mutans составила - по 3-му классу, что соответствует КОЕ>106/мл; статистически значимых различий не выявлено. Обсемененность вестибулярной поверхности зуба - 1 класс / КОЕ<105/мл, межзубного промежутка - 1 класс, что соответствует КОЕ<105/мл. В данном клиническом случае мы не назначали аппликации коллоидного серебра с наночастицами Ag+ в концентрации 30 ppm. Ребенку провели разработанный нами комплекс лечебно-профилактических мероприятий, включающий в себя: санацию полости рта, нормализацию характера и режима питания с устранением углеводного фактора, аппликацию фторидов местно 1 раз в 3 месяца, консультацию у педиатра. После демонстрации образцов с выросшими колониями патогенных бактерий для повышения мотивации, родителей обучали гигиене полости рта с использованием зубной нити. После проведения комплекса лечебно-профилактических мероприятий без использования геля с коллоидным серебром, показатели стоматологического статуса также улучшились, обсемененность кариесогенными бактериями уменьшилась. Значение кпу осталось прежним - 4, но в структуре индекса изменился компонент «к» - «0», «п» - 4. Анализ полученных результатов показал достоверное уменьшение ГИ - 0,20, значения кариесогенности зубного налета улучшились до 1 балла. Выявили, что обсемененность слизистой спинки языка и язычной поверхности зубов кариесогенными бактериями Streptococcus mutans соответствует 1-у классу / КОЕ<105/мл; статистически значимых различий не выявлено. Обсемененность вестибулярной поверхности зуба - 1 класс / КОЕ<105/мл, межзубного промежутка - 1 класс, что соответствует КОЕ<105/мл. В течение диспансерного наблюдения выявили прирост одного очага кариозного поражения зубов.
Колонизация Streptococcus mutans вестибулярной и язычной поверхностей зубов, межзубного промежутка и слизистой оболочки спинки языка
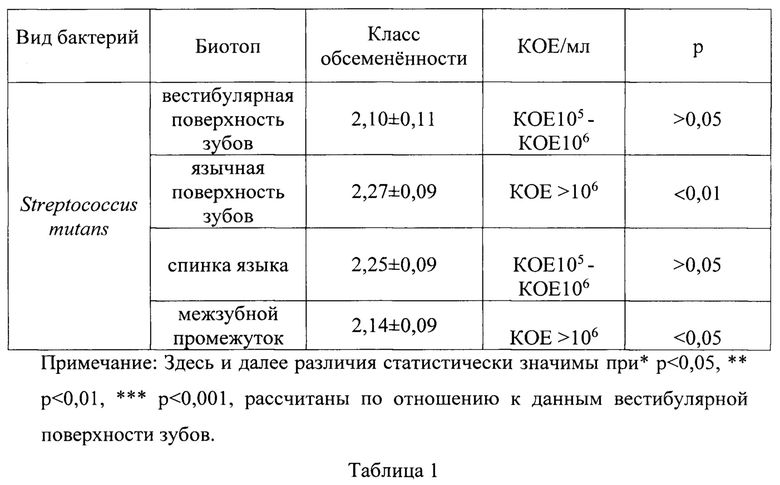
Динамика индекса кпу зубов у детей 3-х лет при проведении профилактических мероприятий(М±m)
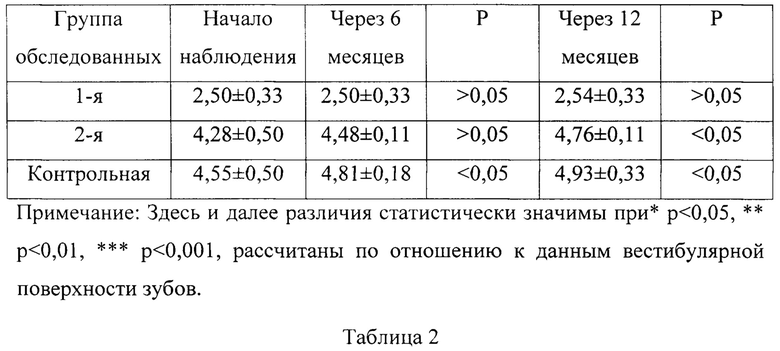
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ профилактики кариеса зубов у детей раннего возраста воздействием на управляемые факторы риска его развития | 2017 |
|
RU2685492C1 |
| Способ профилактики кариеса зубов при односеансовой санации полости рта у детей | 2023 |
|
RU2814391C1 |
| Микробиома языка как прогностическая модель для определения обсеменённости кариесогенными бактериями Streptococcus mutans твёрдых тканей зубов у детей раннего возраста | 2017 |
|
RU2661609C1 |
| Микроскопический способ определения обезвоженности тканей полости рта на модели микробиома языка | 2017 |
|
RU2668498C1 |
| Способ прогнозирования тяжести пародонтитов по составу условно-пародонтопатогенных видов микробиома корня языка | 2021 |
|
RU2773275C1 |
| Способ прогнозирования развития кариеса по результатам анализа продуктов кислотного метаболизма микрофлоры зубного налета | 2024 |
|
RU2826091C1 |
| Способ комплексного лечения и профилактики воспалительных заболеваний пародонта и слизистой оболочки рта у лиц с йододефицитом | 2023 |
|
RU2813153C1 |
| КОМПОЗИЦИЯ ДЛЯ УХОДА ЗА ПОЛОСТЬЮ РТА И ПРОФИЛАКТИКИ ЗАБОЛЕВАНИЙ ЗУБОВ И МЯГКИХ ТКАНЕЙ ПОЛОСТИ РТА И СРЕДСТВО ДЛЯ УХОДА ЗА ПОЛОСТЬЮ РТА | 2009 |
|
RU2413500C2 |
| КОМПОЗИЦИЯ НА ОСНОВЕ БРОМЕЛАИНА И ЛИЗАТА БАКТЕРИЙ ДЛЯ ПРОФИЛАКТИКИ ЗАБОЛЕВАНИЙ ПОЛОСТИ РТА | 2017 |
|
RU2748594C2 |
| Способ прогнозирования негативных последствий в полости рта при ортодонтическом лечении зубочелюстных аномалий несъемной техникой | 2014 |
|
RU2639476C2 |

Изобретение относится к области медицины, в частности к стоматологии/детской стоматологии и микробиологии/бактериологии, и может быть использовано для неспецифической профилактики и входить в комплексное лечение кариеса молочных зубов воздействием на кариесогенные S. mutans в составе микробиома языка и зубного налета язычной поверхности зубов у детей раннего возраста. Способ включает проведение стоматологического обследования детей и диагностику обсеменения бактериями S. mutans язычной поверхности молочных зубов нижней челюсти и слизистой оболочки средней трети спинки языка, использование аппликаций коллоидного серебра в виде геля с концентрацией наночастиц серебра Ag+ 30 ppm. Аппликация геля осуществляется в максимально обсемененные биотопопы S. mutans - на язычные поверхности зубов нижней челюсти и на слизистую оболочку средней трети спинки языка. В течение трехмесячного базового курса проводят аппликацию 2 раза в день утром натощак и вечером перед сном в течение 7 дн, следующие 7 дн перерыв, трехмесячный поддерживающий курс включает аппликацию 1 раз в день перед сном в течение 14 дн, следующие 14 дн перерыв. При этом перед проведением обработки биотопов гелем с наночастицами Ag+ предварительно проводят гигиеническую чистку зубов, дают ребенку 30,0-50,0 мл чистой воды. Изобретение обеспечивает безвредность применения, возможность опосредованного неспецифического лечения и профилактики кариеса зубов, воздействия в местах донации S. mutans путем применения коллоидного серебра. 1 ил., 2 табл., 5 пр.
Способ неспецифической донозологической профилактики и лечения кариеса зубов у детей раннего возраста, включающий предварительное проведение комплекса стоматологического обследования и микробиологической диагностики обсеменения бактериями Streptococcus mutans язычной поверхности временных зубов нижней челюсти и слизистой оболочки средней трети спинки языка у детей, использование аппликаций коллоидного серебра с концентрацией наночастиц серебра Ag+ 30 ppm в виде геля, отличающийся тем, что в группе с острым и хроническим течением кариеса аппликация геля с наносеребром осуществляется непосредственно в биотопы - источники Streptococcus mutans, вискозным тампоном-аппликатором, каждый раз в количестве двух капель: первую каплю геля диаметром 2,5-3 мм выдавливают из флакона, последовательно наносят на язычные поверхности зубов нижней челюсти слева и затем справа, вторую каплю наносят на среднюю треть спинки языка круговыми движениями от центра к периферии, слева направо, захватывая всю поверхность слизистой оболочки средней трети спинки языка, при этом в течение базового курса проводят аппликацию коллоидным серебром 2 раза в день утром натощак и вечером перед сном в течение 7 дн, следующие 7 дн перерыв, всего 3 мес, утром предварительно проводят гигиеническую чистку зубов, дают ребенку 30,0-50,0 мл чистой воды и через 5-7 мин последовательно наносят гель с наночастицами Ag+ на язычную поверхность зубов и спинки языка, принимают пищу через 20-30 мин; вечером перед сном, не ранее, чем через час после приема пищи и/или напитков, проводят гигиеническую чистку зубов, дают ребенку 30,0-50,0 мл чистой воды и через 5-7 мин проводят последовательную обработку язычных поверхностей зубов нижней челюсти и спинки языка, наносят гель с наночастицами Ag+; поддерживающий курс длится 3 мес, в течение 14 дн проводят аппликацию коллоидным серебром 1 раз в день перед сном, следующие 14 дн перерыв, это позволяет достичь отсутствия прироста кариеса на этапах диспансерного наблюдения.
| СПОСОБ ПЛОМБИРОВАНИЯ КАРИОЗНОЙ ПОЛОСТИ | 2015 |
|
RU2602496C1 |
| Способ финишной обработки поверхности пломбы кариозной полости | 2015 |
|
RU2610114C1 |
| СПОСОБ ЛЕЧЕНИЯ КАРИЕСА ЗУБОВ | 2013 |
|
RU2539422C1 |
| СПОСОБ ЛЕЧЕНИЯ КАРИЕСА НИТРАТОМ СЕРЕБРА | 2003 |
|
RU2243775C1 |
| JULIANA MATTOS CORRÊA et al | |||
| Int j biomater Silver Nanoparticles in Dental Biomaterials | |||
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
| Найдено в PubMed, PMCID: PMC4312639. | |||
Авторы
Даты
2018-07-17—Публикация
2017-08-14—Подача