Изобретение относится к области медицины, а именно к сердечно-сосудистой хирургии, и может быть использовано при выборе метода проведения эндокардиальных электродов в правые отделы сердца.
Имплантация постоянных электрокардиостимуляторов (ЭКС) в настоящее время является распространенным способом лечения брадисистолических нарушений сердечного ритма. Ежегодно в Российской Федерации отмечается увеличение количества этих вмешательств.
Несмотря на высокую распространенность данных операций, их протокол, включая метод проведения эндокардиальных электродов в правые отделы сердца, детально не регламентирован. Чаще операторы выполняют хирургический доступ - венесекцию v. cephalica в подключичной области, реже эндокардиальные электроды проводят через v. subclavia или v. axillaris с установкой в нее по проводнику разрывного интродьюсера без предшествующей попытки выполнить хирургический доступ к v. cephalica (Poole J., Gleva M., Mela Т. et al. Complication rates associated with pacemaker or implantable cardioverter-defibrillator generator replacements and upgrade procedures: results from the REPLACE registry. Circulation. 2010, Oct 19; 122(16):1553-61; Bongiorni M., Proclemer A., Dobreanu D. et al. Preferred tools and techniques for implantation of cardiac electronic devices in Europe: results of the European Heart Rhythm Association survey. Europace. 2013, Nov; 15(11):1664-8).
Последний вариант, по данным ряда авторов, ассоциирован с более высоким риском развития интраоперационных осложнений. В ряде случаев хирурги переходят к пункционному методу проведения эндокардиальных электродов после неудачной попытки провести их в правые отделы сердца через v. cephalica (Poole J., Gleva M., Mela Т. et al. Complication rates associated with pacemaker or implantable cardioverter-defibrillator generator replacements and upgrade procedures: results from the REPLACE registry. Circulation. 2010, Oct 19; 122(16): 1553-61; Furman S. Venous cutdown for pacemaker implantation. Ann Thorac Surg. 1986 Apr; 41(4):438-9). Оценка типа анатомического строения v. cephalica, а также вариантов ее впадения в v. axillaris, в большинстве случаев, не учитывается. В связи с этим выбор метода проведения эндокардиальных электродов, как правило, основан лишь на предпочтениях хирурга (Raatikainen M.J., Arnar D.O., Zeppenfeld К. et al. Statistics on the use of cardiac electronic devices and electrophysiological procedures in the European Society of Cardiology countries: 2014 report from the European Heart Rhythm Association. Europace. 2015 Jan; 17, i1-i75; Parsonnet V., Bernstein A., Lindsay В. et al. Pacemaker-implantation complication rates: an analysis of some contributing factors. J Am Coll Cardiol. 1989, Mar 15; 13(4):917-21).
Известен способ выбора метода проведения эндокардиальных электродов в правые отделы сердца без предоперационной оценки морфологических особенностей вен верхних конечностей. Предлагают первично выполнять попытку хирургического доступа к v. cephalica. Если v. cephalica не найдена или ее диаметр расценен как недостаточный, то считают целесообразным проводить поиск боковых притоков v. axillaris с последующим проведением через них эндокардиальных электродов в правые отделы сердца как напрямую, так и через разрывной интродьюсер, установленный по проводнику. Переход к пункционному методу выполняют, если не удалось провести эндокардиальные электроды через v. cephalica. Оценка вариантов анатомического строения вен верхних конечностей по данным ангиографии выполняется только после трех неудачных попыток выполнить пункционный доступ (Kolettis Т. М. et al. Improved 'cut-down'technique for transvenous pacemaker lead implantation // Europace. - 2010. - T. 12. - №. 9. - C. 1282-1285.). Однако известный аналог имеет недостатки: высокая травматичность вмешательства, в случае если не удается обнаружить v. cephalica в типичном месте. В такой ситуации дополнительные манипуляции с тканями, а также их разъединение при поиске боковых притоков v. axillaris связаны с более длительным периодом заживления; повышением риска развития осложнений в случае, если не удалость пунктировать и катетеризировать по проводнику v. subclavia. Повторные попытки выполнить пункцию v. subclvia могут быть ассоциированы с более высоким риском развития пневмоторакса. Перечисленные недостатки обусловлены тем, что морфологические особенности вен верхних конечностей по данным ангиографии оценивают только после трех неудачных попыток проведения эндокардиальных электродов в правые отделы сердца.
Известен способ выбора метода проведения эндокардиальных электродов в правые отделы сердца (TSE, HUNG FAT, CHU РАК LAU, AND SUM KIN LEUNG. "A cephalic vein cutdown and venography technique to facilitate pacemaker and defibrillator lead implantation." Pacing and Clinical Electrophysiology 24.4 (2001): 469-473). Авторы предлагают провести эндокардиальные электроды через v. cephalica, установив в нее по проводнику разрывной интродьюсер. Ангиографию вен верхних конечностей для уточнения особенностей их анатомического строения выполняют, если провести эндокардиальные электроды в правые отделы сердца не удалось. Переход к пункционному методу выполняют, если не удалось провести эндокардиальные электроды через v. cephalica или если она не была обнаружена в ране. Использование данного известного метода также сопряжено с повышением риски травматичности вмешательства в случае, если не удается обнаружить v. cephalica в типичном месте или провести эндокардиальные электроды через нее не удалось. В такой ситуации дополнительные манипуляции с тканями, а также их разъединение при поиске v. cephalica, связаны с более длительным периодом заживления. Это обусловлено тем, что морфологические особенности сосудистого русла по данным ангиографии оценивают только в том случае, если провести эндокардиальные электроды в правые отделы сердца не удалось.
Наиболее близким аналогом разработанного нами метода является способ оценки анатомических особенностей v. cephalica при имплантации антиаритмических устройств (Tokano Takashi et al. Variations in cephalic vein venography for device implantation-Relationship to success rate of lead implantation. Journal of Arrhythmia. Volume 29, Issue 1, February 2013, Pages 9-12). Перед проведением эндокардиальных электродов в правые отделы сердца выполняется ангиография вен верхних конечностей. Анатомические особенности вен верхних конечностей в подключичной области описываются тремя типами v. cephalica: ровный тип, извитой тип, а также отсутствие v. cephalica в подключичной области. Извитой тип v. cephalica разделен на: L-образный, сигмовидный, а также прохождение v. cephalica над ключицей. В результате описано пять анатомических вариантов. Ровный тип v. cephalica расценен как наиболее благоприятный для проведения эндокардиальных электродов в правые отделы сердца. Недостатками известного способа являются: не описан способ выбора подхода к имплантации эндокардиальных электродов в зависимости от выявленного типа v. cephalica, гладкий тип v. cephalica расценен как наиболее благоприятный для успешного проведения эндокардиальных электродов в правые отделы сердца, не представлены четкие критерии для классификации анатомических вариантов v. cephalica. При этом, например, разделение v. cephalica на L-образной и извитой тип может быть не однозначно воспроизведено различными операторами.
Недостатки прототипа обусловлены отсутствием описания угла впадения v. cephalica в v. axillaris в классификации морфологических особенностей вен верхних конечностей в подключичной области. Дополнительное разделение извитого типа v. cephalica на подтипы может быть не однозначно интерпретировано во время операции, в связи с отсутствием четких критериев для классификации.
Технической проблемой, на решение которой направлено настоящее изобретение, является оптимизация выполнения операции по имплантации электрокардиостимуляторов.
Техническим результатом, достигаемым при реализации разработанного метода, является снижение риска развития интраоперационных осложнений при имплантации электрокардиостимуляторов, а также сокращение длительности выполнения оперативного вмешательства.
Нами выявлено 4 варианта анатомического строения v. cephalica в подключичной области. Выявлено, что наиболее благоприятным вариантом анатомического строения является впадение v. cephalica в подключичную вену под углом менее 90°. Это обусловлено отсутствием затруднений при проведении эндокардиальных электродов в правые отделы сердца. При угле впадения более 90° вероятность успешного проведения ниже в связи с тем, что в этих случаях электрод продвигается в v. axillaris не в дистальном, а в проксимальном направлении. В этом случае проведение электрода в правые отделы сердца возможно при моделировании стилета эндокардиального электрода, тракции v. cephalica, использовании коронарных катетеров.
Несмотря на то что применение этих подходов, в ряде случаев, позволяет провести эндокардиальные электроды в правые отделы сердца, продолжительность операции значительно возрастает. При отсутствии v. cephalica в подключичной области необходима пункция подключичной вены.
Предоперационное определение анатомического строения v. cephalica в подключичной области позволяет добиться снижения времени рентгеноскопии, продолжительности операции и лучевой нагрузки у больных, которым выполняется ангиография v. cephalica непосредственно перед имплантацией ЭКС. Этот результат может быть объяснен тем, что хирург учитывает индивидуальные особенности анатомического строения вен верхних конечностей при проведении эндокардиальных электродов.
Таким образом, разработанный способ, благодаря предварительной оценке варианта впадения v. cephalica в v. axillaris позволяет оптимизировать оперативное вмешательство и выбрать наиболее подходящий метод проведения эндокардиальных электродов.
Пациенту перед имплантацией ЭКС выполняют ангиографию v. cephalica, определяя угол впадения v. cephalica в v. axillaris:
1) угол впадения v. cephalica в v. axillaris (L) - острый (составляет менее 90°), в этом случае применяется метод проведения эндокардиальных электродов в правые отделы сердца через v. cephalica;
2) угол впадения v. cephalica в v. axillaris - прямой (составляет около 90°), в этом случае применяется метод проведения эндокардиальных электродов в правые отделы сердца через v. cephalica. Если провести эндокардиальные электроды в правые отделы сердца через v. cephalica не удается, то переходят к пункционному методу: пунктируется v. subcalvia, по проводнику устанавливается разрывной интродьюсер, через который в правые отделы сердца проводятся эндокардиальные электроды;
3) угол впадения v. cephalica в v. axillaris - тупой (составляет более 90°), эндокардиальные электроды проводят в правые отделы сердца, используя пункционный метод: пунктируется v. subcalvia, по проводнику устанавливается разрывной интродьюсер, через который в правые отделы сердца проводятся эндокардиальные электроды;
4) v. cephalica в подключичной области на ангиограммах не визуализирована, эндокардиальные электроды проводят в правые отделы сердца, используя пункционный метод: пунктируется v. subcalvia, по проводнику устанавливается разрывной интродьюсер, через который в правые отделы сердца проводятся эндокардиальные электроды.
В исследование включено 94 пациента в возрасте 23-93 года, которым выполнена имплантация ЭКС в ГБУЗ «Городская клиническая больница им. В.М. Буянова Департамента здравоохранения г. Москвы» (таблица 1).
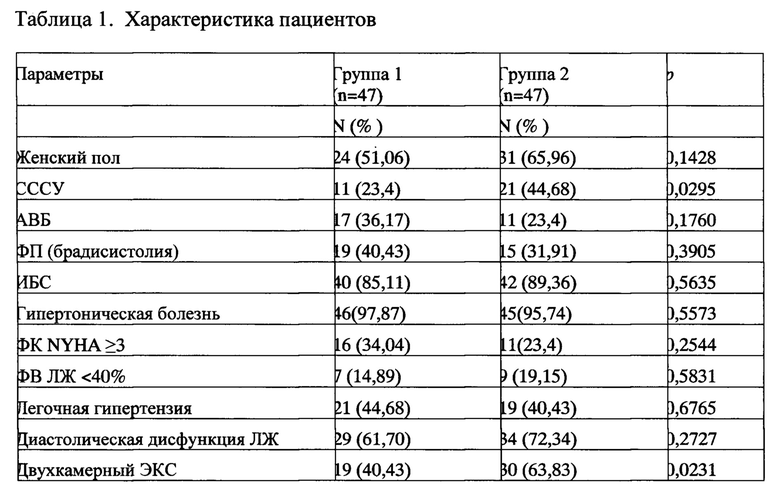
Сокращения: n - количество пациентов; N - абсолютное значение; СССУ - синдром слабости синусового узла; АВБ - атриовентрикулярная блокада; ФП - фибрилляция предсердий; ИБС - ишемическая болезнь сердца; ФК NYHA - функциональный класс недостаточности кровообращения по классификации Нью-Йоркской кардиологической ассоциации; ЛЖ - левый желудочек; р - вероятность ошибочно отвергнуть нулевую гипотезу об отсутствии различий.
В группе 1 (n=47) пациентам выполнена ангиография v. cephalica через ранее установленный катетер в области запястья левой верхней конечности в условиях рентгеноперационной непосредственно перед имплантацией ЭКС во время подготовки больного к оперативному вмешательству. При выполнении ангиографии использовали 10 мл контрастного средства Ультравист 370.
В группе 2 (n=47) имплантация ЭКС выполнялась без предшествующей ангиографии v. cephalica.
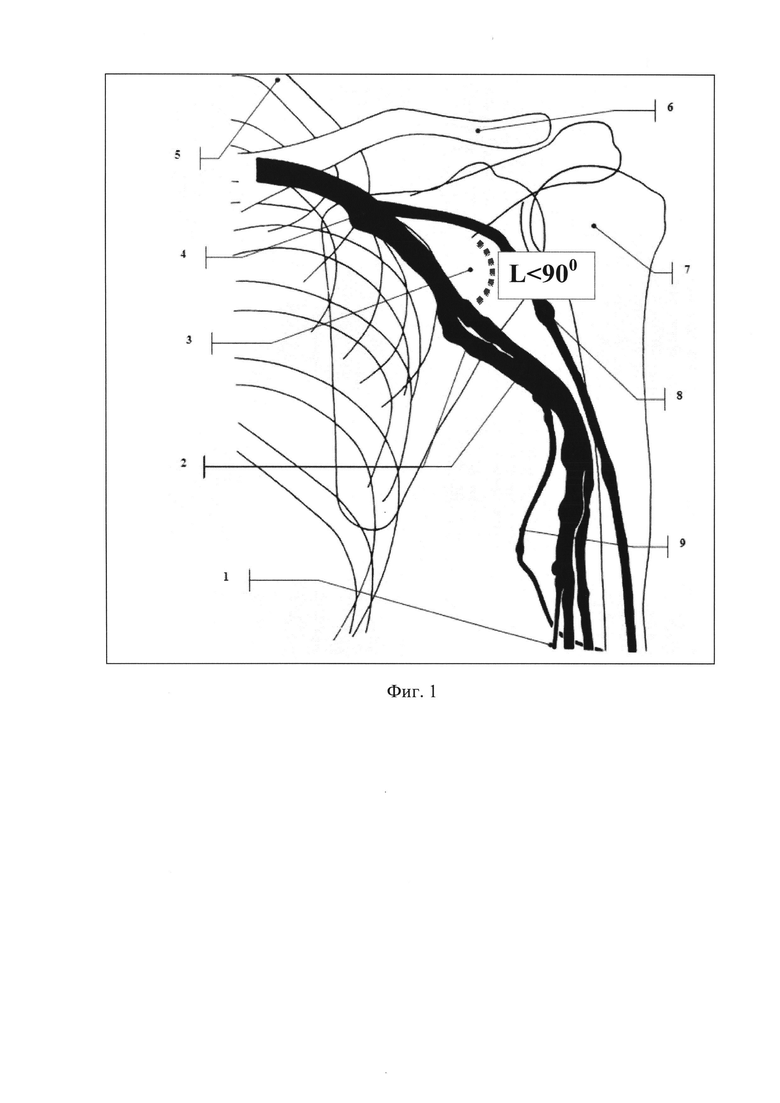
Во время выполнения ангиографии левая верхняя конечность была приведена к туловищу. При анализе результатов ангиографии оценивался угол впадения (от латерального к медиальному участку) v. cephalica в v. axillaris (фиг. 1, где 1 - V. basilica; 2 - Vv. brachiales; 3 - Scapula; 4 - V. axillaris; 5 - Costae; 6 - Clavicula; 7 - Humerus; 8 - V. cephalica; 9 - V. collateralis ulnaris).
В обеих группах кожный разрез выполнялся в левой подключичной области.
Показания к имплантации антиаритмических устройств определялись в соответствии с клиническими рекомендациями Всероссийского научного общества специалистов по клинической электрофизиологии, аритмологии и кардиостимуляции (Бокерия Л.А. и др. Клинические рекомендации по проведению электрофизиологических исследований, катетерной абляции и применению имплантируемых антиаритмических устройств [Электронный ресурс] // vnoa.ru: рекомендации всероссийского научного общества аритмологов. 2017. URL: https://vnoa.ru/upload/edition_june2017/1-1_eks.pdf).
Оперативные вмешательства выполнялись в условиях рентгеноперационной на цифровом ангиографическом комплексе. Имплантация ЭКС выполнялась под комбинированной анестезией. Во всех случаях использовались ЭКС одного производителя с пассивным типом фиксации эндокардиальных электродов.
При анализе результатов исследования в группе 1 изучалась взаимосвязь между вариантами анатомического строения v. cephalica и возможностью провести через нее эндокардиальные электроды. При сравнении групп между собой оценивались продолжительность операции и рентгеноскопии, лучевая нагрузка, осложнения.
У всех больных отсутствовали противопоказания к введению контрастных средств для выполнения ангиографии.
При сравнении результатов исследования выявлено, что в группе 1 время рентгеноскопии и продолжительность операции были статистически значимо меньше, чем в группе 2 (р=0,0002 и р<0,0001 соответственно) (Таблица 2).

Примечания: n - количество пациентов; Me - медиана; IQR - интерквартильный размах;
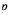 - вероятность ошибочно отвергнуть нулевую гипотезу об отсутствии различий.
- вероятность ошибочно отвергнуть нулевую гипотезу об отсутствии различий.
Анализ результатов ангиографии v. cephalica в группе 1 позволил выделить 4 варианта хода v. cephalica в подключичной области:
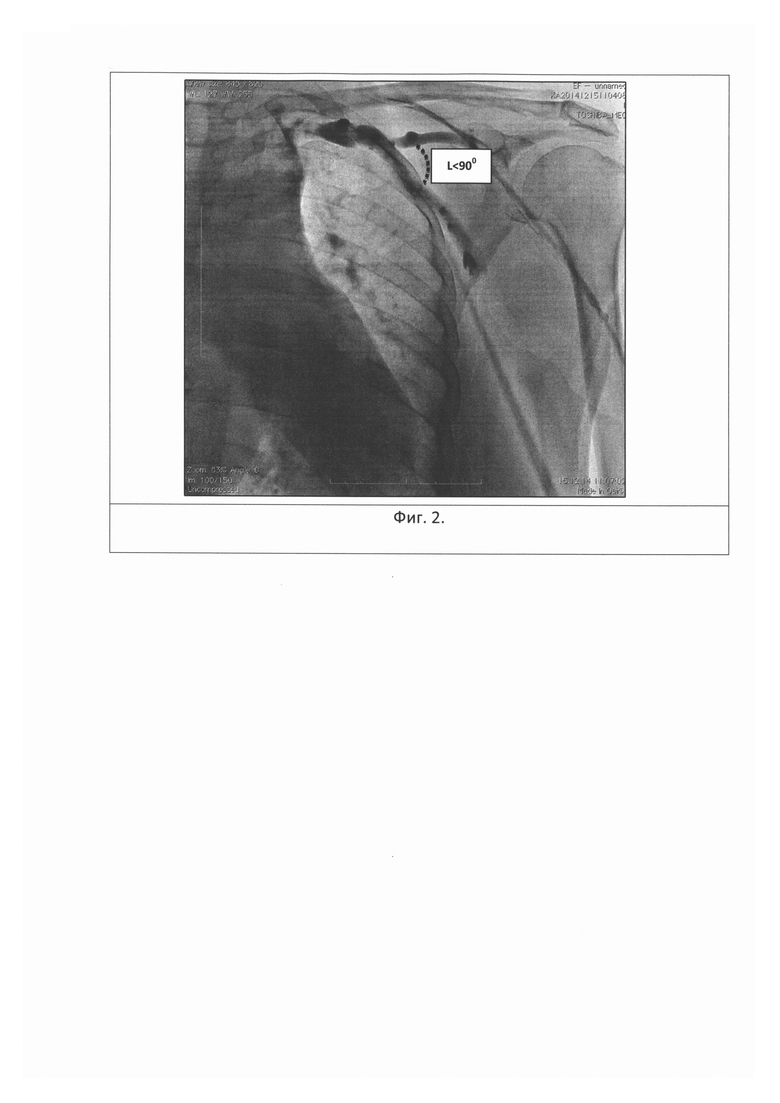
- угол впадения v. cephalica в v. axillaris (L) составляет менее 90° (n=22; 46,8%) (фиг. 2 - ангиография вен левой верхней конечности). Данный вариант впадения v. cephalica в v. axillaris является наиболее оптимальным для проведения эндокардиальных электродов в правые отделы сердца в связи с тем, что оператор не встречает анатомические препятствия, продвигая эндокардиальные электроды в дистальном направлении. При этом выявлено, что при таком анатомическом расположении эндокардиальные электроды удается провести в правые отделы сердца через v. cephalica во всех случаях;
- угол впадения v. cephalica в v. axillaris прямой (составляет около 90°) (n=9; 19,2%) (фиг. 3). Данный вариант анатомического строения ассоциирован с меньшей частотой успешного проведения эндокардиальных электродов: провести их в правые отделы сердца через v. cephalica без пункции v. subclavia удается менее чем в половине случаев (n=4; 44,44%) в связи с продвижением эндокардиальных электродов в проксимальный отдел v. axillaris;
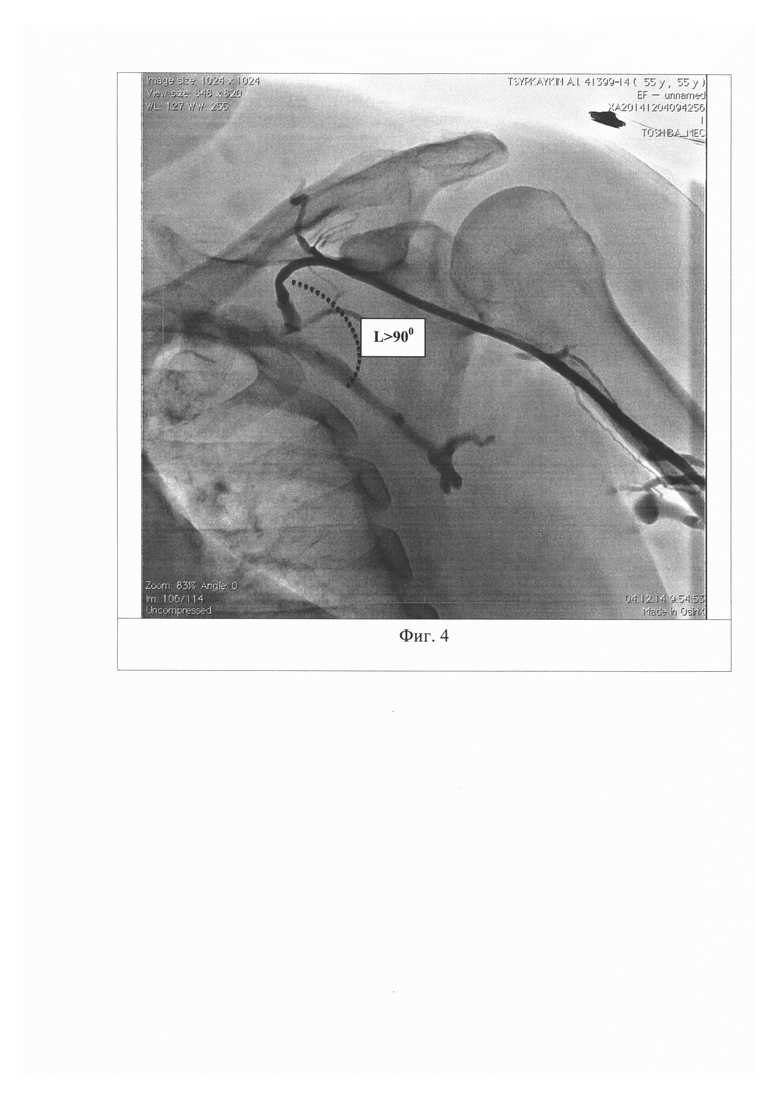
- угол впадения v. cephalica в v. axillaris (L) более 90° (n=11; 23,4%) (фиг. 4). Впадение v. cephalica в v. axillaris под углом более 90° вызывает наибольшие затруднения для проведения в правые отделы сердца эндокардиальных электродов, которые при их поступательном движении вперед продвигаются в проксимальные отделы v. axillaris. При данном варианте анатомического строения провести эндокардиальные электроды через v. cephalica в правые отделы сердца не удалось ни в одном случае и потребовалась пункция подключичной вены;
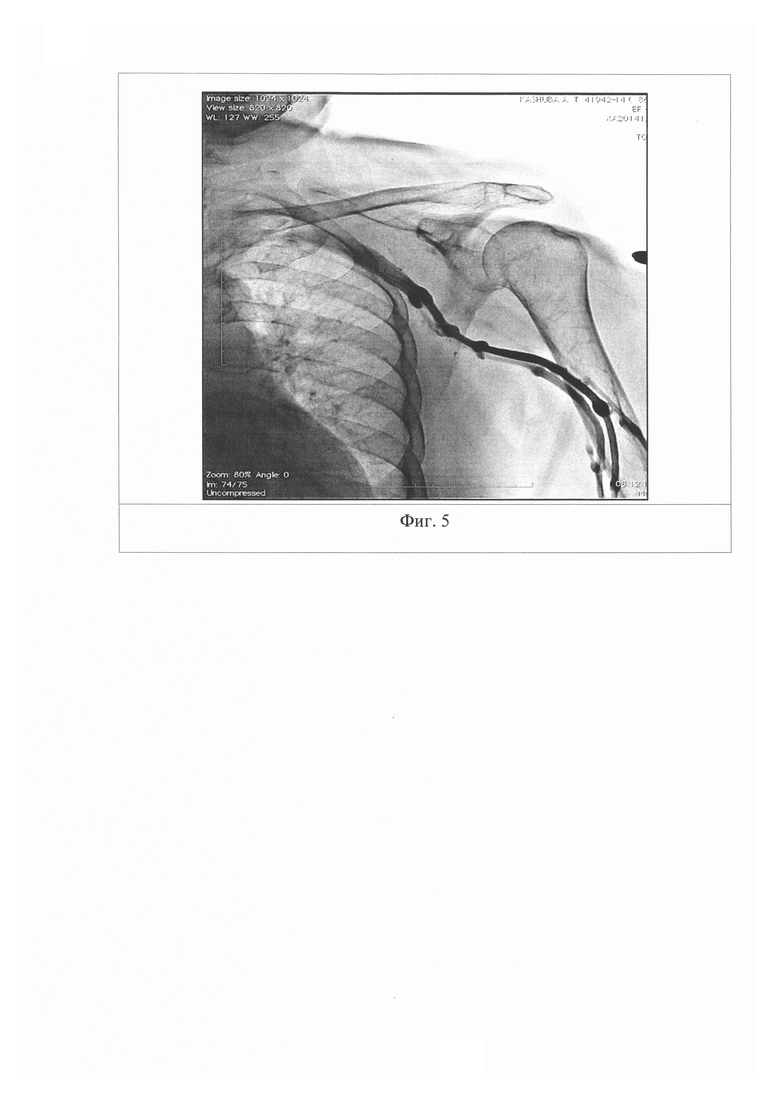
- v. cephalica в подключичной области на ангиограммах не визуализирована (n=5; 10,6%) (фиг. 5). В данном случае для проведения эндокардиальных электродов необходима пункция v. subclavia.
При анализе интраоперационных осложнений в группе 1 отмечено, что у одного больного развился гемоперикард в раннем послеоперационном периоде. В данном случае потребовалось выполнение пункции и дренирование полости перикарда на фоне проведения гемостатической терапии. В группе 2 у двух больных проведение эндокардиальных электродов оказалось невозможно в связи с окклюзией v. subclavia. В этих случаях рана ушивалась и имплантация ЭКС выполнялась с противоположной стороны после выполнения ангиографии для оценки возможности провести эндокардиальные электроды в правые отделы сердца. Также в группе 2 отмечено развитие пневмоторакса у 2 больных, которым выполнялся пункционный доступ к v. subclavia (группа 2) (Таблица 2). В этих случаях выполнялось дренирование плевральной полости. Летальных исходов не было в обеих группах.
Таким образом, проведение эндокардиальных электродов в правые отделы сердца является одним из важных этапов имплантации антиаритмического устройства. Хирургический доступ к v. cephalica, является более предпочтительным по сравнению с использованием пункционного доступа. Это объясняется тем, что пункция подключичной вены может быть ассоциирована с развитием пневмоторакса и риском перелома эндокардиальных электродов. Несмотря на риск развития пневмоторакса, по данным Европейского общества кардиологов для проведения электродов в правые отделы сердца в 40% случаев первично выполняется пункционный доступ (Bongiorni М., Proclemer A., Dobreanu D. et al. Preferred tools and techniques for implantation of cardiac electronic devices in Europe: results of the European Heart Rhythm Association survey. Europace. 2013, Nov; 15(11):1664-8). Как правило, операторы предпочитают такой подход в связи с тем, что в ряде случаев не удается провести электроды через v. cephalica. Данное обстоятельство может быть объяснено выраженностью анатомической вариабельности вен верхних конечностей.
По данным различных авторов, в 9-36% случаев проведение эндокардиальных электродов через v. cephalica не представлялось возможным. Среди причин, препятствующих использованию v. cephalica для проведения эндокардиальных электродов, отмечают технические сложности при хирургическом выделении v. cephalica, ее недостаточный диаметр, извитость, стеноз и окклюзию (Tse Н., Lau С, Leung S. et al. А cephalic vein cutdown and venography technique to facilitate pacemaker and defibrillator lead implantation. Pacing Clin Electrophysiol. 2001 Apr; 24(4 Pt 1):469-73; Knight В., Curlett K., Oral H. et al. Clinical predictors of successful cephalic vein access for implantation of endocardial leads. J Interv Card Electrophysiol. 2002 Oct; 7(2): 177-80).
Таким образом, разработанный метод, благодаря предварительной оценке варианта впадения v. cephalica в v. axillaris, позволяет оптимизировать оперативное вмешательство за счет выбора наиболее подходящего способа проведения эндокардиальных электродов, что позволяет минимизировать риск развития осложнений.
Клинический пример 1
Пациент М., 58 лет. Диагноз - Преходящая атриовентрикулярная блокада III степени с приступами Морганьи-Эдамса-Стокса.
Выполнена ангиография вен левой верхней конечности через ранее установленный катетер в области запястья в условиях рентгеноперационной непосредственно перед имплантацией ЭКС во время подготовки больного к оперативному вмешательству. При выполнении ангиографии использовали 10 мл контрастного средства Ультравист 370. Во время выполнения ангиографии левая верхняя конечность была приведена к туловищу. При анализе результатов ангиографии оценивался угол впадения (от латерального к медиальному участку) v. cephalica в v. axillaris (фиг.1.).
Выявлено, что v. cephalica впадает в v. axillaris под углом менее 90° (фиг.2). Принято решение провести эндокардиальные электроды в правые отделы сердца через v. cephalica.
Под местной анестезией Sol. Novocaini 0,25% - 150 мл в левой подключичной области выделена v. cephalica. Проведена ее венесекция. Через v. cephalica в правые отделы сердца проведены предсердный и желудочковый эндокардиальные электроды с последующей их установкой в области ушка правого предсердия и верхушки правого желудочка соответственно. Затруднений при проведении эндокардиальных электродов не было. В области дна раны фиксированы проксимальные участки эндокардиальных электродов, к которым подключен ЭКС с последующей его имплантацией в ранее сформированное ложе в подкожно-жировой клетчатке. Рана послойно ушита.
Благодаря предварительной оценке варианта впадения v. cephalica в v. axillaris выбран наиболее оптимальный способ проведения эндокардиальных электродов в правые отделы сердца.
Клинический пример 2
Пациент Б., 86 лет. Диагноз - Синдром слабости синусового узла с приступами Морганьи-Эдамса-Стокса.
Выполнена ангиография вен левой верхней конечности через ранее установленный катетер в области запястья в условиях рентгеноперационной непосредственно перед имплантацией ЭКС во время подготовки больного к оперативному вмешательству. При выполнении ангиографии использовали 10 мл контрастного средства Ультравист 370. Во время выполнения ангиографии левая верхняя конечность была приведена к туловищу. При анализе результатов ангиографии оценивался угол впадения (от латерального к медиальному участку) v. cephalica в v. axillaris (фиг. 3).
Выявлено, что v. cephalica впадает в v. axillaris под прямым углом (угол 90°). Принято решение выполнить попытку провести эндокардиальные электроды в правые отделы сердца через v. cephalica.
Под местной анестезией Sol. Novocaini 0,25% - 150 мл в левой подключичной области выделена v. cephalica. Проведена ее венесекция. Предпринята попытка провести предсердный и желудочковый эндокардиальные электроды в правые отделы сердца через v. cephalica. Под флюороскопическим контролем выполнено проведение эндокардиальных электродов в правые отделы сердца с предотвращением их установки в проксимальные отделы v. axillaris. В области дна раны фиксированы проксимальные участки эндокардиальных электродов, к которым подключен ЭКС с последующей его имплантацией в ранее сформированное ложе в подкожно-жировой клетчатке. Рана послойно ушита.
Благодаря предварительной оценке варианта впадения v. cephalica в v. axillaris выбран наиболее оптимальный способ проведения эндокардиальных электродов в правые отделы сердца. Флюороскопический контроль продвижения эндокардиальных электродов позволил предотвратить их установку в проксимальные отделы v. axillaris и успешно завершить операцию.
Клинический пример 3
Пациент Т., 55 лет. Диагноз - Постоянная форма фибрилляции предсердий, брадисистолия. Приступы Морганьи-Эдамса-Стокса.
Выполнена ангиография вен левой верхней конечности через ранее установленный катетер в области запястья в условиях рентгеноперационной непосредственно перед имплантацией ЭКС во время подготовки больного к оперативному вмешательству. При выполнении ангиографии использовали 10 мл контрастного средства Ультравист 370. Во время выполнения ангиографии левая верхняя конечность была приведена к туловищу. При анализе результатов ангиографии оценивался угол впадения (от латерального к медиальному участку) v. cephalica в v. axillaris (фиг. 4).
Выявлено, что v. cephalica впадает в v. axillaris под углом более 90°. Принято решение провести через разрывной интродьюсер, установленный пункционным способом в v. subclavia, без предшествующей попытки провести эндокардиальный электрод в правые отделы сердца через v. cephalica.
Под местной анестезией Sol. Novocaini 0,25% - 150 мл в левой подключичной области кожные покровы разъединены острым путем, сформировано ложе ЭКС в подкожно-жировой клетчатке. Из раны пунктирована v. subclavia с последующей установкой по проводнику разрывного интродьюсера, через который в правые отделы сердца проведен эндокардиальный электрод. В области дна раны фиксирован проксимальный участок эндокардиального электрода, к которому подключен ЭКС с последующей его имплантацией в ранее сформированное ложе в подкожно-жировой клетчатке. Рана послойно ушита.
Благодаря предварительной оценке варианта впадения v. cephalica в v. axillaris выбран наиболее оптимальный способ проведения эндокардиальных электродов в правые отделы сердца.
Клинический пример 4
Пациент К., 86 лет. Диагноз - Постоянная форма фибрилляции предсердий, брадисистолия. Приступы Морганьи-Эдамса-Стокса.
Выполнена ангиография вен левой верхней конечности через ранее установленный катетер в области запястья в условиях рентгеноперационной непосредственно перед имплантацией ЭКС во время подготовки больного к оперативному вмешательству. При выполнении ангиографии использовали 10 мл контрастного средства Ультравист 370. Во время выполнения ангиографии левая верхняя конечность была приведена к туловищу. При анализе результатов ангиографии оценивался угол впадения (от латерального к медиальному участку) v. cephalica в v. axillaris (фиг. 4).
Выявлено, что v. cephalica не визуализирована (Вариант 4). Принято решение провести через разрывной интродьюсер, установленный пункционным способом в v. subclavia, без предшествующих попыток поиска v. cephalica в ране.
Под местной анестезией Sol. Novocaini 0,25% - 150 мл в левой подключичной области кожные покровы разъединены острым путем, сформировано ложе ЭКС в подкожно-жировой клетчатке. Из раны пунктирована v. subclavia с последующей установкой по проводнику разрывного интродьюсера, через который в правые отделы сердца проведен эндокардиальный электрод. В области дна раны фиксирован проксимальный участок эндокардиального электрода, к которому подключен ЭКС с последующей его имплантацией в ранее сформированное ложе в подкожно-жировой клетчатке. Рана послойно ушита.
Благодаря предварительной оценке варианта впадения v. cephalica в v. axillaris выбран наиболее оптимальный способ проведения эндокардиальных электродов в правые отделы сердца.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЭНДОВАСКУЛЯРНОЙ ИМПЛАНТАЦИИ ЭНДОКАРДИАЛЬНОГО ЭЛЕКТРОДА | 2019 |
|
RU2727881C1 |
| СПОСОБ ЗАМЕНЫ ЭНДОКАРДИАЛЬНЫХ ЭЛЕКТРОДОВ ИМПЛАНТИРУЕМЫХ АНТИАРИТМИЧЕСКИХ УСТРОЙСТВ ПОСЛЕ ОРТОТОПИЧЕСКОЙ ТРАНСПЛАНТАЦИИ СЕРДЦА ПО БИАТРИАЛЬНОЙ МЕТОДИКЕ | 2014 |
|
RU2562104C1 |
| СПОСОБ ЭКСТРАКЦИИ ПЕТЛИ ЭЛЕКТРОДА ПОСТОЯННОЙ КАРДИОСТИМУЛЯЦИИ ИЗ ПРАВЫХ ОТДЕЛОВ СЕРДЦА ЧЕРЕЗ БЕДРЕННЫЙ ДОСТУП | 2018 |
|
RU2698990C2 |
| Способ удаления эндокардиальных электродов под контролем видеоторакоскопии у больных высокого риска повреждения системы верхней полой вены | 2020 |
|
RU2743616C1 |
| СПОСОБ ПУНКЦИИ И КАНЮЛЯЦИИ ПОДМЫШЕЧНОЙ ВЕНЫ | 2017 |
|
RU2641385C1 |
| Способ моделирования устойчивой фибрилляции предсердий у животных (варианты) | 2021 |
|
RU2760087C1 |
| Способ имплантации электрокардиостимулятора для постоянной кардиостимуляции | 2016 |
|
RU2618445C1 |
| Способ хирургического лечения недостаточности миокарда левого желудочка | 2017 |
|
RU2648883C1 |
| СПОСОБ ГИБРИДНОГО ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ С ВЫПОЛНЕНИЕМ ТРАНСКАТЕТЕРНОЙ ИМПЛАНТАЦИИ ЛЕГОЧНОГО КЛАПАНА ТРАНСАПИКАЛЬНЫМ ДОСТУПОМ | 2020 |
|
RU2777182C2 |
| СПОСОБ КАТЕТЕРИЗАЦИИ СЕРДЦА ДЛЯ УСТАНОВКИ ЭНДОКАРДИАЛЬНОГО ЭЛЕКТРОДА ДЛЯ ВРЕМЕННОЙ ЭЛЕКТРОКАРДИОСТИМУЛЯЦИИ У ПАЦИЕНТОВ С ОСТРЫМ КОРОНАРНЫМ СИНДРОМОМ, С ПОДЪЕМОМ СЕГМЕНТА ST, ОСЛОЖЕННЫМ НАРУШЕНИЯМИ ПРОВОДИМОСТИ (ВАРИАНТЫ) | 2015 |
|
RU2594243C1 |

Изобретение относится к области медицины, а именно к сердечно-сосудистой хирургии. По данным ангиографии визуализируют v. cephalica и определяют угол впадения v. cephalica в v. axillaris, в зависимости от которого определяют метод проведения эндокардиальных электродов (ЭЭ), а именно: если угол впадения v. cephalica в v. axillaris острый, в этом случае ЭЭ проводят в правые отделы сердца через v. cephalica; если угол впадения v. cephalica в v. axillaris прямой - ЭЭ проводят в правые отделы сердца через v. cephalica, если провести ЭЭ в правые отделы сердца через v. cephalica не удается, то используют пункционный метод: пунктируют v. subcalvia, по проводнику устанавливают разрывной интродьюсер, через который в правые отделы сердца проводят ЭЭ; если угол впадения v. cephalica в v. axillaris тупой - используют пункционный метод: пунктируют v. subcalvia, по проводнику устанавливают разрывной интродьюсер, через который в правые отделы сердца проводят ЭЭ; в том случае, если по данным ангиографии v. cephalica не визуализирована, ЭЭ проводят в правые отделы сердца, используя пункционный метод: пунктируют v. subcalvia, по проводнику устанавливают разрывной интродьюсер, через который в правые отделы сердца проводят ЭЭ. Способ позволяет снизить риск развития интраоперационных осложнений при имплантации электрокардиостимуляторов, а также сократить длительность выполнения оперативного вмешательства. 5 ил., 2 табл., 4 пр.
Способ выбора метода проведения эндокардиальных электродов в правые отделы сердца при имплантации антиаритмических устройств, включающий выполнение перед имплантацией электрокардиостимуляторов ангиографии,
отличающийся тем, что
по данным ангиографии визуализируют v. cephalica и определяют угол впадения v. cephalica в v. axillaris, в зависимости от которого определяют метод проведения эндокардиальных электродов (ЭЭ), а именно:
если угол впадения v. cephalica в v. axillaris острый, в этом случае ЭЭ проводят в правые отделы сердца через v. cephalica;
если угол впадения v. cephalica в v. axillaris прямой - ЭЭ проводят в правые отделы сердца через v. cephalica, если провести ЭЭ в правые отделы сердца через v. cephalica не удается, то используют пункционный метод: пунктируют v. subcalvia, по проводнику устанавливают разрывной интродьюсер, через который в правые отделы сердца проводят ЭЭ;
если угол впадения v. cephalica в v. axillaris тупой - используют пункционный метод: пунктируют v. subcalvia, по проводнику устанавливают разрывной интродьюсер, через который в правые отделы сердца проводят ЭЭ;
в том случае, если по данным ангиографии v. cephalica не визуализирована, ЭЭ проводят в правые отделы сердца, используя пункционный метод: пунктируют v. subcalvia, по проводнику устанавливают разрывной интродьюсер, через который в правые отделы сердца проводят ЭЭ.
| Tokano Takashi et al | |||
| Variations in cephalic vein venography for device implantation-Relationship to success rate of lead implantation | |||
| Journal of Arrhythmia | |||
| Солесос | 1922 |
|
SU29A1 |
| СПОСОБ ВЫБОРА ХИРУРГИЧЕСКОГО СПОСОБА ДОСТАВКИ ЛЕВОЖЕЛУДОЧКОВОГО ЭЛЕКТРОДА ПРИ ЛЕЧЕНИИ СИНДРОМА ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ | 2010 |
|
RU2493779C2 |
| АГЕЕВ Ф.Т., ДАНИЕЛЯН М.О., МАРЕЕВ В.Ю | |||
| и др | |||
| Больные с хронической сердечной недостаточностью в российской амбулаторной практике: особенности контингента, диагностики и лечения (по материалам исследования ЭПОХА-О-ХСН) | |||
| - Сердечная недостаточность, 2004; 5(1):4-7 | |||
| TSE, HUNG FAT, CHU РАК LAU, AND SUM KIN LEUNG | |||
| Пишущая машина для тюркско-арабского шрифта | 1922 |
|
SU24A1 |
Авторы
Даты
2018-07-25—Публикация
2018-03-16—Подача