Предлагаемое изобретение относится к области органической химии, в частности, к способу получения 3-циклоалкил-1,5,8-тритиа-3-азациклодеканов общей формулы (1):
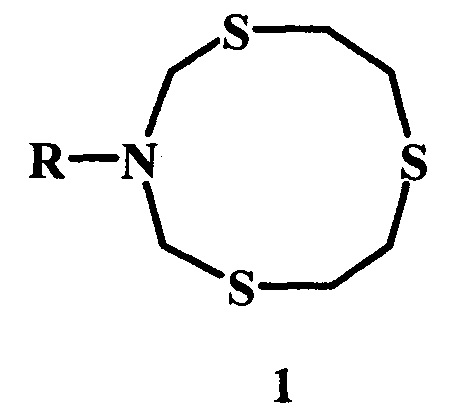
R = цикло-С3Н5, цикло-C5H9, цикло-С6Н11, цикло-С5Н9О, цикло-С7Н13, цикло-С8Н15
S,N-Содержащие макрогетероциклы находят применение в качестве селективных комплексообразователей меди и цинка [W.A. Freeman, W.L. Mock, N.-Y. Shih // J. Am. Chem. Soc., 1981, 103, 7367], ртути [Granzhan A., Ihmels H., Tian M. Arkivoc, 2015, vi, 494], а также эффективных сорбентов для выделения и очистки драгоценных металлов [Хираока М. Краун-соединения: свойства и применение. М.: Мир, 1986; Akhmetova V.R., Rakhimova Е.В., Vagapov R.A., Minnebaev A.B., Kopylova E.V., Buslaeva T.M., Kunakova R.V. // Trends in Heterocyclic Chemistry, 2011, 15(9), 33; Behcini A., Bianchi A., Dappoto P.J. // Chem. Soc. Chem. Commun., 1990, 1382; Bencini A., Bianchi A., Dapporto P. // Inorg. Chem., 1993, 32, 1204], ионофоров [Granzhan A., Ihmels H., Tian M. Arkivoc, 2015, vi, 494].
Известен способ [M.W. Glenny, L.G.A. van de Water, J.M. Vere, A.J. Blake, C. Wilson, W.L. Driessen, J. Reedijk, M. Schroder. Polyhedron, 2006, 25, 599] получения нитрофенил-1,4,7-тритиа-10-азациклододекана (2) взаимодействием бис-тозилпроизводного N,N-бис(гидроксиэтил)-N-нитрофениламина с 3-тиа-1,5-пентандитиолом в присутствии Cs2CO3.

Известным способом не могут быть получены 3-циклоалкил-1,5,8-тритиа-3-азациклодеканы общей формулы (1).
Известен способ [Pop А.М. Abstract PhD Thesis, Cluj-Napoca, 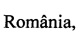 2012] получения (2-бромбензил)-1,4,7-тритиа-10-азациклододекана (3) взаимодействием 1,4,7-тритиа-10-азациклододекана со стехиометрическим количеством 2-бромбензилбромида в присутствии K2CO3 при кипячении.
2012] получения (2-бромбензил)-1,4,7-тритиа-10-азациклододекана (3) взаимодействием 1,4,7-тритиа-10-азациклододекана со стехиометрическим количеством 2-бромбензилбромида в присутствии K2CO3 при кипячении.

Известным способом не могут быть получены 3-циклоалкил-1,5,8-тритиа-3-азациклодеканы общей формулы (1).
Известен способ [Makhmudiyarova N.N., Mudarisova L.V., Meshcheryakova E.S., Ibragimov A.G., Dzhemilev U.M. Tetrahedron, 2015, 71, 259] получения 3-арил-1,5,3-дитиазеканов (4) взаимодействием N,N-бис(метоксиметил)-N-ариламинов с 1,5-пентандитиолом в присутствии Sm(NO3)3/γ-Al2O3 в качестве катализатора.

Ar=Ph, СН3С6Н4, СН3ОС6Н4, ClC6H4, BrC6H4
Известным способом не могут быть получены 3-циклоалкил-1,5,8-тритиа-3-азациклодеканы общей формулы (1).
Таким образом, в литературе отсутствуют сведения по получению 3-циклоалкил-1,5,8-тритиа-3-азациклодеканов общей формулы (1).
Предлагается новый способ получения 3-циклоалкил-1,5,8-тритиа-3-азациклодеканов общей формулы (1).
Сущность способа заключается во взаимодействии циклоалкиламина (циклопропил-амин, или циклопентил-амин, или циклогексил-амин, или тетрагидропиранил-амин или циклогептил-амин, или циклооктил-амин) с 1-окса-3,6,9-тритиациклодеканом в присутствии катализатора SmCl3⋅6H2O, взятыми в мольном соотношении циклоалкиламин: 1-окса-3,6,9-тритиациклодекан: SmCl3⋅6H2O = 1:1:(0.03-0.07), предпочтительно 1:1: 0.05, при комнатной температуре (~20°С) и атмосферном давлении в среде растворителей этанол-хлороформ (1:1, объемное соотношение) в течение 2.5-3.5 ч. Выход 3-циклоалкил-1,5,8-тритиа-3-азациклодеканов (1) составляет 72-95%. Реакция протекает по схеме:

3-Циклоалкил-1,5,8-тритиа-3-азациклодеканы общей формулы (1) образуются только лишь с участием циклоалкиламина и 1-окса-3,6,9-тритиациклодекана, взятых в стехиометрических количествах. При другом соотношении исходных реагентов снижается селективность реакции. Без катализатора SmCl3⋅6H2O реакция идет с выходом, не превышающим 30%. Проведение реакции в присутствии катализатора SmCl3⋅6H2O больше 7 мол. % не приводит к существенному увеличению выхода целевого продукта (1). Использование в реакции катализатора SmCl3⋅6H2O менее 3 мол % снижает выход (1), что связано с уменьшением каталитически активных центров в реакционной массе. Реакции проводили при комнатной температуре ~20°С. При более высокой температуре (например, 60°С) увеличиваются энергозатраты, при меньшей температуре (например, 0°С) снижается скорость реакции. Опыты проводили в среде растворителей этанол-хлороформ (1:1, объемное соотношение), т.к. в них хорошо растворяются исходные реагенты и целевые продукты.
Существенные отличия предлагаемого способа:
В известном способе реакция идет с участием в качестве исходных реагентов N,N-бис(метоксиметил)-N-ариламинов и 1,5-пентандитиола в присутствии катализатора Sm(NO3)3/γ-Al2O3 с образованием 3-арил-1,5,3-дитиазеканов (4). Известный способ не позволяет получать 3-циклоалкил-1,5,8-тритиа-3-азациклодеканы общей формулы (1).
В предлагаемом способе в качестве исходных реагентов применяются циклоалкиламины и 1-окса-3,6,9-тритиациклодекан. Реакция осуществляется в присутствии катализатора SmCl3⋅6H2O.
Предлагаемый способ обладает следующими преимуществами:
Способ позволяет получать 3-циклоалкил-1,5,8-тритиа-3-азациклодеканы общей формулы (1), синтез которых в литературе не описан.
Способ поясняется следующими примерами:
ПРИМЕР 1. Синтез 1-окса-3,6,9-тритиациклодекана: смесь 6 мл 37% водного раствора формалина и 2.6 мл 3-тиа-1,5-пентандитиола перемешивают 3 ч при 20°С, экстрагируют CHCl3, упаривают и выделяют 1-окса-3,6,9-тритиацикло декан.
ПРИМЕР 2. В круглодонную колбу, установленную на магнитной мешалке, помещают 57 мг (1 ммоль) циклопропиламина в 5 мл этанола, 18 мг (0.05 ммоль) SmCl3⋅6H2O и 196 мг (1 ммоль) 1-окса-3,6,9-тритиациклодекана в 5 мл хлороформа. Реакционную смесь перемешивают при температуре ~20°С в течение 3 ч, колоночной хроматографией на SiO2 выделяют 3-циклопропил-1,5,8-тритиа-3-азациклодекан с выходом 90%.
Другие примеры, подтверждающие способ, приведены в таблице 1.

Все опыты проводили при комнатной температуре (~20°С) в среде растворителей этанол-хлороформ (1:1, объемное соотношение), т.к. в них растворяются исходные и целевые продукты.
Спектральные характеристики 3-циклопропил-1,5,8-тритиа-3-азациклодекана1: (1Контроль реакции осуществляли методом ТСХ на пластинах Sorbfil (ПТСХ-АФ-В), проявляли парами I2. Для колоночной хроматографии использовали силикагель КСК (100-200 мкм). Спектры ЯМР 1D (1Н, 13С) и 2D (COSY, HSQC, НМВС) сняты на спектрометре Bruker Avance 400 (100.62 МГц для 13С и 400.13 МГц для 1Н) по стандартным методикам фирмы Bruker, внутренний стандарт Me4Si, растворитель - CDCl3).
Элюент толуол-этилацетат-ацетон 4:1:1, Rf 0.8.
Спектр ЯМР 1Н (CDCl3, δ, м.д.): 0.43 уш. с (2Н, СН2, На-12,13), 0.57 уш. с (2Н, СН2, Hb-12,13), 2.19 т (1H, СН, Н-11, J 6.4 и 3.2 Гц), 2.74 уш. с (8Н, СН2, Н-6,7,9,10), 4.13 уш. с (4Н, СН2, Н-2,4).
Спектр ЯМР 13С (CDCl3, δ, м.д.): 7.94 (С-12, С-13), 32.34 (С-7, С-9), 32.71 (С-6, С-10), 34.08 (С-11), 56.11 (С-2, С-4).

Элюент гексан-этилацетат 1:5, Rf 0.7.
Спектр ЯМР 1Н (CDCl3, δ, м.д.): 1.37-1.42 м (2Н, СН2, На-13,14), 1.57-1.62 м (2Н, СН2, На-12,15), 1.69-1.74 м (2Н, СН2, Hb-12,15), 1.86-1.91 м (2Н, СН2, Hb-13,14), 2.78 уш. с (8Н, СН2, Н-6,7,9,10), 3.05-3.13 м (1Н, СН, Н-11), 4.16 уш. с (4Н, СН2, Н-2,4).
Спектр ЯМР 13С (CDCl3, δ, м.д.): 23.58 (С-13, С-14), 31.16 (С-12, С-15), 31.95 (С-7, С-9), 32.83 (С-6, С-10), 55.02 (С-2, С-4), 62.05 (С-11).

Элюент хлороформ-ацетон-метанол 1:2:1, Rf 0.9.
Спектр ЯМР 1H (CDCl3, δ, м.д.): 1.05-1.14 м (1Н, СН2, На-14), 1.21-1.31 м (4Н, СН2, На-12,13,15,16), 1.58-1.67 м (1Н, СН2, Hb-14), 1.75-1.85 м (4Н, СН2, Hb-12,13,15,16), 2.61-2.75 м (8Н, СН2, Н-6,7,9,10; 1Н, СН, Н-11), 4.10-4.18 м (4Н, СН2, Н-2,4).
Спектр ЯМР 13С (CDCl3, δ, м.д.): 25.88 (С-13, С-14, С-15), 30.63 (С-12, С-16), 31.55 (С-7, С-9), 32.71 (С-6, С-10), 54.13 (С-2, С-4), 59.40 (С-11).

Элюент хлороформ-ацетон-метанол 1:2:1, Rf 0.7.
Спектр ЯМР 1Н (CDCl3, δ, м.д.): 1.58-1.65 м (2Н, СН2, На-12,16), 1.71-1.79 м (2Н, СН2, Hb-12,16), 2.79 уш. с (4Н, СН2, Н-7,9), 2.81 уш. с (4Н, СН2, Н-6,10), 3.01-3.07 м (1Н, СН, Н-11), 3.36-3.42 м (2Н, СН2, На-13,15), 3.99-4.05 м (2Н, СН2, Hb-13,15), 4.12 уш. с (4Н, СН2, Н-2,4).
Спектр ЯМР 13C (CDCl3, δ, м.д.): 30.76 (С-12, С-16), 31.77 (С-7, С-9), 32.73 (С-6, С-10), 53.88 (С-2, С-4), 56.20 (С-11), 67.40 (С-13, С-15).
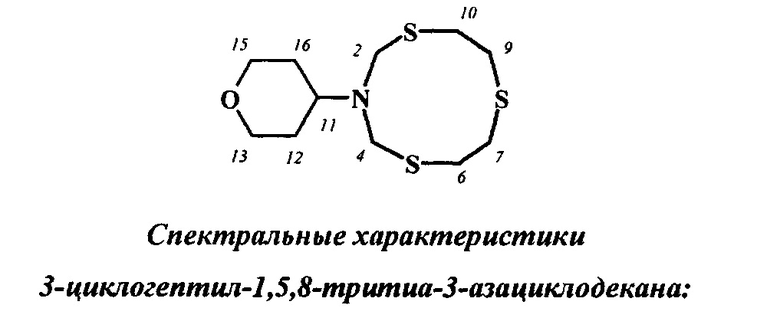
Элюент толуол-этилацетат-ацетон 4:1:1, Rf 0.8.
Спектр ЯМР 1Н (CDCl3, δ, м.д.): 1.38-1.49 м (6Н, СН2, На-12,13,14,15,16,17), 1.55-1.62 м (2Н, СН2, Hb-14,15), 1.65-1.72 м (2Н, СН2, Hb-13,16), 1.78-1.85 м (2Н, СН2, Hb-12,17), 2.77-2.84 м (8Н, СН2, Н-6,7,9,10), 2.95-3.05 м (1H, СН, Н-11), 3.99-4.09 м (4Н, СН2, Н-2,4).
Спектр ЯМР 13С (CDCl3, δ, м.д.): 25.29 (С-13, С-16), 27.69 (С-14, С-15), 31.21 (С-7, С-9), 31.95 (С-12, С-17), 32.65 (С-6, С-10), 53.82 (С-2, С-4), 60.99 (С-11).

Спектральные характеристики 3-циклооктил-7,5,8-тритиа-3-азациклодекана:
Элюент толуол-этилацетат-ацетон 4:1:1, Rf 0.7.
Спектр ЯМР 1Н (CDCl3, δ, м.д.): 1.42-1.58 м (10Н, СН2, На-12,14,16,18; Н-13,15,17), 1.65-1.72 м (4Н, СН2, Hb-12,14,16,18), 2.65-1.78 м (8Н, СН2, Н-6,7,9,10), 2.95-3.05 м (1H, СН, Н-11), 4.04 уш. с (4Н, СН2, Н-2,4).
Спектр ЯМР 13С (CDCl3, δ, м.д.): 25.11 (С-14, С-16), 26.16 (С-15), 26.57 (С-13, С-17), 31.26 (С-12, С-18), 31.31 (С-7, С-9),, 32.74 (С-6, С-10), 53.92 (С-2, С-4), 60.70 (С-11).

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ МЕТИЛ 2-(1, 5, 8-ТРИТИА-3-АЗАЦИКЛОДЕКАН-3-ИЛ)АЛКАНОАТОВ И ДИМЕТИЛ 2, 2'-(1, 5, 8, 11, 15, 18-ГЕКСАТИА-3, 13-ДИАЗАЦИКЛОИКОЗАН-3, 13-ДИИЛ)ДИАЛКАНОАТОВ | 2016 |
|
RU2632672C1 |
| СПОСОБ ПОЛУЧЕНИЯ 6-ЦИКЛОАЛКИЛ-1,11-ДИОКСА-4,8-ДИТИА-6-АЗАЦИКЛОТРИДЕКАНОВ | 2017 |
|
RU2664659C2 |
| СПОСОБ ПОЛУЧЕНИЯ БИС-(1,5,3-ДИТИАЗЕПАН-3-ИЛ)ЦИКЛОГЕКСАНОВ | 2014 |
|
RU2574069C1 |
| СПОСОБ ПОЛУЧЕНИЯ МЕТИЛ 2-(1,5,3-ДИТИАЗЕПАН-3-ИЛ)АЛКАНОАТОВ | 2015 |
|
RU2605448C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-ЦИКЛОГЕКСИЛЗАМЕЩЕННЫХ 1,5,3-ДИТИАЗЕПАНОВ | 2014 |
|
RU2574074C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-ЦИКЛОПЕНТИЛЗАМЕЩЕННЫХ 1,5,3-ДИТИАЗЕПАНОВ | 2014 |
|
RU2565790C1 |
| СПОСОБ ПОЛУЧЕНИЯ 12-ЦИКЛОАЛКИЛ-12,13,13b,13c-ТЕТРАГИДРО-6Н,11Н,14Н-4b,5a,10b,12,13a-ПЕНТААЗАДИБЕНЗО[a,h]ЦИКЛОГЕПТА[1,2,3,4-def]ФЛУОРЕНОВ | 2020 |
|
RU2735740C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,7-ДИАЛКИЛ-2,3а,5а,7,8а,10а-ГЕКСААЗАПЕРГИДРОПИРЕНОВ | 2014 |
|
RU2561506C1 |
| СПОСОБ ПОЛУЧЕНИЯ N,N-БИС-[(1,5,3-ДИТИАЗЕПАН-3-ИЛ)АЛКИЛ]АМИНОВ | 2014 |
|
RU2591196C2 |
| СПОСОБ ПОЛУЧЕНИЯ N-ЦИКЛОАЛКИЛЗАМЕЩЕННЫХ 1,5,3-ДИТИАЗЕПАНОВ | 2017 |
|
RU2664654C2 |
Изобретение относится к способу получения 3-циклоалкил-1,5,8-тритиа-3-азациклодеканов общей формулы (1):
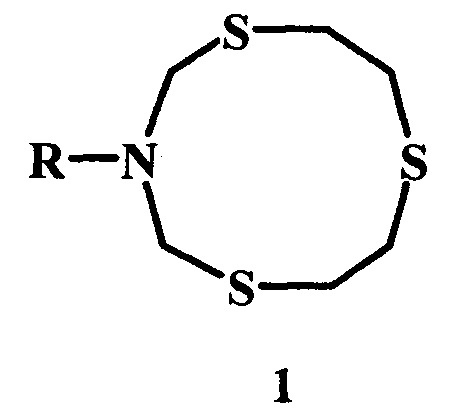
где R = цикло-С3Н5, цикло-C5H9, цикло-С6Н11, цикло-С5Н9О, цикло-С7Н13, цикло-С8Н15,
в котором циклоалкиламин (циклопропил-амин, или циклопентил-амин, или циклогексил-амин, или тетрагидропиранил-амин или циклогептил-амин, или циклооктил-амин) подвергают взаимодействию с 1-окса-3,6,9-тритиациклодеканом в присутствии катализатора SmCl3⋅6H2O при мольном соотношении циклоалкиламин : 1-окса-3,6,9-тритиациклодекан : SmCl3⋅6H2O = 1:1:(0.03-0.07) при комнатной температуре (~20°C) в среде растворителей этанол-хлороформ (1:1, объемное соотношение) в течение 2.5-3.5 ч. Технический результат: предложен способ получения 3-циклоалкил-1,5,8-тритиа-3-азациклодеканов общей формулы (1) с высоким выходом. 1 табл., 2 пр.
Способ получения 3-циклоалкил-1,5,8-тритиа-3-азациклодеканов общей формулы (1):
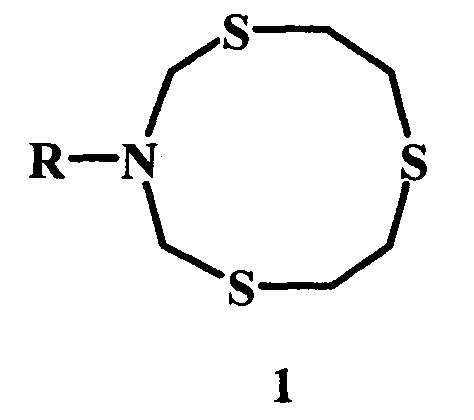
где R = цикло-С3Н5, цикло-C5H9, цикло-С6Н11, цикло-С5Н9О, цикло-С7Н13, цикло-С8Н15,
отличающийся тем, что циклоалкиламин (циклопропил-амин, или циклопентил-амин, или циклогексил-амин, или тетрагидропиранил-амин или циклогептил-амин, или циклооктил-амин) подвергают взаимодействию с 1-окса-3,6,9-тритиациклодеканом в присутствии катализатора SmCl3⋅6H2O при мольном соотношении циклоалкиламин : 1-окса-3,6,9-тритиациклодекан : SmCl3⋅6H2O = 1:1:(0.03-0.07) при комнатной температуре (~20°C) в среде растворителей этанол-хлороформ (1:1, объемное соотношение) в течение 2.5-3.5 ч.
| СПОСОБ ПОЛУЧЕНИЯ N-ЦИКЛОПЕНТИЛЗАМЕЩЕННЫХ 1,5,3-ДИТИАЗЕПАНОВ | 2014 |
|
RU2565790C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-ЦИКЛОГЕКСИЛЗАМЕЩЕННЫХ 1,5,3-ДИТИАЗЕПАНОВ | 2014 |
|
RU2574074C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-ЦИКЛОАЛКИЛЗАМЕЩЕННЫХ 1, 5, 3-ДИТИАЗЕПАНОВ | 2015 |
|
RU2601313C1 |
| M | |||
| W | |||
| Glenny et al | |||
| "Improved syntheticmethods to mixed-donor thiacrown ethers" Polyhedron, vol.25, 2006, 599-612 | |||
| N | |||
| N | |||
| Makhmudiyarova et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Контрольный стрелочный замок | 1920 |
|
SU71A1 |
Авторы
Даты
2018-08-21—Публикация
2017-02-20—Подача