Область техники, к которой относится изобретение
Настоящее изобретение относится к области лечебного питания и, в частности, относится к композиции, применяемой для улучшения или сохранения функциональной синаптической связи и/или улучшения или сохранения сетевой организации головного мозга, в частности, применяемой для исправления нарушения функциональной синаптической связи в областях головного мозга и/или улучшения или сохранения сетевой организации головного мозга у субъекта, в частности у субъекта, имеющего нарушенную функциональную связь или имеющего нарушенную сетевую организацию головного мозга.
Более конкретно, настоящее изобретение относится к композиции, применяемой для улучшения или сохранения функциональной синаптической связи и/или сетевой организации головного мозга, в частности, применяемой для исправления нарушения функциональной синаптической связи в областях головного мозга и/или улучшения или сохранения сетевой организации головного мозга у субъекта, в частности у субъекта, имеющего неврологическое расстройство или имеющего риск развития такого расстройства, в частности нейродегенеративное заболевание и/или нарушенную функциональную связь и/или нарушенную сетевую организацию головного мозга, в частности у пациентов, страдающих болезнью Альцгеймера или имеющих риск развития такого заболевания.
Описание уровня техники
Связи головного мозга являются наиболее важными при изучении того, как нейроны и нейронные сети обрабатывают информацию, а также они лежат в основе многих нейродегенеративных последствий. В этой области существует фундаментальное различие между структурой анатомических взаимосвязей («анатомическая связь»), статистическими зависимостями нейрофизиологических или других динамических рядов, формирующихся в различных участках головного мозга («функциональная связь»), и причинно-следственными взаимодействиями («эффективная связь»), все в рамках общего понятия связей головного мозга [Horwitz (2003)].
Термин «анатомическая связь» относится к сети физических или структурных (синаптических) связей, соединяющих множества нейронов или нейрональных элементов, а также к связанным с ними структурным биофизическим свойствам, определяемым такими параметрами, как синаптическая сила или эффективность. Физическая структура анатомических связей является относительно стабильной в течение коротких промежутков времени (от секунд до минут). В течение более длинных промежутков времени (от часов до дней) структурный характер связи, вероятно, подвергается значительным морфологическим изменениям и пластичности.
Функциональная связь отражает функциональные взаимодействия между соответствующими участками головного мозга. Она определяется как «временные корреляции между пространственно удаленными нейрофизиологическими событиями» (Lee et al., 2003 и Friston et al., 1993a). Как правило, способ оценки функциональной связи включает в себя отклонения от статистической независимости между распределенными и часто пространственно удаленными нейрональными единицами. Статистическая зависимость может быть оценена путем измерения корреляции или ковариации, спектральной когерентности или фазовой синхронизации. Функциональная связь часто измеряется между всеми элементами системы, независимо от того, соединены ли эти элементы непосредственными структурными связями. В отличие от структурной связи, функциональная связь в высокой степени зависит от времени. Статистические связи между нейрональными элементами изменяются в течение множественных промежутков времени, некоторые из которых составляют от десятков до сотен миллисекунд. Следует отметить, что функциональная связь не имеет никакого явного отношения к конкретным направленным действиям или лежащей в их основе структурной модели.
Эффективную связь можно рассматривать как объединение структурной и функциональной связи, так как она описывает сети направленных действий одного нейронального элемента через другой.
Подобно функциональной связи, понятие сетевой организации головного мозга известно из уровня техники и описано в следующих источниках: D.S. Bassett (2009), Bullmore (2009), Cabral (2011) и Bassett (2006), все включены в настоящее изобретение путем ссылки. В данной области техники было установлено, что оптимальной сетевой организацией головного мозга является так называемая сеть «тесного мира», подобно тому, как это было обнаружено для многих других естественных сетей. По-видимому, связи головного мозга не являются случайными, а оптимально организованы. Сетевая организация головного мозга связана с когнитивной деятельностью [van den Heuvel (2009); Lange (2009); обе эти работы включены в настоящее изобретение путем ссылки], и функциональные исследования сети показали, что оптимальная сеть «тесного мира» нарушена у пациентов с болезнью Альцгеймера по сравнению с контрольной группой и имеет дезорганизованную случайную топологию. Эту дезорганизацию сетевой организации головного мозга можно отслеживать при помощи стандартных методов визуализации, таких как ЭЭГ, МЭГ и фМРТ. Существует ряд нейродегенеративных заболеваний, характеризующихся пониженной функциональной связью, потерей синапсов и нарушенной сетевой организацией головного мозга. Болезнь Альцгеймера является таким нейродегенеративным заболеванием и основной причиной деменции, при которой потеря синапсов сильнейшим образом структурно коррелирует с когнитивным нарушением. Основные паталогические признаки болезни Альцгеймера включают в себя накопление бета-амилоидных бляшек и нейрофибриллярных клубков, что обусловлено ненормальным процессингом белка. С самого начала процесса заболевания, до того как заболевание будет диагностировано, имеет место потеря синапсов и снижение синаптической активности и связи в конкретных областях головного мозга, а также ухудшение сетевой организации головного мозга. Это приводит к классическим клиническим признакам болезни Альцгеймера: ухудшению памяти, нарушению речи и дисфункции целенаправленной деятельности и зрительно-пространственных способностей. Считается, что ухудшение сетевой организации головного мозга и потеря синапсов имеют самую непосредственную корреляцию с когнитивной деятельностью при болезни Альцгеймера, даже большую, чем количество бляшек или клубков или степень потери нейронов. Как указано выше, связь между сетевой организацией головного мозга, в частности изменениями в ней, и когнитивной функцией или интеллектом изучалась в данной области техники. Таким образом, считается, что улучшение синаптического состояния и сохранение или поддержание сетевой организации головного мозга, вероятно, может быть первичной терапевтической целью при болезни Альцгеймера.
В последнее десятилетие уридин, холин и омега-3 жирные кислоты, такие как ДГК, привлекли внимание в качестве активных компонентов при лечении связанных с болезнью Альцгеймера функциональных симптомов, таких как когнитивная дисфункция и возрастное нарушение памяти (ВНП), см., например, WO 2007/089703 (Massachusetts Institute of Technology) и WO 2009/002165 (N.V. Nutricia). В соответствии с этим, улучшение памяти при приеме лечебного питания, содержащего комбинацию конкретных питательных веществ ДГК/ЭПК, УМФ, холин, фосфолипиды и витамины B, C и E и селен, было показано у не получавших медикаментозного лечения пациентов с легкой формой болезни Альцгеймера в независимых рандомизированных контролируемых испытаниях (см., например, Scheltens et al., «Efficacy of a medical food in mild Alzheimerʹs disease: A randomized controlled trial» Alzheimerʹs & Dementia 6 (2010), 1-10). Было сделано предположение о связи между воздействием и образованием синапсов на ранней стадии болезни Альцгеймера.
В данной области техники существует потребность в улучшении и/или поддержании синаптической функции, особенно направления функциональной связи головного мозга, и/или потребность в сохранении сетевой организации головного мозга, для лечения неврологических расстройств, в частности расстройств ЦНС, и предпочтительно нейродегенеративных заболеваний, таких как болезнь Альцгеймера, возможно еще на доклинических стадиях заболевания.
Сущность изобретения
Авторы настоящего изобретения обнаружили, что после введения продукта, содержащего (i) одно или несколько из следующих веществ: уридин и цитидин или их соли, фосфаты, ацильные производные или сложные эфиры, и (ii) липидную фракцию, содержащую, по меньшей мере, одну из докозагексаеновой кислоты (22:6; ДГК), эйкозапентаеновой кислоты (20:5; ЭПК) и докозапентаеновой кислоты (22:5; ДПК), или их сложные эфиры, нарушенная функциональная синаптическая связь в головном мозге субъекта может быть улучшена и/или сохранена, а также сохранена сетевая организация головного мозга, в частности у субъекта, страдающего нейродегенеративным заболеванием или имеющего (высокий или повышенный) риск развития такого заболевания, которое характеризуется нарушенной функциональной связью и/или нарушенной сетевой организацией головного мозга, в частности болезнью Альцгеймера.
В данной области техники функциональная связь отражает корреляции между пространственно удаленными нейрофизиологическими событиями, характеризуя тем самым функциональные взаимодействия в головном мозге. В контексте настоящего изобретения термины «функциональная связь», «функциональная связь головного мозга» и «функциональная синаптическая связь» используются взаимозаменяемо и относятся к понятию статистических взаимозависимостей между сигналами активности головного мозга как предполагаемого показателя функциональных взаимодействий. Это определение взято из работы Stam et al. Hum Brain Map 28 (2007) 1178-93. Как уже изложено в описании уровня техники, существует фундаментальное различие между функциональной связью (временные корреляции между удаленными нейрофизиологическими событиями) и эффективной связью (влияние одной нейронной системы на другую), и функциональная связь также отличается от структурной или анатомической связи, отражающей физические или структурные синаптические соединения. Обзор дан в Friston Human Brain Mapping 2: 56-78 (1994), его содержание включено в настоящее изобретение путем ссылки. В области нейровизуализации функциональная связь является хорошо известным и отдельным понятием.
Понятие «сетевая организация головного мозга» известно в данной области техники. В контексте настоящего изобретения термины «ухудшенная сетевая организация головного мозга», «поврежденная сетевая организация головного мозга», «нарушенная сетевая организация головного мозга» и «дезорганизованная сетевая организация головного мозга» все используются взаимозаменяемо по всему тексту данной заявки и отражают изменения в сетевой организации головного мозга по сравнению с оптимальной сетевой организацией по типу сети «тесного мира». Сетевая организация головного мозга может быть оценена на основе измерений функциональной связи, для которой могут быть построены и проанализированы так называемые графы, обеспечивающие понимание скорее конкретной организации, чем силы связей. Организация по таким графам может быть количественно определена, используя основы теории графов, см., например, van Steen (2010) и Watts (1998), содержание этих работ включено в настоящее изобретение путем ссылки. При том, что существует множество способов оценки сетевой организации головного мозга, общепринятая методика определения параметров сетевой организации головного мозга, также применяемая в клинических испытаниях и описанная в настоящем изобретении, предполагает использование «коэффициента кластеризации C», показывающего взаимосвязанность соседних точек или местную связь, и «длины пути L», которая показывает общую связь, интеграцию или эффективность. Термин «здоровая сетевая организация головного мозга» относится к сети «тесного мира», объединяющей высокую местную связь с короткой длиной пути. Оптимальный здоровый головной мозг имеет индекс сети «тесного мира» [ИСТМ], представленный высоким коэффициентом кластеризации и низким значением длины пути. Более подробно это показано на фиг. 1, обсуждаемой ниже.
Авторы настоящего изобретения впервые установили, что нарушенную функциональную связь и/или нарушенную сетевую организацию головного мозга у субъекта можно с успехом исправлять путем введения вышеописанной композиции, используя электроэнцефалографию (ЭЭГ) для мониторинга изменений функции головного мозга. Полученные результаты более подробно обсуждаются ниже. Владея этой информацией, терапию заболеваний, связанных с нарушенной функциональной связью и/или нарушенной сетевой организацией головного мозга, таких как болезнь Альцгеймера, можно было бы проводить более эффективно.
Список предпочтительных вариантов осуществления изобретения
1. Применение композиции для производства продукта для улучшения или сохранения функциональной связи головного мозга и/или функциональной синаптической активности и/или сетевой организации головного мозга у нуждающегося в этом субъекта, и/или замедления возникновения, предотвращения или восстановления нарушенной функциональной связи головного мозга и/или нарушенной функциональной синаптической активности и/или нарушенной сетевой организации головного мозга у нуждающегося в этом субъекта, где указанная композиция содержит:
i) одно или несколько из следующих веществ: уридин и цитидин или их соли, фосфаты, ацильные производные или сложные эфиры; и
ii) липидную фракцию, содержащую, по меньшей мере, одну из докозагексаеновой кислоты (22:6; ДГК), эйкозапентаеновой кислоты (20:5; ЭПК) и докозапентаеновой кислоты (22:5; ДПК), или их сложные эфиры.
2. Применение композиции для производства продукта для лечения нуждающегося в этом субъекта, где указанная композиция содержит:
i) одно или несколько из следующих веществ: уридин и цитидин или их соли, фосфаты, ацильные производные или сложные эфиры; и
ii) липидную фракцию, содержащую, по меньшей мере, одну из докозагексаеновой кислоты (22:6; ДГК), эйкозапентаеновой кислоты (20:5; ЭПК) и докозапентаеновой кислоты (22:5; ДПК), или их сложные эфиры,
и где указанный субъект подвергается процедуре визуализации с целью оценки или мониторинга функциональной связи головного мозга и/или сетевой организации головного мозга.
3. Способ улучшения или сохранения функциональной связи и/или сетевой организации головного мозга у нуждающегося в этом субъекта, где указанный способ включает в себя введение указанному субъекту композиции, содержащей:
i) одно или несколько из следующих веществ: уридин и цитидин или их соли, фосфаты, ацильные производные или сложные эфиры; и
ii) липидную фракцию, содержащую, по меньшей мере, одну из докозагексаеновой кислоты (22:6; ДГК), эйкозапентаеновой кислоты (20:5; ЭПК) и докозапентаеновой кислоты (22:5; ДПК), или их сложные эфиры,
и где указанный субъект при необходимости подвергается процедуре визуализации с целью оценки или мониторинга функциональной связи головного мозга и/или сетевой организации головного мозга.
4. Применение или способ в соответствии с вариантами осуществления изобретения 2 или 3, где указанная процедура визуализации включает в себя электроэнцефалографию (ЭЭГ), функциональную магнитно-резонансную томографию (фМРТ) и/или магнитоэнцефалографию (МЭГ).
5. Применение или способ в соответствии с любым из предшествующих вариантов осуществления изобретения, где указанный субъект страдает неврологическим расстройством, в частности нейрокогнитивным расстройством, нарушением, связанным с развитием нервной системы, или депрессивным расстройством, более предпочтительно, нейрокогнитивное расстройство выбрано из группы, состоящей из болезни Альцгеймера, умеренного когнитивного нарушения (УКН), болезни Паркинсона и болезни Хантингтона, или нарушение, связанное с развитием нервной системы, выбрано из группы, состоящей из синдрома дефицита внимания с гиперактивностью и расстройства аутистического спектра, или депрессивное расстройство выбрано из группы, состоящей из депрессии и хронического депрессивного расстройства.
6. Применение или способ в соответствии с вариантом осуществления изобретения 5, где указанный субъект страдает нарушением памяти или когнитивным расстройством, ухудшением памяти или когнитивной дисфункцией, такими как возрастное нарушение памяти (ВНП), болезнь Альцгеймера, рассеянный склероз, сосудистая деменция, лобно-височная деменция, семантическая деменция или деменция с тельцами Леви, или имеет риск развития этих заболеваний.
7. Применение или способ в соответствии с вариантом осуществления изобретения 5, где указанный субъект страдает болезнью Альцгеймера, деменциями, УКН, нарушениями памяти, болезнью Паркинсона, обсессивно-компульсивным расстройством, синдромом Туретта, депрессией, шизофренией, расстройствами аутистического спектра (РАС), посттравматическим стрессовым расстройством (ПТСР), травматическим повреждением головного мозга, ФКУ, алкоголизмом, синдромом Дауна, эпилепсией, БАС, ВИЧ, биполярным расстройством, рассеянным склерозом, болезнью Хантингтона, синдромом дефицита внимания с гиперактивностью и аутизмом (синдромом Аспергера), или имеет риск развития этих заболеваний.
8. Применение или способ в соответствии с любым из предшествующих вариантов осуществления изобретения, где указанный субъект страдает болезнью Альцгеймера или синдромом деменции, включая легкую или продромальную форму болезни Альцгеймера или деменции, или имеет риск развития этих заболеваний.
9. Способ в соответствии с вариантом осуществления изобретения 8, где указанное нейродегенеративное заболевание представляет собой болезнь Альцгеймера или синдром деменции.
10. Применение или способ в соответствии с любым из предшествующих вариантов осуществления изобретения, где указанная композиция содержит холин или его соли или сложные эфиры, предпочтительно 200-600 мг холина на суточную дозу или на 100 мл композиции.
11. Применение или способ в соответствии с любым из предшествующих вариантов осуществления изобретения, где указанная композиция содержит, по меньшей мере, один, предпочтительно, по меньшей мере, два, наиболее предпочтительно, все витамины B, выбранные из группы, состоящей из витамина B6, витамина B12 и витамина B9.
12. Применение или способ в соответствии с любым из предшествующих вариантов осуществления изобретения, где указанная композиция содержит на суточную дозу или, предпочтительно, на 100 мл композиции, по меньшей мере, 500 мг ДГК, предпочтительно, по меньшей мере, 600 мг ДГК и, по меньшей мере, 50 мг уридина, предпочтительно, по меньшей мере, 100 мг уридина.
13. Применение или способ в соответствии с любым из предшествующих вариантов осуществления изобретения, где данная композиция содержит на суточную дозу или, предпочтительно, на 100 мл композиции:
50-1000 мг фосфолипидов,
0,5-3 мг витамина B6,
50-500 мкг фолиевой кислоты,
1-30 мкг витамина B12.
14. Применение или способ в соответствии с любым из предшествующих вариантов осуществления изобретения, где данная композиция содержит на суточную дозу или, предпочтительно, на 100 мл композиции:
100-500 мг, предпочтительно, 200-400 мг ЭПК,
1000-1500 мг, предпочтительно, 1100-1300 мг ДГК,
50-600 мг, предпочтительно, 60-200 мг фосфолипидов,
200-600 мг, предпочтительно, 300-500 мг холина,
400-800 мг, предпочтительно, 500-700 мг УМФ (уридинмонофосфата),
20-60 мг, предпочтительно, 30-50 мг витамина E (альфа-ТЭ),
60-100 мг, предпочтительно, 70-90 мг витамина C,
40-80 мкг, предпочтительно, 50-70 мкг селена,
1-5 мкг, предпочтительно, 2-4 мкг витамина B12,
0,5-3 мг, предпочтительно, 0,5-2 мг витамина B6, и
200-600 мкг, предпочтительно, 300-500 мкг фолиевой кислоты.
15. Применение ЭЭГ, фМРТ и/или МЭГ для мониторинга функциональной синаптической связи и/или синаптической функции и/или сетевой организации головного мозга в интервенционных исследованиях, в которых нуждающемуся в этом субъекту вводят композицию, содержащую:
i) одно или несколько из следующих веществ: уридин и цитидин или их соли, фосфаты, ацильные производные или сложные эфиры; и
ii) липидную фракцию, содержащую, по меньшей мере, одну из докозагексаеновой кислоты (22:6; ДГК), эйкозапентаеновой кислоты (20:5; ЭПК) и докозапентаеновой кислоты (22:5; ДПК), или их сложные эфиры.
16. Композиция, применяемая для улучшения или сохранения функциональной связи головного мозга и/или сетевой организации головного мозга у нуждающегося в этом субъекта, где указанная композиция содержит:
i) одно или несколько из следующих веществ: уридин и цитидин или их соли, фосфаты, ацильные производные или сложные эфиры; и
ii) липидную фракцию, содержащую, по меньшей мере, одну из докозагексаеновой кислоты (22:6; ДГК), эйкозапентаеновой кислоты (20:5; ЭПК) и докозапентаеновой кислоты (22:5; ДПК), или их сложные эфиры.
17. Композиция в соответствии с вариантом осуществления изобретения 16, где указанный субъект подвергается процедуре визуализации с целью оценки или мониторинга функциональной связи головного мозга и/или сетевой организации головного мозга.
Список фигур
Фиг. 1 представляет собой схематическое изображение сетевой модели, основанной на коэффициенте кластеризации C и длине пути L. Слева: упорядоченная модель с высоким C и высокой L, в центре: модель «тесного мира» с высоким C и низкой L; справа: стохастическая модель с низким C и низкой L. Источник: Watts and Strogatz, Nature (1998).
На фиг. 2 показаны различные стадии когнитивного ухудшения при болезни Альцгеймера. Источник: Sperling et al. Toward defining the preclinical stages of Alzheimerʹs disease: recommendations from the National Institute on Aging and the Alzheimerʹs Association workgroup. Alzheimers Dement (2011).
На фиг. 3 показаны пиковая частота (фиг. 3A) и ИСФ (фиг. 3B) в 24-недельном интервенционном исследовании с использованием композиции (треугольники; «эксперимент») настоящего изобретения. Было показано, что пиковая частота (показатель активности головного мозга) замедлялась в контрольной группе и оставалась относительно стабильной в экспериментальной группе (p=0,019). Кроме того, анализ функциональной связи (ИСФ) выявил значимое влияние приема композиции в экспериментальной группе через 24 недели (p=0,011). Этот параметр соответствует функциональной связи головного мозга в соответствии с настоящим изобретением.
На фиг. 4 показаны средний нормализованный коэффициент кластеризации (фиг. 4a) и средняя нормализованная длина пути (фиг. 4b) в бета-диапазоне в 24-недельном интервенционном исследовании. Было показано, что оба сетевых параметра оставались стабильными в экспериментальной группе и снижались в контрольной группе, при этом различия между группами были статистически значимыми (p=0,009 и p=0,053 для нормализованного коэффициента кластеризации и нормализованной длины пути, соответственно). Пояснение: C = коэффициент кластеризации, гамма = нормализованный коэффициент кластеризации; L = длина пути, лямбда = нормализованная длина пути.
Подробное описание изобретения
В одном аспекте настоящее изобретение относится к применению композиции (для производства продукта) для применения для:
- улучшения или сохранения функциональной связи головного мозга и/или функциональной синаптической активности у нуждающегося в этом субъекта, и/или
- замедления возникновения, предотвращения или восстановления нарушенной функциональной связи головного мозга и/или нарушенной функциональной синаптической активности; и/или
- сохранения и/или улучшения сетевой организации головного мозга у нуждающегося в этом субъекта; и/или
- замедления возникновения или предотвращения ухудшения сетевой организации головного мозга, где указанная композиция содержит:
i) одно или несколько из следующих веществ: уридин и цитидин или их соли, фосфаты, ацильные производные или сложные эфиры; и
ii) липидную фракцию, содержащую, по меньшей мере, одну из докозагексаеновой кислоты (22:6; ДГК), эйкозапентаеновой кислоты (20:5; ЭПК) и докозапентаеновой кислоты (22:5; ДПК), или их сложные эфиры.
В частности, настоящее изобретение относится к применению композиции (для производства продукта) для применения для улучшения или сохранения функциональной (синаптической) связи и/или сохранения сетевой организации головного мозга, где указанная композиция содержит:
i) одно или несколько из следующих веществ: уридин и цитидин или их соли, фосфаты, ацильные производные или сложные эфиры; и
ii) липидную фракцию, содержащую, по меньшей мере, одну из докозагексаеновой кислоты (22:6; ДГК), эйкозапентаеновой кислоты (20:5; ЭПК) и докозапентаеновой кислоты (22:5; ДПК), или их сложные эфиры.
В предпочтительном варианте осуществления изобретения композиция дополнительно содержит iii) холин или его соли или сложные эфиры.
Вклад авторов настоящего изобретения основан на интервенционном исследовании с использованием ЭЭГ для мониторинга функциональной связи головного мозга и сетей функциональной связи (при помощи анализа данных ЭЭГ на основе теории графов). Замечено, что ЭЭГ является одним из биомаркеров, пригодных для мониторинга функциональной связи головного мозга и функциональных сетей головного мозга при нейродегенеративной патологии. Другими подходящими методами непосредственной визуализации, доступными для измерения или функции мозга или ее производных (таких как кровообращение или метаболизм), являются магнитоэнцефалография (МЭГ), функциональная магнитно-резонансная томография (фМРТ), фтордезоксиглюкоза-позитронно-эмиссионная томография (ФДГ-ПЭТ), спектроскопия в ближней инфракрасной области (БИК-спектроскопия), однофотонная эмиссионная компьютерная томография (ОФЭКТ), мечение артериальных спинов (МАС). Это неполный список потенциальных методов мониторинга функциональной связи головного мозга, из которых все могут использоваться в контексте настоящего изобретения.
Функциональная МРТ (фМРТ) позволяет визуализировать регионарный мозговой кровоток и насыщенность крови кислородом, включая области повышенной или пониженной нейронной активности Sorg et al. Curr. Alzheimer Res. 6 (2009) 541-553. При ФДГ-ПЭТ визуализация уровня метаболизма глюкозы в головном мозге происходит благодаря тому, что потребность в глюкозе регулируется синаптическими окончаниями, которые вырабатывают АТФ, необходимую для синтеза, высвобождения и рециркуляции молекул нейромедиаторов, поддержания нормального потенциал покоя и восстановления от потенциалов действия. Уровень церебрального метаболизма глюкозы, измеряемый при помощи ФДГ-ПЭТ, иногда называемый «метаболическая связь» является непосредственным показателем синаптической функции (см., например, Mosconi. et al. Ann. N.Y. Acad. Sci 1147 (2008) 180-195). Содержание всех источников, цитируемых в этом параграфе, включено в настоящее изобретение путем ссылки.
В настоящем изобретении ЭЭГ и МЭГ являются наиболее предпочтительными для оценки функциональной связи и сетей функциональной связи, так как обе они непосредственно измеряют нейронную активность. МЭГ является методикой, позволяющей картировать активность в головном мозге при помощи анализа локализованных колебаний в магнитном поле, порождаемом нейронными токами. Наряду с МЭГ, ЭЭГ регистрирует электрическую активность на волосистой части кожи головы в качестве показателя функциональной связи. Также как МЭГ, ЭЭГ может применяться для выявления прогрессирования нейродегенеративных заболевании, таких как болезнь Альцгеймера, на основе такого признака, как «замедление» рисунка ЭЭГ (МЭГ), и косвенно представляет ценную информацию о синаптической функции и связи. ЭЭГ-электроды могут рассматриваться как узлы сети головного мозга с силой синхронизации или вероятностью между узлами как связи между точками. Это основано на том представлении, что области головного мозга, которые соединены между собой, будут синхронизировать свою активность.
Связь между ЭЭГ и МЭГ с сетями головного мозга у пациентов с болезнью Альцгеймера по сравнению со здоровыми индивидуумами объясняется в работах Stam (2009) и Stam (2010), содержание которых включено в настоящее изобретение путем ссылки. Было отмечено, что у пациентов с болезнью Альцгеймера, помимо прочего, наблюдалось увеличение медленных частотных диапазонов (дельта, тета) и уменьшение быстрых частотных диапазонов (альфа, бета); и замедление пиковой частоты, по сравнению с нормальной контрольной группой. Все эти параметры отражают лежащую в их основе активность/колебания активности головного мозга.
Сетевую организацию головного мозга, как правило, изучают при помощи ЭЭГ, МЭГ и фМРТ. В настоящем изобретении была использована ЭЭГ, но аналогичные результаты также могли быть получены при помощи МЭГ или фМРТ, последний метод имеет преимущество, так как обладает более высоким пространственным разрешением. Величину синхронизации ЭЭГ-сигналов из разных участков головного мозга можно определить путем измерения синхронизации. На основе парных значений синхронизации сети могут быть количественно выражены при помощи сетевого анализа. Сложные сети головного мозга описываются теорией графов (см. Stam (2009)), например, на основе коэффициента кластеризации C, и характеристической длины пути L. Коэффициент кластеризации является мерой местной «взаимосвязанности» графа, в то время как считается, что длина пути является показателем его общей связанности. Согласно Watts (1998), графы с большим количеством местных связей и небольшим количеством случайных удаленных связей характеризуются высоким коэффициентом кластеризации и короткой длиной пути; такие близкие к оптимальной сети обозначаются как сети «тесного мира» с индексом сети «тесного мира» (ИСТМ). Архитектура, подобная сети «тесного мира», может быть оптимальной для синхронизации нейронной активности между разными участками головного мозга. В то время как здоровые субъекты имеют сети головного мозга с топологией сети «тесного мира», характеризующейся комбинацией высокой кластеризации и короткой длины пути, пациенты, страдающие нарушенной функциональной связью головного мозга, имеют более случайные сети головного мозга, что обусловлено потерей критических линий связи. Эти пациенты демонстрируют потерю оптимальной организации головного мозга, что, как считается, указывает на потерю синаптических связей и нарушенную связь между нейронами.
В настоящем интервенционном исследовании, лежащем в основе настоящего изобретения, ЭЭГ показала, что пиковая частота в группе пациентов с болезнью Альцгеймера, имеющих 20 или более баллов по КШОПС, стабилизировалась после введения композиции настоящего изобретения в течение первого периода продолжительностью 12 недель и даже повысилась в последующие 12 недель 24-недельного исследования, при этом та же пиковая частота в контрольной группе продолжала снижаться на всем протяжении исследования. Детали приводятся ниже в подробном описании изобретения и в разделе Примеры.
В другом аспекте настоящее изобретение относится к применению композиции, содержащей (i)-(ii) и, в некоторых случаях, (iii), как указано выше, в производстве продукта для лечения нуждающегося в этом субъекта, и применению к указанному субъекту метода визуализации с целью оценки функциональной связи, предпочтительно, одного или нескольких методов визуализации, выбранных из списка, состоящего из электроэнцефалографии (ЭЭГ), магнитоэнцефалографии (МЭГ), функциональной магнитно-резонансной томографии (фМРТ), фтордезоксиглюкоза-позитронно-эмиссионной томографии (ФДГ-ПЭТ), спектроскопии в ближней инфракрасной области (БИК-спектроскопия), однофотонной эмиссионной компьютерной томографии (ОФЭКТ), мечения артериальных спинов (МАС), предпочтительно, ЭЭГ и/или МЭГ. Предпочтительно, у субъекта проводится оценка функциональной синаптической связи, синаптической активности, синаптической функции и/или синхронной активности синапсов, всех параметров, которые связаны с функциональной связью головного мозга больше чем с анатомической или эффективной связью. В предпочтительном варианте осуществления изобретения метод визуализации выбран из ЭЭГ, МЭГ и фМРТ. Композицию предпочтительно вводят указанному субъекту, по меньшей мере, ежедневно, предпочтительно, в течение, по меньшей мере, 12 недель. Для оценки результатов измерения функциональной связи, полученных при помощи метода визуализации, предпочтительно использовать анализ на основе теории графов, что дает информацию об организации и сетях функциональной связи. Например, могут быть вычислены коэффициент кластеризации C и характеристическая длина пути L. На следующем этапе на основе этих параметров может быть вычислен ИСТМ.
Способ предпочтительно включает в себя мониторинг указанного субъекта при помощи ЭЭГ. В одном аспекте ЭЭГ включает в себя, по меньшей мере, мониторинг изменений индекса сдвига фаз (ИСФ). Передовые методы анализа сигналов ЭЭГ и МЭГ, такие как количественный частотный анализ и анализ функциональной связи, показывают увеличение относительной силы активности в более низких частотных диапазонах (дельта и тета диапазоны), уменьшение относительной силы в более высоких частотных диапазонах (альфа- и бета-диапазоны), замедление пиковой частоты и пониженную функциональную связь между участками мозга у пациентов с болезнью Альцгеймера по сравнению с контролями. Индекс сдвига фаз (ИСФ) в этих частотных диапазонах является хорошим показателем синхронизации функциональной связи головного мозга. Другим показателем является вероятность синхронизации. ИСФ и вероятность синхронизации могут использоваться совместно или независимо для мониторинга прогрессирования болезни Альцгеймера или деменции, в частности функциональной связи. Более подробное описание дается в работах Brenner et al. (1998) и De Haan et al. (2008, 2009), содержание которых считается включенным в настоящее изобретение путем ссылки.
В одном аспекте настоящее изобретение относится к способу мониторинга действия композиции для лечения субъекта с нарушенной или ухудшенной функциональной связью, указанный субъект предпочтительно страдает болезнью Альцгеймера или имеет риск развития этого заболевания, где указанный способ включает в себя измерение или отслеживание индекса сдвига фаз (ИСФ).
В одном аспекте настоящее изобретение относится к способу мониторинга действия композиции для лечения субъекта с нарушенной или ухудшенной сетевой организацией головного мозга, указанный субъект предпочтительно страдает болезнью Альцгеймера или имеет риск развития этого заболевания, где указанный способ включает в себя определение коэффициента кластеризации C, и характеристической длины пути L и, в некоторых случаях, вычисление ИСТМ на основе этих параметров. Подходящим инструментом для получения этих параметров является анализ, основанный на теории графов. Измерения могут быть выполнены при помощи ЭЭГ, МЭГ или фМРТ.
В одном аспекте настоящее изобретение относится к способу мониторинга действия композиции для лечения субъекта, страдающего нейродегенеративным заболеванием и/или нарушенной или ухудшенной функциональной связью и/или нарушенной сетевой организацией головного мозга, или имеющего риск развития таких нарушений, указанный субъект предпочтительно страдает болезнью Альцгеймера или имеет риск развития этого заболевания, где указанный способ включает в себя измерение или отслеживание (изменений или сдвигов) индекса сдвига фаз (ИСФ). В одном аспекте настоящее изобретение относится к способу мониторинга действия композиции, предпочтительно, композиции, содержащей вышеуказанные ингредиенты, и как далее описано ниже, для лечения пожилого субъекта или субъекта, страдающего нейродегенеративным или неврологическим расстройством, предпочтительно расстройством ЦНС, предпочтительно расстройством, связанным с когнитивным нарушением и/или нарушенной или ухудшенной функциональной связью и/или нарушенной сетевой организацией головного мозга, где указанный способ включает в себя определение коэффициента кластеризации C, и характеристической длины пути L и, в некоторых случаях, ИСТМ.
Способ или применение изобретения включает в себя введение композиции, содержащей вышеуказанные ингредиенты, и как далее описано ниже, нуждающемуся в этом субъекту. Профилактический или превентивный аспект включает в себя уменьшение риска возникновения нарушений.
Лечение предпочтительно включает в себя ежедневное введение продукта, предпочтительно, в течение, по меньшей мере, 12 недель. Продукт предпочтительно вводят (ежедневно) в течение, по меньшей мере, 13 недель, более предпочтительно, по меньшей мере, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, наиболее предпочтительно, по меньшей мере, 24 недель.
Функциональная связь
Термины «функциональная синаптическая связь», «функциональная связь головного мозга» и «функциональная нейронная связь» рассматриваются как взаимозаменяемые, и сокращаются в контексте настоящего изобретения как «функциональная связь». Под термином «улучшение или сохранение функциональной синаптической связи (головного мозга)» следует понимать, что нарушенная функциональная синаптическая активность, нарушенная синхронная активность синапсов и/или нарушенная функциональная связь в областях головного мозга, связанные с различными неврологическими расстройствами, в частности различными расстройствами ЦНС (центральной нервной системы), предпочтительно нейродегенеративными заболеваниями, таким как болезнь Альцгеймера, уменьшаются, замедляются в своем развитии, останавливаются или даже возвращаются в норму.
При том, что синаптическую связь у человека невозможно измерить напрямую, функциональную нейронную связь у человека можно изучать при помощи методов визуализации для оценки функциональной связи, например, при помощи таких методов визуализации, как электроэнцефалография (ЭЭГ), магнитоэнцефалография (МЭГ), функциональная магнитно-резонансная томография (фМРТ), фтордезоксиглюкоза-позитронно-эмиссионная томография (ФДГ-ПЭТ), спектроскопия в ближней инфракрасной области (БИК-спектроскопия), однофотонная эмиссионная компьютерная томография (ОФЭКТ), мечение артериальных спинов (МАС), предпочтительно, электроэнцефалография (ЭЭГ) и/или магнитоэнцефалография (МЭГ). Как объяснялось выше, ЭЭГ/МЭГ сигнал является результатом активности многих синапсов, и поэтому он является производным лежащей в их основе синаптической функции. Аналогичным образом, также может использоваться фМРТ.
Сетевая организация головного мозга
Функциональная сетевая организация головного мозга может быть построена по результатам измерений функциональной связи. Эти сети могут быть оценены с точки зрения организации с использованием теории графов, давая информацию о конкретной организации связей. В результате это позволяет оценить степень местной связи и общей интеграции сети. На основе этих сетей при помощи теории графов могут быть вычислены некоторые количественные показатели, характеризующие сети, такие как коэффициент кластеризации и длина пути. Измерение значения коэффициента кластеризации C позволяет оценить взаимосвязанность соседних точек (местная связь), и оно является высоким в случае упорядоченной сети (фиг. 1, слева), и низким в случае стохастической сети (фиг. 1, справа). Значение длины пути L является показателем легкости перемещения по сети (общая связь, интеграция или эффективность). Графы представляют собой данные о структурах, которые имеют узлы и ребра между этими узлами. Коэффициент кластеризации каждого узла вычисляется как соотношение между числом связей между его соседними узлами и максимально возможным числом связей между его соседними узлами. Коэффициент кластеризации (C) сети вычисляется как среднее значение коэффициентов кластеризации всех узлов в этой сети. Средняя минимальная длина пути узла вычисляется как среднее значение минимальных расстояний от этого узла до всех остальных узлов сети. Характеристическая длина пути (L) сети представляет собой среднее значение средних минимальных длин пути всех узлов сети. Коэффициент кластеризации и длина пути полностью несвязанных с сетью узлов имеют значения 0 и «бесконечность», соответственно, и эти узлы, таким образом, исключаются из расчета C и L.
Для того чтобы оценить обладает ли сеть свойствами сети «тесного мира», т.е. определить ИСТМ, коэффициент кластеризации и характеристическая длина пути сети могут быть нормализованы с учетом их полученных соответствующих значений, усредненных по 1000 стохастических сетей с тем же количеством узлов и распределением узлов по числу связей.
В упорядоченной сети, для того чтобы достичь другой стороны сети необходимо сделать много шагов (высокое значение длины пути, фиг. 1, слева), в то время как в стохастической сети для этого необходимо сделать только несколько шагов (низкое значение длины пути, фиг. 1, справа). Сеть «тесного мира» занимает промежуточное положение между упорядоченной и стохастической сетью, объединяя высокую местную связь с короткой длиной пути (фиг. 1, в центре).
На развитых стадиях нейродегенерации она может проявляться через ухудшение способностей к обучению, функции памяти и/или познавательной способности. Однако, как указывалось выше, потеря функциональной связи головного мозга и ухудшение сетевой организации головного мозга могут возникать задолго до наступления этих клинических стадий, и теперь с этим можно бороться с применением композиции настоящего изобретения. Сохранение и улучшение измеряются относительно контрольной группы субъектов, страдающих тем же заболеванием, но не получающих композицию настоящего изобретения.
Субъект
В частности, субъектом является человек, который имеет пониженную/нарушенную/ухудшенную функциональную связь, в частности страдает неврологическим расстройством, более предпочтительно, расстройством ЦНС, или имеет риск развития таких расстройств и состояний. Более конкретно, эти расстройства являются нейрокогнитивными расстройствами, нарушениями, связанными с развитием нервной системы, и депрессивными расстройствами, и более предпочтительно, они являются нейрокогнитивными расстройствами. Предпочтительные нейрокогнитивные расстройства представляют собой дегенеративные нейрокогнитивные расстройства, недегенеративные нейрокогнитивные расстройства и нейрокогнитивные расстройства, связанные с сосудистой патологией, более предпочтительно, дегенеративные нейрокогнитивные расстройства. Следующая классификация, используемая в данной области техники, представители расстройств, связанных с нарушенной функциональной связью головного мозга и ухудшенной сетевой организацией головного мозга, приведены в Таблице 1. Заявленная комбинация предпочтительно применяется для лечения и/или предотвращения (включая уменьшение риска возникновения) любой из категорий расстройств, подкатегорий расстройств и, предпочтительно, расстройств, перечисленных в Таблице 1.
Предпочтительными дегенеративными нейрокогнитивными расстройствами являются болезнь Альцгеймера (Bozzali et al, 2011; Stam, 2010), умеренное когнитивное нарушение (УКН) (Han, 2011 #8924), болезнь Паркинсона (Stam, 2010) и болезнь Хантингтона (Wolf et al, 2008), более предпочтительно, болезнь Альцгеймера и умеренное когнитивное нарушение. Предпочтительными нарушениями, связанными с развитием нервной системы, являются синдром дефицита внимания с гиперактивностью (Cubillo and Rubia, 2010; Konrad and Eickhoff, 2010) и расстройство аутистического спектра (Gepner and Feron, 2009), более предпочтительно, синдром дефицита внимания с гиперактивностью. Предпочтительными депрессивными расстройствами являются депрессия (Cao et al., 2012) и хроническое депрессивное расстройство, более предпочтительно, депрессия. Источники, цитируемые в этом параграфе, указаны ниже. Содержание этих источников включено в настоящее изобретение путем ссылки.
Более конкретно, субъекты имеют риск возникновения или страдают расстройствами, выбранными из нейрокогнитивных расстройств, нарушений, связанных с развитием нервной системы, и депрессивных расстройств, и более предпочтительно, нейрокогнитивных расстройств. Предпочтительно, субъект имеет риск возникновения или страдает дегенеративными нейрокогнитивными расстройствами, недегенеративными нейрокогнитивными расстройствами и нейрокогнитивными расстройствам, связанными с сосудистой патологией, более предпочтительно, дегенеративными нейрокогнитивными расстройствами.
Более конкретно, субъектом является человек, который имеет риск возникновения или страдает нарушением памяти или когнитивным расстройством, ухудшением памяти или когнитивной дисфункцией, такими как возрастное нарушение памяти (ВНП), рассеянный склероз, сосудистая деменция, лобно-височная деменция, семантическая деменция или деменция с тельцами Леви и болезнь Альцгеймера, и/или психическими расстройствами или нарушениями развития, включая обсессивно-компульсивное расстройство, синдром Туретта, депрессия, шизофрения, синдром дефицита внимания с гиперактивностью и аутизм (синдромом Аспергера). При вышеуказанных состояниях известно, что память и когнитивные функции ухудшаются со временем. Возможно, что субъект еще не страдает какими-либо клиническими стадиями, связанными с нарушением функциональной связи и/или ухудшением сетевой организации головного мозга.
В частности, субъектом может быть человек, у которого еще не выявлено (конкретное) заболевание (такое как нейродегенеративное заболевание, например, болезнь Альцгеймера), но который имеет нарушенную функциональную связь и/или нарушенную сетевую организацию головного мозга, что определено и/или измерено любым методом (визуализации), пригодным для оценки функциональной связи и сетевой организации головного мозга.
В предпочтительном варианте осуществления изобретения субъектом является человек, который имеет риск возникновения или имеет пониженную/нарушенную/ухудшенную функциональную связь и/или ослабленную/нарушенную/ухудшенную сетевую организацию головного мозга, в частности страдает болезнью Альцгеймера, деменциями, УКН, нарушениями памяти, болезнью Паркинсона, обсессивно-компульсивным расстройством, синдромом Туретта, депрессией, шизофренией, расстройствами аутистического спектра (РАС), посттравматическим стрессовым расстройством (ПТСР), травматическим повреждением головного мозга, ФКУ, алкоголизмом, синдромом Дауна, эпилепсией, БАС, ВИЧ, биполярным расстройством, рассеянным склерозом, болезнью Хантингтона, синдромом дефицита внимания с гиперактивностью и аутизмом (синдромом Аспергера), более предпочтительно, страдает болезнью Альцгеймера, деменциями, УКН, нарушениями памяти или болезнью Паркинсона. Возможно, что субъект еще не страдает какими-либо клиническими стадиями, связанными с нарушением функциональной связи и/или нарушением сетевой организации головного мозга.
В предпочтительном варианте осуществления изобретения субъектом является человек, который имеет риск возникновения или имеет пониженную/нарушенную/ухудшенную функциональную связь и/или ослабленную/нарушенную/ухудшенную сетевую организацию головного мозга, предпочтительно страдает нарушением памяти или когнитивным расстройством, ухудшением памяти или когнитивной дисфункцией. Данный субъект предпочтительно страдает когнитивной дисфункцией, связанной с болезнью Альцгеймера, болезнью Пика (или лобным вариантом лобно-височной деменции), болезнью телец Леви, болезнью Хантингтона или «синдромом деменции». Синдром деменции включает в себя сосудистую деменцию, лобно-височную деменцию и семантическую деменцию. Возможно, что субъект еще не страдает какими-либо клиническими стадиями, связанными с нарушением функциональной связи и/или нарушением сетевой организации головного мозга.
Субъектом предпочтительно является человек, предпочтительно, пожилой человек, предпочтительно, в возрасте, по меньшей мере, 50 лет. Субъектом предпочтительно является пациент с болезнью Альцгеймера или деменцией. В одном аспекте настоящее изобретение относится к лечению людей, страдающих болезнью Альцгеймера, деменцией и/или, являющихся пожилыми.
В одном варианте осуществления изобретения субъектом предпочтительно является субъект, не получавший медикаментозного лечения, предпочтительно, это субъект не принимал никакого лекарственного препарата для улучшения памяти и/или для лечения болезни Альцгеймера или деменции, по меньшей мере, за 4 недели до введения композиции настоящего изобретения. Предпочтительно, используемый в настоящем изобретении термин «не получавший медикаментозного лечения» относится к субъектам, которые не принимали один или несколько из следующих лекарственных препаратов: ингибиторы холинэстеразы, антагонисты N-метил-D-аспартата (NMDA) и гинко билоба, во время лечения композицией настоящего изобретения, и, предпочтительно, не принимали никаких влияющих на когнитивную способность лекарственных препаратов, по меньшей мере, за 4 недели до этого лечения.
В одном аспекте субъектом является пациент, страдающий умеренным когнитивным нарушением (УКН) (или «пациент с легкой формой болезни Альцгеймера» или «пациент с легкой формой деменции») или пациент с ВНП. Группа пациентов также может включать в себя пациентов с продромальным периодом неврологических расстройств, в частности пациентов с продромальной болезнью Альцгеймера или не получавших медикаментозного лечения пациентов с продромальной деменцией. Пациентом с продромальной деменцией является человек, который не страдает сенильной деменцией, как описано выше, но имеет повышенную вероятность развития сенильной деменции. Аналогично, Пациентом с продромальной болезнью Альцгеймера является человек, который не страдает болезнью Альцгеймера, но имеет повышенную вероятность развития болезни Альцгеймера. Диагностические инструменты, которые применяются для отнесения пациентов к продромальным пациентам, являются доступными из уровня техники, и описаны, например, в международной заявке WO2009/002164, содержание которой включено в настоящее изобретение путем ссылки.
В еще одном способе диагностики пациент может быть выявлен, если он имеет 20-30 баллов по Краткой шкале оценки психического статуса (КШОПС). КШОПС представляет собой стандартизированный тест, разработанный в данной области техники для дифференциального определения различных стадий (предварительных стадий) деменции. Он включает в себя краткую анкету, состоящую из 30 вопросов, которую используют для оценки когнитивной деятельности. В течение примерно 10 минут с его помощью оценивают различные функции, включая память и ориентировку. Тест КШОПС включает в себя простые вопросы и задачи из нескольких областей: время и место теста, повторение списка слов, использование и понимание речи и основные двигательные навыки. Количество баллов 27 или выше (из 30) интерпретируется как практически нормальное; 20-26 свидетельствуют о легкой форме деменции; 10-19 - деменции средней тяжести; и ниже 10 - тяжелой деменции. Авторское право не позволяет авторам настоящего изобретения включить копию этой анкеты в описание изобретения, но ее легко найти в Интернете, а также она доступна через правообладателя Psychological Assessment Resources (PAR). Впервые она была предложена Folstein et al. (Psych Res 12: 189, 1975), и с небольшими изменениями широко используется для оценки когнитивной деятельности. Предпочтительно, в настоящем изобретении субъекты имеют 20-30 баллов по Краткой шкале оценки психического статуса (КШОПС), более предпочтительно, 20-26 баллов, еще более предпочтительно, 24, 25 или 26 баллов по КШОПС. Более предпочтительно, субъект, имеющий количество баллов по КШОПС, находящееся в вышеуказанном диапазоне, имеет или страдает болезнью Альцгеймера, умеренным когнитивным нарушением (УКН), возрастным нарушением памяти (ВНП), рассеянным склерозом, сосудистой деменцией, лобно-височной деменцией, семантической деменцией или деменцией с тельцами Леви.
Наиболее предпочтительно, субъекты, которые подлежат лечению в соответствии с настоящим изобретением, страдают легкой формой болезни Альцгеймера, характеризующейся 20-26 баллами по КШОПС, предпочтительно, 24-26 баллами. В одном варианте осуществления изобретения субъект является субъектом, не получавшим медикаментозного лечения.
Благодаря данным, полученным авторами настоящего изобретения, становится возможным направленно воздействовать на функциональную связь головного мозга и сетевую организацию головного мозга, как основную причину клинических стадий, таких как когнитивное ухудшение и ухудшение памяти. Эти паталогические биомаркеры предшествуют функциональным нарушениям, связанным с вышеуказанными нейродегенеративными состояниями. Таким образом, композиция настоящего изобретения является особенно пригодной для лечения нейродегенеративных заболеваний, как описано выше, в частности расстройств ЦНС, более предпочтительно, расстройств ЦНС, связанных с пониженной/нарушенной/ухудшенной функциональной связью и/или ослабленной/нарушенной/ухудшенной сетевой организацией головного мозга, на ранних стадиях, при дебюте, в особенности на тех стадиях, на которых ухудшение когнитивных способностей еще является незначительным или не наблюдается. Эти новые данные дают возможность начать лечение уже у людей, которые имеют повышенный риск развития вышеуказанных заболеваний за годы до того, как диагноз заболевания может быть поставлен.
Продукт
По всему тексту данной заявки термины «продукт» и «композиция» используются взаимозаменяемо и означают комбинацию ингредиентов, вводимую нуждающемуся в этом субъекту.
В одном аспекте настоящего изобретения композиция настоящего изобретения может применяться в качестве фармацевтического продукта, содержащего один или несколько фармацевтически приемлемых материалов-носителей.
В другом аспекте настоящего изобретения композиция настоящего изобретения может применяться в качестве продукта питания, например, в качестве пищевой добавки, например, в качестве добавки к обычному рациону питания, в качестве обогащающей добавки к обычному рациону питания, или в качестве полноценного питания.
Фармацевтический продукт, предпочтительно для энтерального применения, может быть твердым или жидким галеновым препаратом. Примерами твердых галеновых препаратов являются таблетки, капсулы (например, твердые или мягкие желатиновые капсулы), пилюли, саше, порошки, гранулы и тому подобное, которые содержат активный ингредиент вместе с обычно применяемыми галеновыми носителями. Любой обычно применяемый материал-носитель может быть использован. Материал-носитель может представлять собой органический или неорганический инертный материал-носитель, пригодный для перорального введения. Подходящие носители включают в себя воду, желатин, гуммиарабик, лактозу, крахмал, стеарат магния, тальк, растительные масла и тому подобное. Кроме того, такие добавки, как вкусоароматические добавки, консерванты, стабилизаторы, эмульгаторы, буферы и тому подобное, могут быть добавлены в соответствии с принятой практикой составления фармацевтических композиций. Хотя отдельные активные ингредиенты допустимо вводить в одной композиции, их также можно вводить в отдельных единицах дозирования.
Таким образом, настоящее изобретение также относится к набору компонентов, содержащему i) одно или несколько из следующих веществ: уридин и цитидин или их соли, фосфаты, ацильные производные или сложные эфиры; и ii) липидную фракцию, содержащую, по меньшей мере, одну из докозагексаеновой кислоты (22:6; ДГК), эйкозапентаеновой кислоты (20:5; ЭПК) и докозапентаеновой кислоты (22:5; ДПК), или их сложные эфиры; для вышеуказанного применения или для применения в вышеуказанном способе. В одном варианте осуществления изобретения он предпочтительно включает в себя iii) холин или его соли или сложные эфиры.
Если композиция представляет собой фармацевтический продукт, то такой продукт может содержать суточную дозу в одной или нескольких единицах дозирования. Единица дозирования может быть в жидкой форме или в твердой форме, где в последнем случае суточная доза может быть представлена одной или несколькими твердыми единицами дозирования, например, содержаться в одной или нескольких капсулах или таблетках.
В другом аспекте настоящего изобретения композиция настоящего изобретения может применяться в продукте питания, содержащем, по меньшей мере, один компонент, выбранный из группы, состоящей из жиров, белков и углеводов. Понятно, что продукт питания отличается от фармацевтического продукта наличием питательных веществ, которые обеспечивают питание субъекта, которому вводится эта композиция, в частности наличием белка, жира, перевариваемых углеводов и пищевой клетчатки. Он также может содержать такие ингредиенты, как минералы, витамины, органические кислоты и вкусоароматические агенты. Хотя термин «нутрицевтический продукт» часто используется в литературе, он означает продукт питания, содержащий фармацевтический компонент, или используемый в фармацевтических целях. Таким образом, питательная композиция настоящего изобретения также может применяться в нутрицевтическом продукте.
Продукт настоящего изобретения представляет собой энтеральную композицию, предназначенную для перорального введения. Он предпочтительно вводится в жидком виде. В одном варианте осуществления изобретения этот продукт содержит липидную фракцию и, по меньшей мере, один из углеводов и белков, где липидная композиция обеспечивает от 20 до 50% энергии пищевого продукта. В одном варианте осуществления изобретения пищевой продукт представляет собой жидкую композицию, содержащую от 0,8 до 1,4 ккал на мл.
Предпочтительно, композиция, содержащая (i) и (ii) дополнительно содержит холин.
Предпочтительно, композиция, содержащая (i) и (ii) дополнительно содержит одно или несколько из следующих веществ: фосфолипиды, витамин E, витамин C, селен, витамин B12, витамин B6 и фолиевая кислота.
Более предпочтительно, композиция содержит ДГК, ЭПК, источник уридина (предпочтительно УМФ), фосфолипиды, холин, витамин E, витамин C, селен, витамин B12, витамин B6 и фолиевую кислоту.
ДГК/ЭПК
Композиция содержит, по меньшей мере, одну ω-3 полиненасыщенную жирную кислоту (ДЦ-ПНЖК; имеющую длину цепи 18 и более атомов углерода), выбранную из группы, состоящей из докозагексаеновой кислоты (22:6; ДГК), эйкозапентаеновой кислоты (20:5; ЭПК) и докозапентаеновой кислоты (22:5 ω-3; ДПК), по меньшей мере, одну из ДГК и ЭПК. Предпочтительно, настоящая композиция содержит, по меньшей мере, ДГК, более предпочтительно, ДГК и ЭПК. ЭПК превращается в ДПК (ω-3), увеличивая последующее превращение ДПК в ДГК в головном мозге. Таким образом, настоящая композиция предпочтительно содержит значительное количество ЭПК, для стимулирования дальнейшего образования ДГК in vivo.
ДГК, ЭПК и/или ДПК предпочтительно находятся в форме триглицеридов, диглицеридов, моноглицеридов, свободных жирных кислот или их солей или сложных эфиров, фосфолипидов, лизофосфолипидов, простых эфиров глицерина, липопротеинов, церамидов, гликолипидов или их комбинаций. Предпочтительно, настоящая композиция содержит, по меньшей мере, ДГК в форме триглицеридов.
Что касается суточной дозы, то настоящий способ предпочтительно предусматривает введение от 400 до 5000 мг ДГК+ЭПК+ДПК (предпочтительно, ДГК+ЭПК) в сутки, более предпочтительно, от 500 до 3000 мг (предпочтительно, ДГК+ЭПК) в сутки, наиболее предпочтительно, от 1000 до 2500 мг (предпочтительно, ДГК+ЭПК) в сутки. ДГК предпочтительно вводится в количестве от 300 до 4000 мг в сутки, более предпочтительно, от 500 до 2500 мг в сутки.
Настоящая композиция предпочтительно содержит 1-40 масс.% ДГК от общего количества жирных кислот, предпочтительно, 3-36 масс.% ДГК от общего количества жирных кислот, более предпочтительно, 10-30 масс.% ДГК от общего количества жирных кислот. Настоящая композиция предпочтительно содержит 0,5-20 масс.% ЭПК от общего количества жирных кислот, предпочтительно, 2-10 масс.% ЭПК от общего количества жирных кислот, более предпочтительно, 5-10 масс.% ЭПК от общего количества жирных кислот. Вышеуказанные количества используются с учетом и для оптимизации нескольких аспектов, включая вкус (например, слишком высокие уровни ДЦ-ПНЖК ухудшают вкус, что приводит к ухудшению соблюдения пациентом рекомендаций по приему продукта).
Настоящая композиция предпочтительно содержит, по меньшей мере, одно масло, выбранное из рыбьего жира, масла водорослей и липидов яйца. Предпочтительно, настоящая композиция содержит рыбий жир, содержащий ДГК и ЭПК.
Массовое отношение ДГК к ЭПК предпочтительно составляет более 1, более предпочтительно, от 2:1 до 10:1, более предпочтительно, от 3:1 до 8:1. Вышеуказанные отношения и количества используются с учетом и для оптимизации нескольких аспектов, включая вкус (слишком высокие уровни ДЦ-ПНЖК ухудшают вкус, что приводит к ухудшению соблюдения пациентом рекомендаций по приему продукта), баланс между ДГК и ее предшественником для обеспечения оптимальной эффективности при сохранении небольшого объема препаратов.
Источниками ДГК, возможными источниками ДГК являются: тунцовый жир, (другие) рыбьи жиры, богатые ДГК алкиловые эфиры, масло водорослей, яичный желток или фосфолипиды, обогащенные n-3 ДЦ-ПНЖК, например, фосфатидилсерин-ДГК.
Настоящая композиция предпочтительно содержит очень небольшое количество арахидоновой кислоты (АК). Предпочтительно, массовое соотношение ДГК/АК в настоящей композиции составляет, по меньшей мере, 5, предпочтительно, по меньшей мере, 10, более предпочтительно, по меньшей мере, 15, предпочтительно, до, например, 30 или даже до 60. Настоящий способ предпочтительно предусматривает введение композиции, содержащей менее 5 масс.% арахидоновой кислоты от общего количества жирных кислот, более предпочтительно, менее 2,5 масс.%, например, менее 0,5 масс.%.
АЛК/ЛК
Предпочтительно, чтобы содержание альфа-линоленовой кислоты [АЛК] в композиции поддерживалось на низком уровне. Концентрация АЛК может предпочтительно поддерживаться на уровне ниже 2,0 масс.%, более предпочтительно, ниже 1,5 масс.%, в частности, ниже 1,0 масс.% от массы всех жирных кислот.
Концентрация линолевой кислоты [ЛК] может поддерживаться на нормальном уровне, т.е. от 20 до 30 масс.%, хотя в одном варианте осуществления изобретения концентрация ЛК также значительно уменьшена до количества < 15 г/100 г жирных кислот или даже менее 10 масс.%. Концентрация ЛК предпочтительно составляет, по меньшей мере, 1 масс.% от жирных кислот.
Массовое соотношение омега-6/омега-3 жирных кислот в настоящем продукте предпочтительно составляет менее 0,5, более предпочтительно, менее 0,2, например, менее 0,05 или 0,01. Соотношение ω-6/ω-3 жирных кислот (C20 и выше) в настоящем продукте предпочтительно составляет менее 0,3, более предпочтительно, менее 0,15, например, менее 0,06 или 0,03.
СЦ-ЖК
В одном варианте осуществления изобретения композиция содержит менее 5 масс.%, предпочтительно, менее 2 масс.% жирных кислот, содержащих менее 14 атомов углерода.
Согласно определению, среднецепочечные жирные кислоты [СЦ-ЖК] представляют собой линейные или разветвленные насыщенные карбоновые кислоты, имеющие шесть (C6:0), семь (C7:0), восемь (C8:0), девять (C9:0) или десять (C10:0) атомов углерода. Количество СЦ-ЖК предпочтительно составляет менее 2 масс.%, более предпочтительно, менее 1,5 масс.%, наиболее предпочтительно, менее 1,0 масс.% от общего количества жирных кислот. В одном варианте осуществления изобретения отношение суммы среднецепочечных жирных кислот C6:0+C7:0+C8:0 к сумме C9:0 и C10:0 составляет менее чем 2:1, более предпочтительно, менее чем 1,8:1, наиболее предпочтительно, менее чем 1,6:1.
Насыщенные и мононенасыщенные жирные кислоты
Настоящая композиция предпочтительно содержит насыщенные и/или мононенасыщенные жирные кислоты. Количество насыщенных жирных кислот предпочтительно составляет 6-60 масс.% от общего количества жирных кислот, предпочтительно, 12-40 масс.%, более предпочтительно, 20-40 масс.%, от общего количества жирных кислот. В частности, количество C14:0 (миристиновая кислота) + C16:0 (пальмитиновая кислота) предпочтительно составляет 5-50 масс.%, предпочтительно, 8-36 масс.%, более предпочтительно, 15-30 масс.% от общего количества жирных кислот. Общее количество мононенасыщенных жирных кислот, таких как олеиновая кислота и пальмитолеиновая кислота, предпочтительно составляет от 5 до 40 масс.%, более предпочтительно, от 15 до 30 масс.%. Было обнаружено, что композиция с этими предпочтительными количествами является очень эффективной.
Уридин, УМФ
Настоящая композиция содержит уридин, цитидин и/или их эквивалент, включая соли, фосфаты, ацильные производные и/или сложные эфиры. Что касается уридина, то композиция предпочтительно содержит, по меньшей мере, один уридин или его эквивалент, выбранный из группы, состоящей из уридина (т.е. рибозилурацила), дезоксиуридина (дезоксирибозилурацила), уридинфосфатов (УМФ, дУМФ, УДФ, УТФ), нуклеотидного основания урацил и ацилированных производных уридина. В одном варианте осуществления изобретения также могут использоваться цитидин, ЦМФ, цитиколин (ЦДФ-холин). Предпочтительно, композиция, вводимая в соответствии с настоящим изобретением, содержит источник уридина, выбранный из группы, состоящей из уридина, дезоксиуридина, уридинфосфатов, урацила и ацилированного уридина, и цитидин, более предпочтительно, выбранный из группы, состоящей из уридина, дезоксиуридина, уридинфосфатов, урацила и ацилированного уридина.
Предпочтительно, настоящая композиция содержит уридинфосфат, выбранный из группы, состоящий из уридинмонофосфата (УМФ), уридиндифосфата (УДФ) и уридинтрифосфата (УТФ); и/или цитидинфосфат (ЦМФ, ЦДФ, ЦТФ, предпочтительно, ЦМФ). Наиболее предпочтительно, настоящая композиция содержит УМФ, так как УМФ наиболее эффективно усваивается организмом. Предпочтительно, по меньшей мере, 50 масс.% уридина в настоящей композиции представлено УМФ, более предпочтительно, по меньшей мере, 75 масс.%, наиболее предпочтительно, по меньшей мере, 95 масс.%. Дозы, которые должны вводиться, даны по УМФ. Количество источников урацила может быть рассчитано по молярному эквиваленту количества УМФ (молекулярная масса 324 Дальтон).
Настоящий способ предпочтительно предусматривает введение уридина (совокупного количества уридина, дезоксиуридина, уридинфосфатов, нуклеотидного основания урацил и ацилированных производных уридина) в количестве 0,08-3 г в сутки, предпочтительно, 0,1-2 г в сутки, более предпочтительно, 0,2-1 г в сутки. Настоящий способ предпочтительно предусматривает введение композиции, содержащей уридин в количестве 0,08-3 г УМФ на 100 мл жидкого продукта, предпочтительно, 0,1-2 г УМФ на 100 мл жидкого продукта, более предпочтительно, 0,2-1 г на 100 мл жидкого продукта. Предпочтительно, вводится 1-37,5 мг УМФ на килограмм массы тела в сутки. Вышеуказанные количества также относятся к любым количествам цитидина, цитидинфосфатов и цитиколина, включаемым в композицию или способ.
Предпочтительно, настоящая композиция содержит уридинфосфат, предпочтительно, уридинмонофосфат (УМФ). УМФ очень эффективно усваивается организмом. Поэтому, включение в настоящую композицию УМФ позволяет обеспечить высокую эффективность при введении субъекту минимальной дозы и/или небольшого объема.
Холин
В предпочтительно варианте осуществления изобретения настоящая композиция содержит холин, холиновую соль и/или холиновый сложный эфир. До конца этого параграфа следует считать, что термин «холин» включает в себя все эти эквиваленты. Холиновая соль предпочтительно выбрана из хлорида холина, битартрата холина или стеарата холина. Холиновый сложный эфир предпочтительно выбран из фосфатидилхолина и лизофосфатидилхолина. Настоящий способ предпочтительно предусматривает введение более 50 мг холина в сутки, предпочтительно, от 80 до 2000 мг холина в сутки, более предпочтительно, от 120 до 1000 мг холина в сутки, наиболее предпочтительно, от 150 до 600 мг холина в сутки. Настоящая композиция предпочтительно содержит от 50 мг до 3000 мг холина на 100 мл жидкой композиции, предпочтительно, от 200 мг до 1000 мг холина на 100 мл. Приведенные выше количества указаны для холина, количества эквивалентов холина или его источников могут быть рассчитаны на основе молярного эквивалента холина.
Фосфолипиды
Предпочтительно, настоящая композиция предпочтительно содержит фосфолипиды, предпочтительно, 0,1-50 масс.% фосфолипидов от массы всех липидов, более предпочтительно, 0,5-20 масс.%, более предпочтительно, от 1 до 10 масс.%, наиболее предпочтительно, от 1 до 5 масс.% от массы всех липидов. Общее количество липидов предпочтительно составляет от 10 до 30 масс.% от сухого вещества, и/или от 2 до 10 г липидов на 100 мл жидкой композиции. Композиция предпочтительно содержит от 0,01 до 1 грамма лецитина на 100 мл, более предпочтительно, от 0,05 до 0,5 грамм лецитина на 100 мл. Было обнаружено, что композиция, содержащая эти предпочтительные количества, является очень эффективной. В одном варианте осуществления изобретения фосфолипиды содержат, по меньшей мере, два фосфолипида, выбранных из группы, состоящей из фосфатидилхолина, фосфатидилэтаноламина, фосфатидилинозитола и фосфатидилсерина, предпочтительно, по меньшей мере, ФХ и ФЭ.
Витамины
Настоящая комбинация предпочтительно содержит, по меньшей мере, витамин группы B. Витамин B выбран из группы, состоящей из витамина B1 (тиамин), витамина В2 (рибофлавин), витамина В3 (ниацин или никотинамид), витамина В5 (пантотеновая кислота), витамина B6 (пиридоксин, пиридоксаль или пиридоксамин или пиридоксина гидрохлорид), витамина B7 (биотин), витамина В9 (фолиевая кислота или фолат) и витамина B12 (различные кобаламины). Эти термины включают в себя функциональные эквиваленты.
Предпочтительно, по меньшей мере, один витамин B выбран из группы, состоящей из витамина B6, витамина B12 и витамина В9. Предпочтительно, настоящая композиция содержит, по меньшей мере, два витамина B, выбранных из группы, состоящей из витамина B6, витамина B12 и витамина В9. В частности, хорошие результаты были получены с комбинацией, содержащей витамин B6, витамин B12 и витамин В9. Снова эти термины включают в себя функциональные эквиваленты.
Витамин B вводят в эффективной дозе, эта доза зависит от вида используемого витамина B. Как правило, подходящая минимальная или максимальная доза может быть выбрана на основе известных диетологических рекомендаций, например, рекомендаций Института медицины (ИМ) Национальной академии наук США или Научного комитета по продуктам питания (научный комитет ЕС), раскрытой здесь информации и, в некоторых случаях, ограниченного количества типовых исследований. Минимальная доза может быть определена, исходя из ожидаемой средней потребности (ОСП), хотя более низкая доза уже может оказаться эффективной. Максимальная доза предпочтительно не превышает уровня максимального переносимого потребления (МП), как рекомендовано ИМ.
При наличии в питательной композиции или лекарственном препарате, витамин B6, как правило, находится в количестве, обеспечивающем суточную дозу в диапазоне от 0,1 до 100 мг, в частности, в диапазоне от 0,5 до 25 мг, более конкретно, в диапазоне от 0,5 до 5 мг. Настоящая композиция предпочтительно содержит от 0,1 до 100 мг витамина B6 на 100 г (жидкого) продукта, более предпочтительно, от 0,5 до 25 мг витамина B6 на 100 г (жидкого) продукта, более предпочтительно, от 0,5 до 5 мг витамина B6 на 100 г (жидкого) продукта.
При наличии в питательной композиции или лекарственном препарате, витамин B12, как правило, находится в количестве, обеспечивающем суточную дозу в диапазоне от 0,5 до 15 мкг, в частности, в диапазоне от 1 до 10 мкг, более конкретно, в диапазоне от 1,5 до 5 мкг. Настоящая композиция предпочтительно содержит 0,5-15 мкг витамина B12 на 100 г (жидкого) продукта, более предпочтительно, от 1 до 10 мкг витамина B12 на 100 г (жидкого) продукта, более предпочтительно, от 1,5 до 5 мкг витамина B12 на 100 г (жидкого) продукта. Термин «витамин B12» включает в себя все кобаламиновые эквиваленты, известные из уровня техники.
По всему тексту данной заявки термины «фолиевая кислота», «фолат» и «B9» используются взаимозаменяемо. При наличии в питательной композиции или лекарственном препарате, витамин B9, как правило, находится в количестве, обеспечивающем суточную дозу в диапазоне от 50 до 1000 мкг, в частности, в диапазоне от 150 до 750 мкг, более конкретно, в диапазоне от 200 до 500 мкг. Настоящая композиция предпочтительно содержит от 50 до 1000 мкг фолиевой кислоты на 100 г (жидкого) продукта, более предпочтительно, от 150 до 750 мкг фолиевой кислоты на 100 г (жидкого) продукта, более предпочтительно, от 200 до 500 мкг фолиевой кислоты на 100 г (жидкого) продукта. Фолаты включают в себя фолиевую кислоту, фолиновую кислоту, метилированные, метенилированные и формилированные формы фолатов, их соли или сложные эфиры, а также их производные с одной или несколькими глутаминовыми кислотами, и все или в восстановленной или окисленной форме.
Витамины C, E
Витамин C или его функциональный эквивалент может присутствовать в количестве, обеспечивающем суточную дозу в диапазоне от 20 до 2000 мг, в частности, в диапазоне от 30 до 500 мг, более конкретно, в диапазоне от 75 до 150 мг. В одном варианте осуществления изобретения витамин C или его функциональный эквивалент присутствует в количестве в диапазоне от 20 до 2000 мг, в частности, в диапазоне от 30 до 500 мг, более конкретно, в диапазоне от 75 до 150 мг на 100 мл композиции.
Токоферол и/или его эквивалент (т.е. химическое соединение, обладающее активностью витамина E) может присутствовать в количестве, обеспечивающем суточную дозу в диапазоне от 10 до 300 мг, в частности, в диапазоне от 30 до 200 мг, более конкретно, в диапазоне от 35 до 100 мг, для предотвращения окислительного повреждения, возникающего из-за ПНЖК пищи. В одном варианте осуществления изобретения токоферол и/или его эквивалент присутствует в количестве в диапазоне от 10 до 300 мг, в частности, в диапазоне от 30 до 200 мг, более конкретно, в диапазоне от 35 до 100 мг на 100 мл композиции. Термин «токоферол и/или его эквивалент» и «альфа-ТЭ», используемый в настоящем описании, включает в себя токоферолы, токотриенолы, их фармацевтически и диетологически приемлемые производные, а также любую их комбинацию. Приведенные выше количества указаны для эквивалентов токоферола, признанных в данной области техники.
Селен
Настоящая композиция предпочтительно содержит селен, так как он обладает антиоксидантной активностью. Предпочтительно, настоящий способ предусматривает введение композиции, содержащей от 0,01 до 5 мг селена на 100 мл жидкого продукта, предпочтительно, от 0,02 до 0,1 мг селена на 100 мл жидкого продукта. Вводимое в сутки количество селена предпочтительно составляет более 0,01 мг, более предпочтительно, от 0,01 до 0,5 мг.
Белок
Хотя композиция может дополнительно содержать белковый материал, было установлено, что такой компонент не является необходимым. Фактически, так возможно сконцентрировать активные вещества в небольшом объеме композиции. В случае включения белковой фракции, эта белковая фракция содержит интактные белки, пептиды, которые могут быть получены путем гидролиза интактных белков и путем синтеза, производные пептидов, содержащие более 80 масс.% аминокислот. Азот нуклеозидного материала и холина при расчете не учитывается как белковый.
В одном варианте осуществления изобретения предпочтительно, чтобы количество таурина (включая соли таурина) составляло менее 0,1 г, предпочтительно, менее 0,05 г на суточную дозу. Дополнительно или альтернативно, предпочтительно, чтобы количество таурина (включая соли таурина) составляло менее 5 мг, более предпочтительно, менее 2,5 мг на 100 г композиции.
В одном варианте осуществления изобретения композиция содержит менее 25 мг, более предпочтительно, менее 20 мг, наиболее предпочтительно, менее 15 мг цистеина и таурина на 100 мл (жидкой) композиции. В одном варианте осуществления изобретения композиция содержит менее 25 мг, более предпочтительно, менее 20 мг, наиболее предпочтительно, менее 15 мг цистеина на 100 мл (жидкой) композиции. Предпочтительно, чтобы белковая фракция содержала более 70 масс.% казеина или казеинатов или их гидролизатов, и более предпочтительно, 80 масс.% или более, так как казеины содержат относительно низкие количества цистеина по сравнению с другими белковыми источниками. Также предпочтительным является нагревание жидкой композиции для окисления присутствующих в белке молекул цистеина. Это ухудшает биологическую доступность любых остаточных количеств цистеина, присутствующих в композиции. Предпочтительная тепловая обработка включает в себя стерилизацию. Предпочтительно поддерживать температуру ниже 135°C, предпочтительно, ниже 132°C, в сочетании с промежутком времени, достаточно длительным для получения окисленного цистеина, т.е. более 30 секунд, предпочтительно, более 40 секунд.
В одном варианте осуществления изобретения, предпочтительно, чтобы содержание белка в композиции составляло менее 15% энергии, более предпочтительно, менее 10% энергии, наиболее предпочтительно, менее 5% энергии от общего количества энергии композиции. Процент энергии компонентов рассчитывают с использованием коэффициентов пересчета 9 ккал на грамм жиров, 4 ккал на грамм белка или грамм перевариваемых углеводов, 2 ккал на грамм пищевой клетчатки и ноль ккал для других компонентов композиции. В одном варианте осуществления изобретения предпочтительно, чтобы композиция содержала от менее 0,5 до 10 г белка на 100 мл, более предпочтительно, от менее 1 до 6 грамм белка на 100 мл, наиболее предпочтительно, от 2 до 6 грамм белка на 100 мл.
Предпочтительная композиция настоящего изобретения содержит на суточную дозу или на 100 мл композиции:
100-500 мг, предпочтительно, 200-400 мг ЭПК,
900-1500 мг, предпочтительно, 950-1300 мг ДГК,
50-600 мг, предпочтительно, 60-200 мг фосфолипидов,
200-600 мг, предпочтительно, 300-500 мг холина,
400-800 мг, предпочтительно, 500-700 мг УМФ (уридинмонофосфата),
20-60 мг, предпочтительно, 30-50 мг витамина E (альфа-ТЭ),
60-100 мг, предпочтительно, 60-90 мг витамина C,
40-80 мкг, предпочтительно, 45-65 мкг селена,
1-5 мкг, предпочтительно, 2-4 мкг витамина B12,
0,5-3 мг, предпочтительно, 0,5-2 мг витамина B6, и
200-600 мкг, предпочтительно, 300-500 мкг фолиевой кислоты.
Более предпочтительно, композиция настоящего изобретения содержит на 100 мл композиции:
100-500 мг, предпочтительно, 200-400 мг ЭПК,
900-1500 мг, предпочтительно, 950-1300 мг ДГК,
50-600 мг, предпочтительно, 60-200 мг фосфолипидов,
200-600 мг, предпочтительно, 300-500 мг холина,
400-800 мг, предпочтительно, 500-700 мг УМФ (уридинмонофосфата),
20-60 мг, предпочтительно, 30-50 мг витамина E (альфа-ТЭ),
60-100 мг, предпочтительно, 60-90 мг витамина C,
40-80 мкг, предпочтительно, 45-65 мкг селена,
1-5 мкг, предпочтительно, 2-4 мкг витамина B12,
0,5-3 мг, предпочтительно, 0,5-2 мг витамина B6, и
200-600 мкг, предпочтительно, 300-500 мкг фолиевой кислоты.
Вышеописанные композиции могут применяться в качестве диетотерапии, нутритивной поддержки, лечебного питания, продукта для специальных медицинских целей или в качестве пищевой добавки. Такой продукт может потребляться одной, двумя или тремя порциями от 74 до 200 мл в сутки или на порцию, наиболее предпочтительно, от 90 до 150 мл в сутки, наиболее предпочтительно, примерно 125 мл в сутки в вышеуказанных применениях.
Субъекты, на которых способ и композиция настоящего изобретения могут оказать благоприятное действие, часто имеют проблемы с приемом пищи. Их сенсорные способности и/или контроль мускулатуры могут быть нарушены, также как в некоторых случаях и их желание придерживаться правильного режима питания. Глотание и/или жевание могут оказаться проблематичными. Поэтому, настоящая композиция предпочтительно изготавливается в виде напитка, который можно пить через трубочку.
В связи с этим, композиция настоящего изобретения предпочтительно имеет низкую вязкость, предпочтительно, вязкость от 1 до 2000 мПа⋅c, измеряемую при скорости сдвига 100 сек-1 при температуре 20°C, более предпочтительно, вязкость от 1 до 100 мПа⋅c, измеряемую при скорости сдвига 100 сек-1 при температуре 20°C. В предпочтительном варианте осуществления изобретения настоящая композиция имеет вязкость 1-80 мПа⋅c при скорости сдвига 100 сек-1 при температуре 20°C, более предпочтительно, 1-40 мПа⋅c при скорости сдвига 100 сек-1 при температуре 20°C. Эти измерения вязкости могут быть проведены, например, при помощи системы пластина-конус.
Чтобы быть оптимально приемлемой для субъекта, настоящая композиция предпочтительно имеет осмоляльность от 300 до 800 мОсм/кг. Вместе с тем, энергетическая ценность продукта предпочтительно не является настолько высокой, чтобы нарушать нормальный режим питания. Находясь в жидкой форме, настоящий продукт предпочтительно содержит от 0,2 до 3 ккал/мл, более предпочтительно, от 0,5 до 2, от 0,7 до 1,5 ккал/мл.
В одном аспекте настоящее изобретение относится к способу улучшения или сохранения функциональной связи головного мозга и/или функциональной синаптической активности и/или сохранения сетевой организации головного мозга у нуждающегося в этом субъекта, и/или замедления возникновения, предотвращения или восстановления нарушенной функциональной связи головного мозга и/или нарушенной функциональной синаптической активности и/или нарушенной сетевой организации головного мозга у нуждающегося в этом субъекта, включающему в себя введение указанному субъекту композиции, содержащей вышеуказанные компоненты (i)-(ii), а также дополнительно охарактеризованной здесь выше.
В одном аспекте настоящее изобретение относится к способу улучшения или сохранения функциональной связи и/или сохранения сетевой организации головного мозга у нуждающегося в этом субъекта, включающему в себя введение указанному субъекту композиции, содержащей вышеуказанные компоненты (i)-(ii), а также дополнительно охарактеризованной здесь выше.
В одном аспекте настоящее изобретение относится к способу лечения нуждающегося в этом субъекта, включающему в себя введение, предпочтительно, по меньшей мере, ежедневное, указанному субъекту композиции, содержащей вышеуказанные компоненты (i)-(ii), а также дополнительно охарактеризованной здесь выше; и мониторинг указанного субъекта при помощи метода визуализации с целью оценки функциональной связи, предпочтительно, одного или нескольких методов визуализации, выбранных из списка, состоящего из электроэнцефалографии (ЭЭГ), магнитоэнцефалографии (МЭГ), функциональной магнитно-резонансной томографии (фМРТ), фтордезоксиглюкоза-позитронно-эмиссионной томографии (ФДГ-ПЭТ), спектроскопии в ближней инфракрасной области (БИК-спектроскопия), однофотонной эмиссионной компьютерной томографии (ОФЭКТ), мечения артериальных спинов (МАС), предпочтительно, ЭЭГ, фМРТ и/или МЭГ, во время лечения. В одном аспекте указанный субъект подвергается процедуре мониторинга для выявления изменений ИСФ. В другом аспекте сетевая организация и сетевая функциональная связь может быть охарактеризована при помощи анализа, основанного на теории графов, с получением различных сетевых параметров, таких как коэффициент кластеризации C и характеристическая длина пути L. На следующем этапе на основе этих параметров может быть вычислен ИСТМ.
В другом аспекте настоящее изобретение относится к композиции для применения для улучшения или сохранения функциональной связи головного мозга и/или функциональной синаптической активности и/или сохранения сетевой организации головного мозга у нуждающегося в этом субъекта, и/или замедления возникновения, предотвращения или восстановления нарушенной функциональной связи головного мозга и/или нарушенной функциональной синаптической активности головного мозга и/или нарушенной сетевой организации головного мозга у нуждающегося в этом субъекта, где указанная композиция содержит вышеуказанные компоненты (i)-(ii), а также дополнительно охарактеризована здесь выше; и мониторингу указанного субъекта при помощи метода визуализации с целью оценки функциональной связи, предпочтительно, одного или нескольких методов визуализации, выбранных из списка, состоящего из электроэнцефалографии (ЭЭГ), магнитоэнцефалографии (МЭГ), функциональной магнитно-резонансной томографии (фМРТ), фтордезоксиглюкоза-позитронно-эмиссионной томографии (ФДГ-ПЭТ), спектроскопии в ближней инфракрасной области (БИК-спектроскопия), однофотонной эмиссионной компьютерной томографии (ОФЭКТ), мечения артериальных спинов (МАС), предпочтительно, ЭЭГ и/или МЭГ, во время лечения. В одном аспекте указанный субъект подвергается процедуре мониторинга для выявления изменений ИСФ. В другом аспекте сетевая организация и сетевая функциональная связь может быть охарактеризована при помощи анализа, основанного на теории графов, с получением различных сетевых параметров, таких как коэффициент кластеризации C и характеристическая длина пути L. На следующем этапе на основе этих параметров может быть вычислен ИСТМ.
Предпочтительно, в способе настоящего изобретения увеличение ИСФ является показателем более высокой функциональной (синаптической) связи. В частности, увеличение ИСФ в дельта-диапазоне является показателем более высокой функциональной (синаптической) связи, предпочтительно у субъекта, страдающего нейродегенеративным заболеванием, более предпочтительно, у субъекта, страдающего болезнью Альцгеймера.
В одном аспекте настоящее изобретение относится к применению метода визуализации для оценки функциональной связи и сетевой организации головного мозга, предпочтительно, одного или нескольких методов визуализации, выбранных из списка, состоящего из электроэнцефалографии (ЭЭГ), магнитоэнцефалографии (МЭГ), функциональной магнитно-резонансной томографии (фМРТ), фтордезоксиглюкоза-позитронно-эмиссионной томографии (ФДГ-ПЭТ), спектроскопии в ближней инфракрасной области (БИК-спектроскопия), однофотонной эмиссионной компьютерной томографии (ОФЭКТ), мечения артериальных спинов (МАС), предпочтительно, ЭЭГ, фМРТ и/или МЭГ, для мониторинга функциональной синаптической связи, функциональной синаптической активности и сетевой организации головного мозга (в частности, путем определения коэффициента кластеризации C и характеристической длины пути L) в интервенционном исследовании, в котором указанный субъект, подвергаемый процедуре мониторинга, получает медикаментозное лечение, предпочтительно, композицию, содержащую вышеуказанные компоненты (i)-(ii), а также дополнительно охарактеризованную здесь выше. Более подробная информация об участвующем в интервенционном исследовании субъекте приведена здесь выше.
Примеры
Пример 1: Расфасованная композиция, содержащая на 125 мл:
Энергия 125 ккал; Белок 3,9 г; Углеводы 16,5 г; Жир 4,9 г.
Жир включает в себя 1,5 г ДГК+ЭПК и 106 мг фосфолипидов (соевый лецитин); Холин 400 мг; УМФ (уридинмонофосфат) 625 мг; Витамин E 40 мг альфа-ТЭ; Витамин C 80 мг; Селен 60 мкг; Витамин B12 3 мкг; Витамин B6 1 мг; Фолиевая кислота 400 мкг.
Минералы и микроэлементы: Натрий 125 мг; Калий 187,5 мг; Хлор 156,3 мг; Кальций 100 мг; Фосфор 87,5 мг; Магний 25 мг; Железо 2 мг; Цинк 1,5 мг; Медь 225 мг; Марганец 0,41 мг; Молибден 12,5 мкг; Хром 8,4; Йод 16,3 мкг; Витамины: Витамин A 200 мкг ретинола; Витамин D3 0,9 мкг; Витамин K 6,6 мкг; Тиамин (B1) 0,19 мг; Рибофлавин (В2) 0,2 мг; Ниацин (В3) 2,25 мг НЭ; Пантотеновая кислота (В5) 0,66 мг; Биотин 5 мкг.
Пример 2. Клиническое исследование
В настоящем интервенционном исследовании сетевую связь головного мозга, в частности функциональную сетевую связь головного мозга, изучали с использованием электроэнцефалографии (ЭЭГ). Исследование представляло собой 24-недельное рандомизированное, контролируемое, двойное слепое исследование, проведенной в 27 исследовательских центрах. Не получавшим медикаментозного лечения пациентам с легкой формой болезни Альцгеймера (20 или более баллов по КШОПС) и диагнозом возможная болезнь Альцгеймера по шкале нейропсихологических диагностических критериев, разработанной Национальными институтами неврологических и коммуникативных нарушений и инсульта и Ассоциацией болезни Альцгеймера и родственных нарушений, случайным образом (в соотношении 1:1) были назначены композиция, содержащая компоненты, указанные в Таблице 1, или изокалорийный контрольный продукт. Продолжительность приема этих препаратов составляла 24 недели.
Субъектов подвергали процедуре электроэнцефалографии (ЭЭГ) для оценки текущей осцилляторной активности головного мозга и нейронной сетевой организации в состоянии покоя. ЭЭГ проводили по стандартному для всех исследовательских центров протоколу. Данные регистрировали при помощи цифровых ЭЭГ-систем от 21 электрода в отведениях в системе 10-20: Fp2, Fp1, F8, F7, F4, F3, A2, A1, T4, T3, C4, C3, T6, T5, P4, P3, O2, O1, Fz, Cz, Pz. Использовали средневзвешенную схему отведений. Частота регистрации в разных исследовательских центрах была различной (200, 256, 400, 500, 512 или 1000 Гц), и если это было необходимо для анализа, то разрешение понижали. Онлайн параметры фильтра были 0,16 Гц для фильтра верхних частот и 70 гЦ для фильтра нижних частот. Четыре эпохи из 4096 регистраций, не содержащих артефактов данных (не содержащих моргания глаз, мышечных артефактов, медленных движений глаз или ЭЭГ-артефактов), отбирали для каждой ЭЭГ. Пиковую частоту определяли для теменно-затылочных электродов как медианную частоту между 4 и 13 гЦ. Затем пиковую частоту усредняли для четырех эпох и для электродов.
Функциональную связь между всеми парами электродов устанавливали при помощи индекса сдвига фаз (ИСФ), показателя, который является относительно нечувствительным к объемной проводимости (Stam et al., 2007). Затем к полученным с помощью ЭЭГ данным о функциональной связи применяли анализ, основанный на теории графов. Граф представляет собой сеть головного мозга, где электроды являются узлами графа, а значение ИСФ для пары узлов является ребром. Из этого графа рассчитывали два основных параметра сети: средний коэффициент кластеризации (C) и среднюю кратчайшую длину пути (L). C определяется вероятностью того, что два узла являются связанными, когда они оба связаны с одним и тем же узлом (когда они «имеют общий соседний узел»), что является мерой местной связи. L отражает общую интеграцию сети и определяется и определяется взвешенной кратчайшей длиной пути, вычисленной с помощью алгоритма Дейкстры (VanSteen 2010). Для того чтобы сравнить сети различных субъектов, эти сети были нормализованы путем создания 50 стохастических сетей для каждой сети, случайным образом изменяя значения ИСФ в каждой матрице смежности. Для этих сетей вычисляли C и L. Получая соотношение (сетевые параметры реальной сети делили на соответствующие параметры стохастических сетей), сетевые параметры затем нормализовали для размера сети и силы связи. Полученные нормализованный коэффициент кластеризации (гамма) и нормализованная длина пути (лямбда) использовали для дальнейших анализов.
Результаты
В общей сложности для участия в интервенционном исследовании в течение периода времени более 1,5 лет случайным образом было отобрано 259 пациентов; 130 - в экспериментальную группу и 129 - в контрольную группу. Экспериментальные группы были хорошо подобраны с учетом всех характеристик.
Данные ЭЭГ были доступны для подгруппы из 179 субъектов; 86 - из экспериментальной группы и 93 - из контрольной группы. Анализ функциональной связи для дельта-диапазона показал значимое влияние приема композиции в течение 24-недельного периода исследования (p=0,011). Для пиковой частоты разница в траектории после 24 недель между группами была значимой (p=0,019). Как показано на фиг. 3, пиковая частота замедлялась в контрольной группе в течение 24 недель исследования и оставалась относительно стабильной в экспериментальной группе. Синаптическая связь сохранялась в экспериментальной группе, в то время как она продолжала ухудшаться в контрольной группе. В целом, исследование дало значимые результаты для (1) пиковой частоты (p=0,019); (2) функциональной связи (ИСФ) в дельта-диапазоне (p=0,011); (3) нормализованного коэффициента кластеризации (гамма) в бета-диапазоне (p=0,0009); и (4) нормализованной длины пути (лямбда) в бета-диапазоне (p=0,053).
На фиг. 4a показан средний нормализованный коэффициент кластеризации C, и на фиг. 4b показаны расчеты для средней нормализованной длины пути L. Как показано на фиг. 4a и 4b, сети головного мозга пациентов, получавших контрольный продукт, демонстрировали снижение гамма (т.е. нормализованного коэффициента кластеризации) и снижение лямбда (нормализованной длины пути) в бета-диапазоне. В противоположность этому, пациенты, получавшие исследуемый продукт, демонстрировали стабильные сетевые параметры, что позволяет предположить сохранение у них функциональной сетевой организации головного мозга.
Комбинация уменьшения местной кластеризации и уменьшения длины пути в течение 24 недель исследования в контрольной группе указывает на деградацию сети «тесного мира» в сторону случайной сетевой организации, как это ожидается при прогрессировании болезни Альцгеймера. Стабильные сетевые параметры (сохраненная функциональная ЭЭГ сетевая организация), наблюдаемые в группе, получвшей исследуемый продукт, позволяют предположить, что этот продукт влияет на синаптическую функцию и оказывает биологическое дйствие на головной мозг пациентов с легкой формой болезни Альцгеймера.
Обсуждение
Подводя итог, это исследование показало, что прием в течение 24 недель экспериментальной композиции улучшил функциональную связь и сохранил сетевую организацию головного мозга, а также является хорошо переносимым у не получавших медикаментозного лечения пациентов с легкой формой болезни Альцгеймера.
Ссылки
Список литературных источников


| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ПОЛИНЕНАСЫЩЕННЫЕ ЖИРНЫЕ КИСЛОТЫ (ПНЖК), И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2006 |
|
RU2436571C2 |
| НУТРИТИВНАЯ КОМПОЗИЦИЯ ДЛЯ УЛУЧШЕНИЯ ФУНКЦИИ МОЗГА ПРИ ФЕНИЛКЕТОНУРИИ | 2014 |
|
RU2690660C2 |
| УЛУЧШЕНИЕ ПАМЯТИ У ПАЦИЕНТОВ С ОЦЕНКОЙ 24-26 БАЛЛОВ ПО КРАТКОЙ ШКАЛЕ ОЦЕНКИ ПСИХИЧЕСКОГО СТАТУСА | 2008 |
|
RU2529815C2 |
| УЛУЧШЕНИЕ ПАМЯТИ У ПАЦИЕНТОВ С ОЦЕНКОЙ 24-26 БАЛЛОВ ПО КРАТКОЙ ШКАЛЕ ОЦЕНКИ ПСИХИЧЕСКОГО СТАТУСА | 2014 |
|
RU2677345C2 |
| СПОСОБ УЛУЧШЕНИЯ УПРАВЛЯЮЩИХ ФУНКЦИЙ | 2012 |
|
RU2637089C2 |
| ПИЩЕВАЯ КОМПОЗИЦИЯ ДЛЯ ПАЦИЕНТОВ С ПРОДРОМАЛЬНЫМ СЛАБОУМИЕМ | 2008 |
|
RU2487557C2 |
| УЛУЧШЕНИЕ УЗНАВАНИЯ | 2012 |
|
RU2638809C2 |
| ЖИДКИЙ ПРОДУКТ, СОДЕРЖАЩИЙ НУКЛЕОТИДЫ/НУКЛЕОЗИДЫ | 2008 |
|
RU2446807C2 |
| ТЕРАПЕВТИЧЕСКИЕ КОМБИНАЦИИ ЖИРНЫХ КИСЛОТ | 2001 |
|
RU2276975C2 |
| ЭТИЛ-ЭПК С ВЫСОКОЙ СТЕПЕНЬЮ ЧИСТОТЫ И ДРУГИЕ ПРОИЗВОДНЫЕ ЭПК ДЛЯ ПСИХИАТРИЧЕСКИХ И НЕВРОЛОГИЧЕСКИХ РАССТРОЙСТВ | 2000 |
|
RU2260423C2 |
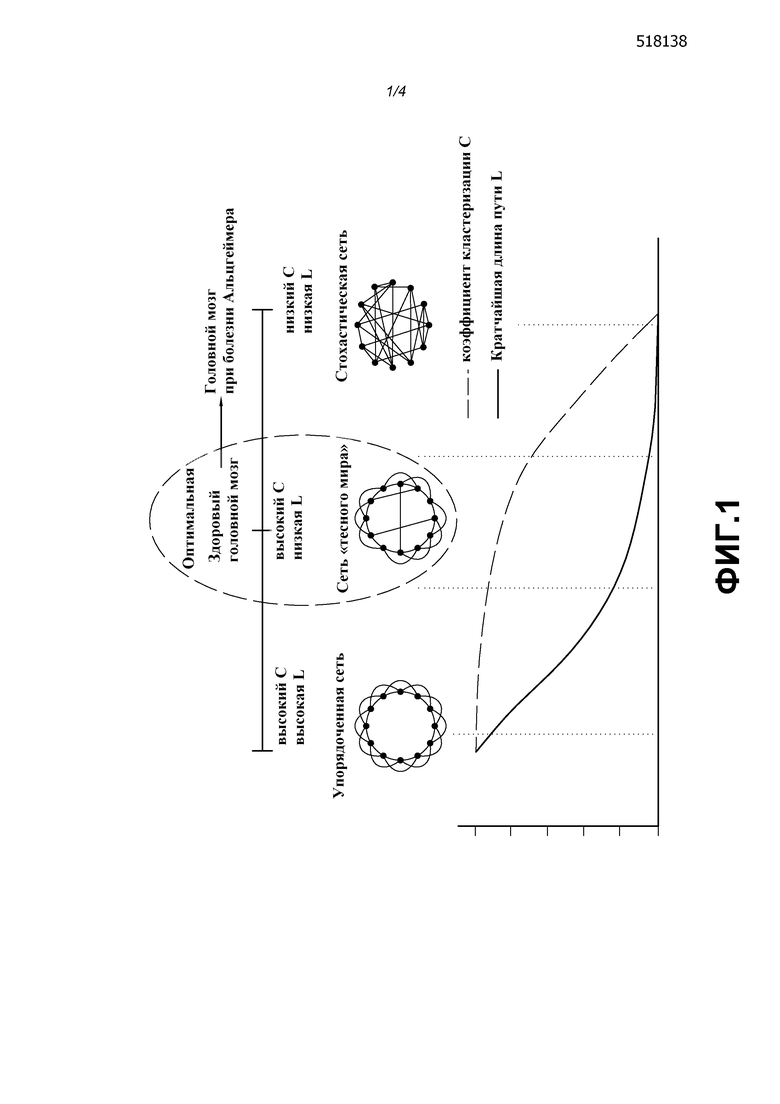
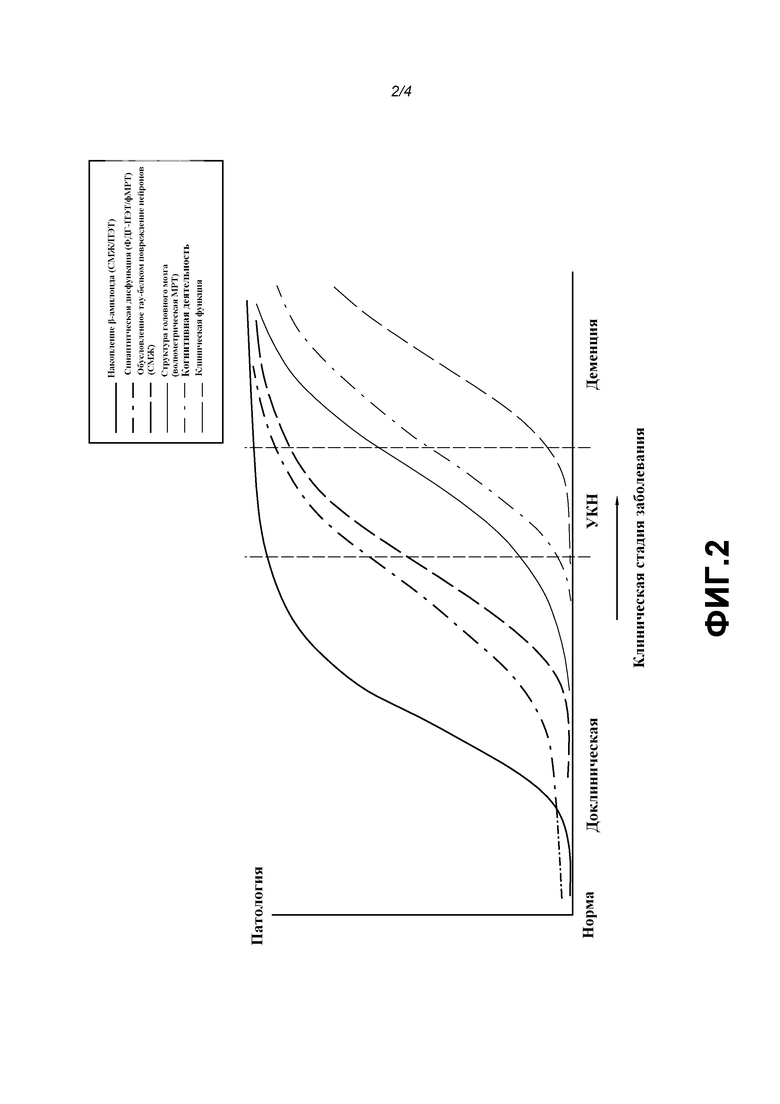
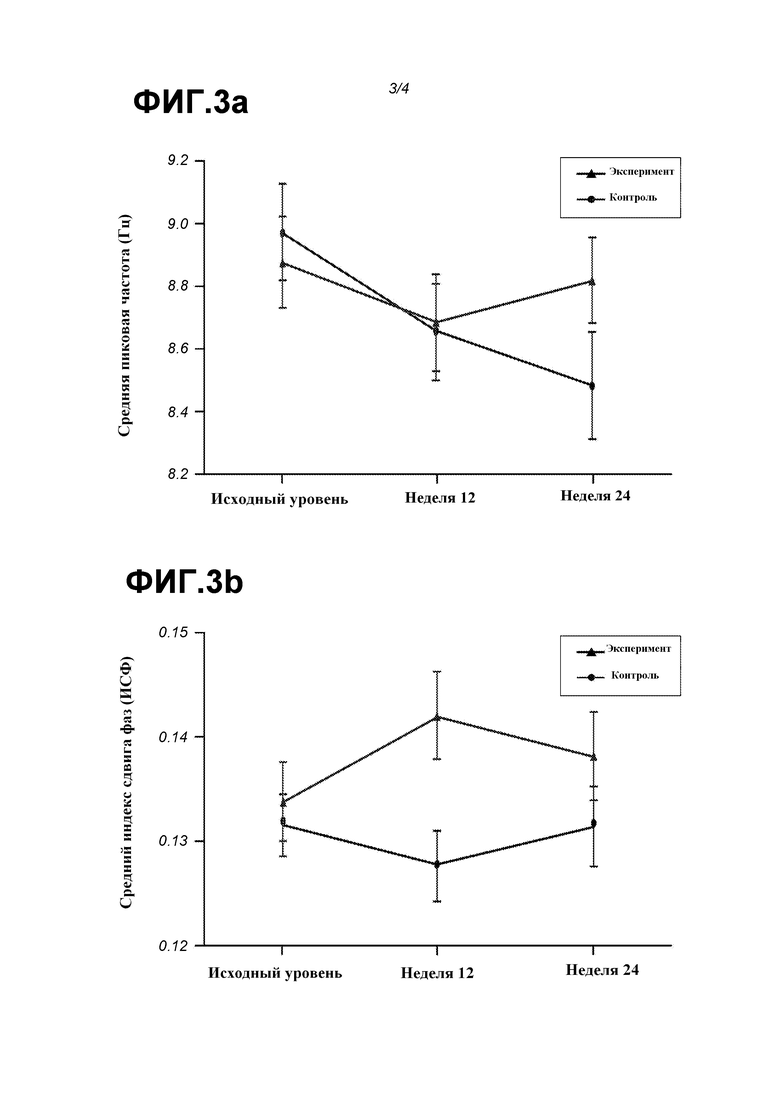
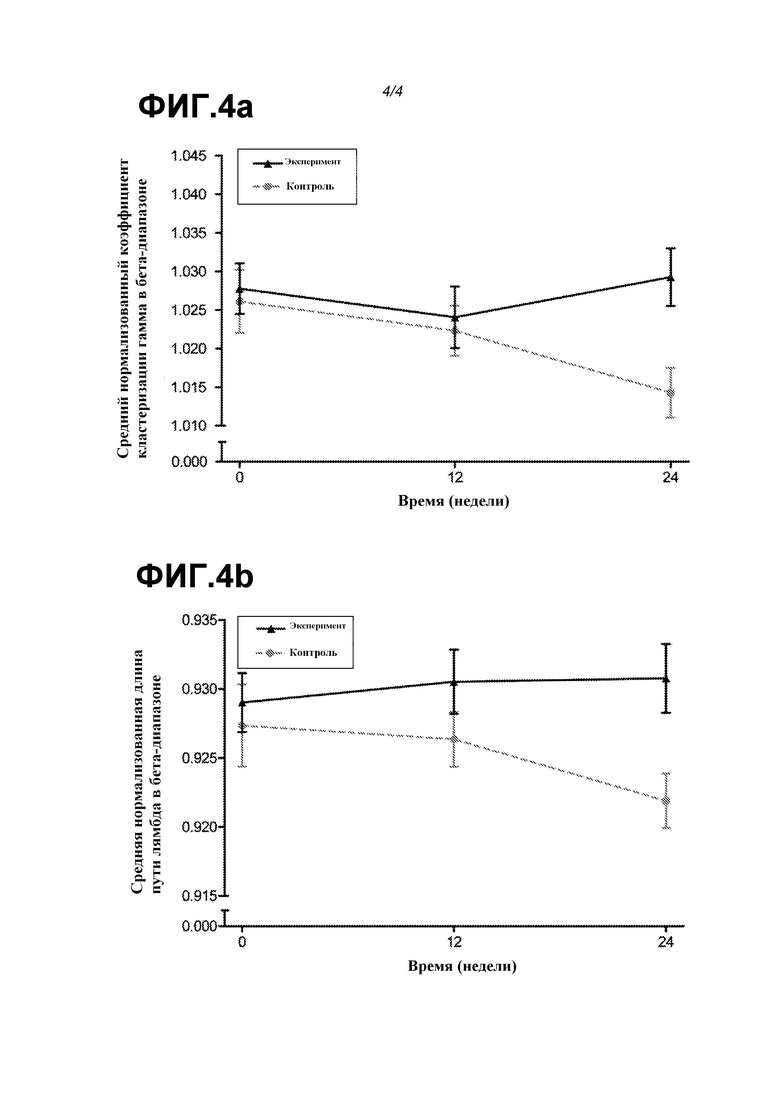
Группа изобретений относится к медицине. Описана композиция, включающая (i) одно или несколько из следующих веществ: уридин и цитидин или их соли, фосфаты, ацильные производные или сложные эфиры; и (ii) липидную фракцию, содержащую по меньшей мере одну из докозагексаеновой кислоты (22:6; ДГК), эйкозапентаеновой кислоты (20:5; ЭПК) и докозапентаеновой кислоты (22:5; ДПК) или их сложные эфиры, iii) холин или его соли или сложные эфиры, iv) меньшей мере два витамина В, для применения для сохранения или улучшения функциональной синаптической связи и/или сохранения сетевой организации головного мозга у нуждающегося в этом субъекта. Композиции применяются для улучшения или сохранения функциональной связи головного мозга и/или сетевой организации головного мозга у субъекта. 4 н. и 5 з.п. ф-лы, 4 ил., 2 табл., 2 пр.
1. Применение
i) одного или нескольких из уридина и цитидина или их солей, фосфатов, ацильных производных или сложных эфиров;
ii) липидной фракции, содержащей по меньшей мере одну из докозагексаеновой кислоты (22:6; ДГК), эйкозапентаеновой кислоты (20:5; ЭПК) и докозапентаеновой кислоты (22:5; ДПК) или их сложные эфиры;
iii) холина или его солей или сложных эфиров; и
iv) по меньшей мере двух витаминов B, выбранных из группы, состоящей из витамина B6, витамина B12 и витамина B9,
для производства композиции для улучшения или сохранения функциональной связи головного мозга и/или сетевой организации головного мозга у субъекта, страдающего от нарушенной функциональной связи и/или нарушенной сетевой организации головного мозга, и/или замедления возникновения, предотвращения или восстановления нарушенной функциональной связи головного мозга и/или нарушенной сетевой организации головного мозга у субъекта, страдающего от нарушенной функциональной связи, и/или нарушенной сетевой организации головного мозга, где указанную композицию вводят указанному субъекту в течение по меньшей мере 24 недель и где указанный субъект страдает или имеет риск развития болезни Альцгеймера или синдрома деменции, включая легкую или продромальную форму болезни Альцгеймера или деменции,
где композиция включает на суточную дозу:
100-500 мг ЭПК,
1000-1500 мг ДГК,
50-600 мг фосфолипидов,
200-600 мг холина,
400-800 мг УМФ (уридинмонофосфата),
20-60 мг витамина E (альфа-ТЭ),
60-100 мг витамина C,
40-80 мкг селена,
1-5 мкг витамина B12,
0,5-3 мг витамина B6 и
200-600 мкг фолиевой кислоты.
2. Применение
i) одного или нескольких из уридина и цитидина или их солей, фосфатов, ацильных производных или сложных эфиров;
ii) липидной фракции, содержащей по меньшей мере одну из докозагексаеновой кислоты (22:6; ДГК), эйкозапентаеновой кислоты (20:5; ЭПК) и докозапентаеновой кислоты (22:5; ДПК) или их сложные эфиры;
iii) холина или его солей или сложных эфиров; и
iv) по меньшей мере двух витаминов B, выбранных из группы, состоящей из витамина B6, витамина B12 и витамина B9,
для производства композиции для лечения субъекта, страдающего от нарушенной функциональной связи и/или нарушенной сетевой организации головного мозга, и где указанный субъект подвергается процедуре визуализации с целью оценки или мониторинга функциональной связи головного мозга и/или сетевой организации головного мозга, где субъект страдает или имеет риск развития таких заболеваний, как болезнь Альцгеймера или синдром деменции, включая легкую или продромальную форму болезни Альцгеймера или деменции, где указанную композицию вводят указанному субъекту в течение по меньшей мере 24 недель,
где указанная композиция включает на суточную дозу:
100-500 мг ЭПК,
1000-1500 мг ДГК,
50-600 мг фосфолипидов,
200-600 мг холина,
400-800 мг УМФ (уридинмонофосфата),
20-60 мг витамина E (альфа-ТЭ),
60-100 мг витамина C,
40-80 мкг селена,
1-5 мкг витамина B12,
0,5-3 мг витамина B6 и
200-600 мкг фолиевой кислоты.
3. Способ улучшения или сохранения функциональной связи и/или сетевой организации головного мозга у субъекта, страдающего от нарушенной функциональной связи и/или нарушенной сетевой организации головного мозга, где указанный способ включает введение указанному субъекту композиции, содержащей:
i) одно или несколько из уридина и цитидина или их солей, фосфатов, ацильных производных или сложных эфиров;
ii) липидную фракцию, содержащую по меньшей мере одну из докозагексаеновой кислоты (22:6; ДГК), эйкозапентаеновой кислоты (20:5; ЭПК) и докозапентаеновой кислоты (22:5; ДПК) или их сложные эфиры;
iii) холин или его соли или сложные эфиры; и
iv) по меньшей мере два витамина B, выбранных из группы, состоящей из витамина B6, витамина B12 и витамина B9, где указанную композицию вводят указанному субъекту в течение по меньшей мере 24 недель, где указанный субъект страдает или имеет риск развития таких заболеваний, как болезнь Альцгеймера или синдром деменции, включая легкую или продромальную форму болезни Альцгеймера или деменции, и где указанный субъект при необходимости подвергается процедуре визуализации с целью оценки или мониторинга функциональной связи головного мозга и/или сетевой организации головного мозга,
где композиция включает на суточную дозу:
100-500 мг ЭПК,
1000-1500 мг ДГК,
50-600 мг фосфолипидов,
200-600 мг холина,
400-800 мг УМФ (уридинмонофосфата),
20-60 мг витамина E (альфа-ТЭ),
60-100 мг витамина C,
40-80 мкг селена,
1-5 мкг витамина B12,
0,5-3 мг витамина B6 и
200-600 мкг фолиевой кислоты.
4. Применение по п.1 или 2, где указанная процедура визуализации включает электроэнцефалографию (ЭЭГ), функциональную магнитно-резонансную томографию (фМРТ) и/или магнитоэнцефалографию (МЭГ).
5. Способ по п.3, где указанная процедура визуализации включает электроэнцефалографию (ЭЭГ), функциональную магнитно-резонансную томографию (фМРТ) и/или магнитоэнцефалографию (МЭГ).
6. Применение по п.1 или 2, где указанная композиция содержит 200-600 мг холина на суточную дозу композиции.
7. Применение по п.1 или 2, где указанная композиция содержит все витамины B, выбранные из группы, состоящей из витамина B6, витамина B12 и витамина B9.
8. Композиция, применяемая для улучшения или сохранения функциональной связи головного мозга и/или сетевой организации головного мозга у нуждающегося в этом субъекта, страдающего от нарушенной функциональной связи и/или нарушенной сетевой организации головного мозга, где указанную композицию вводят указанному субъекту в течение по меньшей мере 24 недель, где указанная композиция содержит:
i) одно или несколько из уридина и цитидина или их солей, фосфатов, ацильных производных или сложных эфиров;
ii) липидную фракцию, содержащую по меньшей мере одну из докозагексаеновой кислоты (22:6; ДГК), эйкозапентаеновой кислоты (20:5; ЭПК) и докозапентаеновой кислоты (22:5; ДПК) или их сложные эфиры;
iii) холин или его соли или сложные эфиры; и
iv) по меньшей мере два витамина B, выбранных из группы, состоящей из витамина B6, витамина B12 и витамина B9,
где указанный субъект страдает или имеет риск развития таких заболеваний, как болезнь Альцгеймера или синдром деменции, включая легкую или продромальную форму болезни Альцгеймера или деменции,
где композиция включает на суточную дозу:
100-500 мг ЭПК,
1000-1500 мг ДГК,
50-600 мг фосфолипидов,
200-600 мг холина,
400-800 мг УМФ (уридинмонофосфата),
20-60 мг витамина E (альфа-ТЭ),
60-100 мг витамина C,
40-80 мкг селена,
1-5 мкг витамина B12,
0,5-3 мг витамина B6 и
200-600 мкг фолиевой кислоты.
9. Композиция по п.8, где указанный субъект подвергается процедуре визуализации с целью оценки или мониторинга функциональной связи головного мозга и/или сетевой организации головного мозга.
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| Колосоуборка | 1923 |
|
SU2009A1 |
| ЛИПИДЫ, СОДЕРЖАЩИЕ ЖИРНЫЕ КИСЛОТЫ ОМЕГА-3 И ОМЕГА-6 | 2004 |
|
RU2362566C2 |
| DANI S | |||
| BASSETT et al, Network Analysis I & II, Department of Physics University of California Santa Barbara, 2011, PNAS | |||
| Alex Fornito et al, Genetic Influences on Cost-Efficient Organization of Human Cortical Functional Networks, J | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
2018-09-25—Публикация
2013-03-04—Подача