Настоящая заявка испрашивает преимущество предварительной заявки США №61/665464 от 28 июня 2012 года, полное содержание которой включено в настоящую заявку путем ссылки для любых целей.
ОБЛАСТЬ ПРИМЕНЕНИЯ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к солнцезащитным композициям для местного применения, содержащим УФ-поглощающие полиэфиры.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Длительное воздействие ультрафиолетового (УФ) излучения, например, солнечных лучей, может привести к образованию световых дерматозов и эритем, а также увеличивает риск развития рака кожи, такого как меланома, и ускоряет старение кожи, например, приводит к потере эластичности и образованию морщин.
В продаже имеются многочисленные солнцезащитные композиции с различной способностью защищать тело от ультрафиолетовых лучей. Вместе с тем в задаче создания солнцезащитных композиций, обеспечивающих надежную защиту от УФ-излучения, по-прежнему остается множество нерешенных проблем.
Проблемы, связанные с созданием солнцезащитных средств, обладающих различными свойствами, например, мягкостью и т.д., дополнительно увеличиваются в случае наложения дополнительных ограничений на солнцезащитную композицию. Настоящее изобретение представляет мягкие, обладающие высокими эстетическими характеристиками композиции, содержащие полимерное солнцезащитное соединение.
ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
В соответствии с одним вариантом изобретения, композиции настоящего изобретения включают дисперсную масляную фазу, которая включает солнцезащитный агент, содержащий полимерную композицию, которая включает линейный поглощающий ультрафиолетовое излучение простой полиэфир, содержащий химически связанный УФ-поглощающий хромофор. Линейный поглощающий ультрафиолетовое излучение полиэфир присутствует в составе композиции в количестве, эффективном для обеспечения композиции с солнцезащитным фактором (SPF) приблизительно 10 или выше. Дисперсная масляная фаза гомогенно распределена в непрерывной водной фазе. Композиция дополнительно включает анионный эмульгатор для эмульсий типа «масло в воде» и неионный эмульгатор для эмульсий типа «масло в воде», содержащий спиртовую функциональную группу, причем весовое соотношение содержания анионного эмульгатора для эмульсий типа «масло в воде» и неионного эмульгатора для эмульсий типа «масло в воде» составляет приблизительно 12 или меньше.
ПОДРОБНОЕ ОПИСАНИЕ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
Все технические и научные термины, используемые в настоящем документе, если не дано иное их определение, имеют общепринятое значение, понятное любому специалисту в области, к которой имеет отношение настоящее изобретение. Все углеводородные группы, упоминаемые в настоящем изобретении, (например, алкильные, алкенильные), если не указано иное, могут представлять собой группы с неразветвленными или разветвленными цепями. Применяемый в настоящем документе термин «молекулярная масса», если не указано иное, относится к средневесовой молекулярной массе (Mw).
Если не указано другое, все концентрации относятся к концентрациям по весу композиции. Кроме того, если специально не указано другое, термин «по существу не содержит», применяемый в отношении того или иного класса компонентов, означает, что тот или иной конкретный компонент(ы) присутствует(ют) в концентрации меньшей, чем это необходимо для эффективности такого конкретного компонента для обеспечения того или иного благоприятного воздействия или свойства, для которого его бы в противном случае применяли, например, приблизительно 1% или менее или приблизительно 0,5% или менее.
Применяемый в настоящем документе термин «УФ-поглощающий» относится к материалу или соединению, например, полимерному или не являющемуся полимерным солнцезащитному агенту или химическому фрагменту, которые поглощают излучение в некоторой части ультрафиолетового спектра (290-400 нм), например, содержащим коэффициент экстинкции по меньшей мере приблизительно 1000 моль-1 см-1, по меньшей мере на одной длине волны в пределах определенного выше ультрафиолетового спектра. Величины SPF, раскрываемые и приведенные ниже в формуле изобретения, определяют с применением способа in vitro, который описан ниже в настоящем документе.
УФ-ПОГЛОЩАЮЩИЙ ПОЛИЭФИР
Варианты осуществления настоящего изобретения относятся к соединениям, содержащим простой полиэфир, поглощающий ультрафиолетовое излучение (т.е. «УФ-поглощающий полиэфир»). Под УФ-поглощающим полиэфиром понимается простой полиэфир, который поглощает излучение в некоторой части ультрафиолетового спектра (длина волны от 290 до 400 нм). УФ-поглощающий полиэфир имеет средневесовую молекулярную массу (Mw), который обеспечивает снижение или предотвращение впитывания хромофора через кожу. В соответствии с одним вариантом осуществления, УФ-поглощающий полиэфир может иметь молекулярную массу Mw больше, чем 500. В одном варианте осуществления Mw находится в диапазоне от приблизительно 500 до приблизительно 50000. В другом варианте осуществления Mw находится в диапазоне от приблизительно 1000 до приблизительно 20000, например, от приблизительно 1000 до приблизительно 10000.
В настоящем документе описана композиция, включающая УФ-поглощающий простой полиэфир. Как понятно специалисту, термин «простой полиэфир» (который в настоящем документе для упрощения часто будет сокращаться до «полиэфир») означает, что УФ-поглощающий полимер содержит множество функциональных групп простого эфира, связанных между собой ковалентными связями. Термин «основная цепь» для УФ-поглощающего полиэфира относится к самой длинной непрерывной последовательности эфирных функциональных групп, связанных между собой ковалентными связями. Другие меньшие группы ковалентно связанных атомов считаются боковыми группами, которые ответвляются от основной цепи.
Согласно некоторым вариантам осуществления, УФ-поглощающий полиэфир содержит глицериловые повторяющиеся звенья и, соответственно, может быть охарактеризован как полиглицерин. Под «глицериловыми повторяющимися звеньями» (также называемыми в данной заявке «глицериловыми остаточными звеньями») понимают звенья глицерина без нуклеофильных групп, таких как гидроксильные группы. Глицериловые остаточные звенья включают функциональные группы простых эфиров и, как правило, могут быть представлены как C3H5O для линейных и дендритных остатков (Rokicki et al. Green Chemistry., 2005 г., 7, 52). Соответствующие целям настоящего изобретения глицериловые остаточные звенья включают дегидратированные формы (т.е. с удаленным одним молем воды) следующих глицериновых звеньев: линейные-1,4 (L1,4) глицериловые звенья; линейные-1,3 (L1,3) глицериловые повторяющиеся звенья; дендритные (D) глицериловые звенья; концевые-1,2 (T1,2) звенья; и концевые-1,3 (T1,3) звенья. Примеры линейных глицериловых остаточных звеньев и концевых звеньев показаны ниже (справа от стрелок). Также показаны соответствующие глицериловые звенья до дегидратации (слева от стрелок; включают гидроксильные группы):
линейные-1,4 (L1,4) глицериловые повторяющиеся звенья:
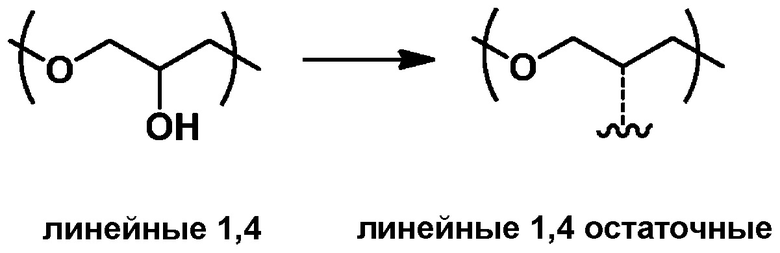
линейные-1,3 (L1,3) глицериловые повторяющиеся звенья:
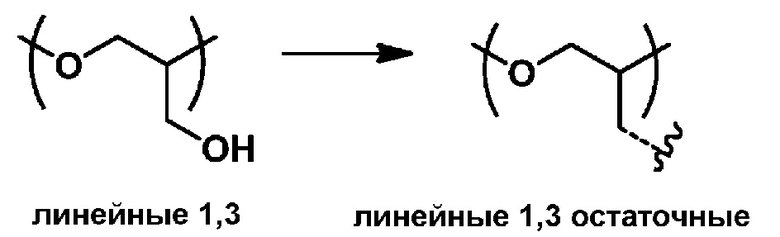
концевые-1,2 (T1,2) звенья:
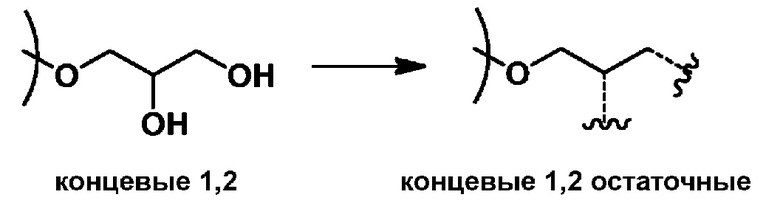
и концевые-1,3 (T1,3) звенья:
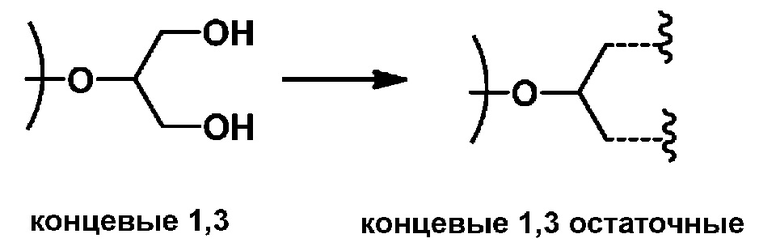
Композиция включает линейный УФ-поглощающий полиэфир, который содержит химически связанный хромофор, поглощающий ультрафиолетовое излучение («УФ-поглощающий хромофор»). Под термином «линейный» подразумевается, что УФ-поглощающий полиэфир имеет основную цепь, которая не имеет ответвлений.
Согласно некоторым вариантам осуществления линейный УФ-поглощающий полиэфир включает любой или оба из повторяющихся звеньев, показанных в приведенных ниже формуле IА и формуле IIB:
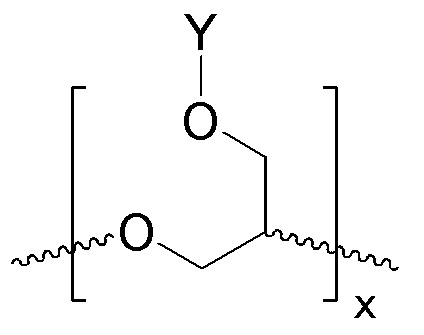
ФОРМУЛА IA. ПОВТОРЯЮЩЕЕСЯ ЗВЕНО ЛИНЕЙНОГО УФ-ПОГЛОЩАЮЩЕГО ПОЛИЭФИРА
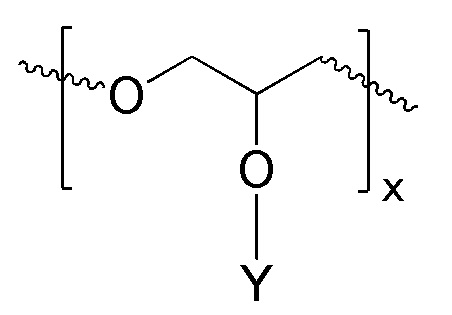
ФОРМУЛА IIB. ПОВТОРЯЮЩЕЕСЯ ЗВЕНО ЛИНЕЙНОГО УФ-ПОГЛОЩАЮЩЕГО ПОЛИЭФИРА
В ФОРМУЛАХ IA и IIB Y представляет собой УФ-поглощающий хромофор, как описано ниже.
Типичный пример линейного поглощающего ультрафиолетовое излучение полиэфира, содержащего химически связанный УФ-поглощающий хромофор, показан в ФОРМУЛЕ IIIC:
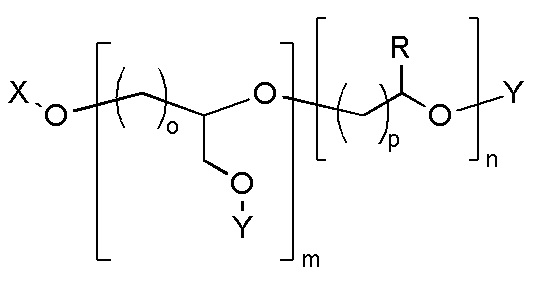
ФОРМУЛА IIIC. ЛИНЕЙНЫЙ УФ-ПОГЛОЩАЮЩИЙ ПОЛИЭФИР
В приведенной ФОРМУЛЕ IIIC X представляет собой либо концевую функциональную группу, либо часть основной цепи полимера; R - боковая группа, присоединенная к основной цепи полимера, а Х - концевая группа.
X и R могут быть одинаковыми или могут различаться. X и R могут независимо выбирать, например, из водорода, линейных алкильной, алкенильной или алкинильной углеводородных цепей, линейных силоксанов и т.п. В одном варианте осуществления группа X представляет собой октадекан. Y представляет собой УФ-поглощающий хромофор; группы, обозначенные как Y, описаны ниже. Доля повторяющихся звеньев эфира, несущих заместитель Y, составляет действительное число, выраженное уравнением 1:
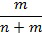 , Уравнение 1
, Уравнение 1
где m и n - действительные числа в диапазоне от 0 до 1, а сумма n и m равна 1. В одном варианте осуществления число m=1, а n=0 (УФ-поглощающий полиэфир является гомополимером и включает повторяющееся звено из ФОРМУЛЫ IA). В другом варианте осуществления число m<1 (полимер является сополимером), и полимер включает боковые группы R и Y. Для сополимеров, содержащих и боковые группы R, и боковые группы Y, распределение боковых групп R и Y вдоль цепи полимера можно изменять для получения оптимальных свойств полимера. В одном варианте осуществления УФ-поглощающий полиэфир является статистическим сополимером, в котором группы R и Y статистически распределены вдоль цепи полимера. В другом варианте осуществления УФ-поглощающий полиэфир является блочным сополимером, состоящим из перемежающихся сегментов основной цепи полимера с увеличенными долями функциональных групп R или Y. В другом варианте осуществления распределение боковых групп R и Y вдоль основной цепи полимера соответствует некоему промежуточному состоянию между вариантами, соответствующими граничным условиям, описывающим блочные и статистические сополимеры. В ФОРМУЛЕ IIIC целые числа o и p представляют собой количество групп CH2 в повторяющихся звеньях, несущих группы Y и R.
Включение различных боковых групп R можно обеспечить использованием других со-мономеров во время реакции полимеризации. Размер, химический состав, массовую долю этих ко-мономеров, а также их расположение в основной цепи можно изменять для изменения физических и химических свойств конечного УФ-поглощающего полиэфира. Примеры со-мономеров, которые могут быть включены в состав УФ-поглощающего полиэфира, без ограничений включают этиленоксид, пропиленоксид и глицидиловые эфиры, такие как н-бутилглицидиловый эфир, 2-этилгексилглицидиловый эфир.
Специалисту в области полимеров понятно, что полиэфиры типа, описанного в ФОРМУЛАХ IA, IIB и IIIC, могут быть получены различными синтетическими путями. Такие пути включают полимеризацию с раскрытием цикла циклических эфирных мономеров и необязательных со-мономеров. Размер цикла в циклических эфирных мономерах определяет величину o или p, а также результирующую структуру основной цепи УФ-поглощающего полиэфира. Для мономеров и со-мономеров, которые являются эпоксидами (трехчленные циклы, содержащие 2 атома углерода и один атом кислорода), величина o или p в результирующем УФ-поглощающем полиэфире равна 1. Повторяющееся звено, получаемое при использовании эпоксидного сомономера, показано в структуре A ФОРМУЛЫ IV. Для сомономеров, которые являются оксетанами (четырехчленные циклы, содержащие три атома углерода и один атом кислорода), величина o или p в результирующем поглощающем УФ-излучение полиэфире равна 2. Повторяющееся звено, получаемое при использовании оксетанового сомономера, показано в структуре B ФОРМУЛЫ IV. Для изменения свойств УФ-поглощающего полиэфира можно подобрать длину алкильной цепи внутри каждого типа мономера. В одном варианте осуществления и o, и p равны 1. Примером такого случая является случай, когда повторяющиеся звенья, несущие группы Y и R, оба получены из мономеров эпоксидов (o=p=1), или когда оба получены из оксетановых мономеров (o=p=2). В другом варианте осуществления o и p не равны. Примером такого случая является случай, когда повторяющиеся звенья, несущие УФ-поглощающий хромофор Y, основаны на эпоксидном мономере (o=1), а повторяющиеся звенья, несущие группу R, основаны на оксетановом мономере (p=2).
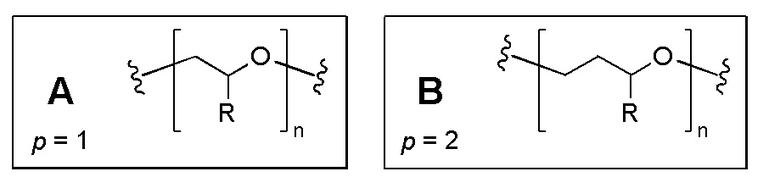
ФОРМУЛА IV. НЕОБЯЗАТЕЛЬНЫЕ ПОВТОРЯЮЩИЕСЯ ЗВЕНЬЯ
Соответствующие целям настоящего изобретения УФ-поглощающие хромофоры, которые можно химически включить в УФ-поглощающие полиэфиры настоящего изобретения, включают УФ-поглощающие триазолы (фрагмент, содержащий пятичленный гетероцикл с двумя атомами углерода и тремя атомами азота), такие как бензотриазолы. В другом варианте осуществления структура, представленная группой Y, содержит или имеет боковой УФ-поглощающий триазин (шестичленный гетероцикл, содержащий три атома азота и три атома углерода). Соответствующие целям настоящего изобретения УФ-поглощающие хромофоры включают те, которые имеют поглощение в диапазоне UVA. Другими соответствующими целям настоящего изобретения поглощающими УФ-излучение хромофорами являются те, которые имеют поглощение в диапазоне UVB. В одном варианте осуществления УФ-поглощающий хромофор способен поглощать излучение как в диапазоне UVA, так и в диапазоне UVB. В одном варианте осуществления, в котором УФ-поглощающий полиэфир формуется в виде пленки, можно получить молярный коэффициент поглощения, равный по меньшей мере для одной длины волны в данном диапазоне длин волн по меньшей мере приблизительно 1000 моль-1см-1, предпочтительно по меньшей мере приблизительно 2000 моль-1см-1, и еще предпочтительнее приблизительно 4000 моль-1см-1. В одном варианте осуществления молярный коэффициент поглощения для по меньшей мере 40% длин волн в данной части спектра составляет по меньшей мере приблизительно 1000 моль-1см-1. Примеры УФ-поглощающих хромофоров, поглощающих в диапазоне UVA, включают триазолы, такие как бензотриазолы, такие как гидроксифенилбензотриазолы; камфоры, такие как бензилиденкамфора и ее производные (такие как терефталилиден-дикамфорсульфоновая кислота); дибензоилметаны и их производные.
В одном варианте осуществления УФ-поглощающий хромофор является бензотриазолом, который обеспечивает как фотостабильность, так и сильное поглощение ультрафиолетового излучения в диапазоне UVA; его структурная формула показана в ФОРМУЛЕ V:
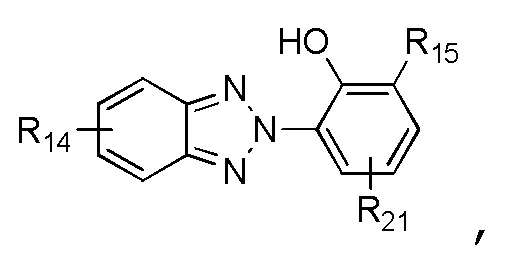
ФОРМУЛА V. БЕНЗОТРИАЗОЛЬНЫЙ УФ-ПОГЛОЩАЮЩИЙ ХРОМОФОР
где каждый R14 независимо выбирают из группы, состоящей из водорода, C1-C20 алкила, алкокси, ацила, алкилокси, алкиламино и галогена; R15 независимо выбирают из группы, состоящей из водорода, C1-C20 алкила, алкокси, ацила, алкилокси и алкиламино, R21 выбирают из C1-C20 алкила, алкокси, ацила, алкилокси и алкиламино. Каждая из групп R15 или R21 может включать функциональные группы, которые позволяют присоединяться к полимеру. Соединения, напоминающие структуру из ФОРМУЛЫ V, описаны в патенте США № 5869030, и без ограничений включают метилен-бис-бензотриазолилтетраметилбутилфенол (соединение, которое продается под торговой маркой TINSORB M производства корпорации BASF, г. Виандот, штат Мичиган). В одном варианте осуществления УФ-поглощающий триазол получен из продукта переэтерификации 3-(3-(2H-бензо[d][1,2,3]триазол-2-ил)-5-(трет-бутил)-4-гидроксифенил) пропановой кислоты с полиэтиленгликолем 300, который продается под торговой маркой TINUVIN 213 и также производится корпорацией BASF. В другом варианте осуществления УФ-поглощающий триазол состоит из сложных эфиров гидрокоричной кислоты и 3-(2H-бензотриазол-2-ил)-5-(1,1-диметилэтил)-4-гидрокси-, C7-9-разветвленных и линейных алкилов и продается под торговой маркой TINUVIN 99, также производства корпорации BASF. В другом варианте осуществления УФ-поглощающая группа содержит триазиновый фрагмент. Примером триазина является 6-октил-2-(4-(4,6-ди([1,1'-бифенил]-4-ил)-1,3,5-триазин-2-ил)-3-гидроксифенокси) пропаноат (соединение, которое продается под торговой маркой TINUVIN 479 производства корпорации BASF, г. Виандот, штат Мичиган).
В другом варианте осуществления УФ-поглощающий хромофор является молекулой, поглощающей в диапазоне UVB. Под хромофором, поглощающим в диапазоне UVB, понимается УФ-поглощающий хромофор, способный поглощать УФ-излучение в части UVB (от 290 до 320 нм) ультрафиолетового спектра. В одном варианте осуществления критерий определения поглощающего в диапазоне UVB хромофора такой же, как критерий, описанный выше для поглощающего в диапазоне UVA хромофора, с разницей в диапазоне волн (от 290 до 320 нм). Примеры соответствующих поглощающих в диапазоне UVB хромофоров включают 4-аминобензойную кислоту и ее алкановые эфиры; орто-аминобензойную кислоту и ее алкановые эфиры; салициловую кислоту и ее алкановые эфиры; гидроксикоричную кислоту и ее алкановые эфиры; дигидрокси-, дикарбокси- и гидроксикарбоксибензофеноны, а также их алкановые эфиры и галогенангидридные производные; дигидрокси-, дикарбокси- и гидроксикарбоксихалконы, а также их алкановые эфиры и галогенангидридные производные; дигидрокси-, дикарбокси- и гидроксикарбоксикумарины, а также их алкановые эфиры и галогенангидридные производные; бензальмалонат (бензилиденмалонат); производные бензимидазола (такие как фенилбензилимидазолсульфоновая кислота, PBSA), производные бензоксазола и другие соответствующим образом функционализированные соединения, способные к со-полимеризации внутри цепи полимера. В другом варианте осуществления УФ-поглощающий полиэфир содержит более одного УФ-поглощающего хромофора или более одного химического класса УФ-поглощающих хромофоров.
УФ-поглощающие полиэфиры настоящего изобретения могут быть синтезированы, согласно некоторым вариантам осуществления, в ходе полимеризации с раскрытием цикла соответствующего циклического эфирного мономера с образованием полиэфира, с последующим ковалентным связыванием УФ-поглощающего хромофора с боковыми функциональными группами («постполимеризационное присоединение»). Согласно некоторым другим вариантам осуществления, УФ-поглощающие полиэфиры могут быть синтезированы в ходе полимеризации циклического эфирного мономера, причем эфир сам включает ковалентно связанный УФ-поглощающий хромофор (т.н. «прямая полимеризация»).
Кроме того, специалисту в данной области будет понятно, что УФ-поглощающие полиэфиры, которые можно использовать в композициях для местного применения настоящего изобретения, получают посредством полимерного синтеза. Синтез УФ-поглощающего полиэфира по существу приводит к продукту взаимодействия, ниже в настоящем документе называемому «полимерной композицией», которая представляет собой смесь УФ-поглощающих полиэфиров с различными молекулярными массами. Полимерная композиция может дополнительно включать (кроме УФ-поглощающей полиэфирной композиции) небольшое количество неполимеризованного материала, который может быть удален из смеси общеизвестными способами. Согласно некоторым вариантам осуществления, неполимеризованный материал (например, частично прореагировавшие и непрореагировавшие мономеры или другие реагенты) может быть частично или полностью удален перед включением в композиции для местного применения, являющиеся предметом настоящего изобретения, с использованием, например, экстракции растворителем или очистки в сверхкритическом CO2.
Согласно некоторым вариантам осуществления, полимерная композиция для введения в состав композиций для местного применения настоящего изобретения содержит приблизительно 50% или более линейного УФ-поглощающего полиэфира, который содержит химически связанный с ним УФ-поглощающий хромофор. Согласно некоторым другим вариантам осуществления, полимерная композиция на 75% или более состоит из линейного УФ-поглощающего полиэфира, который содержит химически связанный с ним УФ-поглощающий хромофор. Согласно некоторым другим вариантам осуществления, полимерная композиция на 90% или более состоит из линейного УФ-поглощающего полиэфира, например, на приблизительно 95% или более. Согласно некоторым другим вариантам осуществления, в дополнение к линейному УФ-поглощающему полиэфиру полимерная композиция содержит разветвленный УФ-поглощающий полиэфир, который не является гиперразветвленным. В другом варианте осуществления полимерная композиция по существу не содержит гиперразветвленных УФ-поглощающих полиэфиров (например, содержит менее 1% вес. гиперразветвленного УФ-поглощающего полиэфира, например, менее 0,1% вес., или, например, совершенно не содержит гиперразветвленных УФ-поглощающих полиэфиров).
Согласно некоторым вариантам осуществления, полимерная композиция имеет низкую полидисперсность. Например, коэффициент полидисперсности может составлять приблизительно 1,5 или менее, например, приблизительно 1,2 или менее. Коэффициент полидисперсности определяется как Mw/MN (т.е. отношение средневесовой молекулярной массы Mw к среднечисленной молекулярной массе MN). Согласно некоторым другим вариантам осуществления, полимерная композиция содержит 50% вес. или более конкретного УФ-поглощающего полиэфира.
Полидисперсность полимерной композиции может удерживаться на низком уровне путем применения, например, специфических методов синтеза, таких как полимеризация с раскрытием цикла циклического эфирного мономера и снятие защитных групп (описано ниже). Кроме того, полимерную композицию можно обработать с применением известных специалистам способов, таких как экстракция в сверхкритическом CO2, для очистки полимерной композиции (например, после присоединения УФ-поглощающего хромофора).
Синтез линейного УФ-поглощающего полиэфира путем постполимеризационного присоединения УФ-поглощающего хромофора может включать стадию полимеризации с раскрытием цикла циклического эфирного мономера с образованием полиэфира, содержащего защитные группы; стадию снятия защитных групп для удаления по меньшей мере нескольких защитных групп из полиэфира; и стадию присоединения УФ-поглощающего хромофора к УФ-поглощающему полиэфиру со снятыми защитными группами с образованием УФ-поглощающего полиэфира, содержащего химически связанный УФ-поглощающий хромофор.
Пример синтеза линейного УФ-поглощающего полиэфира путем постполимеризационного присоединения схематически показан в ФОРМУЛЕ VI. Инициатор I используется для запуска реакции полимеризации циклического эфирного мономера M с образованием полимера P0, в котором боковые функциональные гидроксигруппы защищены защитной группой (P). Полимер P0 подвергается воздействию условий, которые удаляют защитную группу P, давая полимер со снятыми защитными группами Pd. И в завершение к боковым гидроксильным группам полимера Pd присоединяется УФ-поглощающий хромофор, давая требуемый конечный полимер, Pf:
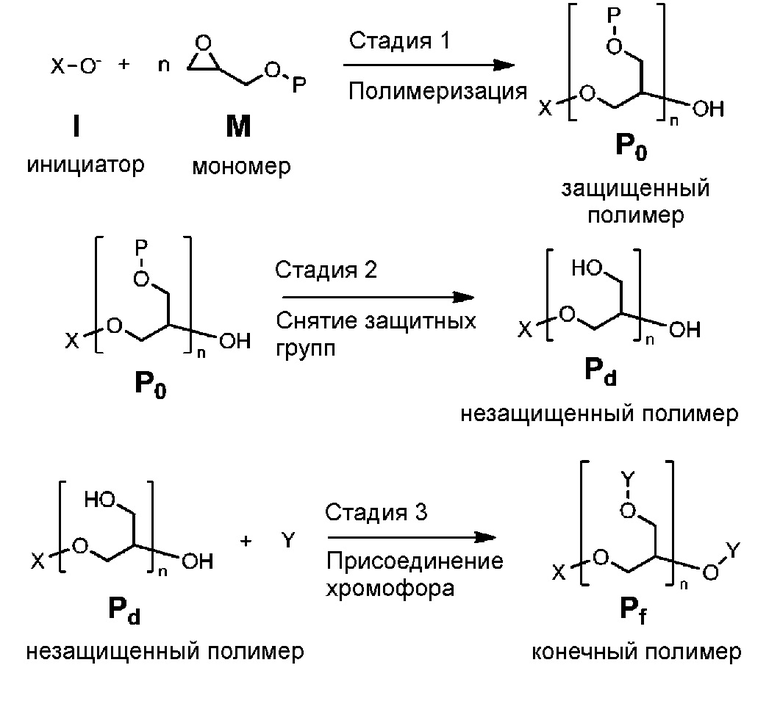
ФОРМУЛА VI. СИНТЕЗ УФ-ПОГЛОЩАЮЩЕГО ХРОМОФОРА ПУТЕМ ПОСТПОЛИМЕРИЗАЦИОННОЙ ФУНКЦИОНАЛИЗАЦИИ
Полимеризацию с раскрытием цикла циклического эфира, такого как мономер M в ФОРМУЛЕ VI, можно проводить различными способами, включая анионную и катионную полимеризацию с раскрытием цикла. В одном варианте осуществления полимеризацию проводят с использованием анионной полимеризации с раскрытием цикла. Мономер M в ФОРМУЛЕ VI представляет собой вид глицида, в котором основная гидроксигруппа закрыта защитной группой Р. В результате полимеризации незащищенного глицида образуются высокоразветвленные полимеры (US7988953B2, Tokar, R. et. al. Macromolecules 1994, 27, 320-322: Sunder, A. et. al. Macromolecules 1999: 4240-4246. Rokicki, G. et. al. Green Chemistry 2005, 7, 529). И наоборот, анионная полимеризация производных глицида, в которых основная гидроксильная группа была защищена, может образовывать линейные полиэфиры, как показано в структурной схеме P0 в ФОРМУЛЕ VI (Taton, D. et. al. Macromolecular Chemistry and Physics 1994, 195, 139-148: Erberich, M. et. al. Macromolecules 2007, 40, 3070-3079: Haouet, A. et. al. European Polymer Journal 1983, 19, 1089-1098: Obermeier, B. et. al. Bioconjugate Chemistry 2011, 22, 436-444: Lee, B. F. et. al. Journal of polymer science. Part A, Polymer chemistry 2011, 49, 4498-4504). Защищенные циклические эфирные мономеры не ограничиваются производными эпоксидов и включают функционализированные циклические эфиры, содержащие от 3 до 6 смежных атомов. В другом варианте осуществления мономер M является производной оксетана, содержащей защищенную основную гидроксильную группу.
Под термином «защищенный» имеется в виду, что функциональная группа в составе многофункциональной молекулы была выборочно дериватизирована с молекулой, которая предотвращает ковалентное изменение функциональной группы. Молекулы, используемые в качестве защитных групп, обычно присоединяются к необходимым функциональным группам с очень высоким химическим выходом и могут быть выборочно удалены с хорошим выходом, освобождая исходную функциональную группу. Защитные группы для гидроксильных групп без ограничений включают простые эфиры, такие как метиловый, метоксиметиловый (MOM), метилтиометиловый (MTM), т-бутилтиометиловый, (фенилдиметилсилил)метоксиметиловый (SMOM), бензилоксиметиловый (BOM), п-метоксибензилоксиметиловый (PMBM), (4-метоксифенокси)метиловый (p-AOM), т-бутоксиметиловый, 4-пентенилоксиметиловый (POM), силоксиметиловый, 2-метоксиэтоксиметиловый (MEM), 2,2,2-трихлорэтоксиметиловый, бис(2-хлорэтокси)метиловый, 2-(триметилсилил)этоксиметиловый (SEMOR), тетрагидропираниловый (THP), аллиловый, 3-бромтетрагидропираниловый, тетрагидротиопираниловый, 1-метоксициклогексиловый, бензилокси-2-фторэтиловый, 2,2,2-трихлорэтиловый, 2-триметилсилилэтиловый, 2-(фенилселенил)этиловый, т-бутиловый, аллиловый, п-хлорфениловый, п-метоксифениловый, 2,4-динитрофениловый, бензиловый, п-метоксибензиловый, 3,4-диметоксибензиловый, о-нитробензиловый, п-нитробензиловый, п-галобензиловый, 2,6-дихлорбензиловый, триметилсилиловый (TMS), триэтилсилиловый (TES), триизопропилсилиловый (TIPS), т-бутилдиметилсилиловый (TBDMS), т-бутилдифенилсилиловый (TBDPS), трибензилсилиловый, сложные эфиры, такие как формиат, бензилформиат, ацетат, хлорацетат, дихлорацетат, трихлорацетат, трифторацетат, метоксиацетат, трифенилметоксиацетат, феноксиацетат, п-хлорфеноксиацетат, 3-фенилпропионат, 4-оксопентонат (левулинат), 4,4-(этилендитио)пентонат (левулиноилдитиоацетат), пивалат, адамантоат, кротонат, 4-метоксикронат, бензоат, п-фенилбензоат, 2,4,6-триметилбензоат (мезитоат), и карбонаты, такие как алкилметилкарбонат, 9-фторэтилметилкарбонат (Fmoc), алкилэтилкарбонат, алкил-2,2,2-трихлорэтилкарбонат (Troc), 2-(триметилсилил)этилкарбонат (TMSEC), 2-(фенилсульфонил)этилкарбонат (Psec), 2-(трифенилфосфонио)этилкарбонат (Peoc), алкилизобутилкарбонат. В одном варианте осуществления защитная группа представляет собой этоксиэтиловый эфир; в другом варианте осуществления защитная группа представляет собой аллиловый эфир.
Снятие защитных групп из защищенного линейного полиэфира P0 для получения незащищенного полимера Pd производится способами, определяемыми выбором защитной группы P; такие способы известны специалистам. В одном варианте осуществления основная гидроксильная группа циклического эфирного мономера защищена как 1-этоксиэтиловый эфир; расщепление этой защитной группы для получения незащищенного полимера производится в водной кислой среде, такой как водный раствор уксусной кислоты, водный раствор соляной кислоты или кислая ионообменная смола. В другом варианте осуществления основная гидроксильная группа циклического эфирного мономера защищена как аллиловый эфир; расщепление этой защитной группы для получения незащищенного полимера производится изомеризацией аллилового эфира до винилового эфира путем его обработки алкоголятом калия с последующей обработкой водным раствором кислоты, изомеризацией с использованием катализаторов на основе переходных металлов с последующим кислотным гидролизом, или прямым удалением с применением катализаторов на основе палладия (0) и нуклеофильного акцептора.
Анионная полимеризация с раскрытием цикла мономера M, показанная в ФОРМУЛЕ VI, инициируется алкоксидной солью I. Примеры алкоголятов, которые могут использоваться для инициации полимеризации с раскрытием цикла циклических эфирных мономеров, без ограничений включают калиевые соли линейных углеводородных спиртов C3-C30, метиловый эфир полиэтиленгликоля и полисилоксаны с карбинольными концевыми группами. В одном варианте осуществления катализатором анионной полимеризации с раскрытием цикла является калиевая соль октадеканола. В другом варианте осуществления настоящего изобретения используются многофункциональные инициаторы, без ограничений включающие полиоксиалкилены, такие как полиэтиленгликоль, полипропиленгликоль или поли(тетраметиленовый эфир)гликоль; сложные полиэфиры, такие как поли(этиленадипат), поли(этиленсукцинат); сополимеры, имеющие в основной цепи и оксиалкиленовые, и сложноэфирные группы, такие как поли[ди(этиленгликоль)адипат]; и низкомолекулярные спирты, такие как 1,4-бутандиол, 1,6-гександиол или неопентилгликоль.
В зависимости от имеющихся на полиэфире боковых функциональных групп, хромофоры можно ковалентно присоединить к основной цепи полимера с использованием различных способов, известных специалистам. Следующие способы приведены в целях иллюстрации и не представляют собой исчерпывающий список возможных способов присоединения поглощающего УФ-излучения хромофора к основной цепи полимера. В случае полимеров со свободными гидроксильными группами (как показано структурой Pd в ФОРМУЛЕ VI) к полимеру можно различными известными специалистам способами присоединить УФ-поглощающий хромофор, содержащий карбоксилатную группу. Для образования ковалентных связей между поглощающими УФ-излучение хромофорами с карбоксильными группами и гидроксильными группами полимеров можно использовать агенты реакции конденсации, получая сложноэфирные связи. В одном варианте осуществления агентом реакции конденсации является N-(3-диметиламинопропил)-N′-этилкарбодиимида гидрохлорид. Карбоксильную группу УФ-поглощающего хромофора также можно присоединить к гидроксильным группам полимера эфирными связями, используя катализ переходными металлами; в одном варианте осуществления катализатором является этилгексаноат олова (II). УФ-поглощающий хромофор также можно присоединить к полимеру путем преобразования карбоксильной группы УФ-поглощающего хромофора в соответствующий хлорангидрид; хлорангидрид вступает в реакцию с гидроксильными группами функционального полимера, образуя эфирные связи. В одном варианте осуществления, такое превращение в хлорангидрид проводится с использованием тионилхлорида. Карбоксильную группу УФ-поглощающего хромофора также можно преобразовать в изоцианат путем перегруппировки Курциуса промежуточного ацилазида; изоцианат хромофора вступает в реакцию с гидроксильными группами функционального полимера, образуя уретановые связи. В другом варианте осуществления карбоксильную группу УФ-поглощающего хромофора можно преобразовать в эфир и присоединить к гидроксильной группе основной цепи путем переэтерификации. Это достигается превращением карбоновой кислоты в эфир в присутствии низкокипящего спирта, такого как метанол; переэтерификацию проводят в реакции эфира хромофора с полимером, содержащим боковые гидроксильные группы, в присутствии кислого катализатора, например, пара-толуолсульфокислоты.
Кроме того, в случае полиэфиров со свободными гидроксильными группами к полиэфиру может быть ковалентно присоединен УФ-поглощающий хромофор, содержащий гидроксильную группу, с применением различных известных специалистам способов. В одном варианте осуществления гидроксильную группу УФ-поглощающего хромофора можно активировать для нуклеофильного замещения с применением таких агентов, как метансульфонилхлорид или п-толуолсульфонилхлорид; гидроксильные группы основной цепи тогда становятся способными вытеснить образующийся мезилат или тозилат при основных условиях для образования эфирных связей между полимером и УФ-поглощающим хромофором. В другом варианте осуществления гидроксильную группу УФ-поглощающего хромофора можно преобразовать в хлорформиат с использованием такого агента, как фосген, дифосген или трифосген; образующийся хлорформиат УФ-поглощающего хромофора может реагировать с гидроксильными группами основной цепи полимера, образуя карбонатную связь между полимером и УФ-поглощающим хромофором.
В случае полимеров со свободными гидроксильными группами (как показано структурой Pd ФОРМУЛЫ VI) к полимеру может быть ковалентно присоединен УФ-поглощающий хромофор, содержащий аминогруппу, с применением различных известных специалистам способов. В одном варианте осуществления гидроксильные группы полимера можно преобразовать в соответствующий хлорформиат с использованием такого агента, как фосген, дифосген или трифосген; затем функционализированный аминогруппой УФ-поглощающий хромофор может прореагировать с хлорформиатами полимера, образуя карбаматную связь между УФ-поглощающим хромофором и полиэфиром.
В другом варианте осуществления некоторые из гидроксильных групп линейной основной цепи УФ-поглощающего полиэфира сохраняются после присоединения УФ-поглощающих хромофоров с карбоксильными, хлорангидридными и изоцианатными функциональными группами. Эти непрореагировавшие гидроксильные группы можно использовать для присоединения других монофункциональных боковых групп для улучшения физических и химических свойств полимера. Примеры реакционноспособных в отношении гидроксила функциональных групп без ограничений включают хлорангидриды и изоцианаты. Конкретные примеры реакционноспособных в отношении гидроксила функциональных боковых групп включают пальмитоилхлорид и стеарилизоцианат. Другие примеры групп, которые могут ответвляться от полимера и представлять собой места для ковалентного присоединения УФ-поглощающих хромофоров, без ограничений включают сопряженные алкены, амины и карбоновые кислоты.
В другом варианте осуществления основная цепь полиэфира является полиглицерином с боковыми гидроксильными или гидрофобными группами, такими как сложный полиглицериловый эфир, например, декаглицерилмоностеарат, доступный в продаже под торговой маркой POLYALDO 10-1-S производства компании Lonza, г. Аллендейл, штат Нью-Джерси, или тетрадекаглицерил, доступный в продаже под торговой маркой POLYALDO 14-1-S производства компании Lonza, г. Аллендейл, штат Нью-Джерси. Боковые гидроксильные группы можно вводить в реакцию с УФ-поглощающим хромофором, содержащим комплементарную функциональную группу, как описано выше, с образованием УФ-поглощающего полиэфира. В данном варианте осуществления полимерная композиция будет, например, продуктом реакции сложного полиглицеринового эфира и УФ-поглощающего хромофора, имеющего соответствующую функциональную группу для ковалентного присоединения к указанному сложному полиглицериновому эфиру. Соответствующие функциональные группы УФ-поглощающего хромофора, наряду с другими функциональными группами, описанными ранее, включают карбоксилаты и изоцианаты. Полученная полимерная композиция может включать линейный УФ-поглощающий полиэфир, содержащий повторяющееся звено, показанное в ФОРМУЛЕ IIB. Полученная полимерная композиция может дополнительно включать некоторое количество нелинейных (например, циклических) компонентов, в зависимости от процентного содержания линейного материала в полиглицерине.
Как описано выше, синтез соответствующих целям настоящего изобретения композиций, содержащих УФ-поглощающие полиэфиры, также можно вести путем полимеризации УФ-поглощающих хромофоров, ковалентно модифицированных циклическими эфирными группами (прямая полимеризация). Это показано в ФОРМУЛЕ VII, где Y представляет собой УФ-поглощающий хромофор, а o является характеристикой размера цикла циклического эфирного мономера:
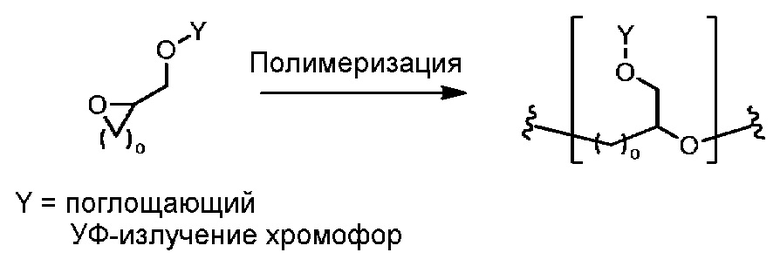
ФОРМУЛА VII. ПРЯМАЯ ПОЛИМЕРИЗАЦИЯ УФ-ПОГЛОЩАЮЩЕГО ХРОМОФОРА, КОВАЛЕНТНО ПРИСОЕДИНЕННОГО К ЦИКЛИЧЕСКОМУ ЭФИРУ
Полимерные композиции, описанные в настоящей заявке, можно использовать в приложениях, требующих поглощения УФ-излучения. Например, полимерную композицию можно использовать для комбинирования с соответствующим косметически приемлемым носителем для косметических применений или для комбинирования полимерной композиции с другими материалами для снижения степени деградации материалов под действием УФ излучения (т.е. смешиванием в расплаве материала и поглощающего УФ излучение полимера или покрытием материала слоем УФ-поглощающего полимера). Включение УФ-поглощающих полиэфиров в такие композиции настоящего изобретения может обеспечивать повышение SPF (преимущественно поглощение в диапазоне UVB), повышение PFA (преимущественно поглощение в диапазоне UVA) или повышение обоих факторов. Косметически приемлемый носитель для местного применения допускает местное нанесение на кожу человека и может включать, например, один или более носитель, такой как вода, этанол, изопропанол, смягчающие средства, увлажняющие средства и/или один или более из ПАВ/эмульгаторов, отдушек, консервантов, водоотталкивающих полимеров и подобных компонентов, часто применяемых в составах косметических средств. Так, используя известные специалистам компоненты, полимерную композицию можно приготовить в виде спрея, лосьона, геля, карандаша или других форм. Аналогичным образом, согласно некоторым вариантам осуществления, кожу человека можно защитить от ультрафиолетового излучения местным применением композиции с полимерной композицией, содержащей УФ-поглощающий полиэфир.
Согласно некоторым вариантам осуществления, солнцезащитный агент, содержащийся в композициях для местного применения настоящего изобретения, может включать или по существу состоять из УФ-поглощающего полиэфира, как описано в настоящем документе. Согласно некоторым другим вариантам осуществления солнцезащитный агент может включать дополнительные УФ-поглощающие полимеры, отличные от УФ-поглощающих полиэфиров, описанных в настоящем документе, и/или не УФ-поглощающие светорассеивающие частицы. Дополнительные УФ-поглощающие полимеры представляют собой молекулы, которые могут быть представлены как содержащие одну или более периодически повторяющуюся, например, по меньшей мере дважды, структурную единицу, с образованием молекулы, и могут представлять собой УФ-поглощающие полиэфиры, отличные от тех, которые определены и приводятся в настоящем описании. В некоторых вариантах осуществления композиции могут по существу не содержать УФ-поглощающих полимеров, отличные от УФ-поглощающих полиэфиров. В ряде других вариантов осуществления композиции могут по существу не содержать УФ-поглощающих полимеров, кроме УФ-поглощающих полиэфиров и неполимерных УФ-поглощающих солнцезащитных агентов (как описано ниже).
Дополнительные УФ-поглощающие полимеры могут иметь молекулярную массу более чем приблизительно 1500. Примеры соответствующих целям настоящего изобретения УФ-поглощающих полимеров включают бензилиденмалонатсиликон, в том числе описанный в патенте США №6193959, выданный Bernasconi et al. Особенно подходящий бензилиденмалонат включает Parsol SLX, серийно выпускаемый компанией DSM (Royal DSM N.V.), г. Херлен, Нидерланды. Другие подходящие дополнительные УФ-поглощающие полимеры раскрываются в US 6962692; US 6899866; и/или US 6800274; включая полимер гександикислоты с 2,2-диметил-1,3-пропандиолом, 3-[(2-циано-1-оксо-3,3-дифенил-2-пропенил)окси]-2,2-диметилпропил-2-октилдодециловым сложным эфиром, который продается под торговой маркой POLYCRYLENE, серийно выпускаемой компанией HallStar Company, г. Чикаго, штат Иллинойс. При использовании такие дополнительные УФ-поглощающие полимеры можно применять в концентрациях приблизительно 1% или более, например приблизительно 3% или более.
Не УФ-поглощающие светорассеивающие частицы не поглощают в УФ-спектре, но могут повышать SPF за счет рассеивания падающего УФ-излучения. Примеры не УФ-поглощающих светорассеивающих частиц включают твердые частицы с размерами, например средним диаметром, от приблизительно 0,1 микрона до приблизительно 10 микрон. В некоторых вариантах осуществления не УФ-поглощающая светорассеивающая частица представляет собой пустотелую частицу, содержащую или по существу состоящую из органического полимера или стекла. Соответствующие органические полимеры включают акриловые полимеры, в том числе акриловые/стирольные сополимеры, например, известные под названием SUNSPHERES, которые серийно производятся компанией Dow Chemical, г. Мидлэнд, штат Мичиган. Соответствующие стекла включают боросиликатные стекла, например, описанные в заявке на патент США № 20050036961A1, озаглавленной «УФ-СОЛНЦЕЗАЩИТНЫЕ СРЕДСТВА С УЛУЧШЕННЫМИ ЭСТЕТИЧЕСКИМИ ХАРАКТЕРИСТИКАМИ И ХАРАКТЕРИСТИКАМИ SPF, СОДЕРЖАЩИЕ СТЕКЛЯННЫЕ МИКРОСФЕРЫ».
КОМПОЗИЦИЯ ДЛЯ МЕСТНОГО ПРИМЕНЕНИЯ
В одном варианте осуществления представлена композиция для местного/косметического применения для нанесения на поверхности тела человека, например, кератинизированные поверхности, например, кожу, волосы, губы или ногти, и, в частности, на кожу. Композиция включает полимерную композицию, содержащую один или более линейных УФ-поглощающих полиэфиров, которые содержат химически связанный УФ-поглощающий хромофор.
Как обсуждалось выше, концентрация поглощающего ультрафиолетовое излучение полиэфира в составе композиции для местного применения может быть достаточной для обеспечения SPF приблизительно 10 или выше при отсутствии или по существу отсутствии дополнительных УФ-поглощающих полимеров или неполимерных УФ-поглощающих солнцезащитных агентов, как описано в настоящем документе. Соответственно, концентрация поглощающего ультрафиолетовое излучение полиэфира может меняться от приблизительно 5% до приблизительно 50%, например, от приблизительно 7% до приблизительно 40%, например, от приблизительно 10% до приблизительно 25% от состава композиции. В некоторых вариантах осуществления концентрация УФ-поглощающего полиэфира составляет приблизительно 10% или более, например, приблизительно 15% или более, например, приблизительно 25% или более от состава композиции. В соответствии с некоторыми вариантами осуществления, в которых солнцезащитный агент по существу состоит из УФ-поглощающего полиэфира, концентрация УФ-поглощающего полиэфира может составлять приблизительно 15% или более.
Концентрация не УФ-поглощающих светорассеивающих частиц, если они присутствуют в составе композиции, может быть приблизительно 1% или более, например, от приблизительно 1% до приблизительно 10%, например, от приблизительно 2% до приблизительно 5%. В некоторых вариантах осуществления, в которых УФ-солнцезащитный агент дополнительно включает не УФ-поглощающий солнцезащитный агент в количествах, описанных выше, композиция настоящего изобретения может иметь SPF приблизительно 20 или более.
Композиции настоящего изобретения, согласно некоторым вариантам осуществления, могут по существу не содержать неполимерных УФ-поглощающих солнцезащитных агентов. Формулировка «могут по существу не содержать неполимерных УФ-поглощающих солнцезащитных агентов» означает, что в настоящем варианте осуществления композиции не содержат неполимерных УФ-поглощающих солнцезащитных агентов в количестве, эффективном для обеспечения композиций с SPF более 2, в отсутствие УФ-поглощающих полиэфиров, что определялось посредством способа in vitro, описанного ниже в настоящем документе. Например, композиции настоящего изобретения будут содержать приблизительно 1% или менее, или приблизительно 0,5% или менее таких неполимерных УФ-поглощающих солнцезащитных агентов. Один из примеров неполимерных УФ-поглощающих солнцезащитных агентов, которых композиция может по существу не содержать, как правило, можно характеризовать как «органическое соединение» (включающее в основном или исключительно атомы, которые выбирают из углерода, водорода, кислорода и азота), не имеющее определенных повторяющихся звеньев и, как правило, с молекулярной массой приблизительно 600 дальтон или менее, например, приблизительно 500 дальтон или менее, например, менее 400 дальтон. Примеры таких соединений, которые иногда называются «мономерными органическими поглотителями УФ-излучения», без ограничений включают: производные метоксициннамата, например, октилметоксициннамат и изоамилметоксициннамат; производные камфоры, например 4-метилбензилиденкамфора, бензалконий-метосульфаткамфора и терефталилиден-дикамфорсульфоновая кислота; производные салицилата, например, октилсалицилат, троламинсалицилат и гомосалат; производные сульфоновой кислоты, например, фенилбензилимидазолсульфоновая кислота; производные бензона, например, диоксибензон, сулизобензон и оксибензон; производные бензойной кислоты, например, аминобензойная кислота и октилдиметил-п-аминобензойная кислота; октокрилен и другие β,β-дифенилакрилаты; диоктилбутамидотриазон; октилтриазон; бутилметоксидибензоилметан; дрометризолтрисилоксан; и ментилантранилат.
Другие неполимерные УФ-поглощающие солнцезащитные агенты, которых композиция может по существу не содержать, могут включать поглощающие ультрафиолет частицы, например, некоторые неорганические оксиды, в том числе двуокись титана, оксид цинка и некоторые другие оксиды переходных металлов. Такие экранирующие ультрафиолетовое излучение частицы, обычно представляют собой твердые частицы, имеющие диаметр от приблизительно 0,1 микрона до приблизительно 10 микрон.
Композиции настоящего изобретения можно применять для различных косметических приложений, в частности, для защиты кожи от УФ-излучения. Поэтому композиции можно применять в самых различных формах доставки. Такие формы без ограничений включают суспензии, дисперсии, растворы или покрытия на водорастворимых или не растворимых в воде субстратах (например, таких субстратах, как органические или неорганические порошки, волокна или пленки). Соответствующие формы продукции включают лосьоны, кремы, гели, карандаши, спреи, мази, муссы и компакт-пудры. Композицию можно применять в различных вариантах конечного использования, например, солнцезащитные средства для отдыха или ежедневного применения, увлажнители, косметика/макияж, очистители/тоники, средства, замедляющие старение, или их комбинации. Композиции настоящего изобретения могут быть приготовлены с применением методологии, которая хорошо известна специалисту в области приготовления косметических составов.
Композиции настоящего изобретения включают непрерывную водную фазу, в которой гомогенно распределена дисперсная масляная фаза, которая включает УФ-поглощающий полиэфир. В некоторых вариантах осуществления УФ-поглощающий полиэфир находится в масляной фазе в растворенном состоянии, а не в диспергированном или суспендированном. В свою очередь, масляную фазу можно стабилизировать в водной фазе. Таким образом, масляная фаза может присутствовать в виде отдельных капель или фрагментов, имеющих средний диаметр от приблизительно одного микрона до приблизительно 1000 микрон, например, от приблизительно 1 микрона до приблизительно 100 микрон.
Относительные концентрации водной фазы и масляной фазы могут различаться. В некоторых вариантах осуществления весовой процент водной фазы составляет от приблизительно 10% до приблизительно 90%, например, от приблизительно 40% до приблизительно 80%, например, от 50% до приблизительно 80%, причем остаток представлен масляной фазой.
Процентная доля воды, включенной в композиции, может составлять от приблизительно 20% до приблизительно 90%, например, от приблизительно 20% до приблизительно 80%, например, от приблизительно 30% до приблизительно 70%, например, от приблизительно 51% до приблизительно 80%, например, от приблизительно 51% до приблизительно 70%, например, от приблизительно 51% до приблизительно 60%.
НОСИТЕЛЬ ДЛЯ МЕСТНОГО ПРИМЕНЕНИЯ
Один или более УФ-поглощающий полимер в композиции можно комбинировать с «косметически приемлемым носителем для местного применения», т.е. носителем для местного применения, который способен диспергировать или растворять другие компоненты, а также имеет приемлемые свойства, делающие его безопасным для местного применения. В связи с этим композиция может дополнительно включать любые различные функциональные компоненты, известные специалистам в данной области косметической химии, например смягчающие средства (в том числе масла и воски), а также другие компоненты, которые широко используются в композициях для личной гигиены, например, среди прочих функциональных компонентов, увлажнители, загустители, замутнители, отдушки, красители, растворители для УФ-поглощающего полиэфира. Соответствующие примеры растворителей для УФ-поглощающего полиэфира включают дикаприлилкарбонат, продаваемый под маркой CETIOL CC компанией Cognis Corporation, г. Эмблер, штат Пенсильвания. Для достижения привлекательных эстетических характеристик в некоторых вариантах осуществления композиция по существу не содержит летучих растворителей, в частности, спиртов C1-C4, например, этанола и изопропанола.
Кроме того, композиция может по существу не содержать компонентов, которые будут приводить к невозможности ее местного применения. Поэтому композиция может по существу не содержать растворителей, например, летучих растворителей, и в частности не содержать летучих органических растворителей, например, кетонов, ксилола, толуола и т.п.
ЭМУЛЬГАТОРЫ
Изобретатели неожиданно обнаружили, что можно изготавливать мягкие солнцезащитные средства с защитой от УФ-излучения, по существу не содержащие неполимерных УФ-поглощающих солнцезащитных агентов, путем создания эмульсии типа «масло в воде», содержащей полимерную композицию, содержащую УФ-поглощающий полиэфир и определенные эмульгаторы в определенном соотношении. В связи с этим композиции настоящего изобретения включают один или более эмульгаторов для эмульсий типа «масло в воде». Под «эмульгатором для эмульсий типа «масло в воде» понимается любая из множества молекул, обеспечивающих эмульгирование отдельных капель масляной фазы в непрерывной водной фазе. Под «низкомолекулярными эмульгаторами» понимаются эмульгаторы, имеющие молекулярную массу приблизительно 2000 дальтон или менее, например, приблизительно 1000 дальтон или менее. Эмульгаторы для эмульсий типа «масло в воде» могут быть способны к снижению поверхностного натяжения чистой деионизированной воды до 45 дин на сантиметр в случае добавления к чистой деионизированной воде в концентрации эмульгатора для эмульсий типа «масло в воде» 0,5% или менее при комнатной температуре. Эмульгаторы для эмульсий типа «масло в воде» иногда характеризуют как вещества, имеющие гидрофильно-липофильный баланс (HLB) приблизительно 8 или более, например, приблизительно 10 или более.
Композиция включает один или более анионных эмульгаторов для эмульсий типа «масло в воде». К примерам соответствующих целям настоящего изобретения химических классов анионных эмульгаторов относятся алкил-, арил-, алкиларил- или ацилмодифицированные производные следующих фрагментов: сульфаты, эфирсульфаты, моноглицерилэфирсульфаты, сульфонаты, сульфосукцинаты, эфирсульфосукцинаты, сульфосукцинаматы, амидосульфосукцинаты, карбоксилаты, амидоэфиркарбоксилаты, сукцинаты, саркозинаты, аминокислоты, таураты, сульфоацетаты и фосфаты. К заслуживающим особого внимания анионным эмульгаторам относятся фосфатэфиры, такие как цетилфосфатные соли, например, цетилфосфат калия. В некоторых вариантах осуществления концентрация одного или нескольких анионных эмульгаторов для эмульсий типа «масло в воде» составляет от приблизительно 1% до приблизительно 10%, например, от приблизительно 2% до приблизительно 8%, например, от приблизительно 3% до приблизительно 8%, например, от приблизительно 4,5% до приблизительно 8%.
Композиция также включает неионный коэмульгатор, содержащий спиртовую функциональную группу. Концентрация неионного коэмульгатора, содержащего спиртовую функциональную группу, может находиться в диапазоне от приблизительно 0,25% до приблизительно 10%, например, от приблизительно 0,5% до приблизительно 8%, например, от приблизительно 1% до приблизительно 8%. Концентрация анионных эмульгаторов и неионного коэмульгатора может соответствовать весовому соотношению анионных эмульгаторов к неионному коэмульгатору, составляющему приблизительно 12 или менее, например от приблизительно 0,25 до приблизительно 12, например, от приблизительно 0,5 до приблизительно 12, например, от приблизительно 1 до приблизительно 12.
Примерами соответствующих целям настоящего изобретения химических классов неионных эмульгаторов, содержащих спиртовую функциональную группу, являются жирные спирты, такие как различные насыщенные или ненасыщенные, линейные или разветвленные, C7-C22 неэтоксилированные, алифатические спирты, такие как спирты, содержащие одну группу -OH. Жирный спирт может быть получен из растительных или животных жиров, содержащих по меньшей мере одну боковую цепь, содержащую углеводород. Жирный спирт может иметь от 14 до приблизительно 22 атомов углерода, например, от приблизительно 16 до приблизительно 18 атомов углерода. Примеры неразветвленных жирных спиртов включают цетиловый спирт и стеариловый спирт. Соответствующие разветвленные жирные спирты могут содержать одно или более разветвлений в основной углеродной цепи молекулы. Примером соответствующего разветвленного жирного спирта является изостеариловый спирт. Другие соответствующие разветвленные жирные спирты включают жирные спирты с одним разветвлением, например, ISALCHEM 123 компании Sasol Chemical Co, г. Бад-Хомбург, Германия.
В некоторых вариантах осуществления анионный эмульгатор для эмульсий типа «масло в воде» и неионные эмульгаторы, содержащие спиртовую функциональную группу, имеют близкую длину углеродной цепи. Например, разница в длине углеродной цепи между анионным эмульгатором для эмульсий типа «масло в воде» и неионным эмульгатором может составлять 2 или менее. В некоторых вариантах осуществления длины углеродной цепи могут быть одинаковыми.
В некоторых вариантах осуществления, в дополнение к эмульгатору (эмульгаторам), описанным выше, композиция включает амфотерный эмульгатор и/или полимерный эмульгатор. Примерами соответствующих целям настоящего изобретения химических классов амфотерных эмульгаторов являются алкилбетаины, амидоалкилбетаины, алкиламфоацетаты; амидоалкилсультаины; амфофосфаты; фосфорилированные имидазолины; карбоксиалкильные алкилполиамины; алкиламинодипропионаты; алкиламфоглицинаты (моно- или ди-); алкиламфопропионаты; N-алкил-β-аминопропионовые кислоты; и алкилполиаминокарбоксилаты. Примерами соответствующих целям настоящего изобретения химических классов полимерных эмульгаторов являются сополимеры на основе акриламидоалкилсульфоновой кислоты, такие как Aristoflex® AVC и Aristoflex® HMB, поставляемые на рынок компанией Clariant Corporation; и Granthix APP, поставляемый на рынок компанией Grant Industries, Inc. В некоторых вариантах осуществления композиция по существу не содержит катионных эмульгаторов, таких как алкилчетвертичные соединения, бензилчетвертичные соединения, сложноэфирные четвертичные соединения, этоксилированные четвертичные соединения и алкиламины.
Пленкообразующие полимеры
В некоторых вариантах осуществления изобретения композиции настоящего изобретения включают пленкообразующий полимер. Под «пленкообразующим полимером» подразумевается полимер, который при растворении, эмульгировании или диспергировании в одном или более разбавителях обеспечивает образование непрерывной или полунепрерывной пленки при распределении жидкой несущей среды по гладкому стеклу и испарении жидкой несущей среды. В связи с этим полимер должен высохнуть на стекле таким образом, чтобы на площади, по которой он распределен, он стал преимущественно непрерывным без формирования множества отдельных структур, подобных островкам. Как правило, толщина пленок, сформированных при нанесении композиций на кожу, в соответствии с вариантами осуществления настоящего изобретения, описанными в настоящем документе, составляет в среднем менее чем приблизительно 100 микрон, например, менее чем приблизительно 50 микрон.
В отличие от полимерных УФ-поглощающих полимеров, пленкообразующие полимеры по существу не поглощают ультрафиолетовое излучение, а следовательно, не соответствуют требованиям, предъявляемым к УФ-поглощающим полимерам. Пленкообразующие полимеры могут оказаться полезными в композициях настоящего изобретения в связи с тем, что они могут усиливать защиту от УФ-излучения (УФ-A, УФ-B или обоих типов), которую обеспечивает композиция, и/или увеличивать водонепроницаемость либо устойчивость композиции к воздействию воды.
Соответствующие пленкообразующие полимеры включают природные полимеры, такие как полисахариды или белки, и синтетические полимеры, такие как полиэфиры, полиакрилаты, полиуретаны, виниловые полимеры, полисульфонаты, полимочевины, полиоксазолины и т.п. Конкретные примеры пленкообразующих полимеров включают, в частности, гидрогенизированный димер сополимера дилинолеила/диметилкарбоната, доступный как COSMEDIA DC от компании Cognis Corporation, г. Эмблер, штат Пенсильвания; сополимер винилпирролидона и длинноцепочечного а-олефина, например, доступный в продаже как GANEX V220 от компании ISP Specialty Chemicals, г. Уэйн, штат Нью-Джерси; сополимеры винилпирролидона/триконтанила, доступные как GANEX WP660, также от компании ISP; диспергируемые в воде сложные полиэфиры, включая такие сульфополиэфиры, как поставляемый на рынок компанией Eastman Chemical EASTMAN AQ 38S. Количество пленкообразующего полимера, присутствующего в композиции, может составлять от приблизительно 0,1% до приблизительно 5%, от приблизительно 0,1% до приблизительно 3% или от приблизительно 0,1% до приблизительно 2%.
В некоторых вариантах осуществления композиция включает умягчитель, используемый для предотвращения или уменьшения сухости кожи, а также для защиты кожи, а также для солюбилизации УФ-поглощающего полиэфира. Соответствующими целям настоящего изобретения умягчителями являются минеральные масла, вазелин, растительные масла (например, триглицериды, такие как каприловый/каприновый триглицерид), воски и другие смеси жирных эфиров, без ограничений включая эфиры глицерина (например, изопропилпальмитат, изопропилмиристат) и силиконовые масла, такие как диметикон. В некоторых вариантах осуществления для солюбилизации УФ-поглощающего полиэфира можно использовать смеси триглицеридов (например, каприловых/каприновых триглицеридов) и эфиров гликолей (например, изопропилмиристат).
В некоторых вариантах осуществления композиция включает пигмент, обеспечивающий придание цвета или кроющей способности. Пигмент может быть одним из пигментов, допустимых для использования в окрашенных косметических продуктах, включая композиции для нанесения на волосы, ногти и/или кожу, особенно кожу лица. Композиции для декоративной косметики без ограничений включают тональные основы, маскирующие средства, основы под макияж, румяна, тушь для ресниц, тени для век, подводку для глаз, губную помаду, лак для ногтей и тональные увлажняющие средства.
Пигмент, обеспечивающий придание цвета или кроющей способности, может содержать оксиды железа, включая красные и желтые оксиды железа, диоксид титана, ультрамарин и красители на основе хрома или гидроксида хрома, а также смеси перечисленных веществ. Пигмент может быть красочным пигментом, например, органическим красителем, таким как азокраситель, индигоидные красители, трифенилметановые, антрахиноновые и ксантиновые красители, которые обозначаются как D&C и FD&C синие, коричневые, зеленые, оранжевые, красные, желтые и т.п., осажденные на инертных связующих веществах, таких как нерастворимые соли. Примеры красочных пигментов включают Red №6, Red №7, Yellow №5 и Blue №1. Пигмент может быть интерферирующим пигментом. Примеры интерферирующих пигментов включают пигменты, содержащие слюдяные подложки, подложки на основе оксихлорида висмута, а также подложки из кремнезема, например, пигменты на основе слюды/оксихлорида висмута/оксида железа, доступные в продаже пигменты CHROMALITE (BASF), пигменты на основе диоксида титана и/или оксидов железа, нанесенных на слюду, такие как доступные в продаже пигменты FLAMENCO (BASF), пигменты на основе слюды/диоксида титана/оксида железа, включая доступные в продаже пигменты KTZ (Kobo products), перламутровые пигменты CELLINI (BASF) и боросиликатсодержащие пигменты, такие как пигменты REFLECKS (BASF).
Композиции настоящего изобретения могут дополнительно содержать один или более косметически активных агентов. «Косметически активный агент» представляет собой соединение, которое оказывает косметическое или терапевтическое воздействие на кожу, например, агенты для сокращения морщин, лечения угревой сыпи или осветления кожи. Косметически активный агент, как правило, будет присутствовать в композиции настоящего изобретения в количестве от приблизительно 0,001% до приблизительно 20% вес. композиции, например, от приблизительно 0,01% до приблизительно 10%, например, от приблизительно 0,1% до приблизительно 5% вес. композиции.
В некоторых вариантах осуществления pH композиции варьируется от приблизительно 4,0 до приблизительно 8,0, например, от приблизительно 5,5 до приблизительно 7,0.
Солнцезащитный фактор (SPF) можно проверить с помощью приведенного ниже СПОСОБА ИСПЫТАНИЙ SPF IN VITRO. Измеряют исходное пропускание пластинки ПММА (подложка) без нанесения на нее каких-либо испытываемых материалов. В качестве испытываемых образцов применяют предоставленные образцы полимера. С помощью такого способа можно также тестировать смеси. Полимер (-ы) можно тестировать без каких-либо дополнительных добавок; с системой растворителей или как часть композиции для личной гигиены, которая может включать растворитель и/или дополнительные компоненты.
Каждый образец по отдельности наносят на пластинку ПММА (поставляются компанией Helioscience, г Марсель, Франция) при плотности нанесения приблизительно 32 на 25 см2 подложки, после чего оператор пальцем растирает его до однородного тонкого слоя и дает высохнуть. Образцы сушат 15 минут до начала измерений поглощения на калиброванном анализаторе УФ-пропускания Labsphere® UV-1000S или анализаторе УФ-пропускания Labsphere® UV-2000S (Labsphere, г. Норт-Саттон, штат Нью-Хэмпшир, США). Показатели поглощения использовали для вычисления индексов SPF и PFA (фактор биологической защиты на основании УФ-A).
SPF и PFA можно вычислить на основании способов, известных специалистам в данной области - см. уравнение (1) ниже для вычисления SPF:
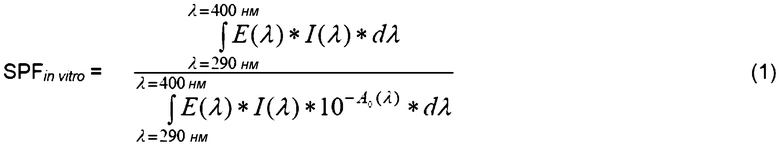 ,
,
где:
E(λ) = спектр, вызывающий покраснение кожи;
I(λ) = спектральная плотность потока излучения, поступающего от источника УФ-излучения;
A0(λ) = средняя монохроматическая поглощающая способность слоя испытываемого продукта до облучения ультрафиолетом;
dλ = шаг длины волны (1 нм).
Композиции настоящего изобретения, как правило, имеют низкую способность к раздражению кожи. Раздражение можно оценить с использованием, например, МОДИФИЦИРОВАННОГО ТЕСТА ТРАНСЭПИТЕЛИАЛЬНОЙ ПРОНИЦАЕМОСТИ (TEP), как описано ниже. Более низкое значение, полученное для композиции при проведении МОДИФИЦИРОВАННОГО ТЕСТА TEP, указывает на меньшее раздражение, связанное с композицией, в сравнении с композициями, для которых было получено большее значение при проведении МОДИФИЦИРОВАННОГО ТЕСТА TEP, указывающее на больший уровень раздражения, вызываемого такими композициями.
Заявители обнаружили, что композиции настоящего изобретения характеризуются неожиданно низкими значениями, получаемыми при проведении МОДИФИЦИРОВАННОГО ТЕСТА TEP/низким уровнем вызываемого раздражения. Например, в некоторых вариантах осуществления изобретения композиции при проведении МОДИФИЦИРОВАННОГО ТЕСТА TEP в соответствии с описанием МОДИФИЦИРОВАННОГО ТЕСТА TEP, приведенным ниже, получали оценку приблизительно 0,45 или менее. В некоторых других вариантах осуществления изобретения при проведении МОДИФИЦИРОВАННОГО ТЕСТА TEP композиции получали оценку приблизительно 0,40 или менее, например, приблизительно 0,35 или менее, например, приблизительно 0,30 или менее. В некоторых других вариантах осуществления изобретения при проведении МОДИФИЦИРОВАННОГО ТЕСТА TEP композиции получали оценку приблизительно 0,27 или менее, например, приблизительно 0,20 или менее.
Композиции настоящего изобретения могут быть получены с применением методологии смешивания и перемешивания, которые хорошо известны специалистам в данной области. В одном из вариантов осуществления настоящего изобретения способ приготовления композиции настоящего изобретения включает приготовление масляной фазы смешиванием по меньшей мере УФ-поглощающего полиэфира с необязательными маслорастворимыми или способными смешиваться с маслом компонентами; и приготовление водной фазы смешиванием воды с необязательными водорастворимыми или способными смешиваться с водой компонентами. Затем масляную фазу и водную фазу можно смешать таким образом, чтобы обеспечить гомогенную дисперсию масляной фазы в водной фазе, так что водная фаза представляет собой сплошную среду, а масляная фаза - дисперсную среду.
Композиции настоящего изобретения можно применять для местного применения у млекопитающих, например, непосредственным наложением или втиранием, или распределением композиции по поверхности кожи или волос человека.
Приведенный ниже МОДИФИЦИРОВАННЫЙ ТЕСТ TEP используют в экспресс-способах и в следующих примерах. В частности, как описано выше, МОДИФИЦИРОВАННЫЙ ТЕСТ TEP используется для того, чтобы определить, когда композиция характеризуется пониженным уровнем вызываемого раздражения в соответствии с настоящим изобретением.
МОДИФИЦИРОВАННЫЙ ТЕСТ ТРАНСЭПИТЕЛИАЛЬНОЙ ПРОНИЦАЕМОСТИ (TEP)
МОДИФИЦИРОВАННЫЙ ТЕСТ TEP предназначен для оценки способности тестируемого материала нарушать барьер проницаемости, образованный слитным монослоем клеток почек собак Мадин-Дарби (MDCK). Для оценки трансэпителиальной проницаемости, которая определяется по проникновению флуоресцеинового красителя через монослой, используют клетки MDCK, культивированные на пористых фильтрах до образования слитного слоя. Барьер проницаемости из клеток MDCK представляет собой модель самых внешних слоев эпителия роговицы, поэтому данную систему можно рассматривать как отражающую ранние изменения в развитии раздражения глаз in vivo.
Для проведения МОДИФИЦИРОВАННОГО ТЕСТА TEP желательно использовать следующее оборудование: систему транспортировки жидкостей Packard Multiprobe 104; промыватель BioTek Washer, модель № ELx405; считывающее устройство для микропланшетов BioTek Powerwave XS с фильтром 490 нм. Одноразовое лабораторное оборудование включает: 24-луночный планшет для клеточных культур с микропористой мембраной Corning Support Transwell, № по каталогу 29445-100 или 29444-580, № производителя 3397; 24-луночный планшет для тканевых культур Corning Receiver, № по каталогу 29444-100, № производителя 3527; одноразовые наконечники на 200 мкл, № по каталогу 82003-196; пипетки Eppendorf Combitips plus на 5 мл, № по каталогу 21516-152; водный раствор хлорида натрия 0,9% (вес/объем), № по каталогу RC72105; и стерильные полипропиленовые пробирки для центрифугирования объемом 15 мл. Реактивы, поставляемые компанией Life Technologies, включают: сбалансированный солевой раствор Хенкса (10x) без фенолового красного, № по каталогу 14065056, и раствор бикарбоната натрия, 7,5%, № по каталогу 25080094, минимальную эссенциальную среду (MEM) (1x), № по каталогу 11095072, фетальную бычью сыворотку HI, № по каталогу 10082147, противогрибковый антибиотик 100x, № по каталогу 15240096, L-глутамин 200 мМ (100x), № по каталогу 25030081, флуоресцеин натрия Sigma, № по каталогу F-6377, поставляется компанией Sigma/Aldrich.
Клеточную линию, ATCC CCL 34 MDCK (NBL-2) (почки: Canis familiaris), поддерживают в соответствии с рекомендациями Американской коллекции типовых культур (ATCC) (г. Манассас, штат Вирджиния). Клеточные культуры собирают путем трипсинизации и высевают в планшеты Support Transwell24, содержащие полную среду MEM, за 48 часов до проведения тестирования в концентрации 5×105 клеток на мл. Готовят реактивы: (1) буферный раствор 1X HBSS путем смешивания 200 мл сбалансированного солевого раствора Хенкса (HBSS) (10x) без фенолового красного с 9,3 мл бикарбоната натрия и доведения объема до 2000 мл дистиллированной водой. Значение pH раствора должно находиться в диапазоне 6,8-7,2, а раствор должен быть подогрет до температуры 37°C; (2) базовый раствор флуоресцеина натрия 200 мкг/мл в буферном растворе HBSS; (3) полную минимальную эссенциальную среду (MEM) готовят путем смешивания 100 мл фетальной бычьей сыворотки, 10 мл противогрибкового антибиотика 100x и 10 мл L-глутамина 200 мМ (100x) с 1000 мл MEM (1x).
Проницаемость мембраны подтверждают путем включения контроля, не содержащего клеток, который закладывают в каждый из дней, когда проводят тестирование. Тестируемые солнцезащитные композиции оценивают как концентрированные.
Вставки промывают для удаления клеточной среды. 24-луночный планшет для клеточных культур Corning, № по каталогу 29445-100, содержащий слитный монослой клеток MDCK, извлекают из инкубатора. Каждый 24-луночный планшет для клеточной культуры включает вставку, которая удерживает поверхность внутренней лунки с микропористой мембраной, где происходит рост клеток, погруженной в нижнюю лунку. Вставку, содержащую клеточные культуры, промывают 5 раз (BioTek Washer) теплым HBSS для удаления культуральной среды и сыворотки. Нижнюю часть 24-луночного планшета для клеточных культур 3 раза промывают теплым HBSS, при последней промывке в каждую нижнюю лунку помещают по 1 мл HBSS.
Для тестирования одной солнцезащитной композиции используют четыре лунки в 24-луночном планшете; таким образом, один 24-луночный планшет можно использовать для тестирования до 6 солнцезащитных композиций. Тестируемые солнцезащитные композиции добавляют непосредственно в лунку на вставке, без разбавления (100%), по 200 мкл на одну лунку на вставке. Затем 24-луночный планшет для клеточных культур возвращают в инкубатор на 1 час инкубационного периода.
После завершения первого этапа инкубации 24-луночный планшет для клеточных культур извлекают из инкубатора и промывают вручную для удаления тестируемой композиции. В каждую внутреннюю лунку добавляют приблизительно 200 мкл HBSS и оставляют приблизительно на 1 минуту. Затем производят декантирование тестируемой композиции и HBSS из отдельных лунок. Все остатки образцов удаляют путем осторожного заполнения вставок HBSS и декантирования. Когда вставка не будет содержать остатки тестируемой композиции, производят 10-кратное промывание (Bio Tek Washer) теплым HBSS. Нижние лунки промывают 3 раза теплым HBSS и при последней промывке в каждую нижнюю лунку добавляют 1 мл HBSS (принимающий буфер).
Вставку помещают обратно в нижний планшет, содержащий 1 мл HBSS (принимающий буфер), в каждую внутреннюю лунку добавляют флуоресцеин натрия, по 200 мкл на лунку, и возвращают планшет в инкубатор на 45 минут.
После 45 минут инкубации из инкубатора извлекают первый планшет, содержащий флуоресцеин натрия, затем извлекают верхнюю вставку и при помощи считывающего устройства для микропланшетов Powerwave XS определяют количество красителя, проникшего в принимающий буфер в нижней лунке. Флуоресценцию определяют спектрофотометрически на длине волны 490 нм. Данные распечатывают и регистрируют.
Затем вставку помещают в пустую, временную 24-луночную нижнюю пластину планшета в промывателе Bio Tek Washer для 10-кратной промывки HBSS. Тщательно следят за тем, чтобы флуоресцеин натрия был полностью вымыт и в верхних (внутренних) или нижних лунках не осталось флуоресцеина.
Промытую вставку помещают в чистую принимающую пластину 24-луночного планшета Corning, № по каталогу 29445-100. Как во внутренние лунки вставки, так и в нижнюю пластину планшета добавляют полную минимальную эссенциальную среду (MEM), Life Technologies, № по каталогу 11095072. В нижние лунки добавляют приблизительно 1 мл MEM, во внутренние лунки - 200 мкл. Затем в течение 3 часов проводят инкубацию 24-луночного планшета для клеточных культур.
После 3 часов инкубации 24-луночный планшет для клеточных культур извлекают из инкубатора. Вставку, содержащую клеточные культуры, промывают 5 раз (BioTek Washer) теплым HBSS для удаления культуральной среды и сыворотки. Нижнюю пластину планшета промывают 3 раза теплым HBSS и при последней промывке в каждую нижнюю лунку добавляют по 1 мл HBSS (принимающий буфер).
В каждую внутреннюю лунку вставки добавляют флуоресцеин натрия, по 200 мкл на лунку, планшет повторно собирают и возвращают в инкубатор на 45 минут.
После 45 минут инкубации из инкубатора извлекают планшет, содержащий флуоресцеин натрия, затем извлекают и убирают вставку и при помощи считывающего устройства для микропланшетов Powerwave XS определяют количество красителя, проникшего в нижнюю лунку. Флуоресценцию определяют спектрофотометрически на длине волны 490 нм. Данные распечатывают и регистрируют.
Результаты спектрофотометрических измерений (проникновение флуоресцеина) по каждой из четырех повторностей для данной тестируемой солнцезащитной композиции используют для вычисления среднего показателя проникновения флуоресцеина для тестируемой солнцезащитной композиции. Также вычисляют средний показатель проникновения флуоресцеина для четырех лунок с «контролем, не содержащим клеток». Оценку по модифицированному тесту TEP вычисляют путем деления среднего показателя проникновения флуоресцеина для тестируемой солнцезащитной композиции на аналогичный показатель для контроля, не содержащего клеток.
Дополнительные сведения о тесте TEP приведены в следующей публикации: Tchao, R. (1988 г.) Trans-epithelial Permeability of Fluorescein In Vitro as an Assay to Determine Eye Irritants. Alternative Methods in Toxicology 6, Progress in In Vitro Toxicology (под ред. A.M. Goldberg), 271.
Приведенные ниже примеры отражают принципы и практическое исполнение настоящего изобретения, которое однако ими не ограничивается. Различные дополнительные варианты осуществления в рамках объема и сущности настоящего изобретения станут очевидными для специалистов в данной области после ознакомления с этим описанием.
ПРИМЕРЫ
ПРИМЕРЫ 1-12. СИНТЕЗ И ОПРЕДЕЛЕНИЕ SPF ПОЛИМЕРНЫХ КОМПОЗИЦИЙ, СОДЕРЖАЩИХ УФ-ПОГЛОЩАЮЩИЕ ПОЛИЭФИРЫ
Пример 1. Синтез защищенной формы глицида.
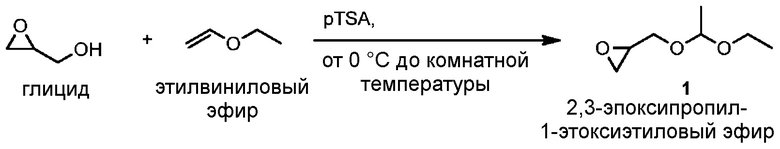
ФОРМУЛА VIII. СИНТЕЗ ЗАЩИЩЕННОГО МОНОМЕРА ЭПОКСИДА
Синтез защищенного мономера эпоксида 1 был проведен, как показано в ФОРМУЛЕ VIII, с использованием варианта процедуры, описанной в литературе (Fitton, A. et. al. Synthesis 1987 г., 1987, 1140-1142). Глицид (53 мл, 0,80 моль) и этилвиниловый эфир (230 мл, 2,40 моль; свежеперегнанный непосредственно перед реакцией) добавили в двугорлую круглодонную колбу объемом 500 мл с якорьком для магнитной мешалки. На колбу установили септу и переходник для термометра; термометр вставили в переходник и установили таким образом, что шарик термометра был погружен в жидкость. Колбу погрузили в баню с рассольным льдом; смесь перемешивали магнитной мешалкой. Когда температура внутри колбы достигла 0°C, небольшими порциями при интенсивном перемешивании добавили гидрат п-толуолсульфоновой кислоты (pTSA⋅H2O, 1,43 г, 7,5 ммоль). При добавлении каждой порции pTSA температура раствора резко повышалась; скорость добавления была достаточно низкой, чтобы не допустить повышение температуры раствора выше 20°C. Последняя порция pTSA была добавлена приблизительно через 5 часов после добавления первой порции и не вызвала экзотермического эффекта; тонкослойная хроматография реакционной смеси не выявила остаточного глицида после добавления последней порции pTSA. Реакционную смесь перенесли в делительную воронку; в воронку медленно влили насыщенный водный раствор NaHCO3 (230 мл). Смесь встряхнули, слоям дали разделиться, органический слой сняли, высушили над сульфатом натрия и профильтровали через бумагу. Раствор сконцентрировали на роторном испарителе и перегнали под вакуумом (60°C дистиллят при 1,1 килопаскаля (8 торр)), получив защищенный мономер эпоксида 1 (79,38 г) в виде бесцветного масла. ЯМР-анализ провели на спектрометре Varian Unity Inova 400 MГц (1H) при температуре 30°C; химические сдвиги приведены в миллионных долях (м.д.) по шкале δ и привязаны к пикам следового количества протонированного растворителя или тетраметилсилана. Спектры, полученные в DMSO-d6, были привязаны к (CHD2)(CD3)SO при δH 2,50. 1H ЯМР (400 MГц, CDCl3) δ м.д. 4,76 (квинт, J=5,2 Гц, 1 H); 3,81 (дд, J=11,5, 3,3 Гц, 1 H); 3,60-3,74 (м, 3 H); 3,38-3,60 (м, 4 H); 3,10-3,20 (м, 2 H); 2,81 (ддд, J=5,1, 4,0, 1,3 Гц, 2 H); 2,63 (ддд, J=14,6, 5,1, 2,7 Гц, 2 H); 1,33 (дд, J=6,2, 5,4 Гц, 6 H); 1,21 (тд, J=7,1, 1,3 Гц, 6 H).
Пример 2A. Синтез линейного полиглицерина.
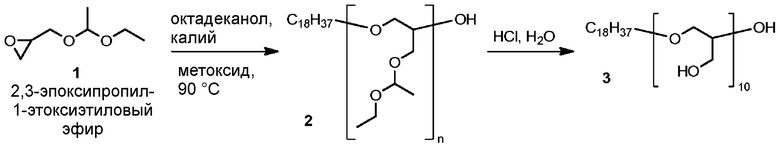
ФОРМУЛА IX. СИНТЕЗ ЛИНЕЙНОГО ПОЛИЭФИРНОГО ПОЛИМЕРА
Полимеризацию защищенного эпоксидного мономера 1 провели, как показано в ФОРМУЛЕ IX. 1-Октадеканол (27,76 г, 102,6 ммоль) добавили в высушенную в сушильном шкафу двугорлую круглодонную колбу объемом 250 мл с якорьком для магнитной мешалки. На колбу установили переходник для подачи азота и резиновую септу. Через септу шприцом в колбу добавили метилат калия (25 вес% в метаноле (MeOH); 6,06 мл, 20,52 ммоль). Круглодонную колбу погрузили в масляную баню, предварительно нагретую до 90°C. Септу прокололи иглой калибра 18 и содержимое колбы перемешивали при постоянной продувке азотом в течение 1 часа, за который спирт расплавился, а метанол испарился из колбы. Септу заменили на выравнивающую давление капельную воронку, содержащую мономер 1 (151 г, 1,04 моль). Воронку закрыли резиновой септой. Мономер 1 добавляли по каплям в перемешиваемую смесь; реакционную смесь перемешивали при температуре 90°C в течение 15 часов. При охлаждении получили сырой полиэфир 2 в виде бледно-коричневого слегка вязкого масла, которое использовали в последующих реакциях без дальнейшей очистки. 1H ЯМР(400 MГц, ХЛОРОФОРМ-d) δ м.д. 4,48-4,80 (м, 10 H); 3,25-3,97 (м, 70 H); 1,41-1,64 (м, 2 H); 1,23-1,40 (м, 60 H); 1,09-1,23 (м, 30 H); 0,88 (т, J=7,0 Гц, 3 H).
Для определения молекулярной массы провели гель-проникающую хроматографию при температуре 35°C при помощи аппарата Waters Alliance 2695 Separations Module (Waters, г. Миллфорд, штат Массачусетс) при скорости потока ТГФ (стабилизированного 0,025% BHT) 0,5 мл/мин. Аппарат 2695 был оборудован двумя последовательными колоннами ГПХ (Waters Corp HR 0,5 и HR3) размером 7,8×300 мм с размером частиц 5 мкм) и рефрактометрическим детектором модели Waters 410. Молекулярные массы образцов определили сравнением с полистирольными стандартами. Стандарты подготовили навешиванием 1-2 мг каждого полистирольного (PS) полимера в 2 мл флакон с растворителем ТГФ (2 стандарта на флакон); перед проведением анализа образцы профильтровали (0,22 мкм). Полистирольные стандарты покрывали диапазон от 70000 до 600 дальтон и были изготовлены тремя поставщиками (Polymer Standards Service-USA, Phenomenex и Shodex). Полученная калибровочная кривая дала r2=0,9999. Экспериментальные образцы растворили в ТГФ в концентрации 3-5 мг/мл и профильтровали (0,22 мкм) перед анализом. ГПХ (ТГФ) для полимера 2: Mw 1724.
Сырой полиэфир 2 перенесли тетрагидрофураном (ТГФ, ~500 мл) в круглодонную колбу объемом 1 л с якорьком для магнитной мешалки. В перемешиваемую реакционную смесь стеклянной пипеткой добавили концентрированный водный раствор HCl (37%, 20 мл). Спустя 16 часов реакционную смесь сконцентрировали на роторном испарителе до состояния масла, которое разбавили метанолом до объема ~500 мл. В интенсивно перемешиваемый раствор порциями добавили твердый NaHCO3, что сопровождалось значительным газовыделением. Когда добавление NaHCO3 перестало вызывать газовыделение (общее количество добавленного NaHCO3 составило 107 г), смесь профильтровали через бумагу для удаления твердого NaHCO3. Фильтрат сконцентрировали на роторном испарителе, получив линейный полиглицерин 3 в виде коричневой пены. 1H ЯМР (400 MГц, DMSO-d6) δ м.д. 4,43 (уш. с., 11 H); 3,20-3,70 (м, 52 H); 1,38-1,55 (м, 2 H); 1,23 (с, 30 H); 0,85 (т, J=7,0 Гц, 3 H).
Пример 2B. Синтез линейного полиглицерина.
Другую партию защищенного сырого полимера 2 (260 г) и метанола (класс чистоты ACS, 1,25 л) поместили в двугорлую круглодонную колбу объемом 2 л. В колбу добавили сухую кислую ионообменную смолу в форме H+ (Dowex DR-2030, Aldrich, 446483; 100,3 г). На центральное горло колбы установили переходник для механического перемешивания и лопастную мешалку; на боковое горло колбы установили переходник для перегонки с водяным охлаждением. Реакционную колбу погрузили в масляную баню. При интенсивном механическом перемешивании реакционную смесь довели до кипения (температура масляной бани 85°C). Метанол (и метиловый эфир, образовавшийся в результате снятия защитных групп) отогнали из колбы. После сбора 750 мл метанола в реакционную смесь добавили дополнительное количество метанола (750 мл). Из колбы отогнали еще 750 мл метанола. В горячую реакционную смесь добавили обесцвечивающий уголь. Смесь быстро перемешали и профильтровали через бумагу. Фильтрат сконцентрировали на роторном испарителе. Остаточный растворитель отогнали под вакуумом, получив конечный линейный полиглицерин в виде желтоватой пены (107 г).
Пример 3A. Синтез бензотриазолкарбоксилата хромофора.
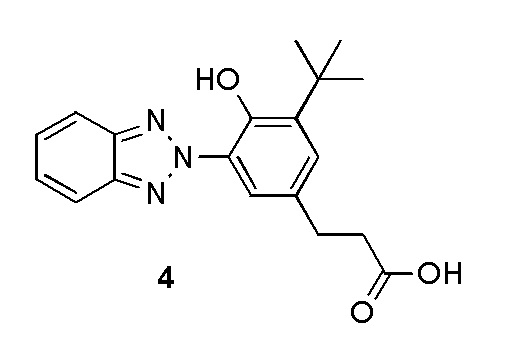
ФОРМУЛА X. БЕНЗОТРИАЗОЛКАРБОКСИЛАТ
Полиэтиленгликолевый эфир 3-[3-(2H-1,2,3-бензотриазол-2-ил)-5-трет-бутил-4-гидроксифенил]пропаноата (хромофор, который продается под торговой маркой TINUVIN 213 производства корпорации BASF, г. Виандот, штат Мичиган) (81,0 г) добавили в круглодонную колбу объемом 2 л с якорьком для магнитной мешалки. В колбу через воронку влили EtOH (600 мл), смесь размешали до гомогенного состояния. Гидроксид натрия (NaOH, 30,8 г) растворили в H2O (400 мл); щелочной раствор перенесли в капельную воронку, расположенную над 2-литровой колбой. Раствор NaOH медленно добавляли в перемешиваемую смесь; бледно-желтый мутный раствор мгновенно стал прозрачным и темно-оранжевым. После окончания добавления смесь перемешивали на протяжении ночи при комнатной температуре. Раствор сконцентрировали на роторном испарителе для удаления большей части EtOH. Полученное оранжевое масло разбавили H2O до 1400 мл. Смесь перемешивали механически и подкислили до pH~1 добавлением 1 M водн. HCl (~700 мл). Образовавшийся белый осадок профильтровали и отжали, чтобы удалить воду, а затем перекристаллизовали из EtOH. Первая партия кристаллов представляла собой длинные, тонкие бесцветные иглы. Супернатант сняли и сконцентрировали на роторном испарителе; вторую партию материала выделили в виде белого аморфного твердого вещества. Две партии объединили и высушили горячей вакуумной сушкой на протяжении ночи, получив УФ-поглощающий хромофор, содержащий карбоксилатную группу, а именно бензотриазолкарбоксилат 4, 3-(3-(2H-бензо[d][1,2,3]триазол-2-ил)-5-(трет-бутил)-4-гидроксифенил) пропановую кислоту (37,2 г), в виде белого твердого вещества; структура показана в ФОРМУЛЕ X. 1H ЯМР (400 MГц, DMSO-d6) δ м.д. 11,25 (уш. с, 1 H); 8,00-8,20 (м, 2 H); 7,95 (д, J = 2,1 Гц, 1 H); 7,50-7,67 (м, 2 H); 7,28 (д, J = 2,1 Гц, 1 H); 2,87 (т, J = 7,5 Гц, 2 H); 2,56 (т, J=7,5 Гц, 2 H); 1,45 (с, 9 H).
Пример 3B. Синтез бензотриазолкарбоксилата хромофора.
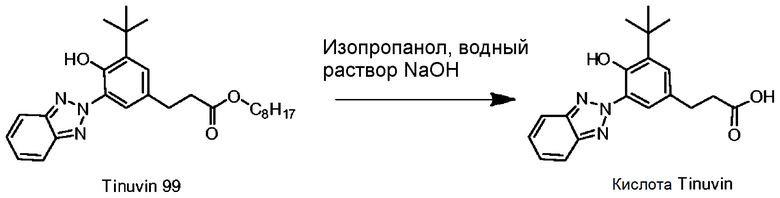
Бензолпропановую кислоту, 3-(2H-бензотриазол-2-ил)-5-(1,1-диметилэтил)-4-гидрокси-, C7-9-разветвленные и линейные алкиловые эфиры, доступные в продаже под торговой маркой TINUVIN 99 производства Корпорации BASF (120 г, 265,7 ммоль) добавили в одногорлую круглодонную колбу объемом 3 л с якорьком для магнитной мешалки. В колбу добавили изопропанол (900 мл, класс чистоты ACS), полученную смесь перемешивали до полного растворения. Гидроксид натрия (36 г, 900 ммоль) растворили в 600 мл дистиллированной воды и раствор влили в реакционную смесь. Полученную непрозрачную смесь, которая через 40 минут превратилась в прозрачный оранжевый раствор, перемешивали при комнатной температуре в течение 24 часов, а затем медленно влили в интенсивно перемешиваемую смесь изопропанола (1800 мл, класс чистоты ACS) и 1Н HCl (1200 мл), охлажденную до температуры 10-15°C. Белый осадок профильтровали, промыли 1,2 л смеси (1:1) изопропанола и 1Н HCl, суспендировали в 2 л 0,25Н HCl, перемешивали в течение 1 часа, профильтровали и высушили при температуре 90°C вакуумной горячей сушкой на протяжении ночи. Получили УФ-поглощающий хромофор, содержащий карбоксилатную группу, а именно бензотриазолкарбоксилат 4 (37,2 г), в виде бледно-желтого кристаллического вещества, 85 г, 94,5%.
Пример 4. Этерификация основной цепи полиэфира бензотриазолкарбоксилатом.
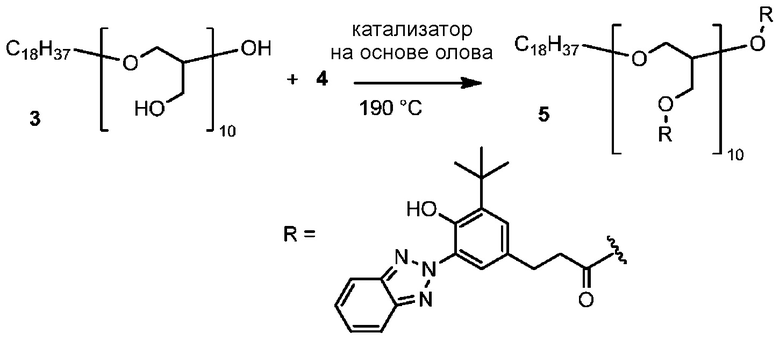
ФОРМУЛА XI. ЭТЕРИФИКАЦИЯ ПОЛИГЛИЦЕРИНА БЕНЗОТРИАЗОЛКАРБОКСИЛАТОМ
ФОРМУЛА XI иллюстрирует этерификацию полиглицерина 3 бензотриазолкарбоксилатом 4 с использованием в качестве катализатора олова. Линейный полиглицерин 3 из примера 2A (5,52 г, 60,1 миллиграмм-эквивалента гидроксила) растворили в метаноле и перелили в двугорлую круглодонную колбу объемом 500 мл. Метанол удалили на роторном испарителе; в колбу добавили бензотриазолкарбоксилат 4 (20,38 г, 60,1 ммоль) и положили якорек для магнитной мешалки. На колбу установили переходник для подачи азота и переходник для вакуумной дистилляции с приемной колбой объемом 100 мл. Колбу вакуумировали (<0,13 килопаскаля (<1 торр)) на 1 час, затем вновь заполнили газообразным азотом. Переходник подачи азота извлекли из колбы объемом 500 мл; под током азота шприцем в колбу добавили этилгексаноат олова (II) (49 мкл, 0,15 ммоль). Аппарат собрали заново и погрузили в масляную баню, предварительно нагретую до 200°C. Когда основная масса твердой фазы расплавилась, масляную баню охладили до 190°C. Реакционную смесь перемешивали при постоянной подаче азота в течение 16 часов. Поддерживая температуру и продолжая перемешивание, колбу затем вакуумировали (<0,13 килопаскаля (<1 торр)) еще на 24 часа. Затем аппарат снова наполнили газообразным азотом и охладили до комнатной температуры. Материал заморозили и разломили и растерли в порошок в ступке. Порошок растворили в минимальном количестве ТГФ. В коническую колбу налили метанол (900 мл) и поместили в нее якорек для магнитной мешалки; колбу поместили на ледяную баню. При интенсивном перемешивании в метанол добавили раствор ТГФ; полученный осадок выделили вакуумным фильтрованием. Остаточный растворитель удалили вакуумированием на протяжении ночи, получив линейный полиглицерин 5 (18,7 г) в виде серовато-белого кристаллического вещества. 1H ЯМР (400 MГц, CDCl3) δ м.д. 11,71 (уш. с, 9 H); 8,03 (уш. с, 9 H); 7,80 (уш. с, 18 H); 7,28-7,48 (м, 18 H); 7,12 (уш. с, 9 H); 5,19 (уш. с, 1 H); 3,98-4,46 (уш. м, 20 H); 3,21-3,61 (уш. м, 32 H); 2,91 (уш. с, 18 H); 2,67 (уш. с, 18 H); 1,38-1,51 (м, 85 H); 1,13-1,35 (м, 28 H); 0,87 (т, J=6,6 Гц, 3 H). ГПХ (ТГФ): Mw 3299; MN 2913.
Пример 5. Превращение бензотриазолкарбоксилата в хлорангидрид (3-(3-(2H-бензо[d][1,2,3]триазол-2-ил)-5-(трет-бутил)-4-гидроксифенил)пропаноилхлорид).
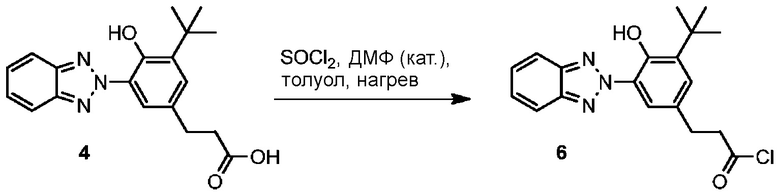
ФОРМУЛА XII. ПРЕВРАЩЕНИЕ БЕНЗОТРИАЗОЛКАРБОКСИЛАТА В БЕНЗОТРИАЗОЛХЛОРАНГИДРИД
Превращение бензотриазолкарбоновой кислоты 4 в соответствующий бензотриазолхлорангидрид 6 показано в ФОРМУЛЕ XII. Бензотриазолкарбоксилат 4 (50 г 147 ммоль, синтезированный как описано в примере 3) добавили в трехгорлую колбу объемом 1000 мл с якорьком для магнитной мешалки; на колбу установили обратный холодильник, переходник для подачи азота и резиновую септу. С помощью канюли через септу в колбу добавили безводный толуол (~500 мл), шприцем добавили в колбу тионилхлорид (16,1 мл, 221 ммоль); затем шприцем добавили в колбу диметилформамид (2,7 мл). Колбу погрузили в масляную баню при температуре 80°C; суспензию перемешали; твердые частицы стали диспергировать, в конечном счете дав прозрачный раствор. Спустя ~4 ч реакционной смеси дали остыть, перелили в круглодонную колбу и сконцентрировали на роторном испарителе. Полученное масло растерли с гексанами, получив твердое вещество бежевого цвета. Суспензию материала перекристаллизовали добавлением дополнительного количества гексанов и нагревом до кипения, фильтрованием через бумагу и медленным охлаждением до комнатной температуры при постоянном перемешивании. Полученные бежевые кристаллы профильтровали и высушили в вакууме при температуре 50°C. Фильтрат сконцентрировали и еще раз провели перекристаллизацию, получив вторую партию кристаллов; масса объединенных партий бензотриазолхлорангидрида 6 составила 44,7 г. 1H ЯМР (400 MГц, CDCl3) δ 11,88 (с, 1 H); 8,16 (д, J = 2,2 Гц, 1 H); 7,91-7,98 (м, 2 H); 7,47-7,54 (м, 2 H); 7,21 (д, J = 2,2 Гц, 1 H); 3,29 (т, J = 7,5 Гц, 2 H); 3,07 (т, J = 7,5 Гц, 2 H); 1,50-1,53 (с, 9 H).
Пример 6. Превращение бензотриазолхлорангидрида в изоцианат (2-(2H-бензо[d][1,2,3]триазол-2-ил)-6-(трет-бутил)-4-(2-изоционатоэтил)фенол).
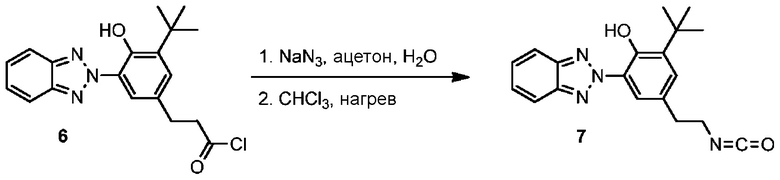
ФОРМУЛА XIII. ПРЕВРАЩЕНИЕ ХЛОРАНГИДРИДА В ИЗОЦИАНАТ
Синтез бензотриазолизоцианата 7, пригодного для присоединения к боковым функциональным группам, показан в ФОРМУЛЕ XIII. Азид натрия (NaN3, 2,5 г, 38 ммоль: ВНИМАНИЕ! NaN3 является сильным ядом) осторожно поместили в одногорлую круглодонную колбу объемом 500 мл с якорьком для магнитной мешалки. В колбу добавили дистиллированную воду (20 мл); NaN3 растворился при перемешивании, образовав прозрачный раствор. Колбу поместили на ледяную баню. Хлорангидрид 6 (7,0 г 20 ммоль) и безводный ацетон (45 мл) поместили в выравнивающую давление капельную воронку в заполненном N2 перчаточном боксе с давлением, превышающем атмосферное. Хлорангидрид растворился в ацетоне с легким бурлением, образовав прозрачный желтый раствор. Капельную воронку с бензотриазолхлорангидридом 6 установили на колбу, содержащую водный раствор NaN3; на верхнюю часть капельной воронки установили переходник для подачи N2, подключенный к вакуумному газовому коллектору. Раствор бензотриазолхлорангидрида 6 по каплям добавили в раствор NaN3. После добавления нескольких капель начал появляться белый осадок, взвешенный в водном растворе. Добавление бензотриазолхлорангидрида 6 завершили в течение 30 минут; перемешивание продолжили в течение 20 минут на ледяной бане. В полученную белую кашицу добавили воду (30 мл); твердые частицы собрали вакуумным фильтрованием через пористую стеклянную воронку. Белый твердый осадок перенесли в делительную воронку, в которую добавили CHCl3 (185 мл). Воронку встряхнули и дали слоям разделиться. Нижний органический слой отделили от небольшого водного слоя и высушили над Na2SO4. Раствор профильтровали; фильтрат поместили в одногорлую круглодонную колбу 500 мл с якорьком для магнитной мешалки; на колбу установили обратный холодильник с переходником для подачи азота и погрузили ее на масляную баню. Раствор медленно нагревали до кипения в течение 30 минут. Окончательная температура масляной бани составила 65°C. После того как температура масла превысила 55°C, в растворе наблюдалось газовыделение. Реакционную смесь кипятили с обратным холодильником в течение 90 мин. Затем на роторном испарителе удалили CHCl3; полученное масло кристаллизировалось при стоянии на протяжении ночи, дав бензотриазолизоцианат 7 (5,8 г) в виде сероватого кристаллического вещества. 1H ЯМР (400 MГц, CDCl3) δ 11,91 (с, 1 H); 8,18 (д, J=1,9 Гц, 1 H); 7,92-7,98 (м, 2 H); 7,47-7,53 (м, 2 H); 7,23 (д, J=2,1 Гц, 1 H); 3,59 (т, J=6,9 Гц, 2 H); 2,96 (т, J=6,9 Гц, 2 H); 1,52 (с, 9 H).
Пример 7. Связывание изоцианата с полиглицерином.
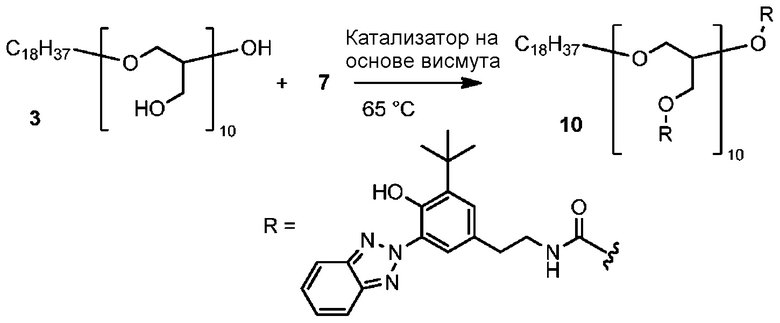
ФОРМУЛА XIV. РЕАКЦИЯ ПОЛИГЛИЦЕРИНА С ИЗОЦИАНАТОМ
Реакция линейного полиглицерина 3 с бензотриазолизоцианатом 7 показана в ФОРМУЛЕ XIV.
Раствор полиглицерина 3 в метаноле сконцентрировали на роторном испарителе; остаточный растворитель удалили в вакуумной печи на протяжении ночи при температуре 75°C. Полимер (2,22 г, 24,1 миллиграмм-эквивалент гидроксила) добавили в двугорлую круглодонную колбу объемом 100 мл с якорьком для магнитной мешалки. Изоцианат 7 (7,65 г, 22,7 ммоль), катализатор на основе висмута (25 мг; висмут-карбоксилатный комплекс, который доступен в продаже под торговой маркой BICAT 8210 производства компании Shepherd Chemical, г. Норвуд, штат Огайо) и ТГФ (17,4 мл, высушенный на молекулярных ситах 3 ангстрем) добавили в колбу. Колбу поместили в разогретую до 65°C масляную баню и установили переходник для подачи газа. Реакционную смесь перемешивали в течение 5 часов в азотной атмосфере, затем дали остыть до комнатной температуры. Для подтверждения исчезновения сильного пика изоцианата при 2250 см-1 использовали Фурье-ИК спектроскопию. Реакционную смесь влили в 160 мл метанола, в результате чего образовался коричневый осадок. Метанол слили, продукт реакции промыли в колбе метанолом (2×75 мл). Остаточный растворитель удалили в вакуумной печи на протяжении ночи при 60°C; материал растерли в мелкий порошок.
Пример 8. Синтез эпоксидного хромофора для способа прямой полимеризации.
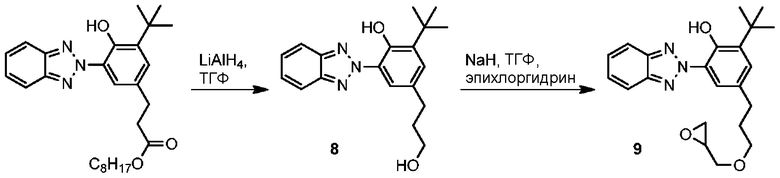
ФОРМУЛА XV. СИНТЕЗ МОНОМЕРА ЭПОКСИДНОГО ХРОМОФОРА
Синтез эпоксидного мономера 9, несущего бензотриазольный хромофор, показан в ФОРМУЛЕ XV. Раствор лития алюмогидрида (LAH) в ТГФ (1 M, 250 мл) с помощью канюли перенесли в азотной атмосфере в высушенную в печи двугорлую круглодонную колбу объемом 500 мл с якорьком для магнитной мешалки, на которую установили резиновую септу и выравнивающую давление капельную воронку. Реакционную колбу погрузили на ледяную баню; начали перемешивание. Бензолпропановую кислоту, 3-(2H-бензотриазол-2-ил)-5-(1,1-диметилэтил)-4-гидрокси, C7-C9 разветвленный и линейный алкил эфир, содержащий 5 вес. % 1-метокси-2-пропилацетата (50,06 г; бензотриазольный УФ-поглощающий продукт, который доступен в продаже под торговой маркой TINUVIN 99-2 производства корпорации BASF, г. Виандот, штат Мичиган) поместили в капельную воронку и растворили в безводном ТГФ (30 мл). Раствор ТГФ, содержащий бензотриазол, добавляли по каплям в раствор, содержащий LAH, что привело к слабому вспениванию. После того как добавление было завершено, в реакционную колбу с помощью канюли добавили дополнительное количество раствора LAH (100 мл). Реакционной смеси дали прогреться до комнатной температуры при перемешивании. Спустя 2 часа реакционную смесь перелили в коническую колбу объемом 1 л, которую поместили на ледяную баню. Раствор перемешивали механической мешалкой, медленно добавляя воду (~60 мл), чтобы погасить остатки LAH (ОСОБОЕ ВНИМАНИЕ: гашение LAH водой является экзотермической реакцией, высвобождающей большое количество легко воспламеняющегося газообразного H2). По завершении гашения LAH (при добавлении воды газ больше не выделялся) серую суспензию разбавили до 1 л 1 M водным раствором HCl. Полученный раствор перенесли в делительную воронку объемом 2 л и экстрагировали этилацетатом (1×400 мл, затем 2×50 мл). Комбинированные слои этилацетата промыли соляным раствором (1×400 мл), высушили над Na2SO4 и профильтровали через бумагу. Растворитель отогнали сначала на роторном испарителе, а затем вакуумной сушкой на протяжении ночи, получив бензотриазоловый спирт 8 (42,16 г) в виде бежевого кристаллического вещества с сильным неприятным запахом. 1H ЯМР (400 MГц, CDCl3) δ м.д. 11,75 (с, 1 H); 8,15 (д, J=2,1 Гц, 1 H); 7,88-7,99 (м, 2 H); 7,43-7,52 (м, 2 H); 7,22 (д, J=2,1 Гц, 1 H); 3,75 (м, 2 H); 3,62 (уш. с, 1 H); 2,77 (т, J=7,7 Гц, 2 H); 1,91-2,06 (м, 2 H); 1,52 (с, 9 H).
Гидрид натрия (6,0 г, 250 ммоль) добавили в высушенную в печи трехгорлую круглодонную колбу с якорьком для магнитной мешалки. На колбу установили выравнивающую давление капельную воронку, переходник для подачи азота и резиновую септу. В колбу с помощью канюли в атмосфере азота добавили безводный ТГФ (300 мл); затем колбу поместили на ледяную баню и начали перемешивание. В капельную воронку добавили бензотриазоловый спирт 8 (20,0 г, 61,5 ммоль) и поместили туда маленький якорек для магнитной мешалки; с помощью канюли в капельную воронку добавили ТГФ и активировали якорек для растворения спирта в ТГФ. Конечный объем раствора спирт/ТГФ составил 65 мл. Раствор добавляли по каплям в холодную перемешиваемую суспензию гидрата натрия. Холодную реакционную смесь перемешивали 1 час, затем шприцем через септу добавили эпихлоргидрин (20 мл, 256 ммоль). Капельную воронку заменили на обратный холодильник с переходником для подачи азота и круглодонную колбу погрузили на масляную баню с температурой 70°C. Смесь перемешивали 19 часов, затем смесь перенесли в делительную воронку с 1M водного раствора HCl (750 мл) и этилацетатом (500 мл). После взбалтывания водный слой удалили. Органический слой промыли водой (2×250 мл) и соляным раствором (1×250 мл), а затем высушили над Na2SO4. Раствор сконцентрировали на роторном испарителе. Сырой продукт очистили хроматографией на силикагеле (6:1 гексан/этилацетат). Фракции, содержащие требуемый продукт, объединили и сконцентрировали на роторном испарителе; остаточный растворитель удалили под вакуумом на протяжении ночи, получив эпоксидный мономер 9, несущий бензотриазольный хромофор (7,35 г), в виде бежевого кристаллического вещества. 1H ЯМР (400 MГц, CDCl3) δ м.д. 11,77 (с, 1 H); 8,14 (д, J=1,9 Гц, 1 H); 7,85-8,00 (м, 2 H); 7,41-7,53 (м, 2 H); 7,21 (д, J=1,9 Гц, 1 H); 3,74 (дд, J=11,5, 3,1 Гц, 1 H); 3,57 (ддт, J=19,8, 9,3, 6,4 Гц, 2 H); 3,43 (дд, J=11,5, 5,8 Гц, 1 H); 3,19 (ддт, J=5,8, 4,0, 2,9 Гц, 1 H); 2,82 (уш. т, J=4,7 Гц, 1 H); 2,76 (уш. т, J=7,7 Гц, 2 H); 2,64 (дд, J=5,1, 2,6 Гц, 1 H); 1,93-2,04 (м, 2 H); 1,52 (с, 9 H).
Пример 9. Этерификация чередующегося полиглицерина с бензотриазоловой кислотой.
Полиглицерин, частично этерифицированный со стеариновой кислотой (2,5 г, 19,8 миллиграмм-эквивалент гидроксила; тетрадекаглицерилмоностеарат, который доступен в продаже под торговой маркой POLYALDO 14-1-S производства компании Lonza, г. Аллендейл, штат Нью-Джерси) и бензотриазолкарбоксилат 4 (8,8 г, 23,8 ммоль) поместили в двугорлую круглодонную колбу объемом 100 мл с якорьком для магнитной мешалки. На колбу установили переходник для подачи азота и переходник для перегонки с приемной колбой объемом 100 мл. Аппарат вакуумировали, затем повторно заполнили азотом. Дистилляционную головку удалили и в реакционную колбу с помощью шприца в токе азота добавили этилгексаноат олова (II) (50 мкл). Аппарат собрали заново и трижды вакуумировали и заново наполняли азотом. Реакционную колбу погрузили на масляную баню, нагретую до 180°C, с постоянной подачей потока азота в двугорлую колбу через переходник для перегонки и с выходом из вакуумного адаптера в помещение. Реакционную смесь перемешивали 3 часа, затем охладили до комнатной температуры в токе азота, получив продукт, УФ-поглощающий полиглицерин, в виде желтого кристаллического вещества. 1H ЯМР (400 MГц, CDCl3) δ м.д. 11,81 (уш. с., 2 H); 8,15 (уш. с., 2 H); 7,75-8,02 (уш. с., 4 H); 7,34-7,58 (уш. с., 4 H); 7,21 (уш. с., 2 H); 4,93-5,32 (уш., 1 H); 3,17-4,50 (уш. м., 38 H); 2,86-3,11 (уш. м., 4 H); 2,54-2,84 (уш. м., 4 H); 2,31 (уш. с., 2 H); 1,61 (уш. с., 2 H); 1,50 (уш. с., 18 H); 1,26 (уш. с., 28 H); 0,89 (т, J=6,3 Гц, 3 H). ГПХ (ТГФ): Mw 1700; MN 950.
Пример 10. Синтез метилового эфира бензотриазоловой кислоты.
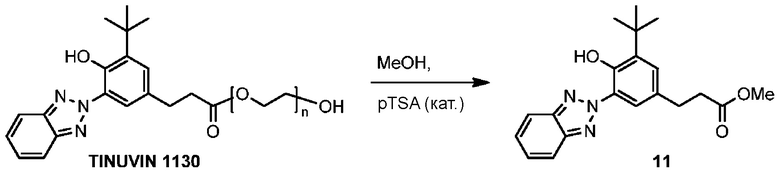
ФОРМУЛА XVI. СИНТЕЗ МЕТИЛОВОГО ЭФИРА 11
Синтез метилового эфира бензотриазольной кислоты 11, предназначенного для переэтерификации с полимером с гидроксильными функциональными группами, показан в ФОРМУЛЕ XVI. Полиэтиленгликолевый 300-эфир бета-[3-(2-H-бензотриазол-2-ил)-4-гидрокси-5-трет-бутилфенил]-пропионовой кислоты (50,1 г; УФ-поглощающий продукт, который доступен в продаже под торговой маркой TINUVIN 1130 производства корпорации BASF, г. Виандот, штат Мичиган) добавили в двугорлую круглодонную колбу объемом 1 л с якорьком для магнитной мешалки. В колбу добавили метанол (500 мл). Колбу погрузили на масляную баню; раствор перемешали. В раствор добавили pTSA⋅H2O (0,63 г). На двугорлую колбу установили обратный холодильник и резиновую септу; реакционную смесь при перемешивании довели до кипения нагреванием масляной бани; кипячение с обратным холодильником продолжали 17 часов. Затем колбу убрали с масляной бани и дали остыть до комнатной температуры, что привело к выпадению продукта в виде белого твердого вещества. Осадок отделили вакуумным фильтрованием и затем перекристаллизовали из метанола; твердое вещество отделили вакуумным фильтрованием при температуре 80°C, получив бензотриазолметиловый эфир 11 (18,27 г) в виде белого твердого вещества. 1H ЯМР (400 MГц, CDCl3) δ м.д. 11,81 (с, 1 H); 8,16 (д, J=2,1 Гц, 1 H); 7,90-7,98 (м, 2 H); 7,45-7,53 (м, 2 H); 7,22 (д, J=2,2 Гц, 1 H); 3,71 (с, 3 H); 3,01 (т, J=7,8 Гц, 2 H); 2,71 (т, J=7,8 Гц, 2 H); 1,51 (с, 9 H).
Пример 11. Переэтерификация бензотриазолметилового эфира с полиглицериновым полимером.
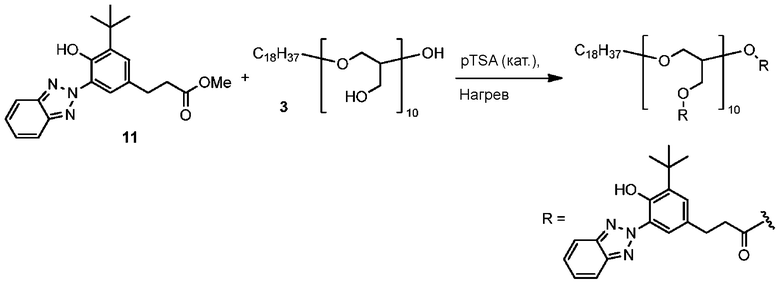
ФОРМУЛА XVII. ПЕРЕЭТЕРИФИКАЦИЯ ПОЛИГЛИЦЕРИНА
Переэтерификация бензотриазолметилового эфира 11 с полиглицерином 3 показана в ФОРМУЛЕ XVII. Раствор полиглицерина 3 в MeOH сконцентрировали на роторном испарителе; остаточный растворитель удаляли в вакууме на протяжении ночи при температуре 75°C. Полиглицерин 3 (1,36 г, 14,9 миллиграмм-эквивалент гидроксила) добавили в двугорлую круглодонную колбу объемом 100 мл с якорьком для магнитной мешалки. В колбу добавили бензотриазолметиловый эфир 11 (4,24 г, 12 ммоль) и pTSA⋅H2O (7,1 мг). На колбу установили переходник для подачи азота и переходник для перегонки с приемной колбой объемом 100 мл. Реакционную колбу погрузили в масляную баню, которую нагрели до 175°C. В течение 20 минут все реагенты расплавились. Реакционную смесь интенсивно перемешивали в токе азота на протяжении ночи. На следующее утро колбу вакуумировали; остаточные УФ-поглощающие хромофоры сублимировались и собрались в переходнике для перегонки. Подогрев в вакууме продолжали всю ночь. Затем реакционную смесь охладили до комнатной температуры; продукт, УФ-поглощающий полиглицерин, получили в виде желтого стекловидного твердого вещества. 1H ЯМР (400 MГц, CDCl3) δ м.д. 11,71 (уш. с., 8 H); 8,05 (уш. с., 8 H); 7,81 (уш. с., 16 H); 7,36 (уш. с., 16 H); 7,14 (уш. с., 8 H); 5,06-5,32 (уш. с., 1 H); 3,86-4,57 (м, 16 H); 3,15-3,82 (м, 30 H); 2,92 (уш. с., 16 H); 2,68 (уш. с., 16 H); 1,45 (уш. с., 76 H); 1,24 (уш. с., 28 H); 0,88 (т, J=6,6 Гц, 3 H).
Из примеров 1-11 видно, что результаты аналитической характеризации полученных УФ-поглощающих полиэфиров соответствовали ожидаемым структурам. Анализ полимеров, описанных в примерах, с использованием высокоэффективной жидкостной хроматографии, подтвердил, что описанные способы полимеризации позволяют получить малые концентрации остаточного УФ-поглощающего мономера.
Пример 12. Краткое описание результатов измерения SPF.
Измерения солнцезащитного фактора (SPF) УФ-поглощающих полимеров проводили с использованием следующего способа анализа защиты от солнца in vitro. Навески образцов полимера поместили в стеклянные флаконы объемом 8 мл. Для получения нужной массовой доли раствора полимера во флакон добавили смешанные C12-C15 алкилбензоаты (косметический масляный растворитель, который доступен в продаже под торговой маркой FINSOLV TN производства компании Innospec, г. Ньюарк, штат Нью-Джерси). Во флакон поместили якорек для магнитной мешалки и закрыли флакон резьбовой крышкой с внутренним тефлоновым покрытием. Раствор полимер/масло перемешивали в алюминиевом реакционном блоке при температуре 100°C до гомогенного состояния. После охлаждения 32 мг раствора полимера нанесли на пластину из полиметилметакрилата (ПММА) (подложка для проведения испытаний, которая доступна в продаже под торговой маркой HELIOPLATE HD6 производства компании Helioscience, г. Марсель, Франция). Раствор равномерно распределяли по пластине одним пальцем с надетым на него латексным напальчником до тех пор, пока вес образца на пластине не снизился до 26 мг. Базовое пропускание измеряли на пластине HD6 без обработки, в полученном от производителя виде. Поглощение измеряли с использованием калибрированного анализатора пропускания УФ-излучения Labsphere UV-1000S UV (Labsphere, г. Норд Саттон, штат Нью-Гемпшир, США). Измерения поглощения использовали для расчета показателя SPF. SPF рассчитывали с применением известных специалистам способов. Уравнение, использованное для расчета SPF, представлено в Уравнении 1:
SPFin vitro = [∫ E(λ) I(λ)dλ]/[∫ E(λ) I(λ) 10-A0(λ) (dλ)], (1)
где:
E(λ) = спектр, вызывающий покраснение кожи;
I(λ) = спектральная плотность потока излучения, поступающего от источника УФ-излучения;
A0(λ) = средняя монохроматическая поглощающая способность слоя испытываемого продукта до облучения ультрафиолетом;
dλ = шаг длины волны (1 нм);
а интегрирование в каждом случае проводится по диапазону длин волн от 290 нм до 400 нм.
Результаты исследования SPF полимера in vitro приведены в примерах 4, 7 и 9 в виде [% весового содержания в FINSOLV TN, среднее значение SPF], а также представлены в таблице 1.
Видно, что описываемые полимерные композиции растворялись в маслах, обычно используемых в косметологии для местного применения. Более того, было показано, что растворы полимеров в этих маслах, использованные в способах исследования SPF in vitro, имели удовлетворительные значения SPF.
ПРИМЕРЫ КОМПОЗИЦИЙ
Следующий пример иллюстрирует низкий уровень раздражения, вызываемого некоторыми композициями настоящего изобретения. Обладающие признаками изобретения композиции (E1-E4) включают линейный поглощающий ультрафиолетовое излучение полиэфир, содержащий химически связанный УФ-поглощающий хромофор. Линейный поглощающий ультрафиолетовое излучение полиэфир был изготовлен в соответствии со способом, описанным в примере 3B и примере 4. Обладающие признаками изобретения композиции (E1-E4) и сравнительный пример C1 были изготовлены, как показано в таблице 2 и описано ниже.
Обладающие признаками изобретения примеры E1-E4 и сравнительный пример C1 изготовили с использованием следующего способа. Водную фазу приготовили путем добавления воды в основной сосуд и нагревания до 80°C при перемешивании. Добавили AMIGEL, PEMULEN TR2 и PHENONIP XB и перемешивали до растворения. Масляную фазу приготовили путем загрузки в сосуд CETIOL CC и CRODACOL C95 при перемешивании. При температуре 60°C добавили УФ-поглощающий полиэфир. Затем добавили AMPHISOL K и нагрели смесь приблизительно до 80°C при перемешивании. Нагретую водную фазу добавили к масляной фазе с умеренным перемешиванием. Во время охлаждения продолжали умеренное перемешивание. Сравнительный пример C1 изготовили с использованием того же способа, за исключением того, что CRODACOL C95 добавлен не был.
Определили оценки по МОДИФИЦИРОВАННОМУ ТЕСТУ TEP для обладающих признаками изобретения примеров E1-E4 и сравнительных примеров C1-C2 с использованием МОДИФИЦИРОВАННОГО ТЕСТА TEP, как описано выше; результаты представлены в таблице 3.
Результаты тестирования с использованием МОДИФИЦИРОВАННОГО ТЕСТА TEP показывают, что примеры, обладающие признаками изобретения, характеризуются очень низкими оценками по МОДИФИЦИРОВАННОМУ ТЕСТУ TEP, что указывает на неожиданно низкий уровень вызываемого ими раздражения. Напротив, композиции сравнения C1, не содержащие неионного эмульгатора для эмульсий типа «масло в воде», содержащего спиртовую функциональную группу, характеризуются намного более высокими оценками по МОДИФИЦИРОВАННОМУ ТЕСТУ TEP.
Помимо этого, было проведено определение SPF для обладающих признаками изобретения примеров E1 и E3.
По 32 мг композиции для местного применения нанесли на пластину из полиметилметакрилата (ПММА Helioplate HD6). Раствор равномерно распределили по пластине с использованием одного пальца в латексном напальчнике. Композицию для местного применения распределили по всей поверхности пластины при легком давлении менее чем за 30 секунд. Затем пластину терли о грубую поверхность при более сильном надавливании в течение периода от 20 до 30 секунд. Зафиксировали среднюю конечную массу образца. Конечная масса обладающего признаками изобретения примера E1 составляла приблизительно 13,5 мг, обладающего признаками изобретения примера E3 - приблизительно 14 мг. Образцы оставили для уравновешивания в темноте, при температуре окружающей среды, по меньшей мере на 15 минут. Базовое пропускание измеряли на пластине HD6 без обработки, в полученном от производителя виде. Поглощение измеряли с использованием калибрированного анализатора пропускания УФ-излучения UV-2000S. Полученные результаты представлены в приведенной ниже таблице 4.
Следует понимать, что, хотя настоящее изобретение было описано путем его подробного описания, представленное выше описание имело целью проиллюстрировать, но не ограничивать объем настоящего изобретения.
Изобретение относится к области косметической промышленности, а именно к солнцезащитной композиции, содержащей компонент эмульгатора, включающий анионный эмульгатор для эмульсий типа «масло в воде» и неионный эмульгатор для эмульсий типа «масло в воде», содержащий спиртовую функциональную группу, при их весовом соотношении 12 или менее, и непрерывную водную фазу, в которой гомогенно диспергирована дисперсная масляная фаза, содержащая солнцезащитный агент, который включает линейный поглощающий ультрафиолетовое излучение простой полиэфир, химически связанный с УФ-поглощающим хромофором, в количестве, эффективном для обеспечения указанной композиции с солнцезащитным фактором (SPF) 10 или более, и который выбирается из: 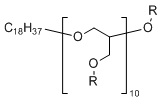 , где
, где 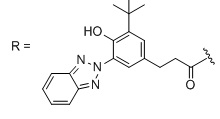 ;
; 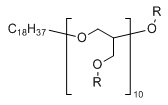 , где
, где 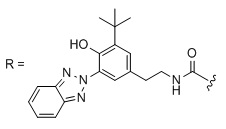 ; или продукта реакции сложного эфира тетрадекаглицерилмоностеарата и
; или продукта реакции сложного эфира тетрадекаглицерилмоностеарата и 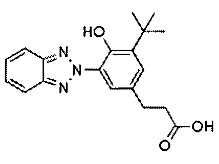 . Изобретение обеспечивает создание солнцезащитной композиции, обладающей мягкостью и удовлетворительными значениями SPF. 18 з.п. ф-лы, 12 пр., 4 табл.
. Изобретение обеспечивает создание солнцезащитной композиции, обладающей мягкостью и удовлетворительными значениями SPF. 18 з.п. ф-лы, 12 пр., 4 табл.
1. Солнцезащитная композиция, содержащая:
непрерывную водную фазу,
дисперсную масляную фазу, гомогенно распределенную в указанной водной фазе, причем указанная масляная фаза содержит полимерную композицию, которая содержит солнцезащитный агент, содержащий линейный поглощающий ультрафиолетовое излучение простой полиэфир, химически связанный с УФ-поглощающим хромофором, причем указанный линейный поглощающий ультрафиолетовое излучение простой полиэфир, химически связанный с УФ-поглощающим хромофором, присутствует в количестве, эффективном для обеспечения указанной композиции с солнцезащитным фактором (SPF) 10 или выше; и
компонент эмульгатора для эмульсий типа «масло в воде», содержащий анионный эмульгатор для эмульсий типа «масло в воде» и неионный эмульгатор для эмульсий типа «масло в воде», содержащий спиртовую функциональную группу, причем весовое соотношение анионного эмульгатора для эмульсий типа «масло в воде» к неионному эмульгатору для эмульсий типа «масло в воде» составляет 12 или меньше;
где указанный линейный поглощающий ультрафиолетовое излучение простой полиэфир, химически связанный с УФ-поглощающим хромофором, выбирают из группы, состоящей из:
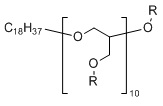 , где
, где 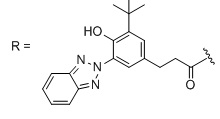 ;
;
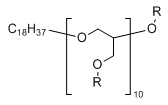 , где
, где 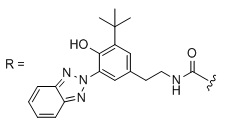 ; и
; и
продукта реакции сложного эфира тетрадекаглицерилмоностеарата и 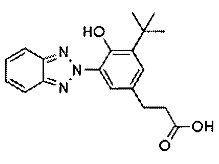 .
.
2. Композиция по п. 1, характеризующаяся тем, что содержит от 5 до 50 вес.% указанного линейного поглощающего ультрафиолетовое излучение простого полиэфира, химически связанного с УФ-поглощающим хромофором.
3. Композиция по п. 1, характеризующаяся тем, что указанная полимерная композиция состоит из указанного линейного поглощающего ультрафиолетовое излучение простого полиэфира, химически связанного с УФ-поглощающим хромофором.
4. Композиция по п. 1, характеризующаяся тем, что содержит от 7 до 40 вес.% указанного линейного поглощающего ультрафиолетовое излучение простого полиэфира, химически связанного с УФ-поглощающим хромофором.
5. Композиция по п. 1, характеризующаяся тем, что содержит от 10 до 25 вес.% указанного линейного поглощающего ультрафиолетовое излучение простого полиэфира, химически связанного с УФ-поглощающим хромофором.
6. Композиция по п. 1, характеризующаяся тем, что не содержит неполимерного УФ-поглощающего солнцезащитного агента.
7. Композиция по п. 6, характеризующаяся тем, что не содержит полимерного солнцезащитного агента, отличного от указанного линейного поглощающего ультрафиолетовое излучение простого полиэфира, химически связанного с УФ-поглощающим хромофором.
8. Композиция по п. 1, характеризующаяся тем, что содержит от 3 до 8 вес.% указанного анионного эмульгатора для эмульсий типа «масло в воде».
9. Композиция по п. 1, характеризующаяся тем, что содержит от 4,5 до 8 вес.% указанного анионного эмульгатора для эмульсий типа «масло в воде».
10. Композиция по п. 7, характеризующаяся тем, что указанный компонент анионного эмульгатора для эмульсий типа «масло в воде» содержит цетилфосфат калия.
11. Композиция по п. 1, характеризующаяся тем, что указанный анионный эмульгатор для эмульсий типа «масло в воде» выбирают из группы, состоящей из алкил-, арил-, алкиларил- или ацилмодифицированных производных сульфатов, эфирсульфатов, моноглицерилэфирсульфатов, сульфонатов, сульфосукцинатов, эфирсульфосукцинатов, сульфосукцинаматов, амидосульфосукцинатов, карбоксилатов, амидоэфиркарбоксилатов, сукцинатов, саркозинатов, аминокислот, тауратов, сульфоацетатов и фосфатов.
12. Композиция по п. 1, характеризующаяся тем, что указанный компонент анионного эмульгатора для эмульсий типа «масло в воде» содержит фосфатэфир.
13. Композиция по п. 1, характеризующаяся тем, что указанный неионный эмульгатор для эмульсий типа «масло в воде» представляет собой жирный спирт, содержащий от 14 до 22 атомов углерода.
14. Композиция по п. 1, характеризующаяся тем, что указанный компонент эмульгатора для эмульсий типа «масло в воде» не содержит катионных эмульгаторов.
15. Композиция по п. 1, характеризующаяся тем, что соотношение указанного анионного эмульгатора к указанному неионному эмульгатору составляет от 0,5 до 12.
16. Композиция по п. 1, которая характеризуется SPF 20 или более.
17. Композиция по п. 1, характеризующаяся тем, что указанный линейный поглощающий ультрафиолетовое излучение простой полиэфир, химически связанный с УФ-поглощающим хромофором, имеет индекс полидисперсности 1,5 или менее.
18. Композиция по п. 1, характеризующаяся тем, что указанная полимерная композиция содержит 50 вес.% или более указанного линейного поглощающего ультрафиолетовое излучение простого полиэфира, химически связанного с УФ-поглощающим хромофором.
19. Композиция по п. 1, характеризующаяся тем, что указанная полимерная композиция содержит 95 вес.% или более указанного линейного поглощающего ультрафиолетовое излучение простого полиэфира, химически связанного с УФ-поглощающим хромофором.
| WO 2011070050 A1, 16.06.2011 | |||
| US 20110117034 A1, 19.05.2011 | |||
| US 4399297 A, 16.08.1983 | |||
| Salah-Eddine Stiriba et al | |||
| Hyperbranched Molecular Nanocapsules: Comparison of the Hyperbranched Architecture with the Perfect Linear Analogue / Journal of the American Chemical Society, 2002, Vol.124, pages 9698-9699 | |||
| RU 2009124703 A, 10.01.2011. |
Авторы
Даты
2018-11-01—Публикация
2013-06-25—Подача