Изобретение относится к медицине, а именно к урологии, и может использоваться при эндовидеохирургическом лечении стриктур пиелоуретерального сегмента.
В настоящее время существуют различные способы малоинвазивного лечения стриктур пиелоуретерального сегмента, которые могут выполняться как перкутанным, трансуретральным доступами (Мартов, А.Г. Эндопиелотомия в лечении стриктур лоханочно-мочеточникового сегмента / А.Г. Мартов, Д.В. Ергаков, А.А. Лисенок, С.А. Серебряный // Пленум Российского общества урологов. Материалы. Екатеринбург, 2006. - С. 220-221), так и лапароскопически (Комяков, Б.К. Лапароскопическая пластика при первичных сужениях пиелоуретерального сегмента / Б. К. Комяков, Б. Г. Гулиев, Р. В. Алиев // Урология. - 2013. - N 6. - С. 81-84).
Наиболее близким к предлагаемому является способ роботассистированного хирургического лечения сужений пиелоуретерального сегмента с использованием слизистой щеки, включающий выполнение эндовидеохирургического доступа к пиелоуретеральному сегменту, рассечение рубцово-стенозированной части с продлением разреза на здоровые ткани не менее чем на 0,5 см в каждую сторону, образовавшийся дефект замещают заплатой, сформированной из аутотрансплантата слизистой щеки и окутывают место имплантации трансплантата сальником (Zampini, А М. Robotic salvage pyeloplasty with buccal mucosal onlay graft: video demonstration of technique and outcomes / A.M. Zampini, R.Nelson, J.J. Zhang [et al.] // Urology. - 2017. pii: S0090-4295(17)30764-1. doi: 10.1016 / j.urology. 2017.07.023). При этом предполагается, что реваскуляризация и питание трансплантата происходит из ткани сальника. Однако установлено, что процент приживляемости аутотрансплантата на жировую ткань составляет около 81% (Беломытцев, С.В. Клинико-морфологическое обоснование использования свободных слизистых лоскутов при уретропластиках у мужчин: автореф. дис. … канд. мед. наук / С.В. Беломытцев. - М.: Моск. обл. науч. - исслед. клин, ин-т им. М.Ф. Владимирского, 2012. - 21 с.).
Технический результат изобретения - улучшение васкуляризации пересаженного аутотрансплантата.
Технический результат изобретения достигается тем, что в способе эндовидеохирургического лечения стриктур пиелоуретерального сегмента, включающем продольное рассечение его стенозированной части с продлением разреза на здоровые ткани не менее чем на 0,5 см в каждую сторону и замещение образовавшегося дефекта заплатой, сформированной из аутотрансплантата слизистой щеки, в сформированную заплату и в сальник с помощью эндоскопического шприца осуществляют инъекции обогащенной тромбоцитами аутоплазмы из расчета 0,5 мл на 1,0 см протяженности заплаты. При этом возникает повышение компенсаторных возможностей микроциркуляторного русла за счет увеличения общей площади капиллярной сети, что достигается путем стимуляции неоангиогенеза в пересаженном аутотрансплантате и в реципиентном ложе. Для улучшения кровообращения используется обогащенная тромбоцитами аутоплазма. Положительный эффект лечения объясняется тем, что при введении богатой тромбоцитами аутоплазмы происходит местная стимуляция репаративного потенциала организма. Проведенные ранее исследования показали, что ангиогенный эффект обогащенной тромбоцитами аутоплазмы проявляется при концентрации тромбоцитов около 1000000 в 1 микролитре, т.е. примерно 3-5 раз превышающий норму (Marx, R.Е. Platelet-rich plasma: evidence to support its use / R.E. Marx // J. Oral Maxillofac. Surg. - 2004. - Vol. 62. - P. 489-496). Механизм действия обогащенной тромбоцитами аутоплазмы обусловлен разрушением α-гранул тромбоцитов, содержащих более 30 факторов роста, основные из них: фактор роста эндотелия сосудов (VEGF), три изомера тромбоцитарных факторов роста (platelet derived growth factor - PDGF-αα, PDGF-αβ, PDGF-ββ), два трансформирующих фактора роста (transforming growth factor - TGF-β1, TGF-β2) и эпителиальный фактор роста (epithelial growth factor EGF), которые являются триггерами тканевой репарации (Martinez-Zapata, М.J. Autologous platelet-rich plasma for treating chronic wounds / M.J. Martinez-Zapata [et al.] // Cochrane Database Syst. Rev. - 2016. - Vol. 5. - p. 68). Преимущество богатой тромбоцитами аутоплазмы в том, что она аутологична, апирогенна и нетоксична, что создает идеальную основу для клеточной инкубации. Отсутствует опасность внесения вируса гепатита, ВИЧ и других инфекций. Способ прост, не требует дорогостоящего оборудования и специальной подготовки медицинского персонала.
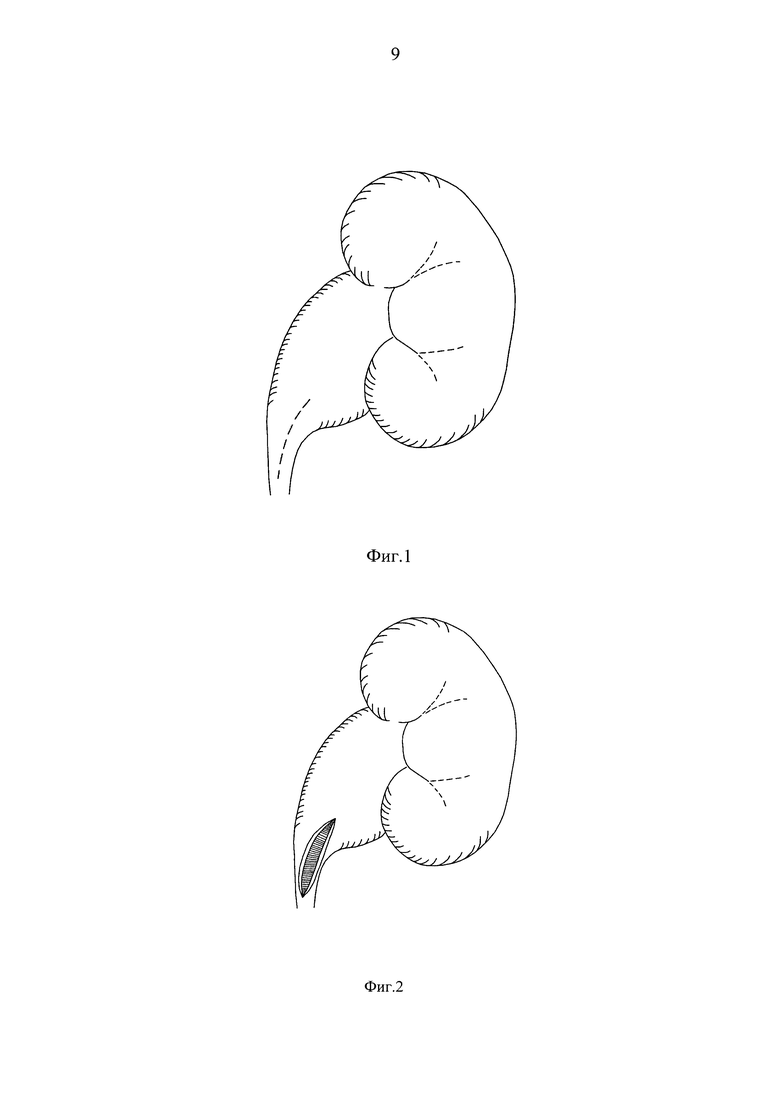
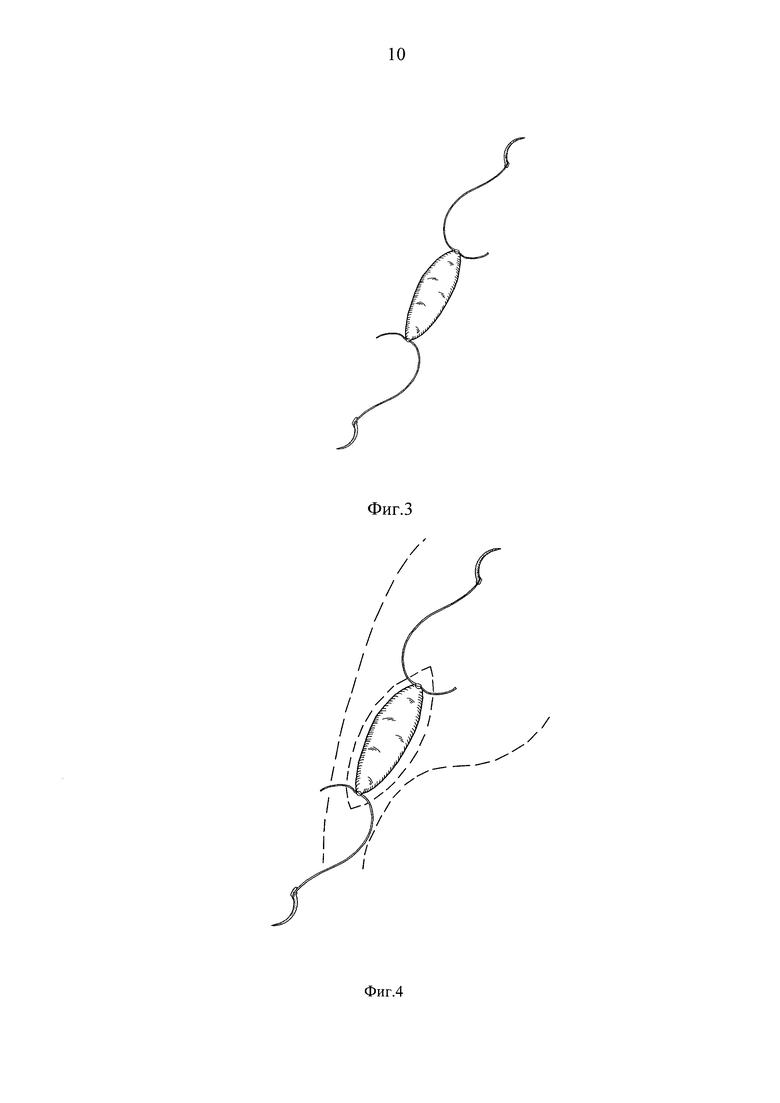
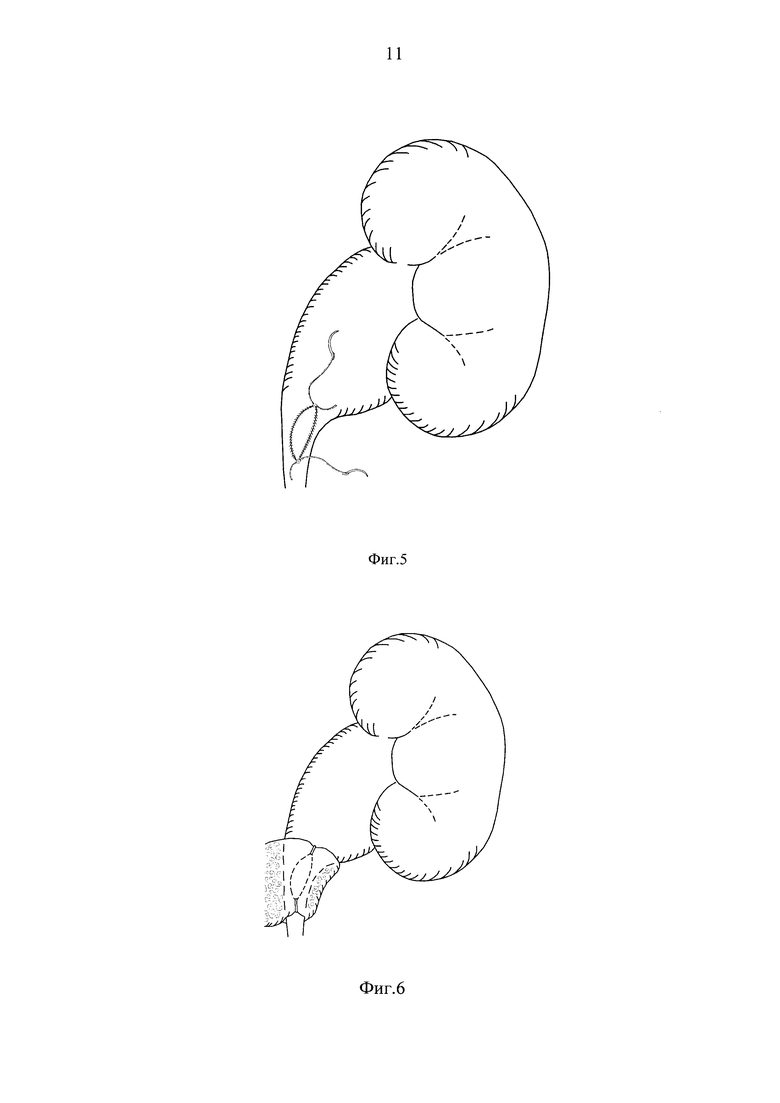
Изобретение поясняется фиг. 1-6. На фиг. 1 показано продольное рассечение суженного участка пиелоуретерального сегмента. На фиг. 2 изображен рассеченный участок пиелоуретерального сегмента с продолжением разреза на здоровые ткани на 0,5 см в каждую сторону. На фиг. 3 изображен аутотрансплантат с фиксированными к противоположным краям атравматического шовного материала, каждый длиной около трех полуокружностей трансплантата. На фиг. 4 приведено расположение аутотрансплантата относительно рассеченного участка пиелоуретерального сегмента. На фиг. 5 изображен, фиксированный к рассеченным краям пиелоуретерального сегмента, аутотрансплантат. На фиг. 6 показана фиксация участка большого сальника к фиксированному аутотрансплантату.
Способ осуществляется следующим образом:
Перед хирургической операцией у пациента в асептических условиях из локтевой вены забирают 20,0 мл крови в стерильные вакуумные пробирки, содержащие по 0,5 мл 3,8% цитрата натрия. Затем кровь центрифугируют при скорости 900 g в течение 5 минут, в результате чего происходит разделение крови на три фракции: плазмы, лейкоцитов и эритроцитарной массы. Полученный верхний слой плазмы подвергали повторному центрифугированию при скорости 1000 g в течение 10 минут. После этого с помощью калиброванного дозатора из пробирок удалялся слой плазмы до отметки 1 мл. В результате получалось около 2,0 мл обогащенной тромбоцитами аутоплазмы. Активация тромбоцитов проводится 0,2 мл 10% раствора кальция хлорида.
Операцию выполняют под эндотрахеальным наркозом. Осуществляют эндовидеохирургический доступ к пораженному пиелоуретеральному сегменту. После выделения стриктуры, ее продольно рассекают как показано на фиг. 1. При этом разрез должен быть с некоторым запасом и заходить на здоровые ткани на 0,5 см (фиг. 2). Это делается с целью лучшей реваскуляризации подшиваемого в эту зону трансплантата. После этого мочеточник интубируют уретеральным стентом 8 Ch. Измеряют общую протяженность дефекта. По общепринятой методике осуществляют забор аутотрансплантата слизистой щеки.
К противоположным краям щечного трансплантата фиксируют атравматический шовный материал длиной около трех полуокружностей трансплантата (фиг. 3). Далее трансплантат фиксируют к рассеченным краям пиелоуретерального сегмента по типу заплаты непрерывными швами по противоположным полуокружностям (фиг. 4-5). Этим же шовным материалом к аутотрансплантату фиксируется большой сальник как показано на фиг. 6. В заплату и большой сальник с помощью эндоскопического шприца инъецируют обогащенную тромбоцитами аутоплазму из расчета 0,5 мл на 1,0 см протяженности реципиентного ложа.
К месту операции забрюшинно подводят страховой дренаж. Стентирование мочеточника осуществляют в течение 8 недель. Страховой дренаж удаляют после прекращения выделения раневого отделяемого.
Существенные отличительные признаки заявляемого способа и причинно-следственная связь между ними и достигаемым результатом:
- В заплату, сформированную из аутотрансплантата слизистой щеки, и в подшиваемую область большого сальника вводят обогащенную тромбоцитами аутоплазму, которая обладает ангиогенным эффектом. Способ позволяет стимулировать развитие и рост сосудов в аутотрансплантате, обеспечивая его реваскуляризацию и приживление.
Таким образом, совокупность отличительных существенных признаков является новой и позволяет улучшить васкуляризацию пересаженного аутотрансплантата.
Приводим клинический пример выполнения способа:
Пример 1. Больная Г. 43 года. Диагноз: Стриктура пиелоуретерального сегмента слева. Гидронефроз 2 стадии слева.
Больной произведена операция следующим образом: Этап А: После обработки операционного поля в положении больной на правом боку под общей анестезией была в околопупочной области по методу Хассона установлен троакар 12 мм. Наложен пневмоперитонеум 12 мм.рт.ст. С помощью лапароскопа выполнен осмотр брюшной полости. Под контролем зрения дополнительно установлено два троакара 5 мм в стандартных положениях. Нисходящий отдел ободочной кишки мобилизован медиальнее Выполнен доступ к пиелоуретеральному сегменту слева. Суженная часть сегмента продольно рассечена на протяжении 3,5 см. В мочеточник установлен мочеточниковый стент 8 Ch.
Этап операции в ротовой полости: после обработки ротовой полости раствором антисептика и гидроперпаровки слизистой левой щеки разрезом прямоугольной формы в пределах подслизистого слоя взят трансплантат 1,5×4,0 см. Лоскут обработан. Гемостаз раны ротовой полости, ушивание дефекта слизистой оболочки непрерывным швом (кетгут 0).
Этап Б: уретеропластики слева: Края рассеченного мочеточника сшиты непрерывным швом с заплатой, сформированной из аутотрансплантата слизистой щеки (викрил 4/0). К аутотрансплантату пошит край большого сальника. С помощью эндоскопического шприца в область аутотрансплантата и большого сальника введено 2,0 мл. обогащенной тромбоцитами аутоплазмы. Контроль наличия инородных тел в ране, счет верен. Контроль гемостаза, сухо. Десуфляция. Троакары излечены под контролем зрения. Послойный шов ран, асептические наклейки. Отторжения аутотрансплантата не наблюдалось.
Осложнений в послеоперационном периоде не наблюдали. Стент слева извлечен через 8 недель после операции. При контрольном обследовании спустя 12 месяцев жалоб со стороны мочевыводящих путей нет, на экскреторных урограммах функция почек удовлетворительная, нарушений уродинамики нет, пиелоуретеральный сегмент проходим хорошо.
Заявляемый способ улучшает васкуляризацию пересаженного аутотрансплантата.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ хирургического лечения протяженных стриктур верхней трети мочеточника и лоханочно-мочеточникового сегмента | 2020 |
|
RU2738002C1 |
| Способ лапароскопического лечения протяженных облитераций верхней трети мочеточника и лоханочно-мочеточникового сегмента | 2021 |
|
RU2760612C1 |
| Способ хирургического лечения протяженных стриктур и облитераций мочеточника и лоханочно-мочеточникового сегмента при его туберкулезном поражении | 2019 |
|
RU2711110C1 |
| СПОСОБ ЛЕЧЕНИЯ ПРОТЯЖЕННЫХ СТРИКТУР ПЕРЕДНЕЙ УРЕТРЫ У МУЖЧИН | 2017 |
|
RU2669049C1 |
| Способ хирургического лечения рецидивных и постлучевых протяженных стриктур и облитераций нижней трети мочеточника | 2019 |
|
RU2709167C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ПРОТЯЖЕННЫХ СТРИКТУР МОЧЕТОЧНИКА | 2016 |
|
RU2625782C1 |
| Способ лечения протяженных стриктур тазового отдела мочеточника с использованием аутотрансплантата из слизистой щеки | 2019 |
|
RU2712863C1 |
| СПОСОБ ЛЕЧЕНИЯ РЕЦИДИВНЫХ СТРИКТУР БУЛЬБОЗНОГО ОТДЕЛА УРЕТРЫ У МУЖЧИН | 2019 |
|
RU2710217C1 |
| СПОСОБ УРЕТЕРОПИЕЛОПЛАСТИКИ БУККАЛЬНЫМ ЛОСКУТОМ ПРИ СТРИКТУРЕ ВЕРХНЕЙ ТРЕТИ МОЧЕТОЧНИКА И ЛОХАНОЧНО-МОЧЕТОЧНИКОВОГО СЕГМЕНТА У ПАЦИЕНТОВ С ЕДИНСТВЕННОЙ ПОЧКОЙ ПРИ ХРОНИЧЕСКОЙ БОЛЕЗНИ ПОЧЕК | 2024 |
|
RU2841225C1 |
| Способ лапароскопического лечения протяженных постлучевых стриктур и облитераций нижней трети мочеточника | 2020 |
|
RU2739115C1 |
Изобретение относится к медицине, а именно к урологии. Выполняют эндовидеохирургическое лечение стриктур пиелоуретерального сегмента, включающее продольное рассечение его стенозированной части с продлением разреза на здоровые ткани не менее чем на 0,5 см в каждую сторону. Замещают образовавшийся дефект мочеточника заплатой, сформированной из аутотрансплантата слизистой щеки. Окутывают место имплантации трансплантата большим сальником. При этом в заплату, сформированную из аутотрансплантата слизистой щеки, и в подшиваемую область большого сальника вводят обогащенную тромбоцитами аутоплазму из расчета 0,5 мл на 1,0 см протяженности заплаты. Способ позволяет улучшить васкуляризацию пересаженного аутотрансплантата. 1 пр. 6 ил.
Способ эндовидеохирургического лечения стриктур пиелоуретерального сегмента, включающий продольное рассечение его стенозированной части с продлением разреза на здоровые ткани не менее чем на 0,5 см в каждую сторону, замещение образовавшегося дефекта мочеточника заплатой, сформированной из аутотрансплантата слизистой щеки, и окутывание места имплантации трансплантата большим сальником, отличающийся тем, что в заплату, сформированную из аутотрансплантата слизистой щеки, и в подшиваемую область большого сальника вводят обогащенную тромбоцитами аутоплазму из расчета 0,5 мл на 1,0 см протяженности заплаты.
| ZAMPINI А М | |||
| Et al | |||
| Robotic salvage pyeloplasty with buccal mucosal onlay graft: video demonstration of technique and outcomes | |||
| Urology,2017, N110, P.253-256 | |||
| СПОСОБ ЭНДОХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ РЕЦИДИВНОГО СУЖЕНИЯ ПИЕЛОУРЕТЕРАЛЬНОГО СЕГМЕНТА | 2009 |
|
RU2426502C1 |
| СПОСОБ УРЕТЕРОПИЕЛОПЛАСТИКИ | 2004 |
|
RU2284162C2 |
| БОРИСОВ В.С | |||
| и др | |||
| Опыт инъекционного введения аутоплазмы при лечении пограничных ожогов II-III степени | |||
| Современные аспекты лечения термической травмы | |||
| Материалы НПК с международным участием, посвященной 70-летию Первого ожогового центра России), 23-24 июня 2016г | |||
| СПб., 2016, С.15-16, абзац 3 | |||
| БОГДАН В.Г., ТОЛСТОВ Д.А | |||
| Клиническая эффективность аутодермопластики с использованием обогащенной тромбоцитами плазмы при пластическом закрытии трофических язв венозной этиологии больших размеров | |||
| Военная медицина, 2015, С.65-69 | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| АЛЯЕВ Ю | |||
| Г | |||
| Трансуретеральные эндоскопические операции на мочеточнике, Хирургия Журнал им | |||
| Н | |||
| И | |||
| Пирогова, 2006, N7, C.12-16 | |||
| CASTILLEJOS-MOLINA R | |||
| A., Surgical treatment of ureteropelvic junction obstruction, Gac Med Мех., 2006, 142(3), 205-208 | |||
| SHAH S., RANKA P., VISNAGARA M | |||
| et al | |||
| Use of buccal mucosa as onlay graft technique for benign ureteric strictures | |||
| Indian J | |||
| Urol | |||
| Способ и приспособление для нагревания хлебопекарных камер | 1923 |
|
SU2003A1 |
| Прибор для промывания газов | 1922 |
|
SU20A1 |
| Видоизменение прибора с двумя приемами для рассматривания проекционные увеличенных и удаленных от зрителя стереограмм | 1919 |
|
SU28A1 |
Авторы
Даты
2019-01-15—Публикация
2018-01-31—Подача