Область техники
Настоящее изобретение относится к медицинской биотехнологии, медицине, травматологии, ортопедии, стоматологии и ортодонтии, а именно к способу получения биологического матрикса, предназначенного для замещения дефектов костной ткани.
Уровень техники
Сокращение сроков реабилитации и повышение эффективности восстановительных операций на опорно-двигательном аппарате остается актуальной социально-экономической и медицинской проблемой. В последнее время все большее внимание уделяется использованию процессов регенерации как альтернативе механического замещения дефектов кости посредством металлических и керамических имплантов.
Использование костных трансплантатов является общепринятым мировым стандартом при лечении переломов, обширных дефектов костной ткани после оперативных вмешательств и травм, а также при замене утраченных костей. Данный тезис подтверждается огромным количеством экспериментального и клинического материала по всему миру. Наиболее распространенным подходом является использование аутотрансплантатов. Однако использование собственного биологического материала имеет ряд серьезных ограничений, в первую очередь связанных с травматичностью, ограниченным ресурсом и такими осложнениями, как ранняя послеоперационная боль, хроническая боль в месте забора трансплантата, хронической вялотекущей инфекцией, рубцами, потерей крови и другими.
В качестве альтернативы предложено использовать аллотрансплантаты, но им не хватает остеоактивного потенциала аутотрансплантатов, и, кроме того, они несут риск контаминации инфекционными агентами и иммунного отторжения вследствие реакции отторжения трансплантата («хозяин против трансплантата»).
Наиболее современные подходы направлены на улучшение эффективности костных трансплантатов или других искусственных эндопротезов путем включения костных клеток-предшественников или незрелых клеток мезенхимального ряда и факторов роста в целях стимуляции роста, дифференцировки клеток и активации процессов регенерации кости.
В то же время идеальный костный трансплантат должен быть изготовлен из биоматериалов, в данном случае костной ткани, которые в полной мере имитируют структуру и свойства естественного костного матрикса (экстрацеллюлярного матрикса кости). Кроме того, данный матрикс должен как включать остеопрогениторные клетки, так и обеспечивать полный спектр метаболических и экологических сигналов, обнаруживаемых в нативной здоровой кости.
Однако создание биоактивной конструкции, которая структурно, функционально и механически сравнима с натуральной костью, полностью моделирующей микросреду, в том числе биохимические и биофизические сигналы, до сих пор является вызовом для исследователей и производителей во всем мире. Наиболее предпочтительным заменителем костной ткани представляется ксеногенный биологический матрикс, полученный с использованием физико-химических методов децеллюляризации и глубокой очистки, вследствие сохранения трехмерной организации коллагена и аморфной формы гидроксиапатита и возможности импрегнации в него различных биологически активных компонентов.
Известен способ (Fages J, et al. (1998) Viral inactivation of human bone tissue using supercritical fluid extraction. ASAIO J 44:289-293), где после распиливания кости проводили обезжиривание биологического матрикса методом сверхкритической флюидной экстракции при следующих условиях: скорость потока CO2 – 2 кг/ч, давление 250 бар, температура 50°C, продолжительность обработки 10 минут на 1 г костной ткани. Настоящий способ включает дополнительные этапы, где проводили удаление белков 35% раствором перекиси водорода (Н2О2) в течение 24 часов при 40°C; удаление остаточных липидов и стерилизацию гидроксидом натрия 1М, 1 час при 20°C с дальнейшей нейтрализацией водным раствором NaH2PO4 в концентрации 12 г/л в течение 30 минут и последующей обработкой 95% этанолом в течение 3 часов при 20°C с дальнейшей обработкой 100% этанолом в течение 2 часов при 20°C; после этого образцы сушили на воздухе 12 часов при 40°C. После упаковки проводили стерилизацию гамма-облучением при 25 кГрей. Данный метод позволяет получить стерильный биологический костный матрикс.
Недостатками данного способа являются недостаточная очистка матрикса от антигенной составляющей вследствие отсутствия ферментативной обработки материала, использование высокой температуры, при которой происходит неизбежная денатурация коллагена, и использование 100% этанола, для которого требуются специальные условия.
Из предшествующего уровня техники известен способ (Bone graft material incorporating demineralized bone matrix and lipids, US7357947 B2, Biomet Inc. (US), 15.04.2008), где свежую костную массу получали из мелких животных - крыс. После нескольких промывок фосфатно-солевым буферным раствором и этанолом кости лиофильно высушивали и размалывали в частицы диаметром 100-500 мкм, которые были далее декальцифицированы 0,6N HCl/1% Тритон X-100. Для полного удаления липидов частицы погружали в смесь хлороформа и метанола 1:1 на 12 часов при комнатной температуре. Данный способ позволяет получить деминерализованный костный матрикс.
Недостатками данного способа являются отсутствие стадии первичной очистки костного материала и малое количество стадий промывки, что не позволяет получить деминерализованный костный матрикс высокой степени чистоты. Кроме того, данный способ позволяет получить костный матрикс только в виде крошки.
Из предшествующего уровня техники известен способ (Demineralized bone matrix compositions and methods, US 8202539 B2, Warsaw Orthopedic, Inc. (US), опубл. 19.06.2012.), где кость, на примере среза бедренной кости человека, размалывали на мельнице радиально для отделения радиальных слоев от диафиза. После удаления губчатых участков кости, кортикальную кость размалывали на трех глубинах: 1,5 мм – периостальный слой, далее еще 1,5 мм – средний слой и далее еще 1,5 мм – эндостальный слой, таким образом получали три глубины – это 1,5, 3 и 4,5 мм. Во избежание случайного попадания костного мозга в материал дальнейшее размалывание не проводили. Далее осуществляли деминерализацию. В качестве переносчика размолотых и деминерализованных частиц выступал глицерол. Было показано, что возможны произвольные комбинации долей частиц из различных слоев. Было продемонстрировано, что деминерализованный костный матрикс из периостального слоя обладает наиболее высокой остеоиндуктивностью, чем из среднего и тем более из эндостального слоя. Данный способ позволяет получить остеоиндуктивный деминерализованный костный матрикс.
Недостатками данного способа являются отсутствие стадии первичной очистки костного материала и малое количество стадий промывки, что не позволяет получить деминерализованный костный матрикс высокой степени чистоты. В данном способе отсутствуют стадии делипидирования и децеллюляризации, вследствие чего значительно повышается риск иммунного ответа на имплантацию полученного биологического матрикса.
Из предшествующего уровня техники известен способ (Process for demineralization of bone matrix with preservation of natural growth factors, US 8992964 B2, Bacterin International, Inc. (US), опубл. 31.03.2015), где для получения деминерализованного губчатого костного матрикса 1-300 г губчатой кости помещали в 10-4500 мл 0,3-2M HCl, далее смесь перемешивали в течение 4-10 часов, в процессе перемешивания раствор HCl заменяли каждые 1-4 часа. Каждые 5-90 минут проводили тест губчатого костного матрикса на полную сжимаемость. Полностью сжимаемые сегменты губчатого костного матрикса помещали в нейтрализующий раствор с pH > 4. Свойства полученного матрикса улучшали обработкой озоном, где матрикс помещали в обогащенный озоном раствор с микропузырьками, причем раствор периодически заменялся, а концентрация озона была от 0,1 до 400 частей на миллион, причем время экспозиции составляло от 0,1 до 7 часов, а температура обогащенного озоном раствора от −20 до 50°C. Такая обработка возможна и перед деминерализацией. Деминерализованный костный матрикс имел концентрацию костного морфогенетического белка (BMP)-2 ≥ 5000 пг/г и сжимаемость до 20 раз. Данная методика позволяет получить деминерализованный костный матрикс с удовлетворительными биофизическими характеристиками.
Недостатками данного способа являются отсутствие стадий первичной очистки костного материала, удаления липидов, промывки и обработки детергентами, что не позволяет получить матрикс высокого качества и степени чистоты и значительно повышает риск иммунных реакций.
Из предшествующего уровня техники известен способ (Bone graft comprising a demineralized bone matrix and a stabilizing agent, US 7959941 B2, Warsaw Orthopedic, Inc., опубл. 14.06.2011), где после ручной очистки от мягких тканей губчатые кости распиливали на большие сегменты, а трубчатые – на малые. Сегменты промывали холодной деионизированной водой. Для удаления липидов и дегидратации костные сегменты помещали в 100% этанол на как минимум 1 час, причем этанол периодически заменяли. На 100 г кости использовали 4 л 100% этанола. Далее для окончательной дегидратации костные сегменты помещались в раствор безводного диэтилового эфира в вытяжном шкафу на 1 час. На 100 г кости использовали 2 л эфира. Обезвоженные костные сегменты замораживали и размалывали в порошок. Далее порошок деминерализовали 0,5M HCl (50 мл на 1 г кости) в течение 3 часов при комнатной температуре или 4°С с постоянным перемешиванием. Далее костные сегменты нейтрализовывали холодной деионизированной водой до достижения раствором pH воды. На промывку уходило 500 мл воды на 1 г костной массы. Деминерализованный костный порошок помещали в 100% этанол в течение 1 часа (200 мл 100% этанола на 1 г кости) и далее в раствор безводного диэтилового эфира в вытяжном шкафу на 1 час (100 мл эфира на 1 г кости). После этого для испарения эфира костные сегменты оставляли на ночь в вытяжном шкафу. Получающиеся частицы не имели запаха, снежно-белые и легко отделялись друг от друга. Для стерилизации использовался холодный этиленоксид или гамма-облучение. Данный способ позволяет получить стерильный деминерализованный костный матрикс.
Недостатками данного способа являются использование больших объемов токсичного диэтилового эфира, что несовместимо с требованиями безопасности. За исключением начального этапа, отсутствуют стадии промывки и обработки детергентами, что не позволяет получить матрикс высокого качества и степени чистоты.
Из предшествующего уровня техники известен способ (Bone matrix compositions and methods, CA2690457 A1, Osteotech, Inc. et al. (US), опубл. 24.12.2008), где после ручной очистки от мягких тканей кость перемалывали в порошок диаметром 2,8-4 мм, который далее помещали в раствор хлороформа и метанола 1:1 на 6 часов для удаления липидов. После высушивания в вытяжном шкафу в течение ночи частицы подвергали дополнительному высушиванию под вакуумом в течение 12 часов. Далее частицы подвергали деминерализации в 0,6N растворе HCl в течение 75 минут и промывали дистиллированной водой до pH ≥ 3. Далее частицы инкубировали в 100 мМ фосфатно-солевом буферном растворе с pH 7,4, содержащем 2 мМ азида натрия (ингибитор ферментов) и 6,0 мМ N-этилмалеимида (ингибитор протеаз) в течение 72 часов при 37°C. Затем частицы дважды промывали водой в течение 15 минут при комнатной температуре и лиофилизировали. Данная методика позволяет получить лиофилизированный деминерализованный костный матрикс в виде порошка или частиц.
Недостатками данного способа являются практически полное отсутствие этапов промывки, а также обработки детергентами, что не позволяет получить матрикс высокого качества и степени чистоты. Данный способ позволяет получить костный матрикс только в виде порошка или крошки, что ограничивает его применимость.
Из предшествующего уровня техники известен способ (Manufacturing method for fibrous demineralized bone matrix, US 9029077 B2, Cg Bio Co., Ltd. (KR) опубл. 12.05.2015), где после ручного удаления мягких тканей с кости, в примере весом 172 г, оставшиеся мягкие ткани, липиды и костный мозг удаляли при помощи детергента, содержащего сурфактант. Кость распиливали пополам и погружали в 20 мл 0,6N раствора HCl на 1 г кости в течение 3 часов для частичной деминерализации. Далее кость помещали в 20 мл дистиллированной воды на 1 г кости для промывки. Кости распиливали слайсером на слои, причем толщина слоя составляла около 0,5 мм. Далее костные слои погружали в 30 мл 0,6N раствора HCl на 1 г кости на 3 часа для полной деминерализации. Преципитирующий деминерализованный костный матрикс пульверизировали в течение 10 минут, нейтрализовывали фосфатно-солевым буферным раствором, промывали дистиллированной водой и лиофилизировали получением около 31 г матрикса в виде волокон. Данная методика позволяет получить лиофилизированный деминерализованный костный матрикс в виде слоев.
Недостатками данного способа является отсутствие детального описания обработки детергентом, при помощи которого предполагается удаление липидов и децеллюляризация, что значительно повышает риск иммунных реакций.
Из предшествующего уровня техники известен способ (Bone matrix compositions and methods, US 8328876 B2, Warsaw Orthopedic Inc. (US), опубл. 11.12.2012), где деминерализованный порошок помещали в раствор, содержащий 50 мМ Tris-HCl (pH 7,4), 5 мМ CaCl2 и 80 ЕД/мл очищенной бактериальной коллагеназы (соотношение 1 г порошка на 3 мл раствора) на 1 час при 37°C с перемешиванием. Далее деминерализованный костный матрикс перемешивали в течение 1 часа в 45 мл 0,1N уксусной кислоты при 4°C. После этого матрикс дважды промывали холодной водой в течение 30 минут и нейтрализовывали в течение 30 минут холодным фосфатно-солевым буферным раствором. Данная методика позволяет увеличить остеоиндуктивные свойства деминерализованного костного матрикса.
Недостатками данного способа являются частичная деградация коллагена в костном матриксе и вымывание костных морфогенетических белков вследствие использования уксусной кислоты, что снижает остеоиндуктивные свойства матрикса.
Из предшествующего уровня техники известен способ (Bone graft material incorporating demineralized bone matrix and lipids, US 6565884 B2, Biomet Manufacturing LLC (US), опубл. 20.05.2003), где заранее деминерализованный костный матрикс смешивали с лецитином с итоговой массовой долей матрикса от 20 до 80% и инкапсулировали в желатин для имплантации. Данная методика позволяет увеличить остеоиндуктивные свойства деминерализованного костного матрикса.
Недостатком данного способа является использование физического смешения компонентов, что не позволяет в полной мере импрегнировать лецитин и желатин в структуру матрикса, что, в свою очередь, снижает его эффективность.
Из предшествующего уровня техники известен способ (Xenograft bone matrix for orthopedic applications, EP 1418866 A2, Aperion Biologics, Inc (US), опубл. 19.05.2004), где замороженные свиные кости промывали дезинфектантом и размораживали с последующей очисткой от мягких тканей. Проксимальный и дистальный метафизы спиливали, а диафиз распиливали на удобные для обработки сегменты, которые помещали в ванну с изопропанолом. Далее сегменты переносили в сосуд с гексаном или метанолом на 12-18 часов при постоянном перемешивании при 4°C. После двукратно промывали водой в течение 10-12 часов при постоянном перемешивании при 4°C. Далее материал подвергали обработке 1,5М NaCl в течение 10-12 часов при постоянном перемешивании при 4°С, а далее промывали в воде и перемалывали в порошок с диаметром < 500 мкм. Затем порошок ресуспендировали в растворе 70% изопропанола и 0,1% Tween-20 и фильтровали через сито с последующим трехкратным повторением процедуры, что в сумме составляло 4 раза. Частицы ресуспендировали в H2O2 и перемешивали в течение 4-6 часов при 4°С. Затем надосадок сливали и к порошку добавляли 0,5N HCl с перемешиванием в течение 20-24 часов при 4°С. После трехкратной промывки водой добавляли раствор α-галактозидазы для снижения иммуногенности на 4-12 часов при 4-26°С с последующим сливанием этого раствора и трехкратной промывкой водой. Финальную стадию подготовки осуществляли лиофилизацией в течение 36-38 часов. Данный способ позволяет получить гипоиммуногенный деминерализованный костный матрикс.
Недостатками данного способа являются высокая длительность процедуры и возможность получения биологического матрикса только в форме порошка.
В качестве прототипа выбран способ (Decellularization and recellularization of organs and tissues, Патент US 8470520 B2, Regents Of The University Of Minnesota (US), опубл. 25.06.2013), описывающий:
(1) Децеллюляризацию биологической ткани полиэтиленгликолем (ПЭГ), где ткани промываются в 200 мл фосфатно-солевого буферного раствора, содержащего 100 ЕД/мл пенициллина, 0,1 мг/мл стрептомицина и 0,25 мкг/мл амфотерицина B в течение 20 минут. Далее ткани децеллюляризируются в 35 мл ПЭГ (1 г/мл) в течение 30 минут. После этого они как минимум дважды промываются в 500 мл фосфатно-солевого буферного раствора в течение 24 часов. Далее ткани экспонируются 35 мл ДНКазы I (70 ЕД/мл) в течение 1 часа и затем промываются в 500 мл фосфатно-солевого буферного раствора в течение 24 часов.
(2) Децеллюляризацию 5% Тритоном X-100, 0,1% NH4OH и 0,05% трипсином, где ткани промываются в 200 мл фосфатно-солевого буферного раствора, содержащего 100 ЕД/мл пенициллина, 0,1 мг/мл стрептомицина и 0,25 мкг/мл амфотерицина B в течение 20 минут. Далее ткани децеллюляризируются в 0,05% трипсине в течение 30 минут, а затем 5% раствором Тритона X-100 и 0,1% NH4OH в 500 мл фосфатно-солевого буферного раствора в течение 6 часов. Затем ткани промываются деионизированной водой в течение 1 часа и фосфатно-солевым буферным раствором в течение 12 часов и после этого промываются трижды 500 мл фосфатно-солевым буферным раствором в течение 24 часов. Далее ткани экспонируются 35 мл ДНКазы I (70 ЕД/мл) в течение 1 часа и еще дважды промываются в 500 мл фосфатно-солевого буферного раствора в течение 24 часов.
(3) Децеллюляризацию 1% додецилсульфатом натрия, где ткани промываются в 200 мл фосфатно-солевого буферного раствора, содержащего 100 ЕД/мл пенициллина, 0,1 мг/мл стрептомицина и 0,25 мкг/мл амфотерицина B в течение 20 минут. Далее ткани децеллюляризируются 500 мл 1% водного раствора додецилсульфата натрия в течение 6 часов. Затем ткани промываются деионизированной водой в течение 1 часа и фосфатно-солевым буферным раствором в течение 12 часов и после этого промываются трижды в 500 мл фосфатно-солевого буферного раствора в течение 24 часов. Далее ткани экспонируются 35 мл ДНКазы I (70 ЕД/мл) в течение 1 часа и еще трижды промываются в 500 мл фосфатно-солевого буферного раствора в течение 24 часов.
(4) Децеллюляризацию 5% Тритоном X-100 и 0,1% NH4OH, где ткани промываются в 200 мл фосфатно-солевого буферного раствора, содержащего 100 ЕД/мл пенициллина, 0,1 мг/мл стрептомицина и 0,25 мкг/мл амфотерицина B в течение 20 минут. Далее ткани децеллюляризируются в 500 мл 5% водного раствора Тритона X-100 и 0,1% NH4OH в течение 6 часов. Затем ткани промываются деионизированной водой в течение 1 часа и фосфатно-солевым буферным раствором в течение 12 часов и после этого промываются трижды в 500 мл фосфатно-солевого буферного раствора в течение 24 часов. Далее ткани экспонируются 35 мл ДНКазы I (70 ЕД/мл) в течение 1 часа и еще трижды промываются в 500 мл фосфатно-солевого буферного раствора в течение 24 часов.
Настоящий способ позволяет получить децеллюляризированный костный матрикс.
Недостатками данного способа являются недостаточная очистка и децеллюляризация больших объемов биологических тканей вследствие ограничения пропитывания толщи биоматериала используемыми реагентами, неполная отмывка и отсутствие дополнительного физического воздействия. Кроме того, весь процесс очистки и децеллюляризации биоматериала проводится при комнатной температуре в течение длительного времени без использования специальных консервантов, что повышает риск деградации биоматериала и его контаминации. Помимо этого, данная методика не позволяет провести деминерализацию биоматериала для получения матрикса с низким содержанием минеральной компоненты.
Таким образом, известные из уровня техники решения имеют важный недостаток – отсутствие одной или более стадий обработки биологического материала: первичной очистки, удаления липидов, промывки или обработки детергентами. Как правило, они не содержат необходимого количества стадий промывки либо стадии обработки детергентами. В то же время полноценная децеллюляризация и очистка инородного имплантируемого биоматериала как аллогенного, так и ксеногенного происхождения должна содержать как минимум: (1) первичную очистку костного материала; (2) удаление пахучих веществ и липидов; (3) обработку детергентами с целью децеллюляризации; (4) деминерализацию с последующей нейтрализацией pH; (5) промывку на всех этапах обработки материала; (6) финальную подготовку образца для непосредственного придания необходимой формы, включая стерилизацию. Кроме того, большинство решений подразумевает получение биологического матрикса только в качестве мелкодисперсного порошка вследствие невозможности пассивной диффузии химических реагентов вглубь объемного матрикса по причине отказа от использования любых физических воздействий. Помимо этого, решения используют неприемлемые для биологической составляющей матрикса внешние условия, при которых происходит либо денатурация белка, либо его вымывание.
Раскрытие изобретения
Задачей настоящего изобретения является разработка эффективного и безопасного биологического матрикса для замещения дефектов костной ткани.
Поставленная задача решается за счет использования многостадийной обработки биологического материала, а именно ксеногенной или аллогенной костной ткани, при сохранении нативной трехмерной организации коллагенового каркаса, сохранения нативной аморфной формы гидроксиапатита и фосфата кальция, наличия в биологическом матриксе активных компонентов, а именно белков экстрацеллюлярного матрикса и модифицирующих биомолекул (включая биоактивные пептиды и факторы роста).
Общим техническим результатом предлагаемой группы изобретений является получение биологического матрикса, обладающего повышенной остео- и биоинтеграцией, оптимальной скоростью биодеградации, высокой биосовместимостью, отсутствием иммунореактивности со стороны реципиента, высокой способностью к остеокондукции, выраженным остеогенным потенциалом при остеосинтезе и костной пластике. Биологический матрикс состоит из костного коллагена, гидроксиапатита и/или фосфата кальция, причем костный коллаген в настоящем матриксе представлен в нативной невосстановленной форме с полностью сохраненной трехмерной структурой, гидроксиапатит и фосфат кальция представлены в нативной аморфной форме, а сам матрикс, очищенный от клеточного дебриса, чужеродных липидов, нуклеиновых кислот и иммуногенов, содержит остаточные количества костных морфогенетических белков и может быть дополнительно модифицирован везикулярным фосфатидилхолином и/или холестерином с включенными гидролизованным коллагеном и/или ателоколлагеном и/или поли(е-капролактоном), а также различными биологически активными веществами (такими как биоактивные пептиды и факторы роста), посредством импрегнации.
Поставленная техническая задача достигается за счет использования многостадийной обработки биологического материала, а именно ксеногенной или аллогенной костной ткани, сохранения нативной трехмерной организации коллагенового каркаса, сохранения нативной аморфной формы гидроксиапатита и фосфата кальция и наличия в биологическом матриксе активных компонентов, а именно белков экстрацеллюлярного матрикса и модифицирующих биомолекул (включая биоактивные пептиды и факторы роста).
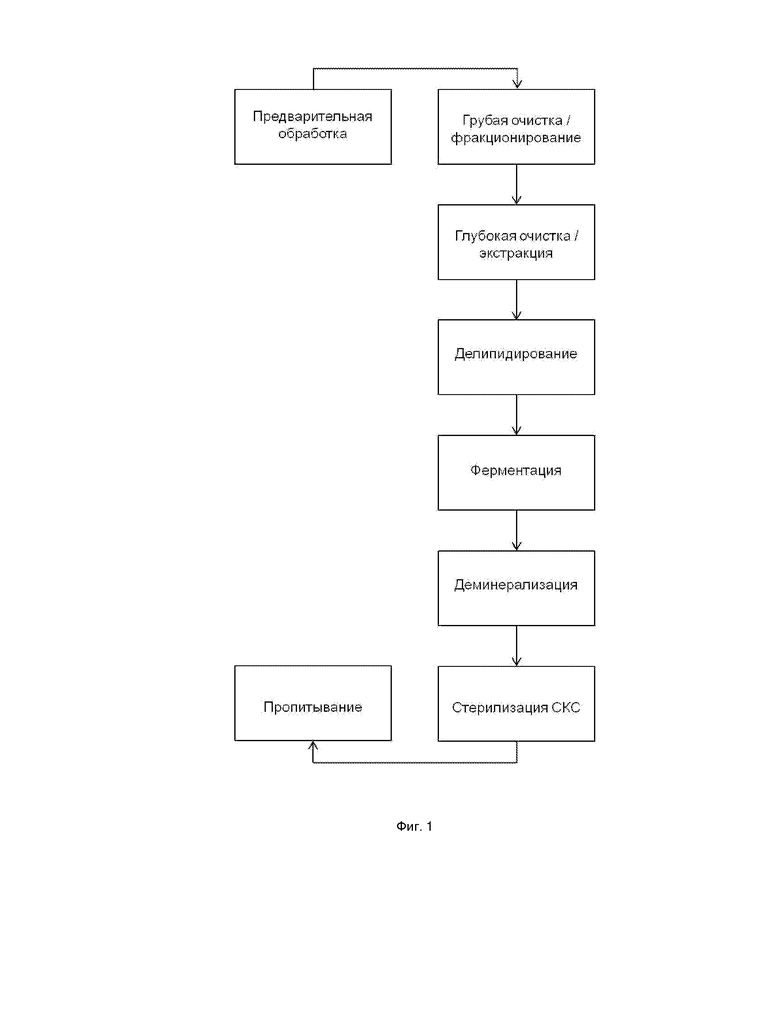
Способ получения биологического матрикса для замещения дефектов костной ткани по настоящему изобретению включает ряд последовательных стадий, в том числе: (1) предварительную обработку биологического материала; (2) грубую очистку и фракционирование; (3) глубокую очистку и экстракцию; (4) делипидирование; (5) ферментацию; (6) деминерализацию; (7) стерилизацию в сверхкритических средах.
Стадия предварительной обработки биологического материала включает замораживание биоматериала при -20 – -40°С, обработку дезинфектантами, включая раствор антибиотиков и антимикотиков, в течение 1-72 часов при температуре 1-8°С; обработку раствором перекиси водорода в концентрации 0,1-5% в течение 1-72 часов при температуре 1-8°С, причем соотношение биологической ткани к раствору составляет от 1:10 до 1:40.
В одном из вариантов осуществления способа в качестве дезинфектантов используют растворы гентамицин/амфотерицин и пенициллин/стрептомицин и/или нистатин и/или фунгизон.
В одном из вариантов осуществления способа обработку дезинфектантами проводят в условиях ультразвуковой ванны при общих условиях, описанных выше.
В одном из вариантов осуществления способа обработку раствором перекиси водорода проводят в условиях ультразвуковой ванны при условиях, описанных выше.
В одном из вариантов осуществления способа раствор для предварительной обработки меняют 1 раз в час.
Стадия грубой очистки и фракционирования включает очистку биологического образца от мягких тканей и фиброзного слоя периоста; фракционирование биологического материала; отмывку в растворе перекиси водорода в концентрации 0,1-5% в течение 1-72 часов при температуре 1-8°С, причем соотношение биологической ткани к раствору составляет от 1:10 до 1:40.
В одном из вариантов осуществления способа очистку биологического образца от мягких тканей проводят непосредственно после стадии предварительной обработки биологического материала.
В одном из вариантов осуществления способа очистку биологического образца от мягких тканей проводят после замораживания предварительного образца при температуре -20°С.
В одном из вариантов осуществления способа фракционирование биологического материала осуществляют отделением губчатого слоя кости от кортикального слоя.
В одном из вариантов осуществления способа фракционирование биологического материала осуществляют отделением диафиза трубчатой кости от метафиза и эпифиза.
В одном из вариантов осуществления способа фракционирование биологического материала осуществляют отделением периостального и среднего слоя от эндостального, причем периостальный и средний слой отделяют на глубину 8-10 мм.
В одном из вариантов осуществления способа обработку раствором перекиси водорода проводят в условиях ультразвуковой ванны.
В одном из вариантов осуществления способа каждый из растворов для грубой очистки меняют 1 раз в час в течение всей стадии отмывки.
В одном из вариантов осуществления способа биологический образец отделяют в форме блока губчатой кости.
В одном из вариантов осуществления способа биологический образец отделяют в форме блока губчатой и кортикальной кости.
В одном из вариантов осуществления способа биологический образец отделяют в форме кортикальной пластины.
В одном из вариантов осуществления способа биологический образец измельчают до состояния крошки или мелкодисперсного порошка кортикальной и/или губчатой кости.
Стадия глубокой очистки и экстракции включает обработку в растворе ионных и амфотерных поверхностно-активных веществ; отмывку матрикса в буферных растворах и/или деионизированной воде; нейтрализацию ионных поверхностно-активных веществ и ренатурацию белков; вторичную отмывку в буферных растворах и/или деионизированной воде; ультразвуковую экстракцию примесей.
В одном из вариантов осуществления способа в качестве ионных поверхностно-активных веществ используют додецилсульфат натрия в концентрации 0,1-10%.
В одном из вариантов осуществления способа в качестве ионных/анионных поверхностно-активных веществ используют лаурил сульфат, Тритон X-200, Тритон XQS-20, Тритон QS-15, Тритон QS-44 по отдельности в концентрации 0,1-10% или в смеси.
В одном из вариантов осуществления способа в качестве амфотерных поверхностно-активных веществ используют (3-[(3-холамидопропил)диметиламмонио]-1-пропансульфонат) в концентрации 0,1-10%.
В одном из вариантов осуществления способа ионные поверхностно-активные вещества и амфотерные поверхностно-активные вещества смешиваются в соотношении от 1:40 до 40:1.
В одном из вариантов осуществления способа обработку в растворе комплекса ионных и амфотерных поверхностно-активных веществ проводят с использованием ультразвукового дезинтегратора.
В одном из вариантов осуществления способа обработку в растворе комплекса ионных и амфотерных поверхностно-активных веществ проводят в течение 1-72 часов при температуре 35-41°С.
В одном из вариантов осуществления способа непосредственно перед стадией обработки в растворе комплекса ионных и амфотерных поверхностно-активных веществ раствор вместе с биологическим материалом сонифицируют с использованием ультразвукового дезинтегратора в течение 5-30 минут при температуре 35-41°С.
В одном из вариантов осуществления способа обработку в растворе комплекса ионных и амфотерных поверхностно-активных веществ проводят при постоянном перемешивании при орбитальной скорости 50-250 оборотов в минуту.
В одном из вариантов осуществления способа отмывку матрикса в буферных растворах и/или бидистиллированной деионизированной воде проводят в течение 1-72 часов при температуре 1-8°С, причем предпочтительным является фосфатно-солевой буферный раствор.
В одном из вариантов осуществления способа нейтрализации ионных поверхностно-активных веществ и ренатурацию белков проводят в растворе неионных поверхностно-активных веществ, включающего Тритон Х-100 в концентрации 0,1-5% и Tween-20 в концентрации 0,005-1%.
В одном из вариантов осуществления способа для нейтрализации ионных поверхностно-активных веществ используют Твин 80, Бридж 35/56/72/76/92V/97/58P, дигитонин, дигитоксигенин по отдельности в концентрации 0,1-10% или в смеси.
В одном из вариантов осуществления способа нейтрализацию и ренатурацию проводят при температуре 35-41°С.
В одном из вариантов осуществления способа нейтрализацию и ренатурацию проводят при постоянном перемешивании при орбитальной скорости 100-250 оборотов в минуту.
В одном из вариантов осуществления способа вторичную отмывку в буферных растворах и/или деионизированной воде проводят в течение 1-72 часов при температуре 1-8°С, причем предпочтительным является фосфатно-солевой буферный раствор.
В одном из вариантов осуществления способа каждый из растворов ионных и амфотерных поверхностно-активных веществ, неионных поверхностно-активных веществ и растворов для промывки меняют 1 раз в час.
В одном из вариантов осуществления способа в промывочный раствор добавляют антибиотики и/или антимикотики.
В одном из вариантов осуществления способа ультразвуковую экстракцию примесей проводят в условиях ультразвуковой ванны.
Предпочтительным способом является сочетание перфузии ионным детергентом, в частности додецилсульфатом натрия в концентрации 1%, растворенным в деионизированной воде, с последующей промывкой фосфатно-солевым буферным раствором и перфузией неионным детергентом, в частности Тритон X-100 в концентрации 1%, для удаления додецилсульфата натрия и ренатурации белков внеклеточного матрикса с последующей промывкой в фосфатно-солевом буферном растворе с антибиотиками в течение 72 часов.
В одном из вариантов осуществления способа непосредственно после отмывки в буферных растворах проводят центрифугирование костного матрикса в фосфатно-солевом буферном растворе при 300-3000 об/мин на горизонтальной центрифуге в течение 10-30 минут.
В одном из вариантов осуществления способа проводят отмывку в буферных растворах с переменной ионной силой.
В одном из вариантов осуществления способа проводят отмывку в растворе NaCl в концентрации 250-800 мМ.
В одном из вариантов осуществления способа отмывку проводят при температуре 0,5-2°С.
Стадия делипидирования включает обработку этанолом и/или смесью этанола и хлороформа; отмывку в буферных растворах или деионизированной воде или делипидирование в спиртах в условиях сверхкритических сред.
В одном из вариантов осуществления способа делипидирование проводят в смеси этанола и этилацетата, причем соотношение компонентов смеси от 1:1 до 1:4 соответственно.
В одном из вариантов осуществления способа после делипидирования в спиртах проводят дополнительную обработку в растворе толуола при 35-41°С в течение 1-72 часов.
В одном из вариантов осуществления способа после обработки в спиртах проводят последующую обработку гидроксидом натрия в концентрации 0,5-20 г/л при температуре 1-8°С в течение 1-72 часов.
Причем все стадии, за исключением того, где указано противоположное, осуществляются при постоянном перемешивании на роторной качалке-шейкере в условиях холодильной камеры при температуре 1-8°С, причем температура не должна превышать 8°С.
Стадия ферментации включает обработку в растворах ферментов – ДНКаза и/или трипсин и последующую отмывку в буферных растворах или деионизированной воде, причем обработку трипсином осуществляют с добавлением ионов магния (Mg2+) в фосфатно-солевом буферном растворе в концентрации 0,1-2%.
В одном из вариантов осуществления способа стадию ферментации осуществляют обработкой в растворе ДНКазы в концентрации 10-500 мкг/мл.
В одном из вариантов осуществления способа стадию ферментации осуществляют обработкой в растворе трипсина в концентрации 0,05-1%.
В одном из вариантов осуществления способа обработку трипсином осуществляют добавлением раствора магния хлорида в концентрации 0,05-5 мМ.
В одном из вариантов осуществления способа стадию ферментации осуществляют при температуре 37°С на орбитальном шейкере при 100-250 оборотов в минуту.
В одном из вариантов осуществления способа каждый из растворов для ферментации меняют 1 раз в час.
В одном из вариантов осуществления способа непосредственно после отмывки в буферных растворах проводят центрифугирование костного матрикса в фосфатно-солевом буферном растворе при 300-3000 об/мин на горизонтальной центрифуге в течение 10-30 минут.
Стадия деминерализации включает обработку в растворе смеси сильной кислоты и неионного детергента с последующей нейтрализацией, коррекцией pH и отмывкой.
В одном из вариантов осуществления способа стадию деминерализации осуществляют при температуре 18-25°С 0,6M раствором HCl в сочетании с 1% Тритон X-100 в течение 1-24 часов с дальнейшей нейтрализацией 0,5М NaOH при температуре 18-25°С и отмывкой в буферных растворах и/или деионизированной воде в течение 1-72 часов при температуре 1-8°С, причем предпочтительным является фосфатно-солевой буферный раствор.
В одном из вариантов осуществления способа перед стадией деминерализации костный материал предварительно высушивают при помощи сушильного шкафа или лиофильной сушки.
В одном из вариантов осуществления способа после отмывки проводят последующую обработку гидроксидом натрия в концентрации 0,5-20 г/л при температуре 1-8°С в течение 1-72 часов и проводят вторичную отмывку в буферных растворах и/или деионизированной воде проводят в течение 1-72 часов при температуре 1-8°С, причем предпочтительным является фосфатно-солевой буферный раствор.
Стадию стерилизации в сверхкритических средах проводят в условиях сверхкритического CO2 при давлении 250 бар и температуре 35-41°С в течение 1-3 часов, причем предпочтительной является температура 37-40°С.
В одном из вариантов осуществления способа изначально проводят статическое насыщение биологического материала сверхкритическим растворителем при температуре 35-41°С в течение 1-3 часов.
В одном из вариантов осуществления способа стерилизацию в сверхкритических средах проводят посредством постоянной подачи CO2 при скорости 1,5-5 кг/ч.
В одном из вариантов осуществления способа соотношение объема камеры и объема стерилизуемой биологической ткани должно составлять 1:20-1:200.
Полученный биологический матрикс может быть импрегнирован фосфатидилхолином и/или холестерином, с включенными желатином (гидролизованным коллагеном), и/или костным ателоколлагеном, и/или поли(е-капролактоном), и/или биологически активными веществами (включая биоактивные пептиды и факторы роста), причем раствор фосфатидилхолина и/или холестерина в этаноле ресуспендируют в круглодонной колбе, водные растворы желатина и/или биологически активных веществ вносят в колбу и выпаривают в роторном испарителе для получения пленки. Далее в колбу вносят предварительно очищенный биологический матрикс и выпаривают на роторном испарителе при скорости вращения 100-300 об/мин и температуре 37°С. Причем соотношение фосфатидилхолина и/или холестерина и добавляемых веществ составляет от 1:20 до 1:100 на сухую массу, соответственно.
Преимуществом добавления ателоколлагена является его уменьшенная иммуногенность. Способы получения ателоколлагена известны, и описаны, например, в заявке US 20130071645 A1.
В одном из вариантов осуществления способа непосредственно после образования пленки раствор ресуспендируют в фосфатно-солевом буферном растворе в присутствии стеклянных шариков, после чего шарики извлекают, а полученный раствор подвергают ультразвуковой сонификации в присутствии предварительно очищенного костного матрикса с использованием погружного ультразвукового сонификатора.
В одном из вариантов осуществления способа сонификацию осуществляют при температуре 1-6°С в течение 2-15 минут.
В одном из вариантов осуществления способа импрегнацию биологически активными веществами проводят на стадии стерилизации в сверхкритических средах.
В одном из вариантов осуществления способа после всех стадий способа проводят лиофилизацию полученного биологического матрикса при температуре -20 – -80°С и давлении 20-130 Па в течение 24-72 часов.
Полученный по данному способу биорезорбируемый биологический матрикс может быть применен для заполнения дефектов костной ткани или в качестве имплантата в хирургии, причем дефекты костной ткани образовались в результате хирургического вмешательства, врожденных патологий, опухолей или травм различного генеза.
При осуществлении изобретения достигаются следующие технические результаты:
- разработан способ получения биологического матрикса, обладающего повышенной остео- и биоинтеграцией, оптимальной скоростью биодеградации, высокой биосовместимостью, отсутствием иммунореактивности со стороны реципиента, высокой способностью к остеокондукции, выраженным остеогенным потенциалом при остеосинтезе и костной пластике.
- разработан биологический матрикс, который состоит из костного коллагена, гидроксиапатита и/или фосфата кальция, причем костный коллаген в настоящем матриксе представлен в нативной невосстановленной форме с полностью сохраненной трехмерной структурой, гидроксиапатит и фосфат кальция представлены в нативной аморфной форме, а сам матрикс, очищенный от клеточного дебриса, чужеродных липидов, нуклеиновых кислот и иммуногенов, содержит остаточные количества костных морфогенетических белков и может быть дополнительно модифицирован везикулярным фосфатидилхолином и/или холестерином, с включенными гидролизованным коллагеном и/или ателоколлагеном и/или поли(е-капролактоном), а также, факультативно, различными биологически активными веществами (такими как биоактивные пептиды и факторы роста), посредством импрегнации.
Краткое описание чертежей
Фиг. 1 Обобщенная схема способа получения биорезорбируемого биологического матрикса в предпочтительном варианте изобретения
Фиг. 2 Макрофотография поверхности биологического матрикса
Фиг. 3 Гистологический срез биологического матрикса (окраска гематоксилин-эозином)
Фиг. 4 Микроэлектронограмма поверхности биологического матрикса
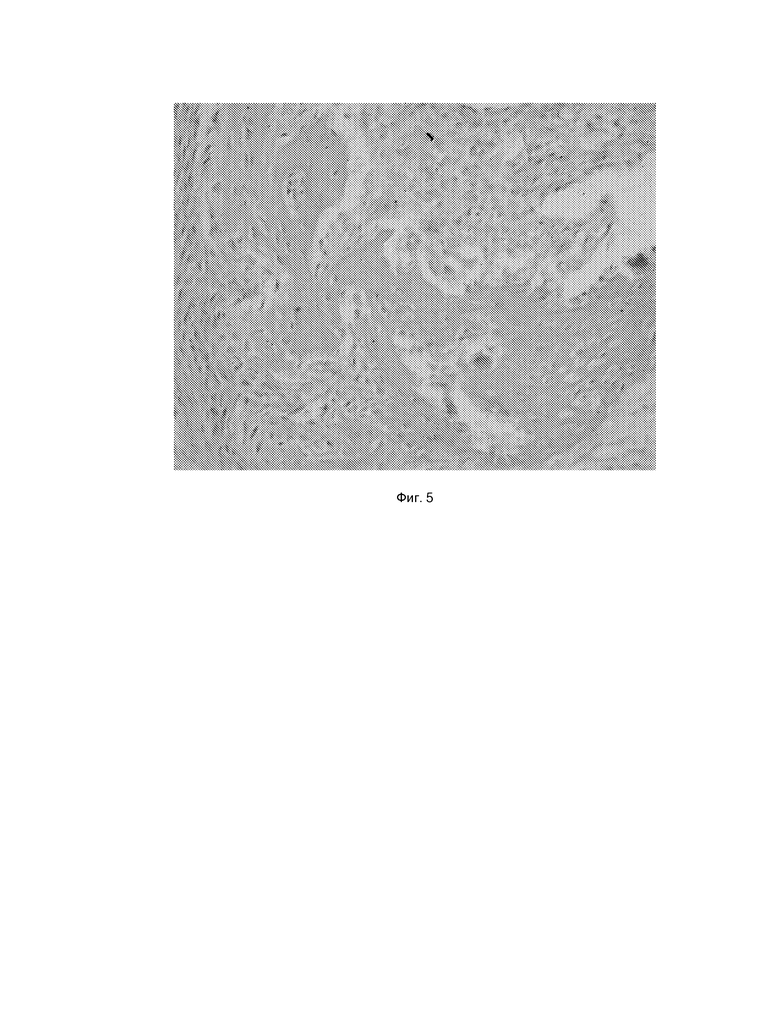
Фиг. 5 Формирование костно-хрящевой мозоли на 30-е сутки
Фиг. 6 Полное сращение костной ткани на 60-е сутки
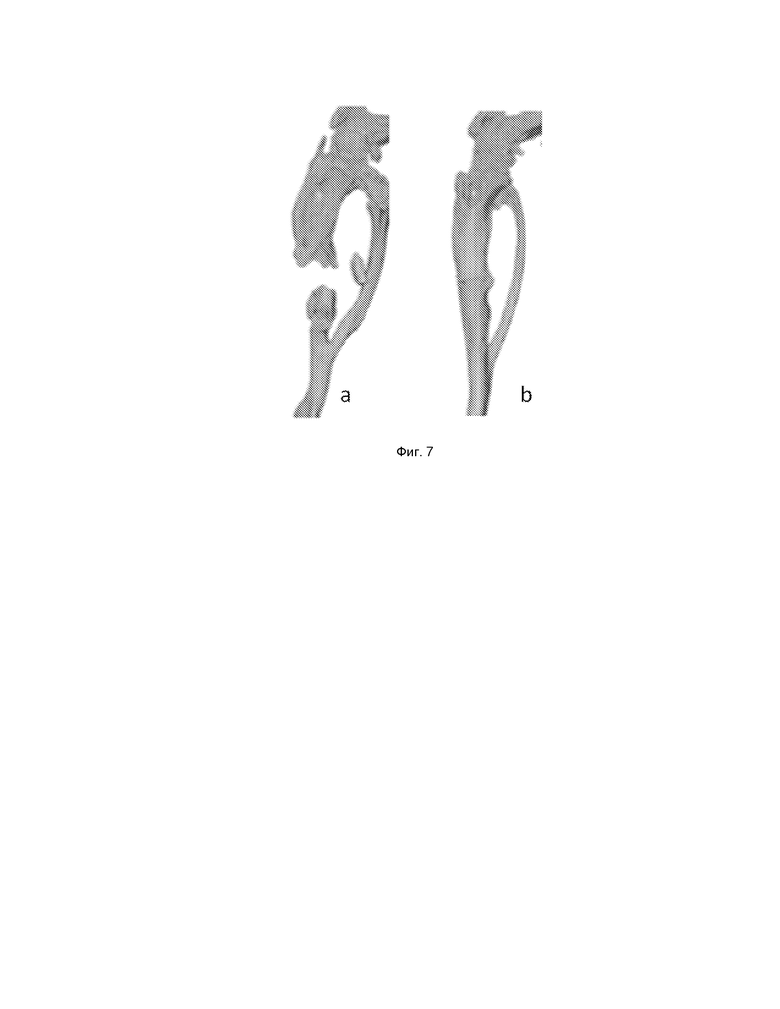
Фиг. 7 Рентгенограмма костного сращения: a – контрольная группа; b – опытная группа
Осуществление изобретения
В описании данного изобретения термины «включает», «включающий» и «включает в себя» интерпретируются как означающие «включает, помимо всего прочего». Указанные термины не предназначены для того, чтобы их истолковывали как «состоит только из».
Если не определено отдельно, технические и научные термины в данной заявке имеют стандартные значения, общепринятые в научной и технической литературе.
В качестве биологического материала для осуществления изобретения может быть использован любой фрагмент органа или ткани млекопитающего. В предпочтительном варианте изобретения используется ауто-, алло- или ксено- материал костной ткани млекопитающего.
Биоактивные пептиды или факторы роста, которые могут быть импрегнированы для повышения остеокондуктивных или остеоиндуктивных свойств в очищенный матрикс, приготовленный в соответствии с одним из вариантов изобретения, включают в себя костные морфогенетические белки (BMP-1, BMP-2, BMP-3, BMP-4, BMP-5, BMP-6, BMP-7, BMP-8, BMP-9, BMP- 10, BMP-1 1, BMP-12, BMP- 13, BMP- 15, BMP-16, BMP-17, BMP-18), факторы роста эндотелия сосудов (VEGF-A, VEGF-B, VEGF-C, VEGF-D, VEGF-E), трансформирующие ростовые факторы бета (TGF-в-l, TGF-в- 2, TGF-в-3), факторы стволовых клеток (SCF), тромбоцитарные факторы роста (PDGF-A, PDGF-B, PDGF-C, PDGF-D), инсулиноподобные факторы роста (IGF), факторы роста фибробластов (FGF), ростовые факторы соединительной ткани (CTGF-1, CTGF-2, CTGF-3), Остеопротегерин (sRANKL).
Нижеследующие примеры приведены в целях раскрытия характеристик настоящего изобретения и их не следует рассматривать как каким-либо образом ограничивающие объем изобретения.
Пример получения биорезорбируемого матрикса
Для получения эффективного и безопасного биорезорбируемого биологического матрикса для замещения дефектов костной ткани был разработан и экспериментально протестирован способ, состоящий из нескольких последовательных стадий – стадия предварительной обработки биологического материала, грубой очистки и фракционирования, глубокой очистки и экстракции, делипидирования, ферментации, деминерализации и стерилизации в сверхкритических средах.
На стадии предварительной обработки в целях очистки от остатков крови, жиров и соединительной ткани биологический образец подвергается нескольким циклам замораживания и оттаивания, обработке в растворе перекиси водорода и антибиотиков/антимикотиков (дезинфектантов), причем замораживание осуществляют при температуре -20 – -40°С, а оттаивание - при комнатной температуре на водяной бане.
На стадии грубой очистки и фракционирования в целях разделения биологического образца, в данном случае костной ткани млекопитающего, осуществляют отделение губчатого слоя от кортикального слоя и/или отделение диафиза от метафиза и эпифиза, и/или отделение периостального и среднего слоя от эндостального, причем периостальный слой отделяют на глубину 8-10 мм.
На стадии глубокой очистки и экстракции, в целях децеллюляризации и очистки от антигенов и дебриса, образец обрабатывают в растворе ионных и амфотерных поверхностно-активных веществ при температуре 37-41°С, далее в целях осаждения поверхностно-активных веществ осуществляют отмывку в буферных растворах при температуре 1-8°С, далее производят нейтрализацию ионных поверхностно-активных веществ, причем в качестве ионных поверхностно-активных веществ используют додецилсульфат натрия и/или 3-[(3-холамидопропил) диметиламмонио]-1-пропансульфонат в концентрации 0,1-10%, для нейтрализации и ренатурации используют Тритон Х-100 в концентрации 0,1-5% и/или Tween-20 в концентрации 0,005-1%, а экстракцию осуществляют с использованием ультразвукового дезинтегратора.
На стадии делипидирования в целях очистки от остатков жирных кислот и липидов образец обрабатывают в растворе этанола и/или этанола-хлороформа и/или этанола-этилацетата и толуола, причем после делипидирования осуществляют обработку гидроксидом натрия в концентрации 0,5-20 г/л.
На стадии ферментации проводят обработку в растворах ДНКазы и/или трипсина, причем обработку трипсином осуществляют в присутствии магния хлорида в концентрации 0,05-5 мМ.
На стадии деминерализации осуществляют обработку раствором сильной кислоты с последующей нейтрализацией гидроксидом натрия; на стадии стерилизации в сверхкритических средах осуществляют обработку сверхкритическим СО2, причем изначально проводят статическое насыщение образца сверхкритическим растворителем при температуре 35-41°С в течение 1-3 часов с дальнейшей постоянной подачей СО2 со скоростью 1,5-5 кг/ч.
В целях улучшения остеоиндуктивных свойств биологического матрикса готовый очищенный биологический образец импрегнируют эмульгированным везикулярным фосфатидилхолином и холестерином с дополнительно включенными веществами. Для этого, раствор фосфатидилхолина и/или холестерина с добавками выпаривают в роторном испарителе для получения околостенной пленки, ресуспендируют в фосфатно-солевом буфере, а импрегнацию осуществляют с использованием ультразвукового дезинтегратора. В качестве дополнительно включенных в жировые везикулы веществ используют желатин (гидролизованный коллаген), и/или костный ателоколлаген, и/или поли-(е-капролактон), а также, в предпочтительном варианте реализации, могут быть включены биологически активные вещества, такие как биоактивные пептиды или факторы роста. Вместо поли(е-капролактона) может быть использован другой биодеградируемый синтетический полимер.
Таким образом, при прохождении процедуры образец биологической ткани подвергается: (1) очистке и дезинфекции; (2) ручной или автоматизированной очистке от мягких тканей и фиброзного слоя периоста с последующим фракционированием и дезинфицирующей отмывкой; (3) стадийной обработке ионными/амфотерными и неионными детергентами с промежуточной и окончательной отмывкой; (4) делипидированию с отмывкой в случае необходимости; (5) ферментации с последующей отмывкой; (6) деминерализации с последующей отмывкой; (7) стерилизации в сверхкритических средах и (8) импрегнации эмульгированным везикулярным фосфатидилхолином/холестерином с включенными биологически активными веществами (в том числе биоактивными пептидами и факторами роста).
Вышеописанный способ позволяет получить биологический матрикс для замещения дефектов костной ткани, состоящий из костного коллагена, гидроксиапатита и/или фосфата кальция, причем костный коллаген в настоящем матриксе представлен в нативной невосстановленной форме с полностью сохраненной трехмерной структурой, гидроксиапатит и фосфат кальция представлены в нативной аморфной форме, а сам матрикс, очищенный от клеточного дебриса, чужеродных липидов, нуклеиновых кислот и иммуногенов, содержит остаточные количества костных морфогенетических белков, обладает остеокондуктивным и остеоиндуктивным потенциалом, удовлетворительными физико-механическими свойствами, является стерильным и может быть представлен в различных формах.
При этом, полученный биорезорбируемый биологический матрикс может быть представлен в форме блока, крошки, мелкодисперсного порошка, пасты, мембраны, пластины. На различных стадиях описанного способа, предпочтительно на стадии стерилизации в условиях сверхкритических сред или непосредственно после данной стадии, в биологический матрикс могут быть импрегнированы синтетический полимер поли-(е-капролактон), гидролизованный коллаген, ателоколлаген, биоактивные пептиды, факторы роста, антибиотики, антисептики, анестетики по отдельности или их комбинации, при этом данные вещества вводятся в составе жировых везикул, состоящих из фосфатидилхолина и/или холестерина.
Причем полученный биорезорбируемый биологический матрикс непосредственно перед применением может быть обогащен аутологичной стромально-васкулярной фракцией, культурой мезенхимальных стволовых клеток, кондиционированной культуральной средой, обогащенной тромбоцитами плазмой или аутокровью. Методы приготовления стромально-васкулярной фракции и культуры мезенхимальных стволовых клеток хорошо известно специалистам, и описано в многочисленных источниках (например, в заявке WO 2016044780 A1).
Полученный вышеуказанным способом биорезорбируемый биологический матрикс может применяться в клинической практике, а именно в травматологии, ортопедии, стоматологии и ортодонтии для заполнения дефектов костной ткани при лечении врожденных патологий, травм различного генеза, доброкачественных опухолей, для использования в качестве имплантата и как носитель лекарственного средства.
Характеризация полученного биорезорбируемого матрикса
Опытные образцы биологического матрикса были получены из бедренной кости крупного рогатого скота. Образцы были отмыты и обработаны дезинфектантами, и приготовлены согласно вышеописанной процедуре. Костный матрикс был фракционирован на удобные для использования блоки, содержащие как кортикальный слой, так и губчатый слой.
В качестве контрольных показателей оценивали морфологию образцов, обсемененность (стерильность) костного матрикса по количеству колониеобразующих единиц (КОЕ) (согласно ГОСТ ISO 11737-2-2011), содержание остаточных липидов (Базарнова Ю.Г., Теоретические основы методов исследования пищевых продуктов, 2014; Скурихина И.М., Химический состав пищевых продуктов, 1987), содержание остаточной ДНК (ДНК-Сорб-С, AmpliSens; детекцию проводили флуорометрическим методом), содержание кальция (согласно ГОСТ ISO 12081-2013), содержание белка (по Кьельдалю по ГОСТ 938.7-68 в модификации – Фармакопейная статья МЗ РФ), уровень pH и влажности (анализатор влагосодержания MB35, Ohaus).
Образцы костного матрикса были поделены на группы: (1) нативная ткань – костная ткань, не подвергавшаяся обработке (n=10); (2) БМ – деминерализованный биологический матрикс (n=10); (3) БМ/СКС – деминерализованный биологический матрикс, дополнительно обработанный в условиях сверхкритических сред; (4) БМ/ИМП – деминерализованный биологический матрикс, импрегнированный везикулярным фосфатидилхолином и холестерином с включенным гидролизованным коллагеном. Результаты сравнительного анализа контрольных показателей испытуемых групп представлен в таблице 1. Данные представлены как среднее и стандартное отклонение – M (у).
Таблица 1
Сравнительный анализ контрольных показателей костного матрикса
Для оценки сохранения структуры проводили ультраструктурное исследование поверхности биологического матрикса на растровом электронном микроскопе. Было показано, что после обработки биологический матрикс полностью сохраняет свою трехмерную организацию. Наиболее показательные результаты представлены на фиг. 2, 3, 4.
Поверхность скола образца представляла собой пористую структуру, состоящую из: микропор размерностью 0,5-1 мкм, которые, переплетаясь, образовывали микропористую сеть: поры размерностью 10-20 мкм, а также больших полостных образований (50-100 мкм). Поры пронизывают всю толщу образца. Инородных включений в порах не наблюдалось. На внешней поверхности пор нет, была видна щелевидная и плотная структура материала.
Для оценки остеоиндуктивности биологического матрикса использовали экспериментальную модель (Мигулева И.Ю. Две новые модели экспериментального дефекта кости на голени крысы для исследования регенерации костной ткани после пластики различными материалами, 2015).
Содержание экспериментальных животных и уход за ними в условиях вивария были стандартными и соответствовали требованиям Европейской конвенции (Страсбург, 1986) и Хельсинской декларации Всемирной медицинской ассоциации о гуманном обращении с животными (1996). Все манипуляции с животными проводились в соответствии со стандартами ISO 10993-1-2003 и ГОСТ Р ИСО 10993.2-2006. При выполнении исследований были соблюдены требования приказа МЗ СССР № 755 от 12.08.1977 г. «О мерах по дальнейшему совершенствованию организационных форм работы с использованием экспериментальных животных», приложения к приказу МЗ СССР № 755 от 12.08.1977 г. «Правила проведения работ с использованием экспериментальных животных» и Федерального закона, принятого Государственной Думой 01.12.1999 г., «О защите животных от жестокого обращения».
Наркотизированным животным открывали доступ к большеберцовой кости, рассекали мышечный слой и надкостницу и на передней поверхности большеберцовой кости выполняли пропил ближе к метафизарной зоне, где кость имеет расширение и более толстую стенку. В образовавшийся дефект вводили биологический матрикс и ушивали рану. На 30-е и 60-е сутки животных выводили из эксперимента.
Результаты исследования показали, что биологический матрикс обладает остеоиндуктивными свойствами и способен вызывать регенерацию костной ткани. На 30 сутки после имплантации во всех опытных группах наблюдается формирование костно-хрящевой мозоли. Наиболее показательные результаты представлены на фиг. 5. Через 60 суток после имплантации при полном отсутствии асептического воспаления наблюдали полное сращение и регенерацию костной ткани во всех опытных группах. Наиболее репрезентативные результаты представлены на фиг. 6. На рентгенограмме на фиг. 7 хорошо видны признаки костного сращения по сравнению с группой контроля, а образовавшаяся костно-хрящевая мозоль по плотности аналогична здоровой костной ткани большеберцовой кости.
Таким образом, в настоящем изобретении описан способ получения биологического матрикса для замещения дефектов костной ткани, включающий в себя стадии: (1) предварительной обработки биологического материала; (2) грубой очистки и фракционирования; (3) глубокой очистки и экстракции; (4) делипидирования; (5) ферментации; (6) деминерализации; (7) стерилизации в сверхкритических средах.
Вышеописанный биологический матрикс, состоящий из костного коллагена, гидроксиапатита и/или фосфата кальция, отличается тем, что костный коллаген представлен в нативной невосстановленной форме с полностью сохраненной трехмерной структурой, гидроксиапатит и фосфат кальция представлены в нативной аморфной форме, а сам матрикс, очищенный от клеточного дебриса, чужеродных липидов, нуклеиновых кислот и иммуногенов, содержит остаточные количества костных морфогенетических белков, обладает остеокондуктивным и остеоиндуктивным потенциалом, удовлетворительными физико-механическими свойствами, является стерильным и может быть представлен в различных формах, причем биологический матрикс может быть импрегнирован везикулярным фосфатидилхолином и/или холестерином, в который дополнительно включены желатин (гидролизованный коллаген), и/или костный ателоколлаген, и/или поли-(е-капролактон) с комплексом биологически активных веществ (таких как биоактивные пептиды или факторы роста), и дополнительно стерилизован и очищен в условиях сверхкритических сред.
Хотя настоящее изобретение было подробно описано на примерах вариантов, которые представляются предпочтительными, необходимо помнить, что эти примеры осуществления изобретения приведены только в целях иллюстрации изобретения. Данное описание не должно рассматриваться как ограничивающее объем изобретения, поскольку в этапы описанных способов и устройств специалистами в области медицинской биотехнологии и клеточной технологии и др. могут быть внесены изменения, направленные на то, чтобы адаптировать их к конкретным устройствам или ситуациям, и не выходящие за рамки прилагаемой формулы изобретения. Специалисту в данной области понятно, что в пределах сферы действия изобретения, которая определяется пунктами формулы изобретения, возможны различные варианты и модификации, включая эквивалентные решения.
Ссылки
1. CA2690457 A1 Patent. Bone matrix compositions and methods. Keyvan Behnam, Guobao Wei, Nanette Forsyth, Todd M. Boyce, Lawrence A. Shimp, 2008.
2. EP 1418866 A2 Patent. Xenograft bone matrix for orthopedic applications. Kevin R. Stone, Thomas J. Turek, 2004.
3. Fages J, Poirier B, Barbier Y, Frayssinet P, Joffret ML, Majewski W, Bonel G, Larzul D. Viral inactivation of human bone tissue using supercritical fluid extraction. ASAIO J. 1998; 44(4):289-93.
4. US 6565884 B2 Patent. Bone graft material incorporating demineralized bone matrix and lipids. Marcel E. Nimni, 2003.
5. US 7959941 B2 Patent. Bone graft comprising a demineralized bone matrix and a stabilizing agent. David Knaack, Kathy Traianedes, Michele Diegman, Nanette Forsyth, John Winterbottom, 2011.
6. US 8202539 B2 Patent. Demineralized bone matrix compositions and methods. Keyvan Behnam, Guobao Wei, James Beisser, 2012.
7. US 8328876 B2 Patent. Bone matrix compositions and methods. Keyvan Behnam, Christopher Cioffi, 2012.
8. US 8470520 B2 Patent. Decellularization and recellularization of organs and tissues. Harald Ott, Doris Taylor, 2013.
9. US 8992964 B2 Patent. Process for demineralization of bone matrix with preservation of natural growth factors. Nancy J. Shelby, Steven M. Scott, Benjamin P. Luchsinger, Gregory A. Juda, Kelly R. Kirker, Jesus Hernandez, Darrel L. Holmes, 2015.
10. US 9029077 B2 Patent. Manufacturing method for fibrous demineralized bone matrix. Seok-beom Song, Goo-Won Jeong, Jung-Won So, Han-Sol Seo, Hyun-Seung Ryu, Giue-Nam Kim, Byoung-Suck Kim, 2015.
11. US7357947 B2 Patent. Bone graft material incorporating demineralized bone matrix and lipids. Marcel E. Nimni, 2008.
12. Базарнова Ю.Г. Теоретические основы методов исследования пищевых продуктов, С-Пб, 2014.
13. Мигулева И.Ю., Савотченко А.М. Две новые модели экспериментального дефекта кости на голени крысы для исследования регенерации костной ткани после пластики различными материалами // Вопросы реконструктивной и пластической хирургии. 2015. № 2(53).
14. Скурихина И.М. Химический состав пищевых продуктов, М., 1987.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ДЕМИНЕРАЛИЗОВАННОГО КОСТНОГО МАТРИКСА В ВИДЕ КРОШКИ | 2011 |
|
RU2456003C1 |
| СПОСОБ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ ВЫСОКООЧИЩЕННОГО МИНЕРАЛЬНОГО МАТРИКСА В ВИДЕ СЕГМЕНТОВ И ГРАНУЛ С ОСТЕОИНДУКТИВНЫМИ СВОЙСТВАМИ ДЛЯ ЗАМЕЩЕНИЯ КОСТНЫХ ДЕФЕКТОВ | 2018 |
|
RU2693606C1 |
| Способ получения средства для регенерации кости, содержащего рекомбинантный белок ВМР-2, и его применение | 2022 |
|
RU2781921C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ КОСТНЫХ ИМПЛАНТОВ | 2013 |
|
RU2526429C1 |
| ЛИОФИЛИЗИРОВАННЫЙ БИОЛОГИЧЕСКИЙ БИОДЕГРАДИРУЕМЫЙ МИНЕРАЛИЗОВАННЫЙ КОСТНОПЛАСТИЧЕСКИЙ МАТЕРИАЛ И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2019 |
|
RU2722266C1 |
| Биокомпозитный сфероид для восстановления костей и способ его получения | 2020 |
|
RU2744732C1 |
| СПОСОБ ПОЛУЧЕНИЯ НИЗКОЩЕЛОЧНОГО МАТЕРИАЛА НА ОСНОВЕ ПРИРОДНОГО ГИДРОКСИАПАТИТА ИЗ КОСТНОЙ ТКАНИ | 2023 |
|
RU2816361C1 |
| Способ получения оптимизированного твердого ген-активированного материала, способ получения твердого матрикса носителя, оптимизированный твердый ген-активированный материал для регенерации тканей | 2016 |
|
RU2623171C1 |
| Способ восстановления резорбированной альвеолярной костной ткани биоинженерной конструкцией из децеллюляризированных тканей зуба человека | 2019 |
|
RU2716594C1 |
| СПОСОБ СОЗДАНИЯ ПЕРСОНАЛИЗИРОВАННОГО ГЕН-АКТИВИРОВАННОГО ИМПЛАНТАТА ДЛЯ РЕГЕНЕРАЦИИ КОСТНОЙ ТКАНИ | 2015 |
|
RU2597786C2 |




Группа изобретений относится к медицине, а именно к биотехнологии, и может быть использована для получения биорезорбируемого биологического матрикса для замещения дефектов костной ткани из ксеногенной или аллогенной костной ткани. Способ включает следующие последовательные стадии: a) стадию предварительной обработки указанной ксеногенной или аллогенной костной ткани, включающую один или более цикл его замораживания при температурах от -20 до -80°C и оттаивания при температурах от +5 до +37°C; b) стадию глубокой очистки и экстракции материала, полученного на предыдущей стадии, включающую обработку этого материала в растворе ионного или ионного и амфотерного детергента в буферном растворе, затем, факультативно, отмывку в буферном растворе, затем дальнейшую обработку в растворе неионного детергента, за которой следует экстракция материала с использованием ультразвукового дезинтегратора; c) стадию делипидирования материала, полученного на предыдущей стадии, включающую обработку материала в растворе этанола, и/или этанола-хлороформа, и/или этанола-этилацетата и толуола, а затем обработку гидроксидом натрия; d) стадию ферментации материала, полученного на предыдущей стадии, включающую в себя обработку материала в растворах ДНКазы и/или трипсина; e) стадию деминерализации материала, полученного на предыдущей стадии, включающую в себя обработку материала раствором сильной кислоты с последующей нейтрализацией гидроксидом натрия; f) стадию пропитывания, включающую в себя импрегнацию материала, полученного на предыдущей стадии, везикулярным фосфатидилхолином и/или холестерином, в который включены желатин (гидролизованный коллаген), и/или костный ателоколлаген, и/или поли-(е-капролактон). Группа изобретений относится также к применению биорезорбируемого биологического матрикса для заполнения дефектов костной ткани или в качестве импланта в хирургии. Использование данной группы изобретений позволяет получить биологический матрикс, обладающий повышенной остео- и биоинтеграцией, высокой биосовместимостью и отсутствием иммунореактивности со стороны реципиента. 3 н. и 19 з.п. ф-лы, 1 табл., 7 ил.
1. Способ получения биорезорбируемого биологического матрикса для замещения дефектов костной ткани из ксеногенной или аллогенной костной ткани, включающий следующие последовательные стадии:
a. стадию предварительной обработки указанной ксеногенной или аллогенной костной ткани, включающую один или более цикл его замораживания при температурах от -20 до -80°C и оттаивания при температурах от +5 до +37°C;
b. стадию глубокой очистки и экстракции материала, полученного на предыдущей стадии, включающую обработку этого материала в растворе ионного или ионного и амфотерного детергента в буферном растворе, затем, факультативно, отмывку в буферном растворе, затем дальнейшую обработку в растворе неионного детергента, за которой следует экстракция материала с использованием ультразвукового дезинтегратора;
c. стадию делипидирования материала, полученного на предыдущей стадии, включающую обработку материала в растворе этанола и/или этанола-хлороформа и/или этанола-этилацетата и толуола, а затем обработку гидроксидом натрия;
d. стадию ферментации материала, полученного на предыдущей стадии, включающую в себя обработку материала в растворах ДНКазы и/или трипсина;
e. стадию деминерализации материала, полученного на предыдущей стадии, включающую в себя обработку материала раствором сильной кислоты с последующей нейтрализацией гидроксидом натрия;
f. стадию пропитывания, включающую в себя импрегнацию материала, полученного на предыдущей стадии, везикулярным фосфатидилхолином и/или холестерином, в который включены желатин (гидролизованный коллаген), и/или костный ателоколлаген, и/или поли-(е-капролактон).
2. Способ по п. 1, характеризующийся тем, что между стадией предварительной обработки/глубокой очистки и стадией экстракции проводят дополнительную стадию грубой очистки и фракционирования материала, полученного на стадии предварительной обработки/глубокой очистки, при которой происходит отделение губчатого слоя от кортикального слоя и/или отделение диафиза от метафиза и эпифиза, и/или отделение периостального и среднего слоя от эндостального.
3. Способ по п. 2, характеризующийся тем, что отделение периостального и среднего слоя от эндостального производят на глубину 8-10 мм.
4. Способ по п. 1, характеризующийся тем, что на стадии глубокой очистки и экстракции в качестве ионного детергента используют додецилсульфат натрия и/или 3-[(3-холамидопропил)диметиламмонио]-1-пропансульфонат в концентрации 0,1-10%, применяемые при температуре 37-41°C; а в качестве неионного детергента используют Тритон Х-100 в концентрации 0,1-5% и/или Tween-20 в концентрации 0,005-1%, применяемые при температуре 1-8°C.
5. Способ по п. 1, характеризующийся тем, что между стадиями деминерализации и пропитывания проводят дополнительную стадию стерилизации материала, полученного на стадии деминерализации, включающую в себя обработку материала сверхкритическим диоксидом углерода.
6. Способ по п. 5, характеризующийся тем, что на стадии стерилизации проводят статическое насыщение материала сверхкритическим диоксидом углерода при температуре 35-41°C в течение 1-3 часов с постоянной подачей диоксида углерода со скоростью 1,5-5 кг/ч.
7. Способ по п. 1, характеризующийся тем, что на стадии пропитывания дополнительно производят импрегнацию материала биоактивными пептидами и/или факторами роста.
8. Способ по п. 1, характеризующийся тем, что на стадии пропитывания импрегнацию материала осуществляют с использованием ультразвукового дезинтегратора.
9. Биорезорбируемый биологический матрикс для замещения дефектов костной ткани, полученный по способу, изложенному по любому из пп. 1-8, состоящий из костного коллагена, гидроксиапатита и фосфата кальция, а также содержащий везикулярный фосфатидилхолин и/или холестерин, в который включены желатин (гидролизованный коллаген), и/или костный ателоколлаген, и/или поли-(ε-капролактон), при этом данный матрикс характеризуется тем, что костный коллаген представлен в нативной невосстановленной форме с сохраненной трехмерной структурой; гидроксиапатит и фосфат кальция представлены в нативной аморфной форме; а сам матрикс, очищенный от клеточного дебриса, чужеродных липидов, нуклеиновых кислот и иммуногенов, обладает остеокондуктивным и остеоиндуктивным потенциалом, является стерильным и может быть представлен в различных формах.
10. Биорезорбируемый биологический матрикс по п. 9, отличающийся тем, что представлен в форме блока.
11. Биорезорбируемый биологический матрикс по п. 9, отличающийся тем, что представлен в форме крошки, мелкодисперсного порошка, пасты, мембраны или пластины.
12. Биорезорбируемый биологический матрикс по п. 9, отличающийся тем, что содержит липиды, в том числе фосфатидилхолин и/или холестерин.
13. Биорезорбируемый биологический матрикс по п. 9, отличающийся тем, что содержит синтетические полимеры, в том числе поли(ε-капролактон).
14. Биорезорбируемый биологический матрикс по п. 9, отличающийся тем, что дополнительно содержит аутологичную стромально-васкулярную фракцию.
15. Биорезорбируемый биологический матрикс по п. 9, отличающийся тем, что дополнительно содержит мезенхимальные стволовые клетки, добавленные в процессе импрегнации.
16. Биорезорбируемый биологический матрикс по п. 9, отличающийся тем, что дополнительно содержит обогащенную тромбоцитами плазму крови человека, добавленную в процессе импрегнации.
17. Биорезорбируемый биологический матрикс по п. 9, отличающийся тем, что дополнительно содержит аутокровь.
18. Биорезорбируемый биологический матрикс по п. 9, отличающийся тем, что содержит ателоколлаген.
19. Биорезорбируемый биологический матрикс по п. 9, отличающийся тем, что содержит биоактивные пептиды и/или факторы роста.
20. Биорезорбируемый биологический матрикс по п. 9, отличающийся тем, что дополнительно содержит антибиотик, антимикотик, антисептик и/или анестетик.
21. Применение биорезорбируемого биологического матрикса по п. 9 для заполнения дефектов костной ткани или в качестве имплантата в хирургии.
22. Применение биорезорбируемого биологического матрикса по п. 21, отличающееся тем, что дефекты костной ткани образовались в результате хирургического вмешательства, врожденных патологий, опухолей или травм различного генеза.
| US 20150190547 A1, 09.07.2015 | |||
| СПОСОБ ПОЛУЧЕНИЯ МАТЕРИАЛА ДЛЯ ОСТЕОПЛАСТИКИ И ПОЛУЧЕННЫЙ ЭТИМ СПОСОБОМ МАТЕРИАЛ | 1992 |
|
RU2104703C1 |
| WO 2009100454 A1, 13.08.2009 | |||
| ADRIANA VINCE et al | |||
| DNA extraction from archival Giemsa-stained bone-marrow slides: comparison of six rapid methods // British Jurnal of Haematology, 1998, 101, 349-351. | |||
Авторы
Даты
2018-09-05—Публикация
2017-03-17—Подача