Заявляемое изобретение относится к области химии и касается способа получения нового сложного оксида лантана, молибдена и теллура, который может быть использован для получения лантансодержащих теллуритно-молибдатных стекол.
К настоящему времени известно единственное соединение, относящееся к сложному оксиду лантана, молибдена и теллура состава La2MoTe3O12, получаемому по твердофазной реакции из оксидов:
La2O3+MoO3+3TeO2→La2MoTe3O12.
Реакцию проводят при температуре 700°С в течение 7 суток (Inorganic Chemistry 44 (2005) 9314-9321). Указанное соединение может быть использовано в качестве компонента шихты для получения многокомпонентных теллуритных стекол.
Недостатком указанного соединения является то, что его состав не входит в область стеклования тройной системы TeO2-MoO3-La2O3. Поэтому соединение La2MoTe3O12 в индивидуальном состоянии не может быть использовано для получения лантансодержащих теллуритно-молибдатных стекол. Кроме этого, еще одним существенным недостатком метода получения указанного сложного оксида La2MoTe3O12 является длительность его синтеза.
Задачей изобретения является разработка нового способа получения нового сложного оксида лантана, молибдена и теллура, который может быть использован не только в качестве компонента шихты наряду с другими соединениями, но и в качестве единственного исходного вещества для синтеза лантансодержащих теллуритно-молибдатных стекол.
Техническим результатом от использования предлагаемого изобретения является упрощение способа получения сложного оксида теллура, молибдена и лантана и лантансодержащих теллуритно-молибдатных стекол.
Это достигается тем, что способ получения сложного оксида лантана, молибдена и теллура La2MoTe6O18 включает растворение исходных соединений по отдельности в дистиллированной воде, в качестве которых используют гексагидрат нитрата лантана La(NO3)3⋅6H2O, тетрагидрат гептамолибдата аммония (NH4)6Mo7O24⋅4H2O и ортотеллуровую кислоту H6TeO6, смешивание полученных растворов, выпаривание полученной смеси досуха, измельчение и прокаливание полученного сухого остатка при температуре 600°С до получения порошка белого цвета, причем используют такие навески исходных компонентов, чтобы выполнялось атомное соотношение La:Mo:Те, равное 2:1:6.
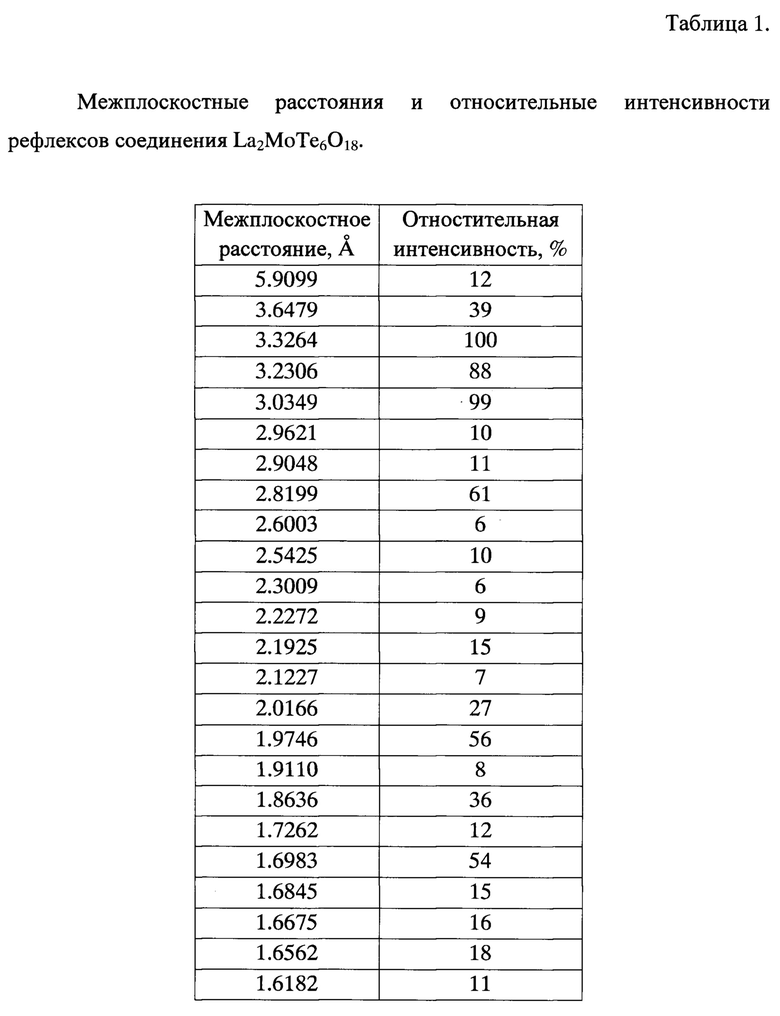
На фиг. 1 представлена порошковая рентгенограмма соединения, зарегистрированная на дифрактометре Shimadzu LabX XRD-6000 (Cu Kα).
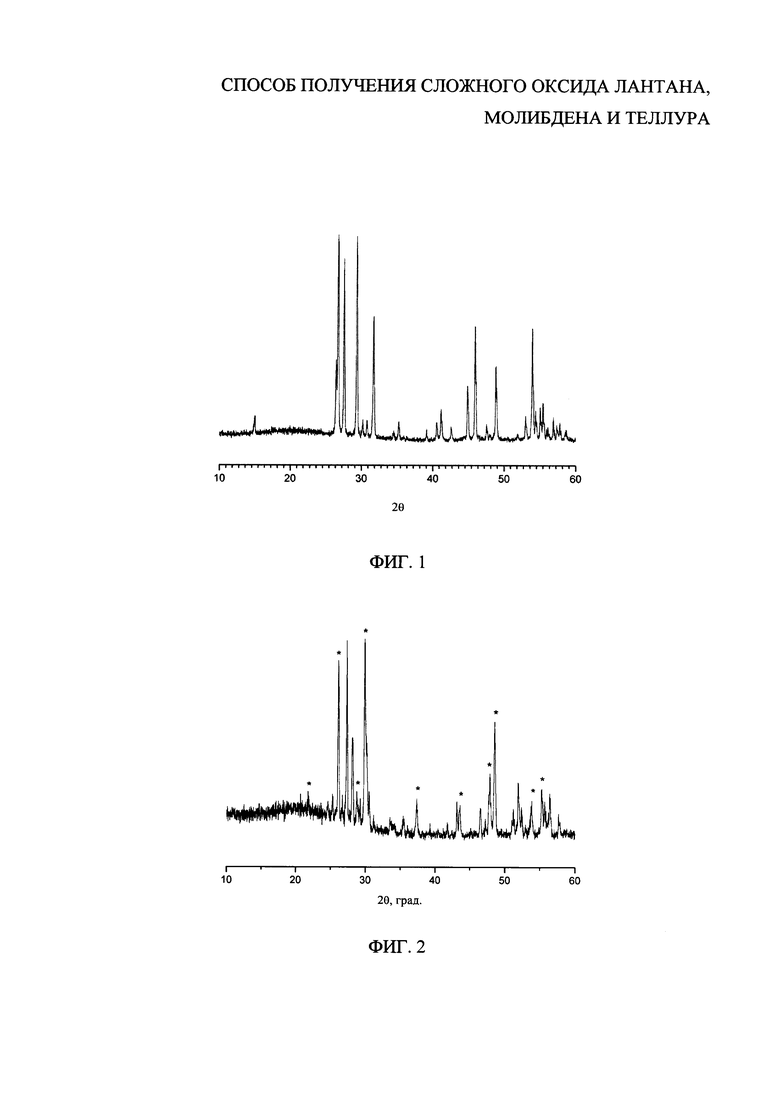
На фиг. 2 представлена порошковая рентгенограмма смеси, в которой атомное отношение La:Mo:Te равно 2:1:7. На рентгенограмме отмечены рефлексы, характерные для TeO2 (JCPDS 01-0870).
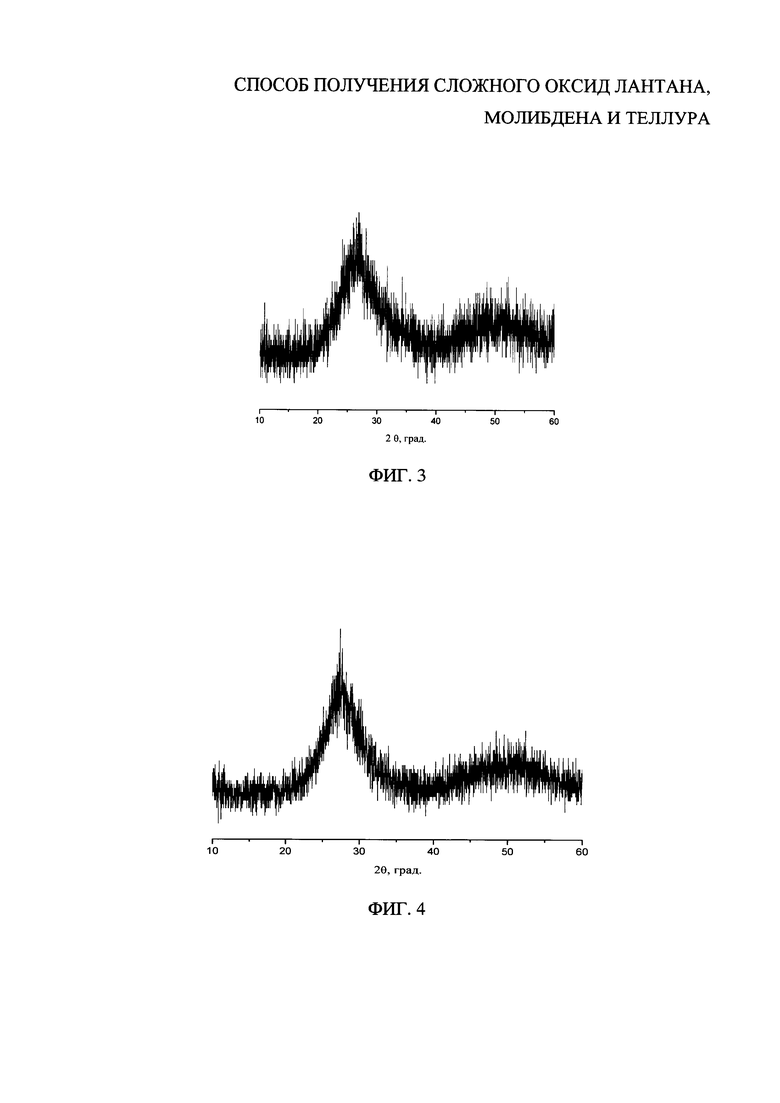
На фиг. 3 представлена рентгенограмма измельченного в порошок стекла, полученного охлаждением расплава сложного оксида La2MoTe6O18.
На фиг. 4 представлена рентгенограмма измельченного в порошок стекла состава 58TeO2-29MoO3-13LaO1.5, полученного из смеси сложного оксида La2MoTe6O18, оксида молибдена МоО3 и оксида теллура TeO2.
В таблице 1 представлены данные порошковой рентгенографии соединения La2MoTe6O18.
Отличительной особенностью предлагаемых исходных соединений является их способность растворяться в воде. Другим характерным свойством предлагаемых исходных соединений является их способность разлагаться при нагревании с образованием оксидов и летучих продуктов. Таким образом, сложный оксид предлагается получать по следующей реакции:
28La(NO3)3⋅6H2O+2(NH4)6Mo7O24⋅4H2O+84H6TeO6→
14La2MoTe6O18+84NO2+54O2+452H2O+6N2
При синтезе сложного оксида La2MoTe6O18 должно выполняться мольное соотношение n(La2O3) : n(МоО3) : n(TeO2), равное 1:1:6, что соответствует мольному отношению n(La(NO3)3⋅6H2O) : n((NH4)6Mo7O24⋅4H2O) : n(H6TeO6), равному 2:1/7:6.
Для получения сложного оксида La2MoTe6O18 отбирают навески исходных соединений таким образом, чтобы на 2 моль гексагидрата нитрата лантана (что соответствует массе 886 г), приходилась 1/7 моль тетрагидрата гептамолибдата аммония (что соответствует массе 176.6 г), и 6 моль ортотеллуровой кислоты (что соответствует массе 1377.6 г). Далее навески исходных соединений по отдельности растворяют в дистиллированной воде. Далее растворы смешивают и полученную смесь выпаривают досуха. При этом образуется мелкодисперсный аморфный осадок, который измельчают и прокаливают при температуре не менее 600°С. Наличие в заявляемом методе синтеза стадии образования мелкодисперсного аморфного осадка позволяет ускорить процесс взаимодействия между исходными веществами, так как скорость гетерогенной реакции зависит от размера реагирующих между собой частиц и увеличивается при уменьшении их размера. Идентификацию полученного предложенным методом нового сложного оксида La2MoTe6O12 проводили методом рентгенофазового анализа.
Полученный сложный оксид лантана, молибдена, теллура имеет химическую формулу La2MoTe6O18. Состав данного соединения входит в область стеклообразования тройной системы TeO2-MoO3-La2O3.
Если при синтезе соединения La2MoTe6O18 нарушить атомное отношение La : Mo : Те, равное 2:1:6, и изменить содержание любого из компонентов, то в результате прокаливания получается смесь веществ. Кроме синтезируемого La2MoTe6O18, в системе будет присутствовать оксид того макрокомпонента, содержание которого было превышено. Температура прокаливания может превышать 600°С, но это не улучшает качество продукта синтеза и поэтому не целесообразно. При температурах ниже 600°С целевая твердая фаза не образуется либо содержит примеси исходных веществ или промежуточных продуктов реакции либо не обладает достаточной кристалличностью.
В рентгенограмме полученного соединения La2MoTe6O18 отсутствуют рефлексы, относящихся к исходным веществам La(NO3)3⋅6H2O, (NH4)6Mo7O24⋅4H2O, H6TeO6 и продуктам их термического разложения La2O3, MoO3 и TeO2. Это свидетельствует о том, что в системе произошло химическое взаимодействие и было получено новое химическое соединение, обладающее собственной кристаллической структурой, которая характеризуется межплоскостными расстояниями, представленными в таблице 1.
В заявленном изобретении недостатки способа по прототипу устраняются за счет того, что в качестве исходных соединений используют не оксиды элементов, а другие производные элементов, а именно, гексагидрат нитрата лантана, тетрагидрат гептамолибдата аммония и ортотеллуровую кислоту, причем используют навески исходных компонентов таких масс, чтобы выполнялось атомное соотношении La : Mo : Те, равное 2:1:6.
Более высокое содержание теллура в полученном соединении по сравнению с известным соединением La2MoTe3O12 обеспечивает возможность использования полученного соединения не только в качестве компонента шихты наряду с другими соединениями, но и в качестве единственного вещества в составе шихты для синтеза лантансодержащих теллуритно-молибдатных стекол.
Ниже представлен пример конкретного осуществления предлагаемого изобретения.
Пример. 1.
Гексагидрат нитрата лантана массой 3.4635 г, тетрагидрат гептамолибдата аммония массой 0.7056 г, ортотеллуровую кислоту массой 5.5246 г растворяли в воде, растворы смешивали, и эту смесь выпаривали досуха на воздухе на электрической плитке. Сухой остаток измельчали в фарфоровой ступке, помещали в фарфоровый тигель и прокаливали при 600°С в течение 5 часов. Дифрактограмму полученного соединения регистрировали на дифрактометре Shimadzu LabX XRD-6000. Дифрактограмма полученного соединения совпадает с дифрактограммой, приведенной в таблице 1.
Пример. 2.
Гексагидрат нитрата лантана массой 3.4635 г, тетрагидрат гептамолибдата аммония массой 0.7056 г, ортотеллуровую кислоту массой 6.4400 г (отношение атомов La : Mo : Те равно 2:1:7) растворяли в воде, растворы смешивали, и эту смесь выпаривали досуха на воздухе на электрической плитке. Сухой остаток измельчали в фарфоровой ступке, помещали в фарфоровый тигель и прокаливали при 600°С в течение 5 часов. Дифрактограмму порошка продукта синтеза регистрировали дифрактометром Shimadzu LabX XRD-6000. В этой дифрактограмме (фиг. 2) присутствуют пики, соответствующие целевому соединению и диоксиду теллура, так как относительное содержание атомов теллура в исходной смеси превышает таковое в целевом соединении.
Пример 3.
Шихту, представляющую собой навеску сложного оксида La2MoTe6O18 массой 3.5929 г, помещали в фарфоровый тигель и подвергали плавлению в муфельной печи при 850°С. Полученный расплав выливали в стальную форму, разогретую до 350°С, и медленно охлаждали до комнатной температуры. После охлаждения расплав представлял собой стекло состава 67TeO2-11MoO3-22LaO1.5. Стеклообразное состояние подтверждено методом рентгенофазового анализа (фиг. 3).
Пример 4.
Для получения стекла необходимого состава в шихту, кроме соединения La2MoTe6O18 добавляли рассчитанные массы бинарных оксидов. Так, для синтеза 5.0000 г стекла состава 58TeO2-29МоО3-13LaO1.5 смешивали навески сложного оксида La2MoTe6O18 массой 2.9789 г, оксида молибдена МоО3 массой 1.0479 г и оксида теллура TeO2 массой 0.9734 г. Далее полученную смесь помещали в фарфоровый тигель и подвергали плавлению в муфельной печи при 850°С. Полученный расплав выливали в стальную форму, разогретую до 350°С, и медленно охлаждали до комнатной температуры. После охлаждения полученный твердый образец представляет собой стекло. Стеклообразное состояние подтверждено методом рентгенофазового анализа (фиг. 4).
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРИМЕНЕНИЕ СЛОЖНОГО ОКСИДА ЛАНТАНА, МОЛИБДЕНА И ТЕЛЛУРА | 2018 |
|
RU2684087C1 |
| СЛОЖНЫЙ ОКСИД ЛАНТАНА, МОЛИБДЕНА И ТЕЛЛУРА | 2018 |
|
RU2683834C1 |
| СПОСОБ ПОЛУЧЕНИЯ МНОГОКОМПОНЕНТНЫХ ТЕЛЛУРИТНЫХ СТЕКОЛ | 2015 |
|
RU2584474C1 |
| ПРИМЕНЕНИЕ СЛОЖНОГО ОКСИДА ПРАЗЕОДИМА, МОЛИБДЕНА И ТЕЛЛУРА PrMoTeO | 2018 |
|
RU2713841C1 |
| СПОСОБ ПОЛУЧЕНИЯ СЛОЖНОГО ОКСИДА ПРАЗЕОДИМА, МОЛИБДЕНА И ТЕЛЛУРА PrMoTeO | 2018 |
|
RU2687420C1 |
| ШИХТА ДЛЯ ПОЛУЧЕНИЯ ТЕЛЛУРИТНЫХ СТЕКОЛ (ВАРИАНТЫ) | 2015 |
|
RU2584482C1 |
| СЛОЖНЫЙ ОКСИД ПРАЗЕОДИМА, МОЛИБДЕНА И ТЕЛЛУРА PrMoTeO | 2018 |
|
RU2690812C1 |
| ПРИМЕНЕНИЕ СЛОЖНОГО ОКСИДА ПРАЗЕОДИМА, МОЛИБДЕНА И ТЕЛЛУРА PrMoTeO | 2018 |
|
RU2686941C1 |
| СПОСОБ ПОЛУЧЕНИЯ СЛОЖНОГО ОКСИДА ЛАНТАНА, ВОЛЬФРАМА И ТЕЛЛУРА LaWTeO | 2018 |
|
RU2686828C1 |
| СПОСОБ ПОЛУЧЕНИЯ СЛОЖНОГО ОКСИДА ПРАЗЕОДИМА, МОЛИБДЕНА И ТЕЛЛУРА PrMoTeO | 2018 |
|
RU2687419C1 |
Изобретение относится к области химии и касается способа синтеза сложного оксида лантана, молибдена и теллура, который может быть использован для получения лантансодержащих теллуритно-молибдатных стекол. Способ получения сложного оксида лантана, молибдена и теллура La2MoTe6O18 включает растворение по отдельности в дистиллированной воде исходных соединений, в качестве которых используют гексагидрат нитрата лантана La(NO3)3⋅6H2O, тетрагидрат гептамолибдата аммония (NH4)6Mo7O24⋅4H2O и ортотеллуровую кислоту H6TeO6. Затем осуществляют смешивание полученных растворов, упаривание выпавшего осадка досуха, измельчение и прокаливание полученного сухого остатка при температуре 600°С до получения порошка белого цвета. При этом используют навески исходных компонентов таких масс, чтобы выполнялось атомное соотношение La:Mo:Te, равное 2:1:6. Полученный La2MoTe6O18 может быть использован не только в качестве компонента шихты наряду с другими соединениями, но и в качестве единственного исходного вещества для синтеза лантансодержащих теллуритно-молибдатных стекол, что значительно упрощает процесс их получения и получение самого оксида. 4 ил., 1 табл., 4 пр.
Способ получения сложного оксида лантана, молибдена и теллура La2MoTe6O18, включающий растворение исходных соединений по отдельности в дистиллированной воде, в качестве которых используют гексагидрат нитрата лантана La(NO3)3⋅6H2O, тетрагидрат гептамолибдата аммония (NH4)6Mo7O24⋅4H2O и ортотеллуровую кислоту H6TeO6, смешивание полученных растворов, выпаривание полученной смеси досуха, измельчение и прокаливание полученного сухого остатка при температуре 600°С до получения порошка белого цвета, причем используют такие навески исходных компонентов, чтобы выполнялось атомное соотношение La:Mo:Те, равное 2:1:6.
| ШИХТА ДЛЯ ПОЛУЧЕНИЯ ТЕЛЛУРИТНЫХ СТЕКОЛ (ВАРИАНТЫ) | 2015 |
|
RU2584482C1 |
| СПОСОБ ПОЛУЧЕНИЯ МНОГОКОМПОНЕНТНЫХ ТЕЛЛУРИТНЫХ СТЕКОЛ | 2015 |
|
RU2584474C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОСОБО ЧИСТЫХ ТЕЛЛУРИТНО-МОЛИБДАТНЫХ СТЕКОЛ | 2011 |
|
RU2484026C1 |
| YUE-LING SHEN et al., Luminescent Lanthanide Selenites and Tellurites Decorated by MoO 4 Tetrahedra or MoO 6 Octahedra: Nd 2 MoSe 2 O 10 , Gd 2 MoTe 3 O 12 , La 2 MoTe 3 O 12 and Nd 2 MoTe 3 O 12 , "Inorganic Chemistry", 2005, 44, 9314-9321. | |||
Авторы
Даты
2019-04-02—Публикация
2018-07-23—Подача