ОБЛАСТЬ ТЕХНИКИ
Изобретение относится к области биотехнологии и может быть использовано для получения биомассы бруцелл в технологии приготовления биопрепаратов на их основе.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
В качестве основы для приготовления различных препаратов для диагностики бруцеллеза в настоящее время широко используется вакцинный штамм 19ВА Brucella abortus [RU 2163141 C1, 20.02.2001]. Кроме того, для специфической профилактики бруцеллеза у сельскохозяйственных животных применяются живые вакцины из штаммов 19 В. abortus и Rev-1 B. melitensis [Наставление по применению вакцины живой сухой против бруцеллеза сельскохозяйственных животных из штамма бруцелла абортус 19 (1996), Наставление по применению вакцины живой нативной из штамма Rev-1 бруцелла мелитензис для иммунизации баранов против инфекционного эпидидимита (1995)]. Основным этапом технологии изготовления указанных препаратов является процесс получения микробной биомассы возбудителя бруцеллеза с необходимой концентрацией и в достаточном объеме. В биотехнологии для получения стандартизованных культур микробов достаточно глубоко разработан и нашел широкое практическое применение способ периодического глубинного культивирования.
Для глубинного выращивания бруцелл в технологии приготовления биопрепаратов чаще всего используют жидкие питательные среды на основе перевара Хоттингера с высоким содержанием белкового компонента с добавлением глицерина, глюкозы и дрожжевого экстракта [Девришов Д.А., Кузнецов С.М., Шведов Д.В. и др. Сравнительная оценка ростовых свойств питательной среды для приготовления живой бруцеллезной вакцины из штамма Rev-1 // Ветеринарная медицина.- 2007. - №1. - С. 6-7, Лузан Н.С. Усовершенствование промышленных технологий производства бруцеллезной вакцины и диагностикумов из штамма Brucella abortus 19. - Дисс… канд. биол. наук. - Щелково, 2001. - 124 с.]. Однако необходимо отметить, что высокое содержание гидролизата ценного пищевого продукта в составе среды существенно удорожает ее стоимость и определяет наличие большого количества балластных примесей в получаемых культурах.
Имеющиеся экспериментальные данные по динамике утилизации свободных аминокислот в процессе выращивания бруцелл позволяют сделать вывод о том, что большинство питательных сред, используемых при получении биопрепаратов, содержат в своем составе белковые гидролизаты в концентрации, значительно превышающей питательные потребности данного микроорганизма [Юдин Ю.И., Жаворонкова Л.В., Шабалин Б.А. и др. Оценка возможности использования «минимизированных» питательных сред на основе различных гидролизатов для глубинного выращивания бруцелл // Материалы Всероссийской научно-практической конференции, посвященной 60-летию филиала ФГУ «48 ЦНИИ Минобороны России - ЦВТП БЗ» «Актуальные проблемы биологической защиты войск и населения. Диагностика, лечение и профилактика опасных инфекционных заболеваний. Эпидемиология и эпизоотология. Микробиология. Биотехнология. Экология», 16 июля 2009 г., Екатеринбург. - Екатеринбург, 2009. - С. 111-113]. Данное обстоятельство указывает на принципиальную возможность снижения количества белкового компонента в используемой питательной среде.
Известен способ получения бруцеллезного антигена из штамма Brucella abortus 19 для изготовления единого бруцеллезного антигена для реакции агглютинации (РА), реакции связывания комплемента (РСК) и реакции длительного связывания комплемента (РДСК), составной частью которого является получение микробной культуры методом глубинного выращивания в биореакторе [RU 2085212 С1, 15.08.1996]. Способ требует использования дорогостоящей питательной среды, при этом уровень накопления микробных клеток в глубинной культуре (около 30 млрд микробов/мл - величина определена при анализе технологической цепочки изготовления препарата) является средним и может быть повышен.
Известен способ получения бруцеллезного антигена штамма Brucella abortus 19 для изготовления единого бруцеллезного антигена для РА, РСК и РДСК, бруцеллезного антигена для Роз-бенгал пробы (РБП) и бруцеллезного антигена для кольцевой реакции (КР) с молоком, способ изготовления бруцеллезной диагностической сыворотки и диагностические наборы [RU 2361610 С1, 20.03.2008]. В приведенной группе изобретений описан наиболее близкий к заявляемому существующий глубинный способ получения микробной культуры штамма В. abortus 19, который имеет ряд недостатков: сравнительно высокий расход белкового гидролизата (перевара Хоттингера) на основе дорогостоящего пищевого сырья для приготовления среды, содержание которого составляет 25% по объему; повышенное содержание балластных примесей в связи с высокой концентрацией белкового компонента в используемой питательной среде (содержание аминного азота от 1,40 до 1,60 г/л); использование высоких концентраций посевного материала (от 3,5 до 5,0 млрд микробов/мл) на стадии производственного глубинного культивирования. Кроме того, в указанном способе не реализован достаточно известный метод подпитки микробной культуры субстратом в процессе глубинного выращивания, обеспечивающий стабильное повышение концентрации клеток в получаемой культуре.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Задачей предлагаемого способа является повышение выхода микробных клеток в глубинной культуре, снижение себестоимости используемой питательной среды, уменьшение содержания балластных примесей в получаемых препаратах.
Технический результат заключается в обеспечении достаточного накопления биомассы бруцелл вакцинных штаммов в глубинной культуре, снижении себестоимости используемой питательной среды и уменьшении содержания балластных примесей.
Для выполнения заявленного технического результата предлагается:
использование минимизированной по содержанию белкового компонента жидкой питательной среды;
культивирование бруцелл вакцинных штаммов в биореакторе в условиях дозирования глюкозы по заданной схеме, поддержания величины рН среды на определенном уровне путем автоматического дозированного введения раствора аммиака и регуляции парциального давления растворенного в культуральной жидкости кислорода на протяжении всего процесса культивирования.
Минимизированная жидкая питательная среда имеет следующий состав: ферментативный гидролизат мяса до содержания аминного азота в среде - от 0,45 до 0,55 г/л; дрожжевой экстракт сухой - 2,50 г/л; Fe2(SO4)3⋅3H2O - 7,00 мг/л; MnSO4⋅5H2O - 2,00 мг/л; KH2PO4 - 1,13 г/л; MgSO4⋅7H2O - 0,23 г/л; никотиновая кислота - 2,00 мг/л; тиамина хлорид - 0,20 мг/л; кальция пантотенат - 1,00 мг/л; глюкоза (суммарное количество за цикл выращивания) - 26,00 г/л, вода дистиллированная - до расчетного объема; рН среды - от 6,8 до 7,2 ед. рН.
Схема дозированного введения глюкозы предусматривает одномоментное введение ее в питательную среду перед засевом в концентрации 10,0 г/л, с 16 по 19 ч роста - непрерывное введение по 1,5 г/л в ч, с 20 по 24 ч роста - непрерывное введение по 2,0 г/л в час. Оптимальную величину показателя рН культуральной жидкости в диапазоне от 6,8 до 7,2 ед. рН поддерживают автоматическим дозированным введением 12,5% водного раствора аммиака.
По отношению к существующему способу предлагаемый способ имеет ряд отличий (таблица 1).

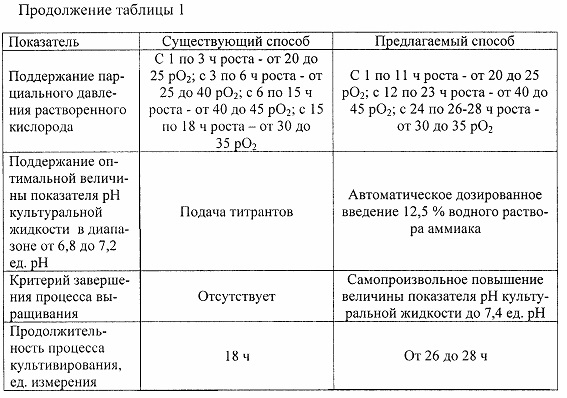
Применение заявляемого способа обеспечивает накопление микробных клеток в глубинной культуре в концентрации до 85-90 млрд микробов/мл, уменьшение себестоимости используемой жидкой питательной среды и снижение содержания белковых балластных примесей в микробной культуре. Продолжительность процесса глубинного культивирования составляет от 26 до 28 ч.
ОСУЩЕСТВЛЕНИЕ ИЗОБРЕТЕНИЯ
Заявляемое изобретение подтверждается следующими примерами практического применения.
Пример 1.
В варочный котел через капроновое сито наливают ферментативный гидролизат мяса и дистиллированную воду из расчета конечной концентрации аминного азота в среде от 0,45 до 0,55 г/л. Смесь тщательно перемешивают, кипятят в течение 5 мин, подщелачивают 20% раствором NaOH до величины рН от 6,8 до 7,2 ед. рН, добавляют навески солей, кипятят в течение 20-25 мин, после чего среду фильтруют через осветляющие пластины и разливают в бутыли вместимостью 20 л. Жидкую питательную среду переносят в биореактор и стерилизуют при температуре от 121 до 125°С в течение 45 мин, после чего охлаждают до температуры от 36 до 38°С. Раствор глюкозы с добавлением витаминов и раствор дрожжевого экстракта готовят отдельно, стерилизуют при температуре от 108 до 112°С в течение 20 мин и вводят в стерильную среду непосредственно перед ее засевом. Расчетная концентрация глюкозы в питательной среде перед засевом составляет 10,0 г/л. Засев питательной среды в биореакторе осуществляют микробной культурой штамма 19ВА В. abortus, выращенной в жидкой питательной среде на основе ферментативного гидролизата мяса аналогичного состава. Посевная доза (концентрация посевного материала) составляет от 0,5 до 1,0 млрд микробов/мл по стандарту мутности оптическому для определения концентрации микробов ОСО 42-28-85-2013.
Глубинное культивирование в биореакторе осуществляют по следующему режиму:
температура культивирования - от 36,5 до 37,5°С;
величина показателя рН культуральной жидкости - от 6,8 до 7,2 ед. рН;
парциальное давление растворенного кислорода (в процентах от насыщения) поддерживают по схеме: с 1 по 11 ч роста - от 20 до 25 pO2; с 12 по 23 ч роста - от 40 до 45 pO2; с 24 по 26-28 ч роста - от 30 до 35 pO2;
введение глюкозы в процессе выращивания осуществляют по схеме: с 16 по 19 ч роста - непрерывно по 1,5 г/л в час; с 20 по 24 ч роста непрерывно по 2,0 г/л в час.
Технологические параметры процесса глубинного культивирования поддерживают следующими управляющими воздействиями:
поддержание температуры - подачей термостатированной воды в рубашку биореактора;
поддержание величины показателя рН культуральной жидкости - автоматическим дозированным введением 12,5% водного раствора аммиака;
поддержание парциального давления растворенного кислорода - регуляцией расхода воздуха на аэрацию и изменением скорости вращения мешалки.
Введение 12,5% водного раствора аммиака в глубинную культуру осуществляют методом автоматического дозирования при снижении величины показателя рН культуральной жидкости менее 6,8 ед. рН. По окончании процесса культивирования при стабилизации величины показателя рН культуральной жидкости на уровне от 7,0 до 7,2 ед. рН перемешивание прекращают и проводят ее аэрацию в течение 0,5-3 ч. Критерием завершения процесса глубинного выращивания является самопроизвольное повышение рН культуральной жидкости до величины 7,4 ед. рН.
В полученной глубинной культуре штамма 19ВА В. abortus оценивают типичность морфологии микробов и наличие посторонней микрофлоры методом микроскопии мазков, окрашенных по Граму, определяют общую концентрацию микробов с использованием стандарта мутности оптического для определения концентрации микробов ОСО 42-28-85-2013 и содержание живых микробов методом высева соответствующих разведений на плотную питательную среду в чашках Петри.
С использованием заявляемого способа были получены 3 серии глубинной культуры штамма 19ВА В. abortus. Продолжительность культивирования составила от 26 до 28 ч.
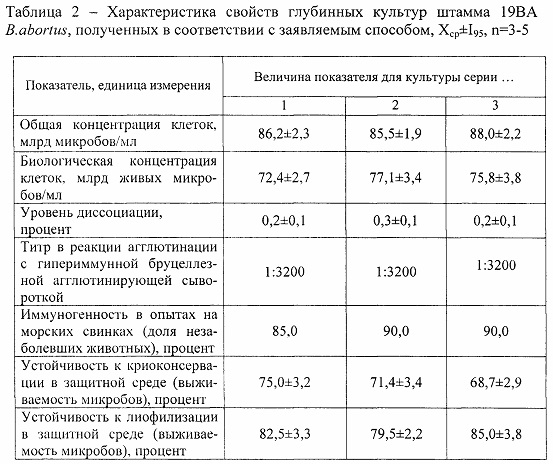
В таблице 2 представлены результаты оценки биологических свойств, антигенных и иммуногенных характеристик серий глубинных культур штамма 19ВА В. abortus с учетом их целевого назначения для использования при приготовлении вакцинных и диагностических препаратов.
При оценке иммуногенности морских свинок иммунизируют подкожно в дозе 2,0 млрд микробов по стандарту мутности оптическому для определения концентрации микробов ОСО 42-28-85-2013, через 28 сут. после иммунизации животных заражают культурой вирулентного штамма 16М В. melitensis в дозе 100 живых микробов. Иммуногенность культуры оценивают по доле незаболевших животных на основании данных бактериологического и серологического обследования через 30 сут. после заражения.
При оценке устойчивости к криоконсервации культуру стабилизируют защитной средой, замораживают при температуре от минус 18 до минус 22°С, хранят при указанной температуре в течение 3 сут., после чего реактивируют в течение 40 мин при температуре от 36 до 38°С и определяют выживаемость микробов.
Пример 2.
Глубинное выращивание культуры бруцелл проводят аналогично примеру 1, но вместо штамма 19ВА В. abortus используют штамм Rev-1 B. melitensis.
В глубинной культуре штамма Rev-1 B. melitensis оценивают типичность морфологии микробов и наличие посторонней микрофлоры методом микроскопии мазков, окрашенных по Граму, также определяют общую концентрацию микробов с использованием стандарта мутности оптического для определения концентрации микробов ОСО 42-28-85-2013 и содержание живых микробов путем посева соответствующих разведений на плотную питательную среду в чашках Петри.
С использованием заявляемого способа были получены 3 серии глубинной культуры штамма штамма Rev-1 B. melitensis. Продолжительность культивирования составила от 26 до 28 ч.
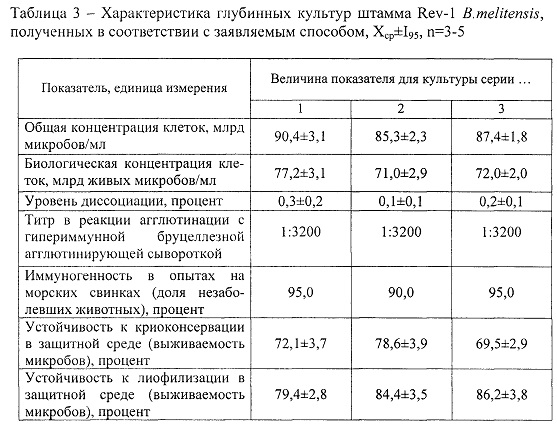
В таблице 3 представлены результаты оценки биологических свойств, антигенных и иммуногенных характеристик серий глубинных культур штамма Rev-1 B. melitensis с учетом их целевого назначения для использования при приготовлении вакцинных и диагностических препаратов. Оценку иммуногенности и устойчивости к криоконсервации осуществляют аналогично примеру 1.
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИГЕН ПОЛИВАЛЕНТНЫЙ КОРПУСКУЛЯРНЫЙ ДЛЯ ИЗГОТОВЛЕНИЯ ЛЕЧЕБНЫХ И ПРОФИЛАКТИЧЕСКИХ БИОПРЕПАРАТОВ ПРОТИВ БРУЦЕЛЛЕЗА | 2006 |
|
RU2330681C1 |
| Универсальная питательная среда плотная для выращивания биомассы бруцелл | 2020 |
|
RU2748808C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВАКЦИНЫ ПРОТИВ БРУЦЕЛЛЕЗА ДЛЯ ИММУНИЗАЦИИ ПОЗВОНОЧНЫХ ЖИВОТНЫХ (варианты) | 2020 |
|
RU2746141C1 |
| ОБОГАЩЕННАЯ ПИТАТЕЛЬНАЯ СРЕДА ПЛОТНАЯ ДЛЯ ВЫРАЩИВАНИЯ БИОМАССЫ БРУЦЕЛЛ | 2020 |
|
RU2756601C1 |
| Транспортная жидкая питательная среда для сохранения жизнеспособности бруцеллезного микроба | 2019 |
|
RU2725733C1 |
| БИФАЗНАЯ ТРАНСПОРТНАЯ ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ ВЫДЕЛЕНИЯ И ВЫРАЩИВАНИЯ БРУЦЕЛЛЕЗНОГО МИКРОБА | 2013 |
|
RU2529364C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОНЦЕНТРАТА КУЛЬТУРЫ КЛЕТОК БРУЦЕЛЛ ИЗ ШТАММА Brucella abortus 19 ДЛЯ ПРИГОТОВЛЕНИЯ БРУЦЕЛЛЕЗНЫХ АНТИГЕНОВ, БРУЦЕЛЛЕЗНЫЕ АНТИГЕНЫ (ТРИ ВАРИАНТА), СПОСОБ ИЗГОТОВЛЕНИЯ БРУЦЕЛЛЕЗНОЙ ДИАГНОСТИЧЕСКОЙ СЫВОРОТКИ И ТЕСТ-СИСТЕМЫ ДЛЯ ДИАГНОСТИКИ БРУЦЕЛЛЕЗА ЖИВОТНЫХ (ТРИ ВАРИАНТА) | 2014 |
|
RU2593712C2 |
| ПИТАТЕЛЬНАЯ СРЕДА ПЛОТНАЯ ДЛЯ КУЛЬТИВИРОВАНИЯ БРУЦЕЛЛ | 2019 |
|
RU2728379C1 |
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ ВЫРАЩИВАНИЯ МИКРООРГАНИЗМОВ | 1973 |
|
SU382682A1 |
| ПИТАТЕЛЬНАЯ СРЕДА ПЛОТНАЯ ДЛЯ КУЛЬТИВИРОВАНИЯ ВОЗБУДИТЕЛЯ БРУЦЕЛЛЁЗА | 2017 |
|
RU2688335C1 |
Изобретение относится к области биотехнологии. Предложен способ получения биомассы бруцелл вакцинных штаммов. Способ включает глубинное выращивание культуры бруцелл на минимизированной по содержанию белкового компонента жидкой питательной среде в условиях регуляции парциального давления растворенного в среде кислорода и дозированной подачи глюкозы по схеме: введение 10,0 г/л глюкозы в питательную среду перед засевом, затем непрерывное дозирование ее по 1,5 г/л в час с 16 по 19 ч роста и по 2,0 г/л в час с 20 по 24 ч роста. Способ обеспечивает повышение выхода биомассы бруцелл. 1 з.п. ф-лы, 3 табл.
Способ получения биомассы бруцелл вакцинных штаммов, заключающийся в том, что глубинное культивирование осуществляют при температуре от 36,5 до 37,5°C в минимизированной по содержанию белкового компонента жидкой питательной среде следующего состава: ферментативный гидролизат мяса и дистиллированная вода в объеме из расчета конечной концентрации аминного азота в среде от 45,0 до 55,0 мг%; дрожжевой экстракт сухой - 2,5 г/л; Fe2(SO4)3⋅3H2O - 7,0 мг/л; MnSO4⋅5H2O - 2,0 мг/л; KH2PO4 - 1,13 г/л; MgSO4⋅7H2O - 0,23 мг/л; никотиновая кислота - 2,0 мг/л; тиамина хлорид - 0,2 мг/л; кальция пантотенат - 1,0 мг/л;
с введением 10,0 г/л глюкозы в питательную среду перед засевом и непрерывным дозированием ее по 1,5 г/л в час с 16 по 19 ч роста и по 2,0 г/л в час с 20 по 24 ч роста;
с поддержанием величины рН культуральной жидкости в пределах от 6,8 до 7, 2 ед. рН путем дозирования 12,5% водного раствора аммиака; с регуляцией парциального давления растворенного в среде кислорода от 20 до 25 pO2 с 1 по 11 ч роста, от 40 до 45 pO2 - с 12 по 23 ч роста, от 30 до 35 pO2 с 24 по 26-28 ч роста.
2. Способ получения биомассы бруцелл вакцинных штаммов по п. 1, отличающийся тем, что концентрация посевного материала составляет от 0,5 до 1,0 млрд микробов/мл среды.
| СПОСОБ ПОЛУЧЕНИЯ КОНЦЕНТРАТА КУЛЬТУРЫ КЛЕТОК БРУЦЕЛЛ ИЗ ШТАММА Brucella abortus 19 ДЛЯ ПРИГОТОВЛЕНИЯ БРУЦЕЛЛЕЗНЫХ АНТИГЕНОВ, БРУЦЕЛЛЕЗНЫЕ АНТИГЕНЫ (ТРИ ВАРИАНТА), СПОСОБ ИЗГОТОВЛЕНИЯ БРУЦЕЛЛЕЗНОЙ ДИАГНОСТИЧЕСКОЙ СЫВОРОТКИ И ТЕСТ-СИСТЕМЫ ДЛЯ ДИАГНОСТИКИ БРУЦЕЛЛЕЗА ЖИВОТНЫХ (ТРИ ВАРИАНТА) | 2014 |
|
RU2593712C2 |
| Привод для запорного клапана насоса | 1931 |
|
SU25856A1 |
| ТОПКА ДЛЯ СЖИГАНИЯ ФРЕЗЕРОВАННОГО ТОРФА | 1929 |
|
SU18859A1 |
Авторы
Даты
2019-05-13—Публикация
2016-12-28—Подача