[0001] ПЕРЕКРЕСТНЫЕ ССЫЛКИ К РОДСТВЕННЫМ ЗАЯВКАМ
[0002] Настоящая заявка испрашивает приоритет предварительной патентной заявки США №62/126804, поданной 2 марта 2015 года, под названием «Модифицированная клетка и ее применение», которая включена в настоящее изобретение в качестве ссылки в полном объеме.
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
[0003] Настоящее изобретение относится к модифицированным клеткам и потребителям, в частности к композициям и способам снижения иммунной толерантности, связанным с CAR Т-клеточной терапией.
УРОВЕНЬ ТЕХНИКИ
[0004] Т-клеточная терапия продемонстрировала эффективность и терапевтический потенциал для лечения рака. Однако ее использование ограничено наличием иммуносупрессивного микроокружения. Иммуносупрессивное микроокружение включает в себя иммунную толерантность, вызванную взаимодействием белком запрограммированной смерти клетки (PD-1) и лигандом PD-L1 (PD-L1). PD-1 является отрицательным корецептором на поверхности Т-клеток и антиген-презентирующих клеток. PD-L1 экспрессируется на поверхности нескольких типов клеток (например, опухолевых клеток и других тканевых клеток) и, по-видимому, динамически регулируется иммунной микросредой. Таким образом, существует потребность в борьбе с иммунной толерантностью, вызванной PD-L1, в целях повышения эффективности Т-клеточной терапии.
Технический результат заявляемого изобретения заключается в обеспечении эффективной Т-клеточной терапии за счет уменьшения иммунной толерантности, индуцированной PD-L1 на опухолевых клетках»
[0005] КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0006] Варианты осуществления настоящего изобретения относятся к изолированной нуклеотидной последовательности, содержащей последовательность нуклеиновой кислоты, которая кодирует модифицированный белок запрограммированной смерти клетки 1 (PD-1), и последовательность нуклеиновой кислоты, которая кодирует химерный антигенный рецептор
(CAR). В некоторых вариантах осуществления изобретения, модифицированные PD-1 и CAR экспрессируются в виде генных продуктов, которые являются отдельными полипептидами.
[0007] В некоторых вариантах осуществления изобретения, CAR специфичен для опухолевого антигена, который присутствует в раковой клетке, и где раковая клетка экспрессирует PD-L1.
[0008] В некоторых вариантах осуществления изобретения, опухолевой антиген включает в себя HER2, CD19, CD20, CD22, каппа-частицы или легкую цепь, CD30, CD33, CD123, CD38, ROR1, ErbB3/4, EGFR, EGFRvIII, EphA2, FAP, карциноэмбриональный антиген, EGP2, EGP40, мезотелин, TAG72, PSMA, лиганды рецептора NKG2D, В7-Н6, IL-13 рецептор α2, IL-11 рецептор α, MUC1, MUC16, СА9, GD2, GD3, HMW-MAA, CD171, антиген Ley, G250/CAIX, HLA-AI MAGE A1, HLA-A2 NY-ESO-1, PSC1, рецептор фолата-α, CD44v7/8, 8H9, NCAM, рецепторы VEGF, 5T4, ацетилхолиновый рецептор фетального типа AchR, лиганды рецептора NKG2D, CD44v6, ТЕМ1, ТЕМ8 или антигены вируса, экспрессированные на опухоли.
[0009] В некоторых вариантах осуществления изобретения, последовательность нуклеиновой кислоты, которая кодирует модифицированный белок PD-1, включает замещение или делецию одного или нескольких нуклеотидов по сравнению с последовательностью нуклеиновой кислоты, кодирующей внутриклеточный домен белка PD-1 широкого типа.
[0010] В некоторых вариантах осуществления изобретения, последовательность нуклеиновой кислоты, которая кодирует модифицированный белок PD-1, включает делецию множества нуклеотидов по сравнению с последовательностью нуклеиновой кислоты, кодирующей внутриклеточный домен белка PD-1 широкого типа. В некоторых вариантах осуществления изобретения, модифицированный белок PD-1 содержит последовательность нуклеиновой кислоты согласно SEQ ID NO: 14.
[0011] В некоторых вариантах осуществления изобретения, последовательность нуклеиновой кислоты, которая кодирует модифицированный белок PD-1, содержит нуклеиновую кислоту, кодирующую усеченный белок PD-1, который не включает внутриклеточный домен. В некоторых вариантах осуществления изобретения, последовательность нуклеиновой кислоты, которая кодирует модифицированный белок PD-1, содержит последовательность нуклеиновой кислоты согласно SEQ ID NO: 12.
[0012] В некоторых вариантах осуществления изобретения, модифицированный белок PD-1 содержит одну или несколько точечных мутаций по сравнению с PD-1 широкого типа. В некоторых вариантах осуществления изобретения, точечная мутация содержит одну или две точечные мутации аминокислот сайтов фосфорилирования PD-1 широкого типа.
[0013] Варианты осуществления изобретения дополнительно относятся к экспрессирующему вектору, содержащему последовательность нуклеиновой кислоты, как описано выше. В некоторых вариантах осуществления изобретения, экспрессирующий вектор представляет собой вирусный вектор, выбранный из группы, состоящей из ретровирусного вектора, лентивирусного вектора, аденовирусного вектора и аденоассоциированного вирусного вектора.
[0014] Варианты осуществления изобретения дополнительно относятся к клетке, содержащей экспрессирующий вектор по настоящему изобретению. В некоторых вариантах осуществления изобретения клетка выбирается из группы, состоящей из Т-клетки, NK-клетки и NKT-клетки.
[0015] Варианты осуществления изобретения дополнительно относятся к фармацевтической композиции, содержащей эффективное количество Т-клеток человека для лечения опухоли, где множество Т-клеток человека включают изолированную нуклеотидную последовательность, как описано выше. В некоторых вариантах осуществления изобретения, ингибирующий эффект лиганда PD-L1 на продуцирование цитокинов Т-клеток человека меньше ингибирующего эффекта лиганда PD-L1 на продуцирование цитокинов Т-клеток человека, которые не содержат, по меньшей мере, часть последовательности нуклеиновой кислоты, кодирующей модифицированный PD-1.
[0016] Варианты осуществления изобретения дополнительно относятся к способу лечения рака у больного человека, причем способ включает введение пациенту фармацевтической композиции, описанной в настоящем изобретении.
[0017] Варианты осуществления изобретения дополнительно относятся к клетке, созданной для экспрессии модифицированных белков PD-1 и химерных антигенных рецепторов (CAR), где модифицированный белок PD-1 не включает трансмембранный домен или внутриклеточный домен PD-1 или их комбинацию. В некоторых вариантах осуществления изобретения, клетка экспрессирует растворимый PD-1, чтобы нарушить взаимодействие PD-1 с PD-L-1. В частности, растворимый PD-1 не присоединяется к клеточной мембране клетки.
[0018] Варианты осуществления изобретения дополнительно относятся к способу лечения и/или ингибирования рака у пациента. Способ включает введение пациенту терапевтически эффективного количества растворимого рецептора, включающего внеклеточный домен белка PD-1. В некоторых вариантах осуществления изобретения, растворимый рецептор связывает белок PD-L1 и прерывает сигнал, поступающий от белка PD-1 о раковых клетках и/или блокирует взаимодействие белков PD-1 и PD-L1. В некоторых вариантах осуществления изобретения, изолированный растворимый рецепторный полипептид включает аминокислотные остатки 20-519 согласно SEQ ID NO: 9.
[0019] Варианты осуществления изобретения дополнительно относятся к модифицированной клетке, включающей рецепторный полипептид, цитоплазменный домен рецепторного полипептида усечен, рецепторный полипептид представляет собой, по меньшей мере, рецепторный полипептид белка запрограммированной смерти клетки 1 (PD-1), рецепторный полипептид связанного белка 4 цитотоксического Т-лимфоцита (CTLA-4), или рецептор В- и Т-лимфоцитарного аттенюатора (BTLA).
[0020] Варианты осуществления изобретения дополнительно относятся к способу лечения пациента. Способ включает введение клетки пациенту, при этом клетка генетически модифицирована для экспрессии рецепторного полипептида, причем цитоплазматический домен рецепторного полипептида усекается, причем рецепторный полипептид представляет собой, по меньшей мере, рецепторный полипептид белка запрограммированной смерти клетки 1 (PD-1), рецепторный полипептид связанного белка 4 цитотоксического Т-лимфоцита (CTLA-4), или рецептор В- и Т-лимфоцитарного аттенюатора (BTLA); химерный антигенный рецептор (CAR) включает домен распознавания антигена специфического антитела и внутриклеточный домен или рецептор модифицированной Т-клетки или рецептор Т-клетки широкого типа, специфическое антитело связывается с антигеном.
[0021] В некоторых вариантах осуществления изобретения, рецепторный полипептид представляет собой рецепторный полипептид PD-1, при этом цитоплазматический домен рецепторного полипептида PD-1 содержит иммунорецепторный тирозиновый мотив.
[0022] Варианты осуществления изобретения дополнительно относятся к модифицированной клетке, содержащей уменьшенное количество одного или нескольких рецепторов по сравнению с соответствующей клеткой дикого типа, один или несколько рецепторов включают, по меньшей мере, белок запрограммированной смерти клетки 1 (PD-1), связанный белок 4 цитотоксического Т-лимфоцита (CTLA-4), или В- и Т-лимфоцитарный аттенюатор (BTLA).
[0023] Варианты осуществления изобретения дополнительно относятся к способу лечения пациента. Способ включает введение клетки пациенту, при этом клетка модифицирована для экспрессии сниженного количества одного или нескольких рецепторов по сравнению с соответствующей клеткой дикого типа, причем один или несколько рецепторов включают, по меньшей мере, белок запрограммированной смерти клетки 1 (PD-1), связанный белок 4 цитотоксического Т-лимфоцита (CTLA-4), или В- и Т-лимфоцитарный аттенюатор (BTLA).
[0024] В некоторых вариантах осуществления изобретения, модифицированная клетка дополнительно включает в себя химерный антигенный рецептор (CAR), содержащий домен распознавания антигена специфического антитела и внутриклеточный домен или рецептор модифицированной Т-клетки или рецептор Т-клетки широкого типа. В некоторых вариантах осуществления изобретения, модифицированная клетка дополнительно включает в себя химерный антигенный рецептор (CAR), содержащий домен распознавания антигена специфического антитела и внутриклеточный домен или рецептор модифицированной Т-клетки или рецептор Т-клетки широкого типа, специфическое антитело связывается с антигеном.
[0025] В некоторых вариантах осуществления изобретения, модифицированная клетка уменьшает экспрессию одного или более генов, связанных путем биосинтеза или переносным путем с одним или несколькими рецепторами по сравнению с соответствующей клеткой дикого типа, или их комбинацией. В некоторых вариантах осуществления модифицированная клетка включает деструкцию одного или нескольких генов. В некоторых вариантах осуществления модифицированная клетка включает частичную или полную делецию одного или нескольких генов. В некоторых вариантах осуществления генетически модифицированная клетка реплицируется в организме пациента.
[0026] В некоторых вариантах осуществления изобретения, модифицированные клетки образуют клетки памяти в организме пациента. В этих случаях модифицированные клетки вводят пациенту внутривенно. В некоторых вариантах осуществления изобретения, модифицированные клетки сохраняются в организме пациента. Например, модифицированная клетка является аутогенной Т-клеткой. В другом примере клетка может включать, по меньшей мере, В-клетку, Т-клетку, NK-клетку, эмбриональную клетку или дендритную клетку.
[0027] В некоторых вариантах осуществления изобретения, заболевание может включать, по меньшей мере, рак, иммунодефицит, аутоиммунное заболевание или ожирение.
[0028] Указанное краткое описание изобретения представлено для знакомства с определениями в упрощенной форме, более подробное описание приводится ниже. Настоящее краткое описание не предназначено для определения ключевых признаков или существенных признаков заявленного предмета изобретения и не предназначено для ограничения объема заявленного предмета.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0029] Приводится подробное описание изобретения со ссылкой на прилагаемые чертежи. Использование одинаковых порядковых номеров на разных рисунках указывает одинаковые или идентичные элементы.
[0030] Фиг. 1 - схематическая диаграмма, иллюстрирующая ДНК-конструкции Р0: CD19BBZETA, P1: CD19BBZETA-ires-растворимых PD1, Р2: CD19BBZETA-ires-усеченных PD1, Р3: CD19BBZETA-ires-точечная-мутация PD1, P4: CD19BBZETA-ires-делецию PD1.
[0031] Фиг. 2, включающая фиг. 2А и 2B, представляет собой серию изображений, показывающих экспрессию химерного антигенного рецептора CAR и модифицированного PD-1 на трансдуцированных клетках 293Т и K562. На фиг. 2А показана экспрессия химерного антигенного рецептора CAR на трансдуцированных клетках 293Т и К562. На фиг. 2В показана экспрессия модифицированного PD-1 на трансдуцированных клетках 293Т и K562.
[0032] Фиг. 3, включающая Фиг. 3А-3С, представляет собой серию изображений, показывающих экспрессию химерного антигенного рецептора CAR и модифицированного PD-1 на первичных Т-клетках. На фиг. 3А показана экспрессия химерного антигенного рецептора CAR на трансдуцированных первичных Т-клетках. На фиг. 3В и 3С показана экспрессия модифицированного PD-1 на трансдуцированных первичных Т-клетках.
[0033] Фиг. 4, включающая фиг. 4А и фиг. 4В, представляет собой серию изображений, показывающих цитотоксичность Т-клеток, трансдуцированных химерным антигенным рецептором CAR и модифицированным PD-1. На фиг. 4А показано выделение интерферон-гамма (IFN-Gamma) Т-клетками в количестве 104, трансдуцированными химерным антигенным рецептором CAR и модифицированными белками PD-1, при Е: Т коэффициент от 10: одно культивирование с клетками CD19 + в течение 24 часов. Фиг. 4В демонстрирует, что клетки CD19 + были разрушены Т-клетками в количестве 104, трансдуцированными химерным антигенным рецептором CAR и модифицированными белками PD-1, при Е: Т коэффициент от 10: одно культивирование в течение 24 часов.
[0034] Фиг. 5 показывает экспрессию PD-L1 на трансдуцированных клетках NalM6.
[0035] Фиг. 6, включающая фиг. 6А и 6В, представляет собой серию изображений, демонстрирующих, что модифицированный PD-1 снижает иммунную толерантность, вызванную лигандом PD-L1. На фиг. 6А показано выделение интерферон-гамма (IFN-Gamma) Т-клетками в количестве 104, трансдуцированными химерным антигенным рецептором CAR и модифицированными белками PD-1, при Е: Т коэффициент от 10: одно культивирование с клетками CD19 + и клетками CD19+/PD-L1+ в течение 24 часов. Эти результаты показывают, что ингибирование цитотоксичности, индуцированной PD-L1, снижается на Т-клетках, трансдуцированных химерным антигенным рецептором CAR и модифицированным PD-1.
[0036] Фиг. 6В иллюстрирует потерю цитотоксичности, индуцированную снижением PD-L1 на Т-клетках, трансдуцированных химерным антигенным рецептором CAR и модифицированным PD-1, по сравнению с Т-клетками, трансдуцированными только химерным антигенным рецептором CAR.
ДЕТАЛЬНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0037] Общее представление
[0038] Настоящее изобретение относится к обнаружению того факта, что иммунная толерантность, индуцированная PD-L1 при терапии Т-клетками с химерными антигенными рецепторами, может быть уменьшена путем экспрессии генетически модифицированного PD-1 на этих Т-клетках. В некоторых вариантах осуществления изобретения, указанные Т-клетки включают последовательность нуклеиновой кислоты, которая кодирует CAR и генетически модифицированный PD-1 таким образом, что модифицированные PD-1 и CAR экспрессируются в виде генных продуктов, которые являются отдельными полипептидами на указанных Т-клетках. Пример генетической модификации включает замещение или делецию одного или нескольких нуклеотидов, связанных с экспрессией или функцией внутриклеточного домена PD-1.
[0039] В некоторых вариантах осуществления, настоящее изобретение относится к Т-клетке, созданной для экспрессии CAR против CD19 и модифицированного PD-1 таким образом, что ингибирующее действие PD-L1 на продукцию цитокинов Т-клеток значительно меньше ингибирующего действия PD-L1 на продукцию цитокинов Т-клеток, которые не включают, по меньшей мере, часть последовательности нуклеиновой кислоты, которая кодирует модифицированный PD-1. В некоторых случаях CAR специфичен для опухолевого антигена, который присутствует в опухолевой клетке, и опухолевая клетка экспрессирует PD-L1. Следовательно, разработанная Т-клетка по настоящему изобретению при введении пациенту, может уменьшить иммунную толерантность, индуцированную PD-L1 на опухолевых клетках, и дополнительно исключить указанные опухолевые клетки в организме пациента.
[0040] Определения
[0041] Если в настоящем изобретении терминам не дано иное определение, все технические и научные термины, используемые здесь, имеют то же значение, которое обычно понимается специалистами в данной области техники, к которым относится изобретение. Несмотря на то, что любые способы и материалы, аналогичные или эквивалентные описанным в настоящем документе, могут быть использованы на практике или испытаниях настоящего изобретения, описаны предпочтительные способы и материалы. В целях реализации настоящего изобретения ниже приведены термины.
[0043] Под термином «около» понимается величина, уровень, значение, число, частота, процент, размерность, объем, количество, вес или длина, которые изменяются на 30, 25, 20, 15, 10, 9, 8, 7, 6, 5, 4, 3, 2 или 1% от эталонной величины, уровня, значения, числа, частоты, процента, размерности, объема, количества, веса или длины.
[0044] Используемый в настоящем документе термин «активация» относится к состоянию Т-клетки, которая была в достаточной степени стимулирована для индуцирования детектируемой клеточной пролиферации. Активация также может быть связана с индуцированным продуцированием цитокинов и детектируемыми эффекторными функциями. Термин «активированные Т-клетки» относится, среди прочего, к Т-клеткам, которые подвергаются делению клеток.
[0045] Термин «антитело» используется в самом широком смысле и конкретно охватывает моноклональные антитела (включая полноразмерные моноклональные антитела), мультиспецифические антитела (например, биспецифические антитела) и фрагменты антител, при условии, что они обладают желательной биологической активностью или функцией. Антитела в настоящем изобретении могут существовать в самых разных формах, включая, например, поликлональные антитела, моноклональные антитела, Fv, Fab и F(ab)2, а также одноцепочечные антитела и гуманизированные антитела (Харлоу и другие, 1999, «Применение антител: Лабораторное руководство», журнал «Cold Spring Harbor Laboratory Press», Нью-Йорк; Харлоу и другие, 1989, «Антитела: Лабораторное руководство», журнал «Cold Spring Harbor», Нью-Йорк; Хьюстон и другие, 1988, Заседание Национальной академии наук (Proc. Natl. Acad. Sci.) США 85: 5879-5883; Бёрд и другие, 1988, Science 242: 423-426).
[0046] Термин «фрагменты антитела» включают часть полноразмерного антитела, обычно антигенсвязывающую или вариабельную область антитела. Примеры фрагментов антител включают Fab, Fab', F(ab')2 и Fv-фрагменты, димеры, линейные антитела, молекулы одноцепочечных антител и мультиспецифические антитела, образованные из фрагментов антител.
[0047] Термин «Fv» представляет собой минимальный фрагмент антитела, который содержит полный антиген-распознающий и антиген-связывающий сайт. Этот фрагмент состоит из димера вариабельного домена одной тяжелой и одной легкой цепи в тесной нековалентной связи. В результате складывания этих двух доменов образуется шесть гипервариабельных петель (по 3 петли из Н-цепи и L-цепи), которые вносят аминокислотные остатки для связывания антигена и придают антигенсвязывающую специфичность антителу. Однако даже один вариабельный домен (или половина Fv, включающая только три области определения комплементарности (CDR), специфичные для антигена), обладает способностью распознавать и связывать антиген, хотя и с более низкой связью по сравнению с сайтом связывания. Термин «тяжелая цепь антитела», используемый в настоящем документе, относится к большему из двух типов полипептидных цепей, присутствующих во всех молекулах антител, в их естественных конформациях. Термин «легкая цепь антитела», используемый в настоящем документе, относится к меньшему из двух типов полипептидных цепей, присутствующих во всех молекулах антител, в их естественных конформациях. Легкие цепи κ и λ относятся к двум основным изотипам легкой цепи антител.
[0048] Термин «синтетическое антитело», используемый в настоящем документе, означает антитело, которое генерируется с использованием технологии рекомбинантной ДНК, такой как, например, антитело, экспрессируемое бактериофагом, описанное в настоящем изобретении. Этот термин также должен быть обозначен как антитело, которое было получено синтезом молекулы ДНК, кодирующей антитело, и какая молекула ДНК экспрессирует антитела, или аминокислотную последовательность, определяющую антитело, где последовательность ДНК или аминокислоты была получена с использованием технологии синтетической ДНК или аминокислоты, которая доступна и хорошо известна в данной области.
[0049] Термин «антиген», используемый в настоящем документе, определяется как молекула, провоцирующую иммунный ответ, который может включать либо продуцирование антител, либо активацию специфических иммунологически компетентных клеток, либо и то, и другое. Антигены могут содержать любую макромолекулу, включая практически все белки или пептиды, или молекулы, полученные из рекомбинантной или геномной ДНК. Например, ДНК, включающая нуклеотидные последовательности или частичную нуклеотидную последовательность, кодирует белок, который вызывает иммунный ответ, соответственно кодирует «антиген», поскольку этот термин используется в настоящем документе. Кроме того, антиген не должен кодироваться исключительно полноразмерной нуклеотидной последовательностью гена. Кроме того, антиген может быть образован, синтезирован или получен из биологического образца, включающего образец ткани, образец опухоли, клетку или биологическую жидкость.
[0050] Термин «противоопухолевый эффект», используемый в настоящем документе, относится к биологическому эффекту, связанному с уменьшением объема опухоли, уменьшением числа опухолевых клеток, уменьшением числа метастаз, увеличением продолжительности жизни пациента, имеющего опухолевые клетки, или улучшением различных физиологических симптомов, связанных с раковым состоянием. Термин «противоопухолевый эффект» также может относится к способностям пептидов, полинуклеотидов, клеток и антител, описанных в настоящем изобретении, к предотвращению возникновения опухоли в первую очередь.
[0051] Термин «авто-антиген» относится к антигену, ошибочно признанному иммунной системой, чужеродным. Авто-антигены включают клеточные белки, фосфопротеины, клеточные поверхностные белки, клеточные липиды, нуклеиновые кислоты, гликопротеины, в том числе клеточные поверхностные рецепторы.
[0052] Термин «аутогенный» используется для описания материала, полученного от того же индивидуума, которому он впоследствии будет повторно введен.
[0053] Термин «аллогенный» используется для описания графта, полученного от другого животного того же вида.
[0054] Термин «ксеногенный» используется для описания графта, полученного от животного другого вида.
[0055] Термин «рак», используемый в настоящем документе, определяется как заболевание, характеризующееся быстрым и неконтролируемым ростом аберрантных клеток. Раковые клетки могут распространяться локально или через кровоток и лимфатическую систему в другие части тела. Примеры различных видов рака включают рак молочной железы, рак предстательной железы, рак яичников, рак шейки матки, рак кожи, рак поджелудочной железы, рак ободочной и прямой кишки, рак почки, рак печени, рак мозга, лимфому, лейкемию, рак легких и др.
[0056] В настоящей спецификации, если контекст не требует иного, слова «содержит», «включает» и «включающий» будут пониматься как подразумевающие включение заявленного этапа или элемента или группы этапов или элементов, но не исключение любого другого этапа или элемента или группы этапов или элементов.
[0057] Термин «состоящий из» включает и ограничивается всем, что следует за фразой «состоящей из». Таким образом, фраза «состоящий из» указывает, что перечисленные элементы являются необходимыми или обязательными и, что никакие другие элементы не могут присутствовать.
[0058] Термин «состоящий в основном из» включает любые элементы, перечисленные после фразы, и ограничивается другими элементами, которые не мешают или не способствуют деятельности или действию, указанным в изобретении для перечисленных элементов. Таким образом, фраза «состоящий в основном из» указывает, что перечисленные элементы являются необходимыми или обязательными, но другие элементы являются необязательными и могут присутствовать или не присутствовать в зависимости от того, влияют ли они на активность или действие перечисленных элементов.
[0059] Термины «комплементарный» и «комплементарность» относятся к полинуклеотидам (то есть последовательности нуклеотидов), связанным с правилами спаривания оснований. Например, последовательность «А-Г-Т» комплементарна к последовательности «Т-Ц-А». Комплементарность может быть «частичной», в которой только некоторые из оснований нуклеиновых кислот сопоставляются в соответствии с правилами спаривания оснований, или может быть «полной» или «общей». Степень комплементарности между цепями нуклеиновых кислот оказывает значительное влияние на эффективность и прочность гибридизации между цепями нуклеиновых кислот.
[0060] Термин «относится» или «относящийся к» означает (а) полинуклеотид, имеющий нуклеотидную последовательность, которая по существу идентична или комплементарна ко всей или части эталонной полинуклеотидной последовательности или кодирует аминокислотную последовательность, идентичную аминокислотной последовательности в пептид или белок или (б) пептид или полипептид, имеющий аминокислотную последовательность, которая по существу идентична последовательности аминокислот в эталонном пептиде или белке.
[0061] «Костимулирующий лиганд» включает молекулу в антиген-презентирующей клетке (например, АРС, дендритная клетка, В-клетка и др.), которая специфически связывает сопутствующую костимулирующую молекулу с Т-клеткой, тем самым производя сигнал, который, в дополнение к первичному сигналу, возникающему, например, при связывании комплекса TCR/CD3 с молекулой МНС, нагруженной пептидом, преобразует Т-клеточную имунную реакцию, включая пролиферацию, активацию, дифференциацию и др. Костимулирующий лиганд может включать молекулы CD7, В7-1 (CD80), В7-2 (CD86), лиганды PD-L1, PD-L2, 4-1BBL, OX40L, индуцируемый костимулирующий лиганд (ICOS-L), молекулу межклеточной адгезии (ICAM), CD30L, CD40, CD70, CD83, HLA-G, MICA, MICB, HVEM, рецептор лимфотоксина-бета, 3/TR6, ILT3, ILT4, HVEM, агонист или антитело, которое связывает лиганд Toll-рецептора и лиганд, который специфически связывается с В7-Н3. Костимулирующий лиганд также охватывает, среди прочего, антитело, которое специфически связывается с костимулирующей молекулой, присутствующей в Т-клетке, такой как CD27, CD28, 4-1ВВ, ОХ40, CD30, CD40, PD-1, ICOS, лимфоцитарный функциональный антиген-1 (LFA-1), CD2, CD7, LIGHT, NKG2C, В7-Н3 и лиганд, который специфически связывается с CD83.
[0062] «Костимулирующая молекула» относится к родственному партнеру по связыванию на Т-клетке, которая специфически связывается с ко-стимулирующим лигандом, тем самым преобразуя костимулирующий ответ Т-клеткой, такой как пролиферация. Костимулирующие молекулы включают молекулу МНС класса I, BTLA и Toll-подобный рецептор.
[0063] «Костимулирующий сигнал» относится к сигналу, который в сочетании с первичным сигналом, таким как лигирование TCR/CD3, приводит к пролиферации Т-клеток и/или к повышению экспрессии или понижению регуляции ключевых молекул.
[0064] Используемые в настоящем документе термины «болезнь» и «состояние» могут применяться взаимозаменяемо или могут отличаться тем, что конкретная болезнь или состояние могут не иметь известного возбудителя болезни (этиология пока не разработана), и поэтому могут быть не признаны на данный момент как болезнь, а только как нежелательное состояние или синдром, при котором практикующие врачи идентифицировали более или менее специфический набор симптомов. Термин «болезнь», используемый в настоящем документе, представляет собой состояние здоровья субъекта, при котором субъект не может поддерживать гомеостаз и состояние субъекта продолжает ухудшаться с прогрессированием заболевания. Напротив, термин «расстройство» у субъекта обозначает состояние здоровья, при котором животное может поддерживать гомеостаз, но в котором состояние здоровья животного менее благоприятно, чем при отсутствии расстройства. При отсутствии лечения расстройство не обязательно приводит к дальнейшему снижению состояния здоровья животного.
[0065] Используемый в настоящем документе термин «эффективный» означает достаточный для достижения желаемого, ожидаемого или предполагаемого результата. Например, «эффективное количество» может представлять собой количество соединения, достаточное для получения терапевтического или профилактического эффекта.
[0066] Термин «кодирование» относится к присущему свойству конкретных последовательностей нуклеотидов в полинуклеотиде, таком как ген, кДНК или мРНК, использоваться в качестве шаблонов для синтеза других полимеров и макромолекул в биологических процессах, имеющих либо определенную последовательность нуклеотидов (например, рРНК, тРНК и мРНК), либо определенную последовательность аминокислот и вытекающих из нее биологических свойств. Таким образом, ген кодирует белок, если транскрипция и трансляция мРНК, соответствующей этому гену, продуцируют белок в клетке или другой биологической системе. Кодирующая цепь, нуклеотидная последовательность которой идентична последовательности мРНК, и обычно предоставляется в списках последовательностей, а также некодирующая цепь, используемая в качестве шаблона для транскрипции гена или кДНК, могут упоминаться для кодирования белка или другого продукта этого гена или кДНК.
[0067] Относительно полинуклеотидов, термин «экзогенный» относится к полинуклеотидной последовательности, которая, не возникает естественным образом в клетке дикого типа или организме, но обычно вводится в клетку с помощью молекулярно-биологических методов. Примеры экзогенных полинуклеотидов включают векторы, плазмиды и/или искусственно созданные конструкции нуклеиновой кислоты, кодирующие желаемый белок. Относительно полинуклеотидов, термин «эндогенный» или «естественный» относится к возникающим естественным путем полинуклеотидным последовательностям, которые могут быть найдены в данной клетке дикого типа или организме. Кроме того, определенная полинуклеотидная последовательность, которая выявлена из первого организма и перенесена во второй организм с помощью молекулярно-биологических методов, обычно считается «экзогенным» полинуклеотидом по отношению ко второму организму. В конкретных вариантах осуществления, полинуклеотидные последовательности могут быть «введены» с помощью молекулярно-биологических методов в микроорганизм, который уже содержит такую полинуклеотидную последовательность, например, для создания одной или нескольких дополнительных копий встречающейся в природе другой полинуклеотидной последовательности и тем самым облегчения сверхэкспрессии кодированного полипептида.
[0068] Термин «экспрессия», используемый в настоящем документе, определяется как транскрипция и/или трансляция определенной нуклеотидной последовательности, приводимой в действие ее промотором.
[0069] Термин «экспрессирующий вектор» относится к вектору, содержащему рекомбинантный полинуклеотид, включающий последовательности, контролирующие экспрессию, функционально связанные с нуклеотидной последовательностью, которая должна быть экспрессирована. Экспрессирующий вектор включает достаточные элементы, действующие в цис-положении, для экспрессии, другие элементы для экспрессии могут быть предоставлены клеткой-хозяином или в системе экспрессии вне организма. Экспрессирующие векторы включают все известные в данной области техники, такие как космиды, плазмиды (например, лишенные оболочки или содержащиеся в липосомах) и вирусы (например, лентивирусы, ретровирусы, аденовирусы и аденоассоциированные вирусы), которые включают рекомбинантный полинуклеотид.
[0070] Термин «гомологичный» относится к сходству последовательности или идентичности последовательности между двумя полипептидами или между двумя молекулами нуклеиновой кислоты. Когда положение в обеих сравниваемых последовательностях занято одной и той же базой или мономерной подгруппой аминокислоты, например, если положение в каждой из двух молекул ДНК занято аденином, то молекулы гомологичны в этом положении. Процент гомологии между двумя последовательностями является функцией количества совпадающих или гомологичных позиций, разделяемых двумя последовательностями, деленными на количество размещенных позиций и умноженными на 100. Например, если 6 из 10 позиций в двух последовательностях совпадают или гомологичны, то две последовательности являются гомологичными на 60%. Например, ДНК-последовательности АТТГЦЦ и ТАТГГЦ имеют 50%-ную гомологию. Как правило, сравнение проводится, когда две последовательности согласовываются, чтобы обеспечить максимальную гомологию.
[0071] Термин «иммуноглобулин» или «Ig» относится к классу белков, которые функционируют как антитела. Пять членов, включенных в этот класс белков, представляют собой IgA, IgG, IgM, IgD и IgE. IgA является первичным антителом, которое присутствует в секрециях организма, таких как слюна, слезы, грудное молоко, желудочно-кишечных секрециях и секрециях слизи дыхательного и мочеполового трактов. IgG является наиболее распространенным циркулирующим антителом. IgM является основным иммуноглобулином, продуцируемым в первичном иммунном ответе у большинства субъектов. Он является наиболее эффективным иммуноглобулином в агглютинации, фиксации комплемента и других антителогенезов и играет важную роль в защите от бактерий и вирусов. IgD представляет собой иммуноглобулин, который не имеет известной функции антител, но может служить в качестве антигенного рецептора. IgE представляет собой иммуноглобулин, который преобразует гиперчувствительность немедленного типа, вызывая выделение медиаторов из тучных клеток и базофилов при воздействии аллергена.
[0072] Под «изолированным» подразумевается материал, который частично или практически свободен от компонентов, которые обычно сопровождают его в своем природном состоянии. Например, термин «изолированный полинуклеотид», используемый в настоящем документе, относится к полинуклеотиду, который был изолирован от последовательностей, которые примыкают с боковых сторон в естественном состоянии, например, фрагмент ДНК, который был удален из последовательностей, обычно смежных с фрагментом. Альтернативно, «изолированный пептид» или «изолированный полипептид» и тому подобное, используемые в настоящем документе, относятся к изоляции и или очистке пептидной или полипептидной молекулы от ее естественной клеточной среды и от связи с другими компонентами клетки вне организма.
[0073] В контексте настоящего изобретения используются следующие сокращения для обычных оснований нуклеиновой кислоты. «А» относится к аденозину, «Ц» относится к цитозину, «Г» относится к гуанозину, «Т» относится к тимидину, а «У» относится к уридину.
[0074] Если не указано иное, «нуклеотидная последовательность, кодирующая последовательность аминокислот» включает в себя все нуклеотидные последовательности, которые являются вырожденными вариантами друг друга и которые кодируют одну и ту же последовательность аминокислот. Фраза «нуклеотидная последовательность, которая кодирует белок или РНК», может также включать интроны в той степени, в которой нуклеотидная последовательность, кодирующая белок, может в некоторой степени содержать интрон(ы).
[0075] Термин «лентивирус», используемый в настоящем документе, относится к виду семейства Retroviridae. Лентивирусы уникальны среди ретровирусов в способности инфицировать не делящиеся клетки, они могут доставлять значительное количество генетического материала в ДНК клетки-хозяина, поэтому они являются одним из наиболее удобных векторов доставки генов. Примерами лентивирусов являются ВИЧ, ВИЧ у обезьян и ВИЧ у кошек. Векторы, полученные из лентивирусов, предлагают средства для достижения значительных уровней переноса генов вне организма.
[0076] Под термином «модуляция», используемым в настоящем документе, подразумевается промежуточное обнаружение увеличения или уменьшения уровня ответа у субъекта по сравнению с уровнем ответа у субъекта в отсутствие лекарства или соединения и/или по сравнению с уровнем ответа у идентичного субъекта до лечения. Этот термин охватывает возмущение и/или воздействие на собственный сигнал или реакцию, тем самым опосредуя полезный терапевтический ответ у субъекта, предпочтительно человека.
[0077] Нуклеиновая кислота «функционально связана», когда она образует функциональную связь с другой последовательностью нуклеиновой кислоты. Например, ДНК для предпоследовательности или секреторного лидера функционально связана с ДНК для полипептида, если она экспрессируется в виде белка-предшественника, который участвует в секреции полипептида; стимулятор или энхансер функционально связывается с кодирующей последовательностью, если он влияет на транскрипцию последовательности, или участок связывания рибосомы функционально связывается с кодирующей последовательностью, если он расположен так, чтобы облегчить трансляцию. Как правило, термин «функционально связанный» означает, что связанные с ним последовательности ДНК являются смежными, а в случае секреторного лидера - смежными и в фазе считывания. Однако энхансеры не должны быть смежными. Связывание осуществляют путем лигирования на удобных сайтах рестрикции. Если таких сайтов не существует, адаптеры или линкеры синтетических олигонуклеотидов используются в соответствии с обычной практикой.
[0078] Термин «сверхэкспрессированный» опухолевый антиген или «сверхэкспрессия» опухолевого антигена предназначен для указания аномального уровня экспрессии опухолевого антигена в клетке из группы заболеваний, такой как солидная опухоль в определенной ткани или органе пациента, относительно уровня экспрессии в нормальной клетке из этой ткани или органа. Пациенты, имеющие солидные опухоли или гемобластоз, характеризующиеся сверхэкспрессией опухолевого антигена, могут быть определены стандартными анализами, известными в данной области.
[0079] «Парентеральное» введение иммуногенной композиции включает, например, подкожный (п/к), внутривенный (в/в), внутримышечный (в/м) или интрастернальный способ введения инъекции или методы инфузии.
[0080] Термины «пациент», «субъект», «индивидуум» и др. используются в настоящем документе взаимозаменяемо и относятся к любому животному или его клеткам, независимо от того, являются ли они искусственными или естественными, поддающимся методам, описанным в настоящем изобретении. В некоторых неограничивающих вариантах осуществления пациент, субъект или индивидуум является человеком. В некоторых вариантах осуществления термин «субъект» включает живые организмы, в которых может быть выявлен иммунный ответ (например, млекопитающие). Примеры субъектов включают людей, собак, кошек, мышей, крыс и их трансгенных видов.
[0081] Термин «полинуклеотид» или «нуклеиновая кислота», используемый в настоящем изобретении, обозначает мРНК, РНК, кРНК, рРНК, кДНК или ДНК. Термин обычно относится к полимерной форме нуклеотидов длиной не менее 10 оснований, либо рибонуклеотидов, либо дезоксинуклеотидов, либо модифицированной форме любого типа нуклеотида. Термин включает одно- и двухцепочечные формы ДНК и РНК.
[0082] Термины «вариант полинуклеотида» и «вариант» и тому подобные термины относятся к полинуклеотидам, демонстрирующим значительную идентичность последовательности с эталонной полинуклеотидной последовательностью или полинуклеотидами, которые гибридизуются с эталонной последовательностью в жестких условиях гибридизации, которые определены ниже. Эти термины также охватывают полинуклеотиды, которые отличаются от эталонного полинуклеотида добавлением, делецией или замещением, по меньшей мере, одного нуклеотида. Соответственно, термины «вариант полинуклеотида» и «вариант» включают полинуклеотиды, в которых один или несколько нуклеотидов были добавлены, удалены или замещены различными нуклеотидами. В этой связи в данной области техники хорошо известно, что определенные изменения, включающие мутации, добавления, делеции и замещения, могут быть получены в эталонном полинуклеотиде, в результате чего измененный полинуклеотид сохраняет биологическую функцию или активность эталонного полинуклеотида или обладает повышенной активностью в отношении к эталонному полинуклеотиду (т.е. оптимизирован). Варианты полинуклеотидов включают, например, полинуклеотиды, имеющие, по меньшей мере, 50% (по меньшей мере, от 51% до, по меньшей мере, 99% и все целые проценты между ними, например, 90%, 95% или 98%) идентичность последовательности с эталонной полинуклеотидной последовательностью, описанной в настоящем документе. Термины «вариант полинуклеотида» и «вариант» также включают встречающиеся в природе аллельные варианты и ортологи, которые кодируют эти ферменты.
[0083] Термины "полипептид, «полипептидный фрагмент», «пептид» и «белок» взаимозаменяемы в настоящем документе и используются для обозначения полимера аминокислотных остатков и их вариантов и синтетических аналогов. Таким образом, эти термины применимы к полимерам аминокислот, в которых один или несколько аминокислотных остатков представляют собой синтетические неприродные аминокислоты, такие как химический аналог соответствующей природной аминокислоты, а также природные полимеры аминокислот. В некоторых вариантах полипептиды могут включать ферментные полипептиды или «ферменты», которые обычно катализируют (то есть увеличивают скорость) различных химических реакций.
[0084] Термин «вариант полипептида» относится к полипептидам, которые отличаются от эталонной полипептидной последовательности добавлением, делецией или замещением, по меньшей мере, одного аминокислотного остатка. В некоторых вариантах осуществления вариант полипептида отличается от эталонного полипептида одной или несколькими замещениями, которые могут быть консервативными или неконсервативными. В некоторых вариантах осуществления вариант полипептида включает консервативные замещения, и в этой связи в данной области хорошо известно, что некоторые аминокислоты могут быть заменены на другие с приблизительно идентичными свойствами без изменения характера активности полипептида. Варианты полипептида также включают полипептиды, в которых одна или несколько аминокислот были добавлены, удалены или замещены различными аминокислотными остатками.
[0085] Термин «стимулятор», используемый в настоящем документе, определяется как последовательность ДНК, распознаваемая синтетическим механизмом клетки или интродуцированным синтетическим механизмом, необходимая для инициирования специфической транскрипции полинуклеотидной последовательности. Выражение «регуляторные последовательности» относится к последовательностям ДНК, необходимым для экспрессии функционально связанной кодирующей последовательности в конкретном организме-хозяине. Регуляторные последовательности, подходящие для прокариотов, например, включают стимулятор, при необходимости, последовательность операторов и участок связывания рибосом. Известно, что эукариотические клетки используют стимуляторы, сигналы полиаденилирования и энхансеры.
[0086] Термин «связывать», «связывается» или «взаимодействует» означает, что одна молекула распознает и присоединяется к определенной второй молекуле в образце или организме, но по существу не распознает или не присоединяется к другим структурно не связанным молекулам в образце. Термин «специфически связывается», используемый в настоящем документе, в отношении антитела, означает антитело, которое распознает специфический антиген, но по существу не распознает или не связывает другие молекулы в образце. Например, антитело, которое специфически связывается с антигеном из одного вида, также может связываться с этим антигеном из одного или нескольких видов. Однако такая межвидовая химическая активность сама по себе не изменяет классификацию антитела как специфическую. В другом примере антитело, которое специфически связывается с антигеном, также может связываться с различными аллельными формами антигена. Однако такая перекрестная химическая активность сама по себе не изменяет классификацию антитела как специфическую. В некоторых случаях термины «специфическое связывание» или «специфически связанные» могут быть использованы в отношении взаимодействия антитела, белка или пептида со вторым химическим видом, что означает, что взаимодействие зависит от присутствия определенной структуры (например, антигенной детерминанты или эпитопа) на химических видах, например, антитело распознает и связывается со специфической структурой белка, а не с белками в целом. Если антитело специфично для эпитопа «А», присутствие молекулы, содержащей эпитоп А (или свободный, немеченый А), в реакции, содержащей меченый «А» и антитело, уменьшит количество меченых А, связанных с антителом.
[0087] «Растворимый рецептор» представляет собой рецепторный полипептид, не связанный с клеточной мембраной. Растворимые рецепторы чаще всего являются лигандсвязывающими рецепторными полипептидами, которые не имеют трансмембранных и цитоплазматических доменов. Растворимые рецепторы могут включать дополнительные аминокислотные остатки, такие как аффинные метки, которые обеспечивают очистку полипептида или обеспечивают сайты для присоединения полипептида к субстрату или последовательностям константных участков иммуноглобулина. Многие рецепторы клеточной поверхности имеют естественные, растворимые аналоги, которые продуцируются протеолизом. Считается, что растворимые рецепторные полипептиды практически не содержат трансмембранных и внутриклеточных сегментов полипептида, когда им не хватает достаточного количества этих сегментов для обеспечения мембранного соединения или сигнальной трансдукции соответственно.
[0088] Под «статистически значимым» подразумевается, что результат вряд ли возник случайно. Статистическая значимость может быть определена любым способом, известным в данной области техники. Обычно используемые меры значимости включают в себя значение вероятности р, которое является частотой или вероятностью, с которой наблюдаемое событие может произойти, если нулевая гипотеза окажется верной. Если полученное значение р меньше уровня значимости, то нулевая гипотеза отклоняется. В простых случаях уровень значимости определяется р-значением, равным 0,05 или менее. «Уменьшенное», «сниженное» или «меньшее» количество обычно является «статистически значимой» или физиологически значимой величиной и может предусматривать уменьшение примерно на 1.1, 1.2, 1.3, 1.4, 1.5, 1.6 1.7, 1.8, 1.9, 2, 2.5, 3, 3.5, 4, 4.5, 5, 6, 7, 8, 9, 10, 15, 20, 30, 40 или 50 или более раз (например, 100, 500, 1000 раз) (включая все целые числа и десятичные числа от 1 и выше, например, 1,5, 1,6, 1,7. 1.8 и т.д.) количество или уровень, описанные в настоящем документе.
[0089] Под термином «стимуляция» подразумевается первичный ответ, индуцированный связыванием стимулирующей молекулы (например, комплекса TCR/CD3) с его когнатным лигандом, тем самым опосредуя событие передачи сигнала, такое как передача сигнала через комплекс TCR/CD3. Стимуляция может опосредовать измененную экспрессию определенных молекул, такую как отрицательную регуляцию TGF-β и/или реорганизации цитоскелетных структур и др.
[0090] «Стимулирующая молекула» относится к молекуле на Т-клетке, которая специфически связывается с когнатным стимулирующим лигандом, присутствующим в антиген-презентирующей клетке.
[0091] «Стимулирующий лиганд» относится к лиганду, который при присутствии в антиген-презентирующей клетке (например, АРС, дендритная клетка, В-клетка и др.), может специфически связываться с когнатным партнером по связыванию (обозначенным здесь как «стимулирующая молекула») на Т-клетке, тем самым опосредуя первичный ответ Т-клеткой, включая активацию, инициирование иммунного ответа, пролиферацию и др. Стимулирующие лиганды хорошо известны в данной области и включают, среди прочего, молекулу МНС класса I, нагруженную пептидом, антитела против CD3-клеток, CD28-суперагонист и CD2-суперагонист.
[0092] Термин «практически изолированная» клетка, согласно настоящему документу, представляет собой клетку, которая по существу не содержит других типов клеток. Практически изолированная клетка также относится к клетке, которая была отделена от других типов клеток, с которыми она обычно связана в ее естественном состоянии. В некоторых случаях популяция практически изолированных клеток относится к гомогенной клеточной популяции. В других случаях этот термин относится просто к клетке, которая была отделена от клеток, с которыми она естественным образом связана в их естественном состоянии. В некоторых вариантах осуществления клетки выращивают вне организма. В других вариантах осуществления клетки не выращивают вне организма.
[0093] Термин «терапевтическое средство», используемое в настоящем документе, означает лечение и/или профилактику. Терапевтический эффект достигается путем подавления, ослабления или устранения болезненного состояния.
[0094] Термин «терапевтически эффективное количество» относится к количеству целевого соединения, которое будет вызывать биологический или медицинский ответ ткани, системы или субъекта, который запрашивается исследователем, ветеринаром, врачом или другим клиницистом. Термин «терапевтически эффективное количество» включает в себя такое количество соединения, которое при введении является достаточным для предотвращения развития или ослабления в какой-либо степени одного или нескольких признаков или симптомов расстройства или заболевания, подлежащего лечению. Терапевтически эффективное количество будет варьироваться в зависимости от соединения, заболевания и его тяжести, а также в зависимости от возраста, веса и т.д. субъекта, подлежащего лечению.
[0095] Термин «лечить» болезнь, используемый в настоящем документе, означает уменьшение периодичности или тяжести, по меньшей мере, одного признака или симптома заболевания или расстройства, испытываемого субъектом.
[0096] Термин «трансфицированный», «трансформированный» или «трансдуцированный», используемый в настоящем документе, относится к способу, посредством которого экзогенная нуклеиновая кислота переносится или вводится в клетку-хозяин. «Трансфицированная», «трансформированная» или «трансдуцированная» клетка представляет собой трансфицированную, трансформированную или трансдуцированную экзогенную нуклеиновую кислоту. Клетка включает в себя основную первичную клетку и вторичные клетки.
[0097] Фраза «под транскрипционным контролем» или «оперативно связанный», используемая в настоящем документе, означает, что стимулятор находится в правильном месте и ориентации по отношению к полинуклеотиду для контроля инициации транскрипции с помощью РНК-полимеразы и экспрессии полинуклеотида.
[0098] «Вектор» представляет собой композицию вещества, которая включает изолированную нуклеиновую кислоту и которая может быть использована для доставки изолированной нуклеиновой кислоты внутрь клетки. В данной области техники известны многочисленные векторы, которые включают линейные полинуклеотиды, полинуклеотиды, связанные с ионными или амфифильными соединениями, плазмиды и вирусы. Таким образом, термин «вектор» включает автономно реплицируемую плазмиду или вирус. Этот термин также должен быть истолкован как включающий неплазмидные и невирусные соединения, которые облегчают перенос нуклеиновой кислоты в клетки, такие как, например, полилизиновые соединения, липосомы и др. Примеры вирусных векторов включают, но не ограничиваются, аденовирусными векторами, аденоассоциированными вирусными векторами, ретровирусными векторами и др. Например, лентивирусы представляют собой сложные ретровирусы, которые помимо общих ретровирусных генов gag, pol и env содержат другие гены с регуляторной или структурной функцией. Лентивирусные векторы хорошо известны в данной области. Некоторые примеры лентивирусов включают вирусы иммунодефицита человека: ВИЧ-1, ВИЧ-2 и вирус иммунодефицита обезьян: SIV. Лентивирусные векторы были получены путем многократного ослабления генов вирулентности ВИЧ, например, гены env, vif, vpr, vpu и nef удаляются, делая вектор биологически безопасным.
[0099] Интервалы: в настоящем изобретении различные варианты осуществления изобретения могут быть представлены в формате интервала. Следует понимать, что описание в формате интервала просто для удобства и краткости и не должно толковаться как строгое ограничение объема изобретения. Соответственно, описание интервала должно рассматриваться как специально раскрывающее все возможные подгруппы, а также отдельные числовые значения в пределах этого интервала. Например, описание интервала, такого как от 1 до 6, следует рассматривать как специально раскрытые подгруппы, такие как от 1 до 3, от 1 до 4, от 1 до 5, от 2 до 4, от 2 до 6, от 3 до 6 и т.д., а также отдельные числа в этом интервале, например, 1, 2, 2.7, 3, 4, 5, 5.3 и 6. Это применяется независимо от ширины интервала.
[0100] Настоящее изобретение относится к изолированным последовательностям нуклеиновой кислоты, векторам, включающим изолированные последовательности нуклеиновой кислоты, клеткам, включающим изолированные последовательности нуклеиновой кислоты, и способам лечения рака с использованием этих клеток.
[0101] Композиции и терапевтическое применение
[0102] Варианты осуществления настоящего изобретения относятся к изолированной нуклеотидной последовательности, содержащей последовательность нуклеиновой кислоты, которая кодирует модифицированный белок запрограммированной смерти клетки 1 (PD-1), и последовательность нуклеиновой кислоты, которая кодирует химерный антигенный рецептор (CAR). В некоторых вариантах осуществления изобретения, модифицированные PD-1 и CAR экспрессируются в виде генных продуктов, которые являются отдельными полипептидами. В этих случаях CAR специфичен для опухолевого антигена, который присутствует в раковой клетке, и раковая клетка экспрессирует PD-L1.
[0103] Химерные антигенные рецепторы CAR представляют собой молекулы, обычно включающие внеклеточный и внутриклеточный домен. Внеклеточный домен включает направленный связующий элемент. Внутриклеточный домен (например, цитоплазматический домен) включает костимулирующий участок передачи сигналов и участок зета-цепочки. Костимулирующий участок передачи сигналов относится к участку CAR, включающему внутриклеточный домен костимулирующей молекулы. Костимулирующими молекулами являются молекулы клеточной поверхности, отличные от рецепторов антигенов или их лигандов, которые необходимы для эффективного ответа лимфоцитов на антиген.
[0104] Между внеклеточным доменом и трансмембранным доменом химерного антигенного рецептора может быть включен спейсерный домен. Используемый здесь термин «спейсерный домен» обычно означает любой олиго- или полипептид, который функционирует для связывания трансмембранного домена с внеклеточным доменом или цитоплазматическим доменом в полипептидной цепи. Спейсерный домен может включать до 300 аминокислот, предпочтительно от 10 до 100 аминокислот и наиболее предпочтительно от 25 до 50 аминокислот.
[0105] В некоторых вариантах осуществления изобретения, направленный связующий элемент химерного антигенного рецептора может распознавать опухолевый антиген. Опухолевые антигены представляют собой белки, которые продуцируются опухолевыми клетками, которые вызывают иммунный ответ, особенно иммунные ответы, опосредуемые Т-клетками. Опухолевые антигены хорошо известны в данной области и включают, например, глиома-ассоциированный антиген, карциноэмбриональный антиген (СЕА), β-человеческий хорионический гонадотропин, альфа-фетопротеин (АФП), лектин-реактивный АФП, тиреоглобулин, рецептор продуктов неферментативного гликозилирования RAGE-1, карбоангидразы MN-CA IX, обратную транскриптазу теломеразы человека, единицы ответа RU1, RU2 (AS), кишечную карбоксиэстеразу, белок теплового тока (mut hsp70-2), макрофагальный колониестимулирующий фактор (M-CSF), простазу, простат-специфический антиген (PSA), простатическую кислую фосфатазу (РАР), антиген NY-ESO-1, LAGE-1a, белок р53, простеин, простатический специфический мембранный антиген (PSMA), мембранный белок Her2/neu, сурвивин и теломеразу, опухолевый антиген-1 рака предстательной железы (РСТА-1), белок MAGE, транслоказу ELF2M, нейтрофил-эластазу, эфрин В2, ген CD22, фактор роста инсулина (IGF)-I, IGF-II, рецептор IGF-I и мезотелин.
[0106] В некоторых вариантах осуществления изобретения, опухолевой антиген включает в себя HER2, CD19, CD20, CD22, каппа-частицы или легкую цепь, CD30, CD33, CD123, CD38, ROR1, ErbB3/4, EGFR, EGFRvIII, EphA2, FAP, карциноэмбриональный антиген, EGP2, EGP40, мезотелин, TAG72, PSMA, лиганды рецептора NKG2D, В7-Н6, IL-13 рецептор α2, IL-11 рецептор α, MUC1, MUC16, СА9, GD2, GD3, HMW-MAA, CD171, антиген Ley, G250/CAIX, HLA-AI MAGE A1, HLA-A2 NY-ESO-1, PSC1, рецептор фолата-α, CD44v7/8, 8H9, NCAM, рецепторы VEGF, 5T4, ацетилхолиновый рецептор фетального типа AchR, лиганды рецептора NKG2D, CD44v6, ТЕМ1, TEM8 или антигены вируса, экспрессированные на опухоли.
[0107] В некоторых вариантах осуществления изобретения, антигенсвязывающий элемент химерного антигенного рецептора CAR согласно изобретению воздействует на В-лимфоцитарный антиген CD19. В некоторых случаях антигенсвязывающий элемент химерного антигенного рецептора CAR согласно изобретению содержит одноцепочечный вариабельный фрагмент В-лимфоцитарного антигена CD19 (anti-CD19 scFV), включающий аминокислотную последовательность согласно SEQ ID NO: 1.
[0108] В некоторых вариантах осуществления, трансмембранный домен химерного антигенного рецептора по настоящему изобретению включает трансмембранный домен CD8 или CD9. В некоторых вариантах осуществления внутриклеточный домен химерного антигенного рецептора по настоящему изобретению включает внутриклеточный домен 4-1ВВ (CD137) или CD28. PD-1, член семейства белков CD28, представляет собой трансмембранный белок 1-го типа с внеклеточным доменом, содержащим один иммуноглобулинподобный вариабельный домен и внутриклеточный домен, содержащий иммунорецепторный тирозиновый ингибирующий мотив. PD-1 экспрессируется на активированных Т-клетках, В-лимфоцитах, естественных клетках-киллерах, дендритных клетках и активированных моноцитах. Взаимодействие между PD-1 и его лигандами PD-L1 и PD-L2 приводит к экстракции, инактивации и апоптозу Т-клеток.
[0109] Экстрагированные Т-лимфоциты теряют способность продуцировать провоспалительные цитокины, включающие интерлейкин-2 (IL-2), фактор некроза опухоли-α и интерферон-γ. Экспрессия PD-L1 различными тканями опосредует периферическую иммунологическую толерантность, а активация пути PD-1/PD-L1 ограничивает повреждение ткани после устойчивого иммунного/воспалительного ответа. PD-1-экспрессирующие лимфоциты, инфильтрующие опухоль, связаны с нарушением противоопухолевого эффекта и повышением активности PD-1, a PD-L1 влияет на результат лечения нескольких типов опухолей.
[0110] Варианты осуществления изобретения относятся к изолированной последовательности нуклеиновой кислоты, включающей последовательность нуклеиновой кислоты, которая кодирует модифицированный PD-1 и последовательности нуклеиновой кислоты, которая кодирует химерный антигенный рецептор (CAR). В некоторых вариантах осуществления изобретения, последовательность нуклеиновой кислоты, которая кодирует модифицированный белок PD-1, включает замещение или делецию одного или нескольких нуклеотидов по сравнению с последовательностью нуклеиновой кислоты, кодирующей внутриклеточный домен белка PD-1 широкого типа. В некоторых вариантах осуществления последовательность нуклеиновой кислоты, которая кодирует модифицированный PD-1, включает делецию одного или нескольких нуклеотидов по сравнению с последовательностью нуклеиновой кислоты, кодирующей внутриклеточный домен PD-1 широкого типа. Например, модифицированный PD-1 представляет собой PD-1 человека, который включает последовательность нуклеиновой кислоты согласно SEQ ID NO: 14.
[0111] В некоторых вариантах осуществления изобретения, последовательность нуклеиновой кислоты, которая кодирует модифицированный PD-1, включает нуклеиновую кислоту, кодирующую усеченный PD-1, который не включает внутриклеточный домен. Например, последовательность нуклеиновой кислоты, которая кодирует модифицированный PD-1, включает последовательность нуклеиновой кислоты согласно SEQ ID NO: 12.
[0112] В некоторых вариантах осуществления изобретения, модифицированный PD-1 включает в себя одну или несколько точечных мутаций по сравнению с PD-1 широкого типа. В некоторых вариантах осуществления точечные мутации могут включать одну или две точечные мутации аминокислот сайтов фосфорилирования PD-1 широкого типа. Например, точечные мутации аминокислот включают точечную мутацию тирозинового остатка 223 и/или тирозинового остатка 248.
[0113] Варианты осуществления настоящего изобретения дополнительно относятся к конструкции ДНК, включающей последовательности, кодирующие CAR и модифицированный PD-1. В некоторых вариантах осуществления CAR может включать любую комбинацию CD3дзета, CD28, 4-1ВВ и др. Например, CAR в настоящем изобретении включает в себя одноцепочечный вариабельный фрагмент В-лимфоцитарного антигена CD19 (anti-CD19 scFV), спейсер-шарнир CD8 человека и трансмембранный домен и сигнальные домены 4-1ВВ и CD3дзета человека. В одном из вариантов осуществления, CAR в настоящем изобретении включает последовательность нуклеиновой кислоты, представленную в SEQ ID NO: 1.
[0114] В некоторых вариантах осуществления, элементы участка внутренней посадки рибосомы (IRES) используются для создания мультигенов, полицистронов или транскриптов. Например, элемент IRES может связывать последовательность нуклеиновой кислоты, кодирующую CAR, и последовательность нуклеиновой кислоты, кодирующую один из различных модифицированных PD-1 (см. Таблицу 1).
[0115] Последовательности нуклеиновой кислоты, кодирующие желаемые молекулы, могут быть получены с использованием рекомбинантных методов, известных в данной области, например, путем отбора генотек из клеток, экспрессирующих ген, путем получения гена из вектора, содержащего данный ген, или путем выделения непосредственно из клеток и тканей, содержащих данный ген, с использованием стандартных методов. В ином случае, ген, представляющий интерес, скорее синтезируют, чем клонируют.
[0116] Варианты осуществления настоящего изобретения дополнительно относятся к векторам, в которые вставлена ДНК по настоящему изобретению. Векторы, полученные из ретровирусов, таких как лентивирус, являются подходящими инструментами для достижения длительного переноса генов, поскольку они позволяют долговременную стабильную интеграцию трансгена и его воспроизведение в дочерних клетках. Лентивирусные векторы обладают дополнительным преимуществом по сравнению с векторами, полученными из опухолевых ретровирусов, таких как вирусы лейкемии мыши, которое заключается в том, что они могут трансдуцировать непролиферирующие клетки, такие как гепатоциты. Преимуществом лентивирусных векторов также является низкая иммуногенность.
[0117] Экспрессия натуральных или синтетических нуклеиновых кислот, кодирующих химерный антигенный рецептор и модифицированный PD-1, обычно достигается путем функционального связывания нуклеиновой кислоты, кодирующей полипептид CAR или его частей, с одним или несколькими стимуляторами, и включения конструкции в экспрессирующий вектор. Векторы могут быть пригодны для репликации и интеграции эукариотов. Типичные векторы для клонирования содержат терминаторы транскрипции и трансляции, последовательности инициации и стимуляторы, полезные для регуляции экспрессии нужной последовательности нуклеиновой кислоты.
[0118] Дополнительная информация, относящаяся к экспрессии синтетических нуклеиновых кислот, кодирующих CAR и модифицированные PD-1, и перенос гена в клетки млекопитающих, представлена в патенте США № US 8,906,682, включенной в качестве ссылки в полном объеме.
[0119] Варианты осуществления изобретения дополнительно относятся к генетически модифицированным клеткам (например, Т-клеткам), экспрессирующим химерный антигенный рецептор и модифицированный PD-1. В некоторых вариантах осуществления, доминантный отрицательный PD-1 вводится в Т-клетки таким образом, что доминантный отрицательный PD-1 ингибирует активность PD-1 широкого типа, индуцированный PD-L1 опухолевой клетки. В некоторых вариантах осуществления, генетически модифицированные Т-клетки экспрессируют нефункционирующий PD-1. Например, генетически модифицированные Т-клетки экспрессируют молекулы PD-1, не включающие внутриклеточный домен, или не включающие внутриклеточный и трансмембранный домены, или включающие точечную мутацию, описанную в настоящем изобретении.
[0120] В некоторых вариантах осуществления, ингибирующий эффект PD-L1 опухолевой клетки на продукцию цитокинов генетически модифицированных Т-клеток настоящего изобретения меньше ингибирующего эффекта PD-L1 на продукцию цитокинов Т-клеток, которые не включают, по меньшей мере, часть последовательности нуклеиновой кислоты, которая кодирует модифицированный PD-1. Например, ингибирующий эффект PD-L1 на продукцию цитокинов генетически модифицированных Т-клеток настоящего изобретения является достаточным для снижения, по меньшей мере, на 5%, по меньшей мере, на 10%, по меньшей мере, на 15%, по меньшей мере, на 20%, по меньшей мере, на 30%, по меньшей мере, на 40%, по меньшей мере, на 50%, по меньшей мере, на 60%, по меньшей мере, на 70%, по меньшей мере, на 80%, по меньшей мере, на 90% ингибирующего действия PD-L1 на продукцию цитокинов Т-клеток, которые не включают, по меньшей мере, части последовательности нуклеиновой кислоты, которая кодирует модифицированный PD-1.
[0121] В некотором варианте осуществления, генетически модифицированные Т-клетки включают последовательность нуклеиновой кислоты, которая кодирует модифицированный PD-1, имеющий одну или более точечных мутаций по сравнению с PD-1 широкого типа. Например, точечная мутация содержит одну или две точечные мутации аминокислот сайтов фосфорилирования PD-1 широкого типа. В некоторых вариантах осуществления, генетически модифицированные Т-клетки включают последовательность нуклеиновой кислоты, которая кодирует модифицированный PD-1 и включает делецию одного или нескольких нуклеотидов по сравнению с последовательностью нуклеиновой кислоты, кодирующей внутриклеточный домен PD-1 широкого типа. Например, последовательность нуклеиновой кислоты, которая кодирует модифицированный PD-1, содержит последовательность нуклеиновой кислоты согласно SEQ ID NO: 12 или SEQ ID NO: 14.
[0122] Варианты осуществления изобретения дополнительно относятся к способам лечения пациента, включающим введение пациенту эффективного количества разработанных клеток согласно настоящему изобретению. В соответствии с настоящими методами можно лечить различные заболевания, включающие рак, такие как рак яичников, карцинома молочной железы, карцинома толстой кишки, мультиформная глиобластома, рак предстательной железы и лейкемия. В некоторых вариантах осуществления, способ включает введение пациенту фармацевтической композиции, содержащей эффективное количество Т-клеток человека для достижения противоопухолевого эффекта, где Т-клетки человека включают Т-клетки, которые содержат последовательность нуклеиновой кислоты, как описано в настоящем изобретении.
[0123] Раковые опухоли, поддающиеся лечению, включают опухоли, которые не васкуляризированы или еще не полностью васкуляризированы, а также васкуляризированные опухоли. Рак может включать в себя несолидные опухоли (такие как гематологические опухоли, например лейкемии и лимфомы) или солидные опухоли. Виды рака, подлежащие лечению с помощью химерного антигенного рецептора по настоящему изобретению, включают, но не ограничиваются, карциному, бластому и саркому, лейкемию или лимфолейкоз, доброкачественные и злокачественные опухоли, злокачественные новообразования, например саркомы, карциномы и меланомы, а также опухоли/раковые образования у взрослых и опухоли/раковые образования у детей.
[0124] Гематологические раковые образования - это рак крови или рак костного мозга. Примерами гематологических (или гематогенных) раковых заболеваний являются лейкемия, включающая острые лейкозы (такие как острый лимфоцитарный лейкоз, острый миелоцитарный лейкоз, острый миелогенный лейкоз и миелобластный, промиелоцитарный, миеломоноцитарный, моноцитарный и эритролейкоз), хронические лейкозы (такие как хронический миелоцитарный (гранулоцитарный) лейкоз, хронический миелогенный лейкоз, хронический лимфоцитарный лейкоз), болезнь Ослера, лимфома, болезнь Ходжкина, неходжкинская лимфома (медленная и быстрая формы), множественная миелома, макроглобулинемия Вальденстрема, болезнь тяжелой цепи, миелодиспластический синдром, лейкоз ворсистых клеток и миелодисплазия.
[0125] Солидные опухоли представляют собой аномальные массы тканей, которые обычно не содержат цисты или жидкие области. Солидные опухоли могут быть доброкачественными или злокачественными. Приведены различные типы солидных опухолей для типа клеток, которые их образуют (например, саркомы, карциномы и лимфомы). Примеры солидных опухолей, таких как саркомы и карциномы, включают фибросаркому, миксосаркому, липосаркому, хондросаркому, остеосаркому и другие саркомы, синовиому, мезотелиому, саркому Юинга, лейомиосаркому, рабдомиосаркому, карциному толстой кишки, лимфолейкоз, рак поджелудочной железы, рак молочной железы, рак легких, рак яичников, рак предстательной железы, печеночно-клеточный рак, плоскоклеточный рак, базально-клеточный рак, аденокарциному, карциному потовых желез, медуллярную карциному щитовидной железы, папиллярную карциному щитовидной железы, медуллярную карциному сальных желез, папиллярную карциному, папиллярные аденокарциномы, медуллярную карциному, бронхогенную карциному, рак почек, гепатому, карциному желчного протока, хориокарциному, опухоль Вильмса, рак шейки матки, опухоль яичка, карциному мочевого пузыря, опухоли ЦНС, (такие как глиома (например, глиома ствола головного мозга и смешанные глиомы), глиобластома (также известная как мультиформная глиобластома) астроцитома, лимфома ЦНС, герминома, медуллобластома, шваннома краниофарингиома, эпендимома, пинеалома, гемангиобластома, акустическая невринома, олигодендроглиома, менангиома, нейробластома, ретинобластома и метастазы в мозг).
[0126] Как правило, описанные в настоящем изобретении активные и размноженные клетки, могут использоваться для лечения и профилактики заболеваний, которые возникают у людей с ослабленным иммунитетом. В частности, разработанные в настоящем изобретении, клетки используются для лечения рака. В некоторых вариантах осуществления, разработанные в настоящем изобретении, клетки используются для лечения пациентов с риском развития рака. Таким образом, настоящее изобретение предоставляет способы лечения или профилактики рака, включающие введение субъекту, нуждающемуся в этом, терапевтически эффективного количества разработанных в настоящем изобретении Т-клеток.
[0127] Разработанные Т-клетки настоящего изобретения могут вводиться либо отдельно, либо в виде фармацевтической композиции в комбинации с разбавителями и/или с другими компонентами, такими как IL-2 или другими цитокинами или клеточными популяциями. Вкратце, фармацевтические композиции настоящего изобретения могут включать популяцию клеток-мишеней, описанных в настоящем изобретении, в комбинации с одним или несколькими фармацевтически или физиологически приемлемыми носителями, разбавителями или эксципиентами. Такие композиции могут включать в себя буферные растворы, такие как нейтральный забуференный физиологический раствор, забуференный фосфатом физиологический раствор и тому подобное; углеводы, такие как глюкоза, манноза, сахароза, декстраны или маннитолы; белки; полипептиды или аминокислоты, такие как глицин, антиоксиданты, хелатирующие агенты, такие как этилендиаминтетрауксусная кислота или глютатион; адъюванты (например, гидроксид алюминия) и консерванты. Композиции настоящего изобретения предпочтительно составлены для внутривенного введения.
[0128] Фармацевтические композиции по настоящему изобретению могут вводиться способом, соответствующим заболеванию, подлежащему лечению (или профилактике). Количество и периодичность введения будут определяться такими факторами, как состояние пациента, тип и тяжесть заболевания пациента, хотя соответствующие дозы могут быть определены клиническими испытаниями.
[0129] После выявления «иммунологически эффективного количества», «эффективного количества противоопухолевого средства», «эффективного количества ингибирующего опухоль средства» или «терапевтической дозы», врач может определить точное количество композиций настоящего изобретения, подлежащих введению, с учетом индивидуальных различий в возрасте, весе, размере опухоли, степени заражения или метастазировании и состоянии пациента (субъекта). В общем случае может быть установлено, что фармацевтическая композиция, содержащая Т-клетки, описанные в настоящем изобретении, может вводиться в дозе от 104 до 109 клеток/кг массы тела, предпочтительно от 105 до 106 клеток/кг массы тела, включая все целые значения в пределах этих диапазонов. Композиции Т-клеток также могут вводиться несколько раз в пределах указанных доз. Клетки можно вводить с использованием методов инфузии, которые широко известны в иммунотерапии (см., например, Розенберг и другие, Медицинский журнал Новой Англии (The New England Journal of Medicine), 319: 1676, 1988). Оптимальная дозировка и режим лечения для конкретного пациента могут устанавливаться исключительно специалистом в области медицины путем диагностики признаков заболевания пациента и соответственно назначения лечения.
[0130] В некоторых вариантах осуществления, может быть желательно вводить активированные Т-клетки субъекту, а затем производить повторный забор крови (или выполнять аферез), активировать Т-клетки из взятой крови в соответствии с настоящим изобретением и повторно вливать кровь пациенту с данными активированными и размноженными Т-клетками. Этот процесс может выполняться несколько раз в течение нескольких недель. В некоторых вариантах осуществления, Т-клетки могут быть активированы из взятой крови в количестве от 10 см3 до 400 см3. В некоторых вариантах осуществления, Т-клетки активируются из взятой крови в количестве 20 см3, 30 см3, 40 см3, 50 см3, 60 см3, 70 см3, 80 см3, 90 см3 или 100 см3. Без ограничения теории, используя этот протокол множественного забора крови/множественной повторной инфузии, можно выделить определенные популяции Т-клеток.
[0131] Введение указанных композиций может осуществляться любым удобным способом, в том числе путем аэрозольной ингаляции, инъекции, перорального введения, переливания, введения под кожу или трансплантации. Композиции, описанные в настоящем изобретении, могут вводиться пациенту в виде инъекции подкожно, внутрикожно, внутрь опухоли, внутрь лимфоузла, интрамедуллярно, внутримышечно, внутривенно (в/в) или внутрибрюшинно. В одном варианте осуществления, композиции Т-клеток по настоящему изобретению вводят пациенту путем внутрикожной или подкожной инъекции. В другом варианте осуществления, композиции Т-клеток по настоящему изобретению предпочтительно вводят с помощью внутривенной инъекции. Композиции Т-клеток могут быть введены непосредственно в опухоль, лимфоузел или очаг инфекции.
[0132] В некоторых вариантах осуществления настоящего изобретения, клетки активируются и размножаются с помощью описанных в настоящем изобретении способов или других способов, известных в данной области, где Т-клетки размножаются до терапевтических уровней и вводятся пациенту в сочетании (например, до, одновременно или после) с любыми соответствующими способами лечения, включающими, но не ограничивающимися, лечением такими средствами, как антивирусотерапия, цидофовир и интерлейкин-2, цитарабин (также известный как ARA-C), лечение натализумабом пациентов с рассеянным склерозом, лечение эфализумабом пациентов с псориазом или другими методами лечения пациентов с прогрессирующей мультифокальной лейкоэнцефалопатией. В других вариантах осуществления, Т-клетки по настоящему изобретению могут использоваться в комбинации с химиотерапией, излучением, иммуносупрессивными препаратами, такими как циклоспорин, азатиоприн, метотрексат, микофенолат и такролимус (FK506), антителами или другими иммунодеструктивными препаратами, такие как Кэмпас (САМ РАТИ), антителами против CD3-клеток или другими антителами, цитоксином, флударибином, циклоспорином, такролимусом (FK506), рапамицином, микофеноловой кислотой, стероидами, депсипептидами (FR901228), цитокинами и облучением. Эти препараты ингибируют кальций-зависимую фосфотазу кальциневрина (циклоспорин и такролимус FK506) или ингибируют киназу p70S6, что важно для сигналов, индуцированных фактором роста (рапамицин). (Лю и другие, журнал «Cell» 66: 807-815, 1991; Хендерсон и другие, журнал «The Journal of Immunology» 73: 316-321, 1991; Биерер и другие, журнал «Current Opinion in Immunology» 5: 763-773, 1993; Изониеми (см. выше)). В еще одном варианте осуществления, композиции на основе клеток по настоящему изобретению вводят пациенту в сочетании (например, до, одновременно или после) с трансплантацией костного мозга, абляционной терапией Т-клетками, используя химиотерапевтические препараты такие, как флударабин, наружную дистанционную лучевую терапию (XRT), циклофосфамид или антитела, такие как OKT3 или САМРАТН. В другом варианте осуществления, композиции на основе клеток по настоящему изобретению вводят после абляционной терапии В-клетками, такими препаратами, которые реагируют с CD20, например, Ритуксан. К примеру, в одном варианте осуществления, субъекты могут пройти стандартное лечение с помощью высокодозной химиотерапии с последующей трансплантацией стволовых клеток периферической крови. В некоторых вариантах осуществления, после трансплантации, субъектам вводится размноженные иммунные клетки по настоящему изобретению. В дополнительном варианте осуществления размноженные клетки вводят до или после операции.
[0133] Доза вышеуказанных препаратов, вводимых пациенту, будет варьироваться в зависимости от точного состояния пациента, подлежащего лечению. Вычисление доз для введения человеку может осуществляться в соответствии с методиками, принятыми в данной области. Доза САМРАТН, например, обычно находится в диапазоне от 1 до 100 мг для взрослого пациента, вводится ежедневно в течение периода от 1 до 30 дней. Предпочтительная суточная доза составляет от 1 до 10 мг в день, хотя в некоторых случаях доза может быть увеличена до 40 мг в день (описанные в патенте США №6,120,766, включенные в качестве ссылки в полном объеме).
[0134] Дополнительная информация о методах лечения рака с использованием разработанных Т-клеток представлена в патенте США № US. 8906,682, включенной в качестве ссылки в полном объеме.
[0135] Варианты осуществления изобретения дополнительно относятся к способу лечения и/или ингибирования рака у пациента. Способ включает введение пациенту терапевтически эффективного количества растворимого рецептора, включающего внеклеточный домен белка PD-1. В некоторых вариантах осуществления изобретения, растворимый рецептор связывает белок PD-L1 и прерывает сигнал, поступающий от белка PD-1 о раковых клетках, и/или блокирует взаимодействие белков PD-1 и PD-L1. В некоторых вариантах осуществления изобретения, изолированный растворимый рецепторный полипептид включает аминокислотные остатки 20-519 согласно SEQ ID NO: 9.
[0136] «Растворимый рецептор» представляет собой рецепторный полипептид, не связанный с клеточной мембраной. Растворимые рецепторы чаще всего являются лигандсвязывающими рецепторными полипептидами, которые не имеют трансмембранных и цитоплазматических доменов. Растворимые рецепторы могут включать дополнительные аминокислотные остатки, такие как аффинные метки, которые обеспечивают очистку полипептида или обеспечивают сайты для присоединения полипептида к субстрату или последовательностям константных участков иммуноглобулина. Многие рецепторы клеточной поверхности имеют естественные, растворимые аналоги, которые продуцируются протеолизом. Считается, что растворимые рецепторные полипептиды практически не содержат трансмембранных и внутриклеточных сегментов полипептида, когда им не хватает достаточного количества этих сегментов для обеспечения мембранного соединения или сигнальной трансдукции соответственно.
[0137] Варианты осуществления изобретения дополнительно относятся к модифицированной клетке, включающей рецепторный полипептид, цитоплазменный домен которого усечен, рецепторный полипептид представляет собой, по меньшей мере, рецепторный полипептид белка запрограммированной смерти клетки 1 (PD-1), рецепторный полипептид связанного белка 4 цитотоксического Т-лимфоцита (CTLA-4), или рецептор В- и Т-лимфоцитарного аттенюатора (BTLA).
[0138] Варианты осуществления изобретения дополнительно относятся к способу лечения пациента. Способ включает введение пациенту клетки, при этом клетка генетически модифицирована для экспрессии рецепторного полипептида, причем цитоплазматический домен рецепторного полипептида усекается, причем рецепторный полипептид представляет собой, по меньшей мере, рецепторный полипептид белка запрограммированной смерти клетки 1 (PD-1), рецепторный полипептид связанного белка 4 цитотоксического Т-лимфоцита (CTLA-4), или рецептор В- и Т-лимфоцитарного аттенюатора (BTLA); химерный антигенный рецептор (CAR) включает домен распознавания антигена специфического антитела и внутриклеточный домен или рецептор модифицированной Т-клетки или рецептор Т-клетки широкого типа, специфическое антитело связывается с антигеном.
[0139] В некоторых вариантах осуществления изобретения, рецепторный полипептид представляет собой рецепторный полипептид PD-1, при этом цитоплазматический домен рецепторного полипептида PD-1 содержит иммунорецепторный тирозиновый мотив.
[0140] Варианты осуществления изобретения дополнительно относятся к модифицированной клетке, содержащей уменьшенное количество одного или нескольких рецепторов по сравнению с соответствующей клеткой дикого типа, один или несколько рецепторов включают, по меньшей мере, белок запрограммированной смерти клетки 1 (PD-1), связанный белок 4 цитотоксического Т-лимфоцита (CTLA-4), или В- и Т-лимфоцитарный аттенюатор (BTLA).
[0141] Варианты осуществления изобретения дополнительно относятся к способу лечения пациента. Способ включает введение пациенту клетки, при этом клетка модифицирована для экспрессии сниженного количества одного или нескольких рецепторов по сравнению с соответствующей клеткой дикого типа, причем один или несколько рецепторов включают, по меньшей мере, белок запрограммированной смерти клетки 1 (PD-1), связанный белок 4 цитотоксического Т-лимфоцита (CTLA-4), или В- и Т-лимфоцитарный аттенюатор (BTLA).
[0142] В некоторых вариантах осуществления изобретения, модифицированная клетка дополнительно включает в себя химерный антигенный рецептор (CAR), содержащий домен распознавания антигена специфического антитела и внутриклеточный домен или рецептор модифицированной Т-клетки или рецептор Т-клетки широкого типа. В некоторых вариантах осуществления изобретения, модифицированная клетка дополнительно включает в себя химерный антигенный рецептор (CAR), содержащий домен распознавания антигена специфического антитела и внутриклеточный домен или рецептор модифицированной Т-клетки или рецептор Т-клетки широкого типа, специфическое антитело связывается с антигеном.
[0143] В некоторых вариантах осуществления изобретения, модифицированная клетка уменьшает экспрессию одного или более генов, связанных путем биосинтеза или переносным путем с одним или несколькими рецепторами по сравнению с соответствующей клеткой дикого типа, или их комбинацией. В некоторых вариантах осуществления модифицированная клетка включает деструкцию одного или нескольких генов. В некоторых вариантах осуществления модифицированная клетка включает частичную или полную делецию одного или нескольких генов. В некоторых вариантах осуществления генетически модифицированная клетка реплицируется в организме пациента.
[0144] В некоторых вариантах осуществления изобретения, модифицированные клетки образуют клетки памяти в организме пациента. В этих случаях модифицированные клетки вводят пациенту внутривенно. В некоторых вариантах осуществления изобретения, модифицированные клетки сохраняются в организме пациента. Например, модифицированная клетка является аутогенной Т-клеткой. В другом примере клетка может включать, по меньшей мере, В-клетку, Т-клетку, NK-клетку, эмбриональную клетку или дендритную клетку.
[0145] В некоторых вариантах осуществления, заболевание может включать, по меньшей мере, рака, иммунодефицит, аутоиммунное заболевание или ожирение.
[0146] Примеры
[0147] Настоящее изобретение далее описано со ссылкой на следующие примеры. Эти примеры приведены только для иллюстрации и не предназначены для ограничения изобретения, если не указано иное. Таким образом, настоящее изобретение никоим образом не должно истолковываться как ограниченное следующими примерами, а скорее должно толковаться как охватывающее любые варианты, которые становятся очевидными в результате обучения, представленного в настоящем документе.
[0148] Пример 1
[0149] Экспрессия CAR и PD-1 на HEK293T и K562клетках
[0150] Были получены лентивирусные векторы, которые кодируют В-лимфоцитарный антиген CD19 химерного антигенного рецептора и модифицированный белок PD-1, разделенные участком внутренней посадки рибосом вируса энцефаломиокардита (см. «Химерные рецепторы, содержащие домены передачи сигнала белка CD137, способствующие повышению выживаемости Т-клеток и повышению антилейкозного эффекта в организме», журнал «Molecular Therapy», №17 ном. 8, 1453-1464 авг. 2009, включенный сюда путем ссылки). Информация о конструкциях ДНК, кодирующих CAR и модифицированный PD-1, представлена на фиг. 1 и таблице 1. Краткое описание этих конструкций и модулей приведена в таблицах 1-3.
[0151] Таблица 1 Конструкции ДНК и модули кодирования
[0152]

[0153] Клетки HEK293T и K562 трансдуцировали лентивирусными векторами. Для определения экспрессии CAR и PD-1 на этих клетках применяли метод проточной цитометрии. Как показано на фиг. 2А и 2В, клетки HEK293T и K562 экспрессируют CAR (фиг. 2А) и PD-1 (фиг. 2В).
[0154] Клетки HEK293T и K562 были получены из Американской коллекции типовых культур (АТСС, Манассас, штат Виргиния). Способы, связанные с выращиванием клеток, разработкой лентивирусных векторов и технологией проточной цитометрии, можно найти в статье «Химерные рецепторы, содержащие домены передачи сигнала белка CD137, способствующие повышению выживаемости Т-клеток и повышению антилейкозного эффекта в организме», (журнал «Molecular Therapy», №17 ном. 8, 1453-1464 авг. 2009), включенной в настоящее описание посредством ссылки.
[0155] Таблица 2 Обозначение последовательностей для различных конструкций
[0156]
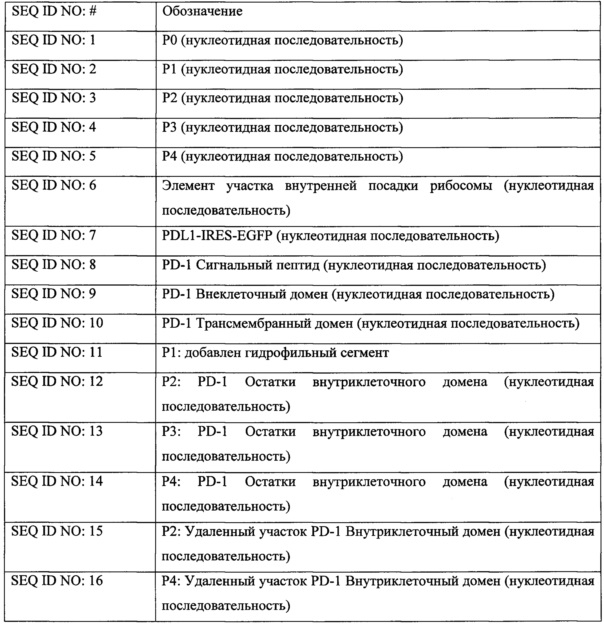
[0157] Пример 2
[0158] Экспрессия CAR и PD-1 на первичных Т-клетках.
[0159] Первичные Т-клетки были получены от пациентов. Полученные первичные Т-клетки трансдуцировали лентивирусными векторами. Для определения экспрессии CAR и PD-1 на первичных Т-клетках применяли метод проточной цитометрии. Как показано на фиг. 3А, 3В и 3С, первичные Т-клетки экспрессируют химерные антигенные рецепторы CAR (фиг. 3А) и белки PD-1 (фиг. 3В и 3С).
[0160] Способы, связанные с выращиванием клеток, разработкой лентивирусных векторов и технологией проточной цитометрии, можно найти в статье «Контроль над обширными развившимися опухолевыми ксенотрансплантатами с генетически перенацеленными Т-клетками человека, содержащими домены белков CD28 и CD137» (3360-3666 PNAS 3 марта 2009 г. №106 ном. 9), включенной в настоящее описание посредством ссылки.
[0161] Перечень последовательностей представлен в таблице 3.
[0162] Пример 3
[0163] Анализ цитотоксических Т-лимфоцитов
[0164] В этом анализе цитотоксичность клеток-мишеней (например, K562-CD19) измерялась путем сравнения выживаемости клеток-мишеней, культивированных эффекторными клетками (т.е. трансдуцированными Т-клетками) относительно выживаемости клеток-мишеней, культивированных отрицательными контрольными клетками (т.е. нетрансдуцированными Т-клетками). Клетки-мишени и эффекторные клетки или отрицательные контрольные клетки культивировали в течение примерно 24 часов, количественное соотношение между клетками-мишенями и эффекторными клетками или отрицательными контрольными клетками составляло около 10:1. Были измерены уровень выживаемости клеток-мишеней и продуцирование интерферон-гамма трансдуцированных Т-клеток и не трансдуцированных Т-клеток. Как показано на фиг. 4А и 4В, трансдуцированные Т-клетки, содержащие последовательности нуклеиновой кислоты, кодирующие CAR и различные PD-1, способны высвобождать интерферон-гамма и убивать клетки CD19. Все планки погрешностей представляют собой стандартное отклонение.
[0165] Способы, связанные с выращиванием клеток, проведением анализа цитотоксических Т-лимфоцитов, можно найти в статье «Контроль над обширными развившимися опухолевыми ксенотрансплантатами с генетически перенацеленными Т-клетками человека, содержащими домены белков CD28 и CD137» (3360-3666 PNAS 3 марта 2009 г. №106 ном. 9), включенной в настоящее описание посредством ссылки.
[0166] Пример 4
[0167] Конструкция PD-L1-ires-EGFP Nalm-6 клеточных линий
[0168] Были разработаны лентивирусные векторы, которые кодируют PD-L1-ires-EGFP (SEQ ID NO: 7). Клетки Nalm-6 трансдуцировали лентивирусными векторами Т-клеток при множественности заражения MOI 30 или MOI 100. Для определения экспрессии CAR и PD-1 на этих клетках применяли метод проточной цитометрии. Как показано на фиг. 5, NalM-6 PD-L1 экспрессировал PD-L1.
[0169] Клетки Nalm-6 были получены из Американской коллекции типовых культур (АТСС, Манассас, штат Виргиния). Способы, связанные с выращиванием клеток, разработкой лентивирусных векторов и технологией проточной цитометрии, можно найти в статье «Лечение развившегося лейкоза у мышей с помощью Т-клеток, содержащих мРНК» (журнал «ГЕНОВАЯ ТЕРАПИЯ ЧЕЛОВЕКА» 22: 1575-1586, декабрь 2011 г.), включенной в настоящее описание посредством ссылки.
[0170] Пример 5
[0171] Ингибирование цитотоксичности, вызванной PD-L1, снижается на Т-клетках, трансдуцированных CAR и модифицированным PD-1.
[0172] Клетки-мишени (напрмер, NalM-6, экспрессирующие PD-L1 или NalM-6) и различные эффекторные клетки (т.е. трансдуцированные Т-клетки) или отрицательные контрольные клетки (т.е. нетрансдуцированные Т-клетки) культивировали в течение примерно 24 часов, количественное соотношение между клетками-мишенями и эффекторными клетками или отрицательными контрольными клетками составляло около 10:1. Было измерено продуцирование интерферон-гамма трансдуцированных Т-клеток. Как показано на фиг. 6А и 6В, продуцирование интерферон-гамма химерными антигенными рецепторами Т-клеток снизилось, что указывало на потерю цитотоксичности в ответ на экспрессию PD-L1 на клетках NalM-6. Кроме того, по сравнению Т-клетками с химерными антигенными рецепторами, не модифицированными PD-1, потеря цитотоксичности, индуцированная PD-L1, снижается на Т-клетках с химерными антигенными рецепторами, трансдуцированными модифицированным PD-1. Например, потеря цитотоксичности Т-клеток, трансдуцированных CAR и PD-1 с точечной мутацией (то есть Р3), составляет около 22%, что на 43% ниже по сравнению с Т-клетками с CAR без модифицированного PD-1 (то есть Р0). Это указывает на то, что ингибирование цитотоксичности, вызванной PD-L1, снижается на Т-клетках, трансдуцированных CAR и модифицированным PD-1. Все планки погрешностей представляют собой стандартное отклонение.
[0173] Способы, связанные с выращиванием клеток, проведением анализа цитотоксических Т-лимфоцитов, можно найти в статье «Химерные рецепторы, содержащие домены передачи сигнала белка CD137, способствующие повышению выживаемости Т-клеток и повышению антилейкозного эффекта в организме», журнал «Molecular Therapy», №17 ном. 8, 1453-1464 авг. 2009, включенный сюда путем ссылки, включенной в настоящее описание посредством ссылки.















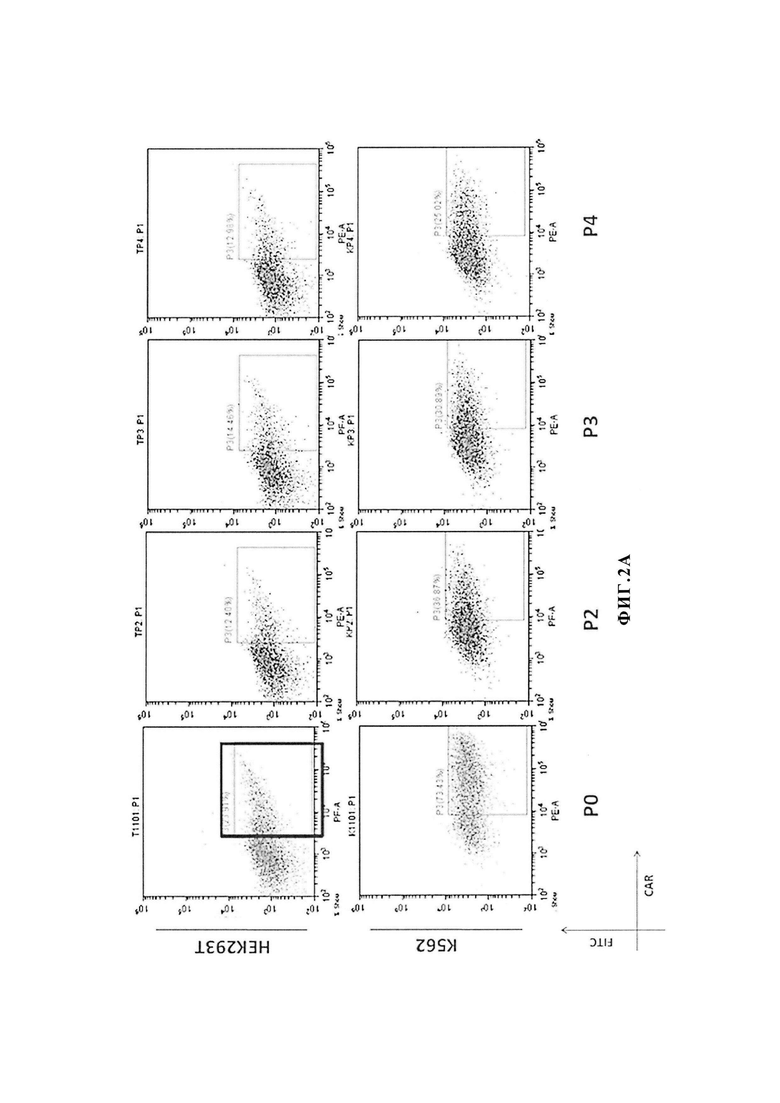

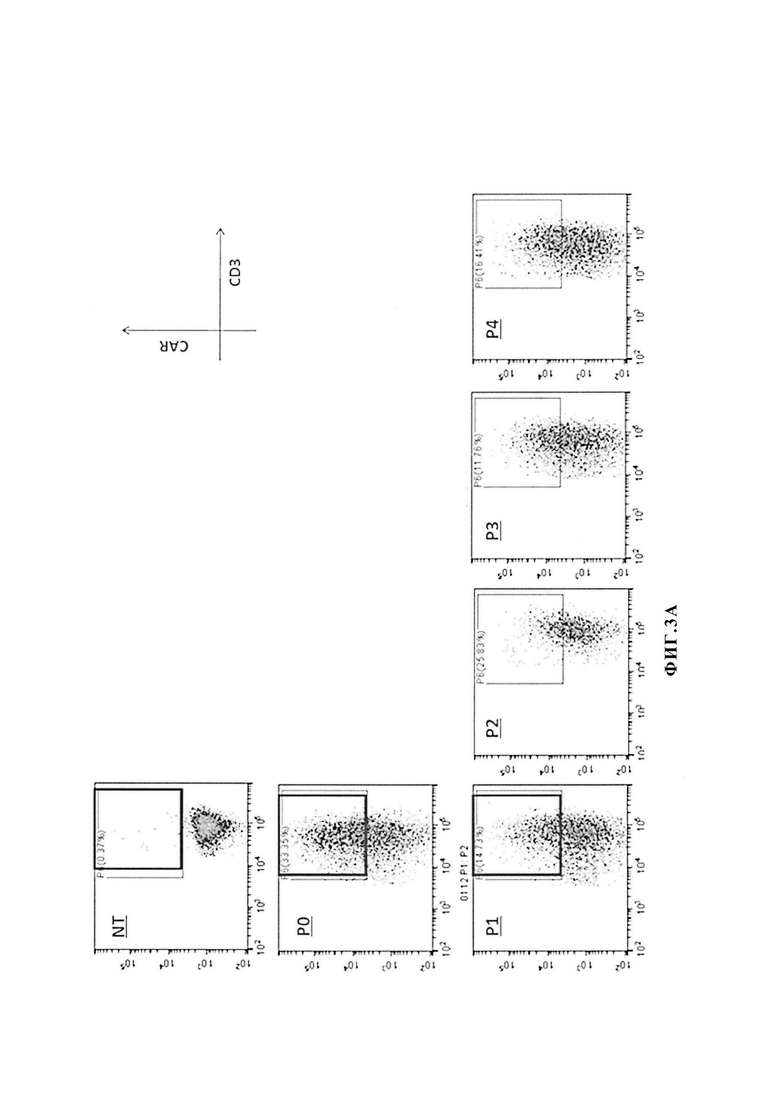



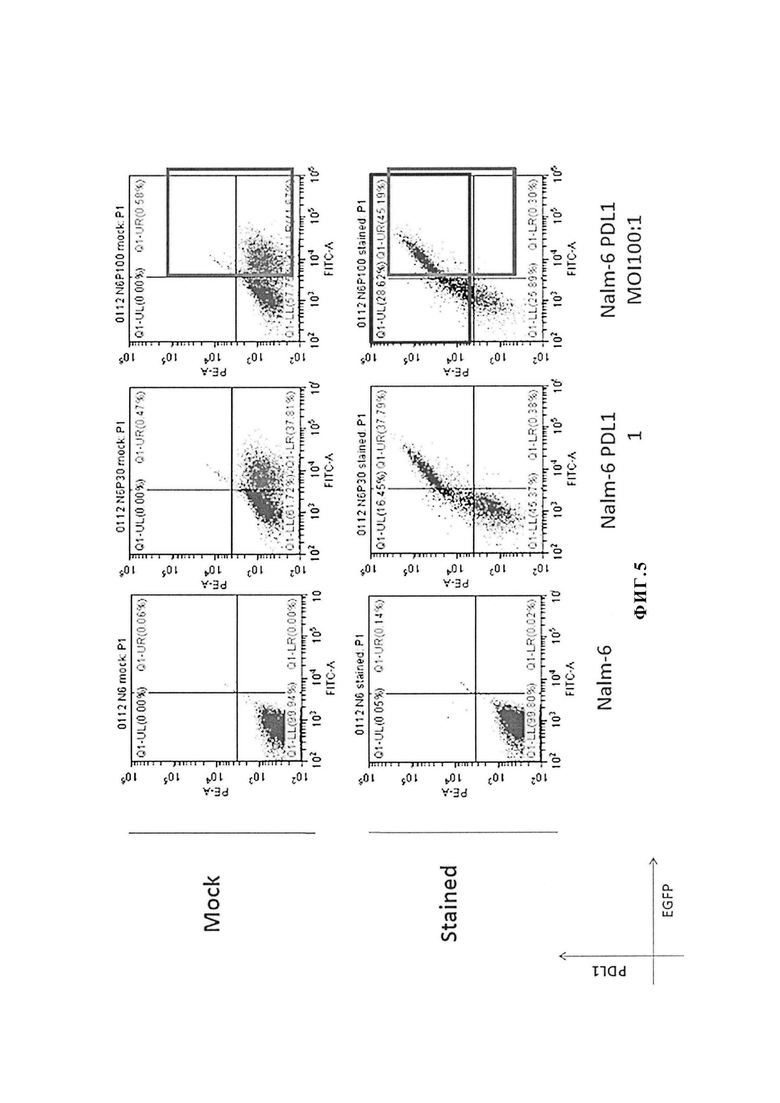
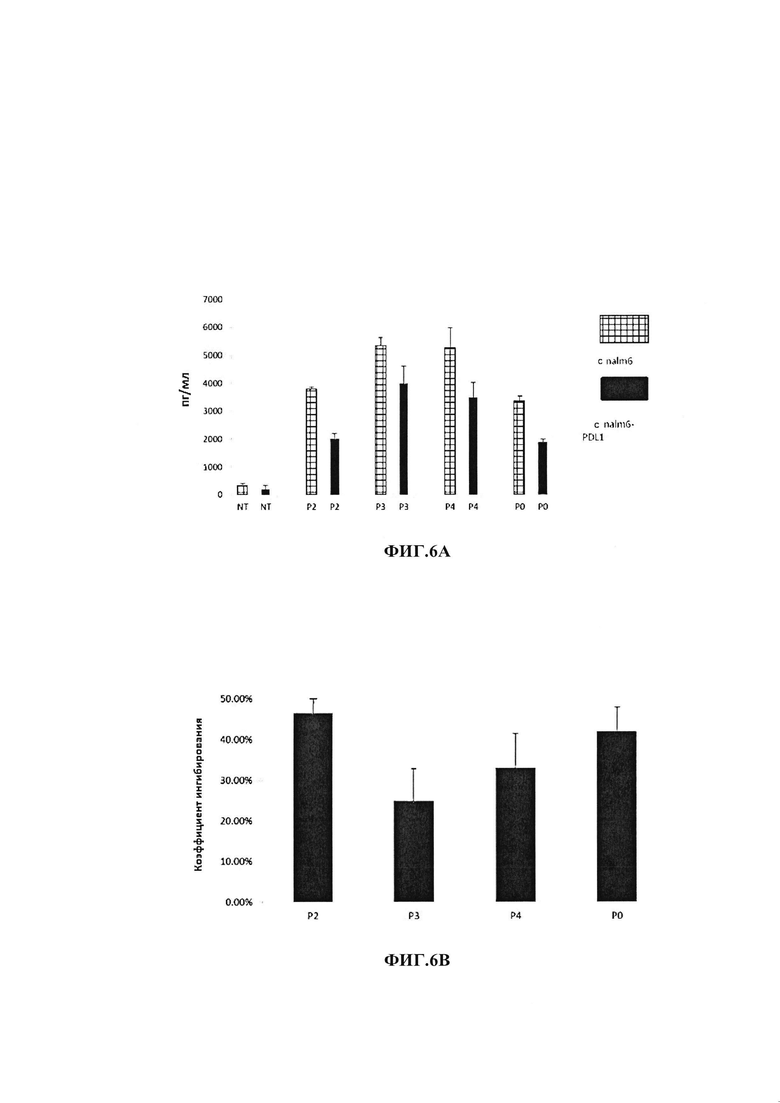
Группа изобретений относится к медицине и касается фармацевтической композиции, обладающей противоопухолевым эффектом, содержащей эффективное количество популяций Т-клеток человека, где Т-клетки человека включают изолированную нуклеотидную последовательность, содержащую нуклеотидную последовательность, кодирующую модифицированный белок запрограммированной смерти клетки 1 (PD-1) и нуклеотидную последовательность, кодирующую химерный антигенный рецептор (CAR), где модифицированный PD-1 и CAR экспрессируются в виде генных продуктов, которые являются отдельными полипептидами, и где модифицированный PD-1 является доминантно-негативным PD-1. Группа изобретений также касается способа снижения ингибирующего эффекта PD-L1 на Т-клетки человека, включающего введение первой нуклеотидной последовательности и второй нуклеотидной последовательности в Т-клетки человека. Где первая нуклеотидная последовательность кодирует модифицированный PD-1, который является доминантно-негативным PD-1, и вторая нуклеотидная последовательность кодирует CAR. Группа изобретений обеспечивает снижение ингибирующего эффекта PD-L1 на Т-клетки. 2 н. и 25 з.п. ф-лы, 5 пр., 6 ил., 3 табл.
1. Фармацевтическая композиция, обладающая противоопухолевым эффектом, содержащая эффективное количество популяций Т-клеток человека, где Т-клетки человека включают изолированную нуклеотидную последовательность, содержащую нуклеотидную последовательность, кодирующую модифицированный белок запрограммированной смерти клетки 1 (PD-1) и нуклеотидную последовательность, кодирующую химерный антигенный рецептор (CAR), где модифицированный PD-1 и CAR экспрессируются в виде генных продуктов, которые являются отдельными полипептидами и где модифицированный PD-1 является доминантно-негативным PD-1.
2. Фармацевтическая композиция по п. 1, отличающаяся тем, что модифицированный PD-1 препятствует взаимодействию между PD-1 Т-клетки человека и PD-L1 определенной клетки.
3. Фармацевтическая композиция по п. 1, отличающаяся тем, что нуклеотидная последовательность кодирует модифицированный PD-1 содержит нуклеиновую кислоту, кодирующую усеченный PD-1, который не включают внутриклеточный домен.
4. Фармацевтическая композиция по п. 1, отличающаяся тем, что модифицированный PD-1 включает внеклеточный домен PD-1 или трансмембранный домен PD-1 или их комбинацию.
5. Фармацевтическая композиция по п. 1, отличающаяся тем, что модифицированный PD-1 содержит аминокислотные последовательности согласно SEQ ID NO: 9 или аминокислотные последовательности согласно SEQ ID NO: 10 или их комбинацию.
6. Фармацевтическая композиция по п. 1, отличающаяся тем, что модифицированный PD-1 представляет собой растворимый рецептор, содержащий внеклеточный домен PD-1, который связывается с PD-L1 определенной клетки.
7. Фармацевтическая композиция по п. 1, отличающаяся тем, что опухолевым антигеном является В-лимфоцитарный антиген CD 19.
8. Фармацевтическая композиция по п. 1, отличающаяся тем, что стимулирующая молекула содержит 4-1 ВВ или CD28 или их комбинацию.
9. Фармацевтическая композиция по п. 1, отличающаяся тем, что модифицированный PD-1 содержит аминокислотную последовательность согласно SEQ ID NO: 12.
10. Фармацевтическая композиция по п. 1, отличающаяся тем, что модифицированный PD-1 содержит аминокислотную последовательность согласно SEQ ID NO: 13.
11. Фармацевтическая композиция по п. 1, отличающаяся тем, что модифицированный PD-1 содержит аминокислотную последовательность согласно SEQ ID NO: 14.
12. Фармацевтическая композиция по п. 1, отличающаяся тем, что модифицированный PD-1 содержит точечные мутации аминокислот сайтов фосфорилирования PD-1 широкого типа.
13. Фармацевтическая композиция по п. 1, отличающаяся тем, что Т-клетка содержит экспрессирующий вектор, представляющий собой вирусный вектор, выбранный из группы, состоящей из ретровирусного вектора, лентивирусного вектора, аденовирусного вектора и аденоассоциированного вирусного вектора.
14. Фармацевтическая композиция по п. 1, отличающаяся тем, что полипептид представляет собой, по меньшей мере, рецепторный полипептид белка запрограммированной смерти клетки 1 (PD-1), рецепторный полипептид связанного белка 4 цитотоксического Т-лимфоцита (CTLA-4), или рецептор В-и Т-лимфоцитарного аттенюатора (BTLA).
15. Фармацевтическая композиция по п. 14, отличающаяся тем, что рецепторный полипептид представляет собой рецепторный полипептид PD-1, при этом цитоплазматический домен рецепторного полипептида PD-1 содержит иммунорецепторный тирозиновый мотив.
16. Способ снижения ингибирующего эффекта PD-L1 на Т-клетки человека, включающий:
введение первой нуклеотидной последовательности и второй нуклеотидной последовательности в Т-клетки человека, где:
первая нуклеотидная последовательность кодирует модифицированный PD-1, который является доминантно-негативным PD-1 и который уменьшает ингибирующий эффект PD-L1 на Т-клетках человека; и
вторая нуклеотидная последовательность кодирует CAR, включающий внеклеточный домен, который распознает опухолевый антиген клетки-мишени, трансмембранный домен и внутриклеточный домен, содержащий сигнальный домен CD3дзета и сигнальный домен костимулирующей молекулы, где модифицированный PD-1 и CAR экспрессируются в виде генных продуктов, которые являются отдельными полипептидами.
17. Способ по п. 16, отличающийся тем, что модифицированный PD-1 препятствует взаимодействию между PD-1 Т-клетки человека и PD-L1 определенной клетки.
18. Способ по п. 16, отличающийся тем, что модифицированный PD-1 содержит нуклеиновую кислоту, кодирующую усеченный PD-1, который не включают внутриклеточный домен.
19. Способ по п. 16, отличающийся тем, что модифицированный PD-1 не включает внеклеточный домен PD-1 или трансмембранный домен PD-1 или их комбинацию.
20. Способ по п. 16, отличающийся тем, что модифицированный PD-1 содержит аминокислотные последовательности согласно SEQ ID NO: 9 или аминокислотные последовательности согласно SEQ ID NO: 10 или их комбинацию.
21. Способ по п. 16, отличающийся тем, что модифицированный PD-1 представляет собой растворимый рецептор, содержащий внеклеточный домен PD-1, который связывается с PD-L1 определенной клетки.
22. Способ по п. 16, отличающийся тем, что растворимый PD-1 не присоединяется к клеточной мембране клетки.
23. Способ по п. 16, отличающийся тем, что опухолевым антигеном является В-лимфоцитарный антиген CD 19.
24. Способ по п. 16, отличающийся тем, что костимулирующая молекула содержит 4-1 ВВ или CD28 или их комбинацию.
25. Способ по п. 16, отличающийся тем, что модифицированный PD-1 содержит аминокислотную последовательность согласно SEQ ID NO: 12.
26. Способ по п. 16, отличающийся тем, что модифицированный PD-1 содержит аминокислотную последовательность согласно SEQ ID NO: 13.
27. Способ по п. 16, отличающийся тем, что модифицированный PD-1 содержит аминокислотную последовательность согласно SEQ ID NO: 14.
| WO 2012079000 A1, 14.06.2012 | |||
| WO 2013019615 A2, 07.02.2013 | |||
| SONG MY | |||
| et al | |||
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| ZHANG X | |||
| et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
Авторы
Даты
2019-05-22—Публикация
2016-03-01—Подача