ПРИТЯЗАНИЯ НА ПРИОРИТЕТ
Данная заявка претендует на приоритет предварительной заявки Соединенных Штатов № 61/769543, поданной 26 февраля 2013 г., содержание которой включено в настоящее описание путем ссылки во всей ее полноте в настоящем документе.
ИНФОРМАЦИЯ О ГРАНТОВОЙ ПОДДЕРЖКЕ
Это изобретение было сделано при правительственной поддержке в рамках грантов №№ CA95152, CA138738, CA059350 и CA08748 от Национального института здравоохранения. Правительство имеет определенные права на изобретение.
Введение
Настоящее изобретение предоставляет способы и композиции для усиления иммунного ответа по отношению к злокачественным опухолям и патогенным микроорганизмам. Это относится к иммунореактивным клеткам, несущим антигенные рецепторы, которые могут представлять собой химерные антигенные рецепторы (CAR), которые экспрессируют введенные лиганды для иммуномодулирующих молекул. В конкретных вариантах осуществления, сконструированные иммунореактивные клетки являются антиген-направляемыми и устойчивыми к иммуносупрессии и/или обладают улучшенными иммунитет-активирующими свойствами.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Большинство зрелых В-клеточных злокачественных опухолей, включая острый лимфобластный лейкоз (ALL), хронический лимфоцитарный лейкоз и неходжкинскую лимфому, являются неизлечимыми, несмотря на имеющиеся в настоящее время способы лечения. Адоптивные способы лечения с помощью генно-инженерных аутологичных Т-клеток продемонстрировали подтверждение терапевтической эффективности при меланоме и индолентных В-клеточных злокачественных новообразованиях. Т-клетки могут быть модифицированы, чтобы быть нацеленными на опухоль-ассоциированные антигены, путем введения генов, кодирующих Т-клеточные рецепторы, называемые химерными антигенными рецепторами (CAR), специфическими для таких антигенов. Иммунотерапия представляет собой терапию открытыми радионуклидами, которая имеет потенциал для обеспечения лечения злокачественной опухоли.
При этом, злокачественные клетки адаптируются для создания иммуносупрессивного микроокружения, чтобы защитить себя от иммунного распознавания и элиминации. Это "враждебное" микроокружение опухоли бросает вызов способам лечения с помощью стимуляции иммунного ответа, таким как адресные Т-клеточные способы лечения. Соответственно, срочно требуются новые терапевтические стратегии для лечения неоплазии.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение в общем предоставляет иммунореактивные клетки (например, Т-клетки, натуральные киллерные (NK) клетки, цитотоксические Т-лимфоциты (CTL) и регуляторные Т-клетки), экспрессирующие антиген-связывающий рецептор (например, CAR или TCR), обладающий активностью активации иммунных клеток, и одноцепочечный вариабельный фрагмент (scFv), который связывает антиген, имеющий иммуносупрессивную активность (например, CD47, PD-1, CTLA-4 и их лиганды), тем самым снижая или устраняя иммуносупрессивную активность антигена.
Изобретение далее предоставляет иммунореактивные клетки (например, Т-клетки, натуральные киллерные (NK) клетки, цитотоксические Т-лимфоциты (CTL) и регуляторные Т-клетки), экспрессирующие антиген-связывающий рецептор (например, CAR или TCR), имеющий активность активации иммунных клеток, и одноцепочечный вариабельный фрагмент (scFv), который связывает антиген, обладающий иммуностимулирующий или провоспалительной активностью (например, CD28, OX-40, 4-1BB, CD40 и их лиганды), повышая тем самым иммуностимулирующую активность антигена.
Изобретение далее предоставляет иммунореактивные клетки (например, Т-клетки, натуральные киллерные (NK) клетки, цитотоксических Т-лимфоцитов (CTL) и регуляторные Т-клетки), экспрессирующие антиген-связывающий рецептор (например, CAR или TCR), имеющий активность активации иммунных клеток, и CD40L, например, экзогенный CD40L (CD40L, который был введен непосредственно или косвенно в клетку (например, посредством вектора незащищенной нуклеиновой кислота, включающего последовательность нуклеиновых кислот, кодирующих CD40L), по сравнению с эндогенным CD40L, возникающим в самой клетке), повышая тем самым иммуностимулирующую активность антигена.
Соответственно, изобретение предоставляет способы применения таких иммунореактивных клеток для лечения неоплазии, инфекционного заболевания и других патологий.
В одном аспекте, изобретение предоставляет выделенную иммунореактивную клетку, имеющую антиген-узнающий рецептор, который связывает антиген, причем связывание активирует иммунореактивную клетку, и растворимый одноцепочечный вариабельный фрагмент (scFv), который связывается с полипептидом, обладающим иммуносупрессивной активностью или иммуностимулирующей активностью.
В другом аспекте, изобретение предоставляет способ лечения или предупреждения неоплазии у индивидуума, включающий введение индивидууму эффективного количества иммунореактивной клетки, имеющей антиген-узнающий рецептор, который связывается с первым антигеном, причем связывание активирует иммунореактивную клетку, и растворимого одноцепочечного вариабельного фрагмента (scFv), который связывается с полипептидом, который обладает иммуносупрессивной активностью или иммуностимулирующей активностью, предоставляя тем самым лечения или предупреждение неоплазии у нидивидуума. В неограничивающих вариантах осуществления антиген-узнающий рецептор представляет собой CAR.
В другом аспекте, изобретение предоставляет способ уменьшения опухолевой массы у индивидуума, включающий введение индивидууму эффективного количества иммунореактивной клетки, имеющей антиген-узнающий рецептор, который связывается с первым антигеном, причем связывание активирует иммунореактивную клетку, и растворимого одноцепочечного вариабельного фрагмента (scFv), который связывается с полипептидом, который обладает иммуносупрессивной активностью или иммуностимулирующей активностью, тем самым вызывая гибель опухолевых клеток у индивидуума. В еще одном аспекте, изобретение предоставляет способ увеличения выживаемости индивидуума, имеющего неоплазию, включающий введение индивидууму эффективного количества иммунореактивной клетки с антиген-узнающим рецептором, который связывается с первым антигеном, причем связывание активирует иммунореактивную клетку, и растворимого одноцепочечного вариабельного фрагмента (scFv), который связывается с полипептидом, который обладает иммуносупрессивной активностью или иммуностимулирующей активностью, увеличивая тем самым выживаемость индивидуума. В неограничивающих вариантах осуществления антиген-узнающий рецептор представляет собой CAR.
В различных неограничивающих вариантах осуществления изобретение предоставляет способ увеличения продуцирования иммунно-активирующих цитокинов в ответ на раковую клетку у индивидуума, включающий введение индивидууму иммунореактивной клетки, имеющей антиген-узнающий рецептор, который связывает антиген раковой клетки, и дополнительно экспрессирующей экзогенный CD40L. В конкретном неограничивающем варианте осуществления, иммунно-активирующим цитокинов является IL-12. В неограничивающих вариантах осуществления антиген-узнающий рецептор представляет собой CAR.
В различных неограничивающих вариантах осуществления изобретение предоставляет способ увеличения продуцирования иммунно-активирующих цитокинов в ответ на патоген в индивидуума, включающий введение индивидууму иммунореактивной клетки, имеющей антиген-узнающий рецептор, который связывает антиген патогена, и дополнительно экспрессирующей экзогенный CD40L. В конкретном неограничивающем варианте осуществления, иммунно-активирующим цитокином является IL-12. В неограничивающих вариантах осуществления антиген-узнающий рецептор представляет собой CAR.
В различных неограничивающих вариантах осуществления изобретение предоставляет способ усиления CD8+-цитотоксического Т-клеточного ответа на раковую клетку у индивидуума, включающий введение индивидууму иммунореактивной клетки, имеющей антиген-узнающий рецептор, который связывает антиген раковой клетки, и дополнительно экспрессирующей экзогенный CD40L. В неограничивающих вариантах осуществления антиген-узнающий рецептор представляет собой CAR.
В различных неограничивающих вариантах осуществления изобретение предоставляет способ усиления CD8+-цитотоксического Т-клеточного ответа на патоген у индивидуума, включающий введение индивидууму иммунореактивной клетки, имеющей антиген-узнающий рецептор, который связывает антиген патогена, и дополнительно экспрессирующей экзогенный CD40L. В неограничивающих вариантах осуществления антиген-узнающий рецептор представляет собой CAR.
В различных неограничивающих вариантах осуществления изобретение предоставляет способ стимулирования созревания дендритных клеток у индивидуума, имеющего злокачественное новообразование, включающий введение индивидууму иммунореактивной клетки, имеющей антиген-узнающий рецептор, который связывает антиген раковой клетки и дополнительно экспрессирующей экзогенный CD40L. В неограничивающих вариантах осуществления антиген-узнающий рецептор представляет собой CAR.
В различных неограничивающих вариантах осуществления изобретение предоставляет способ стимулирования созревания дендритных клеток у индивидуума, имеющего заболевание, вызываемое патогеном, включающий введение индивидууму иммунореактивной клетки, имеющей антиген-узнающий рецептор, который связывает антиген патогена и дополнительно экспрессирующей экзогенный CD40L. В неограничивающих вариантах осуществления антиген-узнающий рецептор представляет собой CAR.
В еще одном аспекте, изобретение предоставляет способ лечения или предупреждения неоплазии у индивидуума, включающий введение индивидууму эффективного количества иммунореактивной клетки, имеющей антиген-узнающий рецептор, который связывается с первым антигеном, причем связывание активирует иммунореактивную клетку, и экспрессирующей экзогенный CD40L, предоставляя тем самым лечение или предупреждение неоплазии у индивидуума. В неограничивающих вариантах осуществления антиген-узнающий рецептор представляет собой CAR.
В другом аспекте, изобретение предоставляет способ уменьшения опухолевой массы у индивидуума, включающий введение индивидууму эффективного количества иммунореактивной клетки, имеющей антиген-узнающий рецептор, который связывается с первым антигеном, причем связывание активирует иммунореактивную клетку, и экспрессирующей экзогенный CD40L, тем самым вызывая гибель опухолевых клеток у индивидуума. В еще одном аспекте, изобретение предоставляет способ увеличения выживаемости у индивидуума, имеющего неоплазию, включающий введение индивидууму эффективного количества иммунореактивной клетки, имеющей антиген-узнающий рецептор, который связывается с первым антигеном, причем связывание активирует иммунореактивную клетку, и экспрессирующей экзогенный CD40L, тем самым увеличивая выживаемость индивидуума.
В еще одном аспекте, изобретение предоставляет способ лечения рака крови у индивидуума, нуждающегося в этом, пау индивидуума, нуждающегося в этом, включающий введение индивидууму терапевтически эффективного количества Т-клеток, имеющих антиген-узнающий рецептор, который связывает CD19, причем связывание активирует иммунореактивную клетку, и растворимого одноцепочечного вариабельного фрагмента (scFv), который связывает один или более из CD47, PD-1, CTLA-4 и их лигандов, предоставляя тем самым лечение рака крови у индивидуума. В неограничивающих вариантах осуществления антиген-узнающий рецептор представляет собой CAR.
В еще одном аспекте, изобретение предоставляет способ лечения рака крови у индивидуума, нуждающегося в этом, включающий введение индивидууму терапевтически эффективного количества Т-клетки, имеющей антиген-узнающий рецептор, который связывает CD19, причем связывание активирует иммунореактивную клетку, и экспрессирующей экзогенный CD40L, предоставляя тем самым лечение рака крови у индивидуума. В неограничивающих вариантах осуществления антиген-узнающий рецептор представляет собой CAR.
В одном аспекте, изобретение предоставляет способ получения антиген-специфической иммунореактивной клетки, включающий введение в иммунореактивную клетку нуклеотидной последовательности, кодирующей одноцепочечный вариабельный фрагмент (scFv), который связывается с полипептидом, обладающим иммуносупрессивной активностью или иммуностимулирующей активностью, причем иммунореактивная клетка имеет антиген-узнающий рецептор, который связывает антиген. В неограничивающих вариантах осуществления антиген-узнающий рецептор представляет собой CAR.
В одном аспекте, изобретение предоставляет способ получения антиген-специфической иммунореактивной клетки, включающий введение в иммунореактивную клетку последовательности нуклеиновых кислот, которая кодирует CD40L, причем иммунореактивная клетка имеет антиген-узнающий рецептор, который связывает антиген. В неограничивающих вариантах осуществления последовательность нуклеиновых кислот, которая кодирует CD40L, функционально связана с промоторным элементом, конститутивно или индуцибельно экспрессируемым в иммунореактивной клетке, дополнительно содержащимся в векторе. В неограничивающих вариантах осуществления антиген-узнающий рецептор представляет собой CAR. В неограничивающих вариантах осуществления изобретение предоставляет нуклеиновую кислоту, включающую последовательность, кодирующую CAR и кодирующую CD40L, каждый из которых необязательно функционально связан с промоторным элементом, конститутивно или индуцибельно экспрессируемым в иммунореактивной клетке, и указанная нуклеиновая кислота может дополнительно содержаться в векторе. В одном аспекте, изобретение предоставляет вектор, имеющий последовательность нуклеиновых кислот, кодирующую антиген-узнающий рецептор, который связывает антиген, и последовательность нуклеиновых кислот, кодирующую растворимый одноцепочечный вариабельный фрагмент (scFv), который связывается с полипептидом, имеющим иммуносупрессивной активностью или иммуностимулирующей активностью. В неограничивающих вариантах осуществления антиген-узнающий рецептор представляет собой CAR.
В одном аспекте, изобретение предоставляет вектор, содержащий последовательность нуклеиновых кислот, кодирующую антиген-узнающий рецептор, который связывает антиген, и последовательность нуклеиновых кислот, кодирующую CD40L. В неограничивающих вариантах осуществления антиген-узнающий рецептор представляет собой CAR. В одном конкретном неограничивающем варианте осуществления, изобретение предоставляет ретровирусный вектор, содержащий анти-CD19 CAR (1928z)- и CD40L- кодирующую нуклеиновую кислоту.
В родственном аспекте изобретение предоставляет фармацевтическую композицию, содержащую эффективное количество иммунореактивной клетки по любому аспекту изобретения, обозначенному в настоящем документе, в фармацевтически приемлемом наполнителе. В другом родственном аспекте изобретение предоставляет фармацевтическую композицию для лечения неоплазии, содержащую эффективное количество опухолевой антиген - специфичной Т-клетки любого аспекта изобретения, обозначенного в настоящем документе, в фармацевтически приемлемом наполнителе.
В дополнительном аспекте, изобретение предоставляет набор для лечения неоплазии, патогенной инфекции, аутоиммунного расстройства или аллогенной трансплантации, содержащий иммунореактивную клетку, имеющую антиген-узнающий рецептор, который связывает антиген и активирует иммунореактивную клетку, и растворимый одноцепочечный вариабельный фрагмент (scFv), который связывается с полипептидом, который обладает иммуносупрессивной активностью или иммуностимулирующей активностью. В неограничивающих вариантах осуществления антиген-узнающий рецептор представляет собой CAR. В конкретных вариантах осуществления набор дополнительно содержит письменные инструкции по использованию клетки для лечения индивидуума, имеющего неоплазию, патогенную инфекцию, аутоиммунное расстройство или аллогенную трансплантацию.
В дополнительном аспекте, изобретение предоставляет набор для лечения неоплазии, патогенной инфекции, аутоиммунного расстройства или аллогенной трансплантации, содержащий иммунореактивную клетку, имеющую антиген-узнающий рецептор, который связывает антигеном и активирует иммунореактивную клетку, и экспрессирующую экзогенный CD40L. В неограничивающих вариантах осуществления антиген-узнающий рецептор представляет собой CAR. В конкретных вариантах осуществления набор дополнительно содержит письменные инструкции по использованию клеток для лечения индивидуума, имеющего неоплазию, патогенную инфекцию, аутоиммунное расстройство или аллогенную трансплантацию.
В дополнительном аспекте, изобретение предоставляет набор для лечения неоплазии, патогенной инфекции, аутоиммунного расстройства или аллогенной трансплантации, содержащий нуклеиновую кислоту, кодирующую CAR, который распознает антиген неоплазии, патогена инфекции, аутоиммунного расстройства или трансплантата, подвергаемого лечению, и нуклеиновую кислоту, кодирующую растворимый одноцепочечный вариабельный фрагмент (scFv), который связывается с полипептидом, обладающим иммуносупрессивной активностью или иммуностимулирующей активностью. При необходимости одна или обе нуклеиновые кислоты могут быть включены в вектор, который может представлять собой один и тот же вектор (бицистронный), или отдельные векторы. Нуклеиновая кислота, кодирующая CAR, и/или нуклеиновая кислота, кодирующая scFv, могут быть функционально связаны с промотором, который может представлять собой один и тот же промотор или разные промоторы. В конкретных вариантах осуществления набор дополнительно содержит письменные инструкции по использованию клеток для лечения индивидуума, имеющего неоплазию, патогенную инфекцию, аутоиммунное расстройство или аллогенную трансплантацию.
В дополнительном аспекте, изобретение предоставляет набор для лечения злокачественного новообразования, содержащий нуклеиновую кислоту, кодирующую CAR, который распознает антиген злокачественного новообразования, и нуклеиновую кислоту, кодирующую растворимый одноцепочечный вариабельный фрагмент (scFv), который связывается с полипептидом, обладающий иммуносупрессивной активностью или иммуностимулирующей активностью. При необходимости одна или обе нуклеиновые кислоты могут быть включены в вектор, который может представлять собой один и тот же вектор (бицистронный), или отдельные векторы. Нуклеиновая кислота, кодирующая CAR, и/или нуклеиновая кислота, кодирующая scFv, могут быть функционально связаны с промотором, который может представлять собой один и тот же промотор или разные промоторы. В конкретных вариантах осуществления набор дополнительно содержит письменные инструкции по использованию клеток для лечения индивидуума, имеющего злокачественное новообразование.
В дополнительном аспекте, изобретение предоставляет набор для лечения злокачественного новообразования или патоген-опосредованного расстройства, содержащий нуклеиновую кислоту, кодирующую CAR 67, который распознает антиген злокачественного новообразования или патогена, и нуклеиновую кислоту, кодирующую растворимый одноцепочечный вариабельный фрагмент (scFv), который связывается с полипептидом, обладающим иммуносупрессивной активностью или иммуностимулирующей активностью. При необходимости одна или обе нуклеиновые кислоты могут быть включены в вектор, который может представлять собой один и тот же вектор (бицистронный), или отдельные векторы. Нуклеиновая кислота, кодирующая CAR, и/или нуклеиновая кислота, кодирующая scFv, могут быть функционально связаны с промотором, который может представлять собой один и тот же промотор или разные промоторы. В конкретных вариантах осуществления набор дополнительно содержит письменные инструкции по использованию клеток для лечения индивидуума, имеющего злокачественное новообразование или расстройство. В дополнительном аспекте, изобретение предоставляет набор для лечения злокачественного новообразования или патоген-опосредованного расстройства, содержащий нуклеиновую кислоту, кодирующую CAR, который распознает антиген злокачественного новообразования или патогена, и нуклеиновую кислоту, кодирующую CD40L. При необходимости одна или обе нуклеиновые кислоты могут быть включены в вектор, который может представлять собой один и тот же вектор (бицистронный), или отдельные векторы. Нуклеиновая кислота, кодирующая CAR, и/или нуклеиновая кислота, кодирующая CD40L, могут быть функционально связаны с промотором, который может представлять собой один и тот же промотор или разные промоторы. В конкретных вариантах осуществления набор дополнительно содержит письменные инструкции по использованию клеток для лечения индивидуума, имеющего злокачественное новообразование или расстройство.
В различных вариантах осуществления любого из аспектов, определенных в настоящем документе, клетку выбирают из группы, состоящей из Т-клетки, природной киллерной (NK) клетки, цитотоксического Т-лимфоцита (CTL), регуляторной Т-клетки, эмбриональной стволовой клетки человека и плюрипотентной стволовой клетки, из которой лимфоидные клетки могут быть дифференцированы. В различных вариантах осуществления любого из аспектов, определенных в настоящем документе, иммунореактивная клетка является аутологичной.
В различных вариантах осуществления любого из аспектов, определенных в настоящем документе, антиген-узнающий рецептор представляет собой Т-клеточный рецептор (TCR) или химерный антигенный рецептор (CAR). В различных вариантах осуществления любого из аспектов, определенных в настоящем документе, антиген-узнающий рецептор является экзогенным или эндогенным. В различных вариантах осуществления любого из аспектов, определенных в настоящем документе, антиген-узнающий рецептор является рекомбинантно экспрессированным. В различных вариантах осуществления любого из аспектов, определенных в настоящем документе, антиген-узнающий рецептор экспрессируется с вектора. В различных вариантах осуществления любого из аспектов, определенных в настоящем документе, домен внутриклеточной сигнализации антиген-узнающего рецептора представляет собой домен сигнализации CDζ-цепи, CD3ζ-цепи, CD97, CD11a-CD18, CD2, ICOS, CD27, CD154, CDS, OX40, 4-IBB, CD28, их части или их комбинации. В неограничивающих вариантах осуществления антиген-узнающий рецептор представляет собой CAR, включающий, по меньшей мере, часть CD28, 4-IBB и/или CD3ζ-цепи (см., например, Zhong et al., 2010, Molecular Ther. 18(2):413-420), вместе с антиген-связывающей частью. В неограничивающих вариантах осуществления антиген-узнающий рецептор представляет собой CAR, описанный в Kohn et al., 2011, Molecular Ther. 19(3):432-438), в котором необязательно антиген-связывающая часть заменяется аминокислотной последовательностью, которая связывается с другим опухолевым или патогенным антигеном. В различных вариантах осуществления клетка экспрессирует рекомбинантный или эндогенный антигенный рецептор, который представляет собой 1928z или 4H1128z.
В различных вариантах осуществления любого из аспектов, определенных в настоящем документе, антиген представляет собой опухолевый или патогенный антиген. В различных вариантах осуществления любого из аспектов, определенных в настоящем документе, опухолевый антиген представляет собой один или более из CD19, MUC16, MUC1, CA1X, СЕА, CDS, CD7, CD10, CD20, CD22, CD30, CD33, CD34, CD38, CD41, CD44, CD49f, CD56, CD74, CD133, CD138, антигена клеток, инфицированных цитомегаловирусом (CMV), EGP-2, EGP-40, EpCAM, eRB-В2,3,4, FBP, эмбрионального ацетилхолинового рецептора, фолатного рецептора-α, GD2, GD3, HER-2, hTERT, IL-13R-a2, κ-легкой цепи, KDR, LeY, молекулы адгезии клеток L1, MAGE-A1, мезотелина, лигандов NKG2D, NY-ESO-1, онкофетального антигена (h5T4), PSCA, PSMA, ROR1, TAG-72, VEGF-R2 или WT-1. В конкретных вариантах осуществления антиген представляет собой CD19 или MUC16. Аминокислотные последовательности, которые специфически связываются с указанными антигенами, известны в рассматриваемой области техники или могут быть подготовлены с применением способов, известных в рассматриваемой области техники; примеры включают иммуноглобулины, вариабельные области иммуноглобулинов (например, вариабельный фрагмент ("Fv") или бивалентный вариабельный фрагмент ("Fab")), одноцепочечные антитела и другие.
В различных вариантах осуществления любого из аспектов, определенных в настоящем документе, растворимый scFv является секретируемым. В различных вариантах осуществления любого из аспектов, определенных в настоящем документе, scFv экспрессируется с вектора. В различных вариантах осуществления любого из аспектов, определенных в настоящем документе, иммуносупрессивный полипептид представляет собой один или более из CD47, PD-1, CTLA-4 и их лигандов. В различных вариантах осуществления любого из аспектов, определенных в настоящем документе, иммуностимулирующий полипептид представляет собой один или более из CD28, OX-40, 4-1BB и их лигандов. В различных вариантах осуществления любого из аспектов, определенных в настоящем документе, растворимый scFv усиливает иммунный ответ иммунореактивной клетки.
В различных вариантах осуществления любого из аспектов, определенных в настоящем документе, иммунореактивная клетка секретирует цитокин. В различных вариантах осуществления любого из аспектов, определенных в настоящем документе, цитокин экспрессируется с вектора. В различных вариантах осуществления любого из аспектов, определенных в настоящем документе, фармацевтическая композиция, содержащая иммунореактивную клетку по изобретению, содержит цитокин. В различных вариантах осуществления любого из аспектов, определенных в настоящем документе, в иммунореактивную клетку по изобретению вводят цитокин. В различных вариантах осуществления любого из аспектов, определенных в настоящем документе, цитокин представляет собой один или более из IL-2, IL-3, IL-6, IL-11 , IL7, IL12, IL15, IL21, гранулоцитарно-макрофагального колониестимулирующего фактора, альфа-, бета- или гамма-интерферона и эритропоэтина.
В различных вариантах осуществления любого из аспектов, определенных в настоящем документе, способ уменьшает количество опухолевых клеток, уменьшает размер опухоли, уничтожает опухоль у индивидуума, уменьшает объем опухолевого поражения у индивидуума и/или искореняет опухолевую массу у индивидуума.
Иллюстративные новообразования, для которых изобретение может применяться, включают, без ограничения, лейкозы (например, острый лейкоз, острый лимфоцитарный лейкоз, острый миелоцитарный лейкоз, острый миелобластный лейкоз, острый промиелоцитарный лейкоз, миеломоноцитарный острый лейкоз, острый моноцитарный лейкоз, острый эритролейкоз, хронический лейкоз, хронический миелобластный лейкоз, хронический лимфоцитарный лейкоз), полицитемию, лимфому (болезнь Ходжкина, неходжкинская болезнь), макроглобулинемию Вальденстрема, болезнь тяжелых цепей и твердые опухоли, такие как саркомы и карциномы (например, фибросаркома, миксосаркома, липосаркома, хондросаркома, остеогенная саркома, хордома, ангиосаркома, эндотелиосаркома, лимфангиосаркома, лимфангиоэндотелиальная саркома, синовиома, мезотелиома, опухоль Юинга, лейомиосаркома, рабдомиосаркома, рак толстой кишки, рак поджелудочной железы, рак молочной железы, рак яичников, рак предстательной железы, плоскоклеточный рак, базально-клеточная карцинома, аденокарцинома, карцинома потовых желез, карцинома сальных желез, папиллярная карцинома, папиллярные аденокарциномы, цистаденокарцинома, медуллярная карцинома, бронхогенной карциномы, почечно-клеточной карциномы, гепатомы, карциномы протоков Нила, хориокарцинома, семинома, эмбриональная карцинома, опухоль Вильма, рак шейки матки, рак матки, рак яичек, рак легких, мелкоклеточный рак легких, рак мочевого пузыря, эпителиальный рак, глиома, астроцитома, медуллобластома, краниофарингиома, эпендимома, пинеалома, гемангиобластома, невринома слухового нерва, олигодендроглиома, шваннома, менингиома, меланома, нейробластома и ретинобластома).
В различных неограничивающих вариантах осуществления любого из аспектов, определенных в настоящем документе, неоплазия представляет собой один или более из рака крови, В-клеточного лейкоза, множественной миеломы, лимфобластного лейкоза (ALL), хронического лимфолейкоза, неходжкинской лимфомы и рак яичников. В некоторых вариантах осуществления рак крови представляет собой один или более из В-клеточного лейкоза, множественной миеломы, острого лимфобластного лейкоза (ALL), хронического лимфоцитарного лейкоза и неходжкинской лимфомы. В конкретных вариантах осуществления неоплазия представляет собой B-клеточный лейкоз, антиген представляет собой CD19 и полипептид, который обладает иммуносупрессивной активностью, представляет собой один или более из CD47, PD-1, CTLA-4 и их лигандов. В конкретных вариантах осуществления неоплазия представляет собой множественную миелому, антиген представляет собой CD19 и полипептид, который обладает иммуносупрессивной активностью, представляет собой один или более из CD47, PD-1, CTLA-4 и их лигандов. В конкретных вариантах неоплазия представляет собой острый лимфобластный лейкоз (ALL), антиген представляет собой CD19 и полипептид, который обладает иммуносупрессивной активностью, представляет собой один или более из CD47, PD-1, CTLA-4 и их лигандов. В конкретных вариантах неоплазия представляет собой хронический лимфоцитарный лейкоз, антиген представляет собой CD19 и полипептид, который обладает иммуносупрессивной активностью, представляет собой один или более из CD47, PD-1, CTLA-4 и его лигандов. В конкретных вариантах неоплазия представляет собой неходжкинскую лимфому, антиген представляет собой CD19 и полипептид, который обладает иммуносупрессивной активностью, представляет собой один или более из CD47, PD-1, CTLA-4 и их лигандов. В конкретных вариантах неоплазия представляет собой рак яичников, антиген представляет собой MUC16 и полипептид, который обладает иммуносупрессивной активностью, представляет собой один или более из CD47, PD-1, CTLA-4 и их лигандов.
Определения
Если не определено иначе, все технические и научные термины, используемые в настоящем документе, имеют значения, которые обычно понятны специалисту в данной области техники, к которой данное изобретение принадлежит. Следующие ссылки предоставляют любому специалисту общее определение многих терминов, используемых в данном изобретении: Singleton et al., Dictionary of Microbiology and Molecular Biology (2nd ed. 1994); The Cambridge Dictionary of Science and Technology (Walker ed., 1988); The Glossary of Genetics, 5th Ed., R. Rieger et al. (eds.), Springer Verlag (1 91); and Hale & Marham, The Harper Collins Dictionary of Biology (1991). Как используется в настоящем документе, следующие термины имеют значения, приписываемые им ниже, если не указано иное.
Под "активирует иммунореактивную клетку" подразумевается индукция передачи сигнала или изменения в экспрессии белков в клетке, приводящие к инициации иммунного ответа. Например, когда CD3 образует кластер в ответ на связывание лиганда и иммунорецепторных ингибиторных мотивов на основе тирозина (ITAM), вырабатывается каскад передачи сигнала. В определенных вариантах осуществления, когда эндогенный TCR или экзогенный CAR связывает антиген, происходит формирование иммунологического синапса, который включает кластеризацию многих молекул около связанного рецептора (например, CD4 или CD8, CD3γ/δ/ε/ζ и др.) Эта кластеризация мембран-связанных сигнальных молекул позволяет ITAM-мотивам, содержащимся в CD3-цепях, становиться фосфорилированными. Это фосфорилирование, в свою очередь, инициирует Т-клеточный путь активации, в конечном счете, активируя факторы транскрипции, такие как NF-κB и AP-1. Эти транскрипционные факторы индуцируют общую экспрессию генов Т-клетки для увеличения продукции IL-2 для пролиферации и экспрессии основных регуляторных белков Т-клетки для того, чтобы инициировать Т-клеточный иммунный ответ. Под "стимулирует иммунореактивную клетку" понимается сигнал, который приводит к прочному и устойчивому иммунному ответу. В разных вариантах осуществления это происходит после активации иммунной клетки (например, Т-клетки) или одновременно опосредуется через рецепторы, включая, в качестве неограничивающих примеров, CD28, CD137 (4-1BB), OX40, CD40 и ICOS. Без привязки к конкретной теории, получение нескольких стимулирующих сигналов важно для установления надежного и долгосрочного Т-клеточного иммунного ответа. Без получения этих стимулирующих сигналов Т-клетки быстро ингибируются и не реагируют на антиген. Несмотря на то, что воздействия этих ко-стимулирующих сигналов различаются и остаются частично понятыми, они, как правило, приводят к увеличению экспрессии генов в целях получения долгоживущих, пролиферативных и анти-апоптозных Т-клеток, которые энергично реагируют на антиген для полной и устойчивой эрадикации.
Термин "антиген-узнающий рецептор", используемый в настоящем документе обозначает рецептор, который может активировать иммунную клетку (например, Т-клетку) в ответ на связывание антигена. Типичные антиген-узнающие рецепторы могут быть природными или эндогенными Т-клеточными рецепторами или химерными антигенными рецепторами, в которых опухолевый антиген-связывающий домен слит с доменом внутриклеточной сигнализации, способным активировать иммунную клетку (например, Т-клетку).
Как используется здесь, термин "антитело" означает не только интактные молекулы антител, но также фрагменты молекул антител, которые сохраняют иммуноген-связывающую способность. Такие фрагменты также хорошо известны в рассматриваемой области техники и постоянно используются как in vitro, так и in vivo. Соответственно, как используется в настоящем документе, термин "антитело" означает не только интактные молекулы иммуноглобулина, но также хорошо известные активные фрагменты F(ab')2 и Fab. Фрагменты F(ab')2 и Fab, которые не имеют Fe фрагмента интактного антитела, быстрее выводятся из кровотока и могут обладать меньшим неспецифическим тканевым связыванием, чем интактное антитело (Wahl et al., J. Nucl. Med. 24:316-325 (1983). Антитела по изобретению включают цельные нативные антитела, биспецифические антитела; химерные антитела; Fab, Fab', одноцепочечные фрагменты V-области (scFv), слитые полипептиды и нетрадиционные антитела.
Как используется в настоящем документе, термин "одноцепочечный вариабельный фрагмент" или "scFv" представляет собой слитый белок вариабельных областей тяжелой (VH) и легкой (VL) цепей иммуноглобулина, ковалентно связанных с образованием гексодимера VH::VL. Тяжелая (VH) и легкая (VL) цепи либо непосредственно связаны, или присоединяются при помощи пептид-кодирующего линкера (например, 30, 15, 20, 25 аминокислот), который соединяет N-конец VH с С-концом VL, или С-конец VH с N-концом VL. Как правило, линкер обогащен глицином для гибкости, а также серином или треонином для растворимости. Несмотря на удаление константных областей и введения линкера, белки scFv сохраняют специфичность исходного иммуноглобулина. Одноцепочечные FV полипептидные антитела можно экспрессировать с нуклеиновой кислоты, включающей VH- и VL-кодирующие последовательности, как описано в Huston, et al. (Proc. Nat. Acad. Sci. USA, 85:5879-5883, 1988). См. также патенты США №№ 5,091,513, 5,132,405 и 4,956,778; и патентные публикации США №№ 20050196754 и 20050196754. Антагонистические scFv, обладающие ингибирующей активностью, были описаны (см., например, Zhao et al., Hyrbidoma (Larchmt) 2008 27(6):455-51; Peter et al., J Cachexia Sarcope ia Muscle 2012 August 12; Shieh et al., J Imunol2009 183(4):2277-85; Giomarelli et al., Thromb Haemost 2007 97(6):955-63; Fife eta., J Clin Invst 2006 1 16(8):2252-61; Brocks et al., Immunotechnology 1997 3(3):173-84; Moosmayer et al., Ther Immunol 1995 2(10:31-40). Агонистические scFv, имеющие стимулирующий характер активности, были описаны (см., например, Peter et al., J Bioi Chern 2003 25278(38):36740-7; Xie et al, Nat Biotech 1997 15(8):768-71; Ledbetter et al., Crit Rev Immunol 1997 17(5-6):427-55; Ho et al., BioChim Biophys Acta 2003 1638(3):257-66).
Под "аффинностью" подразумевается степень прочности связывания. Без привязки к теории, аффинность зависит от точности стереохимического соответствия между объединенными участками антитела и антигенными детерминантами, от размера области контакта между ними и от распределения заряженных и гидрофобных групп. Аффинность также включает в себя термин "авидность", который относится прочности связи антиген-антитело после формирования обратимых комплексов. Способы расчета аффинности антитела к антигену известны в данной области техники, включая использование экспериментов по связыванию для расчета аффинности. Активность антител функциональных тестах (например, анализ способом проточной цитометрии) также отражает аффинность антител. Антитела и аффинности могут быть фенотипически охарактеризованы и сопоставлены с использованием функциональных тестов (например, анализ способом проточной цитометрии).
Термин "химерный антигенный рецептор" или "CAR", как использовано в настоящем документе, относится к антиген-связывающему домену, который слит с внутриклеточным сигнальным доменом, способным активировать или стимулировать иммунную клетку. Чаще всего, внеклеточный связывающий домен CAR состоит из одноцепочечного вариабельного фрагмента (scFv), полученного от слияния вариабельных тяжелой и легкой областей мышиного или гуманизированного моноклонального антитела. Кроме того, могут быть использованы scFv, которые являются производными от Fab (а не из антитела, например, полученные из Fab-библиотек), в различных вариантах осуществления, этот scFv слит с трансмембранным доменом и затем с доменом внутриклеточной сигнализации. К CAR "первого поколения" относятся те, которые обеспечивают исключительно CD3ζ сигналы при связывании антигена, к CAR "второго поколения" относятся те, которые обеспечивают как костимуляцию (например, CD28 или CD137), так и активацию (CD3Q). CAR "третьего поколения" включают те, которые обеспечивают множественную костимуляцию (например, CD28 и CD137) и активацию (CO3Q). В различных вариантах осуществления, CAR выбирают, чтобы иметь высокую аффинность или авидность к антигену.
Под термином "иммуносупрессивная активность" подразумевается индукция сигнальной трансдукции или изменения экспрессии белков в клетке (например, активированная иммунореактивная клетка), приводящая к снижению иммунного ответа. Полипептиды, для которых известно, что они подавляют или снижают иммунный ответ посредством их связывания, включают CD47, PD-1, CTLA-4 и их соответствующие лиганды, в том числе SIRPa, PD-L1, PD-L2, B7-1 и B7-2. Такие полипептиды присутствуют в микроокружении опухоли и подавляют иммунный ответ на опухолевые клетки. В различных вариантах осуществления ингибирование, блокирование или противодействие взаимодействию иммуносупрессивных полипептидов и/или их лигандов повышает иммунный ответ иммунореактивной клетки.
Под термином "иммуностимулирующая активность" понимается индукция сигнальной трансдукции или изменения экспрессии белков в клетке (например, активированной иммунореактивной клетке), приводящая к усилению иммунного ответа. Иммуностимулирующая активность может включать про-воспалительную активность. Полипептиды, для которых известно, что они стимулируют или повышают иммунный ответ посредством их связывания, включают CD28, OX-40, 4-1BB и их соответствующие лиганды, в том числе B7-1, B7-2, OX-40L и 4-1BBL. Такие полипептиды присутствуют в микроокружении опухоли и активируют иммунный ответ на опухолевые клетки. В различных вариантах осуществления активирующие, стимулирующие или агонистические провоспалительные полипептиды и/или их лиганды усиливают иммунный ответ иммунореактивной клетки.
Под "полипептидом CD3ζ" подразумевается белок, имеющий, по меньшей мере, 85, 90, 95, 96, 97, 98, 99 или 100% идентичности с NCBI-ссылочным №: NP_932170 или его фрагментом, который обладает активирующей или стимулирующей активностью. Типичный CD3ζ; приводится ниже [SEQ ID NO: 1].
1 mkwkalftaa ilqaqlpite aqsfglldpk lcylldgilf iygviltalf lrvkfsrsad
61 apayqqgqnq lynelnlgrr eeydvldkrr grdpemggkp qrrknpqegl ynelqkdkma
121 eayseigmkg errrgkghdg lyqglstatk dtydalhmqa lppr
Под "молекулой нуклеиновой кислоты CD3ζ" подразумевается полинуклеотид, кодирующий полипептид CD3ζ.
Под "полипептидом CD28" подразумевается белок, имеющий, по меньшей мере, 85, 90, 95, 96, 97, 98, 99 или 100% идентичности с NCBI-ссылочным №: NP_006130 или его фрагментом, который обладает стимулирующей активностью. Типичный CD28 приводится ниже [SEQ ID NO: 2].
1 mlrlllalnl fpsiqvtgnk ilvkqspmlv aydnavnlsc kysynlfsre fraslhkgld
61 savevc nysqqlqvys ktgfiicdgkl gnesvtfylq nlyvnqtdiy fckievmypp
121 pyldneksng tiihvkgkhl cpsplfpgps kpfwvlvvvg gvlacysllv tvafiifwvr
181 skrsrllhsd ymnmtprrpg ptrkhyqpya pprdfaayrs
Под "молекулой нуклеиновой кислоты CD28" подразумевается полинуклеотид, кодирующий полипептид CD28.
Под "полипептидом CD40L" подразумевается белок, имеющий, по меньшей мере, 85, 90, 95, 96, 97, 98, 99 или 100% идентичности последовательности с NCBI ссылочным №: NP_000065, GenBank ссылочным № GenBank ссылочным №: AAH74950.1 или его фрагментом, который является лигандом CD40, или белок, кодируемый нуклеиновой кислотой, ПЦР-амплифицированной из PBMC, выделенных от здоровых доноров, с использованием следующих праймеров (1) 5'-CACGTGCATGATCGAAACATACAACCAAACTTCTCCCCGATCTGC-'3 [SEQ ID NO: 3] и (2) 5'-CTCGAGGGATCCTCAGAGTTTGAGTAAGCCAAAGGA-3' [SEQ ID NO: 4]( фигура 22А).
Под "молекулой нуклеиновой кислоты CD40L" подразумевается полинуклеотид, кодирующий полипептид CD40L.
По "полипептидом 4-1BB" подразумевается белок, имеющий, по меньшей мере, 85, 90, 95, 96, 97, 98, 99 или 100% идентичности с NCBI-ссылочным №: P41273 или NP_001552 или его фрагментом, который действует как фактор некроза опухоли (TNF). Типичный 4-1BB приводится ниже [SEQ ID NO: 5].
1 mgnscyniva tlllvlnfer trslqdpcsn cpagtfcdnn rnqicspcpp nsfssaggqr
61 tcdicrqckg vfrtrkecss tsnaecdctp gfhclgagcs mceqdckqgq eltkkgckdc
121 cfgtfndqkr gicrpwtncs ldgksvlvng tkerdvvcgp spadlspgas svtppapare
181 pghspqiisf flaltstall fllffltlrf svvkrgrkkl lyifkqpfmr pvqttqeedg
241 cscrfpeeee ggcel
Под "молекулой нуклеиновой кислоты 4-1BBL" подразумевается полинуклеотид, кодирующий полипептид 4-1BBL.
Под " полипептидом OX40L " подразумевается белок, имеющий по меньшей мере 85, 90, 95, 96, 97, 98, 99 или 100% идентичности с NCBI-ссылочным №: BAB18304 или NP_003317 или его фрагментом, который является лигандом фактора некроза опухоли (TNF) [SEQ ID NO: 6].
1 mervqpleen vgnaarprfe rnklllvasv iqglglllcf tyiclhfsal qvshrypriq
61 sikvqfteyk kekgfiltsq kedeimkvqn nsviincdgf ylislkgyfs qevnislhyq
121 kdeeplfqlk kvrsvnslmv asltykdkvy Invttdntsl ddfhvnggel ilihqnpgef
181 cvl
Под "молекулой нуклеиновой кислоты OX40L" подразумевается полинуклеотид, кодирующий полипептид OX40L.
Под "1928z" подразумевается белок, имеющий, по меньшей мере, 85, 90, 95, 96, 97, 98, 99 или 100% идентичности с последовательностью, указанной ниже, которая включает лидерную последовательность CDS с аминокислотами 1-18 и способный связывать CD19 [SEQ ID NO: 7].
MALPVTALLLPLALLLHAEVKLQQSGAELVRPGSSVKISCKASGYAFSSYWMNW
VKQRPGQGLEWIGQIYPGDGDTNYNGKFKGQATLTADKSSSTAYMQLSGLTSED
SAVYFCARKTISSVVDFYFDYWGQGTTVTVSSGGGGSGGGGSGGGGSDIELTQS
PKFMSTSVGDRVSVTCKASQNVGTNVAWYQQKPGQSPKPLIYSATYRNSGVPDR
FTGSGSGTDFTLTITNVQSKDLADYFCQQYNRYPYTSGGGTKLEIKRAAAIEVM
YPPPYLDNEKSNGTIIHVKGKHLCPSPLFPGPSKPFWVLVVVGGVLACYSLLVT
VAFIIFWVRSKRSRLLHSDYMNMTPRRPGPTRKHYQPYAPPRDFAAYRSRVKFS
RSAEPPAYQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPRRKNPQEGLY
NELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQALPPRX
Типичная последовательность нуклеиновой кислоты, кодирующая полипептид 1928z, включающий лидерную последовательность CDS, приводится ниже [SEQ ID NO: 8].
ccatggctctcccagtgactgccctactgcttcccctagcgcttctcctgcatg
cagaggtgaagctgcagcagtctggggctgagctggtgaggcctgggtcctcag
tgaagatttcctgcaaggcttctggctatgcattcagtagctactggatgaact
gggtgaagcagaggcctggacagggtcttgagtggattggacagatttatcctg
gagatggtgatactaactacaatggaaagttcaagggtcaagccacactgactg
cagacaaatcctccagcacagcctacatgcagctcagcggcctaacatctgagg
actctgcggtctatttctgtgcaagaaagaccattagttcggtagtagatttct
actttgacactggggccaagggaccacggtcaccgtctcctcaggtggaggtg
gatcaggtggaggtggatctggtggaggtggatctgacattgagctcacccagt
ctccaaaattcatgtccacatcagtaggagacagggtcagcgtcacctgcaagg
ccagtcagaatgtgggtactaatgtagcctggtatcaacagaaaccaggacaat
ctcctaaaccactgatttactcggcaacctaccggaacagtggagtccctgatc
gcttcacaggcagtggatctgggacagatttcactctcaccatcactaacgtgc
agtctaaagacttggcagactatttctgtcaacaatataacaggtatccgtaca
cgtccggaggggggaccaagctggagatcaaacgggcggccgcaattgaagtta
tgtatcctcctccttacctagacaatgagaagagcaatggaaccattatccatg
tgaaagggaaacacctttgtccaagtcccctatttcccggaccttctaagccct
tttgggtgctggtggtggttggtggagtcctggcttgctatagcttgctagtaa
cagtggcctttattattttctgggtgaggagtaagaggagcaggctcctgcaca
gtgactacatgaacatgactccccgccgccccgggcccacccgcaagcattacc
agccctatgccccaccacgcgacttcgcagcctatcgctccagagtgaagttca
gcaggagcgcagagccccccgcgtaccagcagggccagaaccagctctataacg
agctcaatctaggacgaagagaggagtacgatgttttggacaagagacgtggcc
gggaccctgagatggggggaaagccgagaaggaagaaccctcaggaaggcctgt
acaatgaactgcagaaagataagatggcggaggcctacagtgagattgggatga
aaggcgagcgccggaggggcaaggggcacgatggcctttaccagggtctcagta
cagccaccaaggacacctacgacgcccttcacatgcaggccctgccccctcgcg
Под "4H1128z" подразумевается белок, имеющий, по меньшей мере, 85, 90, 95, 96, 97, 98, 99 или 100% идентичности с последовательностью, приведенной ниже, которая включает лидерную последовательность CDS с аминокислотами 1-18 и способный связывать MUC [SEQ ID NO: 9].
MALPVTALLLPLALLLHAEVKLQESGGGFVKPGGSLKVSCAASGFTFSSYAMSW
VRLSPEMRLEWVATISSAGGYIFYSDSVQGRFTISRDNAKNTLHLQMGSLRSGD
TAMYYCARQGFGNYGDYYAMDY GQGTTVTVSSGGGGSGGGGSGGGGSDIELTQ
SPSSLAVSAGEKVTMSCKSSQSLLNSRTRKNQLAWYQQKPGQSPELLIYWASTR
QSGVPDRFTGSGSGTDFTLTISSVQAEDLAVYYCQQSYNLLTFGPGTKLEIKRA
AAIEVMYPPPYLDNEKSNGTIIHVKGKHLCPSPLFPGPSKPFWVLVVVGGVLAC
YSLLVTVAFIIFWVRSKRSRLLHSDYMNMTPRRPGPTRKHYQPYAPPRDFAAYR
SRVKFSRSAEPPAYQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPRRKN
PQEGLYNELQ ДК AEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQ
ALPPR
Типичная последовательность нуклеиновой кислоты, кодирующей полипептид 4H1128z, включающий лидерную последовательность каппа, приводится ниже [SEQ ID NO: 10].
ccatggctctcccagtgactgccctactgcttcccctagcgcttctcctgcatg
cagaggtgaagctgcaggagtcagggggaggcttcgtgaagcctggagggtccc
tcaaagtctcctgtgcagcctctggattcactttcagtagctatgccatgtcct
gggttcgcctgagtccggagatgaggctggagtgggtcgcaaccattagcagtg
ctggtggttacatcttctattctgacagtgtgcagggacgattcaccatttcca
gagacaatgccaagaacaccctgcacctgcaaatgggcagtctgaggtctgggg
acacggccatgtattactgtgcaaggcagggatttggtaactacggtgattact
atgctatggactactggggccaagggaccacggtcaccgtctcctcaggtggag
gtggatcaggtggaggtggatctggtggaggtggatctgacattgagctcaccc
agtctccatcctccctggctgtgtcagcaggagagaaggtcactatgagctgca
aatccagtcagagtctgctcaacagtagaacccgaaagaaccagttggcttggt
accagcaaaaaccaggacagtctcctgaactgctgatctactgggcatccacta
ggcaatctggagtccctgatcgcttcacaggcagtggatctgggacagatttca
ctctcaccatcagcagtgtgcaggctgaagacctggcagtttattactgccagc
aatcttataatctactcacgttcggtcctgggaccaagctggagatcaaacggg
cggccgcaattgaagttatgtatcctcctccttacctagacaatgagaagagca
atggaaccattatccatgtgaaagggaaacacctttgtccaagtcccctatttc
ccggaccttctaagcccttttgggtgctggtggtggttggtggagtcctggctt
gctatagcttgctagtaacagtggcctttattattttctgggtgaggagtaaga
ggagcaggctcctgcacagtgactacatgaacatgactccccgccgccccgggc
ccacccgcaagcattaccagccctatgccccaccacgcgacttcgcagcctatc
gctccagagtgaagttcagcaggagcgcagagccccccgcgtaccagcagggcc
agaaccagctctataacgagctcaatctaggacgaagagaggagtacgatgttt
tggacaagagacgtggccgggaccctgagatggggggaaagccgagaaggaaga
accctcaggaaggcctgtacaatgaactgcagaaagataagatggcggaggcct
acagtgagattgggatgaaaggcgagcgccggaggggcaaggggcacgatggcc
tttaccagggtctcagtacagccaccaaggacacctacgacgcccttcacatgc
aggccctgccccctcgc
Под "B6H12.2 scFv" подразумевается белок, имеющий, по меньшей мере, 85, 90, 95, 96, 97, 98, 99 или 100% идентичности с последовательностью, представленной ниже, и способный связывать CD47 [SEQ ID NO: 11].
EVQLVESGGDLVKPGGSLKLSCAASGFTFSGYGMSWVRQTPDKRLEWVAT
ITSGGTYTYYPDSVKGRFTISRDNAKNTLYLQIDSLKSEDTAIYFCARSL
AGNAMDYWGQGTSVTVSSGGGGSGGGGSGGGGSDIVMTQSPATLSVTPGD
RVSLSCRASQTISDYLHWYQQKSHESPRLLIKFASQSISGIPSRFSGSGS
GSDFTLSINSVEPEDVGVYYCQNGHGFPRTFGGGTKLEIKEQKLISEEDL
Под "5C4 scFv" подразумевается белок, имеющий, по меньшей мере, 85, 90, 95, 96, 97, 98, 99 или 100% идентичности с последовательностью, представленной ниже, и обладающий способностью связывать PD-1 человека [SEQ ID NO: 12].
QVQLVESGGGVVQPGRSLRLDCKASGITFSNSGMHWVRQAPGKGLEWVAV
IWYDGSKRYYADSVKGRFTISRDNSKNTLFLQMNSLRAEDTAVYYCATND
DYWGQGTLVTVSSGGGGSGGGGSGGGGSEIVLTQSPATLSLSPGERATLS
CRASQSVSSYLAWYQQKPGQAPRLLIYDASNRATGIPARFSGSGSGTDFT
LTISSLEPEDFAVYYCQQSSNWPRTFGQGTKVEIK
Под "J43 scFv" подразумевается белок, имеющий, по меньшей мере, 85, 90, 95, 96, 97, 98, 99 или 100% идентичности c последовательностью, указанной ниже, который включает лидерную последовательность каппа с аминокислотами 1-21 и способный связывать PD-1 человека [SEQ ID NO: 13].
METDTLLLWVLLLWVPGSTGDMGLGLQWVFFVALLKGVHCEVRLLESGGGLVKP
EGSLKLSCVASGFTFSDYFMSWVRQAPGKGLEWVAHIYTKSYNYATYYSGSVKG
RFTISRDDSRSMVYLQMNNLRTEDTATYYCTRDGSGYPSLDFWGQGTQVTVSSA
TTTAPSVYPLAPACDSTTKSGGGGSGGGGSGGGGSYELTQPPSASVNVGETVKI
TCSGDQLPKYFADWFHQRSDQTILQVIYDDNKRPSGIPERISGSSSGTTATLTI
RDVRAEDEGDYYCFSGYVDSDSKLYVFGSGTQLTVLGGPKSSPKVTVFPPSPEE
LRTNKATLVCLVNDFYPGSATVTWKANGATINDGVKTTKPSKQGQNYMTSSYLS
LTADQWKSHNRVSCQVTHEGETVEKSLSPAECLEQKLISEEDL*
Типичная последовательность нуклеиновых кислот, кодирующая полипептид scFv J43, включающий лидерную последовательность каппа, приводится ниже [SEQ ID NO: 14].
ccATGGAGACAGACACACTCCTGCTATGGGTACTGCTGCTCTGGGTTCCAGGTT
CCACTGGTGACatgggattgggactgcagtgggttttctttgttgctcttttaa
aaggtgtccactgtgaggtgcggcttctggagtctggtggaggattagtgaagc
ctgaggggtcactgaaactctcctgtgtggcctctggattcaccttcagtgact
atttcatgagctgggtccgccaggctccagggaaggggctggagtgggttgctc
acatatacacgaaaagttataattatgcaacttattactcgggttcggtgaaag
gcagattcaccatctccagagatgattcccgaagcatggtctacctgcaaatga
acaacctgagaactgaggacacggccacttat actgtacaagagatggaagcg
gatatccctctctggatttctggggtcaagggacccaagtcactgtctcctcag
ccacaacaacagccccatctgtctatcccttggcccctgcctgtgacagcacaa
ccaaatcgggtggaggtggatcaggtggaggtggatctggtggaggtggatctt
atgagctgactcagccaccttcagcatcagtcaatgtaggagagactgtcaaaa
tcacctgctctggggaccaattgccgaaatattttgcagattggtttcatcaaa
ggtcagaccagaccattttgcaagtgatatatgatgataataagcgcccctcgg
ggatccctgaaagaatctctgggtccagctcagggacaacagccaccttgacca
tcagagatgtccgggctgaggatgaaggtgactattactgtttctcaggatatg
ttgatagtgatagcaaattgtatgtttttggcagcggaacccagctcaccgtcc
taggtggacccaagtcttctcccaaagtcacagtgtttccaccttcacctgagg
agctccggacaaacaaagccacactggtgtgtctggttaatgacttctacccgg
gttctgcaacagtgacctggaaggcaaatggagcaactatcaatgatggggtga
agactacaaagccttccaaacagggccaaaactacatgaccagcagctacctaa
gtttgacagcagaccagtggaaatctcacaacagggtttcctgccaagttaccc
atgaaggggaaactgtggagaagagtttgtcccctgcagaatgtctcgaacaaa
aactcatctcagaagaggatctgTAActcgag
Молекулы нуклеиновых кислот, полезные в способах по изобретению, включают любую молекулу нуклеиновой кислоты, которая кодирует полипептид по изобретению или его фрагмент. Такие молекулы нуклеиновой кислоты не должны быть на 100% идентичны эндогенной последовательности нуклеиновой кислоты, но, как правило, обладают существенной идентичностью. Полинуклеотиды, имеющие "значительную идентичность" с эндогенной последовательностью, как правило, способны к гибридизации с, по меньшей мере, одной цепью двухцепочечной молекулы нуклеиновой кислоты. Под "гибридизоваться" подразумевается пара, чтобы образовать двухцепочечную молекулу между комплементарными полинуклеотидными последовательностями (например, ген, описанный в настоящем документе) или их частями, при различных условиях жесткости. (См., например, Wahl, G. M. and S. L. Berger (1987) Methods Enzymol. 152:399; Kimmel, A. R. (1987) Methods Enzymol. 152:507).
Например, жесткая концентрация соли обычно составляет менее чем примерно 750 мМ NaCl и 75 мМ цитрата натрия, предпочтительно, менее чем примерно 500 мМ NaCl и 50 мМ цитрата натрия, и более предпочтительно, менее чем примерно 250 мМ NaCl и 25 мМ цитрата натрия. Гибридизация с низкой жесткостью может быть получена в отсутствии органического растворителя, например, формамида, тогда как гибридизация с высокой жесткостью может быть получена в присутствии, по меньшей мере, примерно 35% формамида, и более предпочтительно, по меньшей мере, примерно 50% формамида. Жесткие температурные условия обычно включают температуру, по меньшей мере, примерно 30°С, более предпочтительно, по меньшей мере, примерно 37°C, и наиболее предпочтительно, по меньшей мере примерно 42°С. Различные дополнительные параметры, такие как время гибридизация, концентрация детергента, например, додецилсульфата натрия (SDS), и включение или исключение ДНК-носителя хорошо известны специалистам в данной области техники. Различные уровни жесткости достигаются путем сочетания этих различных условиях, как требуется. В предпочтительном варианте осуществления, гибридизация будет происходить при 30°С, 750 мМ NaCl, 75 мМ цитрат натрия и 1% SDS. В более предпочтительном варианте, гибридизация происходит при 37°C в 500 мМ NaCl, 50 мМ цитрате натрия, 1% SDS, 35% формамида и 100 мкг/мл денатурированной ДНК спермы лосося (слДНК). В наиболее предпочтительном варианте, гибридизация происходить при 42°C в 250 мМ NaCl, 25 мМ цитрат натрия, 1% SDS, 50% формамид, и 200 мкг/мл слДНК. Подходящие изменения этих условий должны быть очевидны для специалиста в данной области техники.
Для большинства приложений стадии отмывки, которые следуют за гибридизацией, также различаются по жесткости. Условия жесткости отмывки можно определить по концентрации соли и температуре. Как указано выше, жесткость отмывки может быть увеличена за счет уменьшения концентрации соли или путем повышения температуры. Например, жесткая концентрация соли для стадии отмывки составляет предпочтительно менее чем примерно 30 мМ NaCl и 3 мМ цитрата натрия, и наиболее предпочтительно, менее чем примерно 15 мМ NaCl и 1,5 мМ цитрата натрия. Жесткие температурные условия для стадии отмывки обычно включают температуру, по меньшей мере, примерно 25°С, более предпочтительно, по меньшей мере, примерно 42°C и даже более предпочтительно, по меньшей мере, примерно 68°C. В предпочтительном варианте осуществления, стадии отмывки проводят при температуре 25°С в 30 мМ NaCl, 3 мМ цитрате натрия и 0,1% SDS. В более предпочтительном варианте осуществления, стадии отмывки проводят при 42°С в 15 мМ NaCl, 1,5 мМ цитрате натрия и 0,1% SDS. В более предпочтительном варианте осуществления, стадии отмывки проводят при 68°C в 15 мМ NaCl, 1,5 мМ цитрате натрия и 0,1% SDS. Дополнительные вариации этих условий будут очевидны специалистам в данной области техники. Способы гибридизации хорошо известны специалистам в данной области и описаны, например, в Benton and Davis (Science 196: 180, 1977); Grunstein and Rogness (Proc. Natl. Acad. Sci., USA 72:3961, 1975); Ausubel et al. (Current Protocols in Molecular Biology, Wiley Interscience, New York, 2001); Berger and Kimmel (Guide to Molecular Cloning Techniques, 1987, Academic Press, New York); and Sambrook et al, Molecular Cloning; A Laboratory Manual, Cold Spring Harbor Laboratory Press, New York.
Под "в существенной степени идентичный" подразумевается полипептид или молекула нуклеиновой кислоты, демонстрирующая, по меньшей мере, 50% идентичности с аминокислотной последовательностью (например, любой из аминокислотных последовательностей, описанных в данном документе) или последовательностью нуклеиновой кислоты (например, любой из последовательностей нуклеиновых кислот, описанных здесь). Предпочтительно, такая последовательность является, по меньшей мере, на 60%, более предпочтительно, на 80% или 85%, и более предпочтительно, на 90%, 95% или даже 99% идентичной на уровне аминокислот или нуклеиновой кислоты последовательности, используемой для сравнения.
Идентичность последовательностей, как правило, измеряется с помощью программного обеспечения для анализа последовательностей (например, пакет программного обеспечения для анализа последовательностей компьютерной группы генетики, биотехнологический центр университета Висконсина, 1710 University Avenue, Мэдисон, Висконсин 53705, программы BLAST, BESTFIT, GAP или PILEUP/PRETTYBOX). Такое программное обеспечение сопоставляет идентичные или подобные последовательности путем присвоения степеней гомологии различным заменам, делециям и/или другим модификациям. Консервативные замены обычно включают замены внутри следующих групп: глицин, аланин; валин, изолейцин, лейцин; аспарагиновая кислота, глутаминовая кислота, аспарагин, глутамин; серин, треонин; лизин, аргинин; и фенилаланин, тирозин. В типичном подходе для определения степени идентичности может быть использована программа BLAST, с вероятностью попадания от е-3 и е-100, показывающей близкородственные последовательности.
Под "аналогом" подразумевается структурно связанный полипептид или молекулы нуклеиновой кислоты, имеющие функцию референсного полипептида или молекулы нуклеиновой кислоты.
Термин "лиганд", используемый в настоящем документе, относится к молекуле, которая связывается с рецептором. В частности, лиганд связывается с рецептором на другой клетке, что делает возможным узнавание одной клеткой другой и/или взаимодействие.
Термин "конститутивная экспрессия", используемый в настоящем документе, относится к экспрессии при любых физиологических условиях.
Под "болезнью" понимается любое состояние или расстройство, которое повреждает или нарушает нормальную функцию клетки, ткани или органа. Примеры заболеваний включают неоплазию или патогенную инфекцию клетки.
"Эффективное количество" означает количество, достаточное, чтобы иметь терапевтический эффект. В одном варианте осуществления, "эффективное количество" представляет собой количество, достаточное для задержки, смягчения или ингибирования продолжения пролиферации, роста или метастазирования (например, инвазии или миграции) неоплазии.
Под "эндогенной" понимается молекула нуклеиновой кислоты или полипептид, который обычно экспрессируется в клетке или ткани.
Под "принудительной толерантностью" понимается предотвращение активности автономных клеток или иммунореактивных клеток, которые нацелены на трансплантированные органы или ткани.
Под "экзогенной" понимается молекула нуклеиновой кислоты или полипептид, который эндогенно не присутствует в клетке, или не присутствует на уровне, достаточном для достижения функциональных эффектов, полученных при сверхэкспрессии. Термин "экзогенный", таким образом, охватывает любую рекомбинантную молекулу нуклеиновой кислоты или полипептид, экспрессируемый в клетке, такие как чужеродные, гетерологичные и сверхэкспрессируемые молекул нуклеиновых кислот и полипептидов.
Под "гетерологичной молекулой нуклеиновой кислоты или полипептидом" понимается молекула нуклеиновой кислоты (например, кДНК, ДНК или РНК) или полипептид, которые обычно не присутствуют в клетке или образце, полученном из клетки. Эта нуклеиновая кислота может быть из другого организма, или это может быть, например, молекула мРНК, которая обычно не экспрессируется в клетке или образце.
Под "иммунореактивной клеткой" подразумевается клетка, которая выполняет функции в иммунном ответе, или ее предшественник или потомство.
Под "увеличением" подразумевается изменение положительно, по меньшей мере, на 5%. Изменение может быть на 5%, 10%, 25%, 30%, 50%, 75% или даже на 100%.
Под "выделенной клеткой" подразумевается клетка, которая отделена от молекулярных и/или клеточных компонентов, которые естественным образом сопутствуют клетке.
Терминами "изолированная", "очищенный" или "биологически чистый" относятся к материалу, который является в разной степени свободным от компонентов, которые обычно сопутствуют ему, как обнаруживается в его нативном состоянии. "Изолят" обозначает степень сепарации от исходного источника или окружающей среды. "Чистота" обозначает степень отделения, которая выше, чем выделение. "Очищенный" или "биологически чистый" белок является достаточно свободным от других материалов, таких, что любые примеси не оказывают существенного влияния на биологические свойства белка или не вызывают другие неблагоприятные последствия. То есть, нуклеиновая кислота или пептид по настоящему изобретению является очищенной, если она по существу свободна от клеточного материала, вирусного материала или культуральной среды при продуцировании способами рекомбинантной ДНК, или химических предшественников или других химикатов в случае химического синтеза. Чистота и гомогенность, как правило, определяются при помощи способов аналитической химии, например, электрофореза в полиакриламидном геле и высокоэффективной жидкостной хроматографии. Термин "очищенный" может обозначать, что нуклеиновая кислота или белок приводит к образованию, в основном, одной полосы в электрофорезном геле. Для белка, который может быть подвергнут модификации, например, фосфорилированию или гликозилированию, различные модификации могут привести к образованию различных выделенных белков, которые могут быть отдельно очищены.
Термин "опухолевый антиген-связывающий домен", как использовано в настоящем документе, относится к домену, способному специфически связываться с конкретной антигенной детерминантой или набором антигенных детерминант, представленных на опухоли.
Термин "получаемый", как в "получаемое средство", предназначен для включения покупаемого, синтезируемого или иным образом приобретаемого средства (или указанного вещества или материала).
"Линкер", как использовано в настоящем документе, означает функциональную группу (например, химический реагент или полипептид), которая ковалентно соединяет два или более полипептидов или нуклеиновых кислот, так что они соединяются друг с другом. Как используется в настоящем документе, "пептидный линкер" относится к одной или более аминокислот, используемых для соединения двух белков вместе (например, для соединения доменов VH и VL). Типичная линкерная последовательность, используемая в изобретении, представляет собой GGGGSGGGGSGGGGS [SEQ ID NO:51].
Под "модулировать" подразумевают позитивно или негативно изменить. Типичные модуляции включают 1%, 2%, 5%, 10%, 25%, 50%, 75% или 100% замену.
Под "неоплазией" подразумевается заболевание, характеризующееся патологической пролиферацией клетки или ткани и его последующей миграцией или инвазией в другие ткани или органы. Рост неоплазии обычно является неконтролируемым и прогрессирующим, и возникает в условиях, которые не вызывали бы или не приводили бы к прекращению размножения нормальных клеток. Неоплазии могут оказывать влияние на различные типы клеток, тканей или органов, включая, в качестве неограничивающих примеров, орган, выбранный из группы, состоящей из мочевого пузыря, кости, головного мозга, молочной железы, хряща, глии, пищевода, маточной трубы, желчного пузыря, сердца, кишечника, почки, печени, легкого, лимфатического узла, нервной ткани, яичника, поджелудочной железы, предстательной железы, скелетной мышцы, кожи, спинного мозга, селезенки, желудка, семенника, тимуса, щитовидной железы, трахеи, мочеполового тракта, мочеточника, мочеиспускательного канала, матки и влагалища, или ткани или клеточного типа этого. Неоплазии включают злокачественные опухоли, например, саркомы, карциномы или плазмоцитомы (злокачественная опухоль плазматических клеток).
Под "патогенным микроорганизмом" подразумевается вирус, бактерии, грибок, паразит или простейшие, способный вызвать заболевание.
Типичные вирусы включают, в качестве неограничивающих примеров, Retroviridae (например, вирусы иммунодефицита человека, такие как ВИЧ-I (также называемый как HDTV-III, LAVE или HTLV-III/LAV, или ВИЧ-III; и другие изоляты, такие как HIV-LP; Picornaviridae (например, вирусы полиомиелита, вирус гепатита А; энтеровирусы, вирусы Коксаки человека, риновирусы, ЕСНО-вирусы); Calciviridae (например, штаммы, вызывающие гастроэнтерит); Togaviridae (например, вирусы энцефалита лошадей, вирусы краснухи); Flaviridae (например, вирусы лихорадки денге, вирусы энцефалита, вирусы желтой лихорадки); Coronoviridae (например, коронавирусы); Rhabdoviridae (например, вирусы везикулярного стоматита, вирусы бешенства); Filoviridae (например, вирусы эбола); Paramyxoviridae (например, вирусы парагриппа, вирус эпидемического паротита, вирус Кори, респираторно-синцитиальный вирус); Orthomyxoviridae (например, вирусы гриппа); Bungaviridae (например, вирусы Хантаан, бунге-вирусы, флебовирусы и вирусы Наира); Arena viridae (вирусы геморрагической лихорадки); Reoviridae (например, реовирусы, орбивирусы и ротавирусы); Birnaviridae; Hepadnaviridae (вирус гепатита В); Parvovirida (парвовирусы); Papovaviridae (вирусы папилломы, вирусы полиомы); Adenoviridae (большинство аденовирусов); Herpesviridae (вирус простого герпеса (HSV) 1 и 2, вирус ветряной оспы, цитомегаловирус (CMV), вирус герпеса; Poxviridae (вирусы натуральной оспы, вирусы коровьей оспы, вирусы куриной оспы); и Iridoviridae (например, вирус африканской чумы свиней) и неклассифицированные вирусы (например, агент дельта-гепатита (полагают, что является дефектным сателлитом вируса гепатита В), агенты гепатитов, отличных от гепатита А и гепатита B (класс 1 = внутренне передается; класс 2 =передается парентерально (то есть гепатит С); вирус Норволка и связанные вирусы, и астровирусы).
Типичные бактерии включают, в качестве неограничивающих примеров, виды Pasteurella, Staphylococci, Streptococcus, Escherichia coli, Pseudomonas species и Salmonella. Конкретные примеры инфекционные бактерии включают, в качестве неограничивающих примеров, Helicobacter pyloris, Borelia burgdorferi, Legionella pneumophilia, Mycobacteria sps (например, M tuberculosis, M. avium, M. intracellulare, M. kansaii, M. gordonae), Staphylococcus aureus, Neisseria gonorrhoeae, Neisseria meningitidis, Listeria monocytogenes, Streptococcus pyogenes (Streptococcus группы А), Streptococcus agalactiae (Streptococcus группы B), Streptococcus (группа вириданс), Streptococcus faecalis, Streptococcus bovis, Streptococcus (anaerobic sps.), Streptococcus pneumoniae, pathogenic Campylobacter sp., Enterococcus sp., Haemophilus influenzae, Bacillus antracis, corynebacterium diphtheriae, corynebacterhim sp., Erysipelothrix rhusiopathiae, Clostridium perfringers, Clostridium tetani, Enterobacter aerogenes, Klebsiella pneumoniae, Pasturella multocida, Bacteroides sp. , Fusobacterium nucleatum, Streptobacillus moniliformis, Treponema pallidium, Treponema pertenue, Leptospira, Rickettsia и Actinomyces israelii.
Под "рецептором" понимают полипептид или его часть, присутствующий на клеточной мембране, который селективно связывается с одним или более лигандов.
Под "снизить" понимают негативно изменить, по меньшей мере, на 5%. Изменение может быть на 5%, 10%, 25%, 30%, 50%, 75% или даже на 100%.
"Распознает" означает избирательно связывает мишень. Т-клетка, которая распознает вирус, обычно экспрессирует рецептор, который связывает антиген, экспрессируемый вирусом.
Под "референсом" или "контролем" подразумевается стандарт для сравнения. Например, уровень scFv-антиген связывания клеткой, экспрессии CAR и scFv, можно сравнивать с уровнем scFv-антигена связывания в соответствующей клетке, экспрессирующей только CAR.
Под "секретируемым" подразумевается полипептид, который высвобождается из клетки посредством секреторного пути через эндоплазматический ретикулум, аппарат Гольджи и в виде везикул, которые транзиторно сливаются с клеточной плазматической мембраной, высвобождая белки за пределами клетки.
Под "сигнальной последовательностью" или "лидерной последовательностью" подразумевается пептидная последовательность (длиной 5, 10, 15, 20, 25, 30 аминокислот), присутствующая на N-конце вновь синтезируемой полипептидной цепи вновь синтезированных белков, которая направляет их проникновение в секреторный путь. Типичные лидерные последовательности включают лидерную последовательность каппа: METDTLLLWVLLLWVPGSTGD [SEQ ID NO: 15] (человек), METDTLLLWVLLLWVPGSTGD [SEQ ID NO: 16] (мышь); и лидерная последовательность CDS: MALPVTALLLPLALLLHAARP [SEQ ID NO: 17].
Под "растворимым" подразумевается полипептид, который свободно диффундирует в водной среде (напр., не связанный с мембраной).
Под "специфически связывается" подразумевается полипептид или его фрагмент, который распознает и связывается с представляющей интерес биологической молекулой (например, полипептидом), но который в существенной степени не распознает и связывает другие молекулы в образце, например, биологическом образце, который естественным образом включает полипептид по изобретению.
Термин "опухолевый антиген", используемый в настоящем документе, относится к антигену (например, полипептиду), который единственным образом или дифференциально экспрессируется на опухолевых клетках, по сравнению с нормальной или отличной от IS-неопластической клеткой. Касательно изобретения, опухолевый антиген включает любой полипептид, экспрессируемый опухолью, который способен активировать или индуцировать иммунный ответ с помощью антиген-узнающего рецептора (например, CD19, MUCI) или способен подавлять иммунный ответ через связывание рецептор-лиганд (например, CD47, PD-L1/L2, B7.1/2).
Под "вирусным антигеном" подразумевается полипептид, экспрессируемый вирусом, который способен индуцировать иммунный ответ.
Термины "содержит", "содержащий" и предназначены для того, чтобы иметь широкое значение, приданное им в патентном праве США, и могут означать "включает", "включающий" и тому подобное.
Как используется в настоящем документе, "лечение" относится к клиническому вмешательству в попытке изменить течение болезни индивидуума или клетки, подвергаемого лечению, и может проводиться либо для профилактики или в ходе клинической патологии. Терапевтические эффекты лечения включают, без ограничения, предотвращение возникновения или рецидива заболевания, смягчение симптомов, уменьшение любых прямых или непрямых патологических последствий заболевания, предотвращение метастазирования, снижение скорости прогрессирования заболевания, улучшение или временное облегчение болезненного состояния, и ремиссию или улучшение прогноза. Путем предотвращения прогрессирования заболевания или расстройства, лечение может предотвратить ухудшение состояния, вызванное расстройством, у страдающего или диагностированного индивидуума или индивидуума с подозрением на заболевание, но также лечение может предотвратить развитие расстройства или симптома расстройства у индивидуума с риском расстройства или подозрением на это расстройство.
Термин "индивидуум", используемый в настоящем документе, относится к позвоночному, предпочтительно млекопитающему, более предпочтительно, человеку.
Термин "с ослабленным иммунитетом", используемый в настоящем документе, относится к индивидууму, который имеет иммунодефицит. Индивидуум является очень уязвимым для оппортунистических инфекций, инфекций, вызванных организмами, которые обычно не вызывают заболевания у человека со здоровой иммунной системой, но которые могут повлиять на людей с плохо функционирующей или подавленной иммунной системой.
Другие аспекты изобретения описаны в следующих раскрытиях и находятся в рамках изобретения.
КРАТКОЕ ОПИСАНИЕ ФИГУР
Последующее подробное описание, приведенное в качестве примера, но не предназначенное для ограничения изобретения описанными конкретными вариантами осуществления, может быть понято в сочетании с прилагаемыми чертежами.
Фигура 1 иллюстрирует Т-клетки, модифицированные для экспрессии химерного антигенного рецептора (CAR), самостоятельно или в комбинации с секретируемым scFv (например, aPD-1, PD-Ll, CTLA-4 или aCD47). Т-клетки, модифицированные для экспрессии химерного антигенного рецептора (CAR) самого по себе, представляют собой предмет супрессии в пределах неблагоприятного микроокружения опухоли. Без привязки к конкретной теории, дополнительная модификация этих клеток для экспрессии секретируемого scFv, чтобы блокировать иммуносупрессивную сигнализацию, улучшала противоопухолевую функцию благодаря их способности модулировать микроокружение опухоли и сопротивляться супрессирующим факторам.
Фигуры 2A и 2B иллюстрируют структуру конструкций секретируемого анти-CD47 scFv. Фигура 2А иллюстрирует структуру секретируемого анти-CD47 scFv, спроектированного для включения лидерной последовательности каппа (κ), чтобы обеспечить секрецию этого белка. Вариабельные тяжелая (VH) и легкая (VL) цепи были связаны серин-глициновым линкером (G4S), и пептид myc-tag был включен, чтобы дать возможность детектировать scFv. Фигура 2B иллюстрирует секретируемый scFv, связанный с конструкцией 1928z CAR при помощи P2A-элемента, как показано на фигуре.
Фигура 3 иллюстрирует последовательность B6H12.2 scFv, функционально связанной лидерной последовательностью Каппа [SEQ ID NO: 18]. Последовательности вариабельной тяжелой (VH) и вариабельной легкой (VL) гибридомы B6H12.2 были ПЦР-амплифицированы с лидерной последовательностью каппа, тегом с-myc и связаны с серин-глициновым линкером. В последовательности нуклеиновой кислоты и аминокислотная трансляция показаны.
Фигура 4 иллюстрирует последовательность B6H12.2 scFv, функционально связанной лидерной последовательностью CDS [SEQ ID NO:19]. Последовательности вариабельной тяжелой (VH) и вариабельной легкой (VL) гибридомы B6H12.2 были ПЦР-амплифицированы с лидерной последовательностью CDS, тегом с-myc и связаны с серин-глициновым линкером. В последовательности нуклеиновой кислоты и аминокислотная трансляция показаны.
Фигура 5 иллюстрирует последовательность нуклеиновых кислот конструкции 1928z-2А-B6H12.2 (лидер каппа) [SEQ ID NO:20]. Последовательность B6H12.2 scFv была клонирована в экспрессионный вектор SFG для экспрессии с CD19-нацеленным 1928z CAR. Элемент P2A был использован для соединения двух элементов, как показано.
Фигура 6 иллюстрирует последовательность нуклеиновых кислот конструкции 4HH28z-2А-B6H12.2 (лидер каппа) [SEQ ID NO:21]. Последовательность B6H12.2 scFv была клонирована в экспрессионный вектор SFG для экспрессии MUC-CD нацеленного химерного антигенного рецептора 4H1128z (CAR). P2A-элемент был использован для соединения двух элементов, как показано.
Фигуры 7А и 7В иллюстрируют создание упаковочных клеток 1928-2А-B6H12.2 293Glv9. Вирусные упаковочные клетки были получены с использованием вектора 1928z-2А-B6H12.2 или 1928z. Фигура 7 иллюстрирует отбор двух клонов, клонов 5 и 6, основанный на экспрессии 1928z CAR, которая была сопоставима с контрольными клетками 1928z 293Glv9. CAR экспрессии определяли способом проточной цитометрии с окрашиванием и антителом 12dll. Фигура 7В иллюстрирует эксперимент, в котором надосадочную жидкость из 1928z или 1928z-2А-B6H12.2 упаковочных клеток инкубировали с CD47+-опухолевыми клетками, Nalm-6 и Raji, и опухолевые клетки отмывали и окрашивали анти-CD47. Опухолевые клетки, инкубированные в супернатанте 1928z-2А-B6H12.2 (Синие линии), имели уменьшенное анти-CD47 связывание, по сравнению с инкубацией в супернатанте 1928z (Черная линия). Супернатант от гибридомной клетки B6H12.2 использовали в качестве контроля (Красная линия).
Фигуры 8A и 8B иллюстрирует создание Т-клеток 1928z-2А-B6H12.2 периферической крови человека. Т-клетки периферической крови человека трансдуцировали супернатантом упаковочных клеток 1928z или 1928z-2А-B6H12.2. Фигура 6А иллюстрирует анализ способом проточной цитометрии экспрессии CAR с использованием антитела 12d1l, и связанный анти-CD47 scFv окрашивали флуоресцентно меченым антителом к c-myc тегу. Фигура 6В иллюстрирует способность анти-CD47 scFv блокировать CD47, определенную путем окрашивания Т-клеток с помощью антитела анти-CD47. Т-клетки 1928z-2А-B6H12.2 имели уменьшенное связывание анти-CD47 (Синяя линия) по сравнению с Т-клетками 1928z (красная линия). Т-клетки 1928z, инкубированные в супернатанте гибридомы B6H12.2, использовали в качестве контроля (Черная линия).
Фигуры 9А-9С иллюстрируют Т-клетки 1928z-2А периферической крови человека. Проточную цитометрию проводили, чтобы охарактеризовать фенотип Т-клеток 1928z и 1928z-2А-B6H12.2. Фигура 9А иллюстрирует, что Т-клетки 1928z и 1928z-2А имели эквивалентное соотношение СД4:CD8 Т-клеток, и эквивалентную экспрессию активационных маркеров CD69 и CD25. Т-клетки 1928z имели повышенную экспрессию CD62L по сравнению с Т-клетками 1928Z-2А - B6H12.2. Фигура 9b иллюстрирует способность Т-клеток 1928z и 1928z-2А - B6H12.2 секретировать цитокины, как оценивалось способом проточной цитометрии после инкубации с 3Т3 (CD19+/В7.1+) aAPC клетками и ингибиторами транспорта Гольджи, Golgi plug и Golgi Stop. Т-клетки 1928z и 1928z-2А-B6H12.2 производили эквивалентные уровни Il-2 и IFNg после стимуляции клетками 3Т3(CD19+/В7.1+). Фигура 9С иллюстрирует, что Т-клетки 1928z и 1928z-2А-B6H12.2 имеют эквивалентный цитолитический потенциал, как определено при помощи стандартного теста высвобождения 51хрома, используя опухолевые клетки Raji.
Фигуры 10A и 10b иллюстрируют противоопухолевую эффективность Т-клеток 1928z-2А-B6H12.2. Противоопухолевую эффективность Т-клеток 1928z-2А-B6H12.2 in vivo исследовали в доклинической модели на SCID-Beige мышах. Мышей внутривенно инокулировали 1×106 Nalm-6-Firefly люциферазными* опухолевыми клетками и затем лечили с использованием 5,7×106 CAR+ 1928z, 1928z-2А-B6H12.2, или контрольными, нацеленными на рак яичников Т-клетками 4H1128z-2А-B6H12.2, также инокулированными внутривенно. Фигура 10А иллюстрирует, что у мышей, получавших Т-клетки 1928z-2А-B6H12.2, повышалась выживаемость по сравнению с неполучавшими, 1928z или получавшими 4H1128z-2А-B6H12.2 мышами. Фигура 10В иллюстрирует, что получавшие 1928z-2А-B6H12.2 мыши уменьшили опухолевую массу по сравнению с неполучавшими, 1928z или получавшими Т-клетки 4H1128z-2А-B6H12.2 мышами, с использованием биолюминесцентной визуализации для мониторинга опухолевой прогрессии.
Фигура 11 иллюстрирует последовательность 5C4 scFv, функционально связанной с лидерной последовательностью каппа [SEQ ID NO:22]. Последовательности вариабельной тяжелой (VH) и вариабельной легкой (VL) клона 5C4 антитела были спроектированы с лидерной последовательностью каппа, c-myc тэгом и соединены серин-глициновым линкером. Последовательность нуклеиновых кислот и аминокислотная трансляция показаны.
Фигура 12 иллюстрирует последовательность нуклеиновых кислот конструкции 1928z-2А-5C4 (лидер каппа) [SEQ ID NO:23j. Последовательность 5C4 scFv была клонирована в экспрессионный вектор SFG для экспрессии с CD19-нацеленного 1928z CAR. P2A элемент был использован для соединения двух элементов, как показано.
Фигура 13 иллюстрирует последовательность нуклеиновых кислот конструкции 4H1128z-2А-5C4 (лидер каппа) [SEQ ID NO:24]. 5C4 scFv была клонирована в вектор экспрессии SFG, чтобы экспрессироваться с MUC-CD-нацеленным 4H1128z CAR. P2A элемент был использован для объединения двух элементов, как показано.
Фигура 14 иллюстрирует создание 1928z-2А-5C4 (лидер каппа) 293Giv9 клеток. Вирусные упаковочные клетки были получены с использованием 1928z-2А-5C4. Два клона, клоны А6 и В6, были отобраны на основе экспрессии 1928z CAR, который сопоставим с контрольными l928z 293Glv9 клетками. Экспрессию CAR определяли способом проточной цитометрии и окрашивания антителом 12d11.
Фигура 15 иллюстрирует создание 1928z-2А-5C4 (лидер каппа) Т-клетки периферической крови человека. Т-клетки периферической крови человека были трансдуцированы супернатантом от 1928z или 1928z-2А-5C4 упаковочных клеток. Проточная цитометрия использовалась для анализа экспрессии CAR с помощью антитела 12d11 и связанного анти-CD47 scFv с помощью окрашивания флуоресцентно меченым антителом к c-myc тегу.
Фигура 16 иллюстрирует экспрессию PD-L1 на клетках 3Т3(CD19+/В7.1+), Raji и Nalm-6. Проточная цитометрия использовалась для определения экспрессии PD-L1 на клетках 3Т3(CD19+/В7.1+), Raji и Nalm-6, которые были трансдуцированы, чтобы экспрессировать PD-L1. Трансдуцированные клетки, экспрессирующие значительные уровни PD-L1 по сравнению с контрольными нетрансдуцированными клетками и циркулирующие популяции были отсортированы для использования в экспериментах.
Фигура 17 иллюстрирует распространение 1928z и 1928z-2А-5C4 Т-клеток. Т-клетки 1928z и 1928z-2А-5C4 инкубировали с 3Т3(CD19+/В7.1+) или 3Т3(CD19+В7.1+/PD-L1+), Т-клеточное распространение контролировали при помощи трипанового синего, и экспрессию CAR определяли способом проточной цитометрии. Рост и экспрессия CAR коррелировали с таковыми клеток, распространяющихся на клетках 3Т3(CD19+/В7.1+).
Фигура 18 иллюстрирует последовательность J43 scFv, функционально связанной с лидерной последовательностью каппа мыши [SEQ ID NO:25]. Последовательности вариабельной тяжелой (VH) и вариабельной легкой (VL) антитела клона J43 были спроектированы с помощью лидерной последовательности каппа мыши, c-myc тэга и соединены серин-глициновым линкером. Последовательность и аминокислотная трансляция показаны.
Фигура 19 иллюстрирует последовательность нуклеиновых кислот конструкции 19m28mziRESJ43 (лидер каппа мыши) [SEQ ID NO:26]. J43 scFv был клонирован в экспрессионный вектор SFG для экспрессии с CD19-нацеленного 19m28mz CAR. Элемент внутреннего рибосомного входного участка (IRES) используется для соединения двух элементов, как показано.
Фигура 20 иллюстрирует последовательность нуклеиновых кислот конструкции 4H11m28mziRESJ43 (лидер каппа мыши) [SEQ ID NO:27]. J43 scFv был клонирован в вектор экспрессии SFG для экспрессии MUC-CD-нацеленного 4H11m28mz CAR. Элемент внутреннего рибосомного входного участка (IRES) используется для соединения двух элементов, как показано.
Фигура 21 иллюстрирует стратегии, чтобы генетически модифицировать клетки CART для экспрессии молекул scFv ("бронированные CAR Т-клетки"), чтобы преодолеть "враждебное" микроокружение опухоли. CAR* Т-клетки могут быть модифицированы для секреции антагонистических scFv с иммунными регуляторными функциями. При активации CAR родственным антигеном (1), бронированные CAR-модифицированные Т-клетки могут быть индуцированы, чтобы секретировать scFv, антагонистичные по отношению к ингибиторному PD-1 Т-клеточному рецептору как на инфузных CAR модифицированных Т-клетках, так и на эндогенные противоопухолевых Т-клетках, усиливая противоопухолевую эффекторную функцию (2), индуцированную для секреции scFv, антагонистичных по отношению к ингибиторному CTLA-4 Т-клеточному рецептору как на инфузных CAR модифицированных Т-клетках, так и на эндогенные противоопухолевых Т-клетках, усиливая противоопухолевую эффекторную функцию (3), или индуцированную, чтобы секретировать scFv, антагонистичные по отношению к рецептору CD47, экспрессируемому на опухолевой клетке, отменяя маскирование опухолевой клетки от распознавания со стороны врожденного противоопухолевого иммунного ответа хозяина, приводя к распознаванию и искоренению опухоли при помощи макрофагов хозяина.
Фигуры 22А - 22D иллюстрируют конститутивную экспрессию CD40L Т-клетками человека. (А) Схема ретровирусной конструкции, кодирующей вектора с CD40L человека; LTR, длинный терминальный повтор; SD, SA, сплайс-донор и акцептор; Ψ, упаковочный элемент. (B) Проточная цитометрия CD4+ и CD8+ CD40L-модифицированных Т-клеток после ретровирусного переноса генов; х-ось APC-конъюгированные анти-CD40L человека (CD154). (C) Усиленная пролиферация CD40L-модифицированных Т-клеток по сравнению с имитационно трансдуцированными Т-клетками. (D) Усиленная секреция растворимого CD40L (sCD40L), IFN-γ, GM-CSF из CD40L-модифицированных Т-клеток по сравнению c имитационно трансдуцированными Т-клетками. Все результаты представляют, по меньшей мере, три отдельных эксперимента. (* обозначает статистическую значимость)
Фигуры 23А и 23В иллюстрируют увеличенную иммуногенность CD40+ опухолевых клеток CD40L-модифицированными Т-клетками. А) Проточная цитометрия, показывающая повышенную активность костимуляторных молекул (CD80 и CD86), молекул адгезии (CD54, CD58 и CD70), молекул HLA-класса (HLA класса I и HLA-DR) и Fas-рецептора смерти (CD95) на опухолевой линии клеток DOHH2 после совместного культивирования с CD40L-модифицированными Т-клетками (сплошная линия) по сравнению c имитационно трансдуцированными Т-клетками от того же донора (серая линия). (В) CD40 - опухоль (показана NALM6), демонстрирующая отсутствие каких-либо фенотипических изменений после совместного культивирования с CD40L-модифицированными Т-клетками. Все результаты представляют, по меньшей мере, три отдельных эксперимента.
Фигуры 24А и 24В иллюстрируют увеличенную иммуногенность клеток CLL при помощи аутологичных CD40L-модифицированных Т-клеток. (В) Проточная цитометрия полученных от пациента CD40L - модифицированных Т-клеток после ретровирусного генного переноса при помощи CD40L-содержащего ретровирусного вектора; х - ось APC-конъюгированное анти-CD40L человека (CD154). (В) Проточная цитометрия, показывающая повышенную активность костимуляторных молекул (CD80 и CD86), молекул адгезии (CD54, CD58 и CD70), молекул HLA-класса (HLA класса I и HLA-DR) и Fas-рецептора смерти (CD95) на CLL-клетках после совместного культивирования с аутологичными CD40L-модифицированными Т-клетками (сплошная линия) по сравнению c имитационно трансдуцированными Т-клетками от того же донора (серая линия). Все результаты представляют, по меньшей мере, три отдельных эксперимента.
Фигуры 25А и 25В иллюстрируют секрецию IL-12 и созревание моноцит-производных дендритных клеток (moDC) при помощи CD40L-модифицированных Т-клеток. (А) Анализ цитокинов культуральной среды для совместного культивирования (24 часа) moDCs и CD40L-модифицированных Т-клеток от трех отдельных доноров, демонстрирующий повышенную секрецию IL-I2p70. (B) Проточная цитометрия moDC, демонстрирующая созревание после совместного культивирования с CD40L - модифицированными Т-клетками. Все результаты представляют, по меньшей мере, три отдельных эксперимента.
Фигуры 26А-С иллюстрируют эффективную трансдукцию Т-клеток человека при помощи вектора CAR/CD40L, демонстрирующую повышенную цитотоксичность. (А) Схема ретровирусной конструкции, содержащей генов 1928z-IRES-CD40L и PZ1-IRES-CD40L; LTR, длинный терминальный повтор; CD, CA, сплайс-донор и акцептор; Ψ, упаковочный элемент; CD8 показывает CD8 лидерную последовательность; scFv, одноцепочечный вариабельный фрагмент; VH и VL, вариабельные тяжелая и легкая цепи; ТМ, трансмембранный домен. (В) FACS-анализ Т-клеток человека, трансдуцированных для экспрессии вектора 19-28z/CD40L (пре-стимуляция) с последующей усиленной экспрессией CAR/CD40L после совместного культивирования на AAPC (NIH 3Т3 фибробласты, экспрессирующие CD19 и CD80; показаны 1928z/CD40LT-клетки), использованных для экспериментов in vivo. х - ось, PE-конъюгированные 1928z CAR-специфическое антитело (19e3); Y-ось, APC-конъюгированные анти-CD40L человека (CD154). (С) Как определяется в стандартном анализе высвобождения 51Cr, 19-28z/40л Т-клетки имеют значительно увеличенную способность лизировать опухолевые клетки DOHH2 по сравнению с 1928z Т-клетками. Все результаты представляют, по меньшей мере, три отдельных эксперимента. (* обозначает статистическую значимость).
Фигура 27 иллюстрирует ликвидацию опухоли и долгосрочную выживаемость после инфузии 1928z CD40L Т-клеток. Кривая выживаемости SCID-Beige мышей, инокулированных опухолевыми клетками DOHH2 при помощи внутривенных (i.v.) инъекций за 2 дня до однократной i.v. дозы CAR-модифицированных Т-клеток. Усиление долговременной выживаемости было продемонстрировано у мышей, получавших 1928z/CD40L Т-клетки (n=10), по сравнению с панелью контрольных Т-клеток (группа 1928z, n=8; и группа Pz1/40L n=5). Результаты представляют, по меньшей мере, два отдельных эксперимента. (* обозначает статистическую значимость).
Фигура 28 иллюстрирует увеличенную иммуногенность CD40+ опухолевых клеток при помощи sCD40L. А) Проточная цитометрия, показывающая повышенную активность костимуляторной молекулы (CD80), молекул адгезии (CD54, CD58 и CD70), молекулы HLA (HLA класса I и HLA-DR) и Fas-рецептора смерти на опухолевой линии клеток DOHH2 после совместного культивирования с кондиционированными средами (среды CD40L-модифицированных Т-клеток), содержащими повышенные уровни sCD40L (сплошная линия) по сравнению с средами (среды имитационно трансдуцированных Т-клеток) без повышенных уровни sCD40L (серая линия).
Фигура 29 иллюстрирует Т-клетки 1928z/CD40L, демонстрирующие повышенную цитотоксичность. Как определяется в стандартном анализе по высвобождению 51Cr, Т-клетки 19-28z/40л имеют значительно увеличенной способностью лизировать опухолевые клетки Raji по сравнению с Т-клетками 19-28z.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение в целом предоставляет клетки, в том числе генетически модифицированные иммунореактивные клетки (например, Т-клетки, натуральные киллерные (NK) клетки, цитотоксические Т-лимфоциты (CTL) клетки), экспрессирующие, по меньшей мере, комбинацию антиген-распознающего рецептора (например, TCR или CAR) и либо (i) scFv, который связывает иммуносупрессивный антиген (например, aPD-1, aPD-Ll, aCTLA-4 или aCD47)) (ii) scFv, который связывает иммуностимулирующий антиген (например ocCD28, aOX-40, aCD40 или α4-1BB) либо (iii) CD40L, и способы применения таких клеток для лечения неоплазии и других патологий, где увеличение антиген-специфического иммунного ответа является желаемым. Изобретение основано, по меньшей мере, частично, на обнаружении того, что scFv, которые связывают иммуносупрессивный антиген (например, CD47 и PD-L1, как показано в настоящем документе), полезны для активизации и стимуляции иммунореактивной клетки. В частности, scFv по изобретению уменьшают или предотвращают подавление иммунного ответа активированной иммунореактивной клетки в микроокружении опухоли. Злокачественные клетки выработали ряд механизмов для защиты себя от иммунного распознавания и элиминации. Настоящий подход обеспечивает иммуногенность в микроокружении опухоли для эрадикации опухоли, и представляет собой значительный шаг вперед по сравнению с обычной адоптивной Т-клеточной терапией.
Микроокружение опухоли
Опухоли имеют микроокружение, которое враждебно иммунному ответу, включающее ряд механизмов злокачественных клеток для зашиты себя от иммунного распознавания и элиминации. Это "враждебное микроокружение опухоли" включает различные иммуносупрессивные факторы, в том числе проникающие регуляторные CD4+ Т-клетки (Treg), миелоид-производные супрессорные клетки (MDSC), опухолеассоциированные макрофаги (ТАМ), иммуносупрессивные цитокины, в том числе IL-10 и TGF-β, и экспрессию лигандов, ориентированных на иммунные супрессорные рецепторы, экспрессируемые активированными Т-клетками (CTLA-4 и PD-1). Эти механизмы иммунной супрессии играют роль в поддержании толерантности и супрессирования несоответствующих иммунных реакций, однако в микроокружении опухоли эти механизмы предотвращают эффективный противоопухолевый иммунный ответ. В совокупности эти иммуносупрессивные факторы могут индуцировать либо маркированную анергию, либо апоптоз адоптивно переданных CAR модифицированных Т-клеток, после встречи с опухолевыми клетками-мишенями.
Антиген 4 цитотоксических Т-лимфоцитов (CTLA-4)
CTLA-4 является ингибирующим рецептором, экспрессируемым активированными Т-клетками, который при контактировании со своими соответствующими лигандами (CD80 и CD86; В7-1 и В7-2, соответственно) опосредует ингибирование активированных Т-клеток или анергию. Как в предклинических, так и клинических исследованиях, CTLA-4 блокада путем системной инфузии антител, усиливала эндогенный противоопухолевый ответ, хотя и в клинических условиях, со значительными непредвиденными токсичностями. Без привязки к конкретной теории, направленная CTLA-4 блокада посредством доставки антагонистических scFv при помощи опухоль-нацеленных CAR-модифицированных Т-клеток позволяет уменьшить токсичность, а также предоставляет суррогатную "эндогенную" популяцию опухоле-направленных Т-клеток (клеточная популяция CART), защищенных от иммунной супрессии. Доклинические исследования (например, модели человеческих опухолевых ксенотрансплантатов и мышиные опухолевые модели В-клеточных злокачественных опухолей и карцином яичников) могут быть использованы для оценки эффекта секреции scFv как на популяцию CAR модифицированных Т-клеток, а также на эндогенные противоопухолевые иммунные реакции. Анти-CTLA-4 scFv могут быть получены от гибридомы 9D9, которая секретирует мышиные моноклональные антитела против CTLA-4 мыши, или от гибридомы 9H10, которая секретирует моноклональные антитела хомяка против CTLA-4 мыши.
Белок 1 запрограммированной клеточной смерти (PD-1)
PD-1 является негативным иммунным регулятором активированных Т-клеток после взаимодействия с соответствующими лигандами PD-L1 и PD-L2, экспрессированными на эндогенных макрофагах и дендритных клетках. Активация PD-L1 является одним из механизмов, при помощи которого опухолевая клетка может уклониться от иммунной системы хозяина. Опять же, как в доклинических, так и в недавно опубликованных клинических испытаниях, PD-1 блокада антагонистическими антителами индуцировала противоопухолевые реакции, опосредованные через эндогенную иммунную систему хозяина. Модели ксенотрансплантатных и сингенных мышиных опухолей могут использоваться, чтобы показать, что антагонистические анти-PD-1 scFv, секретируемые опухоле-направленными CAR-модифицированными Т-клетками, усиливают противоопухолевую эффективность этих scFv-секретирующих CAR модифицированных Т-клеткок.
CD47
CD47 является мембранный белок с широким распределением в тканях и который, как было показано в недавних доклинических моделях, защищает широкий спектр опухолевых клеток от узнавания макрофагами. В этих моделях, инфузия анти-CD47 моноклональных антител приводила к уменьшению устойчивого прогрессирования опухолей. Иными словами, CD47-блокада на опухолевые клетки подвергает эти опухолевые клетки распознаванию и фагоцитозом макрофагами хозяина. Учитывая достаточно повсеместную экспрессию данного антигена, системная инфузия блокирующего антитела может потенциально приводить токсичности, не связанной с мишенью. Опять же, в соответствии с парадигмой адресной доставки, секреция аналогично блокирующего анти-CD47 scFv, доставляемого непосредственно в микроокружение опухоли при помощи CAR-модифицированных Т-клеток, вызывает/усиливает желаемый противоопухолевый эффект, в этом случае при посредничестве врожденной, а не адаптивной иммунной системы хозяина. Кроме того, этот подход не ограничивается лечением неоплазии, но поддается широкому диапазону применений, где усиление антиген-специфического иммунного ответа является желаемым, такие приложения включают в себя не только лечение неоплазий, но также применимы для повышения иммунного ответа против патогенной инфекции или инфекционного заболевания и для укрепления иммунной толерантности у регуляторных Т-клеток в контексте аутоиммунных заболеваний или аллогенной трансплантации.
CD40L
Лиганд CD40 (CD40L, CD-154), трансмембранный белок типа II, принадлежащий к суперсемейству генов фактора некроза опухоли (TNF), имеет потенциал для усиления опухолеспецифической Т-клеточной функции. Изначально идентифицированный на активированных CD4+ Т-клетках, экспрессия CD40L является индуцируемой в широком спектре иммунных, кроветворных, эпителиальных, эндотелиальных и гладкомышечных клеток. В активированных Т-клетках, CD40L экспрессируется в течение нескольких минут, достигая максимума в течение 6 часов, а затем снижается в течение последующих 12-24 часов. CD40L связывается со своим узнающим рецептором CD40, который конститутивно экспрессируется на различных иммунных и неиммунных клетках, включая В-клетки, макрофаги и дендритные клетки (DC). Существенно, CD40 также экспрессируется на нескольких гематологических и не-гематологических злокачественных опухолях, включая хроническую лимфоцитарную лейкемию (CLL), острый лимфобластный лейкоз (ALL), неходжкинскую лимфому (NHL), лимфому Ходжкина, носоглоточную карциному, остеосаркому, саркому Юинга, меланому, рак молочной железы, яичников и шейки матки, что демонстрирует возможности применения CAR/CD40L Т-клеток для широкого спектра злокачественных новообразований. См. ссылки 8-17, перечисленные ниже в библиографическом списке в примере 6.
Гемопоэтические клеточные линии
Гемопоэтические (кровяные) клетки млекопитающих обеспечивают широкий спектр физиологической активности. Гемопоэтические клетки делятся на лимфоидную, миелоидную и эритроидную линий. Лимфоидная линия, включающая В-, Т-клетки и натуральные киллерные (NK) клетки, обеспечивают выработку антител, регуляцию клеточного иммунитета, выявление чужеродных агентов в крови, обнаружение клеток, чужеродных хозяину, и тому подобное. Термин "Т-клетки", используемый в настоящем документе, относится к лимфоцитам, которые созревают в вилочковой железе и в основном являются ответственными за клеточный иммунитет. Т-клетки участвуют в адаптивной иммунной системе. Термин "естественные киллерные (НК) клетки", используемый в настоящем документе, относится к лимфоцитам, которые являются частью клеточно-опосредованный иммунитета и действуют в течение врожденного иммунного ответа. Они не требуют предварительной активации для осуществления своего цитотоксического действия на клетки-мишени. Цитотоксические Т-клетки (CTL или киллерные Т-клетки) являются подмножеством T-лимфоцитов, способных индуцировать гибель инфицированных соматических или опухолевых клеток.
Клетки, используемые в способах по изобретению
Настоящее изобретение предоставляет клетки, экспрессирующие антиген-распознающий рецептор, который активирует иммунореактивную клетку (например, TCR, CAR), и scFv, который связывает иммуносупрессивный антиген (например, αPD-1, αPD-L1, αCTLA-4 или CD47), и способы применения таких клеток для лечения болезни, которая требует усиленного иммунного ответа. В одном подходе, опухолевые антиген-специфичные Т-клетки, NK-клетки, ЦТЛ-клетки или другие иммунореактивные клетки используют для экспрессии scFv, который связывает иммуносупрессивный антиген, для лечения или предупреждения неоплазии. Например, Т-клетки, экспрессирующие химерный антигенный рецептор 1928z, который узнает CD19, совместно экспрессируют в Т-клетке, которая экспрессирует scFv, который связывает CD47. Такие клетки вводят индивидууму-человеку, нуждающемуся в этом, для лечения или предупреждения онкологических заболеваний крови (например, лейкозов, лимфом и миелом). В другом подходе, вирусные антиген-специфичные Т-клетки, NK-клетки, ЦТЛ-клетки могут применяться для лечения вирусных заболеваний. Например, химерный костимуляторный антигенный рецептор, который распознает первый антиген ЦМВ, и scFv, который связывает PD-1, совместно экспрессируют в цитотоксических Т-лимфоцитах для лечения ЦМВ.
Собственные Т-клетки пациента могут быть генетически модифицированы для опухолевого нацеливания путем введения генов, кодирующих рассматриваемой области техникинные Т-клеточные рецепторы, называемые химерные антигенные рецепторы (CAR). CAR первого поколения обычно состоят из полученного из антитела антиген-узнающего домена, одноцепочечный фрагмент антитела (scFv), слитого с вариабельным транс-мембранным доменом, слитым с цитоплазматическим сигнальным доменом цепи Т-клеточного рецептора. Дополнительное включение одного или двух костимуляторных рецепторных сигнальных доменов, в том числе CD28, 4-1BB и OX-40 проксимальнее С цепи усиливает CAR-сигналлинг, приводя, соответственно, ко второму и третьему поколению CAR.
Опухолевые антиген-специфические Т-лимфоциты (и NK-клетки)
Виды опухолевый антиген-специфических лимфоцитов человека, которые могут быть использованы в способы по изобретению, включают, без ограничения, периферические лимфоциты доноров, генетически модифицированные для экспрессии химерных антигенных рецепторов (CAR) (Sadelain, M., et ah 2003 Nat Rev Cancer 3:35-45), периферические лимфоциты доноров, генетически модифицированные для экспрессии комплекса полноразмерного опухолевый антиген-распознающего Т-клеточного рецептора, состоящего из α- и β-гексодимера (Morgan, R.A., et al, 2006 Science 314: 126-129), культуры лимфоцитов, полученные из опухоле-проникающих лимфоцитов (TIL) в опухолевых биопсиях (Panelli, M.C., et al 2000 J Immunol 164:495-504; Panelli, M.C., et al. 2000 J Immunol 164:4382-4392), и селективно in vitro распространенных антиген-специфических лейкоцитов периферической крови, используя искусственные антиген-представляющие клетки (AAPC) или импульсные дендритные клетки (Dupont, J., et al. 2005 Cancer Res 65:5417-5427; Papanicolaou, G.A., et al. 2003 Blood 102:2498-2505).Т-клетки могут быть аутологичными, аллогенными или полученные in vitro от сконструированных предшественников или стволовых клеток. Любой подходящий опухолевый антиген (антигенный пептид) пригоден для использования в связанных с опухолями вариантах осуществления, описанных в данном документе. Источники антигена включают, в качестве неограничивающих примеров, раковые белки. Антиген можно экспрессировать в виде пептида или в виде интактного белка или его части. Интактный белок или его часть может быть природным или мутагенизированным.
Подходящие антигены включают простата-специфический мембранный антиген (PCMA) и антиген стволовых клеток простаты (PCSA).
Вирусные антиген-специфические Т-лимфоциты (и NK-клетки)
Антигены, подходящие для использования при лечении патогенной инфекции или других инфекционных заболеваний, например, у индивидуума с ослабленным иммунитетом включают, без ограничения, вирусные антигены, присутствующие в цитомегаловирусе (ЦМВ), вирусе Эпштейна-Барра (EBV), вирусе иммунодефицита человека (ВИЧ) и вирусе гриппа.
Неочищенный источник CTL может представлять собой любой источник, известный в данной области техники, такой как костный мозг, плод, новорожденный или взрослый или другой источник гематопоэтических клеток, например, фетальная печень, периферическая кровь или пуповинная кровь. Могут быть использованы различные способы, чтобы отделить клетки. Например, при помощи способов отрицательной селекции можно изначально удалить ЦТЛ. Моноклональные антитела (mAb) особенно полезны для идентификации маркеров, связанных с определенными клеточными линиями и/или стадиями дифференцировки для как положительной, так и отрицательной селекций.
Значительную часть конечно дифференцированных клеток можно изначально удалить при помощи относительно грубой сепарации. Например, сепарации на магнитных бусах может использоваться первоначально для удаления большого количества посторонних клеток. Предпочтительно, по меньшей мере, примерно 80%, как правило, по меньшей мере, 70% от общего количества гемопоэтических клеток удаляется перед клеточным выделением.
Процедуры для разделения включают, в качестве неограничивающих примеров, центрифугирование в градиенте плотности; ресеттинг; соединение с частицами, которые изменяют плотность клеток; магнитную сепарацию с использованием покрытых антителом магнитных шариков; аффинную хроматографию; цитотоксические агенты, присоединенные к или использованные в сочетании с mAb, включая, в качестве неограничивающих примеров, комплемент и цитотоксины; и панорамирование с помощью антител, прикрепленных к твердой матрице, например, планшету, чипу, промывание или любую другую подходящую методику.
Способы разделения и анализа включают, в качестве неограничивающих примеров, проточную цитометрию, которая может иметь различную степень сложности, например, множество цветовых каналов, каналы детекции с низким углом и приглушенного рассеяния света, импедансные каналы.
Клетки могут быть отселектированы от мертвых клеток, используя красители, связывающиеся с мертвыми клетками, такими как пропидия йодида (PI). Предпочтительно, клетки собирают в среде, содержащей 2%-ную эмбриональную телячью сыворотку (FCS) или 0,2% бычьего сывороточного альбумина (BSA), или в любой другой подходящий, желательно стерильной, изотонической среде.
Соответственно, изобретение в целом предоставляет иммунореактивную клетку, такую как вирус-специфическую или опухолеспецифическую Т-клетку, включающую рецептор, который связывает первый антиген и активирует иммунореактивную клетку, и рецептор, который связывает второй антиген и стимулирует иммунореактивную клетку.
Векторы
Генетическую модификацию иммунореактивных клеток (например, Т-клетки, ЦТЛ клеток, NK-клеток) можно достичь путем трансдукции существенно однородной клеточной композиции при помощи конструкции рекомбинантной ДНК. Предпочтительно, ретровирусный (либо гамма-ретровирусных или лентивирусный) вектор используется для введения ДНК-конструкции в клетку. Например, полинуклеотид, кодирующий рецептор, который связывает антиген (например, опухолевый антиген, или вариант, или фрагмент этого), может быть клонирован в ретровирусный вектор, и экспрессия может направляться с его эндогенного промотора, с ретровирусного длинного терминального повтора или с промотора, специфического для типа представляющей интерес клетки-мишени. Невирусные векторы также могут быть использованы.
Для первоначальной генетической модификации клеток для предоставления опухолевый антиген- или вирусный антиген-специфических клеток, ретровирусный вектор обычно используется для трансдукции, однако может использоваться любой другой подходящий вирусный вектор или невирусная система доставки. Для последующей генетической модификации клеток, чтобы предоставить клетки, содержащие антиген-представляющий комплекс, включающий, по меньшей мере, два костимуляторных лиганда, ретровирусный перенос генов (трансдукция) также оказывается эффективный. Комбинации ретровирусного вектора и соответствующая упаковочная линия также подходят, где капсидные белки будут функциональными для инфицирования клеток человека. Различные амфотропные вирус-продуцирующие клеточные линии известны, включая, в качестве неограничивающих примеров, PA 12 (Miller, et al. (1985) Mol Cell Biol. 5:431-437); PA317 (Miller, et al. (1986) Mol. Cell. Biol. 6:2895-2902); и CRIP (Danos, et al (1988) Proc, Natl. Acad. Sci. USA 85:6460-6464). Неамфотропные частицы также подходят, например, частицы, псевдотипированные с VSVG, RD114 или GALV и любые другие, известные в данной области техники.
Возможные способы трансдукции также включают прямое совместное культивирование клеток с продьюсерными клетками, например, способом Bregni, et al. (1992) Blood 80: 1418-1422, или культивирование с вирусным супернатантом самим по себе или концентрированным векторным стоком с соответствующими ростовыми факторами и поликатионами или без них, например, по способу Xu, et al. (1994) Exp. Hemat. 22:223-230; и Hughes, et al. (1992) J. Clin. Invest. 89: 1817.
Другие вирусные векторы могут быть использованы для экспрессии костимуляторных лигандов по изобретению в иммунореактивной клетке. Предпочтительно, выбранный вектор проявляет высокую эффективность инфекции и стабильную интеграцию и экспрессию (см., например, Cayouette et al., Human Gene Therapy 8:423-430, 1997; Kido et al, Current Eye Research 15:833-844, 1996; Bloomer et al, Journal of Virology 71 :6641-6649, 1997; Naldini et al., Science 272:263-267, 1996; and Miyoshi et al., Proc. Natl. Acad. Sci. U.S.A. 94: 10319, 1997). Другие вирусные векторы, которые могут использоваться, включают, например, аденовирусные, лентивирусных, и адена-ассоциированные вирусные векторы, вирус коровьей оспы, вирус папилломы крупного рогатого скота или вирус герпеса, такой как вирус Эпштейна-Барра (также см., например, векторы Миллера, Human Gene Therapy 15-14, 1990; Friedman, Science 244: 1275-1281, 1989; Eglitis et al., BioTechniques 6:608-614, 1988; Tolstoshev et al., Current Opinion in Biotechnology 1 :55-61, 1990; Sharp, The Lancet 337:1277- 1278, 1991 ; Cornetta et al, Nucleic Acid Research and Molecular Biology 36:31 1- 322, 1987; Anderson, Science 226:401-409, 1984; Moen, Blood Cells 17:407-416, 1991 ; Miller et al., Biotechnology 7:980-990, 1989; LeGal La Salle et al, Science 259:988-990, 1993; and Johnson, Chest 107:77S- 83S, 1995). Ретровирусные векторы особенно хорошо разработаны и используются в клинических условиях (Rosenberg et al, N. Engl. J. Med 323:370, 1990; Anderson et al., U.S. Pat. No. 5,399,346).
Невирусные подходы также могут быть использованы для экспрессии белка в клетке. Например, молекулу нуклеиновой кислоты можно вводить в клетку путем введения нуклеиновой кислоты в присутствии липофекции (Feigner et al., Proc. Natl. Acad. Sci. U.S.A. 84:7413, 1987; Ono et al., Neuroscience Letters 17:259, 1990; Brigham et ah, Am. J. Med. Sci. 298:278, 1989; Staubinger et ah, Methods in Enzymology 101 :512, 1983), асиалооросомукоид-полилизиновой конъюгации (Wu et al., Journal of Biological Chemistry 263: 14621, 1988; Wu et al., Journal of Biological Chemistry 264:16985, 1989), или с помощью микро-инъекций в хирургических условиях (Wolff et al., Science 247: 1465, 1990). Другие невирусные средства для переноса генов включают in vitro трансфекцию с использованием фосфата кальция, DEAE-декстрана, электропорацию и слияние протопластов. Липосомы также могут быть потенциально полезны для доставки ДНК в клетку. Трансплантация нормальных генов в пораженных тканях индивидуума может также быть достигнута путем передачи нормальной нуклеиновой кислоты в пригодный для культивирования тип клеток ex vivo (например, аутологичная или гетерологичная первичная клетка или ее потомство), после чего клетку (или его потомков) вводят в ткань-мишень или вводят системно. Рекомбинантные рецепторы могут также быть производными или получены с использованием транспозаз или направленных нуклеаз (например, цинкфингер-нуклеазы, мегануклеазы или нуклеазы TALE). Транзиентную экспрессию можно получить путем РНК-электропорации.
Экспрессию кДНК для использования в способах полинуклеотидной терапии можно направлять с любого подходящего промотора (например, промоутеров цитомегаловируса (ЦМВ) человека, обезьяньего вируса 40 (SV40) или металлотионеина), и регулировать любым соответствующим регуляторным элементом или интроном млекопитающих (например, структура энхансер/промотор/интрон фактора элонгации 1а). Например, при желании, энхансеры, известные преимущественным управлением экспрессии генов в специфических типах клеток, могут быть использованы для управления экспрессией нуклеиновой кислоты. Используемые энхансеры могут включать, в качестве неограничивающих примеров, таковые, которые характеризуются как ткане- или клеточно-специфические энхансеры. Альтернативно, если геномный клон используется в качестве лечебной конструкции, регулирование может быть опосредовано родственными регуляторными последовательностями или, при желании, с помощью регуляторных последовательностей, полученных из гетерологичных источников, в том числе любого из промоторов или регуляторных элементов, описанных выше.
Полученные клетки могут быть выращены в тех же условиях, сходных с таковыми для немодифицированных клеток, вследствие чего немодифицированные клетки могут быть размножены и использованы для различных целей.
Полипептиды и аналоги
Также включенными в изобретение являются полипептиды aCD19, aCD19, CD28, CD3ζ, 4H1128z, B6H12.2 scFv, scFv 5C4 и J43 scFv или их фрагменты, которые модифицированы таким образом, чтобы усилить их анти-опухолевую активность (например, гуманизированное моноклональное антитело) при экспрессировании в иммунореактивной клетке. Изобретение предоставляет способы для оптимизации аминокислотной последовательности или последовательности нуклеиновой кислоты путем проведения изменения в последовательности. Такие изменения могут включать определенные мутации, делеции, инсерции или посттрансляционных модификаций. Изобретение далее включает аналоги любого встречающегося в природе полипептида по изобретению. Аналоги могут отличаться от встречающегося в природе полипептида по изобретению различиями в аминокислотной последовательности, посттрансляционными модификациями или и тем, и другим. Аналоги по изобретению обычно проявляют, по меньшей мере, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности с полной или частью встречающейся в природе аминокислотной последовательности по изобретению. Длина последовательности сравнения составляет, по меньшей мере, 5, 10, 15 или 20 аминокислотных остатков, предпочтительно, по меньшей мере 25, 50 или 75 аминокислотных остатков, и более предпочтительно, более чем 100 аминокислотных остатков. Опять же, в типичном подходе для определения степени идентичности может быть использована программа BLAST, с вероятностью попадания от e-3 до e-100 указывающая близкородственную последовательность. Модификации включают in vivo и in vitro химическую дериватизацию полипептидов, например, ацетилирование, карбоксилирование, фосфорилирования или гликозилирование; такие модификации могут происходить во время полипептидного синтеза или процессинга или после обработки с выделенными модифицирующими ферментами. Аналоги могут также отличаться от встречающихся в природе полипептидов по изобретению по изменениям в первичной последовательности. Они включают генетические варианты, как природные, так и индуцированные (например, в результате случайного мутагенеза путем облучения или воздействия этанметилсульфата или путем сайт-специфического мутагенеза, как описано в Sambrook, Fritsch and Maniatis, Molecular Cloning: A Laboratory Manual (2d ed.), CSH Press, 1989, or Ausubel et al, выше). Кроме того, включенными являются циклизованные пептиды, молекулы и аналоги, которые содержат остатки, отличные от L-аминокислот, например, D-аминокислоты или неприродные или синтетические аминокислоты, например, бета (β) и гамма (γ) аминокислоты.
В дополнение к полноразмерным полипептидам, изобретение также предоставляет фрагменты любого из полипептидов или пептидных доменов по изобретению. Как используется в настоящем документе, термин "фрагмент" означает, по меньшей мере, 5, 10, 13 или 15 аминокислот. В других вариантах осуществления фрагмента представляет собой, по меньшей мере, 20 смежных аминокислот, по меньшей мере, 30 смежных аминокислот или, по меньшей мере, 50 смежных аминокислот, и в других вариантах осуществления, по меньшей мере, от 60 до 80, 100, 200, 300 или более смежных аминокислот. Фрагменты по изобретению могут быть созданы с помощью способов, известных специалистам в данной области или могут возникать в результате нормального процессинга белков (например, удаление аминокислот из растущего полипептида, которые не являются необходимыми для биологической активности, или удаление аминокислот с помощью событий альтернативного сплайсинга мРНК или альтернативного процессинга белка).
Небелковые аналоги имеют химическую структуру, спроектированную для имитации функциональной активности белка по изобретению. Такие аналоги вводят в соответствии со способами по изобретению. У таких аналогов физиологическая активность может превышать таковую исходного полипептида. Способы проектирования аналогов хорошо известны в данной области техники, и синтез аналогов может быть осуществлен с применением этих способов путем изменения химических структур, так что результирующие аналоги превосходят по противоопухолевой активности исходный полипептид, при экспрессии в иммунореактивной клетке. Эти химические модификации включают, в качестве неограничивающих примеров, замену альтернативных R-групп и варьирование степени насыщения в конкретных атомах углерода эталонного полипептида. Предпочтительно, белковые аналоги обладают относительно высокой устойчивостью к деградации in vivo, что приводит к более пролонгированному лечебному эффекту при введении. Тесты для оценки функциональной активности включают, в качестве неограничивающих примеров, таковые, которые описаны в нижеприведенных примерах.
Костимуляторные лиганды
Взаимодействие с, по меньшей мере, одним костимуляторных лигандов обеспечивает сигнал, отличный от антиген-специфического, важный для полной активации иммунных клеток (например, Т-клеток). Костимуляторные лиганды включают, в качестве неограничивающих примеров, лиганды фактора некроза опухолей (TNF), цитокины (таких как IL-2, IL-12, IL-1 или IL21), и лигандов суперсемейства иммуноглобулинов (Ig). Фактор некроза опухолей (TNF) представляет собой цитокин, участвующий в системное воспаление и стимулирует реакции острой фазы. Его основная роль заключается в регуляции иммунокомпетентных клеток. Лиганды фактора некроза опухолей (TNF) имеют ряд общих черт. Большинство лигандов синтезируются как трансмембранные белки II типа (внеклеточный С-конец), содержащие короткий цитоплазматический сегмент и относительно длинную внеклеточную область. TNF-лиганды включают, в качестве неограничивающих примеров,, фактор роста нервов (NGF), CD40L (CD40L)/CD154, CD137L/4-1BBL, фактор некроза опухоли альфа (TNFα), CD134L/OX40L/CD252, CD27L/CD70, FAS-лиганд (FasL), CD30L/CD153, фактор некроза опухоли бета (ΤΝΡβ)/лимфотоксин-альфа (LTα), лимфотоксин-бета (LTβ), CD257/В-клетки-активирующий фактор (BAFF)/Blys/THANK/Tall-1, лиганд глюкокортикоид-индуцируемого TNF-рецептора (GITRL), и TNF-связанных апоптоз-индуцирующий лиганд (TRAIL), LIGHT (TNFSF14). Суперсемейство иммуноглобулинов (Ig) представляет собой большую группу белков клеточной поверхности и растворимых белков, которые участвуют в процессах распознавании, связывании или адгезии в клетках. Эти белки имеют общие структурные особенности с иммуноглобулинами - они обладают иммуноглобулиновым доменом (fold). Лиганды суперсемейства иммуноглобулинов включают, в качестве неограничивающих примеров, CD80 и CD86, как лиганды для CD28.
Введение
Композиции, содержащие генетически модифицированные иммунореактивные клетки по изобретению (например, Т-клетки, NK-клетки, CTL-клетки или их предшественники), могут предоставляться системно или непосредственно индивидууму для лечения неоплазии, патогенной инфекции или инфекционного заболевания. В одном варианте осуществления, клетки по изобретению вводят непосредственно в представляющий интерес орган (например, орган, пораженный неоплазией). Альтернативно, композиции, содержащие генетически модифицированные иммунореактивные клетки, предоставляют опосредованно к представляющему интерес органу, например, путем введения в кровеносную систему (например, опухоли сосудистого русла). Агенты наращивания и дифференциации могут быть предоставлены до, во время или после введения клеток для увеличения продукции Т-клеток, NK-клеток или ЦТЛ-клеток in vitro или in vivo.
Модифицированные клетки можно вводить в любом физиологически приемлемом носителе, обычно внутрисосудисто, хотя они также могут быть введены в кость или в другой удобный участок, где клетки могут найти подходящий участок для регенерации и дифференцировки (напр., вилочковая железа). Как правило, вводят, по меньшей мере, 1×105 клеток, в конечном счете достигая 1×1010 или более. Генетически модифицированные иммунореактивные клетки по изобретению могут включать очищенную популяцию клеток. Специалисты в данной области техники могут легко определить процент генетически модифицированных иммунореактивных клеток в популяции с использованием различных хорошо известных способов, таких как клеточный сортер с возбуждением флуоресценции (FACS). Предпочтительные диапазоны чистоты в популяциях, содержащих генетически модифицированные иммунореактивные клетки, составляют примерно от 50 до примерно 55%, примерно от 55 до примерно 60% и примерно от 65 до примерно 70%. Более предпочтительно, чистота составляет примерно от 70 до примерно 75%, примерно от 75 до примерно 80%, примерно от 80 до примерно 85%; и еще более предпочтительно, чистота составляет примерно от 85 до примерно 90%, примерно от 90 до примерно 95%, и примерно от 95 до примерно 100%. Дозировки могут быть без труда скорректированы с помощью специалиста в данной области техники (например, при снижении чистоты может потребоваться увеличение дозы препарата). Клетки могут быть введены путем инъекции, катетера или тому подобное. При желании также могут быть включены факторы, в том числе, в качестве неограничивающих примеров, интерлейкины, например IL-2, IL-3, IL-6, IL-11, IL7, IL12, ILIS, IL21, а также другие интерлейкины, колоние-стимулирующие факторы, такие как G-, М- и GM-CSF, интерфероны, например, гамма-интерферон и эритропоэтин.
Композиции по изобретению включают фармацевтические композиции, содержащие генетически модифицированные иммунореактивные клетки или их предшественники и фармацевтически приемлемый носитель. Введение может быть аутологичным или гетерологичным. Например, иммунореактивные клетки или предшественники могут быть получены из одного индивидуума, и вводиться тому же индивидууму, или другому, совместимому индивидууму. Полученные из периферической крови иммунореактивные клетки по изобретению или их потомство (например, производные in vivo, ex vivo или in vitro) можно вводить посредством локализованных инъекций, в том числе катетерное введение, системное введение, локализованная инъекция, внутривенная инъекция или парентеральное введение. При назначении терапевтической композиции по настоящему изобретению (например, фармацевтической композиции, содержащей генетически модифицированные иммунореактивные клетки), она, как правило, должна быть составлена в лекарственной форме для инъекции однократной дозы (раствор, суспензия, эмульсия).
Составы
Композиции по изобретению, включающие иммунореактивные генетически модифицированные клетки, могут быть легко сформированы как стерильные жидкие препараты, например, изотонические водные растворы, суспензии, эмульсии, дисперсии или вязкие композиции, которые могут быть буферизованы для обеспечения выбранного уровня pH. Жидкие препараты, как правило, легче подготовить, чем гели, другие вязкие композиции и твердые составы. Кроме того, жидкие композиции являются несколько более удобными при введении, особенно путем инъекции. Вязкие композиции, с другой стороны, могут быть сформулированы в соответствующем диапазоне вязкости для обеспечения более длительных периодов контактирования с конкретными тканями. Жидкие или вязкие композиции могут содержать носители, которые могут представлять собой сольвент или диспергирующую среду, содержащую, например, воду, физиологический раствор, фосфатно-солевой буфер, полиол (например, глицерин, пропиленгликоль, жидкий полиэтиленгликоль и тому подобное) и подходящие их смеси.
Стерильные инъекционные растворы могут быть подготовлены путем внедрения генетически модифицированных иммунореактивных клеток, используемых в практике настоящего изобретения, в необходимом количестве соответствующего сольвента с различными количествами других ингредиентов, как требуется. Такие композиции могут быть в смеси с подходящим носителем, разбавителем или наполнителем, таким как стерильная вода, физиологический раствор, глюкоза, декстроза или тому подобное. Композиции также могут быть лиофилизированными. Композиции могут содержать вспомогательные вещества, такие как смачивающие, диспергирующие или эмульгирующие средства (например, метилцеллюлозу), рН-буферные вещества, гелеобразующие или повышающие вязкость добавки, консерванты, ароматизаторы, красители и тому подобное, в зависимости от пути введения и подготовки желаемого. Стандартные руководства, такие как "REMINGTON'S PHARMACEUTICAL SCIENCE", 17th edition, 1985, включенные в настоящий документ посредством ссылки, можно использовать консультирования с целью подготовки подходящих препаратов, без излишних экспериментов.
Различные добавки, которые повышают стабильность и стерильность композиции, в том числе антимикробные консерванты, антиоксиданты, хелатные средства и буферы, могут быть добавлены. Предотвращение действия микроорганизмов может быть обеспечено различными антибактериальными и противогрибковыми средствами, например, парабенами, хлорбутанолом, фенолом, сорбиновой кислотой и тому подобное. Пролонгированная абсорбция инъекционной фармацевтической формы может быть обеспечена путем использования средств, задерживающих абсорбцию, например, моностеарата алюминия и желатина. В соответствии с настоящим изобретением, тем не менее, любой используемый носитель, разбавитель или добавка должны быть совместимы с генетически модифицированными иммунореактивными клетками или их предшественниками.
Композиции могут быть изотоническим, т.е. они могут иметь то же осмотическое давление, что и кровь и слезная жидкость. Желаемую изотоничность композиций по настоящему изобретению можно осуществить с использованием хлорида натрия или других фармацевтически приемлемых средств, таких как декстроза, борная кислота, тартрат натрия, пропиленгликоль или другие неорганические или органические растворенные вещества. Натрия хлорид является предпочтительным, особенно для буферов, содержащих ионы натрия.
Вязкость композиции, при желании, можно поддерживать на выбранном уровне с помощью фармацевтически приемлемого загустителя. Метилцеллюлоза является предпочтительной, так как она физически и экономически доступна, и с ней легко работать.
Другие подходящие загустители включают, например, ксантановую камедь, карбоксиметилцеллюлозу, гидроксипропилцеллюлозу, карбомер и тому подобное. Предпочтительная концентрация загустителя зависит от выбранного средства. Важным моментом является то, чтобы использовать количество, которое обеспечит достижение требуемой вязкости. Очевидно, выбор подходящих носителей и других добавок будет зависеть от точного способа введения и характера конкретной лекарственной формы, например, жидкой лекарственной формы (например, составлена ли композиция в виде раствора, суспензии, геля или другой жидкой формы, такой форма с временным высвобождением или заполненная жидкостью форма).
Специалисты в данной области техники признают, что компоненты композиций следует выбирать такие, чтобы они были химически инертными и не влияли на жизнеспособность или эффективность генетически модифицированных иммунореактивных клеток, как описано в настоящем изобретении. Это не представляет никаких проблем для специалиста в химических и фармацевтических вопросах, или проблем можно легко избежать путем обращения к стандартным руководствам или путем несложных экспериментов (не привлекая излишнего экспериментирования), из этого раскрытия и документов, цитируемых в настоящем документе.
Одним соображением, касающимся терапевтического применения генетически модифицированных иммунореактивных клеток по изобретению, является количество клеток, необходимых для достижения оптимального эффекта. Количество вводимых клеток варьирует в зависимости от индивидуума, проходящего лечение. В одном варианте, индивидууму-человеку вводят от 104 до 1010, от 105 до 109 или от 106 до 108 генетически модифицированных иммунореактивных клеток по изобретению. Более эффективные клетки можно вводить даже в меньших количествах. В некоторых вариантах, по меньшей мере, приблизительно 1×108, 2×108, 3×108, 4×108 и 5×108 генетически модифицированных иммунореактивных клеток по изобретению вводят индивидууму-человеку. Точное определение того, что считается эффективной дозой, может основываться на факторах, индивидуальных для каждого индивидуума, в том числе их размер, возраст, пол, масса и состояния конкретного индивидуума. Дозировки могут быть легко установлены с помощью специалиста в данной области техники из этого раскрытия и познаний в рассматриваемой области.
Специалист в данной области может легко определить количество клеток и необязательных добавок, средств доставки и/или носителя в композициях и вводимых в способах по изобретению. Как правило, любые добавки (в дополнение к активной клетке(ам) и/или средству(ам)) присутствуют в количестве от 0,001 до 50% (массы) раствора в фосфатно-солевом буфере, и активный ингредиент присутствует в количестве порядка от микрограммов до миллиграммов, например, примерно от 0,0001 до примерно 5 масс.%, предпочтительно, примерно от 0,0001 до примерно 1 масс.%, еще более предпочтительно, примерно от 0,0001 до примерно 0,05 масс.% или примерно от 0,001 до примерно 20 масс.%, предпочтительно, примерно от 0,01 до примерно 10 масс. % и еще более предпочтительно, примерно от 0,05 до примерно 5 масс.%. Конечно, для любой композиции, вводимой в животное или человека, и для любого конкретного способа введения предпочтительно определить поэтому: токсичность, например, путем определения летальной дозы (LD) и LD50 в подходящей модели на животных, например, грызунах, таких как мыши; и, дозировку композиции(й), концентрацию компонентов в ней и сроки введения композиции(й), которые вызывают соответствующий ответ. Такие определения не требуют излишнего экспериментирования на основе компетенции специалиста, этого раскрытия и документов, цитируемых в настоящем документе. И время для последовательных введений может быть установлено без проведения излишних экспериментов.
Способы лечения
В настоящем документе приведены способы лечения неоплазии у индивидуума. Также предусмотренными в настоящем документе являются способы лечения патогенной инфекции или другого инфекционного заболевания у индивидуума, такого как индивидуум-человек с ослабленным иммунитетом. Способы включают введение Т-клеток, NK-клеток или ЦТЛ-клеток по изобретению в количестве, эффективном для достижения желаемого эффекта, будь то временное облегчение существующего состояния или предупреждение рецидива. Для лечения вводимое количество представляет собой количество, эффективное в плане получения желаемого эффекта. Эффективное количество может предоставляться в одно или за несколько введений. Эффективное количество может предоставлять в болюсе или путем непрерывной перфузии.
"Эффективное количество" (или "терапевтически эффективное количество") представляет собой количество, достаточное для осуществления полезного или желаемого клинического результата при лечении. Эффективное количество может вводиться индивидууму в одной или более дозах. В плане лечения, эффективное количество представляет собой количество, которое достаточно, чтобы смягчить, улучшить, стабилизировать, обратить вспять или замедлить прогрессирование болезни, или иным образом уменьшить патологические последствия заболевания. Эффективное количество, как правило, определяет врач на индивидуальной основе и в пределах степени компетенции в рассматриваемой области техники. Несколько факторов обычно учитываются при определении адекватной дозы для достижения эффективного количества. Эти факторы включают возраст, пол и массу индивидуума, состояния, подлежащего лечению, степени тяжести состояния и формы и эффективной концентрации вводимого антиген-связывающего фрагмента.
Для адоптивной иммунотерапии с использованием антиген-специфических Т-клеток проводят инфузию дозы клеток, как правило, в диапазоне 106-1010 (например, 109). При введении генетически модифицированных клеток хозяину и последующей дифференциации, индуцируются Т-клетки, специально направленные против специфического антигена. "Индукция" Т-клеток может включать инактивацию антиген-специфических Т-клеток, например, путем делетирования или анергии. Инактивация особенно полезна для установления или восстановления толерантности, такой как аутоиммунные расстройства. Модифицированные клетки можно вводить любым способом, известным специалистам, включая, в качестве неограничивающих примеров, внутривенный, подкожный, межузловой, внутриопухолевый, интратекальный, внутриплевральный, внутрибрюшинный и непосредственно в тимус.
Терапевтические способы
Изобретение предоставляет способы повышения иммунного ответа у индивидуума, нуждающегося в этом. В одном варианте осуществления изобретение предоставляет способы лечения или предупреждения неоплазии у индивидуума. Изобретение предоставляет способы лечения, которые особенно полезны для лечения индивидуумов, имеющих рак крови (например, лейкозы, лимфомы и миеломы) или рак яичников, которые не поддаются обычным терапевтическим вмешательствам. Подходящие индивидуумы-люди для терапии, как правило, составляют две группы лечения, которые можно отличить по клиническим критериям. Испытуемые с "запущенной болезнью" или "высоким бременем опухоли" представляют собой тех, которые несут клинически измеримые опухоли. Клинически измеримые опухоли могут быть обнаружены на основе опухолевой массы (например, пальпация, томография, УЗИ, маммография или рентген; положительные биохимические или гистопатологический маркеры сами по себе являются недостаточными для идентификации этой популяции). Фармацевтическую композицию, воплощенную в этом изобретении, вводят этим индивидуумам, чтобы добиться противоопухолевого ответа с целью облегчения их состояния. В идеале, в результате происходит снижение опухолевой массы, но любое клиническое улучшение является благоприятным. Клиническое улучшение включает снижение риска или скорости прогрессирования или уменьшение патологических последствий опухоли.
Вторая группа подходящих индивидуумов известна в рассматриваемой области в качестве "вспомогательной группы". Это лица, которые имели историю неоплазии, но были отзывчивы на другой режим терапии. Предшествующая терапия включает, в качестве неограничивающих примеров, хирургическую резекцию, лучевую терапию и традиционную химиотерапию. Как следствие, эти лица не имеют клинически измеримой опухоли. Тем не менее, они подозреваются в том, что имеют риск прогрессирования заболевания, либо недалеко от исходной локализации опухоли, или за счет метастазов. Эта группа можно далее подразделить на лиц с высоким риском и низким риском. Подразделение производится на основе особенностей, наблюдаемых до или после первоначального лечения. Эти особенности известны в клинической области, и являются достаточно определенными для каждой из различных неоплазий. Признаки, характерные для подгрупп с высоким риском, являются такие, при которых опухоль поражала соседние ткани, или которые демонстрируют вовлеченность лимфатических узлов.
Другая группа имеет генетическую предрасположенность к неоплазии, но которая еще не подтверждена клиническими признаками неоплазии. Например, женщины с положительным результатом теста на генетическую мутацию, связанную с раком молочной железы, но еще находящиеся в детородном возрасте, могут желать получать один или более антиген-связывающих фрагментов, описанных в данном документе, при лечении в профилактических целях для предотвращения возникновения неоплазии, пока она не пригодна для проведения превентивной операции.
Индивидуумы-люди с неоплазией, имеющие любую из следующих неоплазий: глиобластому, меланому, нейробластому, аденокарциному, глиому, саркому мягких тканей и разнообразные карциномы (в том числе рак предстательной железы и мелкоклеточный рак легких), являются особенно подходящими индивидуумами. Подходящие карциномы дополнительно включают любые, известные в области онкологии, в том числе, в качестве неограничивающих примеров, астроцитому, фибросаркому, миксосаркому, липосаркому, олигодендроглиому, эпендимому, медуллобластому, примитивную нейрональную эктодермальную опухоль (PNET), хондросаркому, остеогенную саркому, аденокарциному протоков поджелудочной железы, малые и большие клетки аденокарциномы легких, хордому, ангиосаркому, эндотелиосаркому, плоскоклеточный рак, бронхоальвеолярную карциному, эпителиальную аденокарциному и ее метастазы в печени, лимфангиосаркому, лимфангиоэндотелиальную саркому, гепатому, холангиокарциному, синовиому, мезотелиому, опухоль Юинга, рабдомиосаркому, рак ободочной кишки, базально-клеточную карциному, карциному потовых желез, папиллярную карциному, карциному сальных желез, папиллярную аденокарциному, цистаденокарциному, медуллярную карциному, бронхогенную карциному, почечно-клеточный рак, карциному желчных протоков, хориокарциному, семиному, эмбриональную карциному, опухоль Вильмса, опухоль яичка, медуллобластому, краниофарингиому, эпендимому, пинеалому, гемангиобластому, невриному слухового нерва, олигодендроглиому, менингиому, нейробластому, ретинобластому, лейкемию, множественную миелому, макроглобулинемию Вальденстрема и заболевание тяжелых цепей, опухоли молочной железы, такие как протоковая и дольковая аденокарциномы, плоскоклеточный и аденокарциномы шейки матки, эпителиальные карциномы матки и яичников, аденокарциномы предстательной железы, переходный плоскоклеточный рак мочевого пузыря, В- Т-клеточные лимфомы (узловая и диффузная), плазмоцитому, острые и хронические лейкозы, злокачественную меланому, саркомы мягких тканей и лейомиосаркомы.
Индивидуумы могут иметь развитую форму заболевания, в этом случае цель лечения может включать смягчение или нейтрализацию прогрессирования заболевания, и/или уменьшение побочных эффектов. Индивидуумы могут иметь предысторию состояния, для которой они уже проходили лечение, в этом случае терапевтические цели обычно включают снижение или задержку риска рецидива.
Соответственно, изобретение предоставляет способ лечения или предупреждения неоплазии у индивидуума, включающий введение эффективного количества иммунореактивной клетки, содержащей рецептор, который связывается с опухолевым антигеном и активирует иммунореактивную клетку (например, TCR, CAR), и вектор, кодирующий одноцепочечный вариабельный фрагмент (scFv), который связывает антиген, обладающий иммуносупрессивной активностью (например, CD47, PD-1, CTLA-4 и их лиганды). В одном варианте осуществления неоплазия выбрана из группы, состоящей из рака крови (например, лейкозов, лимфом и миелом), рака яичника, рака предстательной железы, рака молочной железы, рака мочевого пузыря, рака мозга, рака толстой кишки, рака кишечника, рака печени, рака легких, рака поджелудочной железы, рака предстательной железы, рака кожи, рака желудка, глиобластомы и рака горла. В другом варианте осуществления опухолевый антиген представляет собой один или более из карбоангидразы IХ (CAIX), карциноэмбрионального антигена (СЕА), CDS, CD7, CDIO, CD19, CD20, CD22, CD30, CD33, CD34, CD38, CD41, CD44, CD49f, CD56, CD74, CD133, CD138, антиген клетки, инфицированной цитомегаловирусом (ЦМВ) (например, антиген клеточной поверхности), эпителиального гликопротеина-2 (EGP-2), эпителиального гликопротеина-40 (EGP-40), молекулы адгезии эпителиальных клеток (EpCAM), рецептора тирозин-протеинкиназ erb-В2,3,4, фолат-связывающего белка (FBP), эмбрионального ацетилхолинового рецептора (AChR), фолатного рецептора-α, ганглиозида G2 (GD2), ганглиозида G3 (GD3), рецептора эпидермального фактора роста 2 человека (HER-2), теломеразной обратной транскриптазы человека (hTERT), субъединицы альфа-2 рецептора интерлейкина-13 (IL-13Rα2), κ-легкой цепи, рецептора киназного инсерционного домена (KDR), Льюис Y (LeY), молекулы клеточной адгезии L1 (L1CAM), семейства А меланомого антигена, (MAGE-A1), муцина 16 (MUC16), муцина 1 (MUC1), мезотелина (MSLN), лигандов NKG2D, антигена рак яичка NY-ESO-1, онкофетального антигена (h5T4), антигена стволовых клеток простаты (PSCA), простат-специфического мембранного антигена (PSMA), опухоль-ассоциированного гликопротеина 72 (TAG-72), сосудистого эндотелиального фактора роста R2 (VEGF-R2) или белка опухоли Вильмса (WT-1).
Как следствие поверхностной экспрессии рецептора, который связывает опухолевый антиген и активирует иммунореактивную клетку (например, ТС, CAR), и вектора, кодирующего одноцепочечный вариабельный фрагмент (scFv), который связывает антиген, обладающий иммуносупрессивной активностью (например, CD47, PD-1, CTLA-4 и их лиганды), адаптивно передаваемые Тор NK-клетки человека наделены дополненной и селективной цитолитической активностью в опухолевом участке. Кроме того, после их локализации в опухолевой или вирусной инфекции и их пролиферации, костимуляторные лиганд-экспрессирующие Т-клетки превращают участок опухолевой или вирусной инфекции в высоко проводящую среду для широкого спектра иммунокомпетентных клеток, участвующих в физиологической противоопухолевой или противовирусной реакции (опухоле-проникающие лимфоциты, NK-, NKT-клетки, дендритные клетки и макрофаги).
В других вариантах осуществления, изобретение предоставляет способы лечения индивидуумов с патогеной инфекцией (например, вирусной инфекцией, бактериальной инфекцией, грибковой инфекцией, паразитарной инфекцией или протозойной инфекцией). Изобретение является особенно полезным для усиления иммунного ответа у индивидуума с ослабленным иммунитетом. Типичные вирусные инфекции, поддающиеся лечению с помощью способа по изобретения, включают, в качестве неограничивающих примеров, инфекции цитомегаловируса (ЦМВ), вируса Эпштейна-Барра (EBV), вируса иммунодефицита человека (ВИЧ) и вируса гриппа.
Соответственно, изобретение предоставляет способ лечения или предотвращения патогенной инфекции у индивидуума, включающий введение эффективного количества иммунореактивной клетки, как описано в настоящем документе.
Наборы
Изобретение предоставляет наборы для лечения или предупреждения неоплазии, патогенной инфекции, иммунного расстройства или аллогенной трансплантации. В одном варианте осуществления набор включает терапевтическую или профилактическую композицию, содержащую эффективное количество иммунореактивной клетки, включающей рецептор активирующего антигена и одноцепочечный вариабельный фрагмент (scFv), который связывает антиген, обладающий иммуносупрессивной активностью, в единичной лекарственной форме. В конкретных вариантах осуществления клетки дополнительно включают костимуляторный лиганд. В некоторых вариантах осуществления, в набор входит стерильный контейнер, который содержит лечебную или профилактическую вакцину; такие контейнеры могут представлять собой коробки, ампулы, бутылки, флаконы, пробирки, пакеты, мешки, блистер-пачки или другие подходящую емкостные формы, известные в рассматриваемой области техники. Такие контейнеры могут быть изготовлены из пластика, стекла, ламинированной бумаги, металлической фольги или других материалов, пригодных для хранения медикаментов.
При желании в иммунореактивная клетка поставляется вместе с инструкциями для введения клетки индивидууму, имеющему или с риском развития неоплазии, патогенной инфекции, иммунного расстройства или аллогенной трансплантации. Инструкции, как правило, содержат информацию об использовании композиции для лечения или предупреждения неоплазии, патогенной инфекции, иммунного расстройства или аллогенной трансплантации. В других вариантах осуществления инструкции включают, по меньшей мере, одно из следующего: описание терапевтического средства; режим дозировки и введения для лечения или предупреждения неоплазии, патогенной инфекции, иммунного расстройства или аллогенной трансплантации или их симптомы; меры предосторожности; предупреждения; показания; противопоказания; информации о передозировке; побочные реакции; фармакология на животных; клинические исследования; и/или ссылки. Инструкции могут быть напечатаны непосредственно на контейнере (при его наличии), или в качестве наклейки, прикрепленной к контейнеру, или в виде отдельного листа, брошюры, карты или папки, поставляемой в контейнере или с контейнером.
ПРИМЕРЫ
В практике настоящего изобретения использует, если не указано иное, общепринятые методики молекулярной биологии (включая рекомбинантные методики), микробиологии, клеточной биологии, биохимии и иммунологии, которые находятся в пределах компетенции специалиста в рассматриваемой области техники. Такие способы подробно описаны в литературе, например, "Molecular Cloning: A Laboratory Manual", second edition (Sambrook, 1989); "Oligonucleotide Synthesis" (Gait, 1984); "Animal Cell Culture" (Freshney, 1987); "Methods in Enzymology" "Handbook of Experimental Immunology" (Weir, 1996); "Gene Transfer Vectors for Mammalian Cells" (Miller and Calos, 1987); "Current Protocols in Molecular Biology" (Ausubel, 1987); "PCR: The Polymerase Chain Reaction", (Mullis, 1994); "Current Protocols in Immunology" (Coligan, 1991). Эти способы применимы для производства полинуклеотидов и полипептидов по изобретению, и, как таковые, могут быть учтены при изготовлении и практическом осуществлении изобретения. Особенно полезные методики для конкретных вариантов осуществления будут рассмотрены в следующих разделах.
Следующие примеры предлагаются для того, чтобы предоставить любому специалисту в рассматриваемой области техники полное раскрытие и описание того, как подготовить и применить способы тестирования, скрининга и лечения по изобретению, и не предназначены для ограничения объема того, что изобретатели считают своим изобретением.
Пример 1. Т-клетки, ко-экспрессирующие химерный антигенный рецептор (CAR) и анти-SCD47 scFv, уничтожали опухоли.
Был создан scFv, который специфически связывается с CD47 человека, и Т-клетки периферической крови человека, модифицированные этим scFv и CAR, распознающий опухолевый антиген (CD19), продемонстрировали in vitro противоопухолевую эффективность, а также повышенную противоопухолевую эффективность в доклинической модели.
Были получены конструкции, включающие 1928z-2А-B6H12.2 (фигуры 1-5), что подтверждено секвенированием последовательностей CAR и scFv. Кроме того, контрольные конструкции были созданы с CAR, специфического для антигена рака яичников, MUC-CD, называемого 4H1128z (фигура 6). Стабильные продуцирующие клеточные линии были созданы для конструкций с использованием лидерной последовательности каппа и проверены способом проточной цитометрии (фигура 7А). Супернатант упаковочных клеточных линий, содержащая секретируемый анти-CD47 scFV, была способна блокировать антитело CD47 от связывания с опухолевыми клетками Nalm-6 и Raji в анализе на основе проточной цитометрии. Опухолевые клетки, инкубированные с супернатантом от упаковочных клеток, также окрашивали антителом к тегу c-myc, чтобы продемонстрировать связывание scFv (фигура 7В).
Упаковочные клетки были использованы для трансдукции Т-клеток периферической крови человека, где эффективность трансдукции оценивали путем анализа способом проточной цитометрии экспрессии CAR (фигура 8А). Секретированный scFv был в состоянии функционировать аутокринным образом, причем антитело анти-CD47 снижало связывание с Т-клетками 1928z-2А-B6H12.2 по сравнению с Т-клетками I928z. Положительное окрашивание антителом к тегу c-myc указывало на связанный scFv (фигура 8В). Фенотип трансдуцированных Т-клеток исследовали способом проточной цитометрии и продемонстрировали сходство между Т-клетками 1928z-2А-B6H12.2 и 1928z, за исключением CD62L, который, как было обнаружено, был снижен в Т-клетках 1928z-2А - B6H12.2 (фигура 9А). Функция Т-клеток, продуцирующих анти-CD47 scFv, была исследована с помощью многопараметрической проточной цитометрии и стандартного анализа высвобождения 51Cr. Показано, что Т-клетки 1928z-2А-B6H12.2 имеют эквивалентную продукцию цитокинов и цитотоксическую функцию по сравнению с Т-клетками 1928z (фигуры 9В и 9С).
Способность Т-клеток 1928z-2А-B6H12.2 реагировать на опухоль in vivo исследовали с помощью доклинической мышиной модели SCID-Beige. Мышам SCID-Beige вводили внутривенно 1×106 опухолевых клеток Nalm-6, модифицированных для экспрессии люциферазы Firefly, через 3 дня мышей лечили с 5,7×106 CAR+ I928z или Т-клетками 1928z-2А-B6H12.2 или контрольными Т-клетками 4H1128z-2А-B6Hl2.2, также вводимыми внутривенно. Рост опухоли контролировали клинически и с помощью биолюминесцентного отображения. Лечение несущих опухоль мышей Т-клетками 1928z-2А-B6HI2.2 уменьшало опухолевую массу и повышало выживаемость несущих опухоль мышей по сравнению с лечением Т-клетками 1928z (фигуры 10А и 10В).
Пример 2. Т-клетки, ко-экспрессирующие химерный антигенный рецептор (CAR) и scFv против PD-1 человека, обладали увеличенной пролиферацией и сохраняли экспрессию CAR.
scFv против PD-1 человека создали на основе VH и VL цепей антитела анти-PD-1 (клон 5C4) (патент США № 8008449). 5C4 scFv был спроектирован, чтобы включить лидерную последовательность каппа, серин-глициновый линкер и c-myc тег (фигура 11). Эту конструкцию scFv клонировали в каркас ретровируса SFG для создания 1928z-2А-5C4 и 4H1128z-2А-5C4 (Фигуры 12 и 13). Для разработки высокоаффинного scFv, который связывается с PD-1 человека (например, для экспрессии в 1928z/4H1128z CART клетках), скринируют библиотеку фагового дисплея антитело человека, чтобы определить scFv, которые специфически связывают PD-1 человека (и потенциально мышиный PD-1).
Стабильные упаковочные клеточные линии 293Glv9 были получены, и экспрессию 1928z CAR и 4H1128z CAR оценивали способом проточной цитометрии (фигура 14). Супернатант от этих упаковочных клеток использовали для трансдукции Т-клеток периферической крови человека, и эффективность трансдукции оценивали способом проточной цитометрии для детектирования экспрессии CAR (фигура 15).
Исследовалась способность этого scFv против PD-1 человека увеличивать пролиферацию Т-клеток в ответ на клетки, представляющие искусственный антиген (aAPC). PD-L1 положительных опухолевых клеток 3Т3 и aAPC были созданы для исследования (фигура 16). После совместного культивирования трансдуцированных Т-клеток с 3Т3 aAPC, экспрессирующих CD19 человека, В7.1 человека и PD-L1 человека, Т-клетки 1928z-2А-С4 увеличили пролиферацию и сохранили экспрессию CAR по сравнению с Т-клетками 1928z (фигура 17). Фенотип и противоопухолевую функцию Т-клеток, ко-экспрессирующих 1928z CAR и анти-PD1 scFV, можно определить с помощью проточной цитометрии, аналитических исследований цитокинов Luminex, анализов высвобождения 51хрома и доклинической модели SCID-Beige для определения противоопухолевой функции in vivo.
Пример 3. Ко-экспрессия химерного антигенного рецептора (CAR) и scFv против PD-1 мыши стимулирует Т-клетки мыши.
scFv против PD-1 мыши был создан на основе VH и VL от клона J43 антитела против PD-1 (патент США № 7858746 к Honjo et al.). J43 scFv была разработан, чтобы включить лидерную последовательность каппа цепи мыши, серин-глициновый линкер и c-myc тег (фигура 18). Эта конструкция scFv была клонирована в каркас ретровируса SFG, экспрессирующего CAR, нацеленного на CD19 человека или MUC-CD человека, который сигнализирует через C28 мыши и CD3zeta мыши, стимулируя тем самым Т-клетки мыши. Эти конструкции 19m28mz-IRES-J43 (фигура 19) и 4H11m28mz-IRES-J43 (фигура 20) используются для создания стабильных упаковочных линий Phoenix и генетически модифицированных первичных мышиных Т-клеток, как описано ранее (Lee et al., Cancer Res 2011, 71(8):2871). Мышиные Т-клетки 19m28mz и 19m28mz-IRES-J43 культивируют с опухолевыми клетками EL4 тимомы, которые были модифицированы для экспрессии CD19 человека и PD-L1 мыши, пролиферации мышиных Т-клеток для мониторинга числа жизнеспособных клеток и CFSE мечения.
Для мышиных Т-клеток, экспрессирующих на 4H11m28mz CAR, который нацелен на антиген MUC-CD, функцию можно оценить в ответ опухолевые клетки IDS, модифицированные для экспрессии MUC-CD и PD-L1 мыши (Chekmasova et al., Clin Cancer Res, 2010, 6:3594). Человеческий scFv, который связывает мышиный PD-1, как описано выше, клонируют в векторные конструкции SFG-19m28mz и 4H11m28mz и используют для модификации мышиных Т-клеток. Доступны сингенные модели для оценки in vivo противоопухолевых эффектов Т-клеток, модифицированных, чтобы экспрессировать scFv человека, который связывает мышиный PD-1: модели раковой опухоли яичника с использованием опухолевых клеток ID8-MUC-CD, которые привиты внутрибрюшинно в мышей C57BL/6; и трансгенные мыши, которые экспрессируют CD19 человека вместо CD19 мыши, которым привиты опухолевые клетки EL4 тимомы, модифицированные для экспрессии CD19 человека (Pegram et al, Blood 2012, 1 19(18):4133). Таким образом, противоопухолевый эффект может быть оценен в иммунокомпетентной модели, что дает возможность оценить влияние анти-PD-1 scFv на микроокружение опухоли.
Пример 4. Ко-экспрессия химерного антигенного рецептора (CAR) и агонистического scFv в иммунных клетках.
В одном варианте осуществления изобретение предоставляет иммунную клетку, которая экспрессирует антиген-связывающий рецептор (например, CAR или TCR), и одноцепочечный вариабельный фрагмент (scFv), который связывает антиген, обладающий агонистической иммуностимулирующей активностью (например, CD28, OX-40, 4-1ВВ и лиганды этого). Для создания агонистических scFv, нацеленных на костимулирующую молекулу 4-1BB, была получена гибридомная клеточная линия 3H3 (Shuford et al., J Exp Med 1997, 186:47-55; предоставленная профессором Миком Крофтом (La Jolla Институт аллергологии и иммунологии)). Для создания агонистических scFv, нацеленных на костимулирующую молекулу OX-40, была получена гибридомная клеточная линия OX-86 (al- Shamkhani et al., Eur J Immunoll996, 26(8): 1695-9; Европейская коллекция клеточных культур (Каталожный номер 96110601)). Гибридомную мРНК выделяли из клеток с использованием набора QIAgen RNAeasy, в соответствии с инструкцией производителя (QIAgen, Калифорния, США), и кДНК затем подготавливали с использованием New England Biolabs Protoscript AMV First strand cDNA synthesis kit в соответствии с инструкцией производителя (New England Biolabs, Массачусетс, США). Вариабельная тяжелая (VH) и легкая (VL) цепи затем ПЦР-амплифицировали с использованием следующих вырожденных праймеров:
Праймеры Orlandi (Orlandi et al., Proc. Natl. Acad. Sci. 1989, 86:3833-37)
VHFOR: 5'- tga gga gac ggt gac cgt ggt ccc tt gсс cca g -3' [SEQ ID NO:28]
VH1BACK: 5'- agg tsm arc tgc ags agt cwg g -3' [SEQ ID NO:29]
VKFOR: 5'- gtt aga tct cca gcttgg tcc c -3' [SEQ ID NO:30]
VK1BACK: 5'- gac att cag ctg acc cag tct cca -3' [SEQ ID NO:31]
Праймеры Cooper (Wang et al., Blood 2002, 99:2459-2467)
Vk 5'-GGCTGCAGSTTCAGTGGCAGTGGRTCWGGRAC-3' [SEQ ID NO:32],
Ck 5'-CTCATTCCTGTTGAAGCTCTTGACAATGGG-3' [SEQ ID O:33];
ПРАЙМЕРЫ RACE (Kettleborough et al., Eur. J Imrnunol 1993, 23:206-211)
VKfrla: Ata tcc atg gca gac gtc cag atg atc cag tct cca [SEQ ID NO:34]
Vkfrlb: ata tcc atg gca gac att gtg ctg act cag tct cc [SEQ ID NO:35]
Vkfrlc: ata tcc atg gca gat gtt gtg atg ace caa act cca [SEQ ID NO: 36]
Vkfrld: ata tcc atg gca caa att gtt ctc acc cag tct cc [SEQ ID NO:37]
Vkfrle: ata tcc atg gca gac att gtg atg aca cag tct cca [SEQ ID NO:38]
Vkfrlf: ata tcc atg gca gat att gtg atg acg cag gct gca [SEQ ID NO:39]
Vkfrl g: ata tcc atg gca gac att gtg atg acc cag tct c [SEQ ID NO:40]
Reverse Kappa: gct tca aca gga atg agt gtt aac teg agg tag [SEQ ID NO:41]
Чтобы собрать VH и VL в scFv, серин-глициновый линкер добавляют во время ПЦР цепей VH и VL, а также c-myc тег и цепь Ig каппа мыши или лидерную последовательность CDS. Полученный полинуклеотид клонируют в существующий ретровирусный вектор экспрессии (каркас SFG), кодирующий химерный антигенный рецептор (CAR) 1928z, для создания SFG-1928z-2А-3H3 или 1928z-2А-OX86.
Стабильные упаковочные клеточные линии создаются, как описано для J43 scFv против PD-1 мыши, и испытаны в подобной мышиной модели адаптивного Т-клеточный переноса.
Результаты, представленные в настоящем документе, указывают, что генетически модифицированные CAR Т-клетки, экспрессирующие молекулы scFv ("бронированные CART-клетки"), являются иммунореактивными и могут преодолевать "враждебное" опухолевое микроокружение, и, таким образом, являются эффективными при лечении неоплазии. CAR+ Т-клетки модифицируют для секретирования антагонистических scFvs с иммунными регуляторными функциями (фигура 21). При активации CAR родственным антигеном (1), бронированные CAR-модифицированные Т-клетки могут быть индуцированы, чтобы секретировать scFv, антагонистичные по отношению к ингибиторному PD-1 Т-клеточному рецептору как на инфузных CAR модифицированных Т-клетках, так и на эндогенные противоопухолевых Т-клетках, усиливая противоопухолевые эффекторные функции (2), индуцированной для секреции scFv, антагонистичных по отношению к ингибиторному CTLA-4 Т-клеточному рецептору как на инфузных CAR модифицированных Т-клетках, так и на эндогенные противоопухолевых Т-клетках, усиливая противоопухолевые эффекторные функции (3), или индуцированные, чтобы секретировать scFv, антагонистичные по отношению к рецептору CD47, экспрессируемому на опухолевой клетке, отменяя маскирование опухолевой клетки от распознавания со стороны врожденного противоопухолевого иммунного ответа хозяина, приводя к распознаванию и искоренению опухоли при помощи макрофагов хозяина.
Результаты, описанные ниже, были получены с использованием следующих способов и материалов, если не указано иное.
Создание анти-CD47 B6H12.2 scFv
Гибридомная линия клеток B6H12.2 была получена из американской коллекции тканевых культур (АТСС, VA, США; каталожный номер НВ-9771). мРНК B6H32.2 выделяли из гибридомных клеток, используя набор QIAgen RNAeasy, в соответствии с инструкции производителя (QIAgen, Калифорния, США), и кДНК получали с использованием New England Biolabs Protoscript AMV First strand cDNA synthesis kit, в соответствии с инструкцией производителя (New England Biolabs, Массачусетс, США). Вариабельные тяжелая (VH) и легкая (VL) цепи были ПЦР-амплифицированы с использованием праймеров, направленных на включение лидерной последовательности каппа, серин-глицинового линкера и c-myc тег (см. Фигура 1) следующим образом:
Праймер 1. Прямой праймер B6H12.2 VH [SEQ ID NO:42]:
5'- CCA TGG AGA CAG ACA CAC TCC TGC TAT GGG TAC TGC TGC TCT GGG TTC CAG GTT CCA CTG GTG ACG AGG TGC TGC AGC TGG TGG AGT CCG GGG -3'
Праймер 2. Обратный праймер B6H12.2 VH [SEQ ID NO:43]:
5'- AGA TCC ACC TCC ACC AGA TCC ACC TCC ACC TGA TCC ACC TCC ACC TGA GGA GAC GGT GAC TGA GGT TCC TTG ACC -3'
Праймер 3. Прямой праймер B6H12.2 VL [SEQ ID NO:44]:
5'- GGT GGA GGT GGA TCA GGT GGA GGT GGA TCT GGT GGA GGT GGA TCT GAC ATT GTG ATG ACT CAG TCT CCA GCC ACC -3'
Праймер 4. Обратный праймер VL B6H12.2 [SEQ ID NO:45]:
5'- CTC GAG TTA CAG ATC CTC TTC TGA GAT GAG TTT TTG TTG TTT GAT TTC CAG CTT GGT GCC TCC ACC GAA CG -3'
В дополнение к вышеприведенному дизайну, был создан scFv с последовательностью CD8L для определения эффективной лидерной последовательности для экспортации scFv из Т-клеток, используя следующий альтернативный прямой праймер:
Праймер 5. B6H12.2 VH CD8L прямой [SEQ ID NO:46]:
5'- TAT ACC ATG GCC TTA CCA GTG ACC GCC TTG CTC CTG CCG CTG GCC TTG CTG CTC CAC GCC GCC AGG CCG GAG GTG CAG CTG GTG GAG TCC GGG -3'
VH и VL ПЦР-продукты были клонированы в pCR2.1TOPO, в соответствии с инструкции производителя (Invitrogen, Нью-Йорк, США). Секвенирование с использованием праймеров M13F2 и M13R2 (Invitrogen) осуществляли в ведущей лаборатории MSKCC по секвенированию ДНК, чтобы подтвердить последовательность продуктов как VH и VL. Перекрывающийся ПЦР проводили с использованием ПЦР-продуктов VH и VL и праймеров 1 или 5 и 4, чтобы создать анти-CD47 scFv (см. фигура 1).
Конструкцию анти-CD47 scFv клонировали в существующий ретровирусный вектор экспрессии (каркас SFG), кодирующий химерный антигенный рецептор (CAR) 1928z, для получения SFG-1928z-2А-B6H12.2. ДНК SFG-1928z-2А-B6H12.2 секвенировали для подтверждения последовательности.
Получение стабильной упаковочной клеточной линии для Т-клеток человека
Для создания стабильных упаковочных клеточных линий, клетки H29 были транзиентно трансфицированы с использованием 10 мкг ДНК SFG-1928z-2А-B6HI2.2 при помощи Promega calcium phosphate transfection kit, в соответствии с инструкцией производителя (Promega). Супернатант от супернатанта H29 использовали для трансдукции клеток 293Glv9, которые впоследствии были суб-клонированы для получения стабильных упаковочных клеток. Отбор двух суб-клонов (клон 5 и клон 6) был основан на экспрессии как 1928z CAR, так и способности супернатанта 293Glv9 трансдуцировать Т-клетки периферической крови человека (как определено способом проточной цитометрии после окрашивания антителом 12dll). Трансдукцию Т-клеток периферической крови человека проводили, как описано ранее (Brentjens et al., Clin Cancer Res 2007, 13(18PtI):5426).
Оценка продуцирования/функции анти-CD47 scFv
Продуцирование анти-CD47 scFv из 1928z-2А-B6H12.2 293Glv9 и трансдукцию Т-клеток периферической крови человека определяли путем инкубации опухолевых клеток CD47+ (Raji и Nalm-6) в супернатанте от этих клеток. Опухолевые клетки затем промывали водой и окрашивали флуоресцентно конъюгированными антителами анти-c-myc тег (Cell Signaling, Массачусетс, США) для выявления полученного из супернатанта белка, связанного с опухолевыми клетками. Опухолевые клетки также окрашивали флуоресцентно конъюгированным анти-CD47 (клон B6H12.2, eBioscience) для детектирования способности B6H12 scFv блокировать CD47.
In vivo модель адаптивной передачи
Мышам вводили внутривенно 1×106 Nalm-6, модифицированных для экспрессии люциферазы Firefly (день 0). На 3 день мышей лечили при помощи 5,7×106 CAR+ Т-клеток, также инокулированных внутривенно. Рост опухоли контролировали клинически и с помощью биолюминесцентной визуализации, как описано ранее (Santos et al., Nature Medicine 2009, 15(3):338).
Получение 5C4 scFv против PD-1 человека
Последовательность антитела, которое специфически связывается с PD-1 человека, клон 5C4, была получена, как описано выше. Эта последовательность была модифицирована, чтобы включить лидерную последовательность каппа, серин-глициновый линкер и c-myc тег и приобретенное от GeneArt (Invitrogen, фигура 9). Клонирование этого scFv в SFG ретровирусный каркас, получение устойчивых упаковочных клеток, трансдукцию Т-клеток периферической крови человека и оценку эффективности трансдукции выполняли, как описано выше.
Оценка функции анти-PD-1 человека
PD-1 лиганд, PD-L1 ПЦР-амплифицировали из опухолевых клеток SKOV3 (АТСС), которые инкубировали с 200 нг/мл рекомбинантного интерферона-гамма человека (RnD systems, Миннесота, США). Праймеры, использованные для амплификации PD-L1 человека, приведены ниже:
Праймер 6. Прямой праймер к PD-L1 человека [SEQ ID NO:47]
5'- CACGTGCCATGGATGAGGATAT TTGCTGTCTT TATAT -3'
Праймер 7. Обратный праймер к PD-L1 человека [SEQ ID NO:48]
5'CTCGAGTTACGTCTCCTCCAAATGTGTATCACTTT3'
Последовательность PD-L1 человека была клонирована в SFG ретровирусный каркас, и трансдуцирована в клеточные линии 3Т3, Raji и Nalm-6, как описано ранее (Brentjens et al., Clin Cancer Res 2007, 13(18 Pt 1):5426). Клетки окрашивали анти-PD-L1 (клон MIH1, BD Pharmingen, Калифорния, США) и FACS-сортировали, чтобы обеспечить общую клеточную популяцию, экспрессирующую PD-L1 (фигура 14).
Т-клетки человека 1928z-2А-5C4 и 1928z культивировали с 3Т3 (CD19 В7.1/PD-L1) aAPC, и подсчет жизнеспособных клеток проводили с использованием исключения трипановым синим, и проточную цитометрию проводили для определения экспрессии CAR. Это коррелировало с размножением Т-клеток при культивировании с 3Т3 (CD19/В7.1) aAPC.
Получение scFv против PD-1 мыши
Была получена последовательность антитела, которое специфически связывается с мышиным PD-1, клон с названием J43, как описано выше. Эта последовательность была модифицирована, чтобы включить лидерную последовательность каппа цепи и последовательность тега c-myc, с серин-глициновым линкером, для образования scFv и закупки от GeneArt (Invitrogen, фигура 16). Она была клонирована в существующий ретровирусный вектор экспрессии (SFG), кодирующий мышиный CAR, где сигналинг опосредуется через молекулы CD28 и CD3 zeta мыши. 19m28mz-IRES-J43 и 4H11m28mz-IRES-J43 создавались для мишеней B-клетки и опухоли яичника, соответственно (рисунки 17 и 18).
Оценка функции анти-PD-1 мыши
Лиганд PD-1, PD-L1 ПЦР-амплифицировали из опухолевых клеток Renca (АТСС), праймеры, использованные для амплифицирования PD-L1 мыши, приведены ниже:
Праймер 8. Прямой праймер PD-L1 мыши [SEQ ID NO:49]
5'- TAT TAC ACG TGT TAC ATG AGG ATA TTT GCT GTC TTT -3'
Праймер 9. Обратный праймер PD-L1 мыши [SEQ ID NO: 50]
5' TAT AGG ATC CTC GAG GAT GTT ACG TCT CCT CCA AAT GTG TA 3'
scFv анти-PD-1 мыши клонировали в SFG ретровирусный каркас, и трансдуцировали в клеточные линии 3Т3 aAPC, IDS и EL4. Клетки, окрашенные scFv анти-PD-L1, (клон MIH1 BD Pharmingen), FACS-сортируют для обеспечения общей клеточной популяции, экспрессирующей PD-L1.
Тест на ЦТЛ-уничтожение по высвобождению хрома
Клетки-мишени, экспрессирующие желаемый антиген, метили 51Cr и совместно культивировали с Т-клетками при уменьшающихся соотношениях эффектор: мишень. После 4 часов культивирования, супернатант отбирали и использовали для измерения радиоактивности, высвобожденной из хрома. Специфический лизис определяли путем вычитания фона радиоактивности клеток-мишеней, не культивированных с клетками 25Т и деления на радиоактивность, измеренную от клеток-мишеней, полностью лизированных с помощью 0,2% Тритона Х-100.
Пример 5. Блокирование CD47 улучшает CAR Т-клеточную терапию.
Т-клетки могут быть генетически модифицированы для целевых опухолевых антигенов путем экспрессии химерного антигенного рецептора (CAR). Адоптивный перенос CD19-специфических CAR Т-клеток показал клиническую эффективность у некоторых пациентов со злокачественными опухолями кроветворной системы, однако пациенты с хроническим лимфоцитарным лейкозом с объемной лимфаденопатией имели субоптимальные ответы на CAR Т-клеточную терапию. Кроме того, CAR Т-клеточная терапия не продемонстрировал эффективности в отношении солидных опухолей в ходе клинических испытаний. В данном примере, клиническая эффективность CAR Т-клеток была повышена путем привлечения врожденного противоопухолевого иммунного ответа посредством секреции CD47-блокирующих одноцепочечных вариабельных фрагментов (scFv) из CAR Т-клеток. Предыдущие исследования показывают, что блокирование взаимодействие между CD47 на опухолевых клетках и SIRPa на макрофаги приводит к фагоцитозу опухолевых клеток. Чтобы использовать этот эффект, Т-клетки были модифицированы, чтобы экспрессировать CD19-специфичный CAR (1928z) и секретировать scFv, специфичный для CD47 человека, клонированных из гибридомы B6H12.2 (Т-клетки 1928z/B6H12.2). Т-клетки 1928z B6H12.2, как было показано, секретируют функциональный scFv, специфичный для CD47 человека, который не влияет на CAR-опосредованную секрецию цитокинов или цитотоксичность in vitro. Супернатант от Т-клеток 1928z/B6H12.2, но не от Т-клеток 1928z стимулировали макрофаги к фагоцитозу опухолевых клеток in vitro. Адоптивный перенос Т-клеток 1928z/B6H12.2 опосредовал усиленные противоопухолевые эффекты и уничтожал опухоли Nalm6 в доклинической мышиной модели. Этот новая стратегия сочетает в себе эффекты, опосредованные CAR Т-клетками, и уничтожение опухолевых клеток, опосредованное природными иммунными клетками, в сторону повышения противоопухолевой эффективности CAR Т-клеточной терапии.
Пример 6. Повышение противоопухолевой эффективности химерный антигенный рецептор модифицированных Т-клеток посредством конститутивной экспрессии CD40L.
Адоптивная клеточная терапия при помощи генетически модифицированных Т-клеток, экспрессирующих химерный антигенный рецептор (CAR), является многообещающей терапией для пациентов с В-ALL. Однако, в большинстве клинических испытаний CAR-модифицированных Т-клетки не сумели продемонстрировать значительный терапевтический эффект, особенно в контексте B-клеточных злокачественных новообразований и солидных опухолей низкого ранга. В экспериментах, представленных в данном разделе примеров, мы дополнительно повышаем противоопухолевую эффективность CAR-модифицированных Т-клеток путем конструирования Т-клеток, конститутивно экспрессирующих лиганд CD40 (CD40L, CD-154). Т-клетки, модифицированные, чтобы конститутивно экспрессировать CD40L (CD40L-модифицированные Т-клетки), увеличивали пролиферацию и секрецию провоспалительных TH1-цитокинов. Далее, CD40L-модифицированные Т-клетки усиливали иммуногенность CD40+ опухолевых клеток путем активации костимуляторных молекул (CD80 и CD86), молекул адгезии (CD54, CD58 и CD70), HLA-молекул (класса I и HLA-DR) и FAS-рецептора смерти (CD95) на поверхности опухолевой клетки. Кроме того, CD40L-модифицированные Т-клетки индуцировали созревание и стимулировали секрецию провоспалительного цитокина IL-12 полученными из моноцитов дендритными клетками. Наконец, опухоль-нацеленные CAR/CD40L Т-клетки повышали цитотоксичность против CD40+ опухолей и удлиняли выживание несущих опухоли мышей в ксенотрансплантатной модели системной лимфомы. Эти предклинические данные подтверждают клиническое применение CAR Т-клеток, дополнительно модифицированных, чтобы конститутивно экспрессировать CD40L, с ожидаемой повышенной противоопухолевой эффективностью и улучшением клинических исходов.
Материалы и способы
Клеточные культуры
Опухолевые клеточные линии DoHH2, Raji и NALM-6 (американская коллекция типовых культур) поддерживали в среде RPMI 1640 (Gibco) с добавлением 10% инактивированной прогреванием эмбриональной бычьей сыворотки (FBS), заменимых аминокислот, пирувата натрия, буфера HEPES (N-2- гидроксиэтилпиперазин-N'-2-этансульфоновая кислота) и 2-меркаптоэтанола (Invitrogen). Ретровирусные продуцирующие клеточные линии 293GP-GLV9 были описаны ранее, и их культивировали в среде DMEM (Invitrogen) с добавлением 10% FBS29. NIH-3Т3 искусственные антиген-представляющие клетки (AAPC) культивировали в среде DMEM, дополненной 10% инактивированной прогреванием донорской телячьей сыворотки (РС), как описано ранее30. Т-клетки человека выделяли из периферической крови здоровых доноров по IRB-утвержденному протоколу 95-054 Мемориального Слоун-Кеттерингского онкологического центра (MSKCC), используя CPT-пробирки вакуумного контейнера BD (Бектон Дикинсон) в соответствии с инструкциями производителя. Т-клетки и клетки CLL пациента получали от пациентов, проходящих лечение по IRB-утвержденному протоколу 06-138 MSKCC, и выделяли с помощью бус Dynabeads ClinExVivo CD3/CD28 (Invitrogen). Т-клетки культивировали в среде RPMI 1640, дополненной 10% FBS и 20 ед/мл IL-2 (R&D Systems). Полученные из моноцитов дендритные клетки (moDC) получали из культуры ткани прилипших к пластику мононуклеарных клеток периферической крови (PBMC) здоровых доноров и культивировали в среде RPMI 1640 с добавлением 1% объединенной человеческой А/В сыворотки, HEPES-буфера, 2-меркаптоэтанола (Invitrogen), интерлейкина-4 (IL-4; 500 МЕ/мл - R&D Systems) и гранулоцитарно-моноцитарного колониестимулирующего фактора (GM-CSF; 1000 МЕ/мл - R&D Systems), как описано ранее.31 Все среды были дополнены 2 ммоль/л L-глутамина (Invitrogen), 100 единиц/мл пенициллина и 100 г/ мл стрептомицина (Invitrogen).
Конструирование ретровирусных конструкций
кДНК CD40L человека ПЦР-амплифицировали из выделенных от здоровых доноров PBMC, используя следующие праймеры (1) 5'- CACGTGCATGATCGAAACATACAACCAAACTTCTCCCCGATCTGC-'3 [SEQ ID NO: 3] и (2) 5 '-CTCGAGGGATCCTCAGAGTTTGAGTAAGCCAAAGGA - 3' [SEQ ID NO:4] (фигура 22А). Гамма-ретровирусный вектор, кодирующий CD40L, человека был сконструирован с использованием SFG векторного каркаса32. Конструкция 1928z и Pz1 (анти-простатический специфический мембранный антиген CAR; анти-PSMA) SFG-вектор уже были описаны ранее33,34. Конструкция 1928z-IRES-40L и Pz1 IRES-40L гамма-ретровирусного вектора была создана с помощью перекрывающегося ПЦР (фигура 26А).
Ретровирусная трансдукция T-лимфоцитов человека
Получение стабильных ретровирусных продуцирующих клеточных линий 293GP-GLV9 и генетическая модификация Т-клеток человека было описано ранее29,36. Для Т-клеточной трансдукции выделенные от здоровых доноров PBMC были активированы фитогемагглютинином (PHA) на 2 мкг/мл (Sigma), в то время как полученные от пациента Т-клетки выделяли, активировали и наращивали с помощью бус Dynabeads ClinExVivo CD3/CD28 в соответствии с рекомендациями производителя. Активированные Т-клетки были ретровирусно трансдуцированы на покрытых ретронектином, обработанных нетканевой культурой планшетах, как описано выше36. Перенос генов оценивали на 7-е сутки способом проточной цитометрии. Контрольные имитационно-трансдуцированные Т-клетки были получены таким же образом, за исключением того, что супернатант был получен из пустых клеточных культур 293GP-GLV9. Пролиферацию CD40L-модифицированных Т-клеток оценивали c использованием счетчика клеток guava®easyCyte™ при помощи реагента guava®ViaCount (EMD Miliipore) в соответствии с инструкциями производителя. Размножение модифицированных Т-клеток для экспериментов in vivo проводили с использованием AAPC, полученных от NIH-3Т3 фибробластов мыши, генно-инженерно измененных для экспрессии антигенов-мишеней (CD19 или PSMA) вместе с костимуляцией (CD80), как описано ранее.
Анализы совместного культивирования
Опухолевые клетки (DOHH2, Raji, Ph+, ALL 3.1, NALM-6) совместно культивировали в соотношении 5:1 с CD40L-модифицированными Т-клетками и имитационно-трансдуцированными Т-клетками. Проточная цитометрия проводилась через три дня для определения фенотипа опухолевых клеток. moDC (2,5×105) совместно культивировали с аутологичными CD40L-модифицированными Т-клетками или имитационно-трансдуцированными Т-клетками в соотношении 1:5, и супернатант культуры ткани анализировали через 24 часа на IL-12p70 в системе Luminex IS100 (см. ниже). moDCs также совместно культивировали в соотношении 5:1 с CD40L-модифицированными Т-клетками и имитационно-трансдуцированными Т-клетками, и фенотип moDC анализировали способом проточной цитометрии через 24 часа.
Анализ цитотоксичности
Цитолитическая способность трансдуцированных Т-клеток определяли с использованием стандартного анализа высвобождения 51Cr, как описано ранее34.
Тестирование детекции цитокинов
Детектирование цитокинов в супернатанте культуры ткани оценивали с помощью системы детекции цитокинов человека MILLIPLEX (Корпорация Miliipore) совместно с системой Luminex IS100 и программным обеспечением IS 2.3 (Корпорация Luminex), следуя инструкциям изготовителя.
Проточная цитометрия
Проточную цитометрию проводили с использованием цитофлуориметра FACScan, и данные анализировали с использованием программного обеспечения FlowJo версии 9.2 (Tree Star). Экспрессию CAR детектировали с помощью CAR специфического моноклонального антитела армянского хомяка 19E3 (1928z) и 12D11 (1928z и Pz1, лаборатория моноклональных антител MSKCC). Экспрессию CD40L детектировали с помощью мышиных анти-CD154 человека (BD Biosciences). Т-клетки человека также окрашивали мышиными анти-CD3 человека (BD Biosciences), CD4 и CD8 (Invitrogen). moDC окрашивали, используя мышь анти-человеческого CD11b, HLA-DR, CD83 и CD86 (Invitrogen). Фенотип опухолевых клеток DOHH2, Raji и NALM6 детектировали с помощью мышиного антитела к CD19 человека, CD40, CD54, CD80, CD86, HLA-I класса и HLA-DR (Invitrogen), CD58, CD70 и CD95 (BD Biosciences).
In vivo исследования CAR Т-клеток
Мы инокулировали 8-12 недельных мышей SCID-Beige (CB17.Cg-PrkdcscidLystbg-J/Cr1) (Charles River Laboratories) опухолевыми клетками DOHH2 (5×105 клеток) путем внутривенной инъекции. Два дня спустя мышам вводили внутривенно трансдуцированные Т-клетки (1×107 CAR Т-клеток). Рост опухоли контролировали клинически, и мышей усыпляли, когда болезнь становилась очевидной клинически (развитие паралича задних конечностей или снижение реакций на стимулы). Все исследования на мышах были проведены в соответствии с утвержденным протоколом (00-05-065) институционального комитета по уходу за животными и их использованию Мемориального Слоан-Кеттерингского онкологического центра.
Статистический анализ
Все анализы были рассчитаны с использованием программного обеспечения Graphpad Prism 5.0, данные выживаемости оценивали с использованием лог-рангового анализа и все другие анализы проводили с использованием теста Манн - Уитни (односторонний).
Результаты
Конститутивная экспрессия CD40L T-клетками человека
Мы изначально трансдуцировали Т-клетки от здоровых доноров ретровирусным вектором CD40L (фигура 22А). Ретровирусная трансдукция Т-клеток с помощью гена CD40L обычно приводила к >40% генному переносу со стабильной экспрессией CD40L в субпопуляциях как CD4+, так и cd8+ Т-клеток (фигура 22Б). Пролиферация CD40L-модифицированных Т-клеток была значительно увеличена по сравнению имитационно-трансдуцированными Т-клетками, полученных от тех же трех доноров (фигура 22С). Среду культуры ткани от CD40L-модифицированных Т-клеток анализировали, и было показано значительное увеличение растворимого CD40L (sCD40L), как ожидалось, а также значительное увеличение секреции провоспалительных цитокинов IFN-γ и GM-CSF по сравнению имитационно-трансдуцированными Т-клетками (фигура 22Е).
CD40L-модифицированные Т-клетки меняют фенотип как опухолевых клеточных линий CD40+, так и полученных от пациентов CLL- клеток
Для исследования способности пути CD40L/CD40 модифицировать фенотип опухолевых клеток выполняли совместное культивирование B-клеточных опухолевых клеток CD40+ и CD40L-модифицированных Т-клеток или имитационно-трансдуцированных Т-клеток. Культивирования с CD40L - модифицированными Т-клетками, но не с имитационно-трансдуцированными Т-клетками приводили к повышению активности костимуляторных молекул (CD80 и CD86), молекул адгезии (CD54, CD58 и CD70), молекул HLA-класса (HLA класса I и HLA-DR) и рецептора гибели FAS (CD95) на поверхности опухолевых клеток DOHH2 (фигура 23 А). Фенотипические изменения также очевидны, когда DOHH2 опухолевые клетки культивируют в кондиционированных средах от CD40L-модифицированной Т-клетки, которая содержит повышенные уровни sCD40L (фигура 28). Чтобы определить, является ли CD40 экспрессия на опухолевой клетке необходимым условием изменения фенотипа опухолевой клетки, проводили совместное культивирование CD40-опухолевой клеточной линии (NALM6) с CD40L-модифицированными Т-клетками и имитационно-трансдуцированными Т-клетками. Эти исследования показали отсутствие изменений в фенотипе, демонстрируя необходимость экспрессии CD40 в опухоли для индуцирования CD40L-опосредованных изменений фенотипа опухолевых клеток (фигура 23В).
Для проведения дальнейшей проверки этого эффекта в клинически релевантной постановке мы совместно культивировали CD40L-модифицированные Т-клетки, полученные от пациентов с CLL, с аутологичными опухолевыми клетками CLL. Ретровирусная трансдукция Т-клеток, полученные от пациентов с CLL, приводила к >40% переносу генов со стабильной экспрессией гена CD40L (фигура 24А). В такой постановке полученные от пациента CD40L-модифицированные Т-клетки, но не имитационно-трансдуцированные Т-клетки, демонстрировали способность увеличения активности костимуляторных молекул, молекул клеточной адгезии, молекул HLA класса и Fas-рецепторов смерти на поверхности аутологичных CLL-клеток (фигура 24Б).
CD40L-модифицированные Т-клетки индуцируют секрецию IL-12p70 и опосредуют созревание moDC
Учитывая роль CD40L в созревании DC и секреции провоспалительного цитокина IL-12, далее мы исследовали, могут ли CD40L-модифицированные Т-клетки вызывать тот же эффект в случае совместного культивирования с аутологичными moDC. Существенно, мы обнаружили индуцированную CD40L-модифицированными Т-клетками секрецию Il-12p70 в совместных культурах, содержащих moDC и аутологичные CD40L-модифицированные Т-клетки от трех отдельных доноров (фигура 25А). Созревание moDC, как определяется по увеличению активности поверхностных костимуляторных молекул (HLA-DR, CD86 и CD83) также было отмечено после совместного культивирования с CD40L-модифицированными Т-клетками, но не после совместного культивирования имитационно-трансдуцированными Т-клетками (фигура 25В).
Экспрессия как CAR, так и CD40L Т-клетках приводит к усилению цитотоксичности in vitro и in vivo
Далее мы провели оценку способности Т-клеток экспрессировать как анти-CD19 CAR (1928z), так и CD40L с помощью бицистронного ретровирусного вектора (1928z/CD40L; фигура 26А). Трансдукция Т-клеток обычно приводила к >40% экспрессии как 1928z, так и CD40L (Т-клетки 1928z/CD40L; фигура 26В). Также были созданы контрольные ретровирусные векторы, содержащие анти-CD19 CAR (1928z) и анти-PSMA CAR (Pz1 и Pz1/CD40L; фигура 26В). Для оценки противоопухолевой активности in vitro 1928z CD40L Т- клеток проводили стандартный 4 часовой анализ высвобождения 51Cr. Конститутивная экспрессия CD40L статистически повышала литическую способность 1928z Т-клеток против CD19+ опухолевых клеток, по сравнению с группой контрольных Т-клеток, включая Т-клетки, модифицированные для экспрессии только 1928z CAR (фигура 26С). Усиленная цитотоксичность также демонстрируется в отношении других CD19+/CD40+ опухолевых клеточных линий (фигура 29).
Для исследования противоопухолевой активности in vivo 1928z/CD40L Т-клеток мы использовали ксенотрансплантную модель системного DOHH2-лимфомы. Мы ранее отмечали, что системные DOHH2 опухолевые клетки заметно устойчивы к CD19-мишенной CAR Т-клеточной терапии у SCID-Beige мышей. Чтобы оценить, может ли дальнейшая модификация CAR Т-клеток с помощью CD40L усиливать противоопухолевую эффективность в этой модели, мы прививали и лечили по SCID-Beige мышей, несущих системную опухоль DOHH2, с использованием CAR/CD40L Т-клеток. Существенно, лечение с использованием 1928z/CD40L Т-клеток по сравнению с лечением 1928z Т-клетками или контрольными Т-клетками (Pz1 и Pz1/CD40L Т-клетки) показало увеличенный выживания и приводило к долговременной выживаемости у 30% мышей, получавших 1928z/40L Т-клетки (фигура 27).
Обсуждение
Адоптивная терапия с использованием CAR Т-клеток продемонстрировала многообещающие клинические реакции у пациентов с В-клеточными злокачественными опухолями2-4. Эти исследования продемонстрировали эффективность CAR Т-клеток в качестве единой противоопухолевой эффекторной клетки. Однако такой подход может иметь ограниченный успех против опухолей с надежным иммуносупрессивным микроокружением опухоли5. Кроме того, в своем нынешнем виде CAR Т-клетки не продемонстрировали способность реагировать на ускользание опухоли после потери антигена-мишени.6 Одним возможным способом преодоления этих ограничений является дальнейшее конструирование CAR Т-клеток посредством конститутивной экспрессии CD40L в усилии по совершенствованию Т-клеточный цитолитического потенциала/пролиферации, усиления иммуногенности опухоли и улучшения DC представления антигена/функции. Модификация CAR Т-клеток посредством конститутивной экспрессии CD40L может также дополнительно активировать эндогенный иммунный ответ, усиливая противоопухолевую эффективность.
Чтобы оценить роль конститутивной экспрессии CD40L Т-клетками, мы сначала разработали ретровирусный вектор, содержащий ген CD40L только. При трансдукции в Т-клетки была продемонстрирована конститутивная экспрессия как в CD4+, так и CD8+ Т-клеточных подмножествах (фигура 22В). Хотя и чаще ассоциируется с СД4+ Т-клетками, недавно сообщалось об экспрессии CD40L и хелперной функции в CD8+ Т-клетках памяти37. CD40L экспрессия, как известно, также повышает Т-клеточную пролиферацию и секрецию провоспалительных TH1-цитокинов (IFN-γ, GM-CSF).21-22 CD40L-модифицированные Т-клетки демонстрируют способность к секреции провоспалительных цитокинов и усиленной пролиферации, по сравнению с аналогичным образом активируемыми, но имитационно-трансдуцированными Т-клетками от того же донора (фигуры 22С и 22D). Оснащение Т-клеток посредством конститутивной экспрессии CD40L имеет потенциал для усиления их противоопухолевой функции/активации.
Подавление белков клеточной поверхности, включая HLA класса I, ко-стимулирующие молекулы и/или молекулы адгезии, часто используется опухолями для избежания иммунного распознавания.5,38,39 Апоптотическая устойчивость может также происходить с потерей Fas рецептора смерти на поверхности злокачественных клеток40. Чтобы избежать этого, CD40L может взаимодействовать с CD40 на злокачественных клетках, чтобы опосредовать увеличение активности костимуляторных молекул (CD80 и CD86), молекул адгезии (CD54, CD58 и CD70), молекул HLA класса (HLA класса I и HLA-D ) и способствовать апоптозу через Fas/FasL путь на злокачественных В-клеточных опухолях41,42. CD40L-модифицированные Т-клетки изменяли фенотип CD40+ опухолевых клеток, приводя в результате к усилению активности этих важнейших поверхностных белков, тем самым противодействуя способности опухолевых клеток к иммунному уклонению (Фигура 2). Этот эффект зависит от экспрессии CD40 опухолевыми клетками, поскольку фенотипические изменения отсутствовали в случае, когда CD40-опухолевые клетки совместно культивировали с CD40L-модифицированными Т-клетками (фигуры 23А-В). Этот эффект был также замечен в более клинически релевантной постановке, в которой совместно культивированные CD40L-модифицированные Т-клетки, полученные от CLL-пациентов, усиливали иммуногенность аутологичных CLL-клеток (фигуры 24А-В). Этот вывод демонстрирует сохраненную способность Т-клеток усиливать иммуногенность аутологичных опухолевых клеток посредством конститутивной экспрессии CD40L. Важно, что межклеточный контакт не является необходимым для изменения фенотипа опухолевых клеток, поскольку среда, содержащая повышенные уровни sCD40L, приводила к сходным фенотипическим изменениям (фигура 28). Увеличение иммуногенности опухолевых клеток через путь CD40L/CD40, как было показано, индуцирует эндогенный противоопухолевый ответ в ранее опубликованных исследованиях вакцины с помощью инфузии аутологичных опухолевых клеток CLL, трансдуцированных аденовирусным вектором, кодирующим CD40L (ad-CD40L клетки CLL).27,28 Инфузия опухоль-специфичных Т-клеток, дополнительно модифицированных, чтобы конститутивно экспрессировать CD40L, могла тоже обладать подобной способностью индуцировать эндогенный противоопухолевый ответ. Это может привести к распространению эпитопа через привлечение эндогенной противоопухолевой Т- или NK-клетки, тем самым ограничивая способность ускользания опухолей через подавление отдельного антигена-мишени.
Функция дендритных клеток (DC) затруднена в микроокружении опухоли. Обычно DC доводят до зрелости, перемещают и представляют антиген в лимфатических узлах, тем самым стимулируя адаптивную ветвь иммунной системы на наличие малигнизации или патогена5. При этом DC, подвергшиеся воздействию подавляющего микроокружения опухоли, имеют парадоксальную функцию индуцирования Tregs и толерогенных опухоль-специфических Т-клеток43. Во избежание этого, путь CD40L/CD40 может повысить DC- представление антигена, продукцию провоспалительного цитокина IL-12 и содействовать цитотоксической функции cd8+ Т-клеток19,20. Агонистические CD40-антитела, как ранее было показано, активируют DC и повышают CD8+ Т-клеточный ответ, заменяя тем самым необходимость СД4+ Т-клеточной помощи.26 Кроме того, CD40L-модифицированные опухоле-специфические CD8+ Т-клетки, как было показано, стимулируют созревание DC и усиливают противоопухолевые реакции адоптивно переданных CD8+ Т-клеток в опухоль-несущих мышах44. Для проверки способности CD40L-модифицированных Т-клеток усиливать функцию DC человека, был использован эксперимент по совместному культивированию in vitro с аутологичными moDC. Существенно, что CD40L - модифицированные Т-клетки стимулировали секрецию IL-12p70 из moDC (фигуры 25А-В). IL-12 является плейотропным цитокином с несколькими иммуно-стимулирующими функциями, в том числе способностью усиливать пролиферацию Т-клеток, цитотоксическую возможность и опосредовать устойчивость к Treg подавлению, как уже было ранее показано нами и другими7,45. Способность CAR/40L Т-клеток к стимуляции продуцирования IL-12 от DC может перевести на улучшенное противоопухолевое действие адоптивно переданных CAR Т-клеток, а также привлечение и активацию эндогенных опухолеспецифических Т-клеток и естественных киллерных (NK) клеток. Путем стимуляции продуцирования IL-12 в непосредственной близости от опухоли мы ожидаем минимальную, связанную с IL-12 токсичностью, в отличие от предыдущих исследований, показывавших тяжелый токсикоз после системного введения IL-12. В дополнение к стимуляции продуцирования IL-12, CD40L-модифицированные Т-клетки стимулируют созревание DC, которое в контексте CAR Т-клеточной цитотоксичности должно дополнительно усиливать DC поглощению опухолевого антигена и представление, приводящее в результате к привлечению/активации эндогенного противоопухолевого ответа при помощи эффекторных Т-клеток и NK-клеток (фигуры 25А-В). Взятые вместе, усиленная DC функция должна приводить к усиленной противоопухолевой эффективности генно-модифицированных опухолеспецифических Т-клеток через привлечение эндогенного противоопухолевого иммунного ответа.
Способность CAR Т-клеток перенаправлять специфичность Т-клеток была продемонстрирована в ряде доклинических и клинических отчетов.1 Мы разработали ретровирусный вектор, содержащий анти-CD19 CAR (1928z) и ген CD40L (фигура 28А). Конститутивная экспрессия как 1928z, так и CD40L Т-клетками легко достижима (фигура 28В). Существенно, при тестировании цитотоксического потенциала 1928z/40L Т-клеток в отношении панели из CD19+ мишеней мы отмечали повышенную цитотоксичность по сравнению с Т-клетками, модифицированными лишь 1928z CAR (фигура 28С). Недавно, Лорэн и его коллеги сообщили о повышенной цитотоксичности CAR Т-клеток против линий опухолевых клеток после CD40/IL-4 зависимого усиления активности поверхностных молекул адгезии, что могло бы также объяснять повышенную цитотоксичность, наблюдаемую в наших экспериментах46. Для проверки in vivo потенциала CAR/CD40L Т-клеток применяли ксенотрансплантатную модель с использованием клеточной линии агрессивной трансформированной фолликулярной лимфомы DOHH2. Эта модель была исторически устойчива к радиации за счет 1928z Т-клеток (фигура 27). Однако, с дополнительной модификацией CD40L наши 1928z/CD40L Т-клетки увеличивали выживаемость опухоле-несущих мышей по сравнению с мышами, получавшими лишь 1928z Т-клетки, и приводили в результате к 30% удлинению выживания в группе, проходившей лечение 1928z/CD40L Т-клетками (фигура 27). Несмотря на то, что эта модель демонстрирует разницу в выживаемости, отсутствие компетентной иммунной системы у SCID-Beige мышей делает данную модель непригодной для исследования максимального преимущества, которое конститутивная экспрессия CD40L в CAR Т-клеток может иметь в ликвидации раковых опухолей. Несмотря на то, что мы наблюдаем усиленную противоопухолевую эффективность в нашей модели, это, вероятно, вызвано усилением цитотоксичности CAR Т-клеток за счет аутокринного/паракринного CD40/CD40L пути, а не посредством привлечения/активации эндогенного иммунного ответа за счет CD40L-модифицированных CAR Т-клеток. Иммунно-компетентная сингенная опухолевая модель может быть использована для исследования полного эффекта конститутивной экспрессии CD40L CAR Т-клетками в микроокружении опухоли и привлечения эндогенных противоопухолевых иммунных реакций. Недавно была разработана Иимунно-компетентная сингенная модель CD19+ B-клеточного злокачественного новообразования человека, и используется для оценки 1928z/CD40L Т-клеток в контексте компетентной иммунной системы.
Конститутивная экспрессия CD40L клетками костного мозга или тимуса, как было показано, приводит в результате к Т-лимфопролиферативным расстройствам после инфузии в CD40L-дефицитных мышей47. Клоновые популяции, которые возникли в пределах тимуса после непрерывной CD40L стимуляции тимоцитов, могут привести к злокачественной трансформации (а не к инсерционному онкогенезу CD40L-модифицированных клеток). Хотя мы уже отмечали минимальную токсичность и отсутствие злокачественной трансформации после инфузии CAR/CD40L Т-клеток, учитывая опасения по поводу злокачественной Т-клеточной трансформации, эффективный "суицидный" ген, такой как iCasp9, может, в соответствии с желанием, быть включен в ретровирусный вектор48.
Ссылки для Примера 6
1. Curran KJ, Pegram HJ, Brentjens RJ. Chimeric antigen receptors for T cell immunotherapy: current understanding and future directions. J Gene Med. 2012; 14(6):405- 15.
2. Brentjens RJ, Davila ML, Riviere I, et al. CD19-Targeted T Cells Rapidly Induce Molecular Remissions in Adults with Chemotherapy-Refractory Acute Lymphoblastic Leukemia. Sci Transl Med. 2013;5(177): 177ra138.
3. Brentjens RJ, Riviere I, Park JH, et al. Safety and persistence of adoptively transferred autologous CD19-targeted T cells in patients with relapsed or chemotherapy refractory B-cell leukemias. Blood. 2011; 118(18):4817-4828.
4. Porter DL, Levine BL, alos M, Bagg A, June CH. Chimeric antigen receptor-modified T cells in chronic lymphoid leukemia. N Engl J Med. 2011;365(8):725-733.
5. Vesely MD, Kershaw MH, Schreiber RD, Smyth MJ. Natural innate and adaptive immunity to cancer. Annu Rev Immunol. 2011;29:235-271.
6. Grupp SA, Kalos M, Barrett D, et al. Chimeric antigen receptor-modified T cells for acute lymphoid leukemia. N Engl J Med. 2013;368(16): 1509-1518.
7. Pegram HJ, Lee JC, Hayman EG, et al. Tumor-targeted T cells modified to secrete IL-12 eradicate systemic tumors without need for prior conditioning. Blood. 2012;119(18):4133-4141.
8. Armitage RJ, Fanslow WC, Strockbine L, et al. Molecular and biological characterization of a murine ligand for CD40. Nature. 1992; 357(6373):80-82.
9. Schonbeck U, Libby P. The CD40/CD154 receptor/Hgand dyad. Cell Mol Life Sci. 2001; 58(l):4-43.
10. Uckun FM, Gajl-Peczalska K, Myers DE, Jaszcz W, Haissig S, Ledbetter JA. Temporal association of CD40 antigen expression with discrete stages of human B-cell ontogeny and the efficacy of anti-CD40 immunotoxins against clonogenic B- lineage acute lymphoblastic leukemia as well as B-lineage non-Hodgkin's lymphoma cells. Blood. 1990;76(12):2449-2456.
11. Grass HJ, Ulrich D, Braddy S, Armitage RJ, Dower SK. Recombinant CD30 ligand and CD40 ligand share common biological activities on Hodgkin and Reed-Sternberg cells. Eur J Immunol. 1995;25(7):2083-2089.
12. Zong YS, Lin H, Choy DT, et al. Nasopharyngeal carcinoma and lymphoinfiltration. Oncology. 1991; 48(4):290-296. 13. Lollini PL, Landuzzi L, Frabetti F, et al. Expression of functional CD40 on human osteosarcoma and Ewing's sarcoma cells. Clin Cancer Res. 1998 4(8): 1843- 1849.
14. van den Oord JJ, Maes A, Stas M, et al. CD40 is a prognostic marker in primary cutaneous malignant melanoma. Am J Pathol. 1996; 149(6): 1953-1961.
15. Wingett DG, Vestal RE, Forcier K, Hadjokas N, Nielson CP. CD40 is functionally expressed on human breast carcinomas: variable inducibility by cytokines and enhancement of Fas-mediated apoptosis. Breast Cancer Res Treat. 1998; 50(l):27-36.
16. Ciaravino G, Bhat M, Manbeian CA, Teng NN. Differential expression ofCD40 and CD95 in ovarian carcinoma. Eur J Gynaecol Oncol. 2004; 25(l):27-32.
17. Altenburg A, Baldus SE, Smola H, Pfister H, Hess S. CD40 ligand-CD40 interaction induces chemokines in cervical carcinoma cells in synergism with IFN- gamma. J Immunol. 199; 1 2(7):4140-4147.
18. Grewal IS, Flavell RA. CD40 and CD 154 in cell-mediated immunity. Annu Rev Immunol. 1998; 16: 111-135.
19. Cella M, Scheidegger D, Palmer-Lehmann K, Lane P, Lanzavecchia A, Alber G. Ligation of CD40 on dendritic cells triggers production of high levels of interleukin-12 and enhances T cell stimulatory capacity: T-T help via APC activation. J Exp Med. 1996;184(2):747-752.
20. Clarke SR. The critical role of CD40/CD40L in the CD4-dependent generation of CD8+ T cell immunity. J Leukoc Biol. 2000; 67(5):607-614.
21. Cayabyab M, Phillips JH, Lanier LL. CD40 preferentially costimulates activation of CD4+ T lymphocytes. J Immunol. 1994; 152(4): 1523-1531.
22. Peng X, Kasran A, Warmerdam PA, de Boer M, Ceuppens JL. Accessory signaling by CD40 for T cell activation: induction of Thl and Th2 cytokines and synergy with interleukin-12 for interferon-gamma production. Eur J Immunol. 1996; 26(7):1621-1627.
23. Bhadra R, Gigley JP, Khan IA. Cutting edge: CD40-CD40 ligand pathway plays a critical CD8-intrinsic and -extrinsic role during rescue of exhausted CDS T cells. J Immunol. 2011; 187(9). 4421-4425.
24. Bourgeois C, Rocha B, Tanchot C. A role for CD40 expression on CD8+ T cells in the generation of CD8+ T cell memory. Science. 2002; 297(5589):2060- 2063.
25. Khong A, Nelson DJ, Nowak AK, Lake RA, Robinson BW. The use of agonistic anti-CD40 therapy in treatments for cancer. Int Rev Immunol. 2012; 31(4):246-266.
26. Vonderheide RH, Glennie MJ. Agonistic CD40 antibodies and cancer therapy. Clin Cancer Res. 2013; 19(5): 1035-1043.
27. Wierda WG, Cantwell MJ, Woods SJ, Rassenti LZ, Prussak CE, ipps TJ. CD40-ligand (CD154) gene therapy for chronic lymphocytic leukemia. Blood. 2000; 96(9):2917-2924.
28. Wierda WG, Castro JE, Aguillon R, et al. A phase I study of immune gene therapy for patients with CLL using a membrane- stable, humanized CD 154. Leukemia. 2010; 24(11):1893-1900.
29. Ghani K, Wang X, de Campos-Lima PO, et al. Efficient human hematopoietic cell transduction using RD114- and GALV-pseudotyped retroviral vectors produced in suspension and serum-free media. Hum Gene Ther. 2009; 20(9):966-974.
30. Brentjens RJ, Latouche JB, Santos E, et al. Eradication of systemic B-cell tuniors by genetically targeted human T lymphocytes co-stimulated by CD80 and interleukin-1. Nat Med. 2003;9(3):279-286.
31. Ratzinger G, Reagan JL, Heller G, Busam KJ, Young JW. Differential CD52 expression by distinct myeloid dendritic ceil subsets: implications for alemtuzumab activity at the level of antigen presentation in allogeneic graft-host interactions in transplantation. Blood. 2003; 101 (4): 1422-1429.
32. Riviere I, Brose K, Mulligan RC. Effects of retroviral vector design on expression of human adenosine deaminase in murine bone marrow transplant recipients engrafted with genetically modified cells. Proc Natl Acad Sci U S A. 1995;92(15):6733-6737.
33. Brentjens RJ, Santos E, Nikhamin Y, et al. Genetically targeted T cells eradicate systemic acute lymphoblastic leukemia xenografts. Clin Cancer Res. 2007;13(18 Pt 1):5426-5435.
34. Gong MC, Latouche JB, rause A, Heston WD, Bander NH, Sadelain M. Cancer patient T cells genetically targeted to prostate-specific membrane antigen specifically lyse prostate cancer cells and release cytokines in response to prostate- specific membrane antigen. Neoplasia. 1999;1(2):123-127.
35. Santos EB, Yeh R, Lee J, et al. Sensitive in vivo imaging of T cells using a membrane-bound Gaussia rinceps luciferase. Nat Med. 2009;15(3):338-344.
36. Quintas-Cardama A, Yeh RK, Hollyman D, et al. Multifactorial optimization of gammaretro iral gene transfer into human T lymphocytes for clinical application. Hum Gene Ther. 2007; 18(12): 1253-1260.
37. Frentsch M, Stark R, Matzmohr N, et al. CD40L expression permits CD8+ T cells to execute immunologic helper functions. Blood. 2013; 122(3):405-412.
38. Greaves P, Gribben JG. The role of B7 family molecules in hematologic malignancy. Blood. 2013; 121(5):734-744.
39. Geijtenbeek TB, van Kooyk Y, van Vliet SJ, Renes MH, Raymakers RA, Figdor CG. High frequency of adhesion defects in B-Iineage acute lymphoblastic leukemia. Blood. 1999; 94(2):754-764.
40. Rieux-Laucat F, Le Deist F, Hivroz C, et al. Mutations in Fas associated with human lymphoproliferative syndrome and autoimmunity. Science. 1995; 268(5215):1347-1349.
41. Schultze JL, Cardoso AA, Freeman GJ, et al. Follicular lymphomas can be induced to present alloantigen efficiently: a conceptual model to improve their tumor immunogenicity. Proc Natl Acad Sci U S A. 1995;92(18):8200-8204.
42. Schattner EJ, Mascarenhas J, Bishop J, et al. CD4+ T-cell induction of Fas-mediated apoptosis in Burkitt's lymphoma B cells. Blood. 1996; 88(4): 1375-1382.
43. O'Neill DW, Adams S, Bhardwaj N. Manipulating dendritic cell biology for the active immunotherapy of cancer. Blood. 2004; 104(8):2235-2246.
44. Higham EM, Wittrup KD, Chen J. Activation of tolerogenic dendritic cells in the tumor draining lymph nodes by CD8+ T cells engineered to express CD40 ligand. J Immunol. 2010;184(7):3394-3400.
45. Trinchieri G. Interleukin-12 and the regulation of innate resistance and adaptive immunity. Nat Rev Immunol. 2003;3(2): 133-146.
46. Laurin D, Marin V, Biagi E, et al. Upregulation of Adhesion Molecules on Leukemia Targets Improves the Efficacy of Cytotoxic T Cells Transduced With Chimeric Anti-CD19 Receptor. J Immunother. 2013; 36(3):181-189.
47. Brown MP, Topham DJ, Sangster MY, et al. Thymic lymphoproliferative disease after successful correction of CD40 ligand deficiency by gene transfer in mice. Nat Med. 1998;4(1 1).T 253- 1260.
48. Di Stasi A, Tey SK, Dotti G, et al. Inducible apoptosis as a safety switch for adoptive cell therapy. N Engl J Med. 2011;365(18): 1673-1683.
Варианты осуществления изобретения
Из вышеизложенного описания очевидно, что вариации и модификации могут быть произведены к изобретению, описанному в настоящем документе, чтобы адаптировать его к различным применениям и условиям. Такие варианты осуществления также находятся в рамках следующих пунктов формулы изобретения.
Перечисление списка элементов в любом определении вариабельной в настоящем документе включает определения этой вариабельной как любого отдельного элемента или комбинации (или подкомбинации) из перечисленных элементов. Перечисление варианта осуществления в настоящем документе включает этот вариант осуществления как любой отдельный вариант осуществления или в сочетании с любыми другими вариантами или их частями.
Некоторое из предмета рассмотрения настоящего приложения может быть связано с патентной заявкой США № 12/593751, которая является заявкой национальной фазы США, в соответствии с 35 U.S.С. §371, международной патентной заявки №: РСТ/US2008/004251, поданной 8 марта 2010, которая утверждает преимущество предварительной заявки США сер. №. 60/921144, поданной 30 марта 2007 года, описания которых этим включены в настоящий документ в их полном объеме при помощи ссылки.
Все патенты и публикации, упомянутые в настоящей спецификации, включены в данном документе посредством ссылки в той же степени, как если бы каждый независимый патент и публикация был конкретно и индивидуально указан для включения при помощи ссылки.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> МЕМОРИАЛЬНЫЙ СЛОАН-КЕТТЕРИНГСКИЙ ОНКОЛОГИЧЕСКИЙ ЦЕНТР
<120> КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ ИММУНОТЕРАПИИ
<130> 072734.0152
<140> PCT/US2014/018667
<141> 2014-02-26
<150> 61/769,543
<151> 2013-02-26
<160> 56
<170> PatentIn version 3.5
<210> 1
<211> 164
<212> PRT
<213> Homo sapiens
<400> 1
Met Lys Trp Lys Ala Leu Phe Thr Ala Ala Ile Leu Gln Ala Gln Leu
1 5 10 15
Pro Ile Thr Glu Ala Gln Ser Phe Gly Leu Leu Asp Pro Lys Leu Cys
20 25 30
Tyr Leu Leu Asp Gly Ile Leu Phe Ile Tyr Gly Val Ile Leu Thr Ala
35 40 45
Leu Phe Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr
50 55 60
Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg
65 70 75 80
Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met
85 90 95
Gly Gly Lys Pro Gln Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn
100 105 110
Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met
115 120 125
Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly
130 135 140
Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala
145 150 155 160
Leu Pro Pro Arg
<210> 2
<211> 220
<212> PRT
<213> Homo sapiens
<400> 2
Met Leu Arg Leu Leu Leu Ala Leu Asn Leu Phe Pro Ser Ile Gln Val
1 5 10 15
Thr Gly Asn Lys Ile Leu Val Lys Gln Ser Pro Met Leu Val Ala Tyr
20 25 30
Asp Asn Ala Val Asn Leu Ser Cys Lys Tyr Ser Tyr Asn Leu Phe Ser
35 40 45
Arg Glu Phe Arg Ala Ser Leu His Lys Gly Leu Asp Ser Ala Val Glu
50 55 60
Val Cys Val Val Tyr Gly Asn Tyr Ser Gln Gln Leu Gln Val Tyr Ser
65 70 75 80
Lys Thr Gly Phe Asn Cys Asp Gly Lys Leu Gly Asn Glu Ser Val Thr
85 90 95
Phe Tyr Leu Gln Asn Leu Tyr Val Asn Gln Thr Asp Ile Tyr Phe Cys
100 105 110
Lys Ile Glu Val Met Tyr Pro Pro Pro Tyr Leu Asp Asn Glu Lys Ser
115 120 125
Asn Gly Thr Ile Ile His Val Lys Gly Lys His Leu Cys Pro Ser Pro
130 135 140
Leu Phe Pro Gly Pro Ser Lys Pro Phe Trp Val Leu Val Val Val Gly
145 150 155 160
Gly Val Leu Ala Cys Tyr Ser Leu Leu Val Thr Val Ala Phe Ile Ile
165 170 175
Phe Trp Val Arg Ser Lys Arg Ser Arg Leu Leu His Ser Asp Tyr Met
180 185 190
Asn Met Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro
195 200 205
Tyr Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser
210 215 220
<210> 3
<211> 45
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический праймер
<400> 3
cacgtgcatg atcgaaacat acaaccaaac ttctccccga tctgc 45
<210> 4
<211> 36
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический праймер
<400> 4
ctcgagggat cctcagagtt tgagtaagcc aaagga 36
<210> 5
<211> 255
<212> PRT
<213> Homo sapiens
<400> 5
Met Gly Asn Ser Cys Tyr Asn Ile Val Ala Thr Leu Leu Leu Val Leu
1 5 10 15
Asn Phe Glu Arg Thr Arg Ser Leu Gln Asp Pro Cys Ser Asn Cys Pro
20 25 30
Ala Gly Thr Phe Cys Asp Asn Asn Arg Asn Gln Ile Cys Ser Pro Cys
35 40 45
Pro Pro Asn Ser Phe Ser Ser Ala Gly Gly Gln Arg Thr Cys Asp Ile
50 55 60
Cys Arg Gln Cys Lys Gly Val Phe Arg Thr Arg Lys Glu Cys Ser Ser
65 70 75 80
Thr Ser Asn Ala Glu Cys Asp Cys Thr Pro Gly Phe His Cys Leu Gly
85 90 95
Ala Gly Cys Ser Met Cys Glu Gln Asp Cys Lys Gln Gly Gln Glu Leu
100 105 110
Thr Lys Lys Gly Cys Lys Asp Cys Cys Phe Gly Thr Phe Asn Asp Gln
115 120 125
Lys Arg Gly Ile Cys Arg Pro Trp Thr Asn Cys Ser Leu Asp Gly Lys
130 135 140
Ser Val Leu Val Asn Gly Thr Lys Glu Arg Asp Val Val Cys Gly Pro
145 150 155 160
Ser Pro Ala Asp Leu Ser Pro Gly Ala Ser Ser Val Thr Pro Pro Ala
165 170 175
Pro Ala Arg Glu Pro Gly His Ser Pro Gln Ile Ile Ser Phe Phe Leu
180 185 190
Ala Leu Thr Ser Thr Ala Leu Leu Phe Leu Leu Phe Phe Leu Thr Leu
195 200 205
Arg Phe Ser Val Val Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe
210 215 220
Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly
225 230 235 240
Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
245 250 255
<210> 6
<211> 183
<212> PRT
<213> Homo sapiens
<400> 6
Met Glu Arg Val Gln Pro Leu Glu Glu Asn Val Gly Asn Ala Ala Arg
1 5 10 15
Pro Arg Phe Glu Arg Asn Lys Leu Leu Leu Val Ala Ser Val Ile Gln
20 25 30
Gly Leu Gly Leu Leu Leu Cys Phe Thr Tyr Ile Cys Leu His Phe Ser
35 40 45
Ala Leu Gln Val Ser His Arg Tyr Pro Arg Ile Gln Ser Ile Lys Val
50 55 60
Gln Phe Thr Glu Tyr Lys Lys Glu Lys Gly Phe Ile Leu Thr Ser Gln
65 70 75 80
Lys Glu Asp Glu Ile Met Lys Val Gln Asn Asn Ser Val Ile Ile Asn
85 90 95
Cys Asp Gly Phe Tyr Leu Ile Ser Leu Lys Gly Tyr Phe Ser Gln Glu
100 105 110
Val Asn Ile Ser Leu His Tyr Gln Lys Asp Glu Glu Pro Leu Phe Gln
115 120 125
Leu Lys Lys Val Arg Ser Val Asn Ser Leu Met Val Ala Ser Leu Thr
130 135 140
Tyr Lys Asp Lys Val Tyr Leu Asn Val Thr Thr Asp Asn Thr Ser Leu
145 150 155 160
Asp Asp Phe His Val Asn Gly Gly Glu Leu Ile Leu Ile His Gln Asn
165 170 175
Pro Gly Glu Phe Cys Val Leu
180
<210> 7
<211> 486
<212> PRT
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<220>
<221> MOD_RES
<222> (486)..(486)
<223> Любая аминокислота
<400> 7
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Glu Val Lys Leu Gln Gln Ser Gly Ala Glu Leu Val Arg Pro
20 25 30
Gly Ser Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Ala Phe Ser
35 40 45
Ser Tyr Trp Met Asn Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu
50 55 60
Trp Ile Gly Gln Ile Tyr Pro Gly Asp Gly Asp Thr Asn Tyr Asn Gly
65 70 75 80
Lys Phe Lys Gly Gln Ala Thr Leu Thr Ala Asp Lys Ser Ser Ser Thr
85 90 95
Ala Tyr Met Gln Leu Ser Gly Leu Thr Ser Glu Asp Ser Ala Val Tyr
100 105 110
Phe Cys Ala Arg Lys Thr Ile Ser Ser Val Val Asp Phe Tyr Phe Asp
115 120 125
Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Glu Leu Thr
145 150 155 160
Gln Ser Pro Lys Phe Met Ser Thr Ser Val Gly Asp Arg Val Ser Val
165 170 175
Thr Cys Lys Ala Ser Gln Asn Val Gly Thr Asn Val Ala Trp Tyr Gln
180 185 190
Gln Lys Pro Gly Gln Ser Pro Lys Pro Leu Ile Tyr Ser Ala Thr Tyr
195 200 205
Arg Asn Ser Gly Val Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr
210 215 220
Asp Phe Thr Leu Thr Ile Thr Asn Val Gln Ser Lys Asp Leu Ala Asp
225 230 235 240
Tyr Phe Cys Gln Gln Tyr Asn Arg Tyr Pro Tyr Thr Ser Gly Gly Gly
245 250 255
Thr Lys Leu Glu Ile Lys Arg Ala Ala Ala Ile Glu Val Met Tyr Pro
260 265 270
Pro Pro Tyr Leu Asp Asn Glu Lys Ser Asn Gly Thr Ile Ile His Val
275 280 285
Lys Gly Lys His Leu Cys Pro Ser Pro Leu Phe Pro Gly Pro Ser Lys
290 295 300
Pro Phe Trp Val Leu Val Val Val Gly Gly Val Leu Ala Cys Tyr Ser
305 310 315 320
Leu Leu Val Thr Val Ala Phe Ile Ile Phe Trp Val Arg Ser Lys Arg
325 330 335
Ser Arg Leu Leu His Ser Asp Tyr Met Asn Met Thr Pro Arg Arg Pro
340 345 350
Gly Pro Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro Pro Arg Asp Phe
355 360 365
Ala Ala Tyr Arg Ser Arg Val Lys Phe Ser Arg Ser Ala Glu Pro Pro
370 375 380
Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly
385 390 395 400
Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro
405 410 415
Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr
420 425 430
Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly
435 440 445
Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln
450 455 460
Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln
465 470 475 480
Ala Leu Pro Pro Arg Xaa
485
<210> 8
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 8
ccatggctct cccagtgact gccctactgc ttcccctagc gcttctcctg catgcagagg 60
tgaagctgca gcagtctggg gctgagctgg tgaggcctgg gtcctcagtg aagatttcct 120
gcaaggcttc tggctatgca ttcagtagct actggatgaa ctgggtgaag cagaggcctg 180
gacagggtct tgagtggatt ggacagattt atcctggaga tggtgatact aactacaatg 240
gaaagttcaa gggtcaagcc acactgactg cagacaaatc ctccagcaca gcctacatgc 300
agctcagcgg cctaacatct gaggactctg cggtctattt ctgtgcaaga aagaccatta 360
gttcggtagt agatttctac tttgactact ggggccaagg gaccacggtc accgtctcct 420
caggtggagg tggatcaggt ggaggtggat ctggtggagg tggatctgac attgagctca 480
cccagtctcc aaaattcatg tccacatcag taggagacag ggtcagcgtc acctgcaagg 540
ccagtcagaa tgtgggtact aatgtagcct ggtatcaaca gaaaccagga caatctccta 600
aaccactgat ttactcggca acctaccgga acagtggagt ccctgatcgc ttcacaggca 660
gtggatctgg gacagatttc actctcacca tcactaacgt gcagtctaaa gacttggcag 720
actatttctg tcaacaatat aacaggtatc cgtacacgtc cggagggggg accaagctgg 780
agatcaaacg ggcggccgca attgaagtta tgtatcctcc tccttaccta gacaatgaga 840
agagcaatgg aaccattatc catgtgaaag ggaaacacct ttgtccaagt cccctatttc 900
ccggaccttc taagcccttt tgggtgctgg tggtggttgg tggagtcctg gcttgctata 960
gcttgctagt aacagtggcc tttattattt tctgggtgag gagtaagagg agcaggctcc 1020
tgcacagtga ctacatgaac atgactcccc gccgccccgg gcccacccgc aagcattacc 1080
agccctatgc cccaccacgc gacttcgcag cctatcgctc cagagtgaag ttcagcagga 1140
gcgcagagcc ccccgcgtac cagcagggcc agaaccagct ctataacgag ctcaatctag 1200
gacgaagaga ggagtacgat gttttggaca agagacgtgg ccgggaccct gagatggggg 1260
gaaagccgag aaggaagaac cctcaggaag gcctgtacaa tgaactgcag aaagataaga 1320
tggcggaggc ctacagtgag attgggatga aaggcgagcg ccggaggggc aaggggcacg 1380
atggccttta ccagggtctc agtacagcca ccaaggacac ctacgacgcc cttcacatgc 1440
aggccctgcc ccctcgcg 1458
<210> 9
<211> 491
<212> PRT
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 9
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Glu Val Lys Leu Gln Glu Ser Gly Gly Gly Phe Val Lys Pro
20 25 30
Gly Gly Ser Leu Lys Val Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser
35 40 45
Ser Tyr Ala Met Ser Trp Val Arg Leu Ser Pro Glu Met Arg Leu Glu
50 55 60
Trp Val Ala Thr Ile Ser Ser Ala Gly Gly Tyr Ile Phe Tyr Ser Asp
65 70 75 80
Ser Val Gln Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr
85 90 95
Leu His Leu Gln Met Gly Ser Leu Arg Ser Gly Asp Thr Ala Met Tyr
100 105 110
Tyr Cys Ala Arg Gln Gly Phe Gly Asn Tyr Gly Asp Tyr Tyr Ala Met
115 120 125
Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Glu Leu
145 150 155 160
Thr Gln Ser Pro Ser Ser Leu Ala Val Ser Ala Gly Glu Lys Val Thr
165 170 175
Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser Arg Thr Arg Lys
180 185 190
Asn Gln Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Glu Leu
195 200 205
Leu Ile Tyr Trp Ala Ser Thr Arg Gln Ser Gly Val Pro Asp Arg Phe
210 215 220
Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Val
225 230 235 240
Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Gln Ser Tyr Asn Leu
245 250 255
Leu Thr Phe Gly Pro Gly Thr Lys Leu Glu Ile Lys Arg Ala Ala Ala
260 265 270
Ile Glu Val Met Tyr Pro Pro Pro Tyr Leu Asp Asn Glu Lys Ser Asn
275 280 285
Gly Thr Ile Ile His Val Lys Gly Lys His Leu Cys Pro Ser Pro Leu
290 295 300
Phe Pro Gly Pro Ser Lys Pro Phe Trp Val Leu Val Val Val Gly Gly
305 310 315 320
Val Leu Ala Cys Tyr Ser Leu Leu Val Thr Val Ala Phe Ile Ile Phe
325 330 335
Trp Val Arg Ser Lys Arg Ser Arg Leu Leu His Ser Asp Tyr Met Asn
340 345 350
Met Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro Tyr
355 360 365
Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser Arg Val Lys Phe Ser
370 375 380
Arg Ser Ala Glu Pro Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr
385 390 395 400
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
405 410 415
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
420 425 430
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
435 440 445
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
450 455 460
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
465 470 475 480
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 10
<211> 1475
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 10
ccatggctct cccagtgact gccctactgc ttcccctagc gcttctcctg catgcagagg 60
tgaagctgca ggagtcaggg ggaggcttcg tgaagcctgg agggtccctc aaagtctcct 120
gtgcagcctc tggattcact ttcagtagct atgccatgtc ctgggttcgc ctgagtccgg 180
agatgaggct ggagtgggtc gcaaccatta gcagtgctgg tggttacatc ttctattctg 240
acagtgtgca gggacgattc accatttcca gagacaatgc caagaacacc ctgcacctgc 300
aaatgggcag tctgaggtct ggggacacgg ccatgtatta ctgtgcaagg cagggatttg 360
gtaactacgg tgattactat gctatggact actggggcca agggaccacg gtcaccgtct 420
cctcaggtgg aggtggatca ggtggaggtg gatctggtgg aggtggatct gacattgagc 480
tcacccagtc tccatcctcc ctggctgtgt cagcaggaga gaaggtcact atgagctgca 540
aatccagtca gagtctgctc aacagtagaa cccgaaagaa ccagttggct tggtaccagc 600
aaaaaccagg acagtctcct gaactgctga tctactgggc atccactagg caatctggag 660
tccctgatcg cttcacaggc agtggatctg ggacagattt cactctcacc atcagcagtg 720
tgcaggctga agacctggca gtttattact gccagcaatc ttataatcta ctcacgttcg 780
gtcctgggac caagctggag atcaaacggg cggccgcaat tgaagttatg tatcctcctc 840
cttacctaga caatgagaag agcaatggaa ccattatcca tgtgaaaggg aaacaccttt 900
gtccaagtcc cctatttccc ggaccttcta agcccttttg ggtgctggtg gtggttggtg 960
gagtcctggc ttgctatagc ttgctagtaa cagtggcctt tattattttc tgggtgagga 1020
gtaagaggag caggctcctg cacagtgact acatgaacat gactccccgc cgccccgggc 1080
ccacccgcaa gcattaccag ccctatgccc caccacgcga cttcgcagcc tatcgctcca 1140
gagtgaagtt cagcaggagc gcagagcccc ccgcgtacca gcagggccag aaccagctct 1200
ataacgagct caatctagga cgaagagagg agtacgatgt tttggacaag agacgtggcc 1260
gggaccctga gatgggggga aagccgagaa ggaagaaccc tcaggaaggc ctgtacaatg 1320
aactgcagaa agataagatg gcggaggcct acagtgagat tgggatgaaa ggcgagcgcc 1380
ggaggggcaa ggggcacgat ggcctttacc agggtctcag tacagccacc aaggacacct 1440
acgacgccct tcacatgcag gccctgcccc ctcgc 1475
<210> 11
<211> 250
<212> PRT
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 11
Glu Val Gln Leu Val Glu Ser Gly Gly Asp Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Gly Tyr
20 25 30
Gly Met Ser Trp Val Arg Gln Thr Pro Asp Lys Arg Leu Glu Trp Val
35 40 45
Ala Thr Ile Thr Ser Gly Gly Thr Tyr Thr Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Ile Asp Ser Leu Lys Ser Glu Asp Thr Ala Ile Tyr Phe Cys
85 90 95
Ala Arg Ser Leu Ala Gly Asn Ala Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Ser Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Asp Ile Val Met Thr Gln Ser Pro Ala Thr Leu
130 135 140
Ser Val Thr Pro Gly Asp Arg Val Ser Leu Ser Cys Arg Ala Ser Gln
145 150 155 160
Thr Ile Ser Asp Tyr Leu His Trp Tyr Gln Gln Lys Ser His Glu Ser
165 170 175
Pro Arg Leu Leu Ile Lys Phe Ala Ser Gln Ser Ile Ser Gly Ile Pro
180 185 190
Ser Arg Phe Ser Gly Ser Gly Ser Gly Ser Asp Phe Thr Leu Ser Ile
195 200 205
Asn Ser Val Glu Pro Glu Asp Val Gly Val Tyr Tyr Cys Gln Asn Gly
210 215 220
His Gly Phe Pro Arg Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
225 230 235 240
Glu Gln Lys Leu Ile Ser Glu Glu Asp Leu
245 250
<210> 12
<211> 235
<212> PRT
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 12
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Asp Cys Lys Ala Ser Gly Ile Thr Phe Ser Asn Ser
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Lys Arg Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Phe
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Thr Asn Asp Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
100 105 110
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
130 135 140
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
145 150 155 160
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
165 170 175
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
180 185 190
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
195 200 205
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Ser Asn Trp Pro Arg
210 215 220
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
225 230 235
<210> 13
<211> 421
<212> PRT
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 13
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Met Gly Leu Gly Leu Gln Trp Val Phe Phe Val
20 25 30
Ala Leu Leu Lys Gly Val His Cys Glu Val Arg Leu Leu Glu Ser Gly
35 40 45
Gly Gly Leu Val Lys Pro Glu Gly Ser Leu Lys Leu Ser Cys Val Ala
50 55 60
Ser Gly Phe Thr Phe Ser Asp Tyr Phe Met Ser Trp Val Arg Gln Ala
65 70 75 80
Pro Gly Lys Gly Leu Glu Trp Val Ala His Ile Tyr Thr Lys Ser Tyr
85 90 95
Asn Tyr Ala Thr Tyr Tyr Ser Gly Ser Val Lys Gly Arg Phe Thr Ile
100 105 110
Ser Arg Asp Asp Ser Arg Ser Met Val Tyr Leu Gln Met Asn Asn Leu
115 120 125
Arg Thr Glu Asp Thr Ala Thr Tyr Tyr Cys Thr Arg Asp Gly Ser Gly
130 135 140
Tyr Pro Ser Leu Asp Phe Trp Gly Gln Gly Thr Gln Val Thr Val Ser
145 150 155 160
Ser Ala Thr Thr Thr Ala Pro Ser Val Tyr Pro Leu Ala Pro Ala Cys
165 170 175
Asp Ser Thr Thr Lys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
180 185 190
Gly Gly Gly Gly Ser Tyr Glu Leu Thr Gln Pro Pro Ser Ala Ser Val
195 200 205
Asn Val Gly Glu Thr Val Lys Ile Thr Cys Ser Gly Asp Gln Leu Pro
210 215 220
Lys Tyr Phe Ala Asp Gln Phe His Gln Arg Ser Asp Gln Thr Ile Leu
225 230 235 240
Gln Val Ile Tyr Asp Asp Asn Lys Arg Pro Ser Gly Ile Pro Glu Arg
245 250 255
Ile Ser Gly Ser Ser Ser Gly Thr Thr Ala Thr Leu Thr Ile Arg Asp
260 265 270
Val Arg Ala Glu Asp Glu Gly Asp Tyr Tyr Cys Phe Ser Gly Tyr Val
275 280 285
Asp Ser Asp Ser Lys Leu Tyr Val Phe Gly Ser Gly Thr Gln Leu Thr
290 295 300
Val Leu Gly Gly Pro Lys Ser Ser Pro Lys Val Thr Val Phe Pro Pro
305 310 315 320
Ser Pro Glu Glu Leu Arg Thr Asn Lys Ala Thr Leu Val Cys Leu Val
325 330 335
Asn Asp Phe Tyr Pro Gly Ser Ala Thr Val Thr Trp Lys Ala Asn Gly
340 345 350
Ala Thr Ile Asn Asp Gly Val Lys Thr Thr Lys Pro Ser Lys Gln Gly
355 360 365
Gln Asn Tyr Met Thr Ser Ser Tyr Leu Ser Leu Thr Ala Asp Gln Trp
370 375 380
Lys Ser His Asn Arg Val Ser Cys Gln Val Thr His Glu Gly Glu Thr
385 390 395 400
Val Glu Lys Ser Leu Ser Pro Ala Glu Cys Leu Glu Gln Lys Leu Ile
405 410 415
Ser Glu Glu Asp Leu
420
<210> 14
<211> 1274
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 14
ccatggagac agacacactc ctgctatggg tactgctgct ctgggttcca ggttccactg 60
gtgacatggg attgggactg cagtgggttt tctttgttgc tcttttaaaa ggtgtccact 120
gtgaggtgcg gcttctggag tctggtggag gattagtgaa gcctgagggg tcactgaaac 180
tctcctgtgt ggcctctgga ttcaccttca gtgactattt catgagctgg gtccgccagg 240
ctccagggaa ggggctggag tgggttgctc acatatacac gaaaagttat aattatgcaa 300
cttattactc gggttcggtg aaaggcagat tcaccatctc cagagatgat tcccgaagca 360
tggtctacct gcaaatgaac aacctgagaa ctgaggacac ggccacttat tactgtacaa 420
gagatggaag cggatatccc tctctggatt tctggggtca agggacccaa gtcactgtct 480
cctcagccac aacaacagcc ccatctgtct atcccttggc ccctgcctgt gacagcacaa 540
ccaaatcggg tggaggtgga tcaggtggag gtggatctgg tggaggtgga tcttatgagc 600
tgactcagcc accttcagca tcagtcaatg taggagagac tgtcaaaatc acctgctctg 660
gggaccaatt gccgaaatat tttgcagatt ggtttcatca aaggtcagac cagaccattt 720
tgcaagtgat atatgatgat aataagcgcc cctcggggat ccctgaaaga atctctgggt 780
ccagctcagg gacaacagcc accttgacca tcagagatgt ccgggctgag gatgaaggtg 840
actattactg tttctcagga tatgttgata gtgatagcaa attgtatgtt tttggcagcg 900
gaacccagct caccgtccta ggtggaccca agtcttctcc caaagtcaca gtgtttccac 960
cttcacctga ggagctccgg acaaacaaag ccacactggt gtgtctggtt aatgacttct 1020
acccgggttc tgcaacagtg acctggaagg caaatggagc aactatcaat gatggggtga 1080
agactacaaa gccttccaaa cagggccaaa actacatgac cagcagctac ctaagtttga 1140
cagcagacca gtggaaatct cacaacaggg tttcctgcca agttacccat gaaggggaaa 1200
ctgtggagaa gagtttgtcc cctgcagaat gtctcgaaca aaaactcatc tcagaagagg 1260
atctgtaact cgag 1274
<210> 15
<211> 21
<212> PRT
<213> Homo sapiens
<400> 15
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp
20
<210> 16
<211> 21
<212> PRT
<213> Mus sp.
<400> 16
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp
20
<210> 17
<211> 21
<212> PRT
<213> Unknown
<220>
<223> Описание неизвестного: лидерный пептид CDS
<400> 17
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro
20
<210> 18
<211> 824
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 18
ccatggagac agacacactc ctgctatggg tactgctgct ctgggttcca ggttccactg 60
gtgacgaggt gcagctggtg gagtccgggg gagacttagt gaagcctgga gggtccctga 120
aactctcctg tgcagcctct ggattcactt tcagtggcta tggcatgtct tgggttcgcc 180
agactccaga caagaggctg gagtgggtcg caaccattac tagtggtggt acttacacct 240
actatccaga cagtgtgaag gggcgattca ccatctccag agacaatgcc aagaacaccc 300
tgtacctgca aatagacagt ctgaagtctg aggatacagc catatatttc tgtgcaagat 360
ccctcgcggg aaatgctatg gactactggg gtcaaggaac ctcagtcacc gtctcctcag 420
gtggaggtgg atcaggtgga ggtggatctg gtggaggtgg atctgacatt gtgatgactc 480
agtctccagc caccctgtct gtgactccag gagatagagt ctctctttcc tgcagggcca 540
gccagactat tagcgactac ttacactggt atcaacaaaa atcacatgag tctccaaggc 600
ttctcatcaa atttgcttcc caatccattt ctgggatccc ctccaggttc agtggcagtg 660
gatcaggctc agatttcact ctcagtatca acagtgtgga acctgaagat gttggagtgt 720
attactgtca aaatggtcac ggctttcctc ggacgttcgg tggaggcacc aagctggaaa 780
tcaaagaaca aaaactcatc tcagaagagg atctgtaact cgag 824
<210> 19
<211> 824
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 19
ccatggcctt accagtgacc gccttgctcc tgccgctggc cttgctgctc cacgccgcca 60
ggccggaggt gcagctggtg gagtccgggg gagacttagt gaagcctgga gggtccctga 120
aactctcctg tgcagcctct ggattcactt tcagtggcta tggcatgtct tgggttcgcc 180
agactccaga caagaggctg gagtgggtcg caaccattac tagtggtggt acttacacct 240
actatccaga cagtgtgaag gggcgattca ccatctccag agacaatgcc aagaacaccc 300
tgtacctgca aatagacagt ctgaagtctg aggatacagc catatatttc tgtgcaagat 360
ccctcgcggg aaatgctatg gactactggg gtcaaggaac ctcagtcacc gtctcctcag 420
gtggaggtgg atcaggtgga ggtggatctg gtggaggtgg atctgacatt gtgatgactc 480
agtctccagc caccctgtct gtgactccag gagatagagt ctctctttcc tgcagggcca 540
gccagactat tagcgactac ttacactggt atcaacaaaa atcacatgag tctccaaggc 600
ttctcatcaa atttgcttcc caatccattt ctgggatccc ctccaggttc agtggcagtg 660
gatcaggctc agatttcact ctcagtatca acagtgtgga acctgaagat gttggagtgt 720
attactgtca aaatggtcac ggctttcctc ggacgttcgg tggaggcacc aagctggaaa 780
tcaaagaaca aaaactcatc tcagaagagg atctgtaact cgag 824
<210> 20
<211> 2337
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 20
atggctctcc cagtgactgc cctactgctt cccctagcgc ttctcctgca tgcagaggtg 60
aagctgcagc agtctggggc tgagctggtg aggcctgggt cctcagtgaa gatttcctgc 120
aaggcttctg gctatgcatt cagtagctac tggatgaact gggtgaagca gaggcctgga 180
cagggtcttg agtggattgg acagatttat cctggagatg gtgatactaa ctacaatgga 240
aagttcaagg gtcaagccac actgactgca gacaaatcct ccagcacagc ctacatgcag 300
ctcagcggcc taacatctga ggactctgcg gtctatttct gtgcaagaaa gaccattagt 360
tcggtagtag atttctactt tgactactgg ggccaaggga ccacggtcac cgtctcctca 420
ggtggaggtg gatcaggtgg aggtggatct ggtggaggtg gatctgacat tgagctcacc 480
cagtctccaa aattcatgtc cacatcagta ggagacaggg tcagcgtcac ctgcaaggcc 540
agtcagaatg tgggtactaa tgtagcctgg tatcaacaga aaccaggaca atctcctaaa 600
ccactgattt actcggcaac ctaccggaac agtggagtcc ctgatcgctt cacaggcagt 660
ggatctggga cagatttcac tctcaccatc actaacgtgc agtctaaaga cttggcagac 720
tatttctgtc aacaatataa caggtatccg tacacgtccg gaggggggac caagctggag 780
atcaaacggg cggccgcaat tgaagttatg tatcctcctc cttacctaga caatgagaag 840
agcaatggaa ccattatcca tgtgaaaggg aaacaccttt gtccaagtcc cctatttccc 900
ggaccttcta agcccttttg ggtgctggtg gtggttggtg gagtcctggc ttgctatagc 960
ttgctagtaa cagtggcctt tattattttc tgggtgagga gtaagaggag caggctcctg 1020
cacagtgact acatgaacat gactccccgc cgccccgggc ccacccgcaa gcattaccag 1080
ccctatgccc caccacgcga cttcgcagcc tatcgctcca gagtgaagtt cagcaggagc 1140
gcagagcccc ccgcgtacca gcagggccag aaccagctct ataacgagct caatctagga 1200
cgaagagagg agtacgatgt tttggacaag agacgtggcc gggaccctga gatgggggga 1260
aagccgagaa ggaagaaccc tcaggaaggc ctgtacaatg aactgcagaa agataagatg 1320
gcggaggcct acagtgagat tgggatgaaa ggcgagcgcc ggaggggcaa ggggcacgaa 1380
ggcctttacc agggtctcag tacagccacc aaggacacct acgacgccct tcacatgcag 1440
gccctgcccc ctcgcggatc tggagcaaca aacttctcac tactcaaaca agcaggtgac 1500
gtggaggaga atcccggacc catggagaca gacacactcc tgctatgggt actgctgctc 1560
tgggttccag gttccactgg tgacgaggtg cagctggtgg agtccggggg agacttagtg 1620
aagcctggag ggtccctgaa actctcctgt gcagcctctg gattcacttt cagtggctat 1680
ggcatgtctt gggttcgcca gactccagac aagaggctgg agtgggtcgc aaccattact 1740
agtggtggta cttacaccta ctatccagac agtgtgaagg ggcgattcac catctccaga 1800
gacaatgcca agaacaccct gtacctgcaa atagacagtc tgaagtctga ggatacagcc 1860
atatatttct gtgcaagatc cctcgcggga aatgctatgg actactgggg tcaaggaacc 1920
tcagtcaccg tctcctcagg tggaggtgga tcaggtggag gtggatctgg tggaggtgga 1980
tctgacattg tgatgactca gtctccagcc accctgtctg tgactccagg agatagagtc 2040
tctcttccct gcagggccag ccagactatt agcgactact tacactggta tcaacaaaaa 2100
tcacatgagt ctccaaggct tctcatcaaa tttgcttccc aatccatttc tgggatcccc 2160
tccaggttca gtggcagagg atcaggctca gatttcactc tcagtatcaa cagtgtggaa 2220
cctgaagatg ttggagtgta ttactgtcaa aatggtcacg gctttcctcg gacgttcggt 2280
ggaggcacca agctggaaat caaagaacaa aaactcatct cagaagagga tctgtaa 2337
<210> 21
<211> 1644
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 21
catggctctc ccagtgactg ccctactgct tcccctagcg cttctcctgc atgcagaggt 60
gaagctgcag gagtcagggg gaggcttcgt gaagcctgga gggtccctca aagtctcctg 120
tgcagcctct ggattcactt tcagtagcta tgccatgtcc tgggttcgcc tgagtccgga 180
gatgaggctg gagtgggtcg caaccattag cagtgctggt ggttacatct tctattctga 240
cagtgtgcag ggacgattca ccatttccag agacaatgcc aagaacaccc tgcacctgca 300
aatgggcagt ctgaggtctg gggacacggc catgtattac tgtgcaaggc agggatttgg 360
taactacggt gattactatg ctatggacta ctggggccaa gggaccacgg tcaccgtctc 420
ctcaggtgga ggtggatcag gtggaggtgg atctggtgga ggtggatctg acattgagct 480
cacccagtct ccatcctccc tggctgtgtc agcaggagag aaggtcacta tgagctgcaa 540
atccagtcag agtctgctca acagtagaac ccgaaagaac cagttggctt ggtaccagca 600
aaaaccagga cagtctcctg aactgctgat ctactgggca tccactaggc aatctggagt 660
ccctgatcgc ttcacaggca gtggatctgg gacagatttc actctcacca tcagcagtgt 720
gcaggctgaa gacctggcag tttattactg ccagcaatct tataatctac tgcaacaaac 780
ttctcactac tcaaacaagc aggtgacgtg gaggagaatc ccggacccat ggagacagac 840
acactcctgc tatgggtact gctgctctgg gttccaggtt ccactggtga cgaggtgcag 900
ctggtggagt ccgggggaga cttagtgaag cctggagggt ccctgaaact ctcctgtgca 960
gcctctggat tcactttcag tggctatggc atgtcttggg ttcgccagac tccagacaag 1020
aggctggagt gggtcgcaac cattactagt ggtggtactt acacctacta tccagacagt 1080
gtgaaggggc gattcaccat ctccagagac aatgccaaga acaccctgta cctgcaaata 1140
gacagtctga agtctgagga tacagccata tatttctgtg caagatccct cgcgggaaat 1200
gctatggact actggggtca aggaacctca gtcaccgtct cctcaggtgg aggtggatca 1260
ggtggaggtg gatctggtgg aggtggatct gacattgtga tgactcagtc tccagccacc 1320
ctgtctgtga ctccaggaga tagagtctct ctttcctgca gggccagcca gactattagc 1380
gactacttac acaggtatca acaaaaatca catgagtctc caaggcttct catcaaattt 1440
gcttcccaat ccatttctgg gatcccctcc aggttcagtg gcagtggatc aggctcagat 1500
ttcactctca gtatcaacag tgtggaacct gaagatgttg gagtgtatta ctgtcaaaat 1560
ggtcacggct ttcctcggac gttcggtgga ggcaccaagc tggaaatcaa agaacaaaaa 1620
ctcatctcag aagaggatct gtaa 1644
<210> 22
<211> 801
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 22
atggagacag acacactcct gctatgggta ctgctgctct gggttccagg ttccactggt 60
gaccaggtgc agctggtgga gtctggggga ggcgtggtcc agcctgggag gtccctgaga 120
ctcgactgta aagcgtctgg aatcaccttc agtaactctg gcatgcactg ggtccgccag 180
gctccaggca aggggctgga gtgggtggca gttatttggt atgatggaag taaaagatac 240
tatgcagact ccgtgaaggg ccgattcacc atctccagag acaattccaa gaacacgctg 300
tttctgcaaa tgaacagcct gagagccgag gacacggctg tgtattactg tgcgacaaac 360
gacgactact ggggccaggg aaccctggtc accgtctcct caggtggagg tggatcaggt 420
ggaggtggat ctggtggagg tggatctgaa attgtgttga cacagtctcc agccaccctg 480
tctttgtctc caggggaaag agccaccctc tcctgcaggg ccagtcagag tgttagtagt 540
tacttagcct ggtaccaaca gaaacctggc caggctccca ggctcctcat ctatgatgca 600
tccaacaggg ccactggcat cccagccagg ttcagtggca gtgggtctgg gacagacttc 660
actctcacca tcagcagcct agagcctgaa gattttgcag tttattactg tcagcagagt 720
agcaactggc ctcggacgtt cggccaaggg accaaggtgg aaatcaaaga acaaaaactc 780
atctcagaag aggatctgta a 801
<210> 23
<211> 2332
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 23
atggctctcc cagtgactgc cctactgctt cccctagcgc ttctcctgca tgcagaggtg 60
aagctgcagc agtctggggc tgagctggtg aggcctgggt cctcagtgaa gatttcctgc 120
aaggcttctg gctatgcatt cagtagctac tggatgaact gggtgaagca gaggcctgga 180
cagggtctag agtggattgg acagatttat cctggagatg gtgatactaa ctacaatgga 240
aagttcaagg gtcaagccac actgactgca gacaaatcct ccagcacagc ctacatgcag 300
ctcagcggcc taacatctga ggactctgcg gtctatttct gtgcaagaaa gaccattagt 360
tcggtagtag atttctactt tgactactgg ggccaaggga ccacggtcac cgtctcctca 420
ggtggaggtg gatcaggtgg aggtggatct ggtggaggtg gatctgacat cgagctcacc 480
cagtctccaa aattcatgtc cacatcagta ggagacaggg tcagcgtcac ctgcaaggcc 540
agtcagaatg tgggtactaa tgtagcctgg tatcaacaga aaccaggaca atctcctaaa 600
ccactgattt actcggcaac ctaccggaac agtggagtcc ctgatcgctt cacaggcagt 660
ggatctggga cagattccac tctcaccatc actaacgtgc agtctaaaga cttggcagac 720
tatttctgtc aacaatataa caggtatccg tacacgtccg gaggggggac caagctggag 780
atcaaacggg cggccgcaat tgaagttatg tatcctcctc cttacctaga caatgagaag 840
agcaatggaa ccattatcca tgtgaaaggg aaacaccttt gtcccaagtc ccctatttcc 900
cggaccttct aagccctttg ggtgctggtg gtggttggtg gagtcctggc ttgctatagc 960
cgctagtaac agtggccttt attattttct gggtgaggag taagaggagc aggctcctgc 1020
acagtgacta catgaacatg actccccgcc gccccgggcc cacccgcaag cattaccagc 1080
cctatgcccc accacgcgac ttcgcagcct atcgctccag agtgaagttc agcaggagcg 1140
cagagccccc cgcgtaccag cagggccaga accagctcta taacgagctc aatctaggac 1200
gaagagagga gtacgatgtt ttggacaaga gacgtggccg ggaccctgag atggggggaa 1260
agccgagaag gaagaaccct caggaaggcc tgtacaatga actgcagaaa gataagatgg 1320
cggaggccta cagtgagatt gggatgaaag gcgagcgccg gaggggcaag gggcacgatg 1380
gcctttacca gggtctcagt acagccacca aggacaccta cgacgccctt cacatgcagg 1440
ccctgccccc tcgcggatct ggagcaacaa acttctcact actcaaacaa gcaggtgacg 1500
tggaggagaa tcccggaccc atggagacag acacactcct gctatgggta ctgctgctct 1560
gggttccagg ttccactggt gaccaggtgc agctggtgga gtctggggga ggcgtggtcc 1620
agcctgggag gtccctgaga ctcgactgta aagcgtctgg aatcaccttc agtaactctg 1680
gcatgcactg ggtccgccag gctccaggca aggggctgga gtgggtggca gttatttggt 1740
atgatggaag taaaagatac tatgcagact ccgtgaaggg ccgattcacc atctccagag 1800
acaattccaa gaacacgctg tttctgcaaa tgaacagcct gagagccgag gacacggctg 1860
tgtattactg tgcgacaaac gacgactact ggggccaggg aaccctggtc accgtctcct 1920
caggtggagg tggatcaggt ggaggtggat ctggtggagg tggatctgaa attgtgttga 1980
cacagtctcc agccaccctg tctttgtctc caggggaaag agccaccctc tcctgcaggg 2040
ccagtcagag tgttagtagt tacttagcct ggtaccaaca gaaacctggc caggctccca 2100
ggctcctcat ctatgatgca tccaacaggg ccactggcat cccagccagg ttcagtggca 2160
gtgggtctgg gacagacttc actctcacca tcagcagcct agagcctgaa gattttgcag 2220
tttattactg tcagcagagt agcaactggc ctcggacgtt cggccaaggg accaaggtgg 2280
aaatcaaaga acaaaaactc atctcagaag aggatctgta actcgaggat cc 2332
<210> 24
<211> 1640
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 24
catggctctc ccagtgactg ccctactgct tcccctagcg cttctcctgc atgcagaggt 60
gaagctgcag gagtcagggg gaggcttcgt gaagcctgga gggtccctca aagtctcctg 120
tgcagcctct ggattcactt tcagtagcta tgccatgtcc tgggttcgcc tgagtccgga 180
gatgaggctg gagtgggtcg caaccattag cagtgctggt ggttacatct tctattctga 240
cagtgtgcag ggacgattca ccatttccag agacaatgcc aagaacaccc tgcacctgca 300
aatgggcagt ctgaggtctg gggacacggc catgtattac tgtgcaaggc agggatttgg 360
taactacggt gattactatg ctatggacta ctggggccaa gggaccacgg tcaccgtctc 420
ctcaggtgga ggtggatcag gtggaggtgg atctggtgga ggtggatctg acattgagct 480
cacccagtct ccatcctccc tggctgtgtc agcaggagag aaggtcacta tgagctgcaa 540
atccagtcag agtctgctca acagtagaac ccgaaagaac cagttggctt ggtaccagca 600
aaaaccagga cagtctcctg aactgctgat ctactgggca tccactaggc aatctggagt 660
ccctgatcgc ttcacaggca gtggatctgg gacagatttc actctcacca tcagcagtgt 720
gcaggctgaa gacctggcag tttattactg ccagcaatct tataatctac tgcaacaaac 780
ttctcactac tcaaacaagc aggtgacgtg gaggagaatc ccggacccat ggagacagac 840
acactcctgc tatgggtact gctgctctgg gttccaggtt ccactggtga ccaggtgcag 900
ctggtggagt ctgggggagg cgtggtccag cctgggaggt ccctgagact cgactgtaaa 960
gcgtctggaa tcaccttcag taactctggc atgcactggg tccgccaggc tccaggcaag 1020
gggctggagt gggtggcagt tatttggtat gatggaagta aaagatacta tgcagactcc 1080
gtgaagggcc gattcaccat ctccagagac aattccaaga acacgctgtt tctgcaaatg 1140
aacagcctga gagccgagga cacggctgtg tattactgtg cgacaaacga cgactactgg 1200
ggccagggaa ccctggtcac cgtctcctca ggtggaggtg gatcaggtgg aggtggatct 1260
ggtggaggtg gatctgaaat tgtgttgaca cagtctccag ccaccctgtc tttgtctcca 1320
ggggaaagag ccaccctctc ctgcagggcc agtcagagtg ttagtagtta cttagcctgg 1380
taccaacaga aacctggcca ggctcccagg ctcctcatct atgatgcatc caacagggcc 1440
actggcatcc cagccaggtt cagtggcagt gggtctggga cagacttcac tctcaccatc 1500
agcagcctag agcctgaaga ttttgcagtt tattactgtc agcagagtag caactggcct 1560
cggacgttcg gccaagggac caaggtggaa atcaaagaac aaaaactcat ctcagaagag 1620
gatctgtaac tcgaggatcc 1640
<210> 25
<211> 1266
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 25
atggagacag acacactcct gctatgggta ctgctgctct gggttccagg ttccactggt 60
gacatgggat tgggactgca gtgggttttc tttgttgctc ttttaaaagg tgtccactgt 120
gaggtgcggc ttctggagtc tggtggagga ttagtgaagc ctgaggggtc actgaaactc 180
tcctgtgtgg cctctggatt caccttcagt gactatttca tgagctgggt ccgccaggct 240
ccagggaagg ggctggagtg ggttgctcac atatacacga aaagttataa ttatgcaact 300
tattactcgg gttcggtgaa aggcagattc accatctcca gagatgattc ccgaagcatg 360
gtctacctgc aaatgaacaa cctgagaact gaggacacgg ccacttatta ctgtacaaga 420
gatggaagcg gatatccctc tctggatttc tggggtcaag ggacccaagt cactgtctcc 480
tcagccacaa caacagcccc atctgtctat cccttggccc ctgcctgtga cagcacaacc 540
aaatcgggtg gaggtggatc aggtggaggt ggatctggtg gaggtggatc ttatgagctg 600
actcagccac cttcagcatc agtcaatgta ggagagactg tcaaaatcac ctgctctggg 660
gaccaattgc cgaaatattt tgcagattgg tttcatcaaa ggtcagacca gaccattttg 720
caagtgatat atgatgataa taagcgcccc tcggggatcc ctgaaagaat ctctgggtcc 780
agctcaggga caacagccac cttgaccatc agagatgtcc gggctgagga tgaaggtgac 840
tattactgtt tctcaggata tgttgatagt gatagcaaat tgtatgtttt tggcagcgga 900
acccagctca ccgtcctagg tggacccaag tcttctccca aagtcacagt gtttccacct 960
tcacctgagg agctccggac aaacaaagcc acactggtgt gtctggttaa tgacttctac 1020
ccgggttctg caacagtgac ctggaaggca aatggagcaa ctatcaatga tggggtgaag 1080
actacaaagc cttccaaaca gggccaaaac tacatgacca gcagctacct aagtttgaca 1140
gcagaccagt ggaaatctca caacagggtt tcctgccaag ttacccatga aggggaaact 1200
gtggagaaga gtttgtcccc tgcagaatgt ctcgaacaaa aactcatctc agaagaggat 1260
ctgtaa 1266
<210> 26
<211> 3325
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 26
catggctctc ccagtgactc ccctactgct acccctagcg ttctcctgca tgcagaggtg 60
aagctgcagc agtctggggc tgagctggtg aggcctgggt cctcagtgaa gatttcctgc 120
aaggcttctg gctatgcatt cagtagctac tggatgaact gggtgaagca gaggcctgga 180
cagggtcttg agtggattgg acagatttat cctggagatg gtgatactaa ctacaatgga 240
aagttcaagg gtcaagccac actgactgca gacaaatcct ccagcacagc ctacatgcag 300
ctcagcggcc taacatctga ggactctgcg gtctatttct gtgcaagaaa gaccattagt 360
tcggtagtag atttctactt tgactactgc ggccaaggga ccacggtcac cgtctcctca 420
ggtggaggtg ggcaggggag gtggatctgg ggaggtggat ctgacattga gctcacccag 480
tctccaaaat tcatgtccac atcagtagga cacagggtca gcgtcacctg caaggccagt 540
cagaatgtgg gtactaatgt agcctggtat caacagaaac caggacaatc tcctaaacca 600
ctgatttact cggcaaccta ccggaacagt ggagtccctg agcgcttcac aggcagtgga 660
tctgggacag atttcactct caccatcact aacgtgcagt ctaaagactt ggcagactat 720
ttctgtcaac aatataacag gtagccgtac acgtccggag gggggaccaa gctggagatc 780
aaacgggcgg ccgcaattga gttcatgtac cctccgcctt acctagacaa cgagaggagc 840
aatggaacta ttattcacat aaaagagaaa catctttgtc atactcagtc atctcctaag 900
ctgttttggg cactggtcgt ggttgtggag tcctgttttg ttatggcttg ctagtgacag 960
tggctcttgt gttatctgga caaatagtag aaggaacaga ctccttcaaa gtgactacat 1020
gaacatgact ccccggaggg cagggctcac tcgaaagcct taccagccct acgcccctgc 1080
cagagacttt gcagcgtacc gccccagagc aaaattcagc aggagtgcag agactgctgc 1140
caacctgcag gaccccaacc agctctacaa tgagctcaat ctagggcgaa gagaggaata 1200
tgacgtcttg gagaagaagc cggctcggga tccagagatg gcagccaaac agcagaggag 1260
caggaacccc caggaaggcg tatacaatgc actgcagaaa gacaagatgg cagaagccta 1320
cagtgagatc ggcacaaaag gcgagaggcg gagaggcaag gggcacgatg gcctttacca 1380
gggtctcagc actgccacca aggacaccta tgatgggctg catatgcaga ccctggcccc 1440
tcgctaacag ccactcgagg atccgcccct ctccctcccc cccccctaac gttactggcc 1500
gaagccgctt ggaataaggc cggtgtgcgt ttgactatat gttattttcc accatattgc 1560
cgtcttttgg caatgtgagg gcccggaaac ctggccctgt cttcttgacg agcattccta 1620
ggggtctttc ccctctcgcc aaaggaatgc agggtctgtt gaatgtcgtg aaggaagcag 1680
ttcctctgga agcttcttga agacaaacaa cgtctgtagc gaccctttgc aggcagcgga 1740
accccccacc tggcgacagg tgcctcagcg accaaaggcc acgtgtataa gatacaccag 1800
caaaggcggc acaaccccag tgccacgttg tgagttggat agttgtggaa agagtcaaat 1860
ggctctcctc aagcgtattc aacaaggggc tgaaggatgc ccagaaggta ccccattgta 1920
tgggatctga tctggggcct cggtcacatg ctttacatgt gtttagtcga ggttaaaaaa 1980
acgtctaggc cccccgaacc acggggacgt ggttttcctt tgaaaaacac gatgataata 2040
tggccacaaa ctgccatgga gacagacaca ctcctgctaa gggtactgct gctctgggtt 2100
ccaggttcca ctggagacat gggattggga ctgcagaggg ttttctttgt tgctctttta 2160
aaaggtgtcc actgtgaggt gcggcttctg gagtctggtg gaggattagt gaagcctgag 2220
gggtcactga aatctcctgt gtggcctcag gattcacctt cagagactat ttcatgagct 2280
gggtccgcca ggctccaggg aaggggctgg agtgggttgc tcacatatac acgaaaagtt 2340
ataattatgc aacttattac tcgggttcgg tgaaaggcag attcaccatc tccagagatg 2400
attcccgaag catggtctac cgcaaatgaa caacctgaga actgaggaca cggccactta 2460
ttactgtaca agagatggaa gcggatatcc ctctctggat ttctggggtc aagggaccca 2520
agtcactgtc tcctcagcca caacaacagc cccatctgtc tatcccttgg cccctgcctg 2580
tgacagcaca accaaatcgg gtggaggtgg atcaggtgga ggtggatctg gtggaggtgg 2640
atcttatgag ctgactcagc caccttcagc atcagtcaat gtaggagaga ctgtcaaaat 2700
cacctgctct ggggaccaat tgccgaaata ttttgcagat tggtttcatc aaaggtcaga 2760
ccagaccatt ttgcaagtga tatatgatga taataagcgc ccctcgggga tccctgaaag 2820
aatctctggg tccagctcag ggacaacagc caccttgacc atcagagatg tccgggctga 2880
ggatgaaggt gactattact gtttctcagg atatgttgat agtgatagca aattgtatgt 2940
ttttggcagc ggaacccagc tcaccgtcct aggtggaccc aagtcttctc ccaaagtcac 3000
agtgtttcca ccttcacctg aggagctccg gacaaacaaa gccacactgg tgtgtctggt 3060
taatgacttc tacccgggtt ctgcaacagt gacctggaag gcaaatggag caactatcaa 3120
tgatggggtg aagactacaa agccttccaa acagggccaa aactacatga ccagcagcta 3180
cctaagtttg acagcagacc agtggaaatc tcacaacagg gtttcctgcc aagttaccca 3240
tgaaggggaa actgtggaga agagtttgtc ccctgcagaa tgtctcgaac aaaaactcat 3300
ctcagaagag gatctgtaac tggag 3325
<210> 27
<211> 3333
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 27
ctctcccagt gactgcccta ctgcttcccc tagcgctact cctgcatgca gaggtgaagc 60
tgcaggagtc agggggaggc ttcgtgaagc ctggagggtc cctcaaagtc tcctgtgcag 120
cctctggatt cactttcagt agctatgcca tgtcctgggt tcgcctgagt ccggagatga 180
ggctggagtg ggtcgcaacc attagcagtg ctggtggtta catcttctat tctgacagtg 240
tgcagggacg attcaccatt tccagagaca atgccaagaa caccctgcac ctgcaaatgg 300
gcagtctgag gtctggggac agggccatgt attactgtgc aaggcaggga tttggtaact 360
acggtgatta ctatgctatg gactactggg gccaagggac cacggtcacc gtctcctcag 420
gtggaggtgg atcaggtgga ggtggatctg gtggaggtgg atctgacatt gagctcaccc 480
agtctccatc ctccctggct gtgtcagcag gagagaaggt cactatgagc tgcaaatcca 540
gtcagagtct gctcaacagt agaacccgaa agaaccagtt ggcttggtac cagcaaaaac 600
caggacagtc tcctgaactg ctgatctact gggcatccac taggcaatct ggagtccctg 660
atcgcttcac aggcagtgga tctgggacag atttcactct caccatcagc agtgtgcagg 720
ctgaagacct ggcagtttat tactgccagc aatcttataa tctactggga ccaagctgga 780
gatcaaacgg gcggccgcaa ttgagttcat gtaccctccg ccttacctag acaacgagag 840
gagcaatgga actattattc acataaaaga gaaacatctt tgtcatactc agtcatctcc 900
taagctgttt tgggcactgg tcgtggttgc tggagtccag ttttgttatg gcttgctagt 960
gacagtggct ctttgtgtta tctggacaaa tagtagaagg aacagactcc ttcaaagtga 1020
ctacatgaac atgactcccc ggaggcctgg gctcactcga aagccttacc agccctacgc 1080
ccctgccaga gactttgcag cgtaccggcc cagagcaaaa ttcagcagga gtgcagagac 1140
tgctgccaac ctgcaggacc ccaaccagct ctacaatgag ctcaatctag ggcgaagaga 1200
ggaatatgac gtcttggaga agaagcggcc tcgggatcca gagatgggag gcaaacagca 1260
gaggaggagc aacccccagg aaggcgtata caatgcactg cagaaagaca agatggcaga 1320
agcctacagt gagatcggca caaaaggcga gaggcggaga ggcaaggggc acgatggcct 1380
ttaccagggt ctcagcactg ccaccaagga cacctatgat gccctgcata tgcagaccct 1440
ggcccctcgc taacagccac tcgaggatcc gcccctctcc ctcccccccc cctaacgtta 1500
ctggccgaag ccgcttggaa taaggccggt gtgcgtttgt ctatatgtta ttttccacca 1560
tattgccgtc ttttggcaat gtgagggccc ggaaacctgg ccctgtcttc ttgacgagca 1620
ttcctagggg tctttcccct ctcgccaaag gaatgcaggg tctgttgaat gtcgtgaagg 1680
aagcagttcc tctggaagct tcttgaagac aaacaacgtc tgtagcgacc ctttgcaggc 1740
agcggaaccc cccacctggc gacaggtgcc tctgcgacca aaggccacgt gtataagata 1800
cacctgcaaa ggcggcacaa ccccagtgcc acgttgtgag ttggatagtt gtggaaagag 1860
tcaaatggct ctcctcaagc gtattcaaca aggggctgaa ggatgcccag aaggtacccc 1920
attgtatggg atctgatctg gggcctcggt cacatgcttt acatgtgttt agtcgaggtt 1980
aaaaaaacgt ctaggccccc cgaaccacgg ggacgtggtt ttcctttgaa aaacacgatg 2040
ataatatggc cacaaactgc catggagaca gacacactcc tgctatgggt actgctgctc 2100
tgggttccag gttccactgg tgacatggga ttgggactgc agtgggtttt ctttgttgct 2160
cttttaaaag gtgtccactg tgaggtgcgg cttctggagt ctggtggagg attagtgaag 2220
cctgaggggt cactgaaact ctcctgtgtg gcctctggat tcaccttcag tgactatttc 2280
atgagctggg tccgccaggc tccagggaag gggctggagt gggttgctca catatacacg 2340
aaaagttata attatgcaac ttattactcg ggttcggtga aaggcagatt caccatctcc 2400
agagatgatt cccgaagcat ggtctacctg caaatgaaca acctgagaac tgaggacacg 2460
gccacttatt actgtacaag agatggaagc ggatatccct ctctggattt ctggggtcaa 2520
gggacccaag tcactgtctc ctcagccaca acaacagccc catctgtcta tcccttggcc 2580
cctgcctgtg acagcacaac caaatcgggt ggaggtggat caggtggagg tggatctggt 2640
ggaggtggat cttatgagct gactcagcca ccttcagcat cagtcaatgt aggagagact 2700
gtcaaaatca cctgctctgg ggaccaattg ccgaaatatt ttgcagattg gtttcatcaa 2760
aggtcagacc agaccatttt gcaagtgata tatgatgata ataagcgccc ctcggggatc 2820
cctgaaagaa tctctgggtc cagctcaggg acaacagcca ccttgaccat cagagatgtc 2880
cgggctgagg atgaaggtga ctattactgt ttctcaggat atgttgatag tgatagcaaa 2940
ttgtatgttt ttggcagcgg aacccagctc accgtcctag gtggacccaa gtcttctccc 3000
aaagtcacag tgtttccacc ttcacctgag gagctccgga caaacaaagc cacactggtg 3060
tgtctggtta atgacttcta cccgggttct gcaacagtga cctggaaggc aaatggagca 3120
actatcaatg atggcgtgaa gactacaaag ccttccaaac agggccaaaa ctacatgacc 3180
agcagctacc taagtttgac agcagaccag tggaaatctc acaacagggt ttcctgccaa 3240
gttacccatg aaggggaaac tgtggagaag agtttgtccc ctgcagaatg tctcgaacaa 3300
aaactcatct cagaagagga tctgtaactc gag 3333
<210> 28
<211> 34
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Description of Artificial Sequence: Synthetic
primer
<400> 28
tgaggagacg gtgaccgtgg tcccttggcc ccag 34
<210> 29
<211> 22
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический праймер
<400> 29
aggtsmarct gcagsagtcw gg 22
<210> 30
<211> 22
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический праймер
<400> 30
gttagatctc cagcttggtc cc 22
<210> 31
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический праймер
<400> 31
gacattcagc tgacccagtc tcca 24
<210> 32
<211> 32
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический праймер
<400> 32
ggctgcagst tcagtggcag tggrtcwggr ac 32
<210> 33
<211> 30
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический праймер
<400> 33
ctcattcctg ttgaagctct tgacaatggg 30
<210> 34
<211> 36
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический праймер
<400> 34
atatccatgg cagacgtcca gatgatccag tctcca 36
<210> 35
<211> 35
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический праймер
<400> 35
atatccatgg cagacattgt gctgactcag tctcc 35
<210> 36
<211> 36
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический праймер
<400> 36
atatccatgg cagatgttgt gatgacccaa actcca 36
<210> 37
<211> 35
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический праймер
<400> 37
atatccatgg cacaaattgt tctcacccag tctcc 35
<210> 38
<211> 36
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический праймер
<400> 38
atatccatgg cagacattgt gatgacacag tctcca 36
<210> 39
<211> 36
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический праймер
<400> 39
atatccatgg cagatattgt gatgacgcag gctgca 36
<210> 40
<211> 34
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический праймер
<400> 40
atatccatgg cagacattgt gatgacccag tctc 34
<210> 41
<211> 33
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический праймер
<400> 41
gcttcaacag gaatgagtgt taactcgagg tag 33
<210> 42
<211> 93
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический праймер
<400> 42
ccatggagac agacacactc ctgctatggg tactgctgct ctgggttcca ggttccactg 60
gtgacgaggt gctgcagctg gtggagtccg ggg 93
<210> 43
<211> 75
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический праймер
<400> 43
agatccacct ccaccagatc cacctccacc tgatccacct ccacctgagg agacggtgac 60
tgaggttcct tgacc 75
<210> 44
<211> 75
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический праймер
<400> 44
ggtggaggtg gatcaggtgg aggtggatct ggtggaggtg gatctgacat tgtgatgact 60
cagtctccag ccacc 75
<210> 45
<211> 71
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический праймер
<400> 45
ctcgagttac agatcctctt ctgagatgag tttttgttgt ttgatttcca gcttggtgcc 60
tccaccgaac g 71
<210> 46
<211> 93
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический праймер
<400> 46
tataccatgg ccttaccagt gaccgccttg ctcctgccgc tggccttgct gctccacgcc 60
gccaggccgg aggtgcagct ggtggagtcc ggg 93
<210> 47
<211> 37
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический праймер
<400> 47
cacgtgccat ggatgaggat atttgctgtc tttatat 37
<210> 48
<211> 35
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический праймер
<400> 48
ctcgagttac gtctcctcca aatgtgtatc acttt 35
<210> 49
<211> 36
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический праймер
<400> 49
tattacacgt gttacatgag gatatttgct gtcttt 36
<210> 50
<211> 41
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический праймер
<400> 50
tataggatcc tcgaggatgt tacgtctcct ccaaatgtgt a 41
<210> 51
<211> 15
<212> PRT
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический праймер
<400> 51
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10 15
<210> 52
<211> 5
<212> PRT
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический праймер
<400> 52
Gly Gly Gly Gly Ser
1 5
<210> 53
<211> 271
<212> PRT
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 53
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Glu Val Gln Leu Val Glu Ser Gly Gly Asp Leu
20 25 30
Val Lys Pro Gly Gly Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Gly Tyr Gly Met Ser Trp Val Arg Gln Thr Pro Asp Lys
50 55 60
Arg Leu Glu Trp Val Ala Thr Ile Thr Ser Gly Gly Thr Tyr Thr Tyr
65 70 75 80
Tyr Pro Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Ile Asp Ser Leu Lys Ser Glu Asp Thr
100 105 110
Ala Ile Tyr Phe Cys Ala Arg Ser Leu Ala Gly Asn Ala Met Asp Tyr
115 120 125
Trp Gly Gln Gly Thr Ser Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Met Thr Gln
145 150 155 160
Ser Pro Ala Thr Leu Ser Val Thr Pro Gly Asp Arg Val Ser Leu Ser
165 170 175
Cys Arg Ala Ser Gln Thr Ile Ser Asp Tyr Leu His Trp Tyr Gln Gln
180 185 190
Lys Ser His Glu Ser Pro Arg Leu Leu Ile Lys Phe Ala Ser Gln Ser
195 200 205
Ile Ser Gly Ile Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Ser Asp
210 215 220
Phe Thr Leu Ser Ile Asn Ser Val Glu Pro Glu Asp Val Gly Val Tyr
225 230 235 240
Tyr Cys Gln Asn Gly His Gly Phe Pro Arg Thr Phe Gly Gly Gly Thr
245 250 255
Lys Leu Glu Ile Lys Glu Gln Lys Leu Ile Ser Glu Glu Asp Leu
260 265 270
<210> 54
<211> 271
<212> PRT
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 54
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Asp Leu
20 25 30
Val Lys Pro Gly Gly Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Gly Tyr Gly Met Ser Trp Val Arg Gln Thr Pro Asp Lys
50 55 60
Arg Leu Glu Trp Val Ala Thr Ile Thr Ser Gly Gly Thr Tyr Thr Tyr
65 70 75 80
Tyr Pro Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Ile Asp Ser Leu Lys Ser Glu Asp Thr
100 105 110
Ala Ile Tyr Phe Cys Ala Arg Ser Leu Ala Gly Asn Ala Met Asp Tyr
115 120 125
Trp Gly Gln Gly Thr Ser Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Met Thr Gln
145 150 155 160
Ser Pro Ala Thr Leu Ser Val Thr Pro Gly Asp Arg Val Ser Leu Ser
165 170 175
Cys Arg Ala Ser Gln Thr Ile Ser Asp Tyr Leu His Trp Tyr Gln Gln
180 185 190
Lys Ser His Glu Ser Pro Arg Leu Leu Ile Lys Phe Ala Ser Gln Ser
195 200 205
Ile Ser Gly Ile Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Ser Asp
210 215 220
Phe Thr Leu Ser Ile Asn Ser Val Glu Pro Glu Asp Val Gly Val Tyr
225 230 235 240
Tyr Cys Gln Asn Gly His Gly Phe Pro Arg Thr Phe Gly Gly Gly Thr
245 250 255
Lys Leu Glu Ile Lys Glu Gln Lys Leu Ile Ser Glu Glu Asp Leu
260 265 270
<210> 55
<211> 266
<212> PRT
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 55
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val
20 25 30
Val Gln Pro Gly Arg Ser Leu Arg Leu Asp Cys Lys Ala Ser Gly Ile
35 40 45
Thr Phe Ser Asn Ser Gly Met His Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ala Val Ile Trp Tyr Asp Gly Ser Lys Arg Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Phe Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Thr Asn Asp Asp Tyr Trp Gly Gln Gly Thr
115 120 125
Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu
145 150 155 160
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln
165 170 175
Ser Val Ser Ser Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala
180 185 190
Pro Arg Leu Leu Ile Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro
195 200 205
Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
210 215 220
Ser Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser
225 230 235 240
Ser Asn Trp Pro Arg Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
245 250 255
Glu Gln Lys Leu Ile Ser Glu Glu Asp Leu
260 265
<210> 56
<211> 422
<212> PRT
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 56
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Met Gly Leu Gly Leu Gln Trp Val Phe Phe Val
20 25 30
Ala Leu Leu Lys Gly Val His Cys Glu Val Arg Leu Leu Glu Ser Gly
35 40 45
Gly Gly Leu Val Lys Pro Glu Gly Ser Leu Lys Leu Ser Cys Val Ala
50 55 60
Ser Gly Phe Thr Phe Ser Asp Tyr Phe Met Ser Trp Val Arg Gln Ala
65 70 75 80
Pro Gly Lys Gly Leu Glu Trp Val Ala His Ile Tyr Thr Lys Ser Tyr
85 90 95
Asn Tyr Ala Thr Tyr Tyr Ser Gly Ser Val Lys Gly Arg Phe Thr Ile
100 105 110
Ser Arg Asp Asp Ser Arg Ser Met Val Tyr Leu Gln Met Asn Asn Leu
115 120 125
Arg Thr Glu Asp Thr Ala Thr Tyr Tyr Cys Thr Arg Asp Gly Ser Gly
130 135 140
Tyr Pro Ser Leu Asp Phe Trp Gly Gln Gly Thr Gln Val Thr Val Ser
145 150 155 160
Ser Ala Thr Thr Thr Thr Ala Pro Ser Val Tyr Pro Leu Ala Pro Ala
165 170 175
Cys Asp Ser Thr Thr Lys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
180 185 190
Ser Gly Gly Gly Gly Ser Tyr Glu Leu Thr Gln Pro Pro Ser Ala Ser
195 200 205
Val Asn Val Gly Glu Thr Val Lys Ile Thr Cys Ser Gly Asp Gln Leu
210 215 220
Pro Lys Tyr Phe Ala Asp Trp Phe His Gln Arg Ser Asp Gln Thr Ile
225 230 235 240
Leu Gln Val Ile Tyr Asp Asp Asn Lys Arg Pro Ser Gly Ile Pro Glu
245 250 255
Arg Ile Ser Gly Ser Ser Ser Gly Thr Thr Ala Thr Leu Thr Ile Arg
260 265 270
Asp Val Arg Ala Glu Asp Glu Gly Asp Tyr Tyr Cys Phe Ser Gly Tyr
275 280 285
Val Asp Ser Asp Ser Lys Leu Tyr Val Phe Gly Ser Gly Thr Gln Leu
290 295 300
Thr Val Leu Gly Gly Pro Lys Ser Ser Pro Lys Val Thr Val Phe Pro
305 310 315 320
Pro Ser Pro Glu Glu Leu Arg Thr Asn Lys Ala Thr Leu Val Cys Leu
325 330 335
Val Asn Asp Phe Tyr Pro Gly Ser Ala Thr Val Thr Trp Lys Ala Asn
340 345 350
Gly Ala Thr Ile Asn Asp Gly Val Lys Thr Thr Lys Pro Ser Lys Gln
355 360 365
Gly Gln Asn Tyr Met Thr Ser Ser Tyr Leu Ser Leu Thr Ala Asp Gln
370 375 380
Trp Lys Ser His Asn Arg Val Ser Cys Gln Val Thr His Glu Gly Glu
385 390 395 400
Thr Val Glu Lys Ser Leu Ser Pro Ala Glu Cys Leu Glu Gln Lys Leu
405 410 415
Ile Ser Glu Glu Asp Leu
420
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ХИМЕРНЫЕ РЕЦЕПТОРЫ АНТИГЕНА, НАЦЕЛЕННЫЕ НА HER2 | 2016 |
|
RU2753695C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ИММУНОТЕРАПИИ | 2014 |
|
RU2729118C2 |
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ, НАЦЕЛЕННЫЕ НА РЕЦЕПТОР, СВЯЗАННЫЙ С G-БЕЛКАМИ, И ИХ ПРИМЕНЕНИЕ | 2015 |
|
RU2762359C2 |
| СПОСОБЫ ПОЛУЧЕНИЯ ЭКСПРЕССИРУЮЩИХ ХИМЕРНЫЙ АНТИГЕННЫЙ РЕЦЕПТОР КЛЕТОК | 2015 |
|
RU2751362C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ ИММУНОТЕРАПИИ | 2013 |
|
RU2832516C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ ИММУНОТЕРАПИИ | 2013 |
|
RU2729401C2 |
| ХИМЕРНЫЕ РЕЦЕПТОРЫ АНТИГЕНА, НАЦЕЛЕННЫЕ НА PSCA | 2016 |
|
RU2759879C2 |
| НЕ РЕСТРИКТИРОВАННЫЕ ПО HLA T-КЛЕТОЧНЫЕ РЕЦЕПТОРЫ И ИХ ПРИМЕНЕНИЕ | 2019 |
|
RU2812917C2 |
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ, НАЦЕЛЕННЫЕ НА АНТИГЕН СОЗРЕВАНИЯ В-КЛЕТОК, И ИХ ПРИМЕНЕНИЕ | 2015 |
|
RU2761632C2 |
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ, НАЦЕЛЕННЫЕ НА ПОДОБНЫЙ FC-РЕЦЕПТОРУ БЕЛОК 5, И ИХ ПРИМЕНЕНИЕ | 2015 |
|
RU2779747C2 |
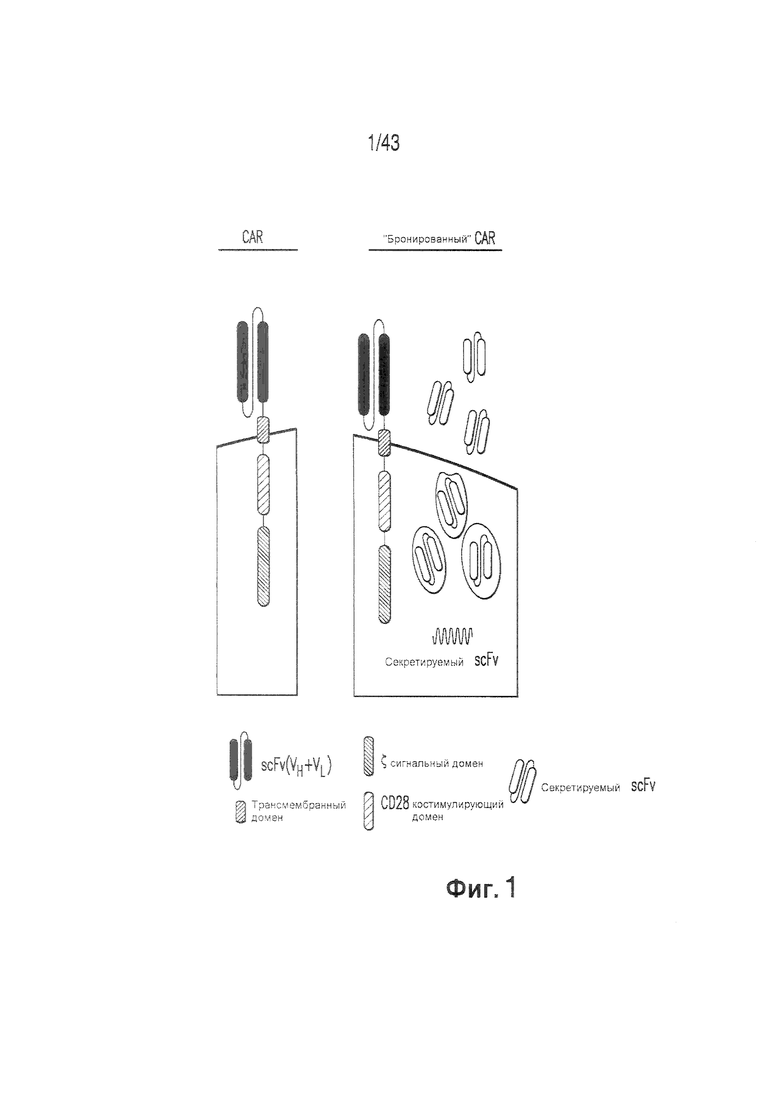

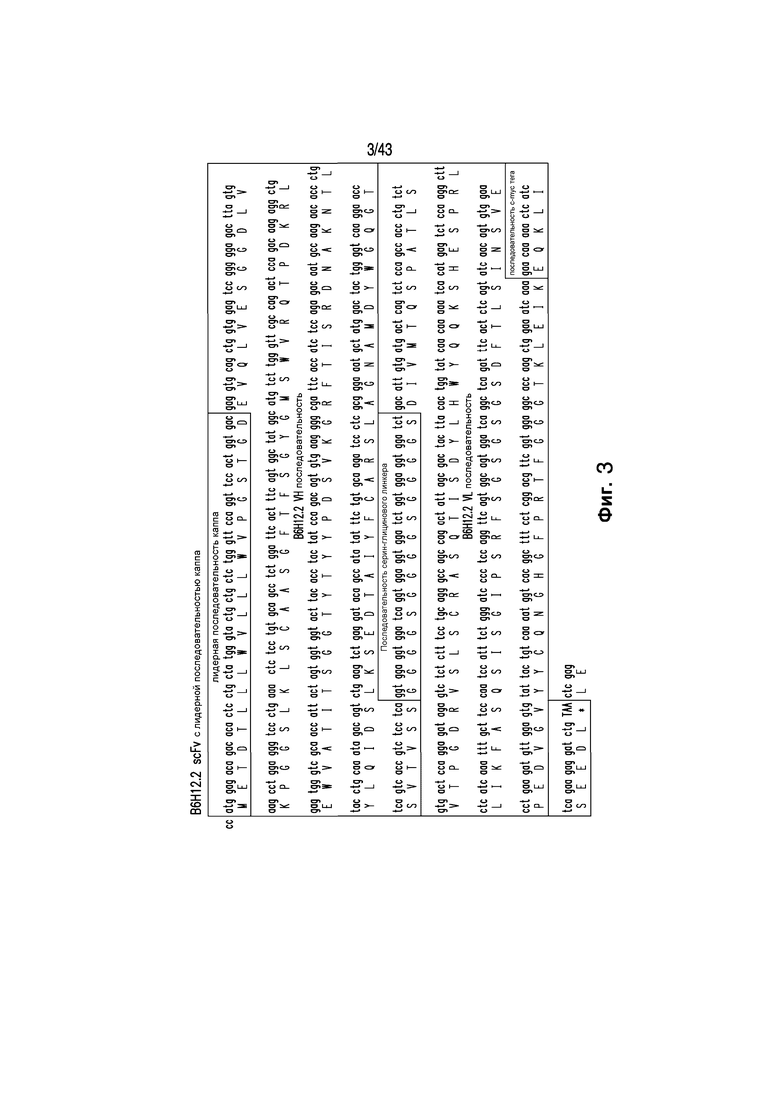
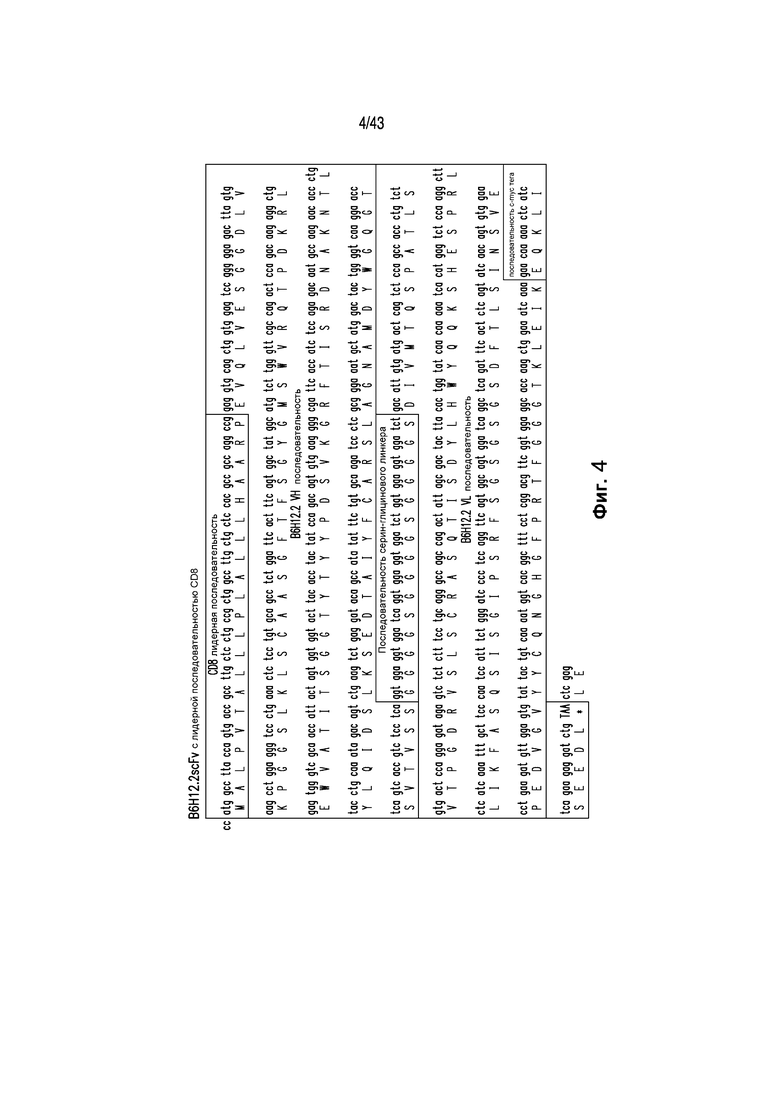


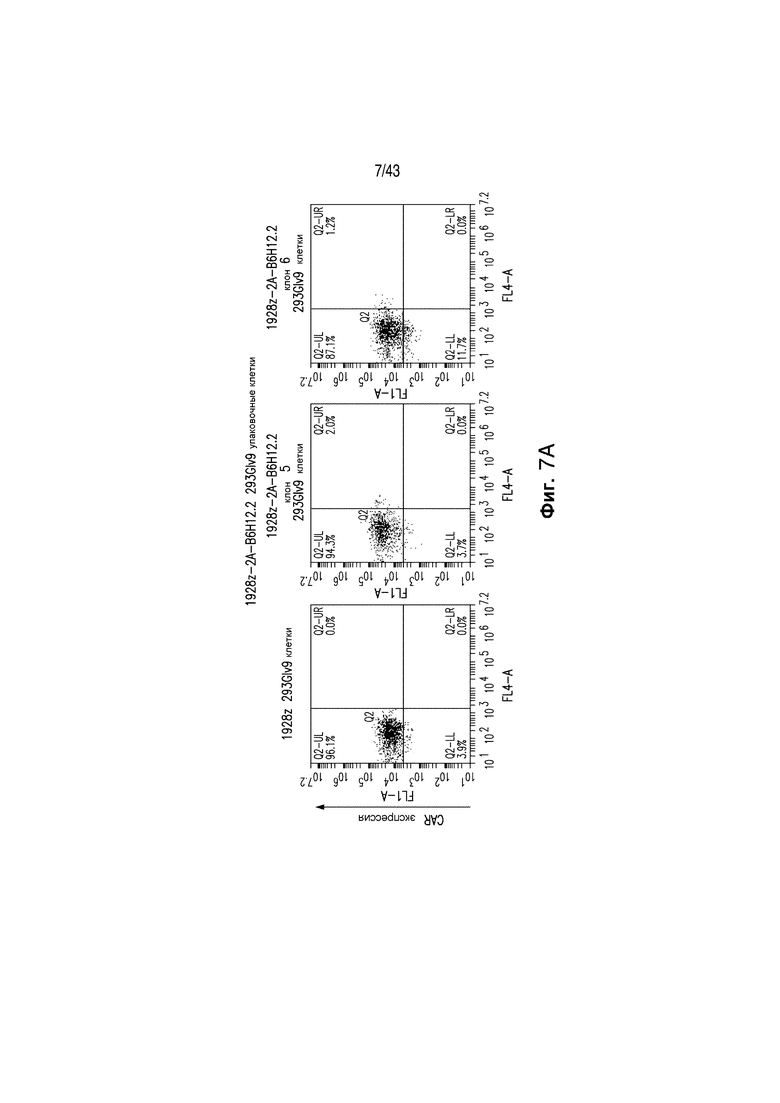
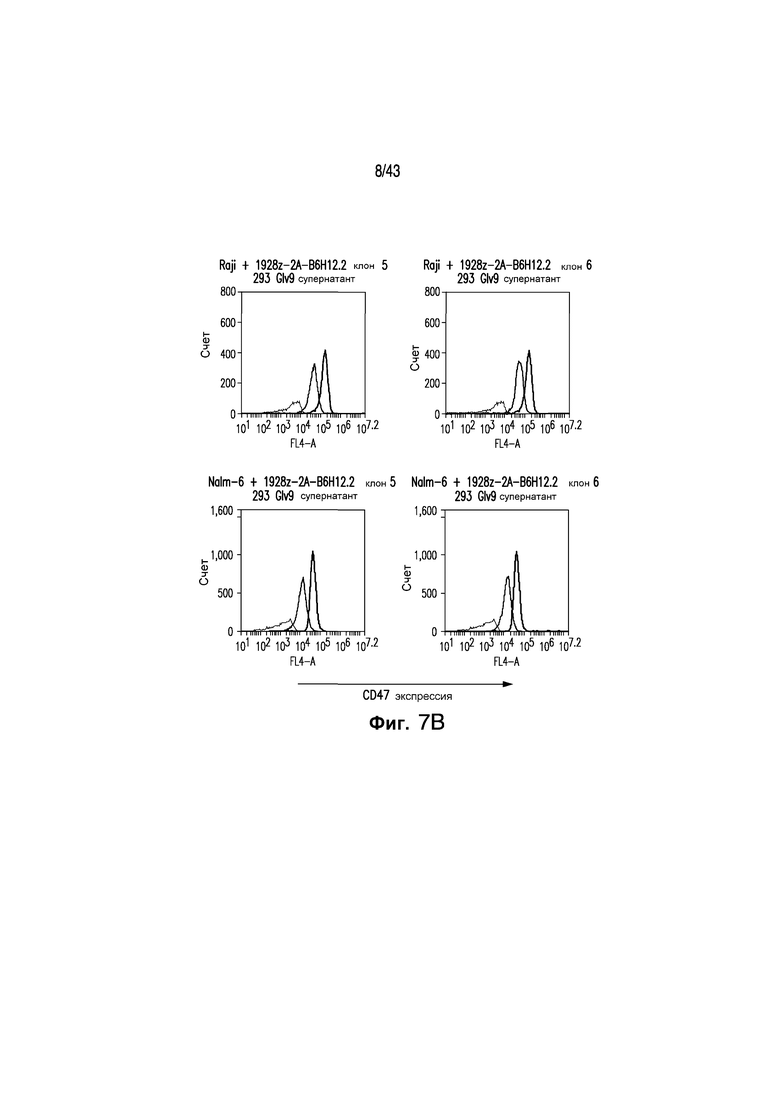
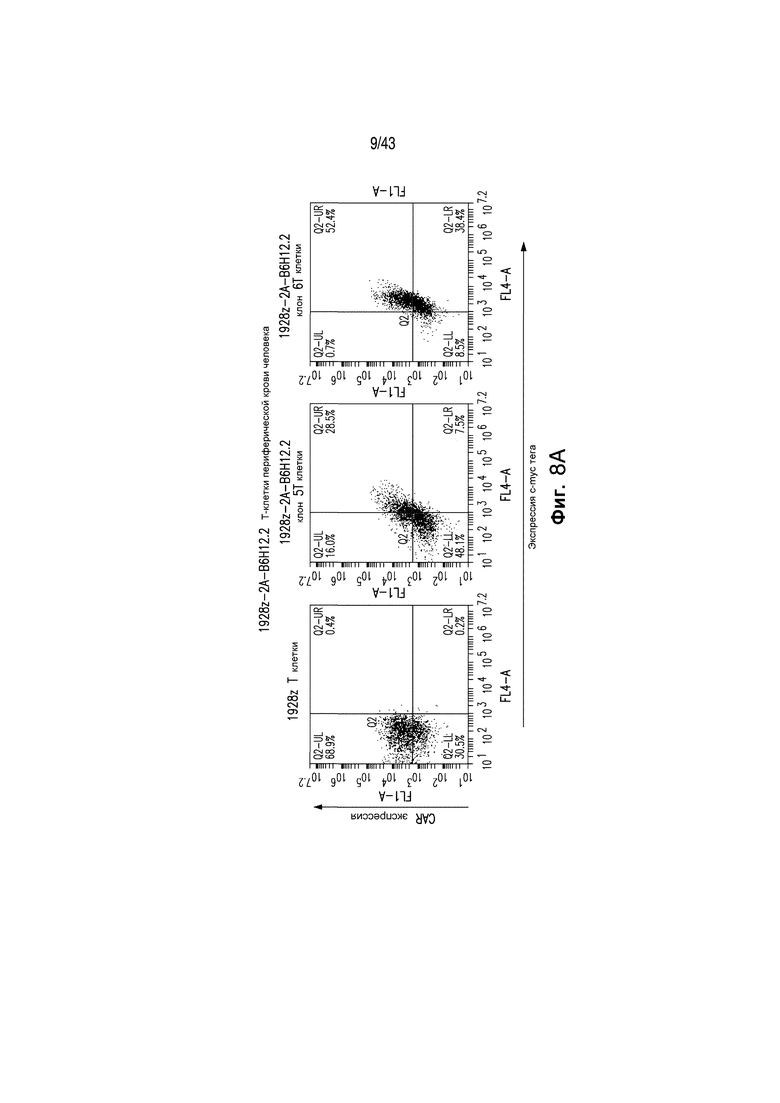
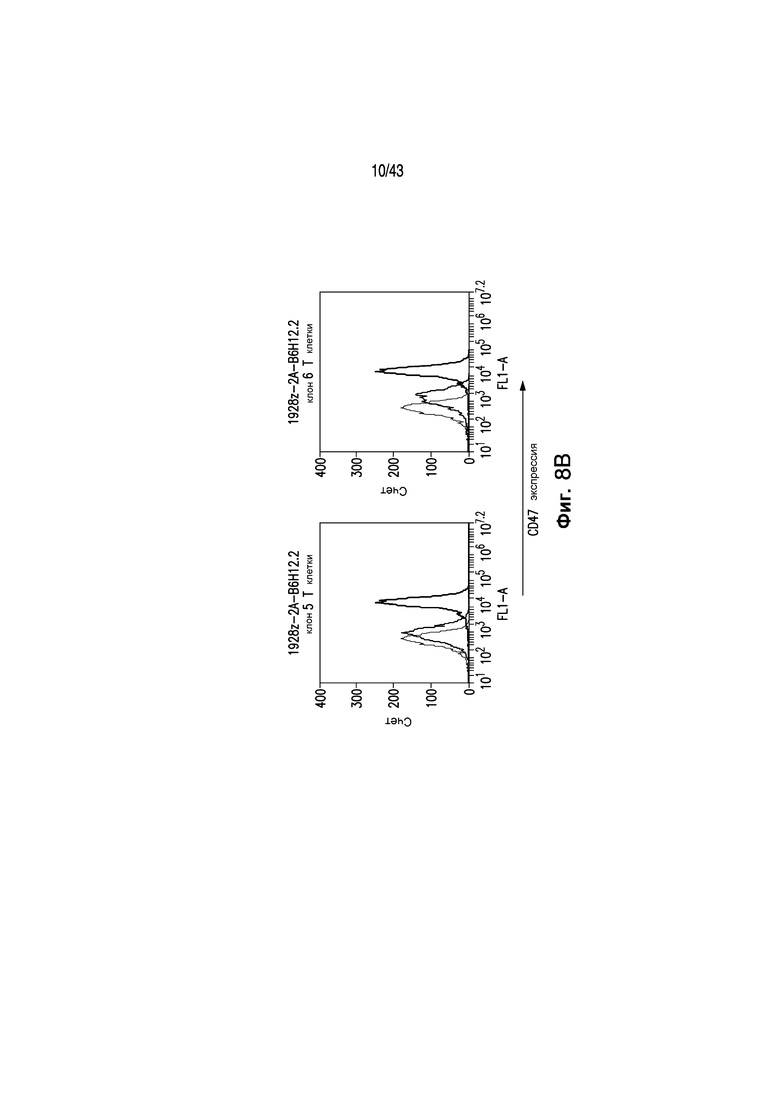
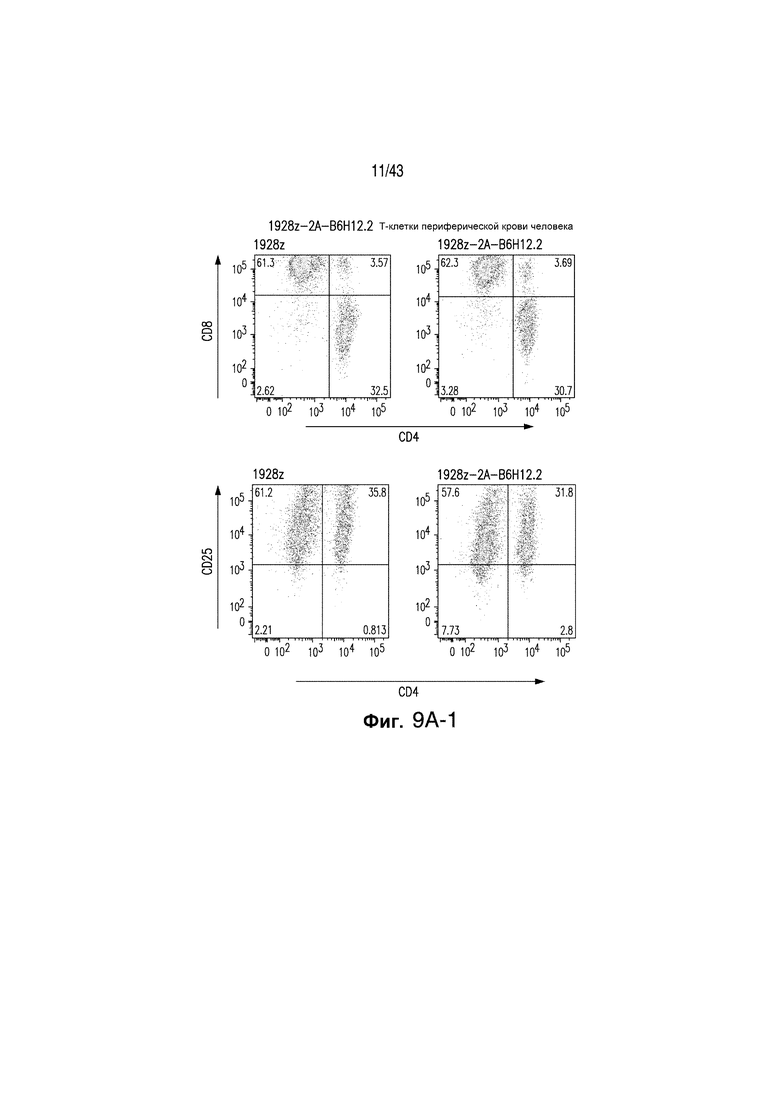
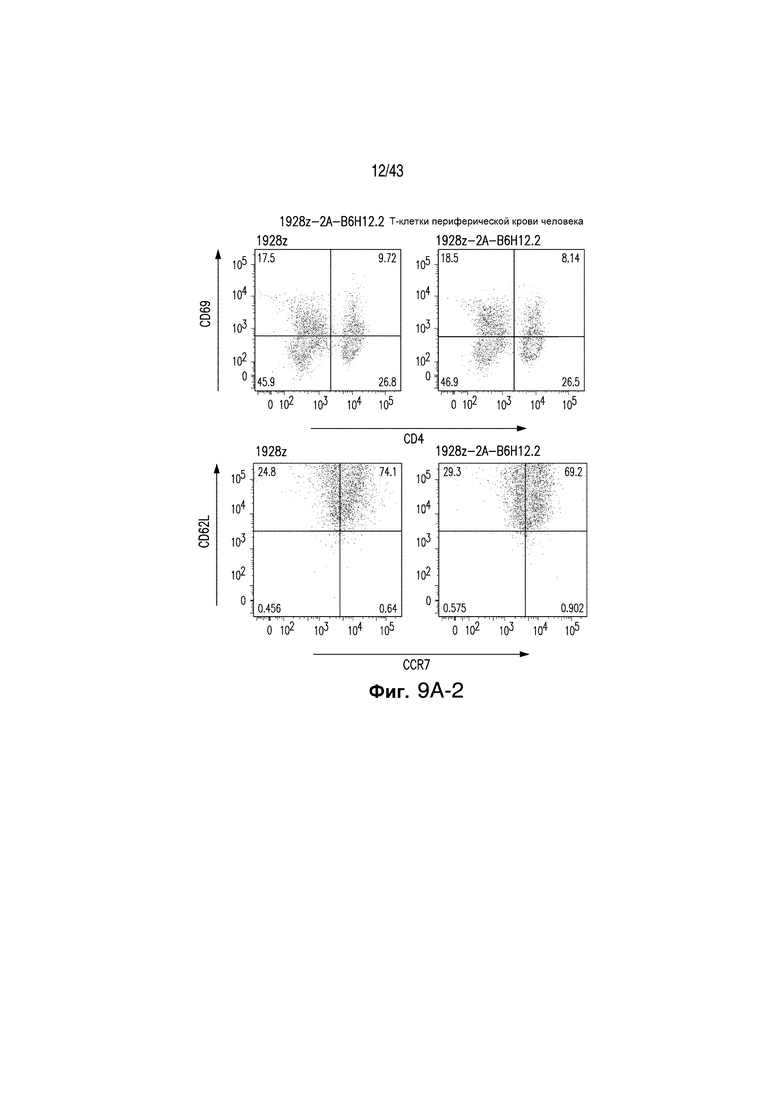
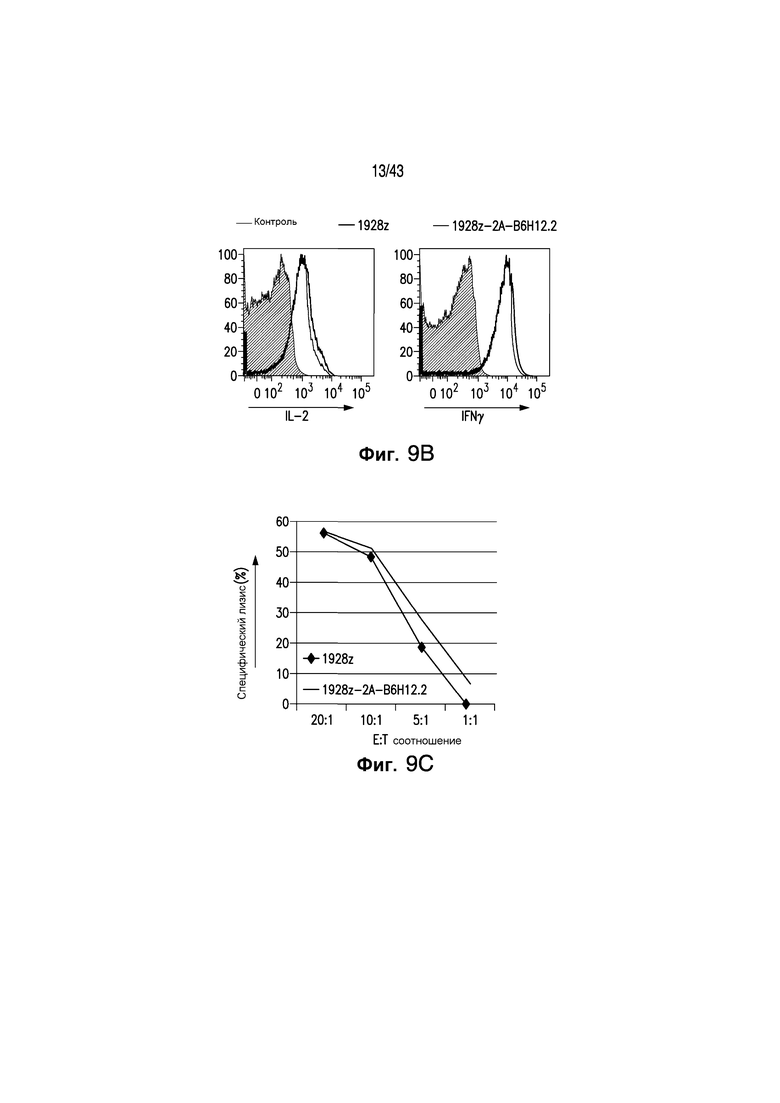
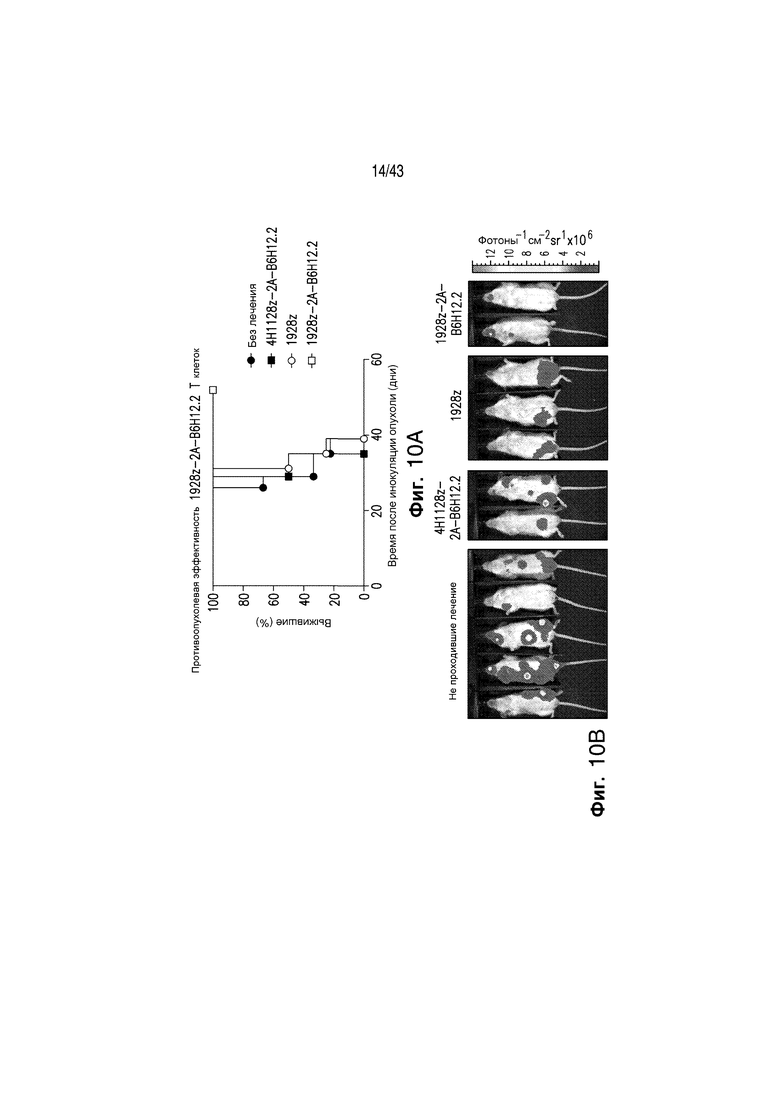
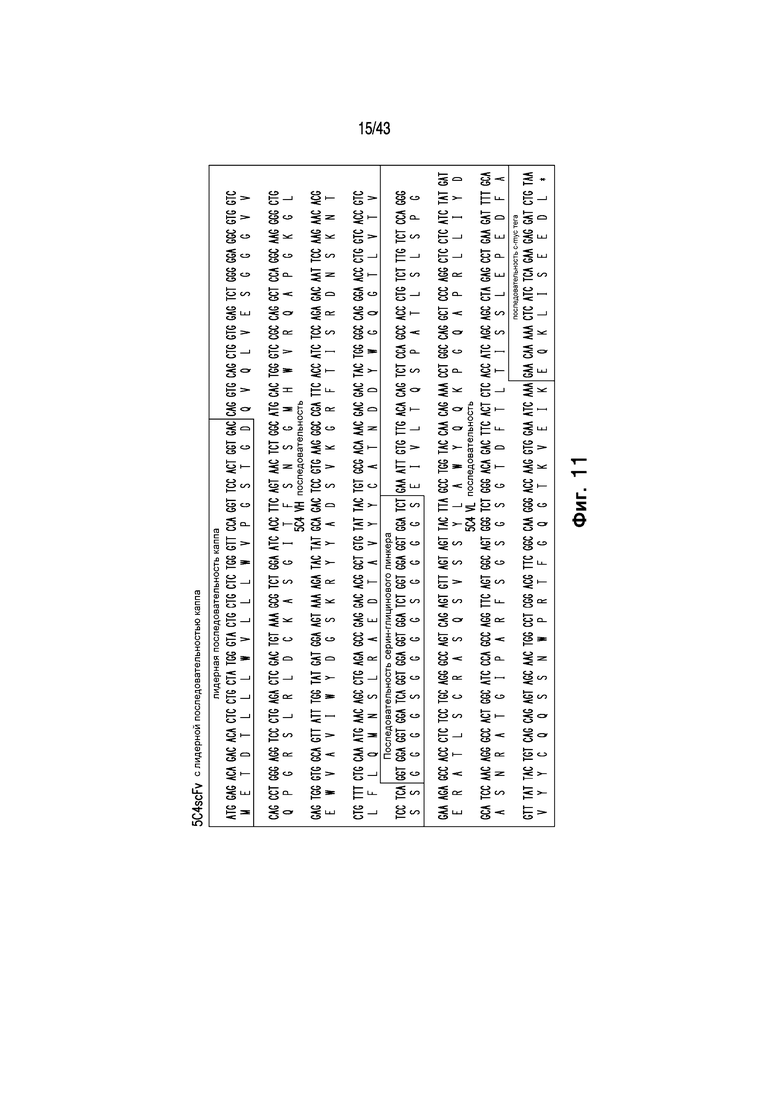


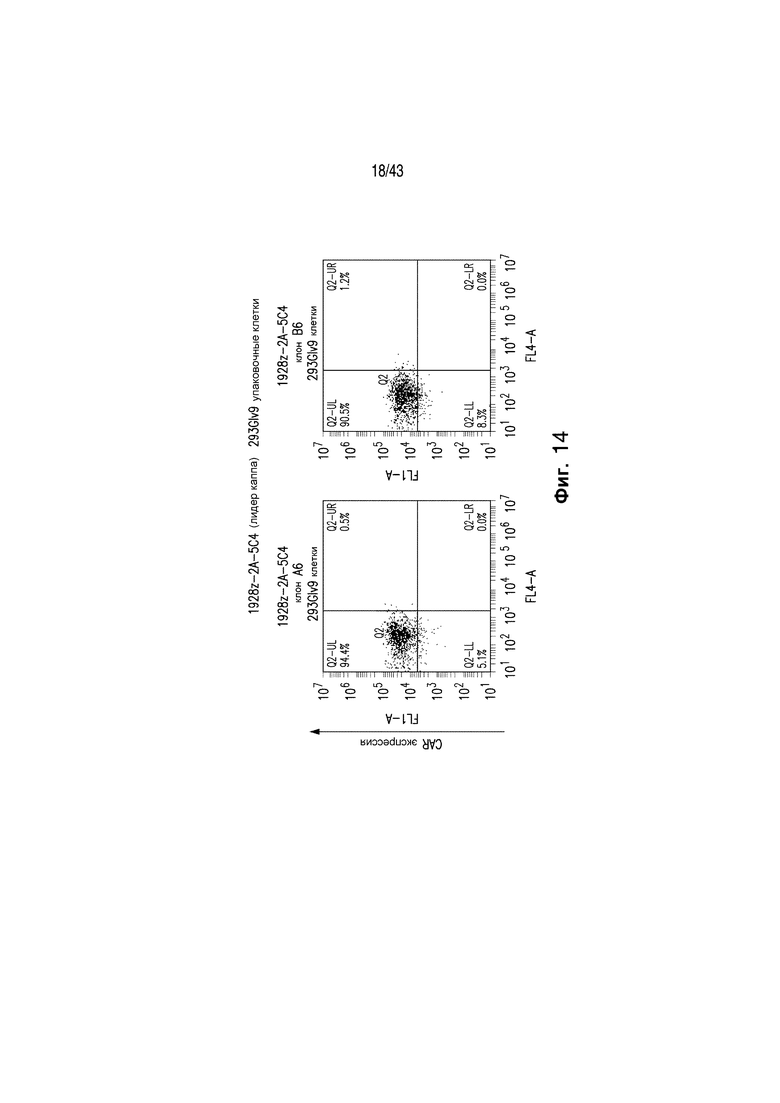
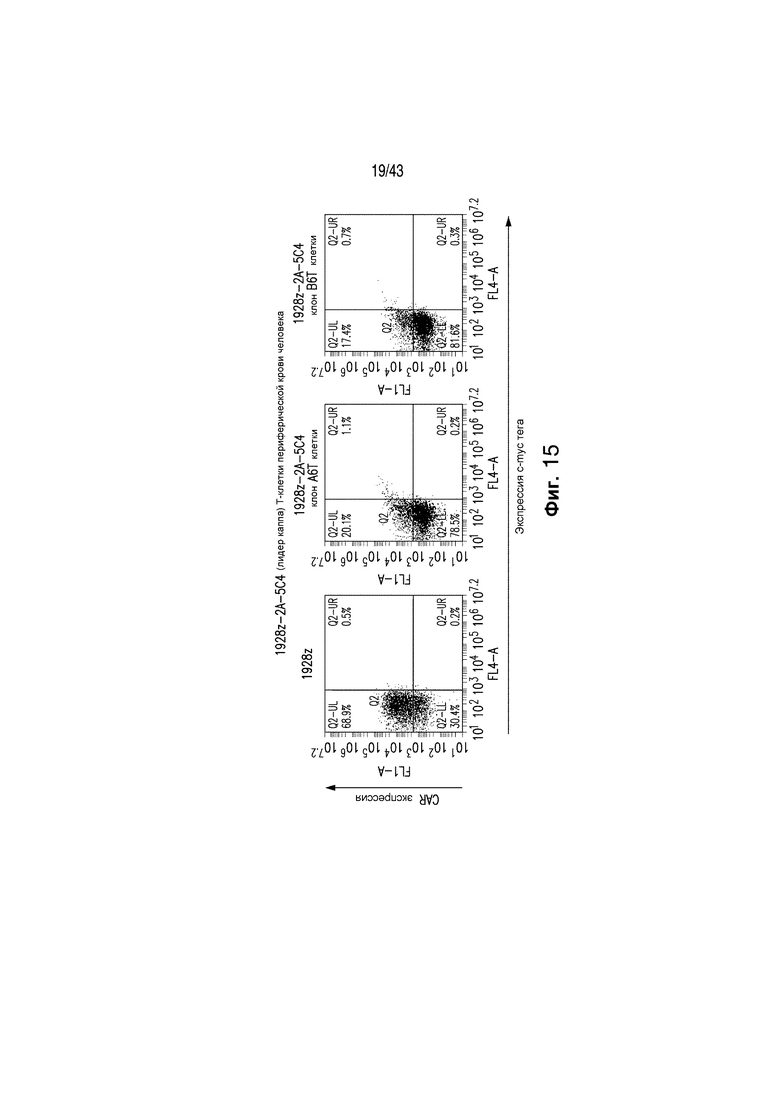
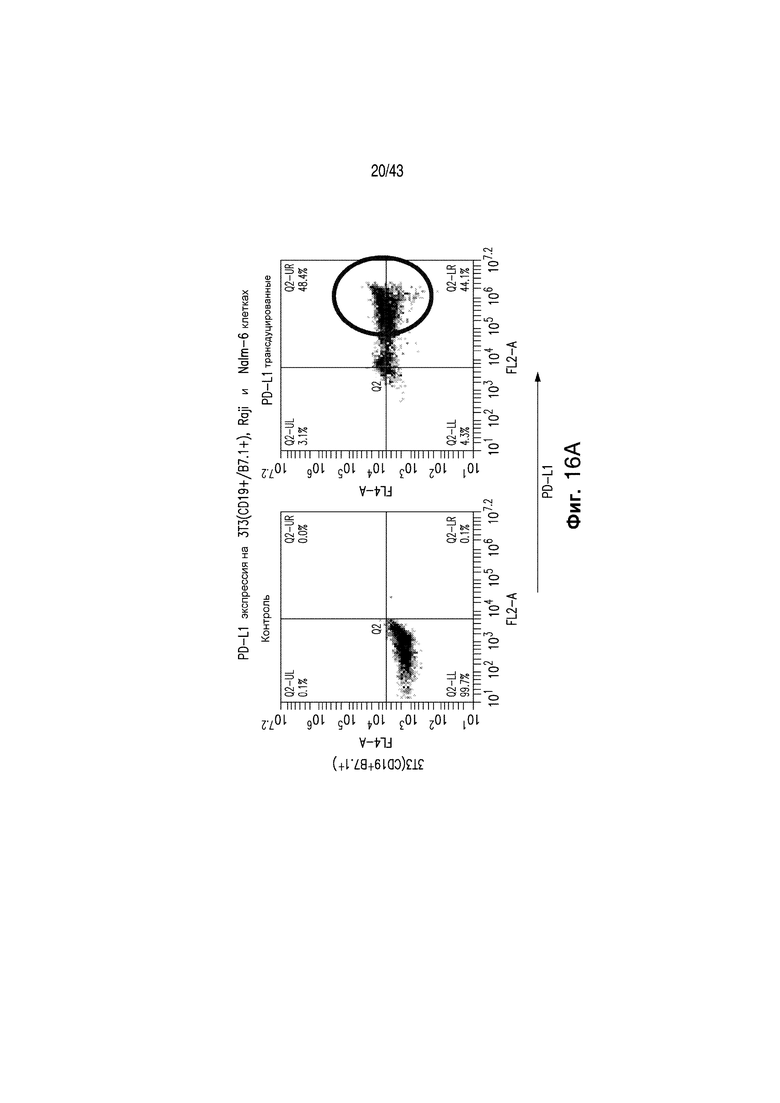
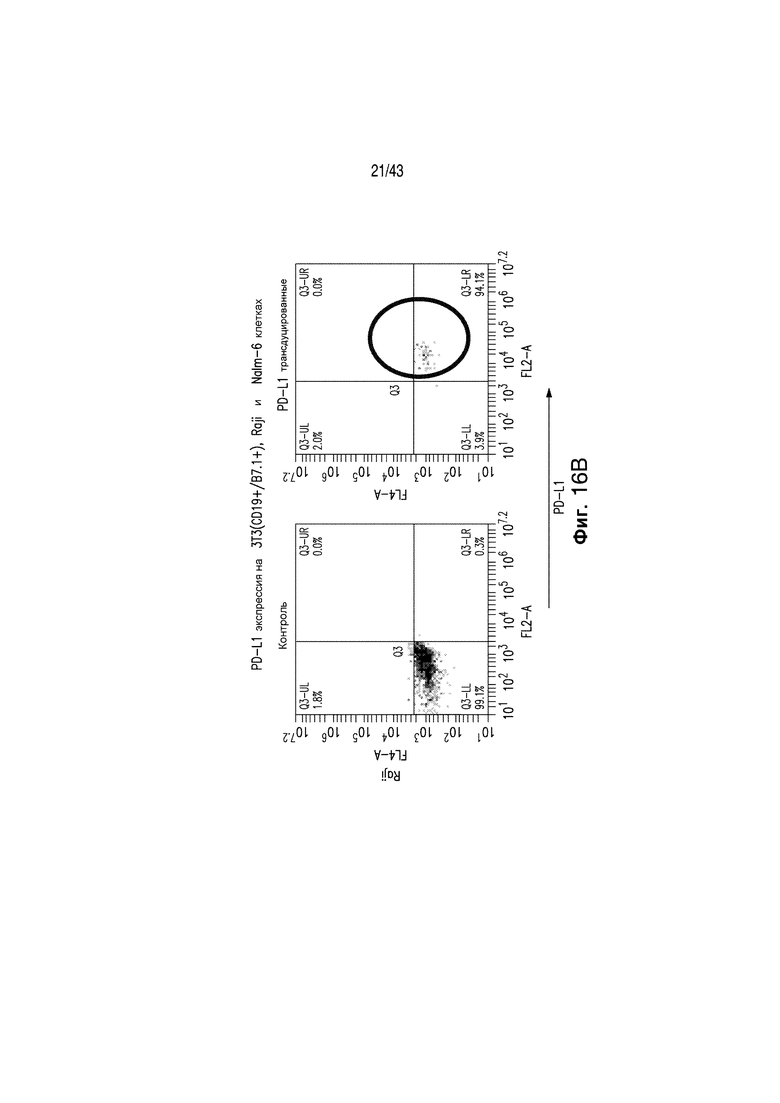
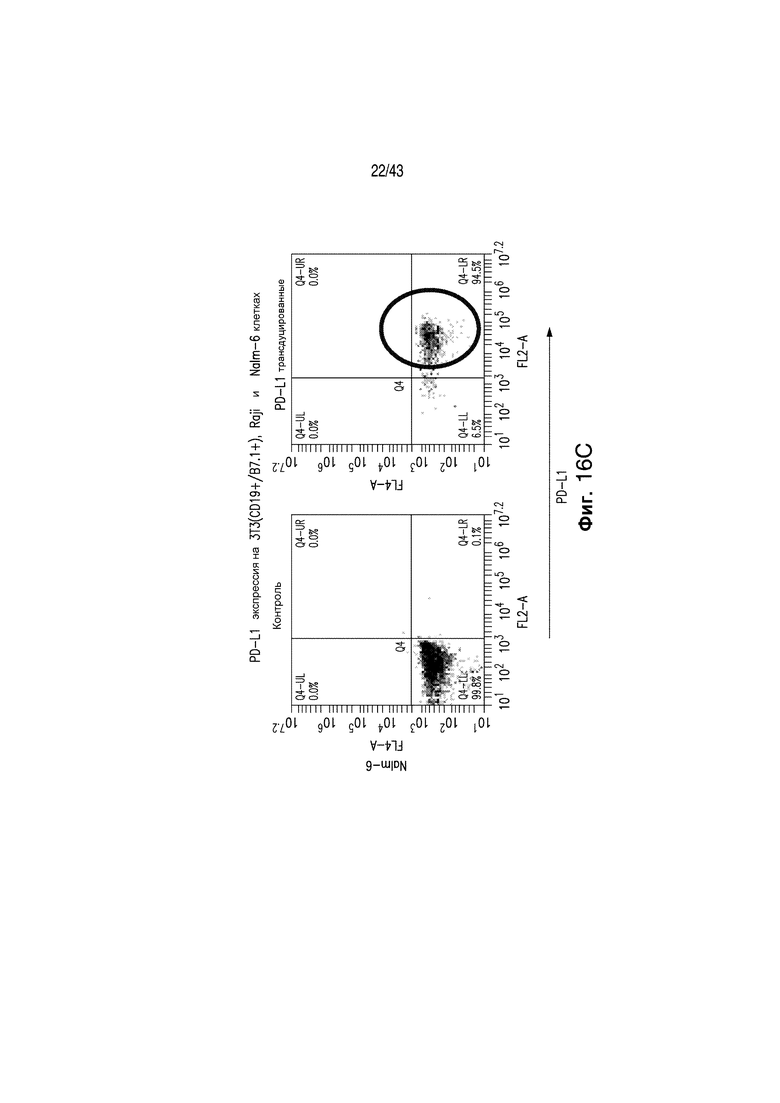
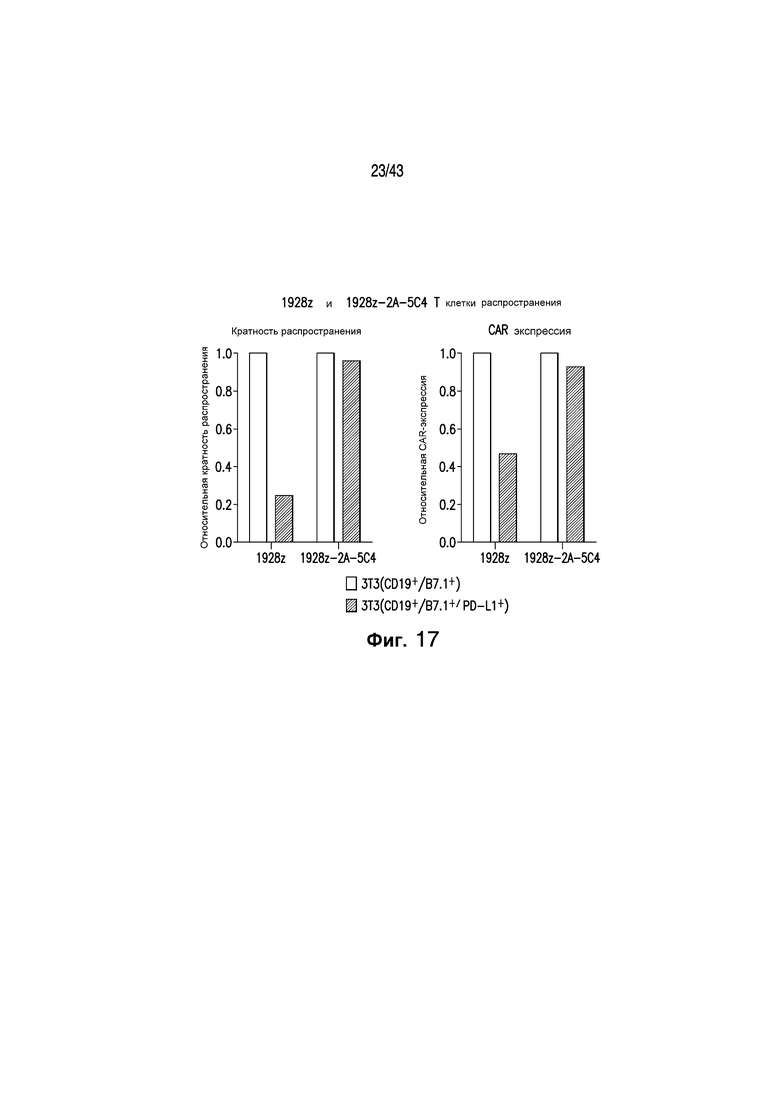
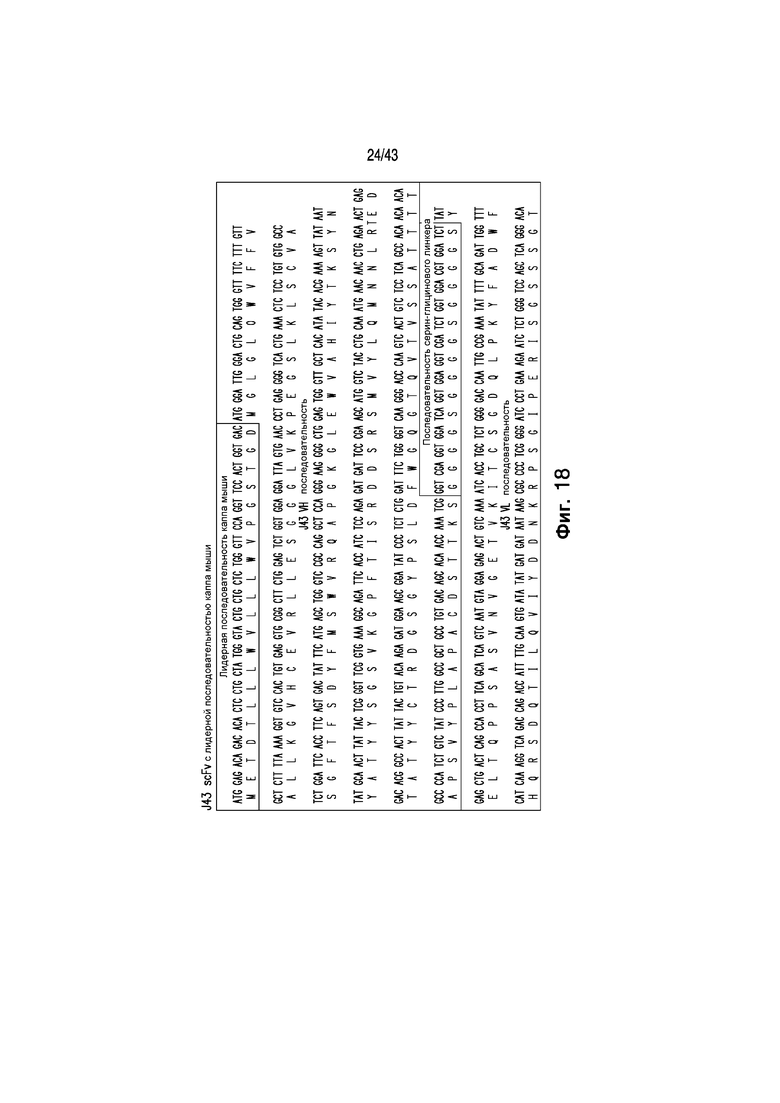
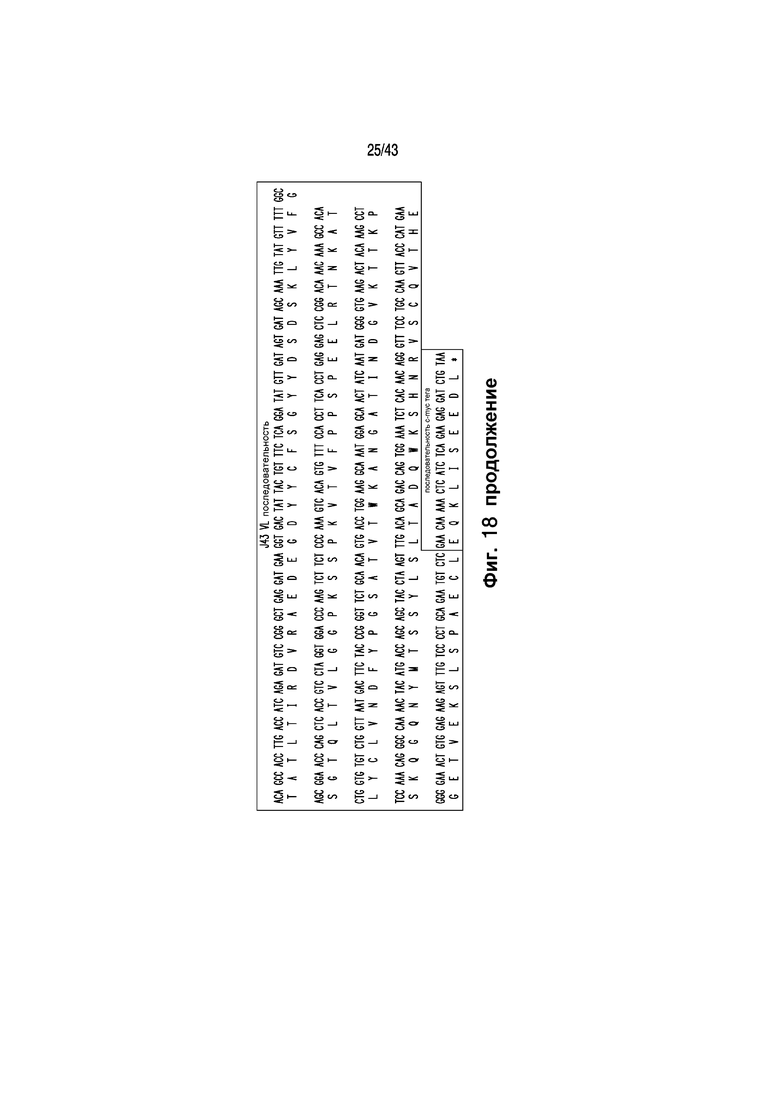


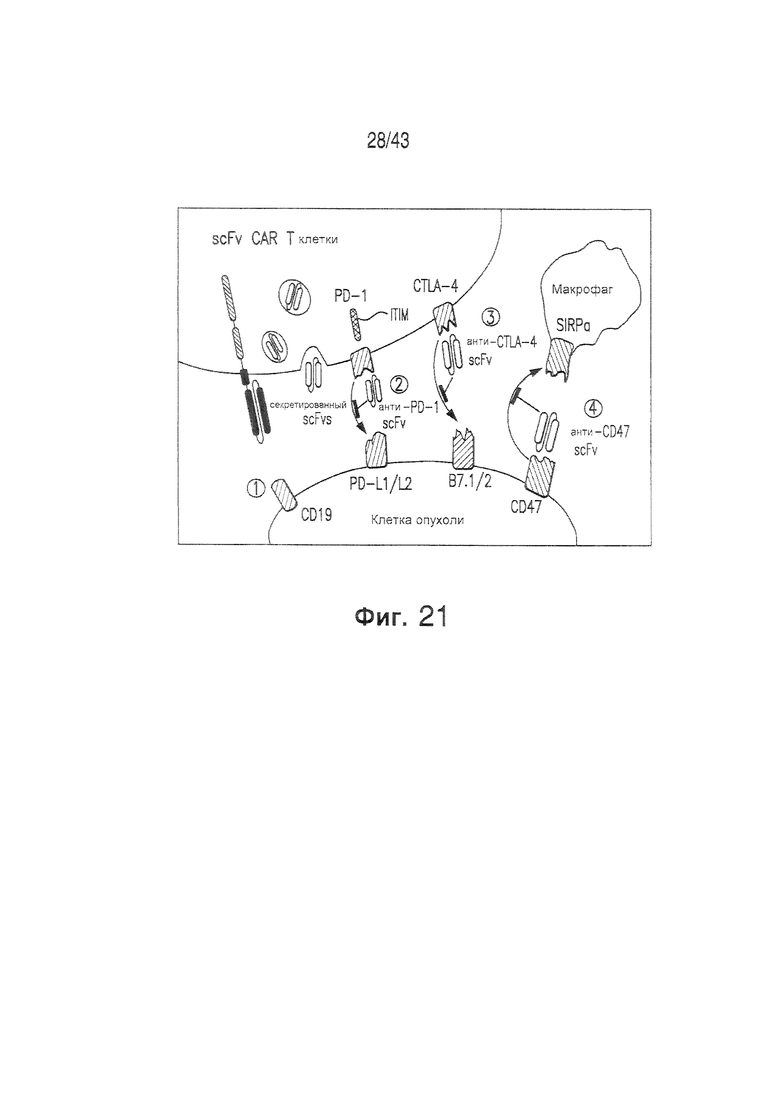
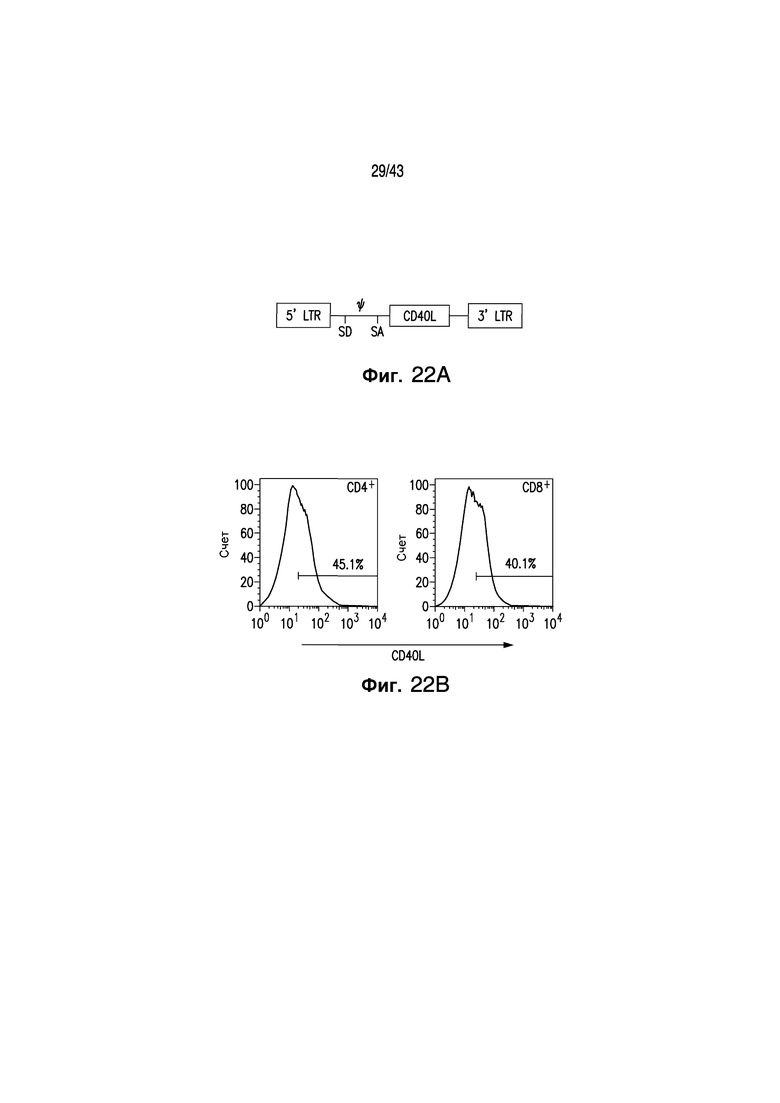
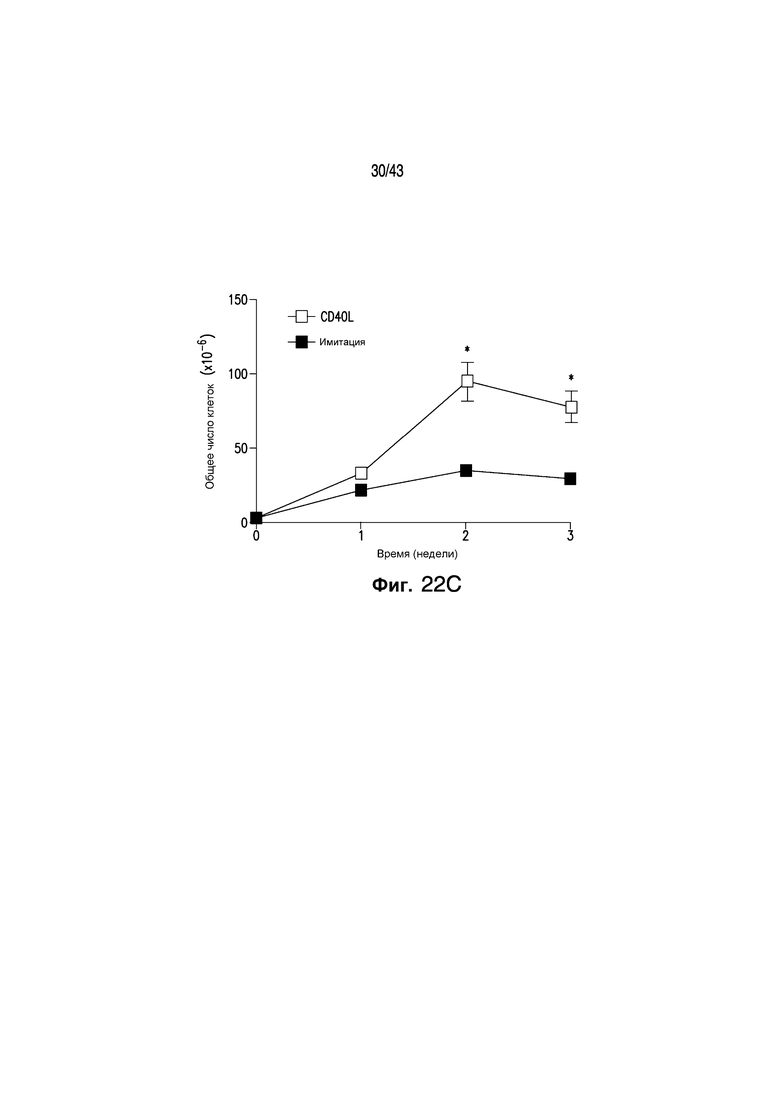
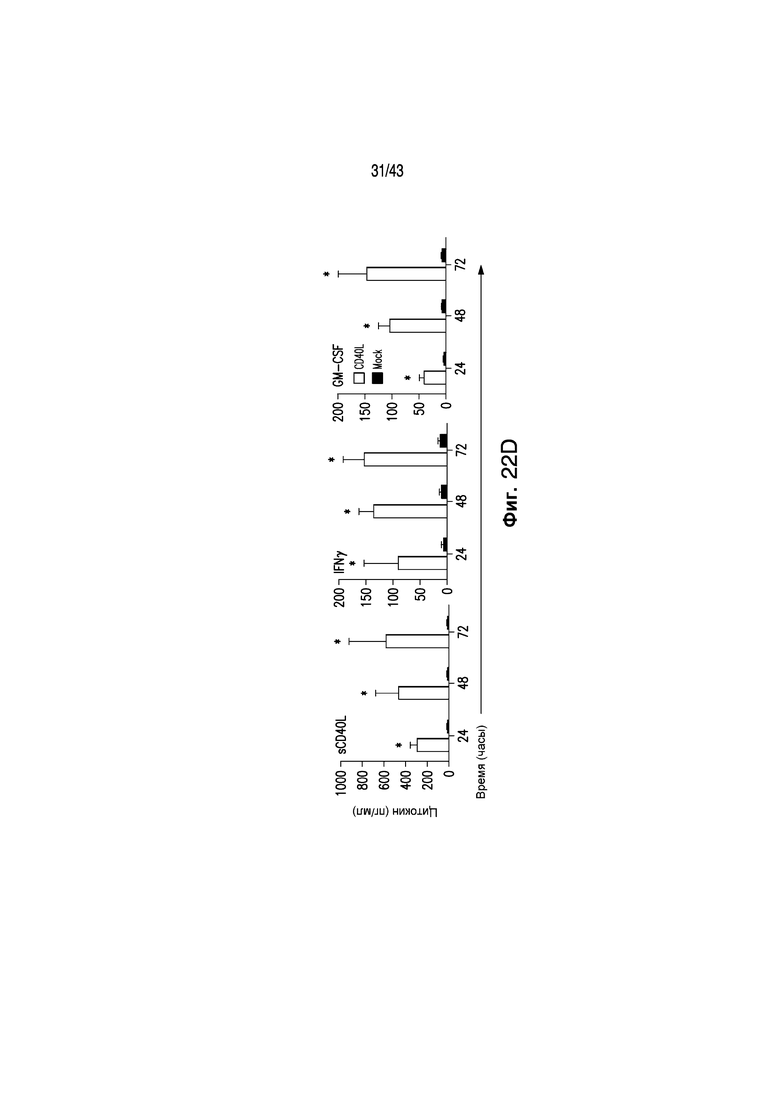
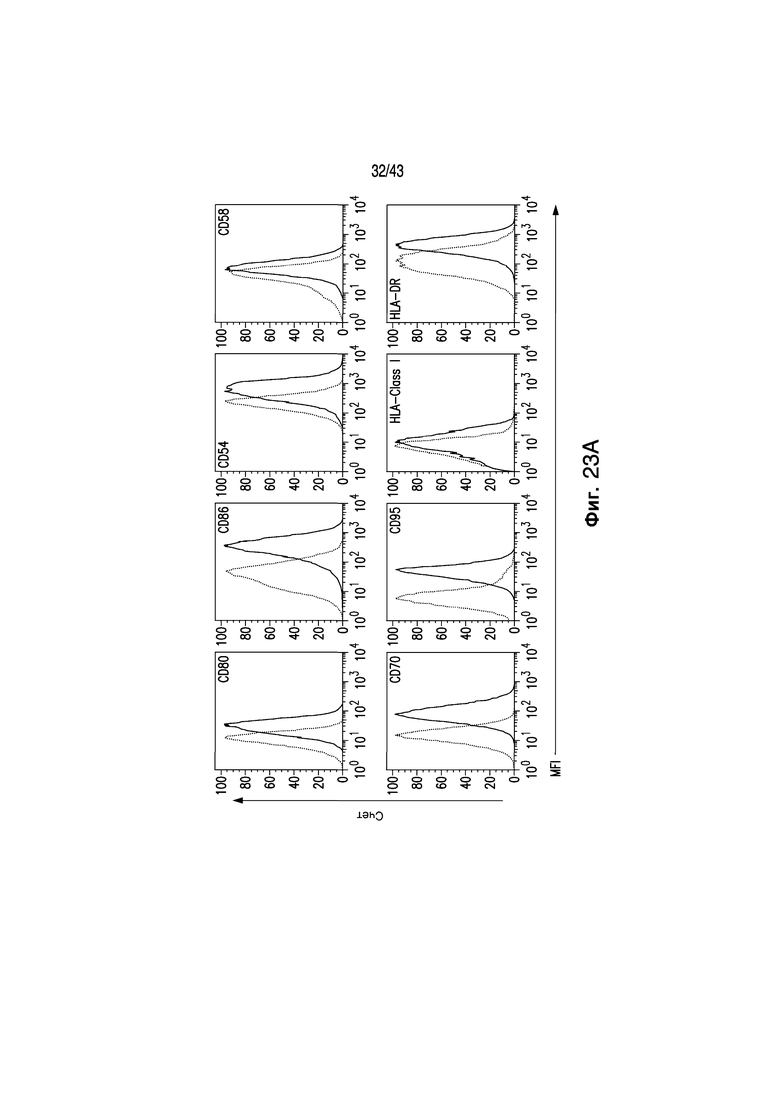
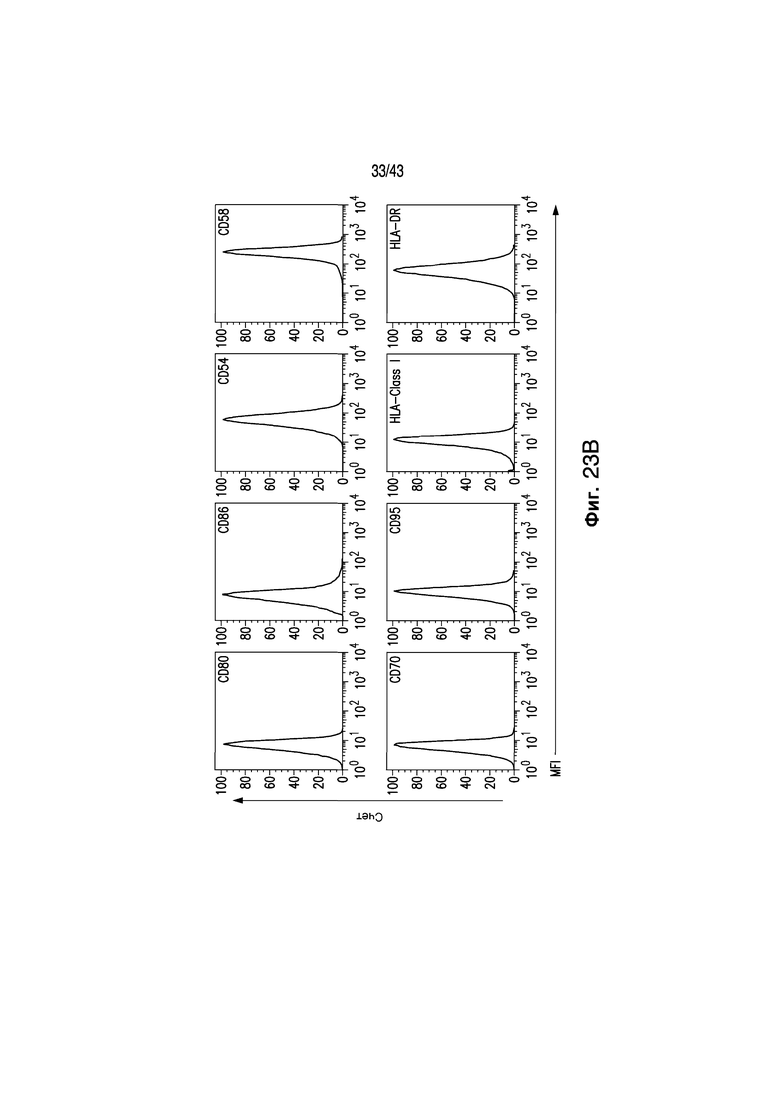
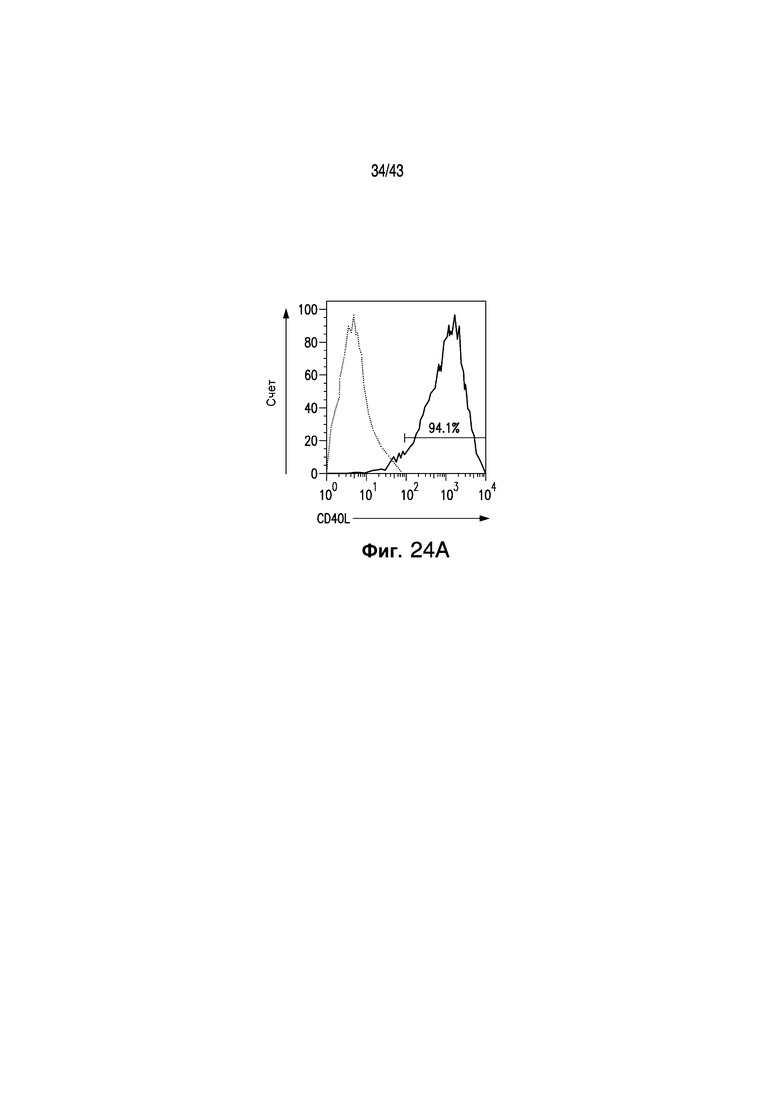
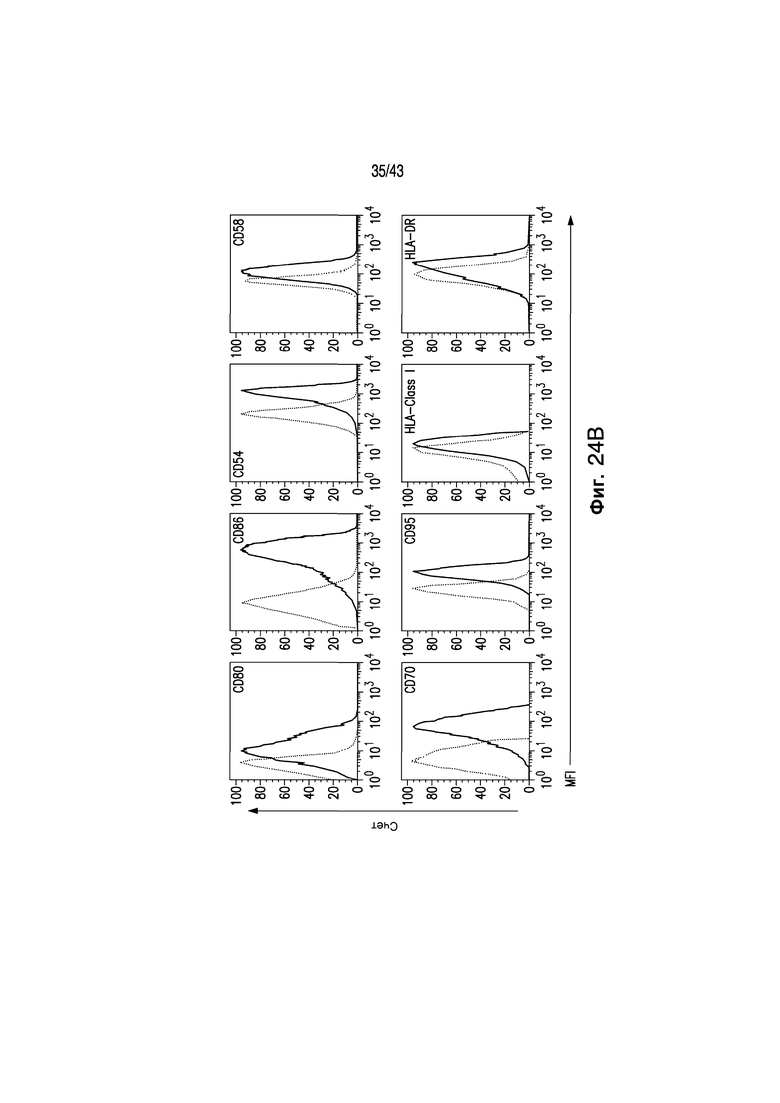

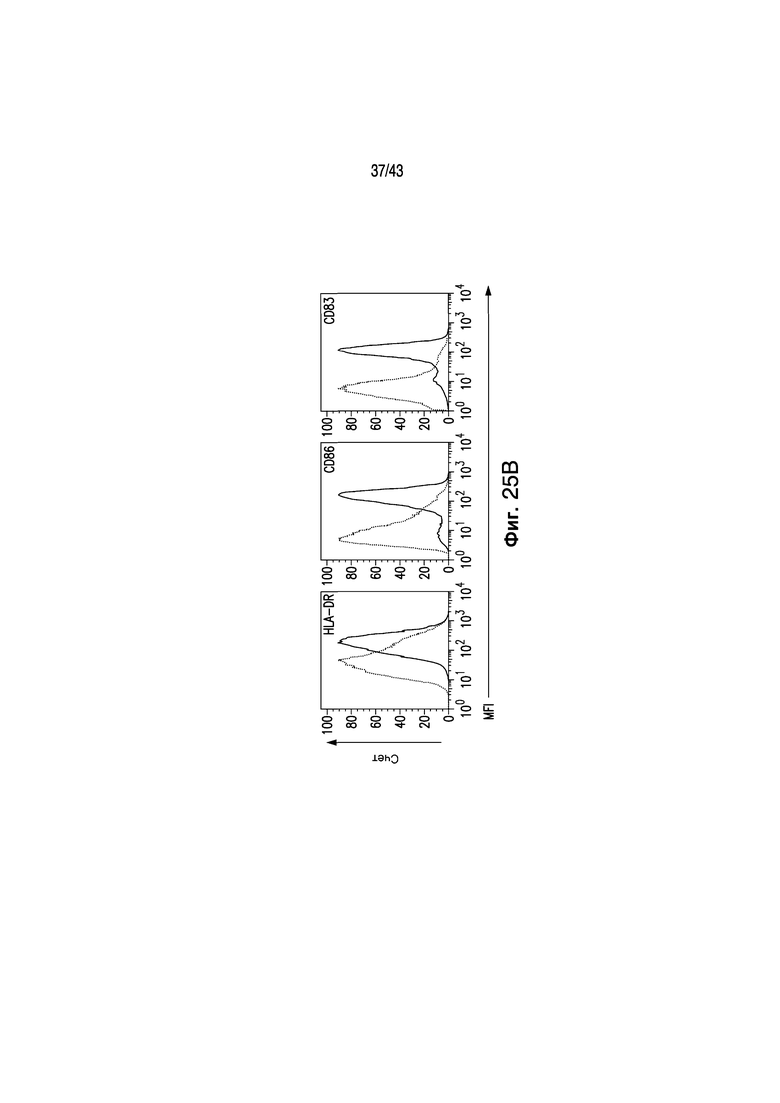

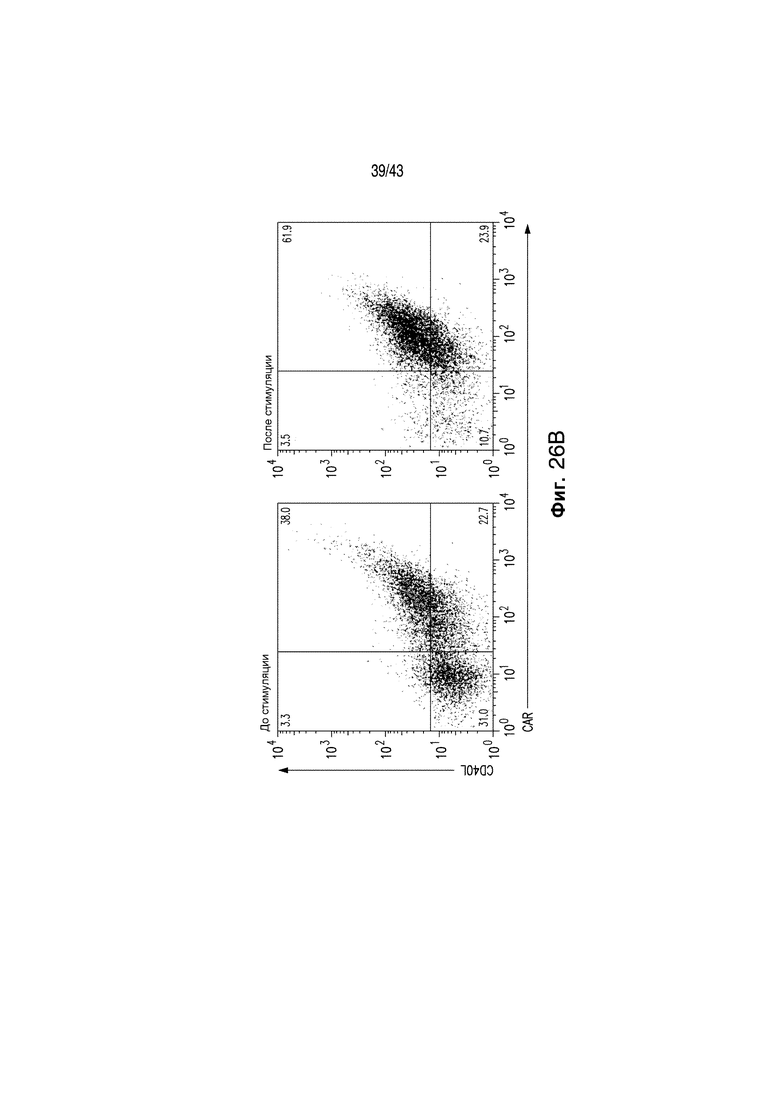
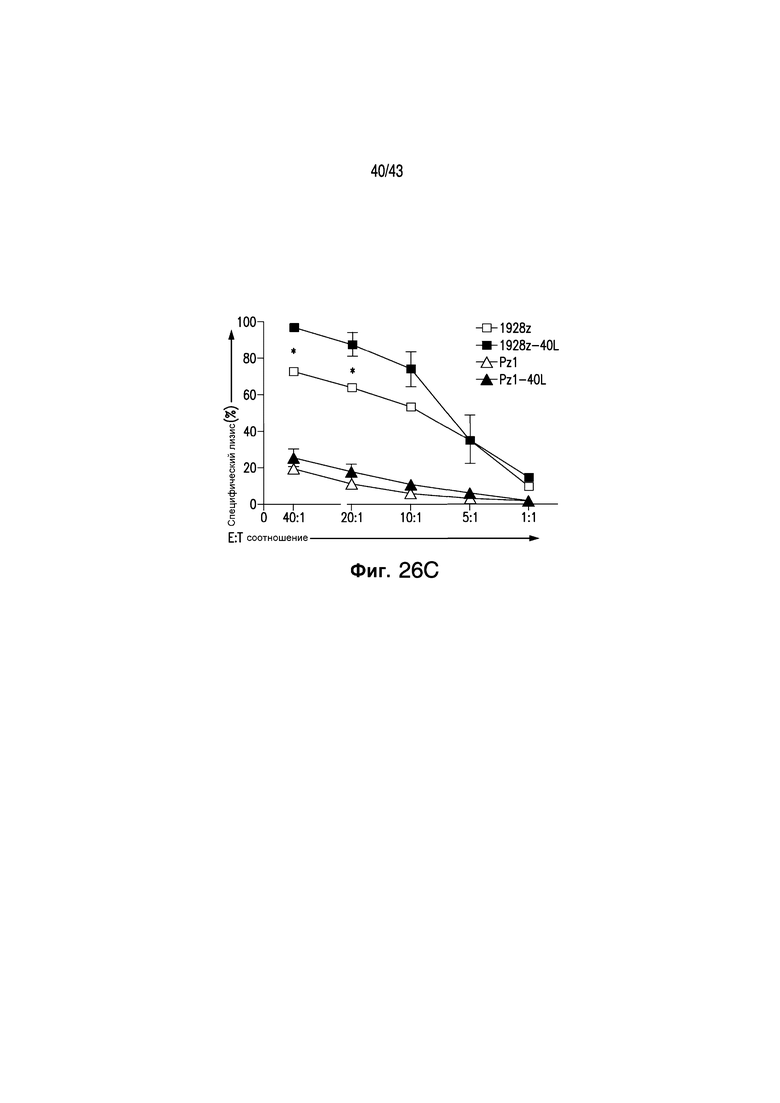
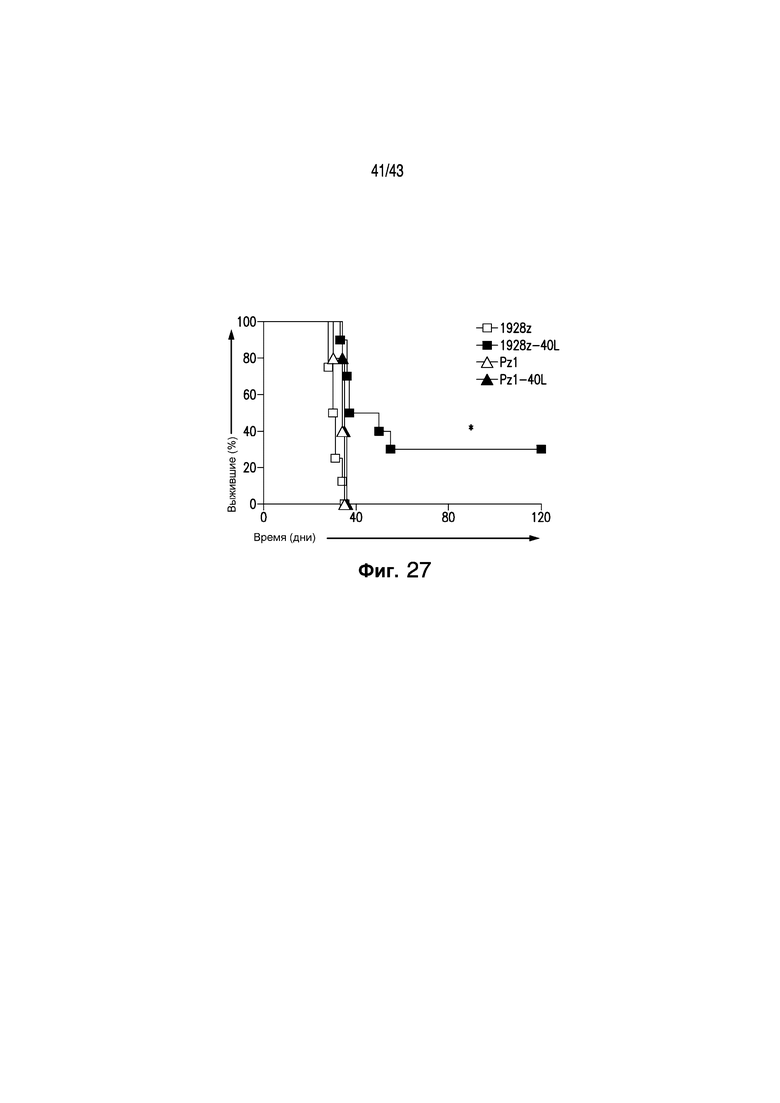
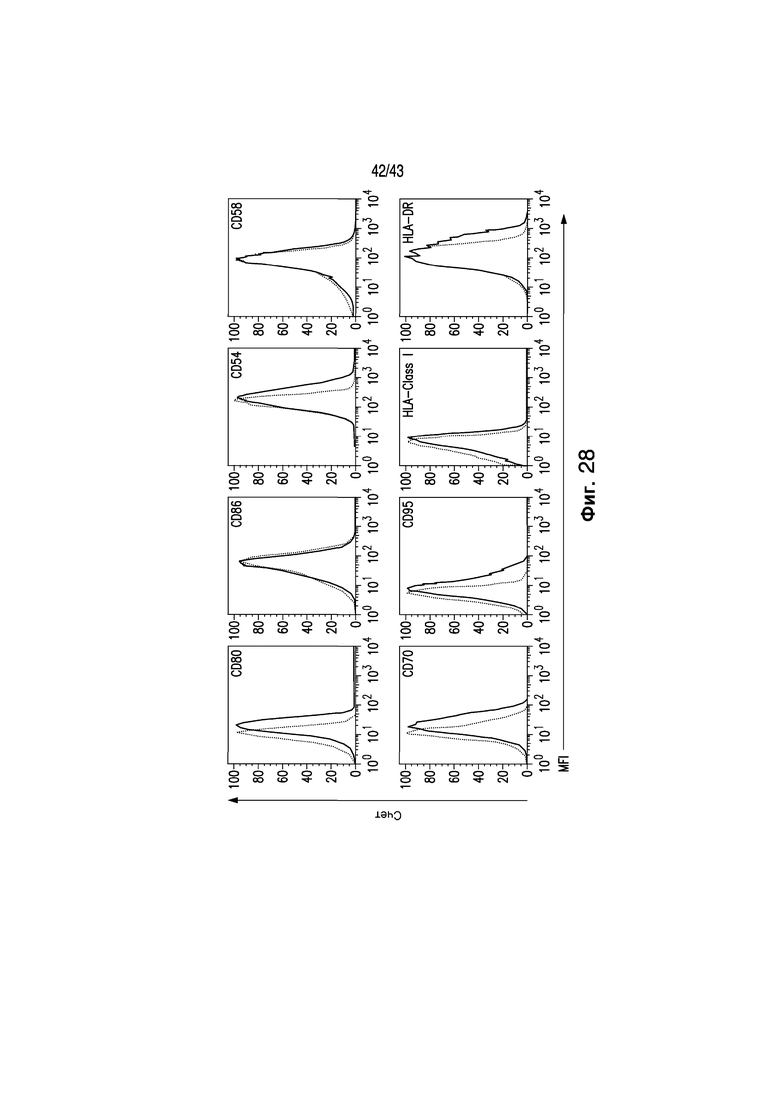
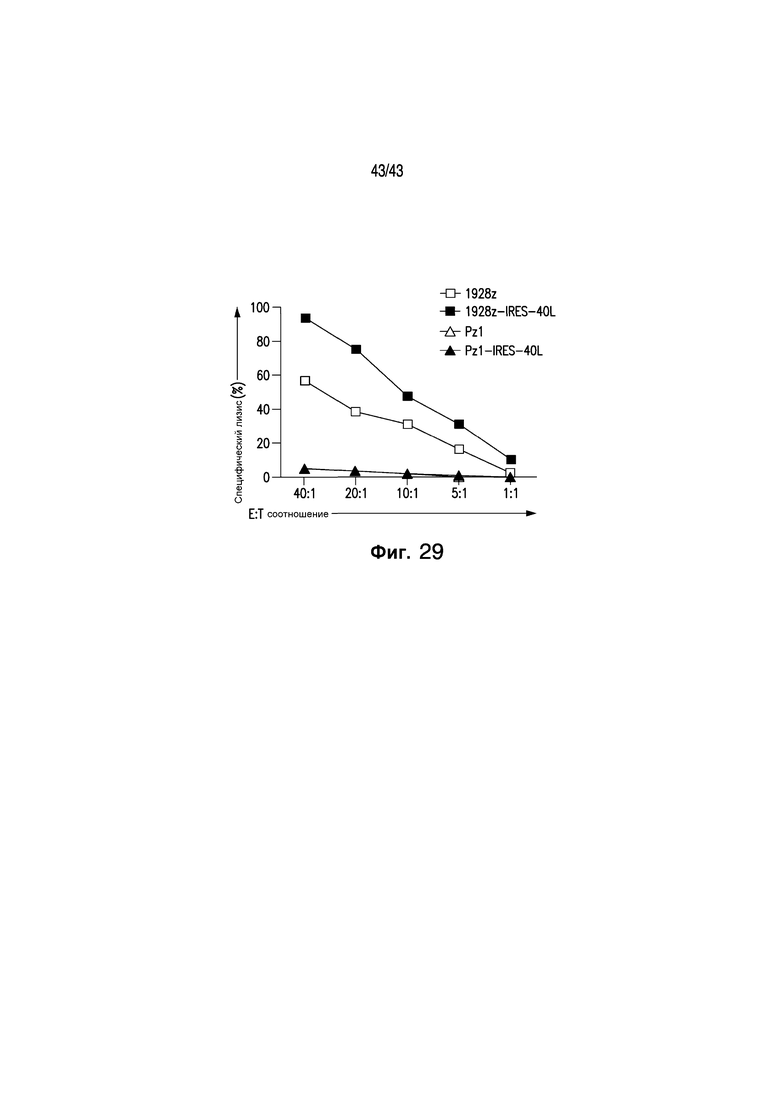
Изобретение относится к области биотехнологии, в частности к иммунореактивной клетке, включающей антиген-узнающий рецептор, который связывает антиген, причем связывание антиген-узнающего рецептора с антигеном активирует иммунореактивную клетку, и растворимый одноцепочечный вариабельный фрагмент (scFv), а также к композиции, ее содержащей. Также раскрыт способ получения иммунореактивной клетки, включающий ведение в иммунореактивную клетку последовательности нуклеиновых кислот, которая кодирует одноцепочечный вариабельный фрагмент (scFv), где иммунореактивная клетка содержит антиген-узнающий рецептор, который связывает антиген. Изобретение эффективно для уменьшения опухолевой массы и повышения выживаемости индивидуума с неоплазией. 7 н. и 30 з.п. ф-лы, 29 ил., 6 пр.
1. Иммунореактивная клетка для иммунотерапии, включающая:
а) антиген-узнающий рецептор, который связывает антиген, причем связывание антиген-узнающего рецептора с антигеном активирует иммунореактивную клетку, и
b) растворимый одноцепочечный вариабельный фрагмент (scFv), который связывается с CD47, PD-1, CTLA-4, CD28, OX-40, 4-1BB и их лигандами,
где иммунореактивную клетку выбирают из группы, состоящей из Т-клетки, натуральной киллерной (NK) клетки, цитотоксического Т-лимфоцита (CTL), регуляторной Т-клетки и плюрипотентной стволовой клетки, из которой лимфоидные клетки могут быть дифференцированы.
2. Иммунореактивная клетка по п. 1, в которой антиген представляет собой антиген опухоли или патогенного микроорганизма.
3. Иммунореактивная клетка по п. 1 или 2, в которой растворимый scFv является секретируемым.
4. Иммунореактивная клетка по любому из пп. 1-3, в которой указанный антиген-узнающий рецептор представляет собой Т-клеточный рецептор (TCR) или химерный антигенный рецептор (CAR).
5. Иммунореактивная клетка по любому из пп. 1-4, в которой указанный антиген-узнающий рецептор является экзогенным или эндогенным.
6. Иммунореактивная клетка по любому из пп. 1-5, в которой указанный антиген-узнающий рецептор является рекомбинантно экспрессируемым.
7. Иммунореактивная клетка по любому из пп. 1-6, в которой антиген-узнающий рецептор экспрессируется с вектора.
8. Иммунореактивная клетка по любому из пп. 1-7, в которой scFv экспрессируется с вектора.
9. Иммунореактивная клетка по любому из пп. 1-8, в которой указанная иммунореактивная клетка является аутологичной.
10. Иммунореактивная клетка по любому из пп. 1-9, в которой антиген представляет собой опухолевый антиген, выбранный из группы, состоящей из CD 19, MUC16, MUC1, CA1X, CEA, CDS, CD7, CD 10, CD20, CD22, CD30, CD33, CD34, CD38, CD41, CD44, CD49f, CD56, CD74, CD133, CD138, антигена клеток, инфицированных цитомегаловирусом (ЦМВ), EGP-2, EGP-40, EpCAM, erb-B2,3,4, FBP, фетального ацетилхолинового рецептора, фолатного рецептора α, GD2, GD3, HER-2, hTERT, IL-13R-a2, к-легкой цепи, KDR, LeY, молекулы адгезии клеток L1, MAGE-A1, мезотелина, лигандов NKG2D, NY-ESO-1, онкофетального антигена (h5T4), PSCA, PSMA, ROR1, TAG-72, VEGF-R2 и WT-1.
11. Иммунореактивная клетка по любому из пп. 1-10, в которой указанный антиген представляет собой СD19 или MUC16.
12. Иммунореактивная клетка по любому из пп. 1-11, в которой домен внутриклеточной сигнализации указанного антиген-узнающего рецептора представляет собой CD3ζ-цепь, CD97, CD11a-CD18, CD2, ICOS, CD27, CD154, CDS, OX40, 4-1BB, сигнальный домен CD28 или их комбинации.
13. Иммунореактивная клетка по любому из пп. 1-12, в которой клетка экспрессирует рекомбинантный или эндогенный антигенный рецептор, который представляет собой 1928z или 4H1128Z.
14. Иммунореактивная клетка по любому из пп. 1-13, в которой растворимый scFv усиливает иммунный ответ иммунореактивной клетки.
15. Фармацевтическая композиция для иммунотерапии, содержащая эффективное количество иммунореактивной клетки по любому из пп. 1-14 и фармацевтически приемлемый наполнитель.
16. Применение иммунореактивной клетки по любому из пп. 1-14 или фармацевтической композиции по п. 15 для уменьшения опухолевой массы у индивидуума.
17. Применение иммунореактивной клетки по любому из пп. 1-14 или фармацевтической композиции по п. 15 для повышения выживаемости индивидуума с неоплазией.
18. Применение иммунореактивной клетки по любому из пп. 1-14 или фармацевтической композиции по п. 15 для уменьшения опухолевой массы и повышения выживаемости индивидуума с неоплазией.
19. Применение по любому из пп. 16-18, в котором клетка или композиция уменьшает число опухолевых клеток, размер опухоли и/или уничтожает опухоль у индивидуума.
20. Применение по любому из пп. 16-19, в котором неоплазия выбрана из группы, состоящей из рака крови, B-клеточного лейкоза, множественной миеломы, лимфобластного лейкоза (ALL), хронического лимфолейкоза, неходжкинской лимфомы и рака яичника.
21. Применение по любому из пп. 16-20, в котором неоплазия представляет собой B-клеточный лейкоз, антиген представляет собой СD19, и scFv связывается с одним или более из CD47, PD-1, CTLA-4 и их лигандов.
22. Применение по любому из пп. 16-20, в котором неоплазия представляет собой множественную миелому, антиген представляет собой СD19, и scFv связывается с одним или более из CD47, PD-1, CTLA-4 и их лигандов.
23. Применение по любому из пп. 16-20, в котором неоплазия представляет собой острый лимфобластный лейкоз (ALL), антиген представляет собой СD19, и scFv связывается с одним или более из CD47, PD-1, CTLA-4 и их лигандов.
24. Применение по любому из пп. 16-20, в котором неоплазия представляет собой хронический лимфоцитарный лейкоз, антиген представляет собой СD19, и scFv связывается с одним или более из CD47, PD-1, CTLA-4 и их лигандов.
25. Применение по любому из пп. 16-20, в котором неоплазия представляет собой неходжкинскую лимфому, антиген представляет собой СD19, и scFv связывается с одним или более из CD47, PD-1, CTLA-4 и их лигандов.
26. Применение по любому из пп. 16-20, в котором неоплазия представляет собой овариальную неоплазию, антиген представляет собой MUC16, и scFv связывается с одним или более из CD47, PD-1, CTLA-4 и их лигандов.
27. Способ получения антиген-специфической иммунореактивной клетки по любому из пп. 1-14, включающий введение в иммунореактивную клетку последовательности нуклеиновых кислот, которая кодирует одноцепочечный вариабельный фрагмент (scFv), который связывается с CD47, PD-1, CTLA-4, CD28, OX-40, 4-1BB и их лигандами, где иммунореактивная клетка содержит антиген-узнающий рецептор, который связывает антиген, и иммунореактивную клетку выбирают из группы, состоящей из Т-клетки, натуральной киллерной (NK) клетки, цитотоксического Т-лимфоцита (CTL), регуляторной Т-клетки и плюрипотентной стволовой клетки, из которой лимфоидные клетки могут быть дифференцированы.
28. Способ по п. 27, в котором растворимый scFv является секретируемым.
29. Способ по п. 27 или 28, в котором scFv экспрессируется с вектора.
30. Способ по любому из пп. 27-29, в котором растворимый scFv усиливает иммунный ответ иммунореактивной клетки.
31. Способ по любому из пп. 27-30, в котором указанный антиген-узнающий рецептор представляет собой T-клеточный рецептор (TCR) или химерный антигенный рецептор (CAR).
32. Способ по любому из пп. 27-31, в котором указанный антиген-узнающий рецептор является экзогенным или эндогенным.
33. Способ по любому из пп. 27-32, в котором указанный антиген-узнающий рецептор является рекомбинантно экспрессируемым.
34. Способ по любому из пп. 27-33, в котором указанный антиген-узнающий рецептор экспрессируется с вектора.
35. Способ по любому из пп. 27-34, в котором внутриклеточный сигнальный домен указанного антиген-связывающего рецептора представляет собой CD3ζ-цепь, CD97, CD11a-CD18, CD2, ICOS, CD27, CD154, CDS, OX40, 4-1BB, сигнального домена CD28 или их комбинации.
36. Применение иммунореактивной клетки по любому из пп. 1-14 или фармацевтической композиции по п. 15 при лечении рака крови у индивидуума, нуждающегося в этом, где иммунореактивная клетка представляет собой Т-клетку, содержащую антиген-узнающий рецептор, который связывает CD19, причем связывание антиген-узнающего рецептора с CD19 активирует иммунореактивную клетку, и где растворимый одноцепочечный вариабельный фрагмент (scFv) связывается с одним или более из CD47, PD-1, CTLA-4 и их лигандов, предоставляя тем самым лечение рака крови у индивидуума.
37. Применение по п. 36, в котором рак крови выбран из группы, состоящей из В-клеточной лейкемии, миеломной болезни, острого лимфобластного лейкоза (ALL), хронического лимфоцитарного лейкоза и неходжкинской лимфомы.
| US 2010178276 A1, 15.07.2010 | |||
| KEICHIRO MIH et al., Synergistic and persistent effect of T-cell immunotherapy with anti-CD19 or anti-CD38 chimeric receptor in conjunction with rituximab on B-cell non-Hodgkin lymphoma, British Journal of Haematology, 2010, Vol | |||
| Двухколейная подвесная дорога | 1919 |
|
SU151A1 |
| DAVID L | |||
| PORTER et al., Chimeric Antigen Receptor-Modified T Cells in | |||
Авторы
Даты
2023-06-21—Публикация
2014-02-26—Подача