Уровень техники
Область техники
Настоящее изобретение относится к применению экстракта Cistanche tubulosa, в частности, относится к применению в получении лекарственных средств или пищевого продукта для защиты клеток глаза.
Описание материалов из уровня техники
Глаза являются окнами души. Благодаря глазам можно увидеть мир в сверхвысоком разрешении. Повседневная жизнь заставляет полагаться на глаза. Наблюдаемые в настоящее время общераспространенные заболевания глаз включают в себя возрастную макулярную дегенерацию (AMD), диабетическую ретинопатию и пролиферативную витреоретинопатию (PVR), причем AMD считается опасным заболеванием глаз, которое вызывает слепоту у взрослых или пожилых людей.
В соответствии с данными Всемирной организации здравоохранения (WHO) AMD, сдерживание развития катаракты, стало наиболее частой причиной плохого зрения (Jager et al 2008). В отчете за 2010 количество случаев ухудшения зрения и слепоты, вызванных AMD, возрастает. В соответствии с данными национального бюро статистики США более 8 миллионов людей страдают от AMD, причем более 10% людей в возрасте от 65 до 74 лет страдают от AMD и более чем 10% людей старше 74 лет страдают от AMD. Оценивается, что более 50% населения будут страдать от AMD в 2020 году (Friedman et al 2004). Распространенность AMD у пожилых людей возрастом более 65 лет составляет приблизительно 10% на Тайване, и эта распространенность AMD ниже, чем в Европе и Америке. Тем не менее, люди имеют ограниченные познания о макулярной дегенерации, и не существует эффективного лечения AMD. Таким образом, в случае, когда у пациентов диагностируют AMD, врачи не могут предложить эффективные методы лечения. Следовательно, макулярная дегенерация стала основной причиной слепоты у людей, и его называют "убийцей зрения номер один". Таким образом, предупреждение AMD является особенно важным. Более того, население Тайваня стареет, и уклад его жизни постепенно меняется в сторону вестернизации. AMD будет широко распространенным и станет основным заболеванием глаз у взрослых людей, если другие причины слепоты будут поддаваться контролю.
Под действием свободных радикалов будут накапливаться повреждения от окислительного стресса в ДНК, белках, липидах и внутриклеточных макромолекулярных материалах, вызывая старение. В дополнение к дегенерации центральной нервной системы, некоторые заболевания глаз (в частности, макулярная дегенерация и ретинопатия) также считаются тесно связанными с повреждениями от окислительного стресса.
Тем не менее, не существует способов эффективного предупреждения, замедления или лечения заболеваний глаз или защиты клеток глаз. Эту проблему следует решить.
Краткое описание
Настоящим изобретением предполагается способ применения экстракта Cistanche tubulosa для получения лекарственных средств или продукта питания для защиты клеток глаза.
В соответствии с вариантом осуществления экстракт Cistanche tubulosa содержит эхинакозид, актеозид, изоактеозид, тубулозид А или их комбинацию.
В соответствии с другим вариантом осуществления лекарственные средства или продукт питания применяют для предупреждения, замедления или лечения заболеваний глаз.
В соответствии с еще одним вариантом осуществления заболевания глаз представляют собой макулярную дегенерацию, макулярное отверстие, ретинопатию или глаукому.
В соответствии с еще одним вариантом осуществления макулярная дегенерация представляет собой возрастную макулярную дегенерацию.
В соответствии с еще одним вариантом осуществления возрастная макулярная дегенерация представляет собой сухую макулярную дегенерацию или влажную макулярную дегенерацию.
В соответствии с еще одним вариантом осуществления ретинопатия представляет собой диабетическую ретинопатию, пигментный ретинит, заболевание сетчатки, окклюзию артерии и вены сетчатки, пролиферативную витреоретинопатию или центральную серозную ретинопатию.
В соответствии с еще одним вариантом осуществления форма лекарственных средств представляет собой капсулу, таблетку, порошок или жидкость.
Экстракт Cistanche tubulosa в соответствии с настоящим раскрытием применяют для получения лекарственных средств или продукта питания, имеющего функцию защиты клеток глаза.
Краткое описание чертежей
Чтобы признаки, преимущества и варианты осуществления настоящего раскрытия стали более очевидными, прилагаемые графические материалы описаны ниже.
Фиг. 1-5 представляют собой диаграммы, на которых показаны результаты исследования цитотоксичности в соответствии с настоящим раскрытием.
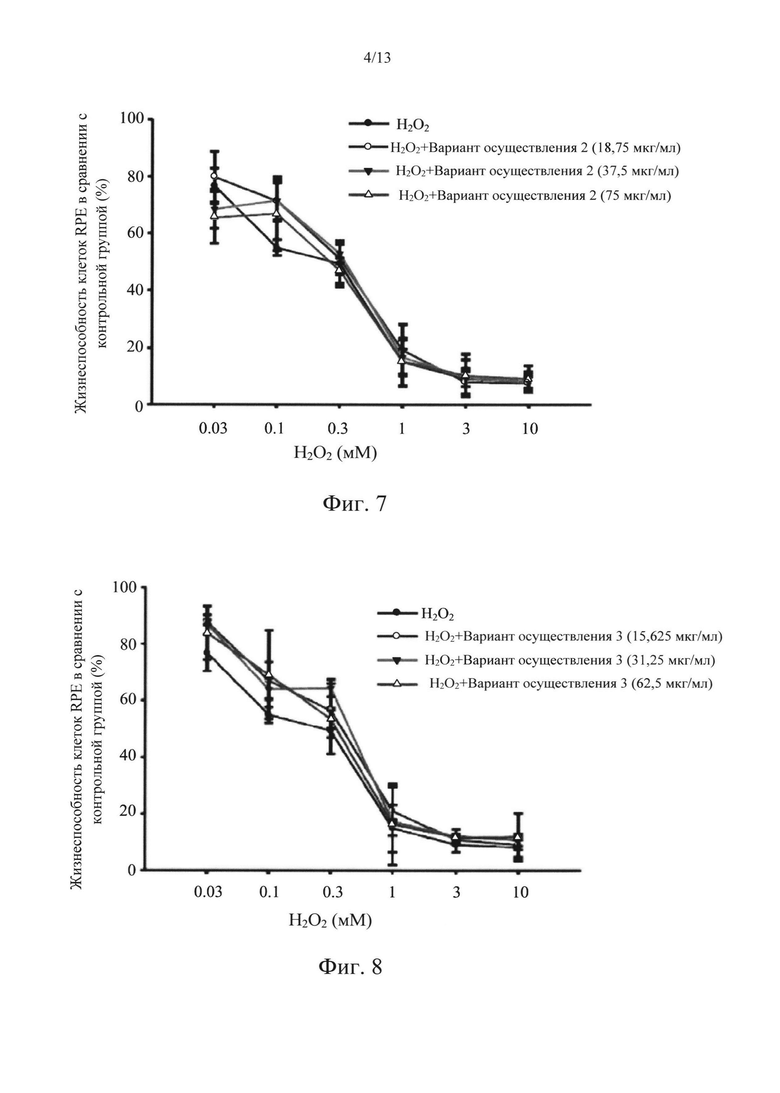
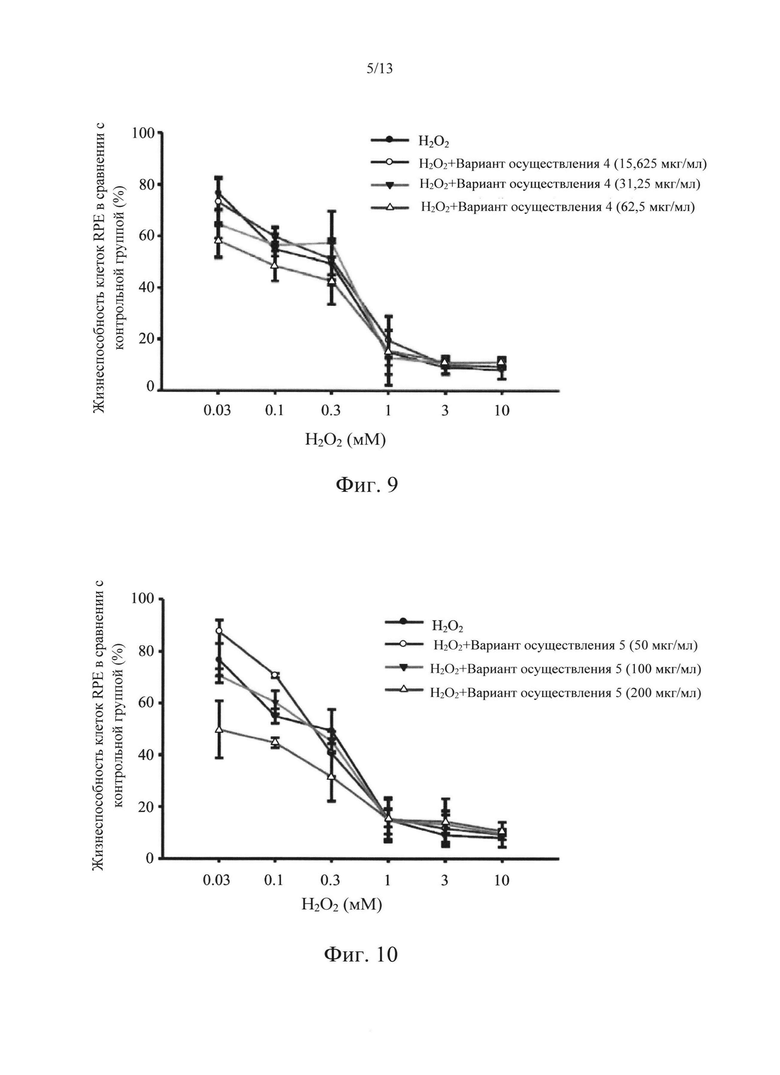
Фиг. 6-10 представляют собой диаграммы, на которых показаны результаты исследования защитного эффекта в соответствии с вариантами осуществления в настоящем раскрытии по отношению к индуцируемой H2O2 цитотоксичности.
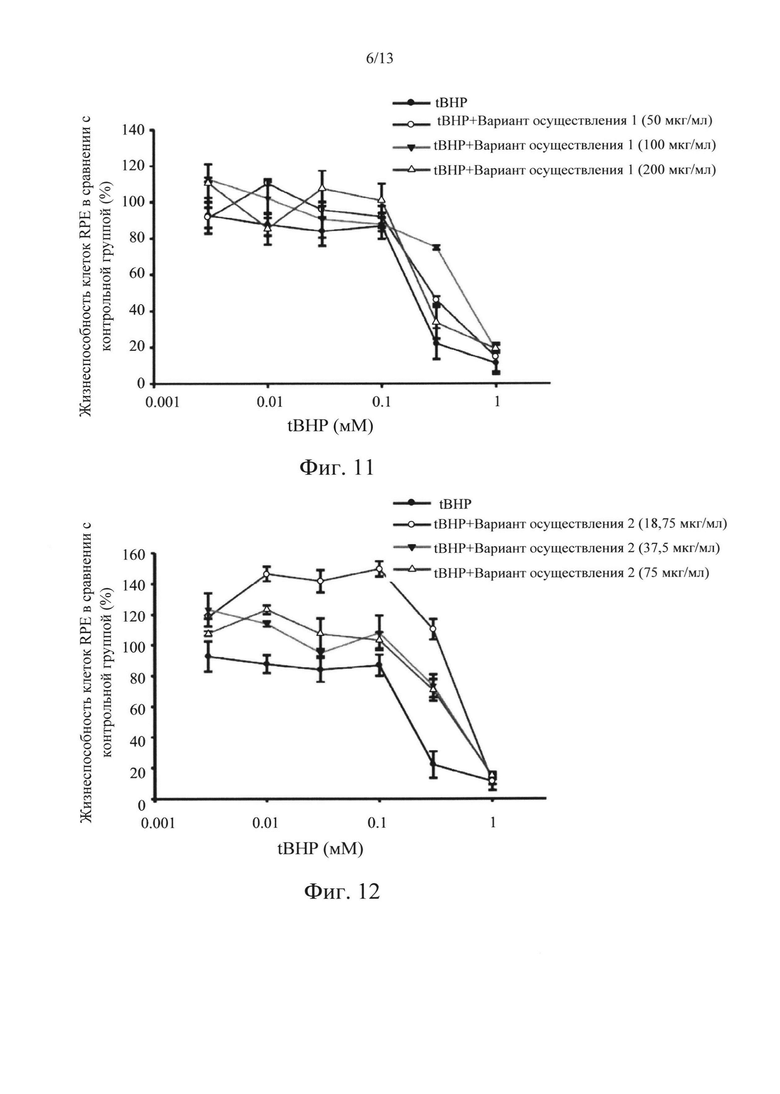
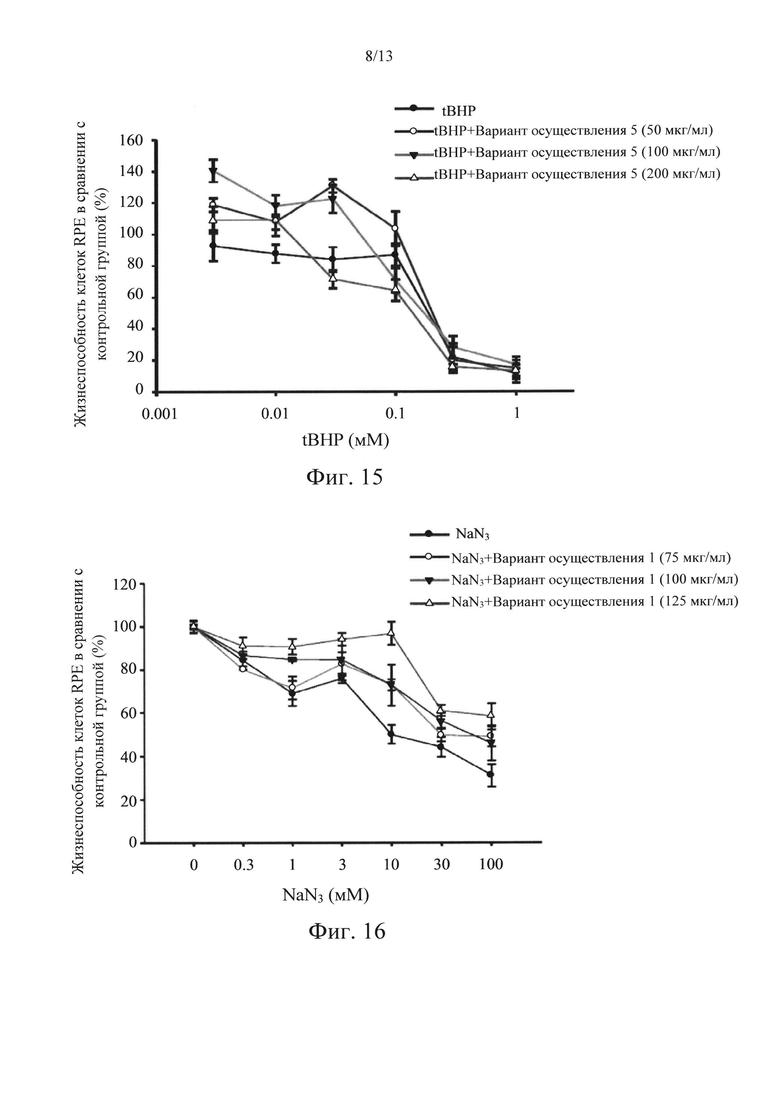
Фиг. 11-15 представляют собой диаграммы, на которых показаны результаты исследования защитного эффекта в соответствии с вариантами осуществления в настоящем раскрытии по отношению к индуцируемой t-BHP цитотоксичности.
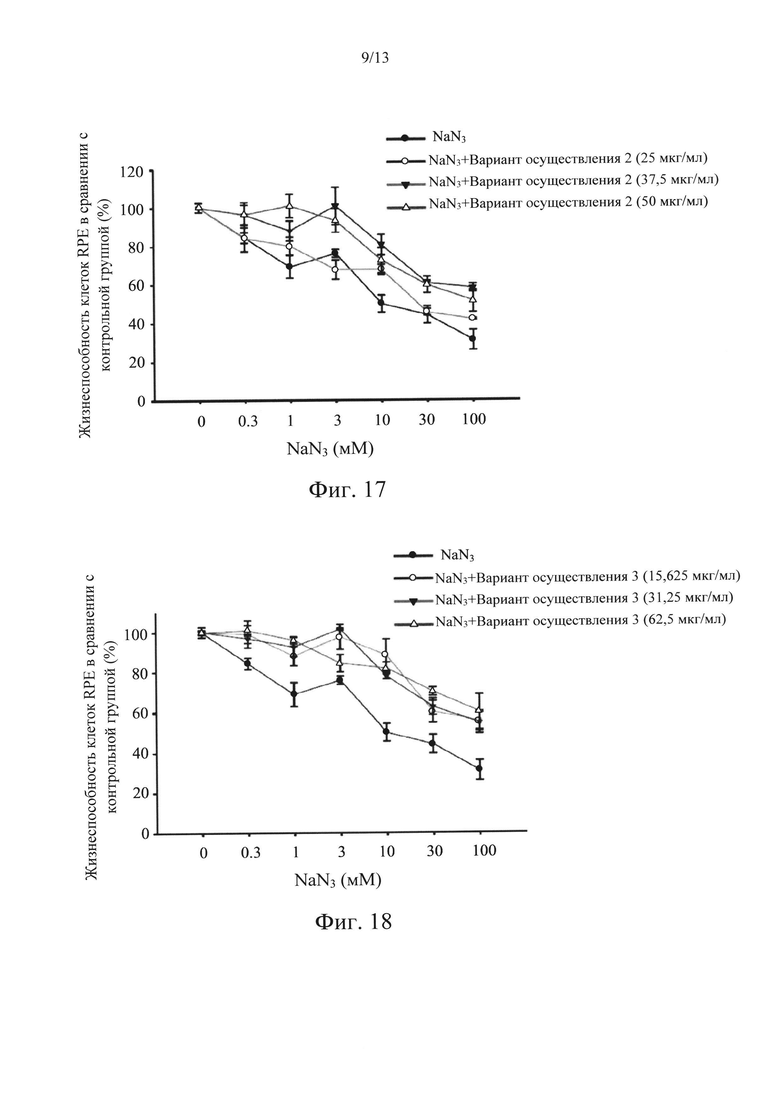
Фиг. 16-20 представляют собой диаграммы, на которых показаны результаты исследования защитного эффекта в соответствии с вариантами осуществления в настоящем раскрытии по отношению к индуцируемой NaN3 цитотоксичности.
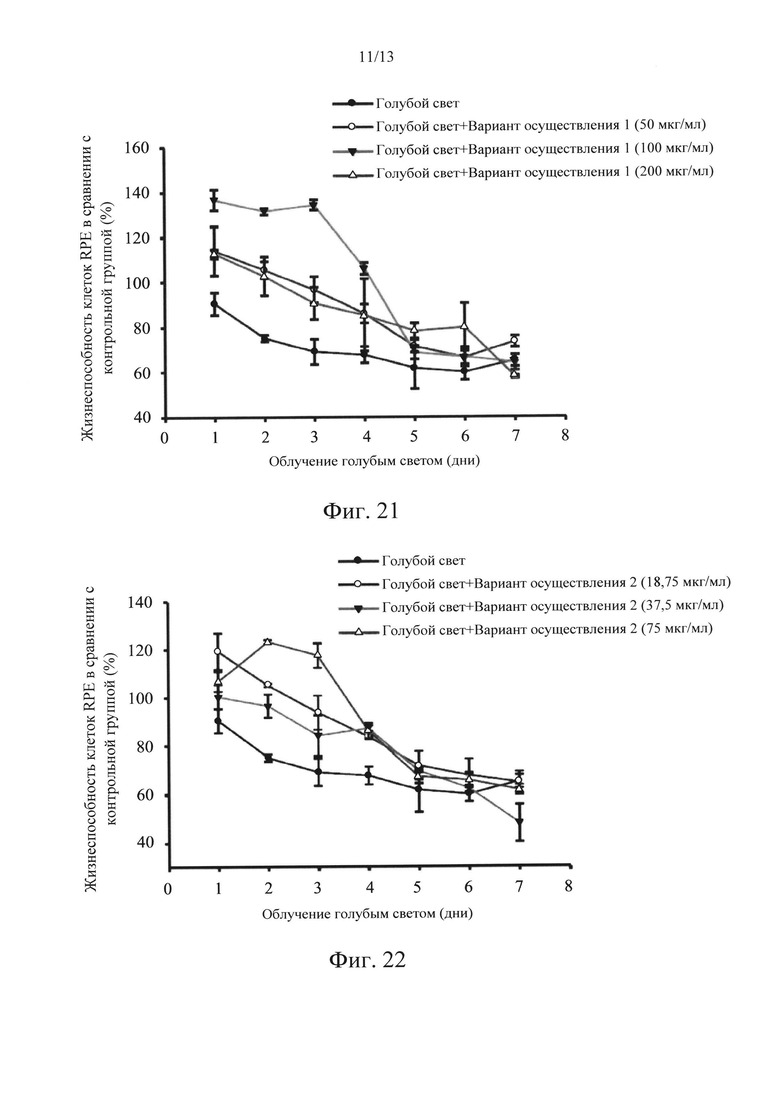
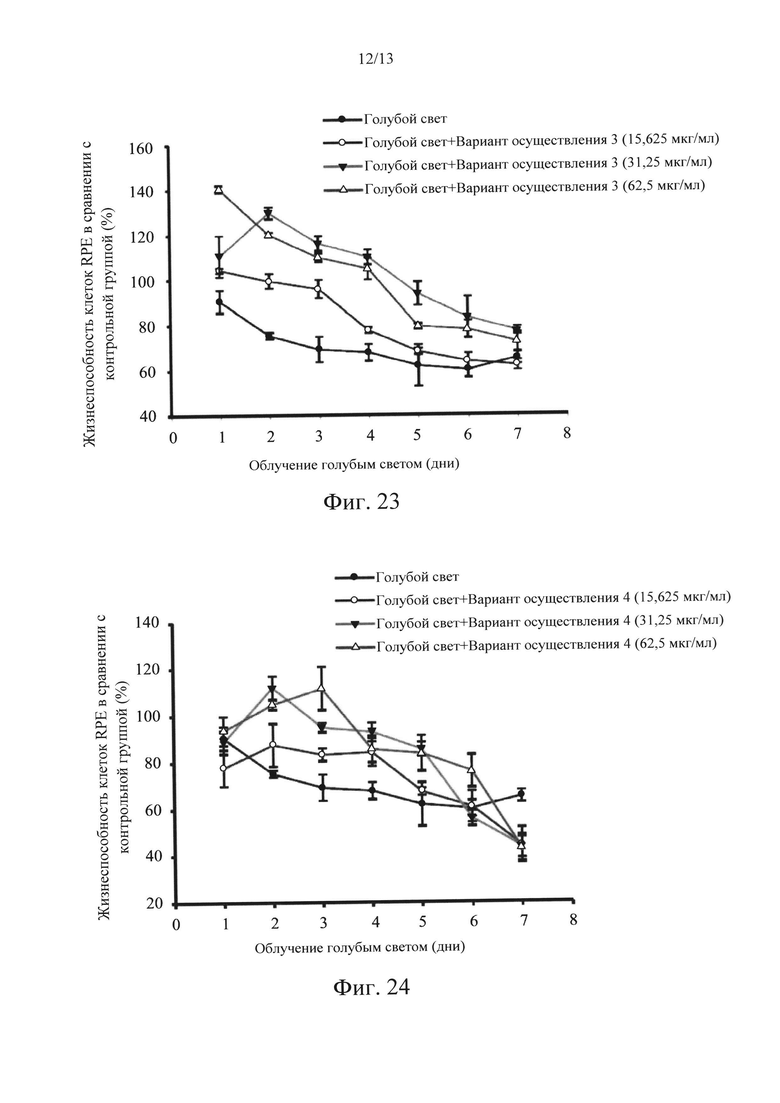
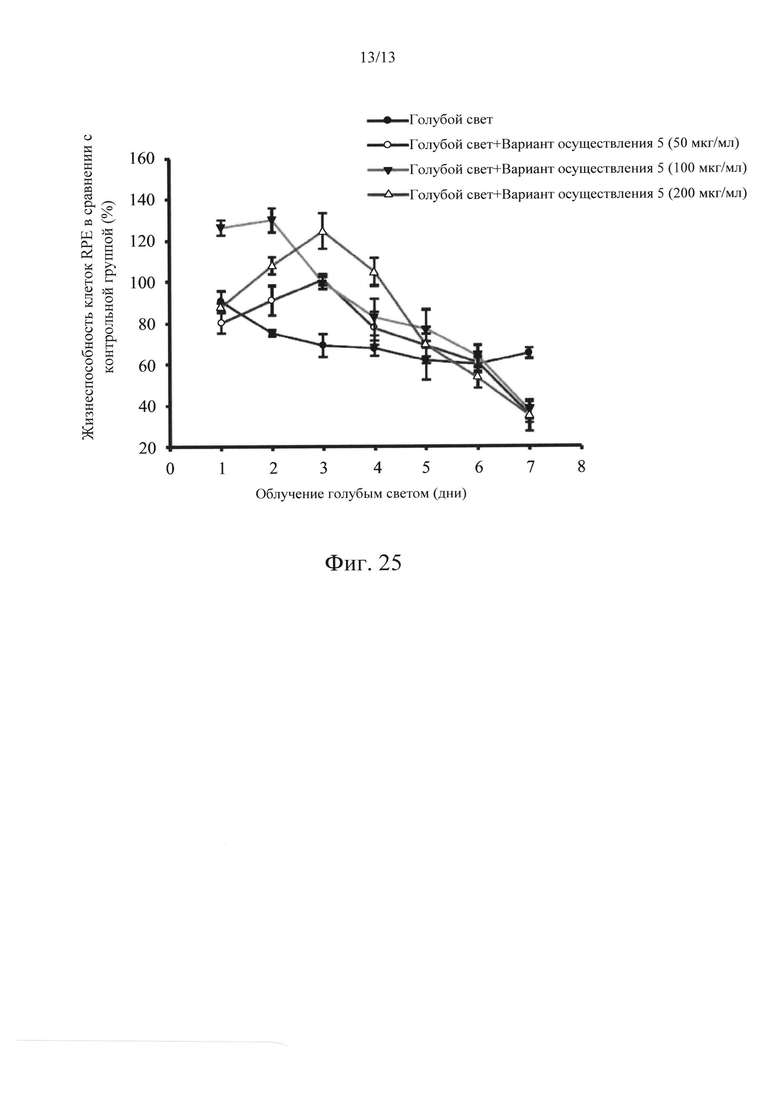
Фиг. 21-25 представляют собой диаграммы, на которых показаны результаты исследования защитного эффекта в соответствии с вариантами осуществления в настоящем раскрытии по отношению к индуцируемой голубым светом цитотоксичности.
Подробное описание
Для того чтобы сделать описание данного раскрытия более подробным и полным, варианты осуществления настоящего раскрытия иллюстративно описаны ниже. Тем не менее, они не являются единственной формой практической реализации или применения вариантов осуществления настоящего раскрытия. Раскрытые различные варианты осуществления могут быть объединены, или они могут заменять друг друга, и один вариант осуществления может быть добавлен к другим вариантам осуществления в ситуации, когда это обеспечивает выгоду. В следующем описании многочисленные конкретные детали будут описаны подробно с целью обеспечить лицу, читающему заявку, полное понимание следующих вариантов осуществления. Тем не менее, варианты осуществления настоящего раскрытия могут реализоваться на практике без определенных конкретных деталей.
Настоящим изобретением предполагается способ применения экстракта Cistanche tubulosa для получения лекарственных средств или продукта питания для защиты клеток глаза.
Cistanche tubulosa также называется "пустынный женьшень" и представляет собой тип Cistanche. Традиционно Cistanche tubulosa представляет собой лекарственное средство, применяемое для оздоровления почек и в качестве афродизиака. Его можно применять для лечения импотенции, бесплодия, слабости, болезненных ощущений в пояснице и коленях и запора. Cistanche tubulosa была включена в Китайскую фармакопею, начиная с редакции 2005 года. Cistanche характеризуется эффектами препятствования окислению, защиты нервных клеток (как например, ингибирования апоптоза нервных клеток), стимуляции секреции фактора роста нервов, регуляции нейромедиаторов в головном мозге, улучшения обучения и памяти и снижения образования амилоида в головном мозге.
В соответствии с вариантом осуществления экстракт Cistanche tubulosa содержит эхинакозид, актеозид, изоактеозид, тубулозид А или их комбинацию. Все из эхинакозида, актеозида, изоактеозида и тубулозида А характеризуются защитным эффектом по отношению к клеткам глаза.
В соответствии с настоящим раскрытием способ получения лекарственных средств или продукта питания для защиты клеток глаза из экстракта Cistanche tubulosa предусматривает обеспечение экстракта Cistanche tubulosa и получение лекарственных средств или продукта питания для защиты клеток глаза из экстракта Cistanche tubulosa. Например, способ получения лекарственных средств или продукта питания для защиты клеток глаза из экстракта Cistanche tubulosa предусматривает получение экстракта из Cistanche tubulosa. Затем к экстрагированным компонентам Cistanche tubulosa добавляют вспомогательные вещества и подвергают обработке с образованием лекарственных средств или продукта питания. В качестве альтернативы, экстрагированные компоненты Cistanche tubulosa можно получать непосредственно и затем добавлять к ним вспомогательные вещества и подвергать непосредственной обработке с образованием лекарственных средств или продукта питания.
Следует отметить, что лекарственные средства и продукт питания, полученные из экстракта Cistanche tubulosa, могут содержать по меньшей мере один из четырех компонентов, описанных выше, и необязательно содержат другие общепринятые вспомогательные вещества, применяемые в лекарственных средствах или продукте питания. Более того, лекарственные средства и продукт питания, полученные из экстракта Cistanche tubulosa, могут присутствовать в любых формах, таких как капсулы, таблетки, порошок или жидкость.
В соответствии с вариантом осуществления настоящего раскрытия лекарственные средства или продукт питания применяют для предупреждения, замедления или лечения заболеваний глаз.
В соответствии с другим вариантом осуществления заболевания глаз представляют собой макулярную дегенерацию, макулярное отверстие, ретинопатию или глаукому.
В соответствии с еще одним вариантом осуществления макулярная дегенерация представляет собой возрастную макулярную дегенерацию. В соответствии с клиническими и патологическими проявлениями возрастную макулярную дегенерацию можно поделить на сухую макулярную дегенерацию и влажную макулярную дегенерацию.
В соответствии с еще одним вариантом осуществления ретинопатия представляет собой диабетическую ретинопатию, пигментный ретинит, заболевание сетчатки, окклюзию артерии и вены сетчатки, пролиферативную витреоретинопатию или центральную серозную ретинопатию.
В соответствии с настоящим раскрытием экстракт Cistanche tubulosa применяют для получения продукта питания или лекарственных средств, причем компоненты экстракта Cistanche tubulosa содержат эхинакозид, актеозид, изоактеозид, тубулозид А или их комбинацию. Эти компоненты могут снижать повреждение от окислительного стресса у клеток глаза и, следовательно, могут делать полученные лекарственные средства или продукт питания способными оказывать защитные эффекты в отношении клеток глаза. На основе экстракта Cistanche tubulosa можно дополнительно разработать лекарственные средства для замедления развития заболеваний глаз, и, в частности, их можно применять для лечения заболеваний, связанных с ретинопатией.
Ниже перечислены несколько вариантов осуществления для разработки способа согласно настоящему раскрытию. Тем не менее, эти варианты осуществления предполагаются в качестве образцов и не используются для ограничения настоящего раскрытия. Таким образом, объем настоящего изобретения должен определяться пунктами прилагаемой формулы изобретения.
Вариант осуществления 1
Вариант осуществления 1 настоящего изобретения предполагает получение экстракта Cistanche tubulosa. Способ предусматривает следующие стадии.
1. 10 кг суккулентного стебля Cistanche tubulosa брали и нарезали ломтиками. Затем нарезанный ломтиками суккулентный стебель погружали в воду в объем, в 8 раз превышающий объем стебля, на 1 час и варили в течение 2 часов. После фильтрования фильтрат собирали.
2. К отфильтрованному остатку добавляли воду в объеме, в 6 раз превышающем объем остатка, и варили дважды, каждый раз в течение 1 часа. Фильтрат собирали.
3. Фильтрат от трех процедур варки объединяли и концентрировали при пониженном давлении при 50°С до тех пор, пока весовое соотношение не составляло 1,10. Этанол добавляли до тех пор, пока концентрация не составляла 60%. После замораживания на 12 часов супернатант выливали, а затем концентрировали при пониженном давлении при 50°С и этанол возвращали для повторного использования до тех пор, пока весовое соотношение не составляло 1,10. Получали 6 кг неочищенных экстрактов.
4. Воду в объеме, равном объему неочищенного экстракта со стадии 3, добавляли и нагревали для растворения неочищенного экстракта на стадии 3. Затем 4-кратный объем воды и 5-кратный объем 40% EtOH использовали для осуществления элюирования. Затем водное средство вливали в колонку, заполненную макропористой смолой. Колонку элюировали 3-кратным объемом воды и водный элюент сливали. После этого колонку элюировали 4-кратным объемом 40% EtOH.
5. Два элюента на основе 40% EtOH на стадии 4 собирали, а затем концентрировали и сушили с получением 1107 г экстракта Cistanche tubulosa. Экстракт Cistanche tubulosa содержит эхинакозид, актеозид, изоактеозид и тубулозид А.
Варианты осуществления 2-5
В настоящем раскрытии эхинакозид применяли в варианте осуществления 2. Актеозид применяли в варианте осуществления 3. Изоактеозид применяли в варианте осуществления 4. Все вышеуказанные материалы были приобретены в ChromaDex, США. Тубулозид А (приобретенный у Tauto Biotech, Шанхай, Китай) применяли в варианте осуществления 5.
Клеточная культура
Пигментный эпителий сетчатки (RPE) располагался между нейроэпителиальным слоем сетчатки и сосудистой оболочкой глаза. RPE является ответственным за многие физиологические функции, таких как гемато-ретинальный барьер, фагоцитоз, участие в цикле превращений родопсина и метаболизме, антиоксидантная функция и секреция факторов роста и т.д. Клетки RPE являются чувствительными к повреждениям от окислительного стресса и, следовательно, к гибели клеток, вызывающей ретинопатию, дисфункцию зрения и даже потеря зрительной функции. Таким образом, клетки RPE обычно используются для изучения клеточной модели заболеваний, связанных с глазами.
В случае возрастной макулярной дегенерации клетки RPE используются в исследовании, поскольку возрастная макулярная дегенерация является тесно связанной с окислительным стрессом или фактором роста сосудистого эндотелия (VEGF), отложением липофусцина (Delori FC et al, 2001), хроническим воспалением и мутацией в системе комплемента. При возрастной макулярной дегенерации окислительный стресс будет вызывать повреждение RPE клеток или хориокапилляра (Boltz A et al, 2010). Повреждение клеток RPE будет вызывать воспаление мембраны Бруха и дисфункцию RPE клеток и запущенное воспаление будет вызывать аномальное отложение внеклеточного матрикса (ЕСМ), воздействуя на биологическую функцию клеток RPE и усиливая развитие возрастной макулярной дегенерации.
RPE клетки (приобретенные у Американской коллекции типовых тканевых культур, сокращается как АТСС) использовали в нижеизложенных вариантах осуществления для оценки защитных эффектов в отношении клеток глаза у вариантов осуществления 1-5 настоящего раскрытия. Культивирование предусматривает следующие стадии.
1. Клоны клеток RPE извлекали из размороженных пробирок в жидком азоте и быстро переносили в стерильный колпачок после оттаивания в 37°С водяной бане в течение 1 минуты. Клоны клеток RPE извлекали и помещали в 10 см чашки, содержащие 10 мл DMEM (среда Игла в модификации Дульбекко). 10% инактивированной фетальной бычьей сыворотки (FBS), 2 мМ L-глутамина, 100 Ед/мл пенициллина и 100 г/мл стрептомицина добавляли в DMEM.
2. Чашки помещали в инкубатор при 37°С и культивировали в условиях смеси газов из 95% воздуха и 5% СО2, а также при влажности 70%. Старые среды заменяли свежими средами каждые 3 дня. Бессывороточную DMEM использовали вместо сред перед осуществлением экспериментов.
3. Когда клетки пролиферировали до уровня, близкому к уровню насыщения, осуществляли подсчет количества клеток с помощью устройства для подсчета клеток. Когда количества клеток достигали приблизительно 2×105 - 1×106 клеток/мл, клетки разводили в соотношении 1:3 для осуществления пассирования. Поскольку клетки RPE представляют собой клетки прикрепляющегося типа, среду, содержащую клетки, переносили в 15 мл центрифужные пробирки, а затем центрифугировали при 72 g в течение 5 минут при комнатной температуре, когда среду заменяли. После центрифугирования супернатант удаляли, а затем добавляли свежую среду для культивирования.
Нижеизложенные примеры использовались для оценки эффектов вариантов осуществления 1-5 настоящего раскрытия при использовании культивируемых клеток RPE.
Пример 1.
Измерение жизнеспособности и роста клеток RPE (МТТ анализ)
Перед экспериментом среду заменяли бессывороточной средой. Фиксированное количество клеток RPE (2×105 клеток/мл) в указанном порядке помещали в 96-луночный планшет. После помещения в инкубатор клетки культивировали в течение 24 часов после обработки различными концентрациями согласно вариантам осуществления 1-5. Затем добавляли 1,0 мг/мл 3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолия бромид (МТТ) и осуществляли реакцию при 37°С в течение 1 часа. Впоследствии 200 мкл диметилсульфоксида (DMSO) добавляли в каждую лунку и встряхивали в темноте при комнатной температуре в течение 10 минут после небольшого перемешивания. После того как оставшиеся клетки полностью растворятся, анализатор для иммуноферментного анализа (ридер MRX для микропланшетов, США) использовали для выявления спектральной поглощающей способности при длине волны 550 нм в каждой лунке. Клетки, не подвергавшиеся обработке с использованием вариантов осуществления, использовали в качестве контрольной группы после культивирования в течение 24 часов.
Одной целью примера 1 является исследование цитотоксичности вариантов осуществления 1-5 в отношении клеток RPE и стимуляция вариантами осуществления 1-5 в отношении роста клеток RPE. Митохондриальный фермент живых клеток может восстанавливать МТТ до формазана в виде пурпурных кристаллов, которые растворяются DMSO. Вкратце, метаболическую активность клеток используют для определения того, являются ли клетки живыми или нет. Измеренная спектральная поглощающая способность растворенного вещества является равной жизнеспособности клеток. Таким образом, чем больше клеток являются живыми, тем выше спектральная поглощающая способность. Расчетная формула для жизнеспособности клеток была показана ниже.
Жизнеспособность клеток (%) = (спектральная поглощающая способность у клеток, обработанных лекарственными средствами в течение 24 часов/ спектральная поглощающая способность у контрольной группы после 24 часов) ×100%
Результаты примера 1 выражали с помощью среднего значения и среднеквадратичной погрешности для количества экспериментов (среднее значение ± S.E.). Статистический анализ осуществляли с помощью t-критерия Стьюдента или однофакторного дисперсионного анализа ANOVA. Если Р<0,05, это указывает на значимое отличие.
Что касается фиг. 1-5, которые представляют собой диаграммы, на которых показаны результаты исследования цитотоксичности в соответствии с настоящим раскрытием, соответственно. На фиг. 1-5 приведены значения IC25, IC50 и IC75 для вариантов осуществления 1-5, и результаты обобщены в таблице 1 ниже.
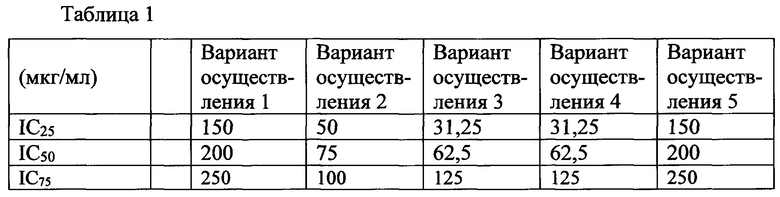
В соответствии с результатами из таблицы 1 IC50 для вариантов осуществления 1-5 сортируют по величине, что показывает следующий порядок: (вариант осуществления 5, вариант осуществления 1) > вариант осуществления 2 > (вариант осуществления 3, вариант осуществления 4). Исследуемую концентрацию, используемую в следующем примере 2, определяли по результату исследования цитотоксичности из примера 1.
Пример 2.
Эффект вариантов осуществления 1-5 в отношении жизнеспособности и роста клеток RPE, обработанных активными формами кислорода (МТТ анализ)
В соответствии с результатом исследования цитотоксичности из примера 1 три концентрации вариантов осуществления 1-5 использовали для исследования повреждения от окислительного стресса в отношении защитного эффекта в примере 2. IC50 для вариантов осуществления 1-5 использовали в качестве наиболее высоких концентрации в примере 2 для повторного подтверждения того, является ли диапазон действия вариантов осуществления 1-5 токсичным, или являются ли они лекарственным средством.
Перед экспериментом среду заменяли бессывороточной средой. Фиксированное количество клеток RPE (2×105 клеток/мл) в указанном порядке помещали в 96-лунок планшета. После помещения в инкубатор клетки обрабатывали разными концентрациями вариантов осуществления 1-5 и культивировали в течение 24 часов. Затем разные концентрации индуктора окислительного стресса добавляли для обработки клеток. Индуктор окислительного стресса, используемый в примере 2, включает в себя перекись водорода (Н2О2, концентрация 0,01-10 мМ), гидроперекись трет-бутила (t-BHP, концентрация 0,01-10 мМ), азид натрия (NaN3, концентрация 0,01-100 мМ) и повреждение, индуцированное голубым светом. Голубой свет, характеризующийся длиной волны 480 нм и освещенностью 350 люкс, испускалось светоизлучающим диодом голубого свечения (LED). Затем после обработки путем облучения голубым светом в течение 7 дней или индуктором окислительного стресса в течение 24 часов добавляли МТТ 0,5 мг/мл и осуществляли реакцию при 37°С в течение 2 часов. После этого 200 мкл DMSO добавляли в каждую лунку. После небольшого перемешивания планшет подвергали действию вибрации в темноте в течение 10 минут. После полного растворения оставшихся клеток анализатор для иммуноферментного анализа использовали для выявления спектральной поглощающей способности в каждой лунке. Клетки, не подвергавшиеся обработке с использованием индукторов окислительного стресса и вариантов осуществления, использовали в качестве контрольной группы. Значения жизнеспособности клеток в сравнении с контрольной группой рассчитывали с использованием формулы расчета жизнеспособности клеток, описанной в примере 1.
Результаты примера 2 выражали с помощью среднего значения и среднеквадратичной погрешности для количества экспериментов (среднее значение ± S.E.). Статистический анализ осуществляли с помощью t-критерия Стьюдента или однофакторного дисперсионного анализа ANOVA. Если Р<0,05, это указывает на значимое отличие.
Механизмы действия индуктора окислительного стресса и токсичных для клеток RPE веществ обобщены в таблице 2 ниже.
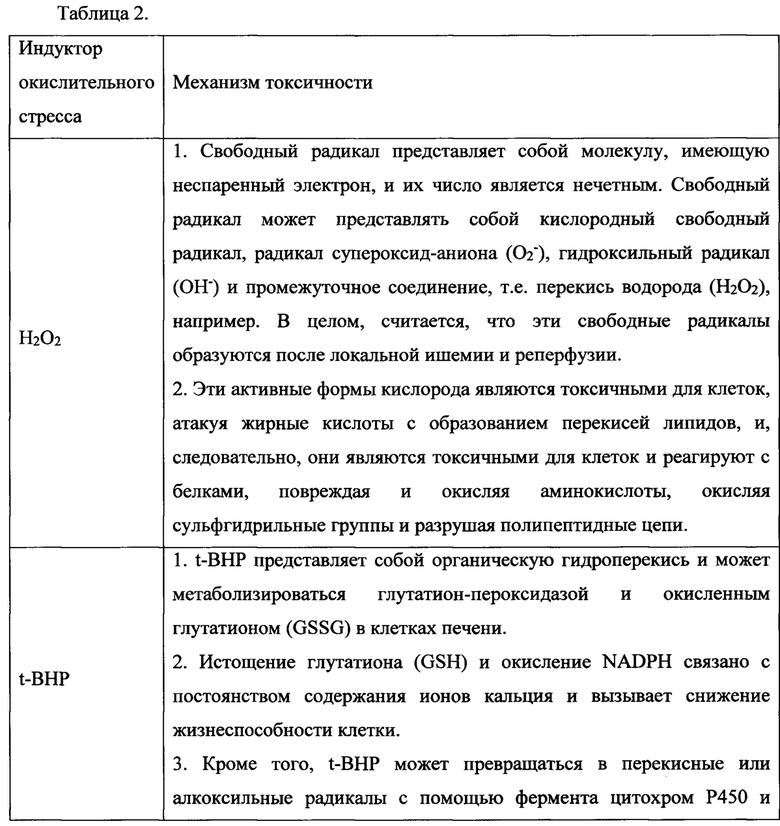

В примере 2 использовались варианты осуществления 1-5 для соответствующей обработки клеток RPE, а затем использовали эти индукторы окислительного стресса для обработки клеток RPE. Защитный эффект вариантов осуществления 1-5 в отношении клеток RPE оценивали по жизнеспособности клеток RPE.
Что касается фиг. 6-10, которые представляют собой диаграммы, на которых показаны результаты исследования защитного эффекта вариантов осуществления 1-5 в отношении цитотоксичности, индуцированной Н2О2. Концентрации варианта осуществления 1 составляли 50, 100 и 200 мкг/мл. Концентрации варианта осуществления 2 составляли 18,75, 37,5 и 75 мкг/мл. Концентрации варианта осуществления 3 составляли 15,625, 31,25 и 62,5 мкг/мл. Концентрации варианта осуществления 4 составляли 15,625, 31,25 и 62,5 мкг/мл. Концентрации варианта осуществления 5 составляли 50, 100 и 200 мкг/мл. Результаты исследования показывали, что 50% клеток RPE погибли после обработки 0,1 мМ Н2О2, т.е. жизнеспособность составляла приблизительно 50%. Вариант осуществления 1, вариант осуществления 2, вариант осуществления 3 и вариант осуществления 5 могут защитить клетки от повреждения, создаваемого при этой концентрации. В частности, вариант осуществления 1 оказывал наиболее сильный защитный эффект, и жизнеспособность повышалась с 50% до 100%, когда вариант осуществления 1 находился в концентрациях 50 мкг/мл и 100 мкг/мл. Более того, когда концентрация варианта осуществления 1 составляла 200 мкг/мл, наблюдали приемлемый цитотоксический ответ, поскольку концентрация практически соответствовала концентрации IC50. Результаты исследования, показанные на фиг. 6-10, также подтверждали, что наиболее эффективно действующий диапазон концентраций варианта осуществления 1 в случае Н2О2 составлял от 50 мкг/мл до 100 мкг/мл.
Что касается фиг. 11-15, которые представляют собой диаграммы, на которых показаны результаты исследования защитного эффекта вариантов осуществления 1-5 в отношении цитотоксичности, индуцированной t-BHP. Концентрации варианта осуществления 1 составляли 50, 100 и 200 мкг/мл. Концентрации варианта осуществления 2 составляли 18,75, 37,5 и 75 мкг/мл. Концентрации варианта осуществления 3 составляли 15,625, 31,25 и 62,5 мкг/мл. Концентрации варианта осуществления 4 составляли 15,625, 31,25 и 62,5 мкг/мл. Концентрации варианта осуществления 5 составляли 50, 100 и 200 мкг/мл. Результаты исследования показывали, что 80% клеток RPE погибли после обработки 0,3 мМ t-BHP, т.е. жизнеспособность составляла приблизительно 20%. Все из вариантов осуществления 1-5 могут защитить клетки от повреждения, создаваемого при этой концентрации. В частности, варианты осуществления 1, 2 и 3 оказывали наиболее сильный защитный эффект, и жизнеспособность клеток повышалась с 20% до более чем 80%, когда варианты осуществления 1, 2 и 3 находились в низких и средних концентрациях. Более того, когда варианты осуществления 1, 2 и 3 находились в высоких концентрациях, наблюдали приемлемый цитотоксический ответ, поскольку высокие концентрации практически соответствовали концентрациям IC50. Результаты исследования, показанные на фиг. 11-15, также подтверждали, что наиболее эффективно действующие диапазоны концентраций вариантов осуществления 1, 2 и 3 в случае t-BHP составляли от низких концентраций до средних.
Что касается фиг. 16-20, которые представляют собой диаграммы, на которых показаны результаты исследования защитного эффекта вариантов осуществления 1-5 в отношении цитотоксичности, индуцированной NaN3. Концентрации варианта осуществления 1 составляли 75, 100 и 125 мкг/мл. Концентрации варианта осуществления 2 составляли 25, 37,5 и 50 мкг/мл. Концентрации варианта осуществления 3 составляли 15,625, 31,25 и 62,5 мкг/мл. Концентрации варианта осуществления 4 составляли 15,625, 31,25 и 62,5 мкг/мл. Концентрации варианта осуществления 5 составляли 75, 100 и 125 мкг/мл. Результаты исследования показывали, что 50% клеток RPE погибли после обработки 10 мМ NaN3, т.е. жизнеспособность составляла приблизительно 50% Все из вариантов осуществления 1-5 могут защитить клетки от повреждения, создаваемого при этой концентрации. В частности, варианты осуществления 1, 4 и 5 оказывали наиболее сильный защитный эффект, и жизнеспособность клеток повышалась до почти 100%, когда варианты осуществления 1, 4 и 5 находились в средних и высоких концентрациях. Варианты осуществления 2 и 3 были на втором месте. Жизнеспособность клеток повышалась с 50% до более чем 80%. Более того, высокие концентрации вариантов осуществления 1-5 при повреждении NaN3 не показывали серьезной токсичности. Этот результат показывал, что IC50 может попадать в диапазон действия лекарственного средства, но дозозависимый эффект не проявлялся. Результаты исследования, показанные на фиг. 16-20, подтверждали, что наиболее эффективно действующий диапазон концентраций вариантов осуществления 1-5 в случае NaN3 составлял от низких концентраций до средних.
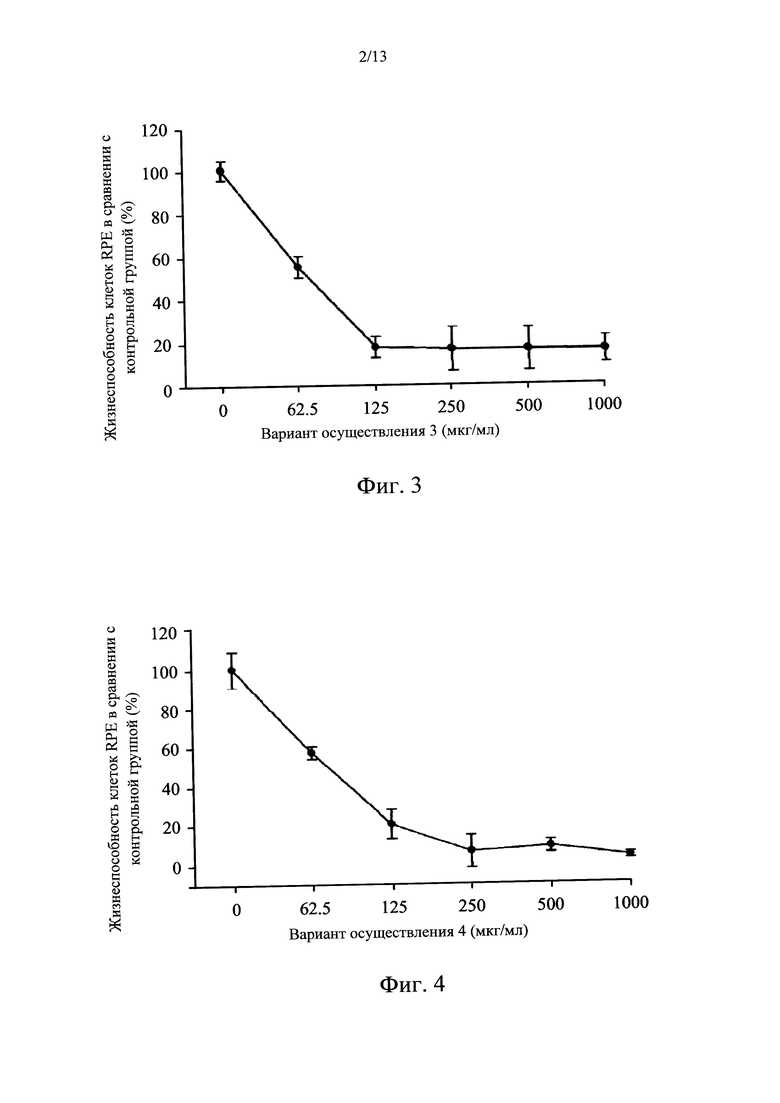
Что касается фиг. 21-25, которые представляют собой диаграммы, на которых показаны результаты исследования защитного эффекта вариантов осуществления 1-5 в отношении цитотоксичности, индуцированной облучением голубым светом. Концентрации варианта осуществления 1 составляли 50, 100 и 200 мкг/мл. Концентрации варианта осуществления 2 составляли 18,75, 37,5 и 75 мкг/мл. Концентрации варианта осуществления 3 составляли 15,625, 31,25 и 62,5 мкг/мл. Концентрации варианта осуществления 4 составляли 15,625, 31,25 и 62,5 мкг/мл. Концентрации варианта осуществления 5 составляли 50, 100 и 200 мкг/мл. Результаты исследования показывали, что 40% клеток RPE погибли после обработки облучением голубым светом (480 нм, 30 люкс) в течение 5 дней, т.е. жизнеспособность составляла приблизительно 60%. Все из вариантов осуществления 1-5 могут защитить клетки от повреждения, создаваемого при этой концентрации. В частности, варианты осуществления 3 и 4 оказывали наиболее сильный защитный эффект, и жизнеспособность клеток повышалась с 60% до более чем 90-100%, когда варианты осуществления 3 и 4 находились в средних концентрациях. Более того, когда варианты осуществления 1-5 находились в высоких концентрациях, наблюдали приемлемый цитотоксический ответ, поскольку высокие концентрации практически соответствовали концентрациям IC50. Результаты исследования, показанные на фиг. 21-25, также подтверждали, что наиболее эффективно действующие диапазоны концентраций вариантов осуществления 3 и 4 в случае облучения голубым светом составляли от низких концентраций до средних.
Анализируя результаты исследований в примерах 1 и 2 согласно настоящему раскрытию, было обнаружено, что в процессе противодействия вариантов осуществления 1-5 повреждению, вызванному индуктором окислительного стресса, варианты осуществления 1-5 могут реагировать с индуктором окислительного стресса, изменяя структуру и вызывая изменение свойств. Свойства вариантов осуществления 1-5 превращались из восстановительных в окислительные. Свойства индуктора окислительного стресса превращались из окислительных в восстановительные. Следовательно, снижался как эффект вариантов осуществления 1-5 против индуктора окислительного стресса, так и повреждение от индуктора окислительного стресса клеток. Эта ситуация становилась все более явной, когда концентрации вариантов осуществления 1-5 и индуктора окислительного стресса возрастали.
Результаты исследований всех индукторов окислительного стресса в примере 2 обобщены в таблице 3 ниже.

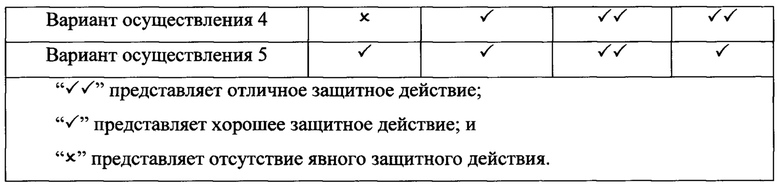
Из краткого описания в таблице 3 можно выяснить, что варианты осуществления 1-5 характеризуются защитным эффектом в отношении повреждения клеток RPE, вызываемого t-BHP, NaN3 и голубым светом, причем варианты осуществления 1 и 4 характеризовались еще более сильным защитным эффектом.
В заключение, настоящим раскрытием предполагается способ применения экстракт Cistanche tubulosa для получения лекарственных средств или продукта питания для защиты клеток глаза. Экстракт Cistanche tubulosa может уменьшать повреждение от окислительного стресса в отношении клеток глаза. Таким образом, лекарственные средства и продукт питания, полученные из экстракта Cistanche tubulosa, характеризуются хорошим защитным эффектом в отношении клеток глаза, и могут быть дополнительно разработать лекарственные средства и продукт питания для предупреждения заболевания глаз или замедления развития заболевания глаз.
Несмотря на то что варианты осуществления настоящего изобретения были раскрыты, как изложено выше, не предполагается, что они ограничивают настоящее изобретение. Любой специалист в данной области техники может создать различные модификации и изменения, не отходя от идеи и объема настоящего изобретения. Таким образом, объем настоящего изобретения должен определяться пунктами прилагаемой формулы изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ РЕГУЛЯЦИИ УРОВНЯ ГЛЮКОЗЫ В КРОВИ | 2014 |
|
RU2637635C2 |
| ТЕРАПЕВТИЧЕСКИЕ И НЕЙРОПРОТЕКТОРНЫЕ ПЕПТИДЫ | 2018 |
|
RU2788097C2 |
| Лечение глазных болезней типа дегенерации желтого пятна, глаукомы и диабетической ретинопатии с помощью лекарственных средств, устраняющих стареющие клетки | 2018 |
|
RU2815482C2 |
| ХИМИЧЕСКИЕ СОЕДИНЕНИЯ, ВОЗДЕЙСТВУЮЩИЕ НА ГЛАЗА, И ИХ ПРИМЕНЕНИЕ ПРИ ЛЕЧЕНИИ ГЛАЗНЫХ ЗАБОЛЕВАНИЙ | 2020 |
|
RU2830634C1 |
| ПРОФИЛАКТИЧЕСКОЕ ИЛИ ТЕРАПЕВТИЧЕСКОЕ СРЕДСТВО ДЛЯ ВОЗРАСТНОЙ ДЕГЕНЕРАЦИИ ЖЕЛТОГО ПЯТНА | 2008 |
|
RU2460526C2 |
| ИНГИБИТОРЫ ГИСТОНДЕАЦЕТИЛАЗЫ ДЛЯ ЛЕЧЕНИЯ ДЕГЕНЕРАТИВНЫХ ЗАБОЛЕВАНИЙ ГЛАЗ | 2003 |
|
RU2324483C2 |
| КОМПОЗИЦИЯ ДЛЯ ПРОФИЛАКТИКИ ИЛИ ЛЕЧЕНИЯ ГЛАЗНЫХ БОЛЕЗНЕЙ, СОДЕРЖАЩАЯ S-АЛЛИЛ-L-ЦИСТЕИН В КАЧЕСТВЕ АКТИВНОГО ИНГРЕДИЕНТА, И ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ, СОДЕРЖАЩИЙ ЕЕ | 2013 |
|
RU2605618C2 |
| МЕСТНЫЙ ГЛАЗНОЙ ПЕПТИДНЫЙ СОСТАВ | 2010 |
|
RU2561585C2 |
| НАНОСТРУКТУРИРОВАННЫЕ КОМПОЗИЦИИ ДЛЯ ДОСТАВКИ СИЛИБИНИНА И ДРУГИХ АКТИВНЫХ ИНГРЕДИЕНТОВ ДЛЯ ЛЕЧЕНИЯ ГЛАЗНЫХ ЗАБОЛЕВАНИЙ | 2015 |
|
RU2726193C2 |
| СОСТАВЫ НА ОСНОВЕ СУНИТИНИБА И СПОСОБЫ ИХ ПРИМЕНЕНИЯ ДЛЯ ЛЕЧЕНИЯ ГЛАЗНЫХ ЗАБОЛЕВАНИЙ | 2015 |
|
RU2729731C2 |




Изобретение относится к фармацевтической и пищевой промышленности, а именно к применению экстракта Cistanche tubulosa для получения продукта для предупреждения, замедления или лечения заболеваний глаз, вызванных окислительным стрессом, индуцированным трет-бутилгидропероксидом (t-BHP), ишемией или синим светом. Применение экстракта Cistanche tubulosa для приготовления лекарственного средства для предупреждения, замедления или лечения заболеваний глаз, вызванных окислительным стрессом, индуцированным трет-бутилгидропероксидом (t-BHP), ишемией или синим светом, причем экстракт Cistanche tubulosa содержит компонент, выбранный из группы, состоящей из эхинакозида, актеозида, изоактеозида, тубулозида А или их комбинации. Применение компонента экстракта Cistanche tubulosa, выбранного из группы, включающей эхинакозид, актеозид, изоактеозид, тубулозид А или их комбинацию, для приготовления лекарственного средства для предупреждения, замедления или лечения заболеваний глаз, вызванных окислительным стрессом, индуцированным трет-бутилгидропероксидом (t-BHP), ишемией или синим светом. Применение экстракта Cistanche tubulosa для приготовления продукта питания для защиты клеток глаза от повреждения, вызванного окислительным стрессом, индуцированным трет-бутилгидропероксидом (t-BHP), ишемией или синим светом, причем экстракт Cistanche tubulosa содержит компонент, выбранный из группы, состоящей из эхинакозида, актеозида, изоактеозида, тубулозида А или их комбинации. Применение компонента экстракта Cistanche tubulosa, выбранного из группы, включающей эхинакозид, актеозид, изоактеозид, тубулозид А или их комбинацию, для приготовления продукта питания для защиты клеток глаза от повреждения, вызванного окислительным стрессом, индуцированным трет-бутилгидропероксидом (t-BHP), ишемией или синим светом. Применение экстракта Cistanche tubulosa для приготовления лекарственного средства для защиты клеток глаза от повреждения, вызванного окислительным стрессом, индуцированным трет-бутилгидропероксидом (t-BHP), ишемией или синим светом, причем экстракт Cistanche tubulosa содержит компонент, выбранный из группы, состоящей из эхинакозида, актеозида, изоактеозида, тубулозида А или их комбинации. Применение компонента экстракта Cistanche tubulosa, выбранного из группы, включающей эхинакозид, актеозид, изоактеозид, тубулозид А или их комбинацию, для приготовления лекарственного средства для защиты клеток глаза от повреждения, вызванного окислительным стрессом, индуцированным трет-бутилгидропероксидом (t-BHP), ишемией или синим светом. Вышеописанные средства эффективны для защиты клеток глаза от повреждения, вызванного окислительным стрессом, индуцированным трет-бутилгидропероксидом (t-BHP), ишемией или синим светом, или для предупреждения, замедления или лечения заболеваний глаз, вызванных окислительным стрессом, индуцированным трет-бутилгидропероксидом (t-BHP), ишемией или синим светом. 6 н. и 13 з.п. ф-лы, 25 ил., 3 табл., 2 пр.
1. Применение экстракта Cistanche tubulosa для приготовления лекарственного средства для предупреждения, замедления или лечения заболеваний глаз, вызванных окислительным стрессом, индуцированным трет-бутилгидропероксидом (t-BHP), ишемией или синим светом,
причем экстракт Cistanche tubulosa содержит компонент, выбранный из группы, состоящей из эхинакозида, актеозида, изоактеозида, тубулозида А или их комбинации.
2. Применение по п. 1, в котором заболевания глаз представляют собой макулярную дегенерацию, макулярное отверстие, ретинопатию или глаукому.
3. Применение по п. 2, в котором макулярная дегенерация представляет собой возрастную макулярную дегенерацию.
4. Применение по п. 3, в котором возрастная макулярная дегенерация представляет собой сухую макулярную дегенерацию или влажную макулярную дегенерацию.
5. Применение по п. 2, в котором ретинопатия представляет собой диабетическую ретинопатию, пигментный ретинит, заболевание сетчатки, окклюзию артерии и вены сетчатки, пролиферативную витреоретинопатию или центральную серозную ретинопатию.
6. Применение по п. 1, в котором форма лекарственного средства представляет собой капсулу, таблетку, порошок или жидкость.
7. Применение компонента экстракта Cistanche tubulosa, выбранного из группы, включающей эхинакозид, актеозид, изоактеозид, тубулозид А или их комбинацию, для приготовления лекарственного средства для предупреждения, замедления или лечения заболеваний глаз, вызванных окислительным стрессом, индуцированным трет-бутилгидропероксидом (t-BHP), ишемией или синим светом.
8. Применение по п. 7 в котором заболевания глаз представляют собой макулярную дегенерацию, макулярное отверстие, ретинопатию или глаукому.
9. Применение по п. 8, в котором макулярная дегенерация представляет собой возрастную макулярную дегенерацию.
10. Применение по п. 9, в котором возрастная макулярная дегенерация представляет собой сухую макулярную дегенерацию или влажную макулярную дегенерацию.
11. Применение по п. 8, в котором ретинопатия представляет собой диабетическую ретинопатию, пигментный ретинит, заболевание сетчатки, окклюзию артерии и вены сетчатки, пролиферативную витреоретинопатию или центральную серозную ретинопатию.
12. Применение по п. 7, в котором форма лекарственного средства представляет собой капсулу, таблетку, порошок или жидкость.
13. Применение экстракта Cistanche tubulosa для приготовления продукта питания для защиты клеток глаза от повреждения, вызванного окислительным стрессом, индуцированным трет-бутилгидропероксидом (t-BHP), ишемией или синим светом, причем экстракт Cistanche tubulosa содержит компонент, выбранный из группы, состоящей из эхинакозида, актеозида, изоактеозида, тубулозида А или их комбинации.
14. Применение компонента экстракта Cistanche tubulosa, выбранного из группы, включающей эхинакозид, актеозид, изоактеозид, тубулозид А или их комбинацию, для приготовления продукта питания для защиты клеток глаза от повреждения, вызванного окислительным стрессом, индуцированным трет-бутилгидропероксидом (t-BHP), ишемией или синим светом.
15. Применение по п. 14, в котором эхинакозид, актеозид, изоактеозид, тубулозид А или их комбинация экстрагированы из растения.
16. Применение экстракта Cistanche tubulosa для приготовления лекарственного средства для защиты клеток глаза от повреждения, вызванного окислительным стрессом, индуцированным трет-бутилгидропероксидом (t-BHP), ишемией или синим светом, причем экстракт Cistanche tubulosa содержит компонент, выбранный из группы, состоящей из эхинакозида, актеозида, изоактеозида, тубулозида А или их комбинации.
17. Применение по п. 16, в котором форма лекарственного средства представляет собой капсулу, таблетку, порошок или жидкость.
18. Применение компонента экстракта Cistanche tubulosa, выбранного из группы, включающей эхинакозид, актеозид, изоактеозид, тубулозид А или их комбинацию, для приготовления лекарственного средства для защиты клеток глаза от повреждения, вызванного окислительным стрессом, индуцированным трет-бутилгидропероксидом (t-BHP), ишемией или синим светом.
19. Применение по п. 18, в котором форма лекарственного средства представляет собой капсулу, таблетку, порошок или жидкость.
| BARNSTABLE CJ | |||
| Mitochondria and the regulation of free radical damage in the eye // Ocul boil dis infor., 2009 sep, 2(3):145-148 | |||
| CN 1526400 A, 08.09.2004 | |||
| Устройство для обнаружения продольного разрыва ленты конвейера | 1959 |
|
SU134169A1 |
| JP 2013023487 A, 04.02.2013. | |||
Авторы
Даты
2019-05-23—Публикация
2015-07-03—Подача