Область техники, к которой относится изобретение
Изобретение относится к новым синтезированным химическим соединениям, имеющим тропность к глазу после перорального введения. Оно также относится к области терапевтических применений и относится к применению указанных химических соединений для улучшения зрения у млекопитающих.
Конкретнее, настоящее изобретение относится к применению соединений для защиты клеток пигментного эпителия сетчатки (RPE), в частности, для лечения возрастной макулярной дегенерации (AMD) или болезни Штаргардта и пигментного ретинита у млекопитающих. Целью изобретения является улучшение зрения лиц, страдающих такими заболеваниями, или по меньшей мере стабилизация прогрессирования таких заболеваний.
Уровень техники
Возрастная макулярная дегенерация (AMD) является наиболее распространенной причиной юридической слепоты среди населения в возрасте 60 лет и старше, в частности, в Европе и Северной Америке (Smith et al., 2001). AMD поражает центральную часть сетчатки, называемую макулой, что приводит к серьезным нарушениям зрения и необратимой потере центрального зрения.
Функция желтого пятна является основой центрального зрения и остроты зрения, высокое разрешение которого связано с его высокой концентрацией в фоторецепторах, специфически ответственных за дневное зрение и восприятие цветов, и называемых колбочками. Ранняя стадия AMD отмечается появлением отложений, называемых друзами, и прогрессирующей потерей фоторецепторов, специализированных для ночного видения, называемых палочками, которые лишь незначительно влияют на дневное зрение. Однако постепенно субъект замечает изменение своего зрения, которое затем диагностируется офтальмологом, это является промежуточной формой или возрастной макулярной дегенерацией (AMD). Поздние фазы AMD могут иметь две формы: влажную форму, также называемую экссудативной или неоваскулярной (характеризуется ростом хорееподобных новых сосудов в субретинальном пространстве), или географическую атрофию (сухая форма), которая характеризуется потерей клеток пигментного эпителия сетчатки (RPE) и фоторецепторов, которые являются клетками, необходимыми для зрительного цикла. Число пациентов, страдающих промежуточной формой AMD или сухой формой, намного больше, чем число субъектов, страдающих влажной формой AMD (Smith et al., 2001). Последние стадии AMD, независимо от ее формы (влажная или сухая), приводят к необратимому разрушению желтого пятна. Прогрессирование экссудативной AMD (влажная форма) может привести к полной слепоте в течение нескольких недель, в то время как прогрессирование сухой AMD обычно происходит медленно.
Хотя конкретные механизмы, вовлеченные в инициировании AMD, многочисленны, показано, что окислительный стресс и воспаление являются важными элементами, которые вносят вклад в ее физиопатологию. Этиологические теории AMD включают гидродинамические модификации в оболочке Бруха, вызванные прогрессирующим накоплением внеклеточного материала, содержащего липиды, и старением RPE, активность которого обязательна для выживания фоторецепторов. Старение, которое является первым фактором риска развития AMD, вызывает ухудшение функции клеток RPE и недостаточность их метаболизма, а также их фагоцитарной активности. Неполная физиологическая переработка внешних сегментов фоторецепторов может привести к образованию друз, которые уменьшают диффузию через оболочку Бруха. С возрастом в RPE накапливается все большее количество липофусцинов. Последние состоят из липидов и белков, которые поступают из фаголизосом, лизосом, присутствующих в клетках RPE, и непосредственно из фоторецепторов. Липофусцины также содержат N-ретинил-N-ретинилиденэтаноламин (A2E), который образуется путем конденсации двух молекул ретинальдегида с одной молекулой этаноламина.
С возрастом наблюдается повышенное накопление A2E в сетчатке у пациентов, страдающих от AMD (Bhosale et al., 2009). Под действием синего света и в присутствии кислорода A2E генерирует реактивные формы, которые вызывают повреждение белков, липидов и ДНК и, следовательно, значительный окислительный стресс в стареющих клетках RPE (Sparrow & Cai, 2001). Такое повреждение нарушает лизосомную активность клеток RPE и вызывает накопление отходов, что в конечном итоге вызывает, от места к месту, гибель клеток RPE, за которой следует гибель фоторецепторов, с которыми они ассоциированы.
Болезнь Штаргардта и пигментный ретинит представляют собой дегенерации сетчатки генетического происхождения, которые могут быть вызваны большим количеством мутаций или генетических полиморфизмов. Эти две патологии можно связать с сухой формой AMD, поскольку они характеризуются прогрессирующей потерей клеток RPE и фоторецепторов, что связано с прогрессирующим накоплением A2E в случае болезни Штаргардта. Как и при сухой форме AMD, дегенерация фоторецепторов и RPE приводит к потере ночного зрения и затем к замедлению центрального зрения у пациентов, страдающих этими двумя генетическими патологиями.
Среди существующих методов лечения известны интравитреальные инъекции антител против VEGF (фактора роста эндотелия сосудов), которые позволяют частично блокировать образование новых сосудов и, таким образом, предлагают терапевтический вариант для влажной формы AMD. В настоящее время на рынке нет средств для лечения сухой формы AMD (AMD и географической атрофии). Подобным образом, в настоящее время не имеется лекарств для лечения болезни Штаргардта или пигментного ретинита. В рамках сухой AMD получены пищевые добавки с характерными антиоксидантными соединениями, а именно минералами и витаминами с антиоксидантными свойствами, например цинка, витаминов А, С и Е. Их терапевтическая эффективность реальна, но ограничена AMD. Формулы нутрицевтиков 1 и 2 AREDS ("Age-Related Eye Disease Study", AREDS 2001) считаются стандартом лечения в Соединенных Штатах для лечения AMD, снижая риск прогрессирования влажной AMD на 25% и потери зрения на 19% в течение пяти лет. Многие продукты предлагают общую основу состава: цинк и витамины С и Е, к которым добавляют различные ингредиенты: лютеин, ресвератрол, жирные кислоты омега-3, однако без каких-либо убедительных данных об эффективности таких дополнительных ингредиентов или о категориях пациентов, способных благоприятно реагировать на такие различные молекулы (Elliot & Williams, 2012).
Каротиноиды (молекулы исключительно из пищи) исследованы подробнее, поскольку некоторые из них (лютеин, зеаксантин = ксантофиллы) присутствуют в макуле от природы (Subczynski et al., 2010), и известно, что эти соединения обладают сильной антиоксидантной способностью и также поглощают синий свет, ограничивая таким образом его токсическое воздействие. Поэтому логично, что эти соединения испытаны (по отдельности или в комбинации) в формулах AREDS. Полученные результаты были разочаровывающими, добавки были эффективны только для подгруппы пациентов с дефицитом этих соединений (Pinazo-Durán et al., 2014). Другие ксантофиллы также были объектом исследований при пероральном приеме отдельно или в комбинации с лютеином и/или зеаксантином (напр., астаксантином - Parisi et al., 2008). Ди-апо-каротиноиды (= каротиноиды, усеченные с обоих концов - химическая номенклатура ИЮПАК) проверены in vitro и in vivo, в частности кроцетин (= 8,8'-диапокаротен-8,8'-диоат) и его гликозиды (кроцины). Кроцины оказывают фотозащитное действие in vitro на первичные культуры фоторецепторов крупного рогатого скота или приматов (Laabich et al., 2006), а кроцетин защищает ганглионарные клетки от окислительного стресса (Yamauchi et al., 2011). Эксперименты также проводились с другим апокаротиноидом биксином (= 6-метилгидро[9Z]-6,6'-диапокаротен-6,6'-диоатом) или некоторыми его производными in vitro на ганглионарных клетках и in vivo путем интравитреальных инъекций для противодействия эффектам стресса эндоплазматического ретикулума (Tsuruma et al., 2012). Ранее разработанный экстракт семян урукума (Bixa orellana) (Bixilia®), обогащенный биксином, показал фотозащитное действие на кожу человека, подвергшуюся воздействию УФ (WO 2010149942; Veillet et al., 2009), и на клетки RPE, подвергшиеся фотоокислительному стрессу (WO 2012156600; Fontaine et al., 2011). Наконец, норбиксин (6,6'-диапокаротин-6,6'-диоат) и, в частности, его форма 9’-цис, позволяет существенно снизить гибель клеток, вызванную освещением синим излучением клеток RPE, предварительно обработанных N-ретинил-N-ретинилиденэтаноламином (A2E) (WO 2016174360; Lafont et al. 2015, Fontaine et al., 2016). Пероральное длительное лечение 9’-цис-норбиксином также позволяет уменьшить накопление A2E в сетчатке мышей с двойным KO (ABCA4-/-, RDH8-/-) (Fontaine et al., 2016). Хотя норбиксин обладает хорошей биодоступностью, его накопление в глазу остается очень низким и поэтому ограничивает его защитную активность в сетчатке.
Раскрытие изобретения
Авторы изобретения создали инновационные соединения путем гемисинтеза. Они также обнаружили, что некоторые из таких соединений имеют лучший фармакокинетический профиль и лучшую тропность к глазу, чем у норбиксина. Кроме того, некоторые из таких соединений обладают фотозащитной активностью для пигментного эпителия сетчатки (RPE), которая эквивалентна или превосходит активность норбиксина.
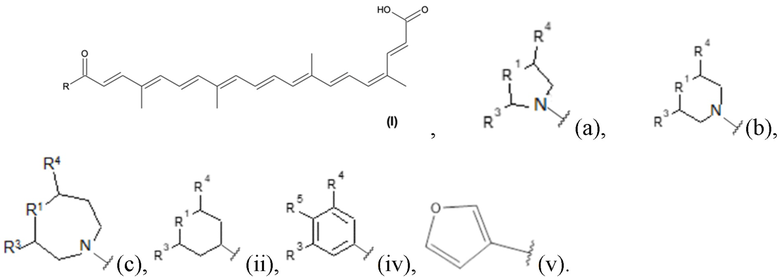
Согласно первому аспекту, изобретение относится к химическому соединению, имеющему следующую общую формулу (I)
[Хим. ф-ла 1]
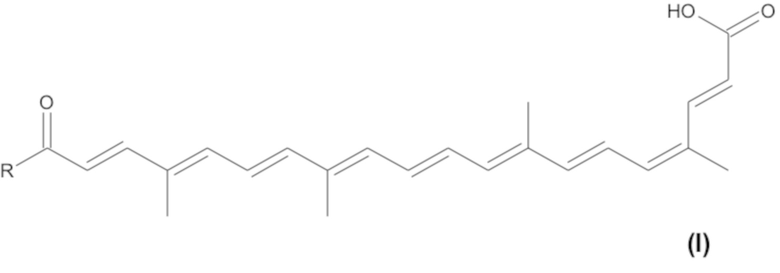 ,
,
где COR представляет собой вторичный или третичный амид, так что -R выбирают из
• -M; -NH-(CH2)n-M и -NH-(CH2)n-C(CH3)(CH3)-M, причем -M выбирают из
а)
[Хим. ф-ла 2]
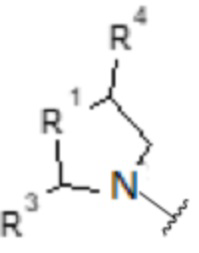 ,
,
b)
[Хим. ф-ла 3]
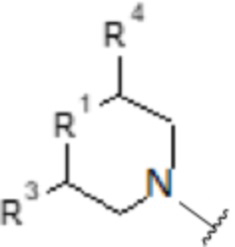 ,
,
с)
[Хим. ф-ла 4]
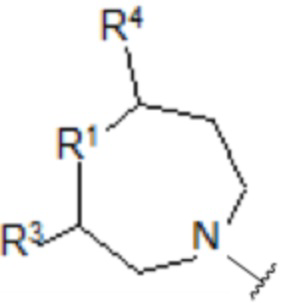 ,
,
в которых
- R1 выбирают из атома кислорода, атома серы, >CH2, >CH-O-(CH2)n-CH3, >CH-(CH2)n-O-(CH2)n-CH3, >CH-(CH2)n-OH, >CH-COOH, >C(OH)фенила или группы >NH;
- R3 выбирают из атома водорода, C1-C6-алкила, -OH или C1-C6-O-алкильной группы;
- R4 выбирают из атома водорода, C1-C6-алкила, -OH или C1-C6-O-алкильной группы;
- n равен целому числу от 0 до 6;
• -NH-(CH2)n-W, причем W представляет собой атом водорода или группу -OH, группу -O-(CH2)n-CH3 или группу, выбранную из
i)
[Хим. ф-ла 5]
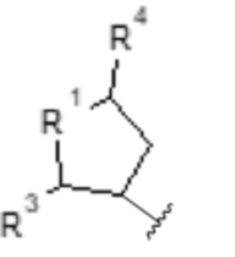 ,
,
ii)
[Хим. ф-ла 6]
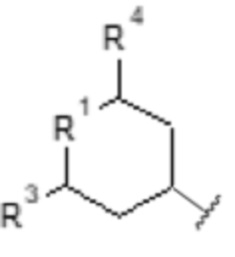 ,
,
iii)
[Хим. ф-ла 7]
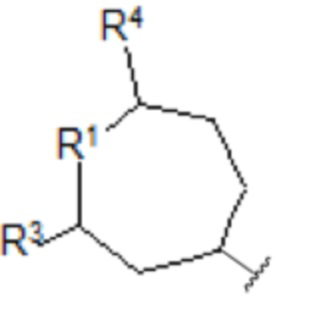 ,
,
iv)
[Хим. ф-ла 8]
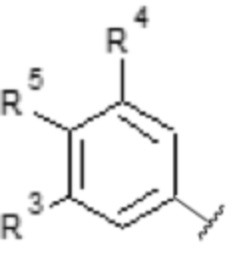 ,
,
v)
[Хим. ф-ла 9]
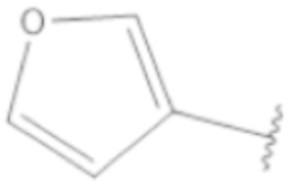 ,
,
в которых
- R1 выбирают из атома кислорода, атома серы, >CH2, >CH-O-(CH2)n-CH3, >CH-(CH2)n-OH, >CH-COOH, >C(OH)фенила или группы >NH;
- R3 выбирают из атома водорода, C1-C6-алкила, -OH или C1-C6-O-алкильной группы;
- R4 выбирают из атома водорода, C1-C6-алкила, -OH или C1-C6-O-алкильной группы;
- R5 выбирают из -CH3, -OH, -O-(CH2)n-CH3, -(CH2)n-OH или группы -COOH;
- n равен целому числу от 0 до 6;
а также фармацевтически приемлемым солям указанного химического соединения.
Термин «химическое соединение» также обозначает изомеры указанного химического соединения и, в частности, стереоизомеры.
В рамках настоящего изобретения «фармацевтически приемлемый» обозначает соединение, которое полезно при получении фармацевтической композиции, которая в целом безопасна, нетоксична и которая не является биологически или иначе нежелательной, и которая приемлема для ветеринарного применения, а также для фармацевтического применения человеком.
В рамках настоящего изобретения термин «фармацевтически приемлемые соли соединения» обозначает соли, которые являются фармацевтически приемлемыми по определению в настоящем описании и которые имеют желательную фармакологическую активность исходного соединения. Такие соли включают
(1) соли присоединения кислот, образованные с минеральными кислотами, такими как хлороводородная кислота, бромоводородная кислота, серная кислота, азотная кислота, фосфорная кислота и подобные; или образованные с органическими кислотами, такими как уксусная кислота, бензолсульфоновая кислота, бензойная кислота, камфорсульфоновая кислота, лимонная кислота, этансульфоновая кислота, фумаровая кислота, глюкогептоновая кислота, глюконовая кислота, глутаминовая кислота, гликолевая кислота, гидроксинафтойная кислота, 2-гидроксиэтансульфоновая кислота, молочная кислота, малеиновая кислота, яблочная кислота, миндальная кислота, метансульфоновая кислота, муконовая кислота, 2-нафталинсульфоновая кислота, пропионовая кислота, салициловая кислота, янтарная кислота, дибензоил-L-винная кислота, винная кислота, п-толуолсульфоновая кислота, триметилуксусная кислота, трифторуксусная кислота и подобные; или
(2) соли, образующиеся, когда кислотный протон, присутствующий в исходном соединении, или заменяется ионом металла, например ионом щелочного металла, ионом щелочноземельного металла или ионом алюминия; или координируется с органическим или неорганическим основанием. Приемлемые органические основания включают диэтаноламин, этаноламин, N-метилглюкамин, триэтаноламин, трометамин и подобные. Приемлемые неорганические основания включают гидроксид алюминия, гидроксид кальция, гидроксид калия, карбонат натрия и гидроксид натрия.
Согласно определенному воплощению изобретение относится к химическому соединению, имеющему общую формулу (I), выбранному из химических соединений, включая следующие:
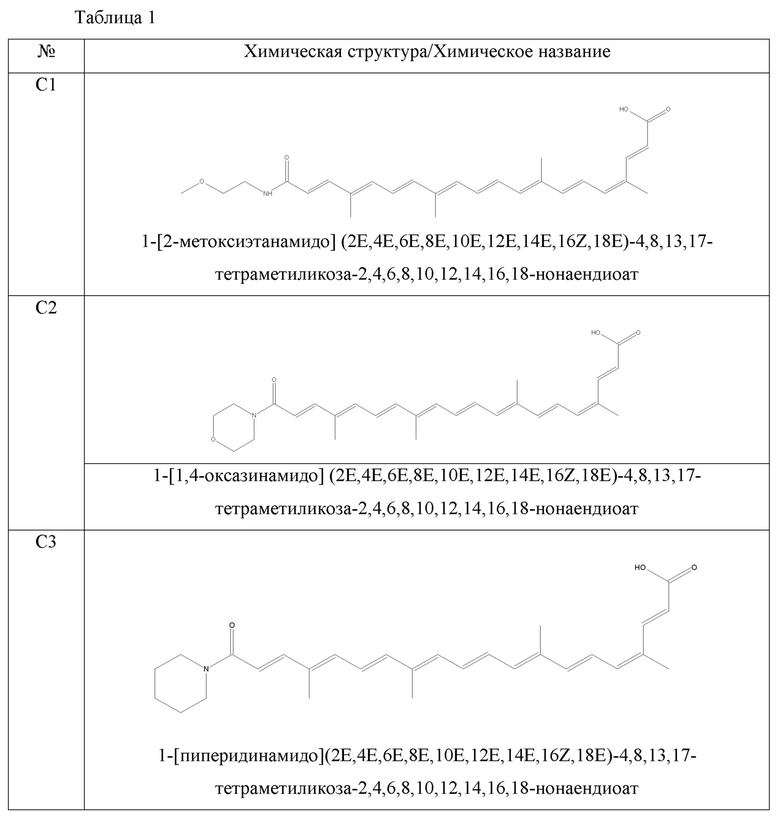
- 1-[2-метоксиэтанамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
- 1-[1,4-оксазинамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
- 1-[пиперидинамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметилкоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
- 1-[2-гидроксиэтанамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
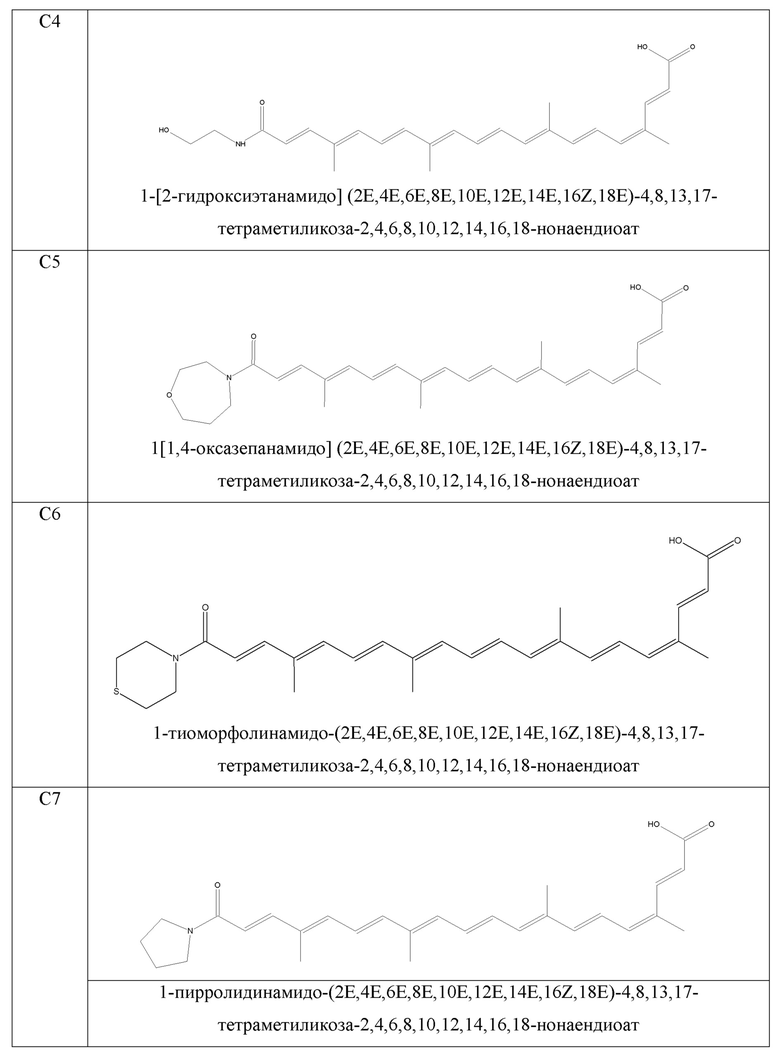
- 1[1,4-оксазепанамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметилкоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
- 1-тиоморфолинамидо-(2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
- 1-пирролидинамидо-(2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметилкоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
- 1-[2-морфолинопропанамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
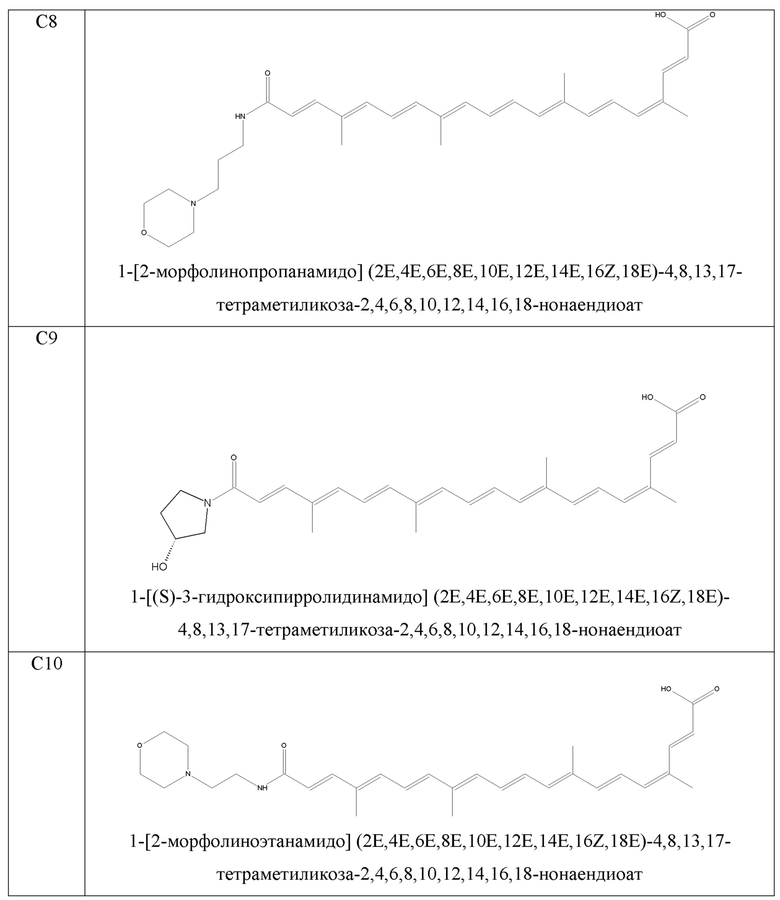
- 1-[(S)-3-гидроксипирролидинамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
- 1-[2-морфолиноэтанамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметилкоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
- 1-[(R)-3-гидроксипирролидинамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
- 1-[4-гидроксипиперидинамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
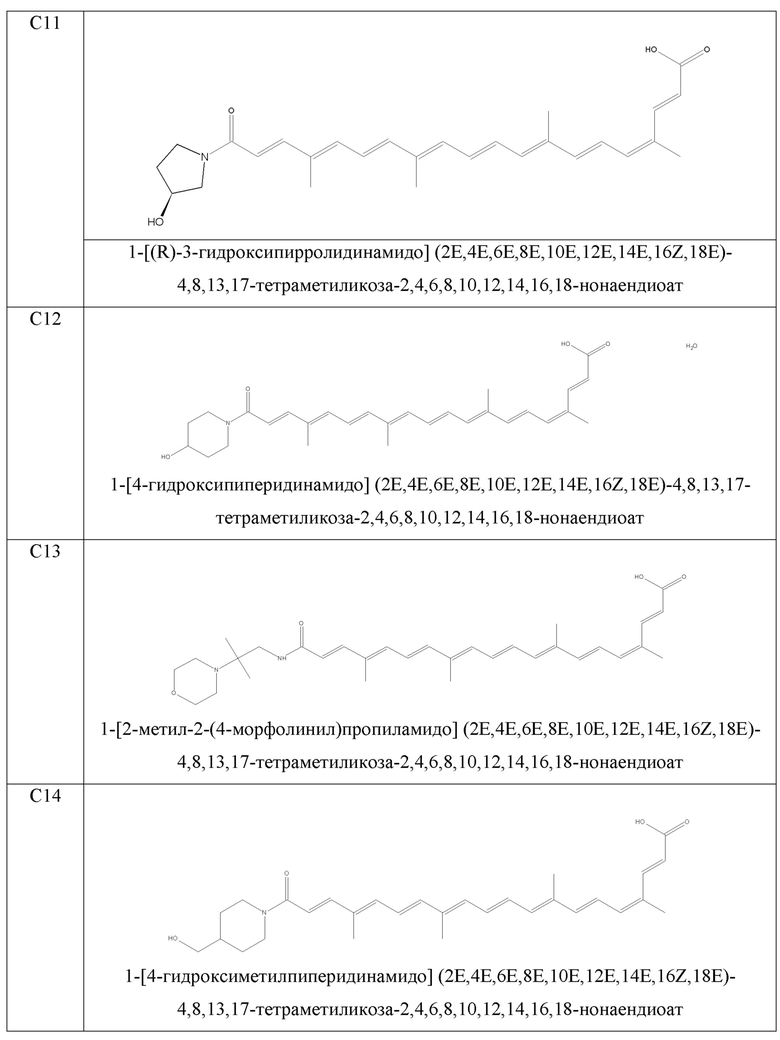
- 1-[2-метил-2-(4-морфолинил)пропиламидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
- 1-[4-гидроксиметилпиперидинамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
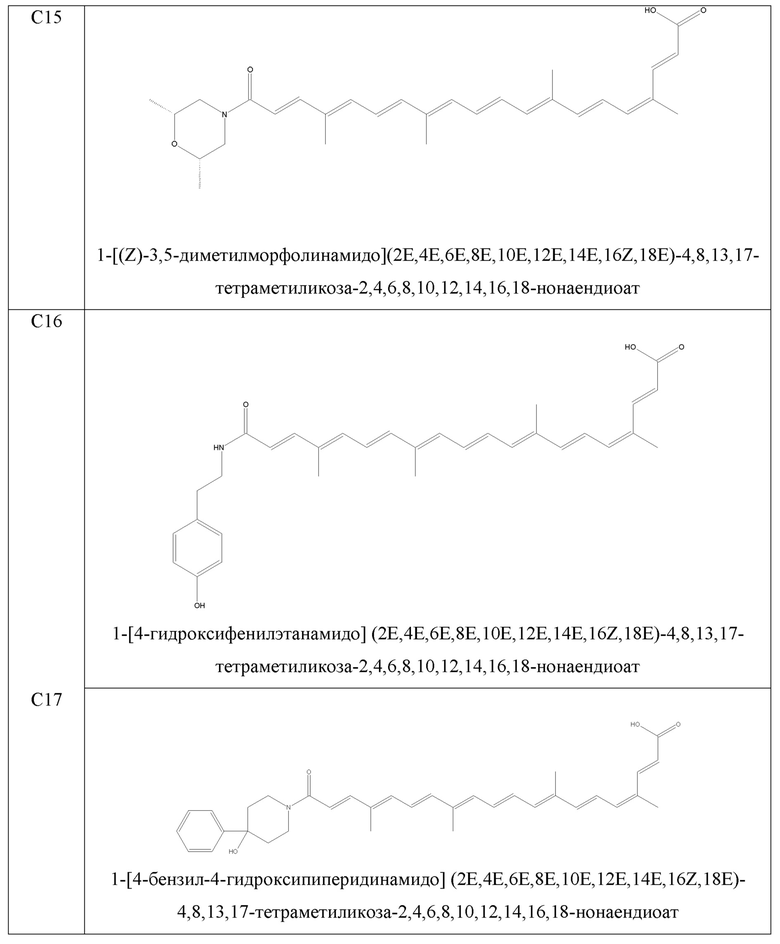
- 1-[(Z)-2,6-диметилморфолинамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
- 1-[4-гидроксифениламидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
- 1-[4-бензил-4-гидроксипиперидинамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
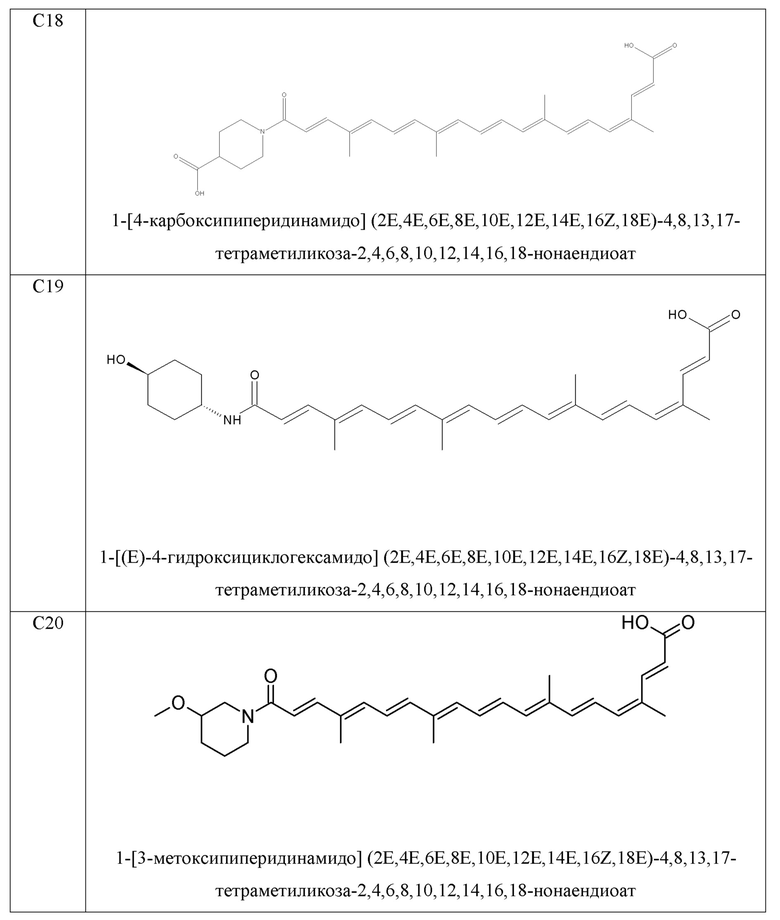
- 1-[4-карбоксипиперидинамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
- 1-[(E)-4-гидроксициклогексамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
- 1-[3-метоксипиперидинамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
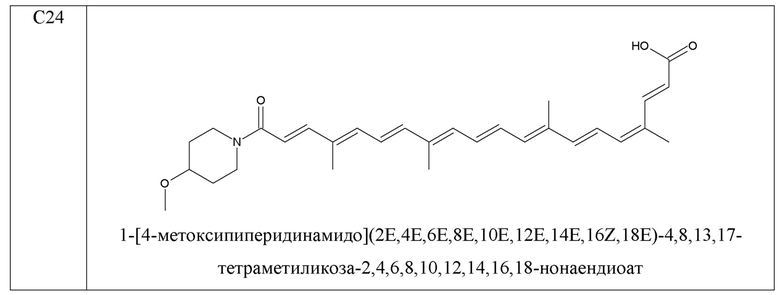
- 1-[4-метоксипиперидинамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
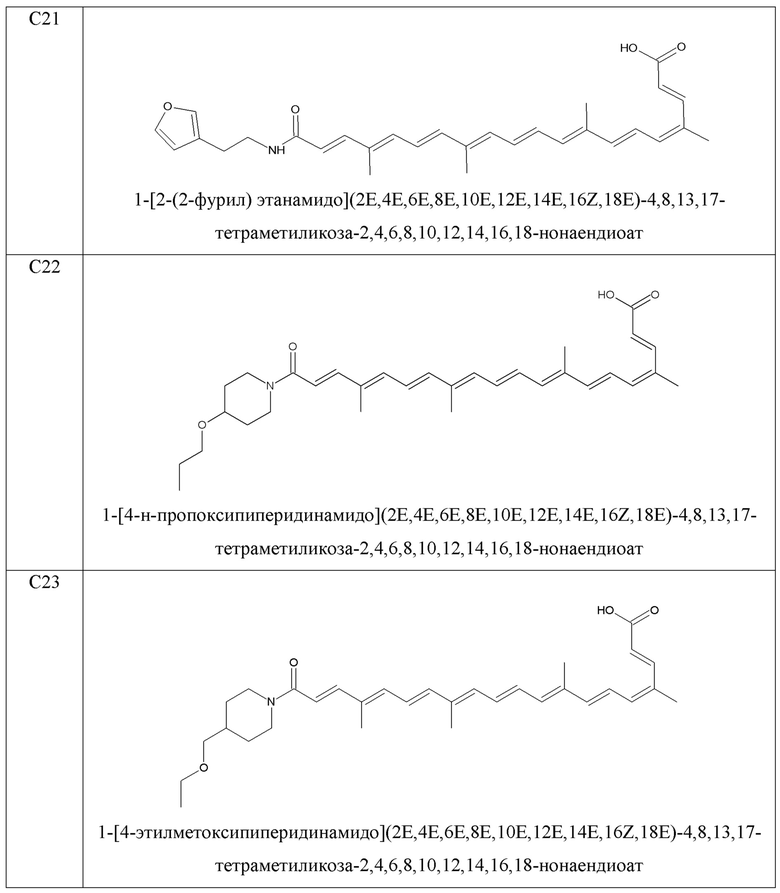
- 1-[2-(2-фурил)этанамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
- 1-[4-н-пропоксипиперидинамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
- 1-[4-этилметоксипиперидинамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат.
Согласно второму аспекту, настоящее изобретение относится к композиции, включающей по меньшей мере одно химическое соединение по настоящему изобретению.
Согласно отдельному воплощению настоящего изобретения композиция включает по меньшей мере один эксципиент. Примерами эксципиентов являются наполнители, разбавители, разрыхлители, лубриканты, консерванты дезинтеграторы, подсластители и т.д. Согласно определенному примеру, по меньшей мере один эксципиент выбирают из масла, воды и спирта, силикона.
Согласно отдельному воплощению настоящего изобретения композиция включает носитель в форме, приспособленной для приема внутрь, введения в глаз или введения в кровь.
Согласно третьему аспекту настоящее изобретение относится к химическому соединению, имеющему общую формулу (I), или к композиции, включающей по меньшей мере одно химическое соединение, имеющее общую формулу (I), для их применения в качестве лекарственного средства.
Согласно одному воплощению изобретение относится к химическому соединению, имеющему общую формулу (I), или к композиции, включающей по меньшей мере одно химическое соединение, имеющее общую формулу (I), для их применения для лечения и/или предупреждения повреждения сетчатки у млекопитающих, вызванному дегенерацией сетчатки.
Согласно одному воплощению изобретение относится к химическому соединению, имеющему общую формулу (I), или к композиции, включающей по меньшей мере одно химическое соединение, имеющее общую формулу (I), для их применения для для фотозащиты клеток пигментного эпителия сетчатки у млекопитающих.
Согласно одному воплощению изобретение относится к химическому соединению, имеющему общую формулу (I), или к композиции, включающей по меньшей мере одно химическое соединение, имеющее общую формулу (I), для их применения для предупреждения повреждения сетчатки у млекопитающих, вызванному воздействием синего цвета, соответствующего синей полосе спектра видимого света, с длиной волны, составляющей от 435 нм до 490 нм.
Согласно одному воплощению изобретение относится к химическому соединению, имеющему общую формулу (I), или к композиции, включающей по меньшей мере одно химическое соединение, имеющее общую формулу (I), для их применения при лечении и/или предупреждении глазных заболеваний у млекопитающих.
Согласно одному воплощению изобретение относится к химическому соединению, имеющему общую формулу (I), или к композиции, включающей по меньшей мере одно химическое соединение, имеющее общую формулу (I), для их применения при лечении и/или предупреждении ретинопатий у млекопитающих.
Согласно одному воплощению изобретение относится к химическому соединению, имеющему общую формулу (I), или к композиции, включающей по меньшей мере одно химическое соединение, имеющее общую формулу (I), для их применения при лечении и/или предупреждении возрастной макулярной дегенерации (AMD) у млекопитающих. Химическое соединение по настоящему изобретению преимущественно позволяет улучшить зрение индивидуумов, страдающих от такого заболевания, или по меньшей мере стабилизировать прогрессирование заболевания.
Согласно другому воплощению изобретение относится к химическому соединению, имеющему общую формулу (I), или к композиции, включающей по меньшей мере одно химическое соединение, имеющее общую формулу (I), для их применения при лечении и/или предупреждении болезни Штаргардта и пигментного ретинита у млекопитающих. Химическое соединение по настоящему изобретению преимущественно позволяет улучшить зрение индивидуумов, страдающих от таких заболеваний.
Краткое описание фигур
Изобретение будет лучше пониматься при чтении следующего далее описания, приведенного с примером, никоим образом не ограничивающего изобретение, и приведенного со ссылкой на фигуры, которые показывают описанное далее.
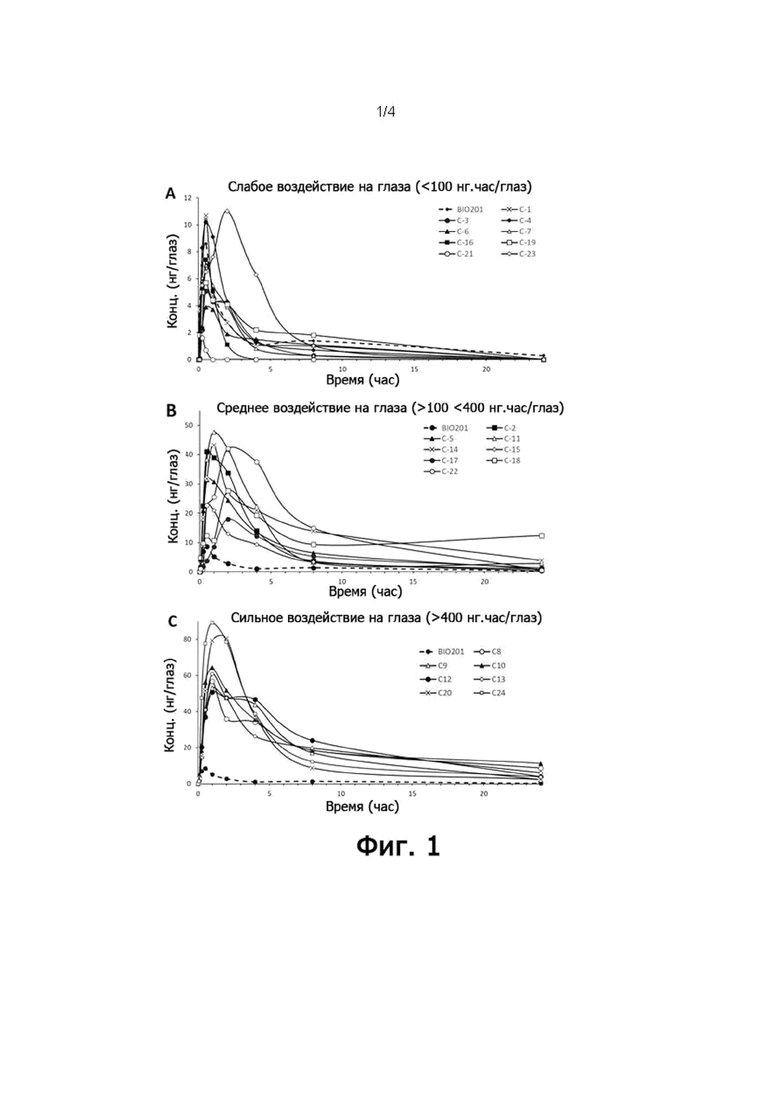
Фигура 1 показывает фармакокинетические профили соединений по настоящему изобретению в глазу. Это графики, показывающие концентрации в глазу как функцию времени после введения химических соединений (C) по настоящему изобретению и норбиксина (BIO201). Все соединения вводят перорально (п.о.) по 50 мг/кг в среде 20% сукцината D-α -токоферилполиэтиленгликоля 1000 (VitE-TPGS) в бикарбонатнатриевом буфере (0,1 М). Фармакокинетические профили соединений, имеющих слабое воздействие на глаза, показаны на фигуре 1 на графике А, соединения, имеющие среднее воздействие на глаза, показаны на фигуре 1 на графике В, и соединения, имеющие сильное воздействие на глаза, показаны на фигуре 1 на графике С.
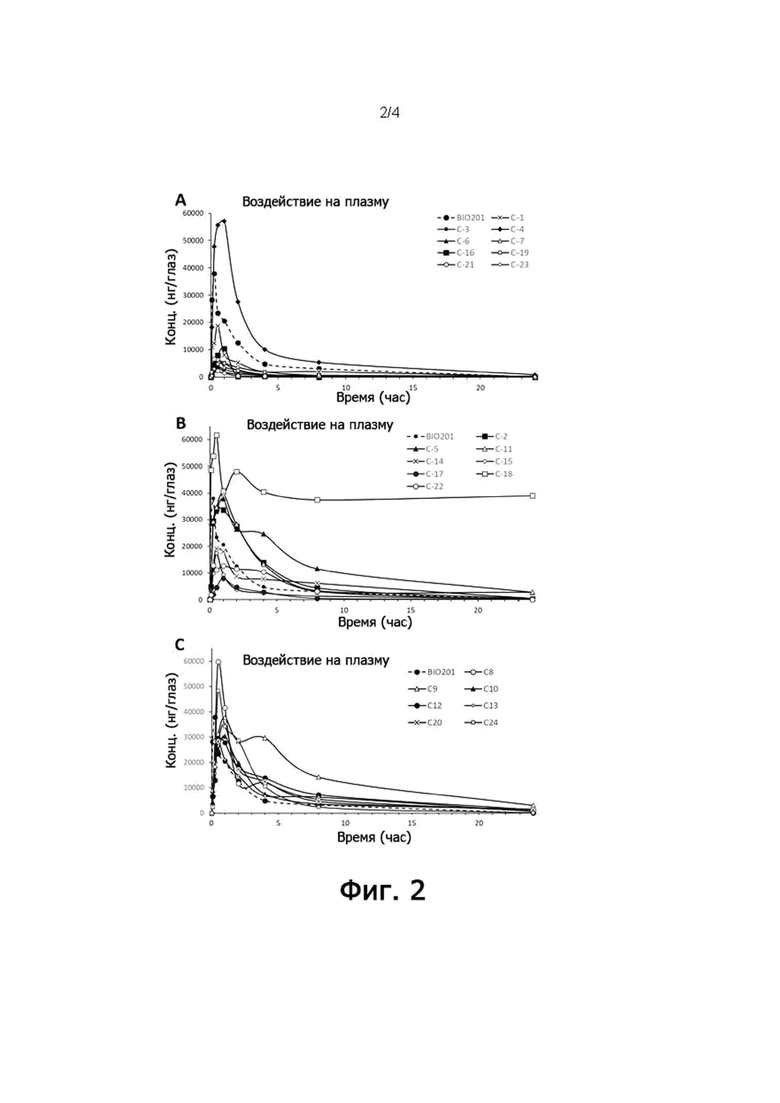
Фигура 2 показывает фармакокинетические профили соединений по настоящему изобретению в плазме. Это графики, показывающие концентрации в плазме как функцию времени после введения соединений (C) и норбиксина (BIO201). Все соединения вводят перорально (п.о.) по 50 мг/кг в среде 20% VitE-TPGS в бикарбонатнатриевом буфере (0,1 М). Фармакокинетические профили соединений, имеющих слабое воздействие на глаза, показаны на фигуре 2 на графике А, соединения, имеющие среднее воздействие на глаза, показаны на фигуре 2 на графике В, и соединения, имеющие сильное воздействие на глаза, показаны на фигуре 2 на графике С.
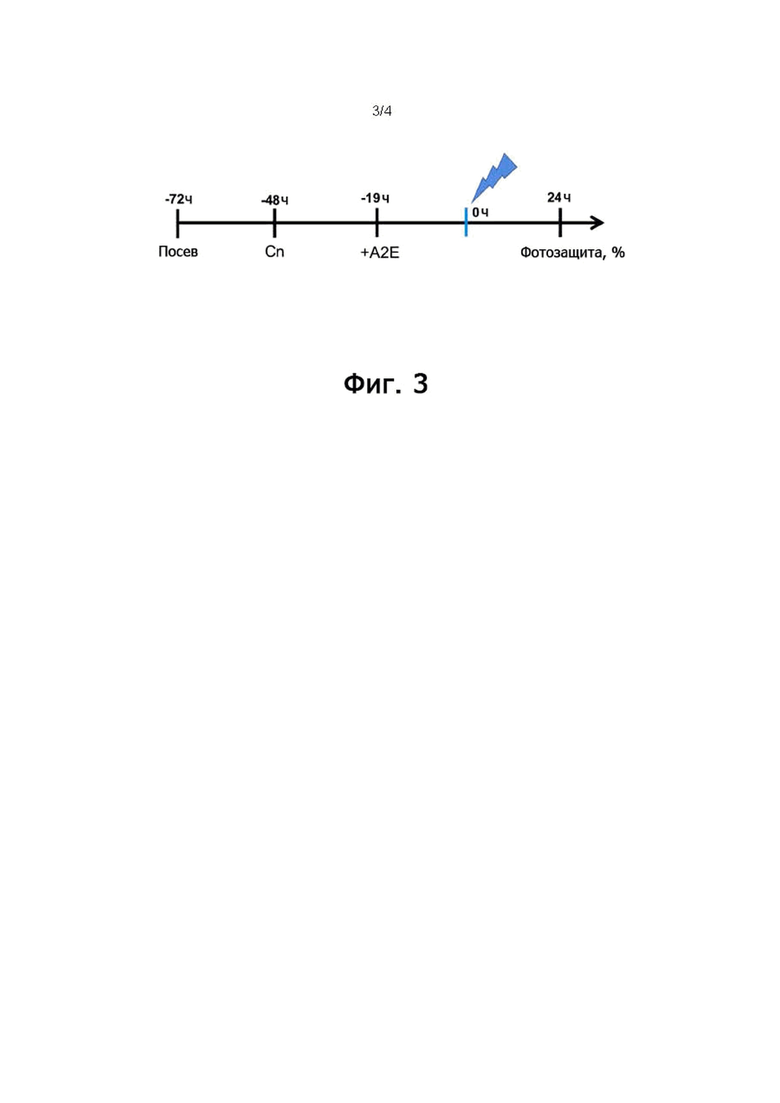
На фигуре 3 показана хронограмма экспериментов по фотозащите клеток пигментного эпителия сетчатки (RPE) соединениями (C) по настоящему изобретению in vitro. Это хронология этапов, выполненных для проверки фотозащитной активности различных химических соединений (C) по сравнению с активностью нативного норбиксина на клетках RPE, помещенных в условия присутствия A2E и подвергнутых освещению.
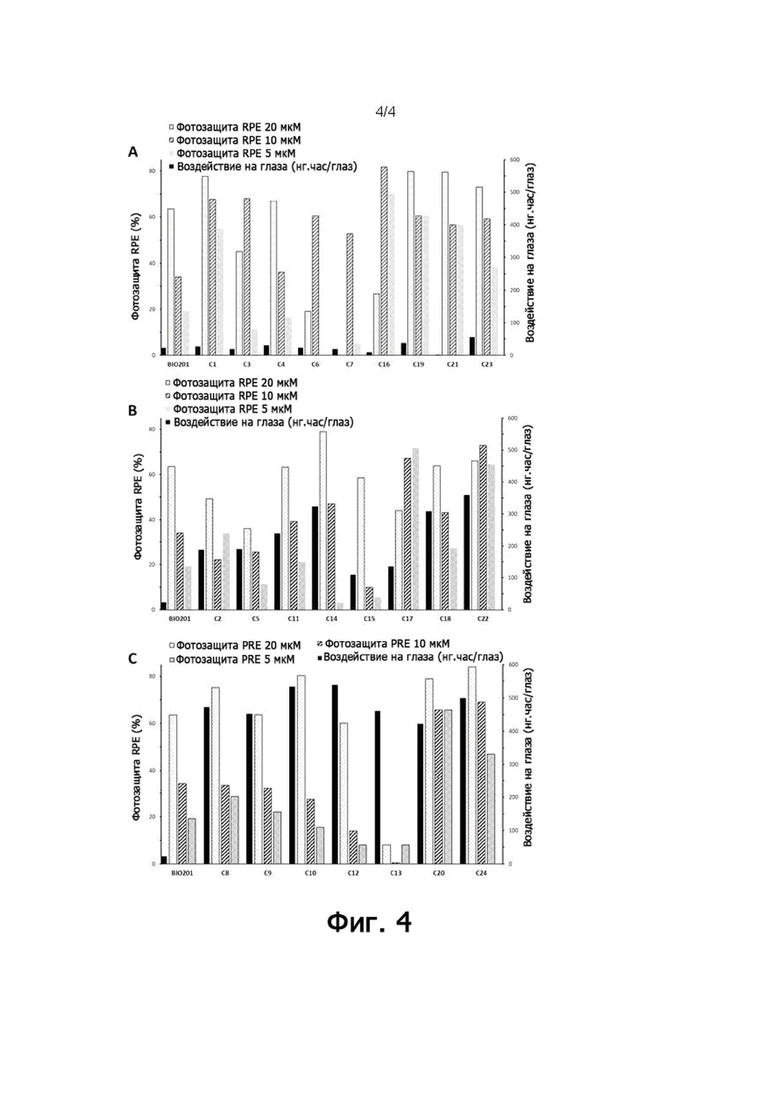
Фигура 4 показывает нацеливание на глаз и процент фотозащиты in vitro соединений по настоящему изобретению. Это гистограммы, показывающие в комбинации области под кривой концентраций в глазах (воздействия на глаза) норбиксина (BIO201) и различных соединений C по настоящему изобретению, и фотозащиту в процентах, полученную с помощью норбиксина и соединений по настоящему изобретению, при 5 мкМ, 10 мкМ и 20 мкМ. Соединения, имеющие слабое воздействие на глаза, показаны на гистограмме А, соединения, имеющие среднее воздействие на глаза, показаны на гистограмме В, и соединения, имеющие сильное воздействие на глаза, показаны на гистограмме С.
Описание воплощений
Химические соединения по настоящему изобретению не существуют в химических базах данных каротиноидов и ди-апо-каротиноидов. Они синтезированы в соответствии со способами, которые можно осуществить в промышленном масштабе, т.е., с минимумом стадий синтеза и оптимальным выходом. Они обладают лучшим фармакокинетическим профилем и лучшей тропностью к глазам, чем у норбиксина. Некоторые из таких соединений, кроме того, обладают фотозащитной активностью RPE, превосходящей таковую у норбиксина.
ОПИСАНИЕ СИНТЕЗА И ОБЩИХ СХЕМ
Химические соединения, имеющие общую формулу (I)
[Хим. ф-ла 1]
 ,
,
можно получить путем применения или адаптации любого способа, известного самого по себе специалисту в данной области техники и/или в пределах объема последнего, который смогли описать, или путем применения или адаптации способов, описанных в следующих далее процедурах.
В последующем описании различные группы имеют определения, приведенные в настоящем описании выше, т.е.
COR представляет собой вторичный или третичный амид, такой, что -R выбирают из
• -M; -NH-(CH2)n-M и -NH-(CH2)n-C(CH3)(CH3)-M, причем -M выбирают из
а)
[Хим. ф-ла 2]
 ,
,
b)
[Хим. ф-ла 3]
 ,
,
с)
[Хим. ф-ла 4]
 ,
,
в которых
- R1 выбирают из атома кислорода, атома серы, >CH2, >CH-O-(CH2)n-CH3, >CH-(CH2)n-O-(CH2)n-CH3, >CH-(CH2)n-OH, >CH-COOH, >C(OH)фенила или группы >NH;
- R3 выбирают из атома водорода, C1-C6-алкила, -OH или C1-C6-O-алкильной группы;
- R4 выбирают из атома водорода, C1-C6-алкила, -OH или C1-C6-O-алкильной группы;
- n равен целому числу от 0 до 6;
• -NH-(CH2)n-W, причем W представляет собой атом водорода или группу -OH, группу -O-(CH2)n-CH3 или группу, выбранную из
i)
[Хим. ф-ла 5]
 ,
,
ii)
[Хим. ф-ла 6]
 ,
,
iii)
[Хим. ф-ла 7]
 ,
,
iv)
[Хим. ф-ла 8]
 ,
,
v)
[Хим. ф-ла 9]
 ,
,
в которых
- R1 выбирают из атома кислорода, атома серы, >CH2, >CH-O-(CH2)n-CH3, >CH-(CH2)n-OH, >CH-COOH, >C(OH)фенила или группы >NH;
- R3 выбирают из атома водорода, C1-C6-алкила, -OH или C1-C6-O-алкильной группы;
- R4 выбирают из атома водорода, C1-C6-алкила, -OH или C1-C6-O-алкильной группы;
- R5 выбирают из -CH3, -OH, -O-(CH2)n-CH3, -(CH2)n-OH или группы -COOH;
- n равен целому числу от 0 до 6.
В рамках настоящего изобретения термин «C1-C6-алкильная группа» обозначает любую алкильную группу с 1-6 атомами углерода, линейную или разветвленную, в частности, метильную, этильную, n-пропильную, изопропильную, н-бутильную, изобутильную, втор-бутильную, трет-бутильную, н-пентильную, н-гексильную группы. Преимущественно это метильная, этильная, изопропильная или трет-бутильная группа, в частности метильная или этильная группа, конкретнее метильная группа.
Схема А для синтеза соединения 1-[2-(2-фурил)этанамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18- нонаендиоата (называемого соединением С21)
Образование амида (первый способ)
[Хим.ф-ла 10]
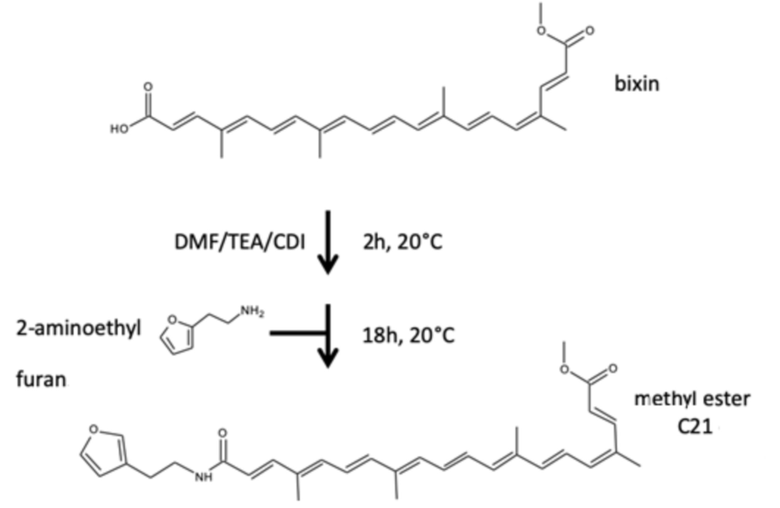
bixin - биксин, DMF - ДМФА, h - час, 2-aminoethyl - 2-аминоэтил, furan - фуран
methyl ester - метиловый эфир
Гидролиз метилового эфира
[Хим.ф-ла 11]
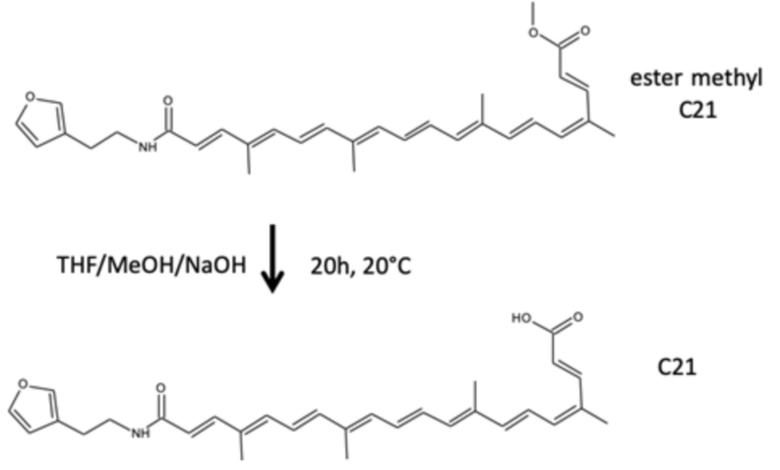
ester methyl- метиловый эфир, THF - ТГФ, h - час
Схема В для синтеза соединения 1-[(E)-4-гидроксициклогексамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18- нонаендиоата (называемого соединением С19)
Образование амида (второй способ)
[Хим.ф-ла 12]
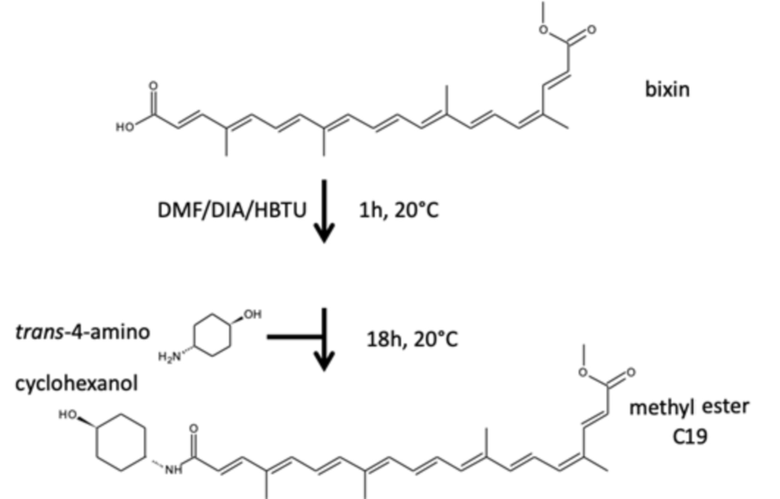
bixin - биксин, DMF - ДМФА, h - час, trans-4-amino - транс-4-амино
cyclohexanol - циклогексанол, methyl ester - метиловый эфир
ДМФА - диметилформамид
ТЕА = триэтиламин
DIA = диизопропиламин
ТГФ = тетрагидрофуран
CDI = карбонилдиимидазол
HBTU = гексафторфосфат (1Н-бензотриазол-1-илокси)(диметиламино)-N,N-диметилметаниминия
Примеры
Оборудование и методы
Спектры ядерного магнитного резонанса (ЯМР) протона (1H) получают на устройстве Bruker Avance DPX 500 (500, 0,7 МГц). Химические сдвиги (δ) измеряют в миллионных долях (м.д.). Спектры калибруют по химическому сдвигу используемого дейтерированного растворителя. Константы взаимодействия (J) выражают в герцах (Гц), и мультиплетность представляют следующим образом: синглет (с), дублет (д), дублет дублета (дд), триплет (т), триплет дублета (тд), квадруплет (к), мультиплет (м). Масс-спектры (МС) получают с помощью спектрометра MSD Agilent Technologies типа G1946A, образцы ионизируются источником «Химическая ионизация атмосферного давления» (APCI).
В качестве иллюстрации примеров изобретения синтезируют молекулы, показанные в таблице 1.
Пример 1 (схема А)
Получение соединения С21
Стадия 1 (типичный способ сочетания амина с карбонилдиимидазолом (CDI): получение метилового эфира С21
Химические реакции проводят в атмосфере аргона. Реагенты и продукты защищают от света алюминиевой фольгой на всех стадиях реакции и на стадии экстрагирования и удаления растворителей. Продукты хранят при 4°C. Биксин (1 г; 2,54 ммоль) растворяют в 10 мл сухого диметилформамида (ДМФА) и триэтиламина (1,06 мл; 7,61 ммоль), и затем добавляют CDI (0,823 г; 5,07 ммоль). Через два часа добавляют 2-аминоэтилфуран (845 мг; 7,61 ммоль), и реакционную смесь перемешивают в течение 18 час при 20°C. Добавляют хлороводородную кислоту (HCl, 1 N; 20 мл), и полученную суспензию центрифугируют. После удаления супернатанта осадок, содержащий метиловый эфир, дважды ресуспендируют в присутствии воды. После еще одного центрифугирования осадок (1,24 г) используют непосредственно на стадии гидролиза.
Стадия 2 (типичная процедура гидролиза): конверсия метилового эфира С21 в С21
Химические реакции проводят в атмосфере аргона и защищают от света алюминиевой фольгой. Продукты хранят при 4°C. Метиловый эфир С21 растворяют в 15 мл тетрагидрофурана (ТГФ) и 13 мл МеОН. Добавляют гидроксид натрия (NaOH, 1 N; 15,3 мл), и реакционную смесь перемешивают в течение 20 час при 20°C. Постепенно добавляют хлороводородную кислоту (HCl; 1 н.; 16 мл). Полученную суспензию центрифугируют, и удаляют супернатант. Затем осадок ресуспендируют и дважды смешивают с водой, затем снова центрифугируют и удаляют супернатант. Полученную пасту, содержащую воду, переносят в грушевидную колбу в присутствии воды и ацетонитрила, лиофилизируют, и получают 1,04 г порошка цвета от оранжевого до красного.
Анализ соединения C21
ЖХ-МС: m/z = 474,3 (MH+), УФ-чистота при 460 нм = 99%.
ЯМР 1H (500 МГц, ДМСО-d6) - δ 8,11 (т, 1H), 7,54 (с, 1H), 6,19 (д, 1H), 3,42-3,38 (м, 2H), 2,78 (т, 2H).
Получение соединения C19
Стадия 1 (типичная процедура для сочетания амина с использованием HBTU): получение метилового эфира С19 (способ используют только для получения метилового эфира С19, так как реакция с использованием CDI является слишком медленной для этого соединения)
Химические реакции проводят в атмосфере аргона. Реагенты и продукты защищают от света алюминиевой фольгой на всех стадиях реакции и на стадии экстрагирования и удаления растворителей. Все продукты хранят при 4°C. Биксин (1,17 г; 2,97 ммоль) растворяют в 20 мл безводного ДМФА и диизопропиламина (1,23 мл; 7,42 ммоль); затем добавляют HBTU ((1Н-бензотриазол-1-илокси)диметиламиногексафторфосфат) N,N’-диметилметаниминия; 1,69 г; 4,45 ммоль). Через 1 час добавляют транс-4-аминоциклогексанол (680 мг; 4,45 ммоль), и реакционную смесь перемешивают в течение 18 час при 20°C. Добавляют шестьдесят миллилитров воды (60 мл), осадок отфильтровывают и дважды промывают 60 мл воды, и получают 1,4 г фиолетового твердого соединения, которое используют как оно есть на стадии гидролиза.
Стадия 2 (типичная процедура гидролиза): конверсия метилового эфира С19 в С19
Химические реакции проводят в атмосфере аргона и защищают от света алюминиевой фольгой. Продукты хранят при 4°C. Растворяют 1,4 г метилового эфира С19 в 10 мл тетрагидрофурана (ТГФ) и 10 мл МеОН (темно-красный раствор). Добавляют пять эквивалентов гидроксида натрия (NaOH, 10 N; 1,43 мл), и реакционную смесь перемешивают в течение 48 час при температуре окружающей среды. При ВЭЖХ-МС наблюдают один пик и отсутствие исходного материала. Добавляют хлороводородную кислоту (HCl; 12N; 1,18 мл). Полученный осадок разбавляют 60 мл воды. Раствор центрифугируют, и удаляют водный супернатант. Затем берут твердый осадок и смешивают с водой (30 мл), затем снова центрифугируют, и удаляют супернатант. Эту стадию повторяют дважды до получения твердой пасты оранжевого цвета (которая образует суспензию в присутствии воды). Твердую пасту разводят в 50 мл воды, получают оранжевую суспензию, замораживают и непосредственно лиофилизируют, и получают оранжевый порошок (1,02 г).
Анализ соединения C19
ЖХ-МС: m/z = 478,2 (MH+), УФ-чистота при 460 нм = 97,3%.
ЯМР 1H (500 МГц, ДМСО-d6) - δ 47,82 (с, 1H), 4,51 (м, 1H), 3,58-3,53 (м, 1H), 3,40-3,36 (м, 1Н), 1,83-1,75 (м, 4Н), 1,26-1,15 (м, 4H).
КАСКАДНЫЙ СКРИНИНГ И ХАРАКТЕРИСТИКА БИОЛОГИЧЕСКИХ ЭФФЕКТОВ ХИМИЧЕСКИХ СОЕДИНЕНИЙ (С), ПОЛУЧЕННЫХ ИЗ НОРБИКСИНА
Разработка скринингового теста инициируется из работ, описанных в литературе, и основывается на характеристиках патологии сухой AMD. На физиопатологическом уровне такое заболевание характеризуется прогрессирующей потерей зрения, вызываемой после дегенерации фоторецепторов и клеток RPE. Клетки RPE играют решающую роль в выживании и правильной работе фоторецепторов, обеспечивая их необходимыми питательными веществами, участвуя в визуальном цикле и удаляя остатки, поступающие из внешних сегментов фоторецепторов и являющиеся результатом этого цикла. Важно скринировать разрабатываемые лекарственные средства на их способность воздействовать предпочтительно на глаз, избегая при этом внутриглазного введения, которое травмирует пациентов и несет риски местных инфекций. Для этого проводят фармакокинетическое исследование химических соединений (С), полученных из норбиксина - предмета настоящего изобретения, на уровне плазмы и глаз, чтобы выбрать химические соединения, имеющие AUC для глаз («площадь под кривой»), которая улучшена по отношению к норбиксину.
Кроме лучшего распределения в ткани-мишени, выбор новых соединений также должен основываться на хорошей фотозащитной активности, которая ограничивает потерю клеток RPE и таким образом уменьшает дегенерацию сетчатки, наблюдаемую при AMD и других дегенеративных заболеваниях, таких как пигментный ретинит и болезнь Штаргардта. На клеточном уровне, на культурах клеток RPE, происходящих из сетчатки свиньи, Fontaine et al. ((2016) показали, что обработка норбиксином (BIO 201) защищает клетки RPE от апоптоза после облучения в присутствии A2E (выживаемость 80% через 24 часа после облучения). Такой же скрининговый тест по проценту фотозащиты используют для определения его модуляции химическими соединениями, полученными по настоящему изобретению из норбиксина (С), в сравнении с фотозащитным эффектом норбиксина, и характеризации таких модуляций со статической точки зрения.
Протоколы
Фармакокинетическое исследование с помощью перорального введения молекул мышам
Фармакокинетическое исследование химических соединений (С) после их перорального введения проводят с использованием мышей C57BL/6 (январь, 53940, The Genest Saint Isle, Франция). Химические соединения, полученные из норбиксина (С), вводят в дозе 50 мг/кг массы тела. После введения берут образцы крови из хвостовой вены при t = 0,25 час; 0,5 час; 1 час; 3 час; 6 час и 8 час. Образцы крови центрифугируют и берут плазму. Дозировка образцов плазмы позволяет определить фармакокинетические параметры, а именно Cmax, которая соответствует максимальной концентрации, наблюдаемой после введения молекулы, Tmax, которое представляет собой время, необходимое для достижения максимальной концентрации после введения молекулы, и AUC: площади под кривой, которая соответствует воздействию на плазму (фигура 2).
Параллельно следующим образом дозируют глазные концентрации химических соединений, полученных из норбиксина (C) (фигура 1): оба глаза каждой мыши помещают в пробирки Precellys и хранят при -80°C до момента дозирования. Затем глаза измельчают в пробирках Precellys с помощью настольного гомогенизатора Fast-prep (Fischer Scientific, Hampton, United States) в смеси органических растворителей, на первой стадии с 500 мкл смеси хлороформ/метанол (1/1, об./об.), затем 500 мкл смеси хлороформ/дихлорметан (1/1, об./об.). На каждой стадии извлекают супернатанты и переносят в 2-мл 96-луночный планшет.
Для количественного определения химических соединений C получают калибровочную кривую с использованием 8 стандартов (от 5 до 5000 нг/мл) в тех же смесях органических растворителей и переносят (100 мкл) в 2-мл 96-луночный планшет.
Супернатанты и стандарты упаривают в EZ2 (Genevac, Ipswich, United Kingdom) без нагревания, и затем растворяют в 100 мкл смеси ДМСО/метанол (20:80, об./об.) перед переносом в 200-мкл 96-луночный планшет.
Анализ ЖХ-МС МС выполняют с помощью ВЭЖХ 1200 Infinity chain (Agilent Technologies, Santa-Clara, United States), УФ-детектора и масс-спектрометра QQQ6420 (Agilent Technologies, Santa-Clara, United States). Объем впрыска составляет 5 мкл. Химические соединения C элюируют на колонке с обратной фазой с C18 (2,1*50 мм, частицы 3 мкм; Ace-C18-Excel, AIT) с градиентом ацетонитрила и воды (содержащей 0,1% муравьиной кислоты) и скоростью потока 0,3 мл/мин. Условия градиента могут изменяться в зависимости от анализируемого химического соединения С. УФ-детектор анализирует при 460 нм, и масс-спектрометр анализирует в режиме MRM - Positive.
Фотозащита клеток RPE
Испытания in vitro фотозащиты различными химическими соединениями C клеток RPE, освещенных в присутствии A2E
Тест in vitro, описанный выше и предназначенный для изучения фотозащитного действия норбиксина, используют для количественной оценки фотозащитного действия различных химических соединений, полученных из норбиксина (C), на клетки RPE, освещенные синим светом в присутствии A2E (фигура 3). Фотозащитное действие молекул оценивают на клеточной модели фототоксичности, индуцированной обработкой A2E с последующим освещением синим светом. Термин «синее излучение» обозначает излучение, соответствующее синей полосе спектра видимого света, т.е. с длиной волны, составляющей от 435 до 490 нм. В этой модели используются первичные культуры RPE взрослых свиней. Выживаемость клеток определяют количественно благодаря тесту на жизнеспособность клеток. Через 48 час добавляют испытываемые соединения (в 5 мМ растворе в ДМСО) для получения конечных концентраций от 1 до 20 мкМ), затем через 19 час A2E (конечная концентрация 30 мкМ), и клетки (время 0 ч) освещают. Через 24 час измеряют выживаемость клеток. Получение изображений, а также их обработку осуществляют с использованием флуоресцентного микроскопа, управляемого программным обеспечением Metamorph и специальной программой количественной оценки. Эксперименты проводят на 96-луночном микропланшете при четырехкратном повторе, и эксперимент воспроизводят по меньшей мере четыре раза. Результаты выражают в виде отношения, представляющего количество живых клеток в лунках, обработанных испытываемыми молекулами, деленное на число живых клеток в контрольных лунках (обработанных разбавляющей средой без A2E). Этот тест позволяет, как описано выше, выявить фотозащитную активность норбиксина (Fontaine et al., 2016).
Результаты
Фармакокинетическое исследование химических соединений С на мышах
В таблице 2 представлены результаты по фармакокинетике химических соединений C после введения п.о. 50 мг/кг в сукцинате D-α-токоферилполиэтиленгликоля 1000 (VitE-TPGS), 20%, в бикарбонатнатриевом буфере (0,1 М).
Таблица 2
(мкг,час/мл)
В таблице 3 приводится в процентах фотозащита клеток RPE химическими соединениями C in vitro: показан процент клеток RPE, выживающих в присутствии N-ретинил-N-ретинилиденэтаноламина (A2E) и различных химических соединений C, полученных из норбиксина (испытания при 5, 10 или 20 мкМ), или норбиксина в тех же концентрациях после облучения.
Таблица 3
БИБЛИОГРАФИЯ
AREDS Report No. 8. 2001. A randomized, placebo-controlled, clinical trial of high-dose supplementation with vitamins C and E, beta carotene, and zinc for age-related macular degeneration and vision loss. Arch Ophthalmol, 119: 1417-1436.
Bhosale P, Serban B, Bernstein PS. 2009. Retinal carotenoids can attenuate formation of A2E in the retinal pigment epithelium. Arch Biochem Biophys, 483: 175-181.
Elliott JG, Williams NS. 2012. Nutrients in the battle against age-related eye diseases. American Optometric Association. doi:10.1016/j.optm.2011. 11.006
Fontaine V, Lafont R, Sahel JA, Veillet S. 2011. Utilisation de composés et composition pour le traitement de la dégénérescence maculaire liée à l’âge (DMLA). Application FR 25506 (filed on 14 May 2011).
Fontaine V, Monteiro E, Brazhnikova E, Lesage L, Balducci C, Guibout L, Feraille L, Elena PP, Sahel JA, Veillet S, Lafont R. 2016. Norbixin protects retinal pigmented epithelium and photoreceptors against A2E-mediated phototoxicity in vitro and in vivo. PLoS ONE (2016): DOI:10.1371/journal.pone.0167793.
Laabich A, Vissvesvaran GP, Lieu KL, Murata K, McGinn TE, Manmoto CC, Sinclair JR, Karliga I, Leung DW, Fawzi A, Kubota R. 2006. Protective effect of crocin against blue light- and white light-mediated photoreceptor cell death in bovine and primate retinal primary cell culture. Invest Ophthalmol Vis Sci, 47: 3156-3163.
Lafont R, Veillet S, Sahel JA, Fontaine V, Elena PP. 2015. Composition pour la protection des cellules de l’épithélium pigmentaire rétinien. Application FR 30891 (filed on 30/04/2015).
Parisi V, Tedeschi M, Gallinaro G, Varano M, Saviano S, Piermarocchi S. 2008. Carotenoids and antioxidants in age-related maculopathy Italian study: multifocal electroretinogram modifications after 1 year. Ophthalmology, 115(2): 324-333.
Pinazo-Durán MD, Gómez-Ulla F, Arias L, Araiz J, Casaroli-Marano R, Gallego-Pinazo R, García-Medina JJ, López-Gálvez MA, Manzanaq L, Salas A, Zapara M, Diaz-Llopis M, García-Layana A. 2014. Do nutritional supplements have a role in age macular degeneration prevention? J Ophthalmology, article ID 901686.
Smith W, Assink J, Klein R, Mitchell P, Klaver CCW, Klein BEK, Hofman A, Jensen S, Wang JJ, de Jong PTVM. 2001. Risk factors for age-related macular degeneration. Pooled findings from three continents. Ophthalmology 108: 697-704.
Sparrow JR, Cai B. 2001. Blue light-induced apoptosis of A2E-containing RPE: involvement of caspase-3 and protection by Bcl-2. Invest Ophthalmol Vis Sci, 42: 1356-1362.
Subczynski WK, Wisniewska A, Widomska J. 2010. Location of macular pigments in the most vulnerable regions of photoreceptor outer-segment membranes. Arch Biochem Biophys, 504: 61-66.
Tsuruma K, Shimazaki H, Nakashima K, Yamauchi M, Sugitani S, Shimazawa M, Iinuma M, Hara H. 2012. Annatto prevents retinal degeneration induced by endoplasmic reticulum stress in vitro and in vivo. Mol Nutr Food Res, 56: 713-724.
Veillet S, Lafont R, Dioh W. 2009. Cosmetic composition for protection from the sun containing urucum extract. Priority Application FR2009-54354 A (25 juin 2009), Application no FR 2009-54354, WO 2010-FR51323.
Yamauchi M, Tsuruma K, Imai S, Nakanishi T, Umigai N, Shimazawa M, Hara H. 2011. Crocetin prevents retinal degeneration induced by oxidative stress and endoplasmic reticulum stress via inhibition of caspase activity. Mol Cell Pharmacol, 650: 110-119.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ ХИНОЛИНА ДЛЯ ПРИМЕНЕНИЯ ПРИ ЛЕЧЕНИИ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ | 2019 |
|
RU2827865C2 |
| ДОНЕКОПРИД КАК НЕЙРОПРОТЕКТОРНЫЙ АГЕНТ ПРИ ЛЕЧЕНИИ НЕЙРОДЕГЕНЕРАТИВНЫХ ЗАБОЛЕВАНИЙ | 2019 |
|
RU2800802C2 |
| ПРОИЗВОДНЫЕ ХИНОЛИНА ДЛЯ ПРИМЕНЕНИЯ В ЛЕЧЕНИИ ИЛИ ПРЕДУПРЕЖДЕНИИ РАКА | 2019 |
|
RU2811417C2 |
| КОНЪЮГИРОВАННЫЕ ЛИПИДНЫЕ ПРОИЗВОДНЫЕ | 2007 |
|
RU2480447C2 |
| АНТИТЕЛА, ОБЛАДАЮЩИЕ СПЕЦИФИЧНОСТЬЮ К BTN2, И ИХ ПРИМЕНЕНИЕ | 2018 |
|
RU2794996C2 |
| ФЕНИЛ/ПИРИДИЛ-N-ФЕНИЛ/ПИРИДИЛЬНЫЕ ПРОИЗВОДНЫЕ ДЛЯ ЛЕЧЕНИЯ РНК-ВИРУСНОЙ ИНФЕКЦИИ | 2019 |
|
RU2790838C2 |
| ПРИМЕНЕНИЕ ЦИКЛИЧЕСКОГО ТРИПЕПТИДА ДЛЯ УЛУЧШЕНИЯ КЛЕТОЧНОГО ЭНЕРГЕТИЧЕСКОГО МЕТАБОЛИЗМА | 2016 |
|
RU2737116C2 |
| ПРОТИВОВИРУСНЫЕ КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ ИНФЕКЦИЙ, СВЯЗАННЫХ С КОРОНАВИРУСАМИ | 2017 |
|
RU2753534C2 |
| КОМПОЗИЦИЯ ВИНИЛИДЕНХЛОРИДНОГО ПОЛИМЕРА, СОДЕРЖАЩАЯ ПО МЕНЬШЕЙ МЕРЕ ОДИН СОРБАТНЫЙ СЛОЖНЫЙ ЭФИР | 2016 |
|
RU2736260C2 |
| АНТИТЕЛА, СПЕЦИФИЧНЫЕ К BTN2, И ИХ ПРИМЕНЕНИЕ | 2020 |
|
RU2821703C2 |
Изобретение относится к химическим соединениям общей формулы (I), где COR представляет собой вторичный или третичный амид, так что -R выбирают из: -M; -NH-(CH2)n-M и -NH-(CH2)n-C(CH3)(CH3)-M, где -M выбирают из (а), (b), (с), в которых R1 выбирают из атома кислорода, атома серы, >CH2, >CH-O-(CH2)n-CH3, >CH-(CH2)n-O-(CH2)n-CH3, >CH-(CH2)n-OH, >CH-COOH или >C(OH)фенила; R3 выбирают из атома водорода, C1-C6-алкила или C1-C6-O-алкильной группы; R4 выбирают из атома водорода, C1-C6-алкила или C1-C6-O-алкильной группы; n равен целому числу от 0 до 3; -NH-(CH2)n-W, где W представляет собой группу -OH, группу -O-(CH2)n-CH3 или группу, выбранную из ii), iv), v), в которых R1 выбирают из >CH-(CH2)n-OH; R3 представляет собой атом водорода; R4 представляет собой атом водорода; R5 представляет собой -OH; n равен целому числу от 0 до 2. Также изобретение относится к композиции на основе соединения формулы (I) для защиты клеток пигментного эпителия сетчатки. Технический результат - получение соединений, применяемых для защиты клеток пигментного эпителия сетчатки (RPE). 2 н. и 10 з.п. ф-лы, 3 табл., 4 ил., 1 пр.
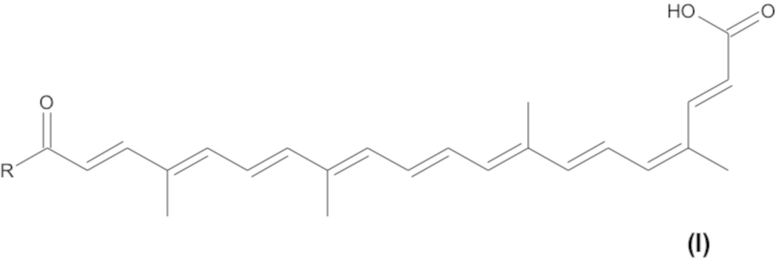
1. Химическое соединение, имеющее следующую общую формулу (I)
[Хим. ф-ла 1]
 ,
,
где COR представляет собой вторичный или третичный амид, так что -R выбирают из:
• -M; -NH-(CH2)n-M и -NH-(CH2)n-C(CH3)(CH3)-M, где -M выбирают из
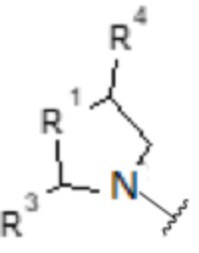
а) [Хим. ф-ла 2]
 ,
,
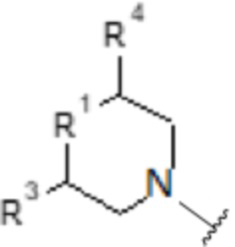
b) [Хим. ф-ла 3]
 ,
,
с) [Хим. ф-ла 4]
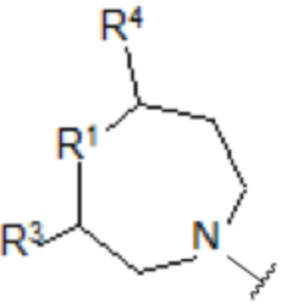 ,
,
в которых
- R1 выбирают из атома кислорода, атома серы, >CH2, >CH-O-(CH2)n-CH3, >CH-(CH2)n-O-(CH2)n-CH3, >CH-(CH2)n-OH, >CH-COOH или >C(OH)фенила;
- R3 выбирают из атома водорода, C1-C6-алкила или C1-C6-O-алкильной группы;
- R4 выбирают из атома водорода, C1-C6-алкила или C1-C6-O-алкильной группы;
- n равен целому числу от 0 до 3;
• -NH-(CH2)n-W, где W представляет собой группу -OH, группу -O-(CH2)n-CH3 или группу, выбранную из
ii) [Хим. ф-ла 6]
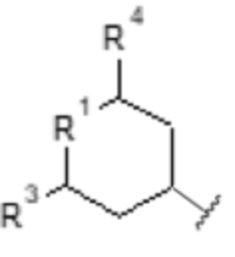 ,
,
iv) [Хим. ф-ла 8]
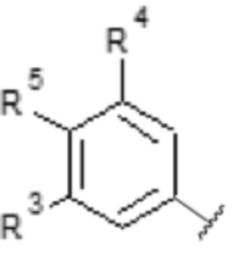 ,
,
v) [Хим. ф-ла 9]
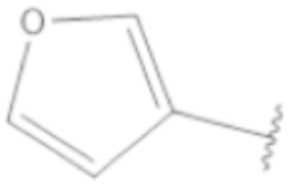 ,
,
в которых
- R1 выбирают из >CH-(CH2)n-OH;
- R3 представляет собой атом водорода;
- R4 представляет собой атом водорода;
- R5 представляет собой -OH;
- n равен целому числу от 0 до 2;
а также фармацевтически приемлемые соли указанного химического соединения.
2. Химическое соединение, имеющее общую формулу (I), по п.1, выбранное из химических соединений, включая следующие:
- 1-[2-метоксиэтанамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
- 1-[1,4-оксазинамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
- 1-[пиперидинамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметилкоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
- 1-[2-гидроксиэтанамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
- 1[1,4-оксазепанамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметилкоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
- 1-тиоморфолинамидо-(2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
- 1-пирролидинамидо-(2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметилкоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
- 1-[2-морфолинопропанамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
- 1-[(S)-3-гидроксипирролидинамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
- 1-[2-морфолиноэтанамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметилкоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
- 1-[(R)-3-гидроксипирролидинамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
- 1-[4-гидроксипиперидинамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
- 1-[2-метил-2-(4-морфолинил)пропиламидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
- 1-[4-гидроксиметилпиперидинамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
- 1-[(Z)-2,6-диметилморфолинамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
- 1-[4-гидроксифенилэтанамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
- 1-[4-бензил-4-гидроксипиперидинамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
- 1-[4-карбоксипиперидинамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
- 1-[(E)-4-гидроксициклогексамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
- 1-[3-метоксипиперидинамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
- 1-[4-метоксипиперидинамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
- 1-[2-(2-фурил)этанамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
- 1-[4-н-пропоксипиперидинамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат;
- 1-[4-этилметоксипиперидинамидо](2E,4E,6E,8E,10E,12E,14E,16Z,18E)-4,8,13,17-тетраметиликоза-2,4,6,8,10,12,14,16,18-нонаендиоат.
3. Композиция для защиты клеток пигментного эпителия сетчатки, включающая по меньшей мере одно химическое соединение по любому из пп. 1 или 2 в качестве активного ингредиента и по меньшей мере один эксципиент.
4. Композиция по п. 3, включающая носитель в форме, приспособленной для приема внутрь, введения в глаз или введения в кровь.
5. Химическое соединение, имеющее общую формулу (I), по любому из пп. 1, 2 или композиция по любому из пп. 3 или 4 для их применения в качестве лекарственного средства для защиты клеток пигментного эпителия сетчатки.
6. Химическое соединение, имеющее общую формулу (I), по любому из пп. 1, 2 или композиция по любому из пп. 3 или 4 для их применения для фотозащиты клеток пигментного эпителия сетчатки у млекопитающих.
7. Химическое соединение, имеющее общую формулу (I), по любому из пп. 1, 2 или композиция по любому из пп. 3 или 4 для их применения для лечения и/или предупреждения повреждения сетчатки у млекопитающих, вызванного воздействием синего цвета, соответствующего синей полосе спектра видимого света с длиной волны, составляющей от 435 до 490 нм.
8. Химическое соединение, имеющее общую формулу (I), по любому из пп. 1, 2 или композиция по любому из пп. 3 или 4 для их применения для лечения и/или предупреждения повреждения сетчатки у млекопитающих, вызванного дегенерацией сетчатки.
9. Химическое соединение, имеющее общую формулу (I), по любому из пп. 1, 2 или композиция по любому из пп. 3 или 4 для их применения при лечении и/или предупреждении глазных заболеваний у млекопитающих.
10. Химическое соединение, имеющее общую формулу (I), по любому из пп. 1, 2 или композиция по любому из пп. 3 или 4 для их применения при лечении и/или предупреждении ретинопатий у млекопитающих.
11. Химическое соединение, имеющее общую формулу (I), по любому из пп. 1, 2 или композиция по любому из пп. 3 или 4 для их применения при лечении и/или предупреждении возрастной макулярной дегенерации (AMD) у млекопитающих.
12. Химическое соединение, имеющее общую формулу (I), по любому из пп. 1, 2 или композиция по любому из пп. 3 или 4 для их применения при лечении и/или предупреждении болезни Штаргардта и пигментного ретинита у млекопитающих.
| FUHRHOP, J.-H | |||
| et al | |||
| Bolaform Amphiphiles with a Rigid Hydrophobic Bixin Core in Surface Monolayers and Lipid Membranes | |||
| Langmuir, 1990, 6(2), p.497-505 | |||
| KOMATSU, T | |||
| et al | |||
| Solid Vesicle Membrane Made of meso-Tetrakis[(bixinylamino)-o-phenyl]porphyrins | |||
| Journal of the American Chemical Society, 1997, 119(48), p.11660-11665 | |||
| FONTAINE, V | |||
| et al |
Авторы
Даты
2024-11-25—Публикация
2020-12-22—Подача