2420-534633RU/042
ЗАЯВЛЕННЫЙ ПРИОРИТЕТ
Настоящая заявка заявляет приоритет по предварительной патентной заявке США регистрационный No. 61/906738, поданной 20 ноября 2013. Вышеуказанная заявка включена в настоящее описание посредством, что эквивалентно ее полному содержанию. Все ссылки, цитированные в настоящем описании, включая, без ограничения, патенты и патентные заявки, включены посредством ссылки полностью.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Кахексия, связанная с раком, представляет собой ослабленное состояние, ассоциированное с потерей мышечной массы, утомляемостью, слабостью и потерей аппетита. Кахексия также ассоциирована с тяжелыми клиническими последствиями, включая мышечную слабость, которая может приводить к затруднению способности к передвижению и легочным осложнениям. Кахексия является существенно важным фактором, способствующим смерти пациентов с раком.
Кахексия характеризуется потерей скелетной мышечной массы, которая не поддается обратному развитию при обычной питательной поддержке, приводя к выраженной потере массы тела, которая существенно влияет на заболеваемость и смертность пациентов. Она развивается более чем у 80% пациентов с раком желудка, поджелудочной железы и пищевода; 70% таковых с раком головы и шеи; и приблизительно 60% пациентов с раком легкого, колоректальным раком и раком предстательной железы. См., например, Muscle (2012) 3, 245-51. Несмотря на влияние кахексии на смертность среди пациентов с раком, не было разработано эффективной терапии для предотвращения или сдерживания прогрессирования кахексии. Например, оценивают, что более чем 85% пациентов с раком поджелудочной железы, включая пациентов с ранними стадиями, теряют в среднем 14% своей массы тела до болезни. См., например, BMC Cancer. 2010 Jul 8; 10:363. Кахектичные пациенты с раком поджелудочной железы часто являются слабыми и усталыми, и имеют более низкую толерантность к терапии и больше нежелательных исходов операций. Следовательно, кахексия является основной причиной смертности при раке поджелудочной железы. К сожалению 5-летняя выживаемость при раке поджелудочной железы остается на уровне 6% в течение последних четырех десятилетий, что является наименьшим среди всех злокачественных новообразований.
С введением новых средств для идентификации кахектических факторов и их эффектов на скелетные мышцы в области кахексии в последнее время были получены значительные продвижения в понимании лежащих в основе механизмов, которые регулируют мышечную атрофию при раке и других хронических заболеваниях. В результате, авторы в настоящее время понимают, как цитокины и системное воспаление регулируют мышечную атрофию, воздействуя на ключевые сигнальные пути, которые действуют изнутри миоволокна. Однако перевод полученных открытий в эффективное лечение был затруднен, и до аспектов, описанных в настоящем описании, эффективное лечение кахексии отсутствовало.
Масса скелетных мышц регулируется, отчасти, относительной скоростью синтеза белка по сравнению с регуляцией белка. Alamdari, N, et al., Acetylation and deacetylation -novel factors in muscle wasting, Metabolism. Jan 2013; 62(1): 1-11. Потеря скелетной мышечной массы развивается, когда скорость разрушения белка больше, чем синтез белка. Там же. Ацетилирование и деацетилирование белка модифицирует факторы транскрипции и транскрипцию генов, которые могут влиять на мышечную массу, делая белки более или менее подверженными деградации. Там же. Гистон-ацетилазы (HAT) и гистон-деацетилазы (HDAC) играют роль в регуляции ацетилирования и деацетилирования белка.
Однако эффекты таких молекул на потерю мышц и кахексию оказались противоречивыми - доказательства предполагают, например, что применение ингибиторов HDAC (например, Трихостатина A (TSA)) приводит к гиперацетилированию, которое может стимулировать деградацию белка, приводящую к повышенной потере мышц и кахексии. Противоречивые результаты были обнаружены Narver et. al., (Sustained improvement of spinal muscular atrophy mice treated with trichostatin A plus nutrition. Ann Neurol. 2008;64:465-70) однако, полученные результаты были под вопросом, так как лечение TSA также сопровождалось агрессивной питательной поддержкой. Alamdari et al., в 5. Следовательно, считают, что ингибиторы HDAC, скорее усиливают, чем уменьшают кахексию, или их применение давало конфликтные и противоречивые результаты.
Развитие и прогрессирование раковой кахексии вызвано комплексными, мультифакториальными патофизиологическими ответами на опухоли в мышечных тканях. К настоящему времени недоступно одобренное FDA лечение для предотвращения или замедления прогрессирования потери мышц у пациентов с кахексией. К настоящему времени несколько исследуемых лекарственных средств, которые нацелены на различные аспекты патогенеза кахексии, проходят исследования у людей, однако, с различными клиническими исходами. Например, тогда как mAb BYM38 от Новартис (бимагрумаб), которое блокирует связывание миостатина и активина с рецепторами активина II типа, получившее обозначение FDA, как терапия прорыва, лекарственное средство от потери мышц GTx's энобосарм, селективный модулятор рецепторов андрогенов, не попали в клинические исследования поздней стадии.
Ацетилирование ядерных гистонов играет важную роль в регуляции транскрипции генов путем регуляции нуклеосомной упаковки ДНК. Деацетилирование гистонов приводит к точной упаковке нуклеосом и транскрипционной репрессии из-за ограниченного доступа факторов транскрипции к мишеням ДНК. Ацетилирование гистонов расслабляет структуры нуклеосом, обеспечивая больший доступ для факторов транскрипции. Баланс между деацетилированием и ацетилированием гистонов модулируется гистон деацетилтрансферазами (HDAC) и гистон ацетилтрансферазами (HAT). Патологический баланс таких факторов коррелирует с ростом патологических клеток и некоторыми формами рака, как обсуждается в патенте США номер 8318808, включенном в виде ссылки в настоящее описание полностью. Ингибиторы HDAC, в частности, изменения баланса между ацетилированием и деацетилированием, приводящие к остановке роста, дифференцировке и апоптозу во множестве типов опухолевых клеток. См., например, патент США номер 8318808.
18 HDAC были идентифицированы у людей и характеризуются как являющиеся цинк-зависимыми или никотинамид аденин динуклеотид (NAD)-зависимыми (Discov Med 10(54):462-470, November 2010) и ассоциированными со следующими классами: класс I (HDAC 1, 2, 3, и 8); класс II (HDAC 4, 5, 6, 7, 9, и 10; класс III (сиртуины 1-7 (SIRT)); и класс IV (HDAC 11).
Среди них особенный интерес представляют ингибиторы HDAC, описанные в патенте США номер 8318808, и основанные на, например, жирных кислотах, связанных с Zn2+-комплексообразующими фрагментами посредством ароматических Ω-аминокислотных линкеров. В различных аспектах, ингибиторы HDAC могут иметь формулу:

где X выбирают из H и CH3; Y представляет собой (CH2)n, где n равно 0-2; Z выбирают из (CH2)m, где m равно 0-3 и (CH)2; A представляет собой гидрокарбильную группу; B представляет собой o-аминофенил или гидроксильную группу; и Q представляет собой галоген, водород, или метил. Один ингибитор HDAC, в частности (N-гидрокси-4-(3-метил-2-фенилбутириламино)бензамид) также известен как AR-42. В одном аспекте структурой AR-42 является следующая:
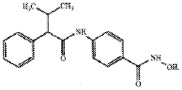
AR-42 представляет собой ингибитор деацетилазы и гистоновых и негистоновых белков широкого спектра с продемонстрированной большей эффективностью и активностью в солидных опухолях и гематологических злокачественных новообразованиях при сравнении с вориностатом (т.е., SAHA). См., например, Lu YS, et al., Efficacy of a novel histone deacetylase inhibitor in murine models of hepatocellular carcinoma, Hepatology. 2007 Oct;46(4):l 119-30; Kulp SK, et al., Antitumor effects of a novel phenylbutyrate-based histone deacetylase inhibitor, (S)-HDAC-42, in prostate cancer, Clin Cancer Res. 2006 Sep 1;12(17):5199-206.
AR-42 также может обладать дополнительными гистон-независимыми механизмами, которые участвуют в его терапевтическом профиле. См., например, Chen MC, et al., Novel mechanism by which histone deacetylase inhibitors facilitate topoisomerase Πα degradation in hepatocellular carcinoma cells, Hepatology. 2011 Jan;53(l): 148-59; Chen CS, et al., Histone acetylation-independent effect of histone deacetylase inhibitors on Akt through the reshuffling of protein phosphatase 1 complexes, J Biol Chem. 2005 Nov 18;280(46):38879-87; Yoo CB, et al., Epigenetic therapy of cancer: past, present and future, Nat Rev Drug Discov. 2006 Jan;5(l):37-50.
AR-42 обладает продемонстрированным ингибирующим эффектом в опухолях, включая, без ограничения, молочную железу, предстательную железу, яичники, клетки крови (например, лимфому, миелому и лейкоз), печень и головной мозг. См., например, Mims A, et. al., Increased anti-leukemic activity of decitabine via AR-42-induced upregulation of miR-29b: a novel epigenetic-targeting approach in acute myeloid leukemia, Leukemia. 2012 Nov 26. doi: 10.1038/leu.2012.342. [Epub ahead of print]; Burns SS, et al., Histone deacetylase inhibitor AR-42 differentially affects cell-cycle transit in meningeal and meningioma cells, potently inhibiting NF2-deficient meningioma growth, Cancer Res. 2013 Jan 15;73(2):792-803; Lu YS, et. al., Radiosensitizing effect of a phenylbutyrate-derived histone deacetylase inhibitor in hepatocellular carcinoma, Int J Radiat Oncol Biol Phys. 2012 Jun 1;83(2); Zimmerman B, et. al., Efficacy of novel histone deacetylase inhibitor, AR42, in a mouse model of, human T-lymphotropic virus type 1 adult T cell lymphoma, Leuk Res. 2011 Nov;35(l l): 1491-7; Zhang S, et al., The novel histone deacetylase inhibitor, AR-42, inhibits gpl30/Stat3 pathway and induces apoptosis and cell cycle arrest in multiple myeloma cells, Int J Cancer. 2011 Jul 1;129(1):204-13.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Аспекты, представленные в настоящем описании, обеспечивают способы подавления кахексии у млекопитающих с раком, включающие введение указанному млекопитающему ингибитора HDAC класса 1 и 2b. Один аспект обеспечивает способ подавления кахексии у млекопитающего с раком путем введения ингибитора HDAC класса 1 и 2b указанному млекопитающему в количестве, эффективном для, по существу, поддержания массы млекопитающего по сравнению с млекопитающим, которое не получает ингибитор HDAC класса 1 и 2b. В другом аспекте, ингибитор HDAC класса 1 и 2b вводят млекопитающему с раком в количестве, эффективном для по существу поддержания, по меньшей мере, около 90% массы тела указанного млекопитающего в течение периода времени, по меньшей мере, пятнадцати дней. В другом аспекте, ингибитор HDAC класса 1 и 2b представляет собой AR-42. В еще одном аспекте млекопитающее с раком имеет, по меньшей мере, одну опухоль и объем опухоли не уменьшается более чем на 6% в течение около первых пятнадцати дней после лечения AR-42.
Другие аспекты, представленные в настоящем описании, обеспечивают способы подавления кахексии путем введения AR-42 млекопитающему с раком, где экспрессия множества медиаторов мышечной атрофии (например, стимуляторов про-кахексии, таких как IL-6, IL-6RCC, LIF, MuRFl, атрогин-I) при раковой кахексии снижена по сравнению с млекопитающим, имеющим рак, который не получает лечение AR-42.
Дополнительные аспекты обеспечивают методы подавления кахексии путем введения AR-42 млекопитающему с раком, где индуцированная кахексией потеря жировой ткани и уменьшение размера скелетно-мышечных волокон по существу восстанавливается по сравнению с млекопитающим, которое не получает AR-42.
Аспекты, описанные в настоящем описании, обеспечивают способы поддержания массы скелетных мышц у млекопитающего, имеющего рак, путем введения ингибитора HDAC класса 1 и 2b указанному млекопитающему в количестве, эффективном для поддержания, по меньшей мере, около 90% массы скелетных мышц указанного млекопитающего в течение периода времени, по меньшей мере, пятнадцати дней по сравнению с млекопитающим, которое не получает ингибитор HDAC класса 1 и 2b.
Дополнительные аспекты обеспечивают способы продления выживаемости млекопитающего, имеющего рак, путем введения ингибитора HDAC класса 1 и 2b млекопитающему в количестве, эффективном для по существу пролонгирования выживаемости млекопитающего по сравнению с млекопитающим, которое не получает ингибитор HDAC класса 1 и 2b.
Как описано в настоящем описании, AR-42 демонстрирует эффективность in vivo в подавлении, уменьшении или блокаде потери мышц и пролонгировании выживаемости в моделях раковой кахексии на животных. Кроме того, эффект AR-42 на рак-связанную кахексию не зависит от эффектов AR-42 на уменьшение опухолевой нагрузки.
ЧЕРТЕЖИ
На фиг. 1A показано примерное подавление кахексии, индуцированной раком, у мышей с опухолями C-26, и изображены изменения общей массы {слева, опухоль включена) и массы тела {в центре, опухоль исключена) в течение 15-дневного исследования у мышей без опухоли, получающих носитель (контроль), по сравнению с мышами с опухолями, получающими носитель (носитель), или пероральный AR-42 в дозе 50 мг/кг через день (AR-42). Стрелки показывают время лечения AR-42. Справа, отсутствие супрессивного эффекта AR-42 на рост опухоли у мышей с опухолями C-26. Данные представлены как среднее ± S.D. Значения P: a, 0,045; b, 0,0027; c, 0,049; d, 0,0048;
На фиг. 1B показаны фотографии характерных мышей с опухолями из каждой группы, изображающие терапевтический эффект AR-42 в отношении раковой кахексии;
На фиг. 1C показано примерное среднее суточное потребление пищи среди трех групп лечения в течение исследования. Данные представлены как среднее ± S.D. (n=8);
На фиг. 1D показаны примерные эффекты AR-42 на массу мышц задних конечностей, включая икроножную, переднюю большеберцовую и четырехглавую (значения P: a, <0,001; b, 0,0042; c, 0,0046) у мышей без опухолей и с опухолями по сравнению с таковыми, получающими носитель мышами с опухолями и без опухолей (n=8);
На фиг. 1E показаны примерные эффекты AR-42 на сердце, жировую ткань и селезенку (P значения: a, <0,001; b, 0,0059; c, 0,001; d, 0,009) у мышей и без опухолей и с опухолями по сравнению с таковыми, получающими носитель мышами с опухолями и без опухолей (n=8);
На фиг. 2A показано примерное сохранение размера мышечных волокон у мышей, имеющих опухоль C-26, изображенное слева, микрофотографии H&E-окрашенных сечений икроножных мышц от контрольных мышей без опухолей и мышей с опухолями, получавших носитель или AR-42. Столбики шкалы, 100 мкм и справа, площади поперечных сечений мышечных волокон в икроножных мышцах, представлены как гистограмма частоты с достоверностью (P < 0,001). Данные представлены как среднее ± S.D.;
На фиг. 2B показаны примерные кривые выживаемости Каплана-Майера для мышей с опухолями, получавших носитель, вориностат (50 мг/кг, п.о., ежедневно), ромидепсин (0,6 мг/кг, и/п, два раза в неделю), или AR-42 (50 мг/кг п.о., через день). Выживаемость определяли в момент времени, в котором потеря массы тела (за исключением опухоли) достигала 20% от исходной массы тела, что служило в качестве человеческой конечной точки для исключения из исследования (*, P<0,001, носитель vs. AR-42; n=8);
На фиг. 2C показаны примерные фотографии характерных мышей из каждой группы, изображающие терапевтический эффект AR-42 относительно вориностата и ромидепсина на раковую кахексию у мышей с опухолями, что оценивали по позе, шерсти и состоянию тела;
На фиг. 2D показан примерный относительный уровень экспрессии мРНК Атрогин-1//MAFbx и MuRFl в скелетных мышцах мышей без опухолей, получавших носитель (n=6), и мышей с опухолями, получавших AR-42 (n=8), вориностат (n=8), или ромидепсин (n=5) по сравнению с таковым мышей с опухолями, получавших носитель (n=8) через 15 дней после инъекции опухолевых клеток. Данные представлены как среднее+S.D. Значения P: a, <0,001; b, 0,016; c, 0,0063;
На фиг. 3A показаны примерные эффекты на уровень промежуточных продуктов, ассоциированных с гликолизом и альтернативными путями метаболизма глюкозы;
На фиг. 3B показаны примерные эффекты AR-42 на метаболизм гликогена в икроножных мышцах мышей без опухолей и с опухолями (n=8 для каждой группы). Мыши с опухолями получали носитель или AR-42 (50 мг/кг, п.о., через день) начиная в день 6 после инъекции опухолевых клеток и заканчивая в день 17. Контрольные мыши без опухолей получали носитель или AR-42 параллельно. Данные представлены в блоках и графиках с разбросами. Низ и верх столбика представляет собой первую и третью квартили и символ "+" и полоса снаружи столбика обозначает среднее значение и медиану, соответственно. Концы усов представляют собой максимальное и минимальное значения в каждой группе;
На фиг. 4 показано, что AR-42 блокирует индуцированные кахексией изменения в уровне свободных аминокислот и метаболитов аминокислот, вовлеченных в регуляцию нейротрансмиссии, и биомаркеров инсулинорезистентности в мышцах мышей с опухолями C-26. Образцы для анализа получали из эксперимента, описанного в отношении фиг. 3 A и 3B. Данные представлены в диаграмме вида «ящик с усами», как описано в отношении чертежей 3A и 3B;
На фиг. 5A показаны примерные (сверху) эффекты AR-42 на уровень цитокинов про-кахексии IL-6 (слева) и LIF (справа) в сыворотке мышей без опухолей по сравнению с мышами с С-26 опухолями, и (снизу) кПЦР анализ эффектов AR-42 на экспрессию мРНК IL-6Ra в скелетных мышцах мышей без опухолей по сравнению с мышами с С-26 опухолями. Данные представлены как среднее ± S.D. P значения: a, <0,001 ; b, 0,006; c, 0,012 (n=3). Мышей лечили, как описано в отношении фиг. 3;
На фиг. 5B показан примерный анализ компонентов данных RNA-seq (слева) и диаграмма Venn (справа), показывающие дифференциально экспрессируемые гены среди четырех групп лечения. TF, без опухолей; T, с опухолями; veh, получающие носитель; AR, получающие AR-42. Мышей лечили, как описано в отношении фиг. 3;
На фиг. 5C показан примерный анализ эффектов AR-42 на уровень транскриптов шести ключевых регуляторов про-кахексии по RNA-seq (P значения: a, 0,024; b, 0,028; c, 0,015; d, 0,007; e, 0,024; f, 0,026; g, 0,01; h, 0,012; i, <0,001; j, 0,014; n=3). Мышей лечили, как описано в отношении фиг. 3;
На фиг. 5D показан примерный анализ эффектов AR-42 на уровни транскриптов шести ключевых регуляторов про-кахексии посредством кПЦР в скелетных мышцах в четырех группах лечения (*, P <0,001; n=6). Данные представлены как среднее ± S.D. Мышей лечили, как описано в отношении фиг. 3;
На фиг. 6A показана супрессия раковой кахексии у мышей, несущих С-26 опухоли, путем отсрочивающего лечения AR-42 до поздних стадий опухолей и кахексии. Изменения массы тела (за исключением опухоли) в течение 18 дневного исследования у контрольных мышей без опухолей, получавших носитель (T/F, Veh) и мышей с опухолями, получавших носитель (T, Veh) по сравнению с таковыми, получавшими перорально AR-42 (показано слева), начиная с дня 6 (T, AR42/D6), дня 10 (T, AR42/D10), или дня 12 (T, AR42/D12). P значения: a, 0,0015; b, 0,023 (n=8). Стрелки показывают временные точки начала лечения AR-42. Данные представлены как среднее. Для ясности представления, S.D. столбики для каждой точки данных не показаны. Справа результаты, показывающие отсутствие супрессивного эффекта AR-42 на рост опухоли у мышей с С-26 опухолями в эксперименте отсроченного лечения. Данные представлены как средние ± S.D. (n=8);
На фиг. 6B показаны примерные фотографии, изображающие терапевтический эффект AR-42 в отношении раковой кахексии у мышей с опухолями, несмотря на отложенное лечение, что проявляется нормальной позой, гладкой шерстью и лучшим состоянием тела, несмотря на большую опухолевую нагрузку;
На фиг. 6C показаны примерные эффекты лечения AR-42, начинаемого на различных стадиях прогрессирования заболевания, как изображено на фиг. 6A, на массу мышц задних конечностей, включая икроножную, переднюю большеберцовую и четырехглавую, у мышей с С-26 опухолями. Данные представлены как среднее ± S.D. (n=8; *, P<0,001);
На фиг. 6D показаны эффекты AR-42 на силу сжатия мышей с опухолями относительно контроля без опухолей и с опухолями, получающего носитель, в день 15 и день 16. Данные представлены как среднее ± S.D. (n=8; P значения: a, 0,01; b, 0,022; c, <0,001; d, 0,0019). Н, Ньютоны;
На фиг. 7 показано, что AR-42 защищает против индуцированной раком потери мышц на мышиной модели кахексии LLC. Показаны примерные эффекты AR-42 по сравнению с носителем в отношении массы мышц задних конечностей, включая икроножную, переднюю большеберцовую и четырехглавую, у мышей без опухолей и с опухолями, по сравнению с мышами с опухолями, получающими носитель. Мышей лечили так же, как описано на фиг. 1A, за исключением того, что мышей умерщвляли в день 20 после инъекции опухолевых клеток. Данные представлены как средние ± S.D. (n=8);
На фиг. 8 показаны примерные последовательности праймеров, используемых для ОТ-ПЦР в реальном времени;
На фиг. 9 показан примерный анализ сложности пути (Ingenuity Pathway Analysis) (IPA) (QIAGEN) дифференциально экспрессируемых генов (>4-крат) относительно мышечных заболеваний или функций между мышами с С-26 опухолями, получавшими AR-42 и носитель (n=6);
На фиг. 10 показан примерный анализ профилей цитокинов от мышей без опухолей и мышей с С-26 опухолями, получавшими носитель или AR-42 (средние ± S.D.; n=3 для каждой группы); и
На фиг. 11 показан примерный анализ RNA-seq дифференциально экспрессируемых генов (> 4-крат) в мышцах от мышей с С-26 опухолями, получавшими AR-42 или носитель (n=3).
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
До описания нескольких примерных аспектов, представленных в настоящем описании, необходимо понимать, что изобретение не ограничено подробностями конструкции или стадий процесса, указанными в следующем описании. Аспекты, описанные в настоящем описании, могут быть осуществлены или проведены различными путями.
Аспекты, представленные в настоящем описании, описывают эффекты перорального AR-42 в отношении облегчения индуцированной кахексией потери массы и атрофии скелетных мышц и удлинения выживаемости в модели раковой кахексии CD2Fi опухоли ободочной кишки 26 (C-26) у мышей. Мышиная модель раковой кахексии CD2Fi описана, например, в BMC Cancer. 2010 Jul 8;10:363, включенном в виде ссылки полностью. Наблюдаемый эффект анти-кахексии был ассоциирован со способностью AR-42 репрограммировать клеточный метаболизм и подавлять уровень IL-6 в пораженных мышечных тканях с подавлением потери мышц и другими эффектами, связанными с кахексией, независимо от эффектов AR-42 на снижение опухолевой нагрузки.
Аспекты, представленные в настоящем описании, описывают эффекты перорального AR-42 в отношении облечения индуцированной кахексией потери массы, атрофии скелетных мышц и удлинения выживаемости в модели раковой кахексии при карциноме легких Льюиса (LLC). См, например, Expert Opin Drug Discov. Nov 1, 2009; 4(11): 1145-1155.
Ингибиторы HDAC, описанные в патенте США номер 8318808, могут быть использованы в различных методах, описанных в настоящем описании. Такие ингибиторы HDAC основаны, например, на жирных кислотах, связанных с Zn2+-хелатирующими фрагментами посредством ароматических Ω-аминокислотных линкеров. В различных аспектах ингибиторы HDAC могут иметь формулу:

где X выбирают из H и CH3; Y представляет собой (CH2)n, где n равно 0-2; Z выбирают из (CH2)m, где m равно 0-3 и (CH)2; A представляет собой гидрокарбильную группу; B представляет собой o-аминофенил или гидроксильную группу; и Q представляет собой галоген, водород или метил.
В другом аспекте в методах, описанных в настоящем описании, используют AR-42, также известный как (S)-N-гидрокси-4-(3-метил-2-фенилбутанамидо)бензамид, имеющий следующую химическую структуру:
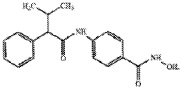
В еще одном аспекте AR-42 включает соли, сольваты, гидраты, безводные, ко-кристаллические и другие кристаллические формы и комбинации. AR-42 могут быть рецептированы во множестве лекарственных форм, имеющих увеличенную стабильность, увеличенную биодоступность, непрерывное высвобождение и другие свойства.
В одном аспекте ингибиторы HDAC классифицируются как цинк-зависимые или никотинамидадениндинуклеотид (NAD)-зависимые (Discov Med 10(54):462-470, November 2010) и их делят на четыре класса с восемью подтипами семейств на основании их субстрата HDAC: класс I (HDAC 1, 2, 3, и 8); класс II (HDAC 4, 5, 6, 7, 9, и 10; класс III (сиртуины 1-7 (SIRT)); и класс IV (HDAC 11). Там же. В другом аспекте ингибиторы HDAC включают, без ограничения, вориностат (SAHA) (ингибитор класс I и II), депсипептид класс I ингибитор, и AR-42 (ингибитор класс I и IIb). См., например, Strahl, B.D. and Allis, CD. (2000) Nature 403:41-45. Другие ингибиторы HDAC (например, трихостатин A или TSA) ингибируют HDAC класс 1 и класс 2. Субстраты для ингибиторов HDAC варьируются на классы и подтипы.
В другом аспекте ингибитор HDAC ингибирует HDAC класса 1 и класса 2b. В еще одном аспекте ингибитором HDAC является AR-42.
В модели раковой кахексии при опухоли ободочной кишки 26 (C-26), фрагмент опухоли C26 пересаживали изогенным мышам BALB/c и у мышей развивалась недифференцированная карцинома. Атрофия скелетных мышц (измеряемая по мышечной силе и устойчивости к усталости) коррелировала с наблюдаемыми биохимическими изменениями и модель была описана как "хорошо стандартизованная экспериментальная модель для исследования раковой кахексии." BMC Cancer. 2010 Jul 8;10:363.
В одном аспекте обеспечивают методы подавления кахексии у млекопитающего с раком путем введения млекопитающему ингибитора HDAC класса 1 и 2b в количестве, эффективном для по существу поддержания массы млекопитающего по сравнению с млекопитающим, которое не получало ингибитора HDAC класса 1 и 2b. В другом аспекте ингибитором HDAC является AR-42.
В еще одном аспекте масса млекопитающего не уменьшается более чем на около 6% после около первых 15 дней после лечения AR-42.
В другом аспекте рак выбирают из группы, состоящей из рака поджелудочной железы, ободочной кишки, головы, шеи, желудка и пищевода. В другом аспекте млекопитающим является человек.
AR-42 можно вводить в количестве от около 1 мг/кг до около 100 мг/кг млекопитающего и вводить, по меньшей мере, один раз в сутки. В другом аспекте, AR-42 вводят два раза в сутки в количестве около 50 мг/кг массы млекопитающего.
В еще одном аспекте, уровни IL-6 снижались на около 56% по сравнению с млекопитающим, которое не получало AR-42. В другом аспекте уровни фактора ингибирования лейкоза (LIF) снижаются на около 88% по сравнению с млекопитающим, которое не получало AR-42. В другом аспекте, экспрессия мРНК Атрогин-1 восстанавливалась до базального уровня по сравнению с млекопитающим, которое не получало AR-42.
В одном аспекте экспрессия мРНК MuRFl восстанавливается до базальных уровней по сравнению с млекопитающим, которое не получало AR-42. В другом аспекте повышение уровня мРНК IL-6RCC, индуцированное кахексией, снижается на около 85% по сравнению с млекопитающим, которое не получало AR-42.
В еще одном аспекте потеря жировой ткани, индуцированная кахексией, по существу восстанавливается по сравнению с млекопитающим, которое не получало AR-42. В другом аспекте, уменьшение размера волокон скелетных мышц, индуцированное кахексией, восстанавливается AR-42 по сравнению с млекопитающим, которое не получало AR-42.
Также обеспечивают методы поддержания массы скелетных мышц у млекопитающего, имеющего рак, включающие введение ингибитора HDAC класса 1 и 2b указанному млекопитающему в количестве, эффективном для поддержания, по меньшей мере, около 90% массы скелетных мышц указанного млекопитающего в течение периода времени, по меньшей мере, пятнадцати дней по сравнению с млекопитающим, которое не получало ингибитора HDAC класса 1 и 2b.
В другом аспекте обеспечивают методы продления выживаемости млекопитающего, имеющего рак, включающие введение ингибитора HDAC класса 1 и 2b млекопитающему в количестве, эффективном для существенного продления выживаемости млекопитающего по сравнению с млекопитающим, которое не получало ингибитор HDAC класса 1 и 2b. В еще одном аспекте млекопитающее выживает в течение, по меньшей мере, около 21 дня после введения млекопитающему AR-42.
В другом аспекте введение AR-42 облегчало потерю массы тела и атрофию скелетных мышц, индуцированные кахексией, и продлевали выживаемость млекопитающих. Без связи с теорией, считают, что антикахектический эффект ассоциирован со способностью AR-42 репрограммировать клеточный метаболизм и подавлять уровни IL-6 в пораженных мышечных тканях с подавлением потери мышц и других эффектов, связанных с кахексией, независимо от эффектов AR-42 на уменьшение опухолевой нагрузки.
В одном аспекте анти-кахектические эффекты AR-42 оценивали путем множества методик, включая кОТ-ПЦР анализ экспрессии установленных медиаторов мышечной атрофии при раке (например, Cancer Cell. 2008 Nov 4;14(5):369-81), измерение уровня противовоспалительных цитокинов в сыворотке и мышечной ткани икроножных мышц (Am J Pathol. 2011 Mar;178(3): 1059-68), анализ метаболомного профилирования (J Cachexia Sarcopenia Muscle. 2013 Jun;4(2): 145-55), измерение уровня свободных аминокислот в мышечной ткани (J Cachexia Sarcopenia Muscle. 2013 Jun;4(2): 145-55; Am J Physiol Endocrinol Metab. 2007 Feb;292(2):E501-12), измерение "гликолитической подписи" кахектичных мышц путем измерения уровня биохимических веществ, ассоциированных с путем гликолиза (Cachexia Sarcopenia Muscle. 2013 Jun;4(2): 145-55), измерение уровня запасов гликогена в ткани кахектичных мышц (Cell Death Differ. 2012 Oct;19(10): 1698-708), анализ метаболизма аминокислот с разветвленной цепью в кахектичных мышцах (Int J Biochem Cell Biol. 2013 Oct;45(10):2163-72), и измерение уровня 2-гидроксибутирата и офтальмата в кахектичных мышцах (PLoS One. 2010 May 28;5(5):el0883; Int J Cancer. 2010 Feb l;126(3):756-63).
Ингибиторы HDAC, как описано в настоящем описании, можно вводить пациенту, нуждающемуся в лечении (например, пациенту, имеющему рак и проявляющему симптомы кахексии). В одном аспекте определенные раки являются особенно ассоциированными с кахексией, включая, без ограничения, рак поджелудочной железы, желудка, головы, шеи и пищевода ("раки, ассоциированные с кахексией"). В другом аспекте, ингибитор HDAC класса 1, 2b (например, AR-42) вводят пациенту, нуждающемуся в лечении.
Как используется в настоящем описании, термин "по существу" относится к "большинству из," "большей части," или, по меньшей мере, 50%, 60%, 70%, 80%, и 90% массы или количества, например, млекопитающего, которое не имеет рака.
Термины "лечить," "уменьшать," "подавлять," "ингибировать," "предотвращать," или сходные термины, как используется в настоящем описании, не обязательно обозначают 100% или полное лечение или профилактику. Более того, такие термины относятся к различным степеням лечения или профилактики определенных заболеваний (например, 100%, 90%, 80%, 70%, 60%, 50%, 40%, 30%, 20%, 10%, 5%, или 1%), что понимают в области техники как полезное.
Термины "лечение" или "профилактика" также относятся к отсрочке развития заболевания в течение периода времени или отсрочки развития бессрочно. Термин "лечение" или "терапия" относится к введению лекарственного средства или лечению пациента, или назначению лекарственного средства пациенту (например, доктором, медсестрой или другим медицинским специалистом), где пациент или третье лицо (например, ухаживающий, член семьи или специалист здравоохранения) вводит лекарственное средство или лечение. Термин "эффективное количество" относится к количеству лекарственного средства или терапии (например, ингибитора HDAC класса I и IIb), которое лечит, уменьшает, подавляет, ингибирует, предотвращает заболевание(я) или состояние(я) (например, кахексию) или продлевает выживаемость млекопитающего с заболеванием или состоянием.
Термин "пролонгировать" или "продление", как используется в настоящем описании, относится к увеличению времени выживаемости млекопитающего, получающего лечение, по сравнению с млекопитающим, которое не получает лечение. В таком аспекте, "увеличенная выживаемость" может относиться к увеличению продолжительности жизни млекопитающего на, например, 1%, 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80% или 90% продолжительности жизни млекопитающего, которое не имеет рака.
Любой из ингибиторов HDAC, описанных в настоящем описании, может вводиться перорально, парентерально (в/в, в/м, депо-в/м, п/к, и депо-п/к), сублингвально, интраназально (ингаляция), интратекально, местно или ректально. Лекарственные формы, известные специалисту в области техники, являются подходящими для доставки ингибиторов HDAC, описанных в настоящем описании.
В одном аспекте, примерные ингибиторы HDAC вводят в пероральной лекарственной форме (например, пилюля, капсула, каплет или таблетка и др.) пациенту с диагнозом рака, ассоциированного с кахексией (например, рак поджелудочной железы, мочевого пузыря, головы и шеи).
Ингибиторы HDAC могут быть рецептированы в подходящие фармацевтические препараты, такие как таблетки, капсулы или эликсиры для перорального введения, или в стерильные растворы или суспензии для парентерального введения. Ингибиторы HDAC, описанные в настоящем описании, могут быть рецептированы в фармацевтические композиции с использованием методик и процедур, хорошо известных в области техники.
В одном аспекте от около 0,1 до 1000 мг, от около 5 до около 100 мг, или от около 10 до около 50 мг ингибитора НDAC (например, AR-42), или его физиологически приемлемой соли или сложного эфира, может быть смешано с физиологически приемлемой основой, носителем, вспомогательным веществом, вяжущим веществом, консервантом, стабилизатором, ароматизатором и др. в стандартной лекарственной форме, как принято в фармацевтической практике. Количество активного вещества в композициях или препаратах, включающих ингибиторы HDAC, является таким, чтобы получить подходящую дозировку в указанном диапазоне.
В другом аспекте композиции могут быть рецептированы в стандартной лекарственной форме, каждая лекарственная форма содержит от около 1 до около 500 мг, или от около 10 до около 100 мг активного ингредиента. Термин "стандартная лекарственная форма" относится к физически отдельным единицам, подходящим в качестве стандартных дозировок для пациентов людей и других млекопитающих, каждая единица содержит заранее определенное количество активного вещества, рассчитанное для получения желаемого терапевтического эффекта, в ассоциации с подходящим фармацевтическим вспомогательным веществом.
В одном аспекте один или более ингибиторов HDAC смешивают с подходящим фармацевтически приемлемым носителем для получения композиций. При смешивании или добавлении соединения(й), полученная смесь может быть раствором, суспензией, эмульсией или подобным. Липосомальные суспензии или любые другие системы доставки наночастиц также могут быть использованы в качестве фармацевтически приемлемых носителей. Они могут быть получены в соответствии с методами, известными специалисту в области техники. Форма полученной смеси зависит от ряда факторов, включая предназначенный путь введения и растворимость соединения в выбранном носителе или основе. В одном аспекте эффективная концентрация является достаточной для уменьшения или облегчения, по меньшей мере, одного симптома заболевания, расстройства или состояния, которое лечат, и может быть определена эмпирически.
В еще одном аспекте, AR-42 подавляет потерю мышц при кахексии, как показано в моделях кахексии при опухолях C-26 и LLC. Провоспалительные цитокины, IL-6 и TNF, представляют собой основные прокахектические факторы в двух моделях (31, 32). Анализ профиля цитокинов показывает, что, тогда как AR-42 не оказывает эффекта на уровень TNF сыворотки у мышей с опухолями C-26, он снижает уровень IL-6 сыворотки и внутримышечную экспрессию мРНК IL-6RCC. Тем не менее, мыши с опухолями С-26, получавшие AR-42, все еще демонстрировали повышенный уровень IL-6 сыворотки и мРНК IL-6RCC по сравнению с мышами без опухолей, предполагая, что снижение сигнала IL-6 отвечает не только за AR-42-опосредованное подавление потери мышц.
Механистически, антикахектический эффект AR-42 является уникальным, так как ингибиторы HDAC вальпроевая кислота и трихостатин-A не могут обращать потерю мышц у мышей с опухолями C-26 несмотря на их способность модулировать ось миостатина/фоллистатина (33). Сходным образом полученные открытия показали, что в отличие от AR-42, вориностат и ромидепсин были неэффективными в облегчении индуцированной кахексией потери массы тела в модели C-26. Такое расхождение может быть обусловлено большей способностью AR-42 подавлять экспрессию мРНК E3 лигаз атрогин-1 и MuRFl в мышцах мышей с опухолями, что может отражать различия в их соответствующих способностях модулировать глобальную экспрессию генов в скелетных мышцах. Последние доказательства предполагают механистическую связь между патологическим ацетилированием/экспрессией факторов транскрипции и потерей мышц в пораженных мышцах, приводя к дисрегуляции экспрессии генов, ассоциированных с кахексией [обзор: (34)]. Сообщают, что активность гистон-ацетилтрансферазы p300/CBP дифференциально регулирует транскрипционную активность и ядерную локализацию факторов транскрипции семейства Foxo в скелетных мышцах (35), и таковую класса 1 HDAC, особенно HDAC1, которая играет критическую роль в опосредовании мышечной атрофии из-за лишения питания или отсутствия использования мышц в результате регуляции экспрессии Foxo и его мишеней атрогин-1 и MuRFl (22).
Анализ RNA-seq выявил способность AR-42 обращать индуцированный опухолью сдвиг экспрессии генов. Всего были идентифицированы 677 генов, которые дифференциально экспрессировались в 4-крат или больше при сравнении мышей с опухолями, получавшими AR-42 и носитель. Возможно, такое большое количество дифференциально экспрессируемых генов может возникать в результате действия AR-42 на транскрипционную активность и/или экспрессию множества факторов/регуляторов транскрипции. В добавление к Foxol, AR-42 также модулирует экспрессию множества других факторов/регуляторов транскрипции, включая C/EBPδ, Fos, Jun-b, DAXX, ERN1, HIF3a, MAFF, MAFK, и Mef2c (фиг. 11). Среди указанных факторов транскрипции важность Mef2c в развитии скелетных, сердечных и гладких мышц хорошо документирована (36), и сигнальный каскад AP-1 был вовлечен в ассоциированную с раком потерю мышц (37).
Было предположено, что кахектические мышцы у мышей с опухолями C-26 демонстрировали физиологию опухоли Варбурга, характеризуемую высокой скоростью гликолиза (38). Метаболомные данные выявили выраженное репрограммирование метаболизма скелетных мышц у мышей с опухолями C-26, который полностью обращался AR-42. Более того, супрессивный эффект AR-42 на продукцию 2-гидроксибутирата и офтальмата, биомаркеров инсулинорезистентности (17) и окислительного стресса (18), является примечательным, как существенное доказательство, ассоциированное с инсулинорезистентностью (39, 40) и окислительным стрессом (41) с кахексией.
Механистически способность AR-42 поддерживать целостность скелетных мышц у мышей с опухолями возникает в результате его отдельных, кумулятивных эффектов на индуцированные опухолью изменения во множестве транскрипционных программ и метаболическом фенотипе. Терапевтически важно, что пероральное введение AR-42 на поздней стадии роста опухоли было все еще эффективным в замедлении прогрессирования потери мышц у мышей с опухолями C-26. Вместе полученные результаты показывают, что ингибиторы HDAC (например, AR-42) могут быть использованы как часть эффективной терапевтической стратегии для раковой кахексии, как описано в настоящем описании.
Фармацевтические носители или основы, подходящие для введения ингибиторов HDAC, описанные в настоящем описании, включают любые такие носители, подходящие для определенного пути введения. Кроме того, активные вещества также могут быть смешаны с другими активными веществами, которые не нарушают желаемого действия, или веществами, которые дополняют желаемое действие или имеют другое действие. Соединения могут быть рецептированы как единственный фармацевтически активный ингредиент в композиции или могут быть смешаны с другими активными ингредиентами.
В другом аспекте, если ингибиторы HDAC проявляют недостаточную растворимость, могут быть использованы способы для повышения растворимости. Такие способы известны и включают, без ограничения, использование со-растворителей, таких как диметилсульфоксид (DMSO), использование поверхностно-активных веществ, таких как TWEEN, и растворение в водном бикарбонате натрия. Производные соединений, такие как соли или пролекарства, также могут быть использованы в рецептировании эффективных фармацевтических композиций.
Концентрация соединения является эффективной для доставки количества при введении, которое уменьшает или облегчает, по меньшей мере, один симптом заболевания, для которого вводят соединение. Обычно композиции рецептируют для введения одной дозы.
В другом аспекте ингибиторы HDAC, описанные в настоящем описании, могут быть получены с носителями, которые защищают их от быстрого удаления из организма, такими как композиции медленного высвобождения или оболочки. Такие носители включают композиции регулируемого высвобождения, такие как, без ограничения, микроинкапсулированные системы доставки. Активное соединение может быть включено в фармацевтически приемлемый носитель в количестве, достаточном для получения терапевтически применимого эффекта в отсутствие нежелательных побочных эффектов у пациента, получающего лечение. Терапевтически эффективная концентрация может быть определена эмпирически путем исследования соединений в известных системах моделей in vitro и in vivo для заболеваний, которые лечат.
В другом аспекте ингибиторы HDAC и композиции, описанные в настоящем описании, могут быть включены в контейнеры с множеством доз или одной дозой. Включенные соединения и композиции могут быть обеспечены в наборах, например, включая составляющие, которые могут быть объединены для применения. Например, AR-42 в лиофилизированной форме и подходящий разбавитель могут быть обеспечены как отдельные компоненты для смешивания перед использованием. Набор может включать AR-42 и второе терапевтическое средство для совместного введения. AR-42 и второе терапевтическое средство могут быть обеспечены в виде отдельных составляющих частей. Набор может включать множество контейнеров, каждый контейнер содержит одну или более стандартных доз соединений, описанных в настоящем описании. В одном аспекте контейнеры могут быть адаптированы для желаемого пути введения, включая, без ограничения, таблетки, гелевые капсулы, капсулы длительного высвобождения и подобные для перорального введения; депо продукты, предварительно заполненные шприцы, ампулы, флаконы и подобные для парентерального введения; и пластыри, подушечки, кремы и подобные для местного введения.
Концентрация примерного ингибитора HDAC в фармацевтической композиции будет зависеть от абсорбции, инактивации и скорости экскреции активного соединения, схемы введения и вводимого количества, а также от других факторов, известных специалисту в области техники.
В другом аспекте активный ингредиент можно вводить однократно, или он может быть разделен на ряд меньших доз для введения с интервалами времени. Понимают, что точная дозировка и продолжительность лечения являются функцией заболевания, которое лечат, и могут быть определены эмпирически с использованием известных протоколов исследования или путем экстраполяции из данных исследований in vivo или in vitro. Необходимо отметить, что концентрации и значения дозировок могут также варьироваться в зависимости от тяжести состояния, которое облегчают. Также понимают, что для любого определенного субъекта специфические схемы введения необходимо регулировать с течением времени в соответствии с индивидуальными потребностями и профессиональным мнением лица, которое вводит или наблюдает за введением композиций, и диапазоны концентраций, указанные в настоящем описании, являются только примерными и не предназначены для ограничения рамок или осуществления заявленных композиций.
Если желательно пероральное введение, соединение может быть обеспечено в композиции, которая защищает его от кислого окружения в желудке. Например, композиция может быть рецептирована в кишечнорастворимой оболочке, которая сохраняет его целостность в желудке и высвобождает активное соединение в кишечнике. Композиция также может быть рецептирована в комбинации с антацидом или другим таким ингредиентом.
Пероральные композиции обычно включают инертный разбавитель или съедобный носитель и могут быть прессованы в таблетки или заключены в желатиновые капсулы. Для целей перорального терапевтического введения активное соединение или соединения могут быть включены с вспомогательными веществами и использованы в форме таблеток, капсул или пастилок. Фармацевтически совместимые вяжущие вещества и материалы добавки могут быть включены как часть композиции.
Таблетки, пилюли, капсулы, пастилки и подобные могут содержать любой из следующих ингредиентов или соединения сходной природы: вяжущее вещество, такое как, без ограничения, трагакантовая камедь, гуммиарабик, кукурузный крахмал или желатин; вспомогательное вещество, такое как микрокристаллическая целлюлоза, крахмал или лактоза; дезинтегрирующее вещество, такое как, без ограничения, альгиновая кислота и кукурузный крахмал; смазывающее вещество, такое как, без ограничения, стеарат магния; глидант, такой как, без ограничения, коллоидный диоксид кремния; подсластитель, такой как сахароза или сахарин; и ароматизатор, такой как мята перечная, метилсалицилат или фруктовые ароматизаторы.
Когда стандартной лекарственной формой является капсула, она может содержать, в добавление к материалу вышеуказанного типа, жидкий носитель, такой как жирное масло. В добавление стандартные лекарственные формы могут содержать различные другие материалы, которые модифицируют физическую форму лекарственной формы, например, оболочки сахара и другие кишечнорастворимые агенты. Соединения также можно вводить как компонент эликсира, сиропа, вафли, жевательной резинки и подобного. Сироп может содержать, в добавление к активным соединениям, сахарозу в качестве подсластителя и определенные красители, пигменты и краски, и ароматизаторы.
Активные материалы также могут быть смешаны с другими активными материалами, которые не нарушают желательного действия, или с материалами, которые дополняют желательное действие. Ингибиторы HDAC могут быть использованы, например, в комбинации с противоопухолевым веществом, гормоном, стероидом или ретиноидом. Противоопухолевым агентом может быть одно из множества химиотерапевтических средств, таких как алкилирующее вещество, антиметаболит, гормональное вещество, антибиотик, колхицин, алкалоид винка, L-аспарагиназа, прокарбазин, гидроксимочевина, митотан, нитрозомочевины или имидазола карбоксамид. Подходящие агенты включают такие агенты, которые обеспечивают деполяризацию тубулина. Примеры включают колхицин и алкалоиды винка, включая винбластин и винкристин.
В другом аспекте ингибиторы HDAC, описанные в настоящем описании, могут быть введены совместно или введены до или после иммунизации пациента вакциной для усиления иммунного ответа на вакцину. В одном аспекте вакциной является ДНК вакцина, например, вакцина HPV.
В одном аспекте растворы или суспензии, используемые для парентерального, внутрикожного, подкожного или местного применения, могут включать любой из следующих компонентов: стерильный разбавитель, такой как вода для инъекций, солевой раствор, нелетучее масло, натуральные растительные масла, такие как кунжутное масло, кокосовое масло, арахисовое масло, хлопковое масло и подобные, или синтетический жирный носитель, такой как этилолеат, и подобные, полиэтиленгликоль, глицерин, пропиленгликоль или другие синтетические растворители; антимикробные агенты, такие как бензиловый спирт и метилпарабены; антиоксиданты, такие как аскорбиновая кислота и бисульфит натрия; комплексообразующие агенты, такие как этилендиаминтетрауксусная кислота (EDTA); буферы, такие как ацетаты, цитраты и фосфаты; и средства для регуляции тонуса, такие как хлорид натрия и декстроза. Парентеральные препараты могут быть заключены в ампулы, одноразовые шприцы или многодозовые флаконы, сделанные из стекла, пластика или другого подходящего материала. Буферы, консерванты и подобные могут быть включены по требованию.
При введении внутривенно, подходящие носители включают, без ограничения, физиологический солевой раствор, фосфатный буферный раствор (PBS), и растворы, содержащие загустители и растворяющие агенты, такие как глюкоза, полиэтиленгликоль, полипропиленгликоль и их смеси. Липосомальные суспензии или любые другие системы доставки наночастиц, включая тканеспецифичные липосомы, также могут быть подходящими в качестве фармацевтически приемлемых носителей. Они могут быть получены в соответствии с методами, известными в области техники.
В другом аспекте ингибиторы HDAC могут быть получены с носителями, которые защищают соединение от быстрой элиминации из организма, такие как композиции с отсроченным высвобождением или оболочки. Такие носители включают композиции с регулируемым высвобождением, такие как, без ограничения, импланты и микроинкапсулированные системы доставки, и биоразлагаемые, биосовместимые полимеры, такие как коллаген, этиленвинилацетат, полиангидриды, полигликолевая кислота, полиортоэфиры, полимолочная кислота и подобные. Способы для получения таких композиций известны специалисту в области техники.
В еще одном аспекте соединения, используемые в способах по описанию, могут вводиться энтерально или парентерально. При введении перорально, соединения, используемые в способах настоящего описания, могут вводиться в обычных лекарственных формах для перорального введения, как хорошо известно специалисту в области техники. Такие лекарственные формы включают обычные твердые лекарственные формы таблеток и капсул, а также жидкие лекарственные формы, такие как растворы, суспензии и эликсиры. Когда используют твердые лекарственные формы, они могут быть типа длительного высвобождения, так что соединения, используемые в способах, описанных в настоящем описании, необходимо вводить только один или два раза в сутки.
Пероральные лекарственные формы можно вводить пациенту 1, 2, 3, или 4 раза в сутки. Ингибиторы HDAC, описанные в настоящем описании, можно вводить или три или меньше раз, или даже один или два раза в сутки. Следовательно, соединения ингибиторы HDAC, используемые в способах настоящего описания, вводят в пероральной лекарственной форме. Какая бы пероральная лекарственная форма не использовалась, они могут быть созданы таким образом, чтобы защитить соединения, используемые в методах, описанных в настоящем описании, от кислого содержимого желудка. Таблетки в кишечнорастворимой оболочке хорошо известны специалисту в области техники. Кроме того, капсулы, заполненные мелкими сферами, каждая покрытая оболочкой для защиты их от кислого желудка, также хорошо известны специалисту в области техники.
Термины "терапевтически эффективное количество" и "терапевтически эффективный период времени" используют для обозначения лечения в дозировках и в течение периодов времени, эффективных для уменьшения роста неопластических клеток. Как отмечено выше, такое введение может быть парентеральным, пероральным, сублингвальным, трансдермальным, местным, интраназальным, или интраректальным. В одном аспекте при системном введении, терапевтическую композицию можно вводить в достаточной дозировке для достижения уровня соединений в крови от около 0,1 мкМ до около 100 мM. Для локализованного введения, существенно меньшие концентрации, чем такие, могут быть эффективными, и существенно большие концентрации могут быть переносимыми. Специалист в области техники понимает, что такой терапевтический эффект, приводящий к меньшей эффективной концентрации ингибитора HDAC или AR-42, может существенно варьироваться в зависимости от ткани, органа и определенного животного или пациента, которого лечат. Также понимают, что тогда как пациент может начинать с одной дозы, такая доза может варьироваться в течение времени, если состояние пациента изменяется.
Специалисту в области техники очевидно, что точная дозировка и частота введения будет зависеть от определенных соединений, используемых в способах используемого описания, определенного состояния, которое лечат, тяжести состояния, которое лечат, возраста, массы и других препаратов, которые пациент может принимать, как хорошо известно назначающему врачу, который является специалистом в области техники.
ПРИМЕРЫ
Следующие неограничивающие примеры иллюстрируют аспекты, описанные в настоящем описании.
Пример 1
Модели раковой кахексии
Модель C-26
В одном аспекте опухоли получают путем подкожной инъекции клеток C-26 (0,5×106 клеток в 0,1 мл) в правый бок самцов мышей CD2F1 (в возрасте приблизительно 6 недель; Harlan Laboratories, Indianapolis, IN)(11). Мышей с опухолями, а также мышей без опухолей, служащих в качестве контроля без кахексии, рандомизировали в группы, которых лечили или AR-42 (50 мг/кг, п.о. через зонд, через день; Arno Therapeutics, Inc., Flemington, NJ) или носителем (0,5% метилцеллюлозы (масс/об) и 0,1% Tween-80 (об/об) в стерильной воде), начиная через 6 дней после инъекции клеток. Для оценки эффекта отложенного лечения, лечение лекарственным средством и/или носителем начинали через 6, 10 и 12 дней после инъекции раковых клеток.
В другом аспекте эффекты AR-42 сравнивали с другими ингибиторами HDAC. В таком аспекте дополнительные группы мышей с опухолями C-26 лечили вориностатом (50 мг/кг, п.о., один раз в сутки) и ромидепсином (0,6 мг/кг; и.п., два раза в неделю) (ChemieTek (Indianapolis, IN)).
Модель LLC
В другом аспекте подкожные опухоли получали у самцов мышей C57BL/6 (в возрасте приблизительно 6 недель; Harlan) путем инъекции 0,5×106 LLC клеток в правый бок. Лечение AR-42 и носителем проводили, как для модели C-26, начиная с 6 дня после инъекции клеток. В обеих моделях массу тела и потребление пищи отслеживали ежедневно и размер опухолей измеряли не реже, чем каждые два дня. Мыши голодали в течение 2 часов до умерщвления, когда забирали мышцы передних лап, сердце, селезенку, эпидидимальный жир и кровь и измеряли массу солидных тканей. Образцы мышц замораживали в 2-метилбутане, охлажденном жидким азотом, и затем хранили при -80°C до анализа.
Пример 2
Измерение силы сжатия
Силу сжатия передней лапы измеряли у мышей с использованием цифрового измерителя силы сжатия (Columbus Instruments, Columbus, OH). Пять измерений получали от каждой мыши, среднее из которых обозначали, как силу сжатия мыши.
Морфометрический анализ размера мышечных волокон
Десяти-мкм сечения нарезали из замороженных образцов скелетных мышц с использованием криостата (Leica) и затем окрашивали H&E. Изображения получали с использованием микроскопа Olympus BX51 (Olympus America, Inc.) и площади сечения мышечных волокон определяли с использованием программного обеспечения Olympus CellSens 1.11. Измерения получали из пяти различных сечений мышц от каждой из пяти мышей из каждой группы.
Выделение РНК, кОТ-ПЦР и анализ RNA-seq
Общую РНК выделяли из гомогенизированных икроножных мышц (n =3/группу) с реагентом TRIzol (Life Technologies, Carlsbad, CA) и затем очищали с использованием набора RNAeasy Mini Kit (Qiagen, Valencia, CA). кОТ-ПЦР проводили, как описано ранее (42), с использованием системы детекции ПЦР в реальном времени Bio-Rad CFX96 с iQ SYBR Green Supermix (Bio-Rad, Hercules, CA). Последовательности праймеров перечислены на фиг. 8. Создание библиотеки RNA-seq и анализ данных проводили в The Ohio State University Comprehensive Cancer Center (OSUCCC) Nucleic Acid Shared Resource.
Метаболомный и цитокиновый профиль
Икроножные мышцы и сыворотку собирали на 17 день после инъекции клеток для каждой группы лечения (n=8/группу). Мышцы подвергали Metabolon, Inc. (Durham, NC) для метаболомного анализа 270 метаболических промежуточных продуктов посредством собственной разработанной платформы масс-спектрометрии. Сыворотку подвергали Eve Technologies (Alberta, Canada) для анализа 32 цитокинов с использованием набора мышиных цитокинов (32-plex панель).
Статистический анализ
Анализ данных проводили с использованием программного обеспечения SAS 9.3 (SAS, Inc; Cary, NC). Для экспериментов с повторными измерениями данные анализировали моделью смешанных эффектов, включающей наблюдательные зависимости по каждому субъекту. Для других экспериментов, включающих независимые группы, данные анализировали посредством ANOVA. Для экспериментов типа время-до-события (фиг. 2B), различия в функциях выживаемости сравнивали посредством логарифмического рангового критерия. Множества уравновешивали методом Холмса для регуляции общей групповой вероятности ошибки при 0,05. Данные RNA-seq анализировали с использованием программного обеспечения Ingenuity Pathway Analysis (IPA) (Ingenuity Systems, Redwood City, CA). Только гены с >4-кратным изменением и P<0,05 выбирали для анализа пути.
Пример 3
AR-42 подавляет раковую кахексию в модели аденокарциномы ободочной кишки C-26
В одном аспекте мышей лечили перорально через зонд AR-42 (50 мг/кг) или носителем через день, начиная через 6 дней после инъекции клеток C-26, когда образовывались пальпируемые опухоли. Тогда как группа носителя показала большое снижение массы тела, начиная с 12 дня, мыши, получавшие AR-42, сохраняли свою массу на уровне, сравнимом с таковой контроля без опухолей (фиг. 1A, слева). К конечной точке исследования (день 15), величина потери массы, после вычитания массы опухолей (1 см3 объем=1 грамм массы), достигала >20% для группы, получавшей носитель, и 6% для мышей, получавших AR-42 (центр). Такой эффект не мог быть обусловлен снижением опухолевой нагрузки, так как AR-42 не изменял рост опухоли относительно носителя (справа), или увеличением потребления пищи, так как среднее суточное потребление пищи было сравнимо в группах, получавших AR-42 и носитель, и меньше, чем таковое у мышей без опухоли (фиг. 1C). Мыши, получавшие AR-42, несмотря на большую опухолевую нагрузку, были живыми, реагирующими, активными, не сутулились и не имели неровного шерстяного покрова, наблюдаемых у сородичей, получавших носитель, в конечной точке настоящего исследования (фиг. 1B).
Пример 4
AR-42 защищает мышцы от атрофии, индуцированной кахексией
В соответствии с сохранением массы тела, масса скелетных мышц сохранялась у мышей с опухолями, получавших AR-42. Показательно для кахексии, масса икроножных, передних большеберцовых и четырехглавых мышц от мышей с опухолями, получающих носитель (с опухолями/носитель) мышей снижалась на 20,6%, 10,5%, и 18,1%, соответственно, относительно соответствующих мышц от контрольных мышей без опухолей, тогда как таковые у мышей с опухолями, получавшими AR-42, (с опухолями/AR-42) мышами снижались на 9,6%, 0,8%, и 5,8%, соответственно (фиг. 1D).
Мыши с опухолями/носитель проявляли все признаки кахексии, включая значительную потерю массы сердечной и, особенно, жировой ткани (29,3±6,0% контроля без опухолей), что облегчалось лечением AR-42 (фиг. 1E, вверху). Интересно, AR-42 достоверно снижал массу жировой ткани на, приблизительно, 50% у мышей без опухолей, также восстанавливая потерю массы жировой ткани у мышей с опухолями до уровня, совместимого с таковым мышей без опухолей/AR-42, дихотомический эффект предполагает его способность поддерживать гомеостаз липидов.
В другом аспекте мыши с опухолями C-26 имели существенно увеличенные селезенки, относительно контрольных мышей без опухолей (11), которые не улучшались AR-42 (фиг. 1E, внизу). Так как спленомегалия у мышей с опухолями C-26 возникала в результате экспансии супрессорных клеток миелоидного происхождения и других иммунных клеток в селезенке (12), такое открытие предполагает, что AR-42 действовал скорее на мышцы, чем через иммунологический механизм.
Защитный эффект AR-42 от потери мышц проявлялся устранением индуцированного кахексией уменьшения размера волокон скелетных мышц. Мыши с опухолями/носитель проявляли снижение на 48,2% относительно контроля без опухолей по средней площади сечения мышечных волокон в день 15 (1297,6±638,8 по сравнению с 2503,5±917,5 мкм2), которое восстанавливалось AR-42 (2146,3±923,4 мкм2)(фиг. 2A, слева). Заметный сдвиг в распределении размера волокон к меньшей площади поперечного сечения в кахектичных мышцах мышей с опухолями/носитель обращался посредством AR-42 (фиг. 2A, справа)
AR-42 удлиняет выживаемость мышей с опухолями C-26
Эффекты AR-42 сравнивали с другими ингибиторами НDAC (т.е., вориностатом и ромидепсином) у мышей с опухолями C-26. Начиная с 6 дня после инъекции опухолевых клеток, мышей лечили длительно AR-42 (50 мг/кг через день, перорально), вориностатом [50 мг/кг один раз в сутки, перорально (13)], ромидепсином [0,6 мг/кг два раза в неделю, и.п. (14)], или носителем, до потери массы, что определяли посредством ежедневного определения массы тела и вычитания массы опухоли, достигающего 20% исходной массы. Как показано, пероральный AR-42 был эффективен в защите указанных мышей от исхудания, ассоциированного с опухолью, с 100% кумулятивной выживаемостью в день 21, когда объем опухоли достигал порога для эвтаназии (фиг. 2B). Наоборот, вориностат и ромидепсин показали ограниченный или не показали заметного эффекта на массу тела. Более того, мыши с опухолями/AR-42 были оживленными, отвечающими, активными и казались здоровыми через 21 день после инъекции опухолевых клеток, в противоположность мышам, которым вводили носитель (день 15), ромидепсин (день 16), и вориностат (день 18)(фиг. 2C).
Пример 3
Различные эффекты на регуляцию обмена белка скелетных мышц
Масса скелетных мышц регулируется балансом между синтезом и разрушением белка. Без связи с теорией, считают, что различные анти-кахектические эффекты AR-42 по сравнению с вориностатом и ромидепсином могут быть обусловлены различиями в их способности регулировать пути, управляющие обменом белка. Это поддерживается супрессивным эффектом AR-42 на экспрессию мРНК атрогин-1/MAFbx и, MuRFl, двух E3 лигаз, вовлеченных в разрушение белка скелетных мышц, опосредованного убиквитином (15, 16) (фиг. 2D).
кПЦР анализ икроножных мышц выявил достоверное увеличение уровня мРНК атрогин-1 и MuRFl (29,4±3,5-кратно и 25,8±3,9-кратно, соответственно) в кахектичных мышцах (с опухолями/носитель; n=8) относительно контроля без опухолей/носитель (n=6). AR-42 оказался способным восстанавливать экспрессию мРНК Атрогин-1 (2,7±0,7-кратно) и MuRF1 (1,1±0,2-кратно) до базальных уровней (n=8). Вориностат (n=8) и ромидепсин (n=5) также достоверно снижали экспрессию мРНК указанных двух E3 лигаз в кахектичных мышцах, но в меньшей степени, чем AR-42 (атрогин-l/MuRFl: вориностат, 9,6±1,8/5,5±1,1-кратно; ромидепсин, 19,6±3,l/14,6±3,3-кратно)(фиг. 2D).
Для подтверждения того, что анти-кахектическая активность AR-42 была неспецифической для модели C-26, ее также оценивали в модели LLC. Мышей с опухолями C57BL/6, несущих подкожные опухоли LLC, лечили AR-42 (50 мг/кг п.о, через день), начиная на 6 день после инъекции опухолевых клеток, и продолжали до 20 дня, когда мышцы передних конечностей получали при умерщвлении. Как показано на фиг. 7, AR-42 защищал мышей C57B1/6 с опухолями LLC от потери мышечной массы (икроножная: носитель, 81,7±3,7% некахектичного контроля; AR-42, 92,2±3,5%; передняя большеберцовая: носитель, 80,3±4,0%; AR-42, 93,4±3,9%; четырехглавая: носитель, 84,4±4,6%; AR-42, 93,4±4,8%; все значения P <0,05, n=8).
Пример 4
AR-42 поддерживает метаболическую целостность мышц у мышей с опухолями
При кахексии скелетные мышцы подвергаются комплексным метаболическим изменениям в ответ на воспалительные и нейроэндокринные стрессовые факторы опухоли и организма-хозяина (1). Соответственно, авторы провели анализ метаболического профиля для исследования эффекта AR-42 на индуцированные кахексией сдвиги в метаболическом фенотипе скелетных мышц. Мышей без опухолей и с опухолями C-26 лечили носителем или AR-42, как упомянуто выше, и икроножные мышцы забирали на 17 день для метаболомного анализа. Сравнение биохимических профилей мышц среди четырех групп (n=8/группу) выявило способность AR-42 восстанавливать индуцированные кахексией метаболические изменения в скелетных мышцах, которые суммированы далее.
Гликолиз. Кахектичные мышцы от мышей с опухолями/носитель показали достоверно более низкие уровни глюкозы и ключевых промежуточных продуктов гликолиза, чем контроль без опухоли (фиг. 3A). AR-42 обращал указанные метаболические изменения, восстанавливая внутримышечный уровень глюкозы и промежуточных продуктов до, в некоторых случаях, и выше исходного уровня, определяемого у мышей без опухолей/носитель. Более того, повышенная глюкоза уходила в биосинтез сорбита-фруктозы и пентозофосфатный путь, приводя к повышенной продукции сорбита, фруктозы и рибозы, метаболита, происходящего из пентозофосфатного пути.
Запасы гликогена. Мышцы от мышей с опухолями/носитель показали достоверное снижение короткоцепочечных мальто-олигосахаридов и глюкозо-1-фосфата (фиг. 3B), предполагая истощение запасов гликогена в кахектичных мышцах. Лечение AR-42 достоверно восполняло такие промежуточные продукты метаболизма гликогена.
Свободные аминокислоты. В соответствии с повышенным разрушением белка, что характеризует потерю мышц, большое количество свободных аминокислот было достоверно повышено в кахектичных мышцах от мышей с опухолями/носитель, относительно такового у мышей без опухолей/носитель (фиг. 4), демонстрируя кахектический фенотип. Сходным образом несколько производных/метаболитов аминокислот, которые действуют как нейтротрансмиттеры, включая кинуренин, N-ацетил-аспартилглютамат и γ-аминобутират, были повышены. Наоборот, аланин, который высвобождается из мышц для поддержания глюконеогенеза печени, снижался в кахектичных мышцах. Такой кахектичный фенотип обращался лечением AR-42, показывая его способность блокировать деградацию мышечного белка.
Органические кислоты. Метаболиты аминокислот 2-гидроксибутират и офтальмат являются биомаркерами инсулинорезистентности (17) и окислительного стресса (18), соответственно. Повышение двух указанных органических кислот в мышцах мышей с опухолями/носитель (фиг. 4), предполагает, что кахексия запускает инсулинорезистентность и окислительный стресс, которые, в свою очередь, усугубляют потерю мышц. AR-42 драматически снижал оба биомаркера до уровня, сравнимого с уровнями, сравнимыми с таковыми, измеряемыми у мышей без опухолей.
Пример 5
AR-42 подавляет раковую кахексию путем нацеливания на множество пусковых факторов про-кахексии
Чтобы осветить механизм, посредством которого AR-42 осуществляет свой противораковый эффект, сыворотку и икроножные мышцы от мышей без опухолей и с опухолями С-26, получавших носитель или AR-42, использовали для анализа профиля цитокинов и полного секвенирования короткого транскриптома (RNA-seq), соответственно.
Профили цитокинов. Из 32 исследуемых цитокинов (фиг. 10), IL-6 и фактор, ингибирующий лейкоз (LIF), два хорошо известных пусковых фактора кахексии (19), были достоверно повышены в сыворотке мышей с опухолями/носитель относительно таковой мышей без опухолей/носитель (IL-6; 230±105 относительно 2,9±1,3 пг/мл; LIF, 19,7±9,3 относительно 1,7±1,5 пг/мл) (Фиг. 5A, вверху), тогда как достоверные различия не были отмечены для других цитокинов. AR-42 снижал уровни IL-6 и LIF на 56% и 88%, соответственно, у мышей с опухолями (IL-6, 102±38 пг/мл; LIF, 3,8±1,6 пг/мл) по сравнению с другими, получавшими носитель. В свете способности AR-42 притуплять ассоциированное с кахексией повышение IL-6, авторы исследовали эффект AR-42 на внутримышечный уровень мРНК альфа цепи рецептора IL-6 (IL-6Rα). мРНК IL-6Rα была достоверно повышена (13±1,4-кратно) в мышцах мышей с опухолями/носитель (n=9) по сравнению с таковой у мышей без опухолей (n=6). AR-42 снижал такое индуцированное кахексией повышение на 85% (2,0±0,2-кратно; n=10) (фиг. 5, внизу). Такие открытия предполагают, что AR-42 ингибирует потерю мышц, отчасти, путем блокирования передачи сигнала IL-6.
Анализ RNA-seq. Анализ основных компонентов данных RNA-seq выявил заметный эффект опухоли C-26 на вариант глобальной экспрессии генов в мышцах мышей с опухолями/носитель относительно сородичей без опухолей/носитель (фиг. 5B, слева). Тогда как AR-42 не оказывал заметного эффекта на вариант экспрессии генов в некахектичных мышцах мышей без опухолей, он обращал индуцированный опухолью сдвиг экспрессии генов в кахектичных мышцах до состояния, близкого к таковому у мышей без опухолей. В соответствии с этим, авторы проводили попарный анализ дифференциально экспрессируемых генов между мышами с опухолями/носитель и другими тремя группами лечения, результаты чего представлены в диаграмме Venn (фиг. 5B, справа). Широко перекрывающиеся площади между парными анализами предполагают, что AR-42 восстанавливает, в большой степени, индуцированные опухолью изменения в глобальной экспрессии генов.
Попарное сравнение экспрессии генов в мышцах от мышей с опухолями, получавшими носитель и AR-42, выявил всего 677 генов с 4-кратно или большей дифференциальной экспрессией (376 стимулированных и 301 подавленных) (фиг. 10). Анализ таких геномных данных в отношении их функциональных и патологических ассоциаций с использованием Ingenuity Pathway Analysis (IPA) выявил, что 66 из таких дифференциально экспрессируемых генов были приписаны к категориям атрофии, сократимости, развития и мышечной морфологии и размеру клеток скелетных мышц, смерти мышечных клеток и катаболизма белка (фиг. 11).
Из таких генов, ассоциированных с мышечной функцией и патологиями, эффекты AR-42 на следующие шесть генов были заметными в свете их продемонстрированной связи с кахексией, индуцированной раком. Они включают Foxo1 (кодирующий трансформаторный белок Forkhead 01) (20-23) и его гены мишени Trim63 (MuRFl) и Fbxo32 (Атрогин-1) (24, 25), PNPLA2 [адипоз триглицерид липазу (ATGL)] (26, 27), UCP3 (несвязывающий белок 3) (28, 29), и Mef2c [фактор усиления миогенной транскрипции фактора миоцитов] (30) (фиг. 5C). Подтверждение данных RNA-seq для указанных шести генов посредством кОТ-ПЦР выявило высокую корреляцию между группами данных для относительных уровней экспрессии мРНК среди четырех групп лечения (фиг. 5D).
Пример 6
Отложенное лечение AR-42 остается эффективным в подавлении потери мышц
Вышеуказанные открытия демонстрируют эффективность перорального AR-42 в подавлении потери мышц, ассоциированной с раком, путем восстановления метаболических профилей и профилей генной экспрессии в скелетных мышцах. В проведенных экспериментах лечение начинали рано при прогрессировании кахексии, когда явные признаки потери были неопределимы. Для исследования, остается ли более позднее начало лечения AR-42 защитным от кахексии, мышей с опухолями C-26 лечили AR-42 (50 мг/кг, п.о., через день), начиная через 6, 10 и 12 дней после инъекции опухолевых клеток.
В соответствии с более ранними данными (фиг. 1), мыши с опухолями/носителем теряли 19% массы тела (за исключением опухоли) к 17 дню. Наоборот, лечение AR-42, начиная с 6 дня (D6), 10 (D10), или 12 (D12) ограничивало потерю массы до 6%, 11%, и 12%, соответственно (n=8) (фиг. 6A, слева), без заметных эффектов на рост опухоли (справа). Более того, мыши, получавшие AR-42, проявляли признаки лучшего состояния здоровья, чем их сородичи, получавшие носитель (фиг. 6B). Такой защитный эффект AR-42 отражался в сохранении массы икроножной мышцы и в меньшей степени, таковой передней большеберцовой и четырехглавой мышц (фиг. 6C). В соответствии с защитным эффектом на мышечную массу, ручной динамометр показал, что AR-42 помогал сохранять мышечную силу передних конечностей относительно контроля, получавшего носитель в дни 15 и 16 (фиг. 6D).
Пример 7
Мыши с опухолями/носитель проявляли другие признаки кахексии, включая достоверную потерю массы сердечной и, особенно жировой ткани (29,3±6,0% контроля без опухоли), что облегчалось лечением AR-42 (фиг. 1E, вверху). Интересно, AR-42 достоверно снижал массу жировой ткани на приблизительно 50% у мышей без опухолей, все еще восстанавливая потерю массы жировой ткани у мышей с опухолями до уровня, сравнимого с таковым мышей без опухолей/AR-42, двойной эффект предполагает его способность поддерживать гомеостаз липидов.
Мыши с опухолями C-26 имели крайне увеличенные селезенки относительно контрольных мышей без опухолей (11), что не улучшалось AR-42 (фиг. 1E, снизу). Так как спленомегалия у мышей с опухолями C-26 возникала в результате экспансии миелоидных супрессорных клеток и других иммунных клеток в селезенке (12), такое открытие предполагает, что AR-42 действует преимущественно на мышцы, скорее, чем посредством иммунологического метаболизма.
Защитный эффект AR-42 против потери мышц проявлялся в виде устранения индуцированного кахексией уменьшения размера волокон скелетных мышц. Мыши с опухолями/носитель проявляли 48,2% снижение относительно контроля без опухолей по средней площади поперечного сечения мышечных волокон в день 15 (1297,6±638,8 относительно 2503,5±917,5 мкм2), которое восстанавливалось посредством AR-42 (2146,3±923,4 мкм2) (фиг. 2A, слева). Заметный сдвиг распределения размера волокон до меньшей площади поперечного сечения в кахектичных мышцах мышей с опухолями/носитель обращали посредством AR-42 (фиг. 2A, справа).
Пример 8
Дифференциальные эффекты на регуляцию обмена белка скелетных мышц
Поскольку масса скелетных мышц регулируется балансом между синтезом и разрушением белка, дифференциальный антикахектический эффект AR-42 относительно вориностата и ромидепсина может быть обусловлен различиями в их способности регулировать пути, управляющие обменом белка. Это поддерживалось супрессивным Атрогин-1/MAFbx и, MuRFl, двух лигаз E3, вовлеченных и убиквитин-опосредованную деградацию белка скелетных мышц (15, 16) (фиг. 2D). Как ожидали, кПЦР анализ икроножных мышц выявил достоверное увеличение уровня Атрогин-1 и MuRFl (с опухолями/носитель; n=8) относительно контроля без опухолей/носитель (n=6). AR-42 оказался способен восстанавливать экспрессию атрогин-1 (2,7±0,7-кратно) и MuRFl (1,1±0,2-кратно) мРНК до базального уровня (n=8). Вориностат (n=8) и ромидепсин (n=5) также достоверно снижали экспрессию мРНК указанных двух лигаз в кахектичных мышцах, но в меньшей степени, чем AR-42 (атрогин-1/MuRF1: вориностат, 9,6±1,8/5,5±1,1-кратно; ромидепсин, 19,6±3,1/14,6±3,3-кратно) (фиг. 2D).
Пример 9
Клетки
Культивируемые C-26 и LLC клетки выдерживали в эмбриональной бычьей сыворотке, (FBS)-дополненной (10%) RPMI 1640 среде и DMEM среде (Invitrogen, Carlsbad, CA), соответственно, при 37°C в увлажненном инкубаторе с 5% CО2. Для инъекции мышам для моделей раковой кахексии клетки собирали трипсинизацией, осаждали в FBS-дополненной культуральной среде и затем ресуспендировали в стерильном PBS в концентрации 5x106 клеток/мл.
Мыши
Мышей CD2F1 и C57BL/6 размещали по группам в условиях постоянного фотопериода (12-часов света/12-часов темноты), температуры и влажности с доступом к воде и стандартному питанию по потребности. Мышей коротко анестезировали (изофлуран, 3-4%) во время введения лекарственных средств (AR-42, вориностат, носитель) при помощи перорального зонда. Потребление пищи оценивали путем взвешивания пищи в каждой клетке ежедневно и деления суточного уменьшения пищи на количество мышей в клетке. Объем опухоли рассчитывали из измерений циркулем с использованием стандартной формулы (длина x ширина x π/6).
Измерение силы сжатия
Дли измерения силы сжатия передней лапы, каждую мышь держали за основание хвоста и опускали над прибором пока ее передние лапы не нажимали на педаль. Затем мышь аккуратно опускали горизонтально по прямой от измерителя силы до того как мышь выпускала кнопку, и записывали максимальную применяемую силу. Пять измерений получали для каждой мыши, и среднее обозначали как сила сжатия мыши.
Создание библиотеки RNA-seq и канала анализа данных
Качество РНК оценивали на биоанализаторе Agilent 2100 с использованием матрицы РНК и входящее общее количество РНК оценивали с использованием анализа РНК Agilent Qubit. Библиотеки транскриптомов получали с использованием набора для получения образцов РНК Illumina TruSeq V2. Полученные библиотеки оценивали в отношении качества и количества с использованием ДНК анализа Agilent Qubit и анализа PerkinElmer Labchip DNA GX, соответственно. Все библиотеки смешивали в равных пропорциях, генерируя пулы образцов, которые давали приблизительно 40 миллионов пропущенных считок фильтра, при секвенировании на секвенаторе Illumina HiSeq 2500. Исходные данные секвенирования от канала Illumina HiSeq CASAVA оценивали в отношении качества с использованием программного обеспечения FastQC, RNASeQC и RSeQC. Последующие анализы были следующими: чтения секвенирования демультиплексного пропускающего фильтра выравнивали с GRCm38/мм10 с использованием TopHat 2 (v2.0.7) RNAseq установка; CuffLinks 2 (c2.1.1) использовали для сборки выровненных чтений для обозначения гена UCSC мм10; CuffCompare и CuffMerge использовали для составления выровненных чтений в гены мм10 и сортировали собранные транскрипты в обозначение специального гена; CuffDiff использовали для сравнения дифференциальной экспрессии генов, ассоциированной с каждой группой лечения.
Пример 10
Для подтверждения, что антикахектическая активность AR-42 была неспецифичной для модели C-26, ее также оценивали в модели LLC. Мышей C57BL/6, несущих подкожные опухоли 11 LLC, лечили AR-42 (50 мг/кг п.о., через день), начиная с 6 дня после инъекции опухолевых клеток, и продолжая до 20 дня, когда получали мышцы задней лапы при умерщвлении.
Как показано на фиг. 7, AR-42 защищает от индуцированной раком потери мышц в мышиной модели кахексии LLC. Эффекты AR-42 относительно носителя на массу мышц задних конечностей, включая икроножную, переднюю большеберцовую и четырехглавую, у мышей без опухолей и с опухолями сравнивали с таковыми мышей с опухолями, получающими носитель. Мышей лечили тем же образом, как описано в фиг. 1A, за исключением того, что мышей умерщвляли в день 20 после инъекций опухолевых клеток. Данные представлены как среднее ±S.D. (n=8); (икроножная: носитель, 81,7±3,7% некахектичного контроля; AR-42, 92,2±3,5%; передняя большеберцовая: носитель, 80,3±4,0%; AR-42, 93,4±3,9%; четырехглавая: носитель, 84,4±4,6%; AR-42, 93,4±4,8%; все значения P <0,05, n=8).
ССЫЛКИ
1. Fearon KC, Glass DJ, Guttridge DC. Cancer cachexia: mediators, signaling, and metabolic pathways. Cell Metab 2012; 16: 153-66.
2. Tisdale MJ. Cachexia in cancer patients. Nat Rev Cancer 2002; 2:862-71.
3. von Haehling S, Anker SD. Cachexia as a major underestimated and unmet medical need: facts and numbers. J Cachexia Sarcopenia Muscle 2010; 1: 1-5.
4. Tisdale MJ. Mechanisms of cancer cachexia. Physiol Rev 2009;89: 381-410.
5. Lee SJ, Glass DJ. Treating cancer cachexia to treat cancer. Skelet Muscle 2011; 1: 2.
6. Maccio A, Madeddu C, Mantovani G. Current pharmacotherapy options for cancer anorexia and cachexia. Expert Opin Pharmacother 2012; 13: 2453-72.
7. Kulp SK, Chen CS, Wang DS, Chen CY, Chen CS. Antitumor effects of a novel phenylbutyrate -based histone deacetylase inhibitor, (S)-HDAC-42, in prostate cancer. Clin Cancer Res 2006; 12: 5199-206.
8. Lu YS, Kashida Y, Kulp SK, Wang YC, Wang D, Hung JH, et al. Efficacy of a novel histone deacetylase inhibitor in murine models of hepatocellular carcinoma. Hepatology 2007; 46: 1119-30.
9. Sargeant AM, Rengel RC, Kulp SK, Klein RD, Clinton SK, Wang YC, et al. OSU-HDAC42, a histone deacetylase inhibitor, blocks prostate tumor progression in the transgenic adenocarcinoma of the mouse prostate model. Cancer Res 2008; 68: 3999-4009.
10. Yang YT, Balch C, Kulp SK, Mand MR, Nephew KP, Chen CS. A rationally designed histone deacetylase inhibitor with distinct antitumor activity against ovarian cancer. Neoplasia 2009; 11: 552-63, 3 p following 63.
11. Acharyya S, Ladner KJ, Nelsen LL, Damrauer J, Reiser PJ, Swoap S, et al. Cancer cachexia is regulated by selective targeting of skeletal muscle gene products. J Clin Invest 2004; 114: 370-8.
12. Mundy-Bosse BL, Lesinski GB, Jaime-Ramirez AC, Benninger K, Khan M, Kuppusamy P, et al. Myeloid-derived suppressor cell inhibition of the IFN response in tumor-bearing mice. Cancer Res 2011; 71: 5101-10.
13. Lucas DM, Alinari L, West DA, Davis ME, Edwards RB, Johnson AJ, et al. The novel deacetylase inhibitor AR-42 demonstrates pre-clinical activity in B-cell malignancies in vitro and in vivo. PLoS One 2010; 5: el 0941.
14. Sasakawa Y, Naoe Y, Inoue T, Sasakawa T, Matsuo M, Manda T, et al. Effects of FK228, a novel histone deacetylase inhibitor, on human lymphoma U-937 cells in vitro and in vivo. Biochem Pharmacol 2002; 64: 1079-90.
15. Bodine SC, Latres E, Baumhueter S, Lai VK, Nunez L, Clarke BA, et al. Identification of ubiquitin ligases required for skeletal muscle atrophy. Science 2001; 294: 1704-8.
16. Lecker SH, Jagoe RT, Gilbert A, Gomes M, Baracos V, Bailey J, et al. Multiple types of skeletal muscle atrophy involve a common program of changes in gene expression. FASEB J 2004; 18: 39-51.
17. Gall WE, Beebe K, Lawton KA, Adam KP, Mitchell MW, Nakhle PJ, et al. alpha-hydroxybutyrate is an early biomarker of insulin resistance and glucose intolerance in a nondiabetic population. PLoS One 2010; 5: el0883.
18. Soga T, Baran R, Suematsu M, Ueno Y, Ikeda S, Sakurakawa T, et al. Differential metabolomics reveals ophthalmic acid as an oxidative stress biomarker indicating hepatic glutathione consumption. J Biol Chem 2006; 281: 16768-76.
19. Tisdale MJ. Biology of cachexia. J Natl Cancer Inst 1997; 89:1763-73.
20. Kamei Y, Miura S, Suzuki M, Kai Y, Mizukami J, Taniguchi T, et al. Skeletal muscle FOXOl (FKHR) transgenic mice have less skeletal muscle mass, down-regulated Type I (slow twitch/red muscle) fiber genes, and impaired glycemic control. J Biol Chem 2004; 279: 41114-23.
21. Reed SA, Sandesara PB, Senf SM, Judge AR. Inhibition of FoxO transcriptional activity prevents muscle fiber atrophy during cachexia and induces hypertrophy. FASEB J 2012; 26: 987-1000.
22. Beharry AW, Sandesara PB, Roberts BM, Ferreira LF, Senf SM, Judge AR. HDACl activates FoxO and is both sufficient and required for skeletal muscle atrophy. J Cell Sci 2014; 127: 1441-53.
23. Sandri M, Sandri C, Gilbert A, Skurk C, Calabria E, Picard A, et al. Foxo transcription factors induce the atrophy-related ubiquitin ligase atrogin-1 and cause skeletal muscle atrophy. Cell 2004; 117: 399-412.
24. Gumucio JP, Mendias CL. Atrogin-1, MuRF-1, and sarcopenia. Endocrine 2013; 43: 12-21.
25. Bonaldo P, Sandri M. Cellular and molecular mechanisms of muscle atrophy. Dis Model Mech 2013; 6: 25-39.
26. Das SK, Hoefler G. The role of triglyceride lipases in cancer associated cachexia. Trends Mol Med 2013; 19: 292-301.
27. Young SG, Zechner R. Biochemistry and pathophysiology of intravascular and intracellular lipolysis. Genes Dev 2013; 27: 459-84.
28. Collins P, Bing C, McCulloch P, Williams G. Muscle UCP-3 mRNA levels are elevated in weight loss associated with gastrointestinal adenocarcinoma in humans. Br J Cancer 2002; 86: 372-5.
29. Constantinou C, Fontes de Oliveira CC, Mintzopoulos D, Busquets S, He J, Kesarwani M, et al. Nuclear magnetic resonance in conjunction with functional genomics suggests mitochondrial dysfunction in a murine model of cancer cachexia. Int J Mol Med 2011; 27: 15-24.
30. Shum AM, Mahendradatta T, Taylor RJ, Painter AB, Moore MM, Tsoli M, et al. Disruption of MEF2C signaling and loss of sarcomeric and mitochondrial integrity in cancer-induced skeletal muscle wasting. Aging (Albany NY) 2012; 4: 133-43.
31. Sherry BA, Gelin J, Fong Y, Marano M, Wei H, Cerami A, et al. Anticachectin/tumor necrosis factor-alpha antibodies attenuate development of cachexia in tumor models. FASEB J 1989; 3: 1956-62.
32. Strassmann G, Fong M, Kenney JS, Jacob CO. Evidence for the involvement of interleukin 6 in experimental cancer cachexia. J Clin Invest 1992; 89: 1681-4.
33. Bonetto A, Penna F, Minero VG, Reffo P, Bonelli G, Baccino FM, et al. Deacetylase inhibitors modulate the myostatin/follistatin axis without improving cachexia in tumor-bearing mice. Curr Cancer Drug Targets 2009; 9: 608-16.
34. Alamdari N, Aversa Z, Castillero E, Hasselgren PO. Acetylation and deacetylation- novel factors in muscle wasting. Metabolism 2013; 62: 1-11.
35. Senf SM, Sandesara PB, Reed SA, Judge AR. p300 Acetyltransferase activity differentially regulates the localization and activity of the FOXO homologues in skeletal muscle. Am J Physiol Cell Physiol 2011; 300: C1490-501.
36. Black BL, Olson EN. Transcriptional control of muscle development by myocyte enhancer factor-2 (MEF2) proteins. Annu Rev Cell Dev Biol 1998; 14: 167-96.
37. Moore-Carrasco R, Garcia-Martinez C, Busquets S, Ametller E, Barreiro E, Lopez-Soriano FJ, et al. The AP-l/CJUN signaling cascade is involved in muscle differentiation: implications in muscle wasting during cancer cachexia. FEBS Lett 2006; 580: 691-6.
38. Der-Torossian H, Wysong A, Shadfar S, Willis MS, McDunn J, Couch ME. Metabolic derangements in the gastrocnemius and the effect of Compound A therapy in a murine model of cancer cachexia. J Cachexia Sarcopenia Muscle 2013; 4: 145-55.
39. Asp ML, Tian M, Wendel AA, Belury MA. Evidence for the contribution of insulin resistance to the development of cachexia in tumor-bearing mice. Int J Cancer 2010; 126: 756-63.
40. Honors MA, Kinzig KP. The role of insulin resistance in the development of muscle wasting during cancer cachexia. J Cachexia Sarcopenia Muscle 2012; 3: 5-11.
41. Moylan JS, Reid MB. Oxidative stress, chronic disease, and muscle wasting. Muscle Nerve 2007; 35: 411-29.
42. Chu PC, Kulp SK, Chen CS. Insulin-like growth factor-I receptor is suppressed through transcriptional repression and mRNA destabilization by a novel energy restriction-mimetic agent. Carcinogenesis 2013; 34: 2694-705.
Хотя вышеуказанное описание относится к определенным аспектам, необходимо понимать, что такие аспекты являются только иллюстративными. Специалисту в области техники очевидно, что различные модификации и вариации могут быть осуществлены с методами, описанными в настоящем описании. Следовательно, настоящее описание включает модификации и вариации, которые находятся в рамках приложенной формулы изобретения и их эквивалентов.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРИМЕНЕНИЕ АНТАГОНИСТОВ МИОСТАТИНА, СОДЕРЖАЩИЕ ИХ КОМБИНАЦИИ И ИХ ПРИМЕНЕНИЕ | 2016 |
|
RU2781401C2 |
| ЛЕЧЕНИЕ РАКА С ПОМОЩЬЮ АНТИТЕЛА К СЕМАФОРИНУ 4D В КОМБИНАЦИИ С ЭПИГЕНЕТИЧЕСКИМ МОДУЛИРУЮЩИМ АГЕНТОМ | 2018 |
|
RU2783535C2 |
| КОМБИНАЦИЯ ИНГИБИТОРА ГИСТОНДЕАЦЕТИЛАЗЫ И ИНГИБИТОРА ПРОТЕИНКИНАЗЫ И ЕЕ ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2019 |
|
RU2770754C1 |
| СПОСОБЫ ЛЕЧЕНИЯ РАКА С ПРИМЕНЕНИЕМ ИНГИБИТОРА АУТОФАГИИ НА ОСНОВЕ ТИОКСАНТОНА | 2011 |
|
RU2627588C2 |
| СПОСОБЫ ИНДУКЦИИ КОНЕЧНОЙ ДИФФЕРЕНЦИРОВКИ | 2010 |
|
RU2530648C2 |
| СПОСОБЫ ИНДУКЦИИ КОНЕЧНОЙ ДИФФЕРЕНЦИРОВКИ | 2003 |
|
RU2394022C2 |
| АНТИТЕЛО ПРОТИВ РЕЦЕПТОРА IGF-I | 2018 |
|
RU2785305C2 |
| ПРИМЕНЕНИЕ ПИТАТЕЛЬНОЙ КОМПОЗИЦИИ ДЛЯ УЛУЧШЕНИЯ МЫШЕЧНОЙ ФУНКЦИИ И СУТОЧНОЙ АКТИВНОСТИ | 2009 |
|
RU2636162C2 |
| ПИТАТЕЛЬНАЯ КОМПОЗИЦИЯ ДЛЯ УЛУЧШЕНИЯ МЫШЕЧНОЙ ФУНКЦИИ И СУТОЧНОЙ АКТИВНОСТИ | 2009 |
|
RU2506825C2 |
| ИНГИБИТОРЫ ГИСТОНДЕЗАЦЕТИЛАЗЫ ИЗ НОВЫХ ПРОИЗВОДНЫХ БЕНЗАМИДА С СИЛЬНОЙ ДИФФЕРЕНЦИРОВОЧНОЙ И АНТИПРОЛИФЕРАТИВНОЙ АКТИВНОСТЬЮ | 2004 |
|
RU2364589C2 |
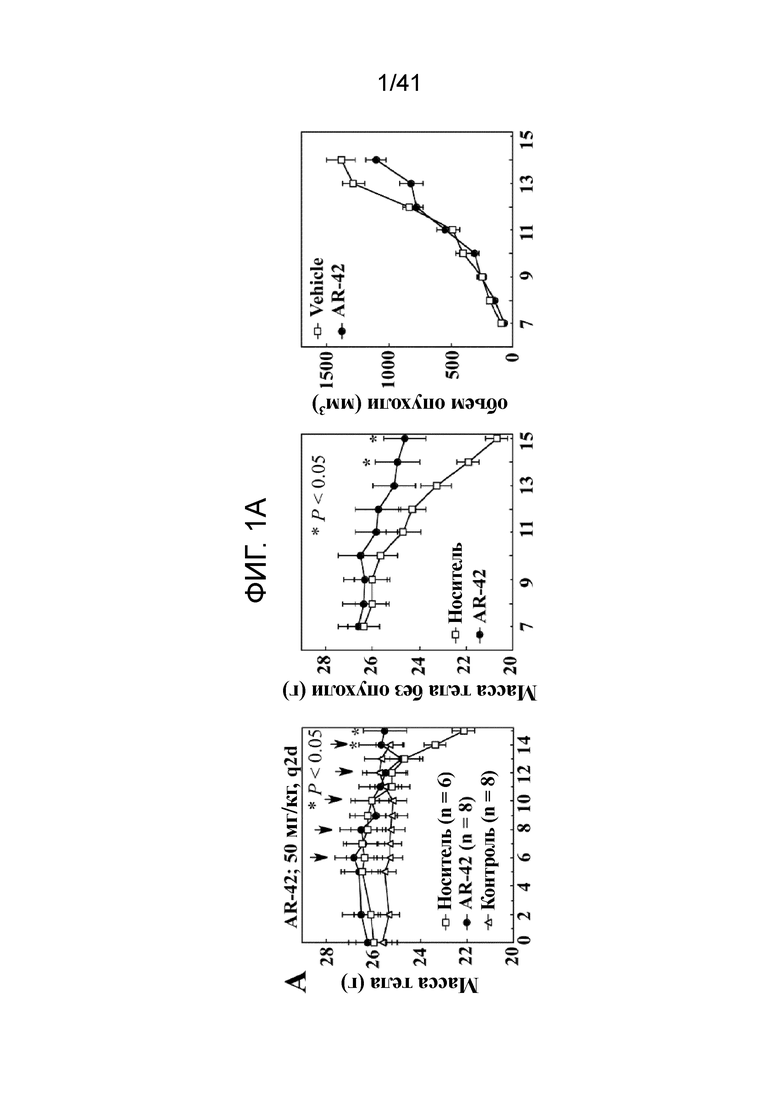
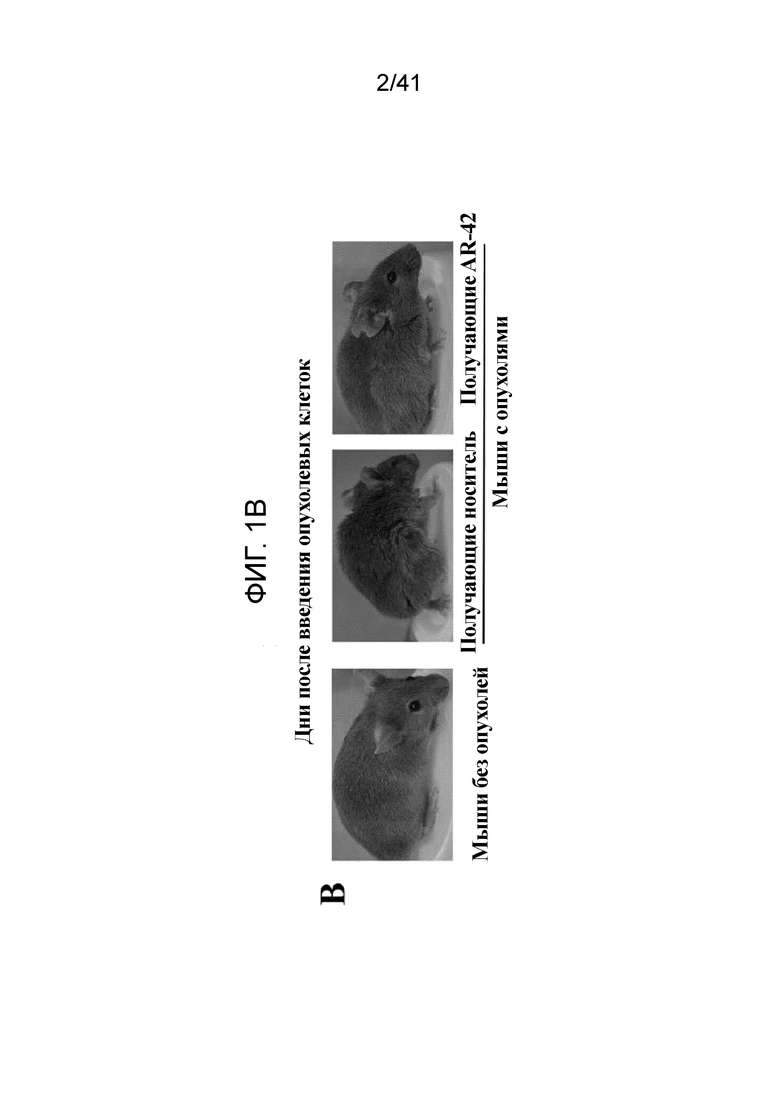

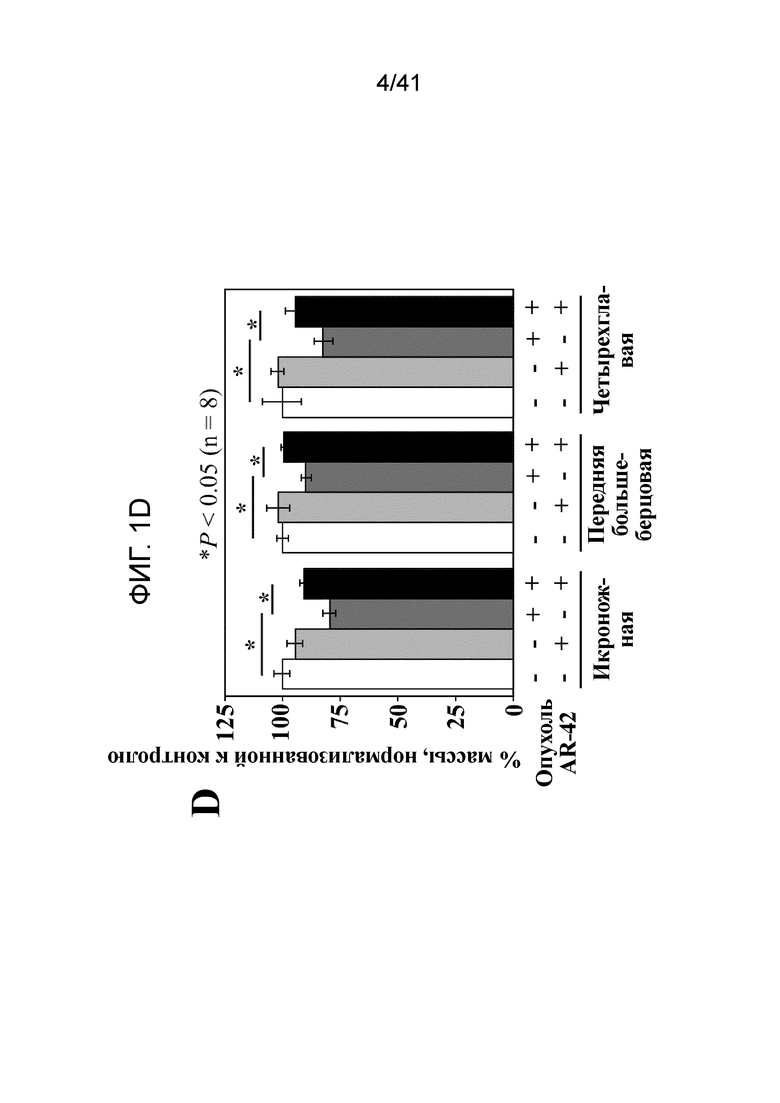

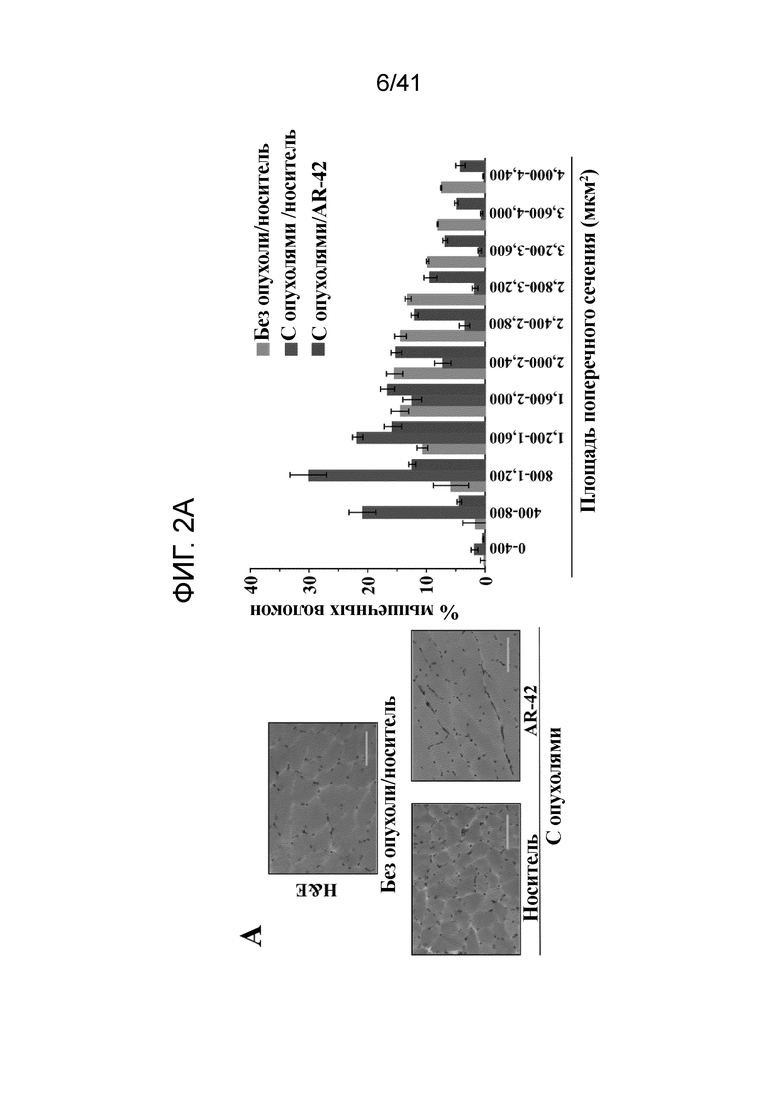

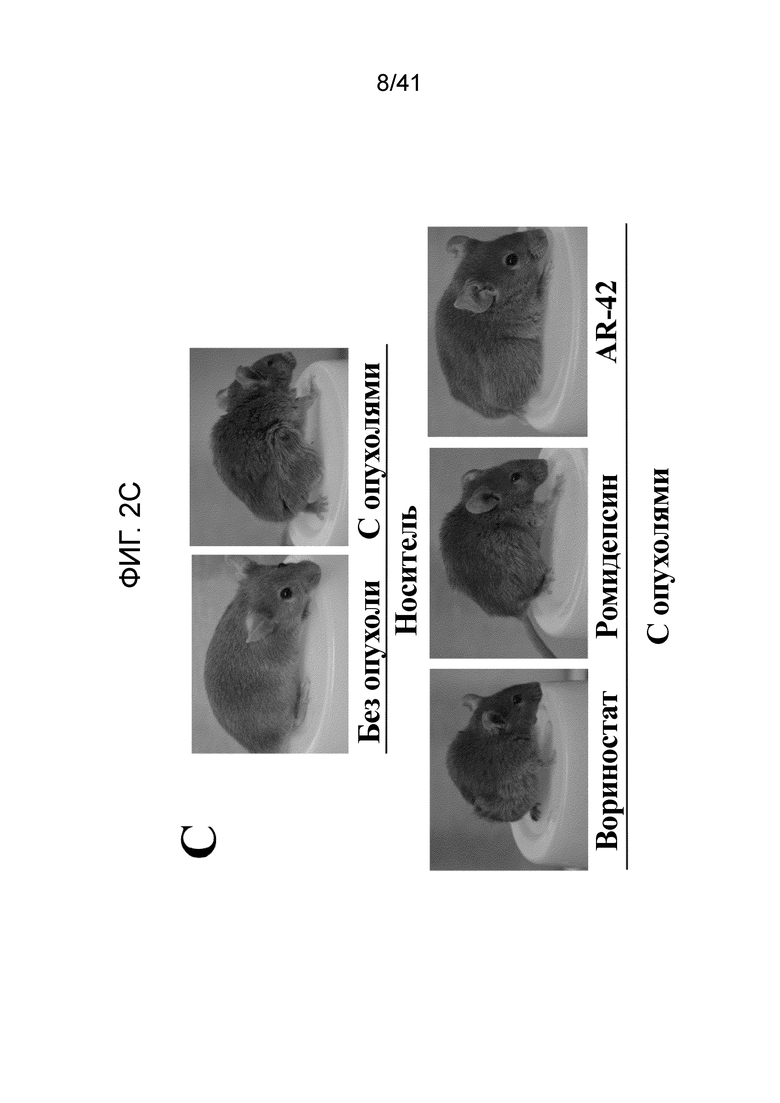
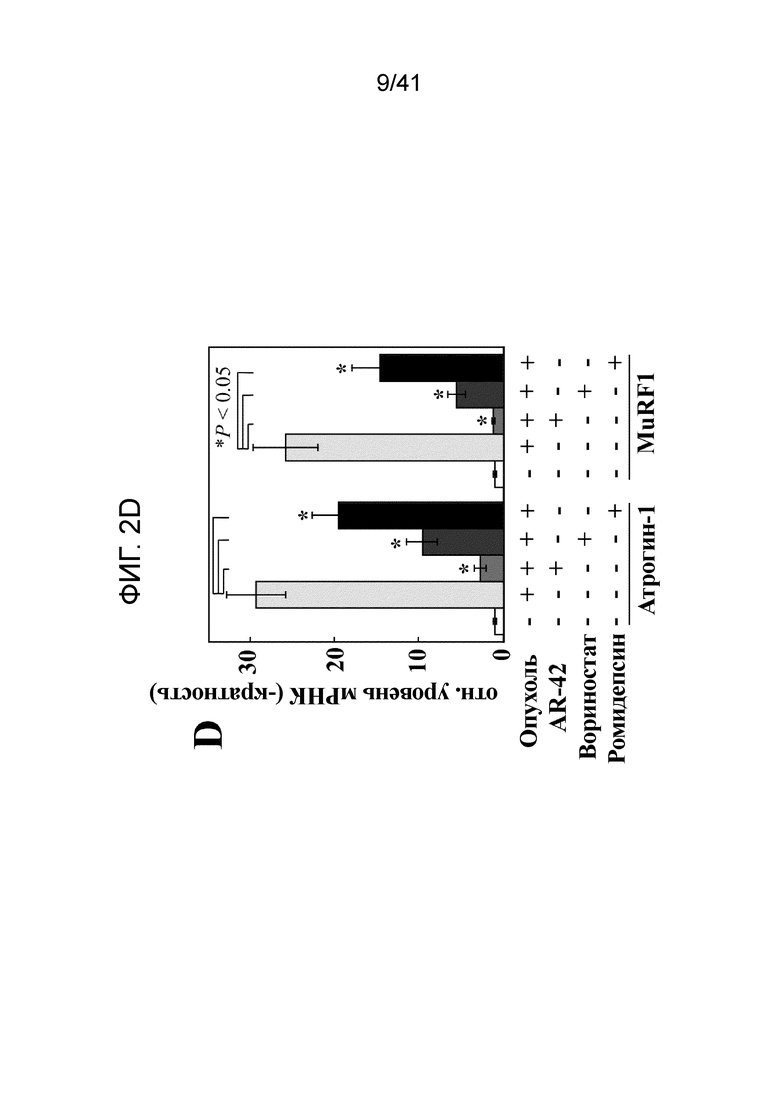
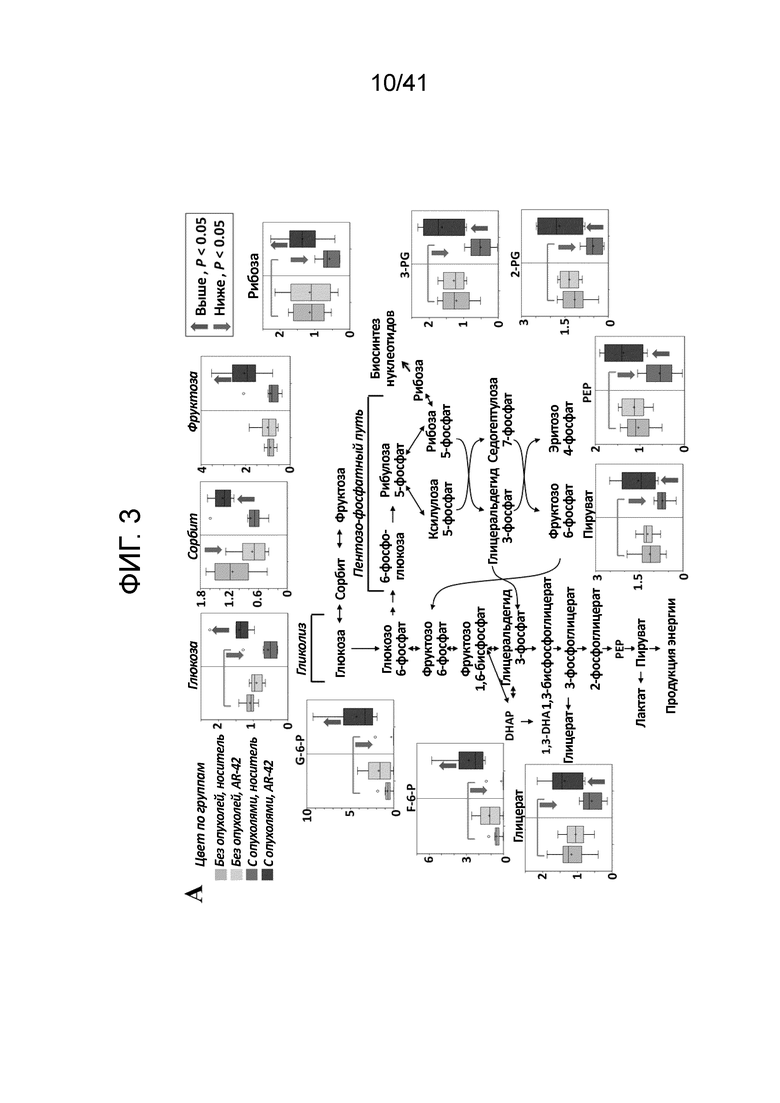
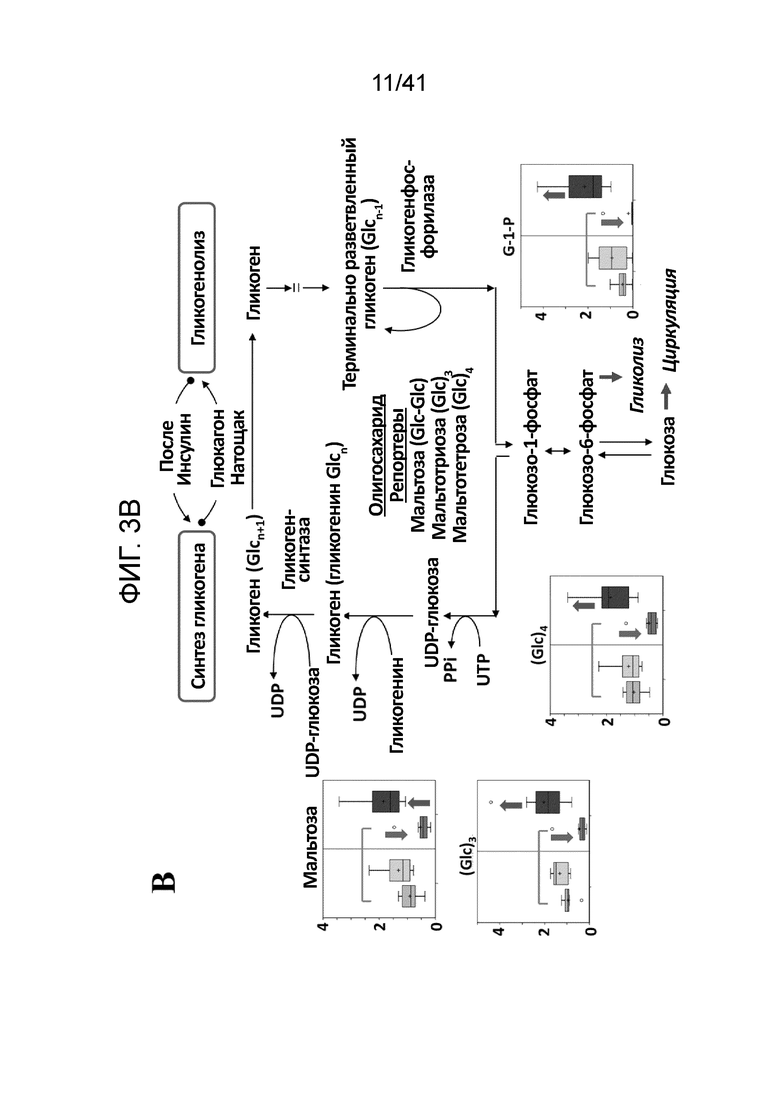
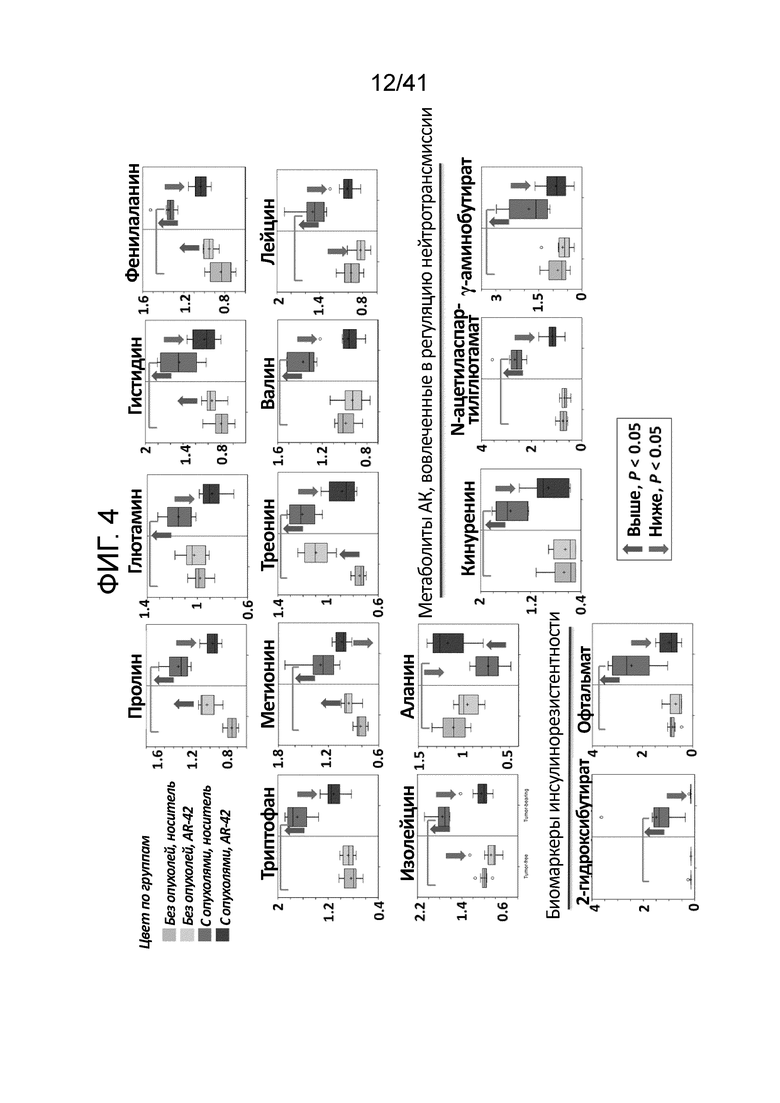
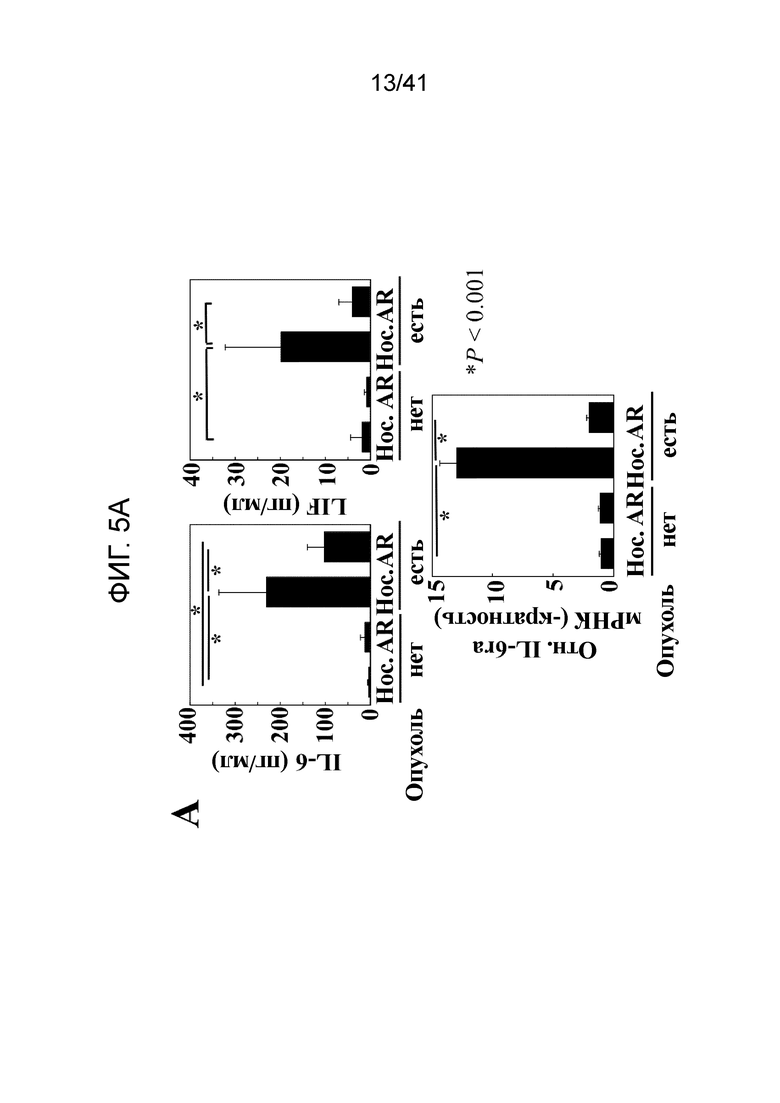
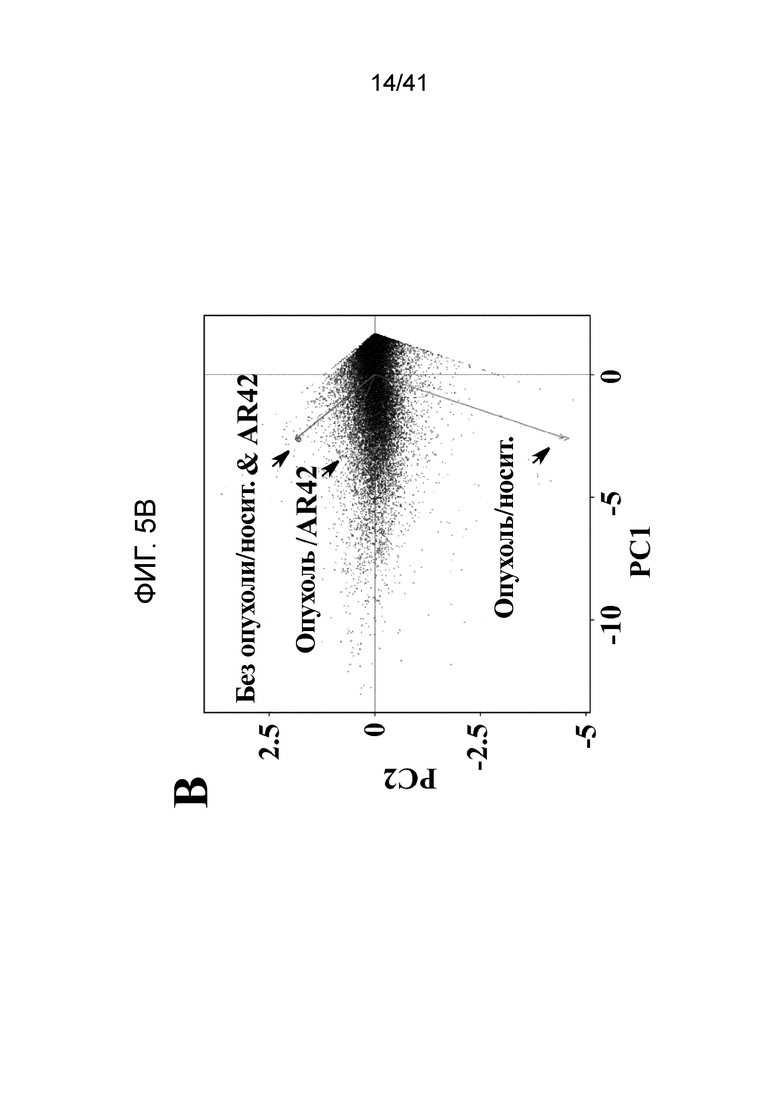
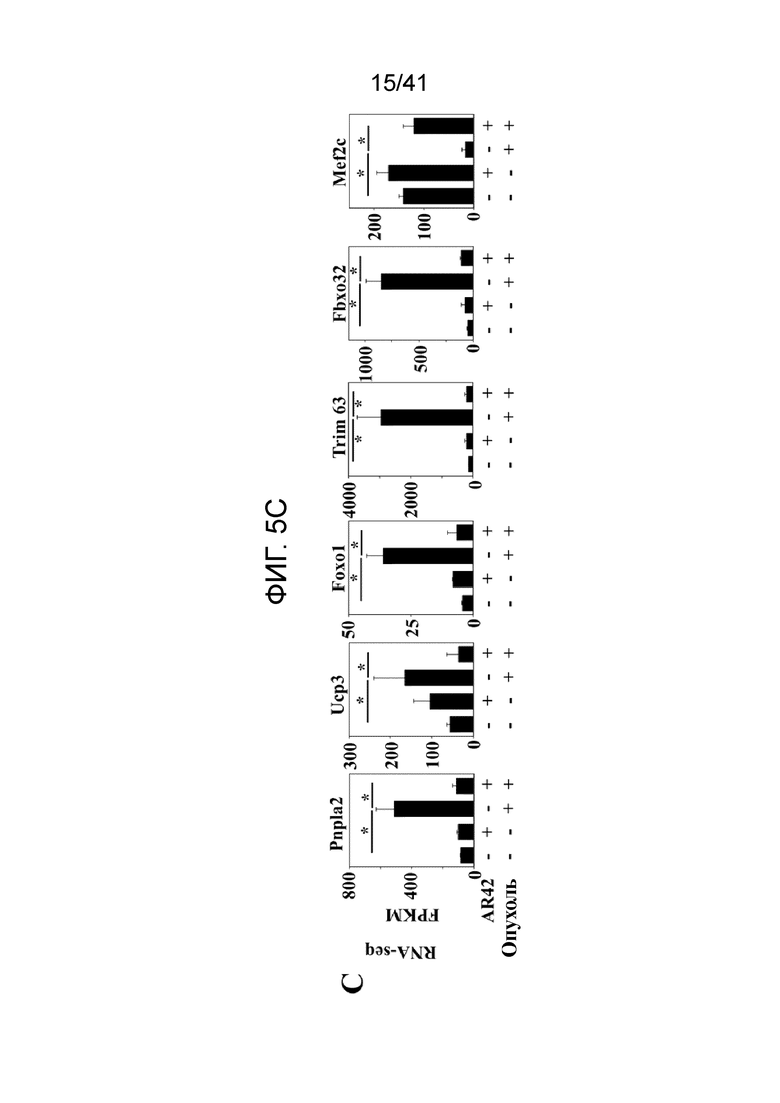

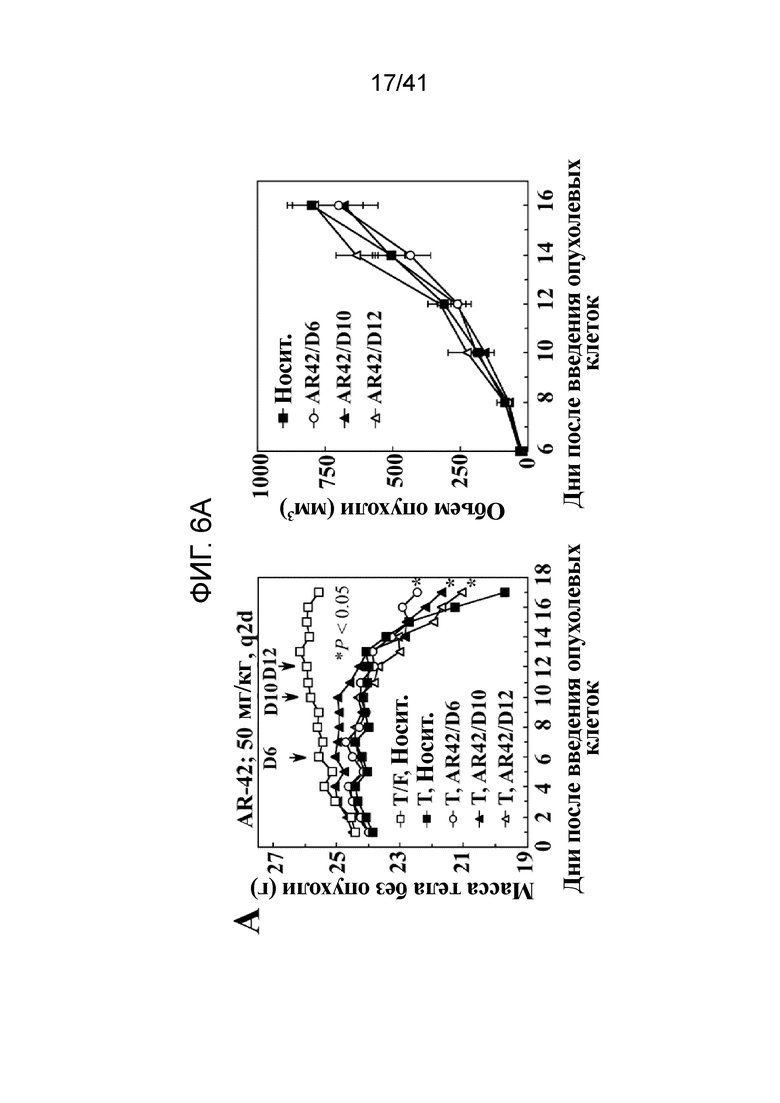
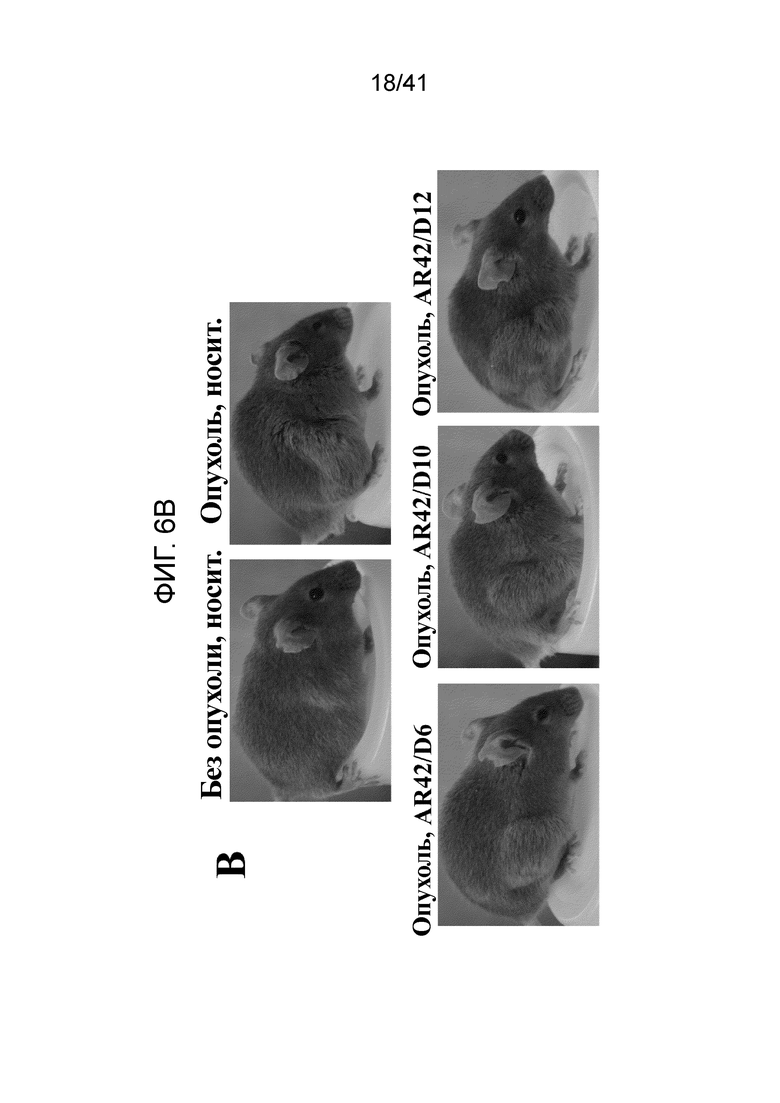
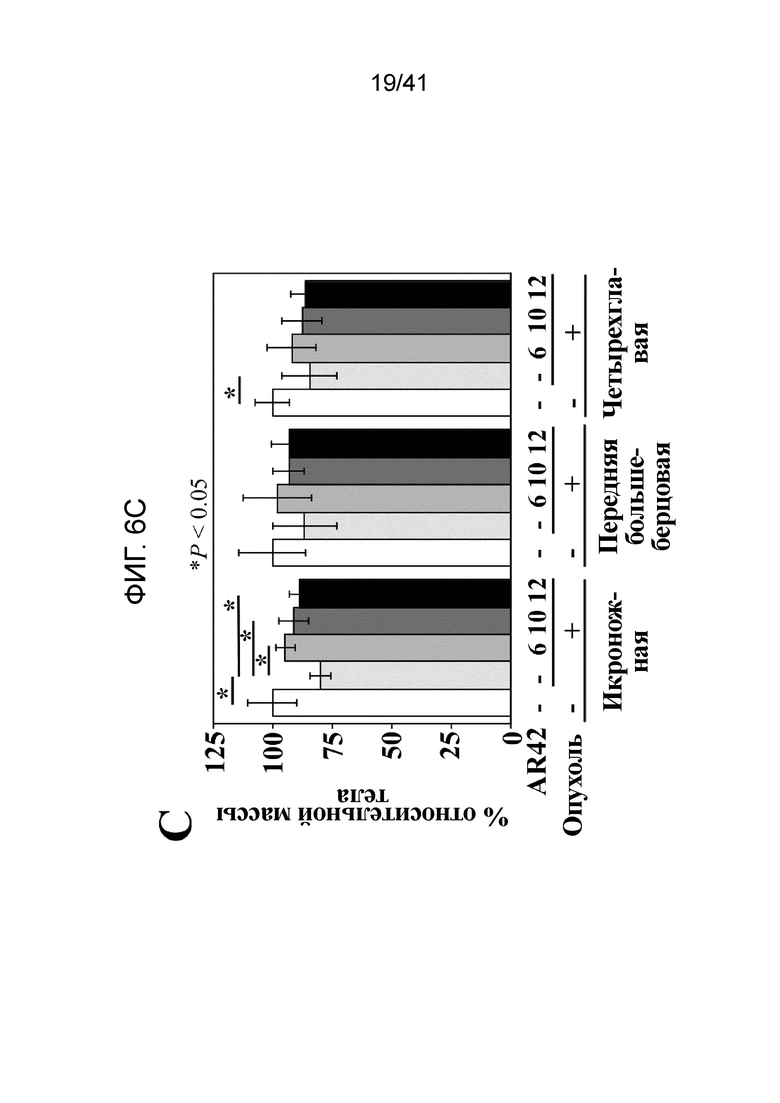
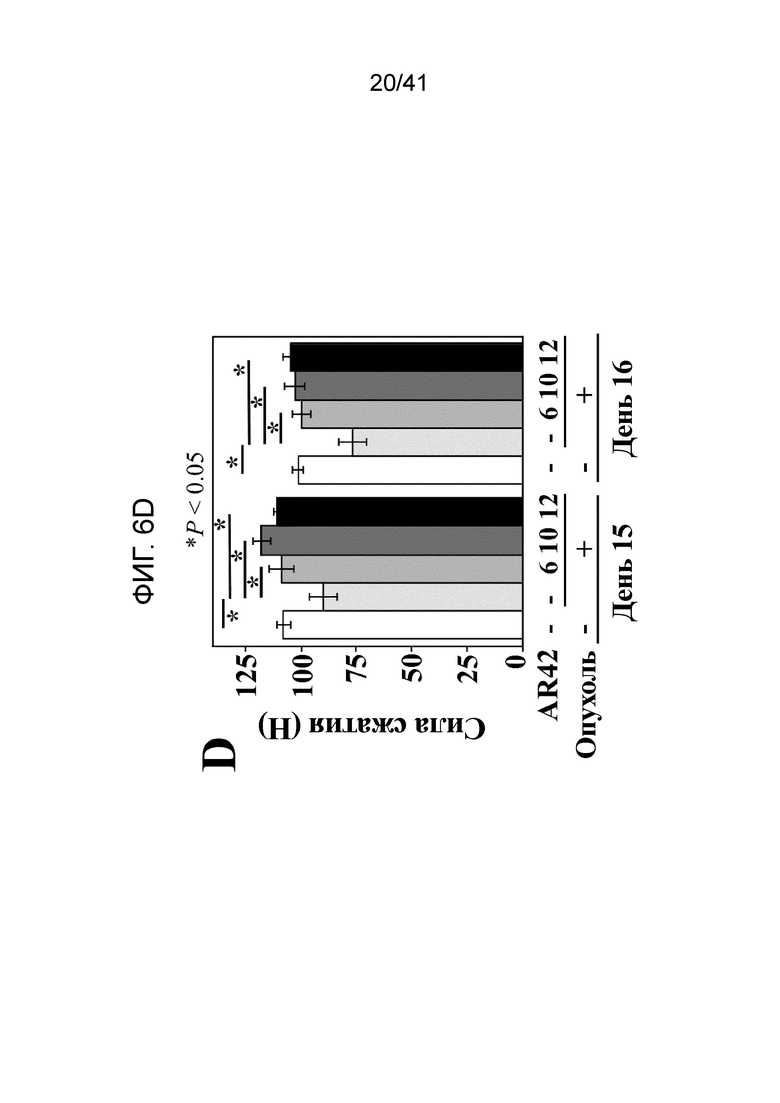




















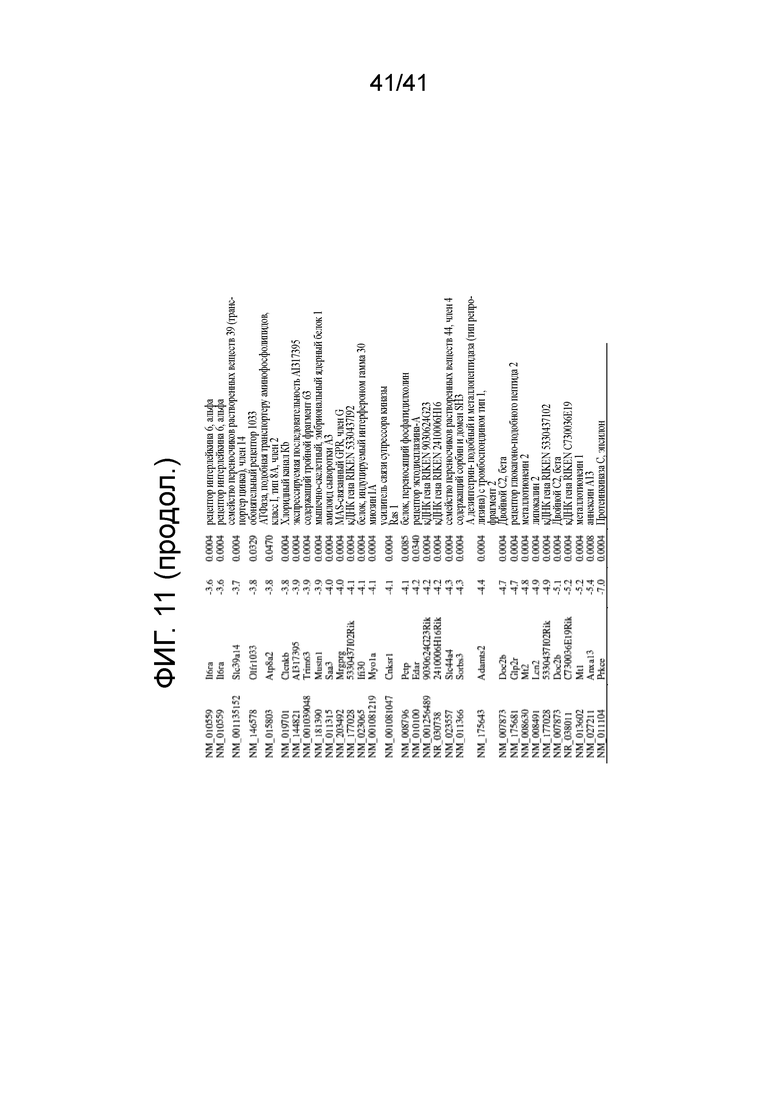
Группа изобретений относится к медицине и касается способа уменьшения индуцированной раком кахексии у млекопитающего, включающего введение ингибитора HDAC класса 1 и 2b указанному млекопитающему в количестве, эффективном для сохранения массы тела млекопитающего, по сравнению с млекопитающим, которое не получает ингибитор HDAC класса 1 и 2b. Группа изобретений также касается способа поддержания массы скелетных мышц у млекопитающего, имеющего рак, где масса скелетных мышц снижается вследствие рака, включающего введение ингибитора HDAC класса 1 и 2b указанному млекопитающему. Группа изобретений обеспечивает уменьшение индуцированной раком кахексии. 2 н. и 7 з.п. ф-лы, 10 пр., 11 ил.
1. Способ уменьшения индуцированной раком кахексии у млекопитающего, включающий введение ингибитора HDAC класса 1 и 2b указанному млекопитающему в количестве, эффективном для сохранения массы тела млекопитающего, по сравнению с млекопитающим, которое не получает ингибитор HDAC класса 1 и 2b.
2. Способ по п. 1, где ингибитором HDAC является AR-42.
3. Способ по п. 1, где рак выбирают из группы, состоящей из рака поджелудочной железы, ободочной кишки, головы, шеи, желудка и пищевода.
4. Способ по п. 1, где млекопитающим является человек.
5. Способ по п. 2, где AR-42 вводят в количестве от 1 мг/кг до 100 мг/кг млекопитающего.
6. Способ по п. 5, где AR-42 вводят, по меньшей мере, один раз в сутки.
7. Способ по п. 6, где AR-42 вводят два раза в сутки в количестве 50 мг/кг млекопитающего.
8. Способ поддержания массы скелетных мышц у млекопитающего, имеющего рак, где масса скелетных мышц снижается вследствие рака, включающий введение ингибитора HDAC класса 1 и 2b указанному млекопитающему.
9. Способ по п. 8, где ингибитором HDAC класса 1 и 2b является AR-42.
| US20060275370 A1, 07.12.2006 | |||
| WO2012009475 A1, 19.01.2012 | |||
| LEE SY., et al., Histone deacetylase inhibitor AR-42 enhances E7-specific CD8⁺ T cell-mediated antitumor immunity induced by therapeutic HPV DNA vaccination.J Mol Med (Berl) | |||
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
Авторы
Даты
2019-06-27—Публикация
2014-11-19—Подача