ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к новым 1,2,4-триазоло[4,3-a]пиридиновым соединениям в качестве положительных аллостерических модуляторов (PAM) метаботропных глутаматных рецепторов подтипа 2 ("mGluR2"). Настоящее изобретение также относится к фармацевтическим композициям, содержащим такие соединения, способам получения таких соединений и композиций и применению таких соединений и композиций для предупреждения или лечения расстройств, в которые вовлечены метаботропные рецепторы подтипа mGluR2.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Глутамат является основной нейромедиаторной аминокислотой в центральной нервной системе млекопитающих. Глутамат играет главную роль в многочисленных физиологических функциях, таких как обучение и память, а также сенсорная чувствительность, выработка синаптической пластичности, двигательный контроль, дыхание и регуляция функции сердечно-сосудистой системы. Кроме того, глутамат играет центральную роль в нескольких различных неврологических и психических заболеваниях, при которых имеет место нарушение глутаматергической нейротрансмиссии.
Глутамат опосредует синаптическую нейротрансмиссию посредством активации ионных каналов типа ионотропных глутаматных рецепторов (iGluR), а также NMDA-, AMPA- и каинатных рецепторов, отвечающих за быструю передачу возбуждения.
В дополнение, глутамат активирует метаботропные глутаматные рецепторы (mGluR), которые играют более модулирующую роль, способствующую тонкой настройке синаптической эффективности.
Глутамат активирует mGluR посредством связывания с крупным внеклеточным аминоконцевым доменом рецептора, называемым в данном документе ортостерическим участком связывания. Это связывание вызывает конформационное изменение рецептора, что приводит к активации G-белка и внутриклеточных сигнальных путей.
Рецепторы подтипа mGluR2 сопряжены с аденилатциклазой по принципу обратной связи посредством активации Gαi-белка, и их активация приводит к ингибированию высвобождения глутамата в синапсе. В центральной нервной системе (CNS) рецепторы mGlu2 широко распространены главным образом во всей коре головного мозга, в областях таламуса, дополнительной обонятельной луковице, гиппокампе, миндалевидном теле, дорсолатеральном отделе стриатума и прилежащем ядре.
В клинических испытаниях было показано, что активация mGluR2 является эффективной в лечении тревожных расстройств (что касается исследований ортостерических агонистов mGlu2/3, см. Michelson et al. Neuropharmacology 2005, 49(S1), 84-257; Dunayevich et al. Neuropsychopharmacology 2008, 33(7), 1603-10), LY354740 ранее оценивался в неклинических и клинических модельных системах, предсказывающих его полезность в лечении тревожных расстройств помимо генерализованной тревожной депрессии (GAD), например, панического расстройства (см., Dunayevich et al. 2008). Неклинические исследования позволяют предположить роль рецепторов как mGlu2, так и mGlu3 в анксиолизисе (Linden et al. Neuropharmacology 2005, 49, 120-134), хотя было выдвинуто предположение, что положительное аллостерическое модулирование mGluR2 может быть достаточным для анксиолитического эффекта (Johnson et al. Psychopharmacology (Berl) 2005, 179(1), 271-283).
В дополнение, было показано, что активация mGluR2 является потенциально эффективной для лечения
(a) шизофрении (Patil et al. Nat Med 2007, 13(9), 1102-7); более поздние исследования, однако, не подтверждают лечения острых приступов шизофрении с помощью агониста или аллостерического модулятора mGluR2 (Adams et al. BMC Psychiatry 2013, 13(1), 143; Kinon et al. J Clin Psychopharmacol. 2013, 31(3), 349-55; Litman et al. (2013) конференция NCDEU (реферат)), но не исключают применение в отношении других конкретных симптомокомплексов (например, негативных симптомов (Kent et al. "Safety, tolerability and potential therapeutic efficacy of a novel glutamate modulator as adjunctive treatment in patients with schizophrenia" реферат № 3160 и стендовый доклад NR10-47, 166-я ежегодная конференция Американской ассоциации психиатров 2013 г. (APA 2013), 18-22 мая 2013 г., Сан-Франциско, Калифорния, США)) или в отношении других фаз заболевания (например, остаточных симптомов);
(b) эпилепсии - на основании неклинических исследований непосредственных эффектов в отношении комбинированных агонистов рецепторов mGlu2/3 (Moldrich et al. Eur J Pharmacol. 2003, 476, 3-16; Barton et al. Epilepsy Research 2003, 56, 17-26); продолжительное введение агониста mGlu2/3 парадоксальным образом вызывало судорожную активность в долгосрочных токсикологических исследованиях (Dunayevich et al. (2008), этот парадоксальный эффект может быть связан с вызываемыми агонистами изменениями чувствительности рецепторных систем (тахифилаксии); положительные аллостерические модуляторы, напротив, модулируют существующую нейротрансмиссию, но не являются ее непосредственными стимуляторами, снижая, таким образом, риск развития тахифилаксии;
(c) наркомании/лекарственной зависимости (Barrett, Neuropsychopharmacology 2010, 35, 2007-2008; Foster, Curr Drug Abuse Rev 2009, 2, 83-98);
(d) болезни Паркинсона (см., например, Johnson et al. CNS Neurol Disord Drug Targets 2009, 8, 475-491; Konieczny et al. Naunyn Schmiedebergs Arch. Pharmacol. 1998, 358 (4), 500-502);
(e) боли (Chiechio и Nicoletti, Curr Opin Pharmacol 2012, 12, 28-34; Jones et al. Neuropharmacology 2005, 49, 206-218; Neugebauer, [Review] Pain 2002, 98 (1-2),
1-8; Simmons et al. Pharmacology, Biochemistry and Behavior 2002, 73, 419-427);
(f) нарушений сна (Ahnaou et al. European Journal of Pharmacology 2009, 603, 62-72);
(f) болезни Хантингтона (на основании потенциального болезнь-модифицирующего эффекта (Schiefer et al. Brain Res 2004, 1019, 246-254), подлежащего дополнительному подтверждению); и
(g) депрессии (хотя по первичному критерию эффективности не был выявлен сигнал эффективности, при дополнительном введении JNJ-40411813/ADX71149 в диапазоне доз, тестируемом в многоцентровом, двойном слепом, плацебо-контролируемом исследовании у взрослых с большим депрессивным расстройством с симптомами тревожности, были показаны сигналы эффективности по некоторым вторичным критериям эффективности как для депрессии, так и для тревожности (Kent et al. "Efficacy and Safety of a Novel mGlu2 Receptor Positive Allosteric Modulator as an Adjunctive Treatment to an SSRI/SNRI in the Treatment of Anxious Depression", реферат к стендовому и устному докладу, ежегодная конференция Американского общества клинической психофармакологии (ASCP) 2014 г., 16-19 июня 2014 г., Westin Diplomat, Холливуд, Флорида)).
Новой возможностью для разработки селективных соединений, действующих на mGluR, является идентификация соединений, действующих посредством аллостерических механизмов, модулируя рецепторы путем связывания с участком, отличным от высококонсервативного ортостерического участка связывания.
Недавно появились положительные аллостерические модуляторы mGluR в качестве новых фармакологических объектов, предлагающих эту привлекательную альтернативу.
Было продемонстрировано, что такие соединения сами по себе не активируют рецепторы. Скорее, они позволяют с помощью рецепторов вызывать усиленный ответ на концентрацию глутамата, которая сама по себе вызывает минимальный ответ. Мутационный анализ однозначно продемонстрировал, что связывание положительных аллостерических модуляторов mGluR2 происходит не по ортостерическому участку, а, вместо этого, по аллостерическому участку, расположенному в семиспиральной трансмембранной области рецептора.
Данные, полученные на животных, позволяют предположить, что положительные аллостерические модуляторы mGluR2 обладают эффектами в моделях тревожности и психоза, сходными с достигаемыми в случае ортостерических агонистов. Было показано, что аллостерические модуляторы mGluR2 являются активными в моделях тревожности c реакцией испуга, усиленной состоянием страха (Johnson et al. J Med Chem 2003, 46, 3189-3192; Johnson et al. Psychopharmacology 2005, 179, 271-283), и с гипертермией, вызванной стрессом (Johnson et al. 2005). Кроме того, было показано, что такие соединения являются активными в устранении гиперлокомоции, вызываемой кетамином (Govek et al. Bioorg Med Chem Lett 2005, 15(18), 4058-4072) или амфетамином (Galici et al. J Pharm Exp Ther 2005, 315(3), 1181-1187), и в устранении вызываемого амфетамином нарушения преимпульсного ингибирования эффекта акустической реакции испуга (Galici et al. 2005) в моделях шизофрении.
PAM mGlu2 JNJ-40411813/ADX71149 (который у крыс также проявляет активность антагонизма 5-HT2A, обусловленную образованием метаболита, специфического для крыс) подвергался клиническим испытаниям в отношении лечения шизофрении и тревожной депрессии (см., например, www. Clinicaltrials.gov). Данные неклинических исследований в модели паники, вызванной лактатом, у грызунов позволяют предположить, что он может обладать потенциалом при лечении дополнительных тревожных расстройств, таких как паническое расстройство и фобии, такие как агорафобия (Shekhar et al. Neuropsychopharmacology 2013, 38, S435-S593 (W220). Также наблюдали, что JNJ-40411813 снижает тягу и ослабляет вызываемые отказом от курения дефициты внимания и эпизодической памяти по сравнению с плацебо (Salih et al. Journal of Psychopharmacology, подано к публикации), а также демонстрирует сигнал эффективности относительно вызываемых S-кетамином негативных симптомов у здоровых добровольцев и пациентов с преобладающими негативными симптомами шизофрении (De Boer и соавт. Общество биологической психиатрии, 68-й ежегодный съезд ученых Общества биологической психиатрии, 16-18 мая 2013 г., Hilton Union Square, Сан-Франциско, Калифорния, реферат 2013-P-1060-SOBP).
Положительные аллостерические модуляторы обеспечивают усиление ответа на глутамат, но было показано, что они также усиливают ответ на ортостерические агонисты mGluR2, такие как LY379268 или DCG-IV. Эти данные подтверждают еще один новый терапевтический подход к лечению вышеупомянутых неврологических и психических заболеваний, в которые вовлечены mGluR2, в котором может применяться комбинация положительного аллостерического модулятора mGluR2 вместе с ортостерическим агонистом mGluR2.
Различные соединения были описаны как положительные аллостерические модуляторы mGluR2. В WO2010/130424, WO2010/130423, WO2010/130422, а также WO2012/062750, WO2012/062751 и WO2012/062759, опубликованных 18 ноября 2010 г. и 18 мая 2012 г., соответственно, раскрыты производные 1,2,4-триазоло[4,3-a]пиридина в качестве положительных аллостерических модуляторов mGluR2.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к производным 1,2,4-триазоло[4,3-a]пиридина формулы (I):
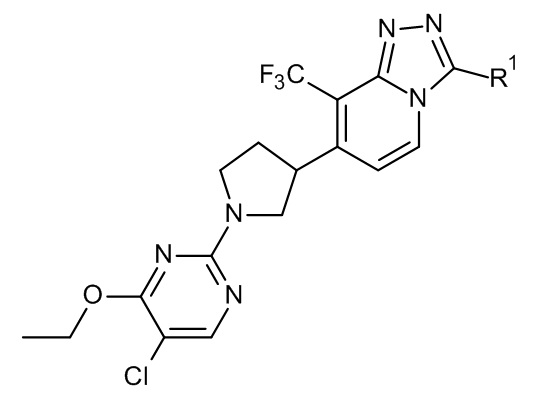 (I),
(I),
и их стереохимически изомерным формам, где
R1 выбран из C1-6алкила, (C3-8циклоалкил)C1-3алкила и (C1-3алкилокси)C1-3алкила;
а также к их фармацевтически приемлемым солям и сольватам.
Настоящее изобретение также относится к фармацевтической композиции, содержащей терапевтически эффективное количество соединения формулы (I) и фармацевтически приемлемый носитель или наполнитель.
Дополнительно, настоящее изобретение относится к соединению формулы (I) для применения в качестве лекарственного препарата и к соединению формулы (I) для применения в качестве лекарственного препарата для лечения или предупреждения неврологических и психических расстройств, в которые вовлечены mGluR2.
Настоящее изобретение также относится к применению соединения формулы (I) или фармацевтической композиции согласно настоящему изобретению для изготовления лекарственного препарата для лечения или предупреждения неврологических и психических расстройств, в которые вовлечены mGluR2.
Дополнительно, настоящее изобретение относится к применению соединения формулы (I) в комбинации с дополнительным фармацевтическим средством для изготовления лекарственного препарата для лечения или предупреждения неврологических и психических расстройств, в которые вовлечены mGluR2.
Дополнительно, настоящее изобретение относится к способу получения фармацевтической композиции согласно настоящему изобретению, характеризующемуся тем, что фармацевтически приемлемый носитель тщательно перемешивают с терапевтически эффективным количеством соединения формулы (I).
Настоящее изобретение также относится к продукту, содержащему соединение формулы (I) и дополнительное фармацевтическое средство, в качестве комбинированного препарата для одновременного, раздельного или последовательного применения в лечении или предупреждении неврологических или психических расстройств и заболеваний.
Настоящее изобретение относится, в частности, к соединениям формулы (I), определенным выше в данном документе, и к их стереоизомерным формам, где
R1 представляет собой (C3-8циклоалкил)C1-3алкил, (C1-3алкилокси)C1-3алкил и C1-3алкил;
и их фармацевтически приемлемые соли и сольваты.
Настоящее изобретение относится, в частности, к соединениям формулы (I), определенным выше в данном документе, и к их стереоизомерным формам, где
R1 представляет собой (циклопропил)метил или (этилокси)метил;
и их фармацевтически приемлемые соли и сольваты.
В дополнительном варианте осуществления настоящее изобретение относится к соединениям формулы (I), определенным в данном документе, имеющим формулу (Ia):
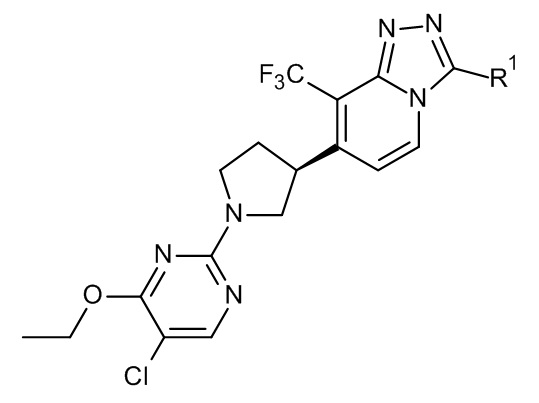 (Ia),
(Ia),
где R1 определен в формуле (I) в данном документе, а также к их фармацевтически приемлемым солям и сольватам.
В дополнительном варианте осуществления настоящее изобретение относится к соединениям формулы (I), определенным в данном документе, имеющим формулу (Ib):
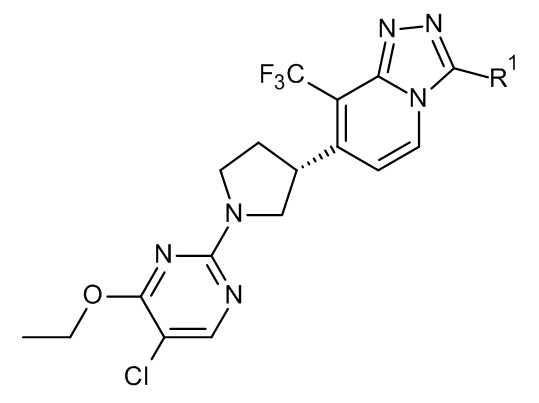 (Ib),
(Ib),
где R1 определен в формуле (I) в данном документе, а также к их фармацевтически приемлемым солям и сольватам.
Конкретные соединения могут быть выбраны из группы
7-[1-(5-хлор-4-этокси-пиримидин-2-ил)пирролидин-3-ил]-3-(циклопропилметил)-8-(трифторметил)-[1,2,4]триазоло[4,3-a]пиридина;
7-[(3*R)-1-(5-хлор-4-этокси-пиримидин-2-ил)пирролидин-3-ил]-3-(циклопропилметил)-8-(трифторметил)-[1,2,4]триазоло[4,3-a]пиридина;
7-[(3*S)-1-(5-хлор-4-этокси-пиримидин-2-ил)пирролидин-3-ил]-3-(циклопропилметил)-8-(трифторметил)-[1,2,4]триазоло[4,3-a]пиридина;
7-[1-(5-хлор-4-этокси-пиримидин-2-ил)пирролидин-3-ил]-3-(этоксиметил)-8-(трифторметил)-[1,2,4]триазоло[4,3-a]пиридина;
7-[(3*R)-1-(5-хлор-4-этокси-пиримидин-2-ил)пирролидин-3-ил]-3-(этоксиметил)-8-(трифторметил)-[1,2,4]триазоло[4,3-a]пиридина;
7-[(3*S)-1-(5-хлор-4-этокси-пиримидин-2-ил)пирролидин-3-ил]-3-(этоксиметил)-8-(трифторметил)-[1,2,4]триазоло[4,3-a]пиридина.
В объем данного перечня включены их стереоизомерные формы, фармацевтически приемлемые соли и сольваты.
Названия соединений согласно настоящему изобретению были составлены согласно правилам номенклатуры, принятым Химической реферативной службой (C.A.S.), с использованием программного обеспечения Advanced Chemical Development, Inc. (версия продукта ACD/Name 10.01.0.14105, октябрь 2006 г.). В случае таутомерных форм составляли название представленной таутомерной формы структуры. Тем не менее, следует понимать, что другая не представленная таутомерная форма также включена в объем настоящего изобретения.
Определения
Обозначение "C1-3алкил" или "C1-6алкил", используемое в данном документе отдельно или в качестве части другой группы, определяет насыщенный углеводородный радикал с прямой или разветвленной цепью, содержащий, если не указано иное, от 1 до 3 или от 1 до 6 атомов углерода, например, метил, этил,
1-пропил, 1-метилэтил, бутил, 1-метил-пропил, 2-метил-1-пропил, 1,1-диметилэтил, 3-метил-1-бутил, 1-пентил, 1-гексил и т. п.
Обозначение ʺC3-8циклоалкилʺ, используемое в данном документе отдельно или в качестве части другой группы, определяет насыщенный циклический углеводородный радикал, содержащий от 3 до 8 атомов углерода, например, циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и циклооктил.
Обозначение "галоген" или "галогеновый радикал", используемое в данном документе отдельно или в качестве части другой группы, относится к фтору, хлору, брому или йоду, при этом фтор или хлор являются предпочтительными.
Термин "терапевтически эффективное количество", используемый в данном документе, означает такое количество активного соединения или фармацевтического средства, которое вызывает биологический или медицинский эффект в системе тканей, у животного или человека, который стремится получить исследователь, ветеринар, врач или другой клиницист, который включает облегчение симптомов заболевания или расстройства, подлежащего лечению.
Подразумевается, что используемый в данном документе термин "композиция" охватывает продукт, содержащий определенные ингредиенты в определенных количествах, а также любой продукт, который получают, прямо или опосредованно, в результате комбинаций определенных ингредиентов в определенных количествах.
Следует понимать, что некоторые из соединений формулы (I), а также их фармацевтически приемлемые соли присоединения и их сольваты могут содержать один или несколько центров хиральности и существовать в виде стереоизомерных форм.
Подразумевается, что термин "соединения согласно настоящему изобретению", используемый в данном документе, включает соединения формулы (I), а также их соли и сольваты.
Любая химическая формула, применяемая в данном документе, связи в которой показаны только в виде сплошных линий, а не в виде сплошных клиновидных или пунктирных клиновидных связей, или иным образом показанная как имеющая конкретную конфигурацию (например, R, S) возле одного или нескольких атомов, предусматривает каждый возможный стереоизомер или смесь двух или более стереоизомеров.
Выше и ниже в данном документе подразумевается, что термин "соединение формулы (I)" включает его стереоизомеры и его таутомерные формы.
Термины "стереоизомеры", "стереоизомерные формы" или "стереохимически изомерные формы" выше или ниже в данном документе используются взаимозаменяемо.
Настоящее изобретение включает все стереоизомеры соединений по настоящему изобретению либо в виде чистого стереоизомера, либо в виде смеси двух или более стереоизомеров. Энантиомеры представляют собой стереоизомеры, которые представляют собой несовпадающие при наложении зеркальные отображения друг друга. Смесь 1:1 пары энантиомеров представляет собой рацемат или рацемическую смесь. Диастереомеры (или диастереоизомеры) представляют собой стереоизомеры, которые не являются энантиомерами, т. е. они не относятся к зеркальным отображениям. Если соединение содержит двойную связь, то заместители могут находиться в E- или Z-конфигурации. Заместители на двухвалентных циклических (частично) насыщенных радикалах могут находиться либо в цис-, либо в транс-конфигурации; например, если соединение содержит дизамещенную циклоалкильную группу, то заместители могут находиться в цис- или транс-конфигурации.
Таким образом, настоящее изобретение включает энантиомеры, диастереомеры, рацематы, E-изомеры, Z-изомеры, цис-изомеры, транс-изомеры и их смеси во всех случаях, когда это возможно с точки зрения химии. Значения всех этих терминов, т. е. энантиомеры, диастереомеры, рацематы, E-изомеры, Z-изомеры, цис-изомеры, транс-изомеры и их смеси, известны специалисту в данной области.
Абсолютную конфигурацию определяют в соответствии с системой Кана-Ингольда-Прелога. Конфигурацию при асимметрическом атоме определяют либо как R, либо как S. Выделенные стереоизомеры, абсолютная конфигурация которых неизвестна, могут обозначаться как (+) или
(-) в зависимости от направления, в котором они вращают плоскость поляризации света. Например, выделенные энантиомеры, абсолютная конфигурация которых неизвестна, могут обозначаться как (+) или (-) в зависимости от направления, в котором они вращают плоскость поляризации света.
Если указан конкретный стереоизомер, это означает, что указанный стереоизомер практически не содержит другие изомеры, т. е. связан с менее 50%, предпочтительно с менее 20%, более предпочтительно с менее 10%, еще более предпочтительно с менее 5%, в частности с менее 2% и наиболее предпочтительно с менее 1% других изомеров. Таким образом, если соединение формулы (I), например, указано как (R), то это означает, что соединение практически не содержит изомер (S); если соединение формулы (I), например, указано как E, то это означает, что соединение практически не содержит изомер Z; если соединение формулы (I), например, указано как цис-, то это означает, что соединение практически не содержит транс-изомер.
Некоторые соединения формулы (I) могут существовать также в их таутомерной форме. Предполагается, что такие формы, ввиду того, что они могут существовать, хотя явно и не показаны вышеприведенной формулой, включены в объем настоящего изобретения.
Из этого следует, что одно соединение может существовать как в стереоизомерных, так и в таутомерных формах.
Для терапевтического применения соли соединений формулы (I) являются такими, противоион которых является фармацевтически приемлемым. Однако соли кислот и оснований, которые не являются фармацевтически приемлемыми, также могут находить применение, например, при получении или очистке фармацевтически приемлемого соединения. Все соли, независимо от того, являются ли они фармацевтически приемлемыми или нет, включены в объем настоящего изобретения.
Предполагается, что фармацевтически приемлемые соли присоединения кислоты и основания, упоминаемые выше или ниже в данном документе, включают терапевтически активные нетоксичные формы солей присоединения кислоты или основания, которые могут образовывать соединения формулы (I). Фармацевтически приемлемые соли присоединения кислоты в целях удобства можно получать путем обработки основной формы такой соответствующей кислотой. Соответствующие кислоты включают, например, неорганические кислоты, такие как галогенводородные кислоты, например, хлористоводородная или бромистоводородная кислота, серная, азотная, фосфорная кислоты и т. п.; или органические кислоты, такие как, например, уксусная, пропановая, гидроксиуксусная, молочная, пировиноградная, щавелевая (т. е. этандиовая), малоновая, янтарная (т. е. бутандиовая кислота), малеиновая, фумаровая, яблочная, винная, лимонная, метансульфоновая, этансульфоновая, бензолсульфоновая, п-толуолсульфоновая, цикламовая, салициловая, п-аминосалициловая, памовая кислоты и т. п. И наоборот, указанные формы солей можно превратить путем обработки соответствующим основанием в форму свободного основания.
Соединения формулы (I), содержащие кислотный протон, также можно превратить в формы их нетоксичных солей присоединения металла или амина путем обработки соответствующими органическими и неорганическими основаниями. Соответствующие формы основных солей включают, например, соли аммония, соли щелочных и щелочноземельных металлов, например, соли лития, натрия, калия, магния, кальция и т. п., соли органических оснований, например, первичных, вторичных и третичных алифатических и ароматических аминов, таких как метиламин, этиламин, пропиламин, изопропиламин, четыре изомера бутиламина, диметиламин, диэтиламин, диэтаноламин, дипропиламин, диизопропиламин, ди-н-бутиламин, пирролидин, пиперидин, морфолин, триметиламин, триэтиламин, трипропиламин, хинуклидин, пиридин, хинолин и изохинолин; соли бензатина, N-метил-D-глюкамина, гидрабамина, а также соли аминокислот, таких как, например, аргинин, лизин и т. п. И наоборот, форму соли можно превратить путем обработки кислотой в форму свободной кислоты.
Термин "сольват" включает формы присоединения растворителя, а также их соли, которые могут образовывать соединения формулы (I). Примерами таких форм присоединения растворителя являются, например, гидраты, алкоголяты и т. п.
В рамках данной заявки элемент, в частности, при упоминании в отношении соединения формулы (I), включает все изотопы и смеси изотопов этого элемента, либо встречающиеся в природе, либо полученные синтетическим путем, либо с природным изотопным составом, либо в изотопно-обогащенной форме. Меченные радиоактивным изотопом соединения формулы (I) могут содержать радиоактивный изотоп, выбранный из группы 3H, 11C, 18F, 122I, 123I, 125I, 131I, 75Br, 76Br, 77Br и 82Br. Радиоактивный изотоп предпочтительно выбран из группы 3H, 11C и 18F.
Получение
Соединения согласно настоящему изобретению в целом можно получать при помощи последовательности стадий, каждая из которых известна специалисту в данной области. В частности, соединения можно получать согласно следующим способам синтеза.
Соединения формулы (I) можно синтезировать в виде рацемических смесей энантиомеров, которые можно отделить друг от друга согласно известным в данной области техники процедурам разделения. Рацемические соединения формулы (I) можно превращать в соответствующие формы диастереомерных солей посредством реакции с подходящей хиральной кислотой. Указанные формы диастереомерных солей затем разделяют, например, с помощью селективной или фракционной кристаллизации, и энантиомеры выделяют оттуда с помощью щелочи. Альтернативный способ разделения энантиомерных форм соединений формулы (I) включает жидкостную хроматографию или сверхкритическую флюидную хроматографию (SFC) с применением хиральной неподвижной фазы. Указанные чистые стереохимически изомерные формы можно также получать из соответствующих чистых стереохимически изомерных форм соответствующих исходных веществ при условии, что реакция протекает стереоспецифически.
A. Получение конечных соединений
Экспериментальная процедура 1
Конечные соединения формулы (I) можно получить посредством реакции промежуточного соединения формулы (II) с 2,5-дихлор-4-этокси-пиримидином в присутствии фторида цезия, основания, такого как DIPEA, и в соответствующем растворителе, таком как, например, DMSO, в течение подходящего периода времени, позволяющего завершить реакцию, такого как, например, 2 ч., при температуре 80-100°C, например, 90°C. На схеме реакции 1 R1 определен в формуле (I).
Схема реакции 1
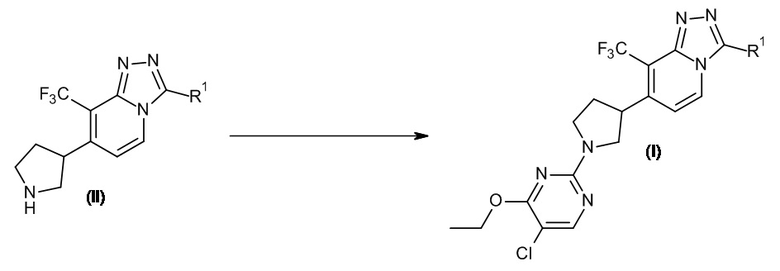
B. Получение промежуточных соединений
Экспериментальная процедура 2
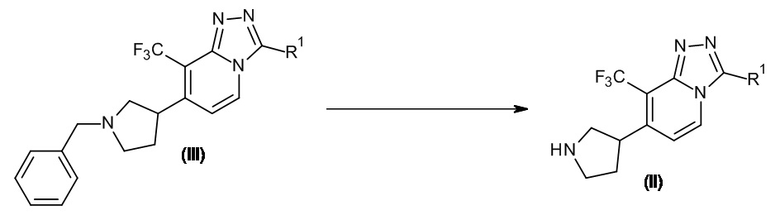
Промежуточные соединения формулы (II) можно получить путем отщепления бензильной защитной группы в пирролидиновом кольце в промежуточном соединении формулы (III) в соответствии с условиями, известными специалисту в данной области, такими как, например, подвергание промежуточного соединения формулы (III) реакции с 1-хлорэтилхлорформиатом в присутствии DIPEA в DCM в течение подходящего периода времени, позволяющего завершить реакцию, например, нескольких минут при к.т. На схеме реакции 2 R1 определен как в формуле (I).
Схема реакции 2
Экспериментальная процедура 3
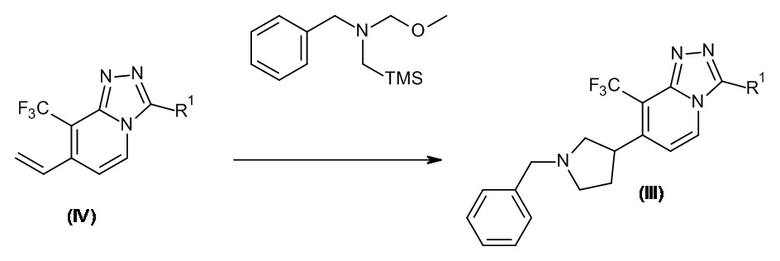
Промежуточные соединения формулы (III) можно получить посредством реакции промежуточного соединения формулы (IV) с N-метоксиметил-N-(триметилсилилметил)бензиламином в присутствии кислоты, такой как TFA, и в подходящем растворителе, таком как DCM, в течение периода времени, позволяющего завершить реакцию, например, 1 ч. при к.т. На схеме реакции 2 R1 определен как в формуле (I).
Схема реакции 3
Экспериментальная процедура 4
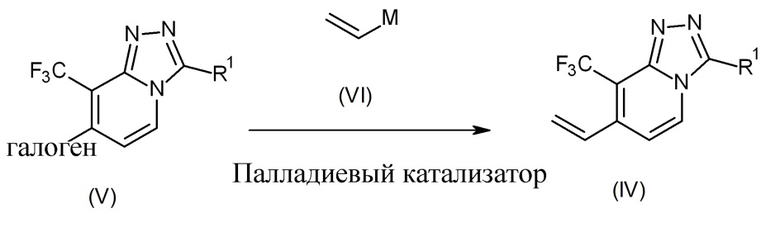
Промежуточные соединения формулы (IV) можно получить посредством реакций сочетания, таких как реакции Стилле или Сузуки, промежуточного соединения формулы (V) с соединением формулы (VI) в условиях, известных специалистам в данной области. Способ можно необязательно осуществлять в растворителе, таком как 1,4-диоксан, вода, и, как правило, при температурах от приблизительно равных к.т. до приблизительно 200°C в присутствии основания. Это проиллюстрировано на схеме реакции (4), где все переменные определены, как упомянуто в данном документе выше, где M представляет собой триалкилолово, бороновую кислоту или сложный боронатный эфир, и присутствует палладиевый катализатор, а галоген представляет собой хлор, бром или йод.
Схема реакции 4
Экспериментальная процедура 5
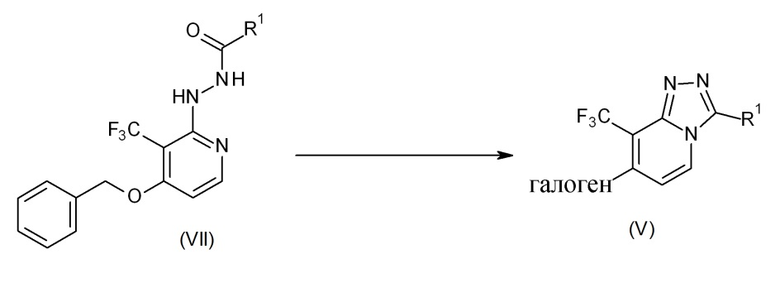
Промежуточные соединения формулы (V) можно получить согласно процедурам, известным из уровня техники, путем циклизации промежуточного соединения формулы (VII) в присутствии галогенирующего средства, такого как, например, оксихлорид фосфора (V) (POCl3), в подходящем растворителе, таком как, например, дихлорэтан, при перемешивании под действием микроволнового излучения в течение подходящего периода времени, позволяющего завершить реакцию, например, 5 мин., при температуре 140-200°C. На схеме реакции (5) R1 определен как в формуле (I), а галоген представляет собой хлор, бром или йод.
Схема реакции 5
Экспериментальная процедура 6
Промежуточные соединения формулы (VII) можно получить согласно процедурам, известным из уровня техники, посредством реакции гидразинового промежуточного соединения формулы (VIII) с галогенангидридами формулы (IX). Реакцию можно осуществлять с применением инертного растворителя, такого как, например, DCM, в присутствии основания, такого как, например, триэтиламин, например, при к.т. в течение подходящего периода времени, позволяющего завершить реакцию, например, 20 мин. На схеме реакции (6) R1 определен как в формуле (I).
Схема реакции 6
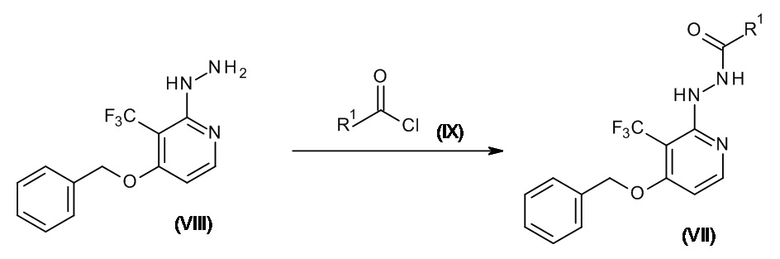
Экспериментальная процедура 7
Промежуточные соединения формулы (VIII) можно получить посредством реакции промежуточного соединения формулы (X) с гидразином согласно схеме реакции (7), эту реакцию выполняют в подходящем реакционно-инертном растворителе, таком как, например, этанол, THF или 1,4-диоксан, в таких температурных условиях, как, например, нагревание реакционной смеси, например, при 160°C под действием микроволнового излучения в течение 30 мин. или путем классического термического нагревания при 70°C в течение 16 ч. На схеме реакции (7) галоген представляет собой хлор, бром или йод.
Схема реакции 7
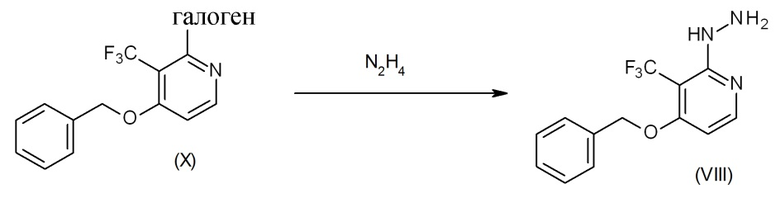
Экспериментальная процедура 8
Промежуточные соединения формулы (X) можно получить посредством реакции промежуточного соединения формулы (XI) с бензиловым спиртом согласно схеме реакции (8), эту реакцию выполняют в подходящем реакционно-инертном растворителе, таком как, например, DMF, в присутствии подходящего основания, такого как, например, гидрид натрия, при к.т. в течение подходящего периода времени, позволяющего завершить реакцию, например, 1 ч. На схеме реакции (8) галоген представляет собой хлор, бром или йод.
Схема реакции 8
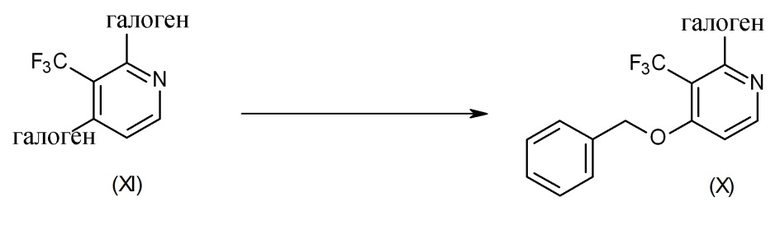
Экспериментальная процедура 9
Промежуточные соединения формулы (XI) можно получить посредством реакции промежуточного соединения формулы (XII) с подходящим трифторметилирующим средством, таким как, например, метиловый сложный эфир фторсульфонил(дифтор)уксусной кислоты, согласно схеме реакции (9). Эту реакцию выполняют в подходящем реакционно-инертном растворителе, таком как, например, DMF, в присутствии подходящего средства для сочетания, такого как, например, йодид меди(I), в таких температурных условиях, как, например, нагревание реакционной смеси, например, при 160°C под действием микроволнового излучения в течение 45 мин. На схеме реакции (9) галоген представляет собой хлор, бром или йод.
Схема реакции 9
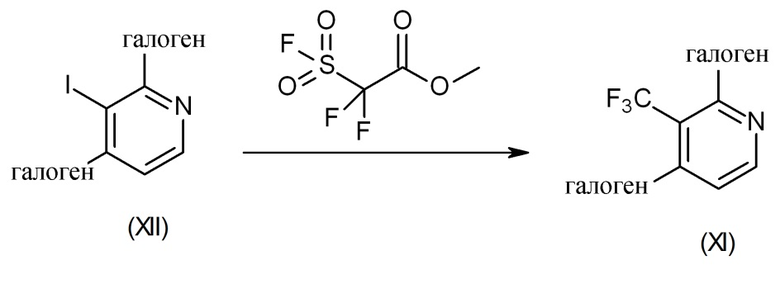
Экспериментальная процедура 10
Промежуточные соединения формулы (XII) можно получить посредством реакции промежуточного соединения формулы (XIII) с сильным основанием, таким как, например, н-бутиллитий, и дополнительной обработки йодирующим средством, таким как, например, йод. Эту реакцию выполняют в подходящем реакционно-инертном растворителе, таком как, например, THF, при низкой температуре, такой как, например -78°C, в течение периода времени, позволяющего завершить реакцию, например, 2 ч. На схеме реакции (10) галоген может представлять собой хлор, бром или йод.
Схема реакции 10
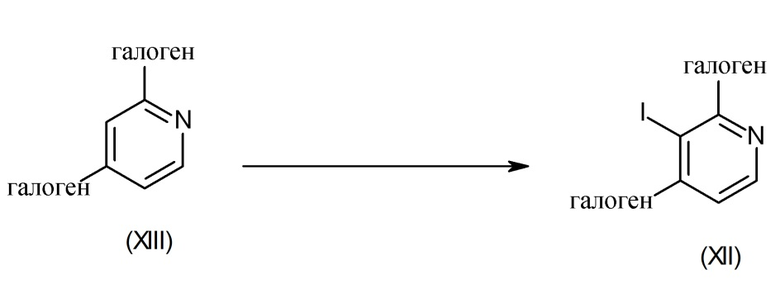
Исходный материал согласно формуле (XIII) является либо коммерчески доступным, либо его можно получить в соответствии с традиционными реакционными процедурами, общеизвестными для специалистов в данной области.
Фармакология
Соединения, представленные в настоящем изобретении, являются положительными аллостерическими модуляторами (PAM) метаботропных глутаматных рецепторов, в частности, они являются положительными аллостерическими модуляторами mGluR2. Соединения по настоящему изобретению, по-видимому, связываются не с участком распознавания глутамата, участком для ортостерического лиганда, а вместо этого с аллостерическим участком в семиспиральной трансмембранной области рецептора. В присутствии глутамата или агониста mGluR2 соединения по настоящему изобретению усиливают ответ mGluR2. Предполагается, что соединения, представленные в настоящем изобретении, оказывают свой эффект на mGluR2 благодаря своей способности к усилению ответа таких рецепторов на глутамат или агонисты mGluR2.
Подразумевается, что используемый в данном документе термин "лечение" относится ко всем способам, которые могут предусматривать замедление, нарушение, подавление или прекращение прогрессирования заболевания или облегчение симптомов, но не обязательно означает полное устранение всех симптомов.
Следовательно, настоящее изобретение относится к соединению общей формулы (I), его стереоизомерным формам и таутомерам и его фармацевтически приемлемым солям присоединения кислоты или основания и сольватам для применения в качестве лекарственного препарата.
Настоящее изобретение также относится к применению соединения общей формулы (I), его стереоизомерных форм и таутомеров и его фармацевтически приемлемых солей присоединения кислоты или основания и сольватов или фармацевтической композиции согласно настоящему изобретению для изготовления лекарственного препарата.
Настоящее изобретение также относится к соединению общей формулы (I), его стереоизомерным формам и таутомерам и его фармацевтически приемлемым солям присоединения кислоты или основания и сольватам или к фармацевтической композиции согласно настоящему изобретению для применения в лечении или предупреждении, в частности, в лечении, состояния у млекопитающего, в том числе у человека, лечение или предупреждение которого зависит от нейромодуляторного эффекта аллостерических модуляторов mGluR2, в частности, их положительных аллостерических модуляторов, или облегчается им.
Настоящее изобретение также относится к применению соединения общей формулы (I), его стереоизомерных форм и таутомеров и его фармацевтически приемлемых солей присоединения кислоты или основания и сольватов или фармацевтической композиции согласно настоящему изобретению для изготовления лекарственного препарата для лечения или предупреждения, в частности, лечения, состояния у млекопитающего, в том числе у человека, лечение или предупреждение которого зависит от нейромодуляторного эффекта аллостерических модуляторов mGluR2, в частности, их положительных аллостерических модуляторов, или облегчается им.
Настоящее изобретение также относится к соединению общей формулы (I), его стереоизомерным формам и таутомерам и его фармацевтически приемлемым солям присоединения кислоты или основания и сольватам или к фармацевтической композиции согласно настоящему изобретению для применения в лечении, предупреждении, уменьшении интенсивности проявлений, контроле или снижении риска развития различных неврологических и психических расстройств, ассоциированных с нарушением глутаматергической передачи сигнала, у млекопитающего, в том числе у человека, лечение или предупреждение которых зависит от нейромодуляторного эффекта положительных аллостерических модуляторов mGluR2 или облегчается им.
Настоящее изобретение также относится к применению соединения общей формулы (I), его стереоизомерных форм и таутомеров и его фармацевтически приемлемых солей присоединения кислоты или основания и сольватов или фармацевтической композиции согласно настоящему изобретению для изготовления лекарственного препарата для лечения, предупреждения, уменьшения интенсивности проявлений, контроля или снижения риска развития различных неврологических и психических расстройств, ассоциированных с нарушением глутаматергической передачи сигнала, у млекопитающего, в том числе у человека, лечение или предупреждение которых зависит от нейромодуляторного эффекта положительных аллостерических модуляторов mGluR2 или облегчается им.
В частности, неврологические и психические расстройства, ассоциированные с нарушением глутаматергической передачи сигнала, включают одно или несколько из следующих состояний или заболеваний: острые неврологические и психические расстройства, такие как, например, формы церебральной недостаточности после операции аортокоронарного шунтирования сердца, инсульт, ишемия головного мозга, травма спинного мозга, травма головы, перинатальная гипоксия, остановка сердца, повреждение нейронов при гипогликемии, деменция (в том числе деменция, вызванная AIDS), болезнь Альцгеймера, хорея Хантингтона, боковой амиотрофический склероз, поражение органа зрения, ретинопатия, когнитивные расстройства, идиопатическая и лекарственная болезнь Паркинсона, мышечные спазмы и расстройства, ассоциированные с мышечной спастичностью, включающие приступы тремора, эпилепсию, судороги, мигрень (в том числе мигренозная головная боль), недержание мочи, зависимость от химических веществ/злоупотребление химическими веществами, синдром отмены химических веществ (подразумевающий такие вещества, как, например, опиаты, никотин, табачные изделия, алкоголь, бензодиазепины, кокаин, успокоительные средства, снотворные средства и т.п.), психоз, шизофрения, тревожность (в том числе генерализованное тревожное расстройство, паническое расстройство и обсессивно-компульсивное расстройство), расстройства настроения (в том числе депрессия, большое депрессивное расстройство, терапевтически резистентная депрессия, мания, биполярные расстройства, такие как биполярная мания), посттравматическое стрессовое расстройство, невралгия тройничного нерва, потеря слуха, шум в ушах, дегенерация желтого пятна глаза, рвота, отек головного мозга, боль (включающая острые и хронические состояния, сильную боль, неустранимую боль, нейропатическую боль и посттравматическую боль), поздняя дискинезия, расстройства сна (включающие нарколепсию), синдром дефицита внимания и гиперактивности и кондуктивное расстройство.
В частности, состояние или заболевание является расстройством центральной нервной системы, выбранным из группы тревожных расстройств, психотических расстройств, расстройств личности, расстройств, связанных с употреблением химических веществ, расстройств пищевого поведения, расстройств настроения, мигрени, эпилепсии или судорожных расстройств, расстройств детского возраста, когнитивных расстройств, нейродегенерации, аутических расстройств, нейротоксичности и ишемии.
В частности, расстройство центральной нервной системы представляет собой тревожное расстройство, выбранное из группы агорафобии, генерализованного тревожного расстройства (GAD), смешанного тревожно-депрессивного расстройства, обсессивно-компульсивного расстройства (OCD), панического расстройства, посттравматического стрессового расстройства (PTSD), социофобии и других фобий. Дополнительным тревожным расстройством является паническая атака.
В частности, расстройство центральной нервной системы представляет собой психотическое расстройство, выбранное из группы шизофрении, бредового расстройства, шизоаффективного расстройства, шизофреноформного расстройства и психотического расстройства, вызванного употреблением химических веществ; более конкретно, негативные симптомы или остаточные симптомы шизофрении. При таких расстройствах в качестве ярко выраженного симптома проявляется психоз. Таким образом, настоящее изобретение также относится к соединению общей формулы (I), его стереоизомерным формам и таутомерам и его фармацевтически приемлемым солям присоединения кислоты или основания и сольватам или к фармацевтической композиции согласно настоящему изобретению для применения в лечении, предупреждении, уменьшении интенсивности проявлений, контроле или ослаблении психоза.
В частности, расстройство центральной нервной системы представляет собой расстройство личности, выбранное из группы обсессивно-компульсивного расстройства личности, пограничного расстройства личности и шизоидного, шизотипического расстройства.
В частности, расстройство центральной нервной системы представляет собой расстройство, связанное со злоупотреблением химическими веществами или употреблением химических веществ, выбранное из группы злоупотребления алкоголем, алкоголизма, алкогольной зависимости, синдрома отмены алкоголя, синдрома отмены алкоголя с делирием, психотического расстройства, вызванного употреблением алкоголя, амфетаминовой наркомании, амфетаминовой зависимости, синдрома отмены амфетамина, кокаиновой наркомании, кокаиновой зависимости, синдрома отмены кокаина, никотиновой наркомании, никотиновой зависимости, синдрома отмены никотина, опиоидной зависимости и синдрома отмены опиоидов. Лечение или предупреждение упоминаемых в данном документе расстройств, связанных со злоупотреблением химическими веществами или употреблением химических веществ, может включать предупреждение их рецидивов.
В частности, расстройство центральной нервной системы представляет собой расстройство пищевого поведения, выбранное из группы нервной анорексии и нервной булимии.
В частности, расстройство центральной нервной системы представляет собой расстройство настроения, выбранное из группы биполярных расстройств (I и II типа), циклотимического расстройства, депрессии, дистимического расстройства, большого депрессивного расстройства, терапевтически резистентной депрессии, биполярной депрессии и расстройства настроения, вызванного употреблением химических веществ.
В частности, расстройство центральной нервной системы представляет собой мигрень.
В частности, расстройство центральной нервной системы представляет собой эпилепсию или судорожное расстройство, выбранное из группы эпилепсии с генерализованными бессудорожными приступами, эпилепсии с генерализованными судорожными приступами, эпилептического статуса малых припадков, эпилептического статуса больших припадков, парциальной эпилепсии с нарушением сознания или без него, младенческих судорог, постоянной парциальной эпилепсии и других форм эпилепсии. Дополнительные расстройства, охватываемые эпилепсией или судорожным расстройством, включают любое расстройство, при котором субъект (предпочтительно взрослый человек, ребенок или младенец) испытывает один или несколько эпилептических припадков и/или приступов тремора. Подходящие примеры включают без ограничения эпилепсию (в том числе без ограничения локализационно-обусловленные формы эпилепсии, генерализованные формы эпилепсии, формы эпилепсии как с генерализованными, так и с локальными припадками и т. п.), парциальные припадки с генерализацией или без нее, миоклонические припадки, первичные генерализованные тонико-клонические припадки, в особенности у пациентов с идиопатической генерализованной эпилепсией, припадки, ассоциированные с синдромом Леннокса-Гасто, припадки в качестве осложнения заболевания или состояния (как, например, припадки, ассоциированные с энцефалопатией, фенилкетонурией, ювенильной формой болезни Гоше, прогрессирующей миоклонической эпилепсией Лундборга, инсультом, травмой головы, стрессом, гормональными изменениями, употреблением лекарственных средств или отменой лекарственных средств, употреблением алкоголя или отменой алкоголя, лишением сна, лихорадкой, инфекцией и т. п.), эпилептический статус (судорожный или бессудорожный), эссенциальный тремор, синдром беспокойных конечностей и т. п. Расстройство предпочтительно выбрано из эпилепсии (независимо от типа, первопричины или происхождения), эссенциального тремора или синдрома беспокойных конечностей. Более предпочтительно, расстройство представляет собой эпилепсию (независимо от типа, первопричины или происхождения) или эссенциальный тремор. В частности, расстройство представляет собой эпилепсию (независимо от типа, первопричины или происхождения). Более конкретным примером эпилепсии является рефрактерная эпилепсия, также называемая эпилепсией, устойчивой к лечению или терапии. Этот термин часто используется, если применение пациентами трех или более противоэпилептических лекарственных средств (AED) было безуспешным. Рефрактерная эпилепсия также включает рефрактерную парциальную эпилепсию и рефрактерную генерализованную эпилепсию (в том числе идиопатическую или симптоматическую).
В частности, расстройство центральной нервной системы представляет собой синдром дефицита внимания и гиперактивности.
В частности, расстройство центральной нервной системы представляет собой аутическое расстройство, выбранное из аутизма и расстройств аутистического спектра, таких как синдром Аспергера.
В частности, расстройство центральной нервной системы представляет собой когнитивное расстройство, выбранное из группы делирия, персистирующего делирия, вызванного употреблением химических веществ, деменции, деменции вследствие заболевания, вызываемого HIV, деменции вследствие болезни Хантингтона, деменции вследствие болезни Паркинсона, деменции альцгеймеровского типа, поведенческих и психологических симптомов деменции, персистирующей деменции, вызванной употреблением химических веществ, и умеренного когнитивного нарушения.
Конкретные примеры поведенческих и психологических симптомов деменции (BPSD) включают без ограничения агрессивность, возбуждение и психоз.
В частности, расстройство центральной нервной системы выбрано из группы шизофрении, поведенческих и психологических симптомов деменции, большого депрессивного расстройства, терапевтически резистентной депрессии, биполярной депрессии, тревожности, депрессии, генерализованного тревожного расстройства, посттравматического стрессового расстройства, биполярной мании, эпилепсии, синдрома дефицита внимания и гиперактивности, злоупотребления химическими веществами и смешанного тревожно-депрессивного расстройства.
В частности, расстройство центральной нервной системы выбрано из группы шизофрении, эпилепсии, обсессивно-компульсивного расстройства, алкоголизма, кокаиновой наркомании, никотиновой наркомании, пограничного расстройства личности, биполярного расстройства, поведенческих и психологических симптомов деменции, синдрома Аспергера, большого депрессивного расстройства, терапевтически резистентной депрессии, тревожности, депрессии, генерализованного тревожного расстройства и смешанного тревожно-депрессивного расстройства.
В частности, расстройство центральной нервной системы выбрано из группы шизофрении (в частности, ее негативных симптомов или остаточных симптомов), генерализованного тревожного расстройства, биполярного расстройства (I или II типа), мигрени, поведенческих и психологических симптомов деменции, эпилепсии или судорожных расстройств, панического расстройства, смешанного тревожно-депрессивного расстройства и агорафобии.
В частности, расстройство центральной нервной системы выбрано из группы шизофрении (в частности, ее негативных симптомов или остаточных симптомов), генерализованного тревожного расстройства, биполярного расстройства (I или II типа), мигрени, эпилепсии, панического расстройства, смешанного тревожно-депрессивного расстройства и агорафобии. Из расстройств, упомянутых выше, особенно важным является лечение психоза, шизофрении, поведенческих и психологических симптомов деменции, большого депрессивного расстройства, терапевтически резистентной депрессии, биполярной депрессии, тревожности, депрессии, генерализованного тревожного расстройства, посттравматического стрессового расстройства, биполярной мании, злоупотребления химическими веществами и смешанного тревожно-депрессивного расстройства.
Из расстройств, упомянутых выше, особенно важным является лечение генерализованного тревожного расстройства, биполярного расстройства (I или II типа), эпилепсии, панического расстройства и агорафобии.
Из расстройств, упомянутых выше, особенно важным является лечение тревожности, шизофрении, мигрени, депрессии и эпилепсии.
Из расстройств, упомянутых выше, особенно важным является лечение тревожности и эпилепсии.
На сегодняшний день четвертое издание Руководства по диагностике и статистике психических расстройств (DSM-IV) Американской психиатрической ассоциации обеспечивает средства диагностики для идентификации расстройств, описанных в данном документе. Специалист в данной области примет во внимание, что для неврологических и психических расстройств, описанных в данном документе, существуют альтернативные системы номенклатуры, нозологические подходы и системы классификации, и что они видоизменяются вместе с прогрессом в области медицины и научным прогрессом.
Специалисту в данной области хорошо известны альтернативные системы номенклатуры, нозологические подходы и системы классификации для заболеваний или состояний, упоминаемых в данном документе. Например, в "American Psychiatric Association: Diagnostic and Statistical Manual of Mental Disorders, Fifth Edition. Arlington, VA, American Psychiatric Association, 2013" (DSM-5TM) используются такие термины, как тревожные расстройства, в частности, агорафобия, генерализованное тревожное расстройство, паническое расстройство, социальное тревожное расстройство (социофобия) и паническая атака; расстройства шизофренического спектра и другие психотические расстройства, в частности, шизофрения, бредовое расстройство, шизоаффективное расстройство, шизофреноформное расстройство, расстройство, вызванное употреблением химических веществ/лекарственных препаратов, и психотическое расстройство; расстройства личности, в частности, обсессивно-компульсивное расстройство личности, пограничное расстройство личности, шизоидное расстройство личности и шизотипическое расстройство личности; связанные с употреблением химических веществ и аддиктивные расстройства, в частности, расстройство, связанное с употреблением алкоголя, синдром отмены алкоголя, расстройство, связанное с употреблением опиоидов, синдром отмены опиоидов, расстройство, связанное с употреблением стимуляторов (химического вещества амфетаминового типа, кокаина), синдром отмены стимуляторов (химического вещества амфетаминового типа, кокаина), расстройство, связанное с употреблением табака, и синдром отмены табака; депрессивные расстройства, в частности, большое депрессивное расстройство, персистирующее депрессивное расстройство (дистимия) и депрессивное расстройство, вызванное употреблением химических веществ/лекарственных препаратов; биполярные и родственные им расстройства, в частности, биполярное расстройство I типа, биполярное расстройство II типа, циклотимическое расстройство, биполярное и родственное ему расстройство, вызванное употреблением химических веществ/лекарственных препаратов; обсессивно-компульсивное расстройство и родственные ему расстройства, в частности, обсессивно-компульсивное расстройство; расстройства, связанные с травмами и стресс-факторами, в частности, посттравматическое стрессовое расстройство и острое стрессовое расстройство; расстройство неврологического развития, в частности, расстройство аутистического спектра и синдром дефицита внимания и гиперактивности; нейрокогнитивные расстройства (NCD) (как тяжелые, так и умеренные), в частности, делирий, делирий, связанный с интоксикацией химическими веществами, NCD вследствие болезни Альцгеймера, NCD вследствие HIV-инфекции, NCD вследствие болезни Хантингтона, NCD вследствие болезни Паркинсона и NCD, вызванное употреблением химических веществ/лекарственных препаратов. Такие термины могут применяться специалистом в данной области в качестве альтернативной номенклатуры для некоторых заболеваний или состояний, упоминаемых в данном документе.
Таким образом, настоящее изобретение также относится к соединению общей формулы (I), его стереоизомерным формам и таутомерам и его фармацевтически приемлемым солям присоединения кислоты или основания и сольватам для применения в лечении любого из заболеваний, упомянутых выше в данном документе.
Настоящее изобретение также относится к соединению общей формулы (I), его стереоизомерным формам и таутомерам и его фармацевтически приемлемым солям присоединения кислоты или основания и сольватам для применения в лечении любого из заболеваний, упомянутых выше в данном документе.
Настоящее изобретение также относится к соединению общей формулы (I), его стереоизомерным формам и таутомерам и его фармацевтически приемлемым солям присоединения кислоты или основания и сольватам для лечения или предупреждения, в частности, лечения, любого из заболеваний, упомянутых выше в данном документе.
Настоящее изобретение также относится к применению соединения общей формулы (I), его стереоизомерных форм и таутомеров и его фармацевтически приемлемых солей присоединения кислоты или основания и сольватов для изготовления лекарственного препарата для лечения или предупреждения любого из болезненных состояний, упомянутых выше в данном документе.
Настоящее изобретение также относится к применению соединения общей формулы (I), его стереоизомерных форм и таутомеров и его фармацевтически приемлемых солей присоединения кислоты или основания и сольватов для изготовления лекарственного препарата для лечения любого из болезненных состояний, упомянутых выше в данном документе.
Соединения по настоящему изобретению можно вводить млекопитающим, предпочтительно людям, для лечения или предупреждения любого из заболеваний, упомянутых выше в данном документе.
Ввиду полезности соединений формулы (I) обеспечивается способ лечения теплокровных животных, в том числе людей, страдающих любым из заболеваний, упомянутых выше в данном документе, и способ предупреждения у теплокровных животных, в том числе у людей, любого из заболеваний, упомянутых выше в данном документе.
Указанные способы включают введение, т.е. системное или местное введение, предпочтительно пероральное введение, терапевтически эффективного количества соединения формулы (I), его стереоизомерной формы или таутомера и его фармацевтически приемлемой соли присоединения или сольвата теплокровным животным, в том числе людям.
Таким образом, настоящее изобретение также относится к способу предупреждения и/или лечения любого из заболеваний, упомянутых выше в данном документе, включающему введение терапевтически эффективного количества соединения согласно настоящему изобретению пациенту, нуждающемуся в этом.
Специалисту в данной области будет понятно, что терапевтически эффективным количеством PAM по настоящему изобретению является количество, достаточное для модулирования активности mGluR2, и что это количество варьирует, помимо прочего, в зависимости от типа заболевания, концентрации соединения в терапевтическом составе и состояния пациента. Как правило, количество PAM, подлежащего введению в качестве терапевтического средства для лечения заболеваний, при которых модулирование mGluR2 является целесообразным, таких как расстройства, описанные в данном документе, будет определяться в каждом конкретном случае лечащим врачом.
Как правило, приемлемой дозой является доза, которая дает в результате концентрацию PAM в обрабатываемом участке в диапазоне от 0,5 нM до 200 мкM и в более типичном случае от 5 нM до 50 мкM. Для достижения этих лечебных концентраций пациенту, нуждающемуся в лечении, видимо, будут вводить эффективное терапевтическое суточное количество, составляющее от приблизительно 0,01 мг/кг до приблизительно 50 мг/кг массы тела, предпочтительно от приблизительно 0,01 мг/кг до приблизительно 25 мг/кг массы тела, более предпочтительно от приблизительно 0,01 мг/кг до приблизительно 10 мг/кг массы тела, более предпочтительно от приблизительно 0,01 мг/кг до приблизительно 2,5 мг/кг массы тела, еще более предпочтительно от приблизительно 0,05 мг/кг до приблизительно 1 мг/кг массы тела, более предпочтительно от приблизительно 0,1 мг/кг до приблизительно 0,5 мг/кг массы тела. Количество соединения согласно настоящему изобретению, также называемого в данном документе активным ингредиентом, необходимое для достижения терапевтического эффекта, будет, разумеется, изменяться в каждом конкретном случае, изменяться в зависимости от конкретного соединения, пути введения, возраста и состояния пациента, получающего лечение, и конкретного расстройства или заболевания, подвергаемого лечению. Способ лечения может также включать введение активного ингредиента в режиме от одного до четырех раз в сутки. В таких способах лечения соединения согласно настоящему изобретению предпочтительно составляют перед введением. Как описано в данном документе ниже, подходящие фармацевтические составы получают с помощью известных процедур с применением широко известных и общедоступных ингредиентов.
Поскольку такие положительные аллостерические модуляторы mGluR2, в том числе соединения формулы (I), усиливают ответ mGluR2 на глутамат, преимущественным является использование в способах по настоящему изобретению эндогенного глутамата.
Поскольку положительные аллостерические модуляторы mGluR2, в том числе соединения формулы (I), усиливают ответ mGluR2 на агонисты, подразумевается, что настоящее изобретение распространяется на лечение неврологических и психических расстройств, ассоциированных с нарушением глутаматергической передачи сигнала, посредством введения эффективного количества положительного аллостерического модулятора mGluR2, в том числе соединения формулы (I), в комбинации с агонистом mGluR2 (или агонистом mGluR2/3). Примеры агонистов mGluR2/mGluR2/3 включают, например, LY-379268; DCG-IV; LY-354740; LY-404039; LY-544344; LY-2140023; LY-181837; LY-389795; LY-446433; LY-450477; талаглюметад; MGS0028; MGS0039; (-)-2-окса-4-аминобицикло[3.1.0]гексан-4,6-дикарбоксилат; (+)-4-амино-2-сульфонилбицикло[3.1.0]гексан-4,6-дикарбоновую кислоту; (+)-2-амино-4-фторбицикло-[3.1.0]гексан-2,6-дикарбоновую кислоту; 1S,2R,5S,6S-2-амино-6-фтор-4-оксобицикло-[3.1.0]гексан-2,6-дикарбоновую кислоту; 1S,2R,4S,5S,6S-2-амино-6-фтор-4-гидроксибицикло[3.1.0]гексан-2,6-дикарбоновую кислоту; 1S,2R,3R,5S,6S-2-амино-3-фторбицикло[3.1.0]гексан-2,6-дикарбоновую кислоту; 1S,2R,3S,5S,6S-2-амино-6-фтор-3-гидроксибицикло[3.1.0]гексан-2,6-дикарбоновую кислоту; (+)-4-амино-2-сульфонилбицикло-[3.1.0]гексан-4,6-дикарбоновую кислоту; (+)-2-амино-4-фторбицикло[3.1.0]гексан-2,6-дикарбоновую кислоту; 1S,2R,5S,6S-2-амино-6-фтор-4-оксобицикло[3.1.0]гексан-2,6-дикарбоновую кислоту; 1S,2R,4S,5S,6S-2-амино-6-фтор-4-гидроксибицикло[3.1.0]гексан-2,6-дикарбоновую кислоту; 1S,2R,3R,5S,6S-2-амино-3-фторбицикло[3.1.0]гексан-2,6-дикарбоновую кислоту или 1S,2R,3S,5S,6S-2-амино-6-фтор-3-гидроксибицикло-
[3.1.0]гексан-2,6-дикарбоновую кислоту. Более предпочтительные агонисты mGluR2 включают LY-379268; DCG-IV; LY-354740; LY-404039; LY-544344 или LY-2140023.
Соединения по настоящему изобретению можно использовать в комбинации с одним или несколькими другими лекарственными средствами в лечении, предупреждении, контроле, уменьшении интенсивности проявлений или снижении риска развития заболеваний или состояний, для которых соединения формулы (I) или другие лекарственные средства могут иметь полезность, если лекарственные средства вместе в комбинации являются более безопасными или более эффективными, чем каждое из лекарственных средств в отдельности.
Фармацевтические композиции
В настоящем изобретении также предусматривают композиции для предупреждения или лечения заболеваний, при которых модулирование рецептора mGlu2 является целесообразным, таких как расстройства, описанные в данном документе. Хотя активный ингредиент можно вводить отдельно, предпочтительно, чтобы он был представлен в виде фармацевтической композиции. Соответственно, настоящее изобретение также относится к фармацевтической композиции, содержащей фармацевтически приемлемый носитель или разбавитель и, в качестве активного ингредиента, терапевтически эффективное количество соединения согласно настоящему изобретению, в частности, соединения формулы (I), его фармацевтически приемлемой соли, его сольвата или его стереохимически изомерной формы или таутомера. Носитель или разбавитель должны быть "приемлемыми" в том смысле, что они должны быть совместимыми с другими ингредиентами композиции и не быть вредными для получающих ее пациентов.
Соединения согласно настоящему изобретению, в частности, соединения формулы (I), их фармацевтически приемлемые соли, их сольваты и стереохимически изомерные формы и таутомеры или какая-либо их подгруппа или комбинация могут быть составлены в различные фармацевтические формы для целей введения. В качестве подходящих композиций могут быть упомянуты все композиции, обычно применяемые для системно вводимых лекарственных средств.
Фармацевтические композиции по настоящему изобретению можно получать любыми способами, хорошо известными в области фармации, например, при помощи таких способов, как описанные в Gennaro et al. Remington's Pharmaceutical Sciences (18th ed., Mack Publishing Company, 1990, см. в особенности Part 8: Pharmaceutical preparations and their Manufacture). Для получения фармацевтических композиций по настоящему изобретению терапевтически эффективное количество конкретного соединения, необязательно в форме соли, в качестве активного ингредиента объединяют в однородную смесь с фармацевтически приемлемым носителем или разбавителем, при этом носитель или разбавитель может принимать широкое разнообразие форм в зависимости от формы препарата, желательного для введения. Данные фармацевтические композиции являются желательными в единичной лекарственной форме, приемлемой, в частности, для перорального, местного, ректального или чрескожного введения, введения путем парентеральной инъекции или путем ингаляции. Например, при получении композиций в лекарственной форме для перорального введения можно использовать любую из обычных фармацевтических сред, таких как, например, вода, гликоли, масла, спирты и т. п., в случае жидких препаратов для перорального введения, таких как, например, суспензии, сиропы, эликсиры, эмульсии и растворы; или твердые носители, такие как, например, крахмалы, сахара, каолин, разбавители, смазывающие средства, связующие вещества, разрыхлители и т. п., в случае порошков, пилюль, капсул и таблеток. Благодаря простоте введения пероральное введение является предпочтительным, а таблетки и капсулы представляют собой наиболее предпочтительные единичные лекарственные формы для перорального введения, в случае которых, очевидно, используются твердые фармацевтические носители. В случае композиций для парентерального введения носитель будет, как правило, по меньшей мере в значительной степени содержать стерильную воду, хотя могут быть включены и другие ингредиенты, например, поверхностно-активные вещества, для улучшения растворимости. Например, можно получать растворы для инъекций, в которых носитель содержит физиологический раствор, раствор глюкозы или смесь физиологического раствора и раствора глюкозы. Также можно получать суспензии для инъекций, в случае которых могут использоваться подходящие жидкие носители, суспендирующие средства и т. п. Также включены препараты в твердой форме, которые предназначены для преобразования, непосредственно перед применением, в препараты в жидкой форме. В композициях, подходящих для чрескожного введения, носитель необязательно включает средство, повышающее проницаемость, и/или подходящее смачивающее средство, необязательно в комбинации с подходящими добавками любой природы в минимальных пропорциях, при этом добавки не оказывают значительного вредного воздействия на кожу. Указанные добавки могут облегчать введение через кожу и/или могут быть полезными при получении желаемых композиций. Данные композиции можно вводить различными путями, например, в виде трансдермального пластыря, путем точечного нанесения, в виде мази.
Особенно предпочтительным является составление вышеупомянутых фармацевтических композиций в виде единичной лекарственной формы для простоты введения и равномерности дозирования. Единичная лекарственная форма, используемая в данном документе, относится к физически отдельным единицам, подходящим в качестве единичных доз, при этом каждая единица содержит предварительно установленное количество активного ингредиента, рассчитанного для получения необходимого терапевтического эффекта, в сочетании с требуемым фармацевтическим носителем. Примерами таких единичных лекарственных форм являются таблетки (в том числе делимые таблетки или таблетки, покрытые оболочкой), капсулы, пилюли, пакетики с порошком, облатки, суппозитории, растворы или суспензии для инъекций и т. п., чайные ложки с верхом, столовые ложки с верхом, а также их отдельные множества.
Поскольку соединения согласно настоящему изобретению являются соединениями, вводимыми перорально, фармацевтические композиции, содержащие указанные соединения для перорального введения, являются особенно предпочтительными.
Для повышения растворимости и/или стабильности соединений формулы (I) в фармацевтических композициях может быть предпочтительным использование α-, β- или γ-циклодекстринов или их производных, в частности, замещенных гидроксиалкилом циклодекстринов, например, 2-гидроксипропил-β-циклодекстрина или сульфобутил-β-циклодекстрина. Сорастворители, такие как спирты, также могут улучшать растворимость и/или стабильность соединений согласно настоящему изобретению в фармацевтических композициях.
Точная дозировка и частота введения зависят от конкретного применяемого соединения формулы (I), конкретного состояния, лечение которого осуществляют, тяжести состояния, лечение которого осуществляют, возраста, массы, пола, степени нарушения и общего физического состояния конкретного пациента, а также от другого медикаментозного лечения, которое индивидуум может получать, что хорошо известно специалистам в данной области. Более того, очевидно, что указанное эффективное суточное количество может быть снижено или увеличено в зависимости от реакции подвергаемого лечению субъекта и/или в зависимости от оценки врача, назначающего соединения согласно настоящему изобретению.
В зависимости от способа введения фармацевтическая композиция будет содержать от 0,05 до 99% по весу, предпочтительно от 0,1 до 70% по весу, более предпочтительно от 0,1 до 50% по весу активного ингредиента и от 1 до 99,95% по весу, предпочтительно от 30 до 99,9% по весу, более предпочтительно от 50 до 99,9% по весу фармацевтически приемлемого носителя, при этом все процентные содержания приводятся в пересчете на общий вес композиции.
Количество соединения формулы (I), которое можно объединять с материалом носителя для получения лекарственной формы с однократной дозировкой, будет варьировать в зависимости от заболевания, подвергаемого лечению, вида млекопитающего и конкретного способа введения. Однако, в качестве общего руководства, подходящие стандартные дозы соединений по настоящему изобретению могут, например, предпочтительно содержать от 0,1 мг до приблизительно 1000 мг активного соединения. Предпочтительная стандартная доза составляет от 1 мг до приблизительно 500 мг. Более предпочтительная стандартная доза составляет от 1 мг до приблизительно 300 мг. Еще более предпочтительная стандартная доза составляет от 1 мг до приблизительно 100 мг. Такие стандартные дозы можно вводить более одного раза в сутки, например, 2, 3, 4, 5 или 6 раз в сутки, но предпочтительно 1 или 2 раза в сутки, с тем, чтобы общая дозировка для взрослого человека весом 70 кг находилась в диапазоне от 0,001 до приблизительно 15 мг на кг веса субъекта в расчете на одно введение. Предпочтительная дозировка составляет от 0,01 до приблизительно 1,5 мг на кг массы субъекта в расчете на одно введение, и такая терапия может продолжаться в течение нескольких недель или месяцев, а в некоторых случаях в течение нескольких лет. Однако следует понимать, что определенный уровень дозы для любого конкретного пациента будет зависеть от ряда факторов, в том числе активности определенного используемого соединения; возраста, массы тела, общего состояния здоровья, пола и режима питания индивидуума, подвергаемого лечению; времени и пути введения; скорости выведения; других лекарственных средств, которые были введены ранее; и тяжести конкретного заболевания, подвергаемого терапии, что хорошо понятно специалистам в данной области.
Типичной дозой может быть одна таблетка от 1 мг до приблизительно 100 мг или от 1 мг до приблизительно 300 мг, принимаемая один раз в сутки или несколько раз в сутки, или одна капсула или таблетка пролонгированного действия, принимаемая один раз в сутки и имеющая пропорционально более высокое содержание активного ингредиента. Эффекта пролонгированного действия можно достичь с помощью материалов капсулы, которые растворяются при различных значениях pH, с помощью капсул с медленным высвобождением при осмотическом давлении или с помощью любых иных известных средств, обеспечивающих контролируемое высвобождение.
В некоторых случаях может понадобиться применение дозировок вне этих диапазонов, что будет очевидно специалистам в данной области. Кроме того, следует отметить, что врач-консультант или лечащий врач будут знать, как и когда начинать, прерывать, корректировать или завершать терапию в соответствии с реакцией отдельного пациента.
Как уже отмечалось выше, настоящее изобретение также относится к фармацевтической композиции, содержащей соединения согласно настоящему изобретению и одно или несколько других лекарственных средств, для применения в качестве лекарственного препарата или для применения в лечении, предупреждении, контроле, уменьшении интенсивности проявлений или снижении риска развития заболеваний или состояний, при которых соединения формулы (I) или другие лекарственные средства могут быть полезными. Также предполагается применение такой композиции для изготовления лекарственного препарата, а также применение такой композиции для изготовления лекарственного препарата для лечения, предупреждения, контроля, уменьшения интенсивности проявлений или снижения риска развития заболеваний или состояний, при которых соединения формулы (I) или другие лекарственные средства могут быть полезными. Настоящее изобретение также относится к комбинации соединения согласно настоящему изобретению и ортостерического агониста mGluR2 (или ортостерического агониста mGluR2/3). Настоящее изобретение также относится к такой комбинации для применения в качестве медикамента. Настоящее изобретение также относится к продукту, содержащему (a) соединение согласно настоящему изобретению, его фармацевтически приемлемую соль или его сольват и (b) ортостерический агонист mGluR2 (или ортостерический агонист mGluR2/3), в качестве комбинированного препарата для одновременного, раздельного или последовательного применения в лечении или предупреждении состояния у млекопитающего, в том числе у человека, лечение или предупреждение которого зависит от нейромодуляторного эффекта аллостерических модуляторов mGluR2, в частности, положительных аллостерических модуляторов mGluR2, или облегчается им. Различные лекарственные средства в таких комбинации или продукте могут быть объединены в одном препарате вместе с фармацевтически приемлемыми носителями или разбавителями, или каждое из них может присутствовать в отдельном препарате вместе с фармацевтически приемлемыми носителями или разбавителями.
Следующие примеры предназначены для иллюстрации, но не для ограничения объема настоящего изобретения.
Химия
Некоторые способы получения соединений по настоящему изобретению проиллюстрированы в следующих примерах. Если не указано иное, все исходные материалы получали от частных поставщиков и применяли без дополнительной очистки.
В данном документе "водн." означает водный; "BEH" означает мостиковый гибрид этилсилоксан/диоксид кремния; "CSH" означает гибрид с заряженной поверхностью; "DAD" означает детектор на диодной матрице; "DCM" означает дихлорметан; "DIPEA" означает N,N-диизопропилэтиламин; "DMF" означает N,N-диметилформамид; "DMSO" означает диметилсульфоксид; "Et2O" означает диэтиловый эфир; "EtOAc" означает этилацетат; "ч." означает час(часы); "HPLC" означает высокоэффективную жидкостную хроматографию; "iPr" означает изопропил; "l" или "L" означает литр; "LCMS" означает жидкостную хроматографию/масс-спектрометрию; "MeOH" означает метанол; "мин." означает минуту(минуты); "т. пл." означает температуру плавления; "MSD" означает масс-селективный детектор; "Pd(PPh3)4" означает тетракис(трифенилфосфин)палладий(0); "RP" означает обращенно-фазовый; "к.т." или "К.T." означает комнатную температуру; "с" означает секунды; "насыщ." означает насыщенный; "SFC" означает хроматографию со сверхкритической подвижной фазой; "раств." означает раствор; "SQD" означает одиночный квадрупольный детектор; "TFA" означает трифторуксусную кислоту; "THF" означает тетрагидрофуран; "UPLC" означает сверхэффективную жидкостную хроматографию.
Реакции под воздействием микроволнового излучения осуществляли в однорежимном реакторе: микроволновом реакторе InitiatorTM Sixty EXP (Biotage AB), или в многорежимном реакторе MicroSYNTH Labstation (Milestone, Inc.).
Тонкослойную хроматографию (TLC) проводили на пластинах со слоем силикагеля 60 F254 (Merck) с применением растворителей с высокой степенью чистоты. Капиллярную хроматографию осуществляли на силикагеле с размером пор 230-400 меш (Merck) при 60 Å с применением стандартных методик. Автоматизированную колоночную флэш-хроматографию проводили с использованием готовых к подсоединению картриджей от Merck на силикагеле с частицами неправильной формы, размер которых составлял 15-40 мкм (одноразовые колонки для флэш-хроматографии с нормальными фазами) в системе SPOT или LAFLASH от Armen Instrument.
Абсолютную стереохимическую конфигурацию для некоторых соединений определяли с помощью колебательного кругового дихроизма (VCD). Их измеряли на Bruker Equinox 55, оснащенном PMA 37, в жидкостной кювете с окном из KBr с применением CD2Cl2 в качестве растворителя (PEM: 1350 см-1, LIA: 1 мВ, разрешение: 4 см-1). Описание применения VCD для определения абсолютной конфигурации можно найти в Dyatkin A.B. et. al, Chirality, 14:215-219 (2002).
Во всех случаях обозначение "RS", указанное в данном документе, означает, что соединение представляет собой рацемическую смесь, если не указано иное. Стереохимическая конфигурация для некоторых соединений была обозначена как "R" или "S", если смесь была разделена; для некоторых соединений стереохимическая конфигурация была обозначена как "*R" или "*S", если абсолютная стереохимическая конфигурация не определена, хотя само соединение было выделено в качестве отдельного стереоизомера и является энантиомерно чистым. Энантиомерный избыток соединений, описанных в данном документе, определяли с помощью анализа рацемической смеси посредством хроматографии со сверхкритической подвижной фазой (SFC) с последующим сравнением разделенного(разделенных) энантиомера(энантиомеров) в ходе SFC.
Получение промежуточных соединений
Промежуточное соединение 1 (I-1)
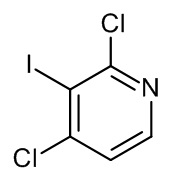
К раствору 2,4-дихлорпиридина (5,2 г, 35,137 ммоль) и диизопропиламина (3,911 г, 38,651 ммоль) в сухом THF (40 мл), охлажденном при -78°C в атмосфере азота, по каплям добавляли н-бутиллитий (24,157 мл, 38,651 ммоль, 1,6 M в гексанах). Полученную реакционную смесь перемешивали при -78°C в течение 45 мин., а затем по каплям добавляли раствор йода (9,81 г, 38,651 ммоль) в сухом THF (20 мл). Смесь перемешивали при -78 °C в течение 1 ч., давали нагреться до к.т., разбавляли EtOAc и гасили NH4Cl (водный насыщ. раствор) и Na2S2O3 (водный насыщ. раствор). Органический слой отделяли, промывали NaHCO3 (водный насыщ. раствор), высушивали (Na2SO4) и концентрировали in vacuo. Неочищенный продукт очищали с помощью колоночной хроматографии (силикагель; гептан/DCM до 20% в качестве элюента). Необходимые фракции собирали и концентрировали in vacuo с получением I-1 (7,8 г, 81%).
Промежуточное соединение 2 (I-2)
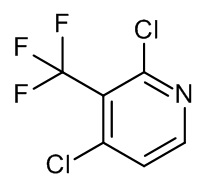
К смеси I-1 (2 г, 7,302 ммоль) в DMF (50 мл) добавляли сложный метиловый эфир фторсульфонил-дифтор-уксусной кислоты ([CAS 680-15-9], 1,858 мл, 14,605 ммоль) и йодид меди (I) (2,796 г, 14,605 ммоль). Реакционную смесь нагревали в герметизированной пробирке при 100°C в течение 5 ч. После охлаждения растворитель выпаривали in vacuo. Неочищенный продукт очищали с помощью колоночной хроматографии (силикагель; DCM в качестве элюента). Необходимые фракции собирали и концентрировали in vacuo с получением I-2 (1,5 г, 95%).
Промежуточное соединение 3 (I-3)
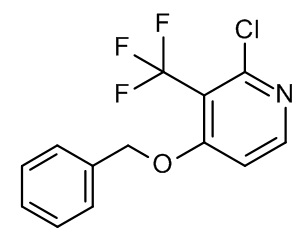
К суспензии NaH (0,487 г, 12,732 ммоль, 60% минеральное масло) в DMF (50 мл), охлажденном при 0°C, добавляли бензиловый спирт (1,262 мл, 12,2 ммоль). Полученную смесь перемешивали в течение 2 мин., затем добавляли I-2 (2,5 г, 11,575 ммоль). Полученную реакционную смесь постепенно нагревали до к.т. и перемешивали в течение 1 ч. Реакционную смесь гасили водой и экстрагировали Et2O. Органический слой отделяли, высушивали (Na2SO4) и концентрировали in vacuo. Неочищенный продукт очищали с помощью колоночной хроматографии (силикагель; градиент гептан/DCM в качестве элюента). Необходимые фракции собирали и концентрировали in vacuo с получением I-3 (1,1 г, 33%).
Промежуточное соединение 4 (I-4)
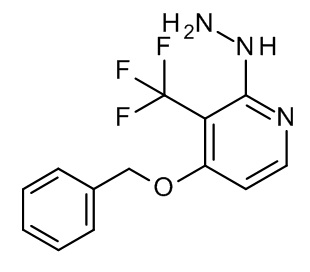
К суспензии I-3 (1,09 г, 3,789 ммоль) в 1,4-диоксане (9 мл) добавляли моногидрат гидразина (3,676 мл, 75,78 ммоль). Реакционную смесь нагревали при 160°C под действием микроволнового излучения в течение 30 мин. После охлаждения полученный раствор концентрировали in vacuo. Полученный таким образом остаток растворяли в DCM и промывали NaHCO3 (водный насыщ. раствор). Органический слой отделяли, высушивали (Na2SO4) и концентрировали in vacuo с получением I-4 (0,890 г, 83%) в виде белого твердого вещества.
Промежуточное соединение 5 (I-5)
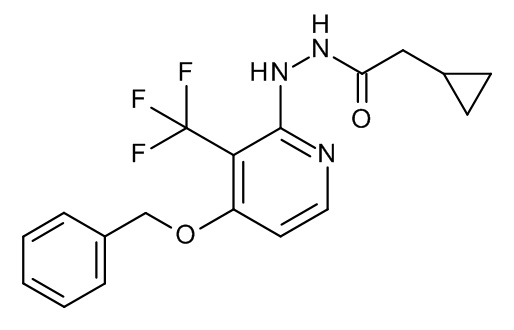
К раствору I-4 (0,890 г, 3,142 ммоль) в сухом DCM (3 мл) добавляли Et3N (0,653 мл, 4,713 ммоль) и циклопропил-ацетилхлорид ([CAS 543222-65-5], 0,373 г, 3,142 ммоль). Полученную реакционную смесь перемешивали при 0°C в течение 20 мин. Полученную смесь затем концентрировали in vacuo с получением I-5 (1,1 г, 96%).
Промежуточное соединение 6 (I-6)
Способом, аналогичным синтезу I-5, синтезировали следующее промежуточное соединение:
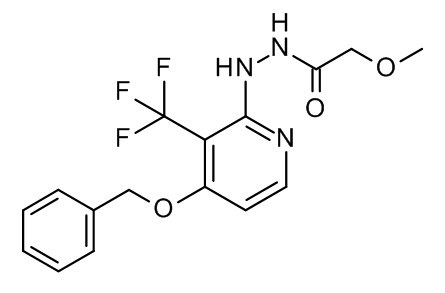
I-6
Добавление осуществляли при 0°C, смесь перемешивали при к.т. в течение 16 ч.; исходный материал: I-4 (8 г), реагент: 2-метокси-ацетилхлорид (3,807 г), с получением I-6 (11,219 г, 97%) в виде масла, осаждающегося при отстаивании.
Промежуточное соединение 7 (I-7)
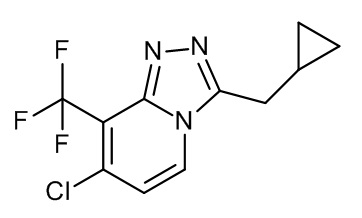
I-5 (1,14 г, 1,872 ммоль) и оксихлорид фосфора (V) (0,349 г, 3,744 ммоль) в CH3CN (10 мл) нагревали при 150°C под действием микроволнового излучения в течение 10 мин. После охлаждения полученную реакционную смесь разбавляли с помощью DCM и промывали с помощью NaHCO3 (водный насыщ. раствор), высушивали (Na2SO4) и концентрировали in vacuo. Неочищенный продукт очищали с помощью колоночной хроматографии (силикагель; DCM/7M раствор NH3 в MeOH до 20% в качестве элюента). Необходимые фракции собирали и концентрировали in vacuo с получением I-7 (0,261 г, 51%) в виде белого твердого вещества.
Промежуточное соединение 8 (I-8)
Способом, аналогичным синтезу I-7, синтезировали следующее промежуточное соединение:
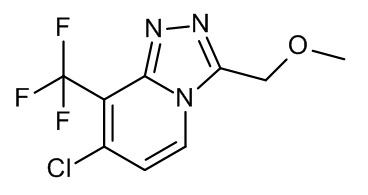
I-8
Реакцию осуществляли в 3 партиях; исходный материал: I-6 (4,7 г), с получением I-8 (2,11 г, 59%) в виде белого твердого вещества.
Промежуточное соединение 9 (I-9)
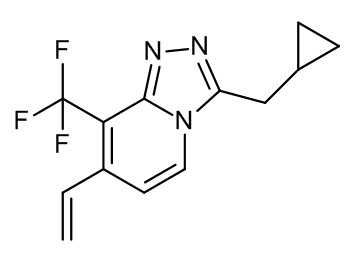
Суспензию I-7 (1,65 г, 5,986 ммоль), сложного пинаколового эфира винилбороновой кислоты (1,218 мл, 7,183 ммоль), Pd(PPh3)4 (0,346, 0,3 ммоль) и NaHCO3 (водный насыщ. раствор, 12,5 мл) в 1,4-диоксане (64,5 мл) нагревали при 150°C под действием микроволнового излучения в течение 13 мин. После охлаждения полученную реакционную смесь разбавляли EtOAc/водой и фильтровали через прокладку из диатомитовой земли. Фильтрат промывали водой и NaCl (водный насыщ. раствор) и экстрагировали с помощью EtOAc. Органический слой отделяли, высушивали (Na2SO4) и концентрировали in vacuo. Остаток снова очищали с помощью колоночной хроматографии (силикагель; DCM/EtOAc от 100/0 до 60/40 в качестве элюента). Необходимые фракции собирали и концентрировали in vacuo с получением I-9 (1,34 г, 83,7%).
Промежуточное соединение 10 (I-10)
Способом, аналогичным синтезу I-9, синтезировали следующее промежуточное соединение:
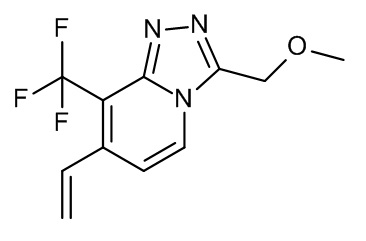
I-10
Исходный материал: I-8 (4,91 г), с получением I-10 (3,65 г, 79%) в виде белого твердого вещества.
Промежуточное соединение 11 (I-11)
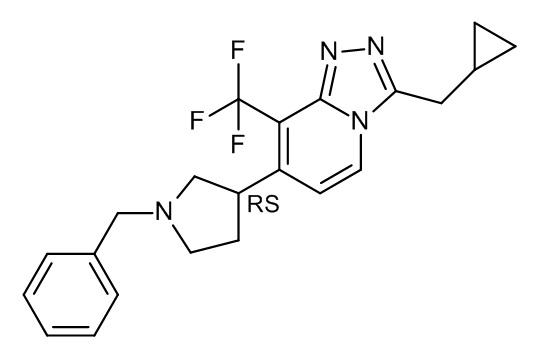
К раствору I-9 (2000 мг, 7,484 ммоль) в DCM (150 мл) при к.т. добавляли TFA (57,269 мкл, 0,748 ммоль), затем по каплям добавляли N-метоксиметил-N-(триметилсилилметил)бензиламин ([CAS 93102-05-7], 5,744 мл, 22,451 ммоль) и полученный раствор перемешивали в течение 3 ч. Затем реакционную смесь промывали водным раствором NaHCO3 (10%). Органический слой отделяли, высушивали (Na2SO4), фильтровали и концентрировали in vacuo. Остаток очищали с помощью колоночной флэш-хроматографии (силикагель; MeOH в DCM от 0/100 до 3/97). Необходимые фракции собирали и концентрировали in vacuo с получением бледно-желтого масла, которое растирали с диизопропиловым эфиром с получением I-11 (1,42 г, 47%) в виде белого твердого вещества. LCMS: Rt 2,29 минуты, масса/заряд 401 [M+H]+, 459 [M+CH3COO]- (Способ 1). 1H ЯМР (400 МГц, DMSO-d6) δ ppm 0,27-0,41 (m, 2 H) 0,49-0,63 (m, 2 H) 1,17-1,33 (m, 1 H) 1,76-1,89 (m, 1 H) 2,31-2,43 (m, 1 H) 2,48 (q, J=8,1 Гц, 1 H) 2,68-2,77 (m, 1 H) 2,81 (dd, J=9,9, 3,9 Гц, 1 H) 3,01 (td, J=8,3, 2,8 Гц, 1 H) 3,10 (d, J=6,9 Гц, 2 H) 3,64-3,79 (m, 2 H) 3,79-3,91 (m, 1 H) 7,28-7,34 (m, 1 H) 7,35-7,46 (m, 5 H) 8,75 (d, J=7,4 Гц, 1 H).
Промежуточное соединение 12 (I-12)
Способом, аналогичным синтезу I-11, также синтезировали следующее промежуточное соединение:
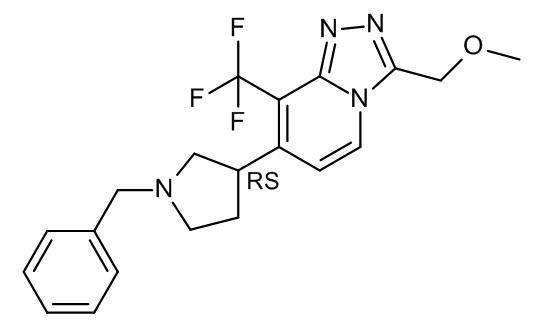
I-12
Исходный материал: I-10 (2,87 г), с получением I-12 (1,5 г, 35%) в виде белого твердого вещества. LCMS: Rt 2,28 минуты, масса/заряд 405 [M+H]+, 463 [M+CH3COO]- (Способ 1). 1H ЯМР (400 МГц, CDCl3) δ ppm 1,21 (t, J=6,9 Гц, 3 H) 1,74-1,89 (m, 1 H) 2,35-2,50 (m, 2 H) 2,68 (dd, J=9,7 Гц, 1 H) 2,86 (dd, J=10,2, 2,8 Гц, 1 H) 3,02-3,15 (m, 1 H) 3,55 (q, J=6,9 Гц, 2 H) 3,63 (d, J=12,9 Гц, 1 H) 3,75 (d, J=12,7 Гц, 1 H) 3,86-4,02 (m, 1 H) 5,05 (s, 2 H) 7,24-7,30 (m, 1 H) 7,31-7,40 (m, 4 H) 7,46 (d, J=7,4 Гц, 1 H) 8,33 (d, J=7,4 Гц, 1 H).
Промежуточное соединение 13 (I-13)
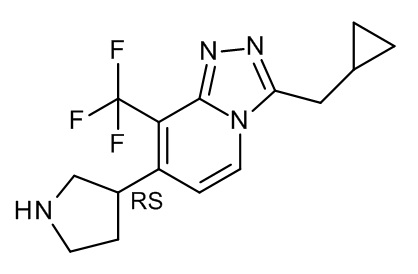
К перемешиваемому раствору I-11 (250 мг, 0,624 ммоль) и DIPEA (376,546 мкл, 2,185 ммоль) в DCM (5 мл) добавляли 1-хлорэтилхлорформиат ([CAS 50893-53-3], 168,407 мкл, 1,561 ммоль) и смесь перемешивали при к.т. в течение 4 ч. Затем добавляли насыщенный раствор NaHCO3 и смесь перемешивали при к.т. в течение 5 мин. Органический слой отделяли, высушивали (MgSO4), фильтровали и растворитель выпаривали in vacuo. Остаток растворяли в MeOH (5 мл) и смесь перемешивали при к.т. в течение 16 ч. Затем растворитель выпаривали и остаток очищали с помощью колоночной флэш-хроматографии (силикагель, 7N NH3 в MeOH в DCM, от 0/100 до 4/96). Необходимые фракции собирали и выпаривали in vacuo с получением I-13 (155 мг, 80%) в виде коричневатого твердого вещества. LCMS: Rt 0,62 минуты, масса/заряд 311 [M+H]+ (Способ 2). 1H ЯМР (400 МГц, CDCl3) δ ppm 0,26-0,42 (m, 2 H) 0,55-0,70 (m, 2 H) 1,10-1,24 (m, 1 H) 1,82 (dq, J=13,4, 7,6 Гц, 1 H) 2,27-2,41 (m, 1 H) 2,95 (dd, J=11,1, 6,2 Гц, 1 H) 3,09 (d, J=6,7 Гц, 2 H) 3,13 (dt, J=10,6, 7,4 Гц, 1 H) 3,23 (dq, J=10,6, 4,2 Гц, 1 H) 3,39 (dd, J=11,1, 8,1 Гц, 1 H) 3,83 (br. quin, J=7,6, 7,6, 7,6, 7,6 Гц, 1 H) 7,06 (d, J=7,4 Гц, 1 H) 8,06 (d, J=7,4 Гц, 1 H).
Промежуточное соединение 14 (I-14)
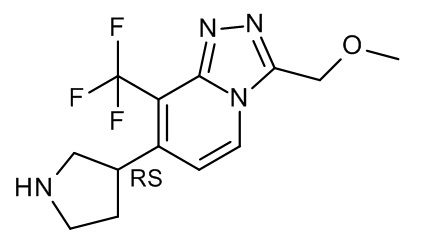
К перемешиваемому раствору I-12 (1,52 г, 3,758 ммоль) и DIPEA (2,267 мл, 13,154 ммоль) в MeOH (30,1 мл, 743,06 ммоль) добавляли 1-хлорэтилхлорформиат ([CAS 50893-53-3], 1,014 мл, 9,396 ммоль) при 0°C и смесь перемешивали при к.т. в течение 4 ч. Затем добавляли насыщенный раствор NaHCO3 и смесь перемешивали при к.т. в течение 5 мин. Органический слой отделяли, высушивали (MgSO4), фильтровали и растворитель выпаривали in vacuo. Остаток растворяли в MeOH и смесь перемешивали при к.т. в течение 48 ч. Затем растворитель выпаривали и остаток очищали с помощью колоночной флэш-хроматографии (силикагель, 7N NH3 в MeOH в CH2Cl2, от 0/100 до 50/50. Необходимые фракции собирали и выпаривали in vacuo с получением I-14 (700 мг, 59%) в виде коричневатого твердого вещества. LCMS: Rt 0,36 минуты, масса/заряд 315 [M+H]+ (Способ 3). 1H ЯМР (400 МГц, CDCl3) δ ppm 1,21 (t, J=6,9 Гц, 3 H) 1,79-1,92 (m, 1 H) 2,28-2,43 (m, 1 H) 2,99 (dd, J=11,1, 6,2 Гц, 1 H) 3,15 (dt, J=10,4, 7,4 Гц, 1 H) 3,27 (dq, J=10,6, 4,2 Гц, 1 H) 3,42 (dd, J=11,1, 8,3 Гц, 1 H) 3,56 (q, J=6,9 Гц, 2 H) 3,85 (br. quin, J=8,1, 8,1, 8,1, 8,1 Гц, 1 H) 5,06 (s, 2 H) 7,12 (d, J=7,4 Гц, 1 H) 8,35 (d, J=7,4 Гц, 1 H).
Синтез конечных соединений
Пример 1
Синтез соединений 1, 1a и 1b (Соед. № 1, соед. № 1a и соед. № 1b)
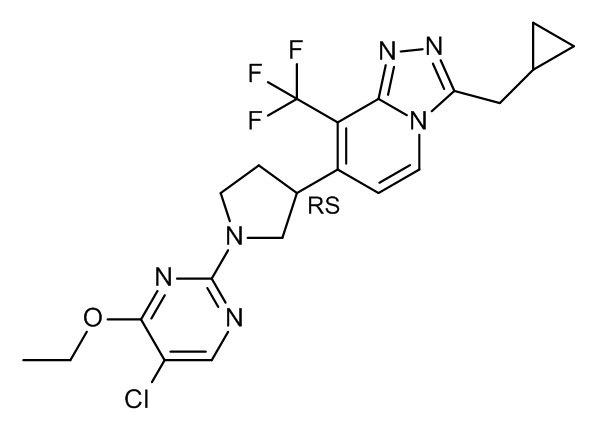
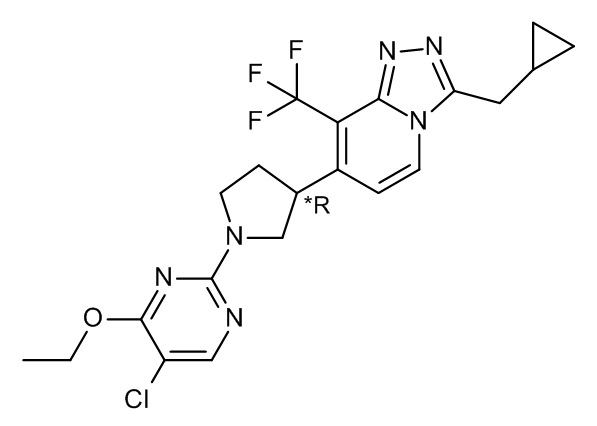
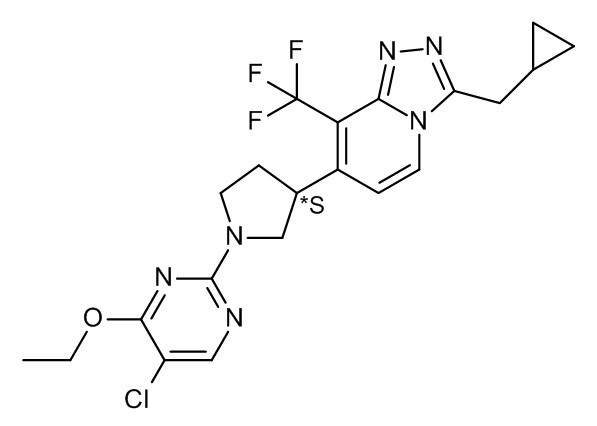
Смесь 2,5-дихлор-4-этоксипиримидина ([CAS 1351762-11-2], 376,88 мг, 1,952 ммоль), I-13 (792 мг, 2,169 ммоль - полученного в результате объединения двух партий) и фторида цезия (988,599 мг, 6,508 ммоль), DIPEA (373,84 мкл, 2,169 ммоль) в DMSO (15 мл) нагревали при 90°C в течение 2 ч. Затем смесь разбавляли насыщенным раствором NaCl и экстрагировали с помощью EtOAc (x3). Объединенные органические слои экстрагировали насыщенным раствором NaCl, высушивали над MgSO4, фильтровали и концентрировали in vacuo. Неочищенное вещество очищали с помощью колоночной флэш-хроматографии (диоксид кремния; 7N NH3 в MeOH в DCM от 0/100 до 2/98). Необходимые фракции собирали и концентрировали in vacuo. Полученный таким образом остаток очищали с помощью RP HPLC (неподвижная фаза: C18 XBridge, 30×100 мм, 5 мкм, подвижная фаза: градиент от 60% 0,1% раствора NH4CO3H/NH4OH с pH 9 в воде, 40% CH3CN до 43% 0,1% раствора NH4CO3H/NH4OH с pH 9 в воде, 57% CH3CN). Необходимые фракции собирали и выпаривали in vacuo с получением соед. № 1 (652 мг, 64%) в виде светло-желтой пены.
Очистку осуществляли с помощью хиральной SFC (неподвижная фаза: Chiralpak AD-H 5 мкм, 250*30 мм, подвижная фаза: 60% CO2, 40% iPrOH) с получением соед. № 1a (262 мг, 26%) и соед. № 1b (243 мг, 24%).
Пример 2
Способом, аналогичным синтезу соединений 1, 1a и 1b, также синтезировали следующие соединения:
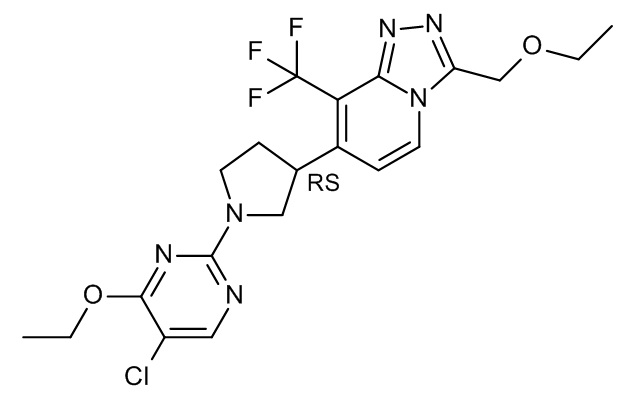
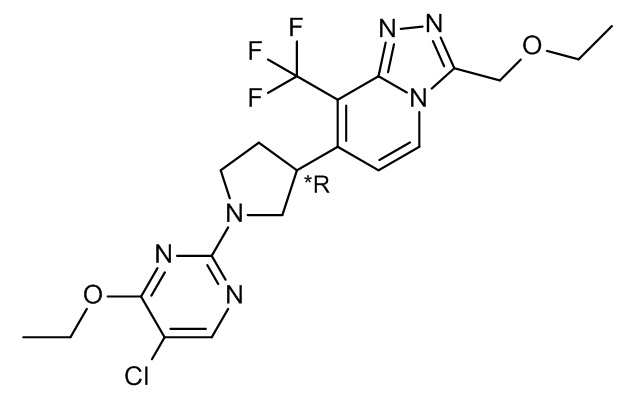
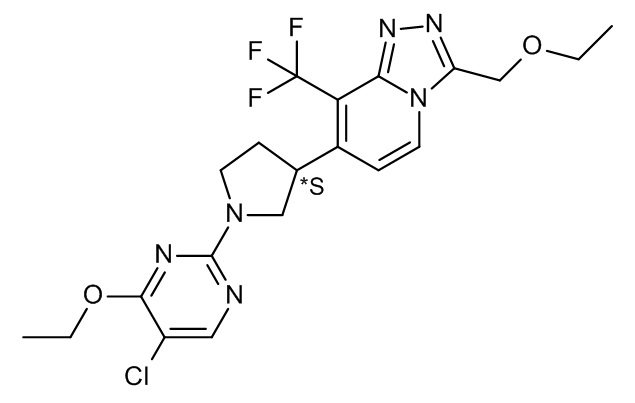
Условия хиральной SFC для соед. № 2 (500 мг после растирания с диизопропиловым эфиром):
неподвижная фаза: Chiralpak AD-H 5 мкм, 250*30 мм, подвижная фаза: 75% CO2, 25% iPrOH (0,3% iPrNH2) с получением 227 мг (22%) соед. № 2a и 223 мг (22%) соед. № 2b.
В таблице 1 ниже представлены дополнительные соединения формулы (I), которые получали по аналогии с вышеприведенными примерами (№ эксп.).
Таблица 1. Типичные соединения формулы (I).
# означает, что экспериментальная процедура описана в примерах.

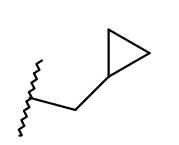


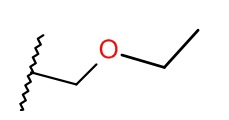


Аналитическая часть
Температуры плавления
Значения представляют собой пиковые значения, и их получают с экспериментальными погрешностями, которые обычно связаны с данным аналитическим способом.
DSC823e (A): Для ряда соединений температуры плавления (т. пл.) определяли с помощью прибора DSC823e (Mettler-Toledo). Точки плавления измеряли с градиентом температуры 10°C/минуту. Максимальная температура составляла 300°C. Регистрировали пиковые значения.
LCMS
Общая процедура
Измерения в ходе высокоэффективной жидкостной хроматографии (HPLC) проводили с помощью насоса для LC, детектора на диодной матрице (DAD) или УФ-детектора и колонки, как определено в соответствующих способах. При необходимости включали дополнительные детекторы (см. приведенную ниже таблицу способов).
Поток из колонки направляли в масс-спектрометр (MS), который был оснащен источником ионизации при атмосферном давлении. В компетенции специалиста в данной области находится установка настраиваемых параметров (например, диапазона сканирования, минимального времени измерения и т. п.) с целью получения ионов, обеспечивающих определение номинального моноизотопного молекулярного веса (MW) соединения и/или точного моноизотопного молекулярного веса. Сбор данных проводили с помощью соответствующего программного обеспечения.
Соединения описывали по их экспериментальному времени удерживания (Rt) и ионам. Если в таблице данных не указано иное, то указанный молекулярный ион соответствует [M+H]+ (протонированной молекуле) и/или [M-H]- (депротонированной молекуле). В случае, если соединение не было способно к непосредственной ионизации, указан тип аддукта (т. е. [M+NH4]+, [M+HCOO]-, [M+CH3COO]- и т. п.). Для молекул со сложными изотопными распределениями (Br, Cl и т. п.) описанное значение является таковым, которое получено для наименьшей изотопной массы. Все результаты получали с экспериментальными погрешностями, которые обычно связаны с применяемым способом.
Таблица 2. Способы LCMS (скорость потока выражена в мл/мин.; температура колонки (T) в °C; время анализа в минутах).
-----T колонки
B: CH3CN
------
50
B: 1/1 CH3CN/
CH3OH
------
60
B: 1/1 CH3CN/ CH3OH,
-------
60
-------
40
Таблица 3. Физико-химические данные для ряда соединений, время удерживания (Rt) в мин., пик, соответствующий [M+H]+ (протонированная молекула), способ LCMS и т. пл. (температура плавления в °C).
(н. о.=не определено).
[M+CH3COO]-
[M+CH3COO]-
[M+CH3COO]-
[M+CH3COO]-
SFC/MS
Общая процедура
Измерения в ходе SFC проводили с применением аналитической системы хроматографии со сверхкритической подвижной фазой (SFC), укомплектованной насосом для двухкомпонентных смесей для доставки диоксида углерода (CO2) и модификатором, автоматическим дозатором, термостатом для колонок с переключающим клапаном для нагревания колонки от комнатной температуры до 80°C, детектором на диодной матрице, оснащенным проточной кюветой для работы под высоким давлением, выдерживающей значения до 400 бар. Поток из колонки направляли в масс-спектрометр (MS), который был оснащен источником ионизации при атмосферном давлении. В компетенции специалиста в данной области находится установка настраиваемых параметров (например, диапазона сканирования, минимального времени измерения и т. п.) с целью получения ионов, обеспечивающих определение номинальной моноизотопной молекулярной массы (MW) соединения. Сбор данных проводили с помощью соответствующего программного обеспечения.
Таблица 4. Аналитические способы SFC-MS (скорость потока выражена в мл/мин.; температура колонки (T) в °C; давление в МПа).
150×4,6 мм, 5 мкм,
Daicel
150×4,6 мм, 5 мкм,
Daicel
Таблица 5. Аналитические данные SFC - Rt означает время удерживания (в минутах), [M+H]+ означает массу протонированного соединения, способ относится к способу, применяемому для анализа энантиомерно чистых соединений с помощью SFC/MS. Измерения сравнивали со смесью.
*A означает первый элюируемый изомер. В означает второй элюируемый изомер.
Углы оптического вращения
Углы оптического вращения измеряли на поляриметре Perkin-Elmer 341 с натриевой лампой и обозначали следующим образом: [α]° (λ, c г/100 мл, растворитель, T°C).
[α]λT=(100α)/(l x c): где l означает длину пробега в дм, а c означает концентрацию в г/100 мл для образца при температуре T (°C) и длине волны λ (в нм). Если применяемая длина волны света составляет 589 нм (D-линия натрия), то вместо этого можно применять символ D. Всегда следует приводить знак направления вращения (+ или -). В случае применения данного уравнения концентрацию и растворитель всегда приводят в круглых скобках после угла вращения. Угол вращения указывают в градусах, а единицы концентрации не приводят (принято, что они представлены в г/100 мл).
Таблица 6: Данные об оптическом вращении.
вес./об. %
Ядерный магнитный резонанс (ЯМР)
Для ряда соединений 1H-ЯМР-спектры регистрировали на спектрометрах Bruker DPX-400 или Bruker AV-500 со стандартными последовательностями импульсов, работающих при 400 МГц и 500 МГц, соответственно. Химические сдвиги (δ) указаны в частях на миллион (ppm) для слабопольного сдвига от тетраметилсилана (TMS), который применяли в качестве внутреннего стандарта.
Таблица 7. NMR.
Фармакологические примеры
A) Фармакология in vitro
Соединения, представленные в настоящем изобретении, являются положительными аллостерическими модуляторами mGluR2. Данные соединения, по-видимому, усиливают ответы на глутамат путем связывания с аллостерическим участком, отличным от глутамат-связывающего участка. В случае присутствия соединений формулы (I) ответ mGluR2 на концентрацию глутамата усиливается. Предполагается, что соединения формулы (I) оказывают свой эффект главным образом на mGluR2 благодаря своей способности к повышению функции рецептора. Эффекты положительных аллостерических модуляторов, тестируемых в отношении mGluR2 с использованием способа анализа связывания [35S]GTPγS, описанного ниже, который подходит для идентификации таких соединений, и, более конкретно соединений формулы (I), показаны в таблице 8.
Анализ связывания [35S]GTPγS
Анализ связывания [35S]GTPγS представляет собой функциональный анализ с использованием мембран, применяемый для изучения функции рецепторов, сопряженных с G-белком (GPCR), в котором определяют включение негидролизуемой формы GTP, [35S]GTPγS (гуанозин-5'-трифосфата, меченного гамма-излучающим 35S). Субъединица α G-белка катализирует обмен гуанозин-5'-дифосфата (GDP) на гуанозинтрифосфат (GTP), и при активации GPCR агонистом [35S]GTPγS включается в структуру и не может быть отщеплена, чтобы продолжить цикл обмена (Harper (1998) Current Protocols in Pharmacology 2.6.1-10, John Wiley & Sons, Inc.). Количество включенного радиоактивного [35S]GTPγS является непосредственным показателем активности G-белка, и, следовательно, можно определить активность агониста. Показано, что рецепторы mGlu2 преимущественно сопряжены с Gαi-белком, что является преимущественным сопряжением для данного способа, и, следовательно, он широко используется для изучения рецепторной активации рецепторов mGlu2 как в рекомбинантных линиях клеток, так и в тканях. В данном документе авторы настоящего изобретения описывают применение анализа связывания [35S]GTPγS с применением мембран клеток, трансфицированных рецептором mGlu2 человека, на основе материалов Schaffhauser et al. (Molecular Pharmacology, 2003, 4:798-810) для выявления свойств положительного аллостерического модулирования (PAM) у соединений согласно настоящему изобретению.
Получение мембран
Клетки CHO культивировали до предконфлюентности и стимулировали 5 мМ бутиратом в течение 24 ч. Затем клетки собирали путем соскабливания в PBS, и суспензию клеток центрифугировали (10 мин. при 4000 об./мин. в настольной центрифуге). Надосадочную жидкость сливали, и осадок осторожно ресуспендировали в 50 мМ Tris-HCl, pH 7,4, путем перемешивания с помощью вихревой мешалки и набора в пипетку и выпуска из пипетки. Суспензию центрифугировали при 16000 об./мин. (Sorvall RC-5C Plus с ротором SS-34) в течение 10 минут и надосадочную жидкость сливали. Осадок гомогенизировали в 5 мМ Tris-HCl, при pH 7,4, с помощью гомогенизатора Ultra Turrax и вновь центрифугировали (18000 об./мин., 20 мин., 4°C). Конечный осадок повторно суспендировали в 50 мМ Tris-HCl, pH 7,4, и хранили при -80°C в соответствующих аликвотах до применения. Концентрацию белка определяли по способу Бредфорда (Bio-Rad, США) с бычьим сывороточным альбумином в качестве стандарта.
Анализ связывания [35S]GTPγS
Измерение активности положительного аллостерического модулирования mGluR2 у тестируемых соединений производили следующим образом. Тестируемые соединения и глутамат разбавляли в аналитическом буфере, содержащем 10 мМ HEPES в форме кислоты, 10 мМ HEPES в форме соли, pH 7,4, 100 мМ NaCl, 3 мМ MgCl2 и 10 мкМ GDP. Мембраны, содержащие рецептор mGlu2 человека, размораживали на льду и разбавляли аналитическим буфером, дополненным 14 мкг/мл сапонина. Мембраны предварительно инкубировали с соединением в отдельности или вместе с глутаматом в предварительно определенной (~EC20) концентрации (анализ PAM) в течение 30 мин. при 30°C. После добавления [35S]GTPγS (конечная концентрация 0,1 нМ), анализируемые смеси встряхивали в течение короткого периода и дополнительно инкубировали для обеспечения включения [35S]GTPγS при активации (30 минут, 30°C). Конечные аналитические смеси содержали 7 мкг мембранного белка в 10 мМ HEPES в форме кислоты, 10 мМ HEPES в форме соли, pH 7,4, 100 мМ NaCl, 3 мМ MgCl2, 10 мкМ GDP и 2 мкг/мл сапонина. Общий объем реакционной смеси составлял 200 мкл. Реакции останавливали путем быстрой фильтрации через планшеты Unifilter-96 GF/B (Perkin Elmer, Массачусетс, США) с помощью универсального коллектора FilterMate для 96-луночных планшетов. Фильтры 6 раз промывали ледяной смесью 10 мМ NaH2PO4/10 мМ Na2HPO4, pH 7,4. Затем фильтры высушивали на воздухе и в каждую лунку добавляли 40 мкл жидкого сцинтилляционного коктейля (Microscint-O). Радиоактивность мембраносвязанных комплексов подсчитывали в сцинтилляционном и люминесцентном счетчике для микропланшетов от Perkin Elmer.
Анализ данных
Построение кривых зависимости концентрация-ответ для иллюстративных соединений по настоящему изобретению, получаемых в присутствии EC20 агониста mGluR2 глутамата, для определения положительного аллостерического модулирования (PAM) осуществляли с помощью программного интерфейса Lexis (разработанного в J&J). Расчет данных производили в виде % от контрольного ответа на глутамат, определяемого как максимальный ответ, вызываемый при добавлении глутамата в отдельности. Сигмоидальные кривые зависимости концентрация-ответ, построенные путем нанесения этих значений в процентах в зависимости от логарифма концентрации тестируемого соединения, анализировали с помощью нелинейного регрессионного анализа. Затем рассчитывали концентрацию, вызывающую полумаксимальный эффект, в виде EC50.
Нижеприведенные значения pEC50 рассчитывали в виде -log EC50, если EC50 выражали в M. Emax определяли как относительный максимальный эффект (т. е. максимальный эффект в % по сравнению с контрольным ответом на глутамат).
В таблице 8 ниже показаны фармакологические данные, полученные для соединений формулы (I).
Таблица 8. Фармакологические данные для соединений согласно настоящему изобретению.
n.c. означает, что pEC50 не могла быть рассчитана.
Значения pEC50 не рассчитывали в случаях, когда кривая зависимости концентрация-ответ не достигала уровня плато.
Все соединения тестировали в присутствии агониста mGluR2 глутамата в предварительно определенной концентрации EC20 для определения положительного аллостерического модулирования. Значения pEC50 рассчитывали из эксперимента по изучению зависимости концентрация-ответ по меньшей мере по 8 концентрациям.
B) Фармакология in vivo
Исследования противосудорожного средства - тест со стимуляцией в 6 Гц у мышей
В предварительно определенном промежутке времени после обработки лекарственным средством (стандарт: 0,5 ч.) отдельных мышей стимулировали электрическим током достаточной силы (32 мА в течение 3 с; подаваемым через электроды на роговице), чтобы вызвать лимбический припадок. Проявления "психомоторного" припадка впервые были описаны Toman (Toman, J.E.P., 1951, "Neuropharmacologic considerations in psychic seizures" Neurology, 1, 444-460; Toman, J.E.P., Evertett, G.M., Richards, R.K., 1952, "The search for new drugs against epilepsy" Tex. Rep. Biol. Med. 10, 96-104). Авторы настоящего изобретения распределили типы поведения на 4 наблюдения: 1) Оглушенность или неподвижность: Изначально мышь может выглядеть как "оглушенная". Это состояние может характеризоваться неподвижностью или отсутствием осознанности в отношении ее окружения, о чем свидетельствуют типы поведения 2 и 3 (клонус передней лапы или лицевые непроизвольные движения). Поза при оглушении чаще всего вертикальная, однако мышь также может упасть на бок во время припадка; передние конечности часто скрещены, а задние конечности широко расставлены. "Оглушению" иногда может предшествовать несколько секунд бега с неровной поступью. 2) Клонус передней лапы или непроизвольное движение: обычно напоминает ситуацию, когда мышь с повторениями поднимает свою переднюю лапу, а затем топает ею по земле. Это обычно повторяется несколько раз, но должно повторяться по меньшей мере дважды, чтобы считаться присутствующим. 3) Лицевое непроизвольное движение: у мыши больше всего напоминает чавканье челюстью или хватание воздуха; это также должно происходить по крайней мере дважды, чтобы считаться присутствующим. 4) Приподнятый хвост или хвост Штрауба, который должен быть приподнят более чем на 45 градусов, чтобы считаться присутствующим. Продолжительность припадка варьирует от 5 до 75 с; в конце припадка животное довольно неожиданно возобновляет нормальную локомоцию и познавательный инстинкт. Каждый из четырех упомянутых выше типов поведения оценивали как отсутствующий (0) или присутствующий (1). Поскольку контрольные крысы почти во всех случаях демонстрируют по меньшей мере 3 из 4 типов поведения, балл 3 или 4 соответствует припадку, а балл 2 или меньше считается защищенным.
Таблица 9. Исследования противосудорожного средства - тест со стимуляцией в 6 Гц у мышей. ED50 означает среднюю эффективную дозу; PO означает пероральный путь; SC означает подкожный путь.
Примеры возможных композиций
"Активный ингредиент", как используется во всех данных примерах, относится к конечному соединению формулы (I), его фармацевтически приемлемым солям, его сольватам и стереохимически изомерным формам и таутомерам.
Типичные примеры рецептур для состава по настоящему изобретению являются следующими:
1. Таблетки
Активный ингредиент от 5 до 50 мг.
Фосфат дикальция 20 мг
Лактоза 30 мг
Тальк 10 мг
Стеарат магния 5 мг
Картофельный крахмал до 200 мг
В данном примере активный ингредиент можно заменить таким же количеством какого-либо из соединений в соответствии с настоящим изобретением, в частности таким же количеством какого-либо из соединений, приведенных в качестве примера.
2. Суспензия
Водную суспензию для перорального введения получают таким образом, что каждый 1 миллилитр содержит от 1 до 5 мг одного из активных соединений, 50 мг карбоксиметилцеллюлозы натрия, 1 мг бензоата натрия, 500 мг сорбита и воды до 1 мл.
3. Форма для инъекций
Композицию для парентерального введения получают путем перемешивания 1,5% по весу активного ингредиента по настоящему изобретению в 10% по объему пропиленгликоля в воде.
4. Мазь
Активный ингредиент 5-1000 мг;
Стеариловый спирт 3 г
Ланолин 5 г
Белый вазелин 15 г
Вода до 100 г
В данном примере активный ингредиент можно заменить таким же количеством какого-либо из соединений в соответствии с настоящим изобретением, в частности, таким же количеством какого-либо из соединений, приведенных в качестве примера.
Допустимые варианты не следует рассматривать как отклонение от объема настоящего изобретения. Будет очевидно, что специалисты в данной области могут изменять описанное таким образом изобретение различными способами.
Изобретение относится к 1,2,4-триазоло[4,3-a]пиридиновым соединениям формулы (I) в качестве положительных аллостерических модуляторов (PAM) метаботропных глутаматных рецепторов подтипа 2 ("mGluR2"), а также к фармацевтической композиции на их основе и способу лечения или предупреждения расстройств центральной нервной системы, таких как шизофрения, мигрень, эпилепсия, паническое расстройство и др. В общей формуле (I) R1 выбран из (C3-8циклоалкил)C1-3алкила и (C1-3алкилокси)C1-3алкила. 3 н. и 5 з.п. ф-лы, 9 табл., 2 пр.
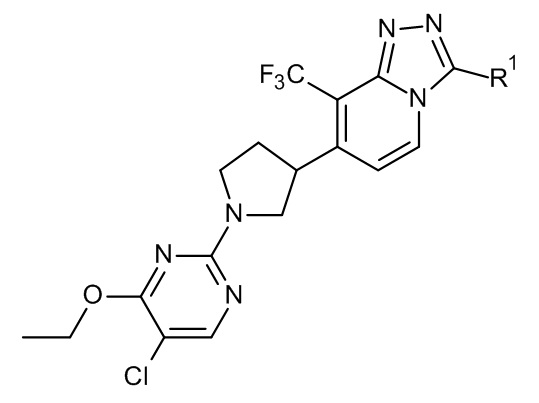 (I)
(I)
1. Соединение формулы (I):
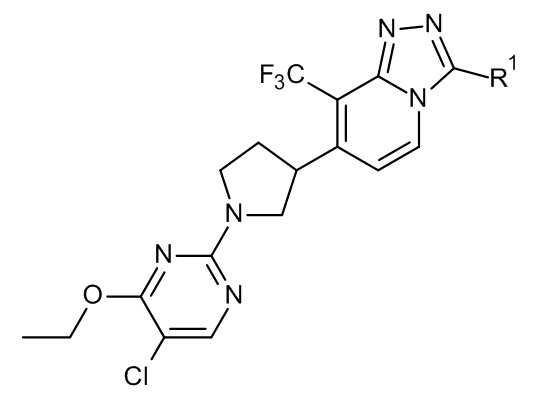 (I),
(I),
или его стереохимически изомерная форма,
где R1 выбран из (C3-8циклоалкил)C1-3алкила и (C1-3алкилокси)C1-3алкила;
или их фармацевтически приемлемая соль.
2. Соединение по п. 1 или его стереоизомерная форма,
где R1 представляет собой (C3-8циклоалкил)C1-3алкил, (C1-3алкилокси)C1-3алкил;
или его фармацевтически приемлемая соль.
3. Соединение по п. 1 или 2,
где R1 представляет собой (циклопропил)метил или (этилокси)метил;
или его фармацевтически приемлемая соль.
4. Соединение по любому из пп. 1-3, где соединение представляет собой
7-[1-(5-хлор-4-этоксипиримидин-2-ил)пирролидин-3-ил]-3-(циклопропилметил)-8-(трифторметил)-[1,2,4]триазоло[4,3-a]пиридин;
7-[(3*R)-1-(5-хлор-4-этоксипиримидин-2-ил)пирролидин-3-ил]-3-(циклопропилметил)-8-(трифторметил)-[1,2,4]триазоло[4,3-a]пиридин;
7-[(3*S)-1-(5-хлор-4-этоксипиримидин-2-ил)пирролидин-3-ил]-3-(циклопропилметил)-8-(трифторметил)-[1,2,4]триазоло[4,3-a]пиридин;
7-[1-(5-хлор-4-этоксипиримидин-2-ил)пирролидин-3-ил]-3-(этоксиметил)-8-(трифторметил)-[1,2,4]триазоло[4,3-a]пиридин;
7-[(3*R)-1-(5-хлор-4-этокси-пиримидин-2-ил)пирролидин-3-ил]-3-(этоксиметил)-8-(трифторметил)-[1,2,4]триазоло[4,3-a]пиридин или
7-[(3*S)-1-(5-хлор-4-этокси-пиримидин-2-ил)пирролидин-3-ил]-3-(этоксиметил)-8-(трифторметил)-[1,2,4]триазоло[4,3-a]пиридин.
5. Фармацевтическая композиция, обладающая свойством положительных аллостерических модуляторов (РАМ) метаботропных глутаматных рецепторов подтипа 2 («mGluR2»), содержащая терапевтически эффективное количество соединения по любому из пп. 1-4 и фармацевтически приемлемый носитель или наполнитель.
6. Соединение по любому из пп. 1-4 или фармацевтическая композиция по п. 5 для применения в качестве лекарственного средства, обладающего свойством положительных аллостерических модуляторов (РАМ) метаботропных глутаматных рецепторов подтипа 2 («mGluR2»).
7. Соединение по любому из пп. 1-4 или фармацевтическая композиция по п. 5 для применения в лечении или предупреждении расстройства центральной нервной системы, выбранного из группы шизофрении (в частности, ее негативных симптомов или остаточных симптомов), генерализованного тревожного расстройства, биполярного расстройства (I или II типа), мигрени, поведенческих и психологических симптомов деменции, эпилепсии или судорожных расстройств, панического расстройства, смешанного тревожно-депрессивного расстройства и агорафобии.
8. Способ лечения или предупреждения расстройства центральной нервной системы, выбранного из группы шизофрении (в частности, ее негативных симптомов или остаточных симптомов), генерализованного тревожного расстройства, биполярного расстройства (I или II типа), мигрени, поведенческих и психологических симптомов деменции, эпилепсии или судорожных расстройств, панического расстройства, смешанного тревожно-депрессивного расстройства и агорафобии, включающий введение субъекту, нуждающемуся в этом, терапевтически эффективного количества соединения по любому из пп. 1-4 или терапевтически эффективного количества фармацевтической композиции по п. 5.
| WO 2010130423 A1, 18.11.2010 | |||
| WO 2012062752 A1, 18.05.2012 | |||
| WO 2010130424 A9, 18.11.2010 | |||
| ПРОИЗВОДНЫЕ АЦЕТИЛЕНИЛ-ПИРАЗОЛО-ПИРИМИДИНА В КАЧЕСТВЕ АНТАГОНИСТОВ mGluR2 | 2006 |
|
RU2412943C2 |
Авторы
Даты
2019-07-25—Публикация
2015-12-10—Подача